Заміщені піролопіразольні похідні як інгібітори кінази
Номер патенту: 81790
Опубліковано: 11.02.2008
Автори: Браска Марія Габріелла, Певарелло Паоло, Руссель Патрік, Фанчеллі Даніелє, Амічі Раффаелла, Вулпетті Анна, Незі Марчелла, Орзіні Паоло, Орці Фабріціо
Формула / Реферат
1. Спосіб лікування захворювань, пов’язаних з проліферацією клітин, які викликані і/або пов’язані із зміненою кіназною активністю, що залежить від клітинного циклу, шляхом введення потребуючому лікування ссавцеві ефективної кількості сполуки, представленої формулою (Іа) і (Іb):
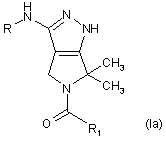 ,
,
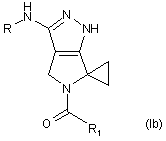 ,
,
де:
R означає групу -CORа, -CONHRa або -CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6-членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝΗ, О або S;
R1 вибирають з групи, що включає:
a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом;
b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом;
c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4-метилпіперазиніл)метилфенільну групу;
d) групу формули (IIа) і (ІІb):
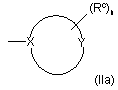 ,
,
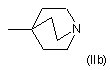 ,
,
де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4;
е) групу формули (IIс) і (IId):
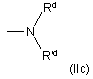 ,
,
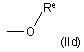 ,
,
де Rd, R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи;
за умови, що у формулі (Іа), коли R1 означає групу формули (IIc) і один із замісників Rd або R’d означає атом водню, в той час як інший з Rd або R’d означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3-бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4-фторфенілметильну, циклопропільну або 2-нафтилметильну групу;
або її фармацевтично прийнятної солі.
2. Спосіб за п. 1, де захворювання, пов’язане з проліферацією клітин, вибирають з групи, що включає рак, хворобу Альцгеймера, вірусні інфекції, аутоімунні захворювання і нейродегенеративні розлади.
3. Спосіб за п. 2, де рак вибирають з групи, що включає карциному, карциному сквамозних клітин, гемопоетичні пухлини мієлоїдної або лімфоїдної клітинної лінії, пухлини мезенхімного походження, пухлини центральної і периферичної нервової системи, меланому, семіному, тератокарциному, остеосаркому, ксеродерму пігментну, кератоксантому, фолікулярний рак щитовидної залози і саркому Капоши.
4. Спосіб за п. 1, де захворювання, пов’язане з проліферацією клітин, вибирають з групи, що включає доброякісну гіперплазію передміхурової залози, сімейний аденоматозний поліпоз, неврофіброматоз, псоріаз, проліферацію гладких клітин судин, пов’язану з атеросклерозом, легеневим фіброзом, артритом, гломерулонефритом і післяхірургічним стенозом і рестенозом.
5. Спосіб за п. 1, який забезпечує придушення ангіогенезу і метастазу пухлин.
6. Спосіб за п. 1, який забезпечує терапію при відторгненні органів при трансплантації і лікування хвороби «хазяїн проти трансплантата».
7. Спосіб за п. 1, який забезпечує лікування і попередження облисіння, викликаного радіотерапією або хіміотерапією.
8. Спосіб за п. 1, який включає також призначення потребуючому лікування ссавцеві радіотерапевтичних і хіміотерапевтичних схем лікування у поєднанні з принаймні одним цитостатичним або цитотоксичним засобом.
9. Спосіб за п. 1, де потребуючим лікування ссавцем є людина.
10. Спосіб інгібування активності циклінзалежної кінази, в якому приводять у контактування вказану кіназу з ефективною кількістю сполуки за п. 1.
11. Сполука, представлена формулою (Іа) і (Іb):
 ,
,
 ,
,
де R означає групу -CORa, -CONHRa або -CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6-членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝΗ, О або S;
R1 вибирають з групи, що включає:
a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом;
b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом;
c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4-метилпіперазиніл)-метилфенільну групу;
d) групу формули (IIа) і (ІІb):
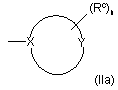 ,
,
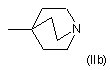 ,
,
де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=О), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4;
e) групу формули (IIc) і (IId):
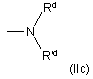 ,
,
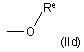 ,
,
де Rd, R’d i Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи;
за умови, що у формулі (Іа), коли R1 означає групу формули (IIc) і один із замісників Rd або R’d означає атом водню, в той час як інший з Rd або R’d означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3-бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4-фторфенілметильну, циклопропільну або 2-нафтилметильну групу;
або її фармацевтично прийнятна сіль.
12. Сполука формули (Іа) або (Іb) за п. 11, де R означає групу -CORa, де значення Ra визначені в п. 11, і R1 означає трет-бутильну групу.
13. Сполука формули (Іа) або (Іb) за п. 11, де R означає групу -CONHRa, де значення Ra визначені в п. 11, і R1 означає трет-бутильну групу.
14. Сполука формули (Іа) або (Іb) за п. 11, де R означає групу -CONRaRb, де значення Ra і Rb визначені в п. 11, і R1 означає трет-бутильну групу.
15. Сполука формули (Іа) або (Іb) за п. 11, де значення R визначені в п. 11, і R1 означає групу формули (IIа), вибрану з
 ,
,
 ,
,
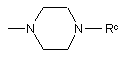 ,
,
 ,
,
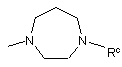 ,
,
де значення n і Rc визначені в п. 11.
16. Сполука формули (Іа) або (Іb) за п. 11, де значення R визначені в п. 11, i R1 означає групу формули (IIа), вибрану з
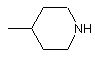 ,
,
 ,
,
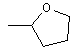 ,
,
де значення Rc визначені в п. 11.
17. Сполука формули (Іа) за п. 11, де R означає групу -CORa, де Ra означає 4-фторфенільну або циклобутильну групу, і значення R1 визначені в п. 11.
18. Сполука формули (Іа) за п. 11, де значення R визначені в п. 11, і R1 означає групу, яку вибирають з трет-бутильної, 1-метилпіперидил-4-ільної, 1-метилпіперазиніл-4-ільної, 2-(R,S)-тетрагідрофураніл-2-ільної, 2-(R)-тетрагідрофураніл-2-ільної або 2-(S)-тетрагідрофураніл-2-ільної групи.
19. Сполука формули (Іа) або (Іb) за п. 11, де будь-яка з груп Ra, Rb і Rc, значення яких визначені в п. 11, необов’язково додатково заміщені, за одним або декількома зі своїх вільних положень, групами, незалежно вибраними з: галогену, нітрогрупи, оксогруп (=O), ціаногрупи, алкільної, поліфторалкільної, поліфторалкокси, алкенільної, алкінільної, гідроксіалкільної, арильної, арилалкільної, гетероциклільної, циклоалкільної, гідрокси, алкоксигрупи, арилоксигрупи, гетероциклілоксигрупи, метилендіоксигрупи, алкілкарбонілоксигрупи, арилкарбонілоксигрупи, циклоалкенілоксигрупи, алкіліденамінооксигрупи, карбокси, алкоксикарбонільної, арилоксикарбонільної, циклоалкілоксикарбонільної, аміногрупи, уреїдогрупи, алкіламіногрупи, діалкіламіногрупи, ариламіногрупи, діариламіногрупи, форміламіногрупи, алкілкарбоніламіногрупи, арилкарбоніламіногрупи, гетероциклілкарбоніламіногрупи, алкоксикарбоніламіногрупи, алкоксііміногрупи, алкілсульфоніламіногрупи, арилсульфоніламіногрупи, формільної, алкілкарбонільної, арилкарбонільної, циклоалкілкарбонільної, гетероциклілкарбонільної, амінокарбонільної, алкіламінокарбонільної, діалкіламінокарбонільної, алкілсульфонільної, арилсульфонільної, аміносульфонільної, алкіламіносульфонільної, діалкіламіносульфонільної, арилтіогрупи і алкілтіогрупи.
20. Сполука формули (Іа) або (Іb) за п. 11, необов’язково у формі фармацевтично прийнятної солі, вибрана з групи, що включає:
N-{6,6-диметил-5-[(1-метилпіперидин-4-іл)карбоніл]-2,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}циклобутанкарбоксамід;
N-[5-(2,2-диметилпропаноїл)-6,6-диметил-1,4,5,6-тетрагідропіроло[3,4-с]піразол-3-іл]-4-фторбензамід;
N-[5-(2,2-диметилпропаноїл)-2,4,5,6-тетрагідропіроло[3,4-с]піразол-6-спіроциклопропан-3-іл]-4-фторбензамід;
N-{6,6-диметил-5-[(2R)-тетрагідрофуран-2-ілкарбоніл]-1,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}-4-фторбензамід;
N-{6,6-диметил-5-[(2S)-тетрагідрофуран-2-ілкарбоніл]-1,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}-4-фторбензамід;
N-{6,6-диметил-5-[(1-метилпіперидин-4-іл-)карбоніл]-2,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}-4-фторбензамід;
N-[5-[(1-метилпіперидин-4-іл)карбоніл]-2,4,5,6-тетрагідропіроло[3,4-с]піразол-3-іл]-4-фторбензамід;
N-{6,6-диметил-5-[(4-метилпіперазин-1-іл)карбоніл]-2,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}-4-фторбензамід;
N-[5-[(4-метилпіперазин-1-іл)карбоніл]-2,4,5,6-тетрагідропіроло[3,4-с]піразол-6-спіроциклопропан-3-іл]-4-фторбензамід;
4-хлор-N-{6,6-диметил-5-(4-піролідин-1-ілметилпіперидин-1-карбоніл)-1,4,5,6-тетрагідропіроло-[3,4-с]піразол-3-іл}бензамід.
21. Сполука формули (Іа) або (Іb) за п. 11, необов’язково у формі фармацевтично прийнятної солі, однозначно ідентифікована в таблицях III, IV, V і VI експериментальної частини опису.
22. Сполука А13-М1-В03 формули (Іа) за п. 11, де R означає групу -CORa, де Ra означає циклобутильну групу, і R1 означає групу формули (IIа), відповідну 1-метилпіперидил-4-ільній групі, як у вільній формі, так і у формі гідрохлоридної або мезилатної солі.
23. Спосіб одержання сполуки формули (Іа) або (Іb) за п. 11 або її фармацевтично прийнятної солі, в якому проводять:
а) взаємодію сполуки формули (ІІІа) або (ІIIb)
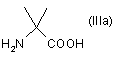 ,
,
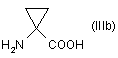
з акрилонітрилом з утворенням відповідного похідного формули (IVa) або (IVb)
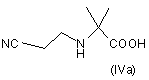 ,
,
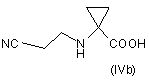 ;
;
b) захист аміногрупи сполуки формули (IVa) або (IVb) з утворенням відповідного похідного формули (Va) або (Vb)
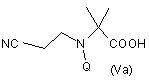 ,
,
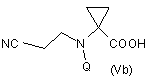 ,
,
де Q означає відповідну амінозахисну групу;
c) взаємодію сполуки формули (Va) або (Vb) з відповідним алкілуючим агентом з утворенням відповідного похідного складного ефіру формули (VIa) або (VIb)
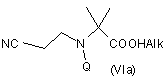 ,
,
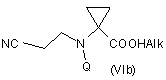 ,
,
де Alk означає відповідну С1-С4алкільну групу;
d) взаємодію сполуки формули (VIa) або (VIb) з гідридом натрію (NaH) з утворенням відповідного похідного формули (VIIa) або (VIIb)
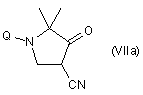 ,
,
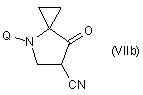 ;
;
e) взаємодію сполуки формули (VIIa) або (VIIb) з гідразингідратом з утворенням відповідного похідного формули (VIIIa) або (VIIIb)
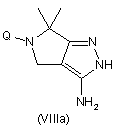 ,
,
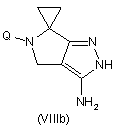 ;
;
f) взаємодію сполуки формули (VIIIa) або (VIIIb) з етилхлорформіатом з утворенням відповідного похідного формули (IХа) або (ІХb), кожне з яких може бути в будь-якій з двох регіоізомерних форм
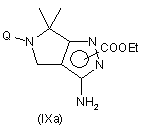 ,
,
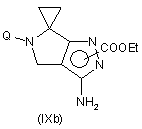 ,
,
і взаємодію сполук формули (IХа) або (ІХb) відповідно до однієї з альтернативних стадій (g.1), (g.2) або (g.3):
g.1) зі сполукою формули (X)
RaCO-Z, (X)
де значення Ra визначені в п. 11, і Ζ означає атом галогену, з утворенням сполуки формули (ХІа) або (ХІb)
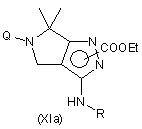 ,
,
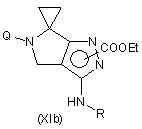 ,
,
де R означає групу -CORa;
g.2) зі сполукою формули (XII)
Ra-NCO, (XII)
де значення Rа визначені в п. 11, з утворенням сполуки формули (ХІа) або (ХІb), де R означає групу –CONHRа; або
g.3) з відповідним аміном формули (XIII) у присутності трифосгену або придатного хлорформіату
HNRaRb , (XIII),
де значення Ra і Rb визначені в п. 11, з утворенням сполуки формули (ХІа) або (ХІb), де R означає групу -CONRaRb;
h) видалення захисту аміногрупи сполуки формули (ХІа) або (ХІb), одержаної за будь-якою зі стадій (g.1)-(g.3), з утворенням відповідного похідного формули (XIVa) або (XIVb)
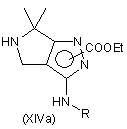 ,
,
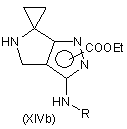 ,
,
де значення R вказані вище; і взаємодію сполук формули (XIVa) або (XIVb) відповідно до будь-якої з альтернативних стадій (і.1), (і.2), (і.3) або (і.4):
і.1) з похідним ацилгалогеніду формули (XV)
R1-COZ , (XV)
де значення R1 визначені в п. 11 в групах (а), (b), (с), (IIа), де Χ означає атом вуглецю, і (ІІb), і Ζ означає атом галогену, з утворенням сполуки формули (XVIa) або (XVIb)
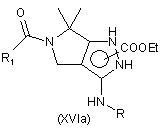 ,
,
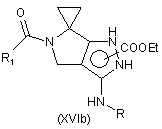 ,
,
де значення R і R1 вказані вище;
і.2) з (5-7)-членною гетероциклічною сполукою формули (XVII) або відповідним аміном формули (XVIII) у присутності трифосгену
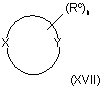 ,
,
![]() , (XVIII)
, (XVIII)
де X означає ΝΗ, і значення Υ, Rc, n, Rd і R’d визначені в п. 11, з утворенням відповідних сполук формули (XVIa) або (XVIb), де значення R визначені вище, і R1 означає або групу формули (IIа), де Х означає атом азоту, і значення R, Y, Rc і n визначені вище, або групу формули (IIc), де значення Rd і R’d визначені вище;
і.3) з карбоновою кислотою формули (XIX) у присутності відповідного конденсуючого агента
R1-COOH (XIX)
з утворенням сполуки формули (XVIa) або (XVIb), де значення R1 визначені вище у формулі (Іа) або (Іb) в групах (а), (b), (с), або означає групу формули (IIа),
де X означає атом вуглецю, або групу формули (ІІb), і значення R, Y, Rc і n визначені вище;
і.4) зі сполукою формули (XX)
R1-COZ, (XX)
де R1 означає групу формули (IId), і Ζ означає атом хлору або брому, з утворенням сполуки формули (XVIa) або (XVIb), де значення R визначені вище, і R1 означає групу формули (IId); і
j) взаємодію сполуки формули (XVIa) або (XVIb), одержаної відповідно до однієї зі стадій від (і.1) до (і.4), у присутності основи з утворенням відповідного похідного формули (Іа) або (Іb), де значення R і R1 визначені вище; і, необов’язково,
k) перетворення їх в інші сполуки формули (Іа) або (Іb), відповідно, і/або в їх фармацевтично прийнятні солі.
24. Спосіб за п. 23, де на стадії (b) Q означає трет-бутоксикарбонільну (bос) групу.
25. Спосіб за п. 23, де на стадії (с) Alk означає метил.
26. Сполуки формули (VIIa) або (VIIb)
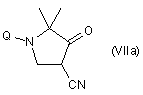 ,
,
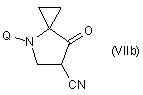 ,
,
де Q означає відповідну захисну азот групу, таку як трет-бутоксикарбонільна (bос) група.
27. Бібліотека, що включає дві або більше сполук формули (Іа)
 ,
,
де
R означає групу -CORa, -СОNHRa або -CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6-членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝΗ, О або S;
R1 вибирають з групи, що включає:
a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом;
b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом;
c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4-метилпіперазиніл)-метилфенільну групу;
d) групу формули (IIа) і (IIb):
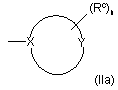 ,
,
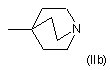 ,
,
де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4;
e) групу формули (IIс) і (IId):
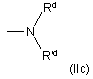 ,
,
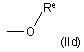 ,
,
де Rd, R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-СОNНСН3) групи;
за умови, що у формулі (Іа), коли R1 означає групу формули (IIc) і один із замісників Rd або R’d означає атом водню, в той час як інший з Rd або R’d означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3-бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4-фторфенілметильну, циклопропільну або 2-нафтилметильну групу;
або їх фармацевтично прийнятну сіль.
28. Бібліотека, що включає дві або більше сполук формули (Іb)

де
R означає групу -CORa, -CONHRa або -CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6-членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з N, NH, О або S;
R1 вибирають з групи, що включає:
a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом;
b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом;
c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4-метилпіперазиніл)-метилфенільну групу;
d) групу формули (IIа) і (ІІb):
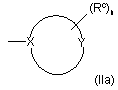 ,
,
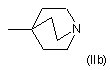 ,
,
де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4;
e) групу формули (IIc) і (IId):
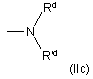
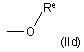 ,
,
де Rd, R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи;
або їх фармацевтично прийнятну сіль.
29. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки формули (Іа) або (Іb), яка визначена в п. 11, і принаймні один фармацевтично прийнятний ексципієнт, носій і/або розріджувач.
30. Фармацевтична композиція за п. 29, яка додатково містить один або декілька хіміотерапевтичних засобів.
31. Продукт або набір, що включає сполуку формули (Іа) або (Іb), яка визначена в п. 11, або її фармацевтичну композицію, яка визначена в п. 29, і один або декілька хіміотерапевтичних засобів як комбінований препарат для одночасного, роздільного або послідовного застосування у протираковій терапії.
32. Сполука формули (Іа) або (Іb), яка визначена в п. 11, для застосування як лікарського засобу.
33. Застосування сполуки формули (Іа) або (Іb), яка визначена в п. 11, для виготовлення лікарського засобу, що має протиракову активність.
Текст
1. Спосіб лікування захворювань, пов’язаних з проліферацією клітин, які викликані і/або пов’язані із зміненою кіназною активністю, що залежить від клітинного циклу, шляхом введення потребуючому лікування ссавцеві ефективної кількості сполуки, представленої формулою (Іа) і (Іb): H H N N N N R R NH NH C2 2 (13) 1 3 81790 Re Rd O N R'd (IId) , 4 контактування вказану кіназу з ефективною кількістю сполуки за п. 1. 11. Сполука, представлена формулою (Іа) і (Іb): (IIc) , де Rd, R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; за умови, що у формулі (Іа), коли R1 означає групу формули (IIc) і один із замісників Rd або R’d означає атом водню, в той час як інший з Rd або R’d означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4фторфенілметильну, циклопропільну або 2нафтилметильну групу; або її фармацевтично прийнятної солі. 2. Спосіб за п. 1, де захворювання, пов’язане з проліферацією клітин, вибирають з групи, що включає рак, хворобу Альцгеймера, вірусні інфекції, аутоімунні захворювання і нейродегенеративні розлади. 3. Спосіб за п. 2, де рак вибирають з групи, що включає карциному, карциному сквамозних клітин, гемопоетичні пухлини мієлоїдної або лімфоїдної клітинної лінії, пухлини мезенхімного походження, пухлини центральної і периферичної нервової системи, меланому, семіному, тератокарциному, остеосаркому, ксеродерму пігментну, кератоксантому, фолікулярний рак щитовидної залози і саркому Капоши. 4. Спосіб за п. 1, де захворювання, пов’язане з проліферацією клітин, вибирають з групи, що включає доброякісну гіперплазію передміхурової залози, сімейний аденоматозний поліпоз, неврофіброматоз, псоріаз, проліферацію гладких клітин судин, пов’язану з атеросклерозом, легеневим фіброзом, артритом, гломерулонефритом і післяхірургічним стенозом і рестенозом. 5. Спосіб за п. 1, який забезпечує придушення ангіогенезу і метастазу пухлин. 6. Спосіб за п. 1, який забезпечує терапію при відторгненні органів при трансплантації і лікування хвороби «хазяїн проти трансплантата». 7. Спосіб за п. 1, який забезпечує лікування і попередження облисіння, викликаного радіотерапією або хіміотерапією. 8. Спосіб за п. 1, який включає також призначення потребуючому лікування ссавцеві радіотерапевтичних і хіміотерапевтичних схем лікування у поєднанні з принаймні одним цитостатичним або цитотоксичним засобом. 9. Спосіб за п. 1, де потребуючим лікування ссавцем є людина. 10. Спосіб інгібування активності циклінзалежної кінази, в якому приводять у R H N N R NH H N N NH CH3 CH3 N O N O R1 , a a де R означає групу -COR , -CONHR або CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝΗ, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4(аміносульфоніл)фенільну, 4(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (ІІb): (Rc)n R1 (Ia) N X Y (IIb) (IIa) , , де у формулі (IIа) цикл означає (5-7)членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=О), (Ib) , 5 алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIc) і (IId): Rd Re 81790 6 метилпіперидил-4-ільної, 1-метилпіперазиніл-4ільної, 2-(R,S)-тетрагідрофураніл-2-ільної, 2-(R)тетрагідрофураніл-2-ільної або 2-(S)тетрагідрофураніл-2-ільної групи. 19. Сполука формули (Іа) або (Іb) за п. 11, де будь-яка з груп Ra, Rb і Rc, значення яких N O визначені в п. 11, необов’язково додатково (IId) , заміщені, за одним або декількома зі своїх вільних d R' положень, групами, незалежно вибраними з: (IIc) , галогену, нітрогрупи, оксогруп (=O), ціаногрупи, де Rd, R’d i Re, які можуть бути однаковими алкільної, поліфторалкільної, поліфторалкокси, або різними, незалежно один від одного алкенільної, алкінільної, гідроксіалкільної, означають атом водню або С1-С6алкільну групу з арильної, арилалкільної, гетероциклільної, прямим або розгалуженим ланцюгом, циклоалкільної, гідрокси, алкоксигрупи, необов’язково заміщену однією або декількома арилоксигрупи, гетероциклілоксигрупи, групами, вибраними з гідрокси (-ОН), метилендіоксигрупи, алкілкарбонілоксигрупи, амінокарбонільної (-CONH2) або арилкарбонілоксигрупи, циклоалкенілоксигрупи, метиламінокарбонільної (-CONHCH3) групи; алкіліденамінооксигрупи, карбокси, за умови, що у формулі (Іа), коли R1 алкоксикарбонільної, арилоксикарбонільної, d означає групу формули (IIc) і один із замісників R циклоалкілоксикарбонільної, аміногрупи, або R’d означає атом водню, в той час як інший з уреїдогрупи, алкіламіногрупи, діалкіламіногрупи, Rd або R’d означає етильну або н-бутильну групу, ариламіногрупи, діариламіногрупи, то R відрізняється від -CORa, де Ra означає 3форміламіногрупи, алкілкарбоніламіногрупи, бромфенільну, бензильну, 4-трет-бутилфенільну, арилкарбоніламіногрупи, 4-трет-бутилфенілметильну, 4гетероциклілкарбоніламіногрупи, фторфенілметильну, циклопропільну або 2алкоксикарбоніламіногрупи, алкоксііміногрупи, нафтилметильну групу; алкілсульфоніламіногрупи, або її фармацевтично прийнятна сіль. арилсульфоніламіногрупи, формільної, 12. Сполука формули (Іа) або (Іb) за п. 11, алкілкарбонільної, арилкарбонільної, де R означає групу -CORa, де значення Ra циклоалкілкарбонільної, гетероциклілкарбонільної, визначені в п. 11, і R1 означає трет-бутильну групу. амінокарбонільної, алкіламінокарбонільної, 13. Сполука формули (Іа) або (Іb) за п. 11, діалкіламінокарбонільної, алкілсульфонільної, де R означає групу -CONHRa, де значення Ra арилсульфонільної, аміносульфонільної, визначені в п. 11, і R1 означає трет-бутильну групу. алкіламіносульфонільної, 14. Сполука формули (Іа) або (Іb) за п. 11, діалкіламіносульфонільної, арилтіогрупи і де R означає групу -CONRaRb, де значення Ra і Rb алкілтіогрупи. визначені в п. 11, і R1 означає трет-бутильну групу. 20. Сполука формули (Іа) або (Іb) за п. 11, 15. Сполука формули (Іа) або (Іb) за п. 11, необов’язково у формі фармацевтично прийнятної де значення R визначені в п. 11, і R1 означає групу солі, вибрана з групи, що включає: формули (IIа), вибрану з N-{6,6-диметил-5-[(1-метилпіперидин-4(Rc)n (Rc)n іл)карбоніл]-2,4,5,6-тетрагідропіроло-[3,4с]піразол-3-іл}циклобутанкарбоксамід; N N NH N N Rc N-[5-(2,2-диметилпропаноїл)-6,6-диметил-1,4,5,6тетрагідропіроло[3,4-с]піразол-3-іл]-4, , , фторбензамід; c) (R n N-[5-(2,2-диметилпропаноїл)-2,4,5,6N тетрагідропіроло[3,4-с]піразол-6N N c спіроциклопропан-3-іл]-4-фторбензамід; , R , N-{6,6-диметил-5-[(2R)-тетрагідрофуран-2c ілкарбоніл]-1,4,5,6-тетрагідропіроло-[3,4-с]піразолде значення n і R визначені в п. 11. 3-іл}-4-фторбензамід; 16. Сполука формули (Іа) або (Іb) за п. 11, N-{6,6-диметил-5-[(2S)-тетрагідрофуран-2де значення R визначені в п. 11, i R1 означає групу ілкарбоніл]-1,4,5,6-тетрагідропіроло-[3,4-с]піразолформули (IIа), вибрану з 3-іл}-4-фторбензамід; O N-{6,6-диметил-5-[(1-метилпіперидин-4-ілNH N N Rc )карбоніл]-2,4,5,6-тетрагідропіроло-[3,4-с]піразол3-іл}-4-фторбензамід; , , , N-[5-[(1-метилпіперидин-4-іл)карбоніл]-2,4,5,6c де значення R визначені в п. 11. тетрагідропіроло[3,4-с]піразол-3-іл]-417. Сполука формули (Іа) за п. 11, де R фторбензамід; a a означає групу -COR , де R означає 4N-{6,6-диметил-5-[(4-метилпіперазин-1фторфенільну або циклобутильну групу, і іл)карбоніл]-2,4,5,6-тетрагідропіроло-[3,4значення R1 визначені в п. 11. с]піразол-3-іл}-4-фторбензамід; 18. Сполука формули (Іа) за п. 11, де значення R визначені в п. 11, і R1 означає групу, яку вибирають з трет-бутильної, 1 7 81790 N-[5-[(4-метилпіперазин-1-іл)карбоніл]-2,4,5,6тетрагідропіроло[3,4-с]піразол-6спіроциклопропан-3-іл]-4-фторбензамід; 4-хлор-N-{6,6-диметил-5-(4-піролідин-1ілметилпіперидин-1-карбоніл)-1,4,5,6тетрагідропіроло-[3,4-с]піразол-3-іл}бензамід. 21. Сполука формули (Іа) або (Іb) за п. 11, необов’язково у формі фармацевтично прийнятної солі, однозначно ідентифікована в таблицях III, IV, V і VI експериментальної частини опису. 22. Сполука А13-М1-В03 формули (Іа) за п. 11, де R означає групу -CORa, де Ra означає циклобутильну групу, і R1 означає групу формули (IIа), відповідну 1-метилпіперидил-4-ільній групі, як у вільній формі, так і у формі гідрохлоридної або мезилатної солі. 23. Спосіб одержання сполуки формули (Іа) або (Іb) за п. 11 або її фармацевтично прийнятної солі, в якому проводять: а) взаємодію сполуки формули (ІІІа) або (ІIIb) 8 e) взаємодію сполуки формули (VIIa) або (VIIb) з гідразингідратом з утворенням відповідного похідного формули (VIIIa) або (VIIIb) Q N COOH з акрилонітрилом з утворенням похідного формули (IVa) або (IVb) NC N H відповідного COOH (IVa) , b) захист аміногрупи сполуки формули (IVa) або (IVb) з утворенням відповідного похідного формули (Va) або (Vb) N Q COOH Q N N COOEt N (IIIb) NC N COOHAlk Q (VIa) , де Alk означає відповідну С1-С4алкільну групу; d) взаємодію сполуки формули (VIa) або (VIb) з гідридом натрію (NaH) з утворенням відповідного похідного формули (VIIa) або (VIIb) Q N O (VIIa) CN COOH , Q N NH2 (IXa) N (IXb) , і взаємодію сполук формули (IХа) або (ІХb) відповідно до однієї з альтернативних стадій (g.1), (g.2) або (g.3): NCg.1) зі сполукою формули (X) N COOH H RaCO-Z, (X) (IVb) де значення Ra визначені в п. 11, і Ζ ; означає атом галогену, з утворенням сполуки формули (ХІа) або (ХІb) NC N N N Q (Va) , де Q означає відповідну амінозахисну групу; c) взаємодію сполуки формули (Va) або (Vb) з відповідним алкілуючим агентом з утворенням відповідного похідного складного ефіру формули (VIa) або (VIb) N (VIIIb) , f) взаємодію сполуки формули (VIIIa) або (VIIIb) з етилхлорформіатом з утворенням відповідного похідного формули (IХа) або (ІХb), кожне з яких може бути в будь-якій з двох регіоізомерних форм Q NC NH2 (VIIIa) H 2N , N NH (IIIa) H2 N Q N HN (XIa) COOEt COOH N (Vb) N , R , де R означає групу -CORa; g.2) зі сполукою формули (XII) Ra-NCO, (XII) де значення Rа визначені в п. 11, з утворенням сполуки формули (ХІа) або (ХІb), де R а NCозначає групу –CONHR ; або N COOHAlk g.3) з відповідним аміном формули (XIII) у присутності Q трифосгену або придатного (VIb) , хлорформіату HNRaRb , (XIII), де значення Ra і Rb визначені в п. 11, з утворенням сполуки формули (ХІа) або (ХІb), де R означає групу -CONRaRb; h) видалення захисту аміногрупи сполуки формули (ХІа) або (ХІb), одержаної за будь-якою зі O Q стадій (g.1)-(g.3), з утворенням відповідного N (VIIb) похідного формули (XIVa) або (XIVb) CN Q ; HN (XIb) 9 HN N COOEt N HN R (XIVa) , де значення R вказані вище; і взаємодію сполук формули (XIVa) або (XIVb) відповідно до будь-якої з альтернативних стадій (і.1), (і.2), (і.3) або (і.4): і.1) з похідним ацилгалогеніду формули (XV) R1-COZ , (XV) де значення R1 визначені в п. 11 в групах (а), (b), (с), (IIа), де Χ означає атом вуглецю, і (ІІb), і Ζ означає атом галогену, з утворенням сполуки формули (XVIa) або (XVIb) O H N N COOEt NH R1 HN R (XVIa) , де значення R і R1 вказані вище; і.2) з (5-7)-членною гетероциклічною сполукою формули (XVII) або відповідним аміном формули (XVIII) у присутності трифосгену (Rc)n X Y (XVII) , де X означає ΝΗ, і значення Υ, Rc, n, Rd і R’d визначені в п. 11, з утворенням відповідних сполук формули (XVIa) або (XVIb), де значення R визначені вище, і R1 означає або групу формули (IIа), де Х означає атом азоту, і значення R, Y, Rc і n визначені вище, або групу формули (IIc), де значення Rd і R’d визначені вище; і.3) з карбоновою кислотою формули (XIX) у присутності відповідного конденсуючого агента R1-COOH (XIX) з утворенням сполуки формули (XVIa) або (XVIb), де значення R1 визначені вище у формулі (Іа) або (Іb) в групах (а), (b), (с), або означає групу формули (IIа), де X означає атом вуглецю, або групу формули (ІІb), і значення R, Y, Rc і n визначені вище; і.4) зі сполукою формули (XX) R1-COZ, (XX) де R1 означає групу формули (IId), і Ζ означає атом хлору або брому, з утворенням сполуки формули (XVIa) або (XVIb), де значення R визначені вище, і R1 означає групу формули (IId); і j) взаємодію сполуки формули (XVIa) або (XVIb), одержаної відповідно до однієї зі стадій від 81790 10 (і.1) до (і.4), у присутності основи з утворенням відповідного похідного формули (Іа) або (Іb), де значення R і R1 визначені вище; і, необов’язково, HN N k) COOEt перетворення їх в інші сполуки формули (Іа) або (Іb), відповідно, і/або в їх N фармацевтично прийнятні солі. 24. Спосіб за п. 23, де на стадії (b) Q H трет-бутоксикарбонільну (bос) групу. означаєN Спосіб за п. 23, де на стадії (с) Alk (XIVb) 25. R , означає метил. 26. Сполуки формули (VIIa) або (VIIb) Q O N Q (VIIa) CN , де Q означає відповідну захисну азот групу, таку як трет-бутоксикарбонільна (bос) група. O 27. Бібліотека, що включає дві або більше сполук формулиH (Іа) H N N COOEt N R1 R N NHNH HN CH3 R (XVIb) CH3 N , O (Ia) R1 , де HN(Rd)R'd , R означає групу -CORa, -СОNHRa або (XVIII) CONRaRb, де Ra і Rb кожний незалежно означає водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝΗ, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6дифторфенільну, 4-(аміносульфоніл)фенільну, 4(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (IIb): N CN 11 81790 (Rc)n X Y (IIa) , де у формулі (IIа) цикл означає (5-7)членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIс) і (IId): Rd 12 R означає групу -CORa, -CONHRa або CONRaRb, де Ra і Rb кожний незалежно означає N водень або необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, (IIb) ,3-С6циклоалкільної, С арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов’язково заміщений 5- або 6членний гетероцикл, що необов’язково містить один додатковий гетероатом або гетероатомну групу, вибрану з N, NH, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6дифторфенільну, 4-(аміносульфоніл)фенільну, 4(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (ІІb): (Rc)n Re O X N R'd (IIc) , де R , R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-СОNНСН3) групи; за умови, що у формулі (Іа), коли R1 означає групу формули (IIc) і один із замісників Rd або R’d означає атом водню, в той час як інший з Rd або R’d означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4фторфенілметильну, циклопропільну або 2нафтилметильну групу; або їх фармацевтично прийнятну сіль. 28. Бібліотека, що включає дві або більше сполук формули (Іb) H N N R NH d (IId) O де R1 , (Ib) , (IIa) , де у формулі (IIа) цикл означає (5-7)членне гетероциклічне кільце, в якому X, безпосередньо зв’язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝΗ, за умови, що принаймні один з Χ і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов’язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIc) і (IId): Rd Re O N R'd N N Y (IIc) де Rd, R’d і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов’язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), (IId) 13 81790 14 амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; або їх фармацевтично прийнятну сіль. 29. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки формули (Іа) або (Іb), яка визначена в п. 11, і принаймні один фармацевтично прийнятний ексципієнт, носій і/або розріджувач. 30. Фармацевтична композиція за п. 29, яка додатково містить один або декілька хіміотерапевтичних засобів. 31. Продукт або набір, що включає сполуку формули (Іа) або (Іb), яка визначена в п. 11, або її фармацевтичну композицію, яка визначена в п. 29, і один або декілька хіміотерапевтичних засобів як комбінований препарат для одночасного, роздільного або послідовного застосування у протираковій терапії. 32. Сполука формули (Іа) або (Іb), яка визначена в п. 11, для застосування як лікарського засобу. 33. Застосування сполуки формули (Іа) або (Іb), яка визначена в п. 11, для виготовлення лікарського засобу, що має протиракову активність. Даний винахід відноситься до піролопіразольних похідних, до способу їх одержання, до фармацевтичних композицій, які містять їх, і до їх застосування як терапевтичних засобів, зокрема, при лікуванні раку і захворювань, пов'язаних з проліферацією клітин. Деякі цитотоксичні ліки, такі як, наприклад, фторурацил (5-FU), доксорубіцин і камптотецини, ушкоджують ДНК або впливають на метаболічний шлях обміну речовин в клітинах і тим самим, в багатьох випадках, спричиняють посереднє гальмування клітинного циклу. Оскільки вони викликають безповоротне пошкодження як нормальних, так і пухлинних клітин, то вказані агенти приводять до значної токсичності і побічних ефектів. У зв'язку з цим необхідні сполуки, здатні виконувати функції високо специфічних протипухлинних засобів, які можуть спричиняти селективне пригноблення і апоптоз пухлинних клітин і при цьому володіють порівнянною ефективністю і меншою токсичністю, у порівнянні з доступними в цей час ліками. Добре відомо, що розвиток клітинного циклу керується серією контрольних точок, інакше названих точками рестрикції, які регулюються сімейством ферментів, відомих як циклінзалежні кінази (Cdk). У свою чергу, самі Cdk регулюються на багатьох рівнях, наприклад, за рахунок зв'язування з циклінами. Координована активація та інактивація різних комплексів Cdk/Cyclin необхідна для нормального розвитку клітинного циклу. Обидва критичних переходи G1-S і G2-M контролюються активацією різної активності Cdk/Cyclin. Вважають, що в G1 початок S-фази опосередковується як Cdk4/Cyclin D, так і Cdk2/Cyclin Ε. Подальший розвиток S-фази вимагає активності Cdk2/Cyclin А, в той час як для початку мітозу необхідна активація Cdc2/Cyclin A (Cdkl) і Cdc2/Cyclin В. Загальне посилання на цикліни і циклінзалежні кінази див., [наприклад, у Kevin R., в Webster et al., Exp. Opin. Invest. Drugs, 1998, Vol.7(6), 865-887]. Контрольні точки в пухлинних клітинах дефектні частково внаслідок розрегулювання активності cdk. Наприклад, в пухлинних клітинах спостерігалась змінена експресія Сусlіn Ε і різні cdk, і було показано, що делеція гена р27 КІР інгібітору cdk у мишей приводить до більш частої захворюваності раком. Все більше підтвердження знаходить уявлення про те, що cdk є ферментами, які обмежують швидкість розвитку клітинного циклу і, таким чином, вони являють собою молекулярні цілі для терапевтичного впливу. Зокрема, пряме інгібування активності cdk/Cyclin кіназ повинно виявитись корисним при обмеженні нерегульованої проліферації пухлинних клітин. Об'єктом винаходу є сполуки, які застосовні при лікуванні клітинних проліферативних захворювань, які викликані і/або пов'язані зі зміненою кіназною активністю, що залежить від клітинного циклу. Іншим об'єктом винаходу є сполуки, які володіють інгібуючою активністю по відношенню до cdk/Cyclin кінази. Автори даного винаходу виявили, що деякі піразольні сполуки володіють інгібуючою активністю по відношенню до cdk/Cyclin кінази і, таким чином, застосовні в терапії як протипухлинні засоби, при цьому у них відсутні, з точки зору, як токсичності, так і побічних ефектів, вищезгадані недоліки, які властиві наявним в наш час протипухлинним лікам. Зокрема, піразольні похідні за даним винаходом застосовні при лікуванні різних ракових захворювань, включаючи, але, не обмежуючись цим, карциному, таку як карцинома сечового міхура, грудей, товстої кишки, нирки, печінки, легені, включаючи дрібноклітинний рак легені, рак стравоходу, жовчного міхура, яєчника, підшлункової залози, шлунку, шиї, щитовидної залози, передміхурової залози і шкіри, включаючи карциному сквамозних клітин; гемопоетичні пухлини лімфоїдної клітинної лінії, включаючи лейкемію, гостру лімфоцитарну лейкемію, гостру лімфобластну лейкемію, лімфому В-клітин, лімфому Т-клітин, лімфому Ходжкіна, лімфому, яка відрізняється від лімфоми Ходжкіна, лімфому ворсистих клітин і лімфому Буркета; гемопоетичні пухлини мієлоїдної клітинної лінії, включаючи гостру і хронічну мієлогенні лейкемії, мієлодиспластичний синдром і промієлоцитарну лейкемію; пухлини мезенхімного походження, включаючи фібросаркому і рабдоміосаркому; пухлини центральної і периферичної нервової системи, включаючи астроцитому, нейробластому, 15 гліому і невриному; інші пухлини, включаючи меланому, семиному, тератокарциному, остеосаркому, ксеродерму пігментну, кератоксантому, фолікулярний рак щитовидної залози і саркому Капоши. Завдяки ключовій ролі, які cdk грають в регулюванні проліферації клітин, вказані піразольні похідні корисні також при лікуванні різних захворювань, викликаних проліферацією клітин, таких як, -наприклад, доброякісна гіперплазія передміхурової залози, сімейний аденоматозний поліпоз, неврофіброматоз, псоріаз, проліферація гладких клітин судин, пов'язана з атеросклерозом, легеневим фіброзом, артритом, гломерулонефритом і післяопераційним стенозом і рестенозом. Сполуки за даним винаходом можуть бути корисні при лікуванні хвороби Альцгеймера, що підтверджується тим фактом, що cdk5 бере участь у фосфорилюванні тау-білка [J. Biochem. 117, 741749, 1995]. Як модулятори апоптозу сполуки за даним винаходом можуть бути також застосовані при лікуванні раку, вірусних інфекцій, для запобігання розвитку синдрому набутого імунодефіциту (СНІД) у ВІЛ-інфікованих індивідів, при лікуванні аутоімунних захворювань і нейродегенеративних розладів. Сполуки за даним винаходом можуть бути застосовані для придушення ангіогенезу і метастазу пухлин, а також для терапії при відторгненні органів при трансплантації і лікування хвороби «хазяїн проти трансплантату». Сполуки за даним винаходом можуть також діяти як інгібітори інших протеїнкіназ, зокрема, протеїнкінази С в різних ізоформах, Met, РАК-4, РАК-5, ZC-1, STLK-2, DDR-2, Aurora 1, Aurora 2, Bub-1, PLK, Chkl, Chk2, HER2, rail, MEK1, МАРК, EGF-R, PDGF-R, FGF-R, IGF-R, PI3K, weel-кінази, Src, Abl, Akt, МАРК, ILK, MK-2, IKK-2, Cdc7, Nek; і, таким чином, ефективні при лікуванні захворювань, пов'язаних з іншими протеїнкіназами. Сполуки за даним винаходом можуть бути також застосовані для лікування і попередження облисіння, що викликається радіотерапією або хіміотерапією. Таким чином, в даному винаході пропонується спосіб лікування захворювань, пов'язаних з проліферацією клітин, які викликані і/або пов'язані зі зміненою кіназною активністю, що залежить від клітинного циклу, шляхом введення потребуючому цього ссавцеві ефективної кількості похідного піразолу, представленого формулами (Іа) і (Іb): де R означає групу -CORa, -CONHR3 або CONRaRb, де Ra і Rb кожний незалежно означає 81790 16 водень або необов'язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов'язково заміщений 5- або 6членний гетероцикл, що необов'язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝN, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (llа) і (llb): де у формулі (llа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо пов'язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝN, за умови, що, принаймні, один з X і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов'язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIс) і (IId): де Rd, R'd і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов'язково заміщену однією або декількома групами, вибраними з гідрокси (-OН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; за умови, що у формулі (Іа), коли R1 означає групу формули (IIс) і один із замісників Rd або R'd означає атом водню, в той час як інший з Rd або 17 R'd означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4фторфенілметильну, циклопропільну або 2нафтилметильну групу; або його фармацевтично прийнятної солі. У переважному варіанті здійснення вищезгаданого способу захворювання, пов'язане з проліферацією клітин, вибирають з раку, хвороби Альцгеймера, вірусних інфекцій, аутоімунних захворювань і нейродегенеративних розладів. Конкретні типи раку, які можна лікувати, включають карциному, карциному сквамозних клітин, гемопоетичні пухлини мієлоїдної або лімфоїдної клітинної лінії, пухлини мезенхімного походження, пухлини центральної або периферичної нервової системи, меланому, семиному, тератокарциному, остеосаркому, ксеродерму пігментну, кератоксантому, фолікулярний рак щитовидної залози і саркому Капоши. В іншому переважному варіанті здійснення вказаного вище способу захворювання, пов'язане з проліферацією клітин, вибирають з групи, що включає доброякісну гіперплазію передміхурової залози, сімейний аденоматозний поліпоз, неврофіброматоз, псоріаз, проліферацію гладких клітин судин, пов'язану з атеросклерозом, легеневим фіброзом, артритом, гломерулонефритом і післяхірургічним стенозом і рестенозом. Крім того, спосіб за даним винаходом забезпечує придушення ангіогенезу і метастазу пухлин, а також терапію при відторгненні органів при трансплантації і лікування «хазяїн проти трансплантату». Спосіб за даним винаходом може також забезпечити придушення клітинного циклу або залежне від cdk/Cyclin інгібування. Крім вищевикладеного, спосіб, що є об'єктом даного винаходу, забезпечує лікування і попередження облисіння, викликаного радіотерапією або хіміотерапією. В даному винаході пропонується також похідне піразолу, представлене формулою (Іа) або (Іb): де R означає групу -CORa, -CONHRa або CONRaRb, де Ra і Rb кожний незалежно означає водень або необов'язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов'язково заміщений 5- або 6членний гетероцикл, що необов'язково містить 81790 18 один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝN, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-С4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (llb): де, у формулі (IIа) цикл означає 5-7 членне гетероциклічне кільце, в якому X, безпосередньо пов'язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝN, за умови, що, принаймні, один з X і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов'язково заміщену групу, вибрану з С1-C6алкільної групи з прямим або розгалуженим ланцюгом, С3С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=О), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIс) і (IId): де Rd, R'd і Re, які можуть однаковими або різними, незалежно один від одного означають атом водню або С1-С6алкільну групу з прямим або розгалуженим ланцюгом, необов'язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; за умови, що у формулі (Іа), коли R1 означає групу формули (IIс) і один із замісників Rd або R'd означає атом водню, в той час як інший з Rd або R'd означає етильну або н-бутильну групу, то R відрізняється від -CORa, і Ra означає 3бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4фторфенілметильну, циклопропільну або 2нафтилметильну групу; або його фармацевтично прийнятна сіль. Даний винахід включає також способи синтезу похідних піразолу, представлених формулами (Іа) 19 або (lb), які, якщо не вказане інше, можуть бути для зручності об'єднані в одну групу і позначені як сполуки формули (І). Фармацевтичні композиції, що містять похідні піразолу формули (І), також включені в даний винахід. Більш повне розуміння даного винаходу і багатьох супутніх йому переваг можна одержати після того, як викладене стане більш зрозумілим завдяки наведеному нижче докладному опису винаходу. В даній галузі відомо декілька гетероциклічних сполук, які є інгібіторами протеїнкінази. Наприклад, 2-карбоксамідопіразоли і 2уреїдопіразоли і їх похідні розкриті як інгібітори протеїнкінази [в публікаціях міжнародних патентних заявок WO 01/12189, WO 01/12188, WO 02/48114 і WO 02/70515], всі подані від імені заявника даної заявки. Конденсовані біциклічні сполуки, що включають паразольні фрагменти і володіють інгібуючою активністю по відношенню до кіназ, розкриті також у [WO 00/69846 і WO 02/12242, а також в WO 03/028720 (РСТ/ЕР02/10534, яка запитує пріоритет згідно із заявкою на патент США №09/962162 від 26 вересня 2001р.) і одночасно поданій заявці РСТ/ЕРОЗ/04862 (яка запитує пріоритет згідно із заявкою на патент США 60/381092 від 17 травня 2002p.)], всі подані від імені заявника даної заявки. Сполуки, які є об'єктом даного винаходу, підпадають під загальну формулу вищезгаданої [заявки WO 02/12242], яка включена в даний опис за допомогою посилання, однак спеціально в ній не описані. Якщо не вказане інше, то при посиланні на самі сполуки формули (І), а також на будь-які їх фармацевтичні композиції або на будь-яку терапію з їх застосуванням, даний винахід включає все можливі гідрати, сольвати, комплекси, метаболіти і проліки сполук за даним винаходом. Проліками є будь-які ковалентно пов'язані сполуки, які in vivo вивільняють активні вихідні ліки, відповідні формулі (І)· Метаболітом сполуки формули (І) є будь-яка сполука, в яку in vivo перетворюється ця ж сама сполука (І), наприклад, після введення потребуючому цього ссавцеві. Як правило, що не є обмежувальним даний винахід прикладом, при введенні сполуки формули (І) це ж саме похідне може перетворюватись в різні сполуки, наприклад, ті, що включають більш розчинні похідні, такі як гідроксильовані похідні, які легше виводяться з організму. Таким чином, в залежності від подальшого метаболічного шляху, будь-яке з вказаних гідроксильованих похідних можуть розглядатись як метаболіти сполук формули (І). Якщо у сполуці за даним винаходом присутній хіральний центр або інший тип центра ізомерії, то передбачається, що даний винахід охоплює всі форми подібного ізомеру або ізомерів, включаючи енантіомери і діастереомери. Сполуки, що містять хіральний центр, можуть бути використані у вигляді рацемічної суміші, енантіомерно збагаченої суміші, або ж рацемічна суміш може 81790 20 бути розділена за допомогою добре відомих методів, та індивідуальні енантіомери можуть бути використані самостійно. У тих випадках, коли сполуки мають ненасичені вуглець-вуглецеві подвійні зв'язки, в об'єм даного винаходу входять як цис-ізомери (Z), так і транс-ізомери (Е). У тих випадках, коли сполуки можуть існувати в таутомерних формах, таких як кето-енольні таутомери, то передбачається, що кожна таутомерна форма входить в об'єм даного винаходу незалежно від того, чи існує вона у рівноважній формі або, переважно, в одній формі. В даному винаході, якщо не вказане інше, під терміном С1-С6алкільна група з прямим або розгалуженим ланцюгом, який тим самим включає і С1-C4алкільну групу, мають на увазі будь-які групи, такі як, наприклад, метильна, етильна, нпропільна, ізопропільна, н-бутильна, ізобутильна, трет-бутильна, втор-бутильна, н-пентильна, нгексильна група і т.д. Під терміном С3-С6циклоалкільна група, якщо не вказане інше, мають на увазі циклоаліфатичне кільце, таке як циклопропільна, циклобутильна, циклопентильна або циклогексильна група. Термін арильна група включає карбоциклічні або гетероциклічні вуглеводні, що містять від 1 до 2 кільцевих фрагментів, як конденсованих, так і пов'язаних один з одним простими зв'язками, в яких, щонайменше, одне з кілець є ароматичним; якщо він присутній, то будь-який ароматичний гетероциклічний вуглеводень, який називають також гетероарильною групою, включає 5- або 6членне кільце, що містить 1-3 гетероатоми абo гетероатомних груп, вибраних з N, NH, О або S. Прикладами арильних груп відповідно до даного винаходу є, наприклад, фенільна, біфенільна, αабо β-нафтильна, дигідронафтильна, тієнільна, бензотієнільна, фурильна, бензофуранільна, піролільна, імідазолільна, піразолільна, тіазолільна, ізотіазолільна, оксазолільна, ізоксазолільна, піридильна, піразинільна, піримідинільна, піридазинільна, індолільна, ізоіндолільна, пуринільна, хінолільна, ізохінолільна, дигідрохінолінільна, хіноксалінільна, бензодіоксолільна, інданільна, інденільна, триазолільна група і т.д. Якщо не вказане інше, термін гетероцикл або гетероциклічна група включає 5-або 6-членні насичені, частково ненасичені або повністю ненасичені гетероцикли, що містять 1-3 гетероатоми або гетероатомних груп, вибраних з N, NH, О або S. Крім повністю ненасичених гетероциклів, позначених вище як ароматичні гетероцикли і які охоплюються терміном арильна група, прикладами насичених або частково ненасичених гетероциклів, відповідно до даного винаходу, є, наприклад, піран, піролідин, піролін, імідазолін, імідазолідин, піразолідин, піразолін, тіазолін, тіазолідин, дигідрофуран, тетрагідрофуран, 1,3діоксолан, піперидин, піперазин, морфолін і т.п. У тому випадку, коли посилаються на сполуки за даним винаходом, де значення R1 наведено в групі (b), сам замісник R1 може являти собою 21 вказану циклоалкільну групу, наприклад, циклопропільну групу; вказану циклоалкілалкільну групу, наприклад, циклопропілметильну групу; або навіть вказану алкілциклоалкільну групу, наприклад, метилциклопропільну групу; всі вони мають наступні формули: У тому випадку, коли посилаються на сполуки за даним винаходом, де R1 є групою формули (IIа), (5-7)-членне гетероциклічне кільце безпосередньо приєднане до залишку молекули за допомогою атома X, як вказано нижче: Приклади цих (5-7)-членних гетероциклов включають (5-6)-членні гетероцикли, які вказані вище, і додатково 7-членні гетероцикли, такі як, наприклад, азепін, діазепін, оксазепін і т.п. Будь-яка група Rc, якщо вона присутня, може знаходитись в будь-якому з вільних положень гетероциклічного кільця у формулі (IIа) за рахунок заміщення атома водню. У тому випадку, коли посилаються на сполуки за даним винаходом, де Ri є групою формули (IIс) або (IId), то таким чином можуть бути позначені уреїдопохїдні і карбамати, що мають наступні підформули: Згідно з даним винаходом і якщо не вказано інше, будь-які з вказаних вище груп Ra, Rb і Rc необов'язково можуть бути заміщені, за будь-яким зі своїх вільних положень, однією або декількома групами, наприклад 1-6 групами, незалежно вибраними з: галогену, нітрогрупи, оксогрупи (=O), ціаногрупи, алкільної, поліфторалкільної, поліфторалкокси, алкенільної, алкінільної, гідроксіалкільної, арильної, арилалкільної, гетероциклільної, циклоалкільної, гідрокси, алкоксигрупи, арилоксигрупи, гетероциклілоксигрупи, метилендіоксигрупи, алкілкарбонілоксигрупи, арилкарбонілоксигрупи, циклоалкенілоксигрупи, алкіліденамінооксигрупи, карбокси, алкоксикарбонільної, арилоксикарбонільної, циклоалкілоксикарбонільної, аміногрупи, уреїдогрупи, алкіламіногрупи, діалкіламіногрупи, ариламіногрупи, діариламіногрупи, форміламіногрупи, алкілкарбоніламіногрупи, 81790 22 арилкарбоніламіногрупи, гетероциклілкарбоніл аміногрупи, алкоксикарбоніламіногрупи, алкоксііміногрупи, алкілсульфоніламіногрупи, арилсульфоніламіногрупи, формільної, алкілкарбонільної, арилкарбонільної, циклоалкілкарбонільної, гетероциклілкарбонільної, амінокарбонільної, алкіламінокарбонільної, діалкіламінокарбонільної, алкілсульфонільної, арилсульфонільної, аміносульфонільної, алкіламіносульфонільної, діалкіламіносульфонільної, арилтіогрупи і алкілтіогрупи. Відповідно до цього під терміном галоген мають на увазі атом фтору, хлору, брому або йоду. Під терміном алкенільна або алкінільна група мають на увазі будь-яку з вказаних вище С2С6алкільних груп з прямим або розгалуженим ланцюгом, які додатково містять подвійний або потрійний зв'язок. Не обмежувальними даний винахід прикладами алкенільних або алкінільних груп є, наприклад, вінільна, алільна, 1пропенільна, ізопропенільна, 1-бутенільна, 2бутенільна, 3-бутенільна, 2-пентенільна, 1гексенільна, етинільна, 2-пропінільна, 4пентинільна група і т.п. Під терміном поліфторалкільна або поліфторалкоксигрупа мають на увазі будь-яку з вказаних вище С1-C6алкільних або алкоксигруп, які заміщені більше ніж одним атомом фтору, такі як, наприклад, трифторметильна, трифторетильна, 1,1,1,3,3,3-гексафторпропільна, трифторметоксигрупа і т.п. Під терміном алкоксигрупа, арилоксигрупа, гетероциклілоксигрупа і їх похідні мають на увазі будь-які вказані вище алкільні, арильні або гетероциклічні групи, приєднані до іншої молекули через атом кисню (-О-). З викладеного вище для фахівця ясно, що будь-яку групу, яка має складову назву, таку як, наприклад, циклоалкілалкільна, арилалкільна, гетероциклілалкільна, алкоксигрупа, алкілтіогрупа, арилоксигрупа, арилалкілоксигрупа, алкілкарбонілоксигрупа, арилалкільна, гетероциклілалкільна група і т.п., потрібно звичайно розглядати виходячи з частин, з яких вони складені. Як приклад, така група як гетероциклілалкілоксигрупа являє собою алкоксигрупу, зокрема, алкілоксигрупу, в якій алкільний фрагмент додатково заміщений гетероциклільною групою, де значення алкільної і гетероциклільної групи вказані вище. Фармацевтично прийнятні солі сполук формули (І) включають кислотно-адитивні солі з неорганічними або органічними кислотами, наприклад, азотною, хлористоводневою, бромистоводневою, сірчаною, перхлорною, фосфорною, оцтовою, трифтороцтовою, пропіоновою, гліколевою, молочною, щавлевою, малоновою, яблучною, малеїновою, винною, лимонною, бензойною, коричною, мигдалевою, метансульфоновою, ізетіоновою і саліциловою кислотою. Кислотно-адитивні солі сполук за даним винаходом переважно вибирають з гідрохлоридів і мезилатів. 23 Фармацевтично прийнятні солі сполук формули (І) включають також солі з неорганічними або органічними основами, наприклад, солі з лужними або лужноземельними металами, зокрема, з гідроксидами натрію, калію, кальцію і магнію, карбонатами або бікарбонатами, ациклічними або циклічними амінами, переважне метиламіном, етиламіном, діетиламіном, триетиламіном, піперидином і т.п. Перший клас переважних сполук формули (Іа) або (lb) представлений похідними, в яких R означає групу -CORa, де значення Ra вказані вище, і R1 означає трет-бутильну групу. Інший клас переважних сполук формули (Іа) або (lb) представлений похідними, в яких R означає групу -CONHRa, де значення Ra вказані вище, і R1 означає трет-бутильну групу. Ще один клас переважних сполук формули (Іа) або (lb) представлений похідними, в яких R означає групу -CONRaRb, де значення Ra і Rb вказані вище, і R1 означає трет-бутильну групу. Інший клас переважних сполук формули (Іа) або (lb) представлений похідними, в яких значення R вказані вище, і R1 означає групу формули (IIа), вибрану з де значення Rc вказані вище. Ще один клас переважних сполук формули (Іа) або (lb) представлений похідними, в яких значення R вказані вище, і R1 означає групу формули (IIа), вибрану з де значення n і Rc вказані вище. З вказаних вище класів сполук найбільш переважними є сполуки формули (Іа), де R означає групу -CORa, де Ra означає 4фторфенільну або циклобутильну групу, і Ri має значення, наведені в загальній формулі. Крім того, найбільш переважними є сполуки формули (Іа), де R має значення, наведені в загальній формулі, і R1 вибирають з третбутильної, 1-метилпиперидил-4-ільної, 1метилпіперазиніл-4-ільної, 2-(R,S)тетрагідрофураніл-2-ільної, 2-(R)тетрагідрофураніл-2-ільної або 2-(S)тетрагідрофураніл-2-ільної групи. Загальні посилання на які-небудь конкретні сполуки формули (І) за даним винаходом, необов'язково у формі фармацевтично прийнятної солі, наведені в експериментальному розділі опису. Як указано вище, ще одним об'єктом даного винаходу є спосіб одержання сполук формули (І). Відповідно до цього, сполуки формули (І) і їх фармацевтично прийнятні солі * можуть бути одержані за способом, який включає: а) взаємодію сполуки формули (lllа) або (lllb) 81790 24 з акрилонітрилом з утворенням відповідного похідного формули (IVa) або (IVb) b) захист аміногрупи сполуки формули (IVa) або (IVb) з утворенням відповідного похідного формули (Va) або (Vb) де Q означає відповідну амінозахисну групу; c) взаємодію сполуки формули (Va) або (Vb) з відповідним алкілуючим агентом з утворенням відповідного складного ефіру формули (Vla) або (VIb) де Alk означає відповідну С1-С4алкільну групу; d) взаємодію сполуки формули (Vla) або (VIb) з гідридом натрію (NaH) з утворенням відповідного похідного формули (Vlla) або (Vllb) e) взаємодію сполуки формули (Vlla) або (Vllb) з гідразингідратом з утворенням відповідного похідного формули (Vllla) або (VlIIb) f) взаємодію сполуки формули (Vllla) або (Vlllb) з етилхлорформіатом з утворенням відповідногопохідного формули (ІХа), або (ІХb), кожне з яких може бути в будь-якій з двох регіоізомерних форм і взаємодію сполук формули (ІХа) або (ІХb) за однією з альтернативних стадій (g.l), (g.2) або (g.3) g.l) зі сполукою формули (X) де значення Ra вказані вище, і Ζ означає атом галогену, з утворенням сполуки формули (ХІа) або (ХІb) 25 де R означає групу -CORa; g.2) зі сполукою формули (XII) де значення Ra вказані вище, з утворенням сполуки формули (ХІа) або (ХІb), де R означає групу -CONHRa; або g.3) з відповідним аміном формули (XIII) у присутності трифосгену або придатного хлор форміату де значення Ra і Rb вказані вище, з утворенням сполуки формули (ХІа) або (ХІb), де R означає групу -CONRaRb; h) видалення захисту аміногрупи сполуки формули (ХІа) або (ХІb), одержаної за будь-якою зі стадій з (g.l) no (g.3), з утворенням відповідного похідного формули (XlVa) або (XlVb) де значення R вказані вище; і взаємодію сполук формули (XlVa) або (XlVb) за будь-якою з альтернативних стадій (і.1), (і.2), (і.3) або (і.4) і.1) з похідним ацилгалогеніду формули (XV) де значення R1 вказані вище у формулі (Іа) або (lb) під групами (а), (b), (с), (IIа), де X означає атом вуглецю, і (llb), і Ζ означає атом галогену, з утворенням сполуки формули (XVIa) або (XVIb) де значення R і R1 вказані вище; і.2) з (5-7)-членною гетероциклічною сполукою формули (XVII) або відповідним аміном формули (XVIII) у присутності трифосгену де X означає NH, і Y, Rc, n, Rd і R'd мають вказане вище значення, з утворенням відповідних сполук формули (XVIa) або (XVIb), де значення R вказані вище, і R1 означає або групу формули (IIа), де X означає атом азоту, і значення R, Y, Rc і n вказані вище, або групу формули (IIс), де значення Rd і R'd вказані вище; і.3) з карбоновою кислотою формули (XIX) у присутності відповідного конденсуючого агента 81790 26 з утворенням сполуки формули (XVIa) або (XVIb), де значення R1 вказані вище у формулі (Іа) або (lb) під групами (а), (b), (с), або означає групу формули (IIа), де X означає атом вуглецю, або групу формули (llb), і значення R, Y, Rc і n вказані вище; і.4) зі сполукою формули (XX) де R1 означає групу формули (IId), і Ζ означає атом хлору або брому, з утворенням сполуки формули (XVIa) або (XVIb), де значення R вказані вище, і R1 означає групу формули (IId); і j) взаємодію сполуки формули (XVIa) або (XVIb), одержаної відповідно до однієї зі стадій (і.1)-(і.4), у присутності основи з утворенням відповідного похідного формули (Іа) або (lb), де значення R і R1 вказані вище; і, необов'язково, k) перетворення їх в інші сполуки формули (Іа) або (lb), відповідно, і/або в їх фармацевтично прийнятні солі. Наведений вище спосіб являє собою аналог, який можна здійснити з використанням методів, добре відомих в даній галузі. З викладеного вище для фахівця повинно бути ясним, що якщо сполука формули (Іа) або (lb), одержана за наведеним вище способом, одержана у вигляді суміші ізомерів, то їх розділення на індивідуальні ізомери формули (Іа) або (lb), яке проводять з використанням звичайних методів, входить в об'єм даного винаходу. Аналогічно, перетворення відповідної солі сполуки формули (Іа) або (lb) у вільну сполуку формули (Іа) або (lb), також входить в об'єм даного винаходу. Згідно зі стадією (а) даного способу, сполуки формули (lllа) або (lllb) піддають взаємодії з акрилонітрилом у присутності відповідної основи, наприклад, гідроксиду натрію. Реакцію переважно проводять у воді при температурі в інтервалі від приблизно -10°С до кімнатної температури. Згідно зі стадією (b) даного способу, аміногрупу сполуки (IVa) або (IVb) захищають, використовуючи звичайні методи, наприклад, за допомогою ангідриду трет-бутоксикарбонілу (Вос2О), і у присутності відповідного розчинника, такого як ацетонітрил або дихлорметан, з одержанням відповідного похідного формули (Va) або (Vb), де амінозахисна група Q означає третбутоксикарбонільну групу (bос). Згідно зі стадією (с) даного способу, карбоксильну групу формули (Va) або (Vb) перетворюють у відповідний алкіловий складний ефір, наприклад, у присутності відповідного алкілгалогеніду, наприклад, метилйодиду. Реакцію проводять у присутності відповідного розчинника, такого як диметилформамід, і у присутності основи, наприклад, при використанні бікарбонату натрію або калію. Згідно зі стадією (d) даного способу, сполуку формули (Vla) або (VIb) перетворюють у відповідне циклічне похідне формули (Vlla) або (Vllb) за реакцією з гідридом натрію. Реакцію проводять у присутності відповідного розчинника, такого як діоксан або тетрагідрофуран при його температурі дефлегмації. 27 Згідно зі стадією (e) даного способу, сполуку формули (Vlla) або (Vllb) піддають взаємодії з гідразингідратом, переважно з лишком моногідрату гідразину, наприклад, аж до 10 еквівалентів, у присутності прийнятного розчинника, такого як галогенвмісні вуглеводні, нижчі спирти або їх суміші. Реакцію переважно проводять у присутності етанолу, додаючи гідразин до розчину сполуки формули (Vlla) або (Vllb) і перемішуючи протягом відповідного часу, наприклад, протягом приблизно 48 годин, в діапазоні температур від приблизно 20°С до приблизно 70°С. Вищезгадану реакцію переважно проводять у присутності крижаної оцтової кислоти. Згідно зі стадією (f) даного способу, сполуку формули (Vllla) або (VllIb) піддають взаємодії з етилхлорформіатом з одержанням відповідного похідного формули (ІХа) або (ІХb). Реакцію здійснюють в добре відомих умовах у присутності відповідної основи, наприклад, діізопропіламіну, і у присутності відповідного розчинника, такого як тетрагідрофуран. Очевидно, що етоксикарбонільна група може бути приєднана до будь-кого з атомів азоту піразолу обох сполук формули (Vllla) або (Vlllb) з утворенням наступних регіоізомерів формули (ІХа) або (ІХb). Відповідно до викладеного, кожна пара регіоізомерів формули (ІХа) або (ІХb) може бути відповідним способом розділена за допомогою добре відомих методів, наприклад, хроматографічно, і потім кожний виділений вказаним способом регіоізомер обробляють. Як альтернатива на подальших стадіях можна ввести в реакцію саму суміш регіоізомерів, не проводячи її розділення. Фактично, оскільки етоксикарбонільна група, яка приводить до двох різних регіоізомерів, видаляється остаточно в кінці процесу, то для фахівця повинно бути ясним, що для одержання сполук формули (Іа) або (lb) за даним винаходом можуть використовуватись обидва з вказаних шляхів. Проте, переважно спосіб здійснюють, спочатку розділяючи і виділяючи регіоізомери формули (ІХа) або (ІХb) з суміші, як указано в робочих прикладах, і потім перетворюють їх в необхідні сполуки. Згідно зі стадією (g.1) даного способу, сполуки формули (ІХа) або (ІХb) піддають взаємодії з відповідною сполукою формули (X), де Ζ означає атом галогену, переважно хлор або бром. 81790 28 Конкретно, сполуку формули (ІХа) або (ІХb) розчиняють у відповідному розчиннику, такому як дихлорметан, диметилформамід, тетрагідрофуран, діоксан і * т.п., і додають прийнятну основу, таку як триметиламін, діізопропілетиламін, карбонат натрію і т.п. Потім додають сполуку формули (X) і суміш перемішують протягом від приблизно 2 до приблизно 15 годин в інтервалі температур від приблизно 20°С до приблизно 80°С. Необов'язково може використовуватись відповідний каталізатор, такий як диметиламінопіридин. Згідно зі стадією (g.2) даного способу, сполуку формули (ІХа) або (ІХb) піддають взаємодії з похідним ізоціанату формули (XII) в тих же умовах, що і вказані на стадії (g.1) даного способу, за винятком того, що в основі немає потреби. Згідно зі стадією (g.3) даного способу, сполуку формули (ІХа) або (ІХb) піддають взаємодії з аміном формули (XIII) у присутності трифосгену або придатного хлорформіату, наприклад, 4нітрофенілхлорформіату, з утворенням відповідного уреїдопохідного. Реакцію проводять в тетрагідрофурані (ТГФ) або у придатному галогенвмісному вуглеводні, переважно в дихлорметані (DCM), у присутності придатного аміну, такого як діізопропілетиламін або триетиламін, при температурі в інтервалі від приблизно -70°С до кімнатної температури. Згідно зі стадією (h) даного способу, у захищеної аміногрупи у формулі (ІХа) або (ІХb) видаляють захист в добре відомих умовах проведення вказаної операції, наприклад, в кислому середовищі у присутності трифтороцтової або хлористоводневої кислоти. Так, сполуки формули (ІХа) або (ІХb) суспендують у відповідному розчиннику, такому як дихлорметан або діоксан, і обробляють концентрованим розчином вибраної кислоти. Альтернативно, з успіхом можуть бути використані комерційно доступні розчини газоподібного хлористого водню в діоксані (4М НСl). Потім суміш перемішують протягом часу від приблизно 2 годин до приблизно 15 годин в інтервалі температур від приблизно 20°С до приблизно 40°С. Відповідно до будь-якої зі стадій (і.1), (і.2), (1.3) або (і.4) даного способу, сполуку формули (XlVa) або (XlVb) потім піддають взаємодії з відповідним похідним з утворенням відповідного карбоксамідо-, уреїдо- і карбаматного похідного формули (XVla) або (XVIb). Стадію (і.1) проводять з використанням ацилгалогеніду, переважно, хлориду, формули (XV) у відповідному розчиннику, такому як дихлорметан, у присутності основи, наприклад, у присутності відповідного аміну, такого як діізопропіламін. Реакція дає можливість одержати карбоксамідопохідне формули (XVIa) або (XVIb), де значення R1 вказані у формулі (І) в групах (а)(с), (llа), де X означає атом вуглецю, і (llb); для фахівця з викладеного вище повинно бути зрозумілим, що атом групи R1, який безпосередньо з'єднаний з карбонільним фрагментом формули (XVIa) або (XVIb), є атомом вуглецю. 29 Стадію (1.2) проводять з гетероциклічним похідним формули (XVII) або аміном формули (XVIII) у присутності трифосгену, в основному як описано для стадії (g.3) даного способу. Відповідно до цього стадія (1.2) дає можливість одержати уреїдопохідне формули (XVIa) або (XVIb), де R1 означає групу формули (IIа), де X означає атом азоту, або формули (Не), де значення Y, Rc, n, Rd і R'd вказані вище. Аналогічно, конденсацію на стадії (1.3) проводять з похідним карбонової кислоти формули (XIX) у присутності відповідного конденсуючого агента, такого як, наприклад, дициклогексилкарбодіімід (DCC), 1-етил-3-(3'диметиламінопропіл)-карбодіімід (EDC) або тетрафторборат Обензотриазолілтетраметилізоуронію (TBTU), застосовуючи добре відомі способи одержання карбоксамідопохідних. Згідно зі стадією (1.4) даного способу, сполуку формули (XIVa) або (XIVb) піддають взаємодії з відповідним похідним формули (XX), де R1 означає групу формули (IId), і значення Re наведено у формулі (Іа) або (lb), і одержують відповідне карбаматне похідне формули (XVIa) або (XVIb). Відповідно до вказаного, сполуку формули (XlVa) або (XlVb) розчиняють у відповідному розчиннику, такому як дихлорметан, диметилформамід, тетрагідрофуран, діоксан і т.п., і в одержану суміш додають відповідну основу, таку як триетиламін, діізопропіламін, карбонат натрію і т.п. Потім додають сполуку загальної формули (XX) і суміш перемішують протягом часу від приблизно 2 годин до приблизно 15 годин в інтервалі температур від приблизно 20°С до приблизно 80°С. Відповідно до переважного варіанту здійснення винаходу, необов'язково може бути використаний відповідний каталізатор, такий як диметиламінопіридин. Згідно зі стадією (j) даного способу, сполуку формули (XVIa) або (XVIb), одержану на будь-якій зі стадій (і.1)-(і.4), піддають взаємодії з відповідною основою, наприклад, триетиламіном, у присутності відповідного розчинника, такого як метанол або етанол, з одержанням необхідної сполуки формули (Іа) або (lb). Нарешті, що стосується стадії (к) даного способу, то вказані вище сполуки формули (Іа) або (lb) необов'язково можуть бути перетворені у фармацевтично прийнятні солі, як указано вище, з використанням звичайних способів або ж перетворені в додаткові сполуки формули (Іа) або (lb). Як не обмежувальний даний винахід прикладу, сполуки формули (Іа) або (lb), що містять карбоксіефірну групу, можуть бути перетворені в різні похідні за допомогою добре відомих в даній галузі способів перетворення карбоксіефірних груп в карбоксаміди, N-заміщені карбоксаміди, Ν,Νдизаміщені карбоксаміди, карбонові кислоти і т.п. Умови проведення реакцій ті ж, що і добре відомі в даній галузі, і вони можуть включати, наприклад, при перетворенні карбоксіефірної групи в карбоксамідну групу, реакцію з аміаком або гідроксидом амонію у присутності відповідного 81790 30 розчинника, такого як нижчий спирт, диметилформамід або їх суміші; переважно реакцію проводять з гідроксидом амонію в суміші метанол/диметилформамід в інтервалі температур від приблизно 50°С до приблизно 100°С. Аналогічні умови проведення реакції застосовують при одержанні N-заміщених або Ν,Νдизаміщених карбоксамідів, де замість аміаку або гідроксиду амонію використовують відповідний первинний або вторинний амін. Аналогічно карбоксіефірні групи можуть бути перетворені в похідні карбонових кислот в умовах основного або кислотного гідролізу, добре відомих в даній галузі. Як додатковий приклад, сполуки формули (Іа) або (lb), що містять аміногрупи, можуть бути легко перетворені у відповідні карбоксамідопохідні або уреїдопохідні. З викладеного вище для фахівця повинно бути зрозумілим, що згідно стадією (к) даного способу, будь-яка сполука формули (Іа) або (lb), що містить функціональну групу, яка може бути далі перетворена в іншу функціональну групу за допомогою способів, добре відомих в даній галузі, і, таким чином, перетворена в інші сполуки формули (Іа) або (lb), також входить в об'єм даного винаходу. У будь-якому з варіантів способу одержання сполук формули (І) вихідні речовини або будь-які інші реагенти добре відомі або легко можуть бути одержані за допомогою відомих способів. Так, наприклад, вихідні сполуки формули (lllа) або (lllb) комерційно доступні, і сполуки формули (X), (XII), (XIII), (XV), (XVII), (XVIII), (XIX) і (XX) відомі або легко можуть бути одержані відповідно до відомих способів. Проміжні сполуки формули (Vlla) або (Vllb) за даним способом де Q означає придатну для атома азоту захисну групу, наприклад, третбутоксикарбонільну групу (bос), є новими і, таким чином, є ще одним об'єктом даного винаходу. Як легко зрозуміти, якщо сполуки формули (І), одержані відповідно до вищеописаного способу, одержують у вигляді суміші ізомерів, то їх розділення на індивідуальні ізомери формули (І) з використанням звичайних методів, входить в об'єм даного винаходу. Звичайні методи розділення рацематів включають, наприклад, дробову кристалізацію солей діастереоізомерів або препаративну хіральну ВЕРХ. Крім того, з викладеного вище повинно бути зрозумілим, що дана сполука формули (Іа) або (lb) може бути одержана або з суміші регіоізомерів формули (ІХа) або (ІХb), або ж з кожного з двох індивідуальних регіоізомерів. При одержанні сполук формули (І) відповідно до одного з вищезгаданих варіантів здійснення даного способу, можливі функціональні групи у вихідній сполуці або в їх проміжних сполуках, які 31 можуть привести до небажаних побічних реакцій, потрібно відповідним чином захистити, використовуючи звичайні методи. Аналогічно, перетворення вказаних захищених похідних в звільнені від захисту сполуки може бути проведено відповідно до відомих методик. Крім того, сполуки формули (І) за даним винаходом можуть бути одержані за допомогою методів комбінаторної хімії, добре відомих в даній галузі, шляхом послідовного проведення вищезгаданих реакцій між декількома проміжними сполуками в умовах твердофазного (SPS) синтезу. Як приклад, сполуки формули (ХІа) і (ХІb), які одержують відповідно до однієї зі стадій (g.l), (g.2) або (g.3), можна нанести на відповідну полімерну смолу. Зокрема, етоксикарбонільну групу формули (ХІа) і (ХІb) можна видалити у присутності основи, наприклад, у присутності триетиламіну або діізопропіламіну, і одержану сполуку приєднати до вказаної вище полімерної матриці безпосередньо через атом азоту піразолу. Одержану вказаним способом іммобілізовану проміжну сполуку потім піддають взаємодії згідно зі стадією (h) або однією зі стадій (1.1), (1.2), (1.3) або (1.4) даного способу і одержують відповідну сполуку формули (Іа) або (lb) за даним винаходом, все ще пов'язаної з полімерною смолою. Подальше розщеплення зв'язку зі смолою, наприклад, в основних або кислотних умовах з використанням відомих методів, дає можливість одержати необхідні сполуки формули (Іа) або (lb). Очевидно, що, послідовно проводячи вказані вище реакції за даним способом, тобто використовуючи комбінаторний підхід, аналогічний описаному вище, можна одержати і виділити декілька сполук формули (Іа) або (lb). Таким чином, ще однією метою даного винаходу є бібліотека, що включає дві або більше сполук формули (Іа) де R означає групу -CORa, -CONHRa або CONRaRb, де Ra і Rb кожний незалежно означає водень або необов'язково заміщену групу, вибрану з Сі-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов'язково заміщений 5- або 6членний, що необов'язково містить один 81790 32 додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝN, О або S; R1 вибирають з групи, що включає: a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-C4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (llb): де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо пов'язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝN, за умови, що, принаймні, один з X і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов'язково заміщену групу, вибрану з С1-С6алкільної групи з прямим або розгалуженим ланцюгом, С3С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIс) і (IId): де Rd, R'd і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-C6алкільну групу з прямим або розгалуженим ланцюгом, необов'язково заміщену однією або декількома групами, вибраними з гідрокси (-ОН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; за умови, що у формулі (Іа), коли R1 означає групу формули (IIс) і один із замісників Rd або R'd означає атом водню, в той час як інший з Rd або R'd означає етильну або н-бутильну групу, то R відрізняється від -CORa, де Ra означає 3бромфенільну, бензильну, 4-трет-бутилфенільну, 4-трет-бутилфенілметильну, 4фторфенілметильну, циклопропільну або 2нафтилметильну групу; або їх фармацевтично прийнятну сіль. Аналогічно, наступною метою даного винаходу є бібліотека, що включає дві або більше сполук формули (lb) 33 де R означає групу -CORa, -C0NHR3 або CONRaRb, де Ra і Rb кожний незалежно означає водень або необов'язково заміщену групу, вибрану з Сі-С6алкільної групи з прямим або розгалуженим ланцюгом, С3-С6циклоалкільної, арильної, арилалкільної, гетероциклільної або гетероциклілалкільної групи; або разом з атомом азоту, до якого вони приєднані, Ra і Rb можуть утворювати необов'язково заміщений 5- або 6членний гетероцикл, що необов'язково містить один додатковий гетероатом або гетероатомну групу, вибрану з Ν, ΝN, О або S; R1 вибирають з групи, що включає: ' a) С3-С4алкільну групу з прямим або розгалуженим ланцюгом; b) циклоалкільну, циклоалкілалкільну або алкілциклоалкільну групу, в якій циклоалкільний фрагмент включає будь-яку С3-С6циклоалкільну групу і в якій алкільний фрагмент включає будь-яку С1-C4алкільну групу з прямим або розгалуженим ланцюгом; c) 3-метилтієніл-2-ільну, 2-тієнільну, фенільну, 2,6-дифторфенільну, 4-(аміносульфоніл)фенільну, 4-(диметиламінометил)фенільну, 4-(4метилпіперазиніл)-метилфенільну групу; d) групу формули (IIа) і (llb): де у формулі (IIа) цикл означає (5-7)-членне гетероциклічне кільце, в якому X, безпосередньо пов'язаний з іншою молекулою, означає атом вуглецю або азоту; Υ означає атом вуглецю, азоту, кисню або сірки або означає групу ΝN, за умови, що, принаймні, один з X і Υ відрізняється від атома вуглецю; групи Rc, незалежно одна від одної і в будь-якому з вільних положень гетероциклічного кільця формули (IIа), означають атом галогену або гідроксильну групу або означають необов'язково заміщену групу, вибрану з С1-C6алкільної групи з прямим або розгалуженим ланцюгом, С3С6циклоалкільної, арильної, арилалкільної, гетероциклільної, гетероциклілалкільної, аміногрупи, амінокарбонільної, карбоксигрупи, оксогрупи (=O), алкоксикарбонільної, алкілкарбонільної або арилкарбонільної групи; і n дорівнює 0 або цілому числу від 1 до 4; e) групу формули (IIс) і (IId): 81790 34 де Rd, R'd і Re, які можуть бути однаковими або різними, незалежно один від одного означають атом водню або С1-C6алкільну групу з прямим або розгалуженим ланцюгом, необов'язково заміщену однією або декількома групами, вибраними з гідрокси (-OН), амінокарбонільної (-CONH2) або метиламінокарбонільної (-CONHCH3) групи; або їх фармацевтично прийнятну сіль. Загальне посилання на вищенаведені бібліотеки сполук формули (І) наведене в експериментальній частині. З викладеного вище для фахівця буде очевидним, що як тільки вказаним чином одержана бібліотека піролопіразольних похідних, наприклад, що включає декілька сотень і навіть декілька тисяч сполук формули (Іа) або (lb), то вказану бібліотеку можна з успіхом використати, як вже повідомлялось вище, для проведення скринінгу по відношенню до наведених кіназ. Загальне посилання на бібліотеки сполук і їх застосування як інструментів для тестування біологічної активності [див. J. Med. Chem., 42, 2373-2382; і Bioorg. Med. Chem. Lett. 10 (2000), 223-226]. Фармакологія Сполуки формули (І) активні як інгібітори протеїнкінази і, таким чином, застосовні, наприклад, для обмеження нерегульованої проліферації пухлинних клітин. У терапії вони можуть бути використані при лікуванні різних пухлин, таких як вказано вище, а також при лікуванні інших захворювань, пов'язаних з проліферацією клітин, таких як псоріаз, пов'язана з атеросклерозом проліферація гладких клітин судин і післяхірургічний стеноз і рестеноз, а також при лікуванні хвороби Альцгеймера. Інгібуючу активність передбачуваних інгібіторів Cdk/Cyclin і ефективність вибраних сполук визначають за допомогою аналізу, основаного на використанні методу SPA (Amersham Pharmacia Biotech). Аналіз полягає в перенесенні кіназою утримуючу радіоактивну мітку фосфатного фрагменту до біотинільованого субстрату. 33 Одержаному Р-міченому біотинільованому продукту дають зв'язатись з покритими стрептавідином SPA кулькам (вміст біотину 130пмол/мг), і світло, що випускається, вимірюють за допомогою сцинтилятору. Аналіз інгібування активності Cdk2/Cyclin A Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 4мкМ субстрату у вигляді біотинільованого самим виробником гістону Н1 (Sigma # Н-5505), 10мкМ АТФ (0,1мкКі Ρ33γ-ΑΤΦ), 4,2нг комплексу Cdk2/Cyclin А, інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл бичачого сироваткового альбуміну [BSA]) з кінцевим об'ємом 30мкл. Через 30хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл забуференого фосфатом сольового розчину (PBS)+32мМ ЕДТУ+0,1% Triton X-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. 35 81790 Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl, для стратифікації кульок вгорі планшету, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Інгібітори випробовують при різних концентраціях в діапазоні від 0,0015 до 10мкм. Експериментальні дані аналізують за допомогою комп'ютерної програми GraphPad Prizm, використовуючи чотирипараметричне логістичне рівняння: у=низ+(верх-низ)/(1+10^(log ІС50-х)(*тангенс нахилу)), де x означає логарифм концентрації інгібітору, у означає реакцію у відповідь; у починається знизу і йде до верху по сигмоподібній кривій. Розрахунок величини Kі: Експериментальний метод: Реакцію проводять в буферному розчині (10мМ Tris з рН7,5, 10мМ MgCl2, 0,2мг/мл BSA, 7,5мМ DTT), який містить 3,7нМ ферменту, гістону і АТФ (постійне відношення неміченого/міченого АТФ 1/3000). Реакцію зупиняють додаванням ЕДТУ і субстрат захоплюють фосфомембраною (96 ямкові планшети Multiscreen від компанії Мillіроrе). Після інтенсивного промивання планшети для мультианалізу зчитують за допомогою приладу top-counter. Визначають контрольне значення (час нуль) для кожної концентрації АТФ і гістону. Планування експерименту: Швидкості реакції визначають за чотирма різними концентраціями АТФ, субстрату (гістону) та інгібітору. Будують матрицю концентрацій, що містить 80 точок, навколо відповідних значень АТФ і Km субстрату і значень ІС50 інгібітору (кратні значенням 0,3; 1; 3; 9 Km або ІС50). Попередні експерименти в залежності від часу за відсутності інгібітору і при різних концентраціях АТФ і субстрату дозволяють провести відбір єдиного часу закінчення (10хв.), в лінійному діапазоні протікання реакції в експерименті з визначення величини Kі. Оцінка кінетичних параметрів: Оцінку кінетичних параметрів проводять за допомогою одночасної нелінійної регресії за методом найменших квадратів з використанням рівняння [Eq.1] (конкурентний інгібітор для АТФ, випадковий механізм) і всього набору даних (80 точок): n= Vm × A × B a × Ka × Kb + a × Ka × B + a × Kb × A + A × B + a × Ka B × I × (Kb + ) b Ki [Eg.1] де А=[АТФ], В=[субстрат], І=[інгібітор], Vm=максимальна швидкість, Kа, Kb, Кі - константи дисоціації АТФ, субстрату та інгібітору, відповідно, α і β -кооперативний фактор, відповідно, між зв'язуванням субстрату з АТФ і між зв'язуванням субстрату з інгібітором зв'язування. Вибрані сполуки додатково характеризують за допомогою панелі серин/треонінкіназ, безпосередньо пов'язаних з клітинним циклом (Cdk2/Cyclin E, Cdkl/Cyclin Bl, Cdk5/p25, Cdk4/Cyclin Dl), а також, з метою визначення специфічності дії по відношенню до МАРК, РКА, EGFR, IGF1-R, Aurora-2 і Akt. Аналіз інгібування активності Cdk2/Cvclin E 36 Кіназна реакція: В кожну ямку 96-ямкового планшету з U-подібним дном додають 10мкМ субстрату у вигляді біотинільованого самим виробником гістону Н1 (Sigma # Н-5505), 30мкМ АТФ (0,3мкКі Ρ33γ-ΑΤΦ), 4нг комплексу GSTCdk2/Cyclin Ε, інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 30мкл. Через 60хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton X-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl для стратифікації кульок вгорі планшета, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності Cdkl/Cyclin B1 Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 4мкМ субстрату у вигляді біотинільованого самим виробником гістону Н1 (Sigma # Н-5505), 20мкМ АТФ (0,2мкКі Ρ33γ-ΑΤΦ), з нг комплексу Cdkl/Cyclin В, інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 30мкл. Через 20хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton X-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl для стратифікації кульок вгорі Optiplate, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності Cdk5/p25 Аналіз інгібування активності Cdk5/p25 проводять за наступною методикою. Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 10мкМ субстрату у вигляді біотинільованого гістону Н1 (Sigma # Н-5505), 30мкМ АТФ (0,3мкКі Ρ33γ-ΑΤΦ), 15нг комплексу CDK5/p25, інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 30мкл. Через 30хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton X-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl для стратифікації кульок вгорі планшета, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності Cdk4/Cvclin D1 Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 0,4мкМ субстраут мишачого GST-Rb (769-921) (# sc-4112 від компанії Santa Cruz), 10мкМ АТФ (0,5мкКі Ρ33γΑΤΦ), юо нг експресованого бакуловірусом GSTCdk4/Cyclin D1, відповідну концентрацію інгібітору 37 в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 50мкл. Через 40хв. інкубування при 37°С реакцію зупиняють додаванням 20мкл ЕДТУ 120мМ. Захоплення: 60мкл з кожної ямки переносять на планшет Multiscreen і дають субстрату зв'язатись з фосфоцелюлозним фільтром. Потім планшети промивають 3 рази таким, що містить Ca++/Mg++, розчином PBS в кількості по 150мкл на ямку і відфільтровують за допомогою фільтруючої системи Multiscreen. Детектування: Фільтрам дають висохти при 37°С, потім додають сцинтилянт в кількості по 100мкл на ямку і 33Р-мічений фрагмент Rb визначають шляхом підрахунку радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності МАРК Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 10мкМ субстрату у вигляді біотинільованого самим виробником МБР (Sigma # М-1891), 15мкМ АТФ (0,15мкКі Ρ33γ-ΑΤΦ), 30 нг комплексу GST-MAPK (Upstate Biotechnology # 14-173), інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 30мкл. Через 30хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton Х-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчини CsCl для стратифікації кульок вгорі Optiplate, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності РКА Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 10мкМ субстрату у вигляді біотинільованого самим виробником гістону Н1 (Sigma # Н-5505), 10мкМ АТФ (0,2мкКі Ρ33γ-ΑΤΦ), 0,45од. РКА (Sigma # 2645), інгібітор в буфері (TRIS HCI 10мМ, рН7,5, MgCl2 10мМ, DTT 7,5мМ+0,2мг/мл BSA) з кінцевим об'ємом 30мкл. Через 90хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton X-100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl для стратифікації кульок вгорі Optiplate, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності EGFR Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 10мкМ субстрату у вигляді біотинільованого самим виробником МБР (Sigma # М-1891), 2мкМ АТФ (0,04мкКі Ρ33γ-ΑΤΦ), 36нг експресованого клітиною комахи GST-EGFR, інгібітор в буфері (Hepes 50мМ, рН7,5, MgCl2 3мМ, МnСl2 3мМ, DTT 1мМ, NaVO3 3мкМ+0,2мг/мл BSA) з кінцевим об'ємом 81790 38 30мкл. Через 20хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл PBS+32мМ ЕДТУ+0,1% Triton Х100+500мкМ АТФ, що містить 1мг SPA кульок. Потім об'єм 110мкл переносять на Optiplate. Через 20хв. інкубування, з метою захоплення субстрату, додають 100мкл 5М розчину CsCl для стратифікації кульок вгорі Optiplate, і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності IGF1-R Аналіз інгібування активності IGF1-R проводять за наступною методикою. Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном вміщують 10мкМ субстрату у вигляді біотинільованого МБР (Sigma # М-1891), 0-20мкМ інгібітору, 6мкМ АТФ, 1мкКі Р33-АТФ і 22,5нг GST-IGF1-R (заздалегідь інкубованого протягом 30хв. при кімнатній температурі разом з 60мкМ міченого АТФ) в буфері (50мМ Hepes, рН7,9, 3мМ МnСl2, 1мМ DTT, 3мкМ NaVO3) з кінцевим об'ємом 30мкл. Через 35хв. інкубування при кімнатній температурі реакцію зупиняють додаванням 100мкл буфера PBS, що містить 32мМ ЕДТУ, 500мкМ холодного АТФ, 0,1% Triton X-100 і 10мг/мл SPA кульок, покритих стрептавидіном. Інкубують протягом 20хв., відбирають суспензію в кількості 110мкл і переносять на 96-ямкові планшети Optiplate, що містять 100мкл 5М розчину CsCl. Через 4 години проводять підрахунок радіоактивності за допомогою вимірника радіоактивності Top-Count компанії Packard. Аналіз інгібування активності Aurora-2 Кіназна реакція: У кожну ямку 96-ямкового планшету з U-подібним дном додають 8мкМ біотинільованого пептиду (4 повтори LRRWSLG), 10мкМ АТФ (0,5мкКі Ρ33γ-ΑΤΦ), 15нг Aurora-2, інгібітор в буфері (HEPES 50мМ, рН7,0, MgCl2 10мМ, 1мМ DTT, 0,2мг/мл BSA, 3мкМ ортованадату) з кінцевим об'ємом 30мкл. Через 30хв. інкубування при кімнатній температурі реакцію зупиняють і біотинільований пептид захоплюють, додаючи 100мкл суспензії кульок. Стратифікація: У кожну ямку додають 100мкл 5М розчину CsCl і залишають на 4 години перед підрахунком радіоактивності за допомогою приладу Top-Count. Визначення величини ІС50: Див. вище. Аналіз інгібування активності Cdc7/dbf4 Аналіз інгібування активності Cdc7/dbf4 проводять за наступною методикою. Субстрат Biotin-MCM2 транс-фосфорилюють за допомогою комплексу Cdc7/Dbf4 у присутності АТФ, міченого за допомогою Ρ33γ-ΑΤΦ. Фосфорильований субстрат Biotin-MCM2 потім захоплюють покритими стрептавідином SPA кульками і міру фосфорилювання оцінюють шляхом підрахунку β-частинок. Аналіз інгібування активності Cdc7/dbf4 проводять на 96-ямковому планшеті за наступною методикою. У кожну ямку планшету додають: 39 10мкл субстрату (біотинільований МСМ2, кінцева концентрація 6мкМ) 10мкл ферменту (Cdc7/Dbf4, кінцева концентрація 12,5нМ) 10мкл тестованої сполуки (12 зростаючих концентрацій в діапазоні від нМ домкМ для побудови кривої залежності реакцію у відповідь від дози) 10мкл суміші неміченого АТФ (кінцева концентрація 10мкМ) і радіоактивного АТФ (1/2500 молярне відношення до неміченому АТФ) потім використовують для ініціації реакції, якій дають протікати при температурі 37°С. Субстрат, фермент і АТФ розбавляють за допомогою розчину 50мМ Hepes з рН7,9, що містить 15мМ MgCl2, 2мМ DTT, 3мкМ NaVO3, 2мМ гліцерофосфату і 0,2мг/мл BSA. Розчинник, що використовується для тестованої сполуки, також містить 10% ДМСО. Після інкубування протягом 20хв. реакцію зупиняють, додаючи в кожну ямку 100мкл PBS з рН7,4, що містить 50мМ ЕДТУ, 1мМ неміченого АТФ, 0,1% Triton X100 і 10мг/мл покритих стрептавідином SPA кульок. Після того, як при кімнатній температурі протягом 15хв. дають взаємодіяти біотинільованому МСМ2 з покритими стрептавідином SPA кульками, кульки вловлюють за допомогою 96-ямкових фільтруючих планшетів (UnifilterR GF/B™), використовуючи пристрій для збирання клітин компанії Packard (Filter-mate), промивають дистильованою водою і потім проводять підрахунок за допомогою приладу Top Count (Packard). З даних підрахунку віднімають дані контрольної проби і потім експериментальні дані (для кожної точки проводять по три експерименти) аналізують, з метою визначення величини ІС50, використовуючи нелінійний регресійний аналіз (Sigma Plot). Відповідно до вищезгаданих аналізів на інгібування, було встановлено, що сполуки формули (І) за даним винаходом володіють значною інгібуючою активністю по відношенню до cdk. Див., наприклад, наступні експериментальні дані (ІС50) двох типових сполук за даним винаходом формули (Іа) і (lb), які були тестовані по відношенню до Cdk2/Cyclin A: Сполука 1: N-[5-(2,2-диметилпропаноїл)-6,6диметил-1,4,5,6-тетрагідропіроло-[3,4-с]піразол-3іл]-4-фторбензамід (ІС50 0,030мкМ) і Сполука 2: N-[5-(2,2-диметилпропаноїл)1,4,5,6-тетрагідропіроло[3,4-с]піразол-6спіроциклопропан-3-іл]-4-фторбензамід (ІС50 0,025мкМ). Несподівано виявилось, що вказана інгібуюча здатність значно перевершує інгібуючу здатність найближчого аналога, відомого з попереднього рівня техніки у [WO 02/12242], в даному описі названого Сполукою порівняння (див. сполука 1143, внизу стор. 76; і приклад 19, сполука на розвороті сторінок 242-3 в [WO 02/12242]), яку використовують з метою порівняння і тестують по відношенню до Cdk2/Cyclin А, як вказано вище: Сполука порівняння: N-[5-ацетил-6,6-диметил4,6-дигідропіроло[3,4-с]піразол-3-іл]-(3бром)бензамід (ІС50 1,7мкМ). 81790 40 порівняння Таким чином, нові сполуки за даним винаходом несподівано володіють інгібуючою активністю по відношенню до cdk, що значно перевищує інгібуючу активність структурно найбільш близького аналога, наведеного у [WO 02/12242] і, таким чином, володіють перевагою при використанні в терапії проти проліферативних захворювань, пов'язаних зі зміненою кіназною активністю, що залежить від клітинного циклу. Сполуки за даним винаходом можуть вводитись у вигляді індивідуального засобу або ж в комбінації з відомими протираковими методами лікування, такими як схеми радіаційної терапії або хіміотерапії разом з цитостатичними або цитотоксичними засобами, антибіотиками, алкілуючими агентами, антиметаболічними засобами, гормональними засобами, імунологічними засобами, агентами інтерферонового типу, інгібіторами циклооксигенази (зокрема, інгібіторами СОХ-2), інгібіторами матричної металопротеази, інгібіторами теломерази, інгібіторами тирозинкінази, засобами проти рецептора фактора зросту, засобами проти HER, засобами проти EGFR, засобами проти ангіогенезу (зокрема, інгібіторами ангіогенезу), інгібіторами фарнезилтрансферази, інгібіторами шляхів передачі сигналу ras-raf, інгібіторами клітинного циклу, іншими інгібіторами cdk, засобами зв'язування тубуліну, інгібіторами топоізомерази І, інгібіторами топоізомерази II і т.п. При одержанні у вигляді певної дози, у вказаній комбінації речовин використовують сполуки за даним винаходом з діапазоні доз, вказаному нижче, та іншу фармацевтично активну сполуку в схваленому діапазоні доз. Сполуки формули (І) можуть бути використані послідовно з відомими протираковими засобами в тому випадку, коли комбінація у вигляді композиції неможлива. Сполуки формули (І) за даним винаходом, придатні для введення ссавцеві, зокрема, людям, можуть вводитись звичайними способами, і рівень дози залежить від віку, маси, стану пацієнта і шляху ведення. Наприклад, відповідне дозування, прийняте для перорального введення сполуки формули (І), може складати діапазон від 10 до 500мг на дозу, від 1 до 5 разів на день. Сполуки за даним винаходом можуть вводитись у вигляді різних дозованих форм, наприклад, перорально у вигляді таблеток, капсул, покритих цукром або плівкою таблеток, рідких розчинів або суспензій; ректально у вигляді супозиторіїв; парентерально, зокрема, внутрішньом'язово або ж за допомогою 41 внутрішньовенної і/або внутрішньооболонкової, і/або інтраспінальної ін'єкції або вливання. Даний винахід включає також фармацевтичні композиції, що містять сполуку формули (І) або її фармацевтично прийнятну сіль в поєднанні з фармацевтично прийнятним ексципієнтом, який може бути носієм або розріджувачем. Фармацевтичні композиції, що містять сполуки за даним винаходом, одержують звичайними способами і вводять у відповідній фармацевтичній формі. Наприклад, тверді пероральні форми разом з активною сполукою можуть містити розріджувач, зокрема, лактозу, декстрозу, сахарозу, целюлозу, кукурудзяний крохмаль або картопляний крохмаль; лубриканти, зокрема, оксид кремнію, тальк, стеаринову кислоту, стеарат магнію або кальцію і/або поліетиленгліколі; зв'язуючі, зокрема, крохмалі, гуміарабік, желатин, метилцелюлозу, карбоксиметилцелюлозу або полівінілпіролідон; дезінтегранти, зокрема, крохмаль, альгінову кислоту, альгінати і гліколят натрію крохмалю; шипучі суміші; барвники; підсолоджувачі; змочувальні агенти, такі як лецитин, полісорбати, лаурилсульфонати; і, в загальному випадку, нетоксичні і фармацевтично неактивні речовини, що використовуються у фармацевтичних композиціях. Вказані фармацевтичні препарати можуть бути виготовлені відомими способами, наприклад, шляхом змішування, гранулювання, таблетування, нанесення покриття з цукру і нанесення покриття у вигляді плівки. Рідкі дисперсії для перорального введення можуть бути, зокрема, сиропами, емульсіями і суспензіями. Наприклад, сиропи можуть містити як носій сахарозу і сахарозу з гліцерином і/або манітом або сорбітом. Суспензії і емульсії можуть містити, як приклад носіїв, природну смолу, агар, альгінат натрію, пектин, метилцелюлозу, карбоксиметилцелюлозу або полівініловий спирт. Суспензії або розчини для внутрішньом'язових ін'єкцій можуть разом з активним агентом включати фармацевтично прийнятний носій, зокрема, стерильну воду, оливкову олію, етилолеат, гліколі, наприклад, пропіленгліколь, і, якщо необхідно, відповідну кількість гідрохлориду лідокаїну. Розчини для внутрішньовенної ін'єкції або внутрішньовенного вливання можуть містити, як носій, стерильну воду або ж, переважно, вони можуть бути у формі стерильних водних ізотонічних фізіологічних розчинів або містити як носій пропіленгліколь. Супозиторії разом з активною сполукою можуть містити фармацевтично прийнятний носій, зокрема, масло какао, поліетиленгліколь, складний ефір жирної кислоти і поліоксіетильованого сорбітану як поверхневоактивну речовину або лецитин. Наступні приклади наведені з метою кращого пояснення даного винаходу, але не з метою внести в нього які-небудь обмеження. Загальні методи Перш ніж розглянути методи синтезу конкретних сполук формули (І) за даним 81790 42 винаходом, наприклад, як указано в наступних прикладах, потрібно звернути увагу на те, що деякі сполуки в даному описі наведені і позначені відповідно до їх хімічної назви, в той час як більшість інших сполук для зручності і однозначності вказані із застосуванням системи кодування разом з їх даними 1Н-ЯМР (див. нижче в таблицях III, IV і V) і даними ВЕРХ/масспектрометрії (див. нижче в таблиці VI). Кожний код, зокрема, ідентифікує єдину конкретну сполуку формули (Іа) або (lb) і складається з трьох одиниць А-М-В. А означає будь-який замісник R [див. формулу (Іа) або (lb)] і приєднаний до іншої молекули через групу -NH; кожна конкретна група А наведена і послідовно пронумерована у наведеній нижче таблиці І. Аналогічно, В означає будь-який замісник R1 [див. формулу (Іа) або (lb)] і приєднаний до іншої молекули через карбонільну (CO) групу; кожна конкретна група В наведена і послідовно пронумерована у наведеній нижче таблиці II. Μ відноситься до центрального ядра двовалентного фрагменту, заміщеного групами А і В; зокрема, Μ може варіювати від М1 або М2, як вказано у наведених нижче формулах, кожна з яких означає центральне ядро сполуки, що має, відповідно, формулу (Іа) або (lb): Щоб простіше посилатись на сполуки за винаходом, всі групи А і В в таблицях І і II ідентифіковані за допомогою відповідної хімічної формули, де також показані точки приєднання по відношенню до іншої частини молекули М. Таким чином, просто як приклад, сполука А06М1-В01 в таблиці III означає сполуку формули (Іа), що має центральне ядро МІ, яке заміщене групою А06 і групою В01 у позиціях, вказаних стрілками; аналогічно, сполука А04-М2-В08 в таблиці V означає сполуку формули (lb), що має центральне ядро М2, яке заміщене групою А04 і групою В08 у позиціях, вказаних стрілками: 43 81790 44 45 81790 46 Приклад 1 N-(2-Ціаноетил)-2-метил аланін 50г (0,48мол) 2-метилаланіну додають до охолодженого розчину (вода/лід) NaOH (19,6г) у воді (100мл). Після того, як розчин стане прозорим, краплями при охолоджуванні додають 34мл (0,50мол) акрилонітрилу. Суміш залишають на ніч. Через 18 години при охолоджуванні (вода/лід) додають 28мл оцтової кислоти; випадає білий осад; в колбу краплями додають 200мл 95%ного етанолу, перемішування продовжують протягом години і потім суміш залишають на 2-3 години в холодильнику. Після фільтрування тверду речовину відділяють і сушать в сушильній шафі при температурі 80°С. Фільтрати упарюють і залишок розчиняють в етанолі (160мл). При охолоджуванні одержують додаткову кількість продукту, який відфільтровують і сушать. Після першого фільтрування одержують 72г вказаної в заголовку сполуки. Загальний вихід 95%. ESI MS: m/z 157(MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 7,47 (с, 1Н), 2,70 (т, 2Η), 2,48 (т, 2Η), 1,18 (с, 6Н). За аналогічною методикою одержують наступну сполуку: 1-[(2-ціаноетил)аміно]циклопропанкарбонова кислота ESI MS: m/z 154 (Μ), 136 (M-H2O), 114-(MCH2CN), 68 (100%, циклопроп-С=О); 1 H-ЯМР (400МГц, ДМСО-d6): δ 7,47 (с, 1H), 2,86 (т, 2Η, J=6,6Гц), 2,48 (т, 2Η, J=6,6Гц), 1,09 (дд, 2Н, J=6,9Гц, J=4,1Гц), 0,86 (дд, 2Н, J=6,9Гц, J=4,1Гц). Приклад 2 N-(Бутоксикарбоніл)-N-(2-ціаноетил)-2-метил аланін 44,5г (0,285мол) N-(2-ціаноетил)-2метилаланіну і 51,7г пентагідрату гідроксиду тетраметиламонію розчиняють в ацетонітрилі (2л) 47 при температурі 40°С і після того, як розчин стане прозорим, додають 112г Вос2О. Суміш залишають при 40°С на 24 години. На наступний день, підтримуючи температуру 40°С, додатково додають ще 20г Вос2О. По 20г Вос2О додають через кожні 8-12 години, так що загальна кількість вказаного реагенту становить 192г. Через 4 дні розчинник упарюють, залишок розчиняють у воді (1000мл) і двічі промивають етиловим ефіром (500мл). Доводять рН водної фракції до 3-4 за допомогою лимонної кислоти і екстрагують етилацетатом, промивають водою (200мл) і концентрують. Одержують 52г вказаної в заголовку сполуки (вихід: 72%). ESI MS: m/z 274 (M+NH4); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 3,52 (т, 2Η, J=6,8Гц), 2,68 (т, 2Η, J=6,8Гц), 1,18-1,38 (м, 15Н). За аналогічною методикою одержують наступну сполуку: 1-[(трет-бутоксикарбоніл)(2ціаноетил)аміно]циклопропанкарбонова кислота ESI MS: m/z 272 (M+NH4), 255 (МН+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 12,55 (шир. с, 1H), 3,33 (м, 2Н), 2,71 (м, 2Н), 0,97-1,63 (м, 13Н). Приклад 3 Метил-N-(трет-бутоксикарбоніл)-N-(2ціаноетил)-2-метилаланінат 62г (0,23мол) N-(трет-бутоксикарбоніл)-N-(2ціаноетил)-2-метилаланіну розчиняють в 350мл ДМФА і додають 50г KНСО3. Після декількох хвилин краплями додають 30мл метилйодиду (МеІ) і суміш перемішують при кімнатній температурі протягом 6 годин. Потім додатково додають 15мл МеІ. Суміш залишають на ніч при кімнатній температурі. Після розбавлення 1,5л води розчин екстрагують етилацетатом (3 рази). Органічну фазу промивають невеликою кількістю води, сушать над сульфатом натрію, упарюють і сушать за допомогою механічного насосу. Одержують 60,5г (97%) метил-N-(третбутоксикарбоніл)-N-(2-ціаноетил)-2метилаланінату. ESI MS: m/z 288 (M+NH4); 1 H-ЯМР (400МГц, ДМСО-d6): δ 3,55 (м, 5Н), 2,70 (т, 2Η, J=6,7Гц), 1,40 (с, 6Н), 1,36 (с, 9Н). За аналогічною методикою одержують наступну сполуку: метил-1-[(трет-бутоксикарбоніл)(2ціаноетил)аміно]циклопропанкарбоксилат ESI MS: m/z 286 (M+NH4); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 3,61 (с, 3Н), 3,42 (т, 2Η, J=6,7Гц), 2,71 (м, 2Н), 1,07-1,62 (м, 13Н). Приклад 4 трет-Бутил-4-ціано-3-гідрокси-2,2-диметил-2,5дигідро-1H-пірол-1-карбоксилат 45г метил-N-(трет-бутоксикарбоніл)-N-(2ціаноетил)-2-метилаланінату розчиняють в діоксані (240мл) в атмосфері азоту і додають 7,9г гідриду натрію. Суміш кип'ятять зі зворотним холодильником протягом 6 годин (температура всередині 120°С) і потім залишають на ніч при кімнатній температурі (ТШХ: СН2Сl2/ЕtOН 90/10). Розчинник упарюють, додають воду (1000мл) і доводять рН суміші до 3-4 за допомогою лимонної 81790 48 кислоти. Водний шар чотири рази екстрагують етилацетатом, екстракти промивають обмеженою кількістю води і упарюють. Залишок розчиняють в гексані, упарюють і перекристалізовують з гексану. Одержують 33,1г трет-бутил-4-ціано-3-гідрокси2,2-диметил-2,5-дигідро-1Н-пірол-1-карбоксилату (вихід: 85%). ESI MS: m/z 237 (M-H-); 1 H-ЯМР (400МГц, ДМСО-d6): δ 4,06-4,10 (2c, 2H, конформери), 1,48 (с, 6Н), 1,47 (с, 9Н). За аналогічною методикою одержують наступну сполуку: трет-бутил-6-ціано-7-оксо-4азаспіро[2.4]гептан-4-карбоксилат ESI MS: m/z 235 (M-H-); 1 H-ЯМР (400МГц, ДМСО-d6): δ 4,63 (т, 1Η, J=9,8Гц), 4,24 (т, 1Η, J=10,2Гц), 3,74 (т, 1H, J=10,2Гц), 1,67-2,16 (м, 2Н), 1,34-1,41 (с, 9Н), 0,931,20 (м, 2Н). Приклад 5 трет-Бутил-3-аміно-6,6-диметил-2,6дигідропіроло[3,4с]піразол-5(4Н)-карбоксилат 32г трет-бутил-4-ціано-3-гідрокси-2,2-диметил2,5-дигідро-1H-пірол-1-карбоксилату (0,134мол) додають до 430мл абсолютного етанолу. До одержаного розчину додають 9мл (0,18мол) гідразингідрату і потім 12мл крижаної оцтової кислоти (1,5екв.). Суміш перемішують при температурі 60°С протягом 60 годин, етанол видаляють, залишок розчиняють в 400мл розчину бікарбонату натрію і декілька разів екстрагують етилацетатом, щоб повністю екстрагувати необхідний продукт. Органічні фази сушать і упарюють. Після очищення флеш-хроматографією (елюент: СНСl3/ЕtOН 97/3) і розтирання в суміші гексан/етилацетат 9/1 одержують 25г вказаної в заголовку сполуки. Загальний вихід 30,5г (вихід: 88%). ESI MS: m/z 253 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 4,06-4,10 (2с, 2Н, конформери), 1,48 (2с, 6Н, конформери), 1,47 (с, 9Н, конформери). За аналогічною методикою одержують наступну сполуку: трет-бутил-3-аміно-2,6-дигідропіроло[3,4с]піразол-6-спіроцикло-пропан-5 (4Н)-карбоксилат ESI MS: m/z 251 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 11,12 (ушир.с, 1Н), 5,13 (ушир.с, 2Н), 4,16-4,33 (м, 2Н), 1,57-1,91 (м, 2Н), 1,38 (с, 9Н), 0,65-0,83 (м, 2Н). Приклад 6 5-трет-Бутил-2-етил-3-аміно-6,6диметилпіроло[3,4-с]піразол-2,5(4Н,6Н)дикарбоксилат і 5-трет-бутил-1-етил-3-аміно-6,6диметил-4,6-дигідропіроло[3,4-с]-піразол-1,5дикарбоксилат 15г трет-бутил-3-аміно-6,6-диметил-2,6дигідропіроло[3,4с]піразол-5(4Н)-карбоксилату (59,4ммол) розчиняють в безводному ТГФ (150мл) і при 0°С в атмосфері Аг спочатку обробляють Ν,Ν-діізопропілетиламіном (50мл) і потім краплями додають СІСО2Еt (4,65мл, 1екв.). Після 90хв. розчинник розбавляють за допомогою ЕtOАс (1л), промивають водою і насиченим розчином солі, сушать над сульфатом натрію і упарюють. 49 Неочищений продукт очищають флешхроматографією (гексан/ЕtOАс 2/8) і одержують 7,3г 5-трет-бутил-2-етил-3-аміно-6,6диметилпіроло[3,4-с]піразол2,5(4Н,6Н)дикарбоксилату у вигляді основної сполуки з виходом 38% разом з 5,7г 5-трет-бутил1-етил-3-аміно-6,6-диметил-4,6-дигідропіроло[3,4с]піразол-1,5-дикарбоксилату з виходом 30%. 5-трет-Бутил-2-етил-3-аміно-6,6диметилпіроло[3,4-с]піразол-2,5(4Н,6Н)дикарбоксилат ESI MS: m/z 325 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 4,35 (кв, 2Н), 4,10 (2с, 2Н, конформери), 1,50-1,51 (м, 6Н), 1,411,43 (2с, 9Н, конформери), 1,29 (т, 3Н). 5-трет-Бутил-1-етил-3-аміно-6,6-диметил-4,6дигідропіроло[3,4-с]піразол-1,5-дикарбоксилат ESI MS: m/z 325 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 4,28 (кв, 2Н, 1=1,1Гц), 4,09-4,14 (2с, 2Н, конформери), 1,66-1,67 (м, 6Н), 1,41-1,44 (2с, 9Н, конформери), 1,27 (т, 3Н, J=7,1Гц). За аналогічною методикою одержують наступні сполуки: 5-трет-бутил-2-етил-3-амінопіроло[3,4с]піразол-6-спіроциклопропан2,5(4Н,6Н)дикарбоксилат ESI MS: m/z 323 (МН+); 1 Н-ЯМР (400МГц, ДMCO-d6): δ 4,30 (кв., 2Η, J=7,1Гц), 4,27 (ушир.с, 2Н), 1,65-2,01 (м, 2Н), 1,38 (с, 9Н), 1,27 (т, 3Н, J=7,1Гц), 0,82-0,96 (м, 2Н). 5-трет-бутил-1-етил-3-аміно-4,6дигідропіроло[3,4-с]піразол-6-спіроциклопропан1,5-дикарбоксилат ESI MS: m/z 323 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 4,26 (ушир.с, 2Η), 4,21 (кв., 2Н, J=7,0Гц), 1,36-1,97 (м, 13Н), 1,23(т, 3Н, J=7,0Гц). Приклад 7 5-трет-Бутил-1-етил-3-[(4-фторбензоїл)аміно]6,6-диметил-4,6-дигідропіроло[3,4-с]піразол-1,5дикарбоксилат 5-трет-Бутил-1-етил-3-аміно-6,6-диметил-4,6дигідропіроло[3,4-с]піразол-1,5-дикарбоксилат (2,0г, 6,16ммол) розчиняють в ТГФ (40мл), спочатку обробляють Ν,Ν-діізопропілетиламіном (5,4мл, 30,80ммол) і потім краплями при 0°С додають 4-фторбензоїлхлорид (800мкл, 6,77ммол), розчинений в ТГФ (8мл). Реакційну суміш перемішують при кімнатній температурі протягом 5 годин, концентрують і розчиняють в DMC, промивають насиченим водним розчином бікарбонату натрію і потім насиченим розчином солі. Органічну фазу сушать над сульфатом натрію, упарюють і залишок очищують флешхроматографією (гексан/ЕtOА 80/20), одержуючи 2,5г вказаної в заголовку сполуки з виходом 90%. ESI MS: m/z 447 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 11, 47 (с, 1Н), 8,04-8,17 (м, 2H), 7,25-7,37 (м, 2Н), 4,44-4,47 (2с, 2Н, конформери), 4,43 (кв., 2Н, J=7,1Гц), 1,73-1,75 (2с, 6Н, конформери), 1,43-1,46 (2с, 9Н, конформери), 1,33 (т, 3Н, J=7,1Гц). За аналогічною методикою одержують наступні сполуки: 81790 50 5-трет-бутил-2-етил-3-[(4-фторбензоїл)аміно]6,6-диметилпіроло[3,4-с]піразол-2,5(4Н,6Н)дикарбоксилат ESI MS: m/z 447 (MH+); 1 H-ΗΜΡ (400МГц, ДМСО-d6): δ 10,78 (с, 1H), 7,95-7,99 (м, 2Н), 7,40-7,47 (м, 2Н), 4,51-4,49 (2с, 2Н, конформери), 4,43 (кв, 2Н, J=7,1Гц), 1,59-1,60 (2с, 6Н), 1,43-1,46 (2с, 9Н, конформери), 1,34 (т, 3Н, J=7,1Гц). 5-трет-бутил-2-етил-3-[(4фторбензоїл)аміно]піроло[3,4-с]піразол-6спіроциклопропан-2,5(4Н,6Н)-дикарбоксилат ESI MS: m/z 445 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 10,81 (с, 1H), 7,95-8,06 (м, 2Н), 7,39-7,49 (м, 2Н), 4,67 (ушир.с, 2Н), 4,41 (кв., 2Н, J=7,1Гц), 1,80-2,10 (м, 2Н), 1,41 (с, 9Н), 1,32 (т, 3Н, J=7,1Гц), 0,93-1,06 (м, 2Н). Приклад 8 5-трет-бутил-1-етил-3-({[(3фторфеніл)аміно]карбоніл}аміно)-6,6-диметил-4,6дигідропіроло[3,4-с]піразол-1,5-дикарбоксилат 5-трет-бутил-1-етил-3-амшо-6,6-диметил-4,6дигідропіроло[3,4-с]піразол-1,5-дикарбоксилат (3,0м, 9,24ммол) розчиняють у безводному ТГФ, додають при кімнатній температурі 3фторфенілізоціанат (1,4м, 10,21ммол, 1,1екв.) і перемішують протягом ночі. Наступного дня реакційну суміш упарюють, розчиняють залишок у DCM і промивають насиченим розчином солі. Органічну фазу сушать над сульфатом натрію і упарюють досуха. Після очищення флешхроматографією (СН2Сl2/МеOН 90/10) одержують 3,05г (вихід 71%) зазначеної в заголовку сполуки. SI MS: m/z 462 (МН+); 1 Н-НМР (400МГц, ДМСО-d6): δ 9,74 (с, 1H), 9,05 (с, 1H), 7,44 (м, 1Н), 7,33 (м, 1H), 7,16 (м, 1H), 6,84 (м, 1Н), 4,43 (м, 4Н), 1,76 (2с, 6Н), 1,48 (2с, 9Н, конформери), 1,36(т,311,1=7,1Гц). Приклад 9 5-трет-бутил-1-етил-3-[(піперидин-1карбоніл)аміно]-6,6-диметил-4,6-дигідропіроло[3,4с]піразол-1,5-дикарбоксилат До розчину трифосгену (550мг, 1,85ммол, 0,4екв.) тетрагідрофурані (50мол) при температурі -40°С додають розчин 5-трет-бутил-1-етил-3аміно-6,6-диметил-4,6-дигідропіроло[3,4-с]піразол1,5-дикарбоксилату (1,5м, 4,62ммол) у тетрагідрофурані (50мол) і Ν,Νдіізопропілетиламін (1,8мол, 2,2екв.). Через 3 години додають розчин піперидину (690мкл, 1,5екв.) і Ν,Ν-діізопропілетиламіну (1,2мол, 1,5екв.) у тетрагідрофурані (25мол). Дають реакційній суміші протягом 2 година нагрітись до кімнатної температури (ТШХ: ЕtOАс/гексан 90/10). Після випарювання розчинника тверду речовину розчиняють у DCM і розчин промивають насиченим розчином солі, органічну фазу сушать над сульфатом натрію і концентрують. Тверду речовину очищають флеш-хроматографією (елюент: EtOAc/гексан 50/50). Одержану тверду речовину розтирають у діізопропіловому ефірі і одержують 1,45 м зазначеної в заголовку сполуки з виходом 72%. ESI MS: m/z 436 (МН+); 51 1 Н-ЯМР (400МГц, ДМСО-d6): δ 9,36 (с, 1H), 4,46 (м, 4Н), 3,40 (м, 4Н), 1,76 (2c, 6H), 1,54 (м, 6Н), 1,44 (2с, 9Η, конформери), 1,36 (т, 3Н, J=7,1Гц). Приклад 10 Гідрохлорид етил-3-[(4-фторбензоїл)аміно]6,6-диметил-5,6-диридропіроло[3,4-с]піразол1(4Н)карбоксилату 5-трет-бутил-1-етил-3-[(4-фторбензоїл)аміно]6,6-диметил-4,6-дигідропіроло[3,4-с]піразол-1,5дикарбоксилат (2,5м, 5,59ммол) розчиняють у діоксані (50мол) і обробляють 4М розчином НСl в діоксані (28мол, 20екв.). Після нагрівання при 40°С протягом 2 годин (ТШХ: СН2Сl2/МеOН 90/10) реакційну суміш концентрують, до залишку додають діетиловий ефір і відфільтровують, одержуючи вказану в заголовку сполуку (2,09г) у вигляді твердої речовини з виходом 98%. ESI MS: m/z 347 (МН+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 11,28 (с, 1H), 8,06-8,11 (м, 2Н), 7,28-7,34 (м, 2Н), 4,40 (кв., 2Н, J=7,1Гц), 3,92 (с, 2Н), 1,42 (с, 6Н), 1,33 (т, 3Н, J=7,1Гц). За аналогічною методикою одержують наступні сполуки: гідрохлорид етил-3-[(4-фторбензоїл)аміно]-6,6диметил-5,6-дигідро-піроло[3,4-с]піразол2(4Н)карбоксилату ESI MS: m/z 347 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 10,92 (с, 1Н), 9,89 (с, 1H), 8,02 (м, 2Н), 7,49 (м, 2Н), 4,61 (с, 2Н), 4,51 (кв., 2Н, J=7,1Гц), 1,69 (с, 6Н), 1,39 (т, 3Н, J=7,1Гц). гідрохлорид етил-3-[(4-фторбензоїл)аміно]-5,6дигідропіроло[3,4-с]піразол-6-спіроциклопропан2(4Н)карбоксилату ESI MS: m/z 345 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 10,87 (ушир.с, 1H), 10,00 (ушир.с, 2Н), 7,93-8,04 (м, 2Н), 7,39-7,53 (м, 2Н), 4,69 (ушир.с, 2Н), 4,41 (кв., 2Н, J=7,1Гц), 1,68 (дд, 2Н, J=8,6Гц, J=6,1Гц), 1,41 (дд, 2Н, J=8,6Гц, J=6,1Гц), 1,33 (т, 3Н, J=7,1Гц). Приклад 11 Етил-5-(2,2-диметилпропаноїл)-3-[(4фторбензоїл)аміно]-6,6-диметил-5,6дигідропіроло[3,4-с]піразол-1(4Н)карбоксилат До розчину гідрохлориду етил-3-[(4фторбензоїл)аміно]-6,6-диметил-5,6дигідропіроло[3,4-с]піразол-1(4Н)карбоксилату (2,0г, 5,77ммол) в дихлорметані (70мл) при 0°С додають Ν,Ν-діізопропілетиламін (1,6мл, 9,2ммол, 1,6екв.) і півалоїлхлорид (780мкл, 6,3ммол, 1,1екв.). Дають реакційній суміші поступово нагрітись до кімнатної температури і перемішують протягом ночі (ТШХ: СН2Сl2/ЕtOАс 90/10). Реакційну суміш промивають насиченим водним розчином бікарбонату натрію і насиченим розчином солі. Органічну фазу сушать над сульфатом натрію, упарюють і очищають флешхроматографією (елюент: СН2Сl2/ЕtOАс 90/10), одержуючи 2,03г казаної в заголовку сполуки з виходом 82%. ESI MS: m/z 431 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): 6 11,51 (с, 1Н), 8,05-8,14 (м, 2Н), 7,23-7,37 (м, 2Н), 4,90 (с, 2Н), 81790 52 4,42 (кв., 2Н, J=7,1Гц), 1,80 (с, 6Н), 1,33 (т, 3Н, J=7,1Гц), 1,22 (с, 9Н). За аналогічною методикою одержують наступну сполуку: етил-5-(2,2-диметилпропаноїл)-3-[(4фторбензоїл)аміно]-5,6-дигідропіроло[3,4с]піразол-6-спіроциклопропан-2(4Н)карбоксилат ESI MS: m/z 429 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 10,81 (ушир.с, 1H), 7,96-8,04 (м, 2Н), 7,38-7,48 (м, 2Н), 5,10 (ушир.с, 2Н), 4,42 (кв., 2Н, J=7,1Гц), 2,33 (дд, 2Н, J=6,8Гц, J=4,2Гц), 1,32 (т, 3Н, J=7,1Гц), 1,22 (с, 9Н), 0,90 (дд, 2Н, J=6,8Гц, J=4,2Гц). Приклад 12 N-[5-(2,2-диметилпропаноїл)-6,6-диметил1,4,5,6-тетрагідропіроло[3,4-с]піразол-3-іл]-4фторбензамід Етил-5-(2,2-диметилпропаноїл)-3-[(4фторбензоїл)аміно]-6,6-диметил-5,6дигідропіроло[3,4-с]піразол-1(4Н)карбоксилат (2,0г, 4,64ммол) розчиняють в метанолі (60мл), додають TEA (6,45мл, 46,4ммол, 10екв.) і перемішують протягом ночі при кімнатній температурі (ТШХ: СН2Сl2/МеOН 95/5). Після упарювання до одержаної твердої речовини додають суміш діетиловий ефір/гексан і відфільтровують, одержуючи 1,43г вказаної в заголовку сполуки з виходом 86%. ESI MS: m/z 359 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 12,41 (шир. с, 1H), 10,91 (шир. с, 1Н), 7,98-8,11 (м, 2Н), 7,20-7,44 (м, 2Н)5 4,66-4,92 (шир. с, 2Н), 1,64 (с, 6Н), 1,21 (с, 9Н). За аналогічною методикою одержують наступні сполуки: N-[5-(2,2-диметилпропаноїл)-2,4,5,6тетрагідропіроло[3,4-с]піразол-6спіроциклопропан-3-іл]-4-фторбензамід ESI MS: m/z 357 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ 11,59-12,47 (ушир.с, 1Н), 10,94 (ушир.с, 1H), 8,02-8,11 (м, 2Н), 1,21-1,31 (м, 2Η), 4,99 (с, 2Н), 2,25 (дд, 2Н, J=6,5Гц, J=4,4Гц), 1,20 (с, 9Н), 0,79 (дд, 2Н, J=6,5Гц, J=4,4Гц). N-{6,6-диметил-5-[(2R)-тетрагідрофуран-2ілкарбоніл)-1,4,5,6-тетрагідропіроло-[3,4-с]піразол3-іл}-4-фторбензамід ESI MS: m/z 373 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 12,49 (ушир.с, 1H), 10,96 (ушир.с, 1Н), 8,09 (м, 2Н), 7,34 (м, 2Н), 4,86 (м, 2H), 4,56 (т, 1H), 3,83 (м, 2H), 2,02 (м, 2Н), 1,86 (м, 2Н), 1,68 (с, 6Н). αD+27,7 (с=0,50, МеОН) N-{6,6-диметил-5-[(2S)-тетрагідрофуран-2ілкарбоніл)-1,4,5,6-тетрагідропіроло-[3,4-с]піразол3-іл}-4-фторбензамід ESI MS: m/z 373 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 12,49 (ушир.с, 1H), 10,96 (ушир.с, 1H), 8,09 (м, 2Н), 7,34 (м, 2Н), 4,86 (м, 2Н), 4,56 (т, 1Н), 3,83 (м, 2Н), 2,02 (м, 2Н), 1,86 (м, 2Н), 1,68 (с, 6Н). αD-25,9 (с=0,76, МеОН) Приклад 13 Метиловий ефір 4-(1-метилпіперидин-4ілокси)бензойної кислоти До розчину 1-метилпіперидин-4-олу (6,8г, 59ммол), PPh3 (трифенілфосфін, 15,5г, 59ммол) і 53 метилового ефіру 4-гідроксибензойної кислоти (6г, 39ммол) в ТГФ (150мл) при 0°С повільно додають розчин діетилазодикарбоксилату (9,5мл, 59ммол) в ТГФ (30мл). Протягом 24 годину дають реакційній суміші нагрітись до кімнатної температури. Потім реакційну суміш упарюють і залишок знову розчиняють в 5%-ному водному розчині лимонної кислоти (700мл). Розчин промивають етилацетатом (3´250мл), підлуговують концентрованим розчином ΝΗ4ΟΗ (рН~8) і екстрагують дихлорметаном (3´250мл). Дихлорметанові екстракти об'єднують і промивають насиченим розчином солі, сушать і упарюють, одержуючи олію, яку очищають флешхроматографією на силікагелі, використовуючи дихлорметан-МеОН (90:10) як елюент, і одержують вказану в заголовку сполуку у вигляді олії жовтого кольору (7,4г, 75%). ESI MS: m/z 250 (MH+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ м.ч. 1,7 (м, 2Н), 2,0 (м, 2Н), 2,2 (м, 5Н), 2,7 (м, 2Н), 3,8 (с, 3Н), 4,5 (м, 1Н), 7,1 (д, J=9,0 biz, 2Н), 7,9 (д, J=9,0Гц, 2Н). Приклад 14 Гідрохлорид 4-(1-метилпіперидин-4ілокси)бензойної кислоти Метиловий ефір 4-(1-метилпіперидин-4ілокси)бензойної кислоти (7,3г, 29ммол) розчиняють в 6н водному розчині НСl (220мл). Після нагрівання до 85°С протягом 6 годин розчинник видаляють у вакуумі. Залишок розчиняють у воді, двічі упарюють і потім залишок ще двічі обробляють ацетоном. Одержану тверду речовину остаточно розтирають в ацетоні іодержують гідрохлоридну сіль у вигляді порошку білого кольору (6,4г, вихід 80%). 1 H ЯМР (400МГц, ДМСО-d6) δ м.ч. 2,0 (м, 4Н), 2,8 (м, 3Н), 3,3 (м, 4Н), 4,7 (м, 1H), 7,1 (м, 2Н), 7,9 (м, 2Н), 9,9 (д, J=20,4Гц, 1H), 12,6 (с, 1H). Приклад 15 Етиловий ефір 4-(4-гідроксипіперидин-1іл)бензойної кислоти Суміш метилового ефіру 4-фторбензойної кислоти (1,68г, 10ммол), піперидин-4-олу (1,12г, 11ммол) і безводного карбонату калію (1,38г, 10ммол) в ДМСО (10мл) нагрівають протягом 6 годин при температурі 120°С. Після охолоджування суміш виливають у воду з льодом (500мл) і екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі, сушать і упарюють. Залишок очищають флеш-хроматографією на силікагелі, використовуючи гексан/ЕtOАс (10/30) як елюент, і одержують вказану в заголовку сполуку у вигляді твердої речовини білого кольору (1,6г, 64%). ESI MS: m/z 250 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ м.ч. 1,3 (т, 3=1, 1Гц, 3Н), 1,4 (м, 2Н), 1,8 (м, 2Н), 3,0 (м, 2Н), 3,7 (м, 2Н), 4,2 (кв., J=7,1Гц, 2Н), 4,7 (д, J=4,3Гц, 1H), 6,9 (м, 2Н), 7,7 (м, 2Н). Приклад 16 Етиловий ефір 4-(4-фторпіперидин-1іл)бензойної кислоти До розчину етилового ефіру 4 (4гідроксипіперидин-1-іл)бензойної кислоти (1,25г, 5мол) в сухому дихлорметані (30мл) при кімнатній 81790 54 температурі в інертній атмосфері повільно додають розчин DAST (0,97г, 6ммол) в дихлорметані (5мл). Реакційну суміш перемішують при кімнатній температурі протягом 1 годин і потім реакцію гасять водним розчином NaHCO3. Органічний шар промивають насиченим розчином солі, сушать і упарюють. Залишок очищають флеш-хроматографією на силікагелі, використовуючи гексан/EtOAc (70/30) як елюент, і одержують вказану в заголовку сполуку у вигляді твердої речовини білого кольору (0,7г, 56%). ESI MS: m/z 252 (МН+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 1,3 (т, J=7,1Гц, 3Н), 1,8 (м, 2Н), 2,0 (м, 2Н), 3,3 (м, 2Н), 3,6 (м, 2Н), 4,2 (с, 2Н), 4,8 (с, 1H), 7,0 (с, 2Н), 7,8 (с, 2Н). Приклад 17 4-(4-Фторпіперидин-1-іл)бензойна кислота Суміш етилового ефіру 4-(4-фторпіперидин-1іл)бензойної кислоти (0,7г, 2,7ммол) в етанолі (50м) і 2н розчин гідроксиду натрію (20мл) перемішують при кімнатній температурі протягом 24 годину. Етанол випарюють, розчин розбавляють водою (20мл) і нейтралізують 2н НСl. Кислоту виділяють у вигляді білої твердої речовини, яку промивають водою і сушать у вакуумі (0,52г, 82%). ESI MS: m/z 224 (МН+); 1 Н-ЯМР (400МГц, ДМСО-d6): δ м.ч. 1,8 (м, 2Н), 2,0 (м, 2Н), 3,3 (м, 2Н), 3,5 (м, 2Н), 5,0 (с, 1Н), 7,0 (с, 2Н), 7,8 (с, 2Н), 12,2 (с, 1H). Відповідно до вищезгаданих методик, описаних в будь-якому з наведених вище прикладів, використовуючи відповідні вихідні речовини і будь-які відповідні реагенти, також одержують додаткові сполуки формули (Іа) і (Іb), як показано в наведеній нижче Таблиці III. Для пояснення системи позначення, застосованої для ідентифікації конкретних сполук формули (Іа) і (Іb), див. розділ "Загальний метод" на початку експериментальної частини даного опису. 55 81790 56 57 81790 58 Приклад 18 N-{6,6-диметил-5-[(1-метилпіперидин-4іл)карбоніл]-2,4,5,6-тетра-гідропіроло[3,4с]піразол-3-іл}-4-фторбензамід До розчину гідрохлориду етил-3-[(4фторбензоїл)аміно]-6,6-диметил-5,6дигідропіроло[3,4-с]піразол-1(4Н)карбоксилату (0,5г, 1,3ммол) в дихлорметані (25мл) додають Ν,Ν-діізопропілетиламін (1,13мл, 6,5ммол, 5екв.) і TBTU (0,542г, 1,69ммол, 1,3екв.), перемішують при кімнатній температурі протягом 1 годину і потім додають гідрохлорид 1-метилпіперидин-4карбонової кислоти (0,29г, 1,61ммол, 1,2екв.). Реакційну суміш перемішують протягом ночі (ТШХ: СН2Сl2/МеOН 90/10). Розчин промивають насиченим водним розчином бікарбонату натрію і насиченим розчином солі, органічну фазу сушать над сульфатом натрію і концентрують. Залишок розчиняють в метанолі (16мл), додають TEA (2мл, 14,3ммол, 11екв.) і перемішують протягом ночі при кімнатній температурі (ТШХ: CH2Cl2/MeOH/NH4OH 90/10/1). Після випарювання тверду речовину очищають флеш-хроматографією (елюент: CH2Cl2/MeOH/NH4OH 90/10/2). Тверду речовину обробляють діізопропіловим ефіром і фільтрують, одержуючи 0,36 г вказаної в заголовку сполуки з виходом 69%. ESI MS: m/z 400 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 12,48 (ушир.с, 1H), 10,97 (ушир.с, 1H), 8,09 (м, 2Н), 7,35 (м, 2Η), 4,75 (ушир.с, 2Η), 2,87 (м, 2Η), 2,40 (м, 1Н), 2,24 (с, 3Н), 2,05 (м, 2Н), 1,67 (м, 10Н). За аналогічною методикою одержують наступну сполуку: N-[5-[1-метилпіперидин-4іл)карбоніл]-2,4,5,6-тетрагідропіроло[3,4-с]піразол6-спіроциклопропан-3-іл]-4-фторбензамід ESI MS: m/z 398 (MH+); 1 H-ЯМР (400МГц, ДМСО-d6): δ 12,20 (ушир.с, 1H), 11,00 (с, 1Н), 8,10 (м, 2Н), 7,36 (м, 2Н), 4,91 (с, 2Н), 2,84 (м, 2Н), 2,40 (м, 1Н), 2,23 (м, 5Н), 2,0 (м, 2Н), 1,65 (м, 4Н), 0,89 (м, 2Н). Відповідно до вищезгаданих методик, використовуючи відповідні вихідні речовини і будь 59 які відповідні реагенти, також одержують додаткові сполуки формули (Іа) і (Іb), як показано у наведеній нижче Таблиці IV. 81790 60
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted derivatives of pyrolopyrazol as kinaze inhibitors
Автори англійськоюBRASCA MARIA GABRIELLA, AMICI RAFFAELLA, DANIELE FANCELLI, NESI MARCELLA, ORSINI PAOLO, ORZI FABRIZIO, ROUSSEL PATRICK, VULPETTI ANNA, PEVARELLO PAOLO
Назва патенту російськоюЗамещенные пиролопиразольные производные как ингибиторы киназы
Автори російськоюБраска Мария Габриэлла, Амичи Раффаэлла, Фанчелли Даниеле, Нэзи Марчелла, Орзини Паоло, Орци Фабрицио, Руссель Патрик, Вульпэтти Анна, Певарэлло Паоло
МПК / Мітки
МПК: C07D 487/04, A61P 35/00, A61P 25/28, A61P 17/00
Мітки: похідні, піролопіразольні, кінази, інгібітори, заміщені
Код посилання
<a href="https://ua.patents.su/39-81790-zamishheni-pirolopirazolni-pokhidni-yak-ingibitori-kinazi.html" target="_blank" rel="follow" title="База патентів України">Заміщені піролопіразольні похідні як інгібітори кінази</a>












