Композиція уповільненої дії, що містить глюкуронатну сіль сполук піперазину, та її застосування
Номер патенту: 96930
Опубліковано: 26.12.2011
Автори: Ерншпергер Ерік С., Алі Кадум, Фавзі Махді Б., Діоріо Крістофер Р., Шах Суед Музафар
Формула / Реферат
1. Композиція уповільненої дії, яка містить сполуку 2:
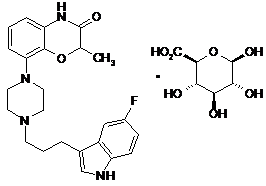 2
2
та компонент, що забезпечує уповільнене виділення.
2. Композиція за п. 1, яка містить гіпромелозу, мікрокристалічну целюлозу та лубрикант.
3. Композиція за п. 1, яка пресована у таблетку.
4. Багатокомпонентна композиція, яка містить ядро-гранулу з вмістом сполуки 2:
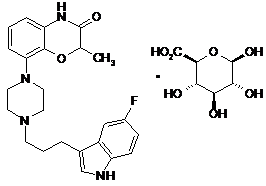 , 2
, 2
суцільне покриття, що не впливає на швидкість виділення сполуки 2, таке як гідроксипропілцелюлоза, гіпромелоза або полівініловий спирт, та функціональне суцільне покриття, що впливає на швидкість виділення сполуки 2, таке як етилцелюлоза та похідні поліметакрилату.
5. Композиція уповільненої дії, яка містить сполуку 2:
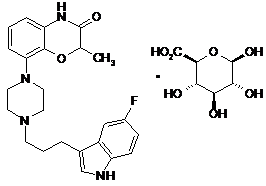 , 2
, 2
для використання у лікуванні або послабленні симптомів одного або кількох розладів, вибраних з хвороби Паркінсона, психозів (наприклад, шизофренії, маніакально-депресивного психозу, гострої депресії та біполярних розладів), депресії, стресу та втомленості, хвороби Альцгеймера, хвороби Гантінгтона, панічного синдрому, синдрому нав'язливих станів, розладів харчування, наркозалежності, соціальних фобій, агресивності або збудження, мігрені, склеродермії та хвороби Рейно, блювання, розладів шлунково-кишкового тракту, пов'язаних з регулюванням перистальтики, синдрому втомлених ніг та секреції пролактину з новоутворень гіпофізу.
6. Композиція за п. 5, де зазначеним розладом є хвороба Паркінсона.
7. Композиція за п. 5, де зазначеним розладом є психоз, вибраний з шизофренії, маніакально-депресивного психозу, гострої депресії та біполярних розладів.
8. Композиція за п. 5, де зазначеним розладом є депресія, стрес/страх, розлади панічного типу, синдром нав’язливих станів, розлади харчування, наркозалежність або соціальна фобія.
9. Композиція за п. 5, де зазначеним розладом є агресивність або збудження.
10. Композиція за п. 5, де зазначеним розладом є хвороба Альцгеймера, хвороба Гантінгтона, мігрень, склеродермія та хвороба Рейно, блювання, розлади шлунково-кишкового тракту, пов'язані з регулюванням перистальтики, синдром втомлених ніг та секреція пролактину з новоутворень гіпофізу.
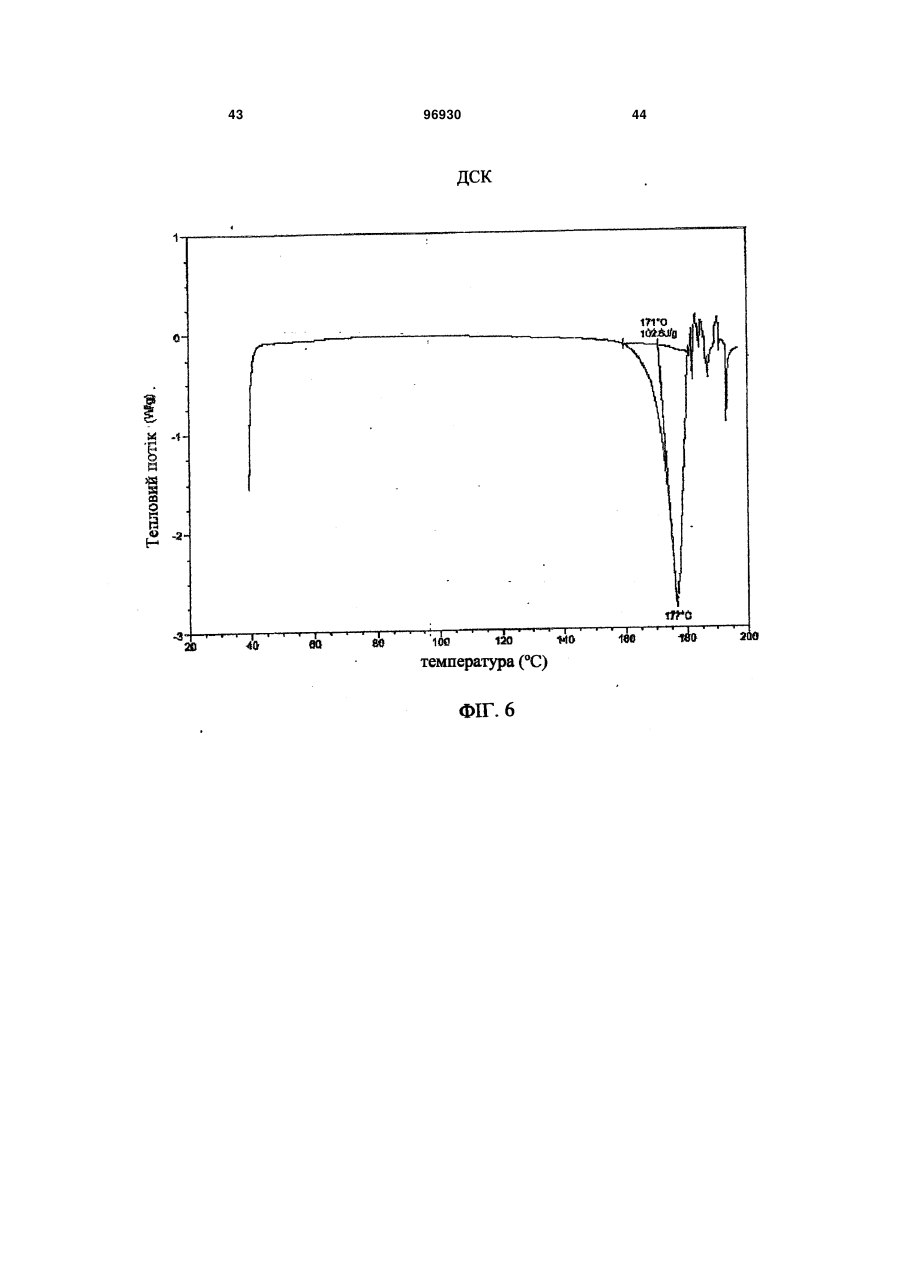
11. Композиція за п. 1, яка містить форму І сполуки 2, що має один або кілька піків, вибраних з близько 17,5, 22,5, 19,9, 3,9 та 12,2 градусів 2-тета, та одну або кілька додаткових твердих форм сполуки 2.
12. Композиція за п. 11, яка містить форму І сполуки 2 та одну або кілька з форми II, що має характерний пік при 18,7 градусах 2-тета на порошковій рентгенодифракційній картині, гідрат сполуки 2, сольват сполуки 2 або аморфну сполуку 2.
13. Застосування сполуки 2
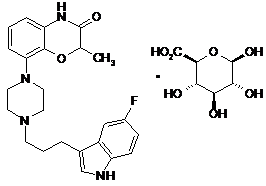 2
2
для одержання препарату у вигляді композиції уповільненої дії для лікування або послаблення симптомів одного або кількох розладів, вибраних з хвороби Паркінсона, психозів, які включають шизофренію, маніакально-депресивний психоз, гостру депресію та біполярні розлади, депресії, стресу/страху, хвороби Альцгеймера, хвороби Гантінгтона, панічного синдрому, синдрому нав'язливих станів, розладів харчування, наркозалежності, соціальних фобій, агресивності або збудження, мігрені, склеродермії та хвороби Рейно, блювання, розладів шлунково-кишкового тракту, пов'язаних з регулюванням перистальтики, синдрому втомлених ніг та секреції пролактину з новоутворень гіпофізу.
Текст
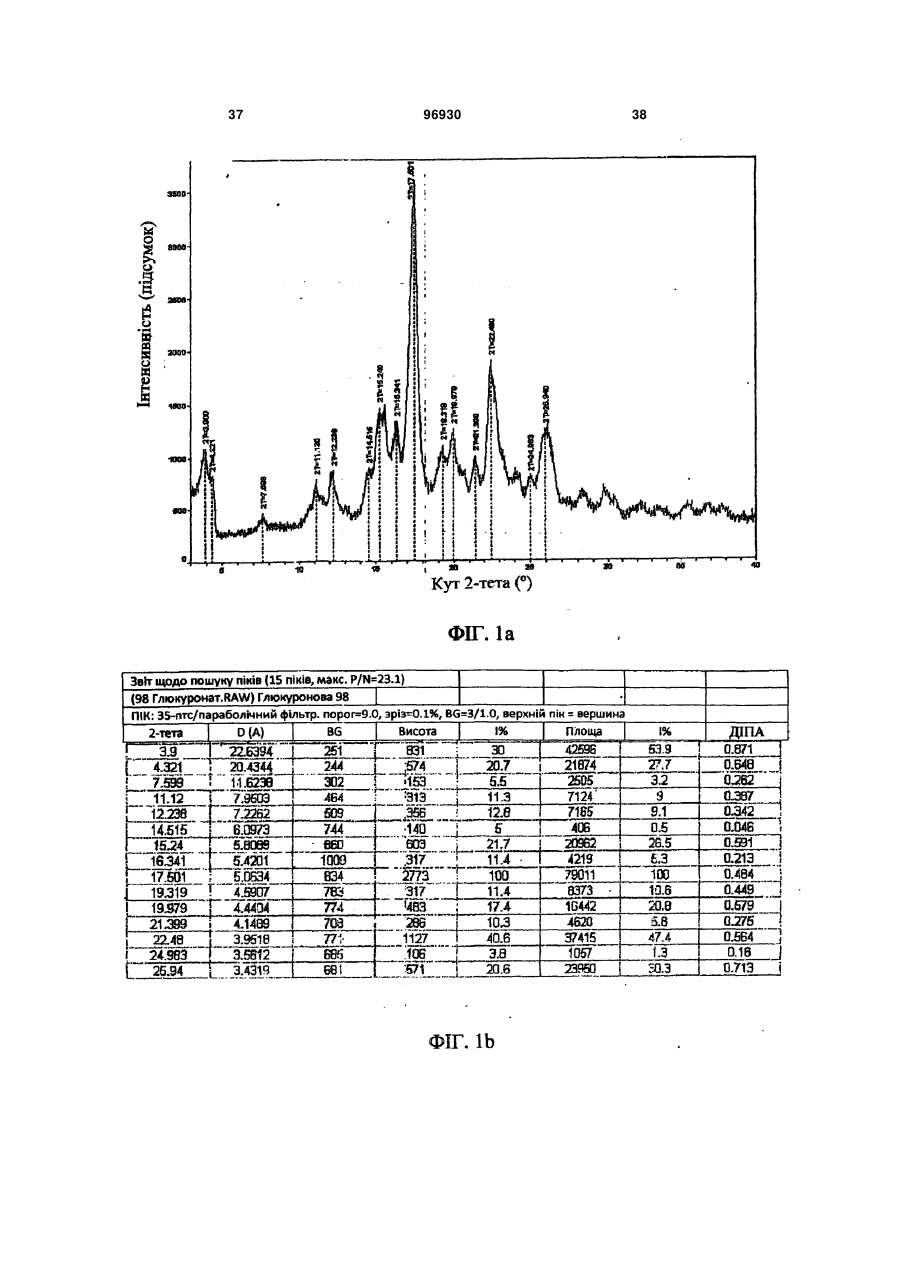
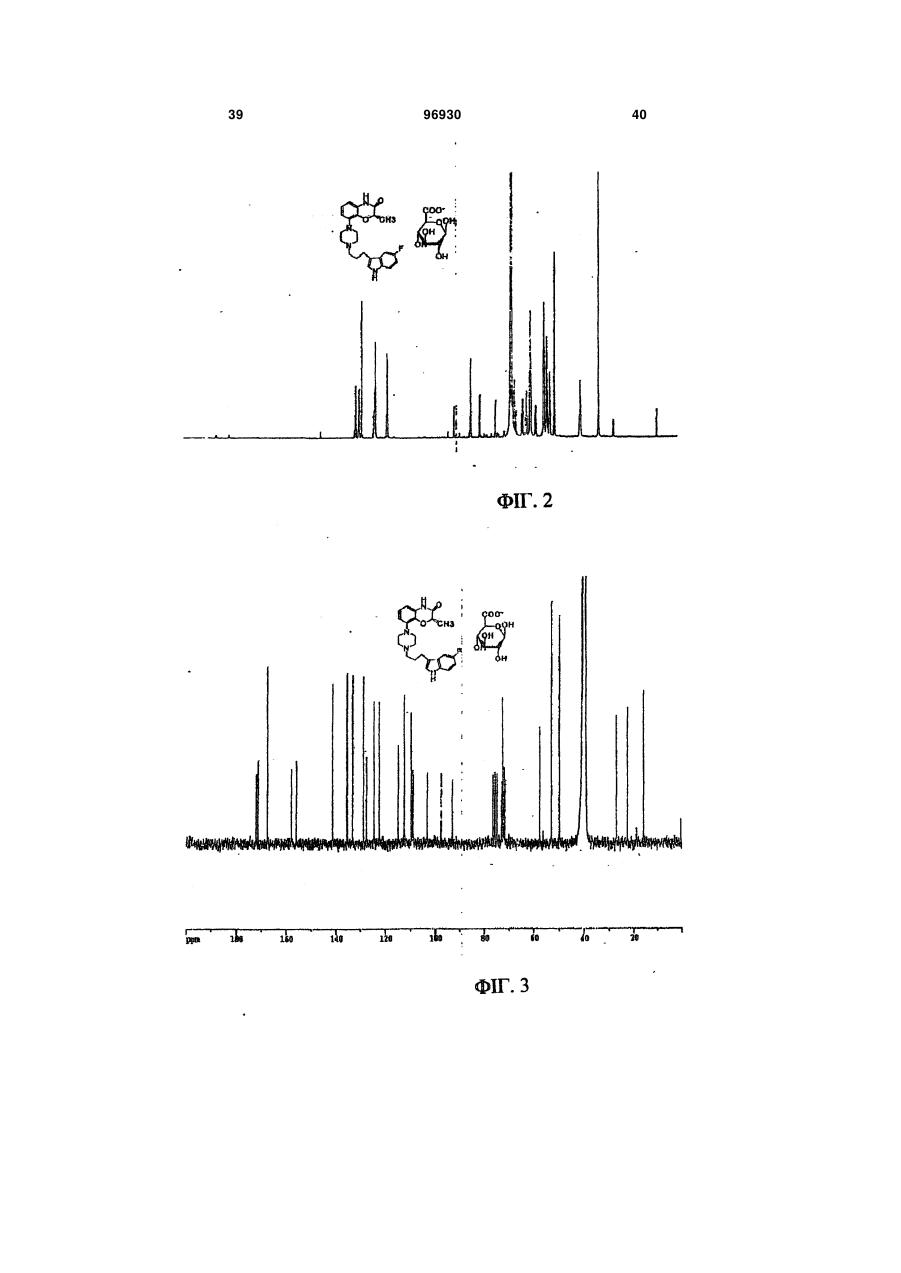
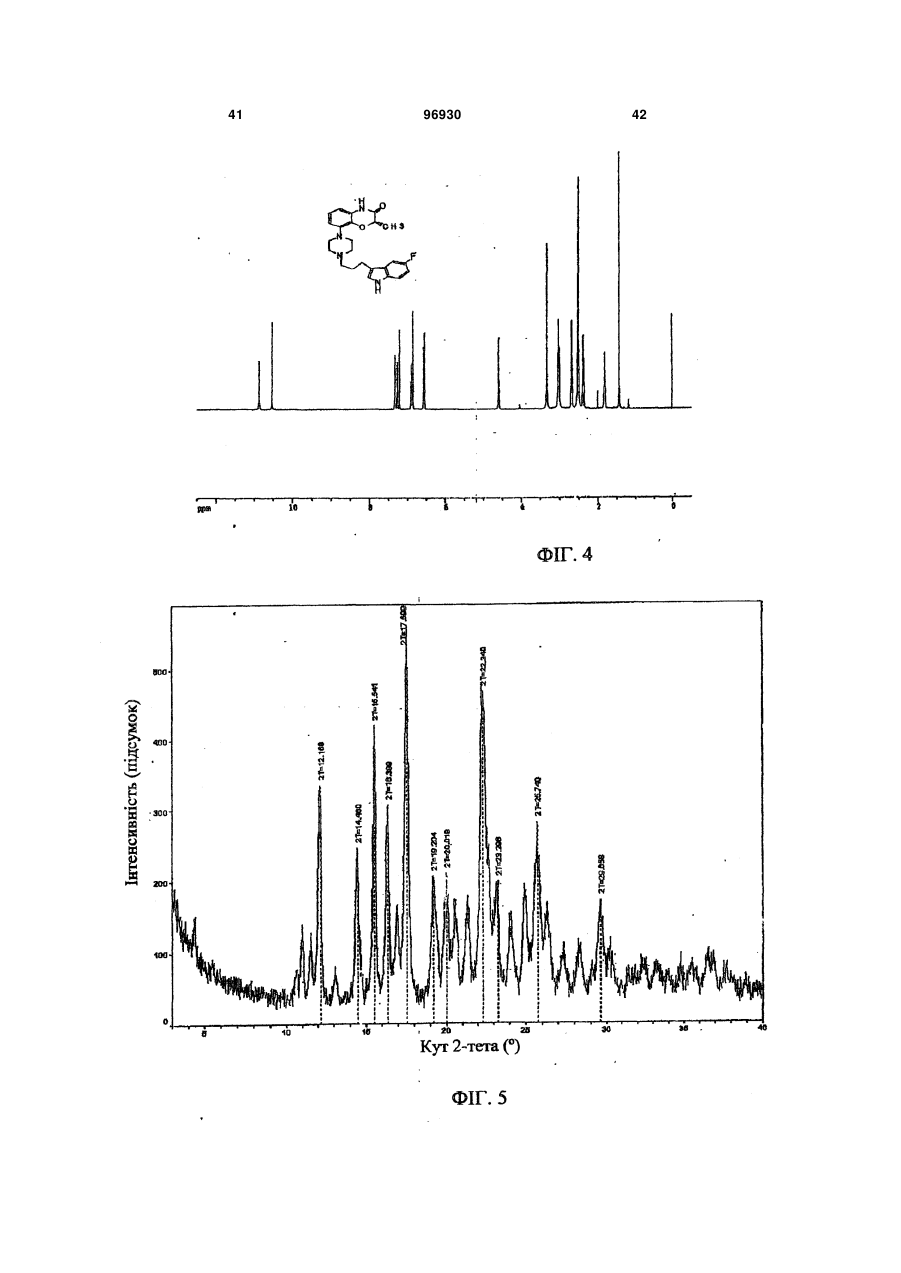
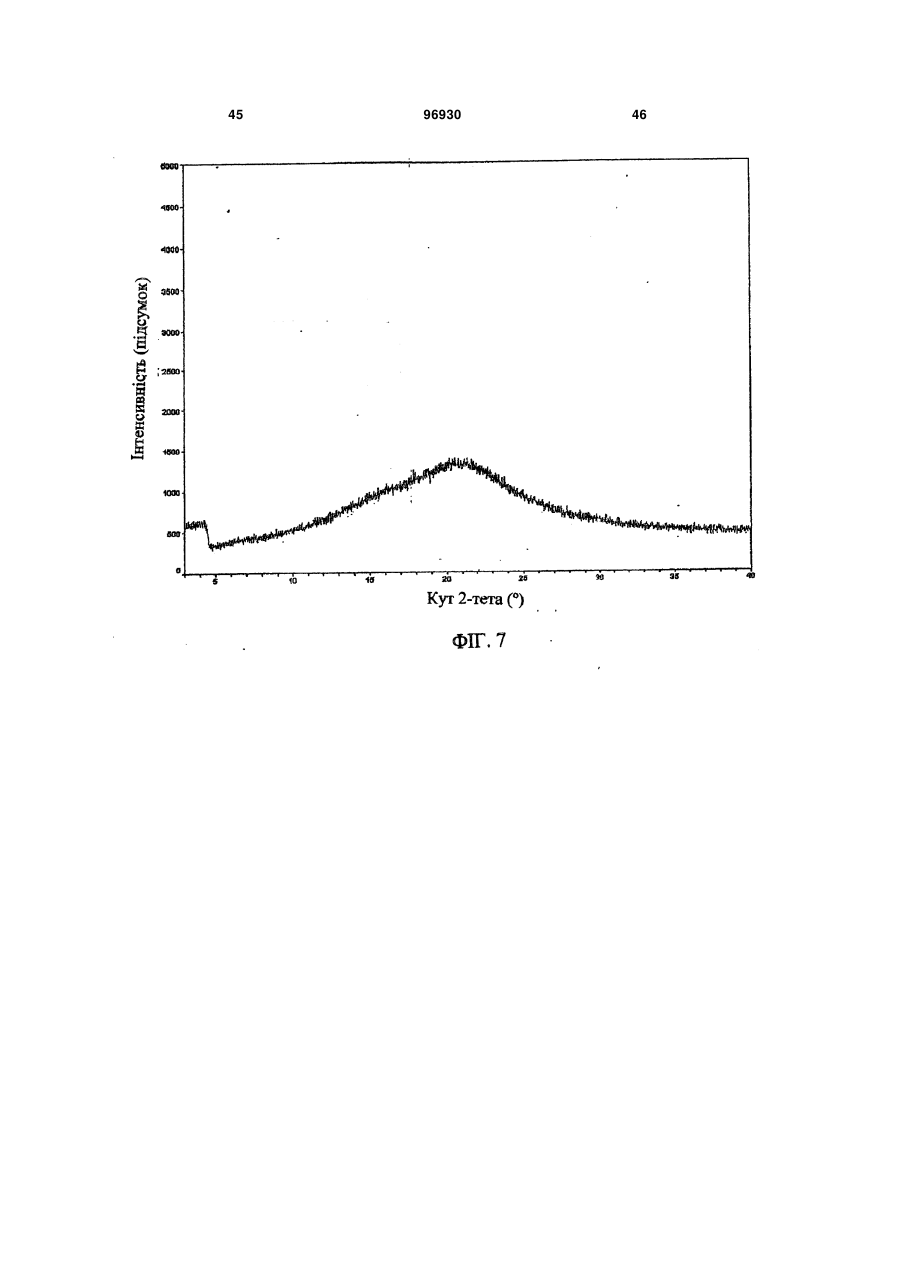
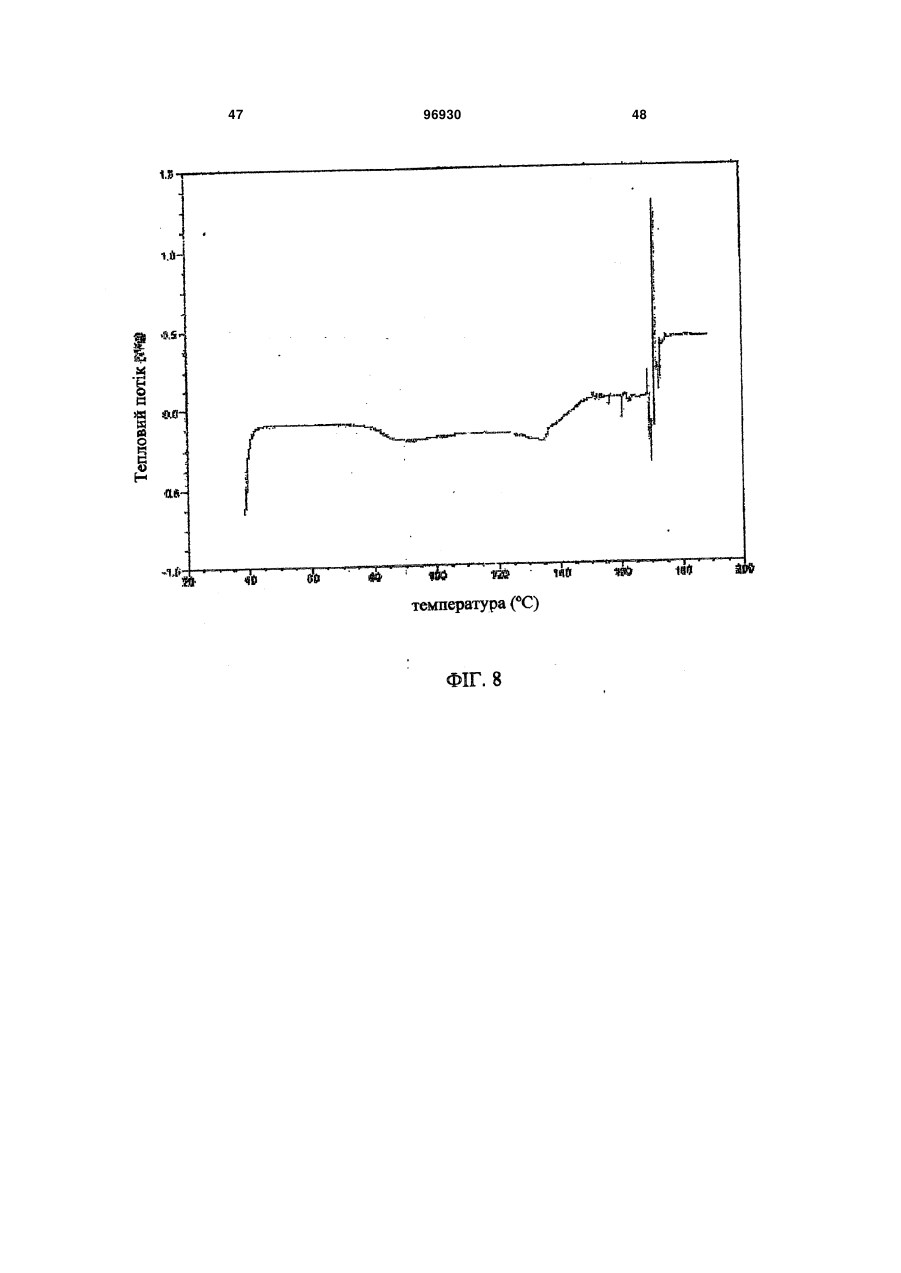
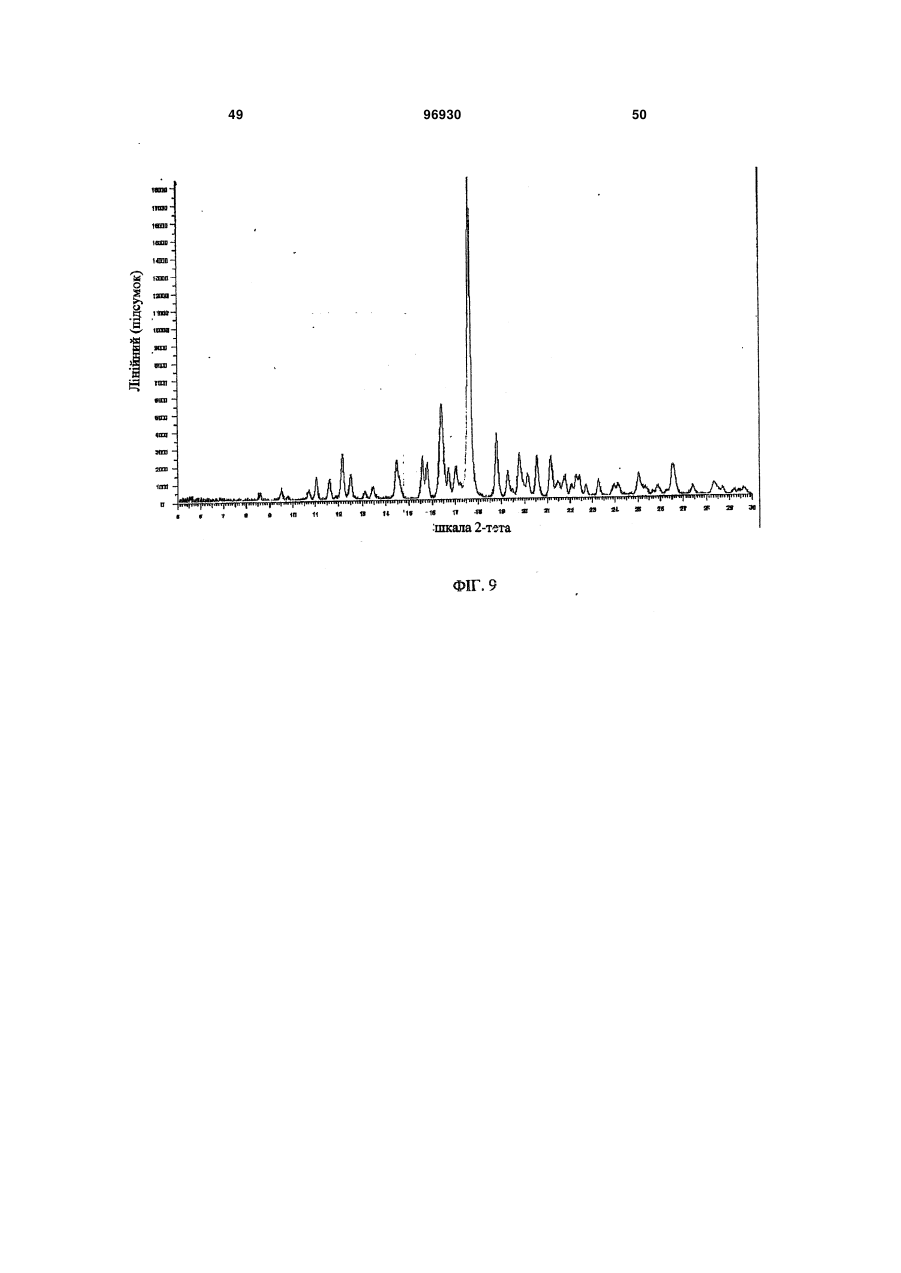
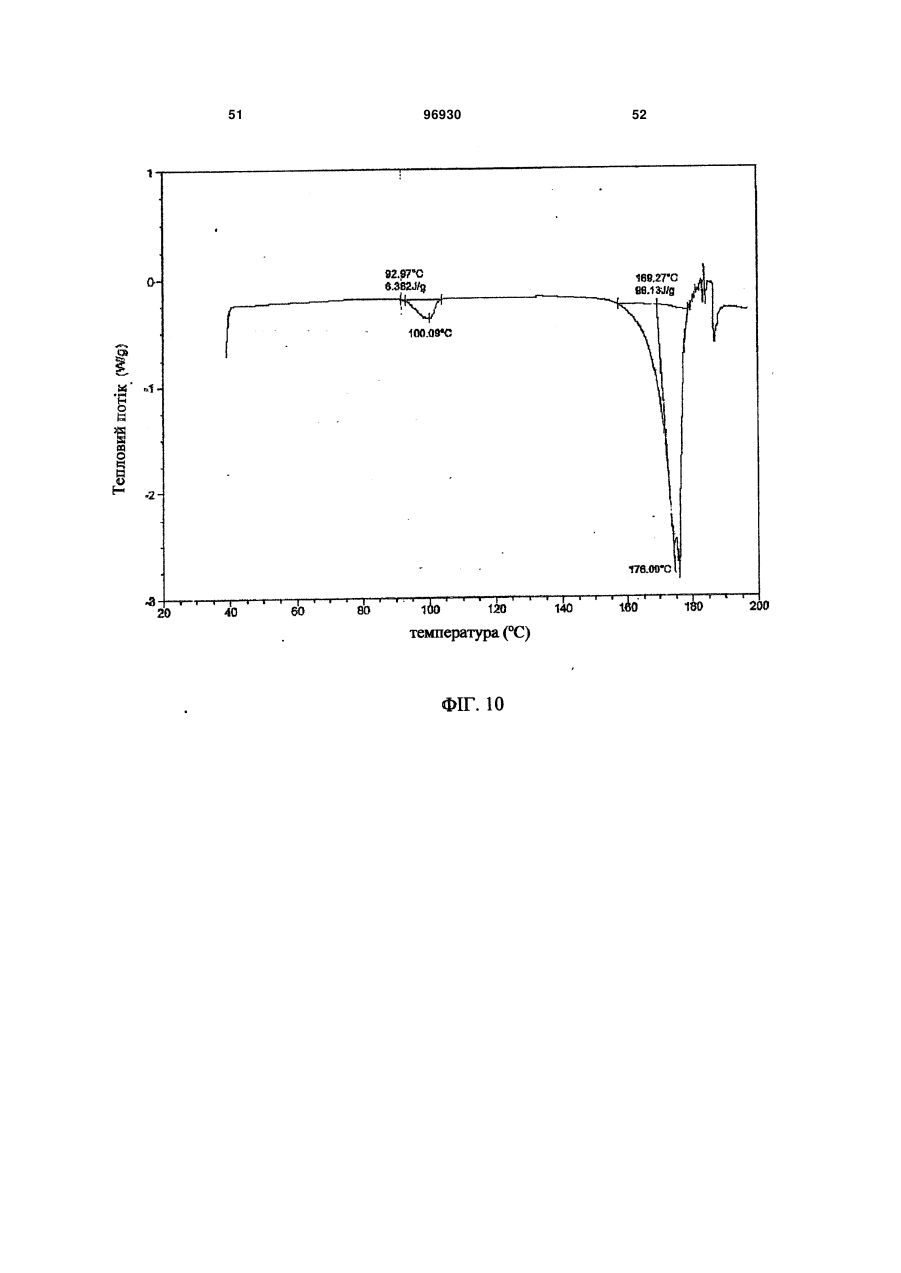
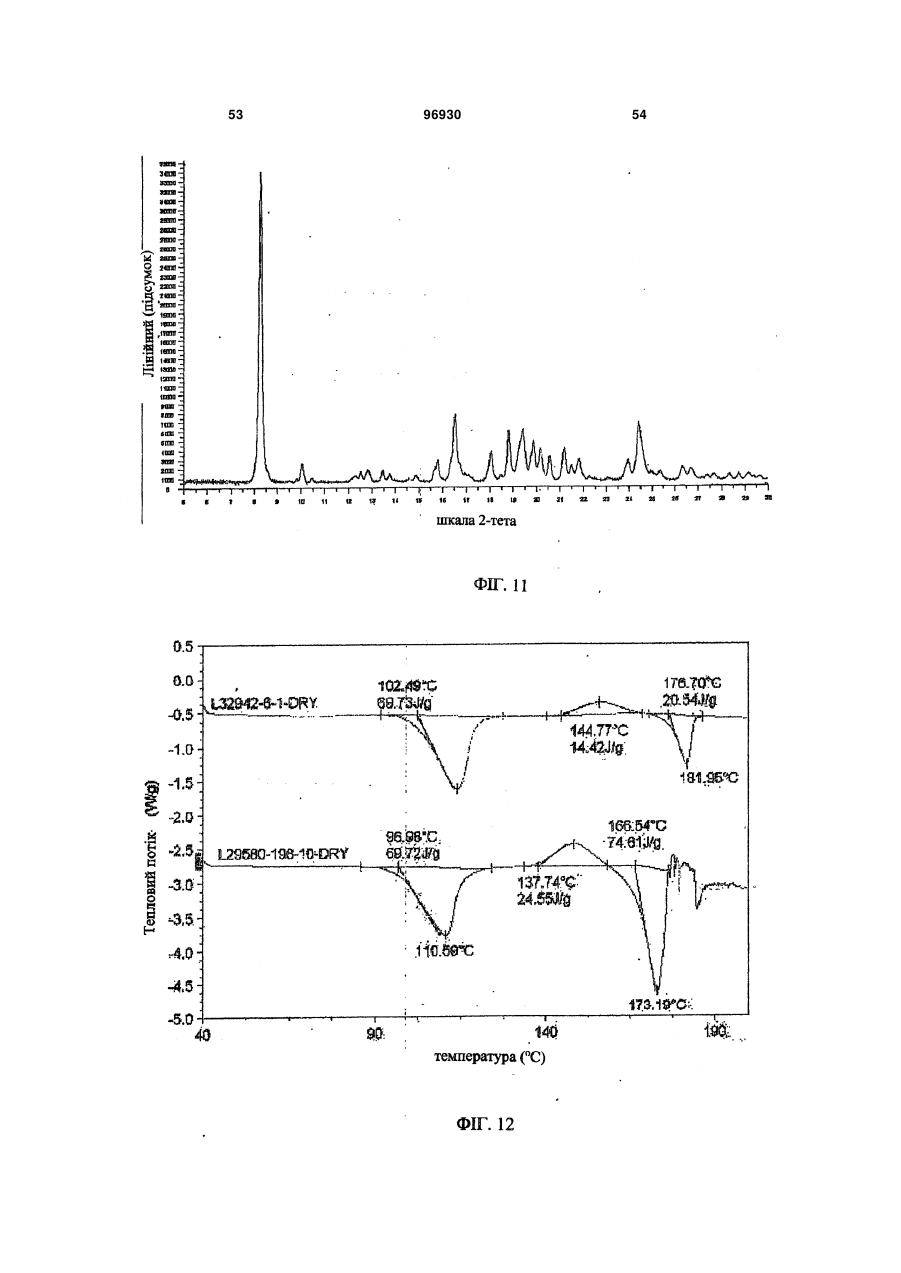
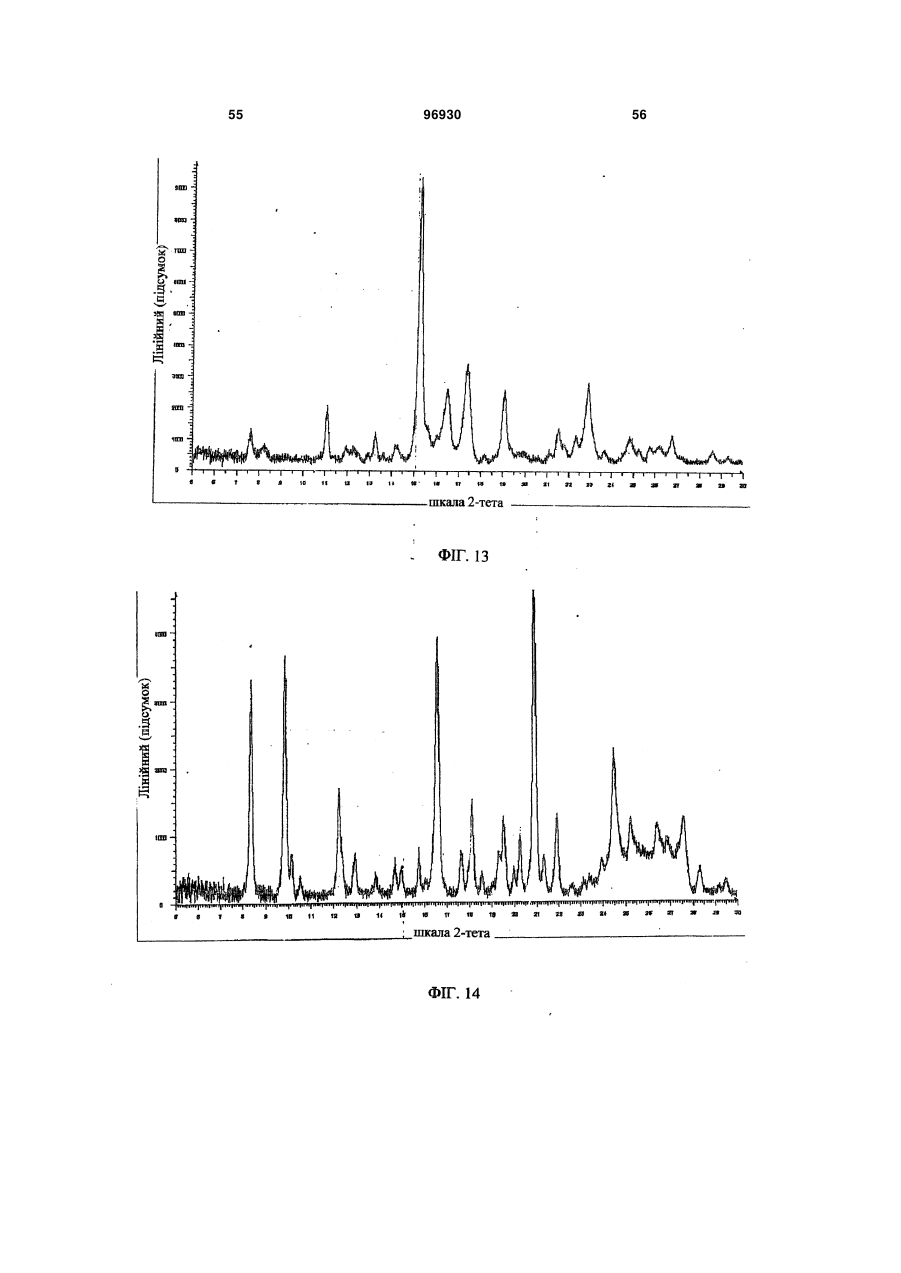
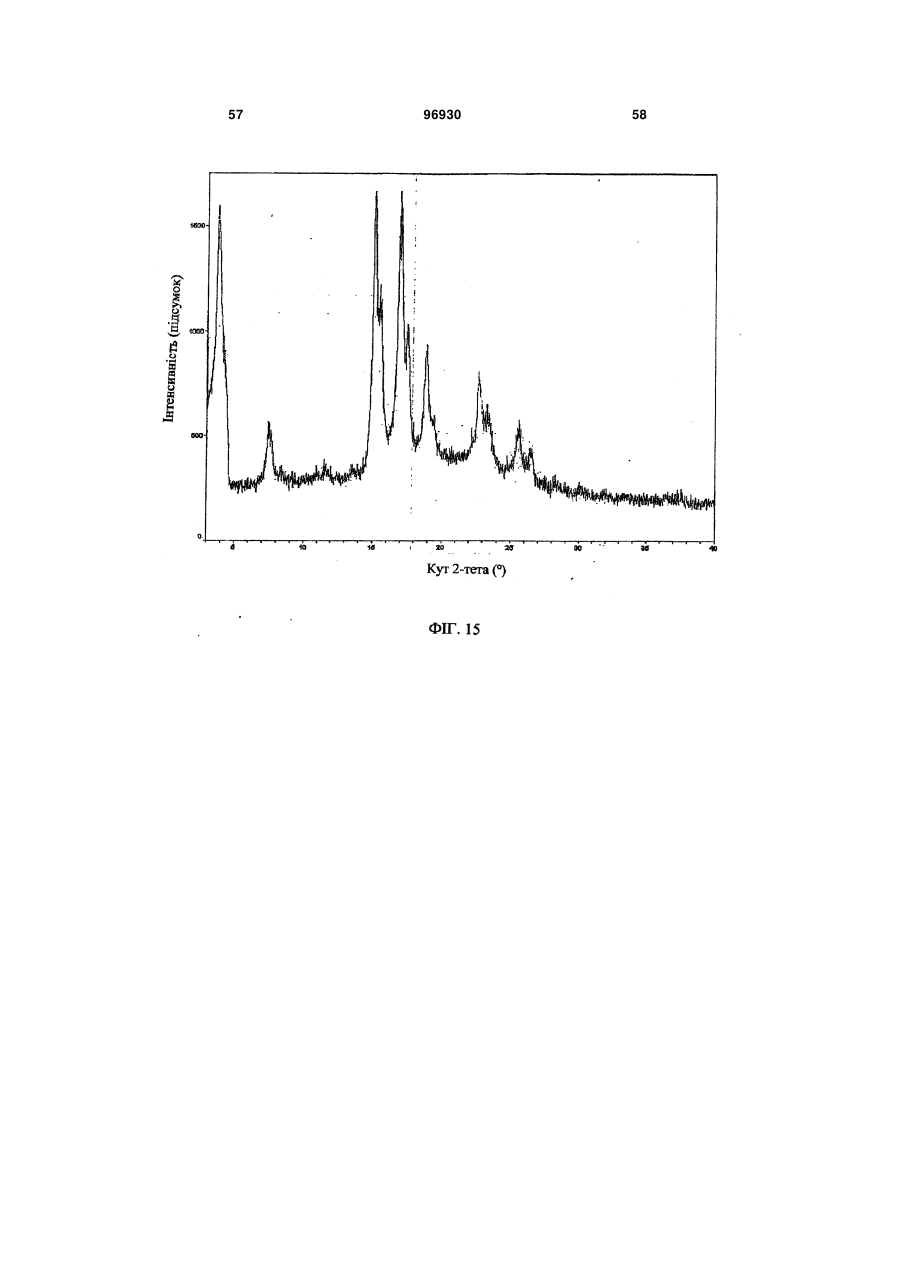
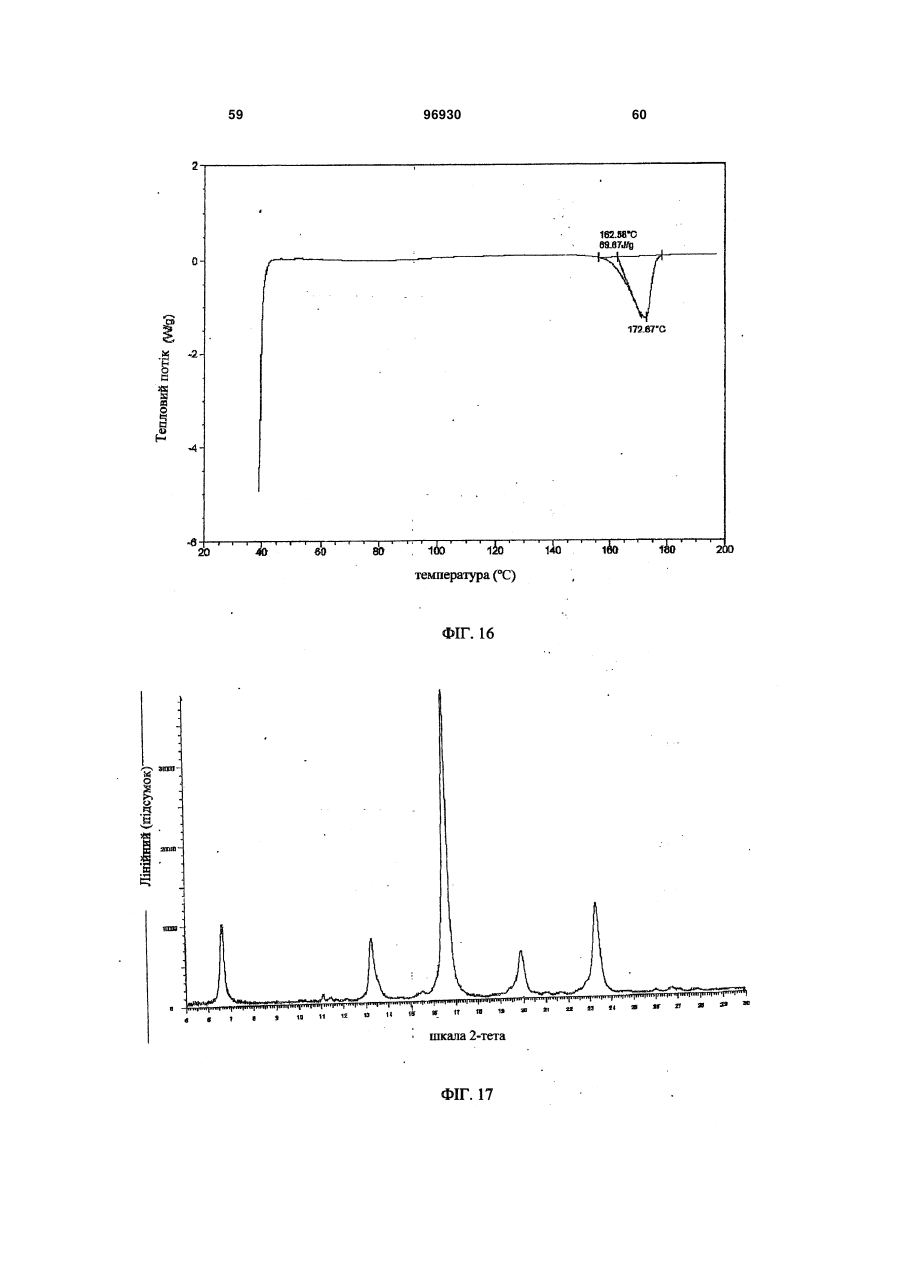
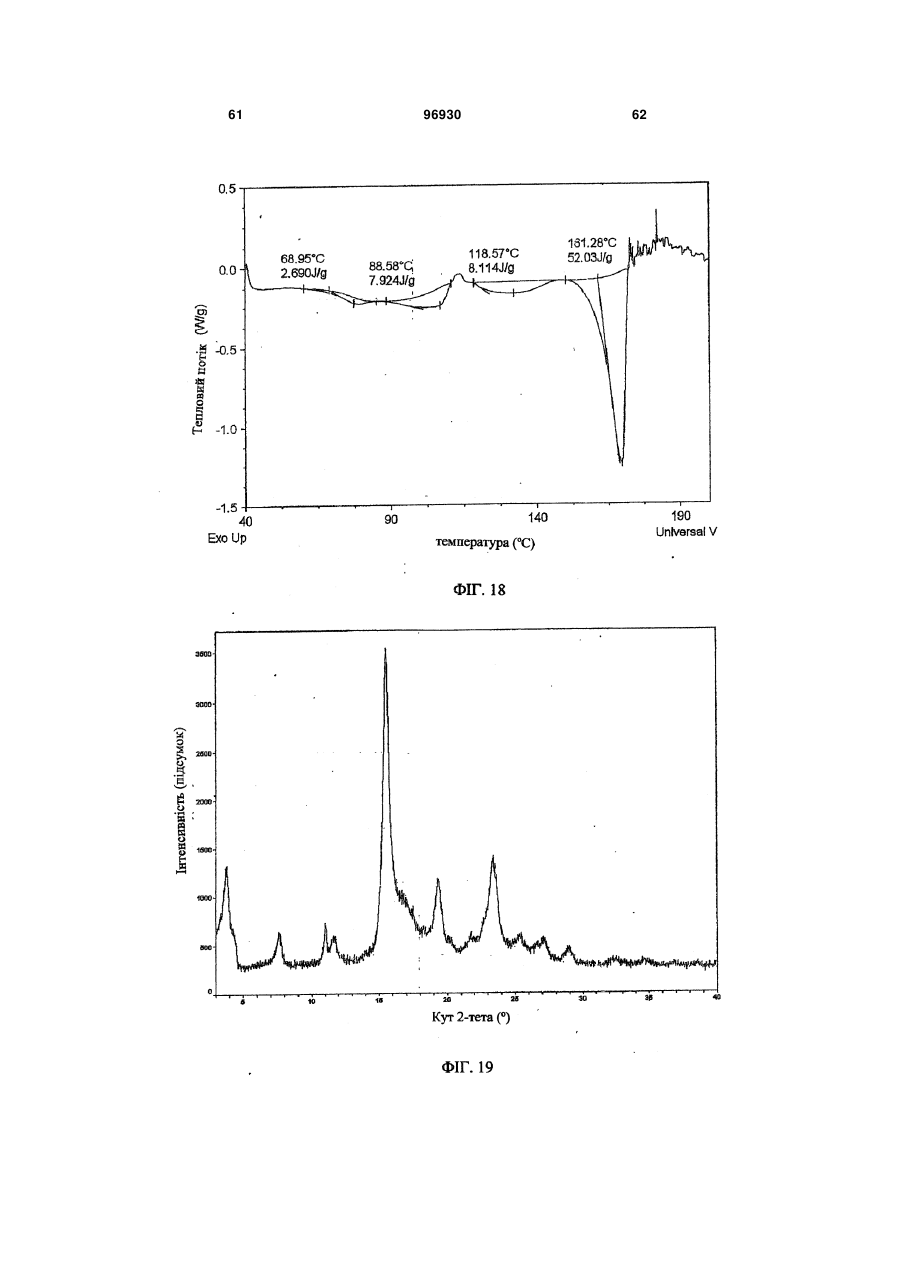
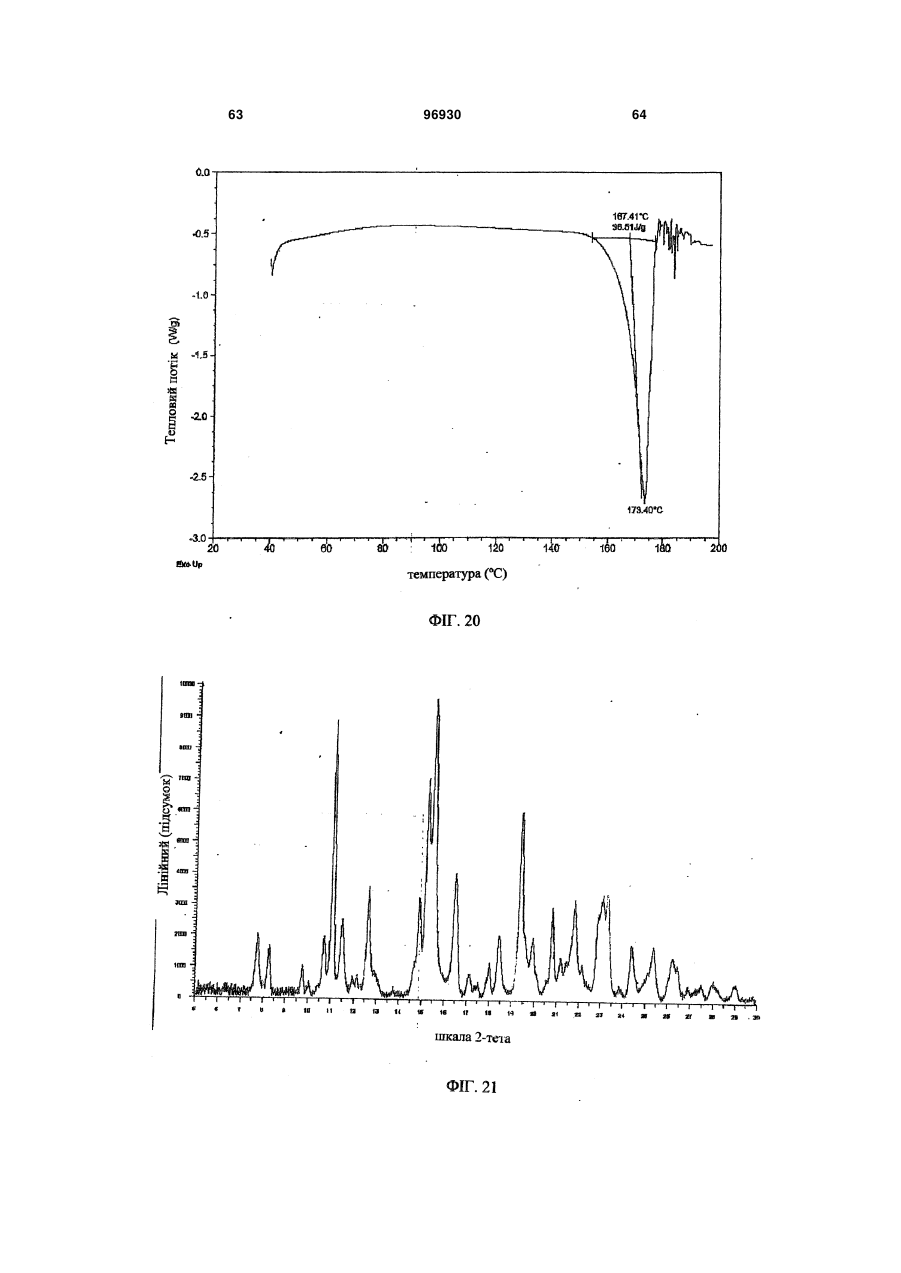
1. Композиція уповільненої дії, яка містить сполуку 2: 3 96930 4 ливих станів, розладів харчування, наркозалежності, соціальних фобій, агресивності або збудження, мігрені, склеродермії та хвороби Рейно, блювання, розладів шлунково-кишкового тракту, пов'язаних з регулюванням перистальтики, синдрому втомлених ніг та секреції пролактину з новоутворень гіпофізу. 6. Композиція за п. 5, де зазначеним розладом є хвороба Паркінсона. 7. Композиція за п. 5, де зазначеним розладом є психоз, вибраний з шизофренії, маніакальнодепресивного психозу, гострої депресії та біполярних розладів. 8. Композиція за п. 5, де зазначеним розладом є депресія, стрес/страх, розлади панічного типу, синдром нав’язливих станів, розлади харчування, наркозалежність або соціальна фобія. 9. Композиція за п. 5, де зазначеним розладом є агресивність або збудження. 10. Композиція за п. 5, де зазначеним розладом є хвороба Альцгеймера, хвороба Гантінгтона, мігрень, склеродермія та хвороба Рейно, блювання, розлади шлунково-кишкового тракту, пов'язані з регулюванням перистальтики, синдром втомлених ніг та секреція пролактину з новоутворень гіпофізу. 11. Композиція за п. 1, яка містить форму І сполуки 2, що має один або кілька піків, вибраних з близько 17,5, 22,5, 19,9, 3,9 та 12,2 градусів 2-тета, та одну або кілька додаткових твердих форм сполуки 2. 12. Композиція за п. 11, яка містить форму І сполуки 2 та одну або кілька з форми II, що має харак терний пік при 18,7 градусах 2-тета на порошковій рентгенодифракційній картині, гідрат сполуки 2, сольват сполуки 2 або аморфну сполуку 2. 13. Застосування сполуки 2 Пріоритет цього винаходу вимагається за тимчасовою заявкою на видачу патенту США № 60/716066 від 12 вересня 2005 p., текст якої повністю включений до цієї заявки як посилальний матеріал. Цей винахід стосується сольових форм та композицій на їх основі, придатних у якості модуляторів одного або кількох GPCR. Родина зв'язуючих G-протеїни рецепторів (GPCR) - це найбільша відома сукупність генів, яка займає 1% геному людини й виконує широку низку біологічних функцій (у тому числі різноманітні аутокринні, паракринні та ендокринні процеси). Надродина генів GPCR найчастіше використовується у фармації для розробки лікувальних сполук. GPCR поділяються на родопсиноподібні GPCR, секретиноподібні GPCR, рецептори цАМФ, сумісні з грибами рецептори феромонів та метаботропні рецептори глутаматів. Родопсиноподібні GPCR - це дуже численна родина, до якої входять рецептори гормонів, нейтротрансмітерів та світла, які передають позаклітинні сигнали шляхом взаємодії з протеїнами, що зв'язують гуанінові нуклеотиди (Gпротеїнами). Хоча ліганди, що активують їх, суттєво розрізняються за структурою та характером, послідовності амінокислот у родопсиноподібних GPCR дуже схожі між собою і, як вважається, посідають спільну структурну форму, яка містить 7 трансмембранних (TM) а-спіралей, і пов'язуються з G-протеїнами усередині клітини, які дисоціюють від рецептора, зв'язуючись з агоністом, та ініцію ють або інгібують сигнальні механізми вторинних месенджерів. Див.: Lander et al. Nature 409:860 th (2001); Basic and clinical pharmacology, 8 Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001). Родина родопсиноподібних GPCR охоплює кілька класів рецепторів, які по-різному розподіляються у центральній нервовій системі (ЦНС) та багатьох периферійних сайтах, проявляючись у найрізноманітніших станах ЦНС та нейропсихічної сфери. До таких належать рецептори допаміну ("D") та 6 або 7 головних підтипів рецепторів серотоніну (5-гідроксітриптаміну, "5НТ") (підтипи рецепторів 5HT1, 2 та 4-7 належать до GPCR, у той час як підтипи рецепторів 5НТ3 - це канали для іонів + + Na /K , які відкриваються лігандами). Допамінні нейрони у хребтовій центральній нервовій системі пов'язані з ініціюванням та виконанням рухів, підтриманням емоційної стабільності та регулюванням функції гіпофізу. Допамін, прив'язуючись до позаклітинних зв'язувальних рівчачків рецепторів D, активує G-протеїни - підтипи рецепторів D1 та D5 ("D1-подібні") прив'язуються до стимулювальних G-протеїнів, а підтипи рецепторів 2-4 ("D2-подібні") - до інгібувальних G-протеїнів. D2-подібні рецептори знаходяться скрізь у мозку, у гладких м'язах та у пресинаптичних нервових закінченнях і справляють інгібувальну дію на нейротрансмісію, коли зв'язуються агоністом. Зокрема, великі скупчення рецепторів D2 зосереджені у смугастому тілі, лімбічній системі, зоровому бугрі, гі H N O O CH3 HO2C . N F O HO OH OH OH N NH 2 для одержання препарату у вигляді композиції уповільненої дії для лікування або послаблення симптомів одного або кількох розладів, вибраних з хвороби Паркінсона, психозів, які включають шизофренію, маніакально-депресивний психоз, гостру депресію та біполярні розлади, депресії, стресу/страху, хвороби Альцгеймера, хвороби Гантінгтона, панічного синдрому, синдрому нав'язливих станів, розладів харчування, наркозалежності, соціальних фобій, агресивності або збудження, мігрені, склеродермії та хвороби Рейно, блювання, розладів шлунково-кишкового тракту, пов'язаних з регулюванням перистальтики, синдрому втомлених ніг та секреції пролактину з новоутворень гіпофізу. 5 поталамусі та гіпофізі. Антагоніст, прив'язуючись до рецепторів D2, інгібує зв'язування агоніста й таким чином запобігає стримуванню праці наступних сигнальних механізмів. Антагоністи рецепторів D2 використовуються при лікуванні психозів (наприклад, шизофренії, манії, гострої депресії, біполярних розладів), вони здатні на короткий час гамувати агресію або збудження (як от амісульприд, клозапин, галоперідол, немонаприд, пімозид, ремоксіприд, спіперон, сульпірид) та лікувати наркозалежність, тоді як агоністи рецепторів D2 є корисні при лікуванні хвороби Паркінсона та для придушення секреції пролактину з новоутворень гіпофізу (наприклад, апоморфін, бромкріптин, дігідроерготамін, пірібедил, хінпірол), а також для лікування синдрому втомлених ніг (RLS), наприклад, праміпексол, ропінірол). Див.: Basic and th clinical pharmacology, 8 Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001); Pharmacology, th 4 Ed., Rang et al. Edinburgh, UK: Harcourt Publishers (2001); Sedvall et al. The Lancet, 346:743749, (1995); Hietala. The Lancet, 346:1130-1131 (1995); Kemppainen et al. Eur J Neurosci., 18:149154 (2003). 5-гідроксітриптамін надзвичайно поширений у рослинних та тваринних організмах. Це важливий нейротрансмітер і локальний гормон у ЦНС та кишковику, який бере участь у безлічі фізіологічних та патофізіологічних процесів. Прив'язування 5гідроксітриптаміну до позаклітинних зв'язувальних рівчачків рецепторів 5HT активує G-протеїни - відомо, що рецептори підтипу 5HT1 прив'язуються до стимулювальних G-протеїнів, а підтипи рецепторів 2, 4, 6 та 7 - до інгібувальних G-протеїнів. При цьому підтипи рецепторів 5HT1 (їх відомо принаймні 5) знаходяться переважно у мозку та мозкових кровоносних судинах, де вони виступають медіаторами нейроінгібування та звуження судин. Специфічні агоністи рецепторів 5HT1 використовуються для лікуванні мігрені (наприклад, суматриптан) та стресу й втомленості (буспірон), а антагоністи рекомендовані для лікування психозів (спіперон, метіотепин). Крім того, регулювання підтипів рецептора 5HT1 має місце при лікуванні наркозалежності, хвороби Альцгеймера, хвороби Паркінсона, депресії, блювання та розладів харчування. Підтипи рецептора 5НТ2 (відомі принаймні 3) розсіяні в усій ЦНС та на багатьох периферійних сайтах, де вони чинять дію на збуджувальні нейрони та гладкі м'язи. Антагоністи рецепторів 5НТ2 лікують мігрені (метисергід) і є перспективними проти склеродермії та хвороби Рейно (кетансерин). Рецептори 5НТ3 розташовані переважно у периферійній нервовій системи, і їх антагоністи слугують протиблювальними засобами (ондансетрон, тропісетрон). Рецептори 5НТ4 знаходяться у мозку, а також у серці, сечовому міхурі та шлунково-кишковому тракті (ШКТ). У ШКТ вони здійснюють збудження нейронів та медіюють стимуляцію перистальтики 5НТ. Специфічні антагоністи рецепторів 5НТ4 лікують розлади ШКТ (метоклопрамід). Підтипи 5 (відомі принаймні 5), 6 та 7 рецепторів HT також розпорошені в усій ЦНС і можуть слугувати цілями для лікарських препаратів з малими розмірами молекул. Наприклад, підтип рецептора 96930 6 5НТ7 рекомендується проти депресії, психозів, хвороби Паркінсона, хвороби Альцгеймера, хвороби Паркінсона, мігрені, стресу та втомленості, розладів харчування та блювання. Див.: Basic and th clinical pharmacology, 8 Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001); Pharmacology, th 4 Ed., Rang et al. Edinburgh, UK: Harcourt Publishers Ltd. (2001); Kleven et al. European Journal of Pharmacology, 281:219-228 (1995); U.S. Pat. No. 5,162,375; Leone et al. Neuro Report, 9:2605-2608(1998); U.S. Pat. No. 4,771,053; WO 01/52855; De Vry et al. European Journal of Pharmacology, 357:1-8 (1998); Wolff et al. European Journal of Pharmacology, 340:217-220 (1997); Alfieri et al. British Journal of Cancer, 72:1013-1015 (1995); Wolff et al, Pharmacology Biochemistry and Behavior, 52:571-575 (1995); Lucot. European Journal of Pharmacology, 253:53-60 (1997); U.S. Pat. No. 5,824,680; U.S. Pat. No. 4,687,772; Rasmussen et al. Annual Reports in Medicinal Chemistry, 30:1-9 (1995); WO 00/16777; U.S. Pat. No. 4,438,119; Millan, Journal of Pharmacology and Experimental Therapeutics, 295:853-861 (2000); WO 93/04681; Miyamoto, et al. Current Opinion in CPNS Investigational Drugs, 2:25 (2000); Hagger, et al. Biol. Psychiatry, 34:702 (1993); Sharma et al. J. Clin. Psychopharmacol., 18:128 (1998); Lee et al. J. Clin. Psychiatry, 55:82 (1994); Fujii, et al. J. Neuropsychiatry Clin. Neurosci., 9:240 (1997); Mason et al. Eur. J. Pharmacol., 221:397 (1992); NewmanTancredi et al Neuropharmacology, 35:119, (1996); Sumiyoshi et al. J. Clin. Pharmacol., 20:386 (2000); Carli et al. Eur. J. Neurosci., 10:221 (1998); Meneses et al. Neurobiol. Learn. Mem., 71:207 (1999); and Glennon et al. Neuroscience and Behavioral Reviews, 14:3547 (1990). Дія 5HT на синапси припиняється завдякийого + + медійованому Na /K повторному засвоюванню крізь пресинаптичну мембрану. Інгібітори повторного засвоювання 5HT використовуються у лікуванні депресії, стресу та втомленості, панічного синдрому, неврозу нав'язливих станів, розладів харчування та соціальних фобій (наприклад, циталопрам, кломіпрамін, флуоксетин, флувоксамін, індатралін, зімелідин) і можуть бути корисні проти мігрені, психозів, хвороби Альцгеймера, хвороби Паркінсона, хвороби Гантінгтона, наркозалежності, розладів харчування, склеродермії та хвороби Рейно, шлунково-кишкових розладів, пов'язаних з регулюванням перистальтики, та/або блювання. th Див.: Basic and clinical pharmacology, 8 Ed., Katzung. USA: The McGraw Hill Companies, Inc. th (2001); Pharmacology, 4 Ed., Rang et al. Edinburgh, UK: Harcourt Publishers Ltd. (2001); Masson et al. Pharm. Rev. 51:439 (1999); а також посилання у попередніх абзацах. Відповідно є бажаним створення сполук, які модулюють GPCR у формі, придатній для введення до організму хворого на будь-який з перелічених розладів. Зокрема, такі сполуки мають посідати додаткові властивості, наприклад, добру розчинність, стабільність, технологічність у виготовленні. Нами встановлено, що нова сольове форма згідно з винаходом та композиції на її основі є ко 7 рисним модулятором одного або кількох GPCR і посідає відповідні характеристики. Зокрема, ця сольова форма та фармацевтично прийнятні композиції на її основі виліковує або полегшує різноманітні хвороби та розлади, серед яких хвороба Паркінсона, психози (наприклад, шизофренія, маніакально-депресивний психоз, гостра депресія та біполярні розлади), депресія, стрес та втомленість, хвороба Альцгеймера, хвороба Гантінгтона, панічний синдром, синдром нав'язливих станів, розлади харчування, наркозалежність, соціальні фобії, агресивність або збудження, мігрень, склеродермія та хвороба Рейно, блювання, розлади шлунково-кишкового тракту, пов'язані з регулюванням перистальтики, синдром втомлених ніг та секреція пролактину з новоутворень гіпофізу. Фіг. 1 - рентгенодифракційна картина форми І сполуки 2. 1 Фіг. 2 - H ЯМР спектрограма сполуки 2. 13 Фіг. 3 - C ЯМР спектрограма сполуки 2. 1 Фіг. 4 - H ЯМР спектрограма сполуки 1. Фіг. 5 - рентгенодифракційна картина форми І сполуки 2. Фіг. 6 - ДСК-грама форми І сполуки 2. Фіг. 7 - рентгенодифракційна картина аморфної сполуки 2. Фіг. 8 - ДСК-грама аморфної сполуки 2. Фіг. 9 - рентгенодифракційна картина гідрату І сполуки 2. Фіг. 10 - рентгенодифракційна картина гідрату І сполуки 2. Фіг. 11 - рентгенодифракційна картина гідрату II сполуки 2.2. Фіг. 12 - ДСК-грами гідрату І (зверху) та гідрату II (знизу) сполуки 2. Фіг. 13 - рентгенодифракційна картина метанолату сполуки 2. Фіг. 14 - рентгенодифракційна картина етанолату І сполуки 2. Фіг. 15 - рентгенодифракційна картина етанолату II сполуки 2. Фіг.16 - ДСК-грама етанолату II сполуки 2. Фіг. 17 - рентгенодифракційна картина ізопропанолату І (+ ДМФ) сполуки 2. Фіг. 18 - ДСК-грама ізопропанолату І (+ ДМФ) сполуки 2. Фіг. 19 - рентгенодифракційна картина ізопропанолату II сполуки 2. Фіг. 20 - ДСК-грама ізопропанолату II сполуки 2. Фіг.21 - рентгенодифракційна картина ацетонату сполуки 2. Загальний опис певних аспектів винаходу: У міжнародній заявці РСТ/ЕР/00/08190 (Міжнародна публікація WO 01/14330) описані різні індолвмісні похідні піперазину, включаючи сполуку 1 (8-{4-[3-(5-фтор-1Н-індол-3-іл)-пропил]піперазин-1-іл}-2-метил-4Н-бенз[1,4]оксазин-3-он, як показано), які виявляють антагоністичну активність щодо рецепторів D2 та інгібувальну активність щодо повторного засвоєння 5HT у терапевтичних моделях. 96930 8 Крім того, сполука 1 виявляє активність у терапевтичних моделях, чутливих до клінічно важливих антипсихотичних засобів, антидепресантів та транквілізаторів, в також до хвороби Паркінсона. Відповідно сполука 1 є корисна при лікуванні хвороби Паркінсона, психозів (наприклад, шизофренії, маніакально-депресивного психозу, гострої депресії та біполярних розладів), депресії, стресу та втомленості, хвороби Альцгеймера, синдрому нав'язливих станів, розладів харчування, наркозалежності, соціальних фобій, агресивності або збудження, мігрені, склеродермії та хвороби Рейно, блювання, розладів шлунково-кишкового тракту, пов'язаних з регулюванням перистальтики, синдрому втомлених ніг та секреції пролактину з новоутворень гіпофізу. Також сполука 1 дає низьку імовірність спричинення каталепсії у гризунів, а отже, появи екстрапірамідальних бічних явищ, у порівнянні з існуючими антипсихотичними засобами. Див.: WO 01/14330; van der Heyden and Bradford. Behav. Brain Res. 31:61 (1988); van der Poel et al. Psychopharmacology, 97:147 (1989); та Ungerstedt. Acta Physiol. Scand. 82: (suppl. 367) 69 (1971). Бажано створити сольову форму сполуки 1, яка у порівнянні із сполукою1 мала б кращу розчинність у воді, стабільність та зручність у виготовленні. Зокрема, підвищена розчинність дозволяє сполуці краще розчинюватися у шлунковокишковому тракті, а це означає кращу біозасвоюваність. Тоді можна зменшити дозу лікарської форми, що призведе до зменшення негативних явищ у шлунково-кишковому тракті, таких, як нудота та блювання. Менша доза дозволяє зменшити розмір лікарської форми (таблетки, капсули), що поліпшує технологічність виготовлення і є приємнішим для хворих, котрі віддають перевагу таблеткам або капсулам меншого розміру. Введення однієї дози на добу замість кількох також є більш прийнятним для хворих, особливо такої категорії, як хворі на шизофренію та інші психози. Отже, цей винахід пропонує глюкуронатну сіль сполуки 1 у формі, придатній для введення до ліків уповільненої дії, що додатково знижує появу таких негативних явищ, як нудота та блювання, бо виділяється менша кількість діючої речовини й обминаються рецептори у верхній частині шлунково-кишкового тракту, які саме і спричинюють зазначені явища. Згідно з одним із варіантів здійснення винаходу, пропонується глюкуронатна сіль сполуки 1, представлена сполукою 2: 9 Фахівцеві зрозуміло, що завдяки іонному зв'язку між глюкуроновою кислотою та сполукою 1 утворюється сполука 2. Ясна річ, сполука 2 може існувати у різноманітних фізичних формах. Наприклад, сполука 2 може бути у розчині, суспензії або у твердій формі. У деяких варіантах здійснення винаходу сполука 2 знаходиться у твердій формі. Тверда форма сполуки 2 може бути аморфною, кристалічною або змішаною. Далі докладно описані приклади твердої форми. Незалежно від структури сполуки 2, описаної тут, термін "сіль глюкуронової кислоти" стосується солі D-глюкуронової кислоти, солі L-глюкуронової кислоти, солі DL-глюкуронової кислоти та їх сумішей. У деяких варіантах сполука 2 є сіллю Dглюкуронової кислоти. В інших варіантах сполука 2 є сіллю D-глюкуронової кислоти, по суті вільною від солі L-глюкуронової кислоти, причому вираз "по суті вільною" означає, що сполука не містить помітних кількостей солі L-глюкуронової кислоти. У деяких варіантах принаймні 95% маси сполуки 2 представляє сіль D-глюкуронової кислоти. Згідно з іншими варіантами здійснення винаходу, принаймні біля 99% маси сполуки 2 представляє сіль Dглюкуронової кислоти. Фахівцю зрозуміло, що сіль глюкуронової кислоти може існувати у циклічній формі, як показано вище, або у формі відкритого кільця. Відповідно, згідно з винаходом глюкуронатна сіль - сполука 2 охоплює як сіль циклічної глюкуронової кислоти, так і сіль глюкуронової кислоти з відкритим кільцем. За іншими варіантами здійснення винаходу сполука 2 по суті не містить домішок. Термін "по суті не містить домішок" означає, що сполука не містить помітних кількостей сторонніх речовин. Такими сторонніми речовинами можуть бути надлишки глюкуронової кислоти, надлишки сполуки 1, залишки розчинників та будь-які інші забруднення, що можуть з'явитися у ході одержання та/або виділення сполуки 2. У певних варіантах сполука 2 становить принаймні біля 95% загальної маси. В інших варіантах частка сполуки 2 становить принаймні біля 99% загальної маси. За одним з варіантів частка сполуки 2 становить принаймні 97, 97.5, 98.0, 98.5, 99, 99.5, 99.8 відсотків від загальної маси. Згідно з іншим варіантом, сполука 2 містить сумарних органічних домішок не більше 2.0 відсотків площі хроматограми, або, у певних варіантах, не більше 1,5 відсотків загальної площі хроматограми. Існують варіанти, де будь-яка окрема домішка займає не більше 0,6 відсотка загальної площі хроматограми, та в деяких варіан 96930 10 тах навіть 0,5 відсотка відносно загальної площі хроматограми. Структура, наведена для сполуки 2, охоплює усі її ізомерні (наприклад, енантіомерні або конформаційні) форми. Наприклад, як R-, так і Sконфігурації на стереогенному вуглеці входять до обсягу винаходу. Отже, винахід охоплює як поодинокі стереохімічні ізомери, так і енантіомерні та конформаційні суміші. Більш того, усі таутомерні форми сполуки 2 також охоплюються винаходом. Крім того, описані структури включають сполуки, які відрізняються лише наявністю одного або кількох ізотопно збагачених атомів. Наприклад, сполуки, що мають наведену структуру, за винятком заміни водню на дейтерій або тритій, або заміни 13 14 вуглецю на C- або С-збагачений вуглець, належать до обсягу винаходу. Тверді форми сполуки 2: Встановлено, що сполука 2 може існувати у різних твердих формах. Це можуть бути чисті кристали, або поліморфи, сольвати, гідрати та аморфні структури. Усі ці форми охоплюються обсягом винаходу. У деяких варіантах сполука 2 за винаходом являє собою суміш однієї або кількох твердих форм, обраних з-поміж поліморфів, сольватів, гідратів та аморфних структур сполуки 2. Термін "поліморф" стосується різних кристалічних структур (несольватних), які може утворювати сполука. Термін "сольват" стосується кристалічної форми, до структури якої включений розчинник у стехіометричній або нестехіометричній кількості. Також, "гідрат" - це кристалічна форма, до структури якої включена вода у стехіометричній або нестехіометричній кількості. У деяких варіантах сполука 2 являє собою кристалічну тверду масу. В інших варіантах сполука 2 є кристалічною твердою масою, по суті вільною від аморфного матеріалу 2. Вираз "по суті вільною від аморфного 2" означає, що сполука не містить у помітній кількості аморфний матеріал 2. У певних варіантах сполука 2 містить принаймні біля 95% кристалічної сполуки 2. В інших варіантах частка кристалічної сполуки 2 становить принаймні біля 99% загальної маси. У деяких варіантах сполука 2 має чисто кристалічну структуру без будь-яких включень води або розчинника. Встановлено, що сполука 2 може існувати у двох різних чисто кристалічних формах, або поліморфах. Ці поліморфні форми надалі називаються форма І та форма II. У деяких варіантах здійснення цього винаходу йдеться про форму І сполуки 2. В одному з аспектів винаходу форма І сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 1 або 5. В іншому варіанті форма І сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній рентгенограмі, обраних зпоміж біля 17.5, 22.5, 19.9, 3.9 та 12.2 градусів 2тета. Вираз «біля» тут означає у зв'язку з градусами 2-тета, що йдеться про наведену величину ± 0.1 градус 2-тета. Способи одержання форми І сполуки 2 описані далі. В інших варіантах йдеться про форму II сполуки 2. За одним з варіантів, форма II сполуки 2 відрізняється тим, що має характерний пік на дифракційній рентгенограмі біля 18.7 11 96930 градусів 2-тета. Способи одержання форми II сполуки 2 описані далі. Згідно з ще одним варіантом здійснення винаходу, сполука 2 являє собою аморфну тверду масу. Рентгенодифракційна картина аморфної сполуки 2 представлена на фіг. 7. Аморфні тверді матеріали добре знайомі фахівцям, звичайно їх одержують шляхом ліофілізації, топлення, осадження із суперкритичної рідини тощо. Інші способи одержання аморфної сполуки 2 описані далі. Встановлено, що сполука 2 може існувати у принаймні двох гідратних формах. Надалі вони називаються гідрат І та гідрат II. 12 У деяких варіантах здійснення цього винаходу йдеться про гідрат І сполуки 2. За одним варіантом, гідрат І сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній рентгенограмі, обраних з-поміж біля 9.49,16.40 та 17.61 градусів 2-тета. В одному з аспектів гідрат І сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 9. Способи одержання гідрату І сполуки 2 описані далі. У табл. 1 наведені рентгенодифракційні піки, що мають місце у гідрату І сполуки 2 (величини у градусах 2-тета). Таблиця 1 Помічені рентгенодифракційні піки для гідрату І сполуки 2 Кут 2-тета ° 9.49 10.68 11.02 11.58 12.14 12.49 13.43 14.46 14.57 15.57 15.77 16.40 16.71 17.02 17.61 18.79 19.27 19.76 Значення d Ангстрем 9.31 8.28 8.02 7.64 7.29 7.08 6.59 6.12 6.07 5.69 5.61 5.40 5.30 5.21 5.03 4.72 4.60 4.49 Інтенсивність % 3.90 3.10 7.00 6.40 14.00 8.00 4.00 12.10 7.30 13.20 11.10 29.50 9.50 9.80 100.00 20.00 8.10 13.40 У деяких варіантах здійснення цього винаходу йдеться про гідрат II сполуки 2. За одним варіантом, гідрат II сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній рентгенограмі, обраних з-поміж біля 8.252, 10.015, 16.511 та 24.42 градусів 2-тета. В одному з аспектів гідрат II сполуки 2 має порошкову рентгено Кут 2-тета ° 20.14 20.55 21.16 21.46 21.76 22.05 22.27 22.41 22.70 23.26 23.94 24.13 25.03 25.89 26.55 27.41 28.33 Значення d Ангстрем 4.41 4.32 4.20 4.14 4.08 4.03 3.99 3.96 3.91 3.82 3.71 3.68 3.55 3.44 3.35 3.25 3.15 Інтенсивність % 7.30 12.80 12.60 4.80 6.20 3.70 6.70 6.60 3.50 5.10 3.50 3.70 7.10 3.20 9.80 3.10 4.10 дифракційну картину, по суті, як зображено на фіг. 11. Способи одержання гідрату II сполуки 2 описані далі. У табл. 1 наведені рентгенодифракційні піки, що мають місце у гідрату II сполуки 2 (величини у градусах 2-тета). Таблиця 2 Помічені рентгенодифракційні піки для гідрату II сполуки 2 Кут 2-тета ° 8.252 10.015 12.505 12.801 13.447 15.793 16.511 18.034 18.796 19.405 Значення d Ангстрем 10.70662 8.82507 7.07304 6.9098 6.57919 5.60677 5.36471 4.91498 4.7173 4.57058 Інтенсивність % 100 6 3.1 3.9 3.6 6.9 21.7 9.6 16.2 16.5 Кут 2-тета ° 19.864 20.163 20.554 21.18 21.5 21.816 23.945 24.42 26.331 26.696 Значення d Ангстрем 4.46613 4.40059 4.31758 4.19146 4.1297 4.07064 3.71326 3.64216 3.38204 3.33663 Інтенсивність % 12.7 10.3 8 10.4 4.8 7.1 6.7 18.7 4.4 3.8 13 96930 Встановлено, що сполука 2 може існувати у кількох сольватних кристалічних формах. У певних варіантах винахід пропонує кристалічний метанолат сполуки 2. В одному аспекті метанолат сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 13. В іншому варіанті метанолат сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній 14 рентгенограмі, обраних з-поміж біля 11.048, 15.211, 17.363, 19.047 та 22.897 градусів 2-тета. Способи одержання метанолату сполуки 2 описані далі. У табл. 3 наведені рентгенодифракційні піки, що мають місце у метанолату сполуки 2 (величини у градусах 2-тета). Таблиця 3 Помічені рентгенодифракційні піки для метанолату сполуки 2 Кут 2-тета ° 5.239 5.422 5.553 5.724 6.01 6.645 6.665 7.591 8.233 11.048 11.902 13.232 14.138 14.215 15.211 16.012 Значення d Ангстрем 16.85421 16.28498 15.90081 15.42685 14.69341 13.29039 13.25056 11.63654 10.73127 8.00213 7.42993 6.68584 6.25942 6.2254 5.82005 5.53058 Інтенсивність % 3.1 4.5 3.5 3.2 3.2 3.2 3.3 10.8 5 19.5 5 9.9 5.6 5 100 9.1 В інших варіантах кристалічна сполука 2 являє собою етанолат. Виявлені дві етанолатні форми сполуки 2. В одному аспекті кристалічним етанолатом сполуки 2 є етанолат І, який має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 14. В іншому варіанті етанолат І сполуки 2 відрізняється тим, що має один або Кут 2-тета ° 16.466 17.363 19.047 19.329 21.514 22.313 22.897 23.641 24.516 24.815 25.265 25.769 25.858 26.778 28.614 Значення d Ангстрем 5.37913 5.10344 4.65574 4.58852 4.12704 3.98108 3.8809 3.76042 3.62806 3.5851 3.52217 3.45441 3.44277 3.32659 3.11719 Інтенсивність % 24.6 34.2 25.2 5.1 11.7 8.8 27.6 3.8 3.1 8.5 4.7 5.8 4.9 9.2 4.4 кілька піків на дифракційній рентгенограмі, обраних з-поміж біля 8.32, 9.81, 16.56, 20.88 та 24.47 градусів 2-тета. Способи одержання етанолату І сполуки 2 описані далі. У табл. 4 наведені рентгенодифракційні піки, що мають місце у етанолату І сполуки 2 (величини у градусах 2-тета). Таблиця 4 Помічені рентгенодифракційні піки для етанолату І сполуки 2 Кут 2-тета ° 5.17 5.55 5.68 5.84 5.98 6.47 6.68 7.10 7.28 7.42 8.00 8.32 8.84 9.81 10.10 10.51 12.20 12.90 13.80 Значення d Ангстрем 17.10 15.91 15.54 15.12 14.76 13.66 13.22 12.44 12.13 11.91 11.04 10.62 9.99 9.01 8.75 8.41 7.25 6.86 6.41 Інтенсивність % 5.00 7.60 5.40 5.10 3.70 4.70 4.10 6.20 3.10 3.00 4.40 70.10 3.50 77.70 13.50 5.90 33.60 13.60 7.50 Кут 2-тета ° 18.10 18.54 19.28 19.49 19.96 20.24 20.88 21.28 21.91 22.61 23.13 23.42 23.93 24.47 25.22 26.39 26.81 27.56 28.31 Значення d Ангстрем 4.90 4.78 4.60 4.55 4.44 4.38 4.25 4.17 4.05 3.93 3.84 3.79 3.72 3.63 3.53 3.37 3.32 3.23 3.15 Інтенсивність % 30.70 7.60 13.60 25.40 8.50 21.50 100.00 12.80 26.00 3.70 5.20 4.60 11.80 47.30 24.80 22.40 18.10 24.90 8.70 15 14.68 14.96 15.73 16.56 17.62 6.03 5.92 5.63 5.35 5.03 96930 12.30 9.40 15.50 83.30 13.70 У певних варіантах кристалічний етанолат сполуки 2 є етанолатом II і має порошкову рентгенодифракційну картину, по суті, як зображено на Фіг. 15. За іншим варіантом етанолат І сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній рентгенограмі, обраних з-поміж 16 29.20 29.50 29.57 3.06 3.03 3.02 3.10 4.40 3.50 біля 15.09 та 16.9 47 градусів 2-тета. Способи одержання етанолату II сполуки 2 описані далі. У табл. 5 наведені рентгенодифракційні піки, що мають місце у етанолату II сполуки 2 (величини у градусах 2-тета). Таблиця 5 Помічені рентгенодифракційні піки для етанолату II сполуки 2 Кут 2-тета ° 7.52 15.09 25.53 16.9 17.52 18.85 22.65 23.4 25.57 26.5 Значення d Ангстрем 11.75 5.87 3.49 5.24 5.06 4.70 3.92 3.80 3.48 3.36 В інших варіантах кристалічна сполука 2 являє собою ізопропанолат. Виявлені дві ізопропанолатні форми сполуки 2. В одному аспекті кристалічним ізопропанолатом сполуки 2 є ізопропанолат І, який містить ДМФ. В одному аспекті ізопропанолат І сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 17, та/або ДСК-граму, як зображено на фіг. 18. За іншим варіантом ізопропанолат І Інтенсивність % 24.81 100.00 69.92 97.74 57.14 51.13 43.61 23.31 23.31 13.53 сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній рентгенограмі, обраних з-поміж біля 6.59, 13.23, 16.55 та 23.31 градусів 2-тета. Способи одержання ізопропанолату І сполуки 2 описані далі. У табл. 6 наведені рентгенодифракційні піки, що мають місце в ізопропанолату І (+ДМФ) сполуки 2 (величини у градусах 2-тета). Таблиця 6 Помічені рентгенодифракційні піки для ізопропанолату І (+ДМФ) сполуки 2 Кут 2-тета ° 6.59 11.04 13.23 15.50 16.55 19.91 23.31 Значення d Ангстрем 13.41 8.00 6.69 5.71 5.35 4.46 3.81 Ще в одному аспекті кристалічним ізопропанолатом сполуки 2 є ізопропанолат II, який не містить ДМФ. В одному аспекті ізопропанолат II сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на фіг. 19. За іншим варіантом ізопропанолат II сполуки 2 відрізняється тим, що має один або кілька піків на ди Інтенсивність % 25.80 2.10 19.50 2.50 100.00 14.40 29.50 фракційній рентгенограмі, обраних з-поміж біля 3.79, 15.54 та 23.32 градусів 2-тета. Способи одержання ізопропанолату II сполуки 2 описані далі. У табл. 7 наведені рентгенодифракційні піки, що мають місце в ізопропанолату II сполуки 2 (величини у градусах 2-тета). 17 96930 18 Таблиця 7 Помічені рентгенодифракційні піки для ізопропанолату II сполуки 2 Кут 2-тета ° 3.79 7.6186 11.07 11.71 15.54 19.36 23.32 25.37 27.08 28.93 Значення d Ангстрем 11.65 5.81 4.01 3.80 2.88 2.32 1.95 1.80 1.69 1.59 В інших варіантах кристалічна сполука 2 являє собою ацетонат. В одному аспекті ацетонат сполуки 2 має порошкову рентгенодифракційну картину, по суті, як зображено на Фіг. 21. За іншим варіантом ацетонат сполуки 2 відрізняється тим, що має один або кілька піків на дифракційній Інтенсивність % 34.00 16.77 19.72 16.26 100.00 33.34 39.38 17.46 15.60 13.48 рентгенограмі, обраних з-поміж 11.04, 15.20, 15.47 та 20.81 градусів 2-тета. Способи одержання ацетонату сполуки 2 описані далі. У табл. 8 наведені рентгенодифракційні піки, що мають місце в ацетонату сполуки 2 (величини у градусах 2-тета). Таблиця 8 Помічені рентгенодифракційні піки для ацетонату сполуки 2 Кут 2-тета ° 7.72 8.24 9.73 10.01 10.68 11.04 11.46 11.94 12.13 12.61 14.68 14.88 15.20 15.47 16.46 17.11 17.51 18.01 18.43 Значення d Ангстрем 11.44 10.72 9.08 8.83 8.28 8.01 7.72 7.41 7.29 7.01 6.03 5.95 5.82 5.72 5.38 5.18 5.06 4.92 4.81 Інтенсивність % 20.30 16.20 9.50 4.20 19.60 93.20 25.50 5.90 6.70 36.50 11.60 33.00 73.90 100.00 41.60 7.20 4.60 11.00 20.40 У деяких варіантах цього винаходу пропонується форма І сполуки 2, яка містить одну або кілька додаткових твердих форм сполуки 2. В інших варіантах винахід стосується форми І сполуки 2, яка містить одну або кілька форм II, гідрат сполуки 2, сольват сполуки 2 або аморфну сполуку 2. Кут 2-тета ° 19.37 19.94 20.59 20.81 21.20 21.81 22.16 22.89 23.07 23 30 24.40 25.38 26.26 26.45 26.93 27.50 28.02 29.01 Значення d Ангстрем 4.58 4.45 4.31 4.27 4.19 4.07 4.01 3.88 3.85 3.81 3.65 3.51 3.39 3.37 3.31 3.24 3.18 3.08 Інтенсивність % 62.70 19.40 5.40 30.20 13.10 32.90 11.10 28.20 34.70 34.80 17.50 17.40 13.50 11.10 4.10 4.80 4.90 4.40 Загальні способи одержання сполуки 2: Сполуку 1 одержують одним із способів, докладно описаних у публікації PCT WO 01/14330, яка повністю включена до цієї заявки як посилальний матеріал. Інший аспект цього винаходу стосується способу одержання сполуки 2: 19 згідно з яким: одержують сполуку 1: з'єднують сполуку 1 з глюкуроновою кислотою у придатному розчиннику; за бажанням виділяють сполуку 2. Придатний розчинник може солюбілізувати один чи кілька реагентів, або ж, навпаки, може полегшити перемішування суспензії одного або кількох реагентів. Придатними у цьому винаході можуть бути протонні, полярні апротонні розчинники або їх суміші. У деяких варіантах придатними розчинниками можуть бути етер, ефір, спирт, кетон або їх суміші. Це, наприклад, метанол, етанол, ізопропанол або ацетон, якщо ці розчинники є безводні або вживаються у сполученні з водою чи гептаном. В інших випадках розчинниками слугують тетрагідрофуран, діметилформамід, діметилсульфоксид, діетиленглікольмонометилетер, діетиленглікольдіметилетер, метил-tбутилетер, t-бутанол, n-бутанол та ацетонітрил. Ще в одному варіанті придатним розчинником є безводний етанол. Згідно з іншим варіантом здійснення винаходу пропонується спосіб одержання сполуки 2: згідно з яким: 96930 20 змішують сполуку 1: з відповідним розчинником, за бажанням при нагріванні, одержуючи її розчин; додають до зазначеного розчину глюкуронову кислоту; за бажанням виділяють сполуку 2. Як зазначалося вище, сполука 1 розчиняється у придатному розчиннику, за бажанням при нагріванні. У деяких варіантах сполуку 1 розчиняють при біля 60 °С. В інших варіантах сполуку 1 розчиняють при біля 40 °С. В окремих випадках сполуку 1 розчиняють при температурі від біля 40 °C до біля 60 °С. Можливо також розчиняти сполуку 1 при температурі кипіння розчинника. Також можливо розчиняти сполуку 1 без нагрівання. У деяких варіантах розчин сполуки 1 фільтрують перед доданням глюкуронової кислоти. В інших варіантах розчин сполуки 1 не фільтрують перед доданням глюкуронової кислоти. У певних варіантах розчин сполуки 1, якщо його нагрівають до будь-якої температури між біля 40 °С та біля 60 °С, охолоджують до будьякої температури між біля 20 °С та біля 40 °С перед доданням глюкуронової кислоти. В інших варіантах розчин сполуки 1, якщо його нагрівали до будь-якої температури між біля 40 °С та біля 60 °С, не охолоджують до нижчої температури перед доданням глюкуронової кислоти. У деяких варіантах до сполуки 1 додають біля 1 еквіваленту глюкуронової кислоти для одержання сполуки 2. В інших варіантах до сполуки 1 додають менше 1 еквіваленту глюкуронової кислоти для одержання сполуки 2. Можливо додавати до сполуки 1 більше 1 еквіваленту глюкуронової кислоти для одержання сполуки 2. У певних випадках до сполуки 1 додають від біля 1,0 до біля 1,2 еквіваленту глюкуронової кислоти для одержання сполуки 2. Або ж до сполуки 1 додають від біля 0,9 до біля 1,1 еквіваленту глюкуронової кислоти для одержання сполуки 2. Нарешті, до сполуки 1 додають від біля 0,99 до біля 1,01 еквіваленту глюкуронової кислоти для одержання сполуки 2. Зрозуміло, що глюкуронову кислоту можна додавати до суміші сполуки 1 з придатним розчинником у будь-якій придатній формі. Наприклад, це може бути тверда маса, розчин або суспензія у відповідному розчиннику. Розчинник може бути той самий, що для сполуки 1, або інший. У деяких варіантах глюкуронову кислоту вміщують до придатного розчинника перед доданням до сполуки 1. В іншому варіанті глюкуронову кислоту додають у вигляді розчину у придатному розчиннику. В інших варіантах придатними 21 розчинниками для глюкуронової кислоти є полярні протонні або апротонні розчинники. У деяких варіантах придатними розчинниками можуть бути вода, спирти, етери та кетони. Це, наприклад, вода, метанол, етанол, ізопропанол або ацетон, тетрагідрофуран, діметилформамід, діметилсульфоксид, діетиленглікольмонометилетер, діетиленглікольдіметилетер, метил-t-бутилетер, tбутанол, n-бутанол та ацетонітрил. В деяких варіантах відповідний розчинник обирається зпоміж перелічених і має бути безводним. В одному з варіантів глюкуронову кислоту розчиняють у воді. У деяких варіантах одержану суміш, яка містить сполуку 2, охолоджують. У випадках, коли суміш з вмістом сполуки 2 нагрівають до температури вище біля 20 °С, розчину дають охолонути до біля 20 °С. В інших варіантах суміш з вмістом сполуки 2 охолоджують до температури нижче біля 20 °С. У певних варіантах сполука 2 осаджується із суміші. В іншому варіанті сполука 2 кристалізується із суміші. Ще в інших випадках сполука 2 кристалізується з розчину після введення затравки (тобто додання кристалів 2 до розчину). Кристалічну чи аморфну сполуку 2 можна осаджувати з реакційної суміші або одержувати шляхом видалення частини або всього розчинника такими способами, як випарювання, дистиляція, фільтрація (наприклад, нанофільтрація, ультрафільтрація), зворотній осмос, абсорбція та реакція з доданням антирозчинника, як от гептан, виморожування та різні комбінації перелічених способів. Як зазначалося вище, сполуку 2 за бажанням можна виділити. Зрозуміло, що сполуку 2 можна виділити будь-яким придатним фізичним способом, відомим фахівцям. У деяких варіантах твердий осад сполуки 2 можна видалити з відстою фільтрацією. Або ж твердий осад сполуки 2 можна видалити з відстою декантацією. У певних варіантах твердий осад сполуки 2 видаляють з відстою фільтрацією. У певних варіантах виділену сполуку 2 сушать на повітрі. В інших випадках виділену сполуку 2 сушать під зниженим тиском, за бажанням при підвищеній температурі. Згідно з іншим варіантом здійснення винаходу, пропонується спосіб одержання сполуки 2: згідно з яким: з'єднують сполуку 1: 96930 22 з придатним розчинником та нагрівають з утворенням розчину; додають водний розчин глюкуронової кислоти до зазначеного розчину; за бажанням виділяють сполуку 2. У певних варіантах спосіб одержання сполуки 2 передбачає стадію дистиляції реакційної суміші. В інших варіантах реакційну суміш дистилюють, вводячи додатковий розчинник, щоб зменшити вміст води. Або ж спосіб передбачає стадію охолодження суспензії, що містить сполуку 2, та виділення сполуки 2 відомими фізичними прийомами. За одним з варіантів, молярне співвідношення глюкуронової кислоти до сполуки 1 обирають у межах від біля 0.5 до біля 1.0. Або ж співвідношення глюкуронової кислоти до сполуки 1 становить від біля 0.8 до біля 2.0. Величина цього співвідношення також може бути у межах від біля 0.9 до біля 1.2. Вона може також становити від біля 0.94 до біля 1.06. У певних випадках застосовують співвідношення від біля 0.94 до біля 0.95. Застосування сполук та фармацевтично прийнятні композиції Як зазначалося вище, цей винахід пропонує сполуку 2, придатну як модулятор рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину й корисну у клінічно значущих моделях для психозів, депресій, стресу й втомленості та хвороби Паркінсона. У деяких варіантах предмет цього винаходу є корисний як модулятор одного або кількох підтипів рецептора D2, повторного засвоєння 5HT або синтезу простагландину. В інших варіантах предмет цього винаходу придатний для лікування психозів, депресій, стресу й втомленості та хвороби Паркінсона. Відповідно за іншим аспектом цього винаходу запропоновані фармацевтично прийнятні композиції, які містять сполуку 2, а за бажанням також фармацевтично прийнятний носій, ад'ювант або наповнювач. У деяких варіантах ці композиції за бажанням містять також одну або кілька додаткових діючих речовин. Як зазначено вище, фармацевтично прийнятні композиції згідно з винаходом додатково містять фармацевтично прийнятний носій, ад'ювант або наповнювач, якими можуть бути будь-які розчинники, розбавники або інші рідкі носії, диспергатори або коагулянти, поверхнево активні речовини, ізотоніки, загусники або емульгатори, консерванти, тверді в'яжучі, мастила тощо, як лічить обраній випускній формі. У Remington's Pharmaceutical Sciences, Sixteenth Edition, E. W. Martin (Mack Publishing Co., Easton, Pa., 1980) 23 описані різноманітні носії для складання фармацевтично прийнятних композицій та відомі способи їх приготування. За винятком тих звичайних носіїв, які можуть виявитися несумісними з сіллю за винаходом завдяки небажаній біологічній дії або шкідливій взаємодії з іншими компонентами фармацевтично прийнятної композиції, усі відомі носії охоплюються обсягом винаходу. До невиключного переліку матеріалів, які можуть використовуватися як фармацевтично прийнятні носії, входять, зокрема, іонообмінні смоли, оксид алюмінію, стеарат алюмінію, лецитин, протеїни сироватки, наприклад, альбумін людської сироватки, буферні речовини, як от фосфати, гліцин, сорбинова кислота або сорбат калію, суміші часткових гліцеридів насичених кислот рослинних олій, вода, солі або електроліти, наприклад, протамінсульфат, дінатрійгідрофосфат, гідрофосфат калію, хлорид натрію, солі цинку, колоїдний кремнезем, трисилікат магнію, полівінілпіролідон, поліакрилати, воски, блок-полімери поліетиленполіоксіпропилену, вовняний жир, сахари, як от лактоза, глюкоза або цукроза, кукурудзяний та картопляний крохмаль, целюлоза та її похідні, наприклад, натрійкарбоксіметилцелюлоза, етилцелюлоза та ацетат целюлози, порошок трагаканту, солод, желатин, тальк, формоутворювачі на зразок масла какао та супозиторних восків, рослинні олії, наприклад, арахісова, бавовняна, сафлорова, кунжутна, маслинова, кукурудзяна та соєва, гліколі, як пропиленгліколь та поліетиленгліколь, ефіри, наприклад, етилолеат та етиллаурат, агар, буферні агенти, як гідроксид магнію та гідроксид алюмінію, альгінова кислота, вода без вмісту пірогенних домішок, ізотонічний фізрозчин, розчин Рінгера, етиловий спирт та фосфатні буферні розчини, а також інші нетоксичні сумісні мастила, наприклад, лаурилсульфат натрію та стеарат магнію, а також фарбники, антиадгезиви, покривні агенти, підсолоджувачі, смакові добавки, запашники, консерванти та антиоксиданти, які, на погляд складача композиції, можуть бути присутні у ній. Ще один аспект винаходу - це лікування або полегшення симптомів розладів, пов'язаних з модулюванням рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину, та/або лікування або полегшення симптомів психозів, депресій, стресу й втомленості та/або хвороби Паркінсона шляхом введення хворому дійової кількості сполуки 2 або фармацевтично прийнятної композиції на її основі. "Дійова кількість" сполуки або фармацевтично прийнятної композиції на її основі у деяких варіантах здійснення винаходу означає кількість, яка ефективно здійснює лікування або полегшення симптомів розладів, пов'язаних з модулюванням рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину, та/або лікування або полегшення симптомів психозів, депресій, стресу й втомленості та/або хвороби Паркінсона. В інших варіантах "дійова кількість" це кількість, достатня, щоб виступати модулятором одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу прос 96930 24 тагландину. "Дійова кількість" сполуки здатна досягти бажаного терапевтичного та/або профілактичного ефекту, тобто попередити або послабити симптоми хвороби, пов'язаної з модулюванням одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину, та/або психозів, депресій, стресу й втомленості та/або хвороби Паркінсона. Сполуку та композиції на її основі згідно із способом за винаходом можна застосовувати у будь-якій кількості та будь-яким шляхом, який виявиться ефективним для лікування або полегшення симптомів розладів, пов'язаних з модулюванням рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину, та/або лікування або полегшення симптомів психозів, депресій, стресу й втомленості та/або хвороби Паркінсона. Точна ефективна кількість буде різною для хворих у залежності від статі, віку та загального стану хворого, тяжкості захворювання, конкретної діючої речовини, способу її введення тощо. Сіль за винаходом переважно вводять до випускних форм у вигляді дозувальних одиниць (наприклад, таблетки, капсули або ампули) з метою полегшити введення та стандартизувати дозування. Термін "дозувальна одиниця" означає фізично дискретну кількість діючої речовини, придатну для конкретного хворого. Втім, цілком зрозуміло, що сумарну добову дозу солі за винаходом та композицій на її основі визначає лікар з точки зору здорового медичного глузду. Ефективна доза ліків для кожного окремого хворого або організму залежить від безлічі чинників, у тому числі від виду та тяжкості захворювання, активності застосованої діючої речовини, складу застосованої композиції, віку, маси тіла, загального стану здоров'я, статі та харчування хворого, часу й шляху введення та швидкості екскреції застосованої сполуки з організму, тривалості курсу лікування, інших одночасно застосованих ліків та інших чинників, які добре відомі у медичній практиці. "Хворий" у даному контексті означає тварину, переважно ссавця, а у першу чергу людину. Фармацевтична прийнятні композиції за винаходом можуть вводитися до організму людини та інших тварин орально, назально, ректально, парентерально, внутрішньопорожнинно, вагінально, внутрішньочеревно, топікально (у вигляді порошків, мазей або крапель), букально тощо, у залежності від тяжкості захворювання. У деяких варіантах сіль за винаходом можна вводити орально чи парентерально у дозах від біля 0,01 мг/кг до біля 50 мг/кг, переважно від біля 1 мг/кг до біля 25 мг/кг маси тіла хворого, один або кілька разів на добу для одержання потрібного терапевтичного ефекту. До рідких дозувальних форм для орального або назального введення належать, зокрема, фармацевтично прийнятні емульсії, мікроемульсії, розчини, суспензії, аерозолі, гелі, сиропи та еліксири. На додаток до діючої солі рідкі дозувальні форми можуть містити відомі фахівцям інертні розбавники, наприклад, воду та інші розчинники, солюбілізатори та емульгатори, як от 25 етиловий спирт, ізопропиловий спирт, етилкарбонат, етилацетат, бензиловий спирт, бензилбензоат, пропиленгліколь, 1,3-бутиленгліколь, діметилформамід, олії (зокрема, бавовняну, арахісову, кукурудзяну, паросткову, маслинову, касторову та кунжутну), гліцерин, тетрагідрофурильний спирт, поліетиленгліколі, сорбітанові ефіри жирних кислот та їх суміші. Крім інертних розбавників, оральні композиції можуть містити такі ад'юванти, як змочувачі, емульгатори та суспендувальні агенти, підсолоджувачі, смакові добавки та запашники. Аерозольні композиції, як правило, містять розчин або тонку суспензію діючої речовини у фізіологічно прийнятному водному або неводному розчиннику; звичайно вони випускаються як одно- чи багатодозові стерильні рідини у зачиненій тарі, яка може являти собою ампулу або поповнюватися для застосування з розпилювачем. Або ж зачинена тара може бути унітарним дозатором, наприклад, одноразовим носовим інгалятором чи аерозольним розпилювачем, оздобленим дозатором, який викидають після того, як вміст упаковки буде вичерпано. Якщо дозувальна форма являє собою аерозольний дозатор, вона містить фармацевтично прийнятний газ-витискувач. Аерозольний дозатор може також мати вигляд розприскувача з насосом. Препарати для ін'єкцій, зокрема, стерильні водні або олійні суспензії для ін'єкцій, можна складати відомими способами з використанням придатних диспергаторів або змочувачів та суспендуючих агентів. Стерильним препаратом для ін'єкцій може бути також стерильний розчин, суспензія або емульсія у нетоксичному парентерально придатному розбавнику або розчиннику, наприклад, розчин у 1,3-бутандиолі. Можна використовувати такі прийнятні носії та розчинники, як вода, розчин Рінгера, розчини хлориду натрію ізотонічний та згідно з фармакопеєю США. Крім того, розчинниками або суспендуючими середовищами можуть бути стерильні нелеткі олії. Для цього можна застосовувати будь-яку легку нелетку олію, в тому числі синтетичні моно- або дігліцериди. При приготування препаратів для ін'єкцій можна ще вживати жирні кислоти, наприклад, олеїнову кислоту. Препарати для ін'єкцій можна стерилізувати, наприклад, фільтрацією крізь фільтр, що затримує бактерії, або введенням стерилізуючих агентів у формі стерильних твердих композицій, які перед вживанням розчиняють або диспергують у стерильній воді або іншому стерильному середовищі, прийнятному для ін'єкцій. Переважно сполука 2, як вона описана тут, добре розчиняється у воді. Відповідно ця сполука є придатна для внутрішньосудинних та внутрішньом'язових ін'єкцій. Не вдаючись до теорій, можна вважати, що висока розчинність сполуки 2 дозволяє зменшити обсяг ін'єкції, тим самим зменшуючи біль та дискомфорт у хворого. Отже, цей винахід також стосується композицій для внутрішньосудинних або внутрішньом'язових ін'єкцій. Щоб подовжити дію сполуки за винаходом, часто буває доцільно уповільнити засвоєння спо 96930 26 луки після підшкірних або внутрішньом'язових ін'єкцій. Для цього можна застосовувати рідку суспензію кристалічного або аморфного матеріалу, який погано розчиняється у воді. Тоді швидкість засвоєння сполуки залежатиме від швидкості її розчинення, а та, у свою чергу, від розміру та форми кристалів. Або ж уповільнене засвоєння парентерально введеної сполуки досягається розчиненням або суспендуванням сполуки в олійному носії. Форми уповільненої дії для ін'єкцій одержують, утворюючи мікрокапсульні матриці сполуки у біорозкладних полімерах, наприклад, поліактид-полігліколиді. У залежності від співвідношення між сполукою та полімером та виду полімеру можна регулювати швидкість виділення. До біорозкладних полімерів належать також полі(ортоефіри) та полі(ангідриди). Форми уповільненої дії для ін'єкцій можна також одержати, впроваджуючи сполуку до ліпосом або мікроемульсій, сумісних із тканинами тіла. Типові парентеральні композиції складаються з розчину або суспензії сполуки або її фізіологічно прийнятної солі у стерильному водному або неводному носії або фізіологічно прийнятній олії, наприклад, у поліетиленгліколі, полівінілпіролідоні, лецитині, арахісній або кунжутній олії. Або ж розчин можна ліофілізувати й потім перерозчинити у придатному розчиннику перед вживанням. Композиції для ректального або вагінального введення звичайно мають форму супозиторіїв, песаріїв, вагінальних петель, пін або клізм. Переважно це супозиторії, які готують змішуванням солі за винаходом з придатними недратівними носіями, наприклад, маслом какао, поліетиленгліколем або супозиторним воском, який є твердим при кімнатній температурі, але розріджується при температурі тіла, а отже, плавиться у прямій кишці або піхві, виділяючи діючу речовину. До твердих форм для орального введення належать капсули, таблетки, пілюлі, порошки та гранули. У цих твердих формах діючу речовину змішують з принаймні одним інертним, фармацевтично прийнятним наповнювачем або носієм, як от цитрат натрію або дікальційфосфат, та/або а) наповнювачами, наприклад, крохмалями, лактозою, цукрозою, глюкозою, манітолом або кремнекислотою, b) в'яжучими, наприклад, карбоксіметилцелюлозою, альгінатами, желатином, полівінілпіролідоном, цукрозою та смолою акації, с) зволожниками, наприклад, гліцерином, d) дезінтегрантами, наприклад, агар-агаром, карбонатом кальцію, картопляним або маніоковим крохмалем, альгіновою кислотою, певними силікатами та карбонатом натрію, е) уповільнювачами розчинення, наприклад, парафіном, f) прискорювачами засвоєння, наприклад, четверними солями амонію, g) змочувачами, наприклад, цетиловим спиртом та гліцеринмоностеаратом, h) абсорбентами, наприклад, каоліном та бентонітовою глиною, і) мастилами, наприклад, тальком, стеаратом кальцію, стеаратом магнію, твердими поліетиленгліколями, лаурилсульфатом натрію та їх сумішами. У разі капсул, таблеток та пілюль до складу також можуть входити буферні агенти. 27 Композиції для смоктання за щокою або під язиком включають таблетки, лозенжі та пастили, у яких діючу речовину змішують з такими носіями, як цукор із смолою акації, трагакант або желатин з гліцерином. Тверді композиції можуть також слугувати наповненням для м'яких або твердих желатинових капсул з такими розбавниками, як лактоза або молочний цукор, а також високомолекулярні поліетиленгліколі тощо. Тверді випускні форми таблетки, драже, капсули, пілюлі та гранули можуть мати покриття чи оболонку, наприклад, шлункові та інші покриття, добре знайомі фахівцям. За бажанням вони можуть містити агенти, що надають непрозорість, або можуть мати такий склад, щоб діюча речовина могла виділятися уповільнено й лише у певних місцях шлунковокишкового тракту. Композиції з включеннями діючої речовини базуються, наприклад, на полімерних речовинах та восках. Тверді композиції такого типу можуть також слугувати наповненням для м'яких або твердих желатинових капсул з такими розбавниками, як лактоза або молочний цукор, а також високомолекулярні поліетиленгліколі тощо. Сполука 2 може мати форму мікрокапсули з одним або кількома з перелічених наповнювачів. Тверді випускні форми - таблетки, драже, капсули, пілюлі та гранули - можуть мати покриття та оболонки, наприклад, шлункові покриття, покриття, що регулюють виділення, тощо, які добре відомі фахівцям. У таких твердих формах до сполуки 2 можна примішувати принаймні одинінертний розбавник, наприклад, цукрозу, лактозу або крохмаль. Такі випускні форми зазвичай містять, крім інертних розбавників, додатково ще мастила й інші таблетувальні речовини, наприклад, стеарат магнію та мікрокристалічну целюлозу. Якщо це капсули, таблетки або пілюлі, можна також додавати буферні агенти. За бажанням вони можуть містити агенти, що надають непрозорість, або можуть мати такий склад, щоб діюча речовина могла виділятися уповільнено й лише у певних місцях шлунково-кишкового тракту. Композиції з включеннями діючої речовини базуються, наприклад, на полімерних речовинах та восках. До композицій для орального введення можна додавати речовини, що захищають діючий компонент від розкладу при проходженні кишково-шлунковим трактом. Це може бути зовнішнє покриття на таблетці або капсулі. В іншому варіанті композиція на основі сполуки 2 розрахована на подовжену або уповільнену дію. Композиція уповільненої дії містить сполуку 2 разом з компонентом, що забезпечує уповільнене виділення. Таким чином досягається цілеспрямоване виділення сполуки 2 у нижній частині шлунково-кишкового тракту, тобто у малому кишковику, великому кишковику, товстій кишці або прямій кишці. У деяких варіантах композиція уповільненої дії на основі сполуки 2 також містить шлункове або чутливе до рН покриття, наприклад, із ацетатфталатів целюлози або інших фталатів (як от полівінілацетатфталат, метакрилати під товарним знаком Eudragit). Або ж 96930 28 композиція уповільненої дії забезпечує регульоване виділення до малого кишковика та/або товстої кишки завдяки наявності рН-чутливого метакрилатного покриття, рН-чутливих полімерних мікросфер або полімерів, які розкладаються шляхом гідролізу. Композиція уповільненої дії може містити гідрофобні або гелеутворювальні наповнювачі чи покриття. Гарантією виділення до товстої кишки можуть бути покриття, які перетравлюються бактеріальними ферментами на зразок амілози або пектину, рН-залежними полімерами, гідрогельними пробками, що набухають з плином часу (Pulsincap), гідрогельними покриттями, що розкладаються з часом, та/або покриттями з акрилової кислоти, зшитої з азоароматичними зв'язками. У деяких варіантах композиції уповільненого виділення за винаходом містять гіпромелозу, мікрокристалічну целюлозу та мастило. Із суміші сполуки 2, гіпромелози та мікрокристалічної целюлози можна готувати таблетку або капсулу для орального введення. У деяких варіантах гаку суміш гранулюють та пресують з неї таблетки. В інших варіантах композиції уповільненого виділення мають багатокомпонентний склад. Суміш сполуки 2 з відповідним полімером гранулюють у кульки, на які наносять покриття. У деяких варіантах кульки герметично скріплюють нефункціональним покриттям. Або ж на кульки спершу наносять нефункціональне, а потім функціональне покриття. У цьому контексті "нефункціональним" є покриття, яке не впливає на швидкість виділення діючої речовини. Нефункціональне покриття може бути виконано, наприклад, з гідроксіпропилцелюлози, гіпромелози або полівінілового спирту. У деяких варіантах нефункціональним покриттям слугує Opadry® Clear, яке містить гідроксіпропилметилцелюлозу та поліетиленгліколь. Під "функціональним покриттям" мається на увазі покриття, яке впливає на швидкість виділення діючої речовини з лікарської форми. Прикладом функціонального покриття може бути етилцелюлоза та похідні поліметакрилату (Eudragit). Відповідно інший варіант виконання передбачає багатокомпонентну композицію, яка складається з ядра-кульки, що містить сполуку 2, нефункціональне суцільне покриття та функціональне суцільне покриття. До випускних форм для топікального або трансдермального введення діючої речовини за винаходом належать мазі, пасти, креми, лосьйони, гелі, порошки, спреї, інгалянти або пластирі. Діючу речовину підмішують за стерильних умов до фармацевтично прийнятного носія та до консервантів, якщо у них є потреба. Офтальмологічні препарати, вушні та очні краплі також належать до обсягу винаходу. Додатково цей винахід передбачає застосування трансдермальних пластирів, перевагою яких є те, що вони забезпечують регульоване надходження діючої речовини до організму. Такі випускні форми можна готувати розчиненням або розподіленням сполуки у належному середовищі. Можна застосовувати прискорювачі абсорбції, щоб збільшити потік 29 сполуки крізь шкіру. Швидкість засвоєння можна регулювати або спеціальною мембраною, або диспергуванням сполуки у полімерній матриці або гелі. Композиції можуть містити від 0.1% до 99 мас. %, переважно 0.1-60 мас. %, краще 0.2-20 мас. %, а оптимально від 0.25 до 12 мас. % сполуки 2 у залежності від способу введення. Як зазначалося вище, сіль згідно з винаходом може слугувати модулятором рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину, отже, винахід також стосується способу лікування (паліативного, консервативного, профілактичного) або полегшення симптомів розладів, пов'язаних з модулюванням одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину. В одному з варіантів сполука 2 є модулятором одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину. Отже, не вдаючись до теорії, сполука та композиції за винаходом є корисні для лікування або полегшення симптомів хвороби, стану або розладу, які мають відношення до модулювання одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину. Коли модулювання одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину мають місце у тій чи іншій хворобі, стані або розладі, їх можна вважати "хворобами, медійованими рецепторами D, рецепторами 5НТ, повторного засвоєння 5HT та синтезу простагландину" або симптомами таких хвороб. У певних варіантах сполуки та композиції згідно з винаходом використовуються у способі лікування або полегшення симптомів одного або кількох захворювань, серед яких хвороба Паркінсона, психози (наприклад, шизофренія, маніакально-депресивний психоз, гостра депресія та біполярні розлади), депресія, стрес та втомленість, хвороба Альцгеймера, хвороба Гантінгтона, панічний синдром, синдром нав'язливих станів, розлади харчування, наркозалежність, соціальні фобії, агресивність або збудження, мігрень, склеродермія та хвороба Рейно, блювання, розлади шлунково-кишкового тракту, пов'язані з регулюванням перистальтики, синдром втомлених ніг та секреція пролактину з новоутворень гіпофізу, причому спосіб полягає у введенні до організму хворого сполуки 2 або композиції на її основі. Зрозуміло, що солі та фармацевтично прийнятні композиції згідно з винаходом можуть вживатися у комбінованій терапії, тобто сполука 2 та композиції на її основі можуть застосовуватися разом, до або після прийому інших ліків або медичних процедур. При призначенні комбінованого режиму лікування беруться до уваги сумісність запропонованих ліків та/або процедур та лікувальний ефект, що досягається. Також треба враховувати, що застосовані ліки можуть чинити дію на той самий розлад (наприклад, препарат за винаходом вводиться разом з іншим препаратом, 96930 30 призначеним для лікування саме цього розладу) або можуть досягати іншого ефекту (наприклад, гамувати небажану бічну дію). У даному контексті додаткові лікарські засоби, що звичайно застосовуються для лікування або профілактики того чи іншого захворювання, вважаються "придатними для хвороби або стану, що його лікують". Кількість додаткового лікарського засобу в композиціях за винаходом не має перевищувати ту, що зазвичай вводиться у композиції, де лікарський засіб є єдиною діючою речовиною. У певних варіантах кількість додаткового лікарського засобу в описаних композиціях становить від 50 до 100% кількості цього засобу у композиціях, де він є єдиною діючою речовиною. Ще один аспект винаходу стосується способу модулювання одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину у біологічному зразку або в організмі хворого, згідно з яким хворому вводять або біологічний зразок приводять у контакт із сполукою 2 або композицією на її основі. До "біозразків" належать, зокрема, клітинні культури або їх екстракти; матеріали, одержані з організму ссавців біопсією, або їх екстракти, а також кров, слина, сеча, кал, сперма, сльози та інші виділення з організму або їх екстракти. Модулювання одного або кількох рецепторів D, рецепторів 5НТ, повторного засвоєння 5HT та синтезу простагландину у біологічному зразку є корисне у багатьох відношеннях, відомих фахівцям. Зокрема, це може бути біопроба. Кількість сполуки 2, яка виявляється ефективною для лікування перелічених розладів, залежить від виду та тяжкості захворювання й маси тіла конкретного хворого. Втім, одинична доза для дорослого, який важить 70 кг, звичайно містить від 0.01 до 100 мг, наприклад, від 0.1 до 50 мг, переважно від 0.5 до 16 мг сполуки за винаходом на добу. Дози можна вводити один або кілька, наприклад, 2, 3 або 4 рази на добу, звичайно від 1 до 3 разів на добу, переважно 1 або 2 рази на добу. Зрозуміло, що наведені величини лише дають орієнтування при виборі дози сполуки 2 для дорослої людини. Дозу для дитини визначає практичний лікар або фахівець, і вона має бути меншою або принаймні не більшою, ніж для дорослого. Одинична доза переважно має форму капсули або таблетки. Усі ознаки кожного з аспектів винаходу поширюються на усі інші аспекти з відповідними змінами. Далі наводяться приклади, що допомагають глибше зрозуміти винахід. Звичайно, ці приклади даються лише для ілюстрації й ніяким чином не обмежують обсяг винаходу. Приклади Загальні процедури Порошкові рентгенодифракційні картини одержують на дифрактометрі Rigaku Miniflex фірми Rigaku MSC Inc. Зразки порошку наносять на держаки зразків з полірованого кремнію на нульовому тлі. Джерелом випромінювання слугує мідна рентгенівська трубка 0,45 кВт з нормальним фокусом, оздоблена нікелевим фільтром K, швидкість розгортай 2 градуси/хв від 3.00 до 40.00 31 градусів 2-тета. Дані обробляють за допомогою пакету програм Jade 6.0. Спектри протонного ядерного магнітного ре1 зонансу ( H ЯМР) одержують на ЯМРспектрометрі Bruker, модель Avance DRX-500 МГц, оздобленому 5-мм зондом QNP. 5-25 мг кожної сполуки розчиняють у 0.6 мл DMSO-d6 (99.9% D), який містить 0.05% тетраметилсилану 1 в якості внутрішнього еталону. Спектри H ЯМР записують при 500.133 Мгц з використанням 30галусних імпульсів при затримці імпульсу на 20 с, вимірювальні точки 32k, 64 розгортки. Експоненційну вирізну функцію з розширюванням спектральних ліній 0.3 Гц прикладають до вимірювальних точок 16k для обробки даних без заповнення нулями, а вміст тетраметилсилану вважається рів13 ним 0.00 ч. на млн. Кількісний C ЯМР визначають при 125.7 МГц із стробованою зворотною розв'язкою, імпульс 30 градусів, затримка 8 с. Дані ДСК одержують на диференційному скануючому калориметрі ТА Q1000. У приладі зразок нагрівають від 40 °C до 200 °C із швидкістю 10 °С/хв та промивають 50 мл/хв азоту. Приклад 1 Одержання сполуки 2 (форма І) Сполуку 1 (500 мг) суспендують у 20 мл безводного етанолу та нагрівають до 60 °C з одержанням прозорого розчину. Розчин фільтрують крізь фільтр 0.45 мкм та охолоджують до 40 °C. До розчину додають 275 мг глюкуронової кислоти (1.2 г-екв). Одержують тонку білу суспензію. її охолоджують до 20 °C та перемішують магнітною мішалкою 16 годин. Суспензію фільтрують, одержану тверду фазу сушать на повітрі при кімнатній температурі й піддають рентгенодифракційному (див. Фіг. 1) та оптичному мікроскопічному аналізу, підтверджуючи одержання кристалічної 1 сполуки 2. На фіг. 2 представлений H ЯМР 13 спектр для сполуки 2. Фіг. 3 представляє C ЯМР 1 спектр для сполуки 2, а фіг. 4 - H ЯМР спектр для сполуки 1. Приклад 2 Одержання сполуки 2 (форма І) реактивною дистиляцією з етанолу та води D-глюкуронову кислоту (4.6 г) додають до 25 мл води та розчиняють при кімнатній температурі. Сполуку 1 (10 г) додають до 320 мл безводного етанолу та нагрівають до 50-70 °C, одержуючи прозорий розчин. Приготований водний розчин глюкуронової кислоти (1 екв) додають до розчину вільної основи та етанолу. Розчин залишається прозорим, і йому дають охолонути до кімнатної температури при перемішуванні протягом 16 годин. Одержаний розчин піддають азеотропічній дистиляції при 78 °С. До розчину додають ще близько 400 мл безводного етанолу - по 200 мл кожні 0,5 години під час дистиляції. Дистиляція дає білий осад. Дистиляцію припиняють, коли буде віддистильовано 600 мл розчину й залишиться 150 мл білої суспензії. її фільтрують та сушать усю ніч у вакуумі при 50 °С, одержуючи сполуку 2. Кінцевий продукт (12 г, вихід 84%) є кристалічним за даними порошкового рентгенодифракційного аналізу (Фіг. 5) та ДСК (Фіг. 6). У табл.9 наведені рентгенодифракційні піки для 96930 32 форми І сполуки 2 (величини у градусах 2-тета). Таблиця 9 Помічені рентгенодифракційні піки для сполуки 2 (форма І) 2-тета 12.158 14.460 15.541 16.399 17.599 19.204 20.018 22.340 23.296 25.740 29.658 Приклад 3 Одержання сполуки 2 (форма І) гетерогенною реакцією в етанолі Сполуку 1 (500 мг) розчиняють у 70 мл безводного етанолу при кімнатній температурі. До розчину вільної основи додають 230 мг глюкуронової кислоти (1.0 екв) з утворенням суспензії. Її перемішують 16 годин при кімнатній температурі та фільтрують. Тверду фазу сушать у вакуумі 50 С, одержуючи сполуку 2. Кінцевий продукт (235 мг, вихід 32.2%) піддають рентгенодифракційному аналізу, ДСК та ЯМР спектроскопії. Приклад 4 Одержання сполуки 2 (форма І) гетерогенною реакцією при 60 °C в етанолі Сполуку 1 (400 мг) суспендують у 13 мл безводного етанолу та нагрівають до 60 °C з одержанням прозорого розчину. Розчин фільтрують крізь фільтр 0.45 мкм та охолоджують до 40 °С. До розчину додають 202 мг глюкуронової кислоти (1.1 екв). Одержують тонку білу суспензію. її охолоджують до 20 °С та перемішують магнітною мішалкою 16 годин. Суспензію фільтрують, одержану тверду фазу (224 мг, вихід 38 %) сушать у вакуумі при 50 °C. Приклад 5 Загальний спосіб одержання сполуки 2 (форма І) Додають 25.3 кг етанолу до 1 кг сполуки 1 й нагрівають суміш до 60 °C. Додають 2 кг води до 0.46 кг глюкуронової кислоти й перемішують, доки вся кислота не розчиниться у воді. Розчин глюкуронової кислоти додають до розчину вільної основи. Розчин має залишатися прозорим. Розчин охолоджують до 50 °C. Реакційний розчин фільтрують при 50 °C крізь фільтр 0.5 мкм, охолоджують до 24 °C та повільно перемішують 16 годин. Реакційний розчин нагрівають до 78 °C, починаючи дистиляцію. Віддистильовують 15.8 кг розчину, додають 15.8 кг етанолу, віддистильовують 15.8 кг розчину, додають 15.8 кг етанолу й нарешті віддистильовують 20 л розчину. (Дистилюють 60 л, додають 40 л, остаточний обсяг розчину 15.5 л). Реакційну суміш охолоджують до 20 33 °C протягом 1 години і ще 1 годину витримують при 20 °С. Маточник відфільтровують, коржик двічі промивають 4.0 кг (усього 8 кг) етанолу. Коржик сушать під вакуумом при 50 °C 12 годин. Приклад 6 Альтернативний спосіб одержання сполуки 2 (форма І) в ацетонітрилі В іншому способі одержання форми І аморфну сполуку 2 суспендують в ацетонітрилі при кімнатній температурі 3 доби. Аморфна тверда фаза перетворюється на чисто кристалічну форму сполуки 2 (форму І). Приклад 7 Одержання аморфної сполуки 2 Спосіб А: 0.92 г D-глюкуронової кислоти додають до 5 мл води й розчиняють при кімнатній температурі. 2 г вільної основи SLV-314 (3279794-01) додають до 20 мл ацетону й нагрівають до 40-50 °C, одержуючи прозорий розчин. До цього розчину додають при перемішуванні приготований водний розчин глюкуронової кислоти (1 екв). Розчин залишається прозорим, і йому дають охолонути до кімнатної температури при перемішуванні протягом 16 годин. Одержаний розчин дистилюють ~56 °С. Під час дистиляції до розчину двічі додають 50 мл ацетону. Протягом дистиляції з'являється трохи білої твердої фази, яка незабаром зникає. Дистиляцію припиняють після того, як буде віддистильовано 35 мл розчину й залишиться 35 мл прозорого розчину. Розчинник випаровують у сушарці при 50 °С під вакуумом, одержуючи коричнювату тверду аморфну масу, яку піддають порошковому рентгенодифракційному аналізу (фіг. 7) та ДСК (фіг. 8). Спосіб В: Сполуку 2 розчиняють у 32 обсягах етанолу та 4 обсягах води при підвищеній температурі. Розчинник випаровують під атмосферним тиском шляхом нагрівання до температури флегми. Одержують гель, який сушать під вакуумом при 50 °С з одержанням аморфної твердої маси. Приклад 8 Одержання сполуки 2 (форма II) Форму І сполуки 2 перетворюють на форму II, суспендуючи форму І у різноманітних розчинниках. Цей процес триває деякий час при кімнатній або підвищеній температурі. Форму І знов суспендують у толуолі, ацетоні, тетрабутилметилефірі, ацетонітрилі або ізопропилацетаті при кімнатній температурі або при 50 °C протягом від 1 до 2 тижнів. Встановлено, що підвищена температура сприяє конверсії. Про утворення форми II свідчить характерний пік при 18.7 градусах 2тета на порошковій рентгенодифракційній картині. Приклад 9 Одержання гідрату І сполуки 2 Форму І сполуки 2 суспендують у воді протягом більше ніж 2 тижнів при кімнатній температурі або при 50 °C. Суцільна конверсія протікає дуже повільно і дає суміш форми І та гідрату І, яка характеризуються порошковою рентгенодифракційною картиною кристалів та ДСК. Див. фіг. 9 та 10. Приклад 10 Одержання гідрату II сполуки 2 Аморфну сполуку 2 суспендують у 6 обсягах 96930 34 води при кімнатній температурі та дають кристалізуватися при кімнатній температурі. Одержану суспензію перемішують усю ніч та відфільтровують цільову сполуку, яка характеризуються порошковою рентгенодифракційною картиною кристалів та ДСК. Див. фіг. 11 та 12 відповідно. Приклад 11 Одержання сольватів сполуки 2 Метанолат Аморфну сполуку 2 суспендують у 6 обсягах метанолу при кімнатній температурі та дають кристалізуватися при кімнатній температурі. Одержану суспензію перемішують усю ніч та відфільтровують твердий метанолат. Див. фіг. 13. Метанолат виявляється нестійким при сушці й перетворюється на форму І. Етанолат Сполуку 1 розчиняють у 32 обсягах етанолу 1J1 при підвищеній температурі. Одразу ж додають стехіометричну кількість розчину глюкуронової кислоти у 3-4 обсягах води. Негайно починається зародкоутворення. Одержану суміш перемішують на кризі 30 хвилин, після чого залишають на ніч без перемішування. Одержану сполуку відфільтровують та визначають порошковою рентгенодифракцією як етанолат І. Див. фіг. 14. При сушці етанолат І перетворюється на форму І. Або ж інший етанолат сполуки 2, етанолат II, одержують розчиненням аморфної сполуки 2 у 6 обсягах етанолу 1J1 (етанол-етилацетат). Суміш перемішують усю ніч та відфільтровують етанолат II. На фіг. 15 зображена рентгенодифракційна картина етанолату II, на фіг. 16 - ДСК етанолат у II. Ізопропанолат Сполуку 2 розчиняють у 10 обсягах діметилформаміду при кімнатній температурі. Через 10 хвилин додають 60 обсягів ізопропилового спирту. Суміш перемішують 30 хвилин. Ізопропанолат І відфільтровують та визначають порошковою рентгенодифракцією й ДСК. Див. фіг. 17 та 18. Вологий коржик являє собою ізопропанолат + ДМФ. При сушці зразок розкладається до аморфної сполуки з вмістом розчинника. Інший ізопропанолат II сполуки 2 одержують, суспендуючи аморфну сполуку 2 в ізопропиловому спирті при кімнатній температурі протягом 2-3 діб. Див. фіг. 19 та 20, де зображені відповідно рентгенодифракційна картина та криві ДСК. Ацетонат Сполуку 1 розчиняють у 32 обсягах ацетону при підвищеній температурі. Одразу ж додають стехіометричну кількість розчину глюкуронової кислоти у 3-4 обсягах води. Негайно починається зародкоутворення. Одержану суміш перемішують на кризі 30 хвилин, після чого залишають на ніч без перемішування. Одержану сполуку відфільтровують. На фіг. 21 наведена рентгенодифракційна картина ацетонату. При сушці ацетонат сполуки 2 перетворюється на форму І. Приклад 12 Інтегровані значення сигналів від глюкуронової кислоти порівнюють з унікальним піком сполуки 1 (фіг. 4), щоб одержати молярне співвідно 35 96930 шення між глюкуроновою кислотою та сполукою 1. Співвідношення кислота : сполука 1 знаходиться у межах 0.94-0.95. 36 Порівняння рівноважних розчинностей гідрохлориду, гідробромиду та глюкуронату сполуки 1 представлено у табл. 10. Таблиця 10 Порівняння рівноважних розчинностей солей сполуки 1 Сіль сполуки 1 вільна основа (1) гідрохлорид мезилат гідробромид глюкуронат (2) Розчинність (мг/мл) (еквівалент вільної основи) 0.22 1.46 0.021 1.26 19.93 Приклад 12 Одержання композиції уповільненої дії Композиція А Таблетки уповільненої дії, які містять сполуку 2 (30 мас. %), мікрокристалічну целюлюзу (29 мас. %), гіпромелозу (40 мас. %) та стеарат магнію (1 мас. %), одержують тонким змішуванням сполуки 2, частини мікрокристалічної целюлози, гіпромелози та частини стеарату магнію з наступним сухим гранулюванням суміші на роликовому пресі. Одержані пресовки далі класифікують подрібненням та/або розсіванням. Домішують решту мікрокристалічної целюлози, змащують гранулят рештою стеарату магнію та пресують таблетки. Композиція В Іншим прикладом композиції уповільненої дії є багатокомпонентна композиція з ядром, утвореним сполукою 2 (70 мас. %) та мікрокристалічною целюлюзою (30 мас. %). Ядро одержують змішуванням компонентів та їх гранулюванням з водою у планетарному змішувачі. Далі за допомогою системи Nica® одержану вологу масу екструдують крізь сито 1,0 мм. Екструдат подають до гранулятора, де протягом 2-3 хвилин на швид рН 4.72 4.82 4.2 4.73 4.25 кості 700 об/хв формуються сферичні гранули. Вологі гранули сушать у сушарці киплячого шару до вологості 2-5%. Висушені гранули розсіюють на грохоті 18 меш, видаляючи надвелику фракцію. Після того на гранули наносять суцільне покриття з Opadry® Clear (5 мас. % ) та води (95 мас. %). Для цього до апарату киплячого шару вставляють колонку Вурстера та донну розпилювальну систему, а далі наносять покриття Opadry® при температурі на вході біля 60 °С, швидкість подачі розчину покриття 5-10 г/хв, тиск розпилювання 1-2 бар. Температура готового продукту становить 38-43 °C. Після того, як досягнуто збільшення маси покриття на 2%, можна наносити покриття з етилцелюлози. Воно містить Surelease® (водну дисперсію етилцелюлози з 25% твердої фази - 5 мас. %) та воду (95 мас. %) й наноситься таким само чином, як і суцільне покриття, становлячи 3-8% маси таблетки. Після нанесення шару етилцелюлози гранули сушать ще 5-10 хвилин. Далі гранули видаляють та розсіюють на грохоті 18 меш, щоб видалити агломерати та надвелику фракцію. 37 96930 38 39 96930 40 41 96930 42 43 96930 44 45 96930 46 47 96930 48 49 96930 50 51 96930 52 53 96930 54 55 96930 56 57 96930 58 59 96930 60
ДивитисяДодаткова інформація
Назва патенту англійськоюSustained-release composition comprising glucuronate salt of piperazine compounds and use thereof
Автори англійськоюAli Kadum, Diorio Christopher R., Ehrnsperger Eric C., Fawzi Mahdi B., Shah Syed Muzafar
Назва патенту російськоюКомпозиция замедленного действия, которая содержит глюкуронатную соль соединений пиперазина и ее применение
Автори російськоюАли Кадум, Диорио Кристофер Р., Эрншпергер Эрик С., Фавзи Махди Б., Шах Суэд Музафар
МПК / Мітки
МПК: A61P 25/06, A61P 25/16, A61P 25/24, A61P 25/18, A61P 25/28, A61K 31/538, A61K 9/22, A61K 9/36
Мітки: уповільненої, піперазину, застосування, сполук, глюкуронатну, дії, композиція, містить, сіль
Код посилання
<a href="https://ua.patents.su/33-96930-kompoziciya-upovilneno-di-shho-mistit-glyukuronatnu-sil-spoluk-piperazinu-ta-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Композиція уповільненої дії, що містить глюкуронатну сіль сполук піперазину, та її застосування</a>
Попередній патент: Спосіб та вимірювальний пристрій для місцевого визначення витрат на обігрів
Наступний патент: Кліть прокатного стана з пристроєм зміщення
Випадковий патент: Спосіб копіювання міжрядь коренеплодів копірами автомата водіння коренезбиральної шестирядної машини і копір для його здійснення