Імідазотриазинонові сполуки та фармацевтична композиція, що їх містить
Номер патенту: 90502
Опубліковано: 11.05.2010
Автори: Остуні Емануель, Кемпбелл Стюарт, Кейтс Стівен, Світнем Пол, Гроган Майкл, Даффі Девід, Шюллер Олівер
Формула / Реферат
1. Сполука формули А
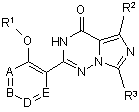 (А)
(А)
або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де
R1 являє собою нижчий алкіл;
R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
А являє собою N або С-Н;
В являє собою N, С-Н, C-(SO2-R4) або C-CO-R4;
D являє собою N, С-Н, C-(SO2-R4) або C-CO-R4;
Е являє собою N або С-Н;
де тільки один з А, В або Е може бути N, і один з В або D являє собою С-(SO2-R4) або C-CO-R4;
R4 являє собою групу, що має формулу:
 , (С)
, (С)
де
кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
і додатково або альтернативно R6 і R5 разом утворюють 5- або 6-членне кільце, або R6 і R7 разом утворюють 3-6-членне кільце;
R9 незалежно вибраний з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
альтернативно R8 і R9 разом з азотом, до якого вони прикріпляються, утворюють 5- або 6-членне кільце; n являє собою 1-4; і m являє собою 1-6.
2. Сполука за п. 1, де:
А являє собою С-Н;
В являє собою С-Н;
D являє собою C-(SO2-R4); і
Е являє собою С-Н.
3. Сполука за п. 2, де m являє собою 1 або 2.
4. Сполука за п. 3, де n являє собою 1.
5. Сполука за п. 1, де:
R1 являє собою етил;
R2 являє собою метил;
R3 являє собою пропіл;
А являє собою С-Н;
В являє собою С-Н;
D являє собою C-(SO2-R4); і
Е являє собою С-Н.
6. Сполука за п. 1, що має формулу:
 ,
,
де
R1, R2, R3 R5, R6, R7, R8 і R9 є такими, як визначено в п. 1 для формули А.
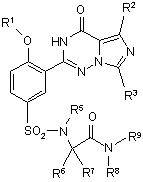
7. Сполука за п. 5, що має формулу:
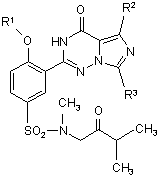 ,
,
де
R1, R2 і R3 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо.
8. Сполука за п. 1, що має формулу:
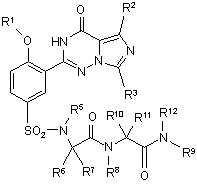 ,
,
де
R1 являє собою нижчий алкіл;
R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщеними одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
R5, R6, R7, R8, R9, R10, R11 і R12 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
і додатково або альтернативно R6 і R5 або R8 і R10 разом утворюють 5- або 6-членне кільце, або R6 і R7 або R10 і R11 разом утворюють 3-6-членне кільце; і R9 і R12 разом із азотом, до якого вони прикріпляються, утворюють 5- або 6-членне кільце.
9. Сполука за п. 8, що має формулу:
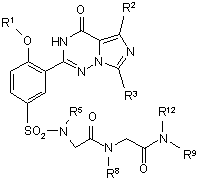 ,
,
де
R1, R2, R3 R5, R8, R9 і R12 є такими, як визначено в п. 8.
10. Сполука за п. 9, що має формулу:
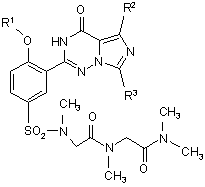 ,
,
де
R1 являє собою нижчий алкіл; і
R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо.
11. Сполука за п. 1, що має формулу, вибрану з:
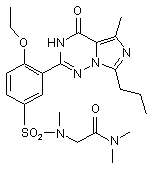 ,
, 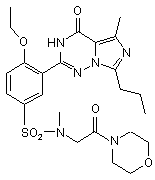 ,
, 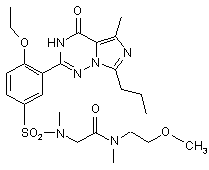 ,
, 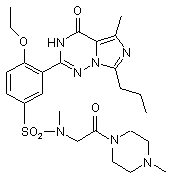 ,
, 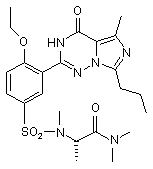 ,
, 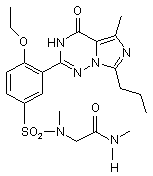 ,
, 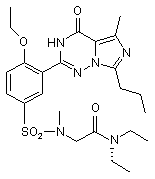 ,
, 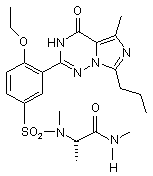 ,
, 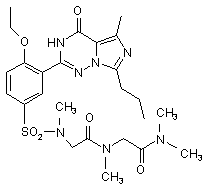 ,
, 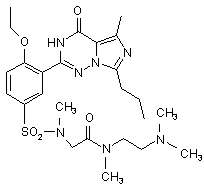 ,
, 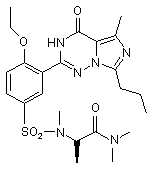 ,
, 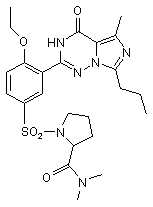 ,
, 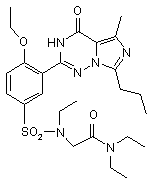 ,
, 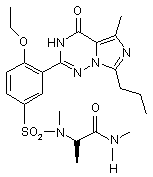 ,
, 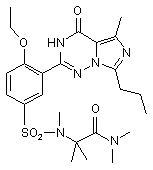 ,
, 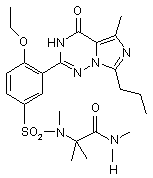 ,
, 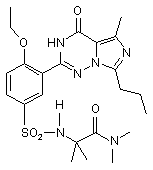 ,
, 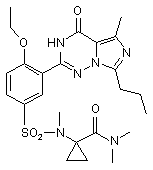 ,
, 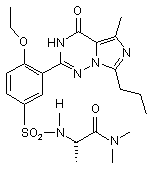 ,
, 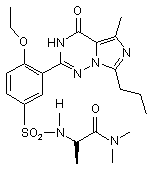 .
.
12. Сполука формули D
 (D)
(D)
або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де:
R1 являє собою нижчий алкіл;
R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо;
А являє собою N або С-Н;
В являє собою N, С-Н, C-(SO2-NH-R13) або C-CO-NH-R13;
D являє собою N, С-Н, C-(SO2-NH-R13) або C-CO-NH-R13;
Е являє собою N або С-Н;
де тільки один з А, В або Е може бути N, і один з В або D являє собою С-(SО2-NH-R13) або C-CO-NH-R13;
R13 являє собою нижчий алкіл.
13. Сполука за п. 12, де R13 являє собою метил.
14. Сполука за п. 12, де R2 і R3 незалежно вибрані з нижчого алкілу.
15. Сполука за п. 12, що має формулу D1:
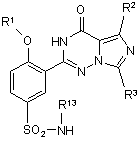 , (D1)
, (D1)
або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де
R1 являє собою нижчий алкіл;
R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо; і
R13 вибраний з нижчого алкілу.
16. Сполука за п. 15, де R13 являє собою метил.
17. Сполука за п. 15, де R2 і R3 незалежно вибрані з нижчого алкілу.
18. Сполука за п. 15, що має формулу
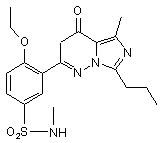 .
.
19. Фармацевтична композиція, що містить сполуку за п. 1 або п. 12 і фармацевтично прийнятний носій.
20. Спосіб лікування еректильної дисфункції, що містить введення людині або тварині ефективної кількості сполуки за п. 1 або п. 12 і фармацевтично прийнятного носія.
Текст
1. Сполука формули А R2 O R1 C2 2 (11) 1 R9 , 3 90502 R1, R2, R3 R5, R6, R7, R8 і R9 є такими, як визначено в п. 1 для формули А. 7. Сполука за п. 5, що має формулу: R2 O R1 O HN N N R3 SO2 R12 O N HN O R10 N N R7 R8 R11 O , де R1, R2, R3 R5, R8, R9 і R12 є такими, як визначено в п. 8. 10. Сполука за п. 9, що має формулу: R2 O R1 O HN N CH3 SO2 N N R3 CH3 O N N N CH3 O CH3 R3 R5 R9 R8 N N N N CH3 N N N O N R6 HN R5 , де R1, R2 і R3 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо. 8. Сполука за п. 1, що має формулу: R2 O 1 R SO2 O N N CH3 O R2 O R1 R3 CH3 SO2 4 R12 N R9 O , де R1 являє собою нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщеними одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо; R5, R6, R7, R8, R9, R10, R11 і R12 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо; і додатково або альтернативно R6 і R5 або R8 і R10 разом утворюють 5- або 6-членне кільце, або R6 і R7 або R10 і R11 разом утворюють 3-6-членне кільце; і R9 і R12 разом із азотом, до якого вони прикріпляються, утворюють 5- або 6-членне кільце. 9. Сполука за п. 8, що має формулу: , де 1 R являє собою нижчий алкіл; і R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо. 11. Сполука за п. 1, що має формулу, вибрану з: O O HN N N N O SO2 N N , O O HN N N N O SO2 N N O , 5 90502 6 O O O HN N O N N HN N O O SO2 N N N SO2 O N CH3 N N H , O O HN N O N N HN N CH3 SO2 N N CH3 O CH3 , , O HN O N N HN N CH3 SO2 N N N N O SO2 N N O N CH3 O N O N N N O SO2 , O CH3 O N N N , CH3 CH3 O , O O HN N N N O HN N O SO2 N O N SO2 H N , O O HN N N , O O N N HN N N N N N O SO2 N SO2 N , O N N , 7 90502 8 O O O HN N O N N HN N O O SO2 N N N SO2 N N N , , O O O O HN N HN N N N H O SO2 N SO2 , N H N SO2 N N N N N H , O HN N N N HN N A B O N N 12. Сполука формули D R2 O R1 O HN N SO2 O . O H N N N , O HN N N O SO2 N , O HN N O N O O SO2 O N H O N N O N , E N N R3 D (D) або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де: R1 являє собою нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо; А являє собою N або С-Н; В являє собою N, С-Н, C-(SO2-NH-R13) або C-CONH-R13; D являє собою N, С-Н, C-(SO2-NH-R13) або C-CONH-R13; Е являє собою N або С-Н; де тільки один з А, В або Е може бути N, і один з В або D являє собою С-(SО2-NH-R13) або C-CO-NHR13; 9 90502 R13 являє собою нижчий алкіл. 13. Сполука за п. 12, де R13 являє собою метил. 14. Сполука за п. 12, де R2 і R3 незалежно вибрані з нижчого алкілу. 15. Сполука за п. 12, що має формулу D1: R2 O R1 O HN N R13 N N 10 R13 вибраний з нижчого алкілу. 16. Сполука за п. 15, де R13 являє собою метил. 17. Сполука за п. 15, де R2 і R3 незалежно вибрані з нижчого алкілу. 18. Сполука за п. 15, що має формулу O O N N N R3 SO2 NH O2S NH , (D1) або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де R1 являє собою нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу, і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогенами, нижчими алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілами і алкілтіо; і . 19. Фармацевтична композиція, що містить сполуку за п. 1 або п. 12 і фармацевтично прийнятний носій. 20. Спосіб лікування еректильної дисфункції, що містить введення людині або тварині ефективної кількості сполуки за п. 1 або п. 12 і фармацевтично прийнятного носія. Фізіологічні і клінічні ефекти інгібіторів фосфодіестерази, специфічної до циклічного гуанозин 3', 5' монофосфату (цГМФ-специфічної PDE) передбачають, що такі інгібітори корисні при різних хворобливих станах, в яких бажаною є модуляція функції гладеньких м'язів, ренальної, гемостатичної, функції запалення та/або ендокринної функції. Тип 5 цГМФ - специфічної фосфодіестерази (PDE5) є головним ферментом, що гідролізує цГМФ гладеньких м'язах судин. Таким чином, інгібітор PDE5 може бути показаний для лікування серцевосудинних порушень, включаючи гіпертензію, цереброваскулярні порушення і порушення сечостатевої системи, зокрема еректильної дисфункції, але не обмежуючись ними. На сьогоднішній день наявні фармацевтичні продукти, що забезпечують селективне інгібування PDE5. Варденафіл, що випускається під торговою назвою Левітра (Levitra ) є сильним і селективним інгібітором PDE5 і на сьогоднішній день назначається для лікування еректильної дисфункції. Існує нагальна потреба для покращення фармакокінетичних властивостей PDE5 інгібіторів. Розробка нового фармацевтичного агенту потребує точної оптимізації хімічних і біологічних властивостей вихідної сполуки. Наприклад, вдалий кандидат на лікарський засіб повинен бути безпечним і ефективним для його передбачуваного використання. Крім того, сполука повинна володіти бажаними фармакокінетичними та фармакодинамічними профілями. Цей важкий процес розробки звичайно вимагає проведення широких експериментів. В багатьох випадках процес визначення оптимальної сполуки може часто вимагати приготування тисячі структурно схожих сполук. Серед властивостей, що можуть обмежувати використання потенційного фармацевтичного агенту є ступінь того, як сполука включається в комплекси з протеїнами in vivo. Якщо високий відсоток сполуки присутній in vivo є неспецифічно зв'язаним, наприклад, з компонентами крові і плазми крові, то це залишає тільки дуже малу кількість вільної сполуки доступною тканині для проявлення її терапевтичної функції. Таким чином, зв'язування сполуки з різними білками та іншими компонентами плазми може вимагати неприйнятно великої дози сполуки для досягнення бажаного терапевтичного ефекту. Підшукують традиційні підходи, що змінюють фармакокінетичні властивості. Пегілювання, спосіб кон'югування або зв'язування біомолекули і систем доставки лікарського засобу, наприклад, ліпосом, білків, ферментів, лікарських засобів, наночастинок з поліетиленгліколем, є відомим способом для змінення фармакокінетичних властивостей шляхом покращення періоду напівциркуляції портеїнних і ліпосомальних фармацевтичних засобів. (Див., Bhadra et al. Pharmazie 2002 Jan; 5791):5-29). Пегільовані лікарські засоби мають оболонку високомолекулярного поліетиленгліколю (PEG) навколо лікарького засобу, що захищає лікарський засіб від ферментативної деградації, і дозволяє лікарському засобу перетинати кишечник, а саме забезпечує пероральну доступність і також діє як захисний пристрій для попередження розпізнавання пегільованого лікарського засобу клітинами імунної системи і захищає лікарський засіб від печінкового кліренсу, (див., Molineux, Cancer Treat Rev. 2002 Apr, 28 Suppl A: 13-16). В результаті, пегільований білок, наприклад, має покращені фармакокінетичні влас 11 тивості завдяки зменшеному гідролізу і більшому періоду напівциркуляції. Протиракові агенти мають субоптимальний фармакокінетичний профіль, що потребує пролонговане або повторне введення лікарського засобу. Показано, що пегільовані портиракові агенти, наприклад, пегфілграстим, пегільований філграстим, підтримує ефективність лікарського засобу і толерантість пацієнту, що є, щонайменше, еквівалентними до цих показників немодифікованого філграстиму з тільки одним введенням на цикл хіміотерапії, (див., Crawford, Cancer Treat Rev. 2002 Apr; 28 Suppl A:7-1 1) Виявлено, що пегільований ліпосомальний доксорубіцин, інший хіміотерапевтичний агент, є більш ефективним і менш кардіотоксичним, ніж непегільований або ліпосомо-інкапсульований доксорубіцин. (Див., Crawford, 2002) Крім покращених фармакокінетичних властивостей, пегільовані лікарські засоби дозволяють зменшити схеми дозування, наприклад, фіксована доза замість дози, що основана на вазі. (See, Yowell і Blackwell, Cancer Treat Rev. 2002 Apr; 28 Suppl A:3-6) 3 огляду на розмір ПЕГ, його геометрію і місце прикріплення до пегільованого терапевтичного агенту, наприклад, білків, визначені фармакокінетичні властивості лікарського засобу, терапевтичні агенти повинні бути створені на основі білок-за-білком. (Див., Harris et al. Clin. Pharmacokinet. 2001, 40(7):539-551) Недоліком пегільованих агентів є потенційне зменшення активності лікарського засобу в місці-мішені через просторову перешкоду великої молекули ПЕГ. Розмір молекули ПЕГ має більше відношення до невеликих молекул, ніж до білків. Даний винахід стосується 2-феніл заміщених імідазотріазинонових сполук із функціональною групою саркозину, що має покращені характеристики неспецифічного зв'язування і фармакокінетичні властивості. Одиниця саркозину слугує для збільшення зв'язування протеїну, таким чином збільшення кількості вільної форми сполука. Функціональні залишки, що прикріплюються до сполуки, відрізняються за їх хімічною структурою від груп, що використовують в ПЕГ технологіях, наприклад, функціональним залишком може бути похідна етиленгліколю, функціональні залишки мають значно меншу молекулярну вагу, наприклад, приблизно MB 100 дальтон, порівняно з 5000 дальтон або більше, що використовують у стандартному пегілюванні. Відповідно, хімічна або біологічна активність сполук, що містять функціональні залишки за даним винаходом не змінюється через меншу просторову перешкоду і більшу доступність лікарського засобу до місця(місць)-мішеней для сполуки. Забезпечується сполука формули А, що має покращені властивості неспецифічного зв'язування і фармакокінетичні властивості: 90502 12 або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; А є N або С-Н; В є N, С-Н, C-(SO2-R4), або C-CO-R4; D є N, С-Н, C-(SO2-R4) або C-CO-R4; Е є N або С-Н; де тільки один з А, В або Е може бути N, і один з В або D є C-(SO2-R4) або С-СО-R4; R4 являє собою групу, що має формулу: в якій кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5 разом утворюють 5або 6-членне кільце, або R6 і R7 разом утворюють 3-6 членне кільце; R9 незалежно вибраний з Н і нижчий алкіл, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце; n є1-4; і m є 1-6. У переважному варіанті здійснення за даним винаходом, забезпечується сполука формули А1 або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий 13 алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; 4 R являє собою групу, що має формулу: в якій кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5 разом утворюють 5або 6-членне кільце, або R6 і R7 разом утворюють 3-6 членне кільце; R9 незалежно вибраний з Н і нижчий алкіл, де нижчий алкіл може бути необов'язково заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце; n є 1-4; і m є 16. У переважних варіантах здійснення сполук формули А1, m є 1 або 2. Також у переважних варіантах здійснення, n є 1. В іншому переважному варіанті здійснення за даним винаходом забезпечується сполука формули В: де R4 є таким, як описано вище для сполуки формули А1. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу: 90502 14 де, R1, R2, R3 R5, R6, R7, R8 і R9 є такими, як визначено вище для сполуки формули А. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу: де, R1, R2 і R3 незалежно вибрані з Н і нижчого алкіл, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу: де, R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; R5, R6, R7, R8, R9, R10, R11 і R12 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R5 і R5, або R8 і 10 R разом утворюють 5- або 6-членне кільце, або R6 і R7, або R10 і R11 разом утворюють 3-6 членне кільце; і R9 і R12 разом з азотом, що прикріплюється до них, утворюють 5- або 6- членне кільце. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу: 15 де, R1, R2, R3 R5, R8, R9 і R12 є такими, як визначено вище. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу: де, R1 є нижчий алкіл; і R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу D: або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де: R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл, і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; А є N або С-Н; В є N, С-Н, C-(SO2-NH-R13), або C-CO-NH-R13; D є N, С-Н, C-(SO2-NH-R13) або C-CO-NH-R13; Е є N або С-Н; 90502 16 де тільки один із А, В або Е може бути N, і один із В або D є C-(SO2-NH-R13) або C-CO-NHR13; R13 є нижчий алкіл. В переважних варіантах здійснення сполук формули D, R13 являє собою метил. В інших переважних варіантах здійснення сполук формули D, R2 і R3 незалежно вибрані з нижчого алкілу. В іншому переважному варіанті здійснення за даним винаходом, забезпечується сполука, що має формулу D1; або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл, і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і R13 вибраний з нижчого алкілу. В переважних варіантах здійснення сполук формули D1, R13 являє собою метил. Також в переважних варіантах здійснення R2 і R3 незалежно вибрані з нижчого алкілу. Даний винахід включає фармацевтичні композиції, що містять сполуки за винаходом і фармацевтично придатний носій та/або розчинники. Даний винахід включає фармацевтичні композиції, що містять по суті чисту сполуку за винаходом, або її фармацевтично прийнятну сіль, стереоізомер або гідрат, і фармацевтично прийнятний носій та/або розчинники. Даний винахід також включає способи лікування еректильної дисфункції, що містять введення людині або тварині ефективної кількості сполук за винаходом. Фігура 1 показує різні сполуки, що відображують варіант здійснення за даним винаходом. Фігура 2 показує різні сполуки, що відображують варіант здійснення за даним винаходом. Фігура 3 показує відому сполуку варденафіл. Сполуки за винаходом забезпечують покращені фармакокінетичні властивості в порівнянні до попередніх 2-феніл заміщених сполук імідазолоатріазинону шляхом модифікації неспецифічного зв'язування in vivo білку зі сполуками. Фармакокінетично покращені сполуки за винаходом переважно дозволяють вводити мінімальну ефективну кількість сполука для досягнення бажаного терапевтичного ефекту незв'язаної сполука, таким чи 17 ном зменшуючи кількість дозування (і може покращити переносимість пацієнтом). В одному варіанті здійснення даний винахід забезпечує сполуку формули А: або її фармацевтично прийнятну сіль, стереоізомер або гідрат, де R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; A єN або C-H; В є N, С-Н, C-(SO2-R4), або C-CO-R4; D є N, C-H, C-(SO2-R4) або C-CO-R4; E є N або C-H; де тільки один із А, В або Е може бути N, і один із В або D є C-(SO2-R4) або С-CO-R4; R4 є групою, що має формулу: в якій кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5 разом утворюють 5або 6-членне кільце, або R6 і R7 разом утворюють 3-6 членне кільце; R9 незалежно вибраний з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщенимі одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце; n є 1-4; і m є 16. В переважному варіанті здійснення, R2 і R3 незалежно вибрані з нижчого алкілу. Вірогідно, що група, яка має формулу С модулює фармакокінетичний та/або фармакодинамічний профіль сполуки і може приводити до покращення фармакокінетичних властивостей у порівнянні до немодифікованої, а саме родинної сполуки. У певних варіантах здійснення, R4 є активним агентом, що має покращені фізико-хімічні властивості, фармакокінетичні властивості, метаболізм або профіль токсичності. В переважному варіанті здійснення, активний агент має кращу 90502 18 розчинність, нижчу ІС50, та/або є значно менше зв'язаним з білком in vivo в порівнянні зі сполукою, в якій не має, щонайменше, одного функціоального залишку. Переважно, сполуки за винаходом включають, але не обмежуються ними, інгібітори й активатори білків і ферментів (наприклад, фосфодіестерази, такі як PDE5, PDE1, PDE3 і PDE6, кінази, рецептори фактору росту і протеази). У варіанті здійснення за даним винаходом забезпечується сполука, що містить, щонайменше, один функціональний залишок, що є похідним саркозину. В переважному варіанті здійснення похідна саркозину має формулу: де кожний R являє собою водень або заміщену або незаміщену групу нижчого алкілу. Переважно, саркозин або залишок саркозину прикріплюється до сполуки ковалентним зв'язком до Nтермінального атому азоту залишку саркозину або олігомеру. В переважному варіанті здійснення за даним винаходом забезпечується сполука формули А1 або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де R1 є нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; R4 являє собою групу, що має формулу: в якій кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатко 19 во або альтернативно R6 і R5 разом утворюють 5або 6-членне кільце, або R6 і R7 разом утворюють 3-6 членне кільце; R9 незалежно вибраний з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщенимі одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце; n є 1-4; і m є 16. В одному варіанті здійснення сполука має наступну формулу: 90502 20 де R4 представляє, щонайменше, один функціональний залишок, що переносить природний піперазин шляхом прикріплення до сірки родинної сполуки шляхом ковалентного зв'язку. В сполуці А, А1 або В, R4 може бути сполукою, що має формулу С: в якій кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5 разом утворюють 56 7 або 6-членне кільце, або R і R разом утворюють 9 3-6 членне кільце; R незалежно вибраний з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце. Переважно, функціональна група, що прикріплюється до сульфонільної групи, є похідною саркозину або олігомером. Переважний варіант здійснення має формулу: де кожний R5, R6, R7 і R8 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5 разом утворюють 5або 6-членне кільце, або R5 і R7 разом утворюють 3-6 членне кільце; R9 незалежно вибраний з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; альтернативно R8 і R9 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце; n є 1-4; і m є 16. У переважному варіанті здійснення, R4 являє собою метил-аміно-диметилацетамід, для отримання сполуки, що має формулу І: в якій R1, R2 і R3 є такими, як визначено вище для сполуки А. У більш переважному варіанті здійснення каркас або скелет може бути PDE5 інгібітором, що має формулу (В): В іншому варіанті здійснення, R4 являє собою метил-аланін-диметиламід, для отримання сполуки, що має формулу II: 21 В іншому варіанті здійснення, R4 являє собою 2-метиламіно-2-триметил-пропіонамід для отримання сполуки, що має формулу III: В інших переважних варіантах здійснення, m є 1 або 2 для R4 (Формула С), що прикріплюється до Сполуки А. Переважно, n є і. Також у варіанті здійснення, сполука має наступну формулу: в якій R1, R2, R3 є такими, як визначено вище для сполуки А; R5, R6, R7, R8, R9, R10, R11 і R12 незалежно вибрані з Н і нижчого алкілу, де нижчий алкіл може бути необов'язково заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; і додатково або альтернативно R6 і R5, або R8 і R10 разом утворюють 5-або 6-членне кільце, або R6 і R7, або R10 і R11 разом утворюють 3-6 членне кільце; і R9 і R12 разом з азотом, що прикріплюється до них, утворюють 5- або 6-членне кільце. Для вищеописаних варіантів здійснення, переважно, кожний R6, R7, R10 і R11 являють собою водень. Більш переважно, димер саркозину прикріплюється до сульфонільної групи, і сполука має формулу: 90502 22 в якій R1, R2 і R3 є такими, як визначено вище для сполуки А. В окремих переважних варіантах здійснення, R1 являє собою етил, R2 являє собою метил, і R3 являє собою пропіл. Термін "гетероатом", як використовується в даному описі означає атом будь-якого елементу, крім вуглецю або водню. Переважні гетероатоми являють собою бор, азот, кисень, фосфор, сірку і селен. Більш переважними є азот або кисень. Термін "алкіл" відноситься до радикалу насичених аліфатичних груп, включаючи нерозгалужені алкільні групи, розгалужені алкільні групи, циклоалкільні (аліциклічні) групи, алкіл заміщені циклоалкільні групи і циклоалкіл заміщені алкільні групи. В переважних варіантах здійснення алкіл з нерозгалуженим і розгалуженим ланцюгом має 30 або менше атомів вуглецю в його скелеті (наприклад, С1-С30 для нерозгалуженого ланцюгу, С3-С30 для розгалуженого ланцюгу), і більш переважно 20 або менше. Аналогічно, переважні циклоалкіли мають 3-10 атомів вуглецю в структурі його кільця, і більш переважно мають 5, 6 або 7 атомів вуглецю в структурі кільця. За винятком числа атомів вуглецю, визначених протилежно, "нижчий алкіл", як використовують в даному описі, означає алкільну групу, як визначено вище, але, що має від одного до десяти атомів вуглецю, і більш переважно від одного до шести атомів вуглецю в структурі його скелету. Аналогічно, "нижчий алкеніл" і "нижчий алкініл" мають схожі довжини ланцюгів. Переважні алкільні групи являють собою нижчі алкіли. В переважних варіантах здійснення замісник, визначений в даному описі як алкіл, являє собою нижчий алкіл. Термін "аралкіл", як використовується в даному описі, відноситься до алкільної групи, заміщеної арильною групою (наприклад, ароматичною або гетероароматичною групою). Терміни "алкеніл" і "алкініл" відносяться до ненасичених аліфатичних груп, аналогічних за довжиною і можливим заміщенням до алкілів, описаних вище, але вони містять, щонайменше, один подвійний або потрійний зв'язок, відповідно. Термін "арил", як використовується в даному описі, включає 5- і 6-членні однокільцеві ароматичні групи, що можуть включати від нуля до чотирьох гетероатомів, наприклад, бензен, пірен, пірол, фуран, тіофен, імідазоол, оксазол, тіазол, триазол, піразол, піридин, піразин, піридазин і піримідин і подібне. Ці арильні групи, що мають гетероатоми в структурі кільця, можуть також називатися "арильні гетероцикли" або "гетероароматичні сполуки". Ароматичне кільце 23 може бути заміщеним в одному або декількох положеннях в кільці замісниками, що описані вище, такими як, галоген, азид, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, алкоксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, силіл, простий ефір, алкілтіо, сульфоніл, сульфонамідо, кетон, альдегід, складний ефір, гетероциклічна, ароматична або гетероароматична частини, - CF3, -CN або подібне. Термін "арил" також включає поліциклічні кільцеві системи, що мають два або кілька циклічних кілець, в яких два або більше атомів вуглецю є спільними для двох суміжних кілець (ці кільця являють собою "конденсовані кільця") де, щонайменше, одне з кілець є ароматичним, наприклад, інші циклічні кільця можуть бути циклоалкілами, циклоалкенілами, арилами та/або гетероциклічними групами. Терміни "гетероциклічний" або "гетероциклічна група" відносяться до 3- -10- членних кільцевих структур, більш переважно 5- або 6-членних кілець, чиї кільцеві структури включають від одного до чотирьох гетероатомів. Гетероцикли можуть також бути поліциклами. Гетероциклічні групи включають, наприклад, тіофен, тіантрен, фуран, піран, ізобензофуран, хромен, ксантен, феноксантіїн, пірол, імідазол, піразол, ізотіазол, ізоксазол, піридин, піразин, піримідин, піридазин, індоолізин, ізоіндол, індол, індазол, пурин, хінолізин, ізохінолін, хінолін, фталазин, нафтиридин, хіноксалін, хіназолін, цинолін, птеридин, карбазол, карболін, фенантридин, акридин, піримідин, фенантролін, феназин, фенарсазин, фенотіазин, фуразан, феноксазин, піролідин, оксолан, тіолан, оксазол, піперидин, піперазин, морфолін, лактони, лактами, такі як азетидинони і піролідинони, султами, султони і подібні. Гетероциклічне кільце може бути заміщеним в одному або декількох положеннях як описано вище, як наприклад, галоген, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, силіл, простий ефір, алкілтіо, сульфоніл, кетон, альдегід, складний ефір, гетероциклічна, ароматична або гетероароматична частина, -CF3, -CN або подібне. Терміни "поліциклічний" або "поліциклічна група" відноситься до двох або декількох кілець (наприклад, циклоалкілів, циклоалкенілів, арилів та/або гетероциклічних сполук), в яких два або декілька атомів вуглецю є спільними для двох суміжних кілець, наприклад, кільця являють собою "конденсовані кільця". Кільця, що поєднуються через несуміжні атоми мають назву "кільце з внутрішнім мостиком". Кожне з кілець поліциклічної групи може бути заміщеним замісниками, що описані вище, такими як, галоген, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, силіл, простий ефір, алкілтіо, сульфоніл, кетон, альдегід, складний ефір, гетероциклічнаи, ароматична або гетероароматична частина, -CF3, -CN або подібне. Як використовується в даному описі, термін "нітро" означає -NO2; термін "галоген" означає -F, СІ, -Вr або -І; термін "сульфгідрил" означає -SH; 90502 24 термін "гідроксил" означає -ОН; і термін "сульфоніл" означає -SO2-. Терміни "амін" та "аміно" є загальноприйнятими в галузі техніки і відносяться як до незаміщених, так і до заміщених амінів, наприклад, частина, що може бути представлена загальною формулою: або де R, R' і R" кожний незалежно представляють групу, що дозволяється правилами валентності, переважно Н, алкіл, алкеніл, алкініл, аралкіл, арил і гетероциклічні групи. Термін "ациламіно" є загальноприйнятим в галузі техніки і відноситься до частини, що може бути представлена загальною формулою: де R і R1 є такими, як визначено вище. Термін "амідо" є загальноприйнятим в галузі техніки як аміно-заміщений карбоніл і включає частину, що може бути представлена загальною формулою: де R, R' є такими, як визначено вище. Переважні варіанти здійснення аміду не будуть включати іміди, які можуть бути нестабільними. Термін "алкілтіо" відноситься до алкільної групи, як визначено вище, що має радикал сірки, приєднаний до нього. В переважних варіантах здійснення частина "алкілтіо" представлена одним із S-алкіл, -S-алкеніл, -S-алкініл, і -S-(CH2)m-R'8, де m і R'8 визначені вище. Типові алкілтіо групи включають метилтіо, етилтіо і подібні. Термін "карбоніл" є загальноприйнятим і включає такі частини, що можуть бути представлені загальною формулою: або 25 де X являє собою зв'язок або представлений киснем або сіркою, і R і R' є такими, як визначено вище. Терміни "алкоксил" або "алкокси", як використовуються в даному описі, відноситься до алкільної групи, як визначено вище, що має радикал кисень, прикріплений до неї. Репрезентативні алкоксильні групи включають метокси, етокси, пропілокси, трет-бутокси і подібні. Термін "сульфонат" є загальноприйнятим і включає частину, що може бути представлена загальною формулою: в якій R41 являє собою електронну пару, водень, алкіл, циклоалкіл або арил. Абревіатури Me, Et, Ph, Tf, Nf, Ts, Ms представляють метил, етил, феніл, трифторметансульфоніл, нанофторбутансульфоніл, р-толуолсульфоніл і метансульфоніл, відповідно. Більш вичерпний список абревіатур, використовуваних хіміками фахівцями в галузі органічної хімії поданий в першому випуску кожного тому Журналу Органічної Хімії (Journal of Органічний Chemistry); цей список звичайно присутній в таблиці, названій Стандартний Список Абревіатур. Абревіатури, що містяться в згаданому списку, і всі абревіатури, що використовуються хіміками - фахівцями в галузі органічної хімії, включені в даний опис шляхом посилання. Термін "сульфат" є загальноприйнятим і включає частину, що може бути представлена загальною формулою: в якій R41 є таким, як визначено вище. Термін "сульфоніламіно" є загальноприйнятим і включає частину, що може бути представлена загальною формулою: Термін "сульфамоїл" є загальноприйнятим і включає частину, що може бути представлена загальною формулою: 90502 26 Термін "сульфоніл", як використовується в даному описі, відноситься до частини, що може бути представлена загальною формулою: в якій R44 вибраний з групи, що містить водень, алкіл, алкеніл, алкініл, циклоалкіл, гетероциклічну сполуки, арил або гетероарил. Термін "сульфоксидо", як використовується в даному описі, відноситься до частини, що може бути представлена загальною формулою: в якій R44 вибраний з групи, що містить водень, алкіл, алкеніл, алкініл, циклоалкіл, гетероциклічну сполуку, аралкіл або арил. "Селеноалкіл" відноситься до алкільної групи, що має заміщену селено групу, приєднану до неї. Наприклалд "селеноефіри", що можуть бути заміщені алкілом, вибрані з одного з -Se-алкілу, -Seалкенілу, -Se-алкінілу і -Se-(CH2)m-R7, m і R7, визначені вище. Аналогічні заміщення можуть бути зроблені на алкеніл і алкінільні групи для отримання, наприклад, аміноалкенілів, аміноалкінілів, амідоалкенілів, амідоалкінілів, іміноалкенілів, іміноалкінілів, тіоалкенілів, тіоалкінілів, карбоніл-заміщених алкенілів або алкінілів. Як використовується в даному описі, мається на увазі, що визначення кожного виразу, наприклад, алкіл, m, n, R, і т.ін., якщо вони зустрічаються більше одного разу в кожній структурі, є незалежними від їх визначення будь-де в однаковій структурі. Потрібно розуміти, що "заміщення" або "заміщений" включає умовне припущення, що таке заміщення знаходиться у відповідності до припустимої валентності заміщеного атому і замісник, і що заміщення приводить до стабільної сполуки, наприклад, яка не підлягає спонтанній трансформації, наприклад, шляхом, перерозподілу, циклізації, зникнення і т.ін. Як використовується в даному описі, термін "заміщений" передбачений, щоб включати всі припустимі замісники органічних сполук. В широкому розумінні припустимі замісники включають ациклічні і циклічні, розгалужені і нерозгалужені, карбоциклічні і гетероциклічні, ароматичні і неароматичні замісники органічних сполук. Ілюстративні замісники включають, наприклад, ті, що описані в даному описі вище. Припустимі замісники можуть бути одним або декількома і однаковими або різ 27 ними для відповідних органічних сполук. Для цілей даного винаходу гетероатоми, наприклад, азот можуть мати водень - замісники та/або будь-які припустимі замісники органічних сполук, описані в даному описі, що задовольняють валентностям гетероатомів. Не припускається, що припустимі замісники органічних сполук у будь-який спосіб обмежують даний винахід. Фраза "захисна група", як використовується в даному описі, означає тимчасові замісники, які захищають потенційно реактивну функціональну групу від небажаних хімічних трансформацій. Приклади таких захисних груп включають складні ефіри карбоксилових кислот, силілові складні ефіри спиртів, і ацеталі і кеталі альдегідів і кетонів, відповідно. Галузь хімії захисних груп була опублікована (Greene, Т. W.; Wuts, P.G.M. Protective Groups in Organic Synthesis, 2nd ed.; Wiley: New York, 1991). Як використовується в даному описі, термін "метаболіт" відноситься до сполуки, що метаболізується в організмі. Наприклад, варіант здійснення винаходу, Сполука 1 (Фігура 2) метаболізуючись в організмі, дає метаболіти, показані на Фігурі 9. Даний винахід також включає метоболіти кожних з вищезазначених сполук. В одному варіанті здійснення винаходу метаболіт може мати структуру, представлену формулою D: де R1 являє собою нижчий алкіл; R2 і R3 незалежно вибрані з нижчого алкілу, і нижчого алкенілу і нижчого алкінілу, де нижчий алкіл, нижчий алкеніл і нижчий алкініл можуть бути необов'язково заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом і алкілтіо; А являє собою N або С-Н; В являє собою N, С-Н, C-(SO2-NH-R13), або CCO-NH-R13; D являє собою N, С-Н, C-(SO2-NH-R13) або CCO-NH-R13; Е являє собою N або С-Н; де тільки один із А, В або Е може бути N, і один із В або D являє собою C-(SO2-NH-R13) або C-CO-NH-R13; R13 являє собою нижчий алкіл. В переважному варіанті здійснення, R2 і R3 незалежно вибрані з нижчого алкілу. В наступному 1 переважному варіанті здійснення, R являє собою метил. Переважні метаболіти включають сполуки, що мають формулу D1: 90502 28 де R1, R2 і R3 є такими, як визначено вище для Сполуки А, і R3 вибраний з нижчого алкілу, переважно метилу. Переважні варіанти здійснення включають сполуку формули Сполуки формули D і D1, або їх фармацевтично прийнятні солі, стереоізомери, гідрати або проліки, можуть бути введені безпосередньо пацієнту. Альтернативно, сполуки формули D і D1 можуть бути утворені в організмі пацієнту після введення родинної сполуки або пролікарського засобу. Таким чином, в одному варіанті здійснення винахід спрямований на способи інгібування PDE, зокрема PDE5, шляхом введення людині сполук формули D або D1. Наступний варіант здійснення за винаходом спрямований на способи інгібування PDE, зокрема PDE5, шляхом введення людині пролікарського засобу формує сполуку формули D або D1 in vivo, наприклад, як результат, отриманий після метаболізму. Таблиця 1-3 підсумовує окремі біологічні і фармакологічні властивості вищеописаних модифікованих сполук А. Таблиця 3 включає індекс селективності проти деяких PDE. Білкове зв'язування, проникність і розчинність вищеозначених сполук відображені в Таблиці 2. Окремі сполуки за даним винаходом можуть існувати в окремих геометричних або стереоізомерних формах. Даний винахід розглядає всі такі сполуки, включаючи цис- і транс-ізомери, R- і Sенантіомери, діастереомери, (D)- ізомери, (L)ізомери, їх рацемічні суміші та їх інші суміші, що охоплюється об'ємом даного винаходу. Додаткові асиметричні атоми вуглецю можуть бути присутніми в заміснику як алкільна група. Всі такі ізомери, а також їх суміші включені в даний винахід. Наприклад, в одному варіанті здійснення сполука або фармацевтична композиція являє собою пермутацію Сполуки 2, що має структуру: 29 Наступні ізомери цієї сполуки включені в даний винахід: 90502 30 Крім того, якщо бажаним є, наприклад, окремий енантіомер сполуки за даним винаходом, то він може бути приготовлений шляхом асиметричного синтезу або шляхом деривації з хіральним допоміжним засобом, де отриману діастереометричну суміш відділяють і допоміжна група, розщеплюючись, забезпечує чисті бажані енантіомери. Альтернативно, якщо молекула містить основну функціональну групу, таку як аміно або кислотну функціональну групу, таку як карбоксил, діастереометричні солі формуються з відповідною оптично-активною кислотою або основою з наступним розкладом діастереомерів, таким чином формуючи шляхом фракційної кристалізації або хроматографічних методів, добре відомих в даній галузі техніки, і наступне відновлення чистих енантіомерів. Даний винахід також включає наступні сполуки: 31 Сполуки за даним винаходом можуть діяти як інгібітори однієї або декількох фосфодіестераз, включаючи, наприклад PDE1, PDE2 і PDE5. Сполуки за даним винаходом можуть застосовуватись в фармацевтичних засобах для лікування станів, що пов'язані з інгібуванням фосфодіестераз, зокрема PDE5. Більш специфічно, сполуки за винаходом можуть бути використані для лікування серцево-судинних порушень, включаючи гіпертензію, цереброваскулярні порушення і порушення сечостатевої системи, зокрема, еректильної дисфункції, але не обмежуючись ними. Таким чином, даний винахід також включає способи лікування серцевосудинних порушень, гіпертензії, цереброваскулярних порушень, порушень сечостатевої системи і еректильної і дисфункції, що містить введення людині або тварині ефективної кількості будь-якої вищезазначеної сполуки. Для цілей даного винаходу хімічні елементи визначають відповідно до Таблиці Періодичної Системи Елементів, CAS версія, Підручник з Хімії та і Фізики, 67th Ed., 1986-87, під обкладинкою. Сполуки за даним винаходом, які модифіковані прикріпленням до них, щонайменше, одного залишку формул С, забезпечують модифіковані фармакокінетичні властивості, включаючи модифікане неспецифічне in vivo білкове зв'язування. Такі оптимальні фармакокінетичні властивості не ставлять під загрозу ані селективність, ані активність модифікованої сполуки. Модифікація білкового зв'язування основане на поверхневій технології, а саме приготування і скринінгу поверхонь за їх здатністю протидіяти адсорбції білків з розчину. Поверхні, що є резистентними до адсорбції білків з розчину відомі фахівцям в даній галузі як "резистентні до білків" поверхні. Функціональні групи можуть бути скринінговані для визначення групи(груп), присутніх в поверхнях, резистентних до білків, як описано, наприклад, в Chapman et al. Surveying for Surfaces that Resist the Adsorption of Proteins, J. Am. Chem. Soc. 2000, 122:8303-8304; Ostuni et al. A Survey of Structure-Property (Relationships of Surfaces that Resist the Adsorption of Protein, Langmuir 2001, і 17:5605-5620; Holmlin, et al. Zwitterionic SAMs that Resist Nonspecific Adsorption of Protein from Водний Buffer, Langmuir 2001, 17:2841-2850; і Ostuni et al. S elf-Assembled Monolayers that Resist the Adsorption of Proteins і the Adhesion of Bacterial і Mammalian Cells, Langmuir 2001, 17:6336-6343. В цілому, білкове зв'язування оцінюють шляхом вимірювання здатності молекул за винаходом 90502 32 зв'язуватись з одним або декількома компонентами сироватки людини або їх імітаторів. В одному варіанті здійснення прийнятні функціональні залишки можуть бути визначеними шляхом сринінгу поверхонь, що містять такі залишки для їх здатності протидіяти адсорбції компонентів сироватки, включаючи білки сироватки і переважно білки сироватки людини, але не обмежуючись ними. Кандидатці залишки можуть бути скринінговані безпосередньо шляхом прикріплення їх до твердої основи і тестуванням основи на білкову резистентність. Альтернативно, кандидатні залишки включають до, або приєднані до молекул необхідного фармацевтичного засобу. Такі сполуки можуть бути синтезовані на твердій основі або приєднані до твердої основи після синтезу. У необмежуючому прикладі аналізу безпосереднього зв'язування, іммобілізовані кандидатні функціональні залишки або молекули, що включають такі залишки тестують на їх здатність зв'язувати компоненти сироватки. Компоненти сироватки можуть бути помічені сигнальною частиною для визначення або може використовуватися поміченим вторинним реагентом, що зв'язується з такими компонентами сироватки. Поверхні, що є резистентними до адсорбції білків з розчину, відомі як "резистентні до білків" поверхні. Функціональні групи можуть бути скринінговані для визначення групи(груп), присутніх в резистентних до білків поверхонь, описаних, наприклад, в Chapman et al. Surveying for Surfaces that Resist the Adsorption of Proteins, J. Am. Chem. Soc. 2000, 122:8303-8304; Ostuni et al. A Survey of Structure-Property Relationships of Surfaces that Resist the Adsorption of Protein, Langmuir 2001, 17:5605-5620; Holmlin, et al. Zwitterionic SAMs that Resist Nonspecific Adsorption of Protein from Aqueous Buffer, Langmuir 2001, 17:2841-2850; і Ostuni et al. S elf- Assembled Monolayers that Resist the Adsorption of Proteins and the Adhesion of Bacterial і Mammalian Cells, Langmuir 2001, 17:6336-6343. При визначення функціонального залишку, що забезпечує таку білкову резистентність, фахівець в даній галузі зможе визначити прийнятний хімічний скелет або каркасвідомого біологічно або хімічно активної сполуки, до якої може бути прикріплений функціональний залишок як шляхом заміщення функціональної групи активної сполуки, так або переміщенням несуттєвої функціональної групи активної сполуки. Наприклад, як описано вище, присутність піперазинової групи на сполуці 33 буде означати, що така група може бути як переміщеною, так і заміщеною функціональним залишком. Фахівець в даній галузі, наприклад, медичний хімік, зможе розпізнати інші прийнятні групи відомих активних сполук, які можуть бути переміщені або заміщені, щонайменше, одним функціональним залишком. Відповідно, комбінаторні бібліотеки сполук, можуть бути утворені як описано нижче, де сполуки являють собою модифіковані сполуки, що містять кон'югат активного сайту сполуки (основний скелет сполуки, що має частково бажану активність), наприклад, сполука А і, щонайменше, один функціональний залишок, прикріплений до неї, де кожний кон'югат має різний функціональний залишок, прикріплений до нього, наприклад, залишки, що має формулу С, де кожна R група вибрана з різних груп, описаних в даному описі. Відповідно, бібліотека може бути використана для скринінгу безлічі різних функціональних залишків для покращення фармакокінетичних та/або фармакодинамічних властивостей, включаючи неспечифічне білкове зв'язування модифікованої сполуки. У переважних варіантах здійснення тверда основа сама по собі вибирається або модифікується для мінімалізації його взаємодії з компонентами сироватки. Приклади таких основ і систем аналізу описані в міжнародних заявках WO 02/48676, WO 03/12392, WO 03/18854, WO 03/54515, включених в даний опис шляхом посилання. Альтернативно, молекули за винаходом можуть бути змішані з одним або декількома компонентами сироватки в рідкій фазі, і визначають кількість незв'язаних молекул. Аналіз прямого зв'язування може бути проведений також в рідкій фазі. Наприклад, тестові сполуки можуть бути змішані з одним або декількома компонентами сироватки в рідкій фазі, і визначають незв'язані молекули. У прикладі переважного варіанту здійснення молекули, що мають зменшене білкове зв'язування, визначаються наступним чином: самоорганізований моношар тіольних молекул, що на кінцях має ангідридні групи, сформований на золотій поверхні. Набір невеликих молекул з аміновими групами на одному кінці, і групами, що розроблені для протидії зв'язування з альбуміном, наприклад, на іншому кінці, потім прикріплюються до поверхні через реакцію між аміном і ангідридом. Набори молекул розміщують на просторово розрізнені ділянки на золотій поверхні для утворення матриці молекул, що можуть протидіяти білковому зв'язуванню. Цю матрицю потім поміщають в розчин, що містить флуоресцентно помічений альбумін. Після відповідного інкубаційного періоду золоту поверхню відмивають і сканують на флуоресцентному сканері. Іммобілізовані хімічні групи, що зв'язують альбумін буде визначатися шляхом присутності флуоресцентного сигналу; групи, що протидіють зв'язування альбуміну буде мати низьку флуоресценцію в цій частині матриці. Якщо флуоресцентний білок не доступний, то антитіла проти досліджуваного білка в комбінаціях з флуоресцентними вторинними антитілами можуть використовуватися для визначення білкового зв'язування з хімічними групами. Якщо антитіло не доступне, то спосіб 90502 34 визначення, що не використовує мітку, такий як резонанс поверхневого плазмону (SPR) або MALDI мас-спекртометрія, може бути використаний для визначення присутності білку на індивідуальних елементах в матриці. SPR також має перевагу в забезпеченні кінетичної інформації щодо зв'язування білка з хімічними групами. Використання цієї системи не обмежується альбуміном; будь-який білок, цікавий з точки зору фармакокінетики, можна тестувати на силу зв'язування. Наприклад, білки крові, що зв'язують невеликі молекули, такі як -кислий глікопротеїн (AAG, AGP) і ліпопротеїни, також можна помістити в матрицю і визначити білкове зв'язування. У варіанті здійснення даного винаходу можна визначити хімічні групи, що протидіють зв'язуванню з Р-глікопротеїном (PGP) і таким чином, мають ! потенціал для зменшення виходу, коли їх додають до терапевтичного засобу з невеликим розміром молекули. Це зокрема важливо для розробки протиракових лікарських засобів, що забезпечує ефективне лікування в той час, як розвивається множинна резистентність до лікарських засобів (MDR). Спосіб можна також використовувати для визначення хімічних груп, що протидіють зв'язуванню з білками, наприклад тромбін, антитромбін і Фактор Ха і, таким чином, мають потенціал для контролю коагуляції. Цей спосіб може бути також корисним для визначення групи, що покращує терапевтичні засоби, що розроблені як додаткова або заміщуюча терапії, де білкове зв'язування і ФК властивості є дуже важливими, наприклад, гормони та їх зв'язувальні білки, і стероїди та їх зв'язувальні білки, такі як тестостерон і глобулін для зв'язування полового гормону (SHBG). Наступні описи основаного на поверхні способу для визначення груп, які можуть покращувати розчинність невеликих молекул. Моношар молекул тіолу, що самоорганізується, обмежений малеамідними групами, формує золоту поверхню. Набір невеликих молекул з тіольними групами на одному кінці, і групи, що є гідрофільними на другому кінці потім прикріплюються до поверхні шляхом реакції між тіолом і малеімідом. Набір молекул нерівномірно розподіляється в просторово відмінних ділянках на золотій поверхні для утворення матриці молекул, що може збільшувати розчинність невеликої молекули. Потім в кожний елемент матриці роблять вкраплення як полярних (наприклад, води), так і гідрофобних (наприклад, октанолу) рідин. Кути змочування двох рідин на кожному елементі потім вимірюють на кожному елементі матриці, використовуючи гоніометр. Альтернативно, здатність до змочування окремою рідини на поверхні, що представляє хімічну групу, можна визначити шляхом вимірювання площі поверхні, вкритої вкропленням, якщо дивитися зверху (високий кут змочування буде давати вкраплення невеликої площі; низькі кути змочування покривають більші площі). Кут змочування рідини на поверхні, що представляє хімічну групу, є зворотно пропорційним до взаєморозчинності цієї хімічної групи з цією рідиною (розчинником). Наприклад, хімічна група, 35 для якої вода має високий кут змочування, якщо вона присутня на поверхні, така як метил (СН3), має низьку взаєморозчинність з водою, а саме, вона буде мати тенденцію до зменшення розчинності невеликої молекули. Навпаки, хімічна група, для якої вода має низький кут змочування, якщо вона присутня на поверхні, така як карбоксил (СООН), має високу взаєморозчинність з водою, а саме, вона буде мати тенденцію до збільшення розчинності невеликої молекули. Набори хімічних груп можуть, таким чином, бути швидко скринінговані, використовуючи кути змочування на поверхнях для визначення груп, що покращують розчинність або зменшують гідрофільність. Цей підхід можна використовувати для дослідження ефекту, що спричиняють хімічні групи, використовувані за даним винаходом, на розчинність. Стандартним параметром для здатності невеликої молекули перетинати ліпідну мембрану клітини є logP, де Р являє собою коефіцієнт розділення сполуки між октанолом і водою. Відносний кут змочування поверхні, що представляє хімічні групи, для октанолу і води, таким чином, пропонує швидкий, емпіричний спосіб для ранжирування великих наборів хімічних груп за їх потенційним ефектом на logP сполуки. Залежність рН від розчинності невеликих молекул може співвідноситись з цим способом шляхом вимірювання кутів змочування розчинів при різних значеннях рН. Параметром, еквівалентним до logP в цьому випадку є logD, де D являє собою коефіцієнт розподілу, визначений як рівновага суми концентрацій всіх видів сполуки в октанолі до суми концентрацій всіх видів сполуки в воді при різних значеннях рН. Кути змочування, виміряні при різних значеннях рН, таким чином, пропонує можливість еквівалентного вимірювання logD. Також буде корисним для скринінгу кандидатних сполук за їх здатністю активно транспортуватися крізь клітинні мембрани і клітини, або за їх стійкістю до такого транспорту. Наприклад, добре відомо, що фармацевтично корисні протиракові молекули можуть бути обмежені в своїй ефективності через активний транспорт з ракових клітинмішеней. Схоже до цього, моношари ендотеліальних клітин капілярів мозку досліджували на односпрямований транспорт вінкристину з базальної частини до апікальної частини, що ефективно запобігає проникненню протиракового агенту в центральну нервову систему. В деяких прикладах, хімічні групи, що мають значення, будуть, на додаток до зменшення неспецифічного білкового зв'язування, покращувати фармакокінетиичні властивості шляхом збільшення пасивного або активного транспорту по напрямку сайту їх дії, та/або інгібування транспорту з сайту їх дії. Мозок являє собою одну із тканин, які є найбільш складними для проникнення невеликих молекул. Нейросудинні контакти є дуже міцними і містять велику кількість активних транспортерів, що є найбільш відповідальними за очищення мозку від невеликих молекул. Параклітинний шлях (між клітинними контактами) не є придатним для невеликих молекул, і тільки трансклітинний шлях є придатним (крізь клітинні мембрани). Класично, 90502 36 молекули, мішенню яких є мозок, такі як бензодіазепіни, є гідрофобними, що дозволяє їм проходити крізь клітинні мембрани. Даний винахід є сумісним з дослідженням хімічних груп, що надають білкову резистентність і полегшують існуючу проблему надмірного білкового зв'язування, що пов'язане з такими молекулами, як бензодіазепіни; це потребує високого дозування для розрахунку високого відсотку зв'язування з білками сироватки. Підхід, описаний раніше для визначення зв'язувальних агентів PGP, зможе допомогти оптимізувати молекули для покращення часу присутності в мозку. В наявності є деякі модельні системи, що використовують моношари різних клітинних типів, для підвищення активного транспорту фармацевтично активних речовин. Наприклад, моношари Сасо-2 інтестинальних епітеліальних клітин можуть бути використані для підвищення активного транспорту речовин між кишечником і кровотоком. Коли поміщають на поверхню, що дозволяє потік марілу з апікального до базолатерального напрямку і зворотно, таки клітини формують біологічні мембрани, які можна використовувати для стимуляції фізіологічної абсорбції і біодоступності. В іншому прикладі, доведено, що лінії ендотеліальних клітин мозку миші (МВЕС) збільшують активний транспорт в і з центральної нервової системи. Іншим прикладом таких клітин є НТ29 клітини карциноми товстої кишки людини. Крім того, моношари, що експресують окремі транспортні білки, можуть бути визначені, використовуючи трансфектовані клітини. Наприклад, Sasaki et al (2002) J. Biol. Chem. 8:6497 використовували подвійно-трансфектований Madin-Darby моношар клітини нирки собаки для вивчення транспорту органічних аніонів. Альтернативи клітинних моношарів можуть, звичайно, бути використані для визначення проникності. Альтернативи звичайно містять біологічну структуру, здатну до активного транспорту і включають органи травного тракту, отримані з лабораторних тварин і відтворені органи або мембрани, створені in vitro з клітин, посіяних в штучній матриці, але не обмежуються ними. В іншому аспекті даний винахід забезпечує фармацевтично прийнятні композиції, що містять терапевтично ефективну кількість однієї або декількох сполук за даним винаходом, включаючи сполуки, описані вище і ті, що показані на Фігурах, але не обмежуючись ними, сформульовані разом з одним або декількома фармацевтично прийнятними носіями (додатковими речовинами) та/або розчинниками. Як описано в деталях нижче, фармацевтичні композиції за даним винаходом можуть бути специфічно сформульованими для введення в твердій або рідкій формі, включаючи ті, що пристосовані для наступного: (1) пероральне введення, наприклад, великі дози (водні або неводні розчини або суспензії), таблетки, наприклад, такі, що спрямовані для букального, сублінгвального введення, і системної адсорбції, болюсів, порошків, гранул, паст для нанесення на язик; (2) парентеральне введення, наприклад, шляхом підшкірної, внутрішньом'язової, внутрішньовенної або епідуральної ін'єкції як, наприклад, стерильний розчин або су 37 спензія, або формуляція уповільненого вивільнення; (3) місцевого нанесення, наприклад, як крем, мазь або пластир контрольованого вивільнення або спрей для нанесення на шкіру; (4) внутрішньовагінально або внутрішньоректально, наприклад, як вагинальний супозиторій, крем або мило; (5) сублінгвально; (6) внутрішньоочно; (7) трансдермально; або (8) назально. Вираз "терапевтично ефективна кількість", як використовується в |даному описі, означає, що кількість сполуки, матеріалу або композиції, що містить сполуку за даним винаходом, що є ефективним для утворення деякого бажаного терапевтичного ефекту в, щонайменше, субпопуляції клітин в тварині при прийнятному співвідношенні перевага/ризик, придатному для будь-якого медичного лікування, наприклад, прийнятних побічних ефектах, придатних для будь-якого медичного лікування. Вираз "фармацевтично прийнятний" використовується в даному описі для визначення тих сполук, матеріалів, композицій та/або дозованих форм, що є, в об'ємі точного медичного призначення, придатними для використання в контакті з тканинами людей і тварин з токсичністю, запаленням, алергічною відповіддю або іншими проблемами або ускладненнями, порівняними з прийнятним співвідношенням перевага/ризик. Вираз "фармацевтично-прийнятний носій", як використовується в даному описі, означає фармацевтично-прийнятний матеріал, композицію або наповнювач, наприклад рідкий або твердий наповнювач, розріджувач, носій, виготовлений допоміжний засіб (наприклад, зволожувач, тальк магнію, кальцію і або цинку стеарат або стеаринова кислота), або розчинний інкапсулюючий матеріал, залучений в перенесенні або транспортуванні досліджуваної сполуки з одного органу або частини тіла до іншого органу або частини тіла. Кожний носій повинен бути "прийнятним" в тому сенсі, що він повинен бути сумісним з іншими інгредієнтами формуляції і не бути шкідливим для пацієнту. Деякі приклади матеріалів, які можуть слугувати в якості фармацевтично-прийнятних носіїв, включають: (1) цукри, такі як лактоза, глюкоза і сахароза; (2) крохмалі, такі як кукурудзяний крохмаль і картопляний крохмаль; (3) целюлоза та її і похідні, такі як натрій карбоксиметил целюлоза, етил целюлоза і целюлози ацетат; (4) порошковий трагакант; (5) солод; (6) желатин; (7) тальк; (8) носії, такі як олія кокао і воски для супозиторіїв; (9) олії, такі як арахісова олія, бавовняна олія, соняшникова олія, сезамова олія, оливкова олія, кукурудзяна олія і соєва олія; (10) гліколі, такі як пропіленгліколь; (11) поліоли, такі як гліцерин, сорбітол, манітол і поліетиленгліколь; (12) складні ефіри, такі як етил олеат і етил лаурат; (13) агар; (14) буферуючі агенти, такі як магнію гідроксид і алюмінію гідроксид; (15) альгінова кислота; (16) апірогенна вода; (17) ізотонічний сольовий розчин; (18) розчин Рингеру; (19) етиловий спирт; (20) рН забуферені розчини; (21) поліефіри, полікарбонати та/або поліангідриди; і (22) інші нетоксичні придатні речовини, що використовуються в фармацевтичних формуляціях. 90502 38 Як зазначено вище, окремі варіанти здійснення даних сполук можуть містити основну функціональну групу, такі як аміно або алкіламіно, і, таким чином, здатні утворювати фармацевтичноприйнятні солі з фармацевтично-прийнятними кислотами. Термін "фармацевтично-прийнятні солі" в цьому випадку, стосується до відносно нетоксичних, неорганічних і органічних кислотноадитивних солей сполук за даним винаходом. Ці солі можуть бути утворені in situ в процесі виготовлення середовища для введення або дозованої форми, або шляхом окремого реагування очищеної сполуки за винаходом в її формі вільної основи з відповідною органічною або неорганічною кислотою кислота, і виділенням солі, що таким чином утворюється протягом відповідного очищення. Типові солі включають солі: гідробромід, гідрохлорид, сульфат, бісульфат, фосфат, нітрат, ацетат, валерат, олеат, палмітат, стеарат, лаурат, і бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептонат,лактобіонат і лаурилсульфонат і подібні. (See, наприклад, Berge et al. (1977) "Pharmaceutical Salts", J Pharm. ScL 66:1-19). Фармацевтично прийнятні солі досліджуваних сполук включають загальноприйняті нетоксичні солі або четвертинні амонієві солі сполук, наприклад, нетоксичних органічних або неорганічних кислот. Наприклад, такі загальноприйняті нетоксичні солі включають ті, що походять з неорганічних кислот, таких як хлористо-воднева, бромистоводнева, сірчана, сульфамінова, фосфорна, азотна і подібне; і солі, отримані з органічних кислот, таких як оцтова, пропіонова, бурштинова, гліколева, стеаринова, молочна, яблучна, винна, лимонна, аскорбінова, пальмітинова, малеїнова, гідроксималеїнова, фенілоцтова, глютамінова, бензойна, саліцилова, сульфанілова, 2ацетоксибензойна, фумарова, толуолсульфонова, метансульфонова, етандисульфонова, щавлева, ізотіонова і подібне. В інших випадках сполуки за даним винаходом можуть містити одну або декілька кислотних функціональних груп і, таким чином, мають здатність до формування фармацевтично-прийнятних солей з фармацевтично-прийнятними основами. Термін "фармацевтично-прийнятні солі" в даних прикладах стосується відносно нетоксичних, неорганічних і органічних основно-адитивних солей сполук за даним винаходом. Ці солі можуть бути аналогічно отриманими in situ в процесі виготовлення середовища для введення або дозованої форми, або шляхом окремого реагування очищеної сполуки в її формі вільної кислоти із відповідною основою, такою як гідроксид, карбонат або бікарбонат фармацевтично-прийнятного катіону металу, з аміаком, або з фармацевтично-прийнятним органічним первинним, вторинним або третинним аміном. Типові лужні або лужно-земельні солі включають солі літію, натрію, каляю, кальцію, магнію і алюмінію і подібне. Типові органічні амімни, корисні для формування основно-адитивні солі включають етиламін, діетиламін, етилендіамін, етаноламін, діетаноламін, піперазин і подібне. (Див., наприклад, Berge et al., вище). 39 Зволожуючі агенти, емульсифікатори і мастильні засоби, такі як натрію лаурил сульфат і магнію стеарат, а також фарбуючі агенти, агенти вивільнення, покривні агенти, підсолоджувачі, агенти, що корегують смак та запах лікарського засобу, консерванти і антиоксиданти можуть також бути присутніми в композиціях. Приклади фармацевтично-прийнятних антиоксидантів включають: (1) водорозчинні антиоксиданти, такі як аскорбінова кислота, цистеїну гідрохлорид, натрію бісульфат, натрію метабісульфат, натрію сульфіт і подібне; (2) жиророзчинні антиоксиданти, такі як аскорбіл пальмітат, бутильований гідроксианізол (ВНА), бутильований гідрокситолуол (ВНТ), лецитин, пропіл галат, альфа-токоферол і подібне; і (3) метал - хелатуючі агенти, такі як лимонна кислота, етиленедіамін тетраоцтова кислота (EDTA), сорбітол, винна кислота, фосфорна кислота і подібне. Формуляції за даним винаходом включають ті, що прийнятні для перорального, назального, місцевого (включаючи трансбукальне і сублінгвальне), ректальне, вагінальне та/або парентеральне введення. Формуляції можуть типово бути присутніми в разовій дозованій формі і можуть бути приготовані будь-якими способами, добре відомими в галузі фармації. Кількість активного інгредієнту, який може бути комбінованим з матеріалом-носієм для отримання одноразової дозованої форми, буде варіювати в залежності від хазяїна, якого необхідно лікувати, окремого шляху введення. Кількість активного інгредієнту, який може бути комбінованим з матеріалом-носієм для отримання одноразової дозованої форми, буде взагалі такою, як кількість сполуки, яка продукує терапевтичний ефект. Взагалі, виходячі зі ста відсотків, ця кількість буде в діапазоні від близько 0,1 відсотку до близько дев'яноста дев'яти відсотків активного інгредієнту, переважно від близько 5 відсотків до близько 70 відсотків, найбільш переважно від близько 10 відсотків до близько 30 відсотків. В окремих варіантах здійснення формуляція за даним винаходом містить носій, вибраний з груп, що включає циклодекстрини, целюлози, ліпосоми, агенти, формуючі міцели, наприклад, жовчні кислоти, і полімерні носії, наприклад, поліефіри і поліангідриди; і сполуку за даним винаходом. В окремих варіантах здійснення вищезгадана формуляція представляє переоральну біодоступну сполуку за даним винаходом. Способи приготування цих формуляцій або композицій включають етапи, на яких приводять до об'єднання сполуки за даним винаходом з носієм і, необов'язково, одним або декількома допоміжними інгредієнтами. Взагалі, формуляції готують шляхом рівномірно і тісно об'єднують сполуку за даним винаходом з рідкими носіями, або кінцево розділеними твердими носіями, або з обома, і потім, якщо необхідно, продуктом, що надає форму. Формуляції за винаходом прийнятні для перорального введення можуть бути в формі капсул, крохмальних капсул, пігулок, таблеток, пастилок (використовуючи ароматизуючу основу, звичайно сахарозу і камедь або трагакант), порошки, гранули, або у вигляді розчину або суспензії у водній 90502 40 або неводній рідині, або у вигляді рідкої емульсії олія-в-воді або вода-в-олії, або у вигляді еліксиру або сиропу, або у коржиків (використовуючи інертну основу, таку як желатин і гліцерин, або сахароза і камедь) та/або у вигляді рідин для полоскання рота і подібне, кожний містить попередньо визначену кількість сполуки за даним винаходом в якості активного інгредієнту. Сполука за даним винаходом може також вводитись у вигляді болюсу, електуарію або мазі. В твердих дозованих формах за винаходом для перорального введення (капсули, таблетки, пігулки, драже, порошки, гранули, пастилки і подібне), активний інгредієнт змішують з одним або декількома фармацевтично-прийнятними носіями, такими як натрію цитрат або дикальцію фосфат, та/або будь-яким з наступного: (1) наповнювачі або добавки, такі як крохмалі, лактоза, сахароза, глюкоза, манітол та/або силіцилова кислота; (2) зв'язувальні засоби, такі як, наприклад, карбоксиметилцелюлоза, альгінати, желатин, полівінілпіролідон, сахароза та/або камедь; (3) зволожувачі, такі як гліцерол; (4) дезінтегруючі агенти, такі як агар-агар, кальцію карбонат, картопляний крохмаль або крохмаль тапіоки, альгінова кислота, окремі силікати і натрію карбонат; (5) агенти, затримуючі розчинення, такі як парафін; (6) підсилювачі абсорбції, такі як четвертинні амонієві сполуки і сурфактанти, такі як полоксамер і натрію лаурил сульфат; (7) зволожуючі агенти, такі як, наприклад, цетиловий спирт, гліцерол момностерарат і неіонні сурфактанти; (8) абсорбенти, такі як каолін і бентонитова глина; (9) мастильні засоби, такі як тальк, кальцію стеарат, магнію стеарат, тверді поліетиленгліколі, натрію лаурил сульфат, цинку стеарат, натрію стеарат, стеаринова кислота та їх суміші; (10) фарбуючі агенти; і (11) агенти контрольованого вивільнення, такі як корсповідон або етилцелюлоза. У випадку капсул, таблеток і пігулок фармацевтичні композиції можуть також містити буферучі агенти. Тверді композиції схожого типу також можуть бути використані в якості наповнювачів в м'яких і тих, що мають тверду оболонку желатинових капсулах, використовуючи такі носії, як лактоза або молочні цукри, а також викокомолекулярні поліетиленгліколі і подібне. Таблетка може бути виконана шляхом стиснення або формування, необов'язково з одним або декількома додатковими інгредієнтами. Таблетки, отримані стисненням можуть бути отримані, використовуючи зв'язувальний засіб (наприклад, желатин або гідроксипропілметилцелюлозу), мастильний засіб, інертний розріджувач, консервант, дезінтегрант (наприклад, натрію крохмаль гліколат або поперечно-зшиту натрій карбоксиметилцелюлозу), поверхнево-активний або диспергуючий агент. Таблетки, отримані формуванням можуть бути утворені шляхом molding у відповідному пристрої суміші порошкової сполуки, зволоженої інертним різким розріджувачем. Таблетки та інші тверді дозовані форми фармацевтичних композицій за даним винаходом, такі як драже, капсули, пілюлі і гранули, можуть необов'язково бути з шорсткою поверхнею або отриманими з покриттями і оболонками, такими як енте 41 ральні покриття та інші покриття, добре відомі у фармацевтичній галузі. Вони також можуть бути сформульовані так, щоб забезпечувати повільне або контрольоване вивільнення з них активного інгредієнту, використовуючи, наприклад, гідроксипропілметил целюлозу в різних пропорціях для забезпечення бажаного профілю вивільнення, інші полімерні матриці, ліпосоми та/або мікросфери. Вони можуть бути сформульовані для швидкого вивільнення, наприклад, ліофілізовані. Вони можуть бути стерилізовані шляхом, наприклад, фільтрації крізь фільтр, що затримує бактерії, або шляхом включення стерилізуючі агенти у формі стерильних твердих композицій, які можуть бути розчинені в стерильній воді, або деякого іншого стерильного середовища для ін'єкції безпосередньо до використання. Ці композиції можуть також необов'язково містити рентгеноконтрасні агенти і можуть належати до композиції так, що вони вивільняють тільки активний інгредієнт(и), або переважно, в окремій ділянці шлунково-кишковоготракту, необов'язково, шляхом затримування. Приклади заливальних композицій, які можуть бути використані, включають полімерні речовини і воски. Активний інгредієнт може також бути у мікро-інкапсульованій формі, якщо доцільно, з одним або декількома вищеописаними носіями. Рідкі дозовані форми для перорального введення сполук за винаходом включають фармацевтично прийнятні емульсії, мікроемульсії, розчини, суспензії, сиропи і еліксири. Крім активного інгредієнту, рідкі дозовані форми можуть містити інертні розчинники, що звичайно використовуються в даній галузі техніки, такі як, наприклад, вода або інші розчинники, солюбілізуючі агенти і емульсифікатори, такі як етиловий спирт, ізопропіловий спирт, етил карбонат, етил ацетат, бензиловий спирт, бензил бензоат, пропіленгліколь, 1,3бутилен гліколь, олії (зокрема, бавовняна, олія земляного горіху, кукурудзяна, олія зародків, оливкова, касторова і сезамова олії), гліцерол, тетрагідрофуриловий спирт, поліетиленгліколі і жирнокислотні ефіри сорбітану та їх суміші. Крім інертних розчинників, пероральні композиції можуть також включають допоміжні речовини, такі як зволожуючі агенти, агенти, що емульсифікують і суспендують, агенти, що підсолоджують, змінюють смак лікарського засобу, офарблюють, ароматизують і консервують. Суспензії, крім активних сполук, можуть містити суспендуючі агенти як, наприклад, етоксильовані ізостеарилові спирти, поліоксіетилен сорбітол і ефіри сорбітану, мікрокристалічну целюлозу, алюмінію метагідроксид, бентолніт, агар-агар і трагакант та їх суміші. Формуляції фармацевтичних композицій за винаходом для ректального або вагінального введення можуть бути представлені в якості супозиторію, що може бути отриманий шляхом змішування однієї або декількох сполук за винаходом з одним або декількома відповідними не подразнюючими наповнювачами або носіями, що містять, наприклад, олію кокао, поліетиленгліколь, воск для супозиторіїв або саліцилат, і що є твердим при кімнатній температурі, але рідким при температурі 90502 42 тіла і, таким чином, буде танути в ректальній або вагінальній порожнині і вивільняти активну сполуку. Формуляції за даним винаходом, які є прийнятними для вагінального введення також включають формуляції: песарії, тампони, креми, гелі, пасти, мила або спреї, що містять такі носії, які є прийнятними, що відомо в галузі техніки. Дозовані форми для місцевого або трансдермального введення сполук за цим винаходом включають порошки, спреї, мазі, пасти, креми, лосьйони, гелі, розчини, пластирі і інгалятори. Активна сполука може бути змішана в стерильних умовах з фармацевтично-прийнятним носієм, і з будь-якими консервантами, буферами або пропелентами, які можуть бути необхідними. Мазі, пасти, креми і гелі можуть містити, крім активної сполуки за цим винаходом, носії, такі як тваринні і рослинні жири, олії, воски, парафіни, крохмаль, трагакант, похідні целюлози, поліетиленгліколі, силікони, бентоніти, кремнієва кислота, тальк і цинку оксид або їх суміші. Порошки і спреї можуть містити, крім сполуки за цим винаходом, носії, такі як лактоза, тальк, кремнієва кислота, алюмінію гідроксид, кальцію силікати і поліамідний порошок або суміші цих речовин. Спреї можуть додатково містити традиційні пропеленти, такі як хлорфтор вуглеводні і летючі незаміщені вуглеводні, такі як бутан і пропан. Трансдермальні пластири мають додаткову перевагу в забезпеченні контрольовану доставку сполуки за даним винаходом в організм. Такі дозовані форми можуть бути утворені шляхом розчинення або диспергування сполуки у відповідному середовищі. Підсилювачі абсорбції можуть також бути використаними для збільшення потоку сполуки крізь шкіру. Швидкість такого потоку можуть контролюватися або шляхом забезпечення мембрани, що контролює швидкість, або диспергуванням сполуки в полімерній матриці або гелі. Також передбачено, що офтальмологічні формуляції, очні мазі, порошки, розчини і подібне знаходяться в межах цього винаходу. Фармацевтичні композиції за цим винаходом, прийнятні для парентерального введення, включають одну або декілька сполук за винаходом в комбінації з одним або декількома фармацевтично-прийнятними стерильними ізотонічними водними або неводними розчинами, дисперсіями, суспензіями або емульсіями, або стерильними порошками, які можуть бути відновлені в стерильні розчини для ін'єкції або дисперсії безпосередньо перед використанням, які можуть включати цукри, спирти, антиоксиданти, буфери, антимікробні добавки, розчини, які роблять формуляцію ізотонічною до крові відповідного реципієнта, або агенти, що суспендують або загущують. Приклади відповідних водних і неводних носіїв, які можуть застосовуватися у фармацевтичних композиціях за винаходом включають воду, етанол, поліоли (такі як гліцерол, пропіленгліколь, поліетиленгліколь і подібне), та їх відповідній суміші, рослинні олії, такі як оливкова олія, і органічні ефіри для ін'єкції, такі як етил олеат. Необхідна плинність може підтримуватися, наприклад, шля 43 хом використання покривних матеріалів, такі як лецетин, шляхом підтримування необхідного розміру часток у випадку дисперсії, і шляхом використання поверхнево-активних речовин. Ці композиції можуть також містити допоміжні речовини, такі як консерванти, зволожуючі агенти, емульсифікуючі агенти і диспергуючі агенти. Запобігання дії мікроорганізмів на досліджувальні сполуки може бути досягнуто включенням різних антибактеріальних і протигрибкових агентів, наприклад, парабену, хлорбутанолу, фенолу сорьинової кислоти і подібне. Також може бути бажаним включити ізотонічні агенти, такі як цукри, натрію хлорид і подібне в композиції. Крім того, пролонговану абсорбцію фармацевтичної форми для ін'єкції може бути досягнуто включенням агентів, які затримують абсорбцію, такі як алюмінію моностеарат і желатин. В деяких випадках, для подовження ефекту лікарського засобу, бажано уповільнити абсорбцію лікарського засобу з підкожної або внутрішньом'язової ін'єкції. Це можна досягти шляхом використання рідкої суспензії кристалічного або аморфного матеріалу, що має низьку розчинність у воді. Швидкість абсорбції лікарського засобу потім залежить від його швидкості розчинення, яка, навпаки, може залежати від розміру кристалу і кристалічної форми. Альтернативно, затримана абсорбція форми лікарського засобу, що вводиться парентерально, досягається шляхом розчинення або суспендування лікарського засобу в олійному носії. Депоновані форми для ін'єкції утворюють шляхом формування мікроінкапсульованих матриць досліджуваних сполук в полімерах, що біологічно розпадаються, такі як полілактидполігліколід. Швидкість вивільнення лікарського засобу може контролюватися в залежності від співвідношення лікарського засобу до полімеру, і природи окремого використовуваного полімеру. Приклади інших полімерів, що біологічно розпадаються, включають полі(ортоефіри) і полі(ангідриди). Депоновані формуляції для ін'єкції також отримують шляхом включення лікарського засобу в ліпосоми або мікроемульсії, що є сумісними з тканинами організму. Якщо сполуки за даним винаходом вводять як фармацевтичні засоби людям і тваринам, то вони можуть бути введені окремо або як фармацевтична композиція, що містить, наприклад, 0,1-99% (більш переважно, 10-30%) активного інгредієнту в комбінації з фармацевтично прийнятним носієм. Препарати за даним винаходом можуть бути введені перорально, парентерально, місцево або ректально. Вони, звичайно, вводять в формах, відповідних для кожного шляху введення. Наприклад, вони вводяться в таблетках або формі капсули, ін'єкцією, інгаляцією, очним лосьйоном, маззю, супозиторієм і т.п. введенням ін'єкцією, інфунзією або інгаляцією; місцевим лосьйоном або маззю; і ректальним супозиторіями. Пероральні введення є переважними. Вираз "парентеральне введення" і "введений парентерально", як використовується в даному описі, означає спосіб введення, що відрізняється від ентерального і місцевого введення, звичайно 90502 44 шляхом ін'єкції, і включає, без обмежень, внутрішньовенну, внутрішньом'язову, внутрішньоаретріальну, і інтратекальну, інтракапсулярну, інтраорбітальну, інтракардіальну, інтрадермальну, інтраперитоніальну, транстрахеальну, підшкірну, внутрішньошкірну, внутрішньосуглобну, підкапсулярну, субарахноїдальну, інтраспінальну і надчеревну ін'єкцію і інфузію. Вираз "системне введення", "введений системно", "периферичне введення" і "введений периферично", як використовується в даному описі, означає введення сполуки, лікарського засобу або іншого матеріалу іншим способом, ніж безпосередньо в центральну нервову систему, таким, що дані засоби входять до системи пацієнту і, таким чином, є предметом метаболізму і інших подібних процесів, наприклад, підкожного введення. Ці сполуки можуть бути введені людям і іншим тваринам для терапії будь-яким відповідним шляхом введення, включаючи перорально, назально, як, наприклад, спреєм, ректально, інтравагінально, парентерально, інтрацистернально і місцево, як порошками, мазями або краплями, включаючи букально і сублінгвально. Незважаючи на вибраний шлях введення, сполуки за даним винаходом, які можуть бути використані у відповідній гідратованій формі та/або фармацевтичні композиції за даним винаходом, сформульовані у фармацевтично-прийнятні дозовані форми загальноприйнятими способами, відомими для фахівців в даній галузі. Дійсні рівні дозування активних інгредієнтів у фармацевтичних композиціях за цим винаходом можуть змінюватися так, щоб отримати кількість активного інгредієнту, що є ефективною для досягнення бажаної терапевтичної відповіді для окремого пацієнта, композиції і способу введення, без проявлення токсичності для пацієнту. Вибраний рівень дозування буде залежати від великої кількості факторів, включаючи активність окремої сполуки використаної за даним винаходом, або її ефіру, солі або аміду, шляху введення, часу введення, швидкості виведення або метаболізму окремої використаної сполуки, швидкості і ступеню абсорбції, тривалості лікування, інших лікарських засобів, сполук та/або матеріалів, використаних в комбінації з окремою використаною сполукою, віку, полу, ваги, стану, загального стану здоров'я i попередньої медичної історії пацієнта, якого лікують, і подібних факторів, добревідомих в медичних галузях. Лікар або ветеринар, який є фахівцем в даній галузі може швидко визначити і призначити ефективну кількість необхідної фармацевтичної композиції. Наприклад, лікар або ветеринар може почати з доз використаних сполук за винаходом у фармацевтичній композиції на рівнях менших, ніж необхідно для того, щоб досягти бажаного терапевтичного ефекту і поступово збільшувати дозування, доки не буде досягнутий бажаний ефект. Взагалі, відповідною щоденною дозою сполуки за винаходом буде така кількість сполуки, яка є найменшою дозою, ефективною у викликанні терапевтичного ефекту. Така ефективна доза буде взагалі залежати від факторів, описаних вище. 45 Взагалі, пероральна, внутрішньовенна, інтрацеребровентрикулярна і підшкірна дози сполук за цим винаходом для пацієнту, при використанні для визначення знеболювальних ефектів, буде знаходитися в діапазоні від близько 0,0001 до близько 100мг на кілограм ваги тіла на день. Якщо бажано, ефективна щоденна доза активної сполуки може бути введена як дві, три, чотири, п'ять, шість або більше суб-доз, що вводять окремо з відповідними інтервалами протягом дня, необов'язково, в одноразових дозованих формах. Переважним дозуванням є одне введення на день. Тоді як можливим для сполуки за даним винаходом бути введеною окремо, переважним є введення сполуки як фармацевтичної формуляції (композиції). Сполуки відповідно винаходу можуть бути сформульовані для введення будь-яким традиційним шляхом для використання в медицині або ветеринарії, по аналогії з іншими фармацевтичними засобами. В іншому аспекті даний винахід забезпечує фармацевтично прийнятні і композиції, які містять терапевтично-ефективну кількість однієї або декількох досліджуваних сполук, як описано вище, сформульованих разом з одним або декількома фармацевтично прийнятними носіями (додатковими речовинами) та/або розчинниками. Як описано в деталях нижче, фармацевтичні композиції за даним винаходом можуть бути спеціально сформульовані для введення в твердій або рідкій формі, включаючи такі, що адаптовані для наступного: (1) перорального введення, наприклад, великі дози (водні або неводні розчини або суспензії), таблетки, болюси, порошки, гранули, пасти для нанесення на язик; (2) парентерального введення, наприклад, шляхом підшкірної, внутрішньом'язової або внутрішньовенної ін'єкції як, наприклад, стерильний розчин або суспензія; (3) місцевого нанесення, наприклад, я крем, мазь або спрей, нанесений на шкіру, легені або слизові оболонки; або (4) інтравагінально або інтраректально, наприклад, як песарій, крем або мило; (5) сублінгвально або букально; (6) очно; (7) трансдермально; або (8) назально. Передбачається, що термін "лікування" включає також профілактику, терапію і курс лікування. Пацієнт, що отримує це лікування, являє собою будь-яку тварину, що потребує такого лікування, включаючи приматів, зокрема, людей, і інших ссавців, таких як коні, велика рогата худоба, свині і вівці; і свійска птиця і домашні тварини взагалі. Сполука за винаходом може бути введена сама по собі або у домішку з фармацевтично прийнятними носіями і може також бути введеною у поєднанні з протимікробними агентами, такими як пеніциліни, цефалоспорини, аміноглікозиди і глікопептиди. Об'єднана терапія, таким чином, включає послідовне, одночасне і окреме введення активної сполуки таким чином, що терапевтичні ефекти першого введення не повністю зникають наступного введення. Додавання активної сполуки за винаходом до їжі тварини переважно виконують шляхом приго 90502 46 тування відповідної преміксу, що містить активну сполуку в ефективній кількості, і включення цієї добавки в повний раціон. Альтернативно, проміжний корм або харчова добавка, що містить активний інгредієнт можуть бути змішані з їжею. Шлях, яким такі премікси і повні раціони можуть бути отримані і введені, описані в книгах, на які посилаються (такі як "Applied Animal Nutrition", W.H. Freedman і CO., San Francisco, U.S.A., 1969 або "Livestock Feeds and Feeding" О and В books, Corvallis, Оre., U.S.A., 1977). Нещодавно фармацевтична промисловість розробила технологію мікроемульсифікації для покращення біодоступності деяких ліпофільних (нерозчинних у воді) фармацевтичних агентів. Приклади включають Триметрин (Dordunoo, S. K., et al., Drug Development and Industrial Pharmacy, 17(12), 1685-1713, 1991 і REV 5901 (Sheen, P. C, et al., J Pharm Sci 80(7), 712-714, 1991). Серед іншого, мікроемульсифікація забезпечує підсилену біодоступність шляхом переважно спрямованої абсорбції до лімфатичної системи замість циркуляторної системи, яка таким чином обходить печінку, і попереджає розпад сполук в гепатобіліарній циркуляції. В одному аспекті винаходу, формуляції містять міцели, утворені із сполуки за даним винаходом і, щонайменше, одним амфіфільним носієм, в якому міцели мають середній діаметр менше ніж близько 100нм. Більш переважні варіанти здійснення забезпечують міцели, що мають середній діаметр менше ніж близько 50нм, і навіть більш переважні варіанти здійснення забезпечують міцели, що мають середній діаметр менше ніж близько 30нм, або навіть менше ніж близько 20нм. Тоді як передбаченими є всі відповідні амфіфільні носії, на теперішній час переважними носіями взагалі є ті, що мають Взагалі-Розпізнані-ЯкБезпечні (Generally-Recognized-as-Safe) (GRAS) статус, і що можуть як розчиняти сполуку за даним винаходом і мікроемульсифікувати її на пізнішій стадії, коли розчин контактує з комплексною водною фазою (така як виявлена в гастроінтестинальному тракті людини). Звичайно, амфіфільні інгредієнти, що задовольняють цим вимогам мають значення ГЛБ (гідрофільно-ліпофільний баланс) (HLB) 2-20, та їх структури містять аліфатичні радикали з нерозгалуженим ланцюгом у діапазоні від С-6 до С-20. Прикладами є поліетиленгліколізовані жирнокислотні гліцериди і поліетиленгліколі. Окремі переважні амфіфільні носії є насиченими і мононенасиченими поліетиленгліколізованими жирнокислотними гліцеридами, такі як ті, що отримують з повністю або частково гідрогенізованих різних рослинних олій. Такі олії можуть переважно містити три-, ди- і моно-жирнокислотні гліцериди і ди- і моно-поліетиленгліколеві ефіри відповідних жирних кислот, з окремою переважною жирнокислотною композицією, включаючи капринову кислоту 4-10, капринову кислоту 3-9, лауринову кислоту 40-50, міристинову кислоту 14-24, пальмітинову кислоту 4-14 і стеаринову кислоту 515%. Інший корисний клас амфіфільних носіїв 47 включає частково етерифікований сорбітан та/або сорбітол, з насиченими або моно-ненасиченими жирними кислотами (SPAN-серії) або відповідними етоксильованими аналогами (TWEEN- серії). Комерційно доступні амфіфільні носії є частково передбаченими, включаюся Гелюцир-серії, Лабрафіл, Лабрасол Лаурогліколь (всі виготовляються і поставляються Gattefosse Corporation, Saint Priest, Франція), ПЕГ-моно-олеат, ПЕГ-диолеат, ПЕГ-моно-лаурат і ди-лаурат, Лецитин, Полісорбат 80 і т.ін. (що виготовляються і поставляються компаніями в США та у світі). Гідрофільні полімери, прийнятні для застосування в даному винаході, є такими, що є водорозчиинними, можуть ковалентно прикріплюватися до ліпіду, що формує везикули, і що є толерантними in vivo без токсичних ефектів (а саме, є біоприйнятними). Прийнятні полімери включають поліетиленгліколь (PEG), полімолочну (також називається полілактид), полігліколеву кислоту (також називається полігліколід), полімолочний-полігліколевий кислий сополімер і полівініловий спирт. Переважними полімерами є ті, що мають молекулярну вагу від близько 100 або 120 дальтон до близько 5000 або 10000 дальтон, і більш переважно від близько 300 дальтон до близько 5000 дальтон. У конкретному переважному варіанті здійснення полімером є поліетиленгліколь, що має молекулярну вагу від близько 100 до близько 5000 дальтон, і більш переважно, що має молекулярну вагу від близько 300 до близько 5000 дальтон. В конкретному переважному варіанті здійснення полімером є поліетиленгліколь 750 дальтон (PEG(750)). Полімери, використовувані в даному винаході, мають значно меншу молекулярну вагу, приблизно 100 дальтон, порівняно з великою МВ 5000 дальтон або більше, ніж ті, що використовуються в стандартних технологіях пегілювання. Полімери можуть бути також визначені числом їх мономерів; в переважному варіанті здійснення за даним винаходом використовувані полімери, щонайменше, близько трьох мономерів, такі як ПЕГ полімери, що включають три мономери (приблизно 150 дальтон). Інші гідрофільні полімери, що можуть бути прийнятні для використання в даному винаході, включають полівінілпіролідон, поліметоксазолін, поліетилоксазолін, полігідроксипропіл метакриламід, поліметакриламід, полідиметилакриламід і дериватизовані целюлози, такі як гідроксиметилцелюлоза або гідроксиетилцелюлоза. В окремих варіантах здійснення формуляція за даним винаходом включає біоприйнятні полімери, вибрані з групи, що містить поліаміди, полікарбонати, поліалкілени, полімери акрилового і метакрилового ефірів, полівнілові полімери, полігліколіди, полісилоксани, поліуретани та їх сополімери, целюлози, поліпропілен, поліетилени, полістирен, полімери молочної кислоти і гліколевої кислоти, поліангідриди, полі(орто)ефіри, полі(масляну кислоту), полі(валеріанову кислоту), полі(лактид-со-капролактон), полісахариди, протеїни, полігіалуронові кислоти, поліціаноакрилати та їх сполучення, суміші або сополімери. Характеристики вивільнення формуляції за даним винаходом залежать від інкапсулуючого 90502 48 матеріалу, концентрації інкапсульованого лікарського засобу і присутності модифікаторів вивільнення. Наприклад, вивільнення може бути керованим так, щоб бути рН-залежним, наприклад, використовуючи рН-чутливе покриття, що вивільнює тільки при низькому рН, як у шлунку, або при вищому рН, як у кишечнику. Внутрішнє покриття може бути використане для попередження вивільнення з оточення тільки після проходження крізь шлунок. Багаторазові покриття або суміші ціанаміду, інкапсульованого в різні матеріали, можуть бути використані для отримання першого вивільнення в шлунку, після якого відбувається пізніше вивільнення в кишечнику. Вивільнення може також бути керованим шляхом включення солей або пороформуючих агентів, які можуть збільшувати входження води або вивільнення лікарського засобу шляхом дифузії з капсули. Носії, що модифікують розчинність лікарського засобу, можуть також бути використані для контролю швидкості вивільнення. Агенти, що збільшують розпад матриці або вивільнення з матриці, можуть також бути включені. Їх можуть додавати до лікарського засобу, який додають в якості відокремленої фази (а саме, як тверді частинки), або може бути сумісно розчиненим в полімерній фазі в залежності від сполуки. В усіх випадках кількість повинна бути між 0,1 і тридцятьма відсотками (вага/вага полімеру). Типи підсилювачів розпаду включають неорганічні солі, такі як амонію сульфат і амонію хлорид, органічні кислоти, такі як лимонна кислота, бензойна кислота і аскорбінова кислота, неорганічні основи, такі як натрію кабонат, калію карбонат, кальцію карбонат, цинку карбонат, і цинку гідроксид, і органічні основи, такі як протамін сульфат, спермін, холін, етаноламін, діетаноламін і триетаноламін і сурфактанти, такі як Tween.RTM. і Pluronic.RTM.. Пороформуючі агенти, які додають мікроструктуру до матриць (а саме, водорозчинні сполуки, такі як неорганічні солі і цукри) додають в якості твердих частинок. Діапазон має бути між одним і тридцятьма відсотками (вага/вага полімеру). Поглинанням можна також керувати шляхом зміни часу утримання частинок у кишечнику. Це може бути досягнуто, наприклад, шляхом покриття частинки або відбору в якості матеріалу для інкапсулювання мукозального адгезивного полімеру. Приклади включають найбільшу кількість полімерів з вільними карбоксильниим групами, такі як хітозан, целюлози і особливо поліакрилати (як використовується в даному описі, поліакрилати стосуються полімерів, включаючи акрилатні групи і модифіковані акрилатні групи, такі як ціаноакрилати і метакрилати). Досліджувальні сполуки можуть бути синтезовані з використанням способів комбінаторного синтезу, описаного в даному розділі. Комбінаторні бібліотеки сполук можуть бути використані для скринінгу фармацевтичної, агрохімічної або іншої біологічної або медично-пов'язаної активності або властивостей, пов'язаних з матеріалом. Комбінаторна бібліотека для цілей даного винаходу являє собою суміш хімічно пов'язаних сполук, які можуть бути скринінговані разом за бажаною властивістю; 49 згаданібібліотеки можуть бути в розчині або ковалентно зв'язані з твердою основою. Отримання багатьох споріднених сполук в окремій реакції набагато зменшує і полегшує кількість процесів скринінгу, які необхідно провести. Скринінг на прийнятну біологічну, фармацевтичну, агрохімічну або фізичну властивість може бути проведена традиційними способами. Різноманітність у бібліотеці може бути утворена на розмаїтті різних рівнів. Наприклад, субстрат арильних груп, використовуваний в комбінаторному підході може бути різними в термінах ядерної арильної частини, наприклад, різноманітність в термінах кільцевої структури, та/або може варіювати в залежності від інших замісників. В даній галузі наявна різноманітність технологій для утворення комбінаторних бібліотек невеликих органічних молекул. Див., наприклад, Blondelle et al. (1995) Trends Anal. Chem. 14:83; Патент США 5,359,115 і 5,362,899 Affymax; Патент США 5,288,514 Ellman;. Публікацію Міжнародної заявки WO 94/08051 Still та ін; Chen et al. (1994) JACS 116:2661; Kerr et al. (1993) JACS 115:252; публікацію Міжнародної заявки WO92/10092, WO93/09668 і WO91/07087; і публікацію Міжнародної заявки WO93/20242 Lerner та ін.). Відповідно, різноманітність бібліотек порядку від близько 16 до 1,000,000 або більше різновидів може бути синтезована і скринінгована щодо часткової активності або властивості. У варіанті здійснення для прикладу бібліотека заміщених різновидів може бути синтезованою з використанням досліджуваної реакцій, адаптованих до технологій, описаних Still та ін. в публікцаії міжнародної заявки WO 94/08051, наприклад, зв'язування з полімерною гранулою групами, що гідролізуються або фосфолізуються, наприклад, розміщених на одному з положень субстрату. Відповідно до технології Still та ін., бібліотеку синтезують на наборі гранул, де кожна гранула включає набір міток, що визначають окремий різновид на цій гранулі. В одному варіанті здійснення, що є частково прийнятним для виявлення ферментативних інгібіторів, гранули можуть бути дисперговані на поверхні проникної мембрани, і різновиди вивільняються з гранул шляхом лізису лінкеру гранули. Різновид з кожної гранули будуть дифундувати крізь мембрану до зони аналізу, де він буде взаємодіяти з ферментативним аналізом. Нижче наведені деталізовані описи кількості комбінаторних методологій. Тенденцією в розвитку галузі комбінаторної хімії є покращення чутливості таких технологій, як мас-спектрометрія (MS), наприклад, яка може бути використана для визначення суб-фемтомолярної кількості сполуки, а також пряме визначення хімічної будови сполуки, вибраної з комбінаторної бібліотеки. Наприклад, там, де забезпечує нерозчинну матрицю-основу, окремі популяції сполук можуть бути першими вивільнені з основи і визначені за допомогою MS. В інших варіантах здійснення, як частина технології приготування MS зразків, такі MS технології, як MALDI, можуть бути використані для вивільнення сполуки з матриці, частково там, де лабільне зв'язування використа 90502 50 не природно для зв'язування сполуки з матрицею. Наприклад, гранула, вибрана з бібліотеки, може бути опромінена на MALDI етапі для того, щоб вивільняти різновид з матриці, та іонізувати різновид для MS аналізу. Бібліотеки досліджуваного способу можуть приймати формат багатошпилькової бібліотеки. Коротко, Geysen і співробітники (Geysen et al. (1984) PNAS 81:3998-4002) розробили спосіб отримання бібліотек сполук шляхом паралельного синтезу на поліакриловій кислоті на поліетиленових шпильках, що розташовані на форматі мікротитрувального планшету. Технологія Geysen може бути використана для синтезу і скринінгу тисяч сполук щотижня, використовуючи багатошпильковий спосіб, і зв'язані сполуки можуть бути багаторазово використовуватись в багатьох аналізах. Частини відповідних лінкерів можуть також додаватися до шпильок так, щоб сполуки могли бути відщеплені від основи після синтезу для оцінювання чистоти і подальшого оцінювання (c.f., Bray et al. (1990) Tetrahedron Lett 31:5811-5814; Valerio et al. (1991) Anal Biochem 197:168-177; Bray et al. (1991) Tetrahedron Lett 32:6163-6166). В іншому варіанті здійснення, неоднорідна бібліотека сполук може забезпечуватися на наборі гранул, використовуючи методику розподілуз'єднання-рекомбінації (див., наприклад, Houghten (1985) PNAS 82:5131-5135; і Патенти США №№ 4,631,211; 5,440,016; 5,480,971). Коротко, як видно з назви, на кожному етапі синтезу, де виродженість вводять в бібліотеку, гранули розділяють на окремі групи, що дорівнюють кількості різних замісників, які додають в окремих положеннях до бібліотеки, різні замісники поєднують в окремих реакціях, і гранули рекомбінують в один пул для наступного циклу. За одним варіантом здійснення принцип розподіл-з'єднання-рекомбінація можна здійснити за допомогою аналогічного підходу так званого способу "чайного пакетику", вперше розробленого Houghten, де синтез сполуки відбувається на смолі, що міститься всередині пористих поліпропіленових пакетів (Houghten et al. (1986) PNAS 82:5131-5135). Замісники приєднуються до смол, що несуть сполуку, при поміщенні пакетиків у відповідні реакційні розчини, тоді як всі традиційні етапи, такі як відмивання смоли і зняття захисних груп, проводять одночасно в реакційному резервуарі. В кінці синтезу кожний пакетик містить окрему сполуку. Схема комбінаторного синтезу, в якому ідентичність сполуки отримують шляхом визначення її місцеположення на субстраті для синтезу, називається просторово-доступний синтез. За одним варіантом здійснення комбінаторний процес проводять шляхом регулювання додавання хімічного реагенту до специфічних місцеположень на твердій основі (Dower et al. С1991) Annu Rep Med Chem 26:271-280; Fodor, S.P.A. (1991) Science 251:767; Pirrung et al. (1992) Патент США №5,143,854; Jacobs et al. (1994) Trends Biotechnol 12:19-26). Просторове розрішення фотолітографії забезпечує мініатюризацію. Ця методика може бути проведена з використанням реакцій захи 51 щення/зняття захисту з фотолабільними захисними групами. Ключові етапи цієї технології проілюстровані у Gallop et al. (1994) J Med Chem 37:1233-1251. Субстрат для синтезу отримують для поєднання через ковалентне прикріплення фотолабільного нітровератрилоксикарбонілу (NVOC), що захищає амінолінкери або інші фотолабільні лінкери. Світло використовують для селективної активації специфічної ділянки основи для синтезу для з'єднання. Видалення фотолабільних захисних груп за допомогою світла (зняття захисних груп) приводить до активації вибраних ділянок. Після активації перший з ряду амінокислотних аналогів, кожний з яких несе фотолабільну захисну групу на амінокінці, наносять на всю поверхню. З'єднання відбувається тільки на ділянках, що доступні для світла в попередньому етапі. Реакцію зупиняють, планшети промивають, а субстрат знову опромінюють світлом крізь другий фотошаблон, активуючи іншу ділянку для реакції з другим захищеним структурним блоком. Патерн фотошаблонів і послідовність реагентів визначає продукти та їх місцеположення. Якщо цей процес використовує технології фотолітографії, кількість сполук, що може бути синтезована, обмежується тільки кількістю сайтів синтезу, які можуть бути визначені з прийнятним розрішенням. Положення кожної сполуки є точно відомим; таким чином, можна безпосередньо визначити її взаємодії з іншими молекулами. В хімічному синтезі, керованому світлом, продукти залежать від патерну опромінення світлом і порядку додавання реагентів. Шляхом варіювання літографічних патернів, багато різних наборів тестованих сполук можуть бути синтезовані одночасно; ця характеристика приводить до утворення багатьох різних методик літографії. За іншим варіантом здійснення досліджуваний спосіб використовує бібліотеку сполук, забезпечену закодованою системою маркування. Останнє удосконалення у визначенні активних сполук з комбінаторних бібліотек використовує системи хімічних індексів, застосовуючи мітки, що унікально кодують етапи реакції, яким підлягає отримана гранула і, як наслідок, структура, що її несе. Суттєво, цей підхід імітує бібліотеки фагових дисплеїв, де активність походить від експресованих пептидів, але структури активних пептидів відтворюють з відповідної геномної послідовності ДНК. При першому кодуванні синтетичних комбінаторних бібліотек застосовували ДНК в якості коду. Опублікована велика кількість інших форм кодування, включаючи кодування з біоолігомерами, для яких можна встановити порядок послідовності (наприклад, олігонуклеотиди і пептиди), і бінарне кодування з додатковими мітками, для яких неможливо встановити порядок послідовності. Принцип використання олігонуклетотидів для кодування комбінаторних синтетичних бібліотек описано в 1992 (Brenner et al. (1992) PNAS 89:5381-5383), і приклад такої бібліотеки з'явився в наступному році (Needles et al. (1993) PNAS 90:10700-10704). Комбінаторна бібліотека номінально 77 (=823543) пептидів, що включала всі ком 90502 52 бінації Arg (аргінін), Gin (глютамін), Phe (фенілаланін), Lys (лізин), Val (валін), D-Val (D-валін) і Thr (треонін) (трибуквений амінокислотний код), кожна з яких кодувалась специфічним динуклеотидом (ТА, ТС, СТ, AT, ТТ, СА і АС, відповідно), була отримана серіями альтернативних циклів пептидного і олігонуклеотидного синтезів на твердій основі. В цій роботі амін, пов'язаний функціонально з гранулою, був специфічно диференційований в напрямку пептидного або олігонуклеотидного синтезу шляхом одночасної преінкубації гранул з реагентами, що утворюють захисні ОН групи для олігонуклеотидного синтезу і захисні NH2 групи для пептидного синтезу (тут, у співвідношенні 1:20). Після завершення мітки, кожна з яких складається з 69-мерів, 14 одиниць яких несуть код. Бібліотеку, зв'язану з гранулою, інкубували з флуоресцентно поміченим антитілом, і гранули, що містять зв'язане антитіло, що має стійку флуоресценцію, були зібрані за допомогою флуоресцентноактивованого клітинного дослідження (FACS). ДНК мітки ампліфікували за допомогою ПЛР (полімеразна ланцюгова реакція), будували послідовності та синтезували передбачені пептиди. Відповідно до таких технологій, бібліотеки сполук можна отримати для використання в дослідному способі, де олігонуклеотидна послідовність мітки визначає послідовні комбінаторні реакції, яким підлягають окрема гранула і, таким чином, забезпечується визначення сполуки на гранулі. Використання олігонуклеотидних міток дозволяє високо чутливий аналіз міток. Тим не менш, спосіб потребує обережного вибору ортогональних положень захисних груп, необхідних для впливу на ко-синтез мітки і члену бібліотеки. Більш того, хімічна лабільність мітки, зокрема з'єднання фосфату і аномерного цукру, може обмежувати вибір реагентів і умов, які можуть бути використані для синтезу неолігомерних бібліотек. В переважних варіантах здійснення бібліотеки використовують лінкери, що дозволяють селективний розрив членів бібліотеки аналізованих сполук для дослідження. Пептиди також використовувались в якості молекул-міток для комбінаторних бібліотек. Два підходи для прикладу описані в попередньому рівні техніки, кожний з яких застосовує розгалужені лінкери до твердої фази, на якій альтернативно розроблені кодуюча і лігандна одноланцюгові нитки. В першому підході (Kerr JM et al. (1993) J Am Chem Soc 115:2529-2531) ортогональність в синтезі досягається шляхом застосування кислотнолабільного захисту для кодування одноланцюгової нитки і основно-лабільного захисту для одноланцюгової нитки сполуки. В альтернативному підході (Nikolaiev et al. (1993) Pept Res 6:161-170), розгалужені лінкери використовують так, щоб кодуюча одиниця і аналізована сполука могли прикріплятися до тієї ж самої функціональної групи на смолі. За варіантом здійснення лінкер, що розщеплюється, може бути розташований між точкою розгалуження і гранулою так, що розщеплення вивільняє молекулу, що містить як код, так і сполуку (Ptek et al. (1991) Tetrahedron Lett 32:3891- 3894). В іншому варіант здійснення, лінкер, що відщеплюється, може бути 53 розташований так, що аналізовану сполуку можна буде селективно відділити від гранули, залишаючи код позаду. Цей останній конструкт є частково значимим, тому що він дозволяє досліджувати аналізовану сполуку без потенційного накладення кодуючих груп. Приклади в попередньому рівні техніки незалежного розщеплення і будування послідовності членів пептидної бібліотеки та їх відповідних міток підтверджують, що мітки можуть точно передбачити пептидну структуру. Альтернативна форма кодування бібліотеки аналізованих сполук використовує набір електрофорних молекул-міток, для яких неможливо встановити послідовність, які використовують в якості бінарного коду (Ohlmeyer et al. (1993) PNAS 90:10922-10926). Експериментально мітки являють собою галоароматичні алкільні ефіри, що визначаються як їх триметилсилілові ефіри на рівнях, менше ніж фемтомолярних за допомогою газової хроматографії з електронним захватом (ECGC). Варіації в довжині алкільного ланцюга, а також природа і положення ароматичних галідних замісників, роблять можливим синтез, щонайменше, 40 таких міток, які по суті можуть кодувати 240 (наприклад, більше 1012) різних молекул. В оригінальній статті (Ohlmeyer et al., вище) мітки зв'язувались з близько 1% наявних амінних груп пептидної бібліотеки через о-нітробензильний лінкер, що розщеплюється світлом. Цей підхід є доцільним при отриманні комбінаторних бібліотек пептидоподібних або інших молекул, що містять амін. Тим не менш, була розроблена більш універсальна система, що дозволяє кодувати по суті будь-яку комбінаторну бібліотеку. Тут, сполука буде прикріплюватися до твердої основи через лінкер, що розщеплюється світлом, і мітка прикріплюється через катехол ефірний лінкер шляхом карбенового вставлення в матрицю гранули (Nestler et al. (1994) J Ore Chan 59:4723-4724). Ця методика ортогонального прикріплення дозволяє селективне відкріплення членів бібліотеки для аналізу в розчині і наступного декодування за допомогою ECGC після окислювального відкріплення від положень міток. Хоча деякі амід-зв'язані бібліотеки в даній галузі застосовують бінарне кодування з електрофорними мітками, що прикріплені до амінних груп, прикріплення цих міток безпосередньо до гранулярної матриці забезпечує набагато більшу гнучкість в структурах, ніж це може бути отримано в закодованих комбінаторних бібліотеках. Прикріплюючись в такий спосіб, мітки та їх лінкер є майже такими ж нереактивними, як і гранулярна матриця сама по собі. Були показані дві бінарно закодовані комбінаторні бібліотеки, де електрофорні мітки прикріплюються безпосередньо до твердої фази (Ohlmeyer et al. (1995) PNAS 92:6027-6031) і забезпечують напрямок для утворення дослідної бібліотеки сполук. Обидві бібліотеки були сконструйовані, використовуючи методику ортогонального прикріплення, в якій член бібліотеки зв'язується з твердою основою за допомогою фотолабільного лінкеру, і мітки прикріпляються тільки через лінкер, що відщеплюється, за допомогою інтенсивного окислення. Через те, що члени бібліотеки можуть бути повторно частково фото екстраговані з твер 90502 54 дої основи, члени бібліотеки можуть бути застосовані в багатократних аналізах. Наступна фотоекстракція також робить можливою методику високопродуктивного циклічного дослідження: перше, багаторазові гранули розміщали в 96-лункові мікротитрувальні планшети; друге, сполуки частково відкріпляли і переміщали на планшети для аналізу; третє, аналізом металевого зв'язування визначали активні лунки; четверте, відповідні гранули переупорядкували окремо в нові мікротитрувальні планшети; п'яте, визначали окремі активні сполуки; і шосте, розшифрували структуру. Приклади Даний винахід, в основному описаний, буде легше зрозуміти за допомогою наступних прикладів, які включені усього лише з метою ілюстрації певних аспектів та варіантів здійснення за даним винаходом та не призначені обмежувати даний винахід. Приклад 1 Отримання Сполуки 1 Сполука 1 Розчин саркозин диметил аміду (0,22ммоль) і триетиламіну (0,6ммоль) в метанол/метилен хлориді (1:9, 1,2мл) обробили сульфоніл хлоридом (0,122ммоль) і перемішували протягом 4 годин при 23°С. Прозорий розчин розбавили метилен хлоридом (10мл) і відмили 10% водною лимонною кислотою. Сепарований водний шар екстрагували дихлорметаном (10мл), і комбіновані органічні шари вимивали сольовим розчином і висушували на натрію сульфаті. Прозору олію з концентрації під вакуумом очищали хроматографією на силікагелі (0,6% води/1,2% метанол в етилацетаті в якості елюенту) до виходу білої твердої речовини з виходом 87%. Приклад 2 Отримання Сполуки 3. 55 Сполука 3 Розчин N-метил-аміноізобутил диметиламіду (0,22ммоль) і сульфоніл хлориду (0,122ммоль) поміщають в колбу і концентрують тричі з сухого 1,2-дихлоретану (10мл). Залишок відновили в сухому дихлорметані і триетиламіні (0,6ммоль), і додали 4-(диметиламіно)піридині (2,5мг). Суміш перемішували протягом 8 годин при 23°С. Прозорий розчин розбавили метилен хлоридом (10мл) і відмили 10% водною лимонною кислотою. Сепарований водний шар екстрагували дихлорметаном (10мл), і комбіновані органічні шари відмили сольовим розчином і сушили на натрію сульфаті. Прозору олію з концентрації під вакуумом очищали хроматографією на силікагелі (0,6% води/1,2% метанолу в етилацетаті в якості елюенту) до виходу білої твердої речовини з виходом 87%. 90502 56 Приклад 3 Варденафіл (Levitra ) являє собою селективний інгібітор PDE5. Структури Варденафілу і аналоги, відомі в даній галузі, були порівняні відносно активності і фармакокінетичних властивостей. Розробка сполук за даним винаходом включає модифікацію молекул, використовуючи функціональні групи для забезпечення нових сполук, що проявляють покращені фармакокінетичні властивості. Функціональні групи розміщають так, щоб впливати скоріше на фармакокінетичні властивості, ніж на активність. Перелік сполук, що розробляють і синтезують, включав елементи, які, припускають, є продуктами метаболізму інших елементів переліку. Білкове зв'язування було визначене стандартними способами ультрафільтрації. Інгібування фосфодіестерази було визначене способами, відомими фахівцям в даній галузі. 57 90502 58 59 90502 60
ДивитисяДодаткова інформація
Назва патенту англійськоюImidazotriazinone compounds and pharmaceutical composition containing thereof
Автори англійськоюCampbell Stewart, Duffy David, Grogan Michael, Kates Steven, Ostuni Emanuele, Schueller Olivier, Sweetnam Paul
Назва патенту російськоюИмидазотриазиноновые соединения и фармацевтическая композиция, которая их содержит
Автори російськоюКемпбелл Стюарт, Даффи Девид, Гроган Майкл, Кейтс Стивен, Остуни Эмануэль, Шюллер Оливер, Свитнем Пол
МПК / Мітки
МПК: A61K 31/53
Мітки: фармацевтична, композиція, містить, сполуки, імідазотриазинонові
Код посилання
<a href="https://ua.patents.su/37-90502-imidazotriazinonovi-spoluki-ta-farmacevtichna-kompoziciya-shho-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">Імідазотриазинонові сполуки та фармацевтична композиція, що їх містить</a>
Попередній патент: Спосіб переробки неорганічних хлоридів
Наступний патент: Спосіб боротьби з ушкодженням матеріалу шкідниками, композиція та капсула
Випадковий патент: Пристрій для регулювання витрати литва