Похідні діарилметиліденпіперидину, спосіб їх отримання (варіанти), фармацевтична композиція на їх основі та їх застосування
Формула / Реферат
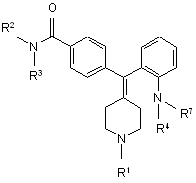
1. Сполука формули ΙΑ, її фармацевтично прийнятна сіль, діастереомери, енантіомери або їх суміші:
 , IA
, IA
де
R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-3-алкіл та C2-9-гетероцикліл-С1-3-алкіл; де вказані С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл;
R2, R3 та R4 незалежно вибрані з групи: гідроген, С1-6-алкіл та С3-6-циклоалкіл; де вказані С1-6-алкіл та С3-6-циклоалкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл;
R7 вибрано з групи: -Н, -ОН, С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл, С2-9-гетероцикліл-С1-6-алкіл, -C(=O)-N-R8R9, -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8, -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Н, С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл, С2-9-гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл, С2-9-гетероцикліл-С1-6-алкіл, застосовувані у визначеннях R7, R8 та R9, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл.
2. Сполука за п. 1,
де R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, бензил та С2-5-гетероцикліл, де вказані С1-6-алкіл, С3-6-циклоалкіл, бензил та С2-5-гетероцикліл, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-6-алкіл, галогенований С1-6-алкіл, -CF3, С1-6-алкоксил, хлор, флуор, бром та йод;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та С1-3-алкіл;
R7 вибрано з групи: -Н, -ОН, феніл, С3-5-гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероцикліл-С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-3-алкіл, -C(=O)-N-R8R9, -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8, -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Η, феніл, С3-5-гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероцикліл-С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-3-алкіл, де вказані феніл, С3-5-гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероцикліл-С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-3-алкіл, застосовувані у визначеннях R7, R8 та R9, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-6-алкіл, галогенований С1-6-алкіл, -CF3, С1-6-алкоксил, хлор, флуор, бром та йод.
3. Сполука за п. 1,
де
R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, бензил, тіадіазолілметил, піридилметил, тієнілметил, фурилметил, імідазолілметил, триазолілметил, піролілметил, тіазолілметил та N-оксидопіридилметил, де вказані С1-6-алкіл, С3-6-циклоалкіл, бензил, тіадіазолілметил, піридилметил, тієнілметил, фурилметил, імідазолілметил, триазолілметил, піролілметил, тіазолілметил та N-оксидопіридилметил, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-6-алкіл, галогенований С1-6алкіл, -CF3, С1-6-алкоксил, хлор, флуор, бром та йод;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та метил;
R7 вибрано з групи: -Н, С1-6-алкіл, феніл-С1-3-алкіл, С3-7-циклоалкіл-С1-3-алкіл, С3-6-циклоалкіл, феніл, С1-6-алкіл, -C(=O)-N-R8R9, -S(=O)2-R8, -C(=O)-O-R8 та -C(=O)-R8, де R8 та R9 незалежно вибрані з групи: -Н, феніл-С1-3-алкіл, С3-7-циклоалкіл-С1-3-алкіл, С3-7-циклоалкіл, феніл та С1-6-алкіл, де вказані феніл-С1-3-алкіл, С3-7-циклоалкіл-С1-3-алкіл, С3-7-циклоалкіл, феніл, С1-6-алкіл, застосовувані у визначенні R7, R8 та R9, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-6-алкіл, галогенований С1-6-алкіл, -CF3, C1-6-алкоксил, хлор, флуор, бром та йод.
4. Сполука за п. 1,
де R1 вибрано з групи: гідроген, пропіл, бензил, тіадіазолілметил, піридилметил, тієнілметил, фурилметил, імідазолілметил, триазолілметил, піролілметил, тіазолілметил та N-оксидопіридилметил;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та метил;
R7 вибрано з групи: -Н, етил, феніл, бензил або фенетил, нафтил, флуорфеніл, хлорфеніл, циклопентил, циклогексил, циклогептил, циклопентилметил, циклогексилметил, -C(=O)-NH-R8, -S(=O)2-R8, -C(=O)-O-R8 та -C(=O)-R8, де R8 вибрано з групи: метил, 2,2,2-трифлуоретил, феніл, бензил, фенетил, метилфеніл, флуорфеніл, бутил, циклогексил та циклогексилметил.
5. Сполука за п. 1, яку вибрано з групи:
СПОЛУКА 1: 4-[[2-(бензоїламіно)феніл]-4-піперидиніліденметил]-N,N-діетилбензамід;
СПОЛУКА 2: N-[2-[[4-[(діетиламіно)карбоніл]феніл]-4-піперидиніліденметил]феніл]бензолацетамід;
СПОЛУКА 3: 4-[[2-[(циклогексилкарбоніл)аміно]феніл]-4-піперидиніліденметил]-N,N-діетилбензамід;
СПОЛУКА 4: N-[2-[[4-[(діетиламіно)карбоніл]феніл]-4-піперидиніліденметил]феніл]бензолпропанамід;
СПОЛУКА 5: 4-[[2-[(циклогексилацетил)аміно]феніл]-4-піперидиніліденметил]-Ν,Ν-діетилбензамід;
СПОЛУКА 6: N,N-діетил-4-[[2-[(2-фенілетил)аміно]феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 7: 4-[[2-[(циклогексилметил)аміно]феніл]-4-піперидиніліденметил]-N,N-діетилбензамід;
СПОЛУКА 8: N,N-діетил-4-[[2-[(фенілметил)аміно]феніл]-4-піперидиніліденметил]-бензамід;
СПОЛУКА 9: 4-[[2-(циклогексиламіно)феніл]-4-піперидиніліденметил]-N,N-діетилбензамід;
СПОЛУКА 10: N,N-діетил-4-[[2-[[(феніламіно)карбоніл]аміно]феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 11: N,N-діетил-4-[[2-(феніламіно)феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 12: N,N-діетил-4-[[2-(метилфеніламіно)феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 13: N,N-діетил-4-[[2-[(фенілсульфоніл)аміно]феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 14: N,N-діетил-4-[[2-[[(фенілметил)сульфоніл]аміно]феніл]-4-піперидиніліденметил]бензамід;
СПОЛУКА 15: N,N-діетил-4-[4-піперидиніліден[2-[[(2,2,2-трифлуоретил)сульфоніл]аміно]феніл]метил]бензамід;
СПОЛУКА 16: 4-[{2-[(циклопентилацетил)аміно]феніл}(піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 17: 4-[{2-[(циклопентилкарбоніл)аміно]феніл}(піперидин-4-іліден)метил]-Ν,Ν-діетилбензамід;
СПОЛУКА 18: N,N-діетил-4-[{2-[(3-фенілпропіл)аміно]феніл}(піперидин-4-іліден)метил]бензамід;
СПОЛУКА 19: 4-[{2-[(2-циклогексилетил)аміно]феніл}(піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 20: 4-[[2-(циклопентиламіно)феніл](піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 21: 4-[[2-(циклогептиламіно)феніл](піперидин-4-іліден)метил]-Ν,Ν-діетилбензамід;
СПОЛУКА 22: 4-[(2-{[(бензиламіно)карбоніл]аміно}феніл)(піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 23: N,N-діетил-4-[[2-(1-нафтиламіно)феніл](піперидин-4-іліден)метил]бензамід;
СПОЛУКА 24: N,N-дieтил-4-[{2-[(3-флyopфeніл)aмiнo]фeнiл}(пiпepидин-4-іліден)метил]бензамід;
СПОЛУКА 25: 4-[{2-[(4-хлорфеніл)аміно]феніл}(піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 26: 4-[{2-[циклогексил(метил)аміно]феніл}(піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 27: N,N-дieтил-4-[(2-{[(4-мeтилфeнiл)cyльфoнiл]aмiнo}фeнiл)(пiпepидин-4-іліден)метил]бензамід;
СПОЛУКА 28: N,N-діетил-4-[(2-{[(2-флуорфеніл)сульфоніл]аміно}феніл)(піперидин-4-іліден)метил]бензамід;
СПОЛУКА 29: 4-[{2-[(бутилсульфоніл)аміно]феніл}(піперидин-4-іліден)метил]-Ν,Ν-діетилбензамід;
СПОЛУКА 31: 4-[[2-(ацетиламіно)феніл](піперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 32: метил 2-[{4-[(діетиламіно)карбоніл]феніл}(піперидин-4-іліден)метил]фенілкарбамат;
СПОЛУКА 30: 4-[(2-амінофеніл)(1-бензилпіперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 33: 4-[[2-(ацетиламіно)феніл](1-бензилпіперидин-4-іліден)метил]-Ν,Ν-діетилбензамід;
СПОЛУКА 34: метил 2-((1-бензилпіперидин-4-іліден){4-[(діетиламіно)карбоніл]феніл}метил)фенілкарбамат;
СПОЛУКА 35: 4-{(2-амінофеніл)[1-(1,3-тіазол-4-ілметил)піперидин-4-іліден]метил}-Ν,Ν-діетилбензамід;
СПОЛУКА 36: 4-{(2-амінофеніл)[1-(1,3-тіазол-5-ілметил)піперидин-4-іліден]метил}-Ν,Ν-діетилбензамід;
СПОЛУКА 37: 4-{[2-(ацетиламіно)феніл][1-(1,3-тіазол-4-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 38: метил 2-{{4-[(діетиламіно)карбоніл]феніл}[1-(1,3-тіазол-4-ілметил)піперидин-4-іліден]метил}фенілкарбамат;
СПОЛУКА 39: 4-{[2-(ацетиламіно)феніл][1-(1,3-тіазол-5-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 40: метил 2-{{4-[(діетиламіно)карбоніл]феніл}[1-(1,3-тіазол-5-ілметил)піперидин-4-іліден]метил}фенілкарбамат;
СПОЛУКА 41: 4-[(2-амінофеніл)(1-бутилпіперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 42: 4-{(2-амінофеніл)[1-(піридин-4-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 43: 4-{(2-амінофеніл)[1-(піридин-3-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 44: 4-{(2-амінофеніл)[1-(піридин-2-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 45: 4-{[2-(ацетиламіно)феніл][1-(піридин-4-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 46: 4-{[2-(ацетиламіно)феніл][1-(піридин-3-ілметил)піперидин-4-іліден]метил}-Ν,Ν-діетилбензамід;
СПОЛУКА 47: 4-[[2-(ацетиламіно)феніл](1-бутилпіперидин-4-іліден)метил]-N,N-діетилбензамід;
СПОЛУКА 48: 4-{[2-(ацетиламіно)феніл][1-(піридин-2-ілметил)піперидин-4-іліден]метил}-N,N-діетилбензамід;
СПОЛУКА 49: метил [2-((1-бутилпіперидин-4-іліден){4[(діетиламіно)карбоніл]феніл}метил)феніл]карбамат;
СПОЛУКА 50: метил (2-{{4-[(діетиламіно)карбоніл]феніл}[1-(піридин-4-ілметил)піперидин-4-іліден]метил}феніл)карбамат;
СПОЛУКА 51: метил (2-{{4-[(діетиламіно)карбоніл]феніл}[1-(піридин-3-ілметил)піперидин-4-іліден]метил}феніл)карбамат;
СПОЛУКА 52: метил (2-{{4-[(діетиламіно)карбоніл]феніл}[1-(піридин-2-ілметил)піперидин-4-іліден]метил}феніл)карбамат;
СПОЛУКА 53: 4-{(1-бутилпіперидин-4-іліден)[2-(етиламіно)феніл]метил}-N,N-діетилбензамід;
СПОЛУКА 54: N,N-діетил-4-{[2-(етиламіно)феніл][1-(піридин-4-ілметил)піперидин-4-іліден]метил}бензамід;
СПОЛУКА 55: N,N-діетил-4-{[2-(етиламіно)феніл][1-(піридин-3-ілметил)піперидин-4-іліден]метил}бензамід;
СПОЛУКА 56: N,N-діетил-4-{[2-(етиламіно)феніл][1-(піридин-2-ілметил)піперидин-4-іліден]метил}бензамід;
та їх фармацевтично прийнятні солі.
6. Сполука за будь-яким з пп. 1-5 для застосування як медикаменту.
7. Застосування сполуки за будь-яким з пп. 1-5 у виробництві медикаменту для терапії болю, тривожності або функціональних шлунково-кишкових розладів.
8. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-5 та фармацевтично прийнятний носій.
9. Спосіб лікування болю у теплокровної тварини, в якому вводять вказаній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-5.
10. Спосіб лікування функціональних шлунково-кишкових розладів у теплокровної тварини, в якому вводять вказаній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-5.
11. Спосіб отримання сполуки формули IIА
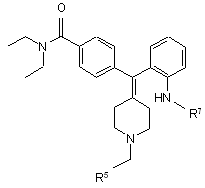 , ІІA
, ІІA
в якому:
здійснюють реакцію сполуки формули IIІА з R5-CH2-X або R5-CHO:
 , ІІІА
, ІІІА
де X - галоген;
R7 вибрано з групи: -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8 та -C(=O)-R8,
R8 вибрано з групи: С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH,
-C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а
R5 вибрано з групи: С6-10-арил та С2-5гетероарил, де вказані С6-10-арил та С2-5гетероарил, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, -CF3, -C(O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл.
12. Спосіб отримання сполуки формули ІІА
 , ІІА
, ІІА
в якому:
здійснюють реакцію сполуки формули IVA з R7-X або R7-O- R7
 , IVA
, IVA
де X - галоген;
R7 вибрано з групи: -C(=O)-O-R8 та -C(=O)-R8, де R8 вибрано з групи: С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи:
-R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а
R5 вибрано з групи: С6-10-арил та С2-5гетероарил де вказані С6-10-арил та С2-5гетероарил, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, -CF3, -C(=O)R, -C(O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл.
13. Спосіб отримання сполуки формули VA
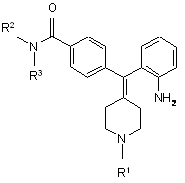 , VA
, VA
в якому відновлюють сполуку формули VIA
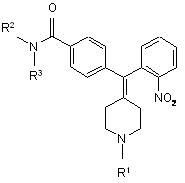 , VIA
, VIA
де
R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл; де вказані С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл;
R2 та R3 незалежно вибрані з групи: гідроген, С1-6-алкіл та С3-6-циклоалкіл, де вказані С1-6-алкіл та С3-6-циклоалкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(O)-OR, де R незалежно представляє гідроген або С1-6-алкіл.
14. Сполука формули І, її фармацевтично прийнятна сіль, її діастереомери, її енантіомери та їх суміші:
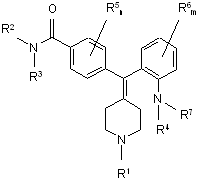 , І
, І
де
R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9-гетероцикліл, як варіант, заміщений С6-10-арил-С1-3-алкіл та, як варіант, заміщений С2-9-гетероцикліл-С1-3-алкіл;
n дорівнює 0, 1 або 2;
m дорівнює 0, 1 або 2;
R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл;
R5 та R6 незалежно вибрані з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, -CF3, -C(=O)R, -С(=О)ОН, -NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а
R7 вибрано з групи: -Н, -ОН, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-8-циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9-гетероцикліл, як варіант, заміщений С6-10-арил-С1-6-алкіл, як варіант, заміщений С2-9-гетероцикліл-С1-6-алкіл, -C(=O)-NR8R9, -C(=O)O-R8, -S(=O)-R8, -S(=O)2-R8, -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Н, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-8-циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9-гетероцикліл, як варіант, заміщений С6-10-арил-С1-6-алкіл, та, як варіант, заміщений С2-9-гетероцикліл-С1-6-алкіл.
15. Сполука за п. 14,
де R1 вибрано з групи: гідроген, С1-6-алкіл-О-С(О)-, як варіант, заміщений С1-6-алкіл, та, як варіант, заміщений С3-6-циклоалкіл;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та С1-3-алкіл;
R7 вибрано з групи: -Н, -ОН, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл, -C(=O)-N-R8R9, -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8, -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл; а
n та m дорівнюють 0.
16. Сполука за п. 14,
де R1 вибрано з групи: гідроген та С1-6-алкіл-О-С(=О)-;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та метил;
R7 вибрано з групи: -Н, феніл-С1-3-алкіл, С3-6-циклоалкіл-С1-3-алкіл, С3-6-циклоалкіл, феніл, як варіант, заміщений С1-6-алкіл, -C(=O)-N-R8R9, -S(=O)2-R8 та -C(=O)-R8, де R8 та R9 незалежно вибрані з групи: -Н, феніл-С1-3-алкіл, С3-6-циклоалкіл-С1-3-алкіл, С3-6-циклоалкіл, феніл, та, як варіант, заміщений С1-6-алкіл; а
n та m дорівнюють 0.
17. Сполука за п. 14, де
R1 представляє гідроген;
R2 та R3 представляють етил;
R4 вибрано з групи: гідроген та метил;
R7 вибрано з групи: -Н, феніл, бензил або фенетил, циклогексил, циклогексилметил, -C(=O)-NH-R8, -S(=O)2-R8 та -C(=O)-R8, де R8 вибрано з групи: 2,2,2-трифлуоретил, феніл, бензил або фенетил, циклогексил та циклогексилметил; а
n та m дорівнюють 0.
18. Спосіб отримання сполуки формули II
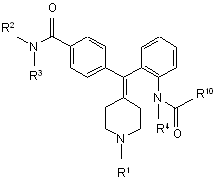 , II
, II
в якому:
здійснюють реакцію сполуки формули III з X1-C(=O)-R10:
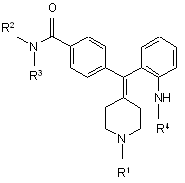 , III
, III
де
R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений C1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл;
X1 вибрано з групи: -ОН, -OR11, -O-C(=O)-R11, -Сl, -Вr та -І, де R11 - С1-6-алкіл;
R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а
R10 вибрано з групи: -H, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл.
19. Спосіб отримання сполуки формули IV
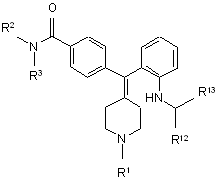 , IV
, IV
в якому:
здійснюють реакцію сполуки формули V з R12-C(=O)-R13:
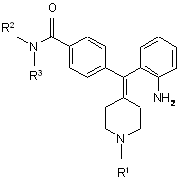 , V
, V
де
R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл;
R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а
R12 та R13 незалежно вибрані з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл, або R12 та R13 разом утворюють частину С3-6-циклоалкільного кільця або С3-5-гетероциклільного кільця.
20. Спосіб отримання сполуки формули VI, в якому:
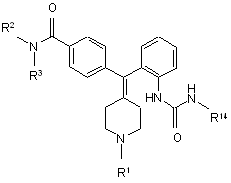 VI
VI
здійснюють реакцію сполуки формули V з R14-NCO:
 , V
, V
де
R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл;
R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а
R14 вибрано з групи: як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл.
21. Спосіб отримання сполуки формули VII
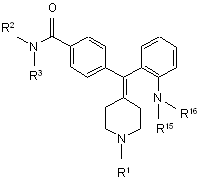 , VII
, VII
в якому:
здійснюють реакцію сполуки формули VIII з R16-X2:
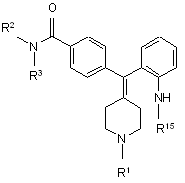 , VIII
, VIII
де
R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл;
R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл;
X2 вибрано з групи: І, Вr та Сl;
R15 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл; а
R16 вибрано з групи: як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл.
22. Спосіб отримання сполуки формули IX
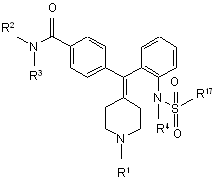 , IX
, IX
в якому:
здійснюють реакцію сполуки формули III з X3-S(=O)2-R17
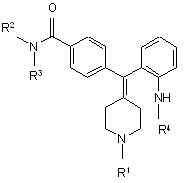 , ІІІ
, ІІІ
де
R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл;
X3 вибрано з групи: -ОН, -OR11, -Сl, -Вr та -І, де R11 - С1-6-алкіл;
R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а
R17 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С1-3-алкіл.
Текст
1. Сполука формули ΙΑ, її фармацевтично прийнятна сіль, діастереомери, енантіомери або їх суміші: O N (ВАРІАНТИ), (19) 1 ОТРИМАННЯ 3 82091 4 R7 вибрано з групи: -Н, -ОН, феніл, С3-5СПОЛУКА 1: 4-[[2-(бензоїламіно)феніл]-4гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероциклілпіперидиніліденметил]-N,N-діетилбензамід; С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7СПОЛУКА 2: N-[2-[[4циклоалкіл-С 1-3-алкіл, -C(=O)-N-R8R9, -C(=O)-O-R8, [(діетиламіно)карбоніл]феніл]-4-S(=O)-R8, -S(=O)2-R8 , -C(=O)-R8 та -SO3H, де R8 та піперидиніліденметил]феніл]бензолацетамід; R9 незалежно вибрані з групи: -Η, феніл, С3-5СПОЛУКА 3: 4-[[2гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероцикліл[(циклогексилкарбоніл)аміно]феніл]-4С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7піперидиніліденметил]-N,N-діетилбензамід; циклоалкіл-С 1-3-алкіл, де вказані феніл, С3-5СПОЛУКА 4: N-[2-[[4гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероцикліл[(діетиламіно)карбоніл]феніл]-4С1-3-алкіл, С1-6-алкіл, С3-7-циклоалкіл, С3-7піперидиніліденметил]феніл]бензолпропанамід; циклоалкіл-С 1-3-алкіл, застосовувані у визначеннях СПОЛУКА 5: 4-[[2R7, R8 та R9, як варіант, заміщені одним або [(циклогексилацетил)аміно]феніл]-4більше замісниками, вибраними з групи: С1-6-алкіл, піперидиніліденметил]-Ν,Ν-діетилбензамід; галогенований С1-6-алкіл, -CF3, С1-6-алкоксил, СПОЛУКА 6: N,N-діетил-4-[[2-[(2хлор, флуор, бром та йод. фенілетил)аміно]феніл]-43. Сполука за п. 1, піперидиніліденметил]бензамід; де СПОЛУКА 7: 4-[[2R1 вибрано з групи: гідроген, С1-6-алкіл-О[(циклогексилметил)аміно]феніл]-4С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, бензил, піперидиніліденметил]-N,N-діетилбензамід; тіадіазолілметил, піридилметил, тієнілметил, СПОЛУКА 8: N,N-діетил-4-[[2фурилметил, імідазолілметил, триазолілметил, [(фенілметил)аміно]феніл]-4піролілметил, тіазолілметил та Nпіперидиніліденметил]-бензамід; оксидопіридилметил, де вказані С1-6-алкіл, С3-6СПОЛУКА 9: 4-[[2-(циклогексиламіно)феніл]-4циклоалкіл, бензил, тіадіазолілметил, піперидиніліденметил]-N,N-діетилбензамід; піридилметил, тієнілметил, фурилметил, СПОЛУКА 10: N,N-діетил-4-[[2імідазолілметил, триазолілметил, піролілметил, [[(феніламіно)карбоніл]аміно]феніл]-4тіазолілметил та N-оксидопіридилметил, як піперидиніліденметил]бензамід; варіант, заміщені одним або більше замісниками, СПОЛУКА 11: N,N-діетил-4-[[2-(феніламіно)феніл]вибраними з групи: С1-6-алкіл, галогенований С14-піперидиніліденметил]бензамід; СПОЛУКА 12: N,N-діетил-4-[[26алкіл, -CF3, С 1-6-алкоксил, хлор, флуор, бром та йод; (метилфеніламіно)феніл]-4R2 та R3 представляють етил; піперидиніліденметил]бензамід; R4 вибрано з групи: гідроген та метил; СПОЛУКА 13: N,N-діетил-4-[[2R7 вибрано з групи: -Н, С1-6-алкіл, феніл[(фенілсульфоніл)аміно]феніл]-4С1-3-алкіл, С3-7-циклоалкіл-С 1-3-алкіл, С3-6піперидиніліденметил]бензамід; циклоалкіл, феніл, С1-6-алкіл, -C(=O)-N-R8R9, СПОЛУКА 14: N,N-діетил-4-[[2S(=O)2-R8, -C(=O)-O-R 8 та -C(=O)-R8, де R8 та R9 [[(фенілметил)сульфоніл]аміно]феніл]-4незалежно вибрані з групи: -Н, феніл-С1-3-алкіл, С3піперидиніліденметил]бензамід; СПОЛУКА 15: N,N-діетил-4-[4-піперидиніліден[27-циклоалкіл-С 1-3-алкіл, С 3-7-циклоалкіл, феніл та С1-6-алкіл, де вказані феніл-С 1-3-алкіл, С3-7[[(2,2,2циклоалкіл-С 1-3-алкіл, С3-7-циклоалкіл, феніл, С1-6трифлуоретил)сульфоніл]аміно]феніл]метил]бенза алкіл, застосовувані у визначенні R7, R8 та R9, як мід; варіант, заміщені одним або більше замісниками, СПОЛУКА 16: 4-[{2вибраними з групи: С1-6-алкіл, галогенований С1-6[(циклопентилацетил)аміно]феніл}(піперидин-4алкіл, -CF3, C1-6-алкоксил, хлор, флуор, бром та іліден)метил]-N,N-діетилбензамід; йод. СПОЛУКА 17: 4-[{24. Сполука за п. 1, [(циклопентилкарбоніл)аміно]феніл}(піперидин-4де R1 вибрано з групи: гідроген, пропіл, іліден)метил]-Ν,Ν-діетилбензамід; бензил, тіадіазолілметил, піридилметил, СПОЛУКА 18: N,N-діетил-4-[{2-[(3тієнілметил, фурилметил, імідазолілметил, фенілпропіл)аміно]феніл}(піперидин-4триазолілметил, піролілметил, тіазолілметил та Nіліден)метил]бензамід; оксидопіридилметил; СПОЛУКА 19: 4-[{2-[(2R2 та R3 представляють етил; циклогексилетил)аміно]феніл}(піперидин-4R4 вибрано з групи: гідроген та метил; іліден)метил]-N,N-діетилбензамід; R7 вибрано з групи: -Н, етил, феніл, СПОЛУКА 20: 4-[[2бензил або фенетил, нафтил, флуорфеніл, (циклопентиламіно)феніл](піперидин-4хлорфеніл, циклопентил, циклогексил, іліден)метил]-N,N-діетилбензамід; циклогептил, циклопентилметил, СПОЛУКА 21: 4-[[2циклогексилметил, -C(=O)-NH-R 8, -S(=O)2-R 8, (циклогептиламіно)феніл](піперидин-4C(=O)-O-R8 та -C(=O)-R8, де R8 вибрано з групи: іліден)метил]-Ν,Ν-діетилбензамід; метил, 2,2,2-трифлуоретил, феніл, бензил, СПОЛУКА 22: 4-[(2фенетил, метилфеніл, флуор феніл, бутил, {[(бензиламіно)карбоніл]аміно}феніл)(піперидин-4циклогексил та циклогексилметил. іліден)метил]-N,N-діетилбензамід; 5. Сполука за п. 1, яку вибрано з групи: 5 82091 6 СПОЛУКА 23: N,N-діетил-4-[[2-(1СПОЛУКА 45: 4-{[2-(ацетиламіно)феніл][1нафтиламіно)феніл](піперидин-4(піридин-4-ілметил)піперидин-4-іліден]метил}-N,Nіліден)метил]бензамід; діетилбензамід; СПОЛУКА 24: N,N-дieтил-4-[{2-[(3СПОЛУКА 46: 4-{[2-(ацетиламіно)феніл][1флyopфeніл)aмiнo]фeнiл}(пiпepидин-4(піридин-3-ілметил)піперидин-4-іліден]метил}-Ν,Νіліден)метил]бензамід; діетилбензамід; СПОЛУКА 25: 4-[{2-[(4СПОЛУКА 47: 4-[[2-(ацетиламіно)феніл](1хлорфеніл)аміно]феніл}(піперидин-4-іліден)метил]бутилпіперидин-4-іліден)метил]-N,NN,N-діетилбензамід; діетилбензамід; СПОЛУКА 26: 4-[{2СПОЛУКА 48: 4-{[2-(ацетиламіно)феніл][1[циклогексил(метил)аміно]феніл}(піперидин-4(піридин-2-ілметил)піперидин-4-іліден]метил}-N,Nіліден)метил]-N,N-діетилбензамід; діетилбензамід; СПОЛУКА 27: N,N-дieтил-4-[(2-{[(4СПОЛУКА 49: метил [2-((1-бутилпіперидин-4мeтилфeнiл)cyльфoнiл]aмiнo}фeнiл)(пiпepидин-4іліден){4[(діетиламіно)карбоніл]феніл}метил)феніл іліден)метил]бензамід; ]карбамат; СПОЛУКА 28: N,N-діетил-4-[(2-{[(2СПОЛУКА 50: метил (2-{{4флуорфеніл)сульфоніл]аміно}феніл)(піперидин-4[(діетиламіно)карбоніл]феніл}[1-(піридин-4іліден)метил]бензамід; ілметил)піперидин-4-іліден]метил}феніл)карбамат; СПОЛУКА 29: 4-[{2СПОЛУКА 51: метил (2-{{4[(бутилсуль фоніл)аміно]феніл}(піперидин-4[(діетиламіно)карбоніл]феніл}[1-(піридин-3іліден)метил]-Ν,Ν-діетилбензамід; ілметил)піперидин-4-іліден]метил}феніл)карбамат; СПОЛУКА 31: 4-[[2-(ацетиламіно)феніл](піперидинСПОЛУКА 52: метил (2-{{44-іліден)метил]-N,N-діетилбензамід; [(діетиламіно)карбоніл]феніл}[1-(піридин-2СПОЛУКА 32: метил 2-[{4ілметил)піперидин-4-іліден]метил}феніл)карбамат; [(діетиламіно)карбоніл]феніл}(піперидин-4СПОЛУКА 53: 4-{(1-бутилпіперидин-4-іліден)[2іліден)метил]фенілкарбамат; (етиламіно)феніл]метил}-N,N-діетилбензамід; СПОЛУКА 30: 4-[(2-амінофеніл)(1СПОЛУКА 54: N,N-діетил-4-{[2бензилпіперидин-4-іліден)метил]-N,N(етиламіно)феніл][1-(піридин-4-ілметил)піперидиндіетилбензамід; 4-іліден]метил}бензамід; СПОЛУКА 33: 4-[[2-(ацетиламіно)феніл](1СПОЛУКА 55: N,N-діетил-4-{[2бензилпіперидин-4-іліден)метил]-Ν,Ν(етиламіно)феніл][1-(піридин-3-ілметил)піперидиндіетилбензамід; 4-іліден]метил}бензамід; СПОЛУКА 34: метил 2-((1-бензилпіперидин-4СПОЛУКА 56: N,N-діетил-4-{[2іліден){4(етиламіно)феніл][1-(піридин-2-ілметил)піперидин[(діетиламіно)карбоніл]феніл}метил)фенілкарбама 4-іліден]метил}бензамід; т; та їх фармацевтично прийнятні солі. СПОЛУКА 35: 4-{(2-амінофеніл)[1-(1,3-тіазол-46. Сполука за будь-яким з пп. 1-5 для ілметил)піперидин-4-іліден]метил}-Ν,Νзастосування як медикаменту. діетилбензамід; 7. Застосування сполуки за будь-яким з СПОЛУКА 36: 4-{(2-амінофеніл)[1-(1,3-тіазол-5пп. 1-5 у виробництві медикаменту для терапії ілметил)піперидин-4-іліден]метил}-Ν,Νболю, тривожності або функціональних шлунководіетилбензамід; кишкових розладів. СПОЛУКА 37: 4-{[2-(ацетиламіно)феніл][1-(1,38. Фармацевтична композиція, що містить тіазол-4-ілметил)піперидин-4-іліден]метил}-N,Nсполуку за будь-яким з пп. 1-5 та фармацевтично діетилбензамід; прийнятний носій. СПОЛУКА 38: метил 2-{{49. Спосіб лікування болю у теплокровної [(діетиламіно)карбоніл]феніл}[1-(1,3-тіазол-4тварини, в якому вводять вказаній тварині, що ілметил)піперидин-4-іліден]метил}фенілкарбамат; потребує такої терапії, терапевтично ефективну СПОЛУКА 39: 4-{[2-(ацетиламіно)феніл][1-(1,3кількість сполуки за будь-яким з пп. 1-5. тіазол-5-ілметил)піперидин-4-іліден]метил}-N,N10. Спосіб лікування функціональних діетилбензамід; шлунково-кишкових розладів у теплокровної СПОЛУКА 40: метил 2-{{4тварини, в якому вводять вказаній тварині, що [(діетиламіно)карбоніл]феніл}[1-(1,3-тіазол-5потребує такої терапії, терапевтично ефективну ілметил)піперидин-4-іліден]метил}фенілкарбамат; кількість сполуки за будь-яким з пп. 1-5. СПОЛУКА 41: 4-[(2-амінофеніл)(1-бутилпіперидин11. Спосіб отримання сполуки формули 4-іліден)метил]-N,N-діетилбензамід; IIА СПОЛУКА 42: 4-{(2-амінофеніл)[1-(піридин-4ілметил)піперидин-4-іліден]метил}-N,Nдіетилбензамід; СПОЛУКА 43: 4-{(2-амінофеніл)[1-(піридин-3ілметил)піперидин-4-іліден]метил}-N,Nдіетилбензамід; СПОЛУКА 44: 4-{(2-амінофеніл)[1-(піридин-2ілметил)піперидин-4-іліден]метил}-N,Nдіетилбензамід; 7 82091 8 O O N N HN HN R7 R7 N N R5 , ІІA в якому: здійснюють реакцію сполуки формули IIІА з R5CH2-X або R5-CHO: O N R5 , ІІА в якому: здійснюють реакцію сполуки формули IVA з R7-X або R7-O- R 7 O N NH 2 HN R7 N H N , ІІІА де X - галоген; R7 вибрано з групи: -C(=O)-O-R8, -S(=O)8 R , -S(=O) 2-R8 та -C(=O)-R 8, R8 вибрано з групи: С1-6-алкіл, С3-8циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10арил-С 1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-6-алкіл та С 2-9гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, NO2, OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та -NRC(=O)OR, де R незалежно представляє гідроген або С 16-алкіл; а R5 вибрано з групи: С6-10-арил та С2де вказані С 6-10-арил та С 25гетероарил, 5гетероарил, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, OR, -Сl, -Вr, -І, -F, -CF3, -C(O)R, -C(=O)OH, -NH 2, SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. 12. Спосіб отримання сполуки формули ІІА R5 , IVA де X - галоген; R7 вибрано з групи: -C(=O)-O-R 8 та -C(=O)8 R , де R8 вибрано з групи: С1-6-алкіл, С3-8циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10арил-С 1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-6-алкіл та С 2-9гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3, -C(=O)R, C(=O)OH, -NH 2, -SH, -NHR, -NR2, -SR, -SO3H, SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а R5 вибрано з групи: С6-10-арил та С2де вказані С 6-10-арил та С 25гетероарил 5гетероарил, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, OR, -Сl, -Вr, -І, -F, -CF3, -C(=O)R, -C(O)OH, -NH 2, SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. 13. Спосіб отримання сполуки формули VA 9 82091 O R2 N R3 NH 2 N R1 , VA в якому відновлюють сполуку формули VIA O R2 N R3 NO2 N R1 , VIA де R1 вибрано з групи: гідроген, С1-6-алкіл-ОС(=О)-, С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-3-алкіл та С 2-9гетероцикліл-С1-3-алкіл; де вказані С1-6-алкіл, С3-6циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10арил-С 1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Вr, -І, -F, CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, -NHR, -NR2, SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; R2 та R3 незалежно вибрані з групи: гідроген, С1-6-алкіл та С 3-6-циклоалкіл, де вказані С1-6-алкіл та С 3-6-циклоалкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -Сl, -Br, -I, -F, -CF3 , -C(=O)R, C(=O)OH, -NH 2, -SH, -NHR, -NR 2, -SR, -SO3H, SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, NRC(=O)R та -NRC(O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. 14. Сполука формули І, її фармацевтично прийнятна сіль, її діастереомери, її енантіомери та їх суміші: R5n R6m O R2 N R3 N R7 N R1 R4 ,І 10 де R1 вибрано з групи: гідроген, С1-6-алкіл-ОС(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9гетероцикліл, як варіант, заміщений С 6-10-арил-С 13-алкіл та, як варіант, заміщений С 2-9-гетероциклілС1-3-алкіл; n дорівнює 0, 1 або 2; m дорівнює 0, 1 або 2; R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; R5 та R6 незалежно вибрані з групи: -R, NO2, -OR, -Сl, -Вr, -І, -F, -CF3 , -C(=O)R, -С(=О)ОН, NH2, -SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а R7 вибрано з групи: -Н, -ОН, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-8циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9-гетероцикліл, як варіант, заміщений С6-10-арил-С 1-6-алкіл, як варіант, заміщений С 2-9-гетероцикліл-С 1-6-алкіл, -C(=O)NR8R9, -C(=O)O-R8, -S(=O)-R8, -S(=O)2-R8 , -C(=O)R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Н, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-8-циклоалкіл, як варіант, заміщений С6-10-арил, як варіант, заміщений С2-9гетероцикліл, як варіант, заміщений С 6-10-арил-С 1та, як варіант, заміщений С2-96-алкіл, гетероцикліл-С1-6-алкіл. 15. Сполука за п. 14, де R1 вибрано з групи: гідроген, С1-6-алкілО-С(О)-, як варіант, заміщений С1-6-алкіл, та, як варіант, заміщений С3-6-циклоалкіл; R2 та R3 представляють етил; R4 вибрано з групи: гідроген та С1-3-алкіл; R7 вибрано з групи: -Н, -ОН, як варіант, заміщений феніл, як варіант, заміщений С3-5гетероцикліл, як варіант, заміщений феніл-С1-3алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл, -C(=O)-N-R8R9, -C(=O)O-R8, -S(=O)-R8, -S(=O) 2-R8, -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5гетероцикліл, як варіант, заміщений феніл-С1-3алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл; а n та m дорівнюють 0. 16. Сполука за п. 14, де R1 вибрано з групи: гідроген та С1-6алкіл-О-С(=О)-; R2 та R3 представляють етил; R4 вибрано з групи: гідроген та метил; R7 вибрано з групи: -Н, феніл-С1-3-алкіл, С3-6-циклоалкіл-С 1-3-алкіл, С3-6-циклоалкіл, феніл, як варіант, заміщений С 1-6-алкіл, -C(=O)-N-R8R9,S(=O)2-R8 та -C(=O)-R 8 , де R8 та R9 незалежно вибрані з групи: -Н, феніл-С1-3-алкіл, С3-6 11 82091 12 циклоалкіл-С 1-3-алкіл, С3-6-циклоалкіл, феніл, та, як O варіант, заміщений С1-6-алкіл; а R2 n та m дорівнюють 0. N 17. Сполука за п. 14, де R1 представляє гідроген; R2 та R3 представляють етил; R3 4 R вибрано з групи: гідроген та метил; R13 HN R7 вибрано з групи: -Н, феніл, бензил або фенетил, циклогексил, циклогексилметил, -C(=O)NH-R8, -S(=O)2-R8 та -C(=O)-R 8, де R8 вибрано з N R12 групи: 2,2,2-трифлуоретил, феніл, бензил або фенетил, циклогексил та циклогексилметил; а n та m дорівнюють 0. R1 , IV 18. Спосіб отримання сполуки формули II в якому: O здійснюють реакцію сполуки формули V з R12C(=O)-R13: R2 O N R2 R3 N N N R10 R3 R4 O NH 2 R1 , II в якому: здійснюють реакцію сполуки формули III з X1C(=O)-R10: O R2 N R3 NH N R1 R4 , III де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений C1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл; X1 вибрано з групи: -ОН, -OR11, -O-C(=O)R11, -Сl, -Вr та -І, де R11 - С1- 6-алкіл; R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R10 вибрано з групи: -H, як варіант, заміщений феніл, як варіант, заміщений С3-5гетероцикліл, як варіант, заміщений феніл-С1-3алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, заміщений С 3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл. 19. Спосіб отримання сполуки формули IV N R1 ,V де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл; R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R12 та R13 незалежно вибрані з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С 3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С 3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С 1-3алкіл, або R12 та R13 разом утворюють частину С 3кільця або С 3-56-циклоалкільного гетероциклільного кільця. 20. Спосіб отримання сполуки формули VI, в якому: O R2 N R3 H N HN R14 N R1 O VI 13 82091 14 здійснюють реакцію сполуки формули V з R14заміщений С3-6-циклоалкіл, як варіант, заміщений NCO: феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, O заміщений С3-5-гетероцикліл-С1-3-алкіл; R2 R2 та R3 незалежно вибрані з групи: N гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; R3 X2 вибрано з групи: І, Вr та Сl; R15 вибрано з групи: -Н, як варіант, NH 2 заміщений феніл, як варіант, заміщений С3-5гетероцикліл, як варіант, заміщений феніл-С1-3алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3N алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, заміщений С 3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл; а R1 ,V R16 вибрано з групи: як варіант, заміщений де феніл-С 1-3-алкіл, як варіант, заміщений С 3-5R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як гетероцикліл, як варіант, заміщений С3-5варіант, заміщений С1-6-алкіл, як варіант, гетероцикліл-С1-3-алкіл, як варіант, заміщений С1-6заміщений С3-6-циклоалкіл, як варіант, заміщений алкіл, як варіант, заміщений С 3-6-циклоалкіл та, як феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл. варіант, заміщений феніл-С 1-3-алкіл та, як варіант, 22. Спосіб отримання сполуки формули IX заміщений С3-5-гетероцикліл-С1-3-алкіл; O R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R14 вибрано з групи: як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6циклоалкіл та, як варіант, заміщений С3-6циклоалкіл-С 1-3-алкіл. 21. Спосіб отримання сполуки формули VII O R 2 N R3 R2 N R3 O N N R17 S R4 O R1 , IX в якому: здійснюють реакцію сполуки формули III з X3S(=O)2-R17 O R2 N R16 N R15 N R3 NH R1 , VII в якому: здійснюють реакцію сполуки формули VIII з R16-X2: O R2 N R3 NH N R1 R15 , VIII де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, N R1 R4 , ІІІ де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл; X3 вибрано з групи: -ОН, -OR11, -Сl, -Вr та І, де R11 - С1- 6-алкіл; R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R17 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5 15 82091 гетероцикліл, як варіант, заміщений феніл-С1-3заміщений алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3заміщений алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, Представлений винахід стосується нових сполук, способу їх отримання, їх застосування та фармацевтичних композицій, що містять нові сполуки. Нові сполуки є корисними у терапії, а зокрема для лікування болю, тривожності та функціональних шлунково-кишкових розладів. Ідентифіковано, що d-рецептор грає роль у багатьох тілесних функціях, як-то циркуляторна та больова системи. Ліганди для d-рецептору можуть тому знайти потенційне застосування як аналгетичні та/або як антигіпертензивні агенти. Ліганди для δ-рецептору, як також показано, виявляють імуномодулятивну активність. Ідентифікація принаймні трьох відмінних родин опіоїдних рецепторів (m, d та k) є зараз добре встановленою та усі три наявні у центральній та периферійній нервових системах багатьох видів, охоплюючи людину. Аналгезію спостерігали у різних тваринних моделях, коли один або більше цих рецепторів є активованими. За небагатьма винятками зараз доступні селективні опіоїдні d-ліганди є пептидними за природою та є непридатними для застосування системними шляхами. Одним приклад непептидного d-агоністу є SNC80 [Bilsky EJ. et al., Journal of Pharmacology та Experimental Therapeutics, 273(1), pp.359-366 (1995)]. Багато сполук d-агоністів, що ідентифіковано у попередньому рівні техніки, мають багато недоліків у тому, що вони мають погану фармакокінетику та не є аналгетиками при застосуванні системними шляхами. Також задокументовано, що багато з цих сполук dагоністів виявляють значну конвульсивну дію при систематичному застосуванні. [Патент США №6187792 Delorme et al.] описує деякі d-агоністи. Однак, є потреба у поліпшених dагоністах. Якщо не визначено інше у цьому описі, номенклатура, застосовувана у цьому описі загалом дотримується прикладів та правил, встановлених у Nomenclature of Organic Chemistry, Sections A, B, C, D, E, F, ma H, Pergamon Press, Oxford, 1979, що наведено як посилання стосовно назв хімічних структур та правил стосовно найменування хімічних структур. Термін "Cm·n" або "група Сm-n", поодинці, чи як префікс, стосується будь-якої групи, що має m-n атомів карбону. Термін "вугле водень", поодинці, чи як суфікс або префікс, стосується будь-якої структури, що містить тільки атоми карбону та гідрогену до 14 атомів карбону. Термін "вуглеводневий радикал" або "гідрокарбіл", поодинці, чи як суфікс або префікс, стосується будь-якої структури, що є результатом видалення одного або більше гідрогенів від вуглеводню. 16 С 3-6-циклоалкіл та, як варіант, С3-6-циклоалкіл-С 1-3-алкіл. Термін "алкіл", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу з лінійним та розгалуженим ланцюгом, що містить приблизно 112 атомів карбону. Термін "алкілен", поодинці, чи як суфікс або префікс, стосується двовалентного вуглеводневого радикалу з лінійним та розгалуженим ланцюгом, що містить приблизно 112 атомів карбону, котрі зв'язують дві структури разом. Термін "алкеніл", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу з лінійним та розгалуженим ланцюгом, що має принаймні один подвійний зв'язок карбон-карбон та містить принаймні приблизно 2-12 атомів карбону. Термін "алкініл", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу з лінійним та розгалуженим ланцюгом, що має принаймні один потрійний зв'язок карбон-карбон та містить принаймні приблизно 2-12 атомів карбону. Термін "циклоалкіл,", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу, що має кільце, що містить принаймні приблизно 3-12 атомів карбону. Термін "циклоалкеніл", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу, що має кільце, що має принаймні один подвійний зв'язок карбон-карбон та містить принаймні приблизно 3-12 атомів карбону. Термін "циклоалкініл", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу, що має кільце, що має принаймні один потрійний зв'язок карбон-карбон та містить приблизно 7-12 атомів карбону. Термін "арил", поодинці, чи як суфікс або префікс, стосується моновалентного вуглеводневого радикалу, що має одне або більше поліненасичених карбонових кілець, що мають ароматичний характер, (наприклад, 4n+2 делокалізованих електронів) та містять приблизно 5-14 атомів карбону. Термін "арилен", поодинці, чи як суфікс або префікс, стосується двовалентного вуглеводневого радикалу, що має одне або більше поліненасичених карбонових кілець, що мають ароматичний характер, (наприклад, 4n+2 делокалізованих електронів) та містять приблизно 5-14 атомів карбону, котрі зв'язують дві структури разом. Термін "гетероцикл", поодинці, чи як суфікс або префікс, стосується кільце-вмісної структури або молекули, що мають один або більше багатовалентних гетероатомів, незалежно вибраних з Ν, Ο, Ρ та S, як частину кільцевої структури, що містить принаймні приблизно 3-20 17 82091 18 атомів у кільцях. Гетероцикл може бути насиченим Прикладами шести-членних кільцевих або ненасиченим, містити один або більше гетероарилів є піридил, піразиніл, піримідиніл, подвійних зв'язків, та гетероцикл може містити Термін "заміщений», застосовуваний як більше одного кільця, коли гетероцикл містить префікс, стосується структури, молекули або більше одного кільця, кільця можуть бути групи, де одного або більше гідрогенів заміщено конденсованими або неконденсованими. одною або більше С 1-6-вуглеводневих гр уп, або Конденсовані кільця звичайно мають принаймні одною або більше хімічних груп, що містять один два кільця, що мають два спільні атоми. або більше гетероатомів, вибраних з N, О, S, F, СІ, Гетероцикл може мати ароматичний характер або Br, І, та Р. Приклади хімічних гр уп, що містять один не мати ароматичний характер. або більше гетероатомів охоплюють -NO2; -OR. Термін "гетероароматичний", поодинці, чи як СІ, -Br, -І, -F, -CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, суфікс або префікс, стосується кільце-вмісної NHR, -NR2, -SR, -SO3H, -SO 2R, -S(=O)R, -CN, -OH, структури або молекули, що мають один або C(=O)OR, -C(=O)NR 2, -NRC(=O)R, оксо (=O), іміно більше багатовалентних гетероатомів, незалежно (=NR), тіо (=S), та оксиміно (=N-OR), де кожний "R" вибраних з Ν, Ο, Ρ та S, як частину кільцевої - С1-6-гідрокарбіл, наприклад, заміщений феніл структури, що містить принаймні приблизно 3-20 може стосуватися нітрофенілу, метоксифенілу, атомів у кільцях, де кільце-вмісна структура або хлорфенілу, амінофенілу, то що, де нітро, метокси, молекула має ароматичний характер (наприклад, хлор, та аміногрупи можуть заміщува ти будь-який 4n+2 делокалізованих електронів). придатний гідроген на фенільному кільці. Термін "гетероциклічна група" "гетероциклічна Термін "заміщений», застосовуваний як суфікс частина," "гетероциклічний" або "гетероцикло", стосовно першої структури, молекули або групи, поодинці, чи як суфікс або префікс, стосується супроводжуваний одною або більше назв хімічних радикалу, похідного від гетероциклу видаленням з груп, стосується другої структури, молекули або нього одного або більше гідрогенів. групи, котрі є результатом заміщення одного або Термін "гетероцикліл", поодинці, чи як суфікс більше гідрогенів першої структури, молекули або або префікс, стосується моновалентного групи одною або більше названих хімічних гр уп, радикалу, похідного від гетероциклу видаленням з наприклад, "феніл заміщений нітро" стосується нього одного гідрогену. нітрофенілу. Термін "гетероциклілен", поодинці, чи як Гетероцикл охоплює, наприклад, моноциклічні суфікс або префікс, стосується двовалентного гетероцикпи, як-то: азиридин, оксиран, тііран, радикалу, похідного від гетероциклу видаленням з азетидин, оксетан, тіетан, піролідин, піролін, нього двох гідрогенів. котрі зв'язують дві структури імідазолщин, піразолідин, піразолін, діо-ксолан, разом. сульфолан 2,3-дигідрофуран, 2,5-дигідрофуран Термін "гетероарил", поодинці, чи як суфікс тетрагідрофуран, тіофан, піперидин, 1,2,3,6або префікс, стосується гетероциклілів, що мають тетрагідро-піридин, піперазин, морфолін, ароматичний характер. тіоморфолін, піран, тіопіран, 2,3-дигідропіран, Термін "гетероциклоалкіл", поодинці, чи як тетрагідропіран, 1,4-дигідропіридин, 1,4-діоксан, суфікс або префікс, стосується гетероциклілів, що 1,3-діоксан, діоксан, гомопіперидии, 2,3,4,7не мають ароматичного характеру. тетрагідро-1Н-азепін, гомопіперазин, 1,3Термін "гетероарилен", поодинці, чи як суфікс діоксепан, 4,7-дигідро-1,3-діоксепін та або префікс, стосується гетероцикліле-нів, що гексаметилен-оксид. мають ароматичний характер. На додаток, гетероцикли охоплюють Термін "гетероциклоалкілен", поодинці, чи як ароматичні гетероцикли, наприклад, піридин, суфікс або префікс, стосується гетероцикліленів, піразин, піримідин, піридазин, тіофен, фуран, що не мають ароматичного характеру. фуразан, пірол, імідазол, тіазол, оксазол, піразол, Термін "шести-членний», застосовуваний як ізотіазол, ізоксазол, 1,2,3-триазол, тетразол, 1,2,3префікс, стосується груп, що мають кільце, що тіадіазол, 1,2,3-оксадіазол, 1,2,4-триазол, 1,2,4містить шість кільцевих атомів. тіадіазол, 1,2,4-оксадіазол, 1,3,4-триазол, 1,3,4Термін "п'яти-членний», застосовуваний як тіадіазол, та 1,3,4-оксадіазол. префікс, стосується груп, що мають кільце, що На додаток, гетероцикли охоплюють містить п'ять кільцевих атомів. поліциклічні гетероцикли, наприклад, індол, П'яти-членний гетероарил є гетероарилом з індолін, ізоіндолін, хінолін, тетрагідрохінолін, кільцем, що має п'ять кільцевих атомів, де 1, 2 або ізохінолін, тетрагідроізохінолін, 1,4-бензодіоксап. 3 кільцеві атоми незалежно вибрані з Ν, Ο та S. кумарин, дигідрокумарин, бензофуран, 2,3Прикладами п'яти-членних кільцевих дигідробензофуран, ізобензофуран, хромен, гетероарилів є тієніл. фурил, піроліл, імідазоліл, хроман, ізохроман, ксантен, феноксатіін, тіантрен, тіазоліл, оксазоліл, піразоліл, ізотіазоліл, індолізин, ізоіндол, індазол, пурин, фталазин, ізоксазоліл, 1,2,3-триазоліл, тетразоліл, 1,2,3нафтиридин, хіноксалін, хіназолін, цинолін, тіадіазоліл, 1,2,3-оксадіазоліл, 1,2,4-триазоліл, піперидин, фенантридин, перимідин, фенантролін, 1,2,4-тіадіазоліл, 1,2,4-оксадіазоліл, 1,3,4феназин, фенотіазин, феноксазин, 1,2триазоліл, 1,3,4-тіадіазоліл, та 1,3,4- оксадіазоліл. бензізоксазол, бензотіофен, бензоксазол, Шести-членним кільцевим гетероарилом є бензтіазол, бензімідазол, бензтриазол, тіоксантин, гетероарил з кільцем, що має шість кільцевих карбазол, карболін, акридин, піролізидин, та атомів, де 1, 2 або 3 кільцеві атоми незалежно хінолізидин. вибрані з Ν, Ο та S. На додаток до вищеописаних поліциклічних гетероциклів, поліциклічні гетероцикли де 19 82091 20 конденсація кілець між двома або більше кільцями загальної формули -NRR', де R та R' незалежно охоплює більше одного зв'язку, спільного для обох вибрані з гідрогену або вуглеводневого радикалу. кілець та більше двох атомів, спільних для обох Галоген охоплює флуор, хлор, бром та йод. кілець. Приклади таких шунтованих гетероциклів "Галогенований", застосовуваний як префікс охоплюють хінуклідин, діазабіцикло[2,2,1]гептан та групи, означає, що один або більше гідрогенів на 7~оксабіцикло[2,2,1]гептан. групі заміщено одним або більше галогенами. Гетероцикліл охоплює, наприклад, В одному аспекті винахід стосується сполуки моноциклічн гетероцикпіли, як-то: азиридиніл, формули І, її фармацевтично прийнятної солі, її оксираніл, тііраніл, азетидиніл, оксетаніл, тіетаніл, діастереомерів, її енантіомерів та їх сумішей: піролідиніл, піролініл, імідазолідиніл, піразолідиніл, піразолініл, діоксоланіл, сульфоланіл, 2,3-дигідрофураніл, 2,5дигідрофураніл, тетрагідрофураніл, тіофаніл, піперидиніл, 1,2,3,6-тетрагідропіридиніл, піперазиніл, морфолініл, тіоморфолініл, піраніл, тіопіраніл, 2,3-дигідропіраніл, тетрагідропіраніл, 1,4-дигідропіридиніл. 1,4-діоксаніл, 1,3-діоксаніл, діоксаніл, гомопіперидиніл, 2,3,4,7-тетрагідро-1Назериніл, гомопіперазиніл, 1,3-діоксераніл, 4,7дигідро-1,3-діоксериніл, та гексаметилен оксидил. На додаток, гетероцикліл охоплює ароматичні де гетероцикпіли або гетероарил, наприклад, R1 вибрано з групи: гідроген, С1-6-алкіл-Опіридиніл, піразиніл, піримідиніл, піридазиніл, С(=О)-, як варіант, заміщений С1-6-алкіл, як тієніл, фурил, фуразаніл, піроліл, іміда-золіл, варіант, заміщений С3-6-циклоалкіл, як варіант, тіазоліл, оксазоліл, піразоліл, ізотіазоліл, заміщений С6-10-арил, як варіант, заміщений С2-9ізоксазоліл, 1,2,3-триазоліл, тетразоліл, 1,2,3гетероцикліл, як варіант, заміщений С2-9-арил-С 1-3тіадіазоліл, 1,2,3-оксадіазоліл, 1,2,4-триазоліл, алкіл та, як варіант, заміщений С2-9-гетероцикпіл1,2,4-тіадіазоліл, 1,2,4-оксадіазоліл, 1,3,4С1-3-алкіл; триазоліл, 1,3,4-тіадіазоліл та 1,3,4 оксадіазоліл. n дорівнює 0, 1 або 2; m дорівнює 0, 1, або 2; На додаток, гетероцикпіл охоплює поліциклічні R2, R3 та R4 незалежно вибрані з групи: гетероцикпіли (охоплюючи ароматичні або гідроген, як варіант, заміщений С1-6-алкіл, та, як неароматичні), наприклад, індоліл, індолініл, варіант, заміщений С3-6-циклоалкіл; ізоіндолініл, хінолініл, тетрагідрохінолініл, R5 та R6 незалежно вибрані з групи: -R, -NO2, ізохінолініл. тетрагідроізохінолініл 1,4OR, -СІ, -Br, -I, -F, -CF 3, -C(=O)R, -С(=О)ОН, -NH2, бензодіоксаніл, кумариніл, дигідрокумариніл, SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, бензофураніл, 2,3-дигідробензофураніл, OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R, та ізобензофураніл, хроменіл, хроманіл, ізохроманіл, NRC(=O)-OR, де R незалежно представляє ксантеніл, феноксатіініл, тіантреніл, індолізиніл, гідроген або С1-6-алкіл; а ізоіндоліл, індазоліл, пуриніл, фталазиніл, R7 вибрано з групи: -Н, -ОН, як варіант, нафтиридиніл, хіноксалініл, хіназолініл, цинолініл, заміщений С1-6-алкіл, як варіант, заміщений С3-6птериддиніл, фенантридиніл, перимідиніл, циклоалкіл, як варіант, заміщений С6-10-арил, як фенантролініл, феназиніл, фенотіазиніл, варіант, заміщений С2-9-гетероцикліл, як варіант, феноксазиніл, 1,2-бензізоксазоліл, бензотіофеніл, заміщений С6-10-арил-С 1-3-алкіл, як варіант, бензоксазоліл, бензтіазоліл, бензімідазоліл, заміщений С 2-9-гетероцикліл-С 1-6-алкіл, -C(=O)бензтриазоліл, тіоксантиніл, карбазоліл, NR8R9, -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8 , -C(=O)карболініл, акридиніл, піролізидиніл, та R8 та -SO3H, де R8 та R9 незалежно вибрані з хінолізидиніл. групи: -Η, як варіант, заміщений С1-6-алкіл, як На додаток до вищеописаних поліциклічних варіант, заміщений С3-6-циклоалкіл, як варіант, гетероцикпілів гетероцикліл охоплює поліциклічні заміщений С6-10-арил, як варіант, заміщений С2-9гетероцикліли, де конденсація кілець між двома гетероцикліл, як варіант, заміщений С2-9-арил-С 1-3або більше кільцями охоплює більше одного алкіл, та, як варіант, заміщений С 2-9-гетероциклілзв'язку, спільного для обох кілець та більше двох С1-6-алкіл. атомів, спільних для обох кілець. Приклади таких Зокрема, сполуки представленого винаходу є шунтованих гетероциклів охоплюють хінуклідиніл, сполуками формули І, де R1 вибрано з групи: діазабіцикло[2,2,1]гептил; та 7гідроген, С1-6-алкіл-О-С(=О)-, як варіант, оксабіцикло[2,2,1]гептил. заміщений С1-6-алкіл, та, як варіант, заміщений С3Термін "алкокси", поодинці, чи як суфікс або 6-циклоалкіл; префікс, стосується радикалів загальної формули R2 та R3 представляють етил; -O-R, де R вибрано з групи: вуглеводневого R4 вибрано з групи: гідроген та С1-3-алкіл; радикалу. Приклади алкокси охоплюють метокси, R7 вибрано з групи: -Н, -ОН, як варіант, етокси, пропокси, ізопропокси, бутокси, третзаміщений феніл, як варіант, заміщений С3-5бутокси, ізобутокси, циклопропілметокси, алілокси. гетероцикпіл, як варіант, заміщений феніл-С1-3та пропаргілокси. алкіл, як варіант, заміщений С3-5-гетероцикліл-С 1-3Термін "амін" або "аміно", поодинці, чи як алкіл, як варіант, заміщений С 1-6-алкіл, як варіант, суфікс або префікс, стосується радикалів заміщений С3-6-циклоалкіл, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл, -C(=O)-N-R8R9, -C(=O) 21 82091 22 O-R8, -S(=O)-R8, -S(=O) 2-R8, -C(=O)-R8 та -SO3H, де групи: -R, -NO2, -OR, -СІ, -Br, -I, -F, -CF3 , -C(=O)R, R8 та R9 незалежно вибрані з групи: -Η, як варіант, C(=O)OH, -NH 2, -SH, -NHR, -NR2, -SR, -SO3H, заміщений феніл, як варіант, заміщений С3-5SO2R, -S(O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, гетероцикліл, як варіант, заміщений феніл-С1-3NRC(=O)R, та -NRC(=O)-OR, де R незалежно алкіл, як варіант, заміщений С3-6-гетероцикліл-С 1-3представляє гідроген або С1-6-алкіл; а алкіл3, як варіант, заміщений С1-6-алкіл, як варіант, R7 вибрано з групи: Н, -ОН, С1-6-алкіл, С3-6заміщений С3-6-циклоалкіл, як варіант, заміщений циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10С3-6-циклоалкіл-С 1-3-алкіл; арил-С 1-3-алкіл, С2-9-гетероцикліл-С1-3-алкіл, а n та m дорівнюють 0. C(=O)-NR 8R9 -C(=O)-O-R8, -S(=O)-R8, -S(=O)2-R8 , Більш конкретно, сполуки представленого C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані винаходу є сполуками формули І, де з групи: -Н, С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, R1 вибрано з групи: гідроген та С1-6-алкіл-ОС2-9-гетероцикліл, С6-10-арил-С 1-3-алкіл, та С1-6С(=О)-, гетероцикліл-С1-3-алкіл, де вказані С1-3-алкіл, С3-6R2 та R3 представляють етил; циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10R4 вибрано з групи: гідроген та метил; арил-С 1-3-алкіл, та С2-9-гетероцикліл-С 1-3-алкіл, R7 вибрано з групи: -Н, феніл-С1-3-алкіл, С3-6застосовувані у визначенні R7, R8 або R9, як циклоалкіл-С 1-3-алкіл, С3-6-циклоалкіл, феніл, як варіант, заміщені одним або більше замісниками, варіант, заміщений С 1-6-алкіл, -C(=O)-N-R8R9, вибраними з групи: -R, -NO2, -OR, -СІ, -Br, -I, -F, S(=O)2-R8, та -C(=O)-R 8, де R8 та R9 незалежно CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, -NHR, -NR23 вибрані з групи: -Н, феніл-С1-3-алкіл; С3-6SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, циклоалкіл-С 1-3-алкіл, С3-6-циклоалкіл, феніл та як C(=O)NR 2, -NRC(=O)R, та -NRC(=O)-OR, де R варіант, заміщений С1-6-алкіл незалежно представляє гідроген або С1-6-алкіл. а n та m дорівнюють 0. В одному втіленні, сполуки представленого Особливо, сполуки представленого винаходу є винаходу представлені формулою ІА, де R1 сполуками формули І, де вибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С3-6R1 представляє гідроген; циклоалкіл, бензил та С2-5гетероарилметил, де R2 та R3 представляють етил; вказані С1-6-алкіл, С3-6-циклоалкіл, бензил та С 2R4 вибрано з групи: гідроген та метил; 5гетероарилметил, як варіант, заміщені одним або 7 R вибрано з групи: -Н, феніл, бензил або більше замісниками, вибраними з групи: С1-6-алкіл, фенетил, циклогексил, циклогексилме-тил, -C(=O)галогенований С1-6-алкіл, -CF3, С1-6-алкокси, хлор, NH-R8, -S(=O)2-R8, та -C(=O)-R8, де R8 вибрано з флуор, бром, та йод; групи: 2,2,2-трифлуоретил, феніл, бензил або R2 та R3 представляють етил; фенетил, циклогексил та циклогексилметил; а R4 вибрано з групи: гідроген та С1-3-алкіл; n та m дорівнюють 0. R7 вибрано з групи: -Н, -ОН, феніл, С3-5У ще одному аспекті винахід стосується гетероцикліл, феніл-С1-3-алкіл, С3-5-гетероциклілсполуки формули ІА, її фармацевтично прийнятної С1-3-алкіл, С1-6алкіл, С3-7-циклоалкіл, С3-7солі, її діастереомерів, її енантіомерів та їх циклоалкіл-С 1-3-алкіл, -C(=O)-N-R8R9, -C(=O)-O-R8, сумішей: -S(=O)-R8, -S(=O)2-R8 , -C(=O)-R8 та -SO3H, де R8 та R9 незалежно вибрані з групи: -Η, феніл, С3-5гетероцикліл, феніл-С1-3алкіл, С3-5-гетероцикліл-С13-алкіл, С 1-6-алкіл, С 3-7-циклоалкіл, С 3-7-циклоалкілС1-3-алкіл, де вказані феніл, С3-5-гетероцикліл, феніл-С 1-3-алкіл, С3-5-гетероцикліл-С 1-3-алкіл, С1-6алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С 1-3-алкіл, застосовувані у визначенні R7, R8Ta R9, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-6-алкіл, галогенований С1-6алкіл, -CF3, С1-6-алкокси, хлор, флуор, бром, та йод. У ще одному втіленні, сполуки представленого де винаходу представлені формулою ІА, де R1 R1 вибрано з групи: гідроген, С1-6-алкіл-Овибрано з групи: гідроген, С1-6-алкіл-О-С(=О)-, С1-6С(=О)-, С1-6-алкіл, С3-6-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-3-алкіл та С 2-9алкіл, С3-6-циклоалкіл, бензил, тіа-діазолілметил, піридилметил, тієнілметил, фурилметил, гетероциклт-С1-3-алкіл; де вказані С 1-6-алкіл, С3-6імідазолілметил, триазолілметил, піролілметил, циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10тіазолілметил та N-оксидо-піридилметил, де арил-С 1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл, як вказані С1-6-алкіл, С3-6-циклоалкіл, бензил, варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -СІ, -Br, -I, -F, тіадіазолілметил, піридилметил, тієнілметил, фурилметил, імідазолілметил, триазолілметил, CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, -NHR, -NR2, піролілметил, тіазолілметил та N-оксидоSR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(O)OR, піридилметил, як варіант, заміщені одним або C(=O)NR2, -NRC(=O)R, та -NRC(=O)-OR. де R більше замісниками, вибраними з групи: С1-6-алкіл, незалежно представляє гідроген або С1-6-алкіл; R2, R3 та R4 незалежно вибрані з групи: галогенований С1-6-алкіл, -CF3, С1-6-алкокси, хлор, флуор, бром, та йод; гідроген, С1-6-алкіл та С 3-6-циклоалкіл, де вказані R2 та R3 представляють етил; С1-6-алкіл та С 3-6-циклоалкіл, як варіант, заміщені R4 вибрано з групи: гідроген та метил; одним або більше замісниками, вибраними з 23 82091 24 R7 вибрано з групи: -Н, С1-6-алкіл, феніл-С 1-3можливо утворювати відповідну сіль лужного алкіл, С3-7-циклоалкіл-С 1-3-алкіл, С3-6-циклоалкіл, металу (як-то натрій, калій, або літій) або лужнофеніл, С1-6-алкіл, -C(=O)-N-R8R9, -S(=O)2-R8, земельного металу (як-то кальцій) обробкою C(=O)-O-R8, та -C(=O)-R8, де R8 та R9 незалежно сполуки представленого винаходу, що має вибрані з групи: -Н, феніл-С1-3-алкіл, С3-7належно кислотний протон, як-то карбонова циклоалкіл-С 1-3-алкіл, С3-7-циклоалкіл, феніл, та кислота або фенол з одним еквівалентом С1-6-алкіл, де вказані феніл-С 1-3-алкіл, С3-7гідроксиду або алкоксиду лужного металу або циклоалкіл-С 1-3-алкіл, С3-7-циклоалкіл, феніл, С1-6лужно-земельного металу (як-то етоксид або алкіл, застосовувані у визначенні R7, R8 та R9, як метоксид), або належно основний органічний амін варіант, заміщені одним або більше замісниками, (як-то холін або меглумін) у водному середовищі, вибраними з групи: С1-6-алкіл, галогенований С1-6а потім звичайними способами очистки. алкіл, -CF3, С1-6-алкокси, хлор, флуор, бром та В одному втіленні, сполуку формули І або ІА йод. вище можна перетворити у фармацевтично У подальшому втіленні, сполуки прийнятну сіль або сольват, зокрема, кислотнопредставленого винаходу представлені формулою адитивну сіль, як-то гідрохлорид, гідро-бромід, ІА, де R1 вибрано з групи: гідроген, пропіл, бензил, фосфа т, ацетат, фумарат, малеат, тартрат, тіадіазолілметил, піридилметил, тієнілметил, цитрат, метансульфонат чи п-толуолсульфонат. фурилметил, імідазолілметил, триазолілметил, Нові сполуки представленого винаходу є піролілметил, тіазолілметил та N-оксидокорисними у терапії, особливо для лікування піридилметил; різних больових станів, як-то хронічний біль, R2 та R3 представляють етил; невропатичний біль, гострий біль, біль при раку, R4 вибрано з групи: гідроген та метил; біль при ревматоїдному артриті, мігрень, R7 вибрано з групи: -Н, етил, феніл, бензил вісцеральний біль тощо. Цей перелік, однак не є або фенетил, нафтил, флуорфеніл, хлор-феніл, повним. циклопентил, циклогексил, циклогептил, Сполуки винаходу є корисними як циклопентилметил, циклогексилметил, -C(=O)-NHімуномодулятори, особливо для автоімунних R8, -S(=O)2-R8 , -C(=O)-O-R8 , та -C(=O)-R 8, де R8 хвороб, як-то артрит, для пересадки шкіри, вибрано з групи: метил, 2,2,2-трифлуоретил, трансплантації органів та подібних хірургічних феніл, бензил, фенетил, метилфеніл, потреб, для колагенових хвороб, різних алергій, флуорфеніл, бутил, циклогексил та для застосування як антипухлинних агентів та циклогексилметил. анти-вірусних агентів. Слід розуміти, що коли сполуки Сполуки винаходу є корисними у станах представленого винаходу містять один або більше хвороб, де наявні чи залучені у цю парадигму хіральних центрів, сполуки винаходу можуть дегенерація або дисфункція опіоїдних рецепторів. існувати в енантіомерних або діастереомерних Це може прилучати застосування мічених формах та бути виділеними як такі, або як ізотопами сполук винаходу у діагностиці та рацемічна суміш. Представлений винахід охоплює інтраскопії, як-то позитронна еміссійна томографія будь-як можливі енантіомери, діастереомери, (PET). рацемати або їх суміші сполук формули І або ІА. Сполуки винаходу є корисними для лікування Оптично активні форми сполуки винаходу можна І діареї, депресії, тривожності та асоційованих зі або ІА. Оптично активні форми сполуки винаходу стресом розладів, як-то посттравматичні стресможна отримувати, наприклад, хіральним розлади, панічний розлад, розлад з хроматографічним розділенням рацемату, генералізованою тривожністю, соціальні фобії, та синтезом з оптично активних вихідних матеріалів обсесивно-компульсивний розлад, невтримання або асиметричним синтезом описаними далі сечі, передчасна еякуляція, різні психічні способами. захворювання, кашель, набряк легенів, різні Слід також розуміти, що деяк сполуки шлунково-кишкові розлади, наприклад, запор, представленого винаходу можуть існувати як функціональні шлунково-кишкові розлади, як-то геометричні ізомери, наприклад, Ε та Ζ ізомери синдром подразненого кишечнику та алкенів. Представлений винахід охоплює будьфункціональна диспепсія, хвороба Паркінсона та який геометричний ізомер сполук формули І або інші моторні розлади, травма мозку, інсульт, ІА. Слід також розуміти, що представлений винахід кардіозахист після інфаркту міокарду, травма охоплює та утомери сполук формули І або ІА. спини та залежність від ліків, охоплюючи лікування Слід також розуміти, що деякі сполуки від зловживання алкоголем, нікотином, опіоїдними представленого винаходу можуть існувати у та іншими ліками, та для розладів симпатичної сольватованій, наприклад, гідратованій, а також нервової системи, наприклад, гіпертензії. несольватованій формах. Слід також розуміти, що Сполуки винаходу є корисними як аналгетики представлений винахід охоплює усі такі для застосування при загальній анестезії та сольватовані форми сполук формули І або ІА. контрольованій анестезії. Комбінації агентів з Рамками винаходу охоплено також солі сполук відмінними властивостями часто застосовують для представленого винаходу, що можна отримувати досягнення збалансованої дії для підтримки стану стандартними способами, добре відомими у рівні анестезії (наприклад, амнезії, аналгезії, релаксації техніки, наприклад, реакцією достатньо основної м'язів та заспокоєння). Залученими у цю сполуки, наприклад, алкіламіну з придатною комбінацію є інгаляційні анестетики, снодійні, кислотою, наприклад, НСІ або оцтовою кислотою, анксіолітики, нейром'язові блокатори та опіоїди. що дає фізіологічно прийнятний аніон. Також 25 82091 26 Також рамки винаходу о хоплюють У порошках носій є мілко подрібненим застосування будь-якої сполуки формул І або ІА твердим матеріалом у суміші з мілко подрібненою вище, для виробництва медикаменту для сполукою винаходу або активним компонентом. У лікування будь-яких вищезазначених станів. таблетках активний компонент змішують з носієм, Наступним аспектом винаходу є спосіб що має необхідні зв'язувальні властивості, у лікування суб'єкту, який потерпає від будь-яких придатній пропорції та пресують до потрібної вищезазначених станів, згідно з яким до пацієнта, форми та розміру. що потребує такого лікування, застосовують Для отримання композиції супозиторію ефективну кількість сполуки формул І або ІА вище. низькоплавкий віск, як-то суміш гліцеридів жирних Відтак, винахід стосується сполуки формули І кислот та масло какао спершу плавлять та або ІА, або її фармацевтично прийнятної солі або диспергують активний інгредієнт, наприклад, сольвату, що визначено вище, для застосування у перемішуванням. Розплавлену гомогенну суміш у терапії. тоді виливають у форму підхожого розміру та У наступному аспекті представлений винахід дають охолонути та затвердіти. стосується застосування сполуки формули І або Придатними носіями є магній карбонат, магній ІА, або її фармацевтично прийнятної солі або стеарат, тальк, лактоза, цукор, пектин, декстрин, сольвату, що визначено вище, у виробництві крохмаль, трагакант, метилцелюлоза, натрій медикаменту для застосування у терапії. карбоксиметилцелюлоза, низькоплавкий віск, У контексті представленого опису, термін масло какао, тощо. "терапія" також охоплює "профілактику" якщо не Термін композиція також охоплює композицію визначено інше. Термін "терапевтичний" та активного компоненту з капсулювальним "терапевтично" слід розуміти відповідно. Термін матеріалом як носієм, що забезпечує капсулу, у "терапія" у контексті представленого винаходу котрій активний компонент (з іншими носіями чи також охоплює застосування ефективної кількості без них) оточено носієм, котрий відтак є в асоціації сполуки представленого винаходу для з ним. Подібно, є залученими саше. пом'якшення вже існуючого стану хвороби, Таблетки, порошки, саше та капсули можна гострого або хронічного чи рекурентного стану. Це застосовувати як тверді форми дозування, визначення також охоплює профілактичні терапії придатні для перорального застосування. для попередження рекурентних станів та Рідкі форм композиції охоплюють розчини, безперервну терапію для хронічних розладів. суспензії та емульсії, наприклад, стерильні водні Сполуки представленого винаходу є або водно-пропіленгліколеві розчини активних корисними у терапії, особливо для терапії різних сполук можуть бути рідкими препаратами, больових станів охоплюючи, але без обмеження: придатними для парентерального застосування. хронічний біль, невропатичний біль, гострий біль, Рідкі композиції можна також формувати у розчині біль у спині, біль при раку та вісцеральний біль. у водно-поліетиленгліколевому розчині. У терапії теплокровної тварини, як-то людини, Водні розчини для перорального застосування сполук винаходу можна застосовувати у формі можна отримувати розчиненням активного звичайної фармацевтичної композиції будь-яким компоненту у воді та додаванням придатних шляхом, охоплюючи пероральний, барвників, ароматизаторів, стабілізаторів та внутрішньом'язовий, підшкірний, місцевий, загусників, за потребою. Водні суспензії для інтраназальний, інтраперитонапьний, перорального застосування можна отримувати інтраторакальний, внутрішньовенний, диспергуванням мілко подрібненого активного епідуральний, інтратекальний, компоненту у воду разом з в'язким матеріалом, якінтрацеребровентрикулярний та ін'єкцією у то природні синтетичні камеді, смоли, суглоби. метилцелюлоза, натрій карбоксиметилцелюлоза В одному втіленні винаходу, шля х та інші суспендувальні агенти, відомі у рівні застосування може бути пероральним, фармацевтичної техніки. внутрішньовенним або внутрішньом'язовим. Залежно від режиму застосування, Дозування залежить від шляху застосування, фармацевтичні композиції переважно містять від суворості хвороби, віку та маси пацієнта та інших 0,05% до 99мас.%, більш переважно від 0,10 до факторів звичайно враховуваних лікарем при 50мас.%, сполуки винаходу. визначенні індивідуального режиму та рівню Терапевтично ефективну кількість для дозування, найприйнятнішого для конкретного здійснення представленого винаходу може пацієнта. визначати застосуванням відомих критеріїв, Для отримання фармацевтичної композиції зі охоплюючи вік, масу та чутливість конкретного сполуки цього винаходу інертні, фармацевтично пацієнта, та інтерпретувати у контексті хвороби, прийнятні носії можуть бути твердими та рідкими. котру лікують або попереджають, фахівець. Тверді форми препаратів охоплюють порошки, Рамками винаходу охоплено застосування таблетки, дисперсивні гранули, капсули, саше та будь-якої сполуки формул І або ІА, що визначено супозиторії. вище, для виробництва медикаменту. Твердий носій може бути одною або більше Також рамки винаходу о хоплюють речовинами, котрі можуть також діяти як застосування будь-якої сполуки формул І або ІА розріджувачі, ароматизатори, солюбілізатори, для виробництва медикаменту для терапії болю. лубриканти, суспендувальні агенти, зв'язуючі, або На додаток запропоновано застосування будьдезинтегратори таблеток; а також як якої сполуки формул І або ІА для виробництва капсулювальний матеріал. медикаменту для терапії різних больових станів 27 82091 28 охоплюючи, але без обмеження: хронічний біль, заміщений С1-3-алкіл, як варіант, заміщений С3-6невропатичний біль, гострий біль, біль у спині, біль циклоалкіл та, як варіант, заміщений С3-6при раку та вісцеральний біль. циклоалкіл-С 1-3-алкіл. Наступним аспектом винаходу є спосіб Зокрема, винахід стосується способу лікування суб'єкту, який потерпає від будь-яких отримання сполуки формули II, що вищеописано, вищезазначених станів, згідно з яким до пацієнта, де R1 - С1-6-алкіл-О-С(=О)-; X1 вибрано з групи: що потребує такої терапії, застосовують ОН, -СІ, -Br та -І; R2 та R3 представляють етил; R4 ефективну кількість сполуки формул І або ІА вище. представляє гідроген; а На додаток, запропоновано фармацевтичну R10 вибрано з групи: феніл, феніл-С1-3-алкіл, композицію, що містить сполуку формули І або І А, С1-3-алкіл С 3-6-циклоалкіл та С 3-6-циклоалкіл-С 1-3або її фармацевтично прийнятну сіль в асоціації з алкіл. фармацевтично прийнятним носієм. У другому втіленні представлений винахід Зокрема, запропоновано фармацевтичну стосується способу отримання сполуки формули композицію, що містить сполуку формули І або І А, IV, що полягає у: або її фармацевтично прийнятну сіль в асоціації з фармацевтично прийнятним носієм для терапії, більш конкретно для терапії болю. Крім того запропоновано фармацевтичну композицію, що містить сполуку формули І або І А або її фармацевтично прийнятну сіль в асоціації з фармацевтично прийнятним носієм застосування у будь-яких з вищезазначених станів. У наступному аспекті представлений винахід стосується способу отримання сполуки формули І або ІА. В одному втіленні, винахід стосується способу реакції сполуки формули V з R12-C(=O)-R13 отримання сполуки формули II, що полягає у: реакції сполуки формули III з X1-C(=O)-R10: де R1 вибрано з групи: С1-6-алкіл-О-С(-О)-3, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл; X1 вибрано з групи: -OR -OR 11, -O-C(=O)-R11 , СІ, -Br та -І, де R11 - С1-6-алкіл; R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R10 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 1-3-алкіл, як варіант, де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, зміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикліл-С1-3-алкіл; R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-3-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R12 та R13 незалежно вибрані з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикпіл, як варіант, заміщений феніл-С 13-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 13-алкіл; як варіант, заміщений С 1-6-алкіл та, як варіант, заміщений С 3-6-циклоалкіл; або R12 та R13 разом утворюють частину С 3-6-циклоалкільного кільця чи С 3-5-гетероциклільного кільця. Зокрема винахід стосується способу отримання сполуки формули IV, де R1 - С1-6-алкіл-О-С(=О)-, R2 та R3 представляють етил; а R12 та R13 незалежно вибрані з групи: -Н, феніл, феніл-С 1-3-алкіл, С1-6-алкіл С 3-6-циклоалкіл та С3-5-гетероцикліл-С1-3-алкіл; або R12 та R13 разом утворюють частину С 3-6-циклоалкільного кільця. 29 82091 У третьому втіленні представлений винахід стосується способу отримання сполуки формули VI, що полягає у: реакції сполуки формули V з R14-NCO: де R1 - С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-3-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С 3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл або, як варіант, заміщений С3-5-гетероцикпіл-С1-3-алкіл; R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R14 вибрано з групи: як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6циклоалкіл та, як варіант, заміщений С3-6циклоалкіл-С 1-3-алкіл. Зокрема, винахід стосується способу отримання сполуки формули VI, що вищеописано, де R1 - С1-6-алкіл-О-С(=О)-; R2 та R3 представляють етил; а R14 вибрано з групи: феніл, феніл-С1-3-алкіл, С1-6-алкіл, С3-6-циклоалкіл та С 3-6-циклоалкіл-С 1-3алкіл. У четвертому втіленні представлений винахід стосується способу отримання сполуки формули VII, що полягає у: 30 де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-5-гетероцикпіл-С1-3-алкіл; R2 та R3 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-3-алкіл та, як варіант, заміщений С3-6-циклоалкіл; X2 вибрано з групи: І, Br та СІ; R15 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 1-3-алкіл, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6циклоалкіл та, як варіант, заміщений С3-6циклоалкіл-С 1-3-алкіл. R16 вибрано з групи: як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5гетероцикліл, як варіант, заміщений С3-5гетероцикліл-С1-6-алкіл, як варіант, заміщений С1-6алкіл, як варіант, заміщений С 3-6-циклоалкіл та, як варіант, заміщений С3-6-циклоалкіл-С 1-3-алкіл. Зокрема, винахід стосується способу отримання сполуки формули VII, що вищеописано, де R1 - С1-6-алкіл-О-С(=О)-; X2 вибрано з групи: -СІ, -Br та -І; R2 та R3 представляють етил; R15 вибрано з групи: гідроген та метил; а R16 вибрано з групи: феніл, феніл-С1-3-алкіл, С1-3-алкіл, С3-6-циклоалкіл та С 3-6-циклоалкіл-С 1-3алкіл. У п'ятому втіленні представлений винахід стосується способу отримання сполуки формули IX, що полягає у: реакції сполуки формули III з X3 -S(=O)2-R17: реакції сполуки формули VIII з R16-X2: 31 82091 де R1 вибрано з групи: С1-6-алкіл-О-С(=О)-, як варіант, заміщений С1-6-алкіл, як варіант, заміщений С3-6-циклоалкіл, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл та, як варіант, заміщений С3-6-гетероцикліл-С1-3-алкіл; X3 вибрано з групи: -ОН, -OR11, -СІ, -Br та -І, де 11 R - С1-6-алкіл; R2, R3 та R4 незалежно вибрані з групи: гідроген, як варіант, заміщений С1-6-алкіл та, як варіант, заміщений С3-6-циклоалкіл; а R17 вибрано з групи: -Н, як варіант, заміщений феніл, як варіант, заміщений С3-5-гетероцикліл, як варіант, заміщений феніл-С 1-3-алкіл, як варіант, заміщений С 3-5-гетероцикліл-С 1-3-алкіл, як варіант, заміщений С1-3-алкіл, як варіант, заміщений С3-6циклоалкіл та, як варіант, заміщений С3-6циклоалкіл-С 1-3-алкіл. Зокрема, винахід стосується способу отримання сполуки формули IX, що вищеописано, де R1 - С1-3-алкіл-О-С(=О)-; X3 вибрано з групи: -СІ, -Br та -І; R2 та R3 представляють етил; R4 представляє гідроген; R17 вибрано з групи: феніл, феніл-С1-3-алкіл, як варіант, заміщений С 1-3-алкіл, С3-6-циклоалкіл та С3-6-циклоалкіл-С 1-3-алкіл. У ще одному втіленні, представлений винахід стосується способу отримання сполуки формули ІІА, що полягає у: реакції сполук формули ІІІА з RS-CH2-X або R5CHO: де X - галоген; 32 R7 вибрано з групи: -C(=O)-O-R8, -S(=O)-R8, S(=O)2-R8 та -C(=O)-R 8, де R8 вибрано з групи: С1-6алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-6-алкіл та С 2-9гетероцикліл-С1-6-алкіл, де вказані С1-6-алкіл, С3-8циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10арил-С 1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -СІ, -Br, -I, -F, CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, -NHR, -NR2, SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, C(=O)NR 2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а R5 вибрано з групи: С6-10-арил та С 2гетероарил, де вказані С 6-10-арил та С25 5гетероарил, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, OR, -СІ, -Br, -I, -F, -CF 3, -C(=O)R, -C(=O)OH, -NH 2, SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. У ще одному втіленні, представлений винахід стосується способу отримання сполуки формули llА, що полягає у: 7 R: реакції сполуки формули IVA з R7-X або R7-O де X - галоген; R7 вибрано з групи: -C(=O)-O-R8 та -C(=O)-R8, де R8 вибрано з групи: С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10-арил-С 1-6-алкіл та С2-9-гетероцикліл-С1-6-алкіл, де вказані С 1-6алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9гетероцикпіл, С6-10-арил-С 1-3-алкіл та С 2-9гетероцикліл-С1-6-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -СІ, -Br, -I, -F, -CF3 , -C(=O)R, C(=O)OH, -NH 2, -SH, -NHR, -NR2, -SR, -SO3H, SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, -C(=O)NR 2, NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а R5 вибрано з групи: С6-10-арил та С 2де вказані С 6-10-арил та С25гетероарил, 5гетероарил, як варіант, заміщені одним або 33 82091 більше замісниками, вибраними з групи: -R, -NO2, OR, -СІ, -Br, -І, -F, -CF3, -C(=O)R5 -C(=O)OH, -NH 2, SH, -NHR, -NR2, -SR, -SO 3H, -SO2R, -S(=O)R5 -CN, OH, -C(=O)OR, -C(=O)NR 2, -NКC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. У подальшому втіленні, представлений винахід стосується способу отримання сполуки формули VA. що полягає у відновленні сполуки формули VIA, де R1 вибрано з групи: гідроген, С1-6-алкіл-ОС(=О)-, С1-6-алкіл, С3-8-циклоалкіл, С6-10-арил, С2-9гетероцикліл, С6-10-арил-С 1-3-алкіл та С 2-9гетероцикліл-С1-3-алкіл; де вказані С1-6-алкіл, С3-8циклоалкіл, С6-10-арил, С2-9-гетероцикліл, С6-10арил-С 1-3-алкіл та С2-9-гетероцикліл-С1-3-алкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, -OR, -СІ, -Br, -І, -F, CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, -NHR, -NR2, SR, -SO3H, -SO2R, -S(=O)R, -CN, -OH, -C(=O)OR, C(=O)NR2, -NRC(=O)R та -NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл; а R2 та R3 незалежно вибрані з групи: гідроген, С1-6-алкіл та С 3-6-циклоалкіл, де вказані С 1-6-алкіл та С3-6-циклоалкіл, як варіант, заміщені одним або більше замісниками, вибраними з групи: -R, -NO2, OR, -СІ, -Br, -I, -F, -CF 3, -C(=O)R, -C(=O)OH, -NH 2, SH, -NHR, -NR2, -SR, -SO3H, -SO2R, -S(=O)R, -CN, OH, -C(=O)OR, -C(=O)NR 2, -NRC(=O)R та NRC(=O)-OR, де R незалежно представляє гідроген або С1-6-алкіл. Зокрема, сполуки представленого винаходу та інтермедіати, застосовувані для їх отримання, можна отримувати шляхами синтезу у схемах 118. 34 35 82091 36 37 82091 Біологічна оцінка Сполуки винаходу виявлені як активні по відношенню до d-рецепторів теплокровної тварини, наприклад, людини. Зокрема сполуки винаходу виявлені як ефективні ліганди dрецептору. In vitro дослідження, нижче, демонструють ці несподівані активності, особливо з точки зору на потужність та ефективність агоністів, як продемонстровано у функціональному дослідженні мозку щурів та/або функціональному дослідженні d-рецептору людини. Ця особливість може стосуватися in vivo активність та може не корелювати лінійно зі спорідненістю до зв'язування. У цих in vitro дослідженнях сполуки тестують на їх активність по відношенню до δрецепторів та отримують ІК50 для визначення селективної активності конкретної сполуки по відношенню до d-рецепторів. У сучасному контексті ІК50 звичайно стосується концентрації сполуки, при котрій спостерігають 50% заміщення стандартного радіоактивного ліганду d-рецептору. Активності сполук по відношенню до рецепторів k та μ також вимірюють у подібному дослідженні. 38 Модель in vitro Культура клітин Клітини 293 S людини, що експресують клоновані рецептори k, d та m людини та є резистентними до неоміцину, вирощують у суспензії при 37°С та 5% СО2 у струшуваних колбах, що містять позбавлений кальцію DMEM10% FBS, 5% BCS, 0,1% Plutonic F-68 та 600мкг/мл генетицину. Мозки щурів зважують та промивають у льодяному PBS (що містить 2,5мМ ЕДТА, рН 7,4). Мозки гомогенізують політроном протягом 30с (щури) у льодяному лізисному буфері (50мМ Трис, рН 7,0, 2,5мМ ЕДТА, з фенілметилсульфонілфлуориді, доданому безпосередньо перед застосуванням до 0,5МмМ від 0,5Μ ви хідного розчину у суміші ДМСО:е танол). Отримання мембран Клітини гранулюють та ресуспендують у лізисному буфері (50мМ Трис, рН 7,0, 2,5мМ ЕДТА, з PMSF, доданому безпосередньо перед застосуванням до 0,1мМ від 0,1Μ вихідного розчину у е танол), інкубують на льоді протягом 15хвил, тоді гомогенізують політроном протягом 30с Суспензію центрифугують при 1000g (макс) протягом 10хвил при 4°С. Надосадковий шар зберігають на льоді та гранули ресуспендують та центрифугують як перед тим. Надосадкові шари від обох центрифугувань поєднують та центрифугують при 46000г (макс) протягом 30хвил. Гранули ресуспендують у холодному буфері Трис (50мМ Трис/СІ, рН 7,0) та центрифугують знов. Кінцеві гранули ресуспендують у мембранному буфері ( 50мМ Трис, 0,32Μ сахароза, рН 7,0). Аліквоти (1мл) у поліпропіленових туба х заморожують у сухому льоді/етанолі та зберігають при -70°С до застосування. Концентрації білку визначають модифікованим дослідженням Лаурі з натрій додецилсульфатом. Дослідження зв'язування Мембрани розморожують при 37°С, охолоджують на льоді, пропускають 3 рази через голку 25 розміру та розбавляють зв'язувальним буфером (50мМ Трис, 3мМ MgCI2 , 1мг/мл BSA (Sigma A-7888), рН 7,4, і зберігають при 4°С після фільтрування через 0,22м фільтр і додають 5мкг/мл апротиніну, 10мкМ бестатину, 10мкМ ліпротину А, без DTT). Аліквоти по 100мкл додають до охолоджених льодом 12x75мм поліпропіленових туб, що містять 100мкл прийнятного радіоліганду та 100мкл тест-сполуки при різних концентраціях. Загальне (ТВ) та неспецифічне (NS) зв'язування визначають у відсутності та присутності 10мкМ налоксону відповідно. Туби перемішують та інкубують при 25°С протягом 60-75хвил, після чого вміст швидко вакуум-фільтр ують та промивають приблизно 12мл/туб охолодженого льодом промивального буферу (50мМ Трис, рН 7,0, 3мМ MgCI2) через фільтри GF/B (Whatman), попередньо просочені протягом принаймні 2 годин у 0,1% поліетиленіміні. Радіоактивність на фільтрах вимірюють бета-лічильником після просочення фільтрів протягом принаймні 12 годин у 39 82091 40 мініколбах, що містять 6-7мл сцинтиляційної 108, відповідно. ІК50 по відношенню до рецептори рідини. Якщо дослідження проводять у 96людини k та m для сполуки винаходу є звичайно у місцевих планшетах з глибокими комірками, межах 1317нМ-9739нМ та 261нМ-9774нМ, фільтрування проводять через 96-місцеві відповідно. просочені поліетиленіміном уніфільтри, котрі Експерименти з насичення рецепторів промивають 3x1мл промивального буферу та Значення Кd радіоліганду визначають сушать у шафі при 55°С протягом 2 годин. Фільтр проведенням дослідження зв'язування на планшети підраховують у TopCount (Packard) після мембранах клітин з прийнятними радіолігандами додавання 50мкл сцинтиляційної рідини MS-20 на при концентрації у межах від 0,2 до 5 разів комірку. оціненого Кd (до 10 разів, якщо кількості потрібного Функціональне дослідження радіоліганду є реальними). Специфічне Агоністичну активність сполук вимірюють зв'язування радіоліганду виражають як пмоль/мг визначенням ступеню до котрого комплекс білку мембран. Значення Кd та Вмакс від сполука-рецептор активує зв'язування GTP до Gіндивідуальних експериментів отримували білків, до котрих рецептори приєднуються. У нелінійною підгонкою специфічно зв'язаного (В) 35 дослідженні зв'язування GTP GTP[g] S проти нМ вільного (F) радіоліганду від індивідуалу поєднували з тест-сполуками та мембранами від згідно з одно-сайтовою моделлю. клітин HEK-293S, що експресують клоновані Визначення механоалодинії тестуванням вон людини опіоїдні рецептори або від Фрея гомогенізованого мозку щура та миші. Агоністи Тестування проводять між 08:00 та 16:00 стимулюють зв'язування GTP[g]35S у цих годинами способом, описаним [Chaplan et al. мембранах. Значення Емакс та Емакс сполук (1994)]. Щурів розміщають у клітках з плексигласу, визначають за кривими доза-відгук. Праві зсуви дротяне дно котрих дозволяє доступ до лап, та кривої доза-відгук дельта-антагоністом дають звикнути протягом 10-15хвил. Тестованою налтриндолом проводять для перевірки, чи зоною є середина підошви лівої задньої лапи, опосередкована агоністична активність дельтауникаючи менш чутливих подушечок лапи. Лапи рецепторами. Значення Емакс визначали відносно торкаються серією з 8 волосинок вон Фрея з стандартного d-агоністу SNC80, тобто, ви ще 100% логарифмічно зростаючою жорсткістю (0,41, 0,69, означає сполуку, що має кращу ефективність, ніж 1,20, 2,04, 3,63, 5,50, 8,51 та 15,14г; Stoelting, 111, SNC80. USA). Волосинку вон Фрея просувають знизу Процедура для мозку щурів GTP підлоги перпендикулярно поверхні підошви з Мембрани мозку щурів розморожують при достатньою силою для виклику слабкого вигину 37°С, пропускають 3 рази через голку 25 розміру із лап та тримають протягом приблизно 6-8с. затупленим кінцем та розбавляють GTPgS Позитивний відгук відмічають, якщо лапа різко зв'язуючим (50мМ Hepes, 20мМ NaOH, 100мМ відсмикується. Здригування негайно після NaCI, 1мМ ЕДТА, 5мМ MgCI 2, рН 7,4, Додають видалення волосинки також вважають позитивним свіжі: 1мМ DTT, 0,1% BSA). Кінцево додають відгуком. Уставання вважають сумнівним відгуком і 120мкМ GDP розбавлень мембран. Значення ЕК50 у таких випадках стимул повторюють. та Емакс сполук оцінюють за 10-точковими кривими Протокол тестування доза-відгук у 300мкл з прийнятною кількістю білку Тварин тестують на добу 1 після операції для мембран (20мкг на комірку) та 100000обробленої FCA групи. 50% поріг відсмикування визначають, застосовуючи спосіб уверх-униз 130000імп/хвил GTPg35S на комірку (0,11-0,14нМ). Діксона (1980). Тестування починають з волосинки Базове та максимальне стимульоване зв'язування 2,04г у середині серії. Стимули завжди визначають у відсутності та присутності 3мкМ застосовують послідовно, підвищуючи або SNC-80. Дані аналізу понижуючи. При відсутності відсмикування лапи як відгук у на спочатку вибрану волосинку Специфічне зв'язування (SB) розраховували застосовують сильніший стимул; у випадку як TB-NS та SB у присутності різних тест-сполук і відсмикування лапи, наступний слабший стимул. виражали як процент контролю SB. Значення lК50 Розрахунок оптимального порогу цим способом та коефіцієнту Хілла (nН) для лігандів у заміщенні специфічно зв'язаного радіоліганду розраховували потребує 6 відгуків у безпосередній близькості до 50% порогу та підрахунок цих 6 відгуки починають, логіт-трансформацією або програмами підгонки коли відбувається перша зміна відгуку, наприклад, кривих, як-то Ligand, GraphPad Prism, SigmaPlot, поріг є вперше перейденим. У випадках, де пороги або ReceptorFit. Значення Кі розраховували за знаходяться за межами стимулів, відповідно рівнянням Ченга-Пруссофа. Значення ІК50±ДІ., Кі та nH представлено для лігандів, тестованих у позначають значення 15,14 (нормальна чутливість) або 0,41 (максимально алодинічно). принаймні трьох кривих заміщення. Результативні позитивні та негативні відгуки На основі вищенаведеного тестування ми груп ують, застосовуючи умовні позначення, знайшли, що сполуки представленого винаходу є X=нема відсмикування: О=відсмикування та 50% активними по відношенню до d-рецептору людини. поріг відсмикування інтерполюють за формулою: Звичайно, lК50 по відношенню до d-рецептору 50%г поріг=10(Xf+kd)/10000 людини для більшості сполук представленого де Xf=значення останньої застосовуваної винаходу є у межах 0,48нМ-17,9нМ. ЕК50 та %Емакс волосинки вон Фрея (логарифмічні одиниці); по відношенню до d-рецептору людини для цих k=табличне значення [від Chaplan et al. (1994)] для сполук є звичайно у межах 18,6нМ-1724нМ та 65позитивних/негативних відгуків; а d значення = 41 82091 42 різниці між стимулами (логарифмічні одиниці). Тут Для симптомів функціональних шлунковокишкових розладів, ефективність може бути d=0,224. Пороги вон Фрея виражають як процент встановленою у дослідженні, описаним [Coutinho SV et al, у American Journal of Physiology максимально можливої дії (% МРЕ), згідно з Gastrointestinal & Liver Physiology. 282(2):G3 07[Chaplan et al. 1994]. Наступне рівняння 16,2002 Feb], у щурів. застосовували для розрахунку %МРЕ: Додаткові протоколи тестування in vivo Суб'єкти та розміщення поріг при лікуванні (г ) - поріг алодинії (г )Х 100 % МРЕ = Необроблених самців щурів Sprague Dawley поріг контролю (г ) - поріг алодинії (г ) (175-200г) розбивають у гр упи по 5 у кімнаті з регульованою температурою (22°С, 40-70% Застосування тест-речовини вологості, 12 годин світло/темрява). Експерименти Щурів ін'єктують (підшкірно, проводять протягом світлової фази циклу. інтраперитонально, внутрішньовенно або Тварини мають їжу та воду досхочу та їх вбивають перорально) тест-речовиною перед тестуванням негайно після отримання даних. вон Фрея, час між застосуванням тест-сполуки та Зразок тестом вон Фрея варіює залежно від природи тестТестування сполуки (ліків) охоплює групи сполуки. щурів, що не отримують будь-якого лікування та Тест на корчення інших, яких обробляють ліпополісахаридом Е. coli Оцтова кислота призводить до абдомінальних (LPS). Для LPS-експерименту, 4 гр упи ін'єктують скорочень при інтраперитональному застосуванні LPS, 1 з 4 груп тоді обробляють носієм, а інші три у мишей, що витягують їх тіло у типовій картині, групи ін'єктують ліками та їх носієм. Другий ряд коли застосовують аналгетичні ліки, цей описаний експериментів проводять, застосовуючи п'ять груп рух спостерігають рідше та ліки вибирають як щурів; усі з котрих не отримують обробки LPS. потенційно гарні. Необроблена група не отримує сполук (ліків) або Повний та типовий рефлекс корчення носія; інші 4 групи обробляють носієм з ліками або вважають наявним тільки коли представлено такі без них. Це проводять для визначення анксіоліелементи: тварина не рухається; нижча частина тичної або седативної дії ліків, котра може сприяти спини слабко пригнічена; підошви обох лап зменшенню USV. доступні для спостереження. У цьому дослідженні Застосування LPS сполуки представленого винаходу демонструють Щурам давали звикнути в експериментальній значне інгібування відгуків корчення після лабораторії протягом 15-20хвил перед лікуванням. перорального застосування 1-100мкмоль/кг. Запалення індукують застосуванням LPS (і) Отримання розчинів (ендотоксин грам-негативного серотипу бактерій Оцтова кислота (АсОН): 120мкл оцтової Е. coli 0111:B4, Sigma). LPS (2,4мкг) ін'єктують кислоти додають до 19,83мл дистильованої води інтрацеребровентрикулярно), у об'ємі 10мкл, до кінцевого об'єму 20мл з кінцевою застосовуючи стандартну стереотаксичну хір ургію концентрацією 0,6% АсОН. Розчин тоді змішують під анестезією ізофлураном. Шкіру між вухами та застосовують для ін'єкцій. рострально зсувають та роблять поздовжній розріз Сполуки (ліки): Кожну сполуку отримують та приблизно 1см для відкриття поверхні черепа. розчиняють у найпридатнішому носії Ділянку проколювання визначають координатами: стандартними способами. 0,8мм позаду тім'я, 1,5мм ліворуч стосовно (іі) Застосування розчинів ламбди (сагітальний шов) та 5мм нижче поверхні Сполуку (ліки) застосовують перорально, черепа (вертикально) у бічному шлуночку. LPS інтраперитонально, підшкірно або ін'єктують через стерильну голку з нержавіючої внутрішньовенно при 10мл/кг (приймаючи до уваги сталі (26-G 3/8) 5мм довжиною, приєднаною до середню масу тіла мишей) за 20, 30 або 40 хвилин шприца Гамільтона на 100-мкл поліетиленовою (згідно з класом сполуки та її характеристиками) трубкою (РЕ20; 10-15см). Стопор 4мм, зроблений з перед тестуванням, коли сполуку доставляють розрізаної голки (20-5 G), розміщають зверху та центрально: інтравентрикулярно або ізолюють від голки 26-G силіконовим клеєм для інтратекально, застосовують об'єм 5мкл. утворення потрібної глибини 5мм. АсОН застосовують інтраперитонально у дво х Після ін'єкції LPS голку залишають протягом ділянках при 10мл/кг (приймаючи до уваги додаткових 10с для дифузії сполуки, тоді середню масу тіла мишей) негайно перед видаляють. Розріз закривають та щура тестуванням, повертають у його клітку та дають спочити (ііі) Тестування протягом мінімум 3,5 годин перед тестуванням. Тварину (мишу) спостерігають протягом 20 Експериментальна установка для стимуляції хвилин та число випадків (рефлекс корчення) ударом повітря занотовують та компілюють в кінці експерименту. Щурів залишають в експериментальній Мишей тримають в індивідуальних клітках лабораторії після ін'єкції LPS та застосування "коробка для взуття" з контактною укладкою. сполуки (ліків). У час тестування усі х щурів Загалом одночасно звичайно спостерігають 4 видаляють та розміщають поза лабораторією. мишей: один контроль та три дози ліків. Одного щура передають у тест-лабораторію та Для симптомів тривожності та подібних розміщають у прозорому боксі (9x9x18см) котрий є тривожності, ефективність встановлено у тоді розміщають у шумопоглинальному конфліктному тесті у щурів вентильованому боксі для вимірювання 43 82091 44 62(ш)х35(г)х46(в)см (BRS/LVE, Div. Tech-Serv Inc). 12 годин, реакційну суміш гасили водою (300мл) та Удари повітря через вихідне сопло повітря 0,32см, екстрагували етилацетатом (3x300мл). Поєднані регулюють системою (AirStim, San Diego органічні фази сушили безводним магній Intruments), здатною спрямовувати удари повітря сульфатом та випарювали, отримуючи сирий фіксованої тривалості (0,2с) та фіксованої продукт, котрий очищали флеш-хроматографією, інтенсивності з частотою 1 удар за 10с Максимум отримуючи інтермедіат 2 як білий твердий продукт застосовують 10 ударів, або доки не подається (5,64г, 35%). голос, котрий іде першим. Перший удар повітря ІЧС (NaCI) 3424, 2974, 2855, 1718, 1688, 1606. означає початок реєстрації. 1427, 1362, 1276см-1; 1 Експериментальна установка для H-ЯМР (CDCI3) d 1,44 (s, 9Н), 2,31 (t, J=5,5Гц, ультразвукової реєстрації 2Н), 2,42 (t, J=5,5Гц, 2Н), 3,37 (t, J=5,5Гц, 2Н), 3,48 Голосіння реєструють протягом 10 хвилин, (t, J=5,5Гц, 2Н), 3,37 (β, 3H, OСН3), 6 ,33 (β, 1Н, застосовуючи мікрофони (G.R.A.S, Vedbaek, СН), 7,20 (d J=6,7Гц, 2Н, Ar-Н), 7,94(d, 7=6,7Гц, 2H, Denmark) розміщають збоку кожного боксу та Ar-Н); 13 регулюють програмою LMS (LMS CAD A-X 3,5В, С ЯМР (CDCI3) d 28,3, 29,2 36,19, 51,9, 123,7, Data Acquisition Monitor, Troy, Michigan). Частоти 127,8, 128,7, 129,4, 140,5, 142,1, 154,6, 166,8. між 0 та 32000Гц реєструють, зберігають та Інтермедіат 3: 4-Бром-4-[бром-(4аналізують тою ж програмою (LMS CAD A-X 3,5В, метоксикарбоніл-феніл)-метил]-піперидин-1Time Data Processing Monitor та UPA (User карбонової кислоти трет-бутиловий естер Programming та Analysis)). У суміш інтермедіату 2 (5,2г, 16ммоль) та калій Сполуки (ліки) карбонат (1,0г) у сухому дихлорметані (200мл) Усі сполуки (ліки) доводять до рН між 6,5 та додавали розчин брому (2,9г, 18ммоль) у 30мл 7,5 та застосовують у об'ємі 4 мл/кг. Після дихлорметану при 0°С. Через 1,5 годин при застосування сполуки (ліків), тварин повертають в кімнатній температурі розчин після фільтрування їх клітки до часу тестування. калій карбонату загусн ув. Залишок тоді розчиняли Аналіз в етилацетаті (200мл), промивали водою (200мл), Реєстрацію пропускають через серію 0,5Μ НСІ (200мл) та розсолом (200мл) та сушили статистичних та Фур'є аналізів до фільтру (між 20безводним магній сульфатом. Видалення 24к Гц) та для розрахунку потрібних параметрів. розчинників дало сирий продукт, котрий Дані виражають як значення ±ДІ. Статистичну перекристалізовували з метанолу, отримуючи значимість оцінюють, застосовуючи для інтермедіат 3 як білий твердий продукт (6,07г, порівняння між необробленими та LPS78%). обробленими щурами Т-тест та одношляхову ІЧС (NaCI) 3425, 2969, 1725,1669, 1426, 1365, ANOVA, а потім тест багатократного порівняння 1279, 1243см -1; 1 Дуннета (після цього), стосовно ефективності ліків. Н-ЯМР (CDCI3) d 1,28 (s, 9H), 1,75 (m, 1H), Різницю між групами вважають значущою з 1,90 (m, 1H), 2,1 (m, 2H), 3,08 (br, 2H), 3,90 (s, 3H, мінімальним р-значенням менше 0,05. ОСН3), 4,08 (br, 3H), 7,57 (d, J=8,4Гц, 2Н, Ar-H) 7,98 Експерименти повторюють мінімум два рази. (d, J=8,4Гц, 2Н, Ar-H); 13 Приклади С-ЯМР(CDCI3) d 28,3, 36,6, 38,3, 40,3, 52,1, Винахід детальніше описано наступними 63,2, 72,9, 129,0, 130,3, 130,4, 141,9, 154,4, 166,3. прикладами, котрі описують способи, де сполуки Інтермедіат 4: 4-[бром-(4-карбоксифеніл)представленого винаходу можна отримувати, метилен]-піперидин-1-карбонової кислоти треточищати, аналізувати та біологічно тестувати, і бутиловий естер котрі не обмежують винахід. Розчин інтермедіату 3 (5,4г 11ммоль) у Інтермедіат 1 метанолі (300мл) та 2,0Μ NaOH (100мл) гріли при Суміш 4-(бромметил)бензойної кислоти 40°С протягом 3 годин. Твердий продукт збирали метилового естеру (11,2г, 49ммоль) та трифільтруванням та сушили протягом ночі під метилфосфіту (25мл) гріли при кипінні під вакуумом. Суху сіль розчиняли у 40% зворотним холодильником під азотом протягом 5 ацетонітрил/води та доводили до рН 2, годин. Надлишок триметилфосфіту видаляли застосовуючи концентровану НСІ. Інтермедіат 4 співдистиляцією з толуолом, отримуючи (3,8г, 87%) виділяли як білий порошок інтермедіат 1 з кількісним виходом. фільтруванням. 1 1 H-ЯМР (CDCI3) d 3,20 (d, 2Н, J=22Гц, СН2), Н ЯМР (CDCI3) d 1,45 (s, 9Н, Ви), 2,22 (dd, 3,68 (d, 3H 10,8Гц, ОСН3), 3,78 (d, 3H, 11,2Гц, J=5,5Гц, 6,1Гц, 2Н), 2,64 (dd, J=5,5Гц, 6,1Гц, 2Н), ОСН3), 3,91 (s, 3H, ОСН3), 7,38 (m, 2H, Ar-Н), 8,00 3,34 (dd, J=5,5Гц, 6,1Гц, 2Н), 3,54 (dd, J=5,5Гц, (d, 2H, J=8Гц, Ar-Н). 6,1Гц, 2Н), 7,35 (d, J=6,7Гц, 2Н, Ar-Н), 8,08 (d, Інтермедіат 2: 4-(4-МетоксикарбонілJ=6,7Гц, 2Н, Ar-Н); 13 бензиліден)-піперидин-1-карбонової кислоти третС ЯМР (CDCI3) d 28,3, 31,5, 34,2, 44,0, 115,3, бутиловий естер 128,7, 129,4, 130,2, 137,7, 145,2, 154,6, 170,3. До розчину інтермедіату 1 у сухому Інтермедіат 5: 4-[бром-(4-діетилкарбамоїлтетрагідрофурані (200мл) додавали краплями літій феніл)-метилен]-піперидин-1-карбонової кислоти діізопропіламід (32,7мл 1,5Μ у гексанах, 49ммоль) трет-бутиловий естер при -78°С. Реакційній суміші тоді давали нагрітися До розчину інтермедіату 4 (1,0г, 2,5ммоль) у до кімнатної температури перед додаванням Nсухому ди хлорметані (10мл) при -20°С додавали трет-бутоксикарбоніл-4-піперидону (9,76г, ізобутилхлорформіат (450мг, 3,3ммоль). Через 49ммоль у 100мл сухого тетрагідрофурану). Через 20хвил при -20°С додавали діетиламін (4мл) та 45 82091 46 реакційній суміші давали нагрітися до кімнатної сушили безводним натрій сульфатом, фільтр ували температури. Через 1,5 годин розчинники та концентрували у вакуумі. Залишок розчиняли у випарювали та залишок розподіляли між дихлорметані (15мл) та додавали трифлуороцтову етилацетатом та водою. Органічну фазу кислоту (2,5мл). Реакційну суміш перемішували промивали розсолом та сушили безводним магній протягом ночі при кімнатній температурі, тоді сульфатом. Видалення розчинників дало сирий концентрували у вакуумі. Залишок очищали продукт, котрий очищали флеш-хроматографією, зворотно-фазовою ВЕРХ (градієнт 10-40% CH3CN отримуючи інтермедіат 5 як білі голки (800мг, у воді з вмістом 0,1% трифлуороцтової кислоти), 73%). отримуючи сполуку І (275мг, 46% виходу) як ІЧС (NaCI) 3051, 2975, 1694, 1633, 1416, 1281, трифлуорацетат. Цей матеріал ліофілізували з 1168, 1115см -1; СН3СN/води, отримуючи безбарвний твердий 1 продукт. Чистота (ВЕРХ); >99%; H-ЯМР (CDCI3) d 1 ,13 (br, 3H, СН3), 1,22 (br, 1 3H, СН3), 1,44 (s, 9H, tВu), 2,22 (t, J=5,5Гц, 2Н), 2,62 Н ЯМР (400МГц, CD3OD) d 1,06 (t J=6,64Гц, (t, J=5,5Гц, 2Н), 3,33 (m, 4Н), 3,55 (m, 4Н), 7,31 (d, 3H), 1,20 (t, J=6,74Гц, 3H), 2,49-2,72 (m, 4H), 3,10J=8,0Гц, 2Н, Ar-Н), 7,36 (d, J=8,0Гц, 2Н, Ar-Н); 3,15 (m, 1H), 3,20-3,31 (m, 4H), 3,31-3,40 (m, 1H), 13 3,43-3,55 (m, 2H), 7,05 (d, J=8,40Гц, 2H), 7,18 (d, С ЯМР (CDCI3) d 12,71, 14,13, 28,3, 31,5, J=8,40Гц, 2H), 7,27-7,31 (m, 1H), 7,37-7,43 (m, 3H), 34,2, 39,1, 43,2, 79,7, 115,9, 126,3, 129,3, 136,8, 7,45 (d, J=8,01Гц, 2H), 7,55 (tt, J =7,42, 1,37Гц, 1H), 137,1, 140,6, 154,6, 170,5. 7,66 (d, J=7,23Гц, 2Η). Виявлено: С, 62,61; Η, 5,92; Інтермедіат 6: 4-[(2-амінофеніл)[4Ν, 6,71. C 30H33N3O 2 x1,2CF3CO2H x1,0Η2O має С, [(діетиламіно)карбоніл]феніл]метилен]-162,52; Η, 5,86; Ν, 6,75 %. піперидинкарбонової кислоти 1,1Сполука 2: N-[2-[[4диметилетиловий естер [(діетиламіно)карбоніл]феніл]-4У суміш інтермедіату 5 (3,0г, 6,65ммоль) та 2піперидиніліденметиліфеніл)бензолацетамід амінофенілборонової кислоти (1,37г, 9,97ммоль) у толуолі (85мл) та етанолі (17мл) додавали 2,0Μ натрій карбонат (13мл). Паладій тетракістрифенілфосфін (774мг, 0,1ммоль) додавали та утворену суміш гріли протягом ночі при 90°С під азотом. Реакційну суміш тоді концентрували у вакуумі та залишок розбавляли розсолом. Водну фазу екстрагували EtOAc (3 х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтрували та концентрували у вакуумі. Сирий продукт очищали флешСпособом для сполуки 1, застосовуючи хроматографією на колонці з силікагелем, елюючи інтермедіат 6 (400мг, 0,36ммоль) та сумішшю 7:3 EtOAc:гексани, отримуючи фенілацетилхлорид (133мг, 0,95ммоль) інтермедіат 6 як світло-коричневий твердий отримували сполуку 2 (381мг, 62% виходу) як продукт (3,14г, кількісний вихід). трифлуорацетат. Цей матеріал ліофілізували з 1 H-ЯМР (400МГц, CDCI3) d 1,12 (br s, 3H), 1,26 СН3СN/води, отримуючи безбарвний твердий (br s, 3H), 1,46 (s, 9H), 2,22 (m, 2H), 2,45 (m, 2H), продукт. Чистота (ВЕРХ): >99%; 1 3,28 (br s, 1H), 3,37 (m, 3H), 3,54 (m, 4H), 3,66 (s, Н ЯМР (400МГц, CD3OD) d 1,09 (t, J=6,74Гц, 2H), 6,69 (dd, J=7,91, 0,88Гц, 1H), 6,73 (td, J=7,42, 3H), 1,22 (t, J=6,93Гц, 3H), 2,34-2,49 (m, 3H), 2,491,17Гц, 1H), 6,95 (dd, J=7,71, 1,46Гц, 1H), 7,09 (td, 2,59 (m, 1H), 2,95-3,04 (m, 1Η), 3,09-3,30 (m, 5H), J=7,62, 1,56Гц, 1H), 7,21 (d, J=8,40Гц, 2H), 7,31 (d, 3,47-3,58 (перекривання d та m, J=5,66Гц, 4H), J=8,40Гц, 2Н). 6,89 (d, J=8,20Гц, 2H), 7,22 (d, J=8,20Гц, 2H), 7,26Сполука 1: 4-[[2-(бензоїламіно)феніл]-47,42 (m, 9Η). Виявлено: С, 63,88: Η, 6,13; Ν, 6,66. піперидиніліденметил]-N,N-діетилбензамід C30H35N3 O2 x1:1CF3CO 2Hx1,0Η2Ο має С, 63,79: Η, 6,14; Ν, 6,72 %. Сполука 3: 4-[[2[(циклогексилкарбоніл)аміно]феніл]-4піперидиніліденметил]-N,N-діетилбензамід До розчину інтермедіату 6 (400мг, 0,86ммоль) у ди хлорметані (15мл) додавали триети-ламін (0,36мл, 2,59ммоль) а потім бензоїлхлорид (133мг, 0,95ммоль). Реакційну суміш перемішували протягом ночі при кімнатній температурі під азотом, розбавляли дихлорме-таном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази Способом для сполуки І, застосовуючи інтермедіат 6 (150мг, 0,32ммоль) та циклогексанкарбонілхлорид (52мг, 0,35ммоль) отримували сполуку 3 (159мг, 83% виходу) як трифлуорацетат. Це матеріал ліофілізували з 47 82091 48 СН3СN/води, отримуючи безбарвний твердий перерозчиняли у дихлорметані (10мл). продукт. Чистота (ВЕРХ): >99%; Трифлуороцтову кислоту (1мл) додавали та 1 реакційну суміш перемішували протягом ночі при Н ЯМР (400МГц, CD3OD) d 1,04-1,24 (m, 6H), кімнатній температурі. Реакційну суміш 1,324-1,39 (m, 4H), 1,46 (dq, J=12,33, 3,03Гц, 1H), концентрували у вакуумі та залишок очищали 1,58-1,91 (m, 5H), 2,22 (tt, J=1,28, 3,47Гц, 1H), 2,43зворотно-фазовою ВЕРХ (градієнт 10-40% CH3CN 2,56 (m, 2H), 2,61 (dt, J=14,84, 5,86Гц, 1H), 2,72 (dt, у воді з вмістом 0,1% трифлуороцтової кислоти), J=15,04, 6,05Гц, 1H), 3,15-3,33 (m, 6H), 3,47-3,55 (m, J=6,83Гц, 2H), 7,19 (d, J=8,40Гц, 2H), 7,26-7,34 отримуючи сполуку 5 (130мг, 67% виходу) як трифлуорацетат. Цей матеріал ліофілізували з (m, 6Η). СН3СN/води, отримуючи безбарвний твердий Виявлено: С, 60,51; Η, 6,33; Ν, 6,27. продукт. Чистота (ВЕРХ): >99%; C30H39N3 O2 x1,6CF3CO 2Hx0,2Η2Ο має С, 60,45; Η, 1 6,26; Ν, 6,37%. H-ЯМР (400МГц, CD3OD) d 0,90-1,06 (m, 2H), Сполука 4: N-[2-[[41,05-1,33 (m, 9H), 1,61-1,80 (m, 6H), 1,97 (dd, [(діетиламіно)карбоніл)феніл)-4J=13,86, 7,23Гц, 1H), 2,13 (dd, J=13,86, 6,64Гц, 1H), піперидиніліденметил]феніл]бензолпропанамід 2,51 (t, J=5,96Гц, 2H), 2,61 (ddd, J=14,84, 6,64, 5,27Гц, 1H), 2,71 (ddd, J=14,84, 6,83, 5,47Гц, 1H), 3,17-3,33 (m, 6H), 3,51 (q, J=6,64Гц, 2H), 7,17 (d, J=8,40Гц, 2H), 7,24-7,37 (m, 6Η). Виявлено: С, 61,10; Η, 6,47; Ν, 6,27. C31H41N3 O2 x1,6CF3CO 2Hx0,1Η2Ο має С, 61,13; Η, 6,42; Ν, 6,25%. Сполука 6: N,N-діетил-4-[[2-[(2фенілетил]аміно]феніл)-4піперидиніліденметил]бензамід Способом для сполуки 1, застосовуючи інтермедіат 6 (150мг, 0,32ммоль) та бензолпропаноїлхлорид (60мг, 0,35ммоль) отримували сполуку 4 (157мг, 79% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи бежевий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,07 (t, J=6,44Гц, 3H), 1,21 (t, J=6,64Гц, 3H), 2,38-2,59 (m, 5H), 2,69 До розчину інтермедіату 6 (300мг, 0,65ммоль) (dt, J=15,04, 5,66Гц, 1H), 2,79-2,94 (m, 2H), 3,18у 1,2-дихлоретані (20мл) додавали 3,31 (m, 6H), 3,50 (br q, J=6,51Гц, 2H), 7,07 (d, фенілацетальдегід (156мг, 1,30ммоль), а потім J=8,20Гц, 2H), 7,15-7,35 (m, 11Η). льодяну оцтову кислоту (0,07мл, 1,30ммоль) та Виявлено: С, 63,05; Η, 5,89; Ν, 6,50. NaBH(OAc)3 (344мг, 1,63ммоль). Реакційну суміш С33Н37N3 О2 x1,4CF3CO 2Hx0,4Η2Ο має С, 63,09; Η, перемішували протягом ночі при кімнатній 5,96; Ν, 6,34%. температурі під азотом. Додавали Сполука 5: 4-[[2трифлуороцтову кислоту (2мл) та реакційну суміш [[циішогексилацетил]аміно]феніл]-4перемішували ще 4 години. Реакційну суміш піперидиніліденметил]-N,N-діетилбензамід розбавляли дихлорметаном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтрували та концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 2045% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 6 До розчину циклогексилоцтової кислоти (74мг, (181мг, 40% виходу) як трифлуорацетат. Цей 0,52ммоль) та HATU (172мг, 0,45ммоль) у матеріал ліофілізували з CH3CN/води, отримуючи диметилформаміді (7мл) додавали бежевий твердий продукт. Чистота (ВЕРХ): >99%; діізопропілетиламін (0,14мл, 0,81ммоль), а потім 1 H-ЯМР (400МГц, CD3OD) d 1,08 (t, J=6,74Гц, інтермедіат 6 (150мг, 0,32ммоль). Реакційну суміш 3H), 1,21 (t J=6,83Гц, 3H), 2,19-2,36 (m, 2H), 2,56 (t, перемішували протягом ночі при кімнатній J=6,05Гц, 2H), 2,84 (t, J=6,64Гц, 2H), 2,96-3,05 (m, температурі під азотом, тоді концентрували у 1H), 3,06-3,14 (m, 1H), 3,13-3,21 (m, 2H), 3,20-3,30 вакуумі. Залишок розчиняли у дихлорметані та (m, 2H), 3,29-3,46 (m, 2H), 3,46-3,56 (m, 2H), 6,63 промивали 1Η NaOH (1x). Шари розділяли та (td, J=7,42, 0,98Гц, 1H), 6,73 (d, J=8,20Гц, 1H), 6,89 водний шар екстрагували додатково (dd, J=7,42, 1,56Гц, 1H), 7,07 (d, J=8,40Гц, 2H), дихлорметаном (2х). Поєднані органічні фази 7,10-7,17 (m, 1H), 7,18-7,27 (m, 5H), 7,27-7,33 (m, сушили безводним натрій сульфатом, фільтр ували 2Η). та концентрували у вакуумі. Продукт очищали Виявлено: С, 65,55; Η, 6,48; Ν, 6,69, флеш-хроматографією на колонці з силікагелем, C31H37N3 Ox1,2CF3CO2H x0,4Η2O має С, 65,58; Η, елюючи сумішшю 1:1 EtOAc:гексани, тоді 6,43; Ν, 6,87%. 49 Сполука 7: [(циклогексилметил]аміно]феніл)-4піперидиніліденметил]-N,N-діетилбензамід 82091 50 4-{[2водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтр ували та концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 20-50% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 8 (203мг, 45% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,11 (brt, J=7,62Гц, 3H), 1,24 (brt, J=7,62Гц, 3H), 2,46-2,52 (m, 2H), До розчину інтермедіату 6 (300мг, 0,65ммоль) 2,64-2,79 (m, 2H), 3,17-3,37 (m, 6H), 3,49-3,58 (m, у 1,2-дихлоретані (20мл) додавали 2H), 4,34 (s, 2H), 6,54-6,57 (m, 1H), 6,61-6,66 (m, циклогексанкарбоксальдегід (146мг, 1,30ммоль) а 1H), 6,96 (dd, J=7,62, 1,56Гц, 1H), 7,01-7,08 (m, 1H), потім льодяну оцтову кислоту (0,07мл, 1,30ммоль) 7,11-7,27 (m, 5H), 7,32-7,37 (m, 4H). та NaBH(OAc)3 (344мг, 1,63ммоль). Реакційну Виявлено: С, 62,71; Η, 5,89; Ν, 6,74. суміш перемішували протягом ночі при кімнатній С30Н35N3 Оx1,5CF3CO2H x0,4Η2Ο має С, 62,73; Η, температурі під азотом. Додавали 5,95; Ν, 6,65%. трифлуороцтову кислоту (2мл) та реакційну суміш Сполука 9: 4-[[2-[циклогексиламіно)феніл)-4перемішували ще 4 години. Реакційну суміш піперидиніліденметил]-N,N-діетилбензамід розбавляли дихлорметаном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтрували та концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 2050% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 7 (190мг, 43% виходу) як трифлуорацетат. Цей У суспензію інтермедіату 6 (200мг, 0,43ммоль) матеріал ліофілізували з CH3CN/води, отримуючи та циклогексанону (47мг, 0,47ммоль) у МеОН безбарвний твердий продукт. Чистота (ВЕРХ): (6мл) додавали декаборан (16мг, 0,3ммоль). >99%; Реакційну суміш перемішували протягом ночі при 1 H-ЯМР (400МГц, CD3OD) d 0,78-0,90 (m, 2H), кімнатній температурі під азотом, тоді 1,05-1,25 (m, 10H), 1,41-1,52 (m, 1H), 1,52-1,72 (m, концентрували у вакуумі. Залишок фільтрували 5H), 2,36-2,50 (m, 2H), 2,64-2,77 (m, 2 HI 2,88 (d, через тонкий шар силікагелю, елюючи сумішшю J=6,64Гц, 2H), 3,12-3,38 (m. 5H), 3,46-5,55 (m, 2Η), 1:1 EtOAc:гексани та концентрували у вакуумі. 6,59-6,66 (у, 2H), 6,96 (dd, J=7,42, 1,37Гц, 1H), 7,12 Залишок розчиняли у дихлорметані (10мл) та (ddd, J=8,70, 7,42, 1,56Гц, 1H), 7,31 (s, 4Η). додавали трифлуороцтову кислоту (1,5мл). Виявлено: С, 63,61; Η, 6,36; Ν, 6,92. Реакційну суміш перемішували протягом ночі при C30H41N3 Ox1,4CF3CO2H має С, 63,61; Η, 6,90; Ν, кімнатній температурі, тоді концентрували у 6,78%. вакуумі. Залишок очищали зворотно-фазовою Сполука 8: N,N-діетил-4-{[2ВЕРХ (градієнт 10-40% CH3CN у воді з вмістом [(фенілметил)аміно]феніл]-40,1% трифлуороцтової кислоти), отримуючи піперидиніліденметил]бензамід сполуку 9 (207мг, 71% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН 3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 0,69-0,82 (m, 1H), 1,05-1,38 (m, 11H), 1,47-1,61 (m, 2H), 1,69 (d, J=12,89Гц, 2H), 1,93 (d, J=11,72Гц, 1H), 2,37-2,51 (m, 2H), 2,66-2,81 (m, 2H), 3,08-3,17 (m, 1H), 3,173,38 (m, 5H), 3,51 (br q, J=6,45Гц, 2H), 6,73-6,79 (m, 2H), 7,06 (dd, J =7,62,1,56Гц, 1H), 7,18 (ddd, J=8,25, До розчину інтермедіату 6 (309мг, 0,67ммоль) 7,37,1,56Гц, 1H), 7,28-7,36 (m, 4Η). у 1,2-дихлоретані (20мл) додавали бензальдегід Виявлено: С, 58,94; Η, 6,47; Ν, 6,31. (140мкл, 1,38ммоль) а потім льодяну оцтову C29H39N3 Ox1,8CF3CO2H x0,7Η2Ο має С, 59,01; Η, кислоту (38мкл, 0,66ммоль) та NaBH(OAc)3 (283мг, 6,41; Ν, 6,33%. 1,34ммоль). Реакційну суміш перемішували Сполука 10: N,N-діетил-4-[[2протягом ночі при кімнатній температурі під [[[феніламіно)карбоніл]аміно]феніл)-4азотом. Додавали трифлуороцтову кислоту (2мл) піперидиніліденметил]бензамід та реакційну суміш перемішували ще 4 години. Реакційну суміш розбавляли дихлорметаном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та 51 82091 52 у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 11 (193мг, 44% виходу) як трифлуорацетат Цей матеріал ліофілізували з СНзСN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 1,01 (t, J=6,83Гц, 3H), 1,19 (t, 3=7,03Гц, 3H), 2,48-2,58 (m, 2H), 2,582,76 (m, 2H), 3,03 (q, J=6,83Гц, 2H), 3,11-3,26 (m, Розчин інтермедіату 6 (200мг, 0,43ммоль) та 4H), 3,46 (q, J=7,03Гц, 2H), 6,71-6,79 (m, 3H), 6,98 феніл ізоціанат (56мг, 0,47ммоль) у 1,2(ddd, J=7,62, 6,25, 2,34Гц, 1H), 7,05-7,11 (m, 2H), дихлоретані (10мл) перемішували протягом ночі 7,16-7,24 (m, 7Η). при 70°С під азотом. Реакційну суміш тоді Виявлено: С, 65,08; Η, 6,11; Ν, 7,20. розбавляли дихлорметаном та промивали C29H33N3 Ox1,1CF3CO2H x0,6Η2Ο має С, 65,08: Η, насиченим водним натрій гідрогенкарбонатом (1х). 6,18; N,7,30%. Шари розділяли та водний шар екстрагували Сполука 12: N,N-діетил-4-[2додатково дихлорметаном (2х). Поєднані органічні (метилфеніламіно)феніл]-4фази сушили безводним натрій сульфатом, піперидиніліденметил]бензамід фільтрували та концентрували у вакуумі. Залишок розчиняли у дихлорметані (10мл) та додавали трифлуороцтову кислоту (1,5мл). Реакційну суміш перемішували протягом 6 годин при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 10-40% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 10 (235мг, 92% виходу) як трифлуорацетат Цей матеріал ліофілізували з СН 3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 0,97 (t, J=6,74Гц, 3H), 1,17 (t, J=7,03Гц, 3H), 2,48 (t, J=6,05Гц, 2H), 2,68 (q, J=5,60Гц, 2H), 3,04 (m, 2H), 3,15-3,27 (m, 4H), 3,39-3,53 (m, 2H), 6,98 (tt, J=7,22, 1,17Гц, 1H), (td, J=7,42, 1,37Гц, 1H), 7,20-7,28 (m, 6H), 7,28-7,30 (m, 1H), 7,30 (dd, 1=1,76, 0,98Гц, 1H), 7,33-7,34 (m, 1H), 7,34-7,37 (m, 1H), 7,60 (dd, J=8,10, 0,88Гц, 1Η). Виявлено: С, 57,39; Η, 5,32; Ν, 7,87. С50Н34N4 O2 x1,9CF3CO 2Hx0,5Η2O має С, 57,32; Η, 5,25; Ν, 7,91%. Сполука 11: N,N-діетил-4-{[2(феніламіно)феніл)-4піперидиніліденметил]бензамід Суміш інтермедіату 6 (300мг, 0,65ммоль), бромбензолу (133мг, 0,85ммоль), Pd2(dba)3 (24мг, 0,026ммоль), NaOtBu (87мг, 0,91ммоль), (+)-BINAP (32мг, 0,052ммоль) у толуолі (3,7мл) поміщали у склянку для мікрохвильової обробки. Колбу промивали азотом, закривали та гріли до 110°С протягом 5хвил, застосовуючи мікрохвильове опромінювання. Утворену суміш охолоджували, концентрували у вакуумі, тоді очищали флешхроматографією на колонці з силікагелем, елюючи сумішшю 2:3 EtOAc:гексани. Продукт розчиняли у дихлорметані (20мл) та додавали трифлуороцтову кислоту (2мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 15-40% CH3CN Суміш інтермедіату 6 (225мг, 0,49ммоль), бромбензолу (99мг, 0,63ммоль), Pd2(dba)3 (18мг, 0,019ммоль), NaOBu (65мг, 0,68ммоль), (±) BINAP (24мг, 0,039ммоль) у толуолі (2,8мл) поміщали у склянку для мікрохвильової обробки. Колбу промивали азотом, закривали та гріли до 110°С протягом 5хвил, застосовуючи мікрохвильове опромінювання. Утворену суміш охолоджували, концентрували у вакуумі, тоді очищали флешхроматографією на колонці з силікагелем, елюючи сумішшю 2:3 EtOAc:гексани. Продукт (260мг, 0,48ммоль) розчиняли у диметилформаміді (11мл) та додавали натрій гідрид (46мг, 1,16ммоль). Реакційну суміш перемішували протягом 1 години при кімнатній температурі. Метилйодид (171мг, 1,21ммоль) тоді додавали та реакційну суміш перемішували протягом ночі при кімнатній температурі. Через 18 годин, реакційну суміш гасили насиченим амоній хлоридом та екстрагували дихлорметаном. Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтр ували та концентрували у вакуумі. Залишок розчиняли у дихлорметані (10мл) та додавали трифлуороцтову кислоту (1,5мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 20-50% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 12 (126мг, 34% виходу за два етапи) як трифлуорацетат. Цей матеріал ліофілізували з СН 3СN/води, отримуючи блідожовтий твердий продукт. Чистота (ВЕРХ): 91% (215нм), 93% (254нм), 86% (280нм); 1 Н ЯМР (400МГц, CD3OD) d 1,04 (br s, 3H), 1,19 (br s, 3H), 2,38-2,57 (m, 3Н), 2,57-2,72 (m, 4H), 2,933,18 (m, 5H), 3,20-3,33 (m, 1H), 3,48 (br s, 2H), 6,27 (d, J=8,20Гц, 2H), 6,60 (t, J=7,32Гц, 1H), 6,92 (d, J=8,01Гц, 2H), 7,01 (t, J=7,81Гц, 2H), 7,13 (d, 53 82091 54 1 J=7,62Гц, 1H), 7,16-7,23 (m, 2H), 7,34 (t, J=7,03Гц, Н ЯМР (400МГц, CD3OD) d 1,02 (t, J=6,83Гц, 1H), 7,43 (dd, J=14,65, 7,42Гц, 2Η). 3H), 1,20 (t, J=6,64Гц, 3H), 2,36-2,52 (m, 2H), 2,52Сполука 13: N,N-діетил-4-[[22,62 (m, 1H), 2,74 (dt, J=15,38, 5,40Гц, 1H), 3,13[[фенілсульфоніл)аміно]феніл)-43,27 (m, 5H), 3,30-3,39 (m, 1H), 3,42-3,55 (m, 2H), піперидиніліденметил]бензамід 4,13 (d, J=13,86Гц, 1H), 4,25 (d, J=13,67Гц, 1H), 7,17 (dt, J=7,22, 1,17Гц, 1H), 7,22-7,36 (m, 12 Н). Виявлено: С, 58,87; Η, 5,76; Ν, 6,31. C30H35N3 O3Sx1,1CF3CO 2Hx0,8Η2Ο має С, 58,82; Η, 5,78; Ν, 6,39%. Сполука 15: N,N-Діетил-4-[4-піперидиніліден[2[[(2,2,2трифлуоретил)сульфоніл]аміно]феніл]метил]бенза мід До розчину інтермедіату 6 (300мг, 0,65ммоль) у піридині (10мл) додавали бензолсульфонілхлорид (230мг, 1,30ммоль). Реакційну суміш перемішували протягом ночі при кімнатній температурі під азотом, тоді концентрували у вакуумі. Залишок розчиняли у дихлорметані та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтр ували та концентрували у вакуумі. Залишок розчиняли у дихлорметані (15мл) та додавали трифлуороцтову кислоту (2мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 10-40% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 13 (298мг, 63% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи жовтий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,11 (t, J=6,64Гц, 3H), 1,22 (t, J=7,03Гц, 3H), 2,43-2,52 (m, 1H), 2,522,61 (m, 2H), 2,72-2,83 (m, 1H), 3,22-3,36 (m, 5H), 3,38-3,48 (m, 1H), 3,47-3,60 (m, 2H), 6,64 (dd, J=S.O1, 0,78Гц, 1H), 7,11 (ddd, J=8,01, 7,03,1,95Гц, 1H), 7,1-7,34 (m, 6H), 7,48-7,53 (m, 2H), 7,60 (tt, J=7,42,1,37Гц, 1H), 7,64-7,69 (m, 2Η). Виявлено: С, 58,37; Η, 5,58; Ν, 6,46. C25H33N3 O3Sx1,1CF3CO 2Hx0,7Η2Ο має С, 58,40; Η, 5,58; Ν, 6,55%. Сполука 14: N,N-діетил-4-[[2[[(фенілметил)сульфоніл]аміно]феніл)-4піперидиніліденметил]бензамід Способом для сполуки 13, застосовуючи інтермедіат 6 (250мг, 0,54ммоль) та бензилсульфонілхлорид (206мг, 1,08ммоль) отримували сполуку 14 (253мг, 63% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи бежевий твердий продукт. Чистота (ВЕРХ): >99%; Способом для сполуки 13, застосовуючи інтермедіат. 6 (203мг, 0,44ммоль) та 2,2,2трифлуоретансульфонілхлорид (0,097мл, 0,88ммоль) отримували сполуку 15 (244мг, 89% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН 3СN/води, отримуючи блідожовтий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,11 (або t, J=6,6Гц, 3H), 1,23 (br t, J=7,0Гц, 3H), 2,42-2,59 (m, 3H), 2,73-2,82 (m, 1H), 3,19-3,40 (m, 6H), 3,53 (q, J=6,8Гц, 2H), 3,95-4,15 (m, 2H), 7,26-7,44 (m, 8Η). Сполука 16: 4-[[2[(циклопентилацетил)аміно]феніл}(піперидин-4іліден)метил]-N,N-діетил]бензам|д Способом для сполуки 1, застосовуючи інтермедіат 6 (175мг, 0,377ммоль) та циклопентилацетилхлорид (61мг, 0,415ммоль) отримували сполуку 16 (180мг, 81%) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи безбарвний Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,06-1,26 (m, 8H), 1,49-1,70 (m, 4H), 1,72-1,87 (m, 2H), 2,08-2,31 (m, 3H), 2,52 (t, J=5,96Гц, 2H), 2,56-2,66 (m, 1H), 2,672,78 (m, 1H), 3,16-3,34 (m, 6H), 3,46-3,56 (brq, J=6,83Гц, 2H), 7,17 (d, J=8,40Гц, 2H), 7,26-7,37. Виявлено: С, 63,23; Η, 6,84; Ν, 6,87. C30H39N3 O3 x1,1CF3CO 2Hx0,7Η2Ο має С, 63,23; Η, 6,84; Ν, 6,87%. Сполука 17: 4-{[2[(циклопентилкарбоніл)аміно]феніл}(піперидин-4іліден)метил]-Ν,Ν-діетилбензамід 55 82091 Способом для сполуки 1, застосовуючи інтермедіат 6 (145мг, 0,313ммоль) та циклопентанкарбонілхлорид (46мг, 0,344ммоль) отримували сполуку 17 (141мг, 79%) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,10 (brt, J=6,35Гц, 3H), 1,21 (brt, J=6,35Гц, 3H), 1,44-1,86 (m, 7H), 1,87-1,99 (m, 1H), 2,47-2,54 (m, 2H), 2,55-2,79 (m, 3H), 3,16-3,34 (m, 6H), 3,51 (brq, J=7,16Гц, 2H), 7,18 (d, J=8,40Гц, 2H), 7,27-7,35 (m, 6Η). Виявлено: С, 60,05; Η, 6,05; Ν, 6,71. C29H37N3 O2 x1,6CF3CO 2Hx0,1Η2Ο має С, 60,07; Η, 6,07; Ν, 6,53%. Сполука 18: N,N-діетил-4-[{2-{[3фенілпропіл)аміно]феніл}(піперидин-4іліден)метил]бензамід До розчину інтермедіату 6 (200мг, 0,43ммоль) у 1,2-дихлоретані (13мл) додавали 3фенілпропіональдегід (93мг, 0,69ммоль) а потім льодяну оцтову кислоту (39мкл, 0,69ммоль) та NaBH(OAc)3 (183мг, 0,86ммоль). Реакційну суміш перемішували протягом ночі при кімнатній температурі під азотом. Додавали трифлуороцтову кислоту (1,5мл) та реакційну суміш тримали протягом ночі при кімнатній температурі. Реакційну суміш розбавляли дихлорметаном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтр ували та концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 20-50% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 18 (112мг, 37% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 0,99 (br t, J=6,69Гц, 3H), 1,18 (br t, J=6,64Гц, 3H), 1,71-1,81 (m, 2H), 2,37-2,56 (m, 4H), 2,64-2,79 (m, 2H), 3,003,27 (m, 7H), 3,30-3,37 (m, 1H), 3,48 (br q, J=6,58Гц, 2 Η) 6,60 (d, J=7,71Гц, 1H), 6,66 (dt, J=7,42, 0,98Гц, 1H), 6,98 (dd, J=7,47,1,61Гц, 1H), 7,04-7,08 (m, 2H), 7,10-7,15 (m, 2H), 7,18-7,24 (m, 2H), 7,29-7,35 (m, 4Η). 56 Виявлено: С, 62,11; Η, 5,88; Ν, 5,69. C32H39N3 Ox1,8CF3CO2H x0,1Η2Ο має С, 62,08; Η, 6,00; Ν, 6,10%. Сполука 19: 4-[(2-[(2циклогексилетил)аміно]феніл}(піперидин-4іліден)метил]-N,N-діетилбензамід До розчину інтермедіату 6 (175мг, 0,377ммоль) у 1,2-дихлоретані (12мл) додавали циклогексилацетальдегід (57мг, 0,453ммоль) а потім льодяну оцтову кислоту (26мкл, 0,453ммоль) та NaBH(OAc)3 (160мг, 0,755ммоль). Реакційну суміш перемішували протягом ночі при кімнатній температурі під азотом. Додавали трифлуороцтову кислоту (1,5мл) та реакційну суміш тримали протягом ночі при кімнатній температурі. Реакційну суміш розбавляли дихлорметаном та промивали насиченим водним натрій гідрогенкарбонатом (1х). Шари розділяли та водний шар екстрагували додатково дихлорметаном (2х). Поєднані органічні фази сушили безводним натрій сульфатом, фільтр ували та концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 20-50% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 19 (89мг, 34% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 0,85-0,98 (m, 2H), 1,10 (br t, J=6,25Гц, 3H), 1,04-1,32 (m, 4H), 1,21 (brt, J=7,08Гц, 3H), 1,32-1,44 (m, 2H), 1,59-1,75 (m, 5H), 2,35-2,48 (m, 2H), 2,63-2,76 (m, 2H), 3,01-3,36 (m, 8H), 3,48-3,56 (m, 2H), 6,62-6,68 (m, 2H), 6,94 (dd, J=7,37,1,32Гц, 1H), 7,14 (ddd, J=8,30, 7,42,1,66Гц, 1H), 7,29-7,35 (m, 4 Η). Виявлено: С, 64,57; Η, 7,10; Ν, 6,95. C31H43N3 Ox1,3CF3CO2H x0,2Η2Ο має С, 64,52; Η, 7,20; Ν, 6,72%. Сполука 20: 4-[[2(циклопентиламіно)феніл][(піперидин-4іліден)метил]-N,N-діетилбензамід Способом для сполуки 9, застосовуючи інтермедіат 6 (200мг, 0,43ммоль) та циклопентанон (40мг, 0,47ммоль) отримували сполуку 20 (210мг, 74%) як трифлуорацетат Цей матеріал ліофілізували з СН 3СN/води, отримуючи 57 82091 58 безбарвний твердий продукт. Чистота (ВЕРХ): 62,35; Η, 5,96; Ν, 8,73. >99%; C31H36N4 O2 x1,2CF3CO2H x0,5Η2Ο має С, 62,44; Η, 1 5,99; Ν, 8,72%. H-ЯМР (400МГц, CD3OD) d 1,05-1,26 (m, 1H), Сполука 23: N,N-діетил-4-[[2-(11,09 (brt, J=6,06Гц, 3H), 1,21 (t, J =6,64Гц,. 3H), нафтиламіно)фенілігпіперидин-4L30-1,67 (m, 5H), 1,71-1,81 (m, 1H), 1,90-2,02 (m, іліден)метил]бензамід 1H), 2,36-2,52 (m, 2H), 2,65-2,79 (m, 2H), 3,14-3,36 (m, 6H), 3,47-3,55 (m, 2H), 3,66-3,74 (m, 1H), 6,696,76 (m, 2H), 7,02 (dd, J=7,32, 1,27Гц, 1H), 7,16 (ddd, J =8,45, 7,18, 1,76Гц, 1H), 7,27-7,35 (m, 4Η). Виявлено: С, 56,62; Η, 5,62; Ν, 6,30. C28H37N3 Ox2,2CF3CO2H x0,2Η2Ο має С, 56,72; Η, 5,82; Ν, 6,12%. Сполука 21: 4-[[2(циклогептиламіно)феніл](піперидин-4іліден)метил]-N,N-діетилбензамід Способом для сполуки 9, застосовуючи 1Η і r.Rlvit,DLA it. 6 (200мг, 0,43ммоль) та циклогептанон (53мг, 0,47ммоль) отримували сполуку 21 (241мг, 81%) як трифлуорацетат. Цей матеріал ліофілізували з СН 3СN/води, отримуючи безбарвний твердий продукт. Чистота (ВЕРХ): >99%; 1 Н ЯМР (400МГц, CD3OD) d 1,05-1,25 (m, 4H), 1,21 (t, J=7,03Гц, 3Н), 1,25-1,70 (m, 11H), 1,8-1,98 (m, 1H), 2,36-2-49 (m, 2H), 2,67-2,80 (m, 2H), 3,133,38 (m, 6H), 3,51 (q, J=6,70Гц, 2H), 6,73 (d, J=8,01Гц, 1H), 6,77 (dt, J=7,42, 1,17Гц, 1H), 7,06 (dd, J=7,32, 1,27Гц, 1H), 7,16 (dq, J =8,45, 7,18, 1,76Гц, 1H), 7,27-7,35 (m, 4Η). Виявлено: С, 57,47; Η, 5,91; Ν, 5,76. C30H41N3 Ox2,3CF3CO2H x0,1 Η2Ο має С, 57,42; Η, 6,06; Ν, 5,81%. Сполука 22: 4-[(2{[(бензиламіно)карбоніл]аміно}феніл(піперидин-4іліден)метил]-Ν,N-діетилбензамід Способом для сполуки 10, застосовуючи інтермедіат 6 (200мг, 0,43ммоль) та бензилізоціанат (63мг, 0,47ммоль) отримували сполуку 22 (193мг, 74%) як трифлуорацетат Цей матеріал ліофілізували з СН 3СN/води, отримуючи бежевий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,08 (t, J=6,64Гц, 3H), 1,23 (t, J=6,64Гц, 3H), 2,44 (t, J=6,05Гц, 2H), 2,55-2,68 (m, 2H), 3,12-3,27 (m, 6H), 3,51 (br q, J=6,44Гц, 2H), 4,23-4,36 (m, 2H), 7,13 (dt, J=7,42,1,37Гц, 1H), 7,17-7,21 (m, 3H), 7,22-7,36 (m, 8H), 7,56 (dd, J=8,20, 0,78Гц, 1Η). Виявлено: С, Суміш інтермедіату 6 (200мг, 0,43ммоль), бромнафталіну (116мг, 0,56ммоль), Pd2(dba)3 (16мг, 0,017ммоль), NaOtBu (58мг, 0,60ммоль), (±)BINAP (21мг, 0,034ммоль) у толуолі (2,4мл) поміщали у склянку для мікрохвильової обробки Колбу промивали азотом, закривали та гріли до 110°С протягом 5мм, застосовуючи мікрохвильове опромінювання. Утворену суміш охолоджували, концентрували у вакуумі, тоді очищали флешхроматографією на колонці з силікагелем, елюючи сумішшю 1:1 EtOAc:гексани. Продукт розчиняли у дихлорметані (10мл) та додавали трифлуороцтову кислоту (1,3мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 20-45% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 23 (133мг, 45% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи бежевий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,00 (t, J=6,54Гц, 3H), 1,19 (t, J=6,74Гц, 3H), 2,54-2,75 (m, 4H), 3,083,21 (m, 4H), 3,23-3,31 (m, 2H), 3,42-3,53 (m, 2H), 6,78 (dd, J=8,01, 0,98Гц, 1H), 6,88 (dd, J=7,42, 0,98Гц, 1H), 6,98 (dt, J=7,47,1,27Гц, 1H), 7,11-7,20 (m, 5H), 7,23-7,33 (m, 3H), 7,42 (dq, J=6,83, 1,17Гц, 1H), 7,47 (d, J=8,20Гц, 1H), 7,56 (d, J=8,40Гц, 1H), 7,80 (d, J=8,20Гц, 1Η). Виявлено: С, 66,35; Η, 5,04; Ν, 6,65. C33H35N3 Ox1,4CF3CO2H має С, 66,22; Η, 5,65; Ν, 6,47%. Сполука 24: N,N-діетил-4-[{2-[(3флуорфеніл)аміно]феніл}(піперидин-4іліден)метил]бензамід Суміш інтермедіату 6 (200мг, 0,43ммоль), 3флуорйодбензолу (124мг; 0,56ммоль), Pd2(dba)3 (16мг, 0,017ммоль), NaOtBu (58мг, 0,60ммоль), (±)BINAP (21мг, 0,034ммоль) у толуолі (2,4мл) поміщали у склянку для мікрохвильової обробки. 59 82091 60 Колбу промивали азотом, закривали та гріли до Виявлено: С, 60,39; Η, 5,29; Ν, 6,65. 110°С протягом 25хвил, застосовуючи C29H3aCIN3 Ox1,4CF3CO2H має С, 60,28; Η, 5,31; Ν, мікрохвильове опромінювання. Утворену суміш 6,63%. охолоджували, концентрували у вакуумі, тоді Сполука 26: 4-[{2очищали флеш-хроматографією на колонці з [циклогексил(метил)аміно]феніл}гпіперидин-4силікагелем, елюючи сумішшю 1:1 EtOAc/гексани. іліден)метил)-N,N-діетилбензамід Продукт розчиняли у дихлорметані (10мл) та додавали трифлуороцтову кислоту (1,3мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали зворотно-фазовою ВЕРХ (градієнт 15-40% CH3CN у воді з вмістом 0,1% трифлуороцтової кислоти), отримуючи сполуку 24 (99мг, 34% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН 3СN/води, отримуючи світло-сирий твердий продукт. Чистота У суспензію інтермедіату 6 (175мг, 0,38ммоль) (ВЕРХ): >95%; та циклогексанону (41мг, 0,42ммоль) у МеОН 1 (5мл) додавали декаборан (14мг, 0,11ммоль). Н ЯМР (400МГц, CD3OD) d 1,00 (t, J=6,83Гц, 3H), 1,18 (t, J=6,83Гц, 3H), 2,47-2,74 (m, 4H), 3,01 Реакційну суміш перемішували протягом ночі при (q, J=6,83Гц, 2H), 3,14-3,27 (m, 4H), 3,46 (q, кімнатній температурі під азотом, тоді концентрували у вакуумі. Залишок фільтрували J=5,86Гц, 2H), 6,32-6,39 (m, 2H), 6,46-6,50 (m, 1H), через тонкий шар силікагелю, елюючи сумішшю 6,97-7,05 (m, 1H), 7,07-7,32 (m, 8Η). Виявлено: С, 62,96; Η, 5,62; Ν, 7,17. 1:1 EtOAc:гексани та концентрували у вакуумі. До C29H3aFN 3Ox1,2CF3CO 2Hx0,2Η2Ο має С, 63,07; Η, розчину продукту (206мг, 0,38ммоль) у МеОН 5,66; Ν, 7,03%. (4мл) додавали формальдегід (37% у воді, 0,084мл, 1,13ммоль). Реакційну суміш Сполука 25: 4-[{2-[(4перемішували протягом 30 хвилин при кімнатній хлорфеніл)аміно]феніл)піперидин-4-іліден)метил]N,N-діетилбензамід температурі. Декаборан (28мг, 0,23ммоль) додавали та реакційну суміш перемішували протягом 1 години при кімнатній температурі під азотом, тоді концентрували у вакуумі. Залишок фільтрували через тонкий шар силікагелю, елюючи сумішшю 1:1 EtOAc:гексани та концентрували у вакуумі. Залишок розчиняли у дихлорметані (10мл) та додавали трифлуороцтову кислоту (1,2мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі, тоді концентрували у вакуумі. Залишок очищали Суміш інтермедіату 6 (200мг, 0,43ммоль), 4зворотно-фазовою ВЕРХ (градієнт 5-30% CH3CN у бромхлорбензолу (107мг, 0,56ммоль), Pd2(dba)3 воді з вмістом 0,1% трифлуороцтової кислоти), t (16мг, 0,017ммоль), NaO Bu (58мг, 0,60ммоль), (+)отримуючи сполуку 26 (181мг, 70% виходу) як BINAP (21мг, 0,034ммоль) у толуолі (2,4мл) трифлуорацетат. Цей матеріал ліофілізували з поміщали у склянку для мікрохвильової обробки. CH3CN/води, отримуючи coloress тверд. Чистота Колбу промивали азотом, закривали та гріли до (ВЕРХ): >99%; 1 110°С протягом 5хвил, застосовуючи H-ЯМР (400МГц, CD3OD) d 0,95 (br s, 3H), 1,08 мікрохвильове опромінювання. Утворену суміш (br t, J=6,35Гц, 3H), 1,21 (br t, J=6,44Гц, 3H), 1,18охолоджували, концентрували у вакуумі, тоді 1,25 (m, 2H), 1,45-1,63 (m, 3H), 1,70 (brs, 2H), 2,39очищали флеш-хроматографією на колонці з 2,54 (m, 2H), 2,71-2,93 (m, 5H), 3,02 (br s, 1H), 3,07силікагелем, елюючи сумішшю 2:3 EtOAc:гексани. 3,21 (m, 2H), 3,22-3,43 (m, 4H), 3,51 (br q, J=6,64Гц, Продукт розчиняли у дихлорметані (10мл) та 2H), 7,35 (s, 5H), 7,50 (brs, 3H). додавали трифлуороцтову кислоту (1,3мл). Виявлено: С, 52,62; Η, 6,35; Ν, 5,00. Реакційну суміш перемішували протягом ночі при C30H41N3 Ox2,5CF3CO2H x3,0Η2Ο має С, 52,63; Η, кімнатній температурі, тоді концентрували у 6,25; Ν, 5,26%. вакуумі. Залишок очищали зворотно-фазовою Сполука 27: N,N-діетал-4-[(2-{[(4ВЕРХ (градієнт 20-50% CH3CN у воді з вмістом метилфеніл)сульфоніл]аміно)феніл)(піперидин-40,1% трифлуороцтової кислоти), отримуючи іліден)метил]бензамід сполуку 25 (139мг, 46% виходу) як трифлуорацетат. Цей матеріал ліофілізували з СН3СN/води, отримуючи бежевий твердий продукт. Чистота (ВЕРХ): >99%; 1 H-ЯМР (400МГц, CD3OD) d 1,01 (t, J=6,83Гц, 3H), 1,18 (t, J=6,83Гц, 3H), 2,46-2,75 (m, 4H), 3,00 (q, J=6,57Гц, 2H), 3,15-3,30 (m, 4H), 3,46 (q, J=6,70Гц, 2H), 6,64-6,69 (у, 2H), 6,98-7,03 (m, 2H), 7,06 (dt, J=7,37, 1,27Гц, 1H), 7,15-7,21 (m, 5H), 7,23-7,28 (m, 2Η).
ДивитисяДодаткова інформація
Назва патенту англійськоюDiarylmethylidene piperidine derivatives, preparation thereof and use thereof
Автори англійськоюGriffin Andrew, Jin Shujuan
Назва патенту російськоюПроизводные диарилметилиденпиперидина, способ их получения (варианты), фармацевтическая композиция на их основе и их применение
Автори російськоюГриффин Эндрю, Джин Шуджван
МПК / Мітки
МПК: C07D 417/06, C07D 211/70, A61P 25/22, C07D 401/06, A61P 25/04
Мітки: основі, отримання, композиція, фармацевтична, спосіб, варіанти, діарилметиліденпіперидину, похідні, застосування
Код посилання
<a href="https://ua.patents.su/41-82091-pokhidni-diarilmetilidenpiperidinu-sposib-kh-otrimannya-varianti-farmacevtichna-kompoziciya-na-kh-osnovi-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні діарилметиліденпіперидину, спосіб їх отримання (варіанти), фармацевтична композиція на їх основі та їх застосування</a>
Попередній патент: Спосіб отримання екстракту бета-каротину
Наступний патент: Заглушка ракетного двигуна малої тяги
Випадковий патент: Стіл "фантом"