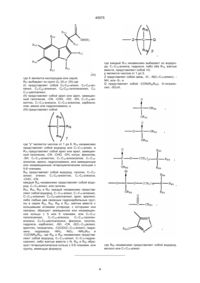
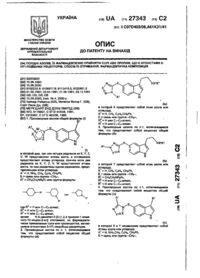
Гідразид 1н-індол-3-оцтової кислоти (варіанти) як інгібітор spla2 та фармацевтична композиція
Номер патенту: 40575
Опубліковано: 15.08.2001
Автори: Бах Ніколас Джеймс, Драхейм Сюзан Елізабет, Діллард Роберт Ділейн, Шевіц Ричард Вальтер, Германн Роберт Белл
Формула / Реферат
1. Гидразид 1Н-индол-3-уксусной кислоты, представленный формулой (I),
и его фармацевтически приемлемые соли,
где X является кислородом или серой,
r1 выбирают из групп (I), (II) и (III), где
(I) представляет собой С4-С20-алкил, С4-С20-алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4-С12-циклоалкил,
(II) представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, -SH, С1-С10-алкилтио, С,-С10-алкокси, С1-С10-алкилом, карбоксилом, амино или гидроксиамино,
(III) представляет собой
где "у" является числом от 1 до 8, R74 независимо представляет собой водород или С1-С10-алкил, a R75 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, С1-С10-алкилтио, С1-С10-алкокси, С1-С10-алкилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами,
R2 представляет собой галоген, С1-С3 алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN,
каждый R3 независимо представляет собой водород, С1-С3-алкил, или галоген, R4, R5, R6 и R7 каждый независимо представляют собой водород, С1-С10-алкил, С1-С10-алкенил, С1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил, или любые две смежные гидрокарбильные группы в серии R4, r5, R6 и R7, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо с 5 или 6 членами, или С1-С10-галогеналкил, С1-С10-алкокси, С1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SH, -CN, -S(С1-С10)алкил, арилтир, тиоацеталь, -С(О)О(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо являются водородом, С1-С10-алкилом, С1-С10-гидроксиалкилом, либо взятые вместе с N, R82 и R83 образуют гетероциклическое кольцо с 5-8 членами, или группу формулы
где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О,
p является числом от 1 до 8,
Ζ представляет собой связь, -О-, -М(С1-С10-алкил)-, -ΝΗ, или -S-, и
Q представляет собой -CON (R82R83), -5-тетразолил, -SO3H,
где R86 независимо выбирают из водорода, металла или С1-С10-алкила.
2. Гидразид 1Н-индол-3-уксусной кислоты, представленный формулой (II),
и его фармацевтически приемлемые соли,
где X является кислородом или серой,
R11 выбирают из групп (I), (II) и (III), где
(I) представляет собой С4-С20-алкил, С4-С20-алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4-С12-циклоалкил,
(II) представляет собой арил или арил, замещенный галогеном, нитро, -CN, -СНО, -ОН, -SH, С1-С10-алкилом, С1-С10-алкилтио, С1-С10-алкоксилом, карбоксилом, амино или гидроксиамино, и
(III) представляет собой -(NH)-(R81), где R81 является группой, указанной для (I) или (II),
R12 представляет собой водород, галоген, С1-С3 алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN,
каждый R13 независимо представляет собой водород, С1-С3-алкил, или галоген,
R14, R15, R16 и R,17 каждый независимо представляет собой водород, С1-С10-алкил, С1-С10-алкенил, С1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил, либо две смежные гидрокарбильные группы в серии R]4, R15, R16 и R17, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо с 5 или 6 членами, или С1-С10-галогеналкил, С1-С10-алкокси, С1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SH, -CN, -S(С1-С10)алкил, арилтио, тиоацеталь, -С(О)О(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо являются водородом, С1-С10-алкилом, С1-С10-гидроксиалкилом, либо R82 и R83, взятые вместе с N, образуют гетероциклическое кольцо с 5-8 членами, или группу формулы
где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, или оба R76, взятые вместе, представляют собой =О,
p является числом от 1 до 8,
Ζ представляет собой связь, -О-, -М(С1-С10-алкил)-, -ΝΗ, или -S-, и Q представляет собой -CON (R82R83), -5-тетразолил, -SO3H,
где R86 независимо представляет собой водород, металл или С1-С10-алкил.
3. Гидразид 1H-индол-3-уксусной кислоты, представленный формулой (V),
и его фармацевтически приемлемые соли, где X является кислородом, R51 представляет собой формулу
где R84 представляет собой водород или С1-С10 алкил, a R87 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, С1-С10-алкилтио, С1-С10-алкилом, С1-С10-алкокси, карбоксилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами,
R52 представляет собой галоген, метилтио, или С1-С3-алкил,
каждый R53 представляет водород или галоген,
R54, R55, r56 и r57 независимо выбирают из групп (а) и (b), где
(a) представляет собой водород, и
(b) является группой формулы
где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой=О,
p является числом от 1 до 8,
Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, -ΝΗ, или -S-, и
Q представляет собой -CON (R82R83), -5-тетразолил, -SO3H
,
где R86 независимо представляет собой водород, металл или С1-С10-алкил.
4. Фармацевтическая композиция, отличающаяся тем, что содержит в качестве активного ингредиента эффективное количество соединения, заявленного по любому из пунктов 1-3, в сочетании с одним или несколькими фармацевтически приемлемыми носителями.
5. Гидразид 1Н-индол-3-уксусной кислоты формулы (VI) или его фармацевтически приемлемая соль, предназначенные для использования в целях ингибирования sPLA2-опосредованного высвобождения арахидоновой кислоты
где X является кислородом или серой,
R61, выбирают из групп (I), (II) и (III),где
(I) представляет собой С4-С20-алкил, С4-С20-алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4-С12-циклоалкил,
(II) представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, -SH, С1-С10-алкилтио, С1-С10-алкокси, С1-С10-алкилом, карбоксилом, амино или гидроксиамино, и
(III) представляет собой
где "у" является числом от 1 до 8, R74 независимо представляет собой водород или С1-С10-алкил, a R75 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, С1-С10-алкилтио, С1-С10-алкоксилом, С1-С10-алкилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами,
R62 представляет собой водород, галоген, С1-С3 алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN,
каждый R63 независимо представляет собой водород, С1-С10-алкил, или галоген,
R64, R65, R66 и R67 каждый независимо представляют собой водород, С1-С10-алкил, С1-С10-алкенил, С1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил, либо любые две смежные гидрокарбильные группы в серии R64, 65, R66 и R67, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное кольцо с 5 или 6 членами, или С1-С10-галогеналкил, С1-С10-алкокси, С1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SH, -CN, -8(С1-С10)алкил, арилтио, тиоацеталь, -С(О)О(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо представляют собой водород, С1-С10-алкил, С1-С10-гидроксиалкил, либо взятые вместе с N, R82 и R83 образуют гетероциклическое кольцо с 5-8 членами, или группу, имеющую формулу
где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О,
p является числом от 1 до 5,
Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, -ΝΗ, или -S-, и
Q представляет собой -CON (R82R83), -5-тетразолил, -SO3H,
где R86 независимо представляет собой водород, металл или С1-С10-алкил.
Текст
1. Гидразид 1Н-индол-3-уксусной кислоты, представленный формулой (I), C2 (54) ГІДРАЗИД 1Н-ІНДОЛ-3-ОЦТОВОЇ КИСЛОТИ (ВАРІАНТИ) ЯК ІНГІБІТОР SPLA2 ТА ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ 40575 и его фармацевтически приемлемые соли, где X является кислородом или серой, R11 выбирают из групп (I), (II) и (III), где (I) представляет собой С4-С20-алкил, С4-С20алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4С12-циклоалкил, (II) представляет собой арил или арил, замещенный галогеном, нитро, -CN, -СНО, -ОН, -SH, С1С10-алкилом, С1-С10-алкилтио, С1-С10-алкоксилом, карбоксилом, амино или гидроксиамино, и (III) представляет собой -(NH)-(R81), где R81 является группой, указанной для (I) или (II), R12 представляет собой водород, галоген, С1-С3алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN, каждый R13 независимо представляет собой водород, С1-С3-алкил, или галоген, R14, R15, R16 и R17 каждый независимо представляет собой водород, С1-С10-алкил, С1-С10-алкенил, С1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил, либо две смежные гидрокарбильные группы в серии R14, R15, R16 и R17, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо с 5 или 6 членами, или С1-С10галогеналкил, С1-С10-алкокси, С1-С10галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SH, -CN, -S(С1С10)алкил, арилтио, тиоацеталь, -С(О)О(С1-С10алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо являются водородом, С1-С10-алкилом, С1-С10гидроксиалкилом, либо R82 и R83, взятые вместе с N, образуют гетероциклическое кольцо с 5-8 членами, или группу формулы где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О, p является числом от 1 до 8, Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, -ΝΗ, или -S-, и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3H, где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, или оба R76, взятые вместе, представляют собой =О, p является числом от 1 до 8, Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, -ΝΗ, или -S-, и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3H, где R86 независимо выбирают из водорода, металла или С1-С10-алкила. 2. Гидразид 1Н-индол-3-уксусной кислоты, представленный формулой (II), ,(II) 2 40575 каждый R53 представляет водород или галоген, R54, R55, R56 и R57 независимо выбирают из групп (а) и (b), где (a) представляет собой водород, и (b) является группой формулы где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О, p является числом от 1 до 8, Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, -ΝΗ, или -S-, и Q представляет собой -CON(R82R83), -5-тетразолил,-SO3H, где R86 независимо представляет собой водород, металл или С1-С10-алкил. 3. Гидразид 1H-индол-3-уксусной кислоты, представленный формулой (V), , (V) и его фармацевтически приемлемые соли, где X является кислородом, R51 представляет собой формулу где R86 независимо представляет собой водород, металл или С1-С10-алкил. 4. Фармацевтическая композиция, отличающаяся тем, что содержит в качестве активного ингредиента эффективное количество соединения, заявленного по любому из пунктов 1-3, в сочетании с одним или несколькими фармацевтически приемлемыми носителями. 5. Гидразид 1Н-индол-3-уксусной кислоты формулы (VI) или его фармацевтически приемлемая соль, предназначенные для использования в целях ингибирования sPLA2-опосредованного высвобождения арахидоновой кислоты где R84 представляет собой водород или С1-С10 алкил, a R87 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, С1-С10-алкилтио, С1-С10-алкилом, С1-С10-алкокси, карбоксилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами, R52 представляет собой галоген, метилтио, или С1С3-алкил, 3 40575 где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О, p является числом от 1 до 5, Ζ представляет собой связь, -О-, -N(С1-С10-алкил)-, ΝΗ, или -S-, и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3H, , (VI) где X является кислородом или серой, R61 выбирают из групп (I), (II) и (III),где (I) представляет собой С4-С20-алкил, С4-С20-алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4С12-циклоалкил, (II) представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, -SH, С1-С10-алкилтио, С1-С10-алкокси, С1-С10-алкилом, карбоксилом, амино или гидроксиамино, и (III) представляет собой где "у" является числом от 1 до 8, R74 независимо представляет собой водород или С1-С10-алкил, a R75 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, С1-С10-алкилтио, С1-С10-алкоксилом, С1-С10алкилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами, R62 представляет собой водород, галоген, С1-С3алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN, каждый R63 независимо представляет собой водород, С1-С3-алкил, или галоген, R64, R65, R66 и R67 каждый независимо представляют собой водород, С1-С10-алкил, С1-С10-алкенил, С1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил, либо любые две смежные гидрокарбильные группы в серии R64, R65, R66 и R67, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное кольцо с 5 или 6 членами, или С1-С10галогеналкил, С1-С10-алкокси, С1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SH, -CN, -S(С1-С10)алкил, арилтио, тиоацеталь, -С(О)О(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо представляют собой водород, С1-С10-алкил, С1-С10-гидроксиалкил, либо взятые вместе с N, R82 и R83 образуют гетероциклическое кольцо с 5-8 членами, или группу, имеющую формулу где R86 независимо представляет собой водород, металл или С1-С10-алкил. ______________________________ 4 40575 В литературе также описываются некоторые соединения типа индола, которые могут быть использованы для лечения артритов. Так, например, в патентах США № 3196162; № 3242162; № 3242163; № 3242193 (см. пример 56, столбец 3, строки 55-60) описаны индолилалифатические кислоты и их соли, сложные эфиры и амиды. Эти соединения по своей структуре близки к индометациновым соединениям; имеют замещенную бензильную группу в 1 положении; и, по всей вероятности, обладают достаточной эффективностью в качестве ингибиторов циклооксигеназы. В статье "Recherches en serie indolique. VI sur tryptamines substitutes" (Marc Julia, Jean Igolen and Hanne Igolen, Bull. Soc. Chim. France, 1962, pp. 1060-1068) описываются некоторые гидразиды индол-3-уксусной кислоты и их превращение в триптаминовые производные. Было бы желательно получить новые соединения, которые можно было бы использовать для лечения sРLА2-индуцированных заболеваний. Краткое описание изобретения Настоящее изобретение относится к новому применению класса соединений, известных как гидразиды 1H-индол-3-уксусной кислоты, а именно к их использованию в качестве ингибиторов высвобождения арахидоновой кислоты, опосредованного секреторной фосфолипазой А2 человека (чел. sPLА2). Настоящее изобретение также относится к новому классу гидразидов 1H-индол-3-уксусной кислоты, обладающих сильным и избирательным действием в качестве ингибиторов чел. sPLA2. Настоящее изобретение также относится к фармацевтическим композициям, содержащим гидразид 1H-индол-3-уксусной кислоты настоящего изобретения. Настоящее изобретение также относится к способу предупреждения и лечения септического шока, предусматривающему использование гидразидов 1H-индол-3-уксусной кислоты настоящего изобретения. Подробное описание изобретения Соединения настоящего изобретения, обладающие способностью ингибировать sPLA2oпocpeдoвaннoe высвобождение арахидоновой кислоты, выбирают из "1Н-индол-3-гидразинов" общей формулы (А): Настоящее изобретение относится к новым гидразидам 1H-индол-3-уксусной кислоты, которые могут быть использованы в целях ингибирования sРLА2-опосредованного высвобождения арахидоновой кислоты для лечения таких состояний, как септический шок. Предшествующий уровень техники Структура и физические свойства непанкреатической секреторной фосфолипазы A2 человека (обозначаемой далее "sРLА2") очень подробно описаны в двух статьях, а именно: "Cloning and Recombinant Expression of Phospholipase A2 Present in Rheumatoid Arthritic Synovial Fluid" (Seilhamer, Jeffrey J.; Pruzanski, Waldemar; Vadas Peter; Plant, Shelley; Miller, Judi A.; Kloss, Jean; and Johnson, Lorin K.; The Journal of Biological Chemistry, vol. 264, № 10, изд. 5 апр., стр. 5335-5338, 1989); и "Structure and Properties of a Human Nonpancreatic Phospholipase A2“ (Kramer, Ruth M.; Hession, Catherine; Johansen, Berit; Hayes, Gretchen; McGray, Paula; Chow, E. Pingchang; Tizard, Richard; and Pepinsky, R. Blake; The Journal of Biological Chemistry, vol. 264, № 10, изд. 5 апр., стр. 5768-5775, 1990); при этом раскрытие указанных работ вводится в. настоящее описание посредством ссылки. Очевидно, что SPLA 2 представляет собой степень ограничивающий фермент в метаболизме арахидоновой кислоты, гидролизующий фосфолипиды мембраны. Таким образом, было бы желательно получить соединения, которые ингибируют sРLА2-опосредованное высвобождение жирных кислот (например, арахидоновой кислоты). Такие соединения могли бы быть с успехом использованы для лечения нарушений, индуцированных и/или поддерживаемых посредством сверхсинтеза sPLA 2; например, таких как септический шок; респираторный дистресс-синдром у взрослых; травмы; бронхиальная астма; аллергические риниты; ревматоидный артрит и т.п. В патенте США № 2825734 описываются индолил-3-замещенные соединения, имеющие глиоксиламидные функциональные группы. Этот патент относится к способу превращения глиоксиламидов в 3-(2-амино-1-гидроксиэтил) индолы. В патенте США № 3271416 описываются индолилалифатические кислоты, используемые в качестве агентов, защищающих от воздействия солнечного света, а также в качестве промежуточных соединений. Эти кислоты могут быть NH2-замещенными (см. определение М в п. 1 формулы изобретения), а в 5 или 6 положении они должны быть обязательно замещенными азотной или серной функциональными группами. В патенте США № 2890223 и в статье "The Synthesis of Tryptamines Related to Serotaonin" (Elliott Shaw, J. Am. Chem. Soc., Vol. 77, 1955, pp. 4319-4324) описываются некоторые амидные производные 3-индолуксусных кислот. Эти соединения использовали при получении 5-(низший алкокси)триптаминов, и при этом было установлено, что они могут быть использованы в целях воздействия на серотонин-ассоциированные функции головного мозга. где Z представляет собой органический двухвалентный радикал, имеющий формулу: 5 40575 а незамещенные положения на индолильном ядре являются независимо насыщенными водородом или нереактивным органическим радикалом. Некоторые гидразиды 1H-индол-3-уксусной кислоты настоящего изобретения, представленные формулой (А), являются предпочтительными, и для определения этих соединений используются нижеследующие термины. В частности, термин "алкил" как таковой или как часть другого заместителя означает, если это не оговорено особо, прямой или разветвленный одновалентный углеводородный радикал, такой как метил, этил, п-пропил, изопропил, п-бутил, трет-бутил, изобутил, втop-бутил, п-пентил, и п-гексил. Термин "алкенил", используемый отдельно или в сочетании с другими терминами, означает прямую или разветвленную одновалентную углеводородную группу, имеющую определенное число атомов углерода, и представленную такими группами, как винил, пропенил, кротонил, изопентенил, и различные изомеры бутенила. Термин "галоген" означает фтор, хлор, бром или йод. Термин "замещенное или незамещенное гетероциклическое кольцо с 5-10 членами" относится к соединениям, имеющим ядро, таким как пиррол, фуран, тиофен, пиридин, пиперидин, азепин, индол, хинолин, имидазол, оксазол, тиазол, пиразин, и пиримидин. Термин "карбоциклическое кольцо" означает органическое ядро, где атомами, образующими кольцо, являются лишь атомы углерода, например, ядро, происходящее от бензола, нафталина, циклопентена, циклогексана или бициклогептадиена. Термин "кислотная группа" означает органическую группу, которая при связывании с индольным ядром посредством соответствующих связующих атомов (например, алкилиденовой цепи) действует как донор протонов, способный связывать водород. Примерами "кислотных групп" являются следующие заместители: где R89 является алкилом. Предпочтительными соединениями, используемыми в настоящем изобретении, являются гидразиды 1H-индол-3-уксусной кислоты, замещенные во 2 положении группами, которые не являются водородом, и представленные формулой (I), а также их фармацевтически приемлемые соли: -5-тетразолил, -SО3Н, (I) 6 40575 где Х является кислородом или серой; R1 выбирают из групп (i), (ii) и (iii), где (i) представляет собой С4-С20-алкил, С4-С20алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4С12-циклоалкил, или (ii) представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, -SH, C1С10-алкилтио, C1-С10-алкокси, С1-С10-алкилом, карбокси, амино, или гидроксиамино; (iii) представляет собой где: "у" является целым числом от 1 до 8, R74 независимо представляет собой водород или C1-С10алкил, a R75 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, C1-С10-алкилтио, С1-С10-алкокси, C1-С10-алкилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами. R2 представляет собой галоген, C1-С3-алкил, этенил, С1-С2-алкилтио, C1-С2-алкокси, -СНО, -CN; каждый R3 независимо представляет собой водород, C1-С3-алкил, или галоген; R4, R5, R6 и R7 каждый независимо представляет собой водород, C1-С10-алкил, C1-С10-алкенил, C1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил; либо любые две смежные гидрокарбильные группы в серии R4, R5, R6 и R7, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо с 5 или 6 членами; или C1-С10галогеналкил, С1-С10-алкокси, C1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SN, -CN, -S(C1-C10-aлкил), арилтио, тиоацеталь, -С(O)O(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(О)NR82R83, где R82 и R83 независимо являются водородом, C1-С10-алкилом, C1-С10-гидроксиалкилом, либо взятые вместе с N, R82 и R83 образуют гетероциклическое кольцо с 5-8 членами; или группу формулы: где R86 независимо выбирают из водорода, металла, или C1-С10-алкила. Другими предпочтительными соединениями, используемыми при осуществлении настоящего изобретения, являются гидразиды уксусной кислоты, замещенные в 1 положении группами, которые не являются бензилом, например, такими как алкил и арил. Указанными гидразидами уксусной кислоты являются соединения формулы (II) и их фармацевтически приемлемые соли; где каждый R76 независимо выбирают из водорода, С1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =O; р является числом от 1 до 8; Z представляет собой связь, -О-, -N(С1-С10алкил)-, -NH, или -S-; и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3Н, (II) 7 40575 где: Х является кислородом или серой; R11 выбирают из групп (i), (ii) и (iii), где: (i) представляет собой С4-С20-алкил, С4-С20алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4С12-циклоалкил, или (ii) представляет собой арил или арил, замещенный галогеном, нитро, -CN, -СНО, -ОН, -SH, С1-С10-алкилом, C1-С10-алкилтио, С1-С10-алкокси, карбокси, амино, или гидроксиамино; и (iii) представляет собой -(NH)-(R81), где R81 является группой, указанной для (i) или (ii); R12 представляет собой водород, галоген, С1-С3-алкил, этенил, С1-С2-алкилтио, С1-С2-алкокси, -СНО, -CN; каждый R13 независимо представляет собой водород, C1-С3-алкил, или галоген; R14, R15, R16 и R17 каждый независимо представляет собой водород, C1-С10-алкил, C1-С10-алкенил, C1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил; либо любые две смежные гидрокарбильные группы в серии R14, R15, R16 и R17, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо с 5 или 6 членами; или C1-С10-галогеналкил, С1-С10-алкокси, C1С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SN, -CN, -S(C1-C10алкил), арилтио, тиоацеталь, -С(O)O(С1-С10-алкил), гидразино, гидразидо, -NH2, -NО2, NR82R83 и -C(O)NR82R83, где R82 и R83 независимо являются водородом, C1-С10-алкилом, С1-С10-гидроксиалкилом, либо R82 и R83, взятые вместе с N, образуют гетероциклическое кольцо с 5-8 членами; или группу формулы: где R86 независимо представляет собой водород, металл, или C1-С10-алкил. Другими предпочтительными соединениями, используемыми при осуществлении настоящего изобретения, являются гидразиды уксусной кислоты, замещенные в 5 или 6 положении группами, которые не являются метокси, например, кислотными группами или простыми производными этих кислотных групп. Такими гидразидами уксусной кислоты являются соединения формулы (III) и их фармацевтически приемлемые соли: где: каждый R76 независимо выбирают из водорода, C1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О; р является числом от 1 до 8; Z представляет собой связь, -О-, -N(С1-С10алкил)-, -NH, или -S-; и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3Н, (III) где: X является кислородом или серой; R21 выбирают из групп (i), (ii) и (iii), где: (i) представляет собой С4-С20-алкил, С4-С20алкенил, С4-С20-алкинил, С4-С20-галогеналкил, С4С12-циклоалкил, или (ii) представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, -SH, C1С10-алкилтио, C1-С10-алкокси, C1-С10-алкилом, карбокси, амино, или гидроксиамино; 8 40575 (iii) представляет собой: где: "у" является целым числом от 1 до 8, R74 независимо представляет собой водород или С1-С10алкил, a R75 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, C1-С10-алкилтио, С1-С10-алкокси, С1-С10-алкилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами; R22 представляет собой водород, галоген, С1-С3-алкил, этенил, С1-С3-алкилтио, С1-С3-алкокси, -СНО, -CN; каждый R23 независимо представляет собой водород, С1-С3-алкил, или галоген; R24, R25, R26 и R27 каждый независимо представляет собой водород, C1-С10-алкил, C1-С10-алкенил, C1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил; или любые две соседние гидрокарбильные группы в серии R24, R25, R26 и R27, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо; или C1С10-галогеналкил, С2-С10-алкокси, C1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SN, -CN, -S(С1-С10-алкил), арилтио, тиоацетил, -С(O)O(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83 и -C(O)NR82R83, где R82 и R83 независимо представляют собой водород, С1-С10-алкил, С1-С10-гидроксиалкил, либо R82 и R83, взятые вместе с N, образуют гетероциклическое кольцо с 5-8-ю членами; или группу формулы: где R86 независимо представляет собой водород, металл, или C1-С10-алкил. Наиболее предпочтительными соединениями являются гидразиды уксусной кислоты формулы (V) и их фармацевтически приемлемые соли: где: каждый R76 независимо выбирают из водорода, C1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =O; р является числом от 1 до 8; Z представляет собой связь, -О-, -N(C1-C10алкил)-, -NH, или -S-; и Q представляет собой –СОN(R82R83), -5тетразолил, -SO3H, (V) где: Х является кислородом; R51 представляет собой 9 40575 где: R84 представляет собой водород, или C1-С10алкил, а R87 представляет собой арил или арил, замещенный галогеном, -CN, -СНО, -ОН, нитро, фенилом, -SH, C1-С10-алкилтио, C1-С10-алкилом, C1-С10-алкоксилом, карбоксилом, амино, гидроксиамино, или замещенным или незамещенным гетероциклическим кольцом с 5-8 членами; R52 представляет собой галоген, метилтио, или C1-С3-алкил; каждый R53 представляет собой водород или галоген; R54, R55, R56 и R57 каждый независимо представляет собой водород, C1-С10-алкил, C1-С10-алкенил, C1-С10-алкинил, С3-С8-циклоалкил, арил, аралкил; или любые две соседние гидрокарбильные группы в серии R54, R55, R56 и R57, взятые вместе с кольцевыми атомами углерода, с которыми они связаны, образуют замещенное или незамещенное карбоциклическое кольцо; или C1-С10-галогеналкил, С2-С10-алкокси, С1-С10-галогеналкокси, С4-С8-циклоалкокси, фенокси, галоген, гидрокси, карбоксил, -SN, -CN, -S(C1-C10-алкил), арилтио, тиоацеталь, -С(О)О(С1-С10-алкил), гидразино, гидразидо, -NH2, -NO2, -NR82R83, и -C(О)NR82R83, где R82 и R83 независимо представляют собой водород, С1-С10-алкил, C1-С10-гидроксиалкил, либо R82 и R83, взятые вместе с N, образуют гетероциклическое кольцо с 5-8 членами; или группу формулы: где R86 независимо представляет собой водород, металл, или C1-С10-алкил. Примерами новых соединений, которые могут быть использованы в целях настоящего изобретения, являются следующие соединения: 5-циклопентокси-2-этил-1-(фенилметил)-1Ниндол-3-уксусной кислоты гидразид; 2-этил-5-метокси-1-(фенилметил)-1Н-индол3-уксусной кислоты гидразид; 2-этил-5-метил-1-(фенилметил)-1Н-индол-3уксусной кислоты гидразид; 5-метокси-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты гидразид; 1-[(3-хлорофенил)метил]-5-метокси-2-метил1Н-индол-3-уксусной кислоты гидразид; 2-хлоро-5-метокси- 1-(фенилметил)- 1H-индол-3-уксусной кислоты гидразид; 2-бромо-5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты гидразид; 5-метокси-2-(метилтио)-1-(фенилметил)-1Ниндол-3-уксусной кислоты гидразид; 5-хлоро-2-метил-1-(фенилметил)-1Н-индол3-уксусной кислоты гидразид; 5-карбокси-[(3-хлорфенил)метил]-2-метил1Н-индол-3-уксусной кислоты гидразид; и их смеси. В другом своем варианте настоящее изобретение относится к солям вышеуказанных гидразидов 1H-индол-3-уксусной кислоты, имеющих формулы I, II, III, V, или к солям вышеперечисленных соединений. Многие из этих солей (полученных из соответствующего функционального исходного соединения индолилуксусной кислоты или сложного эфира) являются в большей степени водорастворимыми и физиологически усвояемыми, чем исходные соединения. Примерами солей, входящими в объем настоящего изобретения, являются соли щелочных металлов, таких как натрий, калий и кальций, а также органических аминов, происходящих из гликозамина, морфолина, холина или диэтиламина. где: каждый R76 независимо выбирают из водорода, C1-С10-алкила, гидрокси, либо оба R76, взятые вместе, представляют собой =О; р является числом от 1 до 8; Z представляет собой связь, -О-, -N(C1-C10алкил)-, -NH, или -S-; и Q представляет собой -CON(R82R83), -5-тетразолил, -SO3Н, 10 40575 Способы синтеза Синтез гидразидов 1H-индол-3-уксусной кислоты, имеющих структуру (I), может быть осуществлен известными способами. Процедуры синте за соединений настоящего изобретения проводили в соответствии с нижеприведенными реакционными схемами: Схема 1 В первой схеме сложные эфиры 1H-индол-3уксусной кислоты, II, могут быть легко алкилированы с использованием алкилгалида или арилалкилгалида в растворителе, таком как N,N-диметилформамид (ДМФ) в присутствии основания (метод а), в результате чего могут быть получены промежуточные сложные эфиры 1-алкил-1Н-индол-3уксусной кислоты, III. Особенно предпочтительными основаниями являются t-бутоксид калия и гидрид натрия. Причем предпочтительно сначала проводить реакцию индола II с основанием, в результате которой образуется соль соединения II, а затем добавлять алкилирующий агент. Реакцию алки лирования предпочтительно проводить при комнатной температуре. В результате обработки сложных эфиров 1-алкил-1Н-индол-3-уксусной кислоты, III, гидразином или гидразингидратом в этаноле (метод b) получают нужные гидразиды 1-алкил-1Н-индол-3-уксусной кислоты, I. Указанную конденсацию с образованием соединения I обычно осуществляют при температуре перегонки растворителя в течение периода времени от 1 ч до 24 ч. Промежуточные сложные эфиры 1H-индол3-уксусной кислоты, II, могут быть синтезированы несколькими путями, например, как проиллюстрировано в схеме 2. Схема 2 11 40575 1H-индол-3-уксусные кислоты, IV, могут быть легко этерифицированы в спирте, таком как метанол, в присутствии сильной кислоты (метод с), такой как серная кислота, с получением соединения II. Замещенные фенилгидразины V могут быть подвергнуты реакции с производными левулиновой кислоты, VI, в соответствии с хорошо известным синтезом по Фишеру (метод d) (см. R.B. Colin и Е.Е. Fisher, J. Am. Chem. soc., 1948, 70, 3421) с непосредственным получением индола II. В этой реакции в качестве растворителя использовали этанол (при температуре перегонки), а в качестве кислотного катализатора использовали хлороводород. Индолы, которые являются незамещенными в 3 положении, VII, могут быть сначала алкилированы с получением цинковых солей соединения VII, а затем эти соли могут быть обработаны алкил 2-бромоалканоатом (метод е) с по лучением II (см. Yochihiko Ito, Hideaki Sato, Masahiro Murakami, J. Org. Chem., 1991, 56, 4864-4867). Цинковые соли соединения VII могут быть получены при помощи реакции индолов VII сначала с пбутиллитием, используя тетрагидрофуран в качестве растворителя, а затем с хлоридом цинка в простом эфире. Для этой реакции растворитель обычно заменяют толуолом путем удаления простого эфира и ТГФ при пониженном давлении и добавления толуола. Многие промежуточные индолы VII являются коммерчески доступными соединениями. Для получения дополнительных замещенных производных индолов VII могут быть использованы реакции, проиллюстрированные в Схеме 3 (см. Robin D. Clark, Joseph M. Muchowski, Lawrence Е. Fisher Lee A. Flippin, David B. Repke, Michel Souchet, Synthesis, 1991, 871-878). Схема 3 Производные орто-нитротолуола, VIII, подвергают каталитическому восстановлению, используя в качестве катализатора палладированный уголь, и получают орто-метиланилины, IX, которые обрабатывают ди-mpem-бутилдикарбонатом в ТГФ при температуре перегонки (метод g), в результате чего получают N-третбутоксикарбониланилины, X. Дианион соединения X, полученный в ТГФ путем обработки двумя эквивалентами втор-бутиллития, подвергают реакции с одним эквивалентом амида Nметокси-N-метиалкановой кислоты, в результа те чего получают (метод h) арилкетон, XI. Посредством обработки трифторуксусной кислотой (метод i), эти кетоны подвергают циклизации и разблокированию у атома азота, и получают индолы, VII. Индолы типа VII, которые являются замещенными в 5 положении нитрогруппой, получают (см. Wayland E. Noland, Lowell R. Smith, и Donald С. Johnson, J. Med. Chem., 1963, 28, 22622266) путем добавления нитрата натрия к соответствующему индолу, предварительно растворенному в серной кислоте (метод j). 12 40575 Производные, где R4 представляет собой 1(гидроксифенил)-метил-, получают путем гидрогенолиза соответствующих 1-(бензилоксифенил) метиловых производных (метод k). Производные, где R4 представляет собой 1-(аминофенил)метил-, могут быть легко получены из соответствующих нитросоединений (метод 1). Для синтеза соединений, где R1-заместителем является гидрокси, метокси-замещенную индол-3 -уксусную кислоту, XII (полученную путем гидролиза соединения III), подвергают деметилированию с помощью реакции с ВВr3 (метод m), в результате чего получают соединение XIII, которые (см. Tsung-Ying Shen and Charles A. Winter, Adv. Drug Res., 1977, 12, 176) подвергают этерификации методом с, и получают соединение XIV. Гидрокси-производные XIV могут быть алкилированы путем обработки арилалкилгалидом в присутствии карбоната калия (метод n) с получением промежуточных сложных эфиров III, где R1 является арилметокси. Схема 4 13 40575 Метокси-замещенные гидразиды 1H-индол-3-уксусной кислоты могут быть подвергнуты деметилированию с непосредственным получением гидрокси-замещенных гидразинов уксусной кислоты (в условиях использования ВВr3, метод о). Эти соединения могут быть подвергнуты прямому алкилированию с помощью сложного эфира бромоалкановой кислоты (метод w) и с использованием гидрата натрия в качестве основания и ДМСО в качестве растворителя, в результате чего может быть получен гидразид кис лого эфира. Этот гидразид кислого эфира гидролизуют методом m и получают гидразид карбоновой кислоты. Соединения структуры I и III, где R1 является фенилом, получают путем фенилирования (см. N. Miyura, Т. Eshiyama, H. Sasaki, M. Ishikawa, M. Saton и A. Suzuki, J. A. Chem. Soc., 1989 111, 3124) промежуточных соединений, где R1 является Вr (метод р). Это фенилирование может быть осуществлено исходя из соответствующего сложного бромо-эфира или бромо-гидразида. Промежуточные сложные эфиры 1H-индол-3-уксусной кислоты, III, где R3 является хлором, получали посредством реакции сложного эфира 1H-индол-3-уксусной кислоты, III, где R3 является водородом, с N-хлоросукцинимидом (метод q). 14 40575 Промежуточное соединение, а именно, сложный эфир 1H-индол-3-уксусной кислоты, III, где R1 является карбокси-группой, получают путем селективной этерификации производного дикарбоновой кислоты (синтезированной посредством гидролиза сложного эфира двухосновной кислоты методом u), в результате чего образуется производное сложного моноэфира 1H-индол-3-уксусной кислоты. Аналогичным образом, в результате обработки N-бромосукцинимидом (метод r) или метансульфенилхлоридом (метод s) получали 2бромо- и 2-метилтиоиндолы, соответственно. 2метилтиоиндол может быть подвергнут окислению с использованием m-хлоропербензойной кислоты, и с получением 2-метилсульфинилиндола (метод t). 15 40575 Представленные ниже примеры осуществления настоящего изобретения приводятся лишь в иллюстративных целях. Однако каждому специалисту очевидно, что указанные примеры не следует рассматривать как некое ограничение объема настоящего изобретения. удаляли, и затем смесь перемешивали еще 1 ч. Полученную смесь выливали в смесь 500 мл эфира и 500 мл 1N раствора НСl. Затем органический слой отделяли, промывали водой и осушали сульфатом натрия. После удаления растворителя получали 17,7 г неочищенного 1-(2-трет-бутоксикарбониламино-5-этоксифенил)-2-пропанола. Этот полученный материал и 25 г трифторуксусной кислоты в 400 мл СН2Сl2 перемешивали при комнатной температуре в течение 16 ч. Полученную смесь дважды промывали водой, насыщенным раствором сульфата натрия и осушали Na2CO3. После удаления растворителя полученный продукт хроматографировали на двуокиси кремния, элюируя толуолом, в результате чего получали 4,95 г (выход 41%) 5-этокси-2-метил-1Н-индола (т. пл. 76-77°С). Элементный анализ для C11H13NO: Вычислено: С, 75,40; Н, 7,48; N, 7,99. Найдено: С, 77,07; Н, 7,83; N, 8,09. E. Метиловый сложный эфир 5-этокси-2-метил-1Н-индол-3-уксусной кислоты К охлажденному раствору 4,85 г (0,0277 М) 5-этокси-2-метил-1Н-индола в 40 мл ТГФ добавляли 17,3 мл (0,0277 М) 1,6М раствора п-бутиллития в гексане, поддерживая температуру ниже -10°С в бане из льда/этанола. Через 0,25 ч к смеси добавляли 27,7 мл (0,0277 М) 1М раствора ZnCl 2 в эфире. После этого охлаждающую баню удаляли, смесь перемешивали в течение 2ч, и концентрировали при пониженном давлении, в результате чего получали воскообразное вещество, которое растворяли в 40 мл толуола. Затем к этому раствору добавляли 2,62 мл (0,0277 М) метил 2-бромоацетата, смесь перемешивали 24 ч и выливали в 100 мл 1N раствора НСl и 100 мл EtOAc. Органический слой промывали дважды водой, осушали сульфатом натрия и концентрировали при пониженном давлении. Полученный остаток хроматографировали на двуокиси кремния и элюировали 5% EtOAc/толуолом, в результате чего получали 5,0 г (73%) 5-этокси-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для С14Н17NО3: Вычислено: С, 68,00; Н, 6,93; N, 5,66. Найдено: С, 68,04; Н, 7,07; N, 5,77. F. 5-этокси-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метиловый сложный эфир Суспензию 80 г (2 мМ) 60% NaH/минерального масла промывали гексаном и помещали в раствор 8 мл ДМФ. После охлаждения в ледяной бане добавляли 494 мг (2 мМ) 5-этокси-2-метил1Н-индол-3-уксусной кислоты метилового сложного эфира, и полученную смесь перемешивали 1 ч, а затем добавляли 0,24 мл бензилбромида, и смесь перемешивали в течение 1,5 ч. После этого смесь разбавляли водой, экстрагировали EtOAc, после чего раствор EtOAc промывали водой/NaCl и осушали сульфатом магния. Полученный раствор концентрировали при пониженном давлении, и полученный продукт хроматографировали на двуокиси кремния, элюируя смесью 25% EtOAc/гексана, в результате чего получали 372 мг (выход 55%) 5-этокси-2-метил-1-(фенилметил)-1Н-индол3-уксусной кислоты метилового сложного эфира, Пример 1 Получение гидразида 5-этокси-2-метил-1 (фенилметил)-1Н-индол-3-уксусной кислоты А. 4-этокси-2-метил-1 -нитробензол Раствор 15,3 г (0,1 М) 3-метил-4-нитрофенола, 23,4 г (0,15 М) йодометана и 27,6 г (0,2 М) К2СО3 в 250 мл метилэтилкетона нагреватели с обратным холодильником в течение 16 ч. После охлаждения реакционную смесь выливали в воду и экстрагировали этилацетатом. После этого EtOAc-раствор промывали водой, 1N раствором NaOH, затем снова водой, и осушали сульфатом натрия. После удаления растворителя при пониженном давлении, получали 16,8 г (выход 93%) 4-этокси-2-метил-1-нитробензола (т. пл. 41-43°С). Элементный анализ для С9Н11NО3: Вычислено: С, 59,66; Н, 6,12; N, 7,73. Найдено: С, 59,58; Н, 6,28; N, 7,79. В. 4-этокси-2-метилаланин 4-этокси-2-метил-1-нитробензол (16,5 г, 0,091 М) гидрогенизировали в течение 4 ч под давлением водорода 60 фунт/кв. дюйм (4218 г/см2) в 135 мл этанола, используя в качестве катализатора 1,6 г Pd/C. Катализатор фильтровали, а полученный продукт подвергали дистилляции при 54-55°С/0,08 мм рт. ст., в результате чего получали 10,62 г (выход 78%) 4-этокси-2-метиланилина. Элементный анализ для C9H13NO: Вычислено: С, 71,49; Н, 8,67; N, 9,26. Найдено: С, 72,07; Н, 8,95; N, 10,42. С. N-трет-бутоксикарбонил-4-этокси-2-метиланилин Раствор 4-этокси-2-метиланилина (10,5 г, 0,0695 М) и 15,5 г (0,071 М) ди-трет-бутилкарбоната в 200 мл тетрагидрофурана медленно нагревали до температуры перегонки, и смесь поддерживали при этой температуре в течение 2 ч. После охлаждения реакционную смесь концентрировали при пониженном давлении, а остаток растворяли в EtOAc. Раствор EtOAc промывали 1N раствором лимонной кислоты, осушали сульфатом натрия и концентрировали при пониженном давлении. В результате кристаллизации полученного остатка из гексана получали 10,26 г (выход 59%) N-трет-бутоксикарбонил-4-этокси-2-метиланилина (т. пл. 55-56°С). Элементный анализ для C14H21NО3: Вычислено: С, 66,91; Н, 8,42; N, 5,57. Найдено: С, 66,69; Н, 8,23; N, 5,52. D. 5-этокси-2-метил-1Н-индол Раствор 1,3 М втop-бутиллития/циклогексана (105,7 мл, 0,137 М) медленно добавляли к 17,25 г (0,0687 М) N-трет-бутоксикарбонил-4-этокси-2-метиланилина в 250 мл ТГФ, поддерживая температуру ниже -40°С в бане из сухого льда/ этанола. Через 0,25 ч по капле добавляли 7,21 г (0,07 М) N-метокси-N-метилацетамида в равном объеме ТГФ. После этого реакционную смесь перемешивали в течение 1 ч, охлаждающую баню 16 40575 который отверждали при отстаивании (точка пл. 82-85°С). Элементный анализ для C21H23NO3: Вычислено: С, 74,75; Н, 6,87; N, 4,15. Найдено: С, 75,60; Н, 7,04; N, 4,03. G. Гидразид 5-этокси-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты Раствор 323 мг (0,95 мМ) 5-этокси-2-метил1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира и 1,5 мл 98% гидразина в 5 мл этанола нагревали с обратным холодильником в течение 16 ч. Полученную смесь охлаждали, разбавляли водой и экстрагировали EtOAc. Раствор EtOAc промывали смесью воды и NaCl, осушали сульфатом магния, и концентрировали при пониженном давлении. Полученный остаток кристаллизовали из МеОН, в результате чего получали 77 мг (выход 23%) гидразида 5-этокси-2-метил1-(фенилметил)-1Н-индол-3-уксусной кислоты (т. пл. 145-148°С). Элементный анализ для C20H23N3O2: Вычислено: С, 71,19; Н, 6,87; N, 12,45. Найдено: С, 71,49; Н, 6,94; N, 12,38. Пример 2 Получение гидразида 5-циклопентокси-2-этил1-(фенилметил)-1Н-индол-3-уксусной кислоты А. 4-циклопентокси-2-метил-1 -нитробензол Используя процедуру, описанную в примере 1 (часть А), 15,3 г (0,1 М) 3-метил-4-нитрофенола подвергали реакции с 16,1 мл (0,15 М) бромоциклопентана и 27,6 г (0,2 М) К2СО3, в результате чего получали 17,5 г (выход 79%) 4-циклопентокси-2метил-1-нитробензола в виде маслообразного вещества. В. 4-циклопентокси-2-метиланилин 4-циклопентокси-2-метил-1-нитробензол (17,5 г, 0,0792 М) гидрогенизировали в соответствии с процедурой, описанной в примере 1 (часть В), и получали 10,3 г (выход 68%) 4-циклопентокси-2метиланилина (т. кип. 100-110°С/0,07 мм рт. ст.). Элементный анализ для C12H17NO: Вычислено: С, 75,35; Н, 8,96; N, 7,32. Найдено: С, 75,50; Н, 9,10; N, 7,57. С. N-трет-бутоксикарбонил-4-циклопентокси2-метиланилин В соответствии с процедурой, описанной в примере 1 (часть С), 10,3 г (0,54 М) 4-циклопентокси-2-метиланилина подвергали реакции с 12,24 г (0,056 М) ди-трет-бутилдикарбоната, в результате чего после кристаллизации из толуола/гексана получали 6,3г (выход 40%) N-трет-бутоксикарбонил-4-циклопентокси-2-метиланилина (т. пл. 75-77°С). Элементный анализ для C17Н25NО3: Вычислено: С, 70,07; Н, 8,65; N, 4,81. Найдено: С, 69,79; H, 8,67; N, 4,60. D. 1-[2-(трет-бутоксикарбониламино)-5-циклопентоксифенил]-2-бутанон Раствор 1,3 М втop-бутиллития/циклогексана (33,3 мл, 0,0433 М) медленно добавляли к 6,3 г (0,0216 М) N-трет-бутоксикарбонил-4-циклопентокси-2-метиланилина в 80 мл ТГФ, поддерживая температуру ниже -40°С в бане из сухого льда/ ацетона. Баню удаляли, температуру повышали до -20°С, а затем баню заменяли. После понижения температуры до -60°С к смеси по капле добавляли 2,57 г (0,022 М) N-метокси-N-метилпропана мида в равном объеме ТГФ. Полученную реакционную смесь перемешивали в течение 1 ч, охлаждающую баню удаляли, а затем перемешивание продолжали еще в течение 1 ч. Полученный раствор выливали в смесь 200 мл эфира и 200 мл 1N раствора НСl. Органический слой отделяли, промывали водой и осушали сульфатом натрия. После удаления растворителя остаток кристаллизовали из гексана и получали 3,58 г (выход 48%) 1(2-(трет-бутоксикарбониламино)-5-циклопентоксифенил)-2-бутанола (т. пл. 71-73°С). Элементный анализ для C20H29NO4: Вычислено: С, 69,14; H, 8,41; N, 4,03. Найдено: С, 69,17; H, 8,42; N, 4,14. E. 5-циклопентокси-2-этил-1Н-индол 1-[2-(трет-бутоксикарбониламино-5-циклопентоксифенил]-2-бутанон (6,45 г, 0,0186 М) в 120 мл метиленхлорида и 20 мл трифторуксусной кислоты перемешивали в течение 20 ч, промывали водой, раствором NaHCО3 и полученный продукт хроматографировали на двуокиси кремния (элюент : 5% EtOAc/толуол), в результате чего получали 2,35% (выход 50%) 5-циклопентокси-2этил-1Н-индола в виде маслообразного вещества. Элементный анализ для C15H19NO: Вычислено: С, 78,56; Н, 8,35; N,6,11. Найдено: С, 78,84; Н, 8,41; N, 6,19. F. 5-циклопентокси-2-этил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 2,33 г (0,0102 М) 5-циклопентокси-2-этил-1Н-индола обрабатывали 6,4мл (0,0102 М) 1,6М раствора п-бутиллития в гексане, 10,2 мл (0,0102 М) 1М раствора ZnCl2 в эфире, и 0,97 мл (0,0102 М) метил 2-бромоацетата, в результате чего после хроматографии на двуокиси кремния (элюент: 5% EtOAc/толуол) получали 1,8 г (59%) 5-циклопентокси-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C18H23NO3: Вычислено: С, 71,74; Н, 7,69; N, 4,65. Найдено: С, 71,64; Н, 7,89; N, 4,70. G. 5-циклопентокси-2-этил- 1-(фенилметил)1H-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 602 мг (2 мМ) 5-циклопентокси-2-этил-1H-индол-3-уксусной кислоты метилового сложного эфира превращали в 427 мг (выход 55%, маслообразное вещество) 5-циклопентокси2-этил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира, очищенного с помощью хроматографии на двуокиси кремния (элюент: смесь 33% EtOAc/гексан). Элементный анализ для C25H29NO3: Вычислено: С, 76,78; Н, 7,47; N, 3,58. Найдено: С, 76,68; H, 7,62; N, 3,62. H. Гидразид 5-циклопентокси-2-этил-1-(фенилметил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G) 417 мг (1,07 мМ) 5-циклопентокси-2-этил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 1,2 мл гидразина, в результате чего получали 163 мг (выход 39%) 5-циклопентокси2-этил-1-(фенилметил)-1Н-индол-3-уксусной кис 17 40575 лоты гидразида (после кристаллизации из МеОН, т.пл. 117-118°С). Элементный анализ для C24H29N3O2: Вычислено: С, 73,62; H, 7,47; N, 10,73. Найдено: С, 73,52; H, 7,61; N, 10,55. Пример 3 Получение гидразида 2-этил-5-метокси-1(фенилметил)-1Н-индол-3-уксусной кислоты А. N-трет-бутоксикарбонил-4-метокси-2-метиланилин В соответствии с процедурой, описанной в примере 1 (часть С), 13,7 г (0,1 М) 4-метокси-2-метиланилина подвергали реакции с 25 г (0,1145 М) ди-трет-бутилдикарбоната, в результате чего после кристаллизации из гексана получали 17,25 г (выход 73%) N-трет-бутоксикарбонил-4-метокси-2метиланилина (т. пл. 80-82°С). Элементный анализ для C13H19NO3: Вычислено: С, 65,80; H, 8,07; N, 5,90. Найдено: С, 65,86; H, 8,15; N, 5,61. В. 1-[2-(трет-бутоксикарбониламино)-5-метоксифенил]-2-бутанон В соответствии с процедурой, описанной в примере 2, (часть D), 11,85 г (0,05 М) N-трет-бутоксикарбонил-4-метокси-2-метиланилина обрабатывали 1,3 М смеси втор-бутиллития/циклогексана (81 мл, 0,105 М) и 6,1 г (0,052 М) N-метокси-N-метилпропанамида, в результате чего получали 10,9 г (выход 74%) 1-[2-(трет-бутоксикарбониламино)-5метоксифенил]-2-бутанона (после хроматографии на двуокиси кремния, используя в качестве элюента смесь 5% EtOAc/толуола) при т. пл. 80-81oС. Элементный анализ для C16H23NO4: Вычислено: С, 65,51; Н, 7,90; N, 4,77. Найдено: С, 65,69; Н, 7,89; N, 4,90. С. 2-этил-5-метокси-1Н-индол В соответствии с процедурой, описанной в примере 2 (часть Е), 1-[2-(трет-бутоксикарбонил)5-метоксифенил]-2-бутанон (7,33 г, 0,025 М) обрабатывали 20 мл трифторуксусной кислоты, и полученный продукт хроматографировали на двуокиси кремния, элюируя смесью 20% EtOAc/гексана, в результате чего получали 2,54 г (выход 58%) 2-этил-5-метокси-1Н-индола в виде белого твердого вещества (т. пл. 49-50°С). Элементный анализ для C11H13NO: Вычислено: С, 75,40; Н, 7,48; N, 7,99. Найдено: С, 75,64; Н, 7,61; N, 8,04. D. 2-этил-5-метокси-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 3,5 г (0,02 М) 5-метокси-2этил-1Н-индола обрабатывали 12,5 мл (0,02 М) 1,6М раствора п-бутиллития в гексане, 20 мл (0,02 М) 1М раствора ZnCl2 в эфире и 1,89 мл (0,02 М) метил 2-бромоацетата, в результате чего после хроматографии на двуокиси кремния (толуол ® 10% EtOAc/толуол) получали 3,32 г (59%) 2-этил-5метокси-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для С14Н17NО3: Вычислено: С, 67,99; Н, 6,93; N, 5,66. Найдено: С, 67,73; Н, 6,94; N, 5,39. Е. 2-этил-5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты метиловый сложный эфир Раствор 2,47 г (0,01 М) 2-этил-5-метокси-1Ниндол-3-уксусной кислоты метилового сложного эфира в 25 мл ДМФ обрабатывали 1,12 г (0,01 М) tбутоксида калия, перемешивали в течение 0,5 ч, а затем добавляли 1,15 мл (0,01 М) бензилхлорида. Через 72 ч реакционную смесь разбавляли водой, экстрагировали EtOAc, и после этого раствор EtOAc промывали 4 раза водой, а затем осушали сульфатом натрия. После концентрирования при пониженном давлении полученный продукт очищали с помощью хроматографии на двуокиси кремния, элюируя градиентом смеси толуола и 10% EtOAc/толуола, в результате чего получали 1,5 г (выход 44%) 2этил-5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C21H23NO3: Вычислено: С, 74,75; Н, 6,87; N, 4,15. Найдено: С, 75,00; Н, 6,99; N, 4,28. F. Гидразид 2-этил-5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 748 мг (2,2 мМ) 2-этил-5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 2,2 мл гидразина, в результате чего получали 552 мг (выход 74%) гидразида 2-этил-5-метокси-1-(фенилметил)-1H-индол-3-уксусной кислоты (т. пл. 138-140°С), который кристаллизовали из реакционной смеси путем охлаждения. Элементный анализ для C20H23N3O2: Вычислено: С, 71,19; Н, 6,87; N, 12,45. Найдено: С, 71,13; Н, 6,86; N, 12,33. Пример 4 Получение гидразида 1-([1,1'-бифенил]-2-илметил)-2-этил-5-метокси-1H-индол-3-уксусной кислоты А. 1-([1,1'-бифенил]-2-илметил)-2-этил-5-метокси-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 483 мг (2 мМ) 2-этил-5-метокси-1Н-индол-3-уксусной кислоты метилового сложного эфира обрабатывали 48 мг (2 мМ) 60% NaH/минерального масла и 0,37 мл (2 мМ) 2-(бромометил)-бифенила, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 362 мг (44%) 1-([1,1'-бифенил]-2-илметил)-2-этил-5-метокси-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для С27Н27NO3: Вычислено: С, 78,42; Н, 6,58; N, 3,39. Найдено: С, 78,70; Н, 6,59; N, 3,43. В. Гидразид 1-([1,1'-бифенил]-2-илметил)-2этил-5-метокси-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 859 мг (2,15 мМ) 1-([1,1'-бифенил]-2-илметил)-2-этил-5-метокси-1Н-индол-3уксусной кислоты метилового сложного эфира подвергали реакции с 2,5, мл гидразина, в результате чего после кристаллизации из МеОН получали 300 мг (выход 36%) гидразида 1-([1,1'-бифенил]-2-илметил)-2-этил-5-метокси-1Н-индол-3уксусной кислоты (т. пл. 123-125°С). Элементный анализ для C26H27N3O2: Вычислено: С, 75,52; Н, 6,58; N, 10,16. Найдено: С, 75,29; Н, 6,65; N, 9,95. 18 40575 Пример 5 Получение гидразида 5-метокси-1-(фенилметил)-2-пропил-1Н-индол-3-уксусной кислоты А. 1-[2-трет-бутоксикарбониламино)-5-метоксифенил]-2-пентанон В соответствии с процедурой, описанной в примере 2 (часть D), 15,17 г (0,064 М) N-трет-бутоксикарбонил-4-метокси-2-метиланилина обрабатывали раствором 1,3 М втор-бутиллития/циклогексана (100 мл, 0,13 М) и 8,4 г (0,064 М) N-метокси-N-метилбутанамида, в результате чего после хроматографии на двуокиси кремния (элюент: 5% EtOAc/толуол) получали 14,31 г (выход 73%) 1(трет-буткосикарбониламино-5-метоксифенил)-2пентанона (т. пл. 77-78°С). Элементный анализ для C17H25NO4: Вычислено: С, 66,43; Н, 8,20; N, 4,56. Найдено: С, 66,42; Н, 8,09; N, 4,71. В. 5-метокси-2-пропил-1Н-индол В соответствии с процедурой, описанной в примере 2 (часть Е), 1-[2-трет-бутоксикарбониламино)-5-метоксифенил]-2-пентанон (14,27 г, 0,0465 М) обрабатывали 20 мл трифторуксусной кислоты, и полученный продукт кристаллизовали из гексана, в результате чего получали 5,5 г (выход 58%) 5-метокси-2-пропил-1Н-индола в виде белого твердого вещества (т. пл. 49-50°С). Элементный анализ для C12H15NO: Вычислено: С, 76,16; Н, 7,99; N, 7,40. Найдено: С, 76,36; Н, 8,07; N, 7,52. С. 5-метокси-2-пропил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 5,125 г (0,0271 М) 5-метокси2-пропил-1Н-индола обрабатывали 16,9 мл (0,0271 М) 1,6М раствора п-бутиллития в гексане, 27,1 мл (0,0271 М) 1М раствора хлорида цинка в эфире, и 2,7 мл (0,0271 М) метил 2-бромоацетата, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 4,65 г (66%) 5-метокси-2-пропил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C15H19NО3: Вычислено: С, 68,94; Н, 7,33; N, 5,36. Найдено: С, 68,69; Н, 7,36; N, 5,63. D. 5-метокси-1-(фенилметил)-2-пропил-1Ниндол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 522 мг (2 мМ) 5-метокси-2пропил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 48 мг (2 мМ) смеси 60% NaH и минерального масла и 0,24 мл (2 мМ) бензилбромида, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 501 мг (71%) 5-метокси-1-(фенилметил)-2-пропил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Е. Гидразид 5-метокси-1-(фенилметил)-2пропил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 480 мг (1,37 мМ) 5-метокси-1(фенилметил)-2-пропил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 1,4 мл гидразина, в результате чего после кристаллизации из МеОН получали 56 мг (выход 74%) 5-метокси-1-(фенилметил)-2-пропил-1Н-индол-3-уксусной кислоты гидразида (т. пл. 140141°С). Элементный анализ для C21H25N3О2: Вычислено: С, 71,77; Н, 7,17; N, 11,96. Найдено: С, 71,98; Н, 7,12; N, 11,98. Пример 6 Получение гидразида 2-этил-5-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты А. N-трет-бутоксикарбонил-2,4-диметиланилин В соответствии с процедурой, описанной в примере 1 (часть С), 27,4 г (0,2 М) 2,4-диметиланилина подвергали реакции с 50 г (0,229 М) ди-третбутилдикарбоната, в результате чего после кристаллизации из гексана получали 18,42 г (выход 76%) N-трет-бутоксикарбонил-2,4-диметиланилина (т. пл. 90-91°С). Элементный анализ для C13H19NО2: Вычислено: С, 70,56; Н, 8,65; N, 6,33. Найдено: С, 67,18; Н, 8,90; N, 5,39. В. 2-этил-5-метил-1Н-индол В соответствии с процедурой, описанной в примере 1 (часть D), 11,05 г (0,05 М) N-трет-бутоксикарбонил-2,4-диметиланилина подвергали реакции с 81 мл 1,3 М втор-бутиллития и 6,1 г (0,05 М) N-метокси-N-метилпропанамида, в результате чего получали неочищенный 1—[2-(трет-бутоксикарбониламино)-5-метилфенил]-2-пентанол. Этот полученный материал обрабатывали трифторуксусной кислотой и кристаллизовали из EtOAc/гексана, в результате чего получали 1,82 г (выход 13%) 2этил-5-метил-1Н-индола (т. пл. 77-78°С). Элементный анализ для C11H13N: Вычислено: С, 82,97; Н, 8,23; N, 8,80. Найдено: С, 83,19; Н, 8,35; N, 8,89. С. 2-этил-5-метил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е) 3,18 г (0,02 М) 2-этил-5-метил1Н-индола обрабатывали 12,5 мл (0,02 М) 1,6М раствора п-бутиллития в гексане, 20 мл (0,02 М) 1М раствора хлорида цинка в эфире, и 1,89 мл (0,02 М) метил 2-бромоацетата, в результате чего после хроматографии на двуокиси кремния (толуол ® 20% EtOAc/гексан) получали 3,23 г (выход 70%) 2-этил-5-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C14H17NO2: Вычислено: С, 72,70; Н, 7,41; N, 6,06. Найдено: С, 70,76; H, 7,29; N, 5,85. D. 2-этил-5-метил-1-(фенилметил)-1Н-индол3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 1,73 г (0,075 М) 2-этил-5-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 0,84 г (0,075 М) t-бутоксида калия и с 0,86 мл (2 мМ) бензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 2% EtOAc/толуол) получали 1,74 г (71%) 2-этил-5-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C21H23NO2: 19 40575 Вычислено: С, 78,47; H, 7,21; N, 4,36. Найдено: С, 78,68; H, 7,30; N, 4,42. Е. Гидразид 2-этил-5-метил-1-(фенилметил)1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G) 1,4 г (0,0044 М) 2-этил-5-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 2 мл гидразина, в результате чего после кристаллизации из МеОН получали 0,77 г (выход 55%) гидразида 2-этил-5-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты (т. пл. 115-125°С). Элементный анализ для C20H23N3O: Вычислено: С, 74,74; H, 7,21; N, 13,07. Найдено: С, 74,73; H, 7,23; N, 13,00. Пример 7 Получение гидразида 2-этил-5-фторо-1-(фенилметил)-1Н-индол-3-уксусной кислоты А. N-трет-бутоксикарбонил-4-фторо-2-метиланилин В соответствии с процедурой, описанной в примере 1 (часть С), 44 г (0,352 М) 4-фторо-метиланилина подвергали реакции с 80,75 г (0,37 М) ди-трет-бутилдикарбоната, в результате чего после кристаллизации из гексана получали 60,1 г (выход 76%) N-трет-бутоксикарбонил-4-фторо-2-метиланилина (т. пл. 93-95°С). Элементный анализ для C12H16FNO2: Вычислено: С, 63,98; Н, 7,16; N, 6,22. Найдено: С, 63,84; Н, 7,32; N, 6,26. В. 1-[2-(трет-бутоксикарбониламино)-5-фторофенил]-2-пентанон В соответствии с процедурой, описанной в примере 2 (часть D), 14,4 г (0,064 М) N-трет-бутоксикарбонил-4-фторо-2-метиланилина подвергали реакции со 100 мл 1,3 М втоp-бутиллития и 7,5 г (0,064 М) N-метокси-N-метилпропанамида, в результате чего после кристаллизации из гексана получали 11,2 г (выход 62%) 1-[2-(трет-бутоксикарбониламино)-5-фторофенил]-2-пентанона (т. пл. 110-112°С). Элементный анализ для С15Н20FNО3: Вычислено: С, 64,04; Н, 7,17; N, 4,98. Найдено: С, 63,02; Н, 7,29; N, 4,93. С. 2-этил-5-фторо-1Н-индол В соответствии с процедурой, описанной в примере 2 (часть Е), 1-[2-(трет-бутоксикарбониламино)-5-фторофенил]-2-пентанон (19,0 г, 0,0676 M) обрабатывали 25 мл трифторуксусной кислоты и полученный продукт хроматографировали на двуокиси кремния (элюент: толуол), в результате чего получали 8,89 г (выход 81%) 2-этил-5-фторо1Н-индола в виде белого твердого вещества (т. пл. 41-42°С). Элементный анализ для C10H10FN: Вычислено: С, 73,60; Н, 6,18; N, 8,58. Найдено: С, 73,37; Н, 6,39; N, 8,31. D. 2-этил-5-фторо-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1, часть Е, 8,8 г (0,054 M) 2-этил-5-фторо1Н-индола обрабатывали 34,4 мл (0,055 M) 1,6М раствора п-бутиллития в гексане 55 мл (0,055 M) 1M раствора хлорида цинка в эфире, и 5,21 мл (0,055 M) метил 2-бромоацетата, в результате чего после хроматографии на двуокиси кремния (элюент: 5% EtOAc/толуол) получали 6,9 г (54%) 2 этил-5-фторо-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для С13Н14FNО2: Вычислено: С, 66,37; Н, 6,00; N, 5,95. Найдено: С, 66,47; Н, 6,15; N, 5,97. Е. 2-этил-5-фторо-1-(фенилметил)-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е) 3,17 г (0,0135 M) 2-этил-5фторо-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 1,5 г (0,0135 M) t-бутоксида калия и 1,55 мл (0,0135 M) бензилбромида, в результате чего после хроматографии на двуокиси кремния (элюент: 5% EtOAc/толуол) получали 3,76 г (71%) 2-этил-5-фторо-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для С20Н20FNO2: Вычислено: С, 73,83; Н, 6,20; N, 4,30. Найдено: С, 74,41; Н, 6,35; N, 4,19. F. Гидразид 2-этил-5-фторо-1-(фенилметил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 3,7 г (0,0114 М) 2-этил-5-фторо1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 10 мл гидразина, в результате чего после кристаллизации из смеси МеОН и воды получали 1,63 г (выход 44%) гидразида 2-этил-5-фторо-1-(фенилметил)-1Ниндол-3-уксусной кислоты (т. пл. 127-128°С). Элементный анализ для C19H20FNO3: Вычислено: С, 70,13; Н, 6,19; N, 12,91. Найдено: С, 70,26; Н, 6,17; N, 12,71. Пример 8 Получение 6-хлоро-2-метил-1-(фенилметил) -1Н-индол-3-уксусной кислоты гидразида А. N-трет-бутоксикарбонил-4-хлоро-2-метиланилин В соответствии с процедурой, описанной в примере 1 (часть С), 28,3 г (0,2 М) 5-хлоро-2-метиланилина подвергали реакции с 48,1 г (0,22 М) ди-трет-бутилдикарбоната, в результате чего после кристаллизации из гексана получали 37,1 г (выход 77%) N-трет-бутоксикарбонил-5-хлоро-2-метиланилина (т. пл. 100-102°С). Элементный анализ для С12Н16СlNО2: Вычислено: С, 59,63; Н, 6,67; N, 5,79. Найдено: С, 59,75; Н, 6,83; N, 5,74. В. 1-[2-(трет-бутоксикарбониламино)-4-хлорфенил]-2-бутанон В соответствии с процедурой, описанной в примере 2 (часть D), 7,73 г (0,032 М) N-трет-бутоксикарбонил-4-хлоро-2-метиланилина подвергали реакции с 50 мл (0,065 М) 1,3 М раствора втор-бутиллития и 3,3 г (0,032 М) N-метокси-N-метилацетамида, в результате чего после кристаллизации из гексана получали 3,49 г (выход 38%) 1-[2(трет-бутоксикарбониламино)-4-хлорфенил]-2-бутанона (т. пл. 89-90°С). Элементный анализ для С14Н18СlNO3: Вычислено: С, 59,26; Н, 6,39; N, 4,94. Найдено: С, 59,14; Н, 6,30; N, 5,16. С. 6-хлоро-2-метил-1Н-индол В соответствии с процедурой, описанной в примере 2 (часть Е), 1-[2-(трет-бутоксикарбонила 20 40575 мино)-4-хлорфенил]-2-бутанон (3,49 г, 0,0123 М) обрабатывали 10 мл трифторуксусной кислоты, и полученный продукт хроматографировали на двуокиси кремния (элюент: градиент смеси толуола и 5% EtOAc/толуола), в результате чего получали 1,2 г (выход 59%) 6-хлоро-2-метил-1Н-индола в виде белого твердого вещества (т. пл. 120-122°С). Элементный анализ для C9H8ClN: Вычислено: С, 65,23; Н, 4,87; N, 8,46. Найдено: С, 65,09; Н, 5,07; N, 8,24. D. 6-хлоро-2-метил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 2,2 г (0,0133 М) 6-хлоро-2-метил-1Н-индола обрабатывали 8,3 мл (0,0133 М) 1,6М раствора п-бутиллития в гексане, 14 мл (0,014 М) раствора хлорида цинка в эфире, и 1,26 мл (0,0133 М) метил 2-бромоацетата, в результате чего получали 2,1 г (66%) 6-хлоро-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества (после хроматографии на двуокиси кремния, элюируя градиентом смеси толуола и 10% EtOAc/толуола). Элементный анализ для C12H12ClNO2: Вычислено: С, 60,64; Н, 5,09; N, 5,89. Найдено: С, 60,78; Н, 5,10; N, 5,84. Е. 6-хлоро-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 1,0 г (0,00421 М) 6-хлоро-2метил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 0,472 г (0,0421 М) t-бутоксида калия и с 0,48 мл (0,00421 М) бензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: толуол ® 10% EtOAc/толуол) получали 0,97 г (выход 70%) 6-хлоро-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира (т. пл. 92-93°С). Элементный анализ для С19Н18СlNО2: Вычислено: С, 69,62; Н, 5,54; N, 4,27. Найдено: С, 69,84; Н, 5,49; N, 4,55. F. Гидразид 6-хлоро-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 0,97 г (2,96 мМ) 6-хлоро-2метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 3 мл гидразида, в результате чего после кристаллизации из МеОН получали 0,4 г (выход 41%) 6-хлоро-2-метил-1-(фенилметил)-1Н-индол3-уксусной кислоты гидразида (т. пл. 179-181°С). Элементный анализ для С18Н18СlN3O: Вычислено: С, 65,95; Н, 5,54; N, 12,82. Найдено: С, 65,54; Н, 5,47; N, 12,21. Пример 9 Получение гидразида 5-бензилокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты А. 5-бензилокси-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть Е), 80 г (0,358 М) 5-бензилокси1Н-индола обрабатывали 222 мл 1,6М раствора пбутиллития в гексане, 360 мл 1М раствора хлорида цинка в эфире, и 39,92 мл этил 2-бромацетата, в результате чего после хроматографии на двуокиси кремния (элюируя градиентом толуола и 5% EtOAc/толуола) получали 30 г (выход 27%) 5бензилокси-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 57-59°С). Элементный анализ для С19Н19NO3: Вычислено: С, 73,77; Н, 6,19; N, 5,43. Найдено: С, 73,75; Н, 6,34; N, 4,50. В. 5-бензилокси-1-(фенилметил)-1Н-индол3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 6,18 г (0,02 М) 5-бензилокси1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 2,24 г (0,02 М) t-бутоксида калия и 2,3 мл (0,02 М) бензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: толуол ® 6% EtOAc/толуол) получали 5,0 г (63%) 5-бензилокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 107-109°С). Элементный анализ для C26H25NO3: Вычислено: С, 78,17; Н, 6,31; N, 3,51. Найдено: С, 78,46; Н, 6,60; N, 3,59. С. Гидразид 5-бензилокси-1-(фенилметил)1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 2,0 г (5 мМ) 5-бензилокси-1(фенилметил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 3 мл гидразина, в результате чего после кристаллизации из МеОН получали 1,25 г (выход 62%) гидразида 5-бензилокси-1-(фенилметил)-1Н-индол-3уксусной кислоты (т. пл. 149-150°С). Элементный анализ для C24H23N3O2: Вычислено: С, 74,78; Н, 6,01; N, 10,90. Найдено: С, 74,91; Н, 6,04; N, 10,97. Пример 10 Получение гидразида 2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты А. 2-метил-1Н-индол-3-уксусной кислоты метиловый сложный эфир К раствору 25 г (0,132 М) 2-метил-1Н-индол-3-уксусной кислоты в 500 мл метанола добавляли 10 мл метансульфоновой кислоты, и полученную смесь перемешивали в течение 24 ч. Затем полученную реакционную смесь разбавляли водой, экстрагировали EtOAc, раствор EtOAc промывали водой, раствором Na2CO3 и после этого снова промывали водой. После осушки сульфатом натрия, растворитель удаляли при пониженном давлении, в результате чего получали 26,62 г (выход 97%) 2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира в виде маслообразного вещества. Элементный анализ для C12H13NO2: Вычислено: С, 70,92; Н, 6,45; N, 6,89. Найдено: С, 70,71; Н, 6,48; N, 7,08. В. 2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 6,09 г (0,03 М) 2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 3,36 г (0,03 М) t-бутоксида калия и 3,45 мл (0,03 М) бензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент-градиент: толуол ® 5% EtOAc/толуол) получали 6,0 г (выход 68%) 2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира (т. пл. 71-73°С). 21 40575 Элементный анализ для C19H19NO2: Вычислено: С, 77,79; Н, 6,53; N, 4,77. Найдено: С, 78,00; Н, 6,51; N, 5,06. С. Гидразид 2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 2,0 г (6,83 мМ) 2-метил-1(фенилметил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 5 мл гидразина, в результате чего получали 1,2 г (выход 60%) 2-метил-1-(фенилметил)-1Н-индол-3уксусной кислоты гидразида (после кристаллизации из МеОН) (т. пл. 140-143°С). Элементный анализ для C18H19N30: Вычислено: С, 73,70; Н, 6,53; N, 14,32. Найдено: С, 73,95; Н, 6,76; N, 14,60. Пример 11 Получение гидразида 1-(2-метокси-1-нафталенилметил)-2-метил-1Н-индол-3-уксусной кислоты А. 1-(2-метокси-1-нафтоленилметил)-2-метил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 4,06 г (0,02 М) 2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 2,24 г (0,03 М) t-бутоксида калия и 4,13 г (0,02 М) 1-хлорометил-2-метоксинафталена, в результате чего после хроматографии на двуокиси кремния (элюент-градиент: толуол ® 5% EtOAc/толуол) получали 4,95 г (66%) 1-(2-метокси-1-нафталенилметил)-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира (т. пл. 120-123°С). Элементный анализ для C24H23NO3: Вычислено: С, 77,19; Н, 6,21; N, 3,75. Найдено: С, 77,45; Н, 6,27; N, 3,69. В. Гидразид 1-(2-метокси-1-нафталенилметил)-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 4,9 г (0,0131 М) 2-метил-1-(2метокси-1-нафталенилметил)-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 10 мл гидразина, в результате чего после кристаллизации из МеОН/СН2Сl2 получали 3,02 г (выход 62%) гидразида 2-метил-1-(2-метокси-1-нафталенилметил)-1Н-индол-3-уксусной кислоты (т. пл. 201-203°С). Элементный анализ для C23H23N3O2: Вычислено: С, 73,97; Н, 6,21; N, 11,52. Найдено: С, 74,24; Н, 6,28; N,11,51. Пример 12 Получение гидразида 1-([1,1'-бифенил]-2-илметил)-5-метокси-1Н-индол-3-уксусной кислоты А. 1-([1,1’-бифенил]-2-илметил)-5-метокси-1Ниндол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 1,2 г (5 мМ) 5-метокси-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 200 мг (5 мМ) 60% NaH/минерального масла, и с 0,9 мл (5 мМ) 2-хлорометилбифенила, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 1,15 г (58%) 1-([1,1’-бифенил]-2-илметил)-5-метокси-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для С26Н25NО3: Вычислено: С, 78,17; Н, 6,31; N, 3,51. Найдено: С, 78,81; H, 6,28; N, 3,47. В. Гидразид 1-([1,1'-бифенил]-2-илметил)-5метокси-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 869 мг (2,15 мМ) 1-([1,1’-бифенил]-2-илметил)-5-метокси-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 2,5 мл гидразина, в результате чего после кристаллизации из МеОН/гексана получали 300 мг (36%) гидразида 1-([1,1’-бифенил]-2-илметил)-5-метокси-1Н-индол-3-уксусной кислоты (т. пл. 123-125°С). Элементный анализ для C24H23N3O2: Вычислено: С, 74,78; H, 6,01; N, 10,90. Найдено: С, 75,01; H, 6,27; N, 10,87. Пример 13 Получение гидразида 5-метокси-2-метил-1(2-метил-1 -пропил)-1H-индол-3-уксусной кислоты А. 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В течение 0,5ч через раствор 27,95 г (0,16 М) гидрохлорида 4-метоксифенилгидразина и 19,72 г (0,17 М) левулиновой кислоты в 500 мл этанола барботировали сухой хлороводород, используя при этом охлаждающую баню из льда и воды. Затем баню удаляли, а реакционную смесь медленно нагревали с обратным холодильником в течение 20 ч. После охлаждения смесь выливали в воду и экстрагировали EtOAc. Раствор EtOAc промывали раствором бикарбоната натрия и осушали сульфатом натрия. После удаления растворителя при пониженном давлении полученный остаток хроматографировали на двуокиси кремния, элюируя смесью 5% EtOAc и толуола, в результате чего получали 14,2 г (выход 36%) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 38-40°С). Элементный анализ для С14Н17NО3: Вычислено: С, 67,99; Н, 6,93; N, 5,66. Найдено: С, 68,24; Н, 6,88; N, 5,75. В. 5-метокси-2-метил-1-(2-метил-1-пропил)1H-индол-3-уксусной кислоты этиловый сложный эфир Раствор 2,06 г (8,34 мМ) 5-метокси-2-метил1Н-индол-3-уксусной кислоты этилового сложного эфира, 3 г карбоната калия и 3 мл 2-метил-1-пропилйодида, нагревали при 65°С в течение 96 ч, а затем полученную смесь выливали в воду. После этого полученный продукт экстрагировали EtOAc, а затем EtOAc четыре раза промывали водой и осушали сульфатом натрия. После хроматографирования на двуокиси кремния, элюируя градиентом толуола и 10% EtOAc/толуола, получали 0,26 г (выход 10%) 5-метокси-2-метил-1-(2метил-1-пропил)-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. С. Гидразид 5-метокси-2-метил-1-(2-метил1-пропил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 230 мг (0,76 мМ) 5-метокси-2метил-1-(2-метил-1 -пропил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1 мл гидразина, в результате чего после перекристаллизации из МеОН получали 10 мг (вы 22 40575 ход 4,5% гидразида 5-метокси-2-метил-1-пропил)1Н-индол-3-уксусной кислоты (т. пл. 113-116°С). Элементный анализ для C16H23N3O2: Вычислено: С, 66,41; Н, 8,01; N, 14,52. Найдено: С, 65,79; Н, 8,10; N, 14,16. Пример 14 Получение гидразида 1-децил-5-метокси-2метил-1Н-индол-3-уксусной кислоты А. 1-децил-5-метокси-2-метил-1Н-индол-3уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 2,47 г (0,01 М) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,12 г (0,01 М) t-бутоксида калия и с 2,07 мл (0,01 М) децилбромида, в результате чего после хроматографии на двуокиси кремния (элюент-градиент: толуол ® 5% EtOAc/толуол) получали 2,16 г (выход 56%) 1децил-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C24H37NO3: Вычислено: С, 74,38; Н, 9,62; N, 3,61. Найдено: С, 74,53; Н, 9,38; N, 3,57. В. Гидразид 1-децил-5-метокси-2-метил-1Ниндол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 2,1 г (0,00545 М) 1-децил-5метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 5 мл гидразина, в результате чего после перекристаллизации из МеОН получали 0,65 г (выход 32%) 1-децил-5-метокси-2-метил-1Н-индол-3-уксусной кислоты гидразида (т. пл. 129-131°С). Элементный анализ для C22H35N3O2: Вычислено: С, 70,74; Н, 9,44; N, 11,25. Найдено: С, 70,79; H, 9,60; N, 11,13. Пример 15 Получение гидразида 5-метокси-2-метил-1октадецил-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-октадецил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 667 мг (2 мМ) октадецилбромида, в результате чего после кристаллизации из МеОН получали 648 мг (65%) 5-метокси-2-метил-1-октадецил-1Н-индол-3-уксусной кислоты метилового сложного эфира (т. пл. 6869°С). Элементный анализ для C32H53NO3: Вычислено: С, 76,91; H, 10,69; N, 2,80. Найдено: С, 76,71; H, 10,50; N, 2,99. В. Гидразид 5-метокси-2-метил-1-октадецил1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 250 мг (0,5 мМ) 5-метокси-2метил-1-октадецил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 0,5 мл гидразина, в результате чего после кристаллизации из реакционной смеси получали 130 мг (выход 54%) гидразида 5-метокси-2-метил-1-октадецил-1Н-индол-3-уксусной кислоты (т. пл. 121123°С). Элементный анализ для С30Н51N3O2: Вычислено: С, 74,18; H, 10,58; N, 8,65. Найдено: С, 74,45; Н, 10,64; N, 8,63. Пример 16 Получение гидразида 5-метокси-2-метил-1(фенилметил)-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-(фенилметил)-1Ниндол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 3 (часть Е), 4,07 г (0,0165 м) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир подвергали реакции с 1,85 г (0,0165 М) t-бутоксида калия и с 1,96 мл (0,0165 М) бензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент-градиент: толуол ® 10% EtOAc/толуол) получали 3,78 г (выход 68%) 5-метокси-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 63-64°С). Элементный анализ для C21H23NO3: Вычислено: С, 74,75; Н, 6,87; N, 4,15. Найдено: С, 74,76; Н, 6,89; N, 4,28. В. Гидразид 5-метокси-2-метил-1-(фенилметил)-1Н-индол-3-уксусной кислоты Раствор 1,0 г (2,96 мМ) 5-метокси-2-метил-1(фенилметил)-1Н-индол-3-уксусной кислоты этилового сложного эфира и 5 мл гидразина в 50 мл МеОН нагревали с обратным холодильником в течение 8 ч, охлаждали, разбавляли водой и экстрагировали EtOAc. После этого раствор EtOAc промывали насыщенным раствором NaCl и осушали сульфатом натрия. Растворитель выпаривали при пониженном давлении, а полученный остаток перетирали с эфиром, в результате чего получали 920 мг (выход 96%) гидразида 5-метокси-2-метил1-(фенилметил)-1Н-индол-3-уксусной кислоты (т. пл. 161-162°С). Элементный анализ для С19Н21N3О2: Вычислено: С, 70,53; Н, 6,54; N, 12,99. Найдено: С, 70,41; Н, 6,58; N, 12,93. Пример 17 Получение гидразида 1-(2-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-(2-хлорофенилметил)-5-метокси-2-метил-1H-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 0,25 мл (2 мМ) орто-хлоробензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 30% EtOAc/гексан) и кристаллизации из МеОН получали 414 мг (56%) 1-(2-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 74-77°С). Элементный анализ для C21H22ClNO3: Вычислено: С, 67,83; Н, 5,95; N, 3,77. Найдено: С, 67,88; Н, 6,09; N, 3,84. В. Гидразид 1-(2-хлорфенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 395 мг (1,06 мМ) 1-(2-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира под 23 40575 вергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 200 мг (выход 53%) гидразида 1-(2-хлорфенилметил)5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 99-100,5°С). Элементный анализ для С19Н20СlN3О2: Вычислено: С, 63,77; Н, 5,63; N, 11,74. Найдено: С, 63,51; Н, 5,77; N, 11,45. Пример 18 Получение гидразида 1-(3-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-(2-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствиис процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 0,25 мл (2 мМ) мета-хлоробензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 33% EtOAc/гексан) и кристаллизации из МеОН получали 409 мг (выход 55%) 1-(3-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 79-81°С). Элементный анализ для C21H22ClNO3: Вычислено: С, 67,83; Н, 5,95; N, 3,77. Найдено: С, 67,55; Н, 5,95; N, 3,76. В. Гидразид 1-(3-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 395 мг (1,06 мМ) 1-(3-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 257 мг (выход 68%) гидразида 1-(3-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 139-140°С). Элементный анализ для С19Н20СlN3О2: Вычислено: С, 63,77; Н, 5,63; N, 11,74. Найдено: С, 63,79; Н, 5,69; N, 11,67. Пример 19 Получение гидразида 1-(4-хлорофенилметил)5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-(4-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 322 мг (2 мМ) пара-хлоробензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 30% EtOAc/гексан) и кристаллизации из МеОН получали 348 мг (47%) 1-(4-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 98-100°С). Элементный анализ для C21H22ClNO3. Вычислено: С, 67,83; Н, 5,95; N, 3,77. Найдено: С, 67,98; Н, 5,92; N, 3,69. В. Гидразид 1-(4-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 333 мг (0,9 мМ) 1-(4-хло рофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 251 мг (выход 78%) гидразида 1-(4-хлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 177-180°С). Элементный анализ для С19Н20СlN3О2: Вычислено: С, 63,77; Н, 5,63; N, 11,74. Найдено: С, 64,02; Н, 5,77; N, 11,45. Пример 20 Получение гидразида 1-(2,5-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-(2,5-дихлорофенилметил)-5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 391 мг (2 мМ) (2,5-дихлорофенил)метилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) и кристаллизации из МеОН получали 236 мг (выход 29%) 1-(2,5-дихлорфенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 146-148°С). Элементный анализ для C21H21Cl2NO3: Вычислено: С, 62,08; Н, 5,21; N, 3,45. Найдено: С, 62,34; Н, 5,23; N, 3,72. В. Гидразид 1-(2,5-дихлорофенилметил)-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 221 мг (0,54 мМ) 1-(2,5-дихлорфенилметил)-5-метокси-2-метил-1Н-индол-3уксусной кислоты этилового сложного эфира подвергали реакции с 0,6 мл гидразина, в результате чего после кристаллизации из МеОН получали 135 мг (выход 64%) гидразида 1-(2,5-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 168-170°С). Элементный анализ для С19Н19Сl2N3О2: Вычислено: С, 58,17; Н, 4,88; N, 10,71. Найдено: С, 58,46; Н, 4,94; N, 10,73. Пример 21 Получение гидразида 1-(2,6-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-(2,6-дихлорофенилметил)-5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и 391 мг (2 мМ) (2,6-дихлорофенилметил)метилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 556 мг (68%) 1-(2,6-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 131-132°С). Элементный анализ для C21H21Cl2NO3: Вычислено: С, 62,08; Н, 5,21; N, 3,45. Найдено: С, 61,79; Н, 5,23; N, 3,751. 24 40575 В. Гидразид 1-(2,6-дихлорофенилметил)-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 533 мг (1,3 мМ) 1-(2,6-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,3 мл гидразина, в результате чего после кристаллизации из МеОН получали 250 мг (выход 61%) гидразида 1-(2,6-дихлорофенилметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 194-196°С). Элементный анализ для C19H19Cl2N3O2: Вычислено: С, 58,17; Н, 4,88; N, 10,71. Найдено: С, 58,65; Н, 4,98; N, 10,68. Пример 22 Получение гидразида 5-метокси-1-[(3-метилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты А. 5-метокси-1-[(3-метилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 0,26 мл (2 мМ) метаметилбензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: смесь 20% EtOAc и гексана) получали 438 мг (выход 62%) 5-метокси-1-[(3-метилфенил)метил]-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для С22Н25NO3: Вычислено: С, 75,19; Н, 7,17; N, 3,99. Найдено: С, 75,46; Н, 7,29; N, 3,97. В. Гидразид 5-метокси-1-[(3-метилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 409 мг (1,17 мМ) 5-метокси-1[(3-метилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,2 мл гидразина, в результате чего после кристаллизации из МеОН получали 157 мг (выход 40%) гидразида 5-метокси-1-[(3-метилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 133-135°С). Элементный анализ для C20H23N3O2: Вычислено: С, 71,19; Н, 6,87; N, 12,45. Найдено: С, 71,42; Н, 6,97; N, 12,66. Пример 23 Получение 5-метокси-2-метил-1-[(3-трифторометилфенил)метил]-2-метил-1Н-индол-3-уксусной кислоты гидразида А. 5-метокси-2-метил-1-[(3-трифторометилфенил)метил]-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) 60% NaH/минерального масла и с 389 мг (2 мМ) мета-трифторометилбензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) и кристаллизации из МеОН получали 410 мг (выход 51%) 5-метокси-2метил-1-[(3-трифторометилфенил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 95-97°С). Элементный анализ для С22Н22F3NО3. Вычислено: С, 65,18; Н, 5,47; N, 3,46. Найдено: С, 65,41; Н, 5,53; N, 3,60. В. Гидразид 5-метокси-2-метил-1-[(3-трифторометилфенил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 390 мг (0,96 мМ) 5-метокси-2метил-1-[(3-трифторометилфенил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,2 мл гидразина, в результате чего после кристаллизации из МеОН получали 166 мг (выход 44%) гидразида 5-метокси-2метил-1-[(3-трифторометилфенил)метил]-1H-индол-3-уксусной кислоты (т. пл. 162-165°С). Элементный анализ для C20H20F3N3O2: Вычислено: С, 61,38; Н, 5,15; N, 10,74. Найдено: С, 61,58; Н, 5,24; N, 10,95. Пример 24 Получение гидразида 1-([1,1’-бифенил]-2-илметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-([1,1'-бифенил]-2-илметил)-5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 483 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира обрабатывали 80 мг (2 мМ) 60% NaH/минерального масла и 0,37мл (2 мМ) 2-(бромометил)бифенила, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 567 мг (выход 69%) 1([1,1'-бифенил]-2-илметил)-5-метокси-2-метил-1Ниндол-3-уксусной кислоты этилового сложного эфира в виде желтого маслообразного вещества. Элементный анализ для С27Н27NО3: Вычислено: С, 78,42; Н, 6,58; N, 3,39. Найдено: С, 78,12; Н, 6,47; N, 3,03. В. Гидразид 1-([1,1'-бифенил]-2-илметил)-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 552 мг (1,34 мМ) 1-([1,1'-бифенил]-2-илметил)-5-метокси-2-метил-1Н-индол-3уксусной кислоты этилового сложного эфира подвергали реакции с 2,0 мл гидразина, в результате чего после хроматографии на двуокиси кремния (элюент: EtOAc) получали 150 мг (выход 28%) гидразида 1-([1,1'-бифенил]-2-илметил)-5-метокси-2метил-1H-индол-3-уксусной кислоты. Элементный анализ для C25H25N3O2: Вычислено: С, 75,16; Н, 6,31; N, 10,52. Найдено: С, 75,01; Н, 6,34; N, 10,26. Пример 25 Получение гидразида 1-([1,1'-бифенил]-3-илметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. Этиловый сложный эфир 1-([1,1'-бифенил]-3-илметил)-5-метокси-2-метил-1Н-индол-3уксусной кислоты В соответствии с процедурами, описанными в примере 1 (часть F), 483 мг (2 мМ) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира обрабатывали 80 мл (2 мМ) смеси 60% NaH/минерального масла и 405 мл (2 мМ) 3-(хлорометил)бифенила, в результате чего после хроматографии на двуокиси кремния (элюент: 33% 25 40575 EtOAc/гексан) получали 510 мг (выход 62%) 1([1,1'-бифенил]-3-илметил)-5-метокси-2-метил-1Ниндол-3-уксусной кислоты этилового сложного эфира в виде желтого маслообразного вещества. В. Гидразид 1-([1,1'-бифенил]-3-илметил)-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 490 мг (1,2 мМ) 1-([1,1'-бифенил]-3-илметил)-5-метокси-2-метил-1Н-индол-3уксусной кислоты этилового сложного эфира подвергали реакции с 1,2 мл гидразина, в результате чего после кристаллизации из МеОН получали 316 мг (выход 66%) гидразида 1-([1,1'-бифенил]-3-илметил)-5-метокси-2-метил-1Н-индол-3-уксусной кислоты. Элементный анализ для C25H25N3O2: Вычислено: С, 75,16; Н, 6,31; N, 10,52. Найдено: С, 74,96; Н, 6,32; N, 10,28. Пример 26 Получение гидразида 5-метокси-1-([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты А. 5-метокси-1-([2-метоксифенил)метил]-2метил-1Н-индол-3-уксусная кислота В соответствии с процедурой, описанной в примере 1 (часть F), 2,0 г (8,12 мМ) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 325 мг (8,12 мМ) смеси 60% NaH/минерального масла и с 1,272 г (8,12 мМ) орто-метоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 1,74 г (выход 52%) 5-метокси-1-([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Полученное маслообразное вещество (1,74 г) в 30 мл МеОН и 15 мл 1N NaOH нагревали с обратным холодильником в течение 20 ч. Затем полученную смесь разбавляли водой и экстрагировали EtOAc, после чего EtOAc-раствор осушали сульфатом натрия, растворитель удаляли при пониженном давлении, а полученный остаток кристаллизовали из МеОН, в результате чего получали 1,1 г (выход 68%) 5-метокси-1-([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 176-180°С) Элементный анализ для C22H21NO4: Вычислено: С, 70,78; Н, 6,24; N, 4,13. Найдено: С, 70,98; Н, 6,42; N, 4,19. В. 5-метокси-1-([2-метоксифенил)метил]-2метил-1Н-индол-3-уксусной кислоты метиловый сложный эфир В соответствии с процедурой, описанной в примере 10 (часть А), 848 мг (2,5 мМ) 5-метокси-1([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты обрабатывали 0,2 мл метансульфоновой кислоты в 20 мл МеОН, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 655 мг (выход 74%) 5-метокси-1-([2-метоксифенил)метил]-2метил-1Н-индол-3-уксусной кислоты метилового сложного эфира (т. пл. 98-100°С). Элементный анализ для C21H23NO4: Вычислено: С, 71,37; Н, 6,56; N, 3,96. Найдено: С, 71,59; Н, 6,74; N, 3,81. С. Гидразид 5-метокси-1-([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 640 мг (1,8 мМ) 5-метокси-1([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты метилового сложного эфира подвергали реакции с 2,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 358 мг (выход 56%) гидразида 5-метокси-1-([2-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 140-143°С). Элементный анализ для C20H23N3O3: Вычислено: С, 67,97; Н, 6,56; N, 11,89. Найдено: С, 68,84; Н, 6,67; N, 11,84. Пример 27 Получение гидразида 5-метокси-1-([3-метоксифенил)метил]-2-метил-1H-индол-3-уксусной кислоты А. 5-метокси-1-([3-метоксифенил)метил]-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 313 мг (2 мМ) мета-метоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) и кристаллизации из МеОН получали 424 мг (выход 58%) 5-метокси-1([3-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 88-90°С). Элементный анализ для C22H25NO4: Вычислено: С, 71,91; Н, 6,86; N, 3,81. Найдено: С, 72,05; Н, 6,99; N, 4,07. В. Гидразид 5-метокси-1-([3-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 406 мг (1,1 мМ) 5-метокси-1([3-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 240 мг (выход 62%) гидразида 5-метокси-1-([3-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 161-163°С). Элементный анализ для C20H23N3O3: Вычислено: С, 67,97; H, 6,56; N, 11,89. Найдено: С, 68,00; H, 6,61; N, 12,02. Пример 28 Получение гидразида 5-метокси-1-([4-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты А. Этиловый сложный эфир 5-метокси-1-([4метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 0,3 мл (2 мМ) пара-метоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 341 мг (выход 46%) 5-метокси-1-([4-метоксифенил)метил]-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C22H25NO4: 26 40575 Вычислено: С, 71,91; H, 6,86; N, 3,81. Найдено: С, 72,62; H, 6,75; N, 3,41. В. Гидразид 5-метокси-1-([4-метоксифенил) метил]-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 317 мг (0,86 мМ) 5-метокси-1([4-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 124 мг (выход 41%) гидразида 5-метокси-1-([4-метоксифенил)метил]-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 161-163°С). Элементный анализ для C20H23N3O3: Вычислено: С, 67,97; Н, 6,56; N, 11,89. Найдено: С, 68,21; Н, 6,65; N, 11,95. Пример 29 Получение гидразида 1-[(3-децилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-[(3-децилоксифенил)метил]-5-метокси2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 565 мг (2 мМ) мета-децилоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 590 мг (выход 60%) 1-[(3-децилоксифенил)метил]-5-метокси2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C31H43NO4: Вычислено: С, 75,42; Н, 8,78; N, 2,84. Найдено: С, 75,21; Н, 9,00; N, 2,78. В. Гидразид 1-[(3-децилоксифенил)метил]-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 571 мг (1,16 мМ) 1-[(3-децилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,5 мл гидразина, в результате чего после кристаллизации из МеОН получали 188 мг (выход 34%) гидразида 1-[(3-децилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 66-76°С). Элементный анализ для С29Н41N3О3: Вычислено: С, 72,62; Н, 8,62; N, 8,76. Найдено: С, 72,92; Н, 8,66; N, 6,99. Пример 30 Получение гидразида 1-[(3-бензилоксифенил) метил]-5-метокси-2-метил-1Н-индол-3 -уксусной кислоты А. 1-[(3-бензилоксифенил)метил]-5-метокси2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 465 мг (2 мМ) мета-бензилоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) и после кристаллизации из МеОН получали 376 мг (выход 42%) 1-[(3 бензилоксифенил)метил]-5-метокси-2-метил-1Ниндол-3-уксусной кислоты (т. пл. 60-70°С). Элементный анализ для C28H29NO4: Вычислено: С, 75,82; Н, 6,59; N, 3,16. Найдено: С, 76,06; Н, 6,56; N, 3,35. В. Гидразид 1-[(3-бензилоксифенил)метил]5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 369 мг (0,83 мМ) 1-[(3-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,83 мл гидразина, в результате чего после кристаллизации из МеОН получали 180 мг (выход 51%) 1-[(3-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты гидразида (т. пл. 130-132°С). Элементный анализ для C26H27N3O3: Вычислено: С, 72,71; Н, 6,34; N, 9,78. Найдено: С, 72,92; Н, 6,50; N, 9,99. Пример 31 Получение гидразида 1-[(3-гидроксифенил) метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-[(3-гидроксифенил)метил]-5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир Раствор 357 мг (0,8 мМ) 1-[(3-бензилоксифенил)метил]-5-метокси-2-метил-1H-индол-3-уксусной кислоты этилового сложного эфира (Пример 31, часть А) в 30мл смеси тетрагидрофурана и ЕtOАс (1:1), в течение 16ч гидрогенизировали под давлением водорода 60 фунт/кв. дюйм (4218 г/см2), используя при этом 90 мг Pd/BaSO4 в качестве катализатора. После этого катализатор фильтровали, а полученный фильтрат концентрировали при пониженном давлении. Полученный остаток растворяли в EtOAc и промывали водой, а затем насыщенным раствором NaCl. После осушки сульфатом магния, полученный продукт хроматографировали на двуокиси кремния, элюируя смесью ЕtOАс/гексана и EtOAc (1:1) в результатечего после кристаллизации из МеОН получали 100 мг (выход 35%) 1-[(3-гидроксифенил)метил]-5-метокси-2-метил-1H-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 114-116°С). Элементный анализ для C21H23NO4: Вычислено: С, 71,37; H, 6,56; N, 3,96. Найдено: С, 71,63; H, 6,49; N, 4,14. В. Гидразид 1-[(3-гидроксифенил)метил]-5метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 76 мг (0,22 мМ) 1-[(3-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,22 мл гидразина, в результате чего после кристаллизации из МеОН получали 35 мг (выход 47%) гидразида 1-[(3-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 201-203°С). Элементный анализ для С19Н21N3О3: Вычислено: С, 67,24; H, 6,24; N, 12,38. Найдено: С, 67,46; H, 6,36; N, 12,33. Пример 32 Получение гидразида 1-[(4-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты 27 40575 А. 1-[(4-бензилоксифенил)метил]-5-метокси2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 465 мг (2 мМ) пара-бензилоксибензилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) и кристаллизации из МеОН получали 347 мг (выход 39%) 1-[(4-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол3-уксусной кислоты этилового сложного эфира (т. пл. 118-119°С). Элементный анализ для C28H29NO4: Вычислено: С, 75,82; Н, 6,59; N, 3,16. Найдено: С, 75,94; Н, 6,60; N, 2,96. В. Гидразид 1-[(4-бензилоксифенил)метил]5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 315 мг (0,7 мМ) 1-[(4-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 246 мг (выход 82%) гидразида 1-[(4-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 179-180°С). Элементный анализ для C26H27N3O3: Вычислено: С, 72,71; Н, 6,34; N, 9,78. Найдено: С, 72,76; Н, 6,43; N, 10,01. Пример 33 Получение гидразида 1-[(4-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-[(4-гидроксифенил)метил]-5-метокси-2метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 32 (часть А), 357 мг (0,8 мМ) 1-[(4-бензилоксифенил)метил]-5-метокси-2-метил-1Н-индол3-уксусной кислоты этилового сложного эфира (пример 33, часть А) гидрогенизировали и хроматографировали на двуокиси кремния (элюент: 25% EtOAc/гексан) в результате чего после кристаллизации из МеОН получали 202 мг (выход 77%) 1-[(4-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 113-115°С). Элементный анализ для C21H23NO4: Вычислено: С, 71,37; Н, 6,56; N, 3,96. Найдено: С, 71,08; Н, 6,57; N, 4,18. В. Гидразид 1-[(4-гидроксифенил)метил]-5метокси-2-метил-1H-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 182 мг (0,5 мМ) 1-[(4-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 110мг (выход 65%) гидразида 1-[(4-гидроксифенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 211-214°С). Элементный анализ для С19Н21N3О3: Вычислено: С, 67,24; Н, 6,24; N, 12,38. Найдено: С, 67,74; Н, 6,32; N, 11,83. Пример 34 Получение гидразида 5-метокси-2-метил-1[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 432 мг (2 мМ) мета-титробензилбромида, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) и кристаллизации из МеОН получали 141 мг (выход 18%) 5-метокси-2метил-1-[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 105106°С). Элементный анализ для C21H22N2O5: Вычислено: С, 65,96; Н, 5,80; N, 7,33. Найдено: С, 65,84; Н, 5,86; N, 7,36. В. Гидразид 5-метокси-2-метил-1-[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 115мг (0,3 мМ) 5-метокси-2метил-1-[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,3 мл гидразина, в результате чего после кристаллизации из МеОН получали 42 мг (выход 38%) гидразида 5-метокси-2-метил-1-[(3нитрофенил)метил]-1Н-индол-3-уксусной кислоты (т. пл. 177-179°С). Элементныйанализ для C19H20N4O4: Вычислено: С, 61,95; Н, 5,47; N, 15,21. Найдено: С, 62,53; Н, 5,56; N, 14,96. Пример 35 Получение гидразида 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты А. 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этиловый сложный эфир Раствор 500 мг (1,3 мМ) 5-метокси-2-метил1-[(3-нитрофенил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира в 50 мл EtOAc гидрогенизировали в течение 16 ч при комнатной температуре под давлением водорода 60 фунт/кв. дюйм (4218 г/см2), используя в качестве катализатора 0,1 г 5% Pd/C. После этого катализатор фильтровали, и полученный фильтрат концентрировали при пониженном давлении. Полученный остаток хроматографировали на двуокиси кремния, элюируя смесью EtOAc и гексана, в результате чего получали 234мг (выход 51%) 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C21H24N2O3: Вычислено: С, 71,57; Н, 6,86; N, 7,95. Найдено: С, 71,18; Н, 6,75; N, 7,52. В. Гидразид 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 192 мг (0,54 мМ) этилового сложного эфира 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты под 28 40575 вергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 73 мг (выход 40%) гидразида 1-[(3-аминофенил)метил]-5-метокси-2-метил-1Н-индол-3-уксусной кислоты (т. пл. 154-156°С). Элементный анализ для C19H22N4O2: Вычислено: С, 67,44; Н, 6,55; N, 16,56. Найдено: С, 67,47; Н, 6,49; N, 16,46. Пример 36 Получение гидразида 5-метокси-2-метил-1(1-фенилэтил)-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-(1-фенилэтил)-1Ниндол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 0,27 мг (2 мМ) (1-бромоэтил)-бензола, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 160 мг (выход 22%) 5-метокси-2-метил-1-(1-фенилэтил)-1Ниндол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для С22Н25NO3: Вычислено: С, 75,19; Н, 7,17; N, 3,99. Найдено: С, 75,45; Н, 7,45; N, 4,40. В. Гидразид 5-метокси-2-метил-1-(1-фенилэтил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 143 мг (0,4 мМ) 5-метокси-2метил-1-(1-фенилэтил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,5 мл гидразина, в результате чего после хроматографии на двуокиси кремния (элюент: EtOAc) получали 80 мг (выход 59%) гидразида 5метокси-2-метил-1-(1-фенилэтил)-1Н-индол-3-уксусной кислоты в виде белого пенистого вещества. Элементный анализ для C20H23N3O2: Вычислено: С, 71,19; Н, 6,87; N, 12,45. Найдено: С, 71,41; Н, 7,07; N, 12,53. Пример 37 Получение гидразида 5-метокси-2-метил-1[(2-пиридил)метил]-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-[(2-пиридил)метил]1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции со 160 мг (4 мМ) смеси 60% NaH/минерального масла и с 328 мг (2 мМ) гидрохлорида 2-пиколилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 50% EtOAc/гексан) получали 510 мг (выход 75%) 5-метокси-2-метил-1-[(2-пиридил)метил]1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C20H22N2O3: Вычислено: С, 70,99; Н, 6,55; N, 8,28. Найдено: С, 71,28; Н, 6,84; N, 8,44. В. Гидразид 5-метокси-2-метил-1-[(2-пиридил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 480 мг (1,4 мМ) 5-метокси-2 метил-1-[(2-пиридил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,4мл гидразина, в результате чего после кристаллизации из МеОН получали 304 мг (выход 67%) гидразида 5-метокси-2-метил-1-[(2-пиридил)метил]-1Н-индол-3-уксусной кислоты (т. пл. 147-148°С). Элементный анализ для C18H20N4O2: Вычислено: С, 66,65; H, 6,22; N, 17,27. Найдено: С, 66,40; H, 6,21; N, 17,34. Пример 38 Получение гидразида 5-метокси-2-метил-1[(3-пиридил)метил]-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-[(3-пиридил)метил]1Н-индол-3-уксусной кислоты этиловый сложный эфир К раствору 247 мг (1 мМ) 5-метокси-2-метил1Н-индол-3-уксусной кислоты этилового сложного эфира в 5 мл ДМСО, добавляли 154 мг 85% раствора КОН. Полученную смесь охлаждали в бане из льда и воды, а затем добавляли 164 мг (1 мМ) гидрохлорида 3-пиколилхлорида. После этого охлаждающую баню удаляли, а смесь перемешивали в течение 4 ч. Затем эту смесь разбавляли водой, полученный продукт экстрагировали EtOAc, a EtOAc-раствор промывали насыщенным раствором NaCl. После осушки сульфатом магния полученный продукт хроматографировали на двуокиси кремния, элюируя смесью 50% EtOAc/гексана, в результате чего после кристаллизации из МеОН получали 75 мг (выход 22%) 5-метокси-2метил-1-[(3-пиридил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира (т. пл. 109111°С). Элементный анализ для C20H22N2O3: Вычислено: С, 70,99; H, 6,55; N, 8,28. Найдено: С, 71,05; H, 6,66; N, 8,20. В. Гидразид 5-метокси-2-метил-1-[(3-пиридил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 340 мг (1,0 мМ) 5-метокси-2метил-1-[(3-пиридил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 54 мг (выход 17%) гидразида 5-метокси-2-метил-1-[(3-пиридил)метил]-1Н-индол-3-уксусной кислоты (т. пл. 153-154,5°С). Элементный анализ для C18H20N4O2: Вычислено: С, 66,65; Н, 6,22; N, 17,27. Найдено: С, 66,84; Н, 6,36; N, 17,17. Пример 39 Получение гидразида 5-метокси-2-метил-1[(4-пиридил)метил]-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-[(4-пиридил)метил]1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции со 160 мг (4 мМ) смеси 60% NaH/минерального масла и с 328 мг (2 мМ) гидрохлорида 4-пиколилхлорида, в результате чего после хроматографии на двуокиси кремния (элюент: 50% EtOAc/гексан) получали 480 мг (выход 71%) 5-метокси-2-метил-1-[(4-пиридил)метил]1Н-индол-3-уксусной кислоты этилового сложного 29 40575 эфира в виде маслообразного вещества, которое отверждали при отстаивании. В. Гидразид 5-метокси-2-метил-1-[(4-пиридил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 410 мг (1,2 мМ) 5-метокси-2метил-1-[(4-пиридил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,2 мл гидразина, в результате чего после кристаллизации из МеОН получали 148 мг (выход 38%) гидразида 5-метокси-2-метил-1-[(4-пиридил)метил]-1Н-индол-3-уксусной кислоты (т. пл. 192-193,5°С). Элементный анализ для C18H20N4O2: Вычислено: С, 66,65; Н, 6,22; N, 17,27. Найдено: С, 66,54; Н, 6,27; N, 17,10. Пример 40 Получение гидразида 5-метокси-2-метил-1[(2-хинолил)метил]-1Н-индол-3-уксусной кислоты А. 5-метокси-2-метил-1-[(2-хинолил)метил]1Н-индол-3-уксусной кислоты этиловый сложный эфир В соответствии с процедурой, описанной в примере 1 (часть F), 525 мг (2,1 мМ) 5-метокси-2метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции со 168 мг (4,2 мМ) смеси 60% NaH/минерального масла и с 450 мг (2,1 мМ) гидрохлорида 2-хлорометил-хинолина, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 466 мг (выход 57%) 5-метокси-2-метил1-[(2-хинолил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. В. Гидразид 5-метокси-2-метил-1-[(2-хинолил)метил]-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 446 мг (1,15 мМ) 5-метокси-2метил-1-[(2-хинолил)метил]-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 1,0 мл гидразина, в результате чего после кристаллизации из МеОН получали 238 мг (выход 55%) гидразида 5-метокси-2-метил-1-[(2-хинолил)метил]-1Н-индол-3-уксусной кислоты (т. пл. 173-175°С). Элементный анализ для C22H22N4O2: Вычислено: С, 70,57; Н, 5,92; N, 14,96. Найдено: С, 70,37; Н, 6,02; N, 14,93. Пример 41 Получение гидразида 5-метокси-2-метил-1(3-фенилпропил)-1Н-индол-3-уксусной кислоты А. Этиловый сложный эфир 5-метокси-2-метил-1-(3-фенилпропил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 0,3 мл (2 мМ) 1-бромо-3-фенилпропана, в результате чего после хроматографии на двуокиси кремния (элюент: 25% EtOAc/гексан) получали 424 мг (выход 58%) 5-метокси-2-метил-1-(3-фенилпропил)1Н-индол-3-уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C23H27NO3: Вычислено: С, 75,59; Н, 7,45; N, 3,83. Найдено: С, 75,71; Н, 7,70; N, 3,90. В. Гидразид 5-метокси-2-метил-1-(3-фенилпропил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 308 мг (0,84 мМ) 5-метокси-2метил-1-(3-фенилпропил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,9 мл гидразина, в результате чего после кристаллизации из МеОН получали 93 мг (выход 31%) гидразида 5-метокси-2-метил-1-(3-фенилпропил)-1Н-индол-3-уксусной кислоты (т. пл. 133-135°С). Элементный анализ для C21H25N3O2: Вычислено: С, 71,77; Н, 7,17; N, 11,96. Найдено: С, 72,02; Н, 7,38; N, 11,98. Пример 42 Получение гидразида 5-метокси-2-метил-1(4-фенилбутил)-1Н-индол-3-уксусной кислоты А. Этиловый сложный эфир 5-метокси-2-метил-1-(4-фенилбутил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть F), 494 мг (2 мМ) 5-метокси-2-метил-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 80 мг (2 мМ) смеси 60% NaH/минерального масла и с 337 мг (2 мМ) 4-хлоробутилбензола, в результате чего после хроматографии на двуокиси кремния (элюент: 20% EtOAc/гексан) получали 234 мг (выход 15%) 5-метокси-2-метил-1-(4-фенилбутил)-1Н-индол-3уксусной кислоты этилового сложного эфира в виде маслообразного вещества. Элементный анализ для C24H29NО3: Вычислено: С, 75,96; Н, 7,70; N, 3,69. Найдено: С, 76,18; Н, 7,73; N, 3,79. В. Гидразид 5-метокси-2-метил-1-(4-фенилбутил)-1Н-индол-3-уксусной кислоты В соответствии с процедурой, описанной в примере 1 (часть G), 215 мг (0,57 мМ) 5-метокси-2метил-1-(4-фенилбутил)-1Н-индол-3-уксусной кислоты этилового сложного эфира подвергали реакции с 0,6 мл гидразина, в результате чего после кристаллизации из МеОН получали 62 мг (выход 30%) гидразида 5-метокси-2-метил-1-(4-фенилбутил)-1Н-индол-3-уксусной кислоты (т. пл. 133135°С). Элементный анализ для C22H27N3O2: Вычислено: С, 72,30; Н, 7,45; N, 11,50. Найдено: С, 72,32; Н, 7,45; N, 11,35. Пример 43 Получение гидразида 2-хлоро-5-метокси-1(фенилметил)-1Н-индол-3-уксусной кислоты А. 5-метокси-1-(фенилметил)-1Н-индол-3-уксусной кислоты фенилметиловый сложный эфир Раствор 2,0 г (10 мМ) 5-метокси-1Н-индол-3уксусной кислоты в 100 мл ДМФ порциями обрабатывали 1,0 г (25 мМ) смеси 60% NaH/минерального масла, а через 10 мин к раствору добавляли 3 мл бензилбромида. Через 22 ч полученную смесь разбавляли водой и экстрагировали EtOAc, а после этого EtOAc-раствор промывали водой, насыщенным раствором NaCl и затем осушали сульфатом натрия. После концентрации при пониженном давлении полученный остаток хроматографировали на двуокиси кремния, элюируя метиленхлоридом, в результате чего получали 3,7 г (выход 96%) 5-метокси-1-(фенилметил)-1Ниндол-3-уксусной кислоты фенилметилового слож 30
ДивитисяДодаткова інформація
Назва патенту англійськоюHydrazide 1h-indole-3-acetic acid (variants) as inhibitor of spla2 and pharmaceutical composition
Автори англійськоюBach Nicolas James, Dillard Robert Dilane, Draheim Suzanne Elizabeth, Hermann Robert Bell, Shevits Richard Walter
Назва патенту російськоюГидразид 1н-индол-3-уксусной кислоты (варианты) в качестве ингибитора spla2 и фармацевтическая композиция
Автори російськоюБах Николас Джеймс, Диллард Роберт Дилейн, Драхейм Сюзан Элизабет, Германн Роберт Белл, Шевиц Ричард Вальтер
МПК / Мітки
МПК: A61P 1/00, A61P 29/00, A61K 31/41, C07D 401/12, C07F 9/572, C07D 417/06, C07D 403/06, A61P 11/08, A61P 27/16, A61K 31/40, A61K 31/47, C07D 401/06, A61K 31/4427, A61K 31/44, A61P 9/00, A61P 43/00, A61K 31/404, A61P 37/08, C07D 417/12, A61K 31/425, C07D 403/12, A61P 11/00, A61K 31/403, C07D 209/22, A61P 31/04, C07D 209/24, C07D 209/20, C07D 209/30
Мітки: варіанти, кислоти, інгібітор, фармацевтична, композиція, гідразид, 1н-індол-3-оцтової, spla2
Код посилання
<a href="https://ua.patents.su/46-40575-gidrazid-1n-indol-3-octovo-kisloti-varianti-yak-ingibitor-spla2-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Гідразид 1н-індол-3-оцтової кислоти (варіанти) як інгібітор spla2 та фармацевтична композиція</a>
Попередній патент: Похідні 17,20-епоксипрегнану, спосіб їх одержання, спосіб одержання похідних кортизону і проміжні сполуки
Наступний патент: Зубчата передача роторного вітродвигуна
Випадковий патент: Гідрофільний гель