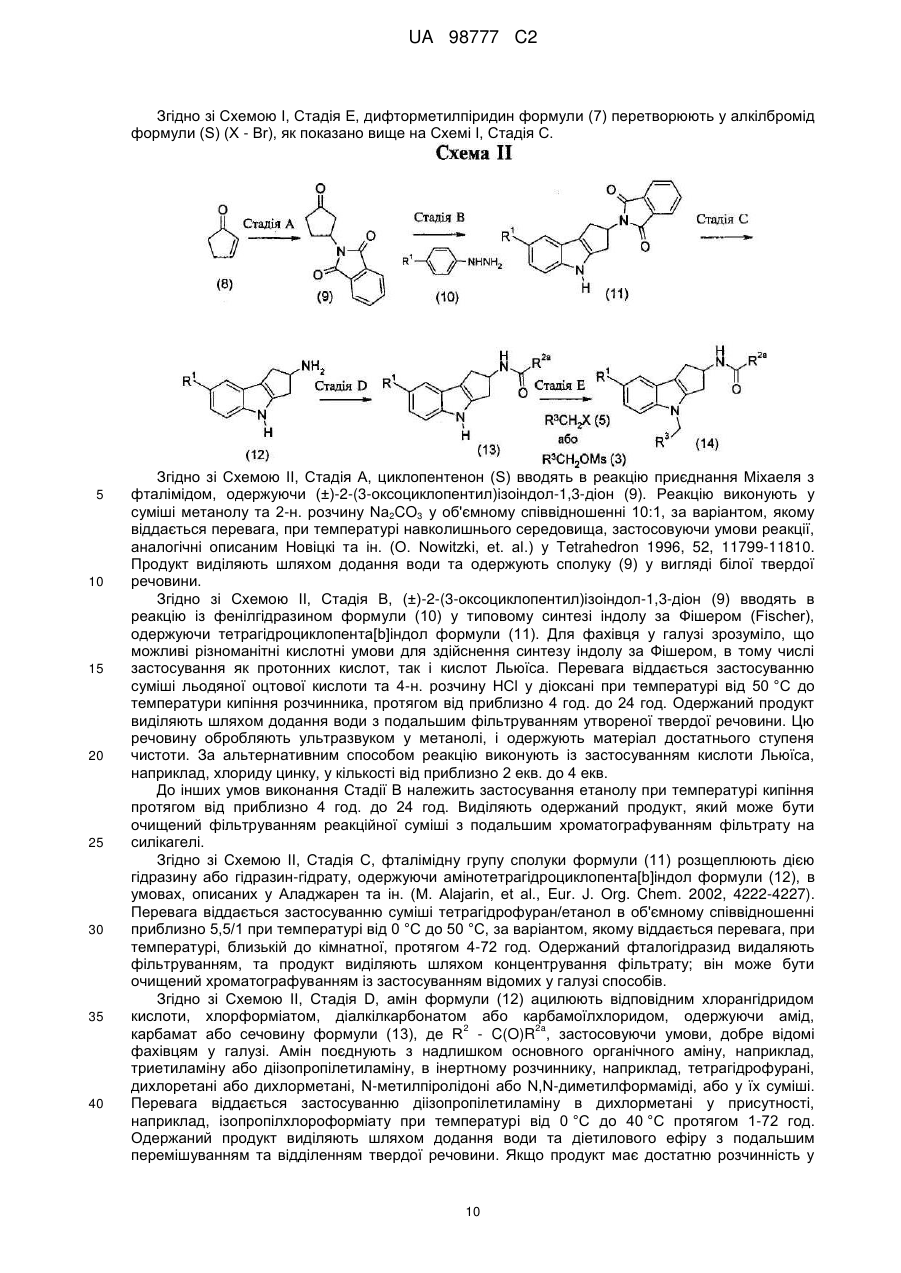
Тетрагідроциклопента[b]індоли як модулятори андрогенових рецепторів
Номер патенту: 98777
Опубліковано: 25.06.2012
Автори: Грін Джонатан Едвард, Джадхав Прабхакар Кондаї, Маттьюз Доналд Пол, Гавардінас Константінос
Формула / Реферат
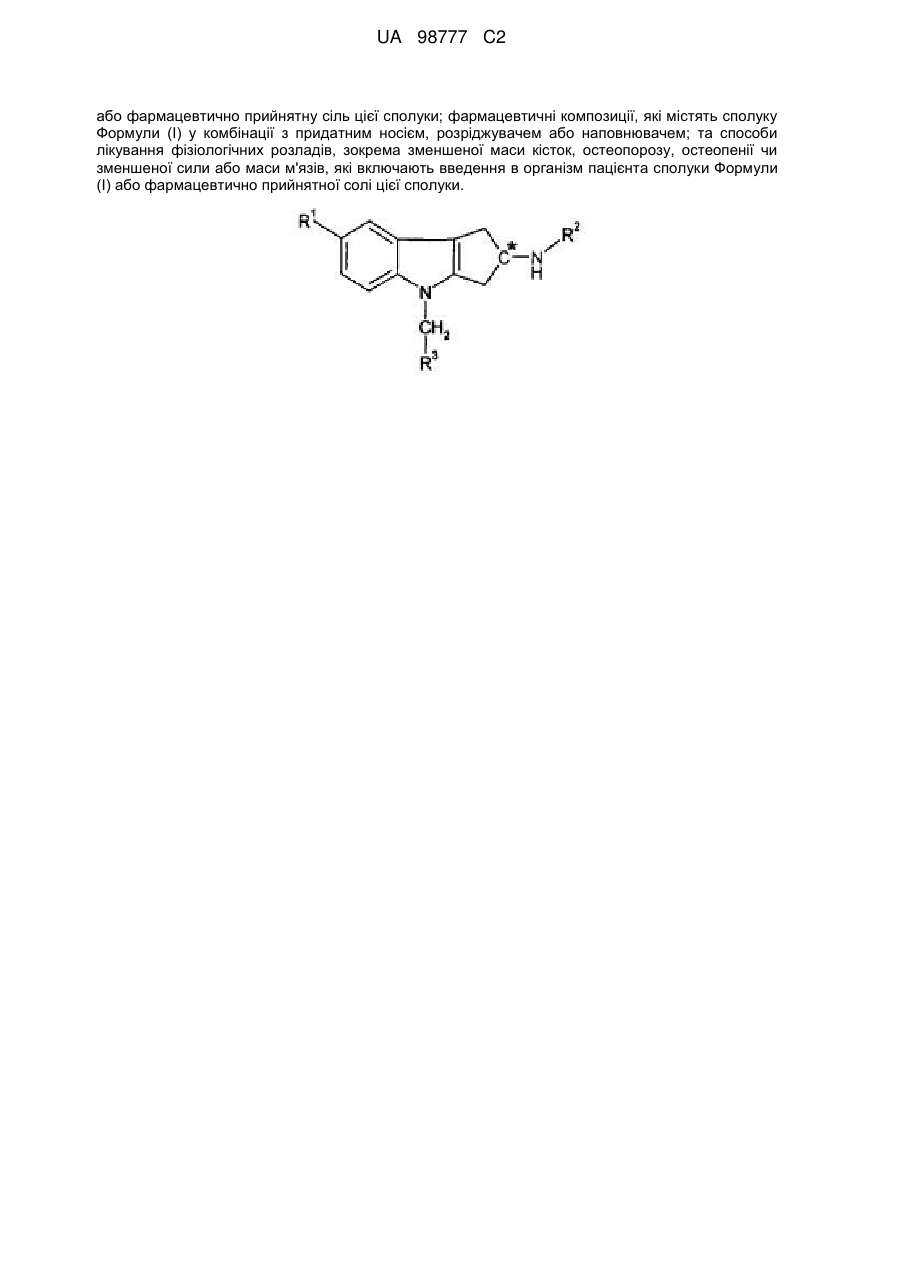
1. Сполука Формули (І):
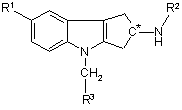 , Формула (І)
, Формула (І)
де
вуглецевий хіральний центр "С*" може бути в R-, S- або R/S-конфігурації;
R1 - ціаногрупа, -CH=NOCH3, -OCHF2 або -OCF3;
R2 - -COR2a або -SO2R2b;
R2a - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або -NRaRb;
R2b - (С1-С4)алкіл, циклопропіл або -NRaRb;
кожний з Ra та Rb незалежно один від одного у кожному випадку є Н або (С1-С4)алкіл; та
R3 - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, етил, бром, хлор, фтор, -CHF2, -CF3, гідроксил, аміногрупа та -NHCH2CO2H;
або фармацевтично прийнятна сіль цієї сполуки.
2. Сполука або сіль за п. 1, де R1 - ціаногрупа або -CH=NOCH3.
3. Сполука або сіль за п. 2, де R1 - ціаногрупа.
4. Сполука або сіль за будь-яким із пп. 1-3, де R2a - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або N(СН3)2, та R2b - (С1-С4)алкіл, циклопропіл, -N(CH3)2 або -N(C2H5)2.
5. Сполука або сіль за п. 4, де R2 - -COR2a, та R2a - етил, ізопропіл, метокси-, етокси-, пропокси-, ізопропокси-, ізобутокси-, тpeт-бутоксигрупа, циклопропіл або -N(СН3)2.
6. Сполука або сіль за п. 5, де R2a - ізопропоксигрупа.
7. Сполука або сіль за п. 4, де R2 - SO2R2b, та R2b - метил, етил, пропіл, циклопропіл, -N(CH3)2 або -N(C2H5)2.
8. Сполука або сіль за п. 7, де R2b - -N(СН3)2.
9. Сполука або сіль за будь-яким із пп. 1-6, де R2 - -COR2a, та вуглецевий хіральний центр "С*" має S-конфігурацію.
10. Сполука або сіль за будь-яким із пп. 1-4, п. 7 або п. 8, де R2 - -SO2R2b, та вуглецевий хіральний центр "С*" має R-конфігурацію.
11. Сполука або сіль за будь-яким із пп. 1-10, де R3 - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, бром, хлор, фтор, CHF2, гідроксил, аміногрупа та -NHCH2CO2H.
12. Сполука або сіль за п. 11, де R3 - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2-амінопіридин-3-іл, 2-карбоксиметиламінопіридин-3-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2-хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4-амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3-хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3-амінопіразин-2-іл або 3-метилпіразин-2-іл.
13. Сполука або сіль за п. 12, де R3 - піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5-іл.
14. Сполука або сіль за п. 1, де
вуглецевий центр "С*" має S-конфігурацію, коли R2 - -COR2a, та R-конфігурацію, коли R2 - -SO2R2b;
R1 - ціаногрупа або -CH=NOCH3;
R2a - етил, ізопропіл, метокси-, етокси-, пропокси-, ізопропокси-, ізобутокси-, тpeт-бутоксигрупа, циклопропіл або N(СН3)2; та R2b - метил, етил, пропіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; та
R3 - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2-амінопіридин-3-іл, 2-карбоксиметиламінопіридин-3-іл, піримідин-4-іл, піримідин-2-іл, 2-хлорпіримідин-4-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2-хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4-амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3-хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3-амінопіразин-2-іл, 3-метилпіразин-2-іл, піридазин-3-іл, 5-бромізотіазол-3-іл, ізотіазол-3-іл, 4,5-дихлорізотіазол-3-іл або [1,2,5]тіадіазол-3-іл.
15. Сполука, вибрана з групи, яку складають
ізопропіловий складний ефір (S)-(7-ціано-4-піридин-2-ілметил-1,2,3,4-тетрагідроциклопента[b]індол-2-іл)карбамінової кислоти;
ізопропіловий складний ефір (S)-(7-ціано-4-тіазол-5-ілметил-1,2,3,4-тетрагідроциклопента[b]індол-2-іл)карбамінової кислоти;
ізопропіловий складний ефір (S)-[4-(2-амінопіридин-3-ілметил)-7-ціано-1,2,3,4-тетрагідроциклопента[b]індол-2-іл]карбамінової кислоти;
(R)-N'-[4-(4-амінотіазол-5-ілметил)-7-ціано-1,2,3,4-тетрагідроциклопента[b]індол-2-іл]-N,N-диметилсульфамід та
ізопропіловий складний ефір (S)-[4-(4-амінотіазол-5-ілметил)-7-ціано-1,2,3,4-тетрагідроциклопента[b]індол-2-іл]карбамінової кислоти,
або фармацевтично прийнятна сіль цієї сполуки.
16. Сполука або сіль за п. 15, яка являє собою ізопропіловий складний ефір (S)-(7-ціано-4-піридин-2-ілметил-1,2,3,4-тетрагідроциклопента[b]індол-2-іл)карбамінової кислоти.
17. Сполука або сіль за будь-яким із пп. 1-16 для застосування в лікуванні гіпогонадизму, зменшеної маси або густини кісток, остеопорозу, остеопенії, зменшеної сили або маси м'язів, саркопенії, пов'язаного з віком послаблення функцій, затримки статевого дозрівання у хлопчиків, анемії, чоловічої або жіночої сексуальної дисфункції, еректильної дисфункції, ослабленого лібідо, депресії або загальмованості.
18. Застосування сполуки або солі за будь-яким із пп. 1-16 для виготовлення лікарського засобу для лікування гіпогонадизму, зменшеної маси або густини кісток, остеопорозу, остеопенії, зменшеної сили або маси м'язів, саркопенії, пов'язаного з віком послаблення функцій, затримки статевого дозрівання у хлопчиків, анемії, чоловічої або жіночої сексуальної дисфункції, еректильної дисфункції, ослабленого лібідо, депресії або загальмованості.
19. Застосування за п. 18 для виготовлення лікарського засобу для лікування зменшеної маси або густини кісток, остеопорозу, остеопенії чи зменшеної сили або маси м'язів.
20. Фармацевтична композиція, яка містить сполуку або сіль за будь-яким із пп. 1-16 у поєднанні з одним або декількома фармацевтично прийнятними носіями, розріджувачами або наповнювачами.
Текст
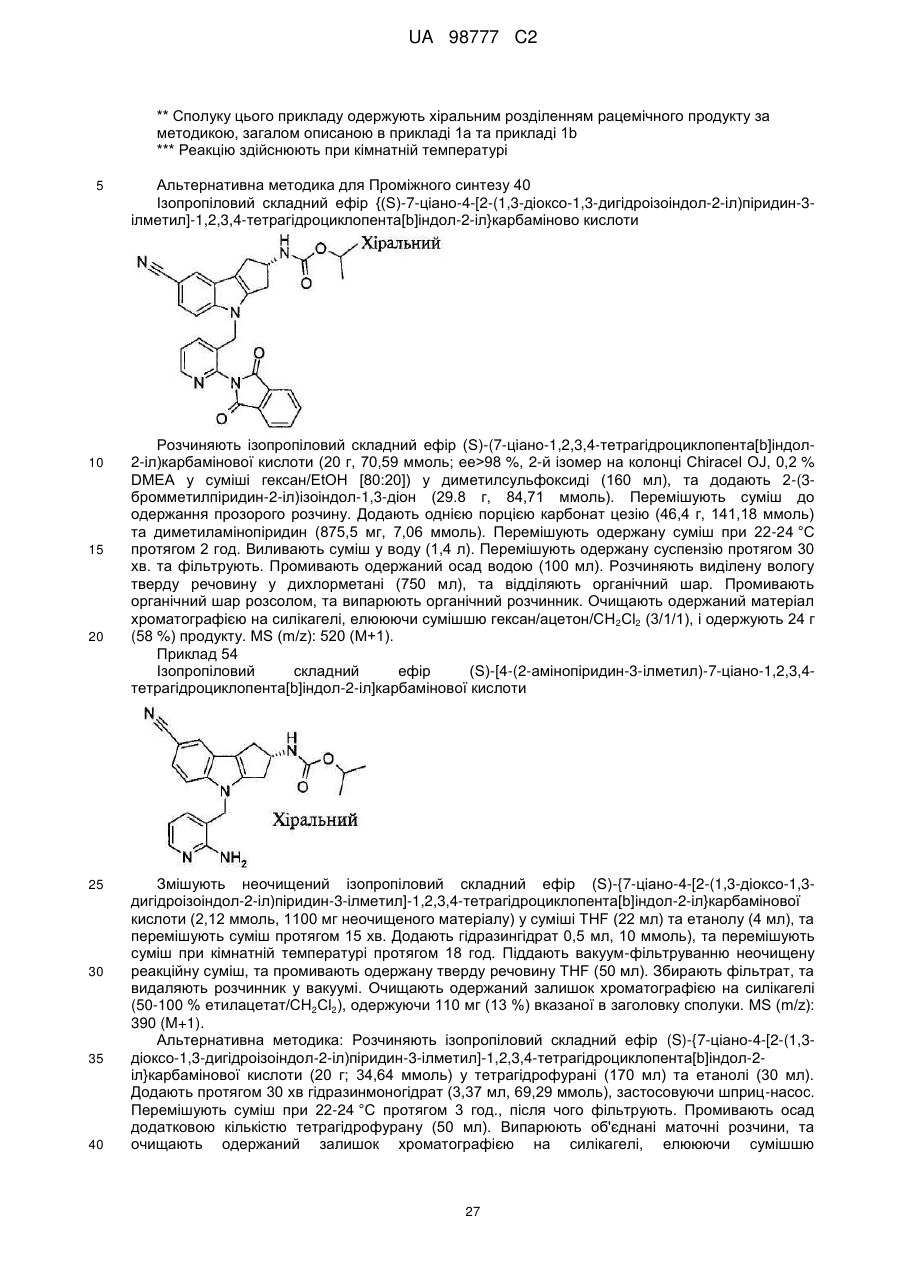
Реферат: Цей винахід описує сполуку формули: R1 R2 C* N N H CH2 R3 , Формула (І) UA 98777 C2 (12) UA 98777 C2 або фармацевтично прийнятну сіль цієї сполуки; фармацевтичні композиції, які містять сполуку Формули (І) у комбінації з придатним носієм, розріджувачем або наповнювачем; та способи лікування фізіологічних розладів, зокрема зменшеної маси кісток, остеопорозу, остеопенії чи зменшеної сили або маси м'язів, які включають введення в організм пацієнта сполуки Формули (І) або фармацевтично прийнятної солі цієї сполуки. UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 Цей винахід стосується тетрагідроциклопента[b]індолів або їх фармацевтично прийнятних солей, корисних як лікувальні засоби, фармацевтичних композицій, які містять згадані сполуки або солі, способів застосування цих сполук або солей для лікування розладів у пацієнтів та проміжних продуктів та способів, корисних при синтезі згаданих сполук. Ендогенні стероїдні андрогени надзвичайно сильно впливають на численні фізіологічні функції. Ефекти стероїдних андрогенів (наприклад, тестостерону та 5α-дигідротестостерону (DHT)) опосередковуються андрогеновим рецептором (AR) та можуть бути охарактеризовані як ефекти анаболічної або андрогенної природи. Після зв'язування андрогену AR зазнає конформаційної зміни, а потім переміщується у ядро клітини, де він приєднується до специфічних послідовностей ДНК, які звуться андроген-чутливими елементами (ARE), для ініціювання або пригнічення транскрипції генів-мішеней. До анаболічних (тобто таких, що спричиняють нарощування тканин) ефектів андрогенів належать збільшення маси та сили м'язів та маси кісток, в той час як до андрогенних (тобто маскулінізаційних) ефектів належать розвиток вторинних чоловічих статевих ознак, наприклад, внутрішніх репродуктивних органів (тобто простати та сім'яних пухирців), зовнішніх статевих органів (пеніса та мошонки), лібідо та волосистості шкіри. Зниження рівнів андрогенів, яке може виникати при старінні, пов'язане зі значними ефектами як у чоловіків, так і в жінок. Наприклад, при старінні чоловіків та зниженні рівнів тестостерону розвивається знеміцнення кісток, посилення розвитку діабету та серцевосудинних захворювань та зниження відношення маси м'язів до маси жиру. У жінок низькі рівні циркулюючого у плазмі тестостерону пов'язане зі зниженням лібідо, непоясненною втомою, загальним погіршенням стану здоров'я та самопочуття та втратою мінеральної міцності кісток у жінок у клімактеричному періоді. У клінічних умовах головним застосуванням андрогенової терапії є лікування гіпогонадизму у чоловіків. Виявлено важливий факт, що заміщувальна андрогенова терапія чоловіків, що страждають на гіпогонадизм, спричиняє зменшення резорбції кісток та збільшення маси кісток. До інших показань, при яких клінічно застосовувалися андрогени, належать лікування затримки статевого дозрівання у хлопчиків, анемії, первинного остеопорозу та захворювань, пов'язаних зі втратою маси м'язів. Крім того, останнім часом заміщувальна андрогенова терапія застосовувалася до старіючих чоловіків та для регулювання чоловічої фертильності. До жінок андрогенова терапія застосовувалася клінічно для лікування статевої дисфункції або послабленого лібідо. Однак андрогенова терапія має певні обмеження. Наприклад, до небажаних побічних ефектів стероїдної андрогенної терапії належать стимуляція росту простати та сім'яних пухирців. Крім того, із застосуванням андрогенів пов'язані стимуляція пухлин простати та підвищення рівня простато-специфічного антигену (PSA) (що є показником підвищеного ризику раку простати). Далі, виявлено, що препарати немодифікованих та модифікованих стероїдних андрогенів зазнають швидкої деградації у печінці, наслідком чого є їхня незадовільна біодоступність при пероральному вживанні та короткочасність дії після парентерального введення, нестабільність концентрацій у плазмі, гепатотоксичність або перехресне реагування з рецепторами інших стероїдних гормонів (наприклад, із рецепторами глюкокортикоїдів (GR), рецепторами мінералокортикоїдів (MR) та рецепторами прогестерону (PR)). Крім того, застосування стероїдних андрогенів до жінок може призвести до гірсутизму (надлишкового оволосіння) або маскулінізації. Таким чином, у галузі залишається постійна потреба в альтернативних засобах для стероїдної андрогенової терапії, які мають позитивні фармакологічні властивості стероїдних андрогенів, але знижену ймовірність або частоту виникнення типових небажаних ефектів, пов'язаних зі стероїдною андрогеновою терапією. Сучасні спроби віднайдення придатних замінників стероїдних андрогенів зосереджуються на пошуках тканино-селективних модуляторів андрогенових рецепторів (SARM), які виявляють диференційовану активність в андрогенних тканинах. Зокрема, такі засоби за варіантом, якому віддається перевага, виявляють активність як агоністи андрогенів в анаболічних тканинах, наприклад, у м'язах або кістках, але є лише частковими агоністами або навіть антагоністами в інших андрогенних тканинах, наприклад, у простаті або сім'яних пухирцях. Таким чином, метою цього винаходу є запропонувати нестероїдні ліганди AR, які виявляють активність як агоністи андрогенів. Більш конкретно, метою винаходу є запропонувати нестероїдні агоністи андрогенів, які зв'язуються з AR з підвищеною спорідненістю у порівнянні з іншими рецепторами стероїдних гормонів. Ще більш конкретно, метою винаходу є запропонувати тканино-селективні модулятори андрогенових рецепторів (SARM), які виявляють активність як агоністи андрогенів у м'язах або кістках, але є лише частковими агоністами, 1 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 частковими антагоністами або антагоністами в андрогенних тканинах, наприклад, у простаті або сім'яних пухирцях. Подані нижче посилання містять приклади сучасного стану галузі стосовно до цього винаходу: Браун - Brown, Endocrinology (2004); 145(12): 5417-5419, пропонує огляд нестероїдних селективних модуляторів андрогенових рецепторів. Каділья та ін. - Cadilla et a!., Curr. Top. Med Chem (2006); 6(3): 245-270 пропонує огляд модуляторів андрогенових рецепторів. Сегал та ін. - Segal et al, Expert Opin. Investig. Drugs (2006); 15(4); 377-387 пропонує огляд модуляторів андрогенових рецепторів. Паралельно розглядана міжнародна заявка PCT/US2006/024122 розкриває похідні тетрагідрокарбазолу як модулятори андрогенових рецепторів. Цей винахід базовано на віднайденні того, що певні похідні тетрагідроциклопента[b]індолу, визначені поданою нижче Формулою (І), мають специфічну активність, яка свідчить про їх корисність при лікуванні розладів, чутливих до стероїдної андрогенової терапії. Відповідно, цей винахід пропонує сполуку Формули (І): , Формула (І) де вуглецевий хіральний центр "С*" може бути в R, S або R/S конфігурації; 1 R - ціаногрупа, -CH=NOCH3, -OCHF2 або -OCF3; 2 2a 2b R - -COR або -SO2R ; 2a a b R - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або -NR R ; 2b a b R - (С1-С4)алкіл, циклопропіл або -NR R ; a b кожний з R та R незалежно один від одного у кожному випадку є Η або (С1-С4)алкіл; та 3 R - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, етил, бром, хлор, фтор, -CHF2, -CF3, гідроксил, аміногрупа та -NHCH2CO2H, або фармацевтично прийнятну сіль цієї сполуки. За іншим варіантом здійснення цей винахід пропонує спосіб лікування гіпогонадизму, зменшеної маси або густини кісток, остеопорозу, остеопенії, зменшеної сили або маси м'язів, саркопенії, пов'язаного з віком послаблення функцій, затримки статевого дозрівання у хлопчиків, анемії, чоловічої або жіночої сексуальної дисфункції, еректильної дисфункції, ослабленого лібідо, депресії або загальмованості, який включає введення в організм пацієнта, який потребує такого лікування, ефективної кількості сполуки Формули (І) або фармацевтично прийнятної солі цієї сполуки. Як більш конкретний варіант здійснення цей винахід пропонує спосіб лікування зменшеної маси або густини кісток, остеопорозу, остеопенії або зменшеної сили або маси м'язів. Крім того, цей винахід пропонує застосування сполуки Формули (І) або фармацевтично прийнятної солі цієї сполуки як засобу для лікування гіпогонадизму, зменшеної маси або густини кісток, остеопорозу, остеопенії, зменшеної сили або маси м'язів, саркопенії, пов'язаного з віком послаблення функцій, затримки статевого дозрівання у хлопчиків, анемії, чоловічої або жіночої сексуальної дисфункції, еректильної дисфункції, ослабленого лібідо, депресії або загальмованості. Більш конкретно, цей винахід пропонує застосування сполуки Формули (І) або фармацевтично прийнятної солі цієї сполуки як засобу для лікування зменшеної маси або густини кісток, остеопорозу, остеопенії чи зменшеної сили або маси м'язів. Крім того, цей винахід пропонує сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки для застосування в терапії. За іншим варіантом здійснення цей винахід пропонує застосування сполуки Формули (І) або фармацевтично прийнятної солі цієї сполуки для виготовлення лікарського засобу для лікування гіпогонадизму, зменшеної маси або густини кісток, остеопорозу, остеопенії, зменшеної сили або маси м'язів, саркопенії, пов'язаного з віком послаблення функцій, затримки статевого 2 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 60 дозрівання у хлопчиків, анемії, чоловічої або жіночої сексуальної дисфункції, еректильної дисфункції, ослабленого лібідо, депресії або загальмованості. Більш конкретно, цей винахід пропонує застосування сполуки Формули (І) для виготовлення лікарського засобу для лікування зменшеної маси або густини кісток, остеопорозу, остеопенії чи зменшеної сили або маси м'язів. Крім того, цей винахід пропонує фармацевтичну композицію, яка містить сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки у комбінації з одним або більше фармацевтично прийнятними носіями, розріджувачами або наповнювачами. Більш конкретно, цей винахід пропонує фармацевтичну композицію для лікування зменшеної маси або густини кісток, остеопорозу, остеопенії чи зменшеної сили або маси м'язів, яка містить сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки у комбінації з одним або більше фармацевтично прийнятними носіями, розріджувачами або наповнювачами. Цей винахід також охоплює нові проміжні сполуки та способи, корисні для синтезу сполуки Формули (І). Цей винахід стосується нових тетрагідроциклопентаіндолів, визначених наведеною у цьому документі Формулою (І). Як доводять дослідження in vitro та in vivo, взяті за приклади сполуки Формули (І) мають активність, яка наводить на думку про їх корисність в лікуванні розладів, чутливих до стероїдної андрогенової терапії. Зокрема, взяті за приклади сполуки Формули (І) є ефективними лігандами AR, які мають спорідненість до андрогенових рецепторів. Крім того, взяті за приклади сполуки Формули (І) більш селективно зв'язуються з AR у порівнянні до кожного з рецепторів MR, GR та PR. Вважають, що сполуки Формули (І) або фармацевтично прийнятні солі цих сполук є корисними при лікуванні розладів, які звичайно лікують із застосуванням андрогенової терапії. Таким чином, способи лікування розладів, чутливих до андрогенової терапії, охоплюються цим винаходом та є одним із важливих варіантів його здійснення. До таких розладів належать гіпогонадизм, зменшена маса або густина кісток, остеопороз, остеопенія, зменшена сила або маса м'язів, саркопенія, пов'язане з віком послаблення функцій, затримка статевого дозрівання у хлопчиків, анемія, чоловіча або жіноча сексуальна дисфункція, еректильна дисфункція, ослаблене лібідо, депресія та загальмованість. До більш конкретних розладів, для лікування яких сполуки Формули (І) є корисними, належать зменшена маса або густина кісток, остеопороз, остеопенія чи зменшена сила або маса м'язів. Цей винахід також стосується сольватів сполуки Формули (І) або фармацевтично прийнятних солей сполук Формули (І). Таким чином, при вживанні в цьому описі термін "Формула (І)", або вказана будь-яка конкретна сполука Формули (І), охоплює в рамках свого значення будь-яку фармацевтично прийнятну сіль та будь-який сольват сполуки або її фармацевтично прийнятної солі. Приклади фармацевтично прийнятних солей та способи їх одержання відомі фахівцям у галузі. Дивись, наприклад, Шталь та ін. "Довідник з фармацевтичних солей: властивості, вибір та застосування" (Stahl et al "Handbook of Pharmaceutical Salts: Properties, Selection та Use, " VCHA/Wiley-VCH, (2002)); Гульд "Добір солей для лікарських речовин основного характеру" (Gould P.L. "Salt selection for basic drugs", International Journal of Pharmaceutics, 33: 201-217 (1986)); Берж та ін. "Фармацевтичні солі" (Berge et al. "Pharmaceutical Salts", Journal of Pharmaceutical Sciences, 66, No. 1, (January 1977)); та Бастен та ін. "Вибір солей та методики оптимізації для нових фармацевтичних хімічних сполук" (Bastin et al. "Salt Selection and Optimization Procedures for Pharmaceutical New Chemical Entities", Organic Process Research and Development, 4: 427-435 (2000)). Сполуки за цим винаходом містять один або декілька хіральних центрів та можуть, таким чином, існувати у різноманітних стереоізомерних конфігураціях. Внаслідок наявності цих хіральних центрів сполуки за цим винаходом можуть зустрічатися у вигляді рацематів, сумішей енантіомерів та індивідуальних енантіомерів, а також діастереомерів та сумішей діастереомерів. За винятком вказаних в цьому описі випадків, всі такі рацемати, енантіомери та діастереомери охоплюються цим винаходом. Енантіомери сполук, запропонованих цим винаходом, можуть бути розділені, наприклад, із застосуванням звичайних способів, відомих у галузі, наприклад, таких як описані у монографії Жак та ін. "Енантіомери, рацемати та їх розділення" (J. Jacques, et al. "Enantiomers, Racemates, and Resolutions",John Wiley and Sons, Inc., 1981), а також способів, запропонованих на схемах та у прикладах цього документа. Терміни "R" та "S" в цьому документі вживаються у їхньому звичайному значенні в органічній хімії для позначення конкретних конфігурацій хірального центра. Терміни "(±)" або "RS" стосуються конфігурації хірального центра, яка відповідає рацемату. Частковий перелік пріоритетів та розгляд питань стереохімії міститься у монографії під редакцією Флетчер та ін. "Номенклатура органічних сполук. Принципи та практика" ("Nomenclature of Organic Compounds: Principles and Practice", J.H. Fletcher, et al, eds., 1974). 3 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 Конкретні стереоізомери та енантіомери сполук Формули І можуть бути одержані пересічним фахівцем у галузі із застосуванням добре відомих способів та процесів, наприклад, описаних у монографіях Ельєл та Уайлен "Стереохімія органічних сполук" (Eliel and Wilen, "Stereochemistry of Organic Compounds", John Wttey & Sons, Inc., 1994), Розділ 7: "Відділення стереоізомерів, розділення та рацемізація"; та Колле та Уайлен "Енантіомери, рацемати та їх розділення" (Collet and Wilen, "Enantiomers, Racemates, and Resolutions", John Wiley & Sons, Inc., 1981). Наприклад, конкретні стереоізомери та енантіомери можна одержати шляхом стереоспецифічних синтезів із застосуванням енантіомерно та геометрично чистих або енантіомерно та геометрично збагачених вихідних матеріалів. Крім того, конкретні стереоізомери та енантіомери можуть бути розділені та виділені, наприклад, способами хроматографії на хіральних стаціонарних фазах, ферментного розділення або фракційної перекристалізації солей з реагентами, застосовуваними для цієї мети. У значенні, вживаному у цьому описі, термін "(С1-С4)алкіл" означає лінійний або розгалужений одновалентний насичений аліфатичний ланцюг з 1-4 атомів вуглецю. У значенні, вживаному у цьому описі, термін "(С1-С4)алкокси(група)" означає атом кисню, до якого приєднаний лінійний або розгалужений одновалентний насичений аліфатичний ланцюг з 1-4 атомів вуглецю. У значенні, вживаному у цьому описі, терміни "гало" або "галоген" означає атоми хлору, брому, йоду або фтору, якщо конкретно не зазначено інше. Як зрозуміло для пересічного фахівця у галузі, деякі гетероарильні фрагменти сполук Формули (І) можуть існувати у формі позиційних ізомерів та як таутомерні форми. Цей винахід охоплює всі позиційні ізомери, індивідуальні таутомерні форми, а також будь-яку їх комбінацію у назвах гетероарильних фрагментів сполук Формули І. Позначення " " означає зв'язок, який виступає над площиною сторінки документа, на якій зображено згадане позначення. Позначення " " означає зв'язок, який заглиблений під площиною сторінки документа, на якій зображено згадане позначення. Позначення " " означає зв'язок, який існує у вигляді суміші зв'язків, які виступають над площиною сторінки документа, на якій зображено згадане позначення, та заглиблені під неї. Як зрозуміло для фахівця у галузі, фізіологічні розлади можуть мати форму "хронічного" стану або "гострого" нападу. Термін "хронічний" у значенні, вживаному у цьому описі, означає стан повільного розвитку та тривалої наявності. У таких випадках хронічний стан лікують після встановлення діагнозу, і лікування триває протягом періоду наявності захворювання. Навпаки, термін "гострий" означає посилений короткочасний напад або період загострення, після якого наступає період ремісії. Таким чином, поняття лікування розладів охоплює лікування як гострих, так і хронічних станів. При гострому стані сполуку застосовують із появою симптомів та припиняють застосування при зникненні симптомів. Як вказано вище, хронічний стан лікують протягом періоду захворювання. У значенні, вживаному у цьому описі, термін "пацієнт" означає людську істоту або іншого ссавця, наприклад, собаку, кота, корову, мавпу, коня, свиню або вівцю. Однак мається на увазі, що серед пацієнтів, до яких можна застосовувати сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки, перевага віддається людині. Термін "лікування" ("лікувати") у значенні, вживаному у цьому описі, охоплює запобігання, профілактику, обмеження, уповільнення, припинення або обернення напрямку розвитку або тяжкості симптому або розладу. Таким чином, способи за цим винаходом охоплюють як терапевтичне, так і профілактичне застосування. Сполуки за цим винаходом можуть бути введені як компоненти до складу фармацевтичних композицій. Таким чином, важливим варіантом здійснення цього винаходу є фармацевтична композиція, яка містить сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки у комбінації з фармацевтично прийнятним носієм, розріджувачем або наповнювачем. Приклади фармацевтичних композицій та способи їх виготовлення добре відомі в галузі. Дивись th наприклад, Remington: The science and practice of pharmacy (A. Gennaro, et al., eds., 19 ed., Mack Publishing (1995)). До прикладів композицій, які містять сполуки Формули (І), належать, наприклад: Сполука Формули (І) у суспензії з 1 % натрієвої карбоксиметилцелюлози, 0,25 % полісорбату-80 та 0,05 % протиспінювального реагенту Antifoam 1510™ (Dow Corning); та сполука Формули (І) у суспензії з 0,5 % метилцелюлози, 0,5 % лаурилсульфату натрію та 0,1 % Antifoam 1510 у 0,01-н. НСl (кінцеве значення рН приблизно 2,5-3). Композиція за цим винаходом, якій віддається перевага, містить сполуку Формули (І) або фармацевтично прийнятну сіль цієї сполуки у лікарській формі капсули або таблетки. Сполуку Формули (І) або 4 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 60 композицію, яка містить сполуку Формули (І), можна вводити в організм будь-яким шляхом, який забезпечує біодоступність сполуки, в тому числі пероральним та парентеральним шляхами. Для фахівця у галузі зрозуміло, що розмір частинок може впливати на розчинення фармацевтичного засобу in vivo, що, у свою чергу, може впливати на засвоєння засобу. Термін "розмір частинок" у значенні, вживаному у цьому описі, означає діаметр частинки фармацевтичного засобу, визначений звичайними способами, наприклад, за розсіянням лазерного світла, дифракцією лазерного променя, розсіянням Мi, фракціонуванням потоку у полі седиментації, кореляційною фотонною спектроскопією тощо. Якщо фармацевтичні засоби мають низьку розчинність, то малий або зменшений розмір частинок може сприяти розчиненню і, отже, підвищенню засвоєння засобу (Амідон та ін. - Amidon et ai, Pharm. Research, 12; 413-420 (1995)). Способи зменшення або регулювання розмірів частинок відомі та включають розмелювання, розтирання мокрим способом, подрібнення до мікрометрового розміру тощо. Інший спосіб регулювання розмірів частинок включає виготовлення фармацевтичного засобу у формі наносуспензії. Конкретним варіантом здійснення цього винаходу є сполука Формули (І) або фармацевтична композиція, яка містить сполуку Формули (І), де згадана сполука має середній розмір частинок менше ніж приблизно 20 мкм або показник розміру частинок d90 (тобто максимальний розмір 90 % частинок) менше ніж приблизно 50 мкм. Варіант здійснення, якому віддається більша перевага, включає сполуку Формули І, яка має середній розмір частинок менше ніж приблизно 10 мкм або показник розміру частинок d90 менше ніж приблизно 30 мкм. У значенні, вживаному у цьому описі, термін "ефективна кількість" означає кількість або дозу сполуки Формули (І), яка при введенні однієї або кількох доз в організм пацієнта забезпечує бажаний ефект у пацієнта, який підлягає діагностуванню або лікуванню. Ефективну кількість може без утруднень визначити лікар-куратор, будучи фахівцем у галузі, з урахуванням численних факторів, наприклад, виду ссавця, його маси тіла, віку та загального стану здоров'я; конкретного захворювання, яке підлягає лікуванню; ступеня розвитку або тяжкості захворювання; індивідуальної реакції пацієнта; конкретної застосовуваної сполуки; способу введення; характеристик біодоступності застосовуваного препарату; обраного режиму дозування; та застосування будь-яких супутніх терапевтичних засобів. При застосуванні у зв'язку зі способами та варіантами застосування за цим винаходом, сполуки та композиції за цим винаходом можна вводити в організм або окремо, або у комбінації зі звичайними терапевтичними засобами, які застосовуються для лікування конкретних розладів або патологічних станів. Якщо сполуки або композиції за цим винаходом застосовуються як складова частина комбінації, то сполуку або комбінацію, яка включає сполуку Формули (І), можна застосовувати окремо або як складову частину лікарської форми, яка містить терапевтичний засіб, з яким згадана сполука має бути скомбінована. Комплексна терапія розрідження кісток, остеопорозу або остеопенії: Звичайні терапевтичні засоби для лікування остеопорозу доцільно комбінувати зі сполуками Формули (І) або композиціями, які містять сполуки Формули (І). До звичайних засобів для лікування остеопорозу належать засоби для заміщувальної гормональної терапії, наприклад, кон'югований кінський естроген (Premarin™), синтетичний кон'югований естроген (Cenestin™), естерифікований естроген (Estratab™ або Menest™), естропіат (Ogen™ або Ortho-est™); а також препарати естрадіолу для черезшкірного введення, наприклад, Alora™, Climara™, Estraderm™ та Vivelle™. На ринку наявні також комплексні естроген-прогестинові лікарські препарати для лікування остеопорозу, в тому числі Prempro™ (кон'югований кінський естроген та ацетат медроксипрогестерону), Premphase™ (кон'югований кінський естроген та норгестимат), OrthoPrefest™ (естрадіол та норгестимат), Femhrt™ (етиніл-естрадіол та ацетат норетиндрону) та Combipatch™ (естрадіол для черезшкірного введення та ацетат норетиндрону). До інших відомих засобів для лікування остеопорозу, які можуть бути скомбіновані зі сполуками або композиціями за цим винаходом, належать бісфосфонати, наприклад, алендронат (Fosamax™), ризендронат (Actonel™) та памідронат (Aredia™); селективні модулятори естрогенових рецепторів (SERM), наприклад, ралоксифен (Evista™); кальцитонін (Calcimar™ або Miacalcin™); паращитоподібний гормон (Forteo™); кальцій; вітамін D; діуретики (для зниження виділення 2+ Са ); фториди та андрогени (наприклад, тестостерон або 5α-дигідротестостерон). Таким чином, композиція для комплексної терапії при лікуванні остеопорозу містить: Інгредієнт (А1): сполука Формули (І); Інгредієнт (А2): один або декілька допоміжних лікарських засобів, які звичайно застосовуються для лікування остеопорозу, вибраних з групи, яку складають премарин (Premarin™), ценестин (Cenestin™), естратаб (Estratab™), менест (Menest™), оген (Ogen™), орто-ест (Ortho-est™), алора (АІоrа™), клімара (Climara™), естрадерм (Estraderm™), вівел 5 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 60 (Vivelle™), премпро (Prempro™), премфаза (Premphase™), орто-префест (Ortho-Prefest™), фемхрт (Femhrt™), комбіпатч (Combipatch™), фосамакс (Fosamax™), актонел (Actonel™), аредія (Aredia™); евіста (Evista™); кальцимар (Calcimar™), міакальцин (Miacalcin™), фортео (Forteo™), кальцій, вітамін D, діуретики, фториди, тестостерон та 5α-дигідротестостерон; та факультативно Інгредієнт (A3): фармацевтично прийнятний носій, розріджувач або наповнювач. Конкретні варіанти здійснення винаходу Нижченаведений перелік включає декілька груп конкретних замісників та конкретні змінні групи для сполук Формули (І). Мається на увазі, що сполуки Формули (І), які містять такі конкретні замісники або змінні групи, а також способи та варіанти застосування таких сполук є конкретними варіантами здійснення цього винаходу. 2 Таким чином, конкретним варіантом здійснення цього винаходу є сполука Формули (І), де R 3 та R мають будь-яке зі значень, визначених у цьому описі, та: 1 (a) R - ціаногрупа, -CH=NOCH3 або -OCF3; або 1 (b) R - ціаногрупа або -CH=NOCH3; або 1 (c) R - ціаногрупа; або 1 (d) R - -CH=NOCH3. 1 3 Іншим конкретним варіантом здійснення винаходу є сполука Формули (І), де R та R мають будь-яке зі значень, визначених у цьому описі, та: 2 2a 2b 2a (a) R - -COR або -SO2R , де R - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або 2b N(CH3)2, та R -(С1-С4)алкіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; або 2 2a 2b 2a (b) R - -COR або -SO2R , де R - етил, ізопропіл, метокси-, етокси-, пропокси-, 2b ізопропокси-, ізобутокси-, трет-бутоксигрупа, циклопропіл або -N(CH3)2, та R - метил, етил, пропіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; або 2 2a 2a (c) R - -COR , де R - етил, ізопропіл, метокси-, етокси-, пропокси-, ізопропокси-, ізобутокси-, трет-бутоксигрупа, циклопропіл або -N(CH3)2; або 2 2a 2a (d) R - -COR , де R - ізопропіл, етокси-, ізопропоксигрупа або циклопропіл; або 2 2a 2a (e) R - -COR , де R - ізопропоксигрупа; або 2 2b 2b (f) R - -SO2R , де R - метил, етил, пропіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; або 2 2b 2b (g) R - -SO2R , де R - циклопропіл або -N(CH3)2; або 2 2b 2b (h) R - -SO2R , де R - -N(CH3)2. 1 3 Іншим конкретним варіантом здійснення винаходу є сполука Формули (І), де R та R мають будь-яке зі значень, визначених у цьому описі, та: 2 2a (a) R - -COR та вуглецевий центр "С*" має S-конфігурацію; або 2 2b (b) R - -SO2R та вуглецевий центр "С*" має R-конфігурацію. Іншим конкретним варіантом здійснення винаходу є сполука 1 2 Формули (І), де R та R мають будь-яке зі значень, визначених у цьому описі, та: 3 (a) R - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, бром, хлор, фтор, -CHF2, гідроксил, аміногрупа та -NHCH2CO2H; або 3 (b) R - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2-амінопіридин-3-іл, 2-карбоксиметиламінопіридин-3-іл, піримідин-4-іл, піримідин-2-іл, 2хлорпіримідин-4-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2-хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3-хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3амінопіразин-2-іл, 3-метилпіразин-2-іл, піридазин-3-іл, 5-бромізотіазол-3-іл, ізотіазол-3-іл, 4,5дихлор-ізотіазол-3-іл або [1,2,5]тіадіазол-3-іл; 3 (c) R - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2-амінопіридин-3-іл, 2-карбоксиметиламінопіридин-3-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4-амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3-амінопіразин-2-іл або 3-метилпіразин-2-іл; 3 (d) R - 6-фторпіридин-2-іл, піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5іл; або 3 (e) R - піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5-іл. Більш конкретним варіантом здійснення цього винаходу є сполука Формули (І), де 2 2a 2 вуглецевий центр "С*" має S-конфігурацію, коли R - -COR , та S-конфігурацію, коли R - 2b SO2R ; 1 R - ціаногрупа або -CH=NOCH3; 2 2a 2b 2a R - -COR або -SO2R , де R - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або -N(CH3)2, 2b та R - (С1-С4)алкіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; та 6 UA 98777 C2 3 5 10 15 20 25 30 35 40 45 50 R - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, бром, хлор, фтор, -CHF2, гідроксил, аміногрупа та -NHCH2CO2H. Ще більш конкретним варіантом здійснення цього винаходу є сполука Формули (І), де, 2 2a 2 вуглецевий центр "С*" має S-конфігурацію, коли R - -COR , та R-конфігурацію, коли R - 2b SO2R ; 1 R - ціаногрупа або -CH=NOCH3; 2 2a 2b 2a R - -COR або -SO2R , де R - етил, ізопропіл, метокси-, етокси-, пропокси-, ізопропокси-, 2b ізобутокси-, трет-бутоксигрупа, циклопропіл або -N(CH3)2, та R - метил, етил, пропіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; та 3 R - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2амінопіридин-3-іл, 2-карбоксиметил-амінопіридин-3-іл, піримідин-4-іл, піримідин-2-іл, 2хлорпіримідин-4-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2-хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3-хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3амінопіразин-2-іл, 3-метилпіразин-2-іл, піридазин-3-іл, 5-бромізотіазол-3-іл, ізотіазол-3-іл, 4,5дихлор-ізотіазол-3-іл або [1,2,5]тіадіазол-3-іл. Ще більш конкретним варіантом здійснення цього винаходу є сполука Формули (І), де 2 2a 2 вуглецевий центр "С*" має S-конфігурацію, коли R - -COR , та R-конфігурацію, коли R - 2b SO2R ; 1 R - ціаногрупа; 2 2a 2b 2a R - -COR або - -SC2R , де R - ізопропіл, етокси-, ізопропоксигрупа або циклопропіл; та 2b R - циклопропіл або -N(СН3)2; та 3 R - 6-фторпіридин-2-іл, піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5-іл. Ще більш конкретним варіантом здійснення цього винаходу є сполука Формули (І), де 2 2a 2 вуглецевий центр "С*" має S-конфігурацію, коли R - -COR , та R-конфігурацію, коли R - 2b SO2R ; 1 R - ціаногрупа; 2 2a 2b 2a 2b R - -COR або -SO2R , де R - ізопропоксигрупа, R - -N(CH3)2; та 3 R - піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5-іл. За іншими конкретними варіантами здійснення винаходу запропоновані нижченаведені сполуки Формули І(а) та Формули І(b). Мається на увазі, що сполукам Формули І(а) та Формули І(b), а також способам та варіантам застосування таких сполук за цим винаходом віддається особлива перевага. Таким чином, за конкретним варіантом здійснення цього винаходу запропоновано сполуку Формули І(а) , Формула І(а) де 1 R - ціаногрупа, -CH=NOCH3 або -OCF3; 2a R - (С1-С4)алкіл, (С1-С4)алкоксигрупа, циклопропіл або -N(CH3)2; та 3 R – гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, бром, хлор, фтор, -CHF2, гідроксил, аміногрупа та -NHCH2CO2H. Ще більш конкретним варіантом здійснення цього винаходу є сполука Формули І(а), де 1 R - ціаногрупа або -CH=NOCH3; 2a R - етил, ізопропіл, метокси-, етокси-, пропокси-, ізопропокси-, ізобутокси-, третбутоксигрупа, циклопропіл або -N(CH3)2; та 3 R - 6-фторпіридин-2-іл, піридин-2-іл, 3-гідроксипіридин-2-іл, 6-дифторметилпіридин-2-іл, 2амінопіридин-3-іл, 2-карбоксиметил-амінопіридин-3-іл, піримідин-4-іл, піримідин-2-іл, 2 7 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 хлорпіримідин-4-іл, тіазол-4-іл, 2-метилтіазол-4-іл, 2-хлортіазол-4-іл, тіазол-2-іл, тіазол-5-іл, 4амінотіазол-5-іл, піразин-2-іл, 5-метилпіразин-2-іл, 3-хлорпіразин-2-іл, 6-метилпіразин-2-іл, 3амінопіразин-2-іл, 3-метилпіразин-2-іл, піридазин-3-іл, 5-бромізотіазол-3-іл, ізотіазол-3-іл, 4,5дихлор-ізотіазол-3-іл або [1,2,5]тіадіазол-3-іл. Іншим конкретним варіантом здійснення цього винаходу є сполука Формули І(а), де 1 R - ціаногрупа; 2a R - ізопропіл, ізопропокси-, етоксигрупа або циклопропіл; та 3 R - 6-фторпіридин-2-іл, піридин-2-іл, 2-амінопіридин-3-іл, тіазол-5-іл або 4-амінотіазол-5-іл. За іншим конкретним варіантом здійснення цього винаходу, запропоновано сполуку І(b) , Формула І(b) де 1 R - ціаногрупа або -CH=NOCH3; 2b R - (С1-С4)алкіл, циклопропіл, -N(CH3)2 або -N(C2H5)2; та 3 R - гетероарил, вибраний з групи, яку складають піридиніл, піримідиніл, піразиніл, піридазиніл, тіазоліл, ізотіазоліл та тіадіазоліл, кожний з яких факультативно заміщений 1-2 замісниками, незалежно один від одного вибраними з групи, яку складають метил, бром, хлор, фтор, -CHF2, гідроксил, аміногрупа та -NHCH2CO2H. Більш конкретним варіантом здійснення цього винаходу є сполука Формули І(b), де 1 R - ціаногрупа або -CH=NOCH3; 2b R - метил, етил, пропіл, циклопропіл, -N(СН3)2 або -N(C2H5)2; та 3 R - ізотіазол-3-іл, 6-фторпіридин-2-іл, піридин-2-іл, 2-амінопіридин-3-іл, піразин-2-іл, тіазол4-іл, тіазол-2-іл, тіазол-5-іл, 4-амінотіазол-5-іл або [1,2,5]тіадіазол-3-іл. За іншим конкретним варіантом здійснення цього винаходу запроповано сполуку І(b), де 1 R - ціаногрупа; 2b R - циклопропіл або -N(CH3)2; та 3 R - тіазол-4-іл, тіазол-2-іл, тіазол-5-іл або 4-амінотіазол-5-іл. Крім того, мається на увазі, що серед найбільш конкретних варіантів здійснення, якими запропоновані сполуки Формули (І), перелічені у цьому описі, найбільша перевага віддається таким сполукам: ізопропіловий складний ефір (S)-(7-ціано-4-піридин-2-ілметил-1,2,3,4тетрагідроциклопента[b]індол-2-іл)карбамінової кислоти; ізопропіловий складний ефір (S)-(7-ціано-4-тіазол-5-ілметил-1,2,3,4тетрагідроциклопента[b]індол-2-іл)карбамінової кислоти; ізопропіловий складний ефір (S)-[4-(2-амінопіридин-3-ілметил)-7-ціано-1,2,3,4тетрагідроциклопента[b]індол-2-іл]карбамінової кислоти; (R)-N'-[4-(4-амінотіазол-5-Ілметил)-7-ціано-1,2,3,4-тетрагідро-циклопента[b]індол-2-іл]-N,Nдиметилсульфамід, або ізопропіловий складний ефір (S)-[4-(4-амінотіазол-5-ілметил)-7-ціано-1,2,3,4тетрагідроциклопента[b]індол-2-іл]карбамінової кислоти. Сполуки за цим винаходом можуть бути одержані хімічним шляхом, наприклад, за описаними нижче способами синтезу, які представлені Схемами, Проміжними синтезами та Прикладами. Однак нижченаведений опис не призначений для обмеження цього винаходу жодним чином. Наприклад, конкретні стадії кожного з описаних способів можуть комбінуватися в різних способах або поєднуватися зі стадіями з різних схем для одержання й інших сполук Формули (І). Замісники, якщо не зазначено інше, відповідають наведеним вище визначенням. Реагенти та вихідні матеріали наявні на ринку. Інші необхідні реагенти та вихідні матеріали можуть бути виготовлені способами, вибраними з-поміж стандартних методів хімії органічних та гетероциклічних сполук, способів, аналогічних способам синтезу сполук, які мають аналогічну структуру, та методик, описаних нижче у Прикладах, в тому числі будь-яких нових способів. 8 UA 98777 C2 3 5 10 15 20 25 30 35 40 3 Схема І ілюструє способи виготовлення сполук R -CH2-X або R -CH2-OMs, призначених для застосування в подальших реакціях алкілування тетрагідроциклопента[b]індолів. Згідно зі Схемою І, Стадія А, спирт формули (2) одержують шляхом відновлення складного ефіру формули (1). Складний ефір одержують, якщо необхідно, з карбонової кислоти за допомогою хлорангідриду кислоти, застосовуючи способи, добре відомі в галузі, наприклад, за допомогою оксалілхлориду. Численні способи відновлення складних ефірів карбонових кислот до спиртів добре відомі пересічним фахівцям у галузі та можуть бути знайдені в публікації Л арок (R.C. Larock) у "Comprehensive Organic Transformations", VCH Publishers, 1989, cтор. 549551. Способом, якому віддається перевага, є відновлення боргідридом літію в апротонному розчиннику, наприклад, у тетрагідрофурані, при температурі у діапазоні від кімнатної температури до температури кипіння протягом приблизно 1-48 год. Згідно зі Схемою І, Стадія В, спирт формули (2) перетворюють у складний ефір метансульфонової кислоти формули (3). Спирт поєднують з органічною основою, наприклад, триетиламіном або діізопропілетиламіном, та обробляють метансульфонілхлоридом в інертному розчиннику, наприклад, дихлорметані. Реакційну суміш витримують при температурі у діапазоні від 0 °C до кімнатної температури протягом періоду часу від 15 хв. до 4 год. Одержаний продукт виділяють із застосуванням способів екстрагування, відомих пересічному фахівцю в галузі. 3 Згідно зі Схемою І, Стадія С, сполуку формули (4), де R - гетероарил, галогенують, одержуючи алкілгалогенід формули (S). Сполуку формули (4) обробляють у присутності ініціатора, який утворює вільні радикали, наприклад, бензоїлпероксиду або 1,1'-азобісізобутиронітрилу або 1,1'-азобіс-циклогексанкарбонітрилу, у тетрахлорметані або етилацетаті N-хлорсукцинімідом або N-бромсукцинімідом з опроміненням або без опромінення ультрафіолетовим світлом. За варіантом, якому віддається перевага, обробляють 1,1'-азобісциклогексанкарбонітрилом або 1,1'-азобіс-ізобутиронітрилом та N-бромсукцинімідом при температурі у діапазоні від приблизно кімнатної температури до температури кипіння тетрахлорметану, протягом приблизно 4-48 год. Продукт може бути очищений із застосуванням звичайних способів, наприклад, відфільтровуванням нерозчинних компонентів з подальшим хроматографуванням на силікагелі. За альтернативним способом за Схемою І, Стадія С, гетероарилметил формули (4) можна хлорувати, одержуючи алкілхлорид, де X - СІ, застосовуючи трихлорізоціанурову кислоту. Реакцію виконують в інертному розчиннику, наприклад, хлороформі, при кипінні зі зворотним холодильником протягом 4-72 год. Одержаний продукт виділяють фільтруванням через шар діоксиду кремнію, з подальшим хроматографуванням. Згідно зі Схемою І, Стадія D, формілпіридин формули (6) перетворюють у дифторметилпіридин формули (7), застосовуючи трифторид біс-(2-метоксіетил)аміносірки. Реакцію виконують в інертному розчиннику, наприклад, дихлорметані, протягом 4-24 год., після чого гасять у насиченому розчині NaHCO3. Потім продукт виділяють звичайними способами екстрагування. 9 UA 98777 C2 Згідно зі Схемою І, Стадія Е, дифторметилпіридин формули (7) перетворюють у алкілбромід формули (S) (X - Br), як показано вище на Схемі І, Стадія С. 5 10 15 20 25 30 35 40 Згідно зі Схемою II, Стадія А, циклопентенон (S) вводять в реакцію приєднання Міхаеля з фталімідом, одержуючи (±)-2-(3-оксоциклопентил)ізоіндол-1,3-діон (9). Реакцію виконують у суміші метанолу та 2-н. розчину Na2CO3 у об'ємному співвідношенні 10:1, за варіантом, якому віддається перевага, при температурі навколишнього середовища, застосовуючи умови реакції, аналогічні описаним Новіцкі та ін. (О. Nowitzki, et. al.) у Tetrahedron 1996, 52, 11799-11810. Продукт виділяють шляхом додання води та одержують сполуку (9) у вигляді білої твердої речовини. Згідно зі Схемою II, Стадія В, (±)-2-(3-оксоциклопентил)ізоіндол-1,3-діон (9) вводять в реакцію із фенілгідразином формули (10) у типовому синтезі індолу за Фішером (Fischer), одержуючи тетрагідроциклопента[b]індол формули (11). Для фахівця у галузі зрозуміло, що можливі різноманітні кислотні умови для здійснення синтезу індолу за Фішером, в тому числі застосування як протонних кислот, так і кислот Льюїса. Перевага віддається застосуванню суміші льодяної оцтової кислоти та 4-н. розчину НСl у діоксані при температурі від 50 °C до температури кипіння розчинника, протягом від приблизно 4 год. до 24 год. Одержаний продукт виділяють шляхом додання води з подальшим фільтруванням утвореної твердої речовини. Цю речовину обробляють ультразвуком у метанолі, і одержують матеріал достатнього ступеня чистоти. За альтернативним способом реакцію виконують із застосуванням кислоти Льюїса, наприклад, хлориду цинку, у кількості від приблизно 2 екв. до 4 екв. До інших умов виконання Стадії В належить застосування етанолу при температурі кипіння протягом від приблизно 4 год. до 24 год. Виділяють одержаний продукт, який може бути очищений фільтруванням реакційної суміші з подальшим хроматографуванням фільтрату на силікагелі. Згідно зі Схемою II, Стадія С, фталімідну групу сполуки формули (11) розщеплюють дією гідразину або гідразин-гідрату, одержуючи амінотетрагідроциклопента[b]індол формули (12), в умовах, описаних у Аладжарен та ін. (М. Alajarin, et al., Eur. J. Org. Chem. 2002, 4222-4227). Перевага віддається застосуванню суміші тетрагідрофуран/етанол в об'ємному співвідношенні приблизно 5,5/1 при температурі від 0 °C до 50 °C, за варіантом, якому віддається перевага, при температурі, близькій до кімнатної, протягом 4-72 год. Одержаний фталогідразид видаляють фільтруванням, та продукт виділяють шляхом концентрування фільтрату; він може бути очищений хроматографуванням із застосуванням відомих у галузі способів. Згідно зі Схемою II, Стадія D, амін формули (12) ацилюють відповідним хлорангідридом кислоти, хлорформіатом, діалкілкарбонатом або карбамоїлхлоридом, одержуючи амід, 2 2a карбамат або сечовину формули (13), де R - C(O)R , застосовуючи умови, добре відомі фахівцям у галузі. Амін поєднують з надлишком основного органічного аміну, наприклад, триетиламіну або діізопропілетиламіну, в інертному розчиннику, наприклад, тетрагідрофурані, дихлоретані або дихлорметані, N-метилпіролідоні або Ν,Ν-диметилформаміді, або у їх суміші. Перевага віддається застосуванню діізопропілетиламіну в дихлорметані у присутності, наприклад, ізопропілхлороформіату при температурі від 0 °C до 40 °C протягом 1-72 год. Одержаний продукт виділяють шляхом додання води та діетилового ефіру з подальшим перемішуванням та відділенням твердої речовини. Якщо продукт має достатню розчинність у 10 UA 98777 C2 5 10 15 20 25 30 35 відповідному органічному розчиннику, його можна виділити із застосуванням способів екстрагування, після чого суспендувати у відповідному органічному розчиннику, наприклад, у гептані, та відділити фільтруванням. Для фахівця у галузі зрозуміло, що аміни, наприклад, аміни формули (12), часто більш доцільно зберігати та обробляти у формі проміжних сполук формули (13), де аміногрупа 2a відповідно захищена, наприклад, трет-бутоксикарбонільною групою (ВОС), де R - О-третбутил, або у формі солей з кислотами. Групу ВОС потім видаляють, і амін ацилюють для одержання бажаного аміду або карбамату сполук за цим винаходом. Згідно зі Схемою II, Стадія Е, тетрагідроциклопента[b] індол формули (13) алкілують 3 3 сполукою R CH2X, де X - СІ або Br, або R CH2OSO2Me (дивись Схему І), одержуючи тетрагідроциклопента[b]індол формули (14). Перевага віддається застосуванню CS2CO3, в інертному розчиннику, наприклад, DMF, DMSO або N-метилпіролідиноні, при температурі від 20 °C до 100 °C, але за варіантом, якому віддається перевага, при 45-60 °C, протягом 2-24 год. Одержаний продукт виділяють із застосуванням способів екстрагування, відомих у галузі, та очищають хроматографуванням на силікагелі. За альтернативним варіантом алкілування можна здійснити із застосуванням сильної основи, наприклад, гідриду натрію, гідриду калію, біс(триметилсиліл)аміду калію або біс(триметилсиліл)аміду натрію, в інертному розчиннику, наприклад, диметилформаміді, TV-метилпіролідоні або тетрагідрофурані. Перевага віддається застосуванню гідриду натрію у диметилформаміді при температурі від 0 °C до 80 °C протягом 448 год. Алкілований продукт формули (14) виділяють способами екстракції та хроматографії, відомими фахівцям у галузі. За Схемою III, Стадія А, тетрагідроциклопента[b]індол формули (15) або формули (17) 3 3 алкілують сполукою R CH2X, де X - СІ, Br, або R CH2OSO2Me, як описано для Схеми II, Стадія Е, одержуючи тетрагідроциклопентан-індол формули (16) або формули (18). За Схемою III, Стадія В, фталімідну групу сполуки формули (16) розщеплюють гідразингідратом або гідразином, одержуючи амінотетрагідроциклопента[b]індол формули (19), як описано для Схеми II, Стадія С. За альтернативним варіантом (Схема III, Стадія С) амінотетрагідроциклопента[b]індол формули (19) можна одержати шляхом відщеплення захисної трет-бутоксикарбонільної групи (ВОС) від захищеного аміну формули (18). Загальноприйняті умови відщеплення групи ВОС добре відомі фахівцям у галузі та можуть бути знайдені в публікації Грін та Вутс (T.W. Green, P.G.M. Wuts) у "Protective Groups in Organic Synthesis", John Wiley & Sons, Inc., 1991, 328-330. Перевага віддається застосуванню 4М розчину хлороводню в діоксані при температурі від приблизно 0 °C до 50 °C протягом від приблизно 10 хв до 24 год. За Схемою III, Стадія D, амін формули (19) перетворюють у сульфамід або сульфонамід формули (20) шляхом проведення реакції з відповідним сульфамоїлхлоридом або сульфонілхлоридом у відповідному розчиннику, наприклад, хлороформі або дихлорметані при 50-60 °C із застосуванням основи, наприклад, триетиламіну, основи Гуніга (Hunig) або 1,4 11 UA 98777 C2 5 10 15 20 25 30 35 40 діазабіцикло[2,2,2]-октану (DABCO). Перевага віддається застосуванню хлороформу з використанням DABCO як основи. За альтернативним варіантом, сполуку (14) можна одержати, як показано на Схемі III, Стадія Е, шляхом проведення реакції відповідного хлорангідриду, хлорформіату або карбамоїлхлориду з аміном формули (19), загалом як описано для Схеми II, Стадія D. За Схемою IV, Стадія А, тетрагідроциклопента[b]індол формули (21) алкілують, як описано для Схеми II, Стадія Е, одержуючи заміщений тетрагідроциклопента[b]індол формули (22). За Схемою IV, Стадія В, нітрил формули (21) або (22) відновлюють до альдегіду формули (23) або (24). Нітрил обробляють алюмінієво-нікелевим каталізатором у суміші розчинників води та мурашиної кислоти у співвідношенні від 1/10 до 1/2. Застосовувана мурашина кислота може мати концентрацію 98 %, 96 % або 88 %. Реакцію виконують при температурі від кімнатної до температури кипіння розчинника протягом від приблизно 2 год. до 48 год. Одержаний продукт виділяють шляхом додання протонного розчинника, наприклад, метанолу, з подальшим фільтруванням та концентруванням фільтрату. Залишок додатково очищають звичайними способами екстрагування, наприклад, розчином бікарбонату натрію та етилацетатом, одержуючи альдегід, або обробленням ультразвуком у присутності етанолу та використовують без подальшого очищення. 2 За альтернативним варіантом (Схема IV, Стадія В), якщо R - трет-бутоксикарбоніл (ВОС), то нітрил формули (21) або формули (22) відновлюють у некислотних умовах, наприклад, металогідридним відновлювачем, наприклад, діізобутилалюміній-гідридом. Реакцію виконують в інертному розчиннику, наприклад, дихлорметані, шляхом додавання діізобутилалюміній-гідриду, потім етилацетату та перемішування протягом періоду часу від 30 хв. до 2 год. при кімнатній температурі. Реакційну суміш перемішують з 20 % водним розчином тартрату натрію протягом 1 год., після чого виділяють способами екстракції. За Схемою IV, Стадія D, альдегід формули (23) або формули (25) перетворюють у метоксим відповідно формули (25) або формули (26). Альдегід обробляють гідрохлоридом метоксиаміну в етанолі або метанолі при 0-100 °C протягом від приблизно 2 год. до 24 год., за варіантом, якому віддається перевага, при кімнатній температурі протягом 1 год., у присутності основи, наприклад, карбонату калію, карбонату натрію або гідроксиду натрію. Одержаний продукт виділяють концентруванням та розтиранням продукту з водою. За альтернативним варіантом реакційну суміш розводять етилацетатом, і продукт виділяють, застосовуючи екстракційні способи; потім його можна очистити із застосуванням звичайних способів, наприклад, хроматографії. За Схемою IV, Стадія Е, метоксим тетрагідроциклопентан-індолу формули (25) алкілують, одержуючи N-заміщений метоксим тетрагідроциклопентан-індолу формули (26), як описано для Схеми II, Стадія Е. Визначення біологічної активності У значенні, вживаному у цьому описі, "Κd" означає рівноважну константу дисоціації для комплексу ліганд-рецептор; "Ki" означає рівноважну константу дисоціації для комплексу лікарський засіб-рецептор та вказує концентрацію лікарського засобу, яка відповідає зв'язуванню з половиною паратопів зв'язування у стані рівноваги; "ІС50" означає концентрацію засобу, яка викликає 50 % максимальної інгібувальної реакції, можливої для цього засобу, або, 12 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 60 за альтернативним варіантом, концентрацію засобу, яка викликає 50 % заміщення ліганду, який зв'язується з рецептором; "ЕС50" означає концентрацію засобу, яка викликає 50 % максимальної реакції, можливої для цього засобу; та "ED50" означає дозу введеного в організм лікувального засобу, яка викликає 50 % максимальної реакції для цього засобу. Випробування зв'язування ядерних рецепторів стероїдних гормонів Для випробувань конкурентного зв'язування рецептор-ліганд із метою визначення Kі застосовують лізати клітин нирок людського ембріону НЕK293 з надлишковою експресією людських GR (рецепторів глюкокортикоїдів), AR (рецепторів андрогенів), MR (рецепторів мінералокортикоїдів) або PR (рецепторів прогестерону). Коротко, випробування конкурентного зв'язування рецепторів стероїдів виконують у буфері, який містить 20 мМ буферу (рН=7,6), 0,2 мМ EDTA, 75 мМ NaCl, 1,5 мМ MgCl 2, 20 % гліцерину, 20 мМ молібдату натрію, 0,2 мМ DTT (дитіотреїтол), 20 мкг/мл апротиніну та 20 мкг/мл лейпептину. У типових випадках випробування зв'язування рецепторів стероїдів включають 3 застосування радіомічених лігандів, наприклад, 0,3 нМ [ Н]-дексаметазону для зв'язування GR, 3 3 0,36 нМ [ Н]-метилтриєнолону для зв'язування AR, 0,25 нМ [ Н]-альдостерону для зв'язування 3 MR та 0,29 нМ [ Н]-метилтриєнолону для зв'язування PR, та або 20 мкг лізату 293-GR, 22 мкг лізату 293-AR, 20 мкг лізату 293-MR або 40 мкг лізату 293-PR на лунку. Як правило, випробування виконують із застосуванням 96-лункового планшета. Конкурентні досліджувані сполуки додають у різних концентраціях у діапазоні від приблизно 0,01 нМ до 10 мкМ. Неспецифічне зв'язування визначають у присутності 500 нМ дексаметазону у випадку зв'язування GR, 500 нМ альдостерону у випадку зв'язування MR або 500 нМ метилтриєнолону у випадку зв'язування AR та PR. Реакційні суміші для випробування зв'язування (140 мкл) інкубують протягом ночі при 4 °C, потім додають до кожної реакційної суміші 70 мкл охолодженого вугільно-декстранового буферу (який містить 0,75 г активного вугілля та 0,25 г декстрану на 50 мл випробувального буферу). Планшети струшують протягом 8 хв. на орбітальному струшувачі при 4 °C. Потім планшети центрифугують при 3000 об/хв. при 4 °C протягом 10 хв. Аліквотні кількості 120 мкл реакційних сумішей для випробування зв'язування потім переносять в інший 96-лунковий планшет, та додають у кожну лунку 175 мкл сцинтиляційної рідини Wallac Optiphase Hisafe 3™. Планшети герметизують та інтенсивно струшують на орбітальному струшувачі. Після інкубування протягом 2 год. планшети сканують із застосуванням лічильника Wallac Microbeta. Одержані дані використовують для обчислення ІС50 та процентної частки інгібування у 3 3 концентрації 10 мкМ. Значення Kd для [ Н]-дексаметазону у випадку зв'язування GR, [ Н]3 метилтриєнолону у випадку зв'язування AR, [ Н]-альдостерону у випадку зв'язування MR або 3 [ Н]-метилтриєнолону у випадку зв'язування PR визначають за показником зв'язування при насиченні. Значення ІС50 для сполук перетворюють у значення Кі, застосовуючи рівняння Ченга-Прусоффа (Cheng-Prusoff). При випробуванні за методикою, яка в основному відповідає описаній вище, взяті за приклади сполуки за цим винаходом виявляють при звязуванні AR K i≤500 нМ. За варіантом, якому віддається перевага, сполуки за цим винаходом виявляють при звязуванні AR K i≤100 нМ та за варіантом, якому віддається більша перевага, ≤50 нМ. Крім того, взяті за приклади сполуки за цим винаходом більш селективно зв'язуються (виявляють менші значення Ki) з AR у порівнянні з людським MR, людським GR та людським PR. Для демонстрування здатності сполук за цим винаходом до модулювання активності рецепторів стероїдних гормонів (тобто здатності діяти як агоністи, часткові агоністи, часткові антагоністи або антагоністи), виконують біологічні випробування, які виявляють функціональну модуляцію експресії генів-мішеней у клітинах, тимчасово трансфікованих протеїном ядерного рецептора та конструктом елемента реакції на гормон із геном-репортером. Розчинники, реагенти та ліганди, які застосовуються при функціональних випробуваннях, легко доступні з комерційних джерел або можуть бути виготовлені фахівцем у галузі. Функціональне випробування модулювання ядерних рецепторів стероїдних гормонів Клітини нирок людського ембріону НЕK293 трансфікують плазмідами рецепторів стероїдних гормонів та генів-репортерів, застосовуючи трансфекційний реагент Fugene™ (Roche Diagnostics). Коротко, плазміду репортера, яка містить дві копії пробазину ARE (андрогенчутливий елемент 5'GGTTCTTGGAGTACT3' (послідовність SEQ ID NO:1)) та промотор ТK (тимідін-кінази) вище у послідовності від кДНK репортера люциферази, трансфікують у клітини НЕK293 з плазмідою, яка конститутивно експресує людський рецептор андрогену (AR), застосовуючи вірусний промотор CMV (цитомегаловірусу). Плазміду репортера, яка містить дві копії (глюкокортикоїд-чутливий елемент 5'TGTACAGGATGTTCT'3 (послідовність SEQ ID NO:2)) та промотор ТK вище у послідовності від кДНK репортера люциферази, трансфікують із 13 UA 98777 C2 5 10 15 20 25 30 35 40 45 50 55 60 плазмідою, яка конститутивно експресує або людський рецептор глюкокортикоїду (GR), людський рецептор мінералокортикоїду (MR) або людський рецептор прогестерону (PR), 2 застосовуючи вірусний промотор CMV. Клітини трансфікують у склянках Т150 см у середовищі DMEM, яке містить 5 % сироватки плоду корови (FBS), очищеної активним вугіллям. Після інкубування протягом ночі трансфіковані клітини обробляють трипсином, висівають у 96-лункові планшети у середовищі DMEM, яке містить 5 % очищеної активним вугіллям FBS, інкубують протягом 4 год., після чого піддають дії різних концентрацій випробовуваної сполуки в діапазоні від приблизно 0,01 нМ до 10 мкМ. При випробуванні в режимі антагонізму до середовища додають низькі концентрації агоністів кожного відповідного рецептора (0,25 нМ дексаметазону для GR, 0,3 нМ метилтриєнолону для AR, 0,05 нМ промегестону для PR та 0,05 нМ альдостерону для MR). Після 24 год. інкубування з випробовуваними сполуками, клітини піддають лізису, і визначають активність люциферази із застосуванням звичайних способів. Для визначення ЕС50 одержані дані апроксимують за чотирипараметровою логістичною кривою. Відносну ефективність (для сполук із максимальною реакцією при насиченні) або відносну максимальну стимуляцію (для сполук із максимальною реакцією, яка не досягає насичення) визначають відносно максимальної стимуляції, досягнутої при застосуванні вказаних нижче еталонних агоністів: 100 нМ метилтриєнолону для проби з AR, 30 нМ промегестону для проби з PR, 30 нМ альдостерону для проби з MR та 100 нМ дексаметазону для проби з GR. Значення ІС50 можна визначити аналогічним чином, застосовуючи результати випробувань в режимі антагонізму. В режимі антагонізму показники інгібування визначають шляхом зіставлення активності випробовуваної сполуки у присутності низької концентрації агоніста (0,25 нМ дексаметазону для GR, 0,3 нМ метилтриєнолону для AR, 0,05 нМ промегестону для PR та 0,05 нМ альдостерону для MR) з реакцією, спричиненою такою самою низькою концентрацією агоніста у відсутності випробовуваної сполуки. Випробування із застосуванням репортера AR/ARE та клітин С2С12 Для індикації активності агоністів у м'язовій тканині виконують випробування із застосуванням репортера AR/ARE та клітин С2С12. Коротко, клітини міобласту С2С12 мишей котрансфікують, застосовуючи реагент Fugene™. Плазміду репостера, яка містить GRE/ARE (глюкокортикоід-чутливий елемент/андроген-чутливий елемент 5'TGTACAGGATGTTCT'3 (послідовність SEQ ID NO:3) та промотор ТK вище у послідовності від кДНK репортера люциферази, трансфікують із плазмідою, яка конститутивно експресує людський рецептор андрогену (AR), застосовуючи вірусний промотор CMV. Клітини трансфікують у склянках Т150 2 см у середовищі DMEM, яке містить 4 % або 10 % сироватки плоду корови (FBS). Після інкубування протягом 5 год. трансфіковані клітини обробляють трипсином, висівають у 96лункові планшети у середовищі DMEM, яке містить 10 % очищеної активним вугіллям FBS, інкубують протягом 2 год., після чого піддають дії різних концентрацій випробовуваної сполуки в діапазоні від приблизно 0,01 нМ до 10 мкМ. Після 48 год. інкубування з випробовуваними сполуками, клітини піддають лізису, і визначають активність люциферази із застосуванням звичайних способів. Для визначення ЕС50 одержані дані апроксимують за чотирипараметровою логістичною кривою. Відносну ефективність у відсотках визначають відносно максимальної стимуляції, досягнутої при застосуванні 10 нМ метилтриєнолону. Пересічний фахівець у галузі може без утруднень розробити методики функціональних випробувань модулювання ядерних рецепторів стероїдних гормонів, аналогічні описаним вище. При випробуванні за методикою, яка в основному відповідає описаній вище, взяті за приклади сполуки за цим винаходом демонструють ЕС50≤1000 нМ у пробі з репортером AR/ARE C2C12. За варіантом, якому віддається перевага, сполуки за цим винаходом демонструють ЕС50≤100 нМ у пробі з репортером AR/ARE C2C12, та за варіантом, якому віддається більша перевага, ≤50 нМ. Модель ефективності та селективності in vivo Самців пацюків лінії (вік 12 тижнів) каструють (шляхом гонадектомії або за схемою "GDX") згідно з затвердженими методиками (Charles River Labs) та залишають для відновлення на 8 тижнів. Готують також пацюків із симульованою операцією відповідного віку (тварини із симульованою операцією є тварини, яких піддано тим самим хірургічним процедурам, що й при кастрації, але без видалення яєчок). Тварин тримають у приміщенні з регульованою температурою (24 °C) із чергуванням 12-годинних періодів освітлення та темряви (темрява з 10.00 до 22.00) при вільному доступі до води та корму. З метою демонстрування ефективності in vivo, сполуки за цим винаходом вводять кастрованим пацюкам у віці 20 тижнів (маса тіла приблизно 400-450 г) щоденно шляхом згодовування або підшкірного впорскування. Перед визначенням схеми дослідження тварин розподіляють по групам за випадковою схемою з урахуванням маси тіла, так щоб вихідні 14 UA 98777 C2 5 10 15 20 25 30 35 значення маси тіла у всіх дослідних групах відрізнялися максимум на 5 %. Випробовувані сполуки вводять тваринам у звичайних носіях. Наприклад, для перорального введення можна застосовувати 1 % натрієвої карбоксиметилцелюлози (CMC) + 0,25 % Tween 80 у стерильній Н2О, а для підшкірних ін'єкцій 6 % етилового спирту (EtOH) + 94 % циклодекстрану (CDX). Пацюків із симульованою операцією, які одержують тільки носій, використовують як позитивний контроль, а кастрованих пацюків, які одержують тільки носій, - як негативний контроль. Піддослідним тваринам вводять на протязі двотижневого періоду перорально або підшкірно дози, наприклад, 0,3 мг/кг/доба, 1 мг/кг/доба, 3 мг/кг/доба, 10 мг/кг/доба або 30 мг/кг/доба сполук за цим винаходом. Після двотижневого оброблення визначають як показник активності масу м'язу Levator Ani (LA) тварин піддослідних груп у вологому стані, та порівнюють це значення з масою того самого м'язу Levator Ani у вологому стані для кастрованих тварин контрольної групи, які одержували тільки носій. Значення маси м'яза у вологому стані, одержані для піддослідної групи та для групи, яка одержувала тільки носій, нормалізують відносно загальної маси тіла. Аналогічним чином порівнюють масу сім'яного пухирця (SV) у вологому стані для тварин піддослідної групи та кастрованої групи, яка одержувала тільки носій, як показник тканиноселективної активності. В цьому разі значення маси пухирців у вологому стані, одержані для піддослідної групи та для групи, яка одержувала тільки носій, також нормалізують відносно загальної маси тіла. Окрім визначення маси м'яза Levator Ani у вологому стані, після аутопсії виділяють ліві великі гомілкові кістки пацюків, і після зняття епіфізів ретельно видаляють м'які тканини, які оточують кістку. Ці проби потім вміщують у розчин, який містить 0,2 % колагенази у буфері Tris (pH 7,5). Одержану ферментну витяжку із зовнішнього надкісничного шару одразу ж піддають випробуванню для визначення активності лужної фосфатази, яка є показником анаболічної активності стосовно до остеобласту та кістки. Коротко, для цієї мети 30 мкл проби вміщують у лунки планшета, які містять 200 мкл буферного субстрату n-нітрофенілфосфату (PNPP) (Pierce, каталожний №37621). Для побудови стандартної кривої застосовують очищену лужну фосфатазу (Sigma, каталожний №Р4252), і вимірюють поглинання проб на довжині хвилі 405 нм (Abs405) Для визначення активності надкісничної лужної фосфатази (PALP). Результати, одержані для піддослідної групи та для групи, яка одержувала носій, можна нормалізувати відносно загальної маси тіла. Відносну ефективність у відсотках (% Eff.) можна визначати, як вказано нижче: % Eff. = ((Волога маса LA або SV, або активність PALP у тварини піддослідної групи / загальна маса тіла тварини піддослідної групи) / (Волога маса LA або SV або активність PALP у контрольної тварини / загальна маса тіла контрольної тварини)) × 100. При випробуванні за методикою, яка в основному відповідає описаній вище, сполука за Прикладом 74 виявила такі показники активності у вищезгаданій моделі ефективності та селективності для пацюків: Маса LA: Доза (мг/кг/доба) % ефективності Шлях введення відносно контролю (GDX) (ANOVA, р98 % (Ізомер 1, Chiralpak AD, EtOH/0,2 % диметилетиламін). Проміжний синтез 42 (±)-2-(1,3-діоксо-1,3-дигідроізоіндол-2-іл)-4-(6-фторпіридин-2-ілметил)-1,2,3,4тетрагідроциклопента[b]індол-7-карбонітрил Розчиняють (±)-2-(1,3-діоксо-1)3-дигідроізоіндол-2-іл)-1,2,3,4-тетрагідроциклопента[b]індол7-карбонітрил (6,88 г, 21,0 ммоль) та 2-бромметил-6-фторпіридин (3,99 г, 21,0 ммоль) у DMF (80 мл). Додають карбонат цезію (7,51 г, 23,1 ммоль, 1,10 екв.), та перемішують реакційну суміш при кімнатній температурі у атмосфері азоту протягом 48 год. Розводять реакційну суміш етилацетатом, промивають водою (3×), сушать над безводним сульфатом натрію, фільтрують, та концентрують до одержання напівтвердої речовини (8,10 г). Очищають неочищений продукт на колонці із 120 г силікагелю, елююючи градієнтом від 0 % до 100 % етилацетат/гексан, і одержують 6,7 г жовтувато-коричневої або коричневої твердої речовини. Суспендують продукт у діетиловому ефірі (100 мл) при кімнатній температурі протягом ночі. Відфільтровують одержану тверду речовину, промивають діетиловим ефіром, та сушать у високому вакуумі, одержуючи вказану в заголовку сполуку у вигляді жовто-коричневої твердої речовини (5,70 г, 62 %). LCMS 437,1 (М+1). Проміжний синтез 43 (±)-2-(1,3-діоксо-1,3-дигідроізоіндол-2-іл)-4-піридин-2-ілметил-1,2,3,4тетрагідроциклопента[b]індол-7-карбонітрил Нагрівають суміш 2-(1,3-діоксо-1,3-дигідроізоіндол-2-іл)-1,2,3,4тетрагідроциклопента[b]індол-7-карбонітрилу (5 г, 15,3 ммоль) у DMF (25 мл) до 40 °C. Додають карбонат цезію (10,4 г, 32,4 ммоль) та гідробромід 2-бромметилпіридину (4,05 г, 16 ммоль). Перемішують суміш при 40 °C протягом 24 год. Виливають суміш у воду (250 мл), та перемішують протягом 1 год. Відфільтровують одержані тверді речовини, та сушать зібраний матеріал у вакуумі. Додають цю тверду речовину до етанолу (25 мл), та кип'ятять зі зворотним холодильником протягом 30 хв. Охолоджують суміш до 22° С та фільтрують. Сушать цю тверду речовину у вакуумі до незмінної маси, одержуючи 4,8 г (75 %) вказаної в заголовку сполуки. MS (m/z): 419 (M+1). Проміжний синтез 44 (±)-2-аміно-4-(6-фторпіридин-2-ілметил)-1,2,3,4-тетрагідроциклопента[b]індол-7-карбонітрил 28
ДивитисяДодаткова інформація
Назва патенту англійськоюTetrahydrocyclopenta[b]indole compounds as androgen receptor modulators
Автори англійськоюGavardinas, Konstantinos, Green, Jonathan, Edward, Jadhav, Prabhakar, Kondaji, Matthews, Donald, Paul
Назва патенту російськоюТетрагидроциклопента[b]индолы как модуляторы андрогенных рецепторов
Автори російськоюГавардинас Константинос, Грин Джонатан Эдвард, Джадхав Прабхакар Кондаи, Маттьюз Доналд Пол
МПК / Мітки
МПК: A61P 9/04, A61P 9/10, A61P 19/02, A61P 11/00, C07D 209/58, A61K 31/404
Мітки: модулятори, рецепторів, андрогенових, тетрагідроциклопента[b]індоли
Код посилання
<a href="https://ua.patents.su/49-98777-tetragidrociklopentabindoli-yak-modulyatori-androgenovikh-receptoriv.html" target="_blank" rel="follow" title="База патентів України">Тетрагідроциклопента[b]індоли як модулятори андрогенових рецепторів</a>
Попередній патент: Спосіб доставки лікарського препарату для посилення синтезу білка в кістках
Наступний патент: Місцевий склад для попередження ампутації інфікованих кінцівок та спосіб його отримання, місцевий ранозагоювальний склад та його спосіб отримання і застосування
Випадковий патент: Спосіб діагностики розвитку остеопорозу