Застосування 4-заміщених 3-карбоксихінолінів як інгібіторів протеїнкінази ск2
Номер патенту: 68984
Опубліковано: 16.08.2004
Автори: Сапелкін Владислав Миколайович, Лукашов Сергій Степанович, Дубініна Галина Григорівна, Голуб Андрій Григорович, Ярмолюк Сергій Миколайович, Бджола Володимир Григорович, Яковенко Олександр Ярославович
Формула / Реферат
Застосування 4-заміщених 3-карбоксихінолінів як інгібіторів протеїнкінази СК2.
Текст
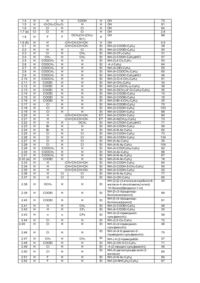
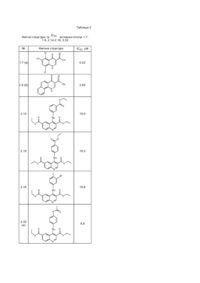
Пропонований винахід стосується винайдення нового класу інгібіторів протеінкінази СК2-4-заміщених 3карбоксихінолінів. Протеїнкіназа СК2 (казеїн кіназа II) є убіквітальною багатосубстратною кіназою, що задіяна в багатьох сигнальних шляха х клітинного росту та проліферації. Інгібуючий вплив кінази на певні клітинні механізми контролю апоптозу, підвищена активність цієї кінази у швидко проліферуючих тканинах та в багатьох пухлинах дозволяє розглядати СК2 як суттєвий фактор процесів пухлиноутворення. СК2 розглядається як перспективна мішень для створення протиракових ліків, а інгібітори СК2 кінази можуть використовува тися у терапії раку [1, 2, 3]. Останнє десятиріччя велика кількість робіт присвячена пошуку противірусних препаратів проти людського цитомегаловірусу (HC MV) та HIV-1. З'ясувалося, що механізм їхньої дії полягає у інгібуванні СК2-кінази, яка опосередковано спричиняє підсилення експресії гену HIV-1 або HCMV на транскрипційному рівні. Таким чином, інгібітори СК2 є інгібіторами транскрипції HIV-1 і можуть бути використані як противірусні препарати [4, 5]. Серед відомих інгібіторів СК2-кінази є поліпептиди [6, 7, 8, 9], флавоноїди, похідні антрахінону, нафталіну, ксантену та флуорену [3], хіназоліну [10], ізохіноліну [11]. Ефективність та специфічність цих інгібіторів, особливо флавоноїдів, є недостатньою для застосування в клінічній фазі досліджень. Отже, пошук високоспецифічних інгібіторів СК2, що пригнічували б активність СК2 у низьких концентраціях є актуальним завданням. Серед похідних хіноліну інгібіторів СК2-кінази раніше знайдено не було. В основу пропонованого винаходу поставлена задача: синтез 4-заміщених 3-карбоксихінолінів, визначення їх інгібіторних властивостей щодо СК2 кінази та селективності по відношенню до інших протеїнкіназ. Поставлена задача вирішується пропонованим винаходом, а саме, застосуванням 4-заміщених 3карбоксихінолінів як інгібіторів протеїнкінази СК2. Суть винаходу пояснюється за допомогою графічних матеріалів: На фіг.1 показано загальну стр уктур у ряду 4-заміщених 3-карбоксихінолінів На фіг.2 показано залежність активності СК2 кінази від концентрації інгібіторів 1.7(в), 1.9(б), 2.32(а) Авторами проведено синтез ряду 4-заміщених 3-карбоксихінолінів та виявлено інгібіторні властивості щодо СК2 кінази. Серед тестованих 62 похідних найвищу активність показали: 4 - (4 - метилкарбоксамідоані ліно) - 3,6 - карбетокси хінолін (а) (ІС50 8,8mМ) ; = 4 - оксо - 3 - карбокси- 1,4 - дигідробензо[h]хінолін (б) (ІС50 2,65mМ) ; = 5,6,8 - трихлоро - 4 - оксо - 14 - дигідро - 3 - карбоксихі , нолін (в) (ІС 50 0,22mМ) = (загальну структуру ряду 4заміщених 3-карбоксихінолінів наведено на фіг.1, хімічні структури сполук а,б,в - в таблиці 2). Матеріали і методи. Контроль за проходженням реакції та чистотою синтезованих сполук здійснювався хроматографічне на пластинах "Silufol UV-254", елюент: хлороформ - метанол (9:1). Структур у одержаних сполук доведено за допомогою ПМР-спектрів. Спектри ПМР записані в ДМСО-Об на приладі "Varian" з робочою частотою 300МГц і внутрішнім стандартом -тетраметилсиланом. Величини хімічних зсувів визначались з точністю до 0.001м. ч. 4-0ксо-1,4-дигідро-3-карбоксихіноліни (1.1-1.9) були синтезовані за методикою [12: Синтези органічних препаратів. Під редакцією Б.А. Казанского. Т.4. -С.240. -М. - "Іноземна література". -1953.], використовуючи при циклізації у якості розчинника діетил(дибутил)фталат замість даутерма. Синтез 4-аніліно-3-карбетоксихінолінів (2.1-2.52). До 10ммоль відповідного 4-хлоро-3-карбетоксихіноліну у 2,5мл ДМФА додають 10,5ммоль аніліну, кип'ятять 5 хвилин, охолоджують, додають 20ммоль триетиламіну, 15мл спірту та нагрівають. До розчину додають воду до початку кристалізації. Осад відфільтровують та висушують. Сполуки 2.9, 2.22 були одержані у вигляді гідрохлоридів за наведеною вище методикою, але без додавання триетиламіну. Виходи продуктів 2.1-2.52: 64-82%. Біологічне тестування. 4-Заміщені 3-карбоксихіноліни були тестовані на інгібування активності СК2 кінази in vitro. Об'єм реакційної суміші був 30мкл. Для буферу використовувалось 20mM Tris-HCI, рН7,5 при 25°С; 50mM KCI; 10mM MgCI. Для кожної реакції брався: 1 мікрограм пептидного субстрату (~ 500mM; EnglandBiolabs) ; 10 одиниць (0.02мкл при концентрації 500000/мл у водному буферному розчині) рекомбінантної людської СК2 кінази (England Biolabs). Реакційна суміш готувалася без додавання АТФ при кімнатній температурі, була поділена на аліквоти по 1,5мл. До реакційної суміші додавали 1-0,5мкл стокового розчину інгібітору у 100% ДМСО з концентрацією 5mM . Кожна реакція повторювалася двічі, одержаний результат не відрізнявся більш, ніж на 10-15%. 32 Розчин АТФ готувався окремо. Для кожної реакції бралося 0 .05mCig - P АТФ . Фінальна концентрація АТФ була 33mМ , загальна концентрація міченої та неміченої АТФ - 40mМ . Реакція починалася після додавання до суміші АТФ. Час реакції - 20 хвилин при Т30°С (у знайдених умовах експотенційна фаза реакції закінчується за 25-30 хвилин). Реакцію зупиняли додаванням 20мкл 5% фосфорної кислоти і переносили продукти реакції на 20мм фільтр із целюлозо-фосфатного паперу (Whatman). Фільтр промивали тричі 0,5% фосфорною кислотою на шейкері в 200мм чашці Петрі при кімнатній температурі і висушували при 36°С. Для детекції мічених продуктів використовали LKB g - лічильник Черенкова. Для позитивного контролю використовували ДМСО без інгібітора у тій же кількості - 1мкл, що і у дослідах з розчином інгібітора в ДМСО. Негативний контроль проводився з використанням відомого інгібітора СК2 кінази - кверцитину, що при концентрації 0,8 - 0,5 mМ інгібував активність СК2 кінази на 70-50%. Контроль над неспецифічною адсорбцією (без додавання ензиму) проводився час від часу і не перевищував 5%. На першому етапі здійснювався прескринінг сполук при концентрації досліджуваної речовини-інгібітора 33mМ . Результати і обговорення. Нами синтезовано та тестовано на інгібування активності СК2 кінази in vitro 62 похідних 4-заміщених 3карбоксихінолінів: 4-гідрокси-3-карбоксихіноліни (4-оксо-1,4-дигідро-3-карбоксихіноліни) (1.1-1.9) та 4-аніліно-3карбетоксихіноліни (2.1-2.52) (фіг.1). Результати прескринінгу, хімічні структури (або назви) замісників R; R1; R2; R3; R4; R5; R6 сполук 1.1-1.9, 2.1-2.52 наведені в Таблиці 1 та на фіг.1. Структур у сполук 1.1-1.9 можна представити двома таутомерними формами, 4-оксо-1,4-дигідро-3-карбоксихінолінова структура є переважною до 4-гідрокси-3-карбоксихінолінової (фіг.1). Дані пре-скринінгу свідчать про те, що сполуки 1.7, 1.9, 2.14-2.16, 2.32 інгібують активність СК2 кінази при концентрації 33mМ більше, ніж на 80%, вони були відібрані для більш детального дослідження при декількох концентраціях. Знайдені для сполук 1.7,1.9, 2.14-2.16, 2.32 величини ICsoTa хімічні структури наведено у Таблиці 2. Найбільш активними інгібіторами виявилися сполуки: 1.7 (ІС50 = 0,22mМ) , 1.9 (ІС50 = 2,65mМ) , 2.32 (ІС50 = 8,8mМ) (фіг.1). З метою дослідження селективності інгібіторів 1.7, 1.9 по відношенню до СК2 кінази було проведено біологічні тести на інгібування інших протеїнкіназ: GSK та CDK5. Встановлено, що для цих кіназ (ІС50 > 10mМ) для обох сполук 1.7, 1.9, тобто ці дані дають можливість говорити про селективну дію сполук 1.7, 1.9 на СК2 кіназу. Для тестованого ряду 62 похідних 4-заміщених 3-карбоксихінолінів можна зробити деякі висновки стосовно залежності інгібіторної активності від структури сполуки. Серед протестованих 52 похідних 4-аніліно-3карбетоксихіноліну (2.1-2.52) чотири сполуки 2.14-2.16, 2.32 виявили значну СК2-інгібіторну активність (ІС50 від 8,8 до18,9mМ) . Спільним фрагментом всіх чотирьох сполук є наявність, крім 3-карбетокси- групи та акцепторних замісників у 4-аніліновому фрагменті, карбетокси- групи в 6 положенні хінолінового циклу. Інші три тестовані сполуки цього ж ряду 2.11-2.13, що мають також 6-карбетокси- групу, теж виявили інгібіторні властивості, але нижчі. Так, сполука 2.11, що має в четвертому положенні /тауоа-толуідин (R6=NН-(4-СН3С6Н4)), при концентрації 33mМ інгібує СК2 кіназу на 66%, сполука 2.12 - на 62%, 2.13 - на 45%. Заміна 6-карбетоксигрупи на 6-карбметокси-групу (сполуки 2.5-2.10, 2.29-2.31) значно знижує інгібіторні властивості. Серед 4-оксо-1,4дигідро-3-карбоксихінолінів (1.1-1.9) знайдено два активних селективних інгібітора 1.7,1.9. Хоча 4-аніліно-3карбетоксихінолінів (2.1-2.52) тестувалося набагато більше, найкращі з них інгібітори 2.14-2.16, 2.32 виявили в декілька разів меншу активність, ніж 4-оксо-1,4-дигідро-3-карбоксихіноліни 1.7, 1.9. Це може свідчити про важливість знаходження в третьому положенні хіноліну саме карбоксильної групи та в четвертому -кето-групи. Так, похідні сполуки 1.9 - 4-оксо-3-карбокси-1,4-дигідробензо[h]хіноліну, в яких в 3 положенні етиловий естер замість карбокси групи, а в четвертому - аніліновий фрагмент, виявляють значно менші інгібіторні властивості (сполуки 2.1, 2.20, 2.33-2.35). Порівнюючи активність ряду 4-оксо-1,4-дигідро-З-карбоксихінолінів, галогенозаміщених по бензольному кільцю хіноліну, можна зробити висновок стосовно критичності атома хлору у 5 положенні хіноліну для виявлення СК2-інгібіторних властивостей. Так, 5,6,8-три хлоро-4-оксо-1,4-дигідро-3карбоксихінолін (1.7) має найвищу серед всіх тестованих сполук активність (ІС50 = 0,22mМ) , 6,8-трихлоро-4-оксо1,4-дигідро-3-карбоксихінолін (1.6), що відрізняється тільки відсутністю атома хлору в 5 положенні, при 33mM інгібує активність СК2 кінази лише на 36%. Низьку активність виявляють сполуки даного ряду з атомом йоду в 6 положенні (сполука 1.1), атомами фтору в 6 і 7 положеннях (сполука 1.8), карбоксильною групою в положеннях 6; 7; 8 (сполуки 1.2-1.4). Отже, знайдено новий клас інгібіторів СК2 кінази - 4-заміщені 3-карбоксихіноліни. Серед тестованих 62 похідних найвищу активність показали: 4-(4-метилкарбоксамідоаніліно)-3,6-карбетоксихінолін (2.32) (ІС50 8. 8mМ) ; 4-оксо-3-карбокси-1,4-дигідробензо[h]хінолін (1.9) (ІС50 = 2.65mМ) ; 5,6,8-трихлоро-4-оксо-1,4= дигідро-3-карбоксихінолін (1.7) (ІС50 = 0,22mМ) , що може бути використано для подальшої оптимізації активних структур і використанні їх для терапії раку та противірусних захворюваннь. Таблиця 1 Результати пре-скринінгу сполук 1.1-1.9, 2.1-2.52 (концентрація потенційного інгібітора - 33mM ) R1 R6 O R2 5 6 4 R3 O 3 7 2 8 R5 N1 R4 1.1-1.9;2.1-2.52 Замісники № 1.1 1.2 1.3 R1 R2 R3 R4 R5 H Н H J COOH H H H COOH H H H H H H R6 OH OH OH Залишкова активність СК2 кінази, % 85 91 74 1.4 1.5 1.6 1.7 (в) Н H H СІ H H -О-CH2-CH2-ОCl H Cl H COOH H Cl Cl OCH2CH-(СН3)F N(1) -CH=CH-CH=CH-CH=CH-CH=CHH Cl H СН3 H СН3 H H H H H H H H H H H H H H H H H H Н Н Н Н Н Н Н Н Н Н Н Н -СН СН-СН СН= = -СН СН-СН СН= = Н ОСН3 Н Н Н Н Н СІ Н СІ Н СІ Н СІ Н Н Н Н Н Н Н Н -СН СН-СН СН= = -СН СН-СН СН= = -СН СН-СН СН= = Сl Сl Сl Сl 1.8 H F 1.9 (б) 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 2.9 2.10 2.11 2.12 2.13 2.14 2.15 2.16 2.17 2.18 2.19 2.20 2.21 2.22 2.23 2.24 2.25 2.26 2.27 2.28 2.29 2.30 2.31 2.32 (a) 2.33 2.34 2.35 2.36 2.37 H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H Cl СН3 СООСН3 СООСН3 СООСН3 СООСН3 СООСН3 СООСН3 COOEt COOEt COOEt COOEt COOEt COOEt СІ СІ СІ Н Н Н Вr Вr Сl Сl Сl Сl СООСН3 СООСН3 СООСН3 COOEt Н Н Н Н Н 2.38 H 2.39 H H H H H Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et ET ET Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et Et ОСН3 Н Н Et H COOEt Н Н Et 2.40 H COOEt Н Н Et 2.41 2.42 H H Н Н Н Н СH3 CF3 Et Et 2.43 H н н СРз Et 2.44 2.45 H H Сl Сl Н Н Н Н Et Et 2.46 H Сl Н Н Et 2.47 2.48 2.49 H H H СН3 COOEt СІ Н H H СН3 H H Et 2.50 H СІ H H Et Et Et 2.51 2.52 H H F F H H H H Et Et H OH OH OH OH OH 73 81 64 2.6 88 OH NН-(3-СООЕt-С6Н4) NН-(4-СООЕt-С6Н4) NH-(3-CF3-C6H4) NН-(3-СООН-С6Н4)xHCl NН-(3,4-СІ2-С6Н3-4-J-C 6H4) NН-(4-ОЕt-С6Н4) NН-(4-СООСН3-С6Н4) NН-(3-СООН-С6Н4)xHCI NН-(3-Сl-4-СН3-С6Н3) NН-(4-СН3-С6Н4) NН-(3,4-(ОСН2-)2-С6Н3) NН-(4-ОСН2-(4'-Сl-С6Н4)-С6Н4) NH-(3-COOEt-C 6H4) NH-(3-COOEt-C 6H4) NН-(3-Вr-4-СН3-С6Н3) NH-(4-COOEt-C 6H4) NН-(3-СООН-С6Н4) NH-(4-COOH-C 6H4) NН-(4-СООН-С6Н4) NН-(4-N(СН3)2-С6Н4) NН-(3-СООН-С6Н4)хНСІ NН-(4-СООН-С6Н4) NН-(4-N-Ас-С6Н4) NН-(3-СООН-С6Н4) NН-(4-СООН-С6Н4) NН-(4-Ас-С6Н4) NН-(4-N-Ас-С6Н4) NН-(4-СООС6Нц-С 6Н4) NН-(4-Ас-С6Н4) NН-(4-N-Ас-С6Н4) NH-(4-N-Ac-C 6H4) NН-(3-СООН-С6Н4) NН-(3-СООН-5-СН3-С6Н4) NН-(4-СООН-С6Н4) NH-(4-N-Ac-C 6H4) NH-(3-OH-C 6H4) NН-{2-[2-(3-етилокси-карбоніл-6метокси-4-хіноліламіно)-етил]1H-бензо[d]імідазол-1-іл} NН-[3-(3-піридилкарбонілокси)пропіл]NН-[3-(4-піридилкарботлокси)пропіл]NH-(3-COOEt-C 6H4) NH-(4-COOEt-C 6H4) NН-(4-(2-піримідинілсульфамоїл)) NН-(2,5-Сl2-С6Н3) NН-(4-(2-піримідинілсульфамоїл)) NН-(4-(4,6-диметил-2піримідиніл-сульфамоїл)) NН-(-4-(2-піримідинілNН-(2-ОН-5-СІ-С6Н4-4-(2-піридил-сульфамоїл)) NН-(5-діетилсульфа-моїл-2метокси) NН-(4-N-Ас-С6Н4) NН-((4-NНС6Н5)-С6Н4) 4.5 38 50 31 57 50 64 55 65 46 91 34 38 55 15 16 20 70 103 68 80 73 71 56 62 73 134 30 104 82 88 67 16 64 50 52 77 65 44 89 91 46 30 58 72 46 75 57 71 46 60 84 67 Таблиця 2 IC 50, Хімічні структури та активних сполук 1.7, 1.9, 2.14-2.16, 2.32 № IC 50, mM Хімічна структура Cl O O Cl OH 1.7 (в) 0.22 N H Cl O O OH 1.9 (б) 2.65 N H O O 2.14 18.9 O NH O O O N O O 2.15 18.3 O NH O O O N Br 2.16 O NH 16.8 O O O N N O 2.32 (a) 8.8 O NH O O O N R1 R2 5 6 4 R2 5 6 R6 O 4 3 7 R3 R4 1.1-1.9 R1 2 8 R4 N R3 R4 O OH 2 N1 H 8 OH R2 OH 3 7 R3 R1 O O N1 O R5 2.1-2.52 Фіг. 1 Література: 1. Pinna L Protein Kinase CK2 // Int. J. Biochem. Cell. Biol. - 1997. - 29. - P. 551-554. 2. Ravi R., Bedi A. Sensitization of Tumor Cells to Apo2 Ligand/TRAIL-induced Apoptosis by Inhibition of Casein Kinase II // Cancer Res. - 2002. -62.-P. 4180-4185. 3. Sarno S., Мого S., Meggio F., Zagotto G., Dal Ben D., Ghisellini P., Battistuta R., Zanotti G., Pinna L. Toward the rational design of protein kinase casein kinase-2 inhibitors (In Process Citation) // Pharmacol Ther. -2002. - 93(2-3). - P. 159. 4. Critchfield J. W., Coligan J. E., Folks T. M., Butera S. T. Casein kinase II is a selective target of HIV-1 transcriptional inhibitors // Biochem. - 1997. -94.-P. 6110-6115. 5. De Clercq E. Current lead natural products for the chemotherapy of human immuno-deficiency virus (HIV-1) infection // Med. Res. Rev. - 2000. -20(5). - P. 323-349. 6. Meggio F., Pinna L. A., Marchiori F., Borin G. PolyglutamyI peptides: a new class of inhibitors oftype-2 casein kinases // FEBS Lett. - 1983. - 162(2). -P. 235-238. 7. Szyszka R., Grankowski N., Felczak K., Shugar D. Halogenated benzimidazoles and benzotriazoles as selective inhibitors of protein kinases CK1 and CK2 from Saccharomyces cerevisiae and other sources // Biochim. Biophys. Res. Commun. - 1995. - 208. - P. 418-424. 8. Sarno S., Reddy H., Meggio F., Ruzzene M., Davies S. P., Donella-Deana A., Shugar D., Pinna L. Selectivity of 4,5,6,7-tetrabromobenzotriazole, an ATP site-directed inhibitor of protein kinase CK2 ("casein kinase") // FEBS Lett. 2001. - 496. - P. 44-48. 9. Battistutta R., De Moliner E., Sarno S., Zanotti G., Pinna L. A. Structural features underlying selective inhibition of protein kinase CK2 by ATP-site directed tetrabromobenzotriazole // Protein Sci. - 2001. - 10. - P. 2200-2206. 10. Liu XG., Liang NC. Inhibitory effect and its kinetic analysis of tyrphostin AG1478 on recombinant human protein kinase CK2 holoenzime // Acta Pharmacol Sin. - 2002. - 23(6). - P. 556-561. 11. Chijiwa Т., Hagiwara M., Hidaka H. A newly synthesized selective casein kinase I inhibitor, N-(2-aminoethyl)-5chloroisoquinoline-8-sulfonamide, and affinity purification of casein kinase I from bovine testis // J. Biol. Chem. - 1989. 264(9). - P. 4924-4927. 12. Синтези органічних препаратів, під редакцією Б.А. Казанского, т. 4. - С. 240. - M. - "Іноземна література". 1953.
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of 4-substituted 3-carboxyquinolines as protein kinase ck2 inhibitors
Назва патенту російськоюПрименение 4-замещенных 3-карбоксихинолинов как ингибиторов протеинкиназы ск2
МПК / Мітки
МПК: A61K 31/47, C07D 215/00, A61P 31/12, A61P 35/00
Мітки: 4-заміщених, застосування, інгібіторів, ск2, протеїнкінази, 3-карбоксихінолінів
Код посилання
<a href="https://ua.patents.su/5-68984-zastosuvannya-4-zamishhenikh-3-karboksikhinoliniv-yak-ingibitoriv-protenkinazi-sk2.html" target="_blank" rel="follow" title="База патентів України">Застосування 4-заміщених 3-карбоксихінолінів як інгібіторів протеїнкінази ск2</a>
Попередній патент: Головоутримувач
Наступний патент: Восковий сплав для обробки прищеп і саджанців
Випадковий патент: Спосіб отримання складних ефірів 13,14-дигідро-15-(r)-17-феніл-18,19,20-тринор-pgf2a