Спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4н-тієно[3′,2′:5,6]піримідо[2,1-b][1,3]тіазин-10-ію
Номер патенту: 76401
Опубліковано: 10.01.2013
Автори: Кіш Анетт Оттівна, Сливка Михайло Васильович, Сливка Марина Василівна, Лендєл Василь Георгійович
Формула / Реферат
Спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію, який включає в себе електрофільну гетероциклізацію 1-R-пропенільних тіоетерів тієно[2,3-d]піримідину під дією галогенів, який відрізняється тим, що в якості вихідних тіоетерів використовують заміщені при 3N-атомові Нітрогену піримідинового циклу сполуки (І), які при галогеногетероциклізації (дія ІВr, Вr2 або I2) перетворюються в солі 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію(ІІ):
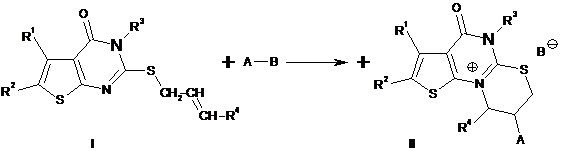
причому
R1, R2 є Alk;
R3, R4 є Аr;
А-В є I-І, Вr-Вr, І-Вr.
Текст
Реферат: Спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію, який включає в себе електрофільну гетероциклізацію 1-R-пропенільних тіоетерів тієно[2,3-d]піримідину під дією галогенів, який 3 відрізняється тим, що як вихідні тіоетерів використовують заміщені при N-атомові Нітрогену піримідинового циклу сполуки (І), які при галогеногетероциклізації (дія ІВr, Вr2 або I2) перетворюються в солі 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію(ІІ): O O 3 R 1 R R N N + S 2 R 3 R 1 N S A CH2 CH B + B S 2 R N S 4 CH R 4 R I причому 1 2 R , R є Alk; 3 4 R , R є Аr; А-В є I-І, Вr-Вr, І-Вr. II A UA 76401 U (54) СПОСІБ ОДЕРЖАННЯ СОЛЕЙ 8-ГАЛОГЕН-4-ОКСО-2,3,5,9-ЗАМІЩЕНИХ-5,7,8,9-ТЕТРАГІДРО-4НТІЄНО[3',2':5,6]ПІРИМІДО[2,1-b][1,3]ТІАЗИН-10-ІЮ UA 76401 U UA 76401 U 5 10 15 20 25 30 Корисна модель відноситься до органічної хімії, а саме до способів одержання конденсованих похідних тієнопіримідинотіазину. Відомі кілька підходів при створенні поліконденсованих систем на основі піримідину. Зокрема, взаємодією натрієвих солей тієно[2,3-d]піримідину із похідними 1,3-дибромопропану можна одержати лише похідні лінійної конденсованої системи тієно[2',3':4,5]піримідо[2,1b][1,3]тіазину [1]. Цей прийом успішно використовується для селективного синтезу лінійних трициклічних тієнопіримідинотіазинів, в яких тіазинова складова є насиченим фрагментом. Електрофільною гетероциклізацією 1-R-пропенільних тіоетерів тієно[2,3-d]піримідину при дії концентрованої сульфатної кислоти автори отримали лінійні тієно[2',3':4,5]піримідо[2,1b][1,3]тіазини [2]. Цей метод є прийнятним для синтезу тієно[2',3':4,5]-піримідо[2,1-b][1,3]тіазинів лінійної будови, є простим у виконанні, але обмеженим в плані можливостей функціоналізації кінцевих продуктів. Найбільш близьким за технічною сутністю до заявленого є спосіб одержання ангулярної системи тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазину, який включає в себе електрофільну гетероциклізацію 1-R-пропенільних тіоетерів тієно[2,3-d]піримідину під дією галогенів [3]. Цей 3 прийом характеризується відсутністю замісників при N-атомові Нітрогену піримідинового циклу у вихідних тіоетерах, внаслідок чого можливо отримати лише протоновані тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазини, що виключає можливість утворення класичного позитивно зарядженого органічного катіону, тобто, солей 8-галоген-4-оксо-2,3,5,9-заміщених5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію. Завданням корисної моделі є розробка способу одержання солей 8-галоген-4-оксо-2,3,5,9заміщених-5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]-піримідо[2,1-b][1,3]тіазин-10-ію, який характеризується універсальністю, простотою експерименту, доступністю реагентів та високими виходами. Поставлене завдання досягається таким чином, що в способі одержання солей 8-галоген-4оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4H-тієно-[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію, який включає в себе електрофільну гетероциклізацію 1-R-пропенільних тіоетерів тієно[2,3d]піримідину під дією галогенів, який відрізняється тим, що як вихідні тіоетерів використовують 3 заміщені при N-атомові Нітрогену піримідинового циклу сполуки (І), які при галогеногетероциклізації (дія ІВr, Вr2 або І2) перетворюються в солі 8-галоген-4-оксо-2,3,5,9заміщених-5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]піримідо[2,1-b] [1,3]тіазин-10-ію (II): O O 3 R R N + S 2 R N S 3 R 1 R 1 A B N + 2 R CH2 CH B S N S 4 CH R 4 R I 35 40 45 50 II A причому 1 2 R , R є Alk; 3 4 R , R є Аr; А-В є I-І, Вr-Вr, І-Вr. Модельним об'єктом для досліджень було використано цинамільні тіоетери тієно[2,3d]піримідину (2), які можна отримати реакцією алкілування натрієвих солей тієно[2,3d]піримідину (1). Із тіоетерів (2) методом електрофільної галогеногетероциклізації, який характеризується простотою виконання, доступністю реактивів та високими виходами, отримують солі 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію (3-5), які містять позитивно заряджений гетероатомом. Склад синтезованих солей (2-5) підтверджено даними елементного аналізу; будову доведено методом спектроскопії протонного магнітного резонансу (ПМР) високого розрішення 13 (300 МГц) та методом спектроскопії ядерного магнітного резонансу на ядрах Карбону (ЯМР С) (75 МГц). Приклад 1. Схема одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Нтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію (3-5) 1 UA 76401 U O O R 3 R R 1 R 1 3 N N SK 2 R + 2 R CH2 CH N S S Cl N S CH2 CH 4 4 CH R CH R 2 1 O R 3 N R 1 R N + S 2 R N S A B + 2 R 10 15 20 25 30 35 40 45 2 N S CH2 CH 4 R 4 1 B S CH R 5 3 R 1 O 3-5 2 A R + R є (СН2)4; 3 4 R , R є С6Н5; A-B є Br-Br (3), I-І (4), I-Br (5); 3-Фенил-2-циннамілтіо-3,4-Н-(5,6,7,8-тетраметилено)тієно[2,3-d]пиримидин-4-он (2). Калієву сіль (1) (0.054 моль) [4] розчиняють в етанолі при нагріванні. Після охолодження утвореного розчину до кімнатної температури, добавляють циннамілхлорид (0.060 моль) в 5 мл етанолу. Реакційну суміш нагрівають на водяній бані протягом 1 години. Кінцевий продукт, який випадає в осад після охолодження реакційної суміші, відфільтровують і перекристалізовують в етанолі. Вихід 82 %, Т. топл. 188 °С. Кристали білого кольору. Спектр ПМР в ДМСО-Д6 (δ, м. ч., J, Гц): 1.76, 1.82 (4Н, 2 м, 2СН2); 2.76, 2.83 (4Н, 2 м, 2СН2); 3.94 (2Н, д, 6.0, SCH2); 6.30 (1Н, м, =СН); 6.66 (1H, д 12.4, =СН); 7.24-7.55 (10Н, м, 2С6Н5). Знайдено, %: С 69.69; Н 5.16; N 6.48; S 14.94. C25H22N2OS2. Вирахувано, %: С 69.74; Н 5.15; N 6.51; S 14.89. 8-Бром-4-оксо-2,3-(тетраметилен)-5,9-дифеніл-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]пірамідо[2,1-b][1,3]тіазин-10-ію бромід (3). Тіоетер (2) (0.001 моль) розчиняють в 20 мл льодяної оцтової кислоти при нагріванні. Після охолодження утвореного розчину до кімнатної температури, по краплях добавляють розчин брому (0.002 моль) в 10 мл льодяної оцтової кислоти. Реакційну суміш перемішують при кімнатній температурі протягом 3 години і залишають на 1 добу. Кінцевий продукт, який випадає в осад, відфільтровують і промивають на фільтрі ацетоном. Вихід 89 %, Т. топл. 208-210 °С. Білий порошок. Спектр ПМР в ДМСО-Д6 (δ, м. ч., J, Гц): 1.77 (4Н, м, 2СН2); 2.77, 2.84 (4Н, 2 м, 2СН2); 3.27 (2Н, дд, 2.7, 15.0, SCH2); 5.51 (1Н, м, СНВr); 6.47 13 (1Н, м, CHPh); 7.52-7.94 (10Н, м, 2С6Н5). Спектр ЯМР С в ДМСО-Д6 (δ, м. ч., J, Гц): 21.73, 22.62, 24.63, 25.47 (4СН2); 33.46 (SCH2); 42.32 (СНВr); 71.14 (CHPh); 121.64 (тіофен); 126.96 (пара-NC6H5); 129.08 (С, орто-NC6H5); 129.34 (С, орто-NC6H5); 129.81 (2С, мета-С6H5); 130.73 (2С, орто-С6H5); 130.98 (С, мета-NC6H5); 131.32 (С, мета-NC6Н5); 131.91 (С, пара-С6Н5); 133.55 (тіофен); 133.97 (тіофен); 134.71 (вузл-NС6Н5); 135.54 (вузл-С6Н5); 150.57 (тіофен); 153.92 (С=О); + 163.65 (С=N ). Знайдено, %: С 50.52; Н 3.70; Вr 28.01; N 4.68; S 10.64. C25H22Br2N2OS2. Вирахувано, %: С 50.86; Н 3.76; Вr 27.07; N 4.74; S 10.86. 8-Йод-4-оксо-2,3-(тетраметилен)-5,9-дифеніл-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]пірамідо[2,1-b][1,3]тіазин-10-ію йодид (4). Тіоетер (2) (0.001 моль) розчиняють в 20 мл льодяної оцтової кислоти при нагріванні. Після охолодження утвореного розчину до кімнатної температури, порціями по 4-5 мл добавляють розчин йоду (0.002 моль) в 50 мл льодяної оцтової кислоти. Реакційну суміш перемішують при кімнатній температурі протягом 72 години. Кінцевий продукт, який випадає в осад, відфільтровують і промивають на фільтрі діетиловим етером. Вихід 91 %, Т. топл. 150 °С. Жовтий порошок. Спектр ПМР в ДМСО-Д6 (δ, м. ч., J, Гц): 1.77 (4Н, м, 2СН2); 2.77, 2.84 (4Н, 2 м, 2СН2); 3.27 (2Н, дд, 2.7, 105.0, SCH2); 5.47 (1Н, м, СНІ); 6.38 (1Н, м, CHPh); 7.51-7.91 (10Н, м, 2С6Н5). Знайдено, %: С 43.58; Н 3.20; I 37.83; N 4.00; S 9.14. C25H22I2N2OS2. Вирахувано, %: С 43.87; Н 3.24; I 37.09; N 4.09; S 9.37. 8-Йод-4-оксо-2,3-(тетраметилен)-5,9-дифеніл-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію бромід (5). До 0.001 моль дрібно розтертого йоду додають 0.001 моль брому в 10 мл льодяної оцтової кислоти і гріють до розчинення; реакційну суміш залишають на одну добу для кількісного утворення броміду йоду. Тіоетер (2) (0.001 моль) розчиняють в 20 мл льодяної оцтової кислоти при нагріванні. Після охолодження утвореного розчину до кімнатної температури, порціями по 4-5 мл добавляють попередньо приготований 2 UA 76401 U 5 10 15 20 розчин броміду йоду (0.001 моль) в 10 мл льодяної оцтової кислоти. Реакційну суміш перемішують при кімнатній температурі протягом 24 години. Кінцевий продукт, який випадає в осад, відфільтровують і промивають на фільтрі діетиловим етером. Вихід 84 %, Т. топл. 184-186 °С. Жовтий порошок. Спектр ПМР в ДМСО-Д6 (δ, м. ч., J, Гц): 1.76 (4Н, м, 2СН2); 2.77, 2.84 (4Н, 2 м, 2СН2); 3.26 (2Н, дд, 2.7, 108.0, SCH2); 5.48 (1Н, м, СНІ); 6.38 (1Н, м, CHPh); 7.51-7.91 (10Н, м, 2С6Н5). Знайдено, %: С 46.92; Н 3.46; N 4.32; S 9.98. C25H22BrIN2OS2. Вирахувано, %: С 47.11; Н 3.48; N 4.40; S 10.06. Таким чином, було розроблено спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених5,7,8,9-тетрагідро-4H-тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію. Спосіб характеризується універсальністю, простотою експерименту, доступністю реагентів та високими виходами. Корисна модель може бути використана у науково-дослідних хімічних та хімікофармацевтичних лабораторіях. Джерела інформації: 1. Ahmed E.K. Synthesis of New Fused Heterocycles by annelation of Thiopyrano[4',3':4,5]thieno[2,3-c]pyrimidines. // Monatsh. Chem. - 1995. - Bd. 126. - № 8/9. - S. 953959. 2. Petra Wippich, Michael Gutschow, Siegfried Leistner. Regioselective Preparation of 1(Bromomethyl)-5H-thiazolo[3,2-a]-quinazolin-5-ones and analogous 5H-Thieno[3,2-e]thiazolo[3,2-a]pyrimidin-5-ones. // Synthesis. - 2000. - No 5.- P. 714-720. 3. Васькевич Р.И., Хрипак С.М., Станинец В.И., Зборовский Ю.Л., Несторенко A.M., Пироженко В.В. Синтез производных тиазинотиенопиримидина и их перегруппировка в тиазолотиенопиримидины. // Укр..Хим.Ж. - 2000. - № 11. - С. 47-52. - Прототип. 4. Хрипак С.М. Синтезы и реакции в ряду тиено[2,3-d]-пиримидина: Диссертация на соискание ученой степени доктора химических наук: 02.00.03. - Киев, 1991. - 336 с. 25 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 30 Спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію, який включає в себе електрофільну гетероциклізацію 1-R-пропенільних тіоетерів тієно[2,3-d]піримідину під дією галогенів, який 3 відрізняється тим, що як вихідні тіоетерів використовують заміщені при N-атомові Нітрогену піримідинового циклу сполуки (І), які при галогеногетероциклізації (дія ІВr, Вr2 або I2) перетворюються в солі 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4Hтієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію(ІІ): O O 3 R R N + S 2 R N S 3 R 1 R 1 A N + B 2 R CH2 CH B S N S 4 CH R 4 R 35 I II A причому 1 2 R , R є Alk; 3 4 R , R є Аr; А-В є I-І, Вr-Вr, І-Вr. 40 Комп’ютерна верстка С. Чулій Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 8-halogeno-4-oxo-2,3,5,9-substituted-5,7,8,9-tetrahydro-4h-thieno[3',2':5,6]pyrimido [2,1-b][1,3]thiazin-10-ium salts
Автори англійськоюSlyvka Mykhailo Vasyliovych, Slyvka Maryna Vasylivna, Kish Anett Ottivna, Lendiel Vasyl Heorhiiovych
Назва патенту російськоюСпособ получения солей 8-галоген-4-оксо-2,3,5,9-замещенных-5,7,8,9-тетрагидро-4н-тиено[3',2':5,6]пиримидо[2,1-b][1,3]тиазин-10-ия
Автори російськоюСливка Михаил Васильевич, Сливка Марина Васильевна, Киш Анетт Оттовна, Лендел Василий Георгиевич
МПК / Мітки
МПК: C07D 279/00, C07D 513/00
Мітки: одержання, спосіб, 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4н-тієно[3',2':5,6]піримідо[2,1-b][1,3]тіазин-10-ію, солей
Код посилання
<a href="https://ua.patents.su/5-76401-sposib-oderzhannya-solejj-8-galogen-4-okso-2359-zamishhenikh-5789-tetragidro-4n-tiehno3256pirimido21-b13tiazin-10-iyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання солей 8-галоген-4-оксо-2,3,5,9-заміщених-5,7,8,9-тетрагідро-4н-тієно[3′,2′:5,6]піримідо[2,1-b][1,3]тіазин-10-ію</a>
Попередній патент: Система утилізації тепла холодильної установки
Наступний патент: Спосіб одержання солей 6-галогено-1,2-дизаміщені-5-арил-1,5,6,7-тетрагідро[1,2,4]триазоло[5,1-b][1,3]тіазин-4-ію
Випадковий патент: Спосіб одержання целюлози









