N-піразинілфенілсульфонаміди, спосіб їх одержання (варіанти), фармацевтична композиція на їх основі, спосіб її одержання, спосіб лікування опосередкованої хемокіном хвороби, спосіб лікування запальної хвороби
Номер патенту: 79255
Опубліковано: 11.06.2007
Автори: Робертс Брайан, Джонсон Тімоті, Бакстер Ендрю, Кіндон Ніколас, Стокс Майкл
Формула / Реферат
1. Сполука формули (І) або її фармацевтичнo прийнятна сіль або сольват:
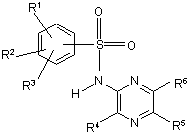 ,
,
в якій:
R1, R2 та R3 незалежно представляють гідроген, галоген, ціаногрупу, CF3, ОСF3, ОС1-6алкіл або С1-6алкіл,
R4 представляє галоген, CO2R12,
С1-6алкоксил, де алкіл може утворювати 3-6-членне насичене кільце або може бути заміщеним 1-3 атомами флуору або ціаногрупою;
С3-6алкенілоксил або С3-6алкінілоксил, де кожний з них може бути, як варіант, заміщений гідроксилом чи NR14R15;
ОС1-6алкіл-Х-С1-6алкіл, де алкіли можуть утворювати 3-6-членне насичене кільце;
ОС1-6алкілR11 або OС2-6алкіл-Х-R11, де алкіл може утворювати 3-6-членне насичене кільце та є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)2R13, S(O)R13 або COR13;
ОС1-6алкілR16;
R5 та R6 незалежно представляють гідроген, ціаногрупу, галоген, CO2R12, CONR14R15;
С1-6алкіл, як варіант, заміщений гідроксилом, NR14R15 або 1-3 атомами флуору;
С1-6алкілR11, XCH(R11)С1-6алкіл або ХCH(R16)С1-6алкіл, де алкіл може бути, як варіант, заміщений 1-3 групами, вибраними з гідроксилу та NR14R15;
NR14R15; N(R11)R11; X-(CH2)qNR14R15; (CH2)nNR14R15; NHC(O)С1-6алкіл, як варіант, заміщений одною або більше гідроксигрупами,
С3-6алкініл або С3-6алкеніл, як варіант, розгалужені та, як варіант, заміщені 1-3 групами, вибраними з гідроксилу, ціаногрупи, галогену та =O;
R11; X-R11; X-R12; Х-С1-6алкілR16; X-R16; X-(CH2)nCO2R12; X-(CH2)nCONR14R15; X-(CH2)nR11; X-(CH2)nCN; X-(CH2)qOR12; (CH2)nOR12; (CH2)n-X-R11; X-(CH2)qNHC(O)NHR12; X-(CH2)qNHC(O)R12; X-(CH2)qNHS(O)2R12; X-(CH2)qNHS(O)2R11; Х-С3-6алкеніл; Х-С3-6алкініл;
n дорівнює 1, 2, 3, 4 або 5;
q дорівнює 2, 3, 4, 5 або 6;
X представляє NR13, O, S, S(O), S(O)2;
R11 представляє арил або 5-7-членне гетероароматичне кільце, що містить 1-4 гетероатоми, вибрані з нітрогену, оксигену або сульфуру, кожний з них може бути, як варіант, заміщеним 1-3 групами, вибраними з галогену, C(O)NR14R15, C(O)OR12, гідроксилу, =O, =S, CN, NO2, COR13, NR14R15, X(CH2)qNR14R5, (CH2)nNR14R15, (СH2)nOH, SR13, S(O)R13, S(O)2R13, С1-6алкіл-Х-С1-6алкіл, С1-6алкіл або С1-6алкоксил, де алкіл може утворювати 3-6-членне кільце або є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)R13, S(O)2R13;
R12 та R13 незалежно представляють гідроген або С1-6алкіл, де алкіл може бути заміщеним 1-3 атоми флуору або може утворювати 3-6-членне насичене кільце;
R14 та R15 незалежно представляють гідроген, С1-6алкіл, С3-6циклоалкіл або (CH2)qOH,
або R14 та R15 разом з атомом нітрогену, до якого вони приєднані, утворюють 4-8-членне насичене кільце, що містить 1-3 гетероатоми, вибрані з нітрогену, оксигену та сульфуру, та, як варіант, заміщене С1-6алкілом, С1-6алкіл-ОН або гідроксилом; а
R16 представляє 4-8-членне насичене кільце, що містить 1-3 гетероатоми, вибраними з нітрогену, оксигену або сульфуру, та, як варіант, заміщене 1-3 групами, вибраними з гідроксилу, ціаногрупи, галогену та =O,
за умови, що
коли R4 представляє галоген або С1-4алкоксил, а R5 представляє гідроген, галоген, С1-4алкіл, С1-2алкоксил, С1-2алкілтіогрупу, трифлуорметил або етиніл, та, коли один з R1,
R2 або R3 представляє С1-6алкіл або С1-6алкоксил та є розташованим у мета-положенні відносно сульфонамідної групи, тоді група, розташована у орто-положенні відносно як сульфонамідної групи, так і С1-6алкілу або С1-6алкоксилу, не є гідрогеном,
коли R4 представляє галоген або С1-4алкоксил, а R5 представляє гідроген, галоген, С1-4алкіл, С1-2алкоксил, С1-2алкілтіогрупу, трифлуорметил або етиніл, та, коли один з R1, R2 або R3 представляє С1-6алкіл або С1-6алкоксил та є розташованим у орто-положенні відносно сульфонамідної групи, тоді група, що є розташованою у орто-положенні відносно С1-6алкілу або С1-6алкоксилу, а також мета-положенні відносно сульфонамідної групи, не представляє гідроген,
коли два з R1, R2, R3 представляють гідроген, а інший представляє метил, що розташований у пара-положенні відносно сульфонаміду, а R4 представляє метоксил, тоді R5 не представляє гідроген або бром,
коли R5 представляє метил, R6 представляє метоксил, а один з R1, R2 або R3 представляє бром або йод, а інші два обидва є гідрогенами, тоді бром або йод не розташовані у орто-положенні відносно сульфонамідної групи, та
коли R5 представляє метил, а R4 представляє метоксил, і один R1, R2 або R3 представляє бром або йод, а інші два обидва є гідрогенами, тоді бром або йод не розташовані у орто-положенні відносно сульфонамідної групи.
2. Сполука за п. 1, в якій один з R1, R2 та R3 представляє гідроген, а інший представляє хлор, бром або метил.
3. Сполука за пп. 1 або 2, в якій R1 та R2 представляють хлор у 2- та 3-положеннях фенольного кільця, а R3 представляє гідроген, або R1 та R3 представляють хлор у 2- та 4- положеннях фенольного кільця, а R2 представляє гідроген, або R1 представляє хлор у 2-положенні, а R2 представляє метил у 3-положенні фенольного кільця, і R3 представляє гідроген.
4. Сполука за будь-яким з пп. 1-3, в якій R4 представляє С1-6алкоксил, як-то метоксил, 2-фуранілметоксил, бром, хлор, 2-метоксіетоксил, (5-метил-3-ізоксазоліл)метоксил, піридилметоксил, 3-піридазинілметоксил, метоксил, 2-(1-імідазоліл)етоксил, (2-метил-4-оксазоліл)метоксил та 4-метоксифенілметоксил.
5. Сполука за будь-яким з пп. 1 -4, в якій R4 представляє метоксил.
6. Сполука за будь-яким з пп. 1-5, в якій R5 представляє гідроген, галоген, як-то бром та хлор, феніл, С1-6алкіл, як-то метил, СН2ОН, ціаногрупу та 2-аміноетантіол.
7. Сполука за будь-яким з пп. 1 - 6, в якій R6 представляє гідроген, С1-6алкіл, СН2ОН та галоген.
8. Сполука за п. 1, якою є:
2,3-дихлор-N-(3-метокси-5-метил-2-піразиніл)-бензолсульфонамід,
N-(6-хлор-3-метокси-2-піразиніл)-2,3,4-трифлуорбензолсульфонамід,
3-хлор-N-(6-хлор-3-метокси-2-піразиніл)-2-метилбензолсульфонамід,
2,3-дихлор-N-(6-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-(5Н-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-2,5-диxлopбeнзoлcyльфoнaмiд,
N-(5-бром-3-метокси-2-піразиніл)-3,5-дихлорбензолсульфонамід,
N-(5-бром-3-метокси-2-піразиніл)-2,3-дихлорбензолсульфонамід,
N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-2,4-диxлopбeнзoлcyльфoнaмiд,
N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-3,4-диxлopбeнзoлcyльфoнaмiд,
N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-4-xлopбeнзoлcyльфoнaмiд,
N-(5-бром-3-метокси-2-піразиніл)-3-хлорбензолсульфонамід,
N-(3-метокси-5-метил-2-піразиніл)-2-флуорбензолсульфонамід,
N-(3-мeтoкcи-5-мeтил-2-пipaзинiл)бeнзoлcyльфoнaмiд,
N-(3-метокси-5-метил-2-піразиніл)-3-флуорбензолсульфонамід,
2-[[(3-метокси-5-метил-2-піразиніл)аміно]сульфоніл]бензонітрил,
N-(5-бром-3-метокси-2-піразиніл)бензолсульфонамід,
N-(5-бром-3-метокси-2-піразиніл)2-йодбензолсульфонамід,
2,3-диxлop-N-[3-(2-фypaнiлмeтoкcи)-5-мeтил-2-пipaзинiл]бeнзoлcyльфoнaмiд,
2,3-дихлор-N-[5-метил-3-(5-метил-3-ізоксазолілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(6-метил-2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(4-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(3-метил-2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(3-піридазинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-(3-метокси-2-піразиніл)бензолсульфонамід,
N-[5-бром-3-(2-піразинілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(1-метил-6-оксо-1,6-дигідро-3-піридинілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бpoм-3-(3-пipидaзинiлмeтoкcи)-2-пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмiд,
N-[5-бpoм-3-(3-пipидинiлмeтoкcи)-2-пipaзинiл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(5-піримідинілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-хлор-3-(3-піридинілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-хлop-3-(5-пipимiдинілмeтoкcи)-2-пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмiд,
2-хлор-N-(6-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
4-хлор-N-(6-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
N-(6-хлop-3-мeтoкcи-2-пipaзинiл)-2,4-диxлopбeнзoлcyльфoнaмiд,
N-(6-хлop-3-мeтoкcи-2-пipaзинiл)-3,4-диxлopбeнзoлcyльфoнaмiд,
3-хлор-N-(3-метокси-5-метил-2-піразиніл)-2-метилбензолсульфонамід,
2-хлор-N-(3-метокси-5-метил-2-піразиніл)бензолсульфонамід,
3-хлор-N-(3-метокси-5-метил-2-піразиніл)бензолсульфонамід,
4-хлop-N-(3-мeтoкcи-5-мeтил-2-пipaзинiл)бeнзoлcyльфoнaмiд,
2,4-диxлop-N-(3-мeтoкcи-5-мeтил-2-пipaзинiл)бeнзoлcyльфoнaмiд,
3,4-диxлop-N-(3-мeтoкcи-5-мeтил-2-пipaзинiл)бeнзoлcyльфoнaмiд,
N-(5-бром-3-метокси-2-піразиніл)-2-трифлуорметоксибензолсульфонамід,
3-хлор-N-(5-хлор-3-метокси-2-піразиніл)-2-метилбензолсульфонамід,
2-хлор-N-(5-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
3-хлор-N-(5-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
4-хлор-N-(5-хлор-3-метокси-2-піразиніл)бензолсульфонамід,
N-(5-хлор-3-метокси-2-піразиніл)-2,4-дихлорбензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-(4-морфолініл)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3,5-диметокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-(1-піролініл)-2-піразиніл]бензолсульфонамід,
3-хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)-2-метилбензолсульфонамід,
2,3-дихлор-N-(5,6-дихлор-3-метокси-2-піразиніл)бензолсульфонамід,
2-хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)бензолсульфонамід,
3-хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)бензолсульфонамід,
4-хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)бензолсульфонамід,
2,4-дихлор-N-(5,6-дихлор-3-метокси-2-піразиніл)бензолсульфонамід,
3,4-диxлop-N-(5,6-диxлop-3-мeтoкcи-2-пipaзинiл)бeнзoлcyльфoнaмiд,
2,3-дихлор-N-(3-метокси-5,6-диметил-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-(6-хлор-3,5-диметокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-метокси-5-(4-морфолініл)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-5-(2-гідроксіетиламіно)-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-5-диметиламіно-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-метокси-5-(2-метоксіетокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-5-гідрокси-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-метокси-5-([2,2']біпіразиніл)]бензолсульфонамід,
4-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілокси]бензойна кислота,
2,3-дихлор-N-(3,5-дихлор-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-{6-хлор-3-метокси-5-[(2-метоксіетил)аміно]-2-піразиніл}бензолсульфонамід,
N-{2-[3-хлор-5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразиніламіно]етил}ацетамід,
2,3-дихлор-N-[5-(4-гідроксиметил-1-піперидиніл)-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-ціано-3-(3-піридинілметокси-2-піразиніл]бензолсульфонамід,
2,3-диxлop-N-(6-xлop-3-мeтoкcи-5-мeтилaмiнo-2-пipaзинiл)бeнзoлcyльфoнaмiд,
2,3-дихлор-N-(3-метокси-5-метилсульфаніл-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-[5-(2,4-дифлуорфеніл)-3-метокси-2-піразиніл]бензолсульфонамід,
[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілсульфаніл]оцтової кислоти
метиловий естер,
[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілсульфаніл]оцтова кислота,
2,3-дихлор-N-[5-(2-хлорбензилсульфаніл)-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-5-(3-гідроксі-1-азетидиніл)-3-метокси-2-
піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-метил-3-(1-окси-3-піразинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(4-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(1-окси-4-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(2-метилсульфанілетокси)-2-піразиніл]бензолсульфонамід,
N-(3-бутокси-5-хлор-2-піразиніл)-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(2-метил-3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(6-метил-2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-диxлop-N-[5-xлop-3-(1-oкcи-2-пipидинiлмeтoкcи)-2-пipaзинiл]бензолсульфонамід,
3-хлор-N-[5-хлор-3-(3-піридинілметокси)-2-піразиніл]-2-метилбензолсульфонамід,
3-хлор-N-[5-хлор-3-(3-піридинілметокси)-2-піразиніл]-2-флуорбензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(4-метоксифенілметокси)-2-піразиніл]бензолсульфонамід,
N-[5-бром-6-хлор-2-піразиніл]-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-(2-піридинілметокси)-2-піразиніл]бензолсульфонамід,
N-[5-(2-аміноетилсульфаніл)-3-(2-піридинілметокси-2-піразиніл)-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(6-метокси-3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
N-[3-(3-бромфенілметокси)-5-хлор-2-піразиніл]-2,3-дихлорбензолсульфонамід,
3-[6-хлор-3-(2,3-дихлорбензолсульфоніламіно)-2-піразинілоксиметил]бензойної кислоти метиловий естер,
3-[6-хлор-3-(2,3-дихлорбензолсульфоніламіно)-2-піразинілоксиметил]бензойна кислота,
2,3-дихлор-N-[5-хлор-3-(3-гідроксиметилфенілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(3-метиламінометилфенілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-{3-([2-гідроксіетиламіно]метил)фенілметокси}-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(4-гідроксиметилфенілметокси)-2-піразиніл]бензолсульфонамід,
2,3-диxлop-N-[5-xлop-3-{4-([2-гiдpoкcieтилaмiнo]мeтил)фeнiлмeтoкcи}-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(4-гідроксиметилфенілметокси)-2-піразиніл]бензолсульфонамід,
2,3-диxлop-N-[5-xлop-3-(2-гiдpoкcимeтилфeнiлмeтoкcи)-2-пipaзинiл]бeнзoлcyльфoнaмiд,
5-(2,3-дихлорбензолсульфоніламіно)-6-метоксипіразин-2-карбонової кислоти метиловий естер,
2,3-дихлор-N-[5-(1-гідрокси-1-метилетил)-3-метокси-2-піразиніл]бензолсульфонамід,
N-[5-(2-амiнoeтoкcи)-3-мeтoкcи-2-пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмiд,
N-{5-[(2-аміноетил)тіо]-6-хлор-3-метокси-2-піразиніл}-2,3-дихлорбензолсульфонамід,
3-[(5-{[(2,3-дихлорфеніл)сульфоніл]аміно}-6-метокси-2-піразиніл)тіо]пропанової кислоти
метиловий естер,
2,3-дихлор-N-[5-бром-3-метокси-6-метил-2-піразиніл]бензолсульфонамід,
5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-3-метилпіразин-2-карбонової кислоти метиловий естер,
2,3-дихлор-N-[5-(гідроксиметил)-3-метокси-6-метил-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5,6-дихлор-3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
3-хлор-N-(5-хлор-3-метокси-2-піразиніл)-2-флуорбензолсульфонамід,
3-хлор-2-флуор-N-[3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
3-{[(2,3-дихлорфеніл)сульфоніл]аміно}піразин-2-карбонової кислоти метиловий естер,
N-(5-бром-6-хлор-3-метокси-2-піразиніл)-2,3-дихлорбензолсульфонамід,
3-хлор-5-{[(2,3-дихлорфеніл)сульфоніл]аміно}-6-метоксипіразин-2-карбонової кислоти
метиловий естер,
2,3-дихлор-N-[6-хлор-5-(гідроксиметил)-3-метоксипіразин-2-іл]бензолсульфонамід,
2,3-дихлор-N-{3-[(6-метокси-3-піридиніл)метокси]-2-піразиніл}бензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-метокси-5-(метоксиметил)-2-піразиніл]бензолсульфонамід,
2-хлор-N-(5-хлор-3-метокси-2-піразиніл]трифлуорбензолсульфонамід,
2-хлор-3-флуор-N-(3-метокси-2-піразиніл)бензолсульфонамід,
2-хлор-3-метокси-N-(3-метокси-2-піразиніл)бензолсульфонамід,
N-[5-бром-3-[(2S)-2-піролідинілметокси]-2-піразиніл]-2,3-дихлорбензолсульфонамід,
5-(2,3-дихлорбензолсульфоніламіно)-6-(3-піридинілметокси)піразин-2-карбонової кислоти метиловий естер,
5-{[(2,3-дихлорфеніл)сульфоніл]аміно}-6-(3-піридинілметокси)-2-піразинкарбоксамід,
2,3-дихлор-N-[5-(4-піридиніл)-3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-(гідроксиметил)-3-(3-піридинілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-(гідроксиметил)-3-метокси-2-піразиніл]бензолсульфонамід,
N-(5-алілокси-3-метокси-2-піразиніл)-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[5-(3-гідрокси-1-пропініл)-3-метокси-2-піразиніл]бензолсульфонамід,
N-{3-[(5-бром-3-піридиніл)метокси]-5-хлор-2-піразиніл}-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-{[6-(гідроксиметил)-2-піридиніл]метокси}-2-піразиніл]бензолсульфонамід,
2,3-диxлop-N-{5-xлop-3-[(2-мeтил-4-oкcaзoлiл)мeтoкcи]-2-пipaзинiл]бeнзoлcyльфoнaмiд,
2,3-дихлор-N-{3-[(2-метил-4-оксазоліл)метокси]-2-піразиніл}бензолсульфонамід,
N-[5-бром-3-(фенілметокси)-2-піразиніл)-2,3-дихлорбензолсульфонамід,
N-[5-бpoм-3-(2-циклoпpoпiлeтoкcи)пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмiд,
N-[5-бром-3-(3-тієнілметокси)піразиніл]-2,3-дихлорбензолсульфонамід,
N-{5-бром-3-[(2-метил-3-фураніл)метокси]-2-піразиніл}-2,3-дихлорбензолсульфонамід,
N-{5-бром-3-[(3-фураніл)метокси]-2-піразиніл}-2,3-дихлорбензолсульфонамід,
N-{5-бром-3-[(4-флуорфеніл)метокси]-2-піразиніл}-2,3-дихлорбензолсульфонамід,
N-{5-бpoм-3-[(3-флyopфeнiл)мeтoкcи]-2-пipaзинiл}-2,3-диxлopбeнзoлcyльфoнaмiд,
N-{5-бром-3-[3-(2-піридиніл)пропокси]-2-піразиніл}-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(пентилокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бpoм-3-(пpoпiлoкcи)-2-пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмiд,
N-[5-бром-3-(2-метоксіетокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(2-етоксіетокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(2-флуоретокси-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-{5-бром-3-[2-(1Н-імідазол-1-іл)етокси]-2-піразиніл}-2,3-дихлорбензолсульфонамід,
N-{5-бpoм-3-[3-(3-пipидинiл)пpoпoкcи]-2-піpaзинiл}-2,3-диxлopбeнзoлcyльфoнaмiд,
N-[5-бром-3-[2-(метиламіно)етокси]-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-[3-(4-гідроксифеніл)пропокси]-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(2-феноксіетокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(циклопропілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[5-бром-3-(3-феноксипропокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-(5-етокси-3-метокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-([1,2,4]-1-триазоліл)-2-піразиніл]бензолсульфонамід,
2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілсульфаніл]-N-метилацетамід,
2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілсульфаніл]ацетамід,
2,3-дихлор-N-[5-(4-флуорбензилсульфаніл)-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-ціанометилсульфаніл-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-([1,2,4]-3-оксадіазолілметилсульфаніл)-2-піразиніл]бензолсульфонамід,
N-[5-(2-амiнoeтилcyльфaнiл)-3-мeтoкcи-2-пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмід,
2,3-дихлор-N-[3-метокси-5-(5-метил-3-ізоксазолілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-(5-диметиламінометил-2-фуранілметокси)-3-метокси-2-піразиніл]бензолсульфонамід,
N-[5-бром-3-(5-диметиламінометил-2-фуранілметокси)-2-піразиніл]-2,3-дихлорбензолсульфонамід,
2,3-диxлop-N-[5-(2-гiдpoкcieтилcyльфaнiл)-3-мeтoкcи-2-пipaзинiл]бeнзoлcyльфoнaмiд,
2,3-дихлор-N-[5-[2-(етилуреїдо)етилсульфаніл]-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(5-диметиламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-хлор-3-(5-диметиламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[6-Дихлор-3-(5-метиламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(5-диметиламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(5-метиламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
N-(5-бром-3-метоксипіразиніл)-2-ціанобензолсульфонамід,
N-(5-бром-3-метоксипіразиніл)-2,3-дихлор-4-флуорбензолсульфонамід,
2,3-диxлop-N-[3-мeтoкcи-5-(4-мopфoлiнiлмeтил)-2-пipaзинiл]бeнзoлcyльфoнaмiд,
N-(3-алілокси-5-хлор-2-піразиніл)-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(2-пропінілокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[3-(2-пропінілокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-(5-ціано-3-метокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-{3-метокси-5-[(2S)-піролідин-2-ілметокси]-2-піразиніл}бензолсульфонаміду
гідрохлорид,
2,3-дихлор-N-{6-хлор-3-метокси-5-[(2R)-2-піролідинілметокси]-2-піразиніл]бензолсульфонаміду гідрохлорид,
2,3-дихлор-N-[3-метокси-5-(2-піридинілметокси)-2-піразиніл]бензолсульфонаміду гідрохлорид,
2,3-дихлор-N-(3-метокси-6-метил-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-(1Н-1,2,4-триазол-1-ілметил)-2-піразиніл]бензолсульфонамід,
N-(3-(5-амінометил-2-фуранілметокси)-5-хлор-2-піразиніл)-2,3-дихлорбензолсульфонамід,
N-(3-(5-амінометил-2-фуранілметокси)-2-піразиніл)-2,3-дихлорбензолсульфонамід,
2,3-дихлор-N-[3-метокси-5-(2-пропін-1-ілокси)-2-піразиніл]бензолсульфонамід,
{[5-(2,3-дихлорфенілсульфоніламіно)-6-метокси-2-піразиніл]оксі}оцтової кислоти метиловий естер,
N-[5-(2,3-диxлopфeнiлcyльфoнiлaмiнo)-6-мeтoкcи-2-пipaзинiл]-2-гiдpoкciaцeтaмiд,
6-(2,3-дихлорфенілсульфоніламіно)-5-метокси-2-піразинілкарбонової кислоти метиловий естер,
2,3-дихлор-N-[6-(гідроксиметил)-3-метокси-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-(5-метансульфоніл-3-метокси-2-піразиніл)бензолсульфонамід,
2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2-піразинілокси]-N,N-діетилацетамід,
2,3-дихлор-N-{5-[2-(диметиламіно)етилсульфаніл]-3-метокси-2-піразиніл}бензолсульфонамід,
2,3-дихлор-N-(5-дифлуорметил-3-метокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-4-флуор-N-(3-метокси-2-піразиніл)бензолсульфонамід,
2,3-дихлор-N-{5-хлор-3-[1-(циклопропіл)етокси]-2-піразиніл}бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(5-форміл-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
2,3-дихлор-N-[5-хлор-3-(5-циклопропіламінометил-2-фуранілметокси)-2-піразиніл]бензолсульфонамід,
N-[5,6-біс-(гідроксиметил)-3-метокси-2-піразиніл]-2,3-дихлорбензолсульфонамід,
N-[3-[(2-аміно-4-оксазоліл)метокси]-5-хлор-2-піразиніл]-2,3-дихлорбензолсульфонамід та їх фармацевтично прийнятні солі або сольвати.
9. Спосіб отримання сполуки (І), що визначена в п. 1, який включає:
реакцію сполуки формули (II):
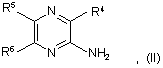
де R4, R5 та R6 визначені у формулі (І) або є їх захищеними похідними, із сполукою формули (III):
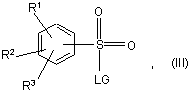
де R1, R2 та R3 визначені у формулі (І) або є їх захищеними похідними, a LG представляє відщеплювану групу,
та, як варіант, після цього
видалення будь-яких захисних груп,
перетворення сполуки формули (І) у наступну сполуку формули (І) або
утворення фармацевтично прийнятної солі.
10. Спосіб отримання сполуки (І), що визначена в п. 1, який включає:
для сполук, в яких R4 представляє С1-6алкоксил, де алкіл може утворювати 3-6-членне насичене кільце або може бути заміщеним 1-3 атоми флуору або ціаногрупою;
С3-6алкенілоксил або С3-6алкінілоксил, причому кожний з них може бути, як варіант, заміщеним гідроксилом чи NR14R15;
ОС1-6алкіл-Х-С1-6алкіл, де алкіли можуть утворювати 3-6-членне насичене кільце;
ОС1-6алкілR11 або ОС2-6алкіл-X-R11, де алкіл може утворювати 3-6-членне насичене кільце та є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)2R13, S(O)R13; або ОС1-6алкіл-R16;
обробку сполуки формули (VI), де LG представляє відщеплювану групу:
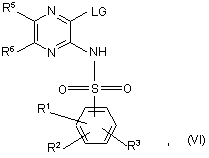
сполукою формули (V) R4-Н
у присутності придатної основи,
та, як варіант, після цього
видалення будь-яких захисних груп,
перетворення сполуки формули (І) у наступну сполуку формули (І) або
утворення фармацевтично прийнятної солі.
11. Спосіб отримання сполуки (І), що визначена в п. 1, який включає:
для сполук структури (І), де R5 представляє, як варіант, заміщений арил або гетероарил, які визначено вище, реакцію сполуки формул (VII), де LG представляє відщеплювану групу, з арил- або гетероарилбороновою кислотою у присутності паладієвого каталізатора та придатної основи при підвищеній температурі:
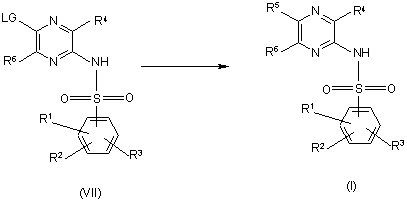
та, як варіант, після цього
видалення будь-яких захисних груп,
перетворення сполуки формули (І) у наступну сполуку формули (І) або
утворення фармацевтично прийнятної солі.
12. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтичнo прийнятну сіль або сольват за п. 1 у поєднанні з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм.
13. Спосіб отримання фармацевтичної композиції, яка визначена у п. 12, який полягає у змішуванні сполуки формули (І) або її фармацевтичнo прийнятної солі або сольвату за п. 1 з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм.
14. Сполука формули (І), що визначена в п. 1, або її фармацевтичнo прийнятна сіль або сольват для застосування у терапії.
15. Спосіб лікування опосередкованої хемокіном хвороби, де хемокін зв'язується з одним або більше рецепторами хемокінів, який полягає у введенні пацієнту терапевтично ефективної кількості сполуки формули (IВ) або її фармацевтичнo прийнятної солі або сольвату:
 , (IB)
, (IB)
в якій:
R1, R2 тa R3 незалежно представляють гідроген, галоген, ціаногрупу, CF3 або С1-6 алкіл;
R4 представляє галоген; CO2R12,
С1-6алкоксил, де алкіл може утворювати 3-6-членне насичене кільце або може бути заміщеним 1-3 атомами флуору або ціаногрупою;
С3-6алкенілоксил або С3-6 алкінілоксил, де кожний з них може бути, як варіант, заміщеним гідроксилом чи NR14R15;
С1-6алкіл-Х-С1-6алкіл, де алкіли можуть утворювати 3-6-членне насичене кільце;
ОС1-6алкілR11 або OC2-6алкіл-Х-R11, де алкіл може утворювати 3-6-членне насичене кільце та є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)2R13, S(O)R13;
ОС1-6алкілR16,
R5 та R6 незалежно представляють гідроген, ціаногрупу, галоген, CO2R12, CONR14R15;
С1-6алкіл, як варіант, заміщений гідроксилом, NR14R15 або 1-3 атомами флуору;
С1-6алкілR11, ХСH(R11)С1-6алкіл або ХСH(R16)С1-6алкіл, де алкіл може бути, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу та NR14R15; NR14R15; N(R11)R11; X-(CH2)qNR14R15; (CH2)nNR14R15;
С3-6алкініл або С3-6алкеніл, як варіант, розгалужені та, як варіант, заміщені 1-3 групами, вибраними з гідроксилу, ціаногрупи, галогену та =O;
R11; X-R11; X-R12; Х- С1-6алкілR16; X-R16; Х-(СН2)nСO2R12; X-(CH2)nCONR14R15; Х-(СН2)nR11; X-(CH2)nCN; X-(CH2)qOR12; (CH2)nOR12; (CH2)n-X-R11; X-(CH2)qNHC(O)NHR12; X-(CH2)qNHC(O)R12; X-(CH2)qNHS(O)2R12; X-(CH2)qNHS(O)2R11; Х-С3-6алкеніл; Х-С3-6алкініл;
n дорівнює 1, 2, 3,4 або 5;
q дорівнює 2, 3, 4, 5 або 6;
X представляє NR13, О, S, S(O), S(O)2;
R11 представляє арил або 5-7-членне гетероароматичне кільце, що містить 1-4 гетероатоми, вибрані з нітрогену, оксигену або сульфуру, кожний з них може бути, як варіант, заміщеним 1-3 групами, вибраними з галогену, C(O)NR14R15, C(O)OR12, гідроксилу, =O, =S, CN, NO2, NR14R15, X(CH2)qNR14R15, (CH2)nNR14R15, (СH2)nОН, SR13, S(O)R13, S(O)2R13,
С1-6алкіл-Х-С1-6алкіл, С1-6алкіл або С1-6алкоксил, де алкіл може утворювати 3-6-членне кільце або є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)R13, S(O)2R13;
R12 та R13 незалежно представляють гідроген або С1-6алкіл, де алкіл може бути заміщеним 1-3 атоми флуору або може утворювати 3-6-членне насичене кільце;
R14 та R15 незалежно представляють гідроген, С1-6алкіл, С3-6циклоалкіл або (CH2)qOH,
або R14 та R15 разом з атомом нітрогену, до якого вони приєднані, утворюють 4-8-членне насичене кільце, що містить 1-3 гетероатоми, вибрані з нітрогену, оксигену та сульфуру, та, як варіант, заміщене С1-6алкілом, С1-6алкіл-ОН або гідроксилом, а
R16 представляє 4-8-членне насичене кільце, що містить 1-3 гетероатоми, вибрані з нітрогену, оксигену або сульфуру, та, як варіант, заміщене 1-3 групами, вибраними з гідроксилу, ціаногрупи, галогену та =O,
16. Спосіб за п. 15, в якому рецептор хемокіну належить до підродини рецепторів хемокіну CCR.
17. Спосіб за п. 15 або 16, в якому рецептор хемокіну представляє рецептор CCR4.
18. Спосіб лікування запальної хвороби у пацієнта, що страждає на вказану хворобу або при наявності її ризику, який полягає у введенні пацієнту терапевтично ефективної кількості сполуки формули (IВ) або її фармацевтичнo прийнятної солі або сольвату за п. 15.
19. Спосіб за п. 15, де хворобою є астма.
Текст
1. Сполука формули (І) або її фармацевтичнo прийнятна сіль або сольват: O S R3 N R6 N R5 (13) O N R2 H R4 , в якій: R1, R2 та R3 незалежно представляють гідроген, галоген, ціаногрупу, CF3, ОСF 3, ОС1-6алкіл або С 16алкіл, R4 представляє галоген, CO2R12, С1-6алкоксил, де алкіл може утворювати 3-6членне насичене кільце або може бути заміщеним 1-3 атомами флуору або ціаногрупою; UA R1 (19) (21) 20040705311 (22) 14.01.2003 (24) 11.06.2007 (86) PCT/SE03/00041, 14.01.2003 (31) 0200119-6 (32) 16.01.2002 (33) SE (31) 0201857-0 (32) 17.06.2002 (33) SE (46) 11.06.2007, Бюл. № 8, 2007 р. (72) Бакстер Ендрю, GB, Джонсон Тімоті, GB, Кіндон Ніколас, GB, Робертс Брайан, GB, Стокс Майкл, GB (73) АСТРАЗЕНЕКА АБ, SE (56) WO 956957 A1, 12.10.1995 DATABASE CAPLUS 'Online! 'Preparation of Nisoxazolyl biphenylsulfonamides and related compounds as dual angiotensin II and endothelin receptor antagonists', XP002964196 Database accession no. 2000:34745 & WO 00 01389 A1 13 January 2000 GB 2295616 A, 05.06.1996 2 79255 1 (11) (54) N-ПІРАЗИНІЛФ ЕНІЛСУЛЬФОНАМІДИ, СПОСІБ ЇХ ОД ЕРЖАННЯ (ВАРІАНТИ), ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ НА ЇХ ОСНОВІ, СПОСІБ ЇЇ ОДЕРЖАННЯ, СПОСІБ ЛІКУВАННЯ ОПОСЕРЕДКОВАНОЇ ХЕМОКІНОМ ХВОРОБИ, СПОСІБ ЛІКУВАННЯ З АПАЛЬНОЇ ХВОРОБИ C2 ДО ПАТЕНТУ НА винахід 3 79255 4 С3-6алкенілоксил або С 3-6алкінілоксил, де кожний з R2 або R3 представляє С 1-6алкіл або С 1-6алкоксил них може бути, як варіант, заміщений гідроксилом та є розташованим у мета-положенні відносно чи NR14R15; сульфонамідної групи, тоді група, розташована у ОС1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утворюорто-положенні відносно як сульфонамідної групи, вати 3-6-членне насичене кільце; так і С 1-6алкілу або С1-6алкоксилу, не є гідрогеном, ОС1-6алкілR11 або OС2-6алкіл-Х-R11, де алкіл може коли R4 представляє галоген або С1-4алкоксил, а утворювати 3-6-членне насичене кільце та є, як R5 представляє гідроген, галоген, С1-4алкіл, С1варіант, заміщеним 1-3 групами, вибраними з гід2алкоксил, С 1-2алкілтіогрупу, трифлуорметил або роксилу, галогену, NR14R15, SR13, S(O) 2R13 , S(O)R13 етиніл, та, коли один з R1, R2 або R3 представляє або COR13; С1-6алкіл або С1-6алкоксил та є розташованим у ОС1-6алкілR16; орто-положенні відносно сульфонамідної групи, R5 та R6 незалежно представляють гідроген, ціанотоді група, що є розташованою у орто-положенні груп у, галоген, CO2R12 , CONR14R15; відносно С1-6алкілу або С 1-6алкоксилу, а також меС1-6алкіл, як варіант, заміщений гідроксилом, та-положенні відносно сульфонамідної групи, не NR14R15 або 1-3 атомами флуор у; представляє гідроген, С1-6алкілR11, XCH(R11)С1-6алкіл або ХCH(R16)С1коли два з R1, R2, R3 представляють гідроген, а інший представляє метил, що розташований у 6алкіл, де алкіл може бути, як варіант, заміщений 1-3 групами, вибраними з гідроксилу та NR14R15 ; пара-положенні відносно сульфонаміду, а R4 14 15 11 11 14 15 NR R ; N(R )R ; X-(CH2)qNR R ; представляє метоксил, тоді R5 не представляє (CH2)nNR14R15; NHC(O)С1-6алкіл, як варіант, замігідроген або бром, щений одною або більше гідроксигрупами, коли R5 представляє метил, R6 представляє метоС3-6алкініл або С 3-6алкеніл, як варіант, розгалужені ксил, а один з R1, R2 або R3 представляє бром або та, як варіант, заміщені 1-3 групами, вибраними з йод, а інші два обидва є гідрогенами, тоді бром гідроксилу, ціаногрупи, галогену та =O; або йод не розташовані у орто-положенні відносно R11; X-R11 ; X-R 12; Х-С1-6алкілR16; X-R16 ; Xсульфонамідної групи, та (CH2)nCO2R12; X-(CH2)nCONR14R15 ; X-(CH2)nR11; Xколи R5 представляє метил, а R4 представляє ме12 12 11 (CH2)nCN; X-(CH2)qOR ; (CH2)nOR ; (CH2)n-X-R ; токсил, і один R1, R2 або R3 представляє бром або 12 12 X-(CH2)qNHC(O)NHR ; X-(CH2)qNHC(O)R ; Xйод, а інші два обидва є гідрогенами, тоді бром (CH2)qNHS(O)2R12; X-(CH2)qNHS(O)2R11; Х-С3або йод не розташовані у орто-положенні відносно сульфонамідної групи. 6алкеніл; Х-С 3-6алкініл; n дорівнює 1, 2, 3, 4 або 5; 2. Сполука за п.1, в якій один з R1, R2 та R3 предq дорівнює 2, 3, 4, 5 або 6; ставляє гідроген, а інший представляє хлор, бром X представляє NR13, O, S, S(O), S(O)2; або метил. R11 представляє арил або 5-7-членне гетероаро3. Сполука за пп.1 або 2, в якій R1 та R2 представматичне кільце, що містить 1-4 гетероатоми, вибляють хлор у 2- та 3-положеннях фенольного кільрані з нітрогену, оксигену або сульфур у, кожний з ця, а R3 представляє гідроген, або R1 та R3 предних може бути, як варіант, заміщеним 1-3 групами, ставляють хлор у 2- та 4- положеннях фенольного вибраними з галогену, C(O)NR14R15, C(O)OR 12, кільця, а R2 представляє гідроген, або R1 предстагідроксилу, =O, =S, CN, NO 2, COR13, NR14R 15, вляє хлор у 2-положенні, а R2 представляє метил у 14 5 2 14 15 13 X(CH2)qNR R , (CH )nNR R , (СH2)nOH, SR , 3-положенні фенольного кільця, і R3 представляє 13 13 S(O)R , S(O)2R , С1- 6алкіл-Х-С 1-6алкіл, С1-6алкіл гідроген. або С1-6алкоксил, де алкіл може утворювати 3-64. Сполука за будь-яким з пп.1-3, в якій R 4 предчленне кільце або є, як варіант, заміщеним 1-3 ставляє С 1-6алкоксил, як-то метоксил, 2групами, вибраними з гідроксилу, галогену, фуранілметоксил, бром, хлор, 2-метоксіетоксил, NR14R15, SR 13, S(O)R13, S(O)2R13; (5-метил-3-ізоксазоліл)метоксил, піридилметоксил, R12 та R13 незалежно представляють гідроген або 3-піридазинілметоксил, метоксил, 2-(1С1-6алкіл, де алкіл може бути заміщеним 1-3 атоми імідазоліл)етоксил, (2-метил-4-оксазоліл)метоксил флуору або може утворювати 3-6-членне насичета 4-метоксифенілметоксил. не кільце; 5. Сполука за будь-яким з пп.1-4, в якій R 4 пред14 15 R та R незалежно представляють гідроген, С1ставляє метоксил. 6. Сполука за будь-яким з пп.1-5, в якій R 5 пред6алкіл, С 3-6циклоалкіл або (CH 2)qOH, 14 15 або R та R разом з атомом нітрогену, до якого ставляє гідроген, галоген, як-то бром та хлор, февони приєднані, утворюють 4-8-членне насичене ніл, С1-6алкіл, як-то метил, СН2ОН, ціаногрупу та 2кільце, що містить 1-3 гетероатоми, вибрані з нітаміноетантіол. рогену, оксигену та сульфур у, та, як варіант, замі7. Сполука за будь-яким з пп.1-6, в якій R6 предщене С1-6алкілом, С1-6алкіл-ОН або гідроксилом; а ставляє гідроген, С1-6алкіл, СН2ОН та галоген. R16 представляє 4-8-членне насичене кільце, що 8. Сполука за п.1, якою є: містить 1-3 гетероатоми, вибраними з нітрогену, 2,3-дихлор-N-(3-метокси-5-метил-2-піразиніл)оксигену або сульфур у, та, як варіант, заміщене 1бензолсульфонамід, 3 групами, вибраними з гідроксилу, ціаногрупи, N-(6-хлор-3-метокси-2-піразиніл)-2,3,4галогену та =O, трифлуорбензолсульфонамід, за умови, що 3-хлор-N-(6-хлор-3-метокси-2-піразиніл)-2коли R4 представляє галоген або С1-4алкоксил, а метилбензолсульфонамід, R5 представляє гідроген, галоген, С1-4алкіл, С12,3-дихлор-N-(6-хлор-3-метокси-2піразиніл)бензолсульфонамід, 2алкоксил, С 1-2алкілтіогрупу, трифлуорметил або етиніл, та, коли один з R1, 5 79255 6 2,3-дихлор-N-(5Н-хлор-3-метокси-22-хлор-N-(6-хлор-3-метокси-2піразиніл)бензолсульфонамід, піразиніл)бензолсульфонамід, N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-2,54-хлор-N-(6-хлор-3-метокси-2диxлopбeнзoлcyльфoнaмiд, піразиніл)бензолсульфонамід, N-(5-бром-3-метокси-2-піразиніл)-3,5N-(6-хлop-3-мeтoкcи-2-пipaзинiл)-2,4дихлорбензолсульфонамід, диxлopбeнзoлcyльфoнaмiд, N-(5-бром-3-метокси-2-піразиніл)-2,3N-(6-хлop-3-мeтoкcи-2-пipaзинiл)-3,4дихлорбензолсульфонамід, диxлopбeнзoлcyльфoнaмiд, N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-2,43-хлор-N-(3-метокси-5-метил-2-піразиніл)-2диxлopбeнзoлcyльфoнaмiд, метилбензолсульфонамід, N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-3,42-хлор-N-(3-метокси-5-метил-2диxлopбeнзoлcyльфoнaмiд, піразиніл)бензолсульфонамід, N-(5-бpoм-3-мeтoкcи-2-пipaзинiл)-43-хлор-N-(3-метокси-5-метил-2xлopбeнзoлcyльфoнaмiд, піразиніл)бензолсульфонамід, N-(5-бром-3-метокси-2-піразиніл)-34-хлop-N-(3-мeтoкcи-5-мeтил-2хлорбензолсульфонамід, пipaзинiл)бeнзoлcyльфoнaмiд, N-(3-метокси-5-метил-2-піразиніл)-22,4-диxлop-N-(3-мeтoкcи-5-мeтил-2флуорбензолсульфонамід, пipaзинiл)бeнзoлcyльфoнaмiд, N-(3-мeтoкcи-5-мeтил-23,4-диxлop-N-(3-мeтoкcи-5-мeтил-2пipaзинiл)бeнзoлcyльфoнaмiд, пipaзинiл)бeнзoлcyльфoнaмiд, N-(3-метокси-5-метил-2-піразиніл)-3N-(5-бром-3-метокси-2-піразиніл)-2флуорбензолсульфонамід, трифлуорметоксибензолсульфонамід, 2-[[(3-метокси-5-метил-23-хлор-N-(5-хлор-3-метокси-2-піразиніл)-2піразиніл)аміно]сульфоніл]бензонітрил, метилбензолсульфонамід, N-(5-бром-3-метокси-22-хлор-N-(5-хлор-3-метокси-2піразиніл)бензолсульфонамід, піразиніл)бензолсульфонамід, N-(5-бром-3-метокси-2-піразиніл)23-хлор-N-(5-хлор-3-метокси-2йодбензолсульфонамід, піразиніл)бензолсульфонамід, 2,3-диxлop-N-[3-(2-фypaнiлмeтoкcи)-5-мeтил-24-хлор-N-(5-хлор-3-метокси-2пipaзинiл]бeнзoлcyльфoнaмiд, піразиніл)бензолсульфонамід, 2,3-дихлор-N-[5-метил-3-(5-метил-3N-(5-хлор-3-метокси-2-піразиніл)-2,4ізоксазолілметокси)-2дихлорбензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[3-метокси-5-(4-морфолініл)-22,3-дихлор-N-[5-метил-3-(2-піридинілметокси)-2піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[3,5-диметокси-22,3-дихлор-N-[5-метил-3-(6-метил-2піразиніл]бензолсульфонамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлор-N-[3-метокси-5-(1-піролініл)-22,3-дихлор-N-[5-метил-3-(3-піридинілметокси)-2піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, 3-хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)-22,3-дихлор-N-[5-метил-3-(4-піридинілметокси)-2метилбензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-(5,6-дихлор-3-метокси-22,3-дихлор-N-[5-метил-3-(3-метил-2піразиніл)бензолсульфонамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2-хлор-N-(5,6-дихлор-3-метокси-22,3-дихлор-N-[5-метил-3-(3-піридазинілметокси)-2піразиніл)бензолсульфонамід, піразиніл]бензолсульфонамід, 3-хлор-N-(5,6-дихлор-3-метокси-22,3-дихлор-N-[3-(2-піридинілметокси)-2піразиніл)бензолсульфонамід, піразиніл]бензолсульфонамід, 4-хлор-N-(5,6-дихлор-3-метокси-22,3-дихлор-N-[3-(3-піридинілметокси)-2піразиніл)бензолсульфонамід, піразиніл]бензолсульфонамід, 2,4-дихлор-N-(5,6-дихлор-3-метокси-22,3-дихлор-N-(3-метокси-2піразиніл)бензолсульфонамід, піразиніл)бензолсульфонамід, 3,4-диxлop-N-(5,6-диxлop-3-мeтoкcи-2N-[5-бром-3-(2-піразинілметокси)-2-піразиніл]-2,3пipaзинiл)бeнзoлcyльфoнaмiд, дихлорбензолсульфонамід, 2,3-дихлор-N-(3-метокси-5,6-диметил-2N-[5-бром-3-(1-метил-6-оксо-1,6-дигідро-3піразиніл)бензолсульфонамід, піридинілметокси)-2-піразиніл]-2,32,3-дихлор-N-(6-хлор-3,5-диметокси-2дихлорбензолсульфонамід, піразиніл)бензолсульфонамід, N-[5-бpoм-3-(3-пipидaзинiлмeтoкcи)-2-пipaзинiл]2,3-дихлор-N-[6-хлор-3-метокси-5-(4-морфолініл)2,3-диxлopбeнзoлcyльфoнaмiд, 2-піразиніл]бензолсульфонамід, N-[5-бpoм-3-(3-пipидинiлмeтoкcи)-2-пipaзинiл]-2,32,3-дихлор-N-[6-хлор-5-(2-гідроксіетиламіно)-3дихлорбензолсульфонамід, метокси-2-піразиніл]бензолсульфонамід, N-[5-бром-3-(5-піримідинілметокси)-2-піразиніл]2,3-дихлор-N-[6-хлор-5-диметиламіно-3-метокси-22,3-дихлорбензолсульфонамід, піразиніл]бензолсульфонамід, N-[5-хлор-3-(3-піридинілметокси)-2-піразиніл]-2,32,3-дихлор-N-[6-хлор-3-метокси-5-(2дихлорбензолсульфонамід, метоксіетокси)-2-піразиніл]бензолсульфонамід, N-[5-хлop-3-(5-пipимiдинілмeтoкcи)-2-пipaзинiл]2,3-дихлор-N-[6-хлор-5-гідрокси-3-метокси-22,3-диxлopбeнзoлcyльфoнaмiд, піразиніл]бензолсульфонамід, 7 79255 8 2,3-дихлор-N-[6-метокси-5N-[3-(3-бромфенілметокси)-5-хлор-2-піразиніл]-2,3([2,2']біпіразиніл)]бензолсульфонамід, дихлорбензолсульфонамід, 4-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси3-[6-хлор-3-(2,3-дихлорбензолсульфоніламіно)-22-піразинілокси]бензойна кислота, піразинілоксиметил]бензойної кислоти метиловий 2,3-дихлор-N-(3,5-дихлор-2естер, піразиніл)бензолсульфонамід, 3-[6-хлор-3-(2,3-дихлорбензолсульфоніламіно)-22,3-дихлор-N-{6-хлор-3-метокси-5-[(2піразинілоксиметил]бензойна кислота, метоксіетил)аміно]-22,3-дихлор-N-[5-хлор-3-(3піразиніл}бензолсульфонамід, гідроксиметилфенілметокси)-2N-{2-[3-хлор-5-(2,3-дихлорбензолсульфоніламіно)піразиніл]бензолсульфонамід, 6-метокси-2-піразиніламіно]етил}ацетамід, 2,3-дихлор-N-[5-хлор-3-(32,3-дихлор-N-[5-(4-гідроксиметил-1-піперидиніл)-3метиламінометилфенілметокси)-2метокси-2-піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-ціано-3-(3-піридинілметокси-22,3-дихлор-N-[5-хлор-3-{3-([2піразиніл]бензолсульфонамід, гідроксіетиламіно]метил)фенілметокси}-22,3-диxлop-N-(6-xлop-3-мeтoкcи-5-мeтилaмiнo-2піразиніл]бензолсульфонамід, пipaзинiл)бeнзoлcyльфoнaмiд, 2,3-дихлор-N-[5-хлор-3-(42,3-дихлор-N-(3-метокси-5-метилсульфаніл-2гідроксиметилфенілметокси)-2піразиніл)бензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-(2,4-дифлуорфеніл)-3-метокси-22,3-диxлop-N-[5-xлop-3-{4-([2піразиніл]бензолсульфонамід, гiдpoкcieтилaмiнo]мeтил)фeнiлмeтoкcи}-2[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-2піразиніл]бензолсульфонамід, піразинілсульфаніл]оцтової кислоти 2,3-дихлор-N-[3-(4-гідроксиметилфенілметокси)-2метиловий естер, піразиніл]бензолсульфонамід, [5-(2,3-дихлорбензолсульфоніламіно)-6-метокси-22,3-диxлop-N-[5-xлop-3-(2піразинілсульфаніл]оцтова кислота, гiдpoкcимeтилфeнiлмeтoкcи)-22,3-дихлор-N-[5-(2-хлорбензилсульфаніл)-3пipaзинiл]бeнзoлcyльфoнaмiд, метокси-2-піразиніл]бензолсульфонамід, 5-(2,3-дихлорбензолсульфоніламіно)-62,3-дихлор-N-[6-хлор-5-(3-гідроксі-1-азетидиніл)-3метоксипіразин-2-карбонової кислоти метиловий метокси-2естер, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-(1-гідрокси-1-метилетил)-32,3-дихлор-N-[5-метил-3-(1-окси-3метокси-2-піразиніл]бензолсульфонамід, піразинілметокси)-2-піразиніл]бензолсульфонамід, N-[5-(2-амiнoeтoкcи)-3-мeтoкcи-2-пipaзинiл]-2,32,3-дихлор-N-[5-хлор-3-(4-піридинілметокси)-2диxлopбeнзoлcyльфoнaмiд, піразиніл]бензолсульфонамід, N-{5-[(2-аміноетил)тіо]-6-хлор-3-метокси-22,3-дихлор-N-[5-хлор-3-(1-окси-4піразиніл}-2,3-дихлорбензолсульфонамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 3-[(5-{[(2,3-дихлорфеніл)сульфоніл]аміно}-62,3-дихлор-N-[5-хлор-3-(2-піридинілметокси)-2метокси-2-піразиніл)тіо]пропанової кислоти піразиніл]бензолсульфонамід, метиловий естер, 2,3-дихлор-N-[5-хлор-3-(2-метилсульфанілетокси)2,3-дихлор-N-[5-бром-3-метокси-6-метил-22-піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, N-(3-бутокси-5-хлор-2-піразиніл)-2,35-(2,3-дихлорбензолсульфоніламіно)-6-метокси-3дихлорбензолсульфонамід, метилпіразин-2-карбонової кислоти метиловий 2,3-дихлор-N-[5-хлор-3-(2-метил-3естер, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-(гідроксиметил)-3-метокси-62,3-дихлор-N-[5-хлор-3-(6-метил-2метил-2-піразиніл]бензолсульфонамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5,6-дихлор-3-(3-піридинілметокси)-22,3-диxлop-N-[5-xлop-3-(1-oкcи-2піразиніл]бензолсульфонамід, пipидинiлмeтoкcи)-2-пipaзинiл]бензолсульфонамід, 3-хлор-N-(5-хлор-3-метокси-2-піразиніл)-23-хлор-N-[5-хлор-3-(3-піридинілметокси)-2флуорбензолсульфонамід, піразиніл]-2-метилбензолсульфонамід, 3-хлор-2-флуор-N-[3-(3-піридинілметокси)-23-хлор-N-[5-хлор-3-(3-піридинілметокси)-2піразиніл]бензолсульфонамід, піразиніл]-2-флуорбензолсульфонамід, 3-{[(2,3-дихлорфеніл)сульфоніл]аміно}піразин-22,3-дихлор-N-[5-хлор-3-(4-метоксифенілметокси)карбонової кислоти метиловий естер, 2-піразиніл]бензолсульфонамід, N-(5-бром-6-хлор-3-метокси-2-піразиніл)-2,3N-[5-бром-6-хлор-2-піразиніл]-2,3дихлорбензолсульфонамід, дихлорбензолсульфонамід, 3-хлор-5-{[(2,3-дихлорфеніл)сульфоніл]аміно}-62,3-дихлор-N-[6-хлор-3-(3-піридинілметокси)-2метоксипіразин-2-карбонової кислоти піразиніл]бензолсульфонамід, метиловий естер, 2,3-дихлор-N-[6-хлор-3-(2-піридинілметокси)-22,3-дихлор-N-[6-хлор-5-(гідроксиметил)-3піразиніл]бензолсульфонамід, метоксипіразин-2-іл]бензолсульфонамід, N-[5-(2-аміноетилсульфаніл)-3-(22,3-дихлор-N-{3-[(6-метокси-3-піридиніл)метокси]піридинілметокси-2-піразиніл)-2,32-піразиніл}бензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[6-хлор-3-метокси-5-(метоксиметил)2,3-дихлор-N-[5-хлор-3-(6-метокси-32-піразиніл]бензолсульфонамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 9 79255 10 2-хлор-N-(5-хлор-3-метокси-2N-[5-бром-3-[3-(4-гідроксифеніл)пропокси]-2піразиніл]трифлуорбензолсульфонамід, піразиніл]-2,3-дихлорбензолсульфонамід, 2-хлор-3-флуор-N-(3-метокси-2N-[5-бром-3-(2-феноксіетокси)-2-піразиніл]-2,3піразиніл)бензолсульфонамід, дихлорбензолсульфонамід, 2-хлор-3-метокси-N-(3-метокси-2N-[5-бром-3-(циклопропілметокси)-2-піразиніл]-2,3піразиніл)бензолсульфонамід, дихлорбензолсульфонамід, N-[5-бром-3-[(2S)-2-піролідинілметокси]-2N-[5-бром-3-(3-феноксипропокси)-2-піразиніл]-2,3піразиніл]-2,3-дихлорбензолсульфонамід, дихлорбензолсульфонамід, 5-(2,3-дихлорбензолсульфоніламіно)-6-(32,3-дихлор-N-(5-етокси-3-метокси-2піридинілметокси)піразин-2-карбонової кислоти піразиніл)бензолсульфонамід, метиловий естер, 2,3-дихлор-N-[3-метокси-5-([1,2,4]-1-триазоліл)-25-{[(2,3-дихлорфеніл)сульфоніл]аміно}-6-(3піразиніл]бензолсульфонамід, піридинілметокси)-2-піразинкарбоксамід, 2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси2,3-дихлор-N-[5-(4-піридиніл)-3-(32-піразинілсульфаніл]-N-метилацетамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси2,3-дихлор-N-[5-(гідроксиметил)-3-(32-піразинілсульфаніл]ацетамід, піридинілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-(4-флуорбензилсульфаніл)-32,3-дихлор-N-[5-(гідроксиметил)-3-метокси-2метокси-2-піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-дихлор-N-[5-ціанометилсульфаніл-3-метоксиN-(5-алілокси-3-метокси-2-піразиніл)-2,32-піразиніл]бензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[3-метокси-5-([1,2,4]-32,3-дихлор-N-[5-(3-гідрокси-1-пропініл)-3-метоксиоксадіазолілметилсульфаніл)-22-піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, N-{3-[(5-бром-3-піридиніл)метокси]-5-хлор-2N-[5-(2-амiнoeтилcyльфaнiл)-3-мeтoкcи-2піразиніл}-2,3-дихлорбензолсульфонамід, пipaзинiл]-2,3-диxлopбeнзoлcyльфoнaмід, 2,3-дихлор-N-[5-хлор-3-{[6-(гідроксиметил)-22,3-дихлор-N-[3-метокси-5-(5-метил-3піридиніл]метокси}-2ізоксазолілметокси)-2піразиніл]бензолсульфонамід, піразиніл]бензолсульфонамід, 2,3-диxлop-N-{5-xлop-3-[(2-мeтил-42,3-дихлор-N-[5-(5-диметиламінометил-2oкcaзoлiл)мeтoкcи]-2фуранілметокси)-3-метокси-2пipaзинiл]бeнзoлcyльфoнaмiд, піразиніл]бензолсульфонамід, 2,3-дихлор-N-{3-[(2-метил-4-оксазоліл)метокси]-2N-[5-бром-3-(5-диметиламінометил-2піразиніл}бензолсульфонамід, фуранілметокси)-2-піразиніл]-2,3N-[5-бром-3-(фенілметокси)-2-піразиніл)-2,3дихлорбензолсульфонамід, дихлорбензолсульфонамід, 2,3-диxлop-N-[5-(2-гiдpoкcieтилcyльфaнiл)-3N-[5-бpoм-3-(2-циклoпpoпiлeтoкcи)пipaзинiл]-2,3мeтoкcи-2-пipaзинiл]бeнзoлcyльфoнaмiд, диxлopбeнзoлcyльфoнaмiд, 2,3-дихлор-N-[5-[2-(етилуреїдо)етилсульфаніл]-3N-[5-бром-3-(3-тієнілметокси)піразиніл]-2,3метокси-2-піразиніл]бензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[3-(5-диметиламінометил-2N-{5-бром-3-[(2-метил-3-фураніл)метокси]-2фуранілметокси)-2-піразиніл]бензолсульфонамід, піразиніл}-2,3-дихлорбензолсульфонамід, 2,3-дихлор-N-[6-хлор-3-(5-диметиламінометил-2N-{5-бром-3-[(3-фураніл)метокси]-2-піразиніл}-2,3фуранілметокси)-2-піразиніл]бензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[6-Дихлор-3-(5-метиламінометил-2N-{5-бром-3-[(4-флуорфеніл)метокси]-2-піразиніл}фуранілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлорбензолсульфонамід, 2,3-дихлор-N-[5-хлор-3-(5-диметиламінометил-2N-{5-бpoм-3-[(3-флyopфeнiл)мeтoкcи]-2-пipaзинiл}фуранілметокси)-2-піразиніл]бензолсульфонамід, 2,3-диxлopбeнзoлcyльфoнaмiд, 2,3-дихлор-N-[3-(5-метиламінометил-2N-{5-бром-3-[3-(2-піридиніл)пропокси]-2-піразиніл}фуранілметокси)-2-піразиніл]бензолсульфонамід, 2,3-дихлорбензолсульфонамід, N-(5-бром-3-метоксипіразиніл)-2N-[5-бром-3-(пентилокси)-2-піразиніл]-2,3ціанобензолсульфонамід, дихлорбензолсульфонамід, N-(5-бром-3-метоксипіразиніл)-2,3-дихлор-4N-[5-бpoм-3-(пpoпiлoкcи)-2-пipaзинiл]-2,3флуорбензолсульфонамід, диxлopбeнзoлcyльфoнaмiд, 2,3-диxлop-N-[3-мeтoкcи-5-(4-мopфoлiнiлмeтил)-2N-[5-бром-3-(2-метоксіетокси)-2-піразиніл]-2,3пipaзинiл]бeнзoлcyльфoнaмiд, дихлорбензолсульфонамід, N-(3-алілокси-5-хлор-2-піразиніл)-2,3N-[5-бром-3-(2-етоксіетокси)-2-піразиніл]-2,3дихлорбензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[5-хлор-3-(2-пропінілокси)-2N-[5-бром-3-(2-флуоретокси-2-піразиніл]-2,3піразиніл]бензолсульфонамід, дихлорбензолсульфонамід, 2,3-дихлор-N-[3-(2-пропінілокси)-2N-{5-бром-3-[2-(1Н-імідазол-1-іл)етокси]-2піразиніл]бензолсульфонамід, піразиніл}-2,3-дихлорбензолсульфонамід, 2,3-дихлор-N-(5-ціано-3-метокси-2N-{5-бpoм-3-[3-(3-пipидинiл)пpoпoкcи]-2-піpaзинiл}піразиніл)бензолсульфонамід, 2,3-диxлopбeнзoлcyльфoнaмiд, 2,3-дихлор-N-{3-метокси-5-[(2S)-піролідин-2N-[5-бром-3-[2-(метиламіно)етокси]-2-піразиніл]ілметокси]-2-піразиніл}бензолсульфонаміду 2,3-дихлорбензолсульфонамід, гідрохлорид, 11 79255 12 2,3-дихлор-N-{6-хлор-3-метокси-5-[(2R)-2утворення фармацевтично прийнятної солі. піролідинілметокси]-210. Спосіб отримання сполуки (І), що визначена в піразиніл]бензолсульфонаміду гідрохлорид, п.1, який включає: 2,3-дихлор-N-[3-метокси-5-(2-піридинілметокси)-2для сполук, в яких R4 представляє С 1-6алкоксил, піразиніл]бензолсульфонаміду гідрохлорид, де алкіл може утворювати 3-6-членне насичене 2,3-дихлор-N-(3-метокси-6-метил-2кільце або може бути заміщеним 1-3 атоми флуопіразиніл)бензолсульфонамід, ру або ціаногрупою; 2,3-дихлор-N-[3-метокси-5-(1Н-1,2,4-триазол-1С3-6алкенілоксил або С 3-6алкінілоксил, причому ілметил)-2-піразиніл]бензолсульфонамід, кожний з них може бути, як варіант, заміщеним N-(3-(5-амінометил-2-фуранілметокси)-5-хлор-2гідроксилом чи NR14R15; піразиніл)-2,3-дихлорбензолсульфонамід, ОС1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утворюN-(3-(5-амінометил-2-фуранілметокси)-2вати 3-6-членне насичене кільце; піразиніл)-2,3-дихлорбензолсульфонамід, ОС1-6алкілR11 або ОС2-6алкіл-X-R11, де алкіл може 2,3-дихлор-N-[3-метокси-5-(2-пропін-1-ілокси)-2утворювати 3-6-членне насичене кільце та є, як піразиніл]бензолсульфонамід, варіант, заміщеним 1-3 групами, вибраними з гід{[5-(2,3-дихлорфенілсульфоніламіно)-6-метокси-2роксилу, галогену, NR14R15, SR 13, S(O)2R 13, піразиніл]оксі}оцтової кислоти метиловий естер, S(O)R13; або ОС 1-6алкіл-R16; N-[5-(2,3-диxлopфeнiлcyльфoнiлaмiнo)-6-мeтoкcиобробку сполуки формули (VI), де LG представляє 2-пipaзинiл]-2-гiдpoкciaцeтaмiд, відщеплювану груп у: R5 6-(2,3-дихлорфенілсульфоніламіно)-5-метокси-2N LG піразинілкарбонової кислоти метиловий естер, 2,3-дихлор-N-[6-(гідроксиметил)-3-метокси-2R6 N NH піразиніл]бензолсульфонамід, 2,3-дихлор-N-(5-метансульфоніл-3-метокси-2S O O піразиніл)бензолсульфонамід, R1 2-[5-(2,3-дихлорбензолсульфоніламіно)-6-метокси, (VI) R3 2-піразинілокси]-N,N-діетилацетамід, R2 2,3-дихлор-N-{5-[2-(диметиламіно)етилсульфаніл]сполукою формули (V) R4-Н 3-метокси-2-піразиніл}бензолсульфонамід, у присутності придатної основи, 2,3-дихлор-N-(5-дифлуорметил-3-метокси-2та, як варіант, після цього піразиніл)бензолсульфонамід, видалення будь-яких захисних гр уп, 2,3-дихлор-4-флуор-N-(3-метокси-2перетворення сполуки формули (І) у наступну спопіразиніл)бензолсульфонамід, луку формули (І) або 2,3-дихлор-N-{5-хлор-3-[1-(циклопропіл)етокси]-2утворення фармацевтично прийнятної солі. піразиніл}бензолсульфонамід, 11. Спосіб отримання сполуки (І), що визначена в 2,3-дихлор-N-[5-хлор-3-(5-форміл-2п.1, який включає: фуранілметокси)-2-піразиніл]бензолсульфонамід, для сполук структури (І), де R5 представляє, як 2,3-дихлор-N-[5-хлор-3-(5-циклопропіламінометилваріант, заміщений арил або гетероарил, які ви2-фуранілметокси)-2значено вище, реакцію сполуки формул (VII), де піразиніл]бензолсульфонамід, LG представляє відщеплювану групу, з арил- або N-[5,6-біс-(гідроксиметил)-3-метокси-2-піразиніл]гетероарилбороновою кислотою у присутності па2,3-дихлорбензолсульфонамід, ладієвого каталізатора та придатної основи при N-[3-[(2-аміно-4-оксазоліл)метокси]-5-хлор-2підвищеній температурі: R5 піразиніл]-2,3-дихлорбензолсульфонамід та їх фаN R4 LG N R4 рмацевтично прийнятні солі або сольвати. R6 9. Спосіб отримання сполуки (І), що визначена в N NH R6 NH N п.1, який включає: O S O реакцію сполуки формули (II): S O O R5 N R4 R6 N NH2 , (II) O S R2 O , R3 R3 R2 де R4, R5 та R6 визначені у формулі (І) або є їх захи щеними похідними, із сполукою формули (III): R1 R1 R1 (III) LG де R1, R2 та R3 визначені у формулі (І) або є їх захи щеними похідними, a LG представляє відщеплювану гр уп у, та, як варіант, після цього видалення будь-яких захисних гр уп, перетворення сполуки формули (І) у наступну сполуку формули (І) або (VII) R3 R2 (I ) та, як варіант, після цього видалення будь-яких захисних гр уп, перетворення сполуки формули (І) у наступну сполуку формули (І) або утворення фармацевтично прийнятної солі. 12. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтичнo прийнятну сіль або сольват за п.1 у поєднанні з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. 13. Спосіб отримання фармацевтичної композиції, яка визначена у п.12, який полягає у змішуванні сполуки формули (І) або її фармацевтичнo прийн 13 79255 14 ятної солі або сольвату за п.1 з фармацевтично R11; X-R11; X-R 12; Х- С1-6алкілR16; X-R16; Хприйнятним ад'ювантом, розріджувачем або носі(СН2)nСO2R12; X-(CH2)nCONR14R15 ; Х-(СН2)nR11; Xєм. (CH2)nCN; X-(CH2)qOR 12; (CH2)nOR 12; (CH2)n-X-R 11; 14. Сполука формули (І), що визначена в п.1, або її X-(CH2)qNHC(O)NHR12; X-(CH2)qNHC(O)R 12; Xфармацевтичнo прийнятна сіль або сольват для (CH2)qNHS(O)2R12; X-(CH2)qNHS(O)2R11; Х-С3застосування у терапії. 6алкеніл; Х-С 3-6алкініл; 15. Спосіб лікування опосередкованої хемокіном n дорівнює 1, 2, 3,4 або 5; хвороби, де хемокін зв'язується з одним або більq дорівнює 2, 3, 4, 5 або 6; ше рецепторами хемокінів, який полягає у введенX представляє NR13, О, S, S(O), S(O)2; ні пацієнту терапевтично ефективної кількості споR11 представляє арил або 5-7-членне гетероаролуки формули (IВ) або її фармацевтичнo матичне кільце, що містить 1-4 гетероатоми, вибприйнятної солі або сольвату: рані з нітрогену, оксигену або сульфур у, кожний з R1 O них може бути, як варіант, заміщеним 1-3 групами, вибраними з галогену, C(O)NR14R15, C(O)OR 12, S O 2 гідроксилу, =O, =S, CN, NO2, NR14R 15, R 14 15 14 15 X(CH2)qNR R , (CH2)nNR R , (СH2)nОН, SR 13, N N R6 R3 S(O)R13, S(O)2R 13, H С1-6алкіл-Х-С 1-6алкіл, С1-6алкіл або С1-6алкоксил, де N R5 R4 алкіл може утворювати 3-6-членне кільце або є, як , (IB) варіант, заміщеним 1-3 групами, вибраними з гідв якій: роксилу, галогену, NR14R 15, SR13 , S(O)R 13, R1, R2 тa R3 незалежно представляють гідроген, S(O)2R13 ; галоген, ціаногрупу, CF3 або С 1-6 алкіл; 4 12 R12 та R13 незалежно представляють гідроген або R представляє галоген; CO2R , С1-6алкіл, де алкіл може бути заміщеним 1-3 атоми С1-6алкоксил, де алкіл може утворювати 3-6флуору або може утворювати 3-6-членне насичечленне насичене кільце або може бути заміщеним не кільце; 1-3 атомами флуору або ціаногрупою; R14 та R15 незалежно представляють гідроген, С1С3-6алкенілоксил або С 3-6 алкінілоксил, де кожний з них може бути, як варіант, заміщеним гідроксилом 6алкіл, С 3-6циклоалкіл або (CH 2)qOH, або R14 та R15 разом з атомом нітрогену, до якого чи NR14R15; вони приєднані, утворюють 4-8-членне насичене С1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утворювати кільце, що містить 1-3 гетероатоми, вибрані з ніт3-6-членне насичене кільце; рогену, оксигену та сульфур у, та, як варіант, заміОС1-6алкілR11 або OC2-6алкіл-Х-R11, де алкіл може щене С1-6алкілом, С1-6алкіл-ОН або гідроксилом, а утворювати 3-6-членне насичене кільце та є, як R16 представляє 4-8-членне насичене кільце, що варіант, заміщеним 1-3 групами, вибраними з гід14 15 13 13 містить 1-3 гетероатоми, вибрані з нітрогену, оксироксилу, галогену, NR R , SR , S(O)2R , гену або сульфуру, та , як варіант, заміщене 1-3 S(O)R13; групами, вибраними з гідроксилу, ціаногрупи, галоОС1-6алкілR16, гену та =O, R5 та R6 незалежно представляють гідроген, ціано16. Спосіб за п.15, в якому рецептор хемокіну нагруп у, галоген, CO2R12 , CONR14R15; лежить до підродини рецепторів хемокіну CCR. С1-6алкіл, як варіант, заміщений гідроксилом, 17. Спосіб за п.15 або 16, в якому рецептор хемоNR14R15 або 1-3 атомами флуор у; кіну представляє рецептор CCR4. С1-6алкілR11, ХСH(R11)С1-6алкіл або ХСH(R16)С118. Спосіб лікування запальної хвороби у пацієнта, 6алкіл, де алкіл може бути, як варіант, заміщеним що страждає на вказану хворобу або при наявнос1-3 групами, вибраними з гідроксилу та NR 14R15; ті її ризику, який полягає у введенні пацієнту тераNR14R15; N(R11)R11; X-(CH2)qNR14R15; певтично ефективної кількості сполуки формули (CH2)nNR14R15; (IВ) або її фармацевтичнo прийнятної солі або С3-6алкініл або С 3-6алкеніл, як варіант, розгалужені сольвату за п.15. та, як варіант, заміщені 1-3 групами, вибраними з 19. Спосіб за п.15, де хворобою є астма. гідроксилу, ціаногрупи, галогену та =O; Представлений винахід стосується сульфонамідних сполук, способів та інтермедіатів, застосовуваних при їх отриманні, фармацевтичних композицій, що їх містять та їх застосу вання у терапії. Деякі сульфонамідні сполуки відомі у рівні техніки, наприклад, [дивись GB2295616, патент США 2002143024, WO 01/44239, ЕР 749964 та Esche, J; Wojahn, H. Arch. Pharm. (1966), 299(2), 147-153.]. Хемокіни грають важливу роль у імунній та запальній реакціях при різних хворобах та розладах, включаючи астму та алергічні хвороби, а також автоімунні патології, як-то ревматоїдний артрит та атеросклероз. Ці слабо-секретовані молекули є збільшуваною над-родиною білків розміром 814кДа, що характеризуються збереженими чотирма цистешо-вими функціональними послідовностями. Зараз надродина хемокінів включає три групи, що виявляють характеристичні структурні функціональні послідовності, родини Cys-X-Cys (С-Х-С), C ys-Cys (С-С) та Cys-X3-C ys (С-Х3-С). Родини С-Х-С та С-С мають подібність по слідовності та відрізняються одна від одної на базі одиничної амінокислотної вставки між NH-прокимальною 15 79255 16 парою цистеїнових залишків. Родина С-Х3-С відріNR14R15, або 1-3 атоми флуору; зняється від інших двох родин на базі того, що має С1-6алкілR11 або XCH(R11) С1-6алкіл або потрійну амінокислотну вставк у між NHХСН(R16)С1-6алкіл, де алкіл може бути, як варіант, прокимальною парою цистеїнових залишків. заміщеним 1-3 групами, вибраними з гідроксилу, Хемокіни С-Х-С включають кілька потужних та NR14R15 ; хемоатрактантів та активаторів нейтрофілів, як-то NR14R15; N(R11)R11 ; X-(CH2)qNR14R15 ; 14 15 інтерлейкін-8 (ІІ-8) та активуючий нейтрофіли пеп(CH2)nNR R ; NHC(О)С1-6алкіл, як варіант, замітид 2 (NAP-2). щений одною або більше гідроксигрупами, Хемокіни С-С включають потужні хемоатракС3-6алкініл або С3-6алкеніл, як варіант, розгатанти моноцитів та лімфоцитів, але не нейтрофілужені та, як варіант, заміщені 1-3 група ми, виблів. Приклади включають хемотактичні білки мораними з гідроксилу, ціаногрупи, галогену та=О; ноцитів людини 1-3 (МСР-1, МСР-2 та МСР-3), R11; X-R11; X-R12; Х-С 1-6алкілR16; X-R16; XRANTES (Regulated on Activation, Normal T (CH2)nCO2R12; X-(CH2)nCONR14R15 ; X-(CH2)nR11; XExpressed and Secreted), еотаксин та запальні біл(CH2)nCN; X-(CH2)qOR 12; (CH2)nOR 12; (CH2)n-X-R 11; ки макрофагів 1а та 1(3 (МІР-1а та МТР-1(3), регуX-(CH2)qNHC(O)NHR12; X-(CH2)qNHC(O)R 12; Xльований тимусом та активацією хемокін (TARC, (CH2)qNHS(O)2R12; X-(CH2)qNHS(O)2R11; Х-С3CCL17) та похідний від макрофагів хемокін (MDC, 6алкеніл; Х-С 3-6алкініл; CCL22). n дорівнює 1,2,3,4 або 5; Хемокін С-Х3-С (також відомий як фрактакін) є q дорівнює 2,3,4, 5 або 6; потужним хемоатрактантом та активатором мікроX представляє NR13, О, S, S(O), S(O)2; глії у центральній нервовій системі, а також, ТR11 представляє арил або 5-7-членне гетероклітин, NK-клітин та тучни х клітин. ароматичне кільце, що містить 1-4 гетероатоми, Дослідження продемонстрували, що дія хемовибрані з нітрогену, оксигену або сульфуру, кожкінів опосередкована підродинами сполучених з Gний з яких може бути, як варіант, заміщеним 1-3 білком рецепторів, серед яких є рецептори, познагрупами, вибраними з галогену, C(O)NR14R15, чені як CCR1, CCR2, CCR2A, CCR2B, CCR3, C(O)OR 12, гідроксилу, =O, =S, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10 CN, NO2, COR13 , NR14R15, X(CH2)qNR14R15 , та CCR11 (для родини С-С); CXCR1, CXCR2, (CH2)nNR14R15, (CH2)nOH, SR13, S(O)R13, S(O) 2R13 CXCR3, CXCR4 та CXCR5 (для родини С-Х-С) та С1-6алкіл-Х-С 1-6алкіл, С1-6алкіл або С1-6алкоксил, де CX3CRI для родини С-Х3-С. Ці рецептори предстаалкіл може утворювати 3-6-членне кільце або є, як вляють гарні цілі для розробки ліків, оскільки засоваріант, заміщеним 1-3 групами, вибраними з гідби, які модулюють ці рецептори, могли б бути короксилу, галогену, KR14R15, SR13 , S(O)R13, рисними при лікуванні розладів та хвороб, як-то S(O)2R13 ; вищезазначених. R12 та R13 незалежно представляють гідроген Відтак представлений винахід стосується споабо С1-6алкіл, де алкіл може бути заміщеним 1-3 луки формули (І) та її фармацевтично прийнятних атомами флуору або може утворювати 3-6-членне солей, сольватів або N-оксидів: насичене кільце; R14 та R15 незалежно представляють гідроген, С1-6алкіл, С3-6циклоалкіл або (CH2)qOH, або R14 та R15 разом з атомом нітрогену, до якого вони приєднані, утворюють 4-8-членне насичене кільце, що містить 1-3 гетероатоми, вибрані з нітрогену, оксигену та сульфур у та, як варіант, заміщені С1-6алкілом, С1-6алкіл-ОН, або гідроксив якій: лом; а R1, R2 тa R3 незалежно представляють гідроR16 представляє 4-8-членне насичене кільце, ген, галоген, ціано, CF3, OCF3, ОС1-6алкіл або С 1що містить 1-3 гетероатоми, вибрані з нітрогену, 6алкіл; оксигену або сульфур у та, як варіант, заміщене 1R4 представляє галоген, CO2R12, 3 групами, вибраними з гідроксилу, ціаногрупи, С1-6алкоксил, де алкіл може утворювати 3-6галогену та =0, членне насичене кільце або може бути заміщеним за умови, що: 1-3 атомами флуору або ціаногрупами; - коли R4 представляє галоген або С 15 С3-6алкенілокси або С3-6алкінілоксил, що мо4алкоксил, a R представляє гідроген, галоген, С 1жуть бути, як варіант, заміщеними гідроксилом чи 4алкіл, С 1-2алкоксил, С 1-2алкілтіогрупу, трифлуорNR14R15; метил або етиніл, та коли один з R1, R2 або R3 ОС1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утвопредставляє С 1-6алкіл або С 1-6алкоксил та метарювати 3-6-членне насичене кільце; розташований стосовно суль фонамідної групи, 11 11 ОС1-6алкілR , або ОС 2-6алкіл-X-R , де алкіл тоді група, орто-розташована стосовно як сульфоможе утворювати 3-6-членне насичене кільце та є, намідної групи, так і С1-6алкілу або С 1-6алкоксилу, як варіант, заміщеним 1-3 групами, вибраними з не представляє гідроген, 14 15 13 13 гідроксилу, галогену, NR R , SR , S(O)2R , - коли R4 представляє галоген або С 113 13 5 S(O)R або COR ; 4алкоксил, a R представляє гідроген, галоген, С 1OС1-6алкілR16; 4алкіл, С 1-2алкоксил, С 1-2алкілтіогрупу, трифлуорR5 та R6 незалежно представляють гідроген, метил або етиніл, та коли один з R1, R2 або R3 12 14 15 ціаногрупу, галоген, CO2R , CONR R ; представляє С 1-6алкіл або С1-6алкоксил та ортоС1-6алкіл, як варіант, заміщений гідроксилом, розташований стосовно сульфонамідної групи, 17 79255 18 тодігрупа, орто-розташована стосовно С1-6алкілу як-то метоксил, 2-фуранілметоксил, бром, хлор, 2або С1-6алкоксилу, а також мета-розташована стометоксіетоксил, (5-метил-3-ізоксазоліл)метоксил, совно сульфонамідної групи, не представляє гід2-, 3або 4-піридилметоксил, 3роген, піридазинілметоксил, метоксил, 2-(1- коли два з R1, R2, R3 представляють гідроген, імідазоліл)етоксил, (2-метил-4-оксазоліл)метокси а інший представляє метил, пара-розташований та 4-метоксифенілметоксил. Більш переважно R4 4 стосовно сульфонаміду, a R представляє метокпредставляє метоксил. сил, тоді R5 не представляє гідрогену або брому, Для R5 та R6 приклади NR14R15 включають та морфолін, піролідин, NMe2, NHCH2CH2OMe, - коли R5 представляє метил, R6 представляє NHMe, та нижченаведені групи: метоксил, а один з R1, R2 або R3 пред ставляє бром або йод, а інші два є обидва гідрогеном, тоді бром або йод не є орто-розташованими стосовно сульфонамідної групи. Термін арил включає феніл та нафтил. Термін алкіл, поодинці, або як частина іншої групи, вклюПриклади X-(CH2)qNR14R15 включають чає лінійні та розгалужені алкіли. Приклади 5-7SCH2CH2NH2 та SCH2CH2NMe2, приклади членного гетероароматично-го кільця, що містить 14 15 (CH2)nNR R включають СН 2морфолін, приклади 1-4 гетероатоми, включають тієніл, фураніл, піроX-R12 включають SMe, OMe, OEt, OH, SO2 Me, приліл, імідазоліл, піридил, піразиніл, піримідил, піриклади Х-С 1-6алкілR16 включають ОСН 2піролідин, дазиніл, триазиніл, оксазоліл, тіазоліл, ізоксазоліл, приклади X-(CH2)nCO2R12 включають SCH2CO2H, піразоліл, оксадіазоліл, тіадіазоліл, триазоліл та SCH2CO2Me, SCH2CH2CO2 Me, приклади Xтетразоліл. Приклади насиченого 4-8-членного (CH2)nCONR14R15 включають SCH2CONH2, кільця, що містить 1-3 гетероатоми, включають SCH2CONHMe, OCH2CONEt2, приклади Xморфолін, піперидин та азетидин. Замісники на (CH2)nR11 включають нижченаведєні групи: будь-яких кільцях можуть бути у будь-якій придатній позиції кільця, включаючи придатні замісники на атомах нітрогену. Деякі сполуки формули (І) можуть бути у стереоізомерних формах. Зрозуміло, що ви нахід Приклади X-(CH2)nCN, включають SCH2CN, охоплює усі геометричні та оптичні ізомери сполук приклади X-(CH2)qOR 12 включають ОСН 2СН2ОМе, формули (І) та їх суміші, включа ючи рацемати. приклади (CH2)nOR 12 включають СН 2ОН, СН2ОМе, Таутомери та їх суміші також утворюють аспект приклади X-(CH2)qNHC(O)NHR12 включають представленого винаходу. SCH2CH2NHC(O)NHEt, а приклади XКращими галогенами для R1, R2 та R3 пред(CH2)qNHC(O)R 12 включають ставляють хлор, бром та флуор. Переваж но один NHCH2CH2NHC(O)Me. Приклади МНС(О)С 1з R1, R2 та R3 представляє гідроген, а інший пред6алкілу, як варіант, заміщеного од ною або більше ставляє хлор, бром або метил Більш переважно гідроксигрупами, включають NHCOCH2OH. R1 та R2 представляють хлор у 2- та 3-позиціях Кращі групи для R5 включають гідроген, галофенільного кільця, a R3 представляє гідроген (тобген, як-то бром та хлор, феніл, С1-6алкіл, як-то мето 2,3-дихлорфеніл), R1 та R3 представляють хлор тил, СН2ОН, ціано та 2-амінотанетіол. Більш переу 2- та 4-позиціях фенільного кільця, a R2 предста1 важно R5 представляє гідроген, метил, СН2ОН або вляє гідроген (тобто 2,4-дихлорфеніл), або R 2 галоген, як-то бром або хлор. представляє хлор у 2-позиції та R представляє 3 Кращі групи для R6 включають гідроген, С1метил у 3-позиції фенільного кільця, a R предста6алкіл, СН 2ОН та галоген, більш переважно гідровляє гідроген (тобто 2-хлор-З-метилфеніл). Найген, метил, СН2ОН або хлор. переважніше R1 та R2 представляють хлор у 2- та 3 Наступний аспект винаходу стосується сполу3-позиціях фенільного кільця, a R представляє ки формули (ІА): гідроген (тобто 2,3-дихлорфеніл). Наступний аспект винаходу стосується сполук формули (І), які визначено вище, але без умов, де R1 та R2 представляють хлор у 2- та 3-позиціях фенільного кільця, a R3 пред ставляє гідроген (тобто 2,3-дихлорфеніл), R1 та R3 представляють хлор у 2- та 4-позиціях фенільного кільця, a R2 представляє гідроген (тобто 2,4-дихлорфеніл), або R1 представляє хлор у 2-позиції, R2 представляє метил у 3-позиції фенільного кільця, a R 3 представляє гідроген (тобто 2-хлор-3-метилфеніл). Для групи R4 приклади С1-6алкенілоксилу включають ОСН 2СН СН2, = приклади С 36алкінілоксилу включають ОСН 2ССН, приклади ОС1-6алкіл-О-С1-6алкіл включають ОСН 2СН2ОМе, приклади ОС 1-6алкілR11 включають OCH2R11, а приклади ОС 1-6алкілR16 включають ОСН 2піролідин. Кращі групи для R4 включають С 1-6алкоксил, в якій R1, R2 тa R3 незалежно представляють гідроген, галоген, ціаногрупу, CF3, OCF3, OС 1-6алкіл або С1-6алкіл; R4 представляє галоген, С1-6алкоксил, або OR9; R5 та R6 незалежно представляють гідроген, С1-6алкоксил, С1-6алкілтіогрупу, ціаногру пу, R9, OR9, NR9R10, SR9 , S(CH2)nCO2H, S(CH2)nCO2R12, S(CH2)nCONR12R13, S(CH2)nR11 або 5-7-членне 19 79255 20 гетероароматичне або насичене кільце, щомістить 1-3 гетероатоми, вибрані з нітрогену, оксигену та сульфуру; n дорівнює 1, 2 або 3; R9 та R10 незалежно представляють гідроген, (ІІІ) С1-6алкіл, як варіант, заміщений гідро ксилом, С19 10 де R1, R2 та R3 визначені у формулі (І), є їх зає, як 6алкоксил, або MНСОС 1-6алкіл, або R та R хи щеними похідними, a LG представляє відщепваріант, заміщеним арилом, С1-6алкіл-арилом або лювану гр уп у, та, як варіант, після цього С1-6алкілR11,або R9 та R10 разом з атомом нітроге- видалення будь-якої захисної групи, ну, до якого вони приєднані, утворюють 4-8-членне - утворення фармацевтично прийнятної солі насичене кільце, що містить 1-3 гетероатоми, вибКращі відщеплювані групи LG включають галорані з нітрогену, оксигену та сульфур у, та як варіген, як-то хлор. Переважно реакцію між сполуками ант, заміщене С1-6алкілом або С1-6алкіл-ОН; а (II) та (III) проводять обробкою сполуки (II) основаR11 представляє 5-7-членне гетероароматичне ми, як-то натрій гідрид або калій трет-бутоксид у кільце, що містить 1-3 гетероатоми, з нітрогену, придатному розчиннику, як-то 1,2-диметоксіетан оксигену та сульфур у, та як варіант, заміщене С 1або тетрагідрофуран. 6алкілом, а Де R4 представляє С 1-6алкоксил, де алкіл моR12 тa R13 незалежно представляють гідроген же утворювати 3-6-членне насичене кіль це або або С1-6алкіл. може бути заміщеним 1-3 атомами флуору або Для сполуки (ІА) R1, R2 тa R3 незалежно предціаногрупою; ставляють гідроген, галоген, ціаногрупу, CF3, С3-6алкенілоксил або С 3,6алкінілоксил, де кожOCF3, С1-6алкеніл або С1-6алкіл, кращим галогеном ний з них може бути, як варіант, заміще ним гідроє хлор. Переважно один з R1, R2 тa R3 представксилом чи NR14R15; ляє метил, етеніл, ціаногрупу, хлор, флуор, йод, С1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утвоабо два представляють хлор, або усі три є флуорювати 3-6-членне насичене кільце; ром. Більш кращими є сполуки, де R1, R2 тa R3 ОС1-6алкілR11, або ОС 1-6алкіл-X-R11, де алкіл paзом з фенілом, до якого вони приєднані, утвоможе утворювати 3-6-членне насичене кільце та є, рюють 3-хлор-2-метилфеніл або 2,3-дихлорфеніл. як варіант, заміщеним 1-3 групами, вибраними з Для сполуки (ІА) кращі групи для R4 включагідроксилу, галогену, NR14R15, SR13, S(O)2R 13, ють галоген, як-то бром та хлор, С1-6алкоксил, як9 9 S(O)R13; або то метоксил та етоксил, С1-6алкіл або OR , де R OС1-6алкілR16; представляє CH2R11, де R11 представляє 5- або 6сполуки формули (II) можна отримувати оброчленне гетероароматичне кільце, що містить 1 або бкою сполуки формули (IV), де LG пред ставляє 2 гетероатоми. відщеплювану груп у (як-то хлор або бром): Більш переважно R4 представляє метоксил, галоген, як-то хлор, або OR9, де R9 пред ставляє CH2R11, де R11 представляє фураніл, 5-метил-3ізоксазоліл, піридил, що як варіант, заміщено метилом, піридазиніл, піразиніл, 1-метил-6-оксо-1,6дигідро-3-піридиніл. сполукою формули (V) Для сполуки (ІА) переважно R5 представляє гіR4-H (V) дроген, метил, бром, хлор, метоксил, морфолініл, у придатному розчиннику (як-то 1,2піролініл, диметиламіно, гідроксил, 2метоксіетоксил, піразиніл, піримідиніл, O-Ph-CO2H, диметоксіетан, N,N-диметилформамід або тетра 2-гідроксіетиламіно, 2-метоксіетиламіно, гідрофуран) з придатними основами, як-то натрій гідрид або калій трет-бутоксид при при датній темNHCH2CH2NHCOMe, ціаногрупу, 4-гідроксиметилпературі, як-то 25°С-60°С. 1-піперидиніл, SMe, NH Me, або 2,4-дифлуорфеніл. Де R4 представляє С 1-6алкоксил, де алкіл моДля сполуки (ІА) переважно R6 представляє гідроген або хлор. же утворювати 3-6-членне насичене кільце або Кращі сполуки формули (І)/(ІА) включають може бути заміщеним 1-3 атомами флуору або ціаногрупою; сполуки, представлені як у формі вільної основи, С3-6алкенілоксил або С 3-6алкінілоксил, де кожтак і фармацевтично прийнятної солі. ний з них може бути, як варіант, заміщеним гідроВинахід також стосується способу отримання сполуки (І), який включає реакцію спо луки формуксилом чи NR14R15; С1-6алкіл-Х-С 1-6алкіл, де алкіли можуть утволи (II): рювати 3-6-членне насичене кільце; ОС1-6алкілR11, або ОС 2-6алкіл-Х-Р11, де алкіл може утворювати 3-6-членне насичене кільце та є, як варіант, заміщеним 1-3 групами, вибраними з гідроксилу, галогену, NR14R15, SR13, S(O)2R 13, 4 5 6 S(O)R13; або де R , R та R визначено у формулі (І), або є OС1-6алкілR16; їх за хищеними похідними, із сполукою формули сполуки формули (І) можна отримувати оброб(III): кою сполуки формули (VI), де LG пред ставляє відщеплювану груп у (як-то хлор або бром): 21 79255 22 роарилбороновою кислотою, як-то фенілборонова кислота, паладієвим каталізатором, як-то [1,1'біс(дифенілфосфіно)фероцен]паладію (II) хлорид, придатною основою, як-то цезій флуорид, натрій ацетат або цезій карбонат, та придатним розчинни ком, як-то метанол або етанол та нагріванням при 40-80°С сполукою формули (V) упридатному розчиннику (як-то 1,2диметоксіетан, N,N-диметилформамід або тетрагідрофуран) з придатними основами, як-то натрій гідрид або калій трет-бутоксид при при датній температурі, як-то 25°С-60°С. Сполуки структури (VIII) можна отримувати сполученням сполуки формули (VII), де LG представляє відщеплювану груп у (як-то хлор або бром) та захищеного сульфонаміду, як наприклад триметилсиліетоксиметиловий етер (SEM) або метоксиметиловий етер (MOM) стандартними літературними способами (як-то SEM-хлорид або МОМхлорид) у придатному розчиннику (як-то тетрагідрофуран) з придатними основами (як-то триетиламін) при придатній температурі (як-то 0-20°С), отримуючи сполуку формули (VIII): 9 Сполуку формули (VIII) можна далі обробляти сполуками формули (IX): де R5-H є первинним або вторинним аміном, тіолом або спиртом, які визначено вище (тобто, де R5 є групою, що містить групу X, де X представляє NR13, О або S), у придатному розчиннику (як-то тетрагідрофуран або ацетонітрил) з придатними основами або без них (як-то натрій гідрид, цезій карбонат або триетиламін) при придатній температурі в межах 25-85°С, отримуючи сполуку формули (X): Захисну гр упу (Р) можна далі видалити стандартними способами, отримуючи сполуку формули (І). Сполуки структур (II) або (І), де R5 є, як варіант, заміщеним арилом або гетероарилом, як визначено у формулі винаходу, можна отримувати сполученням сполуки формули (XI) або (VII), де LG є придатною відщеплюваною групою, як-то бром, хлор або йод, та реакцією цього з арил- або гете Сполуки формули (II) та (І), де R5 або R6 представляють CO2R13 можна отримувати реакцією сполук формули (II) або (І), де R5 або R6 представляють бром або йод, у придатному розчиннику, якто R13OH або діоксан, що містить R13OH, придатний третинний амін, як-то триетиламін, придатний паладієвий каталізатор, як-то [1,1'біс(дифенілфосфіно)фероцен]паладій (II) хлорид, в атмосфері монооксиду карбону звичайно при 210 бар, ідеально при 4-6 бар та при температурі 70-120°С. Сполуки формули (II) та (І), де R5 або R6 представляють CONR14R15, можна отримувати реакцією сполуки формули (II) або (І), де R5 або представляють бром або йод, у придатному розчиннику, як-то діоксан, що містить NHR14R15, придатний третинний амін, як-то триетиламін, придатний паладієвий каталізатор, як-то [1,1'біс(дифенілфосфіно)фероцен]паладію (II) хлорид в атмосфері монооксиду карбону звичайно при 210 бар, ідеально при 4-6 бар, та при температурі 70-120°С. Сполуки формули (І), де R5 або R6 представляють СН 2ОН можна отримувати зі сполуки формули (І), де R5 або R6 представляють CO2R13, відновленням, використовуючи придатний відновник, як-то літію триетилборогідрид у придатному розчиннику, як-то тетрагідрофуран, при температурі 0-10°С. Сполуки формули (І), де R5 або R6 представляють СНО, можна отримувати зі сполуки формули (І), де R5 або R6 представляють СН 2ОН окисненням, використовуючи придатний окисник, як-то манган діоксид або піридиній хлорхромат (РСС) у придатному розчиннику, як-то тетрагідрофуран або дихлорметан, при температурі 0-50°С. Сполуки формули (І), де R5 або R6 представляють CH(OH)R11 або СН(ОН)(С1-5)алкіл можна отримувати зі сполуки формули (І), де R5 або R6 представляють СНО, реакцією із сполукою формули (XII), де М представляє метал, як-то магній або літій, у придатному розчиннику, як-то тетрагідрофуран або діетиловий етер при температурі 010°С С1-5алкіл М чи R11 M 23 79255 Сполуку формули (XV) можна отримати реакцією сполуки формули (XIII), де R4 представляє переважно хлор, бром або алкоксил, a LG є придатною відщеплюваною групою, як-то хлор або бром, із сполукою формули (XIV), використовуючи придатні основи, як-то калій карбонат або цезій карбонат у придатному розчиннику, як-то N,Nдиметилформамід при температурі 40-90°С. Інтермедіати формул (II) та (III) можна отримувати стандартними хімічними способами або вони є у продажу. Фахівцям у рівні техніки треба розуміти, що у способах представленого винаходу, де які функціональні групи, як-то гідроксил або аміногрупи у вихідних реагентах або інтерме-діатах можуть потребувати захисту захисними групами. Отже, отримання сполуки формули (І) може включати, на прийнятному етапі, видалення одної або більше захисної групи. Захист та зняття захисту функціональних груп повністю [описано у 'Protective Groups у Organic Chemistry', вид. J. W. F. McOmie, Plenum Press (1973), та 'Protective Groups у Organic Synthesis', 2-ге вид., Т. W. Greene & P. G. M. Wuts, Wiley-lnterscience (1991)]. Вищезазначені сполуки формули (І) можна перетворити у фармацевтично прийнятну сіль або сольват, переважно основно-адитивну сіль, як-то сіль натрію, калію, кальцію, алюмінію, літію, магнію, цинку, бензатину, хлорпрокаїну, холіну, діетаноламіну, етаноламіну, етилдіаміну, меглуміну, трометаміну або прокаїну, або кислотно-адитивну сіль, як-то гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, оксалат, метансульфонат або n-толуолсульфонат. Деякі сполуки формули (II) та (III), можна думати, є новими та утворюють наступний аспект винаходу. Вищезазначені сполуки формули (І) можна перетворити у фармацевтично прийнятні солі або сольвати, переважно основно-адитивні солі, як-то солі натрію, калію, кальцію, алюмінію, літію, магнію, цинку, бензатину, хлорпрокаїну, холіну, діетаноламіну, етаноламіну, етилдіаміну, меглуміну, трометаміну або прокаїну, або кислотно-адитивну сіль, як-то гідрохлорид, пдробромід, фосфат, ацетат фумарат, малеат, тартрат, цитрат оксалат метансульфонат чи n-толуолсульфонат Сполуки формули (І) мають активність, як фармацевтичні зокрема, як модулятори ак тивності рецептору хемокіну (особливо CCR4), і їх можна застосовувати при лікуванні (терапевтичному або профілактичному) станів/хвороб у людини та тварин, які посилюються або викликаються надлишковим або нерегульованим продукуванням хемокінів. Приклади таких станів/хвороб включають: 24 (1) (респіраторний тракт) обструктивні хвороби дихальних шляхів включаючи хро нічну обстр уктивну хворобу легенів (COPD), астму, як-то бронхіальна, алергічна, властива, набута та пилкова астма, особливо хронічна або застаріла астма (наприклад, пізня астма та гіперчутливість ди хальних шляхів), бронхіт, гострий, алергічний, атрофічний риніт та хронічний риніт, включаючи риніт з утворенням казеозних мас, гіпертрофічний риніт, гнійний риніт, сухий риніт та медикаментозний риніт, мембранний риніт, включаючи крупозний, фібринозний та псевдомембранний риніт та золотушний риніт сезонний риніт включаючи анафілактичний риніт (сінна лихоманка) та вазомоторний риніт, саркоідоз, легені фермера та споріднені хвороби, фіброідні легені та ідіопатична інтерстиціальна пневмонія, (2) (кістки та суглоби) подагра, ревматоїдний артрит, серонегативні спонділоартропатм (включаючи анкілозуючий спонділіт, псоріативний артрит та хвороба Рейтера), хвороба Бекхета, синдром Сьогрена та системний склероз, (3) (шкіра) сверблячка, склеродерма, отит, псоріаз, атопічний дерматит, контактний де рматит та інші екзематозні дермітиди, себорейний дерматит, платиподія Ліхена, пемфігус, бульозний пемфігус, бульозний епідермоліз, кропивниця, анподерміт, васкулітид, еритема, шкірна еозинофілія, увеїт, гніздова алопеція та весняний кон'юнктивіт, вовчак, (4) (шлунково-кишковий тракт) хвороба Коліака, проктит, еозинофільний гастроентерит, мастоцитоз, запальні хвороби кишечнику, як-то хвороба Крона, виразковий коліт, ілеїт та ентерит, споріднені з їжею алергії, як мають ефекти, віддалені від кишок, наприклад, мігрень, риніт та екзема, (5) (центральна та периферійна нервова система) нейродегенеративні хвороби та деменційні розлади, наприклад, хвороба Альцгеймера, аміотрофічний латеральний склероз та інші моторні нейронні хвороби, хвороба Крейцфельда-Якоба та інші пріонові хвороби, ВІЧ-енцефалопатія (СНІД, деменційний комплекс), хвороба Гентингтона, фронтотемпоральна деменція, деменція тіл Леві та васкулярна деменція, полінейропатп, наприклад, синдром Гвілліан-Барре, хронічна запальна демієлінізуюча полірадікулонейропатія, мультифокальна моторна невропатія, плексопатп, демієлінування центральної нервової системи, наприклад, роз сіяний склероз, гострий розсіяний/геморагічний енцефаломієліт, та підгострий склерозуючий паненцефаліт, нейром'язові розлади, наприклад, важка міастенія та синдром Ламберта-Ітона спінальні розлади, наприклад, тропічний спазматичний парапарез, та синдром покляклої людини: паранеопластичну синдроми, наприклад, церебральна дегенерація та енцефаломієліт; травма центральної нервової системи; мігрень; інсульт та коректумні хвороби, як-то менінгіт, (6) (інші тканини та системні хвороби) гепатит, васкуліт, спонділоартропатії, вагініт, гломерулонефрит, міозит, атеросклероз, синдром набутого імунодефіциту (СНІД), червоний вовчак, системний вовчак, ерітематоз, тироїдит Хашимото, діабет 25 79255 26 типу І, нефротичний синдром, еозинофільний фарапія" також включає "профілактику" якщо нема сцит, синдром гіпер ІgЕ, лепроматозна лепра, та специфічних протипоказань. Терміни "терапевтичідіопатична тромбоцитопенічна пурпура; післяопений" та "терапевтично" слід розуміти відповідно. ративне рубцеве зрощення, та сепсис, Винахід крім того стосується способу лікуван(7) (відторгнення алотрансплантату та ксенотня опосередкованої хемокінами хвороби, де хеморансплантату) гостре та хронічне після, наприкін зв'язується з.рецептором хемокіну (особливо клад, трансплантації нирок, серця, печінки, легеCCR4), спосіб включає вживання пацієн том теранів, кісткового мозку, шкіри та роговиці; та хронічна певтично ефективної кількості сполуки формули хвороба трансплантат проти хазяїна, (І), або її фармацевтично прийнятної солі або со(8) рак, карцинома та метастази пухлин, вклюльвату, які вищезазначено. чаючи пухлини сечового міхура, молочної залози, Винахід також стосується способу лікування товстої кишки, нирок, печінки, легенів, яєчнику, респіраторних хвороб, як-то астма та риніт, особпідшлункової залози, шлунка, шиї, щитовидної ливо астма, пацієнта, що потерпає від вказаної залози та шкіри, особливо рак невеликих клітин хвороби, або при її ризику, спосіб вклю чає вжилегенів (NSCLC), злоякісна меланома, рак проставання пацієнтом терапевтично ефективної кількости та сквамозна саркома, гематопоетичні пухлини ті сполуки формули (І), або її фармацевтично прилімфоїдного походження, включаючи гостру лімйнятної солі або сольвату, які вищезазначено. фоцитну лейкемію, лімфому В-клітин та лімфому Для вищезазначених терапевтичних застосуБуркетта, лімфому Ходжкінса, гостру лімфобластвань вживані дози безумовно змінювати муться ну лейкемію, гематопоетичні пухлини мієлоїдного залежно від застосовуваної сполук, способу застопоходження, включаючи гострі та хронічні мієлосування, потрібного лікування та визначеного розгенні лейкемії та промієлоцитну лейкемію. Пухлиладу. ни мезенхімального походження, включаючи фібСполуку формули (І) та її фармацевтично приросаркому та рабдоміосаркому, та інші пухлини, йнятні солі або сольвати можна застосовувати включаючи меланому, семіному, тетратокарцинопоодинці, але загалом їх вживають у формі фарму, нейробластому та гліому, мацевтичної композиції, в якій сполу(9) усі хвороби, що є результатом загального ка/сіль/сольват формули (І) (активний інгредієнт) є дисбалансу імунної системи та призводять до пов асоціації з фармацевтично прийнятним ад'ювансилення атопічних запальних реакцій, том, розріджувачем або носієм. Залежно від спо(10) цистичний фіброз, проникаючі поранення собу застосування, фармацевтична композиція серця мозку, периферійних кінцівок та інших оргапереважно включатиме від 0,05 до 99% (за манів, сою), більш переважно від 0,05 до 80%, ще більш (11) опіки хронічні виразки шкіри, переважно від 0,10 до 70%, а особливо переважно (12) репродуктивні хвороби (наприклад, розвід 0,101 до 50%, активного інгредієнту, усі процелади овуляції, менструації та запліднення, переднти за масою основані на масі композиції. часні пологи, ендометріоз), Представлений винахід також стосується фа(13) тромбоз, рмацевтичної композиції, що містить сполуку фо(14) інфекційні хвороби, як-то ВІЧ-інфекція та рмули (І), або її фармацевтично прийнятну сіль інші вірусні інфекції, бактеріальні інфекції. або сольват, які вищезазначено, в асоціації з фаВідтак представлений винахід стосується спормацевтично прийнятним ад'ювантом, розріджувалук формули (І), або їх фармацевтичночем або носієм. прийнятних солей або сольватів, які вищезазначеВинахід також стосується способу отримання ні, для застосування у терапії. фармацевтичної композиції винаходу, який вклюПереважно сполуки винаходу застосовують чає змішування сполуки формули (І), або її фардля лікування хвороби, в яких рецептор хемокіну мацевтично прийнятної солі або сольвату, як виналежить до підродини рецепторів хемокінів СС, щезазначено, з фармацевтично прийнятним більш переважно цільовий рецептор хемокіну ад'ювантом, розріджувачем або носієм. представляє рецептор CCR4. Фармацевтичні композиції можна вживати місОсобливі стани, як можна лікувати сполукою цево (наприклад, до легенів та/або дихальних винаходу є астма, риніт та запальні розла ди, хвошляхів або до шкіри) у формі розчинів, суспензій, роби шкіри, в яких підвищені рівні TARC, MDC або гептафлуоралканових аерозолів та сухи х порошCCR4. Краще сполуку винаходу за стосовува ти кових композицій; або системно, наприклад, перодля лікування астми та риніту, особливо астми. ральним застосуванням у формі таблеток, капсул, Наступний аспект представленого винаходу сиропів, порошків або гранул, або парентеральним стосується застосування сполук формули (І), або застосуванням у формі розчинів або суспензій, їх фармацевтично прийнятних солей або сольваабо підшкірним застосуванням або ректальним тів, які вищезазначено, у виробництві медикаменту застосуванням у формі супозиторіїв, або трансдедля застосування у терапії. рмально. Переважно сполуку винаходу вживають Подальший аспект представленого винаходу перорально. стосується застосування сполуки формули (І), або Наступний аспект представленого винаходу їх фармацевтично прийнятних солей або сольвастосується застосування сполук формули (І), або тів, які вищезазначено, у виробництві медикаменту їх фармацевтично прийнятних солей або сольвадля лікування хвороб або станів людини, в яких є тів, які вищезазначено, у виробництві медикаменту переважним модулювання активності рецептору для застосування у терапії у комбінації з ліками, хемокіну, особливо активності CCR4. застосовуваними для лікуван ня астми та риніту У контексті представленого опису, термін "те(як-то інгаляційні та пероральні стероїди, інгаля 27 79255 28 Приклад 4 ційні агоністи b2-рецептору та пероральні антаго2,3-Дихлор-N-(6-хлор-3-метокси-2ністи рецептору лейкотриєну). Приклад 1 піразиніл)бензолсульфонамід a) 3-Бром-6-хлор-2-піразинамін 2,3-Дихлор-N-(3-метокси-5-метил-2-піразиніл)бензолсульфонамід Натрій гідрид (0,1г 60%) додавали до 3метокси-5-метил-2-піразинаміну (0,07г) в 1,2диметоксіетані (3мл) під азотом при кімнатній температурі. Після 1 годин при 50° додавали 2,3дихлорбензолсульфонілхлорид (0,15г). Після перемішування протягом 30 хвилин, дода вали 5% водну лимонну кислоту та продукт екстрагували етилацетатом (ХЗ). Поєднані екстракти промивали насиченим розсолом, сушили безводним сульфатом магнію та розчинник випарювали. Хроматографія на діоксиді силіцію, елюючи сумішшю дихлорметан/метанол, дала позначену сполуку, як білий твердий продукт (0,08г). m/е 346/8/350 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 11,27 (1Н, s), 8,06 (1Н, d), 7,93 (1Н, d), 7,60-7,55 (1Н, brs), 7,58 (1Н, t), 3,87 (3Н, s), 2,28 (3Н, s). Приклад 2 N-(6-Хлор-3-метокси-2-піразиніл)-2,3,4трифлуорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,16г) та 2,3,4трифлуорбензолсульфонілхлорид (0,25г), ви хід 0.0Sг, m/е 352/4 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 7,93-7,80 (1Н, m), 7,89 (1Н, s), 7,60-7,50 (1Н, m), 3,91 (3Н, s). Приклад 3 3-Хлор-N-(6-хлор-3-метокси-2-піразиніл)-2метилбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,16г) та Зхлор-2-метилбензолсульфонілхлорид (0,23г). Вихід 0,15г. m/е 346/8/50 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,05 (1Н, d), 7,85 (1Н, s), 7,75 (1Н, d), 7,47 (1Н, t), 3,92 (3Н, s), 2,66 (3Н, s). N-бромсукцинамід (6,9г) додавали порціями протягом 0,5 годин до перемішуваного розчину 6хлор-2-піразинаміну (5,0г) у хлороформі (200мл) гріли під зворотним холодильником. Після завершення додавання реакційну суміш охолоджували, промивали водою та випарювали, отримуючи 3:1 суміш 5-бром-6-хлор-2-піразинаміну та визначеної сполуки, яку розділяли хроматографією на колонці з силікагелем, елюючи дихлорметаном. Вихід 2,0г. Застосовували безпосередньо. b) 6-Хлор-3-метокси-2-піразинамін та 3-бром6-метокси-2-піразинамін 3-Бром-6-хлор-2-піразинамін (1,0г), натрій метоксид (3мл 25% розчин у метанол) та метанол (10мл) гріли під зворотним холодильником протягом 3 годин. Розчинник випарювали та залишок розчиняли у етилацетаті та розсолі. Органічний шар розділяли, сушили безводним сульфатом магнію та розчинник випарювали, отримуючи суміш позначених сполук (співвідношення 10:1). Очистку проводили хроматографією на колонці з силікагелем, елюючи дихлорметаном. Вихід 0,5г. Застосовували безпосередньо. с) 2,3-Дихлор-N-(6-Хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,24г) та 2,3дихлорбензолсульфонілхлорид (0,32г). Вихід 0,24г. m/е 366/8/370/2 (М-I+, 100%) 1 НЯМР (D6-ДМСО) d 8,14 (1Н, d), 7,96 (1Н, d), 7,89 (1Н, s), 7,62 (1Н, t), 3,91 (3Н, s). Приклад 5 2,3-Дихлор-N-(5-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-хлор-3-метокси-2-піразинамін (0,1г) та 2,3дихлорбензолсульфонілхлорид (0,15г). Вихід 29 79255 30 0,05г. m/е 366/8/370/2 (М-I+, 100%) 0,059г. m/e 410/2/4/6 (М-I+, 100%) 1 1 Н ЯМР (D6-ДMCO) d 8,15 (1Н, d), 7,93 (1Н, d), Н ЯМР (D6-ДMCО) d 8,07 (1Н, d), 7,85 (2Н, d), 7,79 (1Н, s), 7,58 (1Н, t), 3,93 (3Н, s). 7,64 (1Н, dd), 3,92 (3Н, s). Приклад 6 Приклад 10 N-(5-Бром-3-метокси-2-піразиніл)-2,5N-(5-бром-3-метокси-2-піразиніл)-2,4дихлорбензолсульфонамід дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,2г) та 2,5дихлорбензолсульфонілхлорид (0,24г). Вихід 0,14г. m/e 410/2/4/6 (М-I+, 100%) 1 H ЯМР (D6-ДMCO) d 8,04 (1Н, d), 7,86 (1Н, s), 7,73 (1Н, dd), 7,66 (1Н, dd), 3,91 (3Н, s). Приклад 7 N-(5-Бром-3-метокси-2-піразиніл-3,5дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,2г) та 3,5дихлорбензолсульфонілхлорид (0,24г). Вихід 0,012г. m/e 410/2/4/6 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 7,96-7,91 (4Н, m),3,93 (3Н, s). Приклад 8 N-(5-Бром-3-метокси-2-піразиніл)-2,3дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-гпіразинамін-(0,1г) та 2,3дихлорбензолсульфонілхлорид (0,2г). Ви хід 0,045г. m/e 410/2/4/6 (М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,06 (1Н, dd), 7,93 (1Н, dd), 7,82 (1Н, s), 7,57 (1Н, t), 3,92 (3Н, s). Приклад 9 N-(5-Бром-3-метокси-2-піразиніл)-2,4дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,2г) та 2,4дихлорбензолсульфонілхлорид (0,24г). Вихід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,15г) та 3,4дихлорбензолсульфонілхлорид (0,15г). Вихід 0,09г. m/е 410/2/4/6 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,14 (1Н, s), 8,00-7,85 (3Н, m), 3,94 (3Н, s). Приклад 11 N-(5-Бром-3-метокси-2-піразиніл)-4хлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,1г) та 4хлорбензолсульфонілхлорид (0,13г). Вихід 0,13г. m/е 376/8/380 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 11,3 (1Н, brs), 7,97 (2Н, d), 7,91 (1Н, s), 7,66 (2Н, d), 3,93 (3Н, s). Приклад 12 N-(5-Бром-3-метокси-2-піразиніл)-3хлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,1г) та 3хлорбензолсульфонілхлорид (0,13г). Вихід 0,14г. m/е 376/8/380 (М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,00-7,90 (3Н, m), 7,75 (1H3d), 7,64 (1Н, t), 3,94 (3Н, s). Приклад 13 N-(3-Метокси-5-Метил-2-піразиніл)-2флуорбензолсульфонамід 31 79255 32 Отримано способом прикладу 1, використову100%) 1 ючи 3-метокси-5-метил-2-піразинамін та 2Н ЯМР (D6-ДMCO) d 8,15 (1Н, dd), 8,05 (1Н, флуорбензолсульфонілхлорид. m/е298(М+1+, dd), 7,85 (1Н, dt), 7,80 (1Н, dt), 7,60 (1Н, s), 3,85 100%) (3Н, s), 2,30 (3Н, s). 1 Н ЯМР (D6-ДМСО) d 11,05 (1Н, br s), 7,85-7,95 Приклад 18 (1Н, m), 7,65-7,75 (1Н, m), 7,50-7,60 (1Н, m), 7,35N-(5-Бром-3-метокси-27,45 (1Н, m), 3,90 (3Н, s), 2,30 (3Н, s). Темп.пл. піразиніл)бензолсульфонамід 150-152°С Приклад 14 N-(3-Метокси-5-метил-2піразиніл)бензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін та бензолсульфонілхлорид. Темп.пл. 138-139°С Приклад 15 N-(3-Метокси-5-метил-2-піразиніл)-2йодбензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін та 2йодбензолсульфоніл хлорид. 1 Н ЯМР (D6-ДMCO) d 10,75 (1Н, br s), 8,05-8,15 (2Н, m), 7,65-7,75 (2Н, m), 7,30 (1Н, dt), 3,90 (3Н, s), 2,30 (3Н, s). Темп.пл. 140-141°С Приклад 16 N-(3-Метокси-5-метил-2-піразиніл)-3флуорбензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін та 3флуорбензолсульфоніл хлорид. Темп.пл. 95-97°С Приклад 17 2-[[(3-Метокси-5-метил-2піразиніл)аміно]сульфоніл]бензонітрил Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін та 2ціанобензолсульфонілхлорид, m/е 305(М+1+, Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін та бензолсульфонілхлорид, m/е344(М+1+, 100%) Приклад 19 N-(5-Бром-3-метокси-2-піразиніл)2йодбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін та 2йодбензолсульфонілхлорид, m/е470 (М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 11,30 (1Н, brs), 8,0-8,1 (2Н, m), 7,80 (1Н, s), 7,60 (1Н, dt), 7,30 (1Н, dt),3,95(3H, s). Приклад 20 2,3-Дихлор-N-[3-(2-фуранілметокси)-5-метил2-піразиніл]бензолсульфонамід а) N-(3 -Бром-5-метил-2-піразиніл)-2,3дихлорбензолсульфонамід Отримано способом прикладу 1, використовуючи 3-бром-5-метил-2-піразинамін (0,84г) та 2,3дихлорбензолсульфонілхлорид (1,1г). Вихід 0,92г. b) 2,3-Дихлор-N-[3-(2-фуранілметокси)-5метил-2-піразиніл]бензолсульфонамід Натрій гідрид (0,04г 60% дисперсії у маслі) додавали до фур фурилового спирту (0,034г) в 1,2диметоксіетані (1мл). Після 5 хвилин додавали N(3-Бром-5-метил-2-піразиніл)-2,3дихлорбензолсульфонамід (Приклад 20 етап а) 33 79255 34 (0,1г) та суміш гріли при 40°С. Через 16 годин доОтримано способом прикладу 20, використодавали 5% водну лимонну кислоту (10мл) та суміш вуючи 6-метилпіридин-2-метанол (0,05г) та N-(3бром-5-метил-2-піразиніл)-2,3екстрагували етилацетатом (2´50мл). Поєднані дихлорбензолсульфонамід (0,1г). Вихід 0,023г., екстракти промивали розсолом, сушили безводm/е439(М+1+, 100%) ним сульфатом магнію та розчинник випарювали. 1 Хроматографія на силікагелі, елюючи дихлорН ЯМР (D6-ДМСО) d 8,05 (1Н, dd), 7,89 (1Н, метаном дала позначену сполуку, як білий тверdd), 7,70 (1Н, t), 7,59 (1Н, br s), 7,54 (1Н, t), 7,34 дий продукт (0,02г). m/е 412(М-І+ 100%) (1Н, d), 7,19 (1Н, d), 5,39 (2Н, s), 2,47 (3Н, s), 2,26 1 (3Н, s). Темп.пл. 164-165°С Н ЯМР (D6-ДMCO) d 11,33 (1Н, brs), 8,01 (1Н, Приклад 24 d), 7,90 (1Н, d), 7,70 (1Н, s), 7,62 (1Н, brs), 7,54 (1Н, 2,3-Дихлор-N-[5-метил-3-(3-піридинілметокси)t), 6,61-6,58 (1Н, m), 6,50-6,45 (1Н, m), 5,33 (2Н, s), 2-піразиніл]бензолсульфонамід 2,32 (3Н, s). Темп.пл. 127-129°C Приклад 21 2,3-Дихлор-N-[5-метил-3-(5-метил-3ізоксазолілметокси)-2-тразиніл]бензолсульфонамід Отримано способом прикладу 20, використовуючи (5-метил-3-ізоксазоліл)метанол (0,05г) та N(3-бром-5-метил-2-піразиніл)-2,3дихлорбензолсульфонамід (0,1г). Вихід 0,05г., m/е 429 (М-Н+, 100%) 1 Н ЯМР (D6-ДMCO) d 11,39 (1Н, brs), 8,03 (1Н, d), 7,91 (1Н, d), 7,64 (1Н, brs), 7,47 (1Н, t), 6,33 (1Н, s), 5,37 (2Н, s), 2,41 (3Н, s), 2,29 (3Н, s). Темп.пл. 155-156°С Приклад 22 2,3-Дихлор-N-[5-метил-3-(2-піридинілметокси)2-піразиніл]бензолсульфонамід Отримано способом прикладу 20, використовуючи піридин-2-метанол (0,05г) та N-(3-бром-5метил-2-піразиніл)-2,3-дихлорбензолсульфонамід (0,1г). Вихід 0,07г., m/е425(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,57-8,54 (1Н, m), 8,05 (1Н, d), 7,89 (1Н, d), 7,83 (1Н, dt), 7,65-7,50 (2Н, m), 7,56 (1Н, t), 7,35-7,30 (1Н, m), 5,44 (2Н, s), 2,26 (3Н, s) Приклад 23 2,3-Дихлор-N-[5-метил-3-(6-метил-2піридинілметокси)-2-піразиніл]бензолсульфонамід Отримано способом прикладу 20, використовуючи піридин-3-метанол (0,05г) та N-(3-бром-5метил-2-піразиніл)-2,3-дихлорбензолсульфонамід (0,1г). Вихід 0,023г, m/е425(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,74 (1Н, d), 8,55 (1Н, dd), 8,03 (1Н, dd), 7,95-7,85 (2Н, m), 7,59 (1Н, br s), 7,54 (1Н, t), 7,42 (1Н, dd), 5,41 (2Н, s), 2,29 (3Н, s). Темп.пл. 160-161°С Приклад 25 2,3-Дихлор-N-[5-метил-3-(4-піридинілметокси)2-піразиніл]бензолсульфонамід Отримано способом прикладу 20, використовуючи піридин-4-метанол (0,05г) та N-(3-бром-5метил-2-піразиніл)-2,3-дихлорбензолсульфонамід (0,1г). Вихід 0,009г. m/е 425(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,57 (2Н, d), 8,05 (1Н, dd), 7,89 (1Н, dd), 7,60 (1Н, s), 7,55 (1Н, t), 7,50 (2Н, d), 5,43 (2Н, s), 2,26 (3Н, s). Темп.пл. 183-184°С Приклад 26 2,3-Дихлор-N-[5-метил-3-(3-метил-2піридинілметокси)-2-піразиніл]-бензолсульфонамід Отримано способом прикладу 20, використовуючи 3-метилпіридин-2-метанол (0,05г) та N-(3бром-5-метил-2-піразиніл)-2,3дихлорбензолсульфонамід (0,1г). Вихід 0,021г, m/е 439(М-Н+, 100%) 35 79255 36 вали. Хроматографія на силі кагелі, елюючи Н ЯМР (D6-ДMCO) d 8,36 (1Н, d), 8,05 (1Н, сумішшю ізогексан/дихлорметан, дала позначену dd), 7,83 (1Н3 dd), 7,64 (1Н, d), 7,60 (1Н, bг s), 7,49 (1Н, t), 7,31 (1Н, dd), 5,40 (2Н, s), 2,33 (3Н, s), 2,29 сполуку, як білий твердий продукт (0,06г). m/е 411 (М-Н+, 100%) (3Н, s). Темп.пл. 137-138°С 1 Приклад 27 Н ЯМР (D6-ДМСО) d S,57 (1Н, d), 8,13 (1Н, d), 2,3-Дихлор-N-[5-метил-3-(37,93 (1Н, d), 7,90-7,75 (2Н, m), 7,75-7,65 (1Н, m), піридазинілметокси)-27,65-7,55 (2Н, m), 7,40-7,30 (1Н, m), 5,49 (2Н, s). піразиніл]бензолсульфонамід Темп.пл. 167-168°С Приклад 29 2,3-Дихлор-N-[3-(3-піридинілметокси)-2піразиніл]бензолсульфонамід 1 Отримано способом прикладу 20, використовуючи піридазин-3-метанол (0,1г) та N-(3-бром-5метил-2-піразиніл)-2,3-дихлорбензолсульфонамід (0,15г). Вихід 0,038г., m/е 424(М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 11,47 (1Н, brs), 9,21 (1Н, dd), 8,05 (1Н, dd), 8,00-7,95 (1Н, m), 7,88 (1Н, d), 7,80-7,75 (1Н, m), 7,62 (1Н, brs), 7,54 (1Н, t), 5,65 (2Н, s), 2,27 (3Н, s). Темп.пл. 119-124°С Приклад 28 2,3-Дихлор-N-[3-(2-піридинілметокси)-2піразиніл]бензолсульфонамід а) 2,3-Дихлор-N-[3-хлор-2піразиніл]бензолсульфонамід 2,3-Дихлорпіразин (2,6г), 2,3дихлорбензолсульфонамід (4,0г) та калій карбонат (10,0г) у N,N-диметилформаміді (50мл) гріли при 75°С. Через 16 годин додавали водну 5% лимонну кислоту (30мл) та суміш екстрагували етилацетатом (2´100мл). Поєднані екстракти промивали розсолом, сушили безводним сульфатом магнію та розчинник випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку (1,5г). b) 2,3-Дихлор-N-[3-(2-піридинілметокси)-2піразиніл]бензолсульфонамід Натрій гідрид (0,05г 60% дисперсії у маслі) додавали до піридин-2-метанолу (0,088г) в 1,2диметоксіетані (3,0мл). Після 5 хвилин 2,3-дихлорN-(3-хлор-2-піразиніл)бензолсульфонамід (0,1г) додавали та суміш гріли при 70°С. Після 4 годин додавали водну 5% лимонну кислоту (10мл) та суміш екстрагували етилацетатом (2´50мл). Поєднані екстракти промивали розсолом, сушили безводним сульфатом магнію та розчинник випарю Отримано способом прикладу 28, використовуючи піридин-3-метанол (0,09г) та 2,3-дихлор-N(3-хлор-2-піразиніл)бензолсульфонамід (0,1г). Вихід 0,042г. m/е 409(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,70 (1Н, s), 8,65 (1Н, d), 8,28 (1Н, dd)3 7,79 (1Н, d), 7,70-7,67 (2Н, m), 7,61 (1Н, d), 7,40-7,35 (2Н, m), 5,45 (2Н, s). Темп.пл 138139°С Приклад 30 2,3-Дихлор-N-(3-метокси-2піразиніл)бензолсульфонамід 2,3-Дихлор-N-(3-хлор-2піразиніл)бензолсульфонамід (Приклад 28 етап а) (0,2г у 10% натрій метоксиді у метанолі (10мл) гріли при 85°С. Після 4 годин 5% водну лимонну кислоту (50мл) додавали та суміш екстрагували етилацетатом (2´150мл). Поєднані екстракти промивали розсолом, сушили безводним сульфатом магнію та розчинник випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,12г), m/е 334(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 11,54 (1Н, br s), 8,10 (1Н, d), 7,94 (1Н, d), 7,85-7,75 (1Н, m), 7,70-7,55 (1Н, m), 7,59 (1Н, t), 3,90 (3Н, s). Темп.пл. 183-184°С Приклад 31 N-[5-Бром-3-(2-піразинілметокси)-2-піразиніл]2,3-дихлорбензолсульфонамід а) 2,3-Дихлор-N-(3,5-дибром-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію про 37 79255 38 водять при кімнатній температурі), використовуювуючи піридазин-3-метанол (0,07г) та 2,3-дихлорчи 3,5-дибром-2-піразинамін (2,9г) та 2,3N-(3,5-дибром-2-піразиніл)бензолсульфонамід дихлорбензолсульфонілхлорид (2,8г). Вихід 4,4 г. (0,15г). Вихід 0,06г. m/е 489(М-r, 100%) 1 b) N-[5-Бром-3-(2-піразинілметокси)-2Н ЯМР (D6-ДMCO) d 9,23 (1Н, d), 8,08 (1Н, піразиніл-2,3-дихлорбензолсульфонамід dd), 7,99 (1Н, dd), 7,92 (1Н, dd), 7,91 (1Н, s), 7,80 (1Н, dd), 7,56 (1Н, t), 5,67 (2Н, s). Темп.пл. 115120°С Приклад 34 N5-Бром-3-(3-піридинілметокси)-2-піразиніл]2,3-дихлорбензолсульфонамід Натрій гідрид (0,05г 60% дисперсії у маслі) додавали до піразин-2-метанолу (0,04г) в 1,2диметоксіетані (3мл). Після 5 хвилин додавали 2,3-Дихлор-N-(3,5-дибром-2піразиніл)бензолсульфонамід (0,12г). Через 0,5 годин додавали водну 5% лимонну кислоту (10мл) та суміш екстрагували етилацетатом (2´30мл). Поєднані екстракти промивали розсолом, сушили безводним сульфатом магнію та розчинник випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,06г). m/е 489(М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 9,00 (1Н, S), 8,66 (2Н, s), 8,08 (1Н, dd), 7,92 (1Н, dd), 7,91 (1Н, s), 7,56 (1Н, t), 5,53 (2Н, s). Темп.пл. 207-209°C Приклад 32 N-[5-Бром-3-(1-метил-6-оксо-1,6-дигідро-3піридинілметокси)-2-піразиніл]-2,3дихлорбензолсульфонамід Отримано способом прикладу 31, використовуючи 5-гідроксиметил-1-метил-1Н-піридин-2-он (0,1г) та 2,3-дихлор-N-(3,5-дибром-2піразиніл)бензолсульфонамід (0,16г). Вихід 0,035г. m/е 521 (М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,04 (1Н, dd), 7,91 (1Н, dd), 7,90-7,87 (2Н, т), 7,60-7,50 (2Н, m), 6,42 (1Н, d), 5,10 (2Н, s), 3,41 (3Н, s) Темп.пл. 169-170°С Приклад 33 N-[5-Бром-3-(3-піридазиніл)метокси)-2піразиніл]-2,3-дихлорбензолсульфонамід Отримано способом прикладу 31, використо Отримано способом прикладу 31, використовуючи піридин-3-метанол (0,44г) та 2,3-дихлор-N(3,5-дибром-2-піразиніл)бензолсульфонамід (1,0г). Вихід 0,6г, m/e 491 (М-r, 100%) 1 Н ЯМР (D6-ДMCO) d 8,78 (1Н, d), 8,58 (1Н, d), 8,06 (1Н, d), 7,99 (1Н, dt), 7,91 (1Н, d), 7,88 (1Н, s), 7,55 (1Н, t), 7,55-7,50 (1Н, m), 5,44 (2Н, s). Темп.пл. 204-206°С Приклад 35 N-[5-Бром-3-(3-піридазиніл)метокси)-2піразиніл]-2,3-дихлорбензолсульфонамід Отримано способом прикладу 31, використовуючи піримідин-5-метанол (0,035г) та 2,3-дихлорN-3,5-дибром-2-піразиніл)бензолсульфонамід (0,16г). Вихід 0,028г., m/е 490(М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 9,21 (1Н, s), 9,02 (2Н, s), 8,07 (1Н, dd), 7,92 (1Н, dd), 7,91 (1Н, s), 7,56 (1H, t), 5,45 (2Н, s). Темп.пл. 208-209°С Приклад 36 N-[5-Хлор-3-(3-піридинілметокси)-2-піразиніл]2,3-дихлорбензолсульфонамід Отримано способом прикладу 31, використовуючи піридин-3-метанол (0,13г) та 2,3-дихлор-N(3,5-дихлор-2-піразиніл)бензолсульфонамід (Приклад 74) (0,3г). Вихід 0,19г. m/е 447(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,78 (1Н, s), 8,59 (1Н, dd), 8,06 (1Н, dd), 7,96 (1Н, dt), 7,91 (1Н, dd), 7,83 (1Н, s), 7,55 (1Н, t), 7,47 (1Н, dd), 5,44 (2Н, s). 39 Темп.пл. 200-204°С Приклад 37 N-[5-Хлор-3-(5-піримідиніл-метокси)-2піразиніл]-2,3-дихлорбензолсульфонамід 79255 Отримано способом прикладу 31, використовуючи піримідин-5-метанол (0,035г) та 2,3-дихлорN-(3,5-дихлор-2-піразиніл)бензолсульфонамід (Приклад 74) (0,07г). Вихід 0,015г. 5 m/е448(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 9,21 (1Н, s), 9,02 (2Н, s), 8,08 (1Н, dd), 7,92 (1Н, dd), 7,86 (1Н, s), 7,56 (1Н, t), 5,46 (2Н, s). Темп.пл. 205-206°С Приклад 38 2-Хлор-N-(6-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,1г) та 2хлорбензолсульфонілхлорид (0,13г). 15 вихід 0,11г., m/е 332(М-I+,100%) 1 Н ЯМР (D6-ДМСО) d 8,15 (1Н, d), 7.S6 (1Н, s), 7,70-7,50 (3Н, m), 3,91 (3Н, s). Темп.пл. 172-173°С. Приклад 39 3-Хлор-N-(6-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,1г) та 3хлорбензолсульфонілхлорид (0,13г) Вихід 0,14г, m/е 332 (М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,05 (1Н, d), 7,93 (1Н, dd), 7,90 (1Н, s), 7,76 (1Н, dd), 7,65 (1Н, t) 3,92 (3Н, s), Темп.пл. 126-127°С Приклад 40 4-Хлор-N-(6-хлор-3-метокси-2піразиніл)бензолсульфонамід 40 Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,1г) та 4хлорбензолсульфонілхлорид (0,13г). Вихід 0,13г, m/е332(М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 7,99 (2Н, dt), 7,89 (1Н, s), 7,70 (2Н, dt), 3,92 (3Н, s), Темп.пл. 174-175°С Приклад 41 N-(6-Хлор-3-метокси-2-піразиніл)-2,4дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,05г) та 2,4дихлорбензолсульфонілхлорид (0,1г). Вихід 0,07г, m/e 368(М-І+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,13 (1Н, d), 7,86 (1Н, s), 7,85 (1Н, d), 7,70 (1H,dd), 3,91 (3Н, s).Темп.пл. 189190°С Приклад 42 N-(6-Хлор-3-метокси-2-піразиніл)-3,4дихлорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 6-хлор-3-метокси-2-піразинамін (0,05г) та 3,4дихлорбензолсульфонілхлорид (0,09г). Вихід 0,08г. m/e 368 (М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,21 (1Н, s), 7,93-7,90 (3Н, m), 3,92 (3Н, s). Темп.пл. 176-177°С Приклад 433-Хлор-N-(3-метокси-5-метил-2-піразиніл)-2метилбензолсульфонамід Отримано способом прикладу 1, використову 41 79255 ючи 3-метокси-5-метил-2-піразинамін (0,1г) та 3хлор-2-метилбензолсульфонілхлорид (0,19г). Вихід 0,08г, m/e 32S(M+1+ 100%) 1 Н ЯМР (D6-ДMCO) d 11,09 (1Н, brs), 7,95 (1Н, d), 7,72 (1Н, d), 7,54 (1Н, brs), 7,41 (1Н, t), 3,88 (3Н, s), 2,64 (3Н, s), 2,27 (3Н, s), Темп.пл. 133-135°С Приклад 44 2-Хлор-N-(3-метокси-5-метил-2піразиніл)бензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін (0,1г) та 2хлорбензолсульфонілхлорид (0,15г). Вихід 0,06г, m/e 314(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 11,07 (1Н, brs), 8,06 (1Н, d), 7,69-7,46 (4Н, m), 3,90 (3Н, s), 2,24 (3Н, s) Приклад 45 3-Хлор-N-(3-метокси-5-метил-2піразиніл)бензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін (0,1г) та 3хлорбензолсульфонілхлорид (0,18г). Вихід 0,042г, m/е 314(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 10,89 (1Н, br s), 7,97 (1Н, d), 7,92 (1Н, d), 7,73 (1Н, d), 7,65-7,58 (2Н, m), 3,90 (3Н, s), 2,29 (3Н, s). Темп.пл. 123-125°С Приклад 46 4-Хлор-N-(3-метокси-5-метил-2піразиніл)бензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін (0,1г) та 4хлорбензолсульфонілхлорид (0,18г). Вихід 0,06г, m/е 314(М+1+,100%) 1 Н ЯМР (D6-ДМСО) d 10,83 (1Н, br s), 7,96 (2Н, d), 7,65 (2Н, d), 7,60 (1Н, s), 3,88 (3Н, s), 2,28 (3Н, s) Темп.пл. 155-156°С Приклад 47 2,4-Дихлор-N-(3-метокси-5-метил-2піразиніл)бензолсульфонамід 42 Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін (0,1г) та 2,4дихпорбензолсульфонілхлорид (0,21г). Вихід 0,041г, m/е348(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,05 (1Н, d), 7,83 (1Н, d), 7,64 (1Н, dd), 7,54 (1Н, br s), 3,87 (3Н, s), 2,27 (3Н, s). Темп.пл. 135-136°С Приклад 48 3,4-Дихлор-N-(3-метокси-5-метил-2піразиніл)бензолсульфонамід Отримано способом прикладу 1, використовуючи 3-метокси-5-метил-2-піразинамін (0,1г) та 3,4дихлорбензолсульфонілхлорид (0,21г). Вихід 0,046г, m/е 348(М+1+, 100%) 1 НЯМР (D6-ДMCO) d 10,97 (1Н, s), 8,14 (1Н, d), 7,91 (1Н, dd), 7,88 (IK, d), 7,63 (1Н, s), 3,89 (3Н, s), 2,27 (3Н, s), Темп.пл. 148-149°С Приклад 49 N-(5-Бром-3-метокси-2-пiразиніл)-2трифлуорметоксибензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-бром-3-метокси-2-піразинамін (0,1г) та 2трифлуорметоксибензолсульфонілхлорид (0,13г). Вихід 0,097г, m/e 428(М-I+, 100%) 'Н ЯМР (D6-ДMCO) d 8,03 (1Н, dd), 7,87 (1Н, s), 7,82-7,74 (1Н, m), 7,60-7,52 (2Н, m), 3,92 (3Н, s), Темп.пл. 156-157°С Приклад 50 3-Хлор-N-(5-хлор-3-метокси-2-піразиніл)-2метилбензолсульфонамід Отримано способом прикладу 1 (реакцію про 43 79255 44 водять при кімнатній температурі), використовуюПриклад 54 чи 5-хлор-3-метокси-2-піразинамін (0,1г) та 3-хлорN-(5-Хлор-3-метокси-2-піразиніл)-2,42-метилбензолсульфонілхлорид (0,15г). Вихід дихлорбензолсульфонамід 0,085г, m/e 346(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,17 (1Н, d), 7,69 (1Н, brs), 7,64 (1Н, s), 7,61 (2Н, d), 7,30 (1Н, t), 4,04 (3Н, s), 2,73 (3Н, s). Темп.пл. 150-152°С Приклад 51 2-Хлор-N-(5-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-хлор-3-метокси-2-піразинамін (0,1г) та 2хлорбензолсульфонілхлорид (0,13г). Вихід 0,082г, m/е 332(М-Н+, 100%) 1 Н ЯМР (CDCI3) d 8,33 (1Н, d), 7,82 (1Н, s), 7,64-7,62 (1Н, m), 7,61 (1Н, s), 7,50-7,42 (2Н, m), 4,04 (3Н, s). Темп.пл. 190-192°С Приклад 52 3-Хлор-N-(5-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-хлор-3-метокси-2-піразинамін (0,1г) та 3хлорбензолсульфонілхлорид (0,13г). Вихід 0,095г, m/е 332(М+1+, 100%) 1 Н ЯМР (СОСІ3) d 8,14 (1Н, s), 8,03 (1Н, d), 7,76 (1Н, s), 7,68-7,53 (2Н, m), 7,46 (1Н, t), 4,02 (3Н, s). Темп.пл. 129-130°С Приклад 53 4-Хлор-N-(5-хлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-хлор-3-метокси-2-піразинамін (0,1г) та 4хлорбензолсульфонілхлорид (0,13г). Вихід 0,05г, m/e332(M+1+, 100%) 1 Н ЯМР (CDCI3) d 8,07 (2Н, d), 7,75 (1Н, s), 7,56 (1Н, s), 7,49 (2Н, d), 4,02 (3Н s). Темп.пл. 179180°C Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5-хлор-3-метокси-2-піразинамін (0,1г) та 2,4дихлорбензолсульфонілхлорид (0,13г). Вихід 0,045г, m/е 368(М-г, 100%) 1 Н ЯМР (CDCI3) d 8,27 (1Н, d), 7,78 (1Н, s), 7,63 (1Н, s), 7,48 (1Н, s), 7,43 (1Н, d), 4,05 (3Н, s). Темп.пл. 170-171°С Приклад 55 2,3-Дихлор-N-[3-метокси-5-(4-морфолініл)-2піразиніл]бензолсульфонамід а) N-5-Бром-3-метокси-2-піразиніл)-2,3дихлор-N-{[2(триметилсиланіл)етокси]метил}бензолсульфонамід Суміш N-(5-Бром-3-метокси-2-піразиніл)-2,3дихлорбензолсульфонаміду (Приклад 8) (0,40г), діізопропілетиламіну (0,26г) та [2(хлорметокси)етил]триметилсилану (0,25г) у дихлорметані (50мл) перемішували при кімнатній температурі. Через 2 години розчин промивали водою, сушили безводним сульфатом магнію та випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,40г). 1 Н ЯМР (CDCI3) d 8,09 (1Н, s), 7,96 (1Н, dd), 7,68 (1Н, dd), 7,29 (1Н, t), 5,24 (2Н, s), 3,92 (3Н, s), 3,77-3,73 (2Н, m), 0,86-0,82 (2Н, m), 0,00 (9Н, s) b) 2,3-Дихлор-N-[3-метокси-5-(4-морфолініл)-2піразиніл]бензолсульфонамід N-(5-Бром-3-метокси-2-піразиніл)-2,3-дихлорN-[{2-(триметилсиланіл)етокси}метил]бензолсульфонамід (0,30г) та морфолін (0,45г) в ацетонітрилі (10мл) гріли при 50°С. Через 16 годин розчин випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/етилацетат, дала позначену сполуку з приєднаною групою SEM як білий твердий продукт. Твердий продукт розчиняли у трифлуороцтовій кислоті (S,0 мл) та дихлорметані (5,0мл). Через 2 години розчин випарювали. 45 79255 46 Хроматографія на силікагелі, елюючи сумішшю хлор-2-метилбензолсульфонілхлорид (0,14г). Виізогек-сан/етилацетат, дала позначену сполуку, як хід 0,13г. m/е 381 (М-I+, 100%) 1 білий твердий продукт (0,06г), m/е417(М-I+, 100%) Н ЯМР (CDCI3) 5 8,25 (1Н, d), 7,65 (1Н, br s), 1 7,62 (1Н, d), 7,35 (1Н, t), 4,04 (3Н, s), 2,73 (3Н, s), Н ЯМР (CDCI3) d 8,17 (1Н, d), 7,65 (1Н, d), 7,41 Темп.пл. 177-178°С (1Н, s), 7,34 (1Н, t), 7,16 (1Н, s), 3.89 (3Н, s), 3,80Приклад 59 3,75 (4Н, m), 3,40-3,35 (4Н, m). Темп.пл. 167-168°С 2,3-Дихлор-N-(5,6-дихлор-3-метокси-2Приклад 56 2,3-Дихлор-N-[3,5-диметокси-2піразиніл)бензолсульфонамід піразиніл]бензолсульфонамід N-(5-Бром-3-метокси-2-піразиніл)-2,3-дихлорN-[{2-(триметилсиланіл)етокси}метил]бензолсульфонамід (0,30г) у метанольному натрій метоксиді (10мл 0,5 молярного розчину) перемішували при кімнатній температурі. Через 16 годин розчин випарювали досуха та додавали дихлорметан (10мл) та трифлуороцтову кислоту (10мл). Через 2 години суміш випарювали досуха, додавали дихлорметан та неорганічні солі видаляли фільтруванням. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,1г). m/е 364 (М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,21 (1Н, d), 7,67 (1Н, d), 7,50 (1Н, s), 7,37 (1Н, t), 7,26 (1Н, s), 3,98 (3Н, s),3.S7(3H, s) Темп.пл. 138-139°С Приклад 57 2,3-Дихлор-N-[3-метокси-5-(1-піролініл)-2піразиніл]бензолсульфонамід Отримано способом прикладу 55, використовуючи піролідин (0,4г) та N-(5-бром-3-метокси-2піразиніл)-2,3-дихлор-N-[{2(триметилсиланіл)етокси}метил]бензолсульфонамід (0,3г). Вихід 0,045г. m/е 403(М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,08 (1Н, d), 7,64 (1Н, d), 7,30 (1Н, t), 7,21 (1Н, s), 6,99 (1Н, s), 3,81 (3Н, s), 3,403,35 (4Н, m), 2,00-1,95 (4Н, m). Темп.пл. 179-180°С Приклад 58 3-Хлор-N-(5,6-дихлор-3-метокси-2-піразиніл)-2метилбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 3 Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 2,3-дихлорбензолсульфонілхлорид (0,15г). Вихід 0,12г. m/е 402(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,31 (1Н, d), 7,81 (1Н, br s), 7,72 (1Н, d), 7,45 (1Н, t), 4,05 (3Н, s). Темп.пл. 172173°С Приклад 60 2-Хлор-N-(5,6-дихлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 2хлорбензолсульфонілхлорид (0,13г). Вихід 0,096 г. m/е 367(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,39 (1Н, d), 7,79 (1Н, br s), 7,58-7,45 (3Н, m), 4,04 (3Н, s). Темп.пл. 217-218°С Приклад 61 3-Хлор-N-(5,6-дихлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 3хлорбензолсульфонілхлорид (0,13г). Вихід 0,047г. m/е 367(М-r, 100%) 1 Н ЯМР (CDCI3) d 8,19 (1Н, s), S,07 (1Н, d), 7,61 (1Н, d), 7,59 (1Н, br s), 7,50 (1Н, t), 4,02 (3Н, s). Темп.пл. 171-172°С Приклад 62 4-Хлор-N-(5,6-дихлор-3-метокси-2піразиніл)бенздлсульфонамід 47 79255 Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 4хлорбензолсульфонілхлорид (0,13г). Вихід 0,9г. m/е 367(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,11 (2Н, d), 7,57 (1Н, br s), 7,50 (2Н, d), 4,02 (3Н, s). Темп.пл. 186-187°С Приклад 63 2,4-Дихлор-N-(5,6-дихлор-3-метокси-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6-дихлор-3-метокси-2-піразинамін (0,1г) та 2,4-дихлорбензолсульфонілхлорид (0,15г). Вихід 0,076г. m/е 402(М-I+, 100%) 1Н ЯМР (CDCI3) d 8,30 (1Н, d), 7,76 (1Н, brs), 7,50 (1Н, s), 7,48 (1Н, d), 4,05 (3Н, s). Темп.пл. 171172°С Приклад 64 3,4-Дихлор-N-(5,6-дихлор-3-метокси-2піразиніл)бензолсульфонамід Отриманииіииииим прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 5,6дихлор-3-метокси-2-піразинамін (0,1г) та 3,4дихлорбензолсульфонілхлорид (0,15г). Вихід 0,11г. m/е 402(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,30 (1Н, s), 8,01 (1Н, d), 7,63 (1Н, d), 7,58 (1Н, br s), 4,03 (3Н, s) Темп.пл. 189191°С Приклад 65 2,3-Дихлор-N-(3-метокси-5,6-диметил-2піразиніл)бензолсульфонамід 48 Отримано способом прикладу 1, використовуючи 3-метокси-5,6-диметил-2-піразинамін (0,07г) та 2,3-дихлорбензолсульфонілхлорид (0,12г). Вихід 0,04г. m/е 360(М-І+, 100%) 1 Н ЯМР (CDCI3) d 8,32 (1Н, d), 7,67 (1Н, s), 7,65 (1Н, d), 7,39 (1Н, t), 3,95 (3Н, s), 2,28 (3Н, s), 2,14(3H, s). Темп.пл. 165-166°С Приклад 66 2,3-Дихлор-N-(6-хлор-335-диметокси-2піразиніл)бензолсульфонамід а) 2,3-Дихлор-N-(5,6-дихлор-3-метокси-2піразиніл)-N-{[2-(триметилсиліл)стокси]метил}бензолсульфонамід До перемішуваного розчину 2,3-Дихлор-N-(5,6дихлор-3-метокси-2піразиніл)бензолсульфонаміду (0,68г) у ди хлорметані (20мл) додавали триетиламін (0,491мл), а потім 2-(триметилсиліл)етоксиметилхлорид (0,328г) та утворену суміш перемішували при кімнатній температурі протягом 1 години. Реакційну суміш виливали у воду (50мл) та ек страгували в етилацетат (3´20мл). Поєднані екстракти сушили безводним сульфатом магнію, фільтрували та концентрували. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,74г). 1 Н ЯМР (CDCI3) d 8,02 (1Н, dd), 7,70 (1Н, dd), 7,34 (1Н, t), 5,22 (2Н, s), 3,96 (3Н, s), 3,73 (2Н, dd), 0,91-0,79 (2Н, m), -0,03(9Н, s) b) 2,3-Дихлор-N-(6-хлор-3,5-диметокси-2піразиніл)бензолсульфонамід 2,3-Дихлор-N-5,6-дихлор-3-метокси-2піразиніл)-N-{[2-(триметилсиліл)етокси]метил}бензолсульфонамід (0,10г) розчиняли у метанолі (1,0мл) та додавали розчин натрій метоксиду у метанолі (0,1мл 25% розчин у метанолі). Реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин та концентрували. Залишок розчиняли у трифлуороцтовій кислоті (2,0мл) та перемішували при кімнатній температурі протягом 30 хвилин. Реакційну суміш концентрували, а хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,028г). m/е 397(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,26 (1Н, d), 7,69 (1Н, d), 7,41 (1Н, t), 7,41 (1Н, brs), 4,02 (3Н, s), 3,91 (3Н, s). Темп.пл. 163-165°С Приклад 67 2,3-Дихлор-N-6-хлор-3-метокси-5-(4 49 морфолініл)-2-піразиніл]бензолсульфонамід 79255 2,3-Дихлор-N-(5,6-дихлор-3-метокси-2піразиніл)-N-{[2-(триметилсиліл)етокси]метил}бензолсульфонамід (Приклад 66 етап а) (0,10г) розчиняли у тетрагідрофурані (1,0мл) та до давали розчин морфоліну (0,05г) у тетрагідрофурані (0,1мл). Реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин та концентрували. Залишок розчиняли у триф луороцтовій кислоті (2,0мл) та дихлорметані (2,0мл) і перемішували при кімнатній температурі протягом 30 хвилин. Реакційну суміш концентрували, а хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,042г). m/е 452(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,28 (1Н, dd), 7,69 (1Н, dd), 7,49 (1Н, br s), 7,43 (1Н, t), 3,96 (3Н, s), 3,79 (4Н, dd), 3,2S (4H, dd). Темп.пл. 150-151°С Приклад 68 2,3-Дихлор-N-[6-хлор-5-гідроксіетиламіно)-3метокси-2-піразиніл]бензолсульфонамід Отримано способом прикладу 67, використовуючи 2-аміноетанол (0,05г) та 2,3-дихлор-N-(5,6дихпор-3-метокси-2-піразиніл)-N-{[2(триметилсиліл)етокси]метил}бензолсульфонамід (0,1г). Вихід 0,015г. m/е 426(М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 10,31 (1Н, s), 7,91 (2Н, dd), 7,52 (1Н, t), 6,89 (1Н, br s), 4,71 (1Н, t), 3,63 (3Н, s), 3,53 (2Н, dd), 3,40 (2Н, dd) Приклад 69 2,3-Дихлор-N-[6-хлор-5-диметиламіно-3метокси-2-піразиніл]бензолсульфонамід Отримано способом прикладу 67, використовуючи диметиламін (5мл 2М розчину у тетрагідрофурані) та 2,3-дихлор-N-(5,6-дихлор-3метокси-2-піразиніл)-N-{[2-(триметилсиліл)етокси]метил}бензолсульфонамід (0,1г). Вихід 0,015г. m/e 410(М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 7,99-7,93 (2Н, m), 7,56 (1Н, t), 3,74 (3Н, s), 2,99 (6Н, s) Темп.пл. 145-146°С Приклад 70 2,3-Дихлор-N-[6-хлор-3-метокси-5-(2метоксіетокси)-2-піразиніл]бензолсульфонамід 50 Натрій гідрид (0,019г 60% дисперсії у маслі) додавали до розчину 2,3-дихлор-N-(5,6-дихлор-3метокси-2-піразиніл)-N-{[2(триметилсиліл)етокси]метил}бензолсульфонаміду (0,25г) у 2-метоксіетанолі (3,0мл) при кімнатній температурі. Через 16 годин розчинник випарювали та додавали трифлуороцтову кислоту (2,0мл). Через 1 годину реакційну суміш концентрували та хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,08г). m/е 442(М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,24 (1Н, dd), 7,70 (1Н, dd), 7,41 (1Н, t), 4,50-4,40 (2Н, m), 3,96 (3Н, s), 3,803,70 (2Н, m), 3,42 (3Н, s). Темп.пл. 193-194°С Приклад 71 2,3-Дихлор-N-[6-хлор-5-гідрокси-3-метокси-2піразиніл]бензолсульфонамід Тетрабутиламоній гідроксид (0,28г 40% водного розчину) додавали до розчину 2,3-дихлор-N(5,6-дихлор-3-метокси-2-піразиніл)-N-[[2(триметилсиліл)етокси]метил)бензолсульфонаміду (0,25г) в 1,2-диметоксіетані (3,0мл) при кімнатній температурі. Через 16 годин розчин розбавляли етилацетатом (20мл). Органічний розчин промивали водною ли монною кислотою (10мл) та розсолом, сушили сульфа том магнію та випарювали. Хроматог рафія на силікагелі, елюючи сумішшю ізогексан/етилацетат, дала позначену сполуку з вмістом групи SEM як білий твердий продукт (0,08г). Твердий продукт розчиняли у трифлуороцтовій кислоті (2,0мл) та дихлорметані (2,0мл) і перемішували при кімнатній температурі протягом 1 години. Реакційну суміш концентрували, а хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,027г). m/e 384(M+1+, 100%) 1 H ЯМР (CDCI3) d 12,56 (1Н, s), 10,87 (1Н, s), 7,96 (2Н, t), 7,56 (1Н, t), 3,74 (3Н, s) Приклад 72 2,3-Дихлор-М-[6-метокси-5([2,2']дипіразиніліл)]бензолсульфонамід 51 79255 52 N-(5-Бром-3-метокси-2-піразиніл)-2,3-дихлорПриклад 75 N-[{2-(триметилсиланіл)етокси}метил]2,3-Дихлор-N-{6-хлор-3-метокси-5-([2бензолсульфонамід (Приклад 55 етап а) (0,70г), метоксіетил)аміно]-2-піразиніл}тетракіс(трифенілфосфін)паладіи(0) (0,1г) та 2бензолсульфонамід (трибутилстананіл)піразин (0.S0 г) у толуол (20мл) гріли під азотом при 100°С. Через 16 годин хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, захищену групою SEM, як білий твердий продукт. Твердий продукт розчиняли у три-флуороцтовій кислоті (2,0мл) та дихлорметані (2,0мл) та перемішували при кімнатній тем пературі протягом 1 Отримано способом прикладу 67, використогодини. Реакційну суміш концентрували, додавали вуючи 2-метоксіетиламін (3мл) та 2,3-дихлор-Nта випарювали толуол. Позначену сполуку криста(5,6-дихлор-3-метокси-2-піразиніл)-N-([2лізували з ацетонітрилу, отримуючи білий твердий (триметилсиліл)етокси]метил}-бензолсульфонамід + продукт (0,38г). m/е 410(М-I ,100%) (0,24г). Вихід 0,08г. m/е 439(М+1+, 100%) 1 1 Н ЯМР (D6-ДМСО) d 9,35 (1Н, s), 8,69 (1Н, d), Н ЯМР (D6-ДMCO) d 10,33 (1Н, s), 7,92 (2Н, 8,67 (1Н, d), 8,40 (1Н, br s), 8,14 (1Н, d), 7,96,(1 dd), 7,52 (1Н, t), 7,00 (1Н, s), 3,64 (3Н, s), 3,47 (4Н, H,d), 7,61 (1H, t), 4,07 (3H,s). Темп.пл. 199-200°С s), 3,24 (2Н, dd). Темп.пл. 177-178°С Приклад 73 Приклад 76 4-[5-(2,3-Дихлорбензолсульфоніламіно)-6N-{2-[3-Хлор-5-(2,3метокси-2-піразинілокси]бензойна кислота дихлорбензолсульфоніламіно)-6-метокси-2піразиніл)аміно]етил}ацетамід 4-Гідроксибензойної кислоти трет-бутиловий естер (0,13г), N-(5-бром-3-метокси-2-піразиніл)-2,3дихлор-N-[{2(метилсиланіл)етокси}метил]бензолсульфонамід (Приклад 55 етап а) (0,35г) та цезій карбонат (0,42г) в ацетонітрилі (10мл) гріли при 50°С. Через 12 годин су міш розбавляли етилацетатом, промивали водою, сушили безводним сульфатом магнію та випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, захищену гр упою SEM та третбутилом, як масло. Масло розчиняли у трифлуороцтовій кислоті (2,0мл) та перемішували при кімнатній температурі протягом 3 годин. Реакційну суміш концентрували, додавали та випарювали толуол, отримуючи позначену сполуку, як білий твердий продукт (0,19г). m/е 468(М-I+, 100%) 1 Н ЯМР (CDCI3) d 8,28 (1Н, d), 8,11 (2Н, d), 7,80 (1Н. brs), 7,71 (1Н, d), 7,45 (2Н, m), 7,12 (2Н, d), 3,89 (3Н, s). Темп.пл. 186-187°C Приклад 74 2,3-Дихлор-N-(3,5-дихлор-2піразиніл)бензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), використовуючи 3,5-дихлор-2-піразинамін (2,0г) та 2,3-дихлор бензолсульфонілхлорид (2,94г). Вихід 3,0г. m/е 372(М-I+, 100%) 1 Н ЯМР (D6 ДМСО) d 8,29 (1Н, s), 8,06 (1Н, dd), 7,94 (1Н, dd), 7,57.(1Н, t). Темп.пл. 181-182°С 2,3-Дихлор-N-(5,6-дихлор-3-метокси-2піразиніл)-N-{[2-(триметилсиліл)етокси]метил}бензолсульфонамід (Приклад 66 етап а) (0,26г) розчиняли в ацетонітрилі (1,0 мл) та Nацетилетилендіаміні (0,055мл) та додавали триетиламін (0,19мл). Через 48 годин реакційну суміш концентрували, а хроматографія на силікагелі, елюючи етилацетатом, дала позначену сполуку, захищену групою SEM, як масло (0,13г). Масло розчиняли у дих-лорметані (2,0мл) та додавали етерат трифлуориду бор у (0,14мл). Через 2 години дода вали етилацетат (20мл) та суміш промивали 5% водною лимонною кислотою (5мл), сушили безводним сульфатом магнію та випарювали. Хроматографія на силікагелі, елюючи етилацетат дала позначену сполуку, як твердий продукт (0,031г). m/е 470(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 10,32 (1Н, s), 7,93-7,88 (2Н, т), 7,52 (1Н, t), 7,10 (1Н, s), 3,65 (ЗН, s), 3,403,10 (4Н, m), 1,75 (3Н, s). Темп.пл. 150-152°С Приклад 77 2,3-Дихлор-N-[5-(4-гідроксиметил-1піперидиніл)-3-метокси-2-піразиніл]бензолсульфонамід Отримано способом прикладу 55, використовуючи 4-(гідроксиметил)піперидин (0,4г) та N-(5бром-3-метокси-2-піразиніл)-2,3-дихлор-N-[(2(триметилсиланіл)етокси}метил] 53 79255 54 бензолсульфонамід (0,3г). Вихід 0,012 піразиніл)бензолсульфонамід г.m/е447(М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,14 (1Н, dd), 7,65 (1Н, dd), 7,33 (1Н, t), 7,20 (1Н, s), 4,20-4,10 (2Н, m), 3,86 (ЗН, s), 3,60-3,50 (2Н, m), 2,90-2,70 (2Н, m), 1,90-1,70 (3Н, m), 1,40-1,20 (3Н, m) Приклад 78 2,3-Дихлор-N-[5-ціано-3-(3-піридинілметокси)2-піразиніл]бензолсульфонамід N-(5-Бром-3-метокси-2-піразин1л)-2,3-дихлор N-[5-Бром-3-(3-піридинілметокси)-2-піразиніл]2,3-дихлорбензолсульфонамід (Приклад 34) (0,15г), тетракіс(трифенілфосфін)паладій(0) (0,04г) та цинк ціанід (0,03г) у N,N-диметилформаміді (5,0мл) філи при 70°С. Через 5 годин суміш розбавляли етилацетатом (30мл) та промивали 5% водною лимонною кислотою (5мл), сушили безводним сульфатом магнію та випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, що містить 1% оцтової кислоти, дала позначену сполуку, як білий твердий продукт (0,058г). m/е 436(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,70 -7,65 (2Н, m), 8,29 (1Н, dd), 7,99 (1Н, s), 7,78 (1Н, d), 7,73 (1Н, dd), 7,46 (1Н, t), 7,40-7,35 (1Н, m), 5,45 (2Н, s). Темп.пл. 222-224°С Приклад 79 2,3-Дихлор-N-(6-хлор-3-метокси-5-метиламіно2-піразиніл)бензолсульфонамід 3-Дихлор-Т-(5,6-дихлор-3-метокси-2піразиніл)-N-{[2-(триметилсиліл)етокси]метил}бензолсульфонамід (Приклад 66 етап а) (0,25г) розчиняли у метанолі (1,0мл) та додавали метиламін (2,0мл 40% водного розчину). Через 16 годин розчин розподіляли між водою та етилацетатом. Органічний шар сушили безводним сульфатом магнію та випарювали. Зали шок розчиняли у дихлорметані (2,0мл) та додавали етерат трифлуориду бору (0,25мл). Че рез 1 годину додавали етилацетат (20мл) та розчин промивали 5% водною лимонною кислотою (5мл), сушили безводним сульфатом магнію та випарювали. Хроматографія на силікаге лі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,05г). m/е 395(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 10,27 (1Н, s), 7,95-7,87 (2Н, m), 7,51 (1Н, dd), 7,10-7,00 (1Н, m), 3,64 (3Н, s), 2,84 (3Н, s). Темп.пл. 185-186°С Приклад 80 2,3-Дихлор-N-(3-метокси-5-метилсульфаніл-2 N-{[2-(триметилсиланіл)етокси]метил}бензолсульфонамід (0,30г) та натрій тіометоксид (0,05г) в ацетонітрилі (10мл) перемішували при кімнатній температурі. Через 2 години розчин випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку з приєднаною групою SEM. Сполуку розчиняли у трифлуороцтовій кислоті (5мл). Через 2 години додавали толуол (20мл) та розчин випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогек-сан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,16г). ь/е380(М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,25 (1Н, d), 7,70 (1Н, s), 7,68 (1Н, d), 7,52 (1Н, s), 7,39 (1Н, t), 4,03 (3Н, s), 2,48 (3Н, s). Темп.пл. 141-142°C Приклад 81 2,3-Диxлop-N-[5-(2,4-дифлyopфeнiл)-3мeтoкcи-2-пipaзинiл]бeнзoлcyльфoнaмiд a) 5-(2,4-дифлуорфеніл)-3-метокси-2піразинамін 5-Бром-3-метокси-2-піразинамін (0,3г), цезій флуорид (0,8г), 2,4-дифлуорбензолборонову кислоту (0,4г) та [1,1'біс(дифенілфосфіно)фероцен]паладій(ІІ) хлорид (0,04г) у метанолі (20мл) гріли при 70°С. Через 6 годин розчинник випарювали та залишок очищали хроматографією на діоксиді силіцію, елюючи сумішшю ізогексан/дихлорметан, отримуючи позначену сполуку (0,2г). b) 2,3-Дихлор-N-[5-(2,4-дифлуорфеніл)-3метокси-2-піразиніл]бензолсульфонамід Отримано способом прикладу 1, використовуючи 5-(2,4-дифлуорфеніл)-3-метокси-2-5 піразинамін (0,2г) та 2,3-дихлорбензолсульфонілхлорид (0,2г). Вихід 0,06г. m/е 444(М-I+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,15 (1Н, d), 8,05-7,95 (2Н, m), 7,93 (1Н, d), 7,60 (1Н, t), 7,45-7,35 (1Н, m), 7,30-7,20 (1Н, m), 4,03 (3Н, s). Темп.пл. 169-170°С Приклад 82 [5-(2,3-Дихлорбензолсульфоніламіно)-6метокси-2-піразинілсульфаніл]оцтової кислоти метиловий естер 55 79255 56 492(M+1+ 100%) 1 Н ЯМР (CDCI3) d 8,26 (1Н, dd), 7,73 (1Н, s), 7,69 (1Н, dd), 7,53 (1Н, s), 7,40-7,30 (3Н, m), 7,207,10 (2Н, m), 4,39 (2Н, s), 4,02 (3Н, s). Темп.пл. 119-120°С Приклад 85 2,3-Дихлор-N-[6-хлор-5-(3-гідрокси-1азетидиніл)-3-метокси-2-піразиніл]N-(5-Бром-3-метокси-2-піразин1л)-2,3-дихлорбензолсульфонамід N-[{2-(триметилсиланіл)етокси}метил]бензолсульфонамід (0,40г), меркаптооцтової кислоти метиловий естер (0,1г) та цезій кар бонат (0,6г) в ацетонітрилі (10мл) перемішували при кімнатній температурі. Через 16 годин розчин розбавляли дихлорметаном, фільтрували та випарювали. Хроматографія на силікагелі, елюючи сумішшю ізогексан/етилацетат, дала позначену сполуку з приєднаною групою SEM. Сполук розчиняли у 2,3-Дихлор-N-(5,6-дихлор-3-метокси-2трифлуороцтовій кислоті (5мл). Через 2 години піразиніл)-N{[2-(триметилсиліл)етокси]метил}толуол (20мл) до давали та розчин випарювали. бензолсульфонамід (Приклад 66 етап а) (0,20г), Хроматографія на силікагелі, елюючи сумішшю азетидин-3-ол гідрохлорид (0,082г) та триетиламін ізогексан/етилацетат, дала позначену сполуку, як (0,25мл) в ацетонітрилі (3мл) і воду (0,5мл) пере+ білий твердий продукт (0,15г). m/e 43S(M+1 , мішували при кімнатній температурі. Через 2 годи100%) ни суміш випарювали та розтирали з діетиловим 1 Н ЯМР (CDCI3) d 8,26 (1Н, dd), 7,73 (1Н, s), 7 етером. Етерний розчин випарювали та залишок ,68 (1Н, dd), 7,59 (1Н, s), 7,41 (1Н, t), 3,99 (3Н, s), розчиняли у 1 молярному розчині тетрабутиламо3,80 (2Н, s), 3,71 (3Н, s)ю Темп.пл. 152-153°С ній флуориду у те-трагідрофурані (6мл). Через 16 Приклад 83 годин реакційну суміш концентрували, а хроматог[5-(2,3-Дихлорбензолсульфоніламіно)-6рафія на илікагелі, елюючи сумішшю ізогекметокси-2-піразинілсульфаніл]оцтова кислота сан/дихлорметан, дала позначену сполуку, як білий твер дий продукт (0,024г). m/е 442(М+1+, 100%) 1 H ЯМР (D6-ДCO) d 10,58 (1Н, s), 7,92 (2Н, d), 7,54 (1Н, t), 5,66 (1Н, s), 4,49 (1Н, s) 5 4,36 (2Н, t), 3,88 (2Н, m, 3,67 (3H, s).Темп.пл. 93-95°С Приклад 86 2,3-Дихлор-N-5-метил-3-(1-окси-3піразинілметокси)-2-піразиніл]бензолсульфонамід [5-(2,3-Дихлорбензолсульфоніламіно)-6метокси-2-піразинілсульфаніл]оцтової кислоти метиловий естер (Приклад 82) (0,1г) та літію гідроксид (0,04г) у метанолі (5мл) та воду (1мл) перемішували при кімнатній температурі. Через 2 години суміш випарювали та додавали на сичену водну лимонну кислоту (5мл). Білий твердий продукт збирали, промивали водою та сушили. Вихід 0,07г. m/е 424(М+1+, 100%) 1 Н ЯМР (CDCI3) d 8,27 (1Н, dd), 7,90 (1Н, br s), 7,70 (1Н, dd), 7,61 (1Н, s), 7,40 (1Н, t), 3,98 (3Н, s), 3,80 (2Н, s). Темп.пл. 138-140°С Приклад 84 2,3-Дихлор-N-5-(2-хлорбензилсульфаніл)-3метокси-2-піразиніл]бензолсульфонамід Отримано способом прикладу 82, використовуючи 2-хлорбензилмеркаптан (0,15г) та N-(5бром-3-метокси-2-піразиніл)-2,3-дихлор-N-[(2(триметилсиланіл)етокси}метил]бензолсульфонамід (0,4г). Вихід 0,18г. m/e 2,3-Дихлор-N-[5метил-3-(3-піридинілметокси)2-піразиніл]бензолсульфонамід (Приклад 24) (0,2г) та 3-хлорпербензойну кислоту (0,35г) у дихлорметані (4мл) перемішували при кімнат ній температурі. Через 0,5 годин хроматографія на силікагелі, елюючи 5% метанолу в етила цетаті, що містить 1% оцтової кислоти, дала позначену сполуку, як білий твердий продукт (0,16г).m/е 441 (М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 11,56 (1Н, br s), 8,60 (1Н, br s), 8,18 (1Н, dt), 8,06 (1Н, dd), 7,90 20 (1Н, dd), 7,61 (1Н, brs), 7,56 (1Н, t), 7,50-7,40 (2Н, m), 5,36 (2Н, s), 2,28 (3Н, s). Темп.пл. 223-228°С Приклад 87 2,3-Дихлор-N-[5-хлор-3-(4-піридинілметокси)-2піразиніл]-бензолсульфонамід 57 79255 * Отримано способом прикладу 31b, використовуючи піридин-4-метанол (0,4г) та 2,3-дихлор-N(3,5-дихлор-2-піразиніл)бензолсульфонамід (Приклад 74) (0,4г). Вихід 0,47г. m/е445(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,63 (2Н, d), 8,08 (1Н, dd), 7,91 (1Н, dd), 7,83 (1Н, s), 7,60 (2Н, d), 7,55 (1Н, t), 5,47 (2Н, s). Темп.пл. 226-229°С з розкладанням Приклад 88 2,3-Дихлор-N-[5-хлор-3-(1-окси-4піридинілметокси)-2-піразиніл]-бензолсульфонамід Отримано способом прикладу 86, використовуючи 2,3-дихлор-N-[5-хлор-3-(4піридинілметокси)-2-піразиніл]бензолсульфонамід (Приклад 87) (0,1г). Вихід 0,4г. m/е 462(М+1+,100%) 'Н ЯМР (D6-ДМСО) d 8,27 (2Н, dt), 8,07 (1Н, dd), 7,92 (1Н, dd), 7,85 (1Н, s), 7,60 (2Н, d), 7,57 (1H,t), 5,38 (2Н, s). Темп.пл. 208-211°С з розкладанням Приклад 89 2,3-Дихлор-N-[5-хлор-3-(2-піридинілметокси)-2піразиніл] Отримано способом прикладу 31b, використовуючи піридин-2-метанол (0,2г) та 2,3-дихлор-N(3,5-дихлор-2-піразиніл)бензолсульфонамід (Приклад 74) (0,2г). Вихід 0,1г. m/е445(М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,58 (1Н, dt), 8,08 (1Н, dd), 7,92 (1Н, dd), 7,80-7,90 (2Н, m), 7,64 (1Н, d), 7,56 (1Н, t), 7,18-7,20 (1Н, m), 5,47 (2Н, s).Темп.пл. 147-14S°C Приклад 90 2,3-Дихлор-N-[5-хлор-3-(2метилсульфанілетокси)-2піразиніл]бензолсульфонамід 58 Виготовлено способом прикладу 31, використовуючи 2-метилсульфанілетанол (0,05г) та 2,3дихлор-N-(3,5-дихлор-2піразиніл)бензолсульфонамід (Приклад 74) (0,1г). Вихід 0,06г. m/e 427(М-I+, 100%) 1 Н ЯМР (D6-ДМСО) d 11,50-12,00 (1Н, brs), 8,09 (1Н, d), 7,95 (1Н, d), 7,81 (1Н, s), 7,60 (1Н, t), 4,47 (2Н, t), 2,86 (2Н, t), 2,14 (3Н, s). Темп.пл. 140141°С Приклад 91 N-(3-Бутокси-5-хлор-2-піразиніл)-2,3дихлорбензолсульфонамід Отримано способом прикладу 31, використовуючи 1-бутанол (0,05г) та 2,3-дихлор-N-(3,5дихлор-2-піразиніл)бензолсульфонамід (Приклад 74) (0,1г). Вихід 0,037г. m/е410(М+1+, 100%) 1 Н-ЯМР (D6-ДMCO) d 8,08 (1Н, d), 7,96 (1Н, d), 7,79 (1Н, s), 7,57 (1Н,1), 4,29 (2Н, t), 1,60-1,75 (2Н, m), 1,40-1,50 (2Н, m), 0,95 (3Н, t), Темп.пл. 133134°С Приклад 92 2,3-Дихлор-N-[5-хлор-3-(2-метил-3піридинілІметокси)-2-піразиніл]бензолсульфонамід Отримано способом прикладу 31, використовуючи (2-метил-3-піридиніл)метанол (0,15г) та 2,3дихлор-N-(3,5-дихлор-2піразиніл)бензолсульфонамід (Приклад 74) (0,15г). Вихід 0,06г. m/e 458(M+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,45 (1Н, dd), 8,05 (1Н, dd), 7,94 (1Н, dd), 7,88 (1Н, dd), 7,80 (1Н, s), 7,53 (1Н, t), 7,32 (1Н, dd), 5,40 (2Н, s), 2,56 (3Н, s). Темп.пл. 214-216°С з розкладанням Приклад 93 2;3-Дихлор-М-[5-хлор-3-(6-метил-2піридинілметокси)-2-піразиніл]-бензолсульфонамід 59 79255 Отримано способом прикладу 31, використовуючи (6-метил-2-піридиніл)метанол (0,15г) та 5 2,3-дихлор-М-(3,5-дихлор-2піразиніл)бензолсульфонамід (Приклад 74) (0,15г). Вихід 0,06г. m/е 461(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,08 (1Н, dd), 7,91 (1Н, dd), 7,84 (1Н, s), 7,75 (1Н, t), 7,55 (1Н, t), 7,42 (1Н, d), 7,24 (1Н, d), 5,42 (2Н, s), 2,52 (3Н, s)ю Темп.пл. 158-159°С Приклад 94 2,3-Дихлор-N-[5-хлор-3-(1-окси-2піридинілметокси)-2-піразиніл]-бензолсульфонамід Отримано способом прикладу 86, використовуючи 2,3-дихлор-N-[5-хлор-3-(2піридинілметокси)-2-піразиніл]бензолсульфонамід (Приклад 89) (0,2г). Вихід 0,1г. m/е 462(М+1+,100%) 1 Н ЯМР (D6-ДMCO) d 8,35-8,40 (1Н, m), 8,09 (1Н, dd)5 7,80-7,90 (2Н, m), 7,88 (1Н, s), 7,58 (1Н, t), 7,40-7,50 (2Н, m), 5,51 (2Н, s). Темп.пл. 222-224°С з розкладанням Приклад 95 3-Хлор-N-[5-хлор-3-(3-піридинтметокси)-2піразинт]-2-5 метилбензолсульфонамід а) 5-Хлор-3-(3-піридинілметокси)-2-піразинамін 3,5-Дихлор-2-піразинамін (1,0г) додавали до перемішуваної суспензії піридин-3-метанолу (1,3г) та натрій гідриду (0,70г 60% дисперсії у маслі) у 1,2-диметоксіетані (10мл). Через 0,5 годин додавали 5% водну лимонну кислоту та суміш екстрагували етилацетатом. Хроматографія на силікагелі, елюючи сумішшю ізогексан/дихлорметан, дала позначену сполуку, як білий твердий продукт (0,2г). Застосовували безпосередньо. b) 3-Хлор-N-[5-хлор-3-(3-піридинілметокси)-2піразиніл]-2-метилбензолсульфонамід 60 Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), викорис товуючи 5-хлор-3-(3-піридинілметокси)-2-піразинамін (Приклад 95а) (0,1г) та 3-хлор-2метилбензолсульфонілхлорид (0,09г). Вихід 0,012г. m/е 425. (М+1+, 100%) 1 Н ЯМР (D6-ДМСО) d 8,78 (1Н, d), 8,58 (1Н, dd), 7,96 (2Н, dt), 7,83 (1Н, s), 7,72 (1Н, d), 7,46 (1Н, dd), 7,40 (1Н, t), 5,44 (2Н, s), 2,63 (3Н, s). Темп.пл. 192-193°С Приклад 96 3-Хлор-N-[5-хлор-3-(3-піридинілметокси)-2піразиніл]-2-флуорбензолсульфонамід Отримано способом прикладу 1 (реакцію проводять при кімнатній температурі), викорис товуючи 5-хлор-3-(3-піридинілметокси)-2-піразинамін (Приклад 95а) (0,1г) та 3-хлор-2флуорбензолсульфонілхлорид (0,1г). Вихід 0,034г. m/е 429(М+1+, 100%) 1 Н ЯМР (D6-ДMCO) d 8,78 (1Н, d), 8,60 (1Н, dd), 7,99 (1Н, dt), 7,80-7,90 (3Н, т), 7,48 (1Н, dd), 7,40 (1H, t), 5,43 (2Н, s). Темп.пл. 177-178°С Приклад 97 2,3-Дихлор-N-[5-хлор-3-(4метоксифенілметокси)-2-піразиніл] бензолсульфонамід Отримано способом прикладу 31, використовуючи 4-метокЬибензиловий спирт (0,3г) та 2,3дихлор-N-(3,5-дихлор-2піразиніл)бензолсульфонамід (Приклад 74) (0,5г). Вихід 0,4г. m/e 475 (M+1 +, 100%) 1 Н ЯМР (D6-ДMCO) d 8,05 (1Н, dd), 7,91 (1Н, dd), 7,81 (1Н, s), 7,58 (1Н, t), 7,42 (2Н, d), 6,94 (2Н, d), 5,32 (2Н, s), 3,77 (3Н, s) Темп.пл. 163-164°С Приклад 98
ДивитисяДодаткова інформація
Назва патенту англійськоюN-pyrazinyl-phenylsulphonamides, process for the preparation thereof (variants), pharmaceutical composition based thereon, process for the preparation thereof, method for treatment of chemokine mediated disease, method for treatment of inflammatory disease
Автори англійськоюStocks Michael
Назва патенту російськоюN-пиразинилфенилсульфонамиды, способ их получения (варианты), фармацевтическая композиция на их основе, способ ее получения, способ лечения опосредованной хемокином болезни, способ лечения воспалительного заболевания
Автори російськоюСтокс Майкл
МПК / Мітки
МПК: A61P 35/00, A61P 3/10, C07D 413/12, A61P 13/12, A61P 15/02, A61P 31/18, C07D 403/04, A61P 25/00, C07F 7/08, A61P 25/06, A61P 31/04, A61P 19/06, A61P 17/04, A61K 31/4965, A61P 7/02, A61P 15/00, A61K 31/501, A61P 17/02, A61P 9/10, A61K 31/506, C07D 521/00, A61P 11/00, A61P 5/14, A61P 1/04, A61P 25/28, A61K 31/5377, C07D 401/12, C07D 401/14, A61P 21/04, A61P 37/02, A61P 17/00, C07B 61/00, A61P 17/06, A61K 31/497, C07D 401/04, C07D 405/12, A61P 25/14, C07D 403/12, A61P 37/06, A61P 11/06, C07D 409/12, A61P 19/02, A61P 37/08, C07D 241/22, A61P 11/02, A61P 29/00, A61P 31/12
Мітки: спосіб, композиція, одержання, варіанти, запальної, основі, опосередкованої, фармацевтична, хвороби, лікування, n-піразинілфенілсульфонаміди, хемокіном
Код посилання
<a href="https://ua.patents.su/54-79255-n-pirazinilfenilsulfonamidi-sposib-kh-oderzhannya-varianti-farmacevtichna-kompoziciya-na-kh-osnovi-sposib-oderzhannya-sposib-likuvannya-oposeredkovano-khemokinom-khvorobi-sposib-li.html" target="_blank" rel="follow" title="База патентів України">N-піразинілфенілсульфонаміди, спосіб їх одержання (варіанти), фармацевтична композиція на їх основі, спосіб її одержання, спосіб лікування опосередкованої хемокіном хвороби, спосіб лікування запальної хвороби</a>












