Заміщені 4-арил-1,4-дигідро-1,6-нафтиридинаміди і їх застосування
Номер патенту: 102065
Опубліковано: 10.06.2013
Автори: Альбрехт-Кюппер Барбара, Берфаккер Ларс, Кляйн Мартіна, Гроссер Рольф, Хартманн Ельке, Мюнтер Клаус, Шлєммер Карл-Хайнц, Колькхоф Петер, Ніче Адам
Формула / Реферат
1. Сполука формули (І)
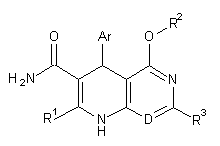 , (I)
, (I)
в якій
D означає CR4, де
R4 означає водень або (С1-С4)-алкіл,
Аr означає групу формули
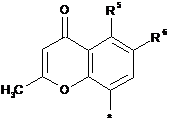 або
або 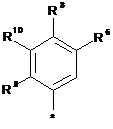 ,
,
в якій
*означає місце приєднання,
R5 означає водень,
R6 означає водень,
R8 означає ціано,
R9 означає (С1-С4)-алкокси, який може бути відповідно до 3 разів заміщений фтором,
R10 означає водень,
R1 означає (С1-С4)-алкіл, який може бути до 3 разів заміщений фтором,
R2 означає (С1-С6)-алкіл,
R3 означає водень або (С1-С4)-алкіл,
або її фармацевтично прийнятна сіль.
2. Сполука формули (І) за пунктом 1, в якій
D означає C-R4, де
R4 означає водень або метил,
Аr означає групу формули
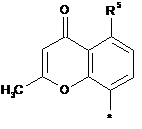 або
або 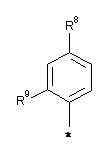 ,
,
в якій
* означає місце приєднання, R5 означає водень,
R8 означає ціано, та
R9 означає (С1-С4)-алокси або трифторметокси,
R1 означає метил або трифторметил,
R2 означає (С1-С4)-алкіл,
R3 означає водень або метил,
або її фармацевтично прийнятна сіль.
3. Сполука формули (І) за пунктом 1 або 2, в якій
D означає C-R4, де R4 означає водень або метил,
Аr означає групу формули
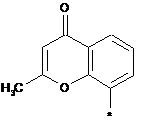 або
або 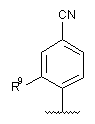 ,
,
в якій
* означає місце приєднання та
R9 означає метокси або трифторметокси,
R1 означає метил або трифторметил,
R2 означає метил, етил, н-пропіл або ізопропіл, та
R3 означає водень або метил,
або її фармацевтично прийнятна сіль.
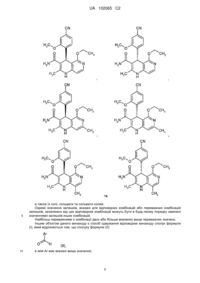
4. Сполука за будь-яким з пунктів 1, 2 або 3, яка має структуру, вибрану з групи, що складається з:
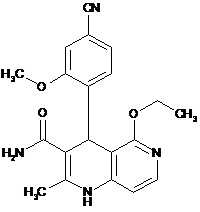 ,
, 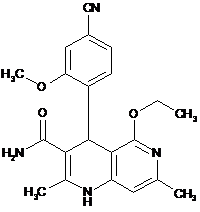 ,
,
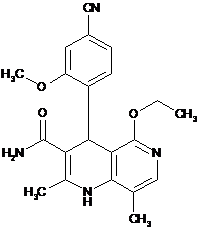 ,
,
або її фармацевтично прийнятна сіль.
5. Сполука за будь-яким з пунктів 1, 2, 3 або 4, яка має структуру, вибрану з групи, що складається з:
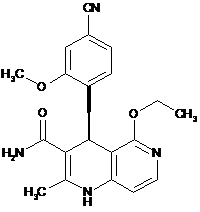 ,
, 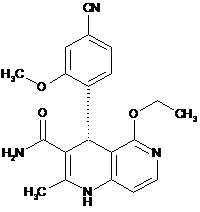 ,
,
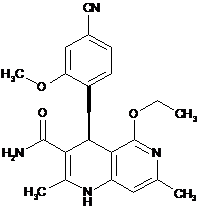 ,
, 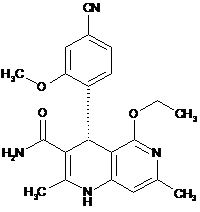 ,
,
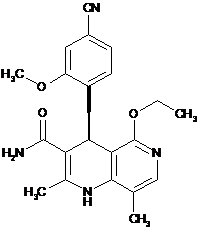 та
та 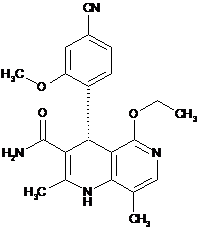 ,
,
або її фармацевтично прийнятна сіль.
6. Спосіб одержання сполук формули (І), визначених у пунктах 1-5, який відрізняється тим, що сполуку формули (II)
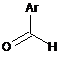 , (II)
, (II)
в якій Аr має вказані у пунктах 1-5 значення, у інертному розчиннику піддають взаємодії зі сполукою формули (III)
 , (III)
, (III)
в якій R1 має вказані у пунктах 1-5 значення, а
Т означає аліл або 2-ціаноетил,
з одержанням сполуки формули (IV)
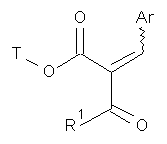 , (IV)
, (IV)
в якій Аr, Т та R1, відповідно, мають вказані вище значення, яку після цього конденсують в інертному розчиннику зі сполукою формули (V)
 , (V)
, (V)
в якій D та R3 мають вказані у пунктах 1-5 значення,
з одержанням сполуки формули (VI)
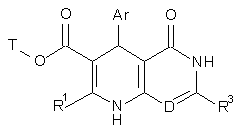 , (VI)
, (VI)
в якій Аr, D, T, R1 та R3, відповідно, мають вказані вище значення, після чого сполуки формули (VI) в інертному розчиннику алкілують сполукою формули (VII) або триалкілоксонієвою сіллю формули (VIII)
![]() ,
,
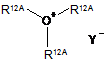 ,
,
(VII)
(VIII)
в яких
R12 означає (С1-С6)-алкіл,
R12A означає метил або етил,
X означає групу, що відщеплюється, таку як, наприклад, галоген, мезилат, тозилат або трифлат, та
Y- означає ненуклеофільний аніон, такий як, наприклад, тетрафторборат, або в присутності кислоти алкілують триалкілортоформіатом формули (IX)
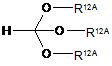 , (IX)
, (IX)
в якій R12A має вказані вище значення, з одержанням сполуки формули (Х-А)
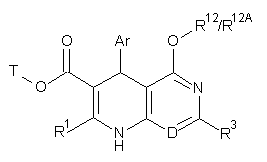 , (Х-А)
, (Х-А)
в якій Аr, D, Т, R1, R3 та R12 або R12A, відповідно, мають вказані вище значення, після чого у сполуках формули (Х-А) естерну групу Т відщеплюють з одержання карбонових кислот формули (XII)
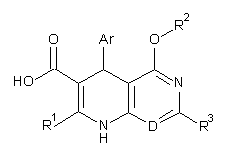 , (XII)
, (XII)
в якій Аr, D, R1, R2 та R3, відповідно, мають вказані у пунктах 1-5 значення, після чого за допомогою 1,1'-карбонілдіімідазолу переводять у імідазолід формули (XIII)
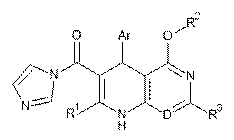 , (XIII)
, (XIII)
в якій Аr, D, R1, R2 та R3, відповідно, мають вказані вище значення,
та ці сполуки у інертному розчиннику піддають взаємодії з аміаком з одержанням амідів формули (І),
та кінцевий продукт виділяють у вільний формі або як фармацевтично прийнятну сіль або у формі енантіомера та/або діастереомеру.
7. Спосіб за пунктом 6, який відрізняється тим, що взаємодію сполуки формули (II) зі сполукою формули (III) здійснюють в присутності кислоти, комбінації кислота/основа та/або дегідратуючого засобу.
8. Спосіб за пунктом 6 або 7, який відрізняється тим, що взаємодію сполуки формули (VI) зі сполукою формули (VII) здійснюють в присутності основи.
9. Спосіб за одним із пунктів 6-8, який відрізняється тим, що взаємодію сполуки формули (XIII) з аміаком здійснюють в присутності допоміжної основи.
10. Застосування сполуки формули (І), визначеної в одному з пунктів 1-5, для одержання лікарського засобу для лікування та/або профілактики альдостеронізму, артеріальної гіпертонії, хронічної серцевої недостатності, наслідків інфаркту міокарда, цирозу печінки, ниркової недостатності та апоплексії.
11. Фармацевтична композиція, яка має властивості антагоніста селективного до мінералокортикоїдного рецептора, що містить сполуку формули (І), визначену в одному з пунктів 1-5, у комбінації з інертною нетоксичною фармацевтично прийнятною допоміжною речовиною.
12. Фармацевтична композиція за пунктом 11 для лікування та/або профілактики альдостеронізму, артеріальної гіпертонії, хронічної серцевої недостатності, наслідків інфаркту міокарда, цирозу печінки, ниркової недостатності та апоплексії.
13. Спосіб лікування або профілактики альдостеронізму, артеріальної гіпертонії, хронічної серцевої недостатності, наслідків інфаркту міокарда, цирозу печінки, ниркової недостатності та апоплексії у людей та тварин, в якому призначають ефективну кількість щонайменше однієї сполуки формули (І), визначеної у одному з пунктів 1-5, або фармацевтичну композицію, визначену в одному з пунктів 11 або 12.
Текст
Реферат: Даний винахід стосується нових заміщених 4-арил-1,4-дигідро-1,6-нафтиридин-3-карбоксамідів, способів їх одержання, їх застосування для лікування та/або профілактики захворювань, а також їх застосування для одержання лікарських засобів для лікування та/або профілактики захворювань, зокрема серцево-судинних захворювань. UA 102065 C2 (12) UA 102065 C2 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід стосується нових заміщених 4-арил-1,4-дигідро-1,6-нафтиридин-3карбоксамідів, способів їх одержання, їх застосування для лікування та/або профілактики захворювань, а також їх застосування для одержання лікарських засобів для лікування та/або профілактики захворювань, зокрема серцево-судинних захворювань. Альдостерон відіграє ключову роль у підтриманні рідинного та електролітичного гомеостазу шляхом сприяння утримуванню натрію та секреції калію в епітелії дистального нефрону, що підтримує постійний зовнішньоклітинний об'єм та допомагає регуляціє кров'яного тиску. Крім того альдостерон проявляє безпосередній вплив на структуру та функцію серцевої та судинної системи, причому основоположні механізми до цього часу ще повністю не розкриті [R.E. Booth, J.P. Johnson, J.D. Stockand, Adv. Physiol. Educ. 26 (1), 8-20 (2002)]. Альдостерон представляє собою стероїдний гормон, який утворюється у корі надниркової залози. Його вироблення опосередковано значним чином регулюється залежно від ниркового кровотоку. Будь-яке зменшення ниркового кровотоку приводить до викиду ферменту реніну у кровообіг. Це активує утворення ангіотензину II, який з одного боку звужує артеріальну судину, а з іншого боку стимулює утворення альдостерону у корі надниркової залози. Таким чином нирка служить так званим датчиком кров'яного тиску і таким чином опосередковано також датчиком об'єму у кровообігу та через систему ренінангіотензин-альдостерон протидіє критичним втратам об'єму, з одного боку шляхом підвищення кров'яного тиску (дія ангіотензину II), а з іншого боку шляхом балансування стану наповнення судинної системи за допомогою підсиленої реабсорбції натрію та води у нирці (дія альдостерону). Ця регуляторна система може бути порушена різними способами. Так, наприклад, хронічне недостатнє кровопостачання у нирках (наприклад, внаслідок серцевої недостатності та спричиненого нею застою крові у венозній системі) призводить до хронічно підвищеного вироблення альдостерону. Це в свою чергу спричиняє збільшення об'єму крові і таким чином підсилює серцеве захворювання через перевищення об'єму у серці. Наслідками можуть бути застій крові у легенях, ядуха та утворення набряків у кінцівках, а також асцит та плевральний випіт; нирковий кровотік продовжує зменшуватись. Крім того надмірна дія альдостерону призводить до зменшення концентрації калію в крові та зовнішньоклітинній рідині. І в без того ушкодженому міокарді може спостерігатися досягнення критичної межі смертельно небезпечних порушень серцевого ритму. У цьому необхідно шукати одну з головних причин раптової серцевої смерті, яка часто спостерігається у пацієнтів із серцевою недостатністю. Додатково альдостерон відповідає також за ряд типових у випадку серцевої недостатності процесів перетворення міокарду. Таким чином гіперальдостеронізм є вирішальним компонентом у патогенезі та прогнозі серцевої недостатності, яка може бути викликана різними порушеннями, такими як, наприклад, інфаркт міокарду, запалення міокарду або артеріальна гіпертонія. Це припущення підтверджується тим фактом, що при проведенні численних клінічних досліджень у групах пацієнтів з хронічною серцевою недостатністю або відповідно після гострого інфаркту міокарду в результаті застосування антагоністів альдостерону загальна смертність значно зменшується [В. Pitt, F. Zannad, W.J. Remme et al., N. Engl. J. Med. 341 709717(1999); B. Pitt, W. Remme, F. Zannad et al, N. Engl. J. Med. 348, 1309-1321 (2003)]. Це досягається зокрема зменшенням кількості випадків раптової серцевої смерті. Відповідно до новітніх досліджень у багатьох пацієнтів, що страждають на ессенціальну гіпертонію, знайшли так званий нормокаліємічний варіант первинного гіперальдостеронізму [переважно до 11% всіх гіпертоніків: L. Seiler und M. Reincke, Der Aldosteron-Renin-Quotient bei sekundarer Hypertonie, Herz 28, 686-691 (2003)]. Як найкращий діагностичний метод у випадку нормокаліємічного гіперальдостеронізму використовують співвідношення відповідної концентрації альдостерон/ренін у плазмі, так що відносне підвищення концентрації альдостерону у порівнянні з концентрацією реніну в плазмі можна діагностувати і лікувати. Тому гіперальдостеронізм, діагностований у зв'язку із ессенціальною гіпертонією, є відправною точкою для каузальної та профілактичної терапії. Набагато більш рідкісними, ніж наведені вище форми гіперальдостеронізму, є такі картини хвороб, в яких порушення спостерігаються у клітинах надниркової залози, що виробляють гормон, або їх кількість та вага збільшені внаслідок гіперплазії або розростання. Аденома або дифузна гіперплазія кори надниркової залози є найрозповсюдженішою причиною первинного гіперальдостеронізму, який також називають синдромом Конна, основними симптомами якого є гіпертонія та гіпокаліємічний алкалоз. І тут поряд із хірургічним видаленням ураженої тканини на першому плані знаходиться медикаментозне лікування антагоністами альдостерону [Н.А. Kühn und J. Schirmeister (Hrsg.), Innere Medizin, 4. Aufl., Springer Verlag, Berlin, 1982]. Іншою типовою картиною хвороби, пов'язаною з підвищенням концентрації альдостерону в плазмі, є прогресуючий цироз печінки. Причина підвищення концентрації альдостерону полягає 1 UA 102065 C2 5 10 15 20 25 30 35 40 переважно у обмеженому розпаді альдостерону внаслідок порушення функцій печінки. Об'ємне перевантаження, набряки та гіпокаліємія є типовими наслідками, які у клінічній практиці можуть бути успішно пом'якшені за допомогою антагоністів альдостерону. Дія альдостерону опосередкована розміщеним у цільових клітинах внутрішньоклітинним мінералокортикоїдним рецептором. Використовувані до цього часу антагоністи альдостерону, як і сам альдостерон, мають базову стероїдну структуру. При цьому обмежують використання таких стероїдних антагоністів шляхом їх взаємодії з рецепторами інших стероїдних гормонів, які частково призводять до виникнення суттєвих побічних ефектів, таких як гінекомастія та імпотенція, або спричиняють переривання терапії [М.А. Zaman, S. Oparil, D.A. Calhoun, Nature Rev. Drug Disc, 1, 621-636 (2002)]. Використання активних нестероїдних антагоністів, селективних для мінералокортикоїдного рецептора, дає можливість, уникнути таких побічних ефектів і таким чином досягти значно ефективнішого лікування. Задача даного винаходу полягала у одержанні нових сполук, які б можна було використовувати як селективні антагоністи мінералокортикоїдного рецептора для лікування захворювань, зокрема серцево-судинних захворювань. В ЕР 0 133 530-А, ЕР 0 173 933-А, ЕР 0 189 898-А та ЕР 0 234 516-А описані 4-арилзаміщені 1,4-дигідро-1,6-нафтиридини або відповідно -нафтиридинони з кальцій-антагоністичною дією для лікування захворювань судин. Фармакологічні властивості цих сполук описані зокрема в G. Werner et al., Naunyn-Schmiedeberg's Arch. Pharmacol. 344 (3), 337-344 (1991). Крім того похідні 1,4-дигідро-1,6-нафтиридину описані в WO 02/10164 як агенти відкривання калієвого каналу для лікування різних передусім урологічних захворювань. Похідні 4-флуореноніл- або 4-хроменоніл1,4-дигідропіридину як антагоністи мінералокортикоїдного рецептора описані в WO 2005/087740 та WO 2007/009670. В WO 2006/066011 описані естери та аміди 4-арил-3-ціано-1,4дигідропіридин-5-карбонової кислоти як частково подвійні модулятори рецепторів стероїдних гормонів та кальцієвого каналу L-типу, а в WO 2005/097118 описані сполуки з основною 4-арил1,4-дигідропіридиновою структурою як антагоністи альдостеронового рецептора. Об'єктом даного винаходу є сполуки загальної формули (І) в якій 4 D означає N або C-R , де 4 R означає водень, фтор, трифторметил або (С1-С4)-алкіл, Аr означає групу формули в якій * означає місце приєднання, 5 R означає водень, фтор, хлор, ціано, нітро, трифторметил або (С 1-С4)-алкіл, 6 R означає водень або фтор, 7 R означає галоген, (С1-С4)-алкіл, трифторметил, (С1-С4)-алкокси або трифторметокси, 8 R означає ціано або нітро, 9 R означає водень, галоген, (С1-С4)-алкіл, (С1-С4)-алкокси, (С1-С4)-алкілтіо або ді-(С1-С4)алкіламіно, причому алкільна група у зазначених (С1-С4)-алкільних залишках, (С1-С4)-алкокси- та (С1-С4)-алкілтіо-залишках може бути відповідно до 3 разів заміщена фтором, 2 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 або феніл, який може бути заміщений галогеном, (С 1-С4)-алкілом або трифторметилом, 10 R означає водень, галоген або (С1-С4)-алкіл, 7 Ε означає СН, C-R або N та n означає число 0, 1 або 2, 7 причому у випадку, якщо замісник R зустрічається кілька разів, його значення можуть бути однаковими або різними, 1 R означає (С1-С4)-алкіл, який може бути до 3 разів заміщений фтором, 2 R означає (С1-С6)-алкіл, який може бути заміщений (С3-С7)-циклоалкілом або до З разів 11 заміщений фтором, або групу формули -SO2-R , в якій 11 R означає (С1-С6)-алкіл, трифторметил, (С3-С7)-циклоалкіл, феніл або 5- або 6-членний гетероарил, що містить до 2 гетероатомів з ряду Ν, Ο та/або S, причому феніл та гетероарил зі свого боку можуть бути відповідно одинабо два рази однаково або по-різному заміщені галогеном, ціано, нітро, (С1-С4)-алкілом, трифторметилом, (С1-С4)-алкокси та/або трифторметокси, та 3 R означає водень, фтор, трифторметил або (С1-С4)-алкіл, а також їх солі, сольвати та сольвати солей. Сполуками згідно з винаходом є сполуки формули (І) та їх солі, сольвати і сольвати солей, охоплені формулою (І) сполуки вказаних нижче формул та їх солі, сольвати і сольвати солей, а також охоплені формулою (І) наведені нижче як приклади виконання сполуки та їх солі, сольвати і сольвати солей, якщо під охопленими формулою (І) наведеними нижче сполуками вже не мають на увазі солі, сольвати та сольвати солей. Сполуки згідно з винаходом залежно від їх структури можуть існувати у стереоізомерних формах (енантіомери, діастереомери) Тому даний винахід стосується також енантіомерів або діастереомерів та їх відповідних сумішей. Із таких сумішей енантіомерів та/або діастереомерів стереоізомерні компоненти можуть бути виділені відомими способами. Якщо сполуки згідно з винаходом можуть існувати у таутомерних формах, то даний винахід включає також всі таутомерні форми. Як солі в рамках даного винаходу переважними є фізіологічно прийнятні солі сполук згідно з винаходом. Винахід включає також солі, які самі є непридатними для фармацевтичного застосування, однак можуть бути використані, наприклад, для виділення або очищення сполук згідно з винаходом. Фізіологічно прийнятними солями сполук згідно з винаходом є кислотно-адитивні солі мінеральних, карбонових та сульфонових кислот, наприклад, солі хлорводневої, бромводневої, сірчаної, фосфорної, метансульфонової, етансульфонової, толуолсульфонової, бензолсульфонової, нафталіндисульфонової, оцтової, трифтороцтової, пропіонової, молочної, винної, яблучної, лимонної, фумарової, малеїнової та бензойної кислоти. Фізіологічно прийнятними солями сполук згідно з винаходом є також солі звичайних основ, такі як, наприклад, переважно солі лужних металів (наприклад, натрію та калію), солі лужноземельних металів (наприклад, кальцію та магнію) та амонієві солі, похідні від аміаку або органічних амінів, що містять від 1 до 16 атомів вуглецю, такі як, наприклад, переважно етиламін, діетиламін, триетиламін, етилдіізопропіламін, моноетаноламін, діетаноламін, триетаноламін, дициклогексиламін, диметиламіноетанол, прокаїн, дибензиламін, Nметилморфолін, аргінин, лізин, етилендіамін та N-метилпіперидин. Сольватами в рамках даного винаходу є такі форми сполук згідно з винаходом, які у твердому або рідкому стані шляхом координації з молекулами розчинника утворюють комплекс. Гідрати - це спеціальна форма сольватів, в яких координація відбувається з водою. Як сольвати в рамках даного винаходу переважними є гідрати. Крім того даний винахід включає також проліки сполук згідно з винаходом. Поняття "проліки" означає сполуки, які самі можуть бути біологічно активними або неактивними, однак під час свого перебування в організмі перетворюються на сполуки згідно з винаходом (наприклад, метаболічно або гідролітично). В рамках даного винаходу замісники, якщо не зазначено нічого іншого, мають такі значення: (С1-С6)-алкіл та (С1-С4)-алкіл в рамках даного винаходу означають нерозгалужений або розгалужений алкільний залишок, що містить від 1 до 6 або відповідно від 1 до 4 атомів вуглецю. Перевагу надають нерозгалуженому або розгалуженому алкільному залишку, що містить від 1 до 4 атомів вуглецю. Переважно як приклад слід назвати: метил, етил, н-пропіл, 3 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, 1-етилпропіл, н-пентил, ізопентил та нгексил. (С3-С7)-циклоалкіл в рамках даного винаходу означає моноциклічну насичену циклоалкільну групу, що містить від 3 до 7 атомів вуглецю. Перевагу надають циклоалкільному залишку, що містить від 3 до 6 атомів вуглецю. Переважно як приклад слід назвати: циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. (С1-С4)-алкокси в рамках даного винаходу означає нерозгалужений або розгалужений алкоксизалишок, що містить від 1 до 4 атомів вуглецю. Переважно як приклад слід назвати: метокси, етокси, н-пропокси, ізопропокси, н-бутокси та трет-бутокси. (С1-С4)-алкілтіо в рамках даного винаходу означає нерозгалужений або розгалужений алкільний тіозамісник, який містить від 1 до 4 атомів вуглецю. Переважно як приклад слід назвати: метилтіо, етилтіо, н-пропілтіо, ізопропілтіо, н-бутилтіо та трет-бутилтіо. (С1-С4)-алкіламіно в рамках даного винаходу означає аміногрупу, що включає два однакових або різних нерозгалужених або розгалужених алкільних замісники, які відповідно містять від 1 до 4 атомів вуглецю. Переважно як приклад слід назвати: Ν,Ν-диметиламіно, Ν,Ν-діетиламіно, N-етил-N-метиламіно, N-метил-N-н-пропіламіно, Ν,Ν-діізопропіламіно, N-ізопропіл-N-нпропіламіно, N-н-бутил-N-метиламіно та N-трет-бутил-N-метиламіно. 5- або 6-членний гетероарил в рамках даного винаходу означає ароматичний гетероцикл (гетероароматичну сполуку), що містить 5 або 6 кільцевих атомів та 1 або 2 кільцевих гетероатоми з ряду Ν, Ο та/або S та приєднаний через кільцевий атом вуглецю. Переважно як приклад слід назвати: фурил, піроліл, тіоніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, ізотіазоліл, піридин, піримідил, піридазиніл та піразиніл. Галоген в рамках даного винаходу включає фтор, хлор, бром та йод. Перевагу надають фтору або хлору. Якщо залишки у сполуках згідно з винаходом є заміщеними, то вони, якщо не зазначено нічого іншого, можуть бути заміщені один або кілька разів. В рамках даного винаходу всі залишки, які зустрічаються неодноразово, мають незалежні один від одного значення. Перевагу надають заміщенню одним, двома або трьома однаковими або різними замісниками. Найбільшу перевагу надають заміщенню одним замісником. Перевагу в рамках даного винаходу надають сполукам формули (І), в якій 4 D означає C-R , де 4 R означає водень, метил або трифторметил, Аr означає групу формули в якій * означає місце приєднання, 5 R означає водень, фтор, хлор або ціано, 8 R означає ціано або нітро та 9 R означає хлор, бром, (С1-С4)-алкіл, трифторметил, (С1-С4)-алокси, трифторметокси, (С1С4)-алкілтіо або трифторметилтіо, 1 R означає метил або трифторметил, 2 11 R означає (С1-С4)-алкіл, трифторметил або групу формули -SO2-R , в якій 11 R означає (С1-С4)-алкіл або трифторметил, та 3 R означає водень, метил або трифторметил, а також їх солям, сольватам та сольватам солей. Особливу перевагу в рамках даного винаходу надають сполукам формули (І), в якій D 4 означає C-R , де 4 R означає водень або метил, Аr означає групу формули 4 UA 102065 C2 5 10 15 в якій * означає місце приєднання та 9 R означає етил, метокси або трифторметокси, 1 R означає метил або трифторметил, 2 R означає метил, етил, н-пропіл або ізопропіл та 3 R означає водень або метил, а також їх солям, сольватам та сольватам солей. Найбільшу перевагу надають сполукам формули (І), що мають такі структури: та а також їх солям, сольватам та сольватам солей. Зокрема перевагу при цьому надають енантіомерним сполукам, що мають такі структури: 5 UA 102065 C2 5 10 а також їх солі, сольвати та сольвати солей. Окремі значення залишків, вказані для відповідних комбінацій або переважних комбінацій залишків, незалежно від цих відповідних комбінацій можуть бути в будь-якому порядку замінені значеннями залишків інших комбінацій. Найбільш переважними є комбінації двох або більше вказаних вище переважних значень. Іншим об'єктом даного винаходу є спосіб одержання відповідних винаходу сполук формули (І), який відрізняється тим, що сполуку формули (II) в якій Аr має вказані вище значення, 6 UA 102065 C2 у інертному розчиннику необов'язково в присутності кислоти, комбінації кислота/основа та/або дегідратувального агенту піддають взаємодії зі сполукою формули (III) 1 5 в якій R має вказані вище значення, а Τ означає аліл або 2-ціаноетил, до одержання сполуки формули (IV) 1 в якій Аr, Τ та R відповідно мають вказані вище значення, яку після цього конденсують в інертному розчиннику зі сполукою формули (V) 10 3 в якій D та R мають вказані вище значення, до одержання сполуки формули (VI) 1 15 20 3 в якій Аr, D, T, R та R відповідно мають вказані вище значення, після чого сполуки формули (VI) в інертному розчиннику необов'язково в присутності основи алкілюють зі сполукою формули (VII) або триалкілоксонієвою сіллю формули (VIII) в яких 12 R означає (С1-С6)-алкіл, який може бути заміщений (С3-С7)-циклоалкілом або до трьох разів заміщений фтором, 12A R означає метил або етил, X означає групу, що відходить, таку як, наприклад, галоген, мезилат, тозилат або трифлат та Y означає ненуклеофільний аніон, такий як, наприклад, тетрафторборат, або в присутності кислоти алкілюють із триалкілортоформіатом формули (IX) 7 UA 102065 C2 в якій R 12A має вказані вище значення, до одержання сполук формули (Х-А) 1 5 в якій R 10 11 12 мають вказані вище значення, до одержання сполук формули (Х-В) 1 3 11 в якій Аr, D, Т, R , R та R відповідно мають вказані вище значення, після чого у сполуках формули (Х-А) або відповідно (Х-В) естерну групу Τ відомими методами відщеплюють до одержання карбонових кислот формули (XII) 1 15 3 в якій Аr, D, Т, R , R та R відповідно мають вказані вище значення, або сполуки формули (VI) в інертному розчиннику в присутності основи піддають взаємодії зі сполукою формули (XI) 2 3 в якій Аr, D, R , R та R відповідно мають вказані вище значення, після чого за допомогою 1,1'-карбонілдіімідазолу переводять у імідазоліди формули (XIII) 8 UA 102065 C2 1 5 10 15 20 25 30 35 40 45 50 2 3 в якій Аr, D, R , R та R відповідно мають вказані вище значення, та ці сполуки у інертному розчиннику необов'язково в присутності допоміжної основи піддають взаємодії з аміаком до одержання амідів формули (І) та необов'язково сполуки формули (І) відомими фахівцям методами розділяють на їх енантіомери та/або діастереомери та/або за допомогою відповідних (і) розчинників та/або (іі) основ або кислот переводять у їх сольвати, солі та/або сольвати солей. Послідовність реакцій (II) + (III) (IV) та (IV) + (V) (VI) можна також здійснювати на одній стадії як 3-компонентну реакцію (II) + (III) + (V) (VI) без виділення проміжної стадії (IV). Стадії (II) + (III) (IV) та (IV) + (V) (VI) або відповідно (II) + (III) + (V) (VI) здійснюють загалом в інертному розчиннику у температурному діапазоні від +20°С до температури кипіння розчинника при нормальному тиску. Як інертні розчинники придатними при цьому є, наприклад, спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол або трет-бутанол, галоген вуглеводні, такі як дихлорметан, трихлорметан, тетрахлорметан, трихлоретан або 1,2-дихлоретан, або інші розчинники, такі як ацетонітрил, тетрагідрофуран, діоксан, 1,2-диметоксиетан, гексан, бензол, толуол, хлорбензол, піридин або льодяна оцтова кислота. Переважно реакції здійснюють у дихлорметані, толуолі, етанолі або ізопропанолі при відповідній температурі кипіння зі зворотнім холодильником при нормальному тиску. Зазначені реакції можна необов'язково вигідно здійснювати в присутності кислоти, комбінації кислота/основа та/або дегідратувального агента, такого як, наприклад, молекулярне сито. Як кислоти придатними є, наприклад, оцтова кислота, трифтороцтова кислота, метансульфонова кислота або п-толуолсульфонова кислота; як основи придатними є зокрема піперидин або піридин [з приводу синтезу 1,4-дигідропіридинів див. також D.M. Stout, A.I. Meyers, Chem. Rev. 1982, 82, 223-243; Η. Meier et al., Liebigs Ann. Chem. 1977, 1888; H. Meier et al., ibid. 1977, 1895; H. Meier et al., ibid. 1976, 1762; F. Bossert et al., Angew. Chem. 1981, 93, 755]. Інертними розчинниками для здійснення стадій (VI) + (VII) (Х-А), (VI) + (VIII) (Х-А) та (VI) + (XI) (Х-В) є, наприклад, етери, такі як діетиловий етер, метил-трет-бутиловий етер, діоксан, тетрагідрофуран, глікольдиметиловий етер або діетиленгліколь-диметиловий етер, вуглеводні, такі як бензол, толуол, ксилол, гексан, циклогексан або фракції нафти, галогенвуглеводні, такі як дихлорметан, трихлорметан, тетрахлорметан, 1,2-дихлоретан, трихлоретан, тетрахлоретан, трихлоретилен, хлорбензол або хлортолуол, або інші розчинники, такі як Ν,Ν-диметилформамід (ДМФА), диметилсульфоксид (ДМСО), Ν,Ν'-диметилпропіленкарбамід (ДМПК), Nметилпіролідон (Ν-ΜΠ), піридин або ацетонітрил. Крім того можна використовувати також суміші зазначених розчинників. Переважно на стадії (VI) + (VII) (Х-А) використовують тетрагідрофуран або диметилформамід, на стадії (VI) + (VIII) (Х-А) використовують дихлорметан, а на стадії (VI) + (XI) (Х-В) - піридин. Варіант способу (VI) + (IX) (Х-А) здійснюють переважно при використанні великого надлишку естеру ортомурашиної кислоти в диметилформаміді або без додавання іншого розчинника; як каталізатору реакції перевагу надають, наприклад, використанню сильних неорганічних кислот, таких як сірчана кислота [див., наприклад, I.I. Barabanov et al., Russ. Chem. Bl. 47(11), 2256-2261 (1998)]. Як основи для здійснення стадії (VI) + (VII) (Х-А) придатними є зокрема карбонати лужних або лужноземельних металів, такі як карбонат літію, натрію, калію, кальцію або карбонат цезію, гідриди лужних металів, такі як гідрид натрію або калію, аміди, такі як біс(триметилсиліл)амід літію, натрію або калію або діізопропіламід літію, металоорганічні сполуки, такі як бутиллітій або феніллітій, або також фосфаценові основи, такі як, наприклад, P2-t-Bu або P4-t-Bu [так звані "основи Швезінгера", див. R. Schwesinger, Η. Schlemper, Angew. Chem. Int. Ed. Engl. 26, 1167 (1987); T. Pietzonka, D. Seebach, Chem. Ber. 124, 1837 (1991)]. Переважно використовують гідрид натрію або фосфаценову основу P4-t-Bu. 9 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 60 Як основи для здійснення стадії (VI) + (XI) (Х-В) придатними є зокрема карбонати лужних або лужноземельних металів, такі як карбонат літію, натрію, калію, кальцію або карбонат цезію, гідриди лужних металів, такі як гідрид натрію або калію, металоорганічні сполуки, такі як бутиллітій або феніллітій, або органічні аміни, такі як триетиламін, N-метилморфолін, Nметилпіперидин, Ν,Ν-діізопропілетиламін, піридин, 1,5-діазабіцикло[4.3.0]нон-5-ен (DBN), 1,8® діазабіцикло[5.4.0]ундец-7-ен (DBU) або 1,4-діазабіцикло[2.2.2]остан (DABCO ). Переважно використовують піридин, який одночасно служить розчинником. Стадію (VI) + (VIII) (Х-А) здійснюють загалом без додавання основи. Реакції (VI) + (VII) (Х-А), (VI) + (VIII) (Х-А) та (VI) + (XI) (Х-В) здійснюють загалом у температурному діапазоні від -20°С до +100°С, переважно від 0°С до +60°С; варіант способу (VI) + (IX) (Х-А) здійснюють, як правило, у температурному діапазоні від +100°С до +150°С. Реакції можна здійснювати при нормальному, підвищеному або пониженому тиску (наприклад, від 0,5 до 5 бар); загалом працюють при нормальному тиску. Відщеплення алілового або відповідно 2-ціаноетилового естеру на стадії (Х-А) або відповідно (Х-В) (XII) здійснюють згідно з відомими з літературних джерел методами. У випадку 2-ціаноетилового естеру при цьому переважно використовують водний розчин гідроксиду лужного металу, такий як, наприклад, розчин їдкого натру або розчин їдкого калію. Реакцію здійснюють загалом при використанні змішуваного з водою інертного співрозчинника, такого як, наприклад, тетрагідрофуран, діоксан або 1,2-диметоксиетан, у температурному діапазоні від 0°С до +40°С. У випадку алілового естеру відщеплення здійснюють переважно за допомогою каталізатора Уілкінсона [хлорилтрис(трифенілфосфін)родію (І)] у суміші вода/спирт/оцтова кислота при температурі від +50°С до +100°С [див., наприклад, Moseley, J.D., Tetrahedron Lett. 46, 3179-3181 (2005)]. Як інертні розчинники для стадії (XII) (XIII) придатними є, наприклад, етери, такі як діетиловий етер, метил-трет-бутиловий етер, діоксан, тетрагідрофуран, глікольдиметиловий етер або діетиленглікольдиметиловий етер, галоген вуглеводні, такі як дихлорметан, трихлорметан, 1,2-дихлоретан, трихлоретан, тетрахлоретан, хлорбензол або хлортолуол, або інші розчинники, такі як Ν,Ν-диметилформамід (ДМФА), диметилсульфоксид (ДМСО), Ν,Ν'диметилпропіленкарбамід (ДМПК), N-метилпіролідон (Ν-ΜΠ), ацетон, ацетонітрил або етилацетат. Крім того можна використовувати також суміші зазначених розчинників. Переважно використовують тетрагідрофуран, диметилформамід або етилацетат. Як правило, реакцію здійснюють у температурному діапазоні від 0° до +40°С. Для стадії (XIII) (І) як інертні розчинники придатними є, наприклад, спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол або трет-бутанол, етери, такі як діетиловий етер, метил-трет-бутиловий етер, діоксан, тетрагідрофуран, глікольдиметиловий етер або діетиленглікольдиметиловий етер, або інші розчинники, такі як Ν,Ν-диметилформамід (ДМФА), диметилсульфоксид (ДМСО), Ν,Ν'-диметилпропіленкарбамід (ДМПК), Nметилпіролідон (Ν-ΜΠ), ацетонітрил або також вода. Крім того можна використовувати також суміші зазначених розчинників. Переважно використовують тетрагідрофуран або диметилформамід. Як джерело аміаку для цієї реакції придатними є розчини газоподібного аміаку в одному із вказаних вище розчинників, зокрема у воді. Реакцію можна необов'язково здійснювати в присутності третинного аміну як допоміжної основи, такого як, наприклад, триетиламін, Nметилморфолін, N-метилпіперидин, Ν,Ν-діізопропілетиламін або 4-Ν,Ν-диметиламінопіридин. Реакцію здійснюють загалом у температурному діапазоні від +20°С до +120°С, переважно від +50°С до +100°С. Сполуки формули (II) наявні у продажу, відомі з літературних джерел або можуть бути одержані аналогічно відомим з літератури способам (див. Наведені нижче схеми реакцій 1-7). Сполуки формул (III), (VII), (VIII), (IX) та (XI) також наявні у продажу, відомі з літературних джерел або можуть бути одержані відомими з літератури способами. Сполуки формули (V) описані в літературних джерелах або можуть бути одержані аналогічно описаним в літературі способам [див., наприклад, Т. Searls, LW. McLaughlin, Tetrahedron 55, 11985-11996 (1999); D. McNamara, P.D. Cook, J. Med. Chem. 30, 340-347 (1987); S. Nesnow, С Heidelberger, J. Heterocycl. Chem. 12, 941-944 (1975); N.C. Hung, E. Bisagni, Synthesis 1984. 765-766; Z. Foldi et ai, Chem. Ber. 75 (7), 755-763 (1942); G.W. Kenneretal., J. Chem. Soc, 388(1943)]. Необов'язково виділення енантіомерів та/або діастереомерів можна здійснювати вже на стадії проміжних сполук (VI), (Х-А), (Х-В) або (XII), які після цього окремо піддають наступним реакціям. Одержання сполук згідно з винаходом наочно можна представити на таких схемах синтезу: 10 UA 102065 C2 5 [а): алілбромід, карбонат калію, кат., йодид калію, ацетон, кип'ятіння зі зворотнім холодильником; b): 230°С, 4 год.; с): біс(бензонітрил)дихлорпаладій (II), толуол, 120°С, 16 год.; d): ацетилхлорид, гідрид натрію, ТГФ, 10-25°С, 16 год.; е): 1. озон, дихлорметан, -60°С, 30 хв.; 2. диметилсульфід]. 11 UA 102065 C2 5 [а): н-бутиллітій, ТГФ, 60°С, 3 год.; b): ангідрид оцтової кислоти, піридин, кип'ятіння зі зворотнім холодильником, 6 год.; с): конц. H 2SO4, HNO3, 0°C, 1 год.; d): N-бромсукцинімід, AIBN, тетрахлорвуглець, кип'ятіння зі зворотнім холодильником; e): N-метилморфолін-N-оксид, ацетонітрил, кип'ятіння зі зворотнім холодильником]. [а): дигідрат хлориду олова (II), етилацетат, 70°С; b): 1. нітрит натрію, сірчана кислота, 0°С, 1,5 год.; 2. ціанід міді (І), ціанід натрію, вода/етилацетат, 0°С, 45 хв.; с): N-бромсукцинімід, AIBN, 12 UA 102065 C2 тетрахлорвуглець, кип'ятіння зі зворотнім холодильником; d): N-метилморфолін-N-оксид, ацетонітрил, кип'ятіння зі зворотнім холодильником]. 5 10 [а): ангідрид трифторметансульфонової кислоти, піридин, 0°С КТ, 30 хв.; b): третбутиловий естер акрилової кислоти, біс(трифенілфосфін)дихлорпаладій (II), ДМФА, 120°С, 24 год.; с): кат. тетроксид осмію, кат. хлорид бензилтриетиламонію, періодат натрію, ТГФ/вода, 2025°С, 2 год.]. [а): н-бутиллітій, ТГФ, -78°С, потім N-формілморфолін; b): ціанід цинку, тетракіс(трифенілфосфін)паладій (0), ДМФА, мікрохвильова піч 250°С / 5 хв.]. 13 UA 102065 C2 [a): Ν,Ν-диметилформаміду диметилацеталь, ДМФА, 140-180°С; b): періодат натрію, ТГФ/вода]. 5 [а): N-бромсукцинімід, AIBN, тетрахлорметан, кип'ятіння зі зворотнім холодильником; b): Nметилморфолін-N-оксид, ацетонітрил, 3Å-молекулярне сито]. 14 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 60 [а): кат. піперидин/оцтова кислота, дихлорметан, кип'ятіння зі зворотнім холодильником, 24 год.; b): ізопропанол, кип'ятіння зі зворотнім холодильником, 12-72 год.; с): алкілтрифлат або йодид, основа, ТГФ або ДМФА, КТ; або тетрафторборат триалкілоксонію, дихлорметан, КТ; або 11 триалкілортоформіат, кат. Сірчана кислота, 100-130°С; або R -SO2-CI, піридин, КТ; d): Τ = 2ціаноетил: водн. NaOH, ДМЕ/вода, КТ; Т = аліл: (PPh3)3RhCI, вода/етанол/оцтова кислота, 75°С; e): 1,1'-карбонілдіімідазол, етилацетат, КТ, 12 год.; f): водн. аміак, ДМФА, 50-100°С, 0,5-12 год.]. Сполуки згідно з винаходом проявляють активність антагоністів мінералокортикоїдного рецептора та непередбачуваний цінний спектр фармакологічної дії. Тому вони є придатними для застосування як лікарські засоби для лікування та/або профілактики захворювань у людей та тварин. Сполуки згідно з винаходом є придатними для профілактики та/або лікування різних захворювань та обумовлених захворюваннями станів, зокрема захворювань, які характеризуються підвищенням концентрації альдостерону в плазмі або зміною концентрації альдостерону в плазмі по відношенню до концентрації реніну в плазмі або пов'язані з цими змінами. Як приклад слід назвати: ідіопатичний первинний гіперальдостеронізм, гіперальдостеронізм при гіперплазії надниркової залози, аденомі надниркової залози та/або карциномі надниркової залози, гіперальдостеронізм при цирозі печінки, гіперальдостеронізм при серцевій недостатності, а також (відносний) гіперальдостеронізм при ессенціальній гіпертонії. Крім того сполуки згідно з винаходом, враховуючи їх механізм дії, є придатними для профілактики раптової серцевої смерті у пацієнтів з високим ризиком раптової серцевої смерті. Це зокрема такі пацієнти, які, наприклад, страждають на одне з таких захворювань: первинна та вторинна гіпертонія, гіпертензивна хвороба серця з або без активної серцевої недостатності, стійка до терапії гіпертонія, гостра та хронічна серцева недостатність, коронарна хвороба серця, стабільна та нестабільна стенокардія, міокардіальна ішемія, інфаркт міокарду, дилатаційна кардіоміопатія, уроджена первинна кардіоміопатія, така як, наприклад, синдром Бругада, кардіоміопатія, викликана хворобою Шагаса, шок, артеріосклероз, артеріальна та шлуночкова аритмія, транзиторні та ішемічні напади, апоплексія, запальні серцево-судинні захворювання, захворювання периферійних та серцевих судин, порушення периферійного кровопостачання, облітерувальний ендартеріїт, такий як синдром Шарко, асимптоматична дисфункція лівого шлуночка, міокардит, гіпертрофічні зміни серця, легенева гіпертонія, спазми коронарних та периферійних артерій, тромбози, тромбоемболічні захворювання, а також васкуліт. Сполуки згідно з винаходом можуть бути використані також для профілактики та/або лікування при утворенні набряків, наприклад, легеневих набряків, ниркових набряків або набряків, обумовлених серцевою недостатністю, та ре стенозів, таких як після тромболітичної терапії, перкутанно-транслюмінальної ангіопластики (РТА) та коронарної ангіопластики (РТСА), трансплантації серця, а також операцій шунтування. Крім того сполуки згідно з винаходом є придатними для застосування як діуретин, що зберігає калій, та при електролітичних порушеннях, таких як, наприклад, гіперкальціємія, гіпернатріємія або гіпокаліємія. Сполуки згідно з винаходом також є придатними для лікування захворювань нирок, таких як гостра та хронічна ниркова недостатність, гіпертензивних захворювань нирок, артеріосклеротичного нефриту (хронічного та інтерстиціального), нефросклерозу, хронічної ниркової недостатності та кістозних захворювань нирок, для запобігання ураженню нирок, що, наприклад, можуть бути спричинені імуносупресантами, такими як циклоспорин А при трансплантації органів, а також при раку нирок. Сполуки згідно з винаходом застосовують також для профілактики та/або лікування цукрового діабету та та пов'язаних з діабетом захворювань, таких як, наприклад, невропатія та нефропатія. Крім того сполуки згідно з винаходом можуть бути застосовані для профілактики та/або лікування мікроальбумінурії, наприклад, обумовленої цукровим діабетом або артеріальною гіпертонією, а також протеїнурії. Сполуки згідно з винаходом придатні для профілактики та/або лікування захворювань, пов'язаних з підвищенням концентрації глікокортикоїду в плазмі або з локальним підвищенням концентрації глікокортикоїдів у тканинах (наприклад, серці). Як приклади слід назвати: порушення функції надниркової залози, що призводить до надмірного вироблення глюкокортикоїдів (синдром Кушинга), пухлини кори надниркової залози, в результаті чого також спостерігається надмірне вироблення глюкокортикоїдів, а також пухлини гіпофізу, які автономно виробляють АСТН (адренокортикотропний гормон) та внаслідок цього призводять до гіперплазії надниркової залози та виникнення пов'язаного з цим синдрому Кушинга. 15 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 Крім того сполуки згідно з винаходом можуть бути використані для профілактики та/або лікування ожиріння, метаболічного синдрому та обструктивного тимчасової зупинки дихання під час сну. Сполуки згідно з винаходом можуть також бути використані для профілактики та/або лікування запальних захворювань, викликаних вірусами, спірохетами, грибками, бактеріями або мікобактеріями, а також запальних захворювань невідомої етіології, таких як поліартрит, Lupus erythematodes (системна червона вовчанка), пері- або поліартеріїти, дерматоміозит, склеродермія та саркоїдоз. Крім того сполуки згідно з винаходом можуть бути використані для лікування захворювань центральної нервової системи, таких як депресії, станів страху та хронічних болів, зокрема мігреней, а також у випадку нейродегенеративних захворювань, таких як хвороба Альцгеймера та синдром Паркінсона. Сполуки згідно з винаходом також є придатними для профілактики та/або лікування ушкоджень судин, наприклад, після втручань, таких як перкутанна транслюминальна коронарна ангіопластика (РТСА), імплантація стентів, коронарна ангіоскопія, реоклюзія або рестеноз після операцій шунтування, а також при ендотеліальній дисфункції, при захворюванні Рейно (Morbus Raynaud), при тромбоангіїти облітерувальному Thrombangiitis obliterans (синдром Бюргера) та при вушних захворюваннях. Іншим об'єктом даного винаходу є застосування сполук згідно з винаходом для лікування та/або запобігання захворюванням, зокрема описаним вище захворюванням. Ще одним об'єктом даного винаходу є застосування сполук згідно з винаходом для одержання лікарського засобу для лікування та/або запобігання захворюванням, зокрема описаним вище захворюванням. Ще одним об'єктом даного винаходу є спосіб лікування та/або запобігання захворюванням, зокрема описаним вище захворюванням, шляхом використання ефективної кількості щонайменше однієї зі сполук згідно з винаходом. Сполуки згідно з винаходом можуть бути застосовані окремо або, в разі потреби, у комбінації з іншими активними речовинами. Ще одним об'єктом даного винаходу є лікарські засоби, що містять щонайменше одну зі сполук згідно з винаходом та одну або кілька інших активних речовин, зокрема для лікування та/або запобігання описаним вище захворюванням. Нижче наведені приклади придатних та переважних компонентів для комбінування: - активні речовини, що знижують тиск, такі як, наприклад, переважно з групи антагоністів кальцію, антагоністів ангіотензину All, інгібіторів АСЕ, антагоністів ендотеліну, інгібіторів реніну, блокаторів альфа-рецепторів, блокаторів бета-рецепторів та інгібіторів Ро-кінази; - діуретики, зокрема петльові діуретики, а також тіазиди та тіазид-подібні діуретики; - антитромботичні засоби, такі як, наприклад, переважно з групи інгібіторів накопичення тромбоцитів, антикоагулянтів або профібринолітичних сполук; - активні речовини, що змінюють обмін речовин, такі як, наприклад, переважно з групи агоністів тироїдних рецепторів, інгібіторів синтезу холестерину, таких як переважно інгібітори HMG-CoA-редуктази або скваленсинтази, АСАТ-інгібіторів, СЕРТ-інгібіторів, МТР-інгібіторів, PPAR-альфа-, PPAR-гама- та/або PPAR-дельта-агоністів, інгібіторів абсорбції холестерину, інгібіторів ліпази, полімерних абсорберів жовчної кислоти, інгібіторів реабсорбції жовчної кислоти та антагоністів ліпопротеїну(нів); - органічні нітрати та NO-донори, такі як, наприклад, нітропрусид натрію, нітрогліцерин, ізосорбідмононітрат, ізосорбіддинітрат, молсидомін або SIN-1, а також інгалятивний NO; - позитивно-інотропні сполуки, такі як серцеві глікозиди (дигоксин), бета-адренергічні та допамінергічні агоністи, такі як ізопротеренол, адреналін, норадреналін, допамін та добутамін; - сполуки, що інгібіють розпад циклічного гуанозинмонофосфату (цГМФ) та/або циклічного аденозинмонофосфату (цАМФ), такі як, наприклад, інгібітори фосфодіестераз (ФДЕ) 1, 2, 3, 4 та/або 5, зокрема інгібітори ФДЕ 5, такі як силденафіл, варденафіл та тадалафіл, а також інгібітори ФДЕ 3, такі як амринон та мілринон; - натрійуретичні пептиди, такі як, наприклад, "атріальний натрійуретичний пептид" (ANP, анаритид), "В-натрійуретичний пептид" або "мозковий натрійуретичний пептид" (BNP, несиритид), "С- натрійуретичний пептид" (CNP), а також уродилатин; сенсибілізатор кальцію, такий як, наприклад, переважно левосимендан; NO-незалежні, однак Häm-залежні стимулятори гуанілатциклази, зокрема описані в WO 00/06568, WO 00/06569, WO 02/42301 та WO 03/095451 сполуки; - NO- та Häm-незалежні активатори гуанілатциклази, зокрема описані в WO 01/19355, WO 01/19776, WO 01/19778, WO 01/19780, WO 02/070462 та WO 02/070510 сполуки; 16 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 - інгібітори нейтрофільної еластази людини (HNE), такі як, наприклад, сивелестат або DX890 (Reltran); - сполуки, що інгібують каскад трансдукції сигналу, такі як, наприклад, інгібітори тиросинкінази, зокрема сорафеніб, іматиніб, гефітиніб та ерлотиніб; та/або - сполуки, що впливають на енергообмін серця, такі як, наприклад, переважно етомоксир, дихлорацетат, ранолазин або триметазидин. У випадку переважної форми виконання винаходу сполуки згідно з винаходом використовують у комбінації з діуретиком, таким як, наприклад, переважно фуроземід, буметанід, торземід, бендрофлуметіазид, хлортіазид, гідрохлортіазид, гідрофлуметіазид, метиклотіазид, політіазид, трихлорметіазид, хлорталідон, індапамід, метолазон, хінетазон, ацетазоламід, дихлорфенамід, метазоламід, гліцерин, ізосорбід, маніт, амілорид або триамтерен. Під засобами, що знижують тиск, переважно розуміють сполуки з групи, що включає антагоністи кальцію, антагоністи андіотензину All, АСЕ-інгібітори, антагоністи ендотеліну, інгібітори реніну, блокатори альфа-рецепторів, блокатори бета-рецепторів, інгібітори Ро-кінази, а також діуретики. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з антагоністом кальцію, таким як, наприклад, переважно ніфедипін, амлодипін, верапаміл або дилтіазем. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з антагоністами рецептору ангіотензину All, такими як, наприклад, переважно лазортан, кандезартан, валзартан, телмізартан або ембузартан. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з АСЕ-інгібітором, таким як, наприклад, переважно, еналаприл, каптоприл, лізиноприл, раміприл, делаприл, фозиноприл, хіноприл, периндоприл або трандоприл. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з антагоністом ендотеліну, таким як, наприклад, переважно бозентан, дарузентан, амбрізентан або ситаксзентан. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з інгібітором реніну, таким як, наприклад, переважно аліскірен, SPP-600, SPP-635, SPP-676, SPP-800 або SPP-1148. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з блокатором альфа-1 -рецепторів, таким як, наприклад, переважно празосин. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з блокатором бета-рецепторів, таким як, наприклад, переважно пропранолол, атенолол, тимолол, піндолол, алпренолол, окспренолол, пенбутолол, бупранолол, метипранолол, надолол, мепіндолол, каразалол, соталол, метопролол, бетаксолол, целіпролол, бісопролол, картеолол, есмолол, лабеталол, карведілол, адапролол, ландіолол, небіволол, епанолол або буциндолол. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з інгібітором Ро-кінази, таким як, наприклад, переважно фазудил, Y-27632, SLx-2119, BF-66851, BF-66852, BF-66853, КІ-23095 або ВА-1049. Під антитромботичними засобами розуміють переважно сполук з групи, що включає інгібітори накопичення тромбоцитів, антикоагулянти або профібронолітичні речовини. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібітором накопичення тромбоцитів, таким як, наприклад, переважно аспірин, клопідогрель, тиклопідин або дипіридамол. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібітором тромбіну, таким як, наприклад, переважно ксимелагатран, мелагатран, бівалірудин або клексан. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з GPIIb/llla-агоністами, такими як, наприклад, переважно тирофібан або абциксимаб. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібітором фактору Ха, таким як, наприклад, переважно рівароксабан (BAY 597939), DU-176b, апіксабан, отаміксабан, фідексабан, разаксабан, фондапаринукс, ідрапаринукс, PMD-3112, YM-150, KFA-1982, EMD-503982, МСN-17, MLN-1021, DX 9065a, DPC 906, JTV 803, SSR-126512 або SSR-128428. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з гепарином або похідною (LМW)-гепарину (з низькою молекулярною вагою). 17 UA 102065 C2 5 10 15 20 25 30 35 40 45 50 55 60 Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з антагоністами вітаміну К, такими як, наприклад, переважно кумарин. Під засобами, що впливають на обмін речовин розуміють, наприклад, переважно сполуки з групи, що включає СЕТР-інгібітори, агоністи тиреоїдних рецепторів, інгібітори синтезу холестерину, такі як інгібітори HMG-CoA-редуктази або скваленсинтази, АСАТ-інгібітори, МТРінгібітори, PPAR-альфа-, PPAR-гама- та/або PPAR-дельта-агоністи, інгібітори абсорбції холестерину, полімерні абсорбери жовчної кислоти, інгібітори реабсорбції жовчної кислоти, інгібітори ліпази, а також антагоністи ліпопротеїнів. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з СЕТР-інгібітором, таким як, наприклад, переважно торцетрапіб (СР-529 414), JJT705, BAY 60-5521, BAY 78-7499 або СЕТР-вакцина (фірми Avant). Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з агоністом тиреоїдного рецептора, таким як, наприклад, переважно D-тироксин, 3,5,3'-трийодотиронін (Т3), CGS 23425 або акситиром (CGS 26214). Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінацію з інгібітором HMG-CoA-редуктази з класу статинів, таких як, наприклад, переважно ловастатин, симвастатин, правастатин, флувастатин, аторвастатин, розувастатин, церивастатин або пітавастатин. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібітором скваленсинтази, таким як, наприклад, переважно BMS-188494 або ТАК475. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з АСАТ-інгібітором, таким як, наприклад, переважно авасиміб, мелінамід, пактиміб, ефлуциміб або SMP-797. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з МТР-інгібітором, таким як, наприклад, переважно імплітапід, BMS-201038, R-103757 або JTT-130. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з PPAR-гама-агоністами, такими як, наприклад, переважно піоглітазон або розиглітазон. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з PPAR-дельта-агоністами, такими як, наприклад, переважно GW 501516 або BAY 685042. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібіторами абсорбції холестерину, такими як, наприклад, переважно езетиміб, тиквезид або памаквезид. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібітором ліпази, таким як, наприклад, переважно орлістат. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з полімерними абсорберами жовчної кислоти, такими як, наприклад, переважно холестирамін, колестипол, колесолвам, холестаГель або колестимід. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з інгібіторами реабсорбції жовчної кислоти, такими як, наприклад, переважно ASBT (= ІВАТ)-інгібітори, наприклад, AZD-7806, S-8921, АК-105, BARI-1741, SC-435 або SC-635. Згідно з переважною формою виконання винаходу сполуки згідно з винаходом вводять у комбінації з антагоністами ліпопротеїну(нів), такими як, наприклад, переважно гемкабен кальцій (СІ-1027) або нікотинова кислота. Ще одним об'єктом даного винаходу є лікарські засоби, що містять щонайменше одну сполуку згідно з винаходом зазвичай у комбінації з однією або кількома інертними, нетоксичними, фармацевтично придатними допоміжними речовинами, а також їх застосування для зазначених вище цілей. Сполуки згідно з винаходом можуть проявляти систематичну та/або локальну дію. Для досягнення цієї мети їх наносять відповідним чином, наприклад, перорально, парентерально, легеневим способом, назально, під язик, на язик, за щоку, ректально, дермально, трансдермально, кон'юктивально, у вухо або у вигляді імплантату або стенту. Для таких видів застосовання згідно сполуки з винаходом можуть бути використані у відповідних формах. Для перорального застосування згідно з рівнем техніки придатними є функціонуючі лікарські форми, що характеризуються швидким та/або модифікованим вивільненням сполук згідно з винаходом та до складу яких ці сполуки входять у кристалічній та/або аморфній та/або 18 UA 102065 C2 5 10 15 20 25 30 35 40 45 розчиненій формі, такі як, наприклад, таблетки (непокриті або покриті оболонками, наприклад, оболонками, стійкими до шлункового соку, або оболонками, які повільно розчиняються або не розчиняються взагалі, що контролюють вивільнення сполуки згідно з винаходом), таблетки або плівки/облатки, плівки/ліофілізати, капсули, які швидко розчиняються у ротовій порожнині (наприклад, тверді або м'які желатинові капсули), драже, грануляти, гранули, порошки, емульсії, суспензії, аерозолі або розчини. Парентеральне застосування може відбуватися при виключенні стадії всмоктування (наприклад, внутрішньовенно, внутрішньоартеріально, внутрішньосерцево, інтраспінально або інтралюмбально) або за умови включення стадії всмоктування (наприклад, внутрішньом'язово, підшкірно, у шкіру, перкутанно або внутрішньобрюшинно). Придатними для парентерального застосування є такі форми, як ін'єкційні та інфузійні композиції у вигляді розчинів, суспензій, емульсій, ліофілізатів або стерильних порошків. Для інших видів застосування придатними є, наприклад, лікарські засоби для інгаляції (а саме порошкові інгалятори, розпилювачі), краплі, розчини або спреї в ніс; таблетки на язик, під язик або за щоку, плівки/облатки або капсули, супозиторії, композиції для вух або очей, вагінальні капсули, водні суспензії (лосьйони, мікстури «бовтушки»), ліпофільні суспензії, мазі, креми, трансдермальні терапевтичні системи (наприклад, пластирі), молочко, пасти, піни, присипки, імплантати або стенти. Перевагу надають пероральному або парентеральному застосуванню, зокрема пероральному та внутрішньовенному застосуванню. Сполуки згідно з винаходом можуть бути переведені у згадані форми застосування. Це можна здійснювати відомими способами шляхом змішування з інертними, нетоксичними, фармацевтично придатними допоміжними речовинами. До таких допоміжних речовин належать зокрема носії (наприклад, мікрокристалічна целюлоза, лактоза, маніт), розчинники (наприклад, рідкі поліетиленгліколі), емульгатори та диспергатори або змочувальні агенти (наприклад, додецилсульфат натрію, олеат поліоксисорбіту), зв'язувальні агенти (наприклад, полівінілпіролідон), синтетичні та природні полімери (наприклад, альбумін), стабілізатори (наприклад, антиоксиданти, такі як аскорбінова кислота), барвники (наприклад, неорганічні пігменти, такі як оксиди заліза) та речовини, що коригують смак та/або запах. Загалом виявили, що при парентеральному застосуванні для досягнення необхідних результатів кількість активної речовини переважно становить від приблизно 0,001 до 1 мг/кг ваги тіла, переважно від прибл. 0,01 до 0,5 мг/кг ваги тіла. При пероральному застосуванні дозування становить прибл. від 0,01 до 100 мг/кг, переважно прибл. від 0,01 до 20 мг/кг та особливо переважно від 0,1 до 10 мг/кг ваги тіла. Крім того при необхідності можна відступати від вказаних кількостей залежно від ваги тіла, форми застосування, індивідуальної реакції на активну речовину, виду композиції та моменту або інтервалу її застосування. Так, наприклад, у деяких випадках достатнім може виявитися застосування меншої кількості, ніж вказана вище мінімальна гранична кількість, а у інших випадках необхідно перевищувати максимальну граничну кількість. У випадку застосування більших кількостей варто розподілити цю кількість на кілька окремих доз для застосування протягом дня. Наведені нижче приклади виконання пояснюють винахід та в жодному разі не обмежують обсяг його охорони. Показники в % у дослідженнях та прикладах, якщо не зазначено нічого іншого, означають мас. %; частини - масові частини. Співвідношення розчинників, коефіцієнти розчинення та показники концентрації розчинів рідина/рідина стосуються відповідно об'єму. Α. Приклади Скорочення та абревіатури: абс. абсолютний ΑΙΒΝ 2,2'-азобіс-2-метилпропаннітрил кат. каталітично XI хімічна іонізація (при МС) Д день(дні) ТХШ тонкошарова хроматографія ДМЕ 1,2-диметоксиетан ДМФА диметилформамід ДМСО диметилсульфоксид від від теоретичного (на виході) теор. 19 UA 102065 C2 Ее ΕΙ ESI ент екв. ESI ГХ-МС мас. % год. ВЕРХ конц. РХ-МС хв. РХСТ МС ЯМР Ph Пу Чу КТ ТГФ об/об водн. 5 10 15 20 25 30 35 енантіомерний надлишок іонізація електронним ударом (при МС) електророзпилювальна іонізація (при МС) енантіомер / чистий від енантіомерів еквівалент(и) іонізація електростатичним розпилюванням (при МС) газова хроматографія при мас-спектроскопії масовий процент година(ни) рідинна хроматографія високого тиску концентрований рідинна хроматографія при мас-спектроскопії хвилина(ни) рідинна хроматографія середнього тиску мас-спектроскопія ядерно-магнітний резонанс феніл показник утримування (при ТШХ) час утримування (при ВЕРХ) кімнатна температура тетрагідрофуран співвідношення об'єм : об'єм (розчину) водний, водний розчин Методи РХ-МС та ГХ-МС: Метод 1 (РХ-МС): Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2мкм Hydro-RP Mercury 20 мм x 4 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 2,5 хв. 30% А 3,0 хв. 5% А 4,5 хв. 5% А; потік: 0,0 хв. 1 мл/хв. 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; термостат колонок: 50°С; УФ-детектування: 210 нм. Метод 2 (РХ-МС): Прилад: Micromass Quattro LCZ з ВЕРХ Agilent серії 1100; колонка: Phenomenex Synergi 2 мкм Hydro-RP Mercury 20 мм x 4 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А -^ 2,5 хв. 30% А 3,0 хв. 5% А 4,5 хв. 5% А; потік: 0,0 хв. 1 мл/хв. 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; термостат колонок: 50°С; УФ-детектування: 208-400 нм. Метод 3 (РХ-МС): Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: HP 1100; УФ DAD; колонка: Phenomenex Gemini 3 мкм 30 мм x 3,00 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 2,5 хв. 30% А 3,0 хв. 5% А 4,5 хв. 5% А; потік: 0,0 хв. 1 мл/хв. 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; термостат колонок: 50°С; УФ-детектування: 210 нм. Метод 4 (РХ-МС): Прилад: Micromass Platform LCZ з ВЕРХ Agilent серії 1100; колонка: Thermo Hypersil GOLD Змкм 20 мм x 4 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 100% А 0,2 хв. 100% А 2,9 хв. 30% А 3,1 хв. 10% А · 5,5 хв. 10% А; термостат колонок: 50°С; потік: 0,8 мл/хв.; УФдетектування: 210 нм. Метод 5 (ГХ-МС): Прилад: Micromass GCT, GC 6890; колонка: Restek RTX-35MS, 30 м x 250 мкм x 0,25 мкм; постійний потік гелію: 0,88 мл/хв.; термостат колонок: 60°С; температура інжектора: 250°С; градієнт: 60°С (0,30 хв. утримування), 50°С/хв. 120°С, 16°С/хв. 250°С, 30°С/хв. 300°С (1,7 хв. утримування). Метод 6 (РХ-МС): Тип приладу МС: Waters ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Onyx Monolithic C18, 100 мм x 3 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 2 хв. 65% А 4,5 хв. 5% А 6 хв. 5% А; потік: 2 мл/хв.; термостат колонок: 40°С; УФ-детектування: 210 нм. 20 UA 102065 C2 5 10 15 20 25 30 35 40 Метод 7 (РХ-МС): Прилад: Micromass Quattro LCZ з ВЕРХ Agilent серії 1100; колонка: Phenomenex Onyx Monolithic С18, 100 мм x 3 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 2 хв. 65% А 4,5 хв. 5% А 6 хв. 5% А; потік: 2 мл/хв.; термостат колонок: 40°С; УФ-детектування: 208-400 нм. Метод 8 (РХ-МС): Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2,5мкм MAX-RP 100A Mercury 20 мм x 4 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 0,1 хв. 90% А 3,0 хв. 5% А 4,0 хв. 5% А 4,01 хв. 90% А; потік: 2 мл/хв.; термостат колонок: 50°С; УФ-детектування: 210 нм. Метод 9 (РХ-МС): Прилад: Micromass Quattro Premier з Waters UPLC Acquity; колонка: Thermo Hypersil GOLD 1,9мкм 50 мм x 1 мм; елюент А: 1 л води + 0,5 мл 50%-ної мурашиної кислоти, елюент В: 1 л ацетонітрилу + 0,5 мл 50%-ної мурашиної кислоти; градієнт: 0,0 хв. 90% А 0,1 хв. 90% А 1,5 хв. 10% А 2,2 хв. 10% А; потік: 0,33 мл/хв.; термостат колонок: 50°С; УФ-детектування: 210 нм. Вихідні та проміжні сполуки: Приклад 1А 1-[2-(алілокси)феніл]етанон 542 г (3,9 моль) 2-гідроксиацетофенону разом з 592 г (4,9 моль) алілброміду, 1000 г (7,2 моль) карбонату калію та 13,2 г (79 ммоль) йодиду калію в 2,4 л ацетону протягом 24 годин перемішують при кип'ятінні зі зворотнім холодильником. Після охолодження до кімнатної температури фільтрують, а розчинник видаляють у вакуумі. Залишок розчиняють в толуолі та промивають 10%-ним розчином їдкого натру і водою. Після концентрування одержують 689 г (98% від теор.) сполуки із заголовку. 1 Н-ЯМР (300 МГц, CDCI3): δ = 2,68 (с, 3Н), 4,68 (дд, 2Н), 5,89 (дд, 2Н), 6,09 (м, 1Н), 6,99 (дд, 2Н), 7,44 (м, 1Н), 7,71 (д, 1Н). Приклад 2А 1-(3-аліл-2-гідроксифеніл)етанон 160 г (0,9 моль) 1-[2-(алілокси)феніл]етанону у ванні рідкого металу протягом 4 годин перемішують при 230-240°С. Після охолодження до кімнатної температури продукт дистилюють на тонкошаровому випарнику при 140°С та 0,4 мбар. Одержують 155 г (97% від теор.) сполуки із заголовку. 1 Н-ЯМР (300 МГц, CDCI3): δ = 2,68 (с, 3Н), 3,44 (д, 2Н), 5,09 (м, 2Н), 6,01 (м, 1Н), 6,85 (т, 1Н), 7,38 (дд, 1Н), 7,62 (дд, 1Н), 12,61 (с, 1Н). Приклад 3А 1-{2-гідрокси-3-[(1Е)-проп-1-ен-1-іл]феніл}етанон 21 UA 102065 C2 5 10 15 20 25 30 40 г (227 ммоль) 1-(3-аліл-2-гідроксифеніл)етанону розчиняють в 120 мл толуолу та додають 2,17 г (5,6 ммоль) біс(бензонітрил)дихлорпаладію (II). Реакційну суміш протягом ночі нагрівають до 120°С. Після охолодження до кімнатної температури фільтрують через силікагель, а розчинник видаляють у вакуумі. Одержують 20,9 г (95% від теор.) сполуки із заголовку, яку без попереднього очищення вводять у реакцію на наступній стадії. + РХ-МС (метод 1): Чу = 2,36 хв.; [М+Н] = 177 1 Н-ЯМР (300 МГц, CDCI3): δ = 1,91 (дд, 3Н), 2,63 (с, 3Н), 6,32 (м, 1Н), 6,73 (дд, 1Н), 6,85 (т, 1Н), 7,59 (м, 2Н), 12,74 (с, 1Н). Приклад 4А 2-метил-8-[(1 Е)-проп-1 -ен-1-іл]-4Н-хромен-4-он 12,52 г (313,2 ммоль) 60%-ного гідриду натрію (суспензія в мінеральному маслі) в атмосфері аргону при 10°С поміщають в 300 мл абсолютного ТГФ. У суспензію повільно по краплях додають 18,4 г (104,4 ммоль) 1-{2-гідрокси-3-[(1Е)-проп-1-ен-1-іл]феніл}-етанону. Через 15 хвилин додають 9 г (114,9 ммоль) ацетилхлориду. Реакційну суміш протягом ночі перемішують при кімнатній температурі. Гідролізують 300 мл води та кілька разів екстрагують етилацетатом. Після промивання органічної фази насиченим розчином хлориду натрію сушать над сульфатом натрію. Потім розчинник видаляють у вакуумі. Залишок поміщають в 200 мл метанолу та разом з 50 мл 20%-ної соляної кислоти протягом 30 хвилин нагрівають до 80°С. Після цього розчинник видаляють у вакуумі, а у залишок додають 400 мл води. Кілька разів екстрагують дихлорметаном. Після сушки органічної фази над сульфатом магнію розчинник видаляють у вакуумі, а залишок очищують колонковою хроматографією (розчинник: дихлорметан/метанол 98:2). Одержують 10,5 г (50,2% від теор.) сполуки із заголовку у вигляді жовтого масла. + РХ-МС (метод 2): Чу = 2,07 хв.; [М+Н] = 201 1 Н-ЯМР (300 МГц, CDCI3): δ = 1,98 (дд, 3Н), 2,43 (с, 3Н), 6,18 (с, 1Н), 6,40 (м, 1Н), 6,85 (дд, 1Н), 7,31 (т, 1Н), 7,72 (дд, 1Н), 8,05 (дд, 1Н). Приклад 5А 2-метил-4-оксо-4Н-хромен-8-карбальдегід 22 UA 102065 C2 5 10 15 20 25 30 35 18,5 г (62,8 ммоль) 2-метил-8-[(1Е)-проп-1-ен-1-іл]-4Н-хромен-4-ону розчиняють в 400 мл дихлорметану та охолоджують до -60°С. Через реакційний розчин протягом 30 хвилин пропускають озон. Потім у реакційну суміш додають диметилсульфід. Після нагрівання до кімнатної температури розчинник видаляють у вакуумі, а залишок змулюють незначною кількістю метанолу. Після фільтрування залишкову тверду речовину перекристалізовують із діетилового етеру. Одержують 9,1 г (77,4% від теор.) сполуки із заголовку. + РХ-МС (метод): Чу = 1,31 хв.; [М+Н] = 189 1 Н-ЯМР (300 МГц, CDCI3): δ = 2,48 (с, 3Н), 6,27 (с, 1Н), 7,51 (м, 1Н), 8,21 (дд, 1Н), 8,46 (дд, 1Н). 10,67 (с, 1Н). Приклад 6А 4-бром-2-(трифторметокси)бензальдегід 20,00 г (54,51 ммоль) 4-бром-2-(трифторметокси)йодбензолу розчиняють в 200 мл ТГФ та охолоджують до -78°С. Потім по краплях додають 26,16 мл (65,41 ммоль) 2,5 Μ розчину нбутиллітію в гексані. Перемішують протягом 30 хвилин та після цього додають 14,43 г (125,37 ммоль) N-формілморфоліну. Після повного перетворення аналізують (ТШХ-контроль) та при 78°С сольволізують ізопропанолом. Після нагрівання до кімнатної температури додають воду та двічі екстрагують дихлорметаном. Об'єднані органічні фази промивають насиченим розчином хлориду натрію, сушать над сульфатом натрію, а розчинник відганяють при пониженому тиску. Залишок очищують колонковою хроматографією (силікагель, розчинник: циклогексан/етилацетат 5:1). Одержують 11,43 г (78% від теор.) сполуки із заголовку. + ГХ-МС (метод 5): Чу = 4,24 хв.; МС (El-поз): m/z = 270 [М+Н] 1 Н-ЯМР (300 МГц, ДMCO-d6): δ = 7,85-7,92 (м, 3Н), 10,20 (с, 1Н). Приклад 7А 4-форміл-3-(трифторметокси)бензонітрил 10,63 г (39,51 ммоль) 4-бром-2-(трифторметокси)бензальдегіду, 3,43 г (29,24 ммоль)ціаніду цинку та 1,37 г (1,19 ммоль) тетракіс(трифенілфосфін)паладію (0) розчиняють в 80 мл ДМФА. Потім реакційну суміш кількома порціями піддають реакції у Single Mode мікрохвильовій печі (Emrys Optimizer, 5 хв. при 220°С). У об'єднані порції додають воду та двічі екстрагують толуолом. Об'єднані органічні фази промивають насиченим розчином хлориду натрію, сушать над сульфатом натрію та після цього розчинник видаляють на ротаційному випарнику. Залишок очищують колонковою хроматографією (силікагель, розчинник: циклогексан/етилацетат 10:1). Одержують 3,32 г (78% від теор.) сполуки із заголовку чистотою 80% (після РХ-МС). + МС (El-поз): m/z = 215[M] 1 Н-ЯМР (300 МГц, ДMCO-d6): δ = 7,85-7,91 (м, 3Н), 10,20 (с, 1Н). Приклад 8А 4-ціано-2-метоксифенілтрифторметансульфонат 23 UA 102065 C2 5 10 15 20 25 До розчину 20 г (134 ммоль) 4-гідрокси-3-метоксибензонітрилу в піридині (80 мл) повільно по краплях додають 24 мл (141 ммоль) ангідриду трифторметансульфонової кислоти, причому реакційну температуру за допомогою льодяної бані утримують нижче 25°С. Суспензію протягом 1 години перемішують при кімнатній температурі. Додають льодяну воду (400 мл) та суспензію знову перемішують до досягнення кімнатної температури. Потім фільтрують, тверду речовину розчиняють в етилацетаті та цей розчин промивають насиченим розчином хлориду натрію. Органічну фазу сушать над сульфатом магнію та концентрують. Одержують 37,13 г (92% від теор.) сполуки із заголовку у вигляді білої твердої речовини. + РХ-МС (метод 3): Чу = 2,54 хв.; МС (El-поз): m/z = 282 [М+Н] 1 Н-ЯМР (300 МГц, ДMCO-d6): δ = 3,97 (с, 3Н), 7,60 (дд, 1Н), 7,71 (д, 1Н), 7,92 (д,1Н). Приклад 9А Трет-бутил (2Е)-3-(4-ціано-2-метоксифеніл)акрилат У дегазований розчин 37,13 г (132 ммоль) 4-ціано-2-метоксифенілтрифторметансульфонату, 35 мл (245 ммоль) трет-бутилакрилату та 90 мл (645 ммоль) триетиламіну в ДМФА (250 мл) додають 4 г (5,7 ммоль) хлориду біс(трифенілфосфін)паладію (II). Розчин протягом 24 годин перемішують в атмосфері захисного газу при 100°С. Потім додають льодяну воду (1000 мл) та суспензію екстрагують етилацетатом (3 x 100 мл). Органічну фазу промивають насиченим розчином хлориду натрію, сушать над сульфатом магнію та концентрують. Залишок очищують колонковою хроматографією (силікагель, розчинник: циклогексан-етилацетат 10:1). Одержують 24,6 г (72% від теор.) сполуки із заголовку у вигляді білої твердої речовини. + РХ-МС (метод 1): Чу = 2,59 хв.; МС (El-поз): m/z = 260 [М+Н] 1 Н-ЯМР (300 МГц, ДMCO-d6): δ = 1,48 (с, 9Н), 3,93 (с, 3Н), 6,65 (д, 1Н), 7,42 (д, 1Н), 7,58 (с, 1Н), 7,74 (д, 1Н), 7,89 (д, 1Н). Приклад 10А 4-форміл-3-метоксибензонітрил 24 UA 102065 C2 5 10 15 20 25 30 35 40 У ретельно перемішаний розчин 48 г (185 ммоль) трет-бутилу (2Е)-3-(4-ціано-2метоксифеніл)акрилату, 207 мг (0,81 ммоль) тетроксиду осмію та 1,4 г (6,14 ммоль) хлориду бензилтриетиламонію в 750 мл води/ТГФ (2:1) порціями додають 79 г (370 ммоль) метаперіодату натрію, причому температуру реакції тримають нижче 30°С. Розчин протягом 1 години перемішують при кімнатній температурі. Додають воду (2000 мл), після чого суміш фільтрують. Тверду речовину, що залишилася, розчиняють в етилацетаті, а розчин промивають насиченим розчином хлориду натрію. Органічну фазу сушать над сульфатом магнію та концентрують. Залишок змішують з петролейним етером. Одержують 21,18 г (71% від теор.) сполуки із заголовку у вигляді білої твердої речовини. + РХ-МС (метод 3): Чу = 1,87 хв.; МС (El-поз): m/z = 162 [М+Н] 1 Н-ЯМР (300 МГц, ДМСО-d6): δ = 3,98 (с, 3Н), 7,53 (д, 1Н), 7,80 (с, 1Н), 7,81 (д, 1Н), 10,37 (с, 1Н). Приклад 11А 4-форміл-3-гідроксибензонітрил У розчин 8 г (49,64 ммоль) 4-форміл-3-метоксибензонітрилу в 80 мл безводного дихлорметану в атмосфері аргону при -78°С по краплях додають 100 мл розчину триброміду бору в дихлорметані (1 М, 100 ммоль). Реакційну суміш перемішують при кімнатній температурі до повного перетворення едукту (прибл. протягом 5 днів). Потім реакційний розчин при 0°С нейтралізують за допомогою насиченого розчину гідрокарбонату натрію. Фази розділяють та органічну фазу промивають насиченим розчином хлориду натрію, сушать над сульфатом магнію та концентрують. Залишок очищують колонковою хроматографією на силікагелі (розчинник: циклогексан/етилацетат 3:1). Одержують 4,5 г (61% від теор.) сполуки із заголовку у вигляді жовтої твердої речовини. РХ-МС (метод 1): Чу = 1,38 хв.; [N-Н] = 146 1 Н-ЯМР (300 МГц, CDCI3): δ = 7,38 (д, 1Н), 7,38 (с, 1Н), 7,77 (д, 1Н), 10,33 (с, 1Н), 11,38 (с, 1Н). Приклад 12А 5-ціано-2-формілфенілтрифторметансульфонат У розчин 2 г (13,59 ммоль) 4-форміл-3-гідроксибензонітрилу та 2,5 мл (14,27 ммоль) Ν,Νдіізопропілетиламіну в 37 мл безводного дихлорметану в атмосфері аргону при 0°С додають 2,4 мл (14,27 ммоль) ангідриду трифторметансульфонової кислоти. Реакційну суміш протягом 1 години перемішують при КТ, потім розріджують 70 мл дихлорметану та послідовно промивають 1 Μ соляною кислотою, насиченим розчином гідрокарбонату натрію і насиченим розчином хлориду натрію. Органічний розчин сушать над сульфатом магнію та концентрують. Залишок очищують колонковою хроматографією на силікагелі (розчинник: циклогексан/етилацетат 7:1). Одержують 2,36 г (62% від теор.) сполуки із заголовку у вигляді білої твердої речовини. + РХ-МС (метод 3): Чу = 2,34 хв.; [М+Н] = 280 1 Н-ЯМР (300 МГц, CDCI3): δ = 8,27 (м, 2Н), 8,33 (с, 1Н), 10,13 (с, 1Н). Приклад 13А 4-форміл-3-вінілбензонітрил 25 UA 102065 C2 5 10 15 20 25 30 35 У розчин 1 г (3,58 ммоль) 5-ціано-2-формілфенілтрифторметансульфонату та 1,15 мл (3,94 ммоль) три-н-бутилвінілстанану в 6 мл безводного та дегазованого ДМФА в атмосфері аргону додають 125 мг (0,18 ммоль) хлориду біс(трифенілфосфін)паладію (II). Потім реакційну суміш протягом 90 хвилин перемішують при 80°С. Після цього додають 100 мл 10%-ного розчину фториду калію та суміш протягом 1 години перемішують при КТ. Суспензію тричі екстрагують відповідно 20 мл етилацетату, а об'єднані органічні фази послідовно промивають насиченим розчином гідрокарбонату натрію та насиченим розчином хлориду натрію. Органічний розчин сушать над сульфатом магнію та концентрують. Залишок (0,6 г) без попереднього очищення використовують на наступній стадії. + ГХ-МС (метод 5): Чу = 5,02 хв.; [М] = 157 1 Н-ЯМР (300 МГц, CDCI3): δ = 5,62 (д, 1Н), 6,05 (д, 1Н), 7,58 (дд, 1Н), 7,95 (д, 1Н), 8,00 (д, 1Н), 8,24 (с, 1Н), 10,32 (с, 1Н). Приклад 14А 3-етил-4-формілбензонітрил У розчин 1,3 г (8,27 ммоль) 4-форміл-3-вінілбензонітрилу в 35 мл етанолу додають 880 мг 10%-ного паладію на вугіллі та протягом 2 годин ретельно перемішують в атмосфері водню. Суспензію фільтрують через шар силікагелю, залишок промивають етанолом, а фільтрат концентрують. Залишок (890 мг) без попереднього очищення використовують на наступній стадії. 1 Н-ЯМР (300 МГц, CDCI3): δ = 1,2 (τ, 1Η), 3,07 (кв, 2Н), 7,88 (д, 1Н), 7,90 (с, 1Н), 7,97 (д, 1Н), 10,32 (с, 1Н). Приклад 15А Метил 4-ціано-2-фторбензоат 13,20 г (79,9 ммоль) 4-ціано-2-фторбензойної кислоти розчиняють в 300 мл ацетону. Потім послідовно додають 22,10 г (159,9 ммоль) карбонату калію та 9,08 мл (95,9 ммоль) диметилсульфату. Протягом 20 хвилин перемішують при кип'ятіння зі зворотнім холодильником. Потім у реакційну суміш додають 300 мл води, а ацетон видаляють на роторному випарнику. Кілька разів екстрагують дихлорметаном. Об'єднані органічні фази промивають насиченим розчином хлориду натрію та сушать над сульфатом натрію. Після цього розчинник видаляють у вакуумі. Тверду речовину, що залишилася, без попереднього очищення використовують на наступній стадії. Одержують 16,1 г (84% від теор.) сполуки із заголовку у вигляді безбарвної твердої речовини. 26 UA 102065 C2 + ГХ-МС (метод 5): Чу = 6,23 хв.; [М] (El-поз): m/z = 179 1 Н-ЯМР (300 МГц, ДМСО-d6): δ = 3,90 (с, 3Н), 7,83 (дд, 1Н), 8,01-8,08 (м, 2Н). Приклад 16А 3-фтор-4-(гідроксиметил)бензонітрил 5 10 15 20 25 30 16,10 г (89,9 ммоль) метил 4-ціано-2-фторбензоату розчиняють в 150 мл метанолу. Потім порціями додають 3,40 г (89,9 ммоль) боргідриду натрію. Після повного перетворення (ТШХконтроль) за допомогою розрідженої соляної кислоти встановлюють значення рН 3 та кілька разів екстрагують дихлорметаном. Об'єднані органічні фази промивають насиченим розчином хлориду натрію та сушать над сульфатом магнію. Потім розчинник видаляють у вакуумі, а залишок очищують колонковою хроматографією (силікагель, розчинник: циклогексан/етилацетат 15:1 3:7). Одержують 3,70 г (27,2% від теор.) сполуки із заголовку. + ГХ-МС (метод 5): Чу = 6,51 хв.; [М] (El-поз): m/z = 151 1 Н-ЯМР (300 МГц, ДMCO-d6): δ = 4,61 (с, 2Н), 5,53 (с, 1Н), 7,61-7,74 (м, 2Н), 7,79 (дд, 1Н). Приклад 17А 3-фтор-4-формілбензонітрил 1,00 г (6,62 ммоль) 3-фтор-4-(гідроксиметил)бензонітрилу розчиняють в 50 мл дихлорметану та додають 9,20 г (105,9 ммоль) оксиду марганцю (IV). Протягом ночі перемішують при кімнатній температурі та після цього фільтрують на через коротку силікагелеву колонку. Розчинник відганяють при пониженому тиску, а залишок очищують колонковою хроматографією (силікагель, розчинник: дихлорметан). Одержують 120 мг (12,1% від теор.) сполуки із заголовку. + ГХ-МС (метод 5): Чу = 5,11 хв.; [М] (El-поз): m/z = 149 1 Н-ЯМР (300 МГц, ДМСО-d6): δ = 7,89 (д, 1Н), 8,00 (т, 1Н), 8,11 (д, 1Н), 10,24 (д, 1Н). Приклад 18А 3-хлор-4-формілбензонітрил 25,0 г (164,91 ммоль) 3-хлор-4-метилбензонітрилу розчиняють в 150 мл ДМФА та додають 25,55 г (214,39 ммоль) диметилацеталю Ν,Ν-диметилформаміду. Протягом 20 годин перемішують при 140°С та після цього протягом 4 годин - при 180°С температури масляної ванни. Леткі компоненти виділяють на ротаціному випарнику, а залишок вводять у подальшу реакцію. 27 UA 102065 C2 5 10 15 20 25 30 35 Одержаний таким чином сирий 3-хлор-4-[2-(диметиламіно)вініл]бензонітрил поміщають в 500 мл ТГФ/води (1:1) та додають 77,6 г (362,9 ммоль) періодату натрію. Протягом 18 годин перемішують при кімнатній температурі, після чого осад виділяють фільтрацією. У фільтрат додають насичений розчин гідрокарбонату натрію та тричі екстрагують етилацетатом. Об'єднані органічні фази сушать над сульфатом натрію, а розчинник випаровують на ротаційному випарнику. Неочищений продукт очищують колонковою хроматографією (силікагель, розчинник: циклогексан/етилацетат 7:3). Одержують 3,0 г (15% від теор.) сполуки із заголовку. + ГХ-МС (метод 5): Чу = 6,64 хв.; [М] (El-поз): m/z = 165 1 Н-ЯМР (300 МГц, ДМСО-d6): δ = 7,97-8,03 (м, 2Н), 8,27 (с, 1Н), 10,34 (д, 1Н). Приклад 19А 4-форміл-1-нафтонітрил 2,50 г (14,95 ммоль) 4-метил-1-нафтонітрилу розчиняють в 40 мл тетрахлорметану та додають 3,19 г (17,94 ммоль) N-бромсукциніміду, а також 245 мг (1,50 ммоль) 2,2’-азобіс-2метилпропаннітрилу. Протягом ночі перемішують при кип'ятінні зі зворотнім холодильником. Після охолодження продукт відфільтровують. Одержують 2,75 г (74,7% від теор.) 4(бромметил)-1-нафтонітрилу чистотою 90%, який без попереднього очищення вводять у подальшу реакцію. 2,75 г (11,17 ммоль) одержаного таким чином броміду розчиняють в 60 мл ацетонітрилу та додають 2 г молекулярного сита (3А). Потім додають 1,44 г (12,29 ммоль) N-метилморфолін-Nоксиду та суміш протягом ночі перемішують при кімнатній температурі. Потім суміш фільтрують через силікагель, а фільтрат концентрують. Залишок очищують через картридж Biotage (40 Μ) (елюент: ізогексан/етилацетат 3:1). Фракції продукту об'єднують, розчинник видаляють на роторному випарнику, а залишок змішують з діетиловим етером, при цьому відбувається кристалізація. Промивають незначною кількістю діетилового етеру та сушать у високому вакуумі. Одержують 254 мг (12,6% від теор.) сполуки із заголовку. + РХ-МС (метод 3): Чу = 2,27 хв.; [М+Н] (El-поз): m/z = 182 1 Н-ЯМР (300 МГц, CDCI3): δ = 7,79-7,87 (м, 2Н), 8,05 (д, 1Н), 8,09 (д, 1Н), 8,37 (м, 1Н), 9,27 (м, 1Н), 10,51 (с, 1Н). Приклад 20А 2-ціаноетил 4-(4-ціано-2-метоксифеніл)-2-метил-5-оксо-1,4,5,6-тетрагідро-1,6-нафтиридин-3карбоксилат 14,63 г (90,81 ммоль) сполуки з прикладу 10А, 10,00 г (90,81 ммоль) 4-амінопіридин-2(1Н)ону [Searls, Т., McLaughlin, L.W., Tetrahedron 55, 11985-11996 (1999)] та 15,65 г (90,81 ммоль) 2ціаноетил-3-оксобутаноату [Yamamoto, Т., et al., Bioorg. Med. Chem. Lett. 16, 798-802 (2006)] розчиняють в 300 мл ізопропанолу та протягом 3 днів перемішують в атмосфері аргону при 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted 4-aryl-1,4-dihydro-1,6-naphthyridinamides and use thereof
Автори англійськоюBarfacker, Lars, Kolkhof, Peter, Schlemmer, Karl-Heinz, Grosser, Rolf, Ninsche, Adam, Klein, Martina, Munter, Klaus, Albrecht-Kupper, Barbara, Hartmann, Elke
Назва патенту російськоюЗамещенные 4-арил-1,4-дигидро-1,6-нафтиридинамиды и их применение
Автори російськоюБерфаккэр Ларс, Колькхоф Пэтэр, Шлеммэр Карл-Хайнц, Гроссер Рольф, Ничэ Адам, Кляйн Мартина, Мюнтэр Клаус, Альбрэхт-Кюппэр Барбара, Хартманн Элькэ
МПК / Мітки
МПК: A61K 31/437, C07D 471/04, A61P 9/10
Мітки: заміщені, 4-арил-1,4-дигідро-1,6-нафтиридинаміди, застосування
Код посилання
<a href="https://ua.patents.su/55-102065-zamishheni-4-aril-14-digidro-16-naftiridinamidi-i-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Заміщені 4-арил-1,4-дигідро-1,6-нафтиридинаміди і їх застосування</a>
Попередній патент: Вузол з двох пар баків і літальна пускова установка, оснащена таким вузлом
Наступний патент: Спосіб і пристрій для підготовки сировини при виготовленні паперу, картону або волокнистих плит
Випадковий патент: Прилад для сепарування сипких матеріалів