Спосіб одержання нітріту лужного металу
Номер патенту: 3795
Опубліковано: 27.12.1994
Автори: Ферд Максим Львович, Бельцер Іосип Ісаакович, Радченко Олександр Андрійович, Гусак Іван Петрович, Пукіш Михайло Данилович, Удовенко Олександр Григорович, Смалій Микола Іванович, Кисільов Віктор Ксенофонтович
Формула / Реферат
Способ получения нитрита щелочного металла, включающий взаимодействие оксидов азота с водным раствором оснований этих металлов в тарельчатой колонне, отличающийся тем, что взаимодействие проводят прямотоком в колонне с ситчатыми тарелками в инжекционном режиме, создаваемом при отношений скорости подачи газа через отверстия тарелки к скорости газа в свободном сечении колонны, равном 15-35.
Текст
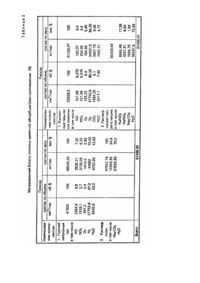
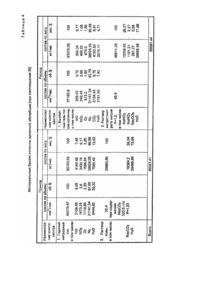
Изобретение относится к химической отрасли и касается получения нитрита щелочного металла путем взаимодействия оксидов азота с водными растворами оснований этих металлов. Наиболее близким из известных является способ получения нитритов, включающий ступени образования смеси горячего газа, содержащего оксиды азота, кислород и водяной пар, охлаждение смеси газа до температуры 300-5000С и мгновенное охлаждение такой газовой смеси в водном растворе основания для избежания контакта горячей смеси газа с холодной поверхностью (1). Полученный товарный продукт содержит до 40 вес. % нитрита натрия, 0,1-0,3 вес. % нитрата натрия, 9-10 вес. % гидроксида натрия, 0,5 вес. % карбоната натрия и 50-60 вес. % воды. Скорость подачи газа 90 кг/час, жидкости - 40-70 кг/час. К недостаткам известного способа относятся: - большое содержание в товарном продукте щелочного компонента (10 вес. %), - невозможность получения готового продукта в кристаллическом виде с малым содержанием нитрата без многократной перекристаллизации. Задачей изобретения является создание способа получения нитрита щелочного металла прямоточным взаимодействием оксидов азота с водным раствором оснований этих металлов при определенных режимах, за счет чего достигается снижение содержания в продукте щелочного компонента. Данный способ позволяет получить готовый продукт в кристаллическом виде без многократной перекристаллизации. Поставленная задача решается тем, что в способе получения нитрита щелочного металла, включающем взаимодействие оксидов азота с водным раствором оснований этих металлов в тарельчатой колонне, взаимодействие проводят прямотоком в колонне с ситчатыми тарелками в инжекционном режиме, создаваемом при отношении скорости подачи газа через отверстия тарелки к скорости газа в свободном сечении колонны, равном 15-35. Изобретение иллюстрируется схематичным изображением колонны, на котором: 1 - корпус колонны, 2 - трубопровод подачи нитрозного газа, 3 - трубопровод подачи раствора Na2CО3, 4 распределитель, 5, 6, 7, 8 - ситчатые тарелки, 9 - отбойная тарелка, 10 - трубопровод вывода нитрозного газа, 11 - трубопровод вывода раствора нитрит-нитрата натрия, 12-линия, 13 - насос, 14 - линия,15 - холодильник,16, 17 линии ввода и вывода воды, 18 - линия. Способ осуществляется следующим образом. Нитрозный газ, полученный окислением аммиака состава (об. %): NО - 5,9, NО2 - 3,9, О2 - 3,6, N2 - 69,8, H 2О 16,8 с температурой 385-4150С по трубопроводу 2 подают в нижнюю часть колонны 1 через распределитель 4. Свежий раствор карбоната натрия концентрацией 260-340 г/л и температурой 900С по трубопроводу 3 также подают в нижнюю часть колонны 1. Под тарелкой 5 осуществляется основной процесс взаимодействия (на 8690%) горячих нитрозных газов с раствором соды по реакциям: NO+NO2+Na2CO3=2NaNO2+CO2 (1) 2NO2+Na2CO3=NaNO2+NaNO3+CO2 (2) В указанной секции образуется основное количество нитрита натрия (88-91%). Остальное количество карбоната натрия срабатывается на вышележащих тарелках. Взаимодействие осуществляется на ситчатых тарелках в инжекционном режиме при относительно высоких скоростях газа и жидкости в отверстиях тарелки. При соотношении скоростей газа в отверстиях тарелки и свободном сечении колонны ниже 15 происходит переток жидкой фазы с верхнележащей на нижележащую тарелку, что приводит к нарушению содержания соды и нитрита натрия в растворе. В колонне начинается процесс инверсии, что не позволяет получить необходимое соотношение NaNO2/NaNO3 в конечном продукте. При соотношении скоростей газа в отверстиях тарелки и свободном сечении колонны выше 35 создается сопротивление в 8-10 раз выше, чем требуется для нормального прохождения газа через колонну. При инжекционном режиме взаимодействия осуществляется интенсивный захват и дробление жидкости, формируется двухфазный динамический слой, в котором сплошная фаза - газ, а дисперсная - жидкость. В слое появляются сплошные газовые каналы, которые активно транспортируют жидкость в сепарационное пространство между тарелками. В этом процессе отсутствует провал жидкости на нижележащие тарелки, что препятствует перемешиванию жидкой фазы по высоте колонны. В секции между тарелками должен быть определенный состав раствора и должно срабатываться определенное количество щелочи и оксидов азота из нитрозных газов, Под первой тарелкой содержание щелочи 6-7 вес. %, на последней тарелке (продукционном растворе)- 0,5 вес. %. Отвод реакционного и физического тепла нитрозных газов осуществляется принудительной циркуляцией по схеме: линия 12, насос 13, линия 14, холодильник 15, линия 18. Охлаждение производят водой, поступающей по линии 17 и отводящей линии 16. Смесь нитрозного газа и раствора соды проходит все тарелки снизу вверх прямотоком. С 8-й тарелки непрореагировавший нитрозный газ по трубопроводу 10 поступает в колонну кислой абсорбции на получение азотной кислоты. Полученный раствор нитрит-нитрата натрия по трубопроводу 11 подают на дальнейшую переработку для получения кристаллического товарного продукта. Изобретение поясняется приведенными ниже примерами. Пример 1 (оптимальный вариант). Полученные окислением аммиака нитрозные газы в количестве 50909,71 кг/ч состава (вес. %): NO-7,48, NO26,17, O2-2,85, N2 - 69,88, H2O - 13,62 с температурой 4000С и давлением 0,6 МПа поступают по тр убопроводу 2 через распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку 5, куда по трубопроводу 3 подают раствор соды в количестве 40333,31 кг/час состава (вес. %): Na2CO3 - 25,75, H2O - 74,25 с температурой 800С и давлением 0,9 МПа, соотношение скоростей 28. Линейная скорость газа в отверстиях тарелки 11,585 м/сек, а линейная скорость в свободном сечении колонны -0,412 м/сек. Смесь нитрозного газа и раствора соды проходит все перфорированные тарелки 5, 6, 7, 8, на которых осуществляется процесс их взаимодействия с получением нитрит-нитрата натрия. С тарелки 8 непрореагировавшии нитрозный газ в количестве 42731,65 кг/час состава (вес. %): NО - 0,19, NО2 - 0,19, О2 - 1,83, N2-83,26, CО2 - 9,81, H2О-4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты. По трубопроводу 11 выводят раствор нитрит-нитрата натрия в количестве 48511,38 кг/час состава (вес. %): NaNO2 - 25,27, NaNO3 - 2,27, Na2CО2 - 0,58, H2O - 71,86 и направляют на дальнейшую переработку для получения кристаллического продукта с соотношением NaNO2/NaNO3 = 11, содержание щелочного компонента 0,58 вес. %. Материальный баланс приведен в таблице 1. Пример 2. Нитрозные газы в количестве 49545,25 кг/час состава (вес. %): NO -7,26, NО2 - 6,33, О2 - 2,86, N2 70,02, H2О -13,53 с температурой 4000С и давлением 0,6 МПа поступают по трубопроводу 2 через распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку 5, куда по трубопроводу 3 подают раствор соды в количестве 41922,78 состава (вес. %): Na 2CО 3-24,8, H 2О - 75,2 с температурой 800С, соотношение скоростей 15 (6,18:0,412 = 15) Смесь (жидкость-газ) проходит все перфорированные тарелки 5, 6, 7, 8, на которых проходит процесс их взаимодействия с получением нитрит-нитрата натрия. С тарелки 8 непрореагировавший нитрозный газ в количестве 41127,77 кг/час состава (вес. %): NO - 0,4, NО 2 – 0,6, О 2 – 0,45, N2 - 91,35, СО - 9,48, H2 О - 4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты. По трубопроводу 11 выводят раствор нитрит-нитрата натрия в количестве 50337,47 кг/час состава (вес. %): NaNО2 -17,27, NaNО3 - 8,64, NаCО3 - 2,00, H2O -72,09 и направляют на дальнейшую переработку для получения кристаллического продукта с соотношением NaNО2/NaNО3 = 2. Содержание щелочного компонента 2,00 вес. %. Материальный баланс приведен в таблице 2 Пример 3. Нитрозные газы в количестве 48349,88 кг/час состава (вес. %): NO -7,29, NО2 - 6,02, О2 - 3,31, N2 69,98, H2O -13,4 с температурой 4000С и давлением 0,6 МПа поступают по трубопроводу 2 через распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку 5, куда по трубопроводу 3 подают раствор соды в количестве 41485,95 состава (вес. %): Na2CО3 - 23,12, H 2О - 76,88 с температурой 800С, соотношение скоростей 20 (8,24 : 0,412 = 20). Смесь (жидкость и газ) проходит все перфорированные тарелки 5, 6, 7, 8, на которых проходит процесс взаимодействия с получением нитрит-нитрата натрия. С тарелки 8 непрореагировавший нитрозный газ в количестве 40640,48 кг/час состава (вес. %): NО - 0,37, NО2 - 0,31, О 2 - 1,98, N2 - 83,26, CО2 - 9,36, H2О - 4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты. По трубопроводу 11 выводят раствор нитрит-нитрата натрия в количестве 49195,32 кг/час состава (вес. %); NaNО2 -20,92, NaNО3 - 4,13, Na2CО3 - 0,85, H2О -74,10 и направляют на дальнейшую переработку для получения кристаллического продукта с соотношением NaNО2/NaNО3 = 5. Содержание щелочного компонента 0,85. Материальный баланс приведен в таблице 3. В таблице 4 приведен материальный баланс при соотношении скоростей равном 35 (14,42:0,412=35). Положительный эффект изобретения по сравнению с известным состоит - в уменьшении щелочного компонента в готовом продукте в 5-20 раз, - в том, что способ дает возможность получать раствор, из которого можно получать кристаллический продукт. Кроме указанных преимуществ необходимо отметить то, что способ успешно можно использовать в промышленных условиях без значительных затрат. Способ можно рассматривать как элемент технологической схемы получения азотной кислоты при повышенном давлении.
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of nitrite of alkali metal
Автори англійськоюUdovenko Oleksandr Hryhorovych, Smalii Mykola Ivanovych, Kisiliov Viktor Ksenofontovych, Pukish Mykhailo Danylovych, Beltser Iosyp Isaakovych, Husak Ivan Petrovych, Ferd Maksym Lvovych, Radchenko Oleksandr Andriiovych
Назва патенту російськоюСпособ получения нитрита щелочного металла
Автори російськоюУдовенко Александр Григорьевич, Смалий Николай Иванович, Киселев Виктор Ксенофонтович, Пукиш Михаил Данилович, Бельцер Иосип Исаакович, Гусак Иван Петрович, Ферд Максим Львович, Радченко Александр Андреевич
МПК / Мітки
МПК: C01B 21/50
Мітки: спосіб, металу, лужного, нітріту, одержання
Код посилання
<a href="https://ua.patents.su/6-3795-sposib-oderzhannya-nitritu-luzhnogo-metalu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання нітріту лужного металу</a>