Композиція для профілактики та лікування раку
Формула / Реферат
1. Композиція, що має профілактичні протиракові ефекти, яка відрізняється тим, що містить від 20 до 99,99 ваг.% продукту біосинтезу мікроорганізму Penicillium oxalicum вар. Armeniaca CCM 8242, отриманого ферментацією живильного середовища, що містить карбогідрати та амонійний азот і від 0,01 до 80 ваг.% фізіологічнo інертного носія, і довільно допоміжних добавок.
2. Композиція за п. 1, яка відрізняється тим, що продукт біосинтезу складається з хромофорного червоного барвника, який є похідним антрахінону формули І
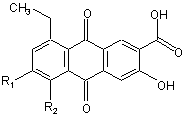 (I),
(I),
в якій R1 є гідрокси і R2 - 3-метил-1,3-бутадієніл, і довільно R1, і R2 - циклізовані разом через атом кисню гідроксильної групи.
3. Композиція за п. 2, яка відрізняється тим, що хромофор є 8-етил-3,6-дигідрокси-5[(1Е)-3-метил-1,3-бутадієніл]-9,10-діоксо-9,10-дигідроантрацен-2-карбоновою кислотою.
4. Композиція за п. 2, яка відрізняється тим, що хромофор є 6-етил-10-гідрокси-3,3-диметил-7,12-дигідро-3Н-нафто[2,3-f]хромен-9-карбоновою кислотою.
5. Композиція за п.1, яка відрізняється тим, що використовується як харчова добавка, яка має профілактичну протиракову активність.
6. Композиція за п.1, яка відрізняється тим, що використовується як фармацевтична композиція для призначення людині з метою інгібування утворення пухлин.
7. Композиція за будь-яким з пп.1-4, яка відрізняється тим, що вона містить від 11 до 75 ваг.% мальтодекстрину як фізіологічно інертного носія.
8. Композиція за п.1, яка відрізняється тим, що вона містить від 30 до 40 ваг.% крохмалю як фізіологічнo інертного носія.
9. Композиція за будь-яким з пп.1-4, яка відрізняється тим, що вона представлена одиничною дозованою формою.
10. Композиція за будь-яким з пп.1-4 або 9, яка відрізняється тим, що вона представлена у формі таблетки, капсули або пілюлі.
11. Композиція за будь-яким з пп.1-5, яка відрізняється тим, що вона включає фізіологічнo прийнятну рідину як носій.
12. Продукт, особливо харчовий продукт, який відрізняється тим, що він включає композицію за будь-яким з пунктів 1-5 або 7-8.
Текст
1. Композиція, що має профілактичні протиракові ефекти, яка відрізняється тим, що містить від 20 до 99,99 ваг.% продукту біосинтезу мікроорганізму Penicillium oxalicum вар. Armeniaca CCM 8242, отриманого ферментацією живильного середовища, що містить карбогідрати та амонійний азот і від 0,01 до 80ваг.% фізіологічнo інертного носія, і довільно допоміжних добавок. 2. Композиція за п.1, яка відрізняється тим, що продукт біосинтезу складається з хромофорного червоного барвника, який є похідним антрахінону формули І C2 2 UA 1 Винахід стосується харчової добавки, що має профілактичні протиракові ефекти. Були відомі різні харчові добавки для доповнення до їжі, особливо людської їжі, які мають корисний вплив на стан здоров'я і, довільно, інгібуючу дію щодо виникнення деяких хвороб. [Чеський патент номер 285721 (WO 99/50434)] розкриває штам мікроорганізму Penicillium oxalicum вар. Armeniaca CCM 8242, що продукує червоний барвник, і використання вказаного барвника як, inter alia, харчового. Штам був задепонованований в Міжнародному Депозитарному Органі ССМ - Чеська Колекція Мікроорганізмів Masaryk 3 76724 Університету, Tvrdeho 14, 602 00 Брно, Чеської Республіки, 19 березня 1998. Це - природний мікроорганізм, отриманий з ґрунту долини нижче гори Арарат. Тепер було знайдено, що продукт, отриманий біосинтезом мікроорганізму Penicillium oxalicum вар. Armeniaca CCM 8242, використовуваний в харчових добавках, надає протиракові властивості згадуваним добавкам. Відповідно, винахід полягає в харчовій добавці, що має профілактичні протиракові ефекти, причому добавки включають від 20 до 99,99ваг.% продукту біосинтезу мікроорганізму Penicillium oxalicum вар. Armeniaca CCM 8242, отриманого ферментацією живильного середовища, що містить карбогідрати й амонійний азот, і від 0,01 до 80ваг.% фізіологічно інертного носія, і необов'язково допоміжні добавки. Щоб одержати продукт біосинтезу, можливо культивувати продуктивний штам загальними процесами ферментації. Коли червоний барвник, отриманий, методом ізолювання від культивувального водного середовища після сепарації біомаси, був підданий спектральному аналізу, було знайдено, що наявність змісту сухої речовини не менше, ніж 85ваг.% , містить не менше, ніж 52ваг.% барвної речовини. Принцип, забарвлення базується на хромофорі типу антрахінону. Барвник складається з суміші субстанцій, що містять, згаданий хромофор і які відрізняються від основної структури бічними ланцюгами, олігопептидів або олігосахаридів. Сам хромофор - пента-заміщений антрахінон, що має три ізольованих водневих каркаси. Така сполука може бути зображена, наприклад, загальною формулою (I) в якій R1 - гідрокси, і R2 - 3-метил-1,3бутадієніл, і необов'язково R1 і R2 - циклізовані разом через атом кисню гідроксилу. Таким чином, формула Іа відповідає основному варіантові, і формула Іb відповідає циклізованому. (Ia) (Iб) 4 Відповідно, формули, la і Іб виразно зображують 8-етил-3,6-дигідрокси-5[(1Е)-3-метил-1,3бутадіеніл]-9,10-діоксо-9,10-дигідроантраценкарбонову кислоту і 6-етил-10-гідрокси-3,3диметил-7,12-дилдро-ЗН-нафто[2,3-f]хромен-9карбонову кислоту, відповідно. У продукті біосинтезу забарвлювальна субстанція може бути присутня у поєднанні з катіонами амонію, калію або натрію, що можуть бути присутнім у надлишку. Як побічні, можуть бути присутні субстанції білкової природи (амінокислоти, пептиди) з початкового живильного середовища у цих продуктах. Щоб одержати червоний барвник, можливо виконати культивування продуктивного штаму в рідких живильних середовищах звичайними методами, наприклад поверхневим методом на тарілках або пластинах або методом занурення у ферментери. Кількість інокульованого матеріалу - від 3 до 7% за об'ємом. Для інокуляції в капусту, зерно або дріжджовий екстракт, дріжджовий аутолізат використовували культури, інкубовані протягом п'яти днів. Оптимальні умови для проведення процесу мікробіологічного синтезу включають температури від 27 до 29°С, безперервне перемішування з вектором периферійної швидкості від 160 до 280хв-1, постачання повітря в пропорціях на 1,2 об'ємів повітря 1,0 об'ємів живильного середовища, тиск в експлуатаційному ферментері від 50 до 80кПа. Вже після ферментації мікроорганізму від 24 до 35 годин, рідина вище культури стає червоною, і інтенсивність червоного кольору - у його максимумі темний світло-вишневий колір - після інкубаційного періоду від 64 до 72 годин. Як компоненти живильного середовища використовуються карбогідрати, різні сахариди, багатоатомні спирти і вуглеводні, і також відходи цукрового виробництва - патока - у кількості від 10 до 20г на 1 літр води. Як постачальники азоту, можуть використовуватись, наприклад зерновий екстракт, аутолізат дріжджів або екстракт, і також сполуки, що містять азот у різних формах (такі як амінокислоти) у кількості азоту від 0,5 до 0,7ваг.%. Фахівець в даній галузі оцінить, що цей винахід не обмежений вище описаним використанням особливо переважного штаму Penicillium oxalicum вар. Armeniaca CCM 8242, але використання інших штамів або мутантів згадуваного мікроорганізму, що продукують червоний барвник, отриманий звичайними методами, наприклад, опромінюючи рентгенівськими променями або УФ, або дією фага і т.п. також охоплені концепцією і областю даного винаходу. Після завершення біосинтезу, отриманий червоний барвник може бути ізольований від живильного середовища звичайними методами відділення. Ферментаційне середовище може бути, після сепарації біомаси або без сепарації біомаси, піддане ультрафільтрації і потім сконцентроване нано-фільтрацією у концентрат, що має зміст від 80 до 100г/л барвника. Альтернативно, рідину фільтрують або центрифугують від живильного середовища у порядку сепарації біомаси. Для осадження 5 барвника, рідину підкислюють до рН від 3,0 до 2,5. Підкислення може бути здійснене будь-якою органічною або неорганічною кислотою, прийнятною в харчовій промисловості. Осадження може бути виконане з сульфатом алюмінію-калію AIK2(SO4)3. Після осадження, барвник відокремлювали від рідини, наприклад центрифугуванням або фільтруванням. В аналітичній оцінці, таким чином ізольований продукт показує наступні характеристики. Барвник темно-червоний до чорного порошку, що є розчинним у лужному середовищі при рН від 8 до 9 (NH3), у крижаній оцтовій кислоті, у яєчному білку, в етиловому спирті, у метанолі, у бутанолі, 76724 6 частково в ацетоні, і нерозчинним в гексані, в ефірі, в бензолі, тетрахлорметані, і утворює нерозчинні у воді хелати з металами. Виготовлені розчини - малиново-червоні до темного червоного, стабільний при значеннях рН від 9 до 4, і вони майже не змінюють відтінок в залежності від значень рН. Забарвлення нейтрального розчину не змінюється (на відміну від карміну, бетаніну, антоціану) навіть при кип'ятінні розчину протягом 30 хвилин. Розчинність у воді приблизно 100г/л. При оцінці хімічної чистоти, в одержаному продукті були знайдені наступні значення (у мас.%): Хімічна чистота: Суха речовина не менше, ніж 85% Зміст забарвлювальної субстанції не менше, ніж 52% Зола не більше, ніж 12% не більше, ніж 2,7% -аміно азот Важкі метали: миш'як: не більше, ніж 3мг/кг свинець не більше, ніж 10мг/кг ртуть не більше, ніж 1мг/кг кадмій не більше, ніж 1мг/кг Мікотоксини: Афлатоксини (сум. В1, В2, G1, G2) не більше, ніж 10нг/кг Охратоксин А не більше, ніж 20мкг/кг Стеригматоцистин не більше, ніж 10мкг/кг Т-2 токсин не більше, ніж 50мкг/кг Секалонова кислота не більше, ніж 12,5мкг/кг Антибіотична активність: відсутня Мікробна чистота: загальна кількість бактерій не більше, ніж 5000/г загальна кількість грибків не більше, ніж 100/г Сальмонелла відсутня в 25г зразка Escherichia coli відсутня в 10г зразка Метод оцінки гравіметрія спектрометрія гравіметрія формольне титрування ААС ААС ААС ААС HPLC-FLD HPLC-FLD TLC-fluoresc. GLC-ECD HPTLC Codex Alimentarius Прим.: AAC - атомно-сорбційна спектрофотометрія; HPLC - високоефективна рідинна хроматографія; TLC - тонкошарова хроматографія; HPTLC - високоефективна тонкошарова хроматографія; GLC - газорідинна хроматографія. Червоний барвник, ізольований при вищезгаданих описаних умовах і наявності вищезгаданих характеристик, тестували на гостру оральну токсичність, на 90-денну субхронічну токсичність, гостре шкірне/очне подразнення, антибіотичний вплив, цитотоксичність, мутагенність і протиракову активність. Гостра оральна токсичність: У тесті на гостру оральну токсичність на мишах, виконаному відповідно до принципів OECD для тестування хімічних сполук, ніякі токсичні ефекти і летальні випадки у тварин не спостерігалися після разової дози 2г/кг ваги тіла. Субхронічна токсичність: При 90-денному субхронічному токсикологічному вивченні на пацюках відповідно до принципів OECD Номер 408, тестований барвник призначався сумарно 120 SPF Han: пацюкам лінії Вістар в дозах 0,5, 10,0 і 25,0мг/кг щодня протягом 90 днів. Пероральне введення здійснювали через зонд. При наступній гістопатологічній експертизі ніякі зміни, приписувані тестованій субстанції не були знайдені; ні гепатотоксичні ні нефротоксичні ефекти не були знайдені. При гістопатологічній експертизі тестована субстанція виявила не достовірну гематотоксичність і при біохімічній експертизі тестована субстанція не мала ніякого явного ефекту при моніторингу біохімічних параметрів. Шкірне/очне подразнення: Тест гострого шкірного подразнення виконували відповідно до принципів OECD, номер 404 і ніякі гострі подразнювальні ефекти не були знайдені. Не спостерігалися ніякі симптоми подразнення протягом до 48 годин після введення. Тест гострого очного подразнення був виконаний відповідно до Принципів OECD Номер 405. Червоний барвник показав помірні ефекти в тесті гострого подразнення (тільки на кон'юнктиві); ніякі ознаки не спостерігались після 72 годин після введення. 7 76724 Антибіотична активність: Субстанція була протестована на штамах Staphylococcus aureus, Escherichia coli, Bacillus cereus, Bacillus circulans, Streptococcus pyogenes і Serratia marcescens виконували на трьох паралельних доріжках для кожного штаму (усього 18 Чашок Петрі). Ніяке гальмування росту не спостерігалося навколо нанесеного диска в кожній із чашок, навіть в тих, що зберігались при зниженій температурі протягом 16 годин перед 24-годинним культивуванням безпосередньо (які повинні були поліпшити прояв субстанцій, що повільно мігрують в агарі). Цитотоксичність: Цитотоксичність була оцінена стандартним мікронуклеарним тестом на мишах. Червоний барвник, призначений в разовій дозі per os 2,15 і 50мг/кг, не показав ніякого цитотоксичного ефекту. Кількість мікроядер в еритроцитах не збільшилися після введення. Субстанція, яку піддавали тестуванню не показала ніякого мутагенного ефекту. Мутагенність: Тест на мутагенність (реверсійно-мутаційний тест на канцерогенність) виконали на гістидинауксотрофному штамі Salmonella typhimurium відповідно до Принципів OECD Номер 471. За даних умов ніякого впливу продукту на мутації бактерій не спостерігалось. Протиракова активність: Червоний барвник виділений згідно з вищеописаними умовами, що мають вищеописані характеристики був підданий скринінговому вивченню на протиракові властивості. Субстанція, що підлягає тестуванню, була введена мишам з асцитичною формою лімфосаркоми Гарднера (IP-LsG). 6-(2-(2-гідроксиетил)аміно етил)-5,11-діоксо-5,6-дигідро-11Н-індено[1,2с]ізохіноліну гідрохлорид, загальної формули C20H18N2O3 HCL використовувався як еталонна сполука. Використовувалися миші жіночої статі С3Н, вагою від 26,1 до 27,3г. Тварини зберігалися в пластмасових контейнерах і знаходились на NOE дієті, розробленій RATIO, s.r.o., Breclav, Чеська Республіка, і вживали питну воду ad libitum. В камері підтримувалася температура, відносна вологість становила 60%, і світловий режим не регулювався. Лімфосаркому Гарднера у СН3 мишах підтримували в асцитичній формі, інокулюючи асцитичні 8 клітини віддалені тижнем після попередньої інокуляції через пункцію черевної порожнини. Мишам вводили 0,2мл асцитичної рідини, розведеної розчином натрію хлориду для ін'єкцій інтраперитонеально до 20 разів. Клітинний матеріал для тестів отримали пункцією черевної порожнини на сьомий день після інокуляції. Для терапевтичного тесту, був введений інокулят асциту, розведений ізотонічним розчином натрію хлориду, 107 клітин в об'ємі 0,2мл і.р. кожній тварині. С3Н миші були 6 тижнів старшими, з вагою від 26,1 до 27,3г, у групах 10 тварин, контроль був загальній. Два типи дозувань використовувалися для кожного шляху введення і для однієї тестованої субстанції. Рівні дозувань: 200 і 100мг/кг x 5 р.о. і 100 і 50мг/кг x 5 s.c. в об'ємі від 0,2 до 0,4мл і від 0,2 до 0,4мл р.о. (еталонної субстанції), відповідно на 20г ваги тіла. Частота введення: 1х щоденню, починаючи з першого дня. Тестована субстанція призначалася по безперервній схемі з першого по 5-й день у дозах, наведених в Таблиці 1 і контрольна субстанція призначались р.о. один раз в 1-ий день. Після завершення введення, тварини були залишені для моніторингу часу виживання. Дозозалежний період виживання був оцінений у порівнянні з необробленим контролем. Період часу як біологічна відповідь був оцінений за допомогою непараметричного тесту згідно Hajek [Fabian V.: Zakladm statisticke metody ("Основні Статистичні Методи"), NCSAV, Прага 1963]. Після того, як експеримент був завершений, був оцінений період часу у випадку оцінки характеристик, використовуючи тест тотожності двох засобів (t-тест Стьюдента) на основі припущення розподілення н-логарифмічних значень часу і на основі припущення різних невідомих дисперсій [Roth Z., Josffko M., Maly V., - Trcka V.: "Статистичні Методи в Експериментальній Медицині"); р.278, SZN, Прага 1962]. Геометричні середні були розраховані від індивідуальних значень часу до смерті. Розходження в середніх значеннях, у яких значення тестового критерію перевищило критичне значення для рівня значимості 5%, були позначені як статистично істотні. Сумарні результати наведені в наступних таблицях: Таблиця 1 Таблиця ілюструє медіани періоду часу до смерті, статистично значимого, оціненого за допомогою непараметричного тесту згідно Hajek при рівні значимості =0,05 і оцінки числа тварин, що виживають, співвіднесених з початковим значенням в залежності від доз субстанцій субстанція контроль Червоний Барвник Lot 290698 Доза мг/кг/день 0 10 Медіана часу до смерті (дні) 14 Виживання К-сть тварин, виживших на 65-й день 0/10 200 р.о. 10 15 1/10 100 р.о. 100 s.с 50 s.c. 10 10 10 14 13 13 0/10 0/10 0/10 n (J) Примітка 1) 9 76724 10 Продовження таблиці 1 еталон 200 р.о. 100 р.о. 10 10 >65 >48 10/10 5/10 1) 1) n - число тварин у групі 1) Статистично істотна різниця проти контролю при рівні значимості =0,05 Таблиця 2 Таблиця ілюструє середні періоди життя, довірчі інтервали для геометричного середнього для Ρ=1= =0,95 і відносні значення середнього часу життя в % контролю в залежності доз субстанцій субстанція контроль Червоний Барвник Lot 290698 Доза мг/кг/день 0 n(J) 10 Геометрич. середня Довірчі інтервали (дні) (дні) 14,05 /12,6; 15,7/ Виживання (% контролю) 100 200 р.о. 10 >17,50 /12,5;24,6/ >125 100 р.о. 100 s. с 50 s.c. 10 10 10 14,33 12,87 13,86 /13,3; 15,4/ /12,3; 13,5/ /11,9; 16,2/ Примітка 102 92 99 n - число тварин у групі Таблиця 3 Таблиця ілюструє середню вагу тварин на початку експериментa і коефіцієнт втрати ваги у порівнянні з контрольною групою в залежності від дозування субстанцій в перший тиждень після початку терапії субстанція контроль Червоний Барвник Lot 290698 еталон Доза мг/кг/день 0 n(J) 10 Середня вага (г) 26,1 Коефіцієнт ваги % 0,00 200 р.о. 10 27,2 -5,00 100 р.о. 100S.C. 50 s.c. 200 р.о. 100 р.о. 10 10 10 10 10 27,2 27,3 26,7 26,7 26,1 Примітка -5,00 -5,99 -1,60 -14,63 -6,67 n - число оцінених тварин у групі Може бути встановлено, базуючись на результатах, наведених у вищезгаданих таблицях, що оптимальна доза може бути знайдена біля найвищої тестованої дози 200мг/кг x 5, тобто при кумулятивній дозі 1г/кг р.о. Можливо передбачити різницю в характеристиці активності кривої при орапьних і підшкірних введеннях, метаболічного перетворення субстанції у печінці. Виходячи з припущення інтенсивного метаболізму, повторна доза 600мг/м2 р.о. може бути визначена як допустима для людини. Ця доза відповідає 16,2мг/кг, р.о., яка відповідає повторній добовій дозі 1135мг р.о. х 5, тобто до сукупної дози 5,67г р.о. для людини вагою 70кг. Тестована субстанція не виявляє токсичності, хоча її введення пов'язане з втратою ваги менше, ніж 10%, особливо у порівнянні з еталонною субстанцією. Крива активності на Фіг. представляє функцію натурального логарифма відносного ризику індексу R в залежності дози субстанції при різних шляхах введення. Приклади Приклад 1 Живильне середовище, що містить 12г/л цукру, 5г/л зернового екстракту, 0,002г/л сірчанокислого цинку і 0,001г/л сульфату магнію інокулювали двох-денною культурою Penicillium oxalicum вар. Armeniaca CCM 8242, який був культивований в інокуляторі, в кількості 4об.% живильного середовища. Після закінчення біосинтезу червоного барвника, рідину від живильного середовища центрифугували для відділення від біомаси. Рідину підкислювали до рН від 3,0 до 2,5 оцтовою кислотою. Осадження виконували з сульфатом калію алюмінію AIK2(SO4)2. Після осадження, барвник відділяли від рідини центрифугуванням. Приклад 2 Живильне середовище, що містить 16г/л цукру, 7г/л екстракту дріжджів, 0,002г/л сірчанокислого цинку і 0,001г/л сульфату магнію інокулювали двох-денною культурою Penicillium oxalicum вар. Armeniaca CCM 8242, що був культивований в інокуляторі, в кількості 6об.% живильного середовища. Після закінчення біосинтезу червоного барв 11 76724 ника, рідину від живильного середовища центрифугували для відділення від біомаси. Рідину підкислювали до рН від 3,0 до 2,5 лимонною кислотою. Осадження виконували сульфатом алюмінію-калію AIK2(SO4)2. Після осадження, барвник відділяли від рідини центрифугуванням і рекристалізовували. Приклад 3 Живильне середовище, що містить 20г/л цукру, 10г/л аутолізата дріжджів, 0,002г/л сірчанокислого цинку і 0,001г/л сульфату магнію інокулювали двох-денною культурою Penicillium oxalicum вар. Armeniaca CCM 8242, що був культивований в інокуляторі, у кількості 8об.% живильного середовища. Після закінчення біосинтезу червоного барвника, живильне середовище піддавали ультрафільтрації, використовуючи 10000 20000 m мембрани, наступному концентруванню за допомогою нано-фільтрації, використовуючи від 200 до 500 m мембрани до концентрату, що містить 100г/л барвнику. Приклад 4 Живильне середовище, що містить 18г/л цукру, 19г/л екстракту дріжджів, 0,002г/л сірчанокислого цинку і 0,001г/л сульфату магнію інокулювали двох-денною культурою Penicilljum oxalicum вар. Armeniaca CCM 8242, що був культивований в інокуляторі, у кількості 8об.%, живильного середовища. Після закінчення біосинтезу червоного барвника, біомасу центрифугували від живильного середовища, і рідину піддавали ультрафільтрації, Комп’ютерна верстка О. Гапоненко 12 використовуючи мембрани від 10000 до 20000 м, концентруванню за допомогою нано-фільтрації, використовуючи мембрани від 200 до 500 м до концентрату, що містить 80г/л барвника. Приклад 5 25г концентрату, отриманого відповідно до Прикладу 3 гомогенізували з 75г мальтодекстрину і висушували розпилюванням при 180-220°С. Приклад 6 65г концентрату, отриманого відповідно до Прикладу 3 гомогенізували з 35г крохмалю і висушували розпилюванням при температурі від 180 до 220°С. Продукти, отримані відповідно до Прикладів 16 можуть бути додані до харчових продуктів, таких як ковбаси, кондитерські вироби, йогурти, безалкогольні та алкогольні напої і т.п. у кількостях від 50 до 400мг/кг харчового продукту. Вони можуть надалі використовуватися для виготовлення водних, спиртових або водно-спиртових розчинів з концентраціями активної субстанції від 2 до 10об.%. Приклад 7 Кристалічний продукт, отриманий відповідно до Прикладу 2, гомогенізували з фармацевтичним екціпієнтом у формі емульсії, гомогенізували з лактозою і пресували в таблетки, що мають зміст активної субстанції 350 і 450 міліграмів. Таблетки можуть бути виготовлені також із глюкозою та з іншими фармацевтично прийнятними носіями. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюComposition having prophylactic and anti-cancer effects
Назва патенту російськоюКомпозиция для профилактики и лечения рака
Автори російськоюSARDARY, Eduard
МПК / Мітки
МПК: A61K 31/352, C09B 23/00, A23L 1/30, A61K 35/74, A23L 1/27, C07D 311/78, C09B 5/00, A61P 35/00, A61K 31/192
Мітки: композиція, раку, лікування, профілактики
Код посилання
<a href="https://ua.patents.su/6-76724-kompoziciya-dlya-profilaktiki-ta-likuvannya-raku.html" target="_blank" rel="follow" title="База патентів України">Композиція для профілактики та лікування раку</a>
Попередній патент: Дротяний радіатор
Наступний патент: Спосіб визначення і контролю режимів роботи апаратів повітряного охолодження
Випадковий патент: Баржа для перевезення навалочного, накочуваного і/чи контейнерного вантажу