Інгібітори c-fms кінази
Номер патенту: 88648
Опубліковано: 10.11.2009
Автори: Менті Карл, Ілліг Карл, Баллентайн Шеллі К., Уолл Марк, Десжарле Рене, Рудольф М., Моллой Крістофер, Чен Джіншенг, Уілсон Кен, Флорес Крістофер, Меегалла Санат
Формула / Реферат
1. Сполуки Формули І:
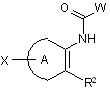 I
I
або їх сольват, гідрат, таутомер або фармацевтично прийнятна сіль, де:
А являє собою
феніл або піридил, кожен з яких може бути заміщений одним замісником, вибраним з хлору, фтору, метилу, -N3, -NH2, -NH(алкіл), -N(алкіл)2, -S(алкіл), -О(алкіл) або 4-амінофеніл;
W являє собою
піроліл, імідазоліл, ізоксазоліл, оксазоліл, 1,2,4-триазоліл або фураніл, кожен з яких може бути приєднаний через будь-який атом вуглецю, де піроліл, імідазоліл, ізоксазоліл, оксазоліл, 1,2,4-триазоліл або фураніл можуть містити один замісник, вибраний з -Сl, -CN, -NO2, -OMe або -CF3, приєднаний до будь-якого іншого вуглецю;
R2 являє собою
циклоалкіл, тіофеніл, дигідросульфонопіраніл, феніл, фураніл, тетрагідропіридил або дигідропіраніл, кожен з яких незалежно може бути заміщений одним або двома замісниками, кожен з яких вибраний з наступного: хлор, фтор та С(1-3)алкіл, за умови, що тетрагідропіридил приєднаний до кільця А - через вуглець-вуглецевий зв'язок;
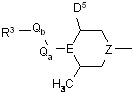
X являє собою
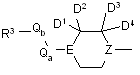 ,
, 
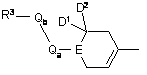 ,
, 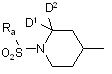 або
або 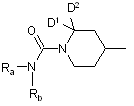 ;
;
Z являє собою
СН або N;
D1 та D2 кожний являє собою
водень або, взяті разом, утворюють подвійний зв'язок з киснем;
D3 та D4 кожний являє собою
водень або, взяті разом, утворюють подвійний зв'язок з киснем;
D5 являє собою
водень або -СН3, де зазначений -СН3 може бути відносно орієнтований син або анти;
Ra та Rb незалежно являють собою
водень, циклоалкіл, галоалкіл, арил, аралкіл, гетероарил або гетероаралкіл;
Е являє собою
N, S, О, SO або SO2, за умови, що Е не може бути N, якщо одночасно мають місце наступні три умови: Qa є відсутнім, Qb є відсутнім, та R3 являє собою аміногрупу або циклічний амінорадикал, де точкою приєднання до Е є N;
Qa є
відсутнім, -СН2-, -СН2СН2- або С(О);
Qb є
відсутнім, -NH-, -СН2-, -СН2СН2- або С(О), за умови, що Qb не може бути С(О), якщо Qa являє собою С(О), та, крім того, за умови, що Qb не може бути -NH-, якщо Е являє собою N та Qa відсутній, крім того, за умови, що Qb не може бути -NH-, якщо R3 являє собою аміногрупу або циклічний амінорадикал, де точкою приєднання до Qb є N;
R3 являє собою
водень, гідроксіалкіламіно, (гідроксіалкіл)2аміно, алкіламіно, аміноалкіл, дигідроксіалкіл, алкокси, діалкіламіно, гідроксіалкіл, -СООН, -CONH2, -CN, -SO2-алкіл-R4, -NH2, або 5- чи 6-членне кільце, яке містить, принаймні, один гетероатом N, та може необов'язково містити додатковий гетерокомпонент, вибраний з S, SO2, N та О, та 5- або 6-членне кільце може бути насиченим, частково ненасиченим або ароматичним, де ароматичний азот в 5 або 6 членному кільці може бути присутній у формі N-оксиду, та 5- або 6-членне кільце необов'язково може бути заміщене метилом, галогеном, алкіламіно або алкокси; R3 також може бути відсутнім, за умови, що R3 не відсутній, коли Е являє собою азот;
R4 являє собою
водень, -ОН, алкокси, карбокси, карбоксамідо або карбамоїл.
2. Сполука за п. 1, яка відрізняється тим, що W заміщений одним -CN.
3. Сполука за п. 1, яка відрізняється тим, що
А являє собою
піридил, який може бути заміщений одним замісником, вибраним з хлору, фтору, метилу, -N3, -NH2, -NH(алкіл), -N(алкіл)2, -S(алкіл), -О(алкіл) або 4-амінофеніл;
W являє собою
імідазоліл, (включаючи 1Н-імідазол-2-іл), який може містити один -CN; та
R2 являє собою
циклоалкіл.
4. Сполука за п. 1, яка відрізняється тим, що:
W являє собою
імідазоліл, 1,2,4-триазоліл або фураніл, кожен з яких може бути приєднаний через будь-який атом вуглецю, де імідазоліл, 1,2,4-триазоліл або фураніл може містити один -Сl або -CN, приєднаний до будь-якого іншого вуглецю;
R2 являє собою
циклоалкіл, тіофеніл, феніл, заміщений С(1-3)алкілом, дигідропіраніл та 1,1-діоксо-тетрагідротіопіраніл;
X являє собою
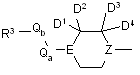 ,
, 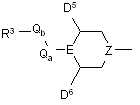 або
або  ;
;
Е являє собою
N або SO2, за умови, що Е не може бути N, якщо одночасно мають місце наступні три умови: Qa є відсутнім, Qb є відсутнім, та R3 являє собою аміногрупу або циклічний амінорадикал, де точкою приєднання до Е є N; та
R3 являє собою
водень, феніл, гідроксіалкіламіно, гідроксіалкіл(алкіл)аміно, алкіламіно, аміноалкіл, дигідроксіалкіл, алкокси, діалкіламіно, гідроксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, або 5- чи 6-членне кільце, вибране з групи, що включає: піперидиніл, морфолініл, імідазоліл та піридил, де 5- або 6-членне кільце необов'язково може бути заміщене метилом, галогеном, алкіламіно або алкокси, R3 також може бути відсутнім, за умови, що R3 не є відсутнім, коли Е являє собою азот.
5. Сполука за п. 1, яка відрізняється тим, що
А являє собою
феніл, який може бути заміщений одним замісником, вибраним з хлору, фтору або метилу;
X являє собою
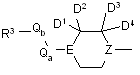 та приєднаний до фенільного кільця А в пара-положенні відносно азотного замісника, як зображено у формулі II;
та приєднаний до фенільного кільця А в пара-положенні відносно азотного замісника, як зображено у формулі II;
 ,II
,II
D3 та D4 являють собою водні;
Е являє собою
N або SO2, за умови, що Е не може бути N, якщо одночасно мають місце наступні три умови: Qa є відсутнім, Qb є відсутнім, та R3 являє собою аміногрупу або циклічний амінорадикал, де точкою приєднання до Е є N; та
R3 являє собою
водень, піперидиніл, алкіламіно, діалкіламіно, гідроксіалкіламіно, (гідроксіалкіл)2аміно, імідазоліл, 1-метилімідазоліл, піридил, піридил N-оксид, гідроксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, морфолініл; R3 також може бути відсутнім, за умови, що R3 не відсутній, коли Е являє собою азот.
6. Сполука за п. 5, яка відрізняється тим, що
А являє собою
феніл;
W являє собою
фуран-2-іл, 1Н-пірол-2-іл або 1Н-імідазол-2-іл, кожен з яких може бути заміщений при 4 або 5 вуглеці -CN;
R2 являє собою
циклоалкіл, дигідросульфонопіраніл, феніл, фураніл, тетрагідропіридил або дигідропіраніл, кожен з яких може бути незалежно заміщений одним або двома замісниками, кожен з яких вибраний з групи, що включає хлор, фтор та С(1-3)алкіл, за умови, що тетрагідропіридил повинен бути приєднаний до кільця А через вуглець-вуглецевий зв'язок.
7. Сполука за п. 6, яка відрізняється тим, що
W являє собою
3Н-2-імідазоліл-4-карбонітрил або 5-ціано-1Н-пірол-2-іл;
R2 являє собою
циклогексеніл або циклопентеніл, кожен з яких може бути заміщений хлором, фтором або однією чи двома С(1-3)алкільними групами;
Е являє собою
N, за умови, що Е не може бути N, якщо одночасно мають місце наступні три умови: Qa є відсутнім, Qb є відсутнім, та R3 являє собою аміногрупу або циклічний амінорадикал, де точкою приєднання до Е є N;
Z являє собою СН.
8. Сполука за п. 7, яка відрізняється тим, що
W являє собою
3Н-2-імідазоліл-4-карбонітрил;
Qa являє собою CO;
R3 являє собою
водень, піперидиніл, гідроксіалкіламіно, (гідроксіалкіл)2аміно, алкіламіно, діалкіламіно, імідазоліл, 1-метилімідазоліл, піридиніл, піридиніл N-оксид, гідроксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, морфолініл.
9. Сполука за п. 1, яка відрізняється тим, що вибрана з групи, яка включає
[4-(4-метил-піперазин-1-іл)-2-(3-метил-тіофен-2-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[4-(4-метил-піперазин-1-іл)-2-(2-метил-тіофен-3-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[4-(1-ацетил-піперидин-4-іл)-2-(1,2,5,6-тетрагідро-піридин-3-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1,1-діоксо-гексагідро-1λ6-тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти.
[2-циклогекс-1-еніл-4-(4-метил-піперазин-1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[2-(3,6-дигідро-2Н-піран-4-іл)-4-(4-метил-піперазин-1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[2-(1,1-діоксо-1,2,3,6-тетрагідро-1λ6-тіопіран-4-іл)-4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[4-(1-ацетил-піперидин-4-іл)-2-(1,1-діоксо-1,2,3,6-тетрагідро-1λ6-тіопіран-4-іл)-феніл]-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
[2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]-амід 5-ціано-фуран-2-карбонової кислоти,
[2'-фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]-амід 5-ціано-фуран-2-карбонової кислоти,
(4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-іл)-оцтову кислоту,
[4-(1-карбамоїлметил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-(4-метил-циклогекс-1-еніл)-4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-гідроксі-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-(4-метил-циклогекс-1-еніл)-4-(1-піридин-2-ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-гідрокси-1-гідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{4-[1-(2-ціано-етил)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл}-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-етил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1-піридин-2-ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклопент-1-еніл-4-[1-(1-метил-1Н-імідазол-2-ілметил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклопент-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1H-пірол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-пірол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-3-карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-4-карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(3-морфолін-4-іл-пропіоніл-)-гаперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(піридин-3-карбоніл)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-гідроксіетил)-амід 4-(4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-3Н-імідазол-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-{1-[2-(1-метил-1Н-імідазол-4-іл)-ацетил]-піперидин-4-іл}-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-3-іл-ацетил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-2-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1-{2-[(2-гідроксі-етил)-метил-аміно]-ацетил}-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-диметиламіно-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{4-[1-(3-аміно-3-метил-бутирил)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4Н-[1,2,4]-триазол-3-карбонової кислоти сіль біс трифтороцтової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 5-хлор-4Н-[1,2,4]-триазол-3-карбонової кислоти сіль трифтороцтової кислоти,
[2-циклогекс-1-еніл-4-(цис-2,6-диметил-піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль біс трифтороцтової кислоти,
[2-циклогекс-1-еніл-4-(транс-2,6-диметил-піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль біс трифтороцтової кислоти,
{2-циклогекс-1-еніл-4-[1-(R)-(+)-(2,3-дигідрокси-пропіоніл)-піперидин-4-іл]-феніл}-амід 5-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1-метокси-піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
[6-(4,4-диметил-циклогекс-1-еніл)-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
{4-[1-(2-аміно-2-метил-пропіоніл-)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
[6-циклогекс-1-еніл-1'-(2-метансульфоніл-етил)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-метиламіно-ацетил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[1'-(2-диметиламіно-ацетил)-6-(4,4-диметил-циклогекс-1-еніл)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти, та
[6-(4,4-диметил-циклогекс-1-еніл)-1’-(2-метансульфоніл-етил)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
10. Сполука за п. 5, яка відрізняється тим, що вибрана з групи, яка включає:
[4-(4-метил-піперазин-1-іл)-2-(3-метил-тіофен-2-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти, та
[4-(4-метил-піперазин-1-іл)-2-(2-метил-тіофен-3-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
11. Сполука за п. 6, яка відрізняється тим, що вибрана з групи, яка включає:
[4-(1-ацетил-піперидин-4-іл}-2-(1,2,5,6-тетрагідро-піридин-3-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1,1-діоксо-гексагідро-116-тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(4-метил-піперазин-1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[2-(3,6-дигідро-2Н-піран-4-іл)-4-(4-метил-піперазин-1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти,
[2-(1,1-діоксо-1,2,3,6-тетрагідро-116-тіопіран-4-іл)-4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[4-(1-ацетил-піперидин-4-іл)-2-(1,1-діоксо-1,2,3,6-тетрагідро-1λ6-тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]-амід 5-ціано-фуран-2-карбонової кислоти, та
[2'-фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]-амід 5-ціано-фуран-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
12. Сполука за п. 7, яка відрізняється тим, що вибрана з групи, яка включає:
(4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-іл)-оцтову кислоту,
[4-(1-карбамоїлметил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-(4-метил-циклогекс-1-еніл)-4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-гідроксі-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-(4-метил-циклогекс-1-еніл)-4-(1-піридин-2-ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-гідрокси-1-гідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{4-[1-(2-ціано-етил)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1-піридин-2-ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклопент-1-еніл-4-[1-(1-метил-1Н-імідазол-2-ілметил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклопент-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Н-пірол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1H-імідазол-2-карбонової кислоти, та
[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-пірол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
13. Сполука за п. 8, яка відрізняється тим, що вибрана з групи, яка включає:
{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-3-карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-4-карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(3-морфолін-4-іл-пропіоніл-)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(піридин-3-карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-гідроксі-етил)-амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-3Н-імідазол-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
(2-циклогекс-1-еніл-4-{1-[2-(1-метил-1Н-імідазол-4-іл)-ацетил]-піперидин-4-іл}-феніл)-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-3-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
{2-циклогекс-1-еніл-4-[1-(2-піридин-2-іл-ацетил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2-карбонової кислоти, та
[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
14. Сполука за п. 1, яка відрізняється тим, що являє собою:
[2-циклогекс-1-еніл-4-(1-{2-[(2-гідроксіетил)-метил-аміно]-ацетил)-піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
15. Сполука, за п. 1, яка відрізняється тим, що являє собою:
{2-циклогекс-1-еніл-4-[1-(2-диметиламіно-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1H-імідазол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
16. Сполука за п. 1, яка відрізняється тим, що являє собою:
{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
17. Сполука за п. 1, яка відрізняється тим, що вибрана з групи, яка включає:
{4-[1-(3-аміно-3-метил-бутирил)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл}-амід 4-ціано-1H-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4Н-[1,2,4]-триазол-3-карбонової кислоти сіль біс трифтороцтової кислоти,
(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 5-хлор-4Н-[1,2,4]-триазол-3-карбонової кислоти сіль трифтороцтової кислоти,
[2-циклогекс-1-еніл-4-(цис-2,6-диметил-гаперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль біс трифтороцтової кислоти,
[2-циклогекс-1-еніл-4-(транс-2,6-диметил-піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль біс трифтороцтової кислоти,
{2-циклогекс-1-еніл-4-[1-(R)-(+)-(2,3-дигідрокси-пропіоніл-)-піперидин-4-іл]-феніл}-амід 5-ціано-1H-імідазол-2-карбонової кислоти,
[2-циклогекс-1-еніл-4-(1-метокси-піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
[6-(4,4-диметил-циклогекс-1-еніл)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
{4-[1-(2-аміно-2-метил-пропіоніл-)-піперидин-4-іл]-2-циклогекс-1-еніл-феніл}-амід 5-ціано-1H-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти, та
[6-циклогекс-1-еніл-1'-(2-метансульфоніл-етил)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
18. Сполука за п. 1, яка відрізняється тим, що вибрана з групи, яка включає:
{2-циклогекс-1-еніл-4-[1-(2-метиламіно-ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової кислоти,
[1'-(2-диметиламіно-ацетил)-6-(4,4-диметил-циклогекс-1-еніл)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти, та
[6-(4,4-диметил-циклогекс-1-єніл)-1’-(2-метансульфоніл-етил)-1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти,
та їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі.
19. Фармацевтична композиція, яка містить сполуку за п. 1 та фармацевтично прийнятний носій.
20. Фармацевтична дозована форма, що містить фармацевтично прийнятний носій та від приблизно 0,5 мг до приблизно 10 г, принаймні, однієї сполуки за п. 1.
21. Дозована форма за п. 20, яка відрізняється тим, що пристосована для парентерального або перорального введення.
22. Спосіб інгібування активності протеїнтирозинкінази, в якому піддають контактуванню кінази з ефективною інгібуючою кількістю принаймні однієї сполуки за п. 1.
23. Спосіб за п. 22, яка відрізняється тим, що протеїнтирозинкіназою є с-fms.
24. Спосіб лікування запалення у ссавця, який включає введення ссавцю терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
25. Спосіб лікування раку у ссавця, який включає введення ссавцю терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
26. Спосіб лікування серцево-судинного захворювання у ссавця, який включає введення ссавцю терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
27. Спосіб лікування хвороб із запальним компонентом, включаючи гломерулонефрит, запальне захворювання кишки, пошкодження протезу, саркоїдоз, застійну обструктивну легеневу хворобу, астму, панкреатит, ВІЛ-інфекцію, псоріаз, діабет, ангіогенез, пов'язаний з пухлиною, макулярну дегенерацію, пов'язану з віком, діабетичну ретинопатію, рестеноз, шизофренію або хворобу Альцгеймера, у ссавця, який включає введення ссавцю терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
28. Спосіб лікування болю, включаючи скелетний біль, викликаний метастазом пухлин або остеоартритом, або вісцеральний, запальний та нейрогенний біль, у ссавця, який включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості, принаймні, однієї сполуки за п. 1.
29. Спосіб лікування остеопорозу, хвороби Пагета та інших хвороб, в яких ресорбція кістки опосередковує захворюваність, включаючи артрит, пошкодження протезу, остеолітичну саркому, мієлому та метастаз пухлини в кістки, який включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості, принаймні, однієї сполуки за п. 1.
30. Спосіб лікування та попередження метастазу, що є результатом раку яєчників, раку маткових труб, раку молочної залози, раку товстої кишки, раку шлунка, лейкозу ворсистих клітин та недрібноклітинної карциноми легені, який включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
31. Спосіб лікування аутоімунних хвороб, таких як системний червоний вовчак, ревматоїдний артрит, синдром Шегрена, розсіяний склероз або увеїт, який включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості принаймні однієї сполуки за п. 1.
Текст
1. Сполуки Формули І: O W 2 (19) 1 3 88648 4 імідазоліл, (включаючи 1Н-імідазол-2-іл), який моD1 же містити один -CN; та O R2 являє собою N циклоалкіл. Ra N 4. Сполука за п. 1, яка відрізняється тим, що: W являє собою Rb імідазоліл, 1,2,4-триазоліл або фураніл, кожен з ; яких може бути приєднаний через будь-який атом Z являє собою вуглецю, де імідазоліл, 1,2,4-триазоліл або фураСН або N; ніл може містити один -Сl або -CN, приєднаний до D1 та D2 кожний являє собою будь-якого іншого вуглецю; водень або, взяті разом, утворюють подвійний R2 являє собою зв'язок з киснем; 3 4 циклоалкіл, тіофеніл, феніл, заміщений С(1D та D кожний являє собою дигідропіраніл та 1,1-діоксо3)алкілом, водень або, взяті разом, утворюють подвійний тетрагідротіопіраніл; зв'язок з киснем; X являє собою D5 являє собою D5 водень або -СН3, де зазначений -СН3 може бути відносно орієнтований син або анти; R3 Qb Ra та Rb незалежно являють собою D3 D2 водень, циклоалкіл, галоалкіл, арил, аралкіл, гете1 Z Qa E D4 Qb D R3 роарил або гетероаралкіл; Е являє собою Z Qa E N, S, О, SO або SO2, за умови, що Е не може бути D6 , N, якщо одночасно мають місце наступні три умоабо ви: Qa є відсутнім, Qb є відсутнім, та R3 являє соD2 бою аміногрупу або циклічний амінорадикал, де D1 точкою приєднання до Е є N; O Qa є N відсутнім, -СН2-, -СН2СН2- або С(О); Ra N Qb є відсутнім, -NH-, -СН2-, -СН2СН2- або С(О), за умоRb ; ви, що Qb не може бути С(О), якщо Qa являє соЕ являє собою бою С(О), та, крім того, за умови, що Qb не може N або SO2, за умови, що Е не може бути N, якщо бути -NH-, якщо Е являє собою N та Qa відсутній, одночасно мають місце наступні три умови: Qa є крім того, за умови, що Qb не може бути -NH-, яквідсутнім, Qb є відсутнім, та R3 являє собою амінощо R3 являє собою аміногрупу або циклічний амігрупу або циклічний амінорадикал, де точкою принорадикал, де точкою приєднання до Qb є N; єднання до Е є N; та R3 являє собою R3 являє собою водень, гідроксіалкіламіно, (гідроксіалкіл)2аміно, водень, феніл, гідроксіалкіламіно, гідроксіалалкіламіно, аміноалкіл, дигідроксіалкіл, алкокси, кіл(алкіл)аміно, алкіламіно, аміноалкіл, дигідроксідіалкіламіно, гідроксіалкіл, -СООН, -CONH2, -CN, алкіл, алкокси, діалкіламіно, гідроксіалкіл, -СООН, SO2-алкіл-R4, -NH2, або 5- чи 6-членне кільце, яке -CONH2, -CN, -SO2CH3, -NH2, або 5- чи 6-членне містить, принаймні, один гетероатом N, та може кільце, вибране з групи, що включає: піперидиніл, необов'язково містити додатковий гетерокомпоморфолініл, імідазоліл та піридил, де 5- або 6нент, вибраний з S, SO2, N та О, та 5- або 6членне кільце необов'язково може бути заміщене членне кільце може бути насиченим, частково неметилом, галогеном, алкіламіно або алкокси, R3 насиченим або ароматичним, де ароматичний азот також може бути відсутнім, за умови, що R3 не є в 5 або 6 членному кільці може бути присутній у відсутнім, коли Е являє собою азот. формі N-оксиду, та 5- або 6-членне кільце необо5. Сполука за п. 1, яка відрізняється тим, що в'язково може бути заміщене метилом, галогеном, А являє собою алкіламіно або алкокси; R3 також може бути відсуфеніл, який може бути заміщений одним заміснитнім, за умови, що R3 не відсутній, коли Е являє ком, вибраним з хлору, фтору або метилу; собою азот; X являє собою R4 являє собою водень, -ОН, алкокси, карбокси, карбоксамідо або D3 D2 карбамоїл. D1 D4 Qb R3 2. Сполука за п. 1, яка відрізняється тим, що W заміщений одним -CN. Z Qa E 3. Сполука за п. 1, яка відрізняється тим, що А являє собою та приєднаний до фенільного кільця А в парапіридил, який може бути заміщений одним замісположенні відносно азотного замісника, як зобраником, вибраним з хлору, фтору, метилу, -N3, жено у формулі II; NH2, -NH(алкіл), -N(алкіл)2, -S(алкіл), -О(алкіл) або 4-амінофеніл; W являє собою D2 5 88648 6 [4-(4-метил-піперазин-1-іл)-2-(2-метил-тіофен-3O W іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти, NH [4-(1-ацетил-піперидин-4-іл)-2-(1,2,5,6-тетрагідропіридин-3-іл)-феніл]-амід 4-ціано-1Н-імідазол-2карбонової кислоти, X R2 ,II [2-циклогекс-1-еніл-4-(1,1-діоксо-гексагідро-1λ6D3 та D4 являють собою водні; тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2Е являє собою карбонової кислоти. N або SO2, за умови, що Е не може бути N, якщо [2-циклогекс-1-еніл-4-(4-метил-піперазин-1-іл)одночасно мають місце наступні три умови: Qa є феніл]-амід 5-ціано-фуран-2-карбонової кислоти, 3 відсутнім, Qb є відсутнім, та R являє собою аміно[2-(3,6-дигідро-2Н-піран-4-іл)-4-(4-метил-піперазингрупу або циклічний амінорадикал, де точкою при1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кисєднання до Е є N; та лоти, R3 являє собою [2-(1,1-діоксо-1,2,3,6-тетрагідро-1λ6-тіопіран-4-іл)водень, піперидиніл, алкіламіно, діалкіламіно, гід4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазолроксіалкіламіно, (гідроксіалкіл)2аміно, імідазоліл, 12-карбонової кислоти, метилімідазоліл, піридил,піридил N-оксид, гідро[4-(1-ацетил-піперидин-4-іл)-2-(1,1-діоксо-1,2,3,6ксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, тетрагідро-1λ6-тіопіран-4-іл)-феніл]-амід 4-ціаноморфолініл; R3 також може бути відсутнім, за умо1H-імідазол-2-карбонової кислоти, ви, що R3 не відсутній, коли Е являє собою азот. [2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]6. Сполука за п. 5, яка відрізняється тим, що амід 5-ціано-фуран-2-карбонової кислоти, А являє собою [2'-фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]феніл; амід 5-ціано-фуран-2-карбонової кислоти, W являє собою (4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3фуран-2-іл, 1Н-пірол-2-іл або 1Н-імідазол-2-іл, циклогекс-1-еніл-феніл}-піперидин-1-іл)-оцтову кожен з яких може бути заміщений при 4 або 5 кислоту, вуглеці -CN; [4-(1-карбамоїлметил-піперидин-4-іл)-2-циклогекс2 R являє собою 1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2циклоалкіл, дигідросульфонопіраніл, феніл, фуракарбонової кислоти, ніл, тетрагідропіридил або дигідропіраніл, кожен з [2-(4-метил-циклогекс-1-еніл)-4-піперидин-4-іляких може бути незалежно заміщений одним або феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кисдвома замісниками, кожен з яких вибраний з групи, лоти, що включає хлор, фтор та С(1-3)алкіл, за умови, що {2-циклогекс-1-еніл-4-[1-(2-гідроксі-етил)тетрагідропіридил повинен бути приєднаний до піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2кільця А через вуглець-вуглецевий зв'язок. карбонової кислоти, 7. Сполука за п. 6, яка відрізняється тим, що [2-(4-метил-циклогекс-1-еніл)-4-(1-піридин-2W являє собою ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Н3Н-2-імідазоліл-4-карбонітрил або 5-ціано-1Німідазол-2-карбонової кислоти, пірол-2-іл; {2-циклогекс-1-еніл-4-[1-(2-гідрокси-1R2 являє собою гідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4циклогексеніл або циклопентеніл, кожен з яких ціано-1Н-імідазол-2-карбонової кислоти, може бути заміщений хлором, фтором або однією {4-[1-(2-ціано-етил)-піперидин-4-іл]-2-циклогекс-1чи двома С(1-3)алкільними групами; еніл-феніл}-амід 4-ціано-1H-імідазол-2-карбонової Е являє собою кислоти, N, за умови, що Е не може бути N, якщо одночасно {2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-етил)мають місце наступні три умови: Qa є відсутнім, Qb піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-23 є відсутнім, та R являє собою аміногрупу або циккарбонової кислоти, лічний амінорадикал, де точкою приєднання до Е є (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4N; ціано-1Н-імідазол-2-карбонової кислоти, Z являє собою СН. {2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-етил)8. Сполука за п. 7, яка відрізняється тим, що піперидин-4-іл]-феніл}-амід 4-ціано-1H-імідазол-2W являє собою карбонової кислоти, 3Н-2-імідазоліл-4-карбонітрил; [2-циклогекс-1-еніл-4-(1-піридин-2-ілметилQa являє собою CO; піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2R3 являє собою карбонової кислоти, водень, піперидиніл, гідроксіалкіламіно, (гідроксіа{2-циклопент-1-еніл-4-[1-(1-метил-1Н-імідазол-2лкіл)2аміно, алкіламіно, діалкіламіно, імідазоліл, 1ілметил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нметилімідазоліл, піридиніл, піридиніл N-оксид, гідімідазол-2-карбонової кислоти, роксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, (2-циклопент-1-еніл-4-піперидин-4-іл-феніл)-амід морфолініл. 4-ціано-1Н-імідазол-2-карбонової кислоти, 9. Сполука за п. 1, яка відрізняється тим, що виб(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4рана з групи, яка включає ціано-1H-пірол-2-карбонової кислоти, [4-(4-метил-піперазин-1-іл)-2-(3-метил-тіофен-2[2-циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Ніл)-феніл]-амід 5-ціано-фуран-2-карбонової кисло[1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1Нти, імідазол-2-карбонової кислоти, 7 88648 8 [4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-енілкарбонової кислоти сіль біс трифтороцтової кислофеніл]-амід 4-ціано-1Н-пірол-2-карбонової кислоти, ти, {2-циклогекс-1-еніл-4-[1-(R)-(+)-(2,3-дигідрокси{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-3пропіоніл)-піперидин-4-іл]-феніл}-амід 5-ціано-1Нкарбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Німідазол-2-карбонової кислоти, імідазол-2-карбонової кислоти, [2-циклогекс-1-еніл-4-(1-метокси-піперидин-4-іл){2-циклогекс-1-еніл-4-[1-(1-окси-піридин-4феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кискарбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нлоти сіль трифтороцтової кислоти, імідазол-2-карбонової кислоти, [6-(4,4-диметил-циклогекс-1-еніл)-1',2',3',4',5',6'{2-циклогекс-1-еніл-4-[1-(3-морфолін-4-ілгексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Нпропіоніл-)-гаперидин-4-іл]-феніл}-амід 4-ціано-1Німідазол-2-карбонової кислоти сіль трифтороцтоімідазол-2-карбонової кислоти, вої кислоти, амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]{4-[1-(2-аміно-2-метил-пропіоніл-)-піперидин-4-іл]3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової 2-циклогекс-1-еніл-феніл]-амід 5-ціано-1Нкислоти, імідазол-2-карбонової кислоти сіль трифтороцто{2-циклогекс-1-еніл-4-[1-(піридин-3-карбоніл)вої кислоти, піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2[6-циклогекс-1-еніл-1'-(2-метансульфоніл-етил)карбонової кислоти, 1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід (2-гідроксіетил)-амід 4-(4-[(4-ціано-1Н-імідазол-25-ціано-1Н-імідазол-2-карбонової кислоти, карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}{2-циклогекс-1-еніл-4-[1-(2-метиламіно-ацетил)піперидин-1-карбонової кислоти, піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2{2-циклогекс-1-еніл-4-[1-(2-3Н-імідазол-4-ілкарбонової кислоти, ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1H[1'-(2-диметиламіно-ацетил)-6-(4,4-диметилімідазол-2-карбонової кислоти, циклогекс-1-еніл)-1’,2',3',4',5',6'-гексагідро{2-циклогекс-1-еніл-4-[1-(2-піридин-4-іл-ацетил)[2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2карбонової кислоти сіль трифтороцтової кислоти, карбонової кислоти, та (2-циклогекс-1-еніл-4-{1-[2-(1-метил-1Н-імідазол-4[6-(4,4-диметил-циклогекс-1-еніл)-1’-(2іл)-ацетил]-піперидин-4-іл}-феніл)-амід 4-ціано-1Нметансульфоніл-етил)-1’,2',3',4',5',6'-гексагідроімідазол-2-карбонової кислоти, [2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2{2-циклогекс-1-еніл-4-[1-(2-піридин-3-іл-ацетил)карбонової кислоти сіль трифтороцтової кислоти, піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2та їх сольвати, гідрати, таутомери та фармацевтикарбонової кислоти, чно прийнятні солі. {2-циклогекс-1-еніл-4-[1-(2-метансульфоніл10. Сполука за п. 5, яка відрізняється тим, що ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нвибрана з групи, яка включає: імідазол-2-карбонової кислоти, [4-(4-метил-піперазин-1-іл)-2-(3-метил-тіофен-2{2-циклогекс-1-еніл-4-[1-(2-піридин-2-іл-ацетил)іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислопіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2ти, та карбонової кислоти, [4-(4-метил-піперазин-1-іл)-2-(2-метил-тіофен-3[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніліл)-феніл]-амід 5-ціано-фуран-2-карбонової кислофеніл]-амід 4-ціано-1Н-імідазол-2-карбонової кисти лоти, та їх сольвати, гідрати, таутомери та фармацевти[2-циклогекс-1-еніл-4-(1-{2-[(2-гідроксі-етил)-метилчно прийнятні солі. аміно]-ацетил}-піперидин-4-іл)-феніл]-амід 4-ціано11. Сполука за п. 6, яка відрізняється тим, що 1Н-імідазол-2-карбонової кислоти, вибрана з групи, яка включає: {2-циклогекс-1-еніл-4-[1-(2-диметиламіно-ацетил)[4-(1-ацетил-піперидин-4-іл}-2-(1,2,5,6-тетрагідропіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2піридин-3-іл)-феніл]-амід 4-ціано-1Н-імідазол-2карбонової кислоти, карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-ацетил)[2-циклогекс-1-еніл-4-(1,1-діоксо-гексагідро-116піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2карбонової кислоти, карбонової кислоти, {4-[1-(3-аміно-3-метил-бутирил)-піперидин-4-іл]-2[2-циклогекс-1-еніл-4-(4-метил-піперазин-1-іл)циклогекс-1-еніл-феніл}-амід 4-ціано-1Н-імідазолфеніл]-амід 5-ціано-фуран-2-карбонової кислоти, 2-карбонової кислоти сіль трифтороцтової кисло[2-(3,6-дигідро-2Н-піран-4-іл)-4-(4-метил-піперазинти, 1-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кис(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід лоти, 4Н-[1,2,4]-триазол-3-карбонової кислоти сіль біс [2-(1,1-діоксо-1,2,3,6-тетрагідро-116-тіопіран-4-іл)трифтороцтової кислоти, 4-піперидин-4-іл-феніл]-амід 4-ціано-1Н-імідазол(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 52-карбонової кислоти, хлор-4Н-[1,2,4]-триазол-3-карбонової кислоти сіль [4-(1-ацетил-піперидин-4-іл)-2-(1,1-діоксо-1,2,3,6трифтороцтової кислоти, тетрагідро-1λ6-тіопіран-4-іл)-феніл]-амід 4-ціано[2-циклогекс-1-еніл-4-(цис-2,6-диметил-піперидин1Н-імідазол-2-карбонової кислоти, 4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової [2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]кислоти сіль біс трифтороцтової кислоти, амід 5-ціано-фуран-2-карбонової кислоти, та [2-циклогекс-1-еніл-4-(транс-2,6-диметил[2'-фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2-іл]піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2амід 5-ціано-фуран-2-карбонової кислоти, 9 88648 10 та їх сольвати, гідрати, таутомери та фармацевти{2-циклогекс-1-еніл-4-[1-(піридин-3-карбоніл)чно прийнятні солі. піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-212. Сполука за п. 7, яка відрізняється тим, що карбонової кислоти, вибрана з групи, яка включає: (2-гідроксі-етил)-амід 4-{4-[(4-ціано-1Н-імідазол-2(4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]-3карбоніл)-аміно]-3-циклогекс-1-еніл-феніл}циклогекс-1-еніл-феніл}-піперидин-1-іл)-оцтову піперидин-1-карбонової кислоти, кислоту, {2-циклогекс-1-еніл-4-[1-(2-3Н-імідазол-4-іл[4-(1-карбамоїлметил-піперидин-4-іл)-2-циклогексацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н1-еніл-феніл]-амід 4-ціано-1Н-імідазол-2імідазол-2-карбонової кислоти, карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-піридин-4-іл-ацетил)[2-(4-метил-циклогекс-1-еніл)-4-піперидин-4-ілпіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кискарбонової кислоти, лоти, (2-циклогекс-1-еніл-4-{1-[2-(1-метил-1Н-імідазол-4{2-циклогекс-1-еніл-4-[1-(2-гідроксі-етил)іл)-ацетил]-піперидин-4-іл}-феніл)-амід 4-ціано-1Hпіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2імідазол-2-карбонової кислоти, карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-піридин-3-іл-ацетил)[2-(4-метил-циклогекс-1-еніл)-4-(1-піридин-2піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Нкарбонової кислоти, імідазол-2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-метансульфоніл{2-циклогекс-1-еніл-4-[1-(2-гідрокси-1ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нгідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4імідазол-2-карбонової кислоти, ціано-1Н-імідазол-2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-піридин-2-іл-ацетил){4-[1-(2-ціано-етил)-піперидин-4-іл]-2-циклогекс-1піперидин-4-іл]-феніл)-амід 4-ціано-1Н-імідазол-2еніл-феніл}-амід 4-ціано-1Н-імідазол-2-карбонової карбонової кислоти, та кислоти, [4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-еніл{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-етил)феніл]-амід 4-ціано-1Н-імідазол-2-карбонової киспіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2лоти, карбонової кислоти, та їх сольвати, гідрати, таутомери та фармацевти(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4чно прийнятні солі. ціано-1Н-імідазол-2-карбонової кислоти, 14. Сполука за п. 1, яка відрізняється тим, що {2-циклогекс-1-еніл-4-[1-(2-метансульфоніл-етил)являє собою: піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2[2-циклогекс-1-еніл-4-(1-{2-[(2-гідроксіетил)-метилкарбонової кислоти, аміно]-ацетил)-піперидин-4-іл)-феніл]-амід 4-ціано[2-циклогекс-1-еніл-4-(1-піридин-2-ілметил1Н-імідазол-2-карбонової кислоти, піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2та їх сольвати, гідрати, таутомери та фармацевтикарбонової кислоти, чно прийнятні солі. {2-циклопент-1-еніл-4-[1-(1-метил-1Н-імідазол-215. Сполука, за п. 1, яка відрізняється тим, що ілметил)-піперидин-4-іл]-феніл)-амід 4-ціано-1Нявляє собою: імідазол-2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-диметиламіно-ацетил)(2-циклопент-1-еніл-4-піперидин-4-іл-феніл)-амід піперидин-4-іл]-феніл}-амід 4-ціано-1H-імідазол-24-ціано-1Н-імідазол-2-карбонової кислоти, карбонової кислоти, (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4та їх сольвати, гідрати, таутомери та фармацевтиціано-1Н-пірол-2-карбонової кислоти, чно прийнятні солі. [2-циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Н16. Сполука за п. 1, яка відрізняється тим, що [1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1Hявляє собою: імідазол-2-карбонової кислоти, та {2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іл-ацетил)[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1-енілпіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2феніл]-амід 4-ціано-1Н-пірол-2-карбонової кислокарбонової кислоти, ти, та їх сольвати, гідрати, таутомери та фармацевтита їх сольвати, гідрати, таутомери та фармацевтично прийнятні солі. чно прийнятні солі. 17. Сполука за п. 1, яка відрізняється тим, що 13. Сполука за п. 8, яка відрізняється тим, що вибрана з групи, яка включає: вибрана з групи, яка включає: {4-[1-(3-аміно-3-метил-бутирил)-піперидин-4-іл]-2{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-3циклогекс-1-еніл-феніл}-амід 4-ціано-1H-імідазолкарбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н2-карбонової кислоти сіль трифтороцтової кислоімідазол-2-карбонової кислоти, ти, {2-циклогекс-1-еніл-4-[1-(1-окси-піридин-4(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н4Н-[1,2,4]-триазол-3-карбонової кислоти сіль біс імідазол-2-карбонової кислоти, трифтороцтової кислоти, {2-циклогекс-1-еніл-4-[1-(3-морфолін-4-іл(2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 5пропіоніл-)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нхлор-4Н-[1,2,4]-триазол-3-карбонової кислоти сіль імідазол-2-карбонової кислоти, трифтороцтової кислоти, амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно][2-циклогекс-1-еніл-4-(цис-2,6-диметил-піперидин3-циклогекс-1-еніл-феніл}-піперидин-1-карбонової 4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти, кислоти сіль біс трифтороцтової кислоти, 11 88648 12 [2-циклогекс-1-еніл-4-(транс-2,6-диметил23. Спосіб за п. 22, яка відрізняється тим, що піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2протеїнтирозинкіназою є с-fms. карбонової кислоти сіль біс трифтороцтової кисло24. Спосіб лікування запалення у ссавця, який ти, включає введення ссавцю терапевтично ефектив{2-циклогекс-1-еніл-4-[1-(R)-(+)-(2,3-дигідроксиної кількості принаймні однієї сполуки за п. 1. пропіоніл-)-піперидин-4-іл]-феніл}-амід 5-ціано-1H25. Спосіб лікування раку у ссавця, який включає імідазол-2-карбонової кислоти, введення ссавцю терапевтично ефективної кілько[2-циклогекс-1-еніл-4-(1-метокси-піперидин-4-іл)сті принаймні однієї сполуки за п. 1. феніл]-амід 5-ціано-1Н-імідазол-2-карбонової кис26. Спосіб лікування серцево-судинного захворюлоти сіль трифтороцтової кислоти, вання у ссавця, який включає введення ссавцю [6-(4,4-диметил-циклогекс-1-еніл)-1’,2',3',4',5',6'терапевтично ефективної кількості принаймні одгексагідро-[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Ннієї сполуки за п. 1. імідазол-2-карбонової кислоти сіль трифтороцто27. Спосіб лікування хвороб із запальним компової кислоти, нентом, включаючи гломерулонефрит, запальне {4-[1-(2-аміно-2-метил-пропіоніл-)-піперидин-4-іл]захворювання кишки, пошкодження протезу, сар2-циклогекс-1-еніл-феніл}-амід 5-ціано-1Hкоїдоз, застійну обструктивну легеневу хворобу, імідазол-2-карбонової кислоти сіль трифтороцтоастму, панкреатит, ВІЛ-інфекцію, псоріаз, діабет, вої кислоти, та ангіогенез, пов'язаний з пухлиною, макулярну де[6-циклогекс-1-еніл-1'-(2-метансульфоніл-етил)генерацію, пов'язану з віком, діабетичну ретинопа1’,2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід тію, рестеноз, шизофренію або хворобу Альцгей5-ціано-1Н-імідазол-2-карбонової кислоти, мера, у ссавця, який включає введення ссавцю та їх сольвати, гідрати, таутомери та фармацевтитерапевтично ефективної кількості принаймні одчно прийнятні солі. нієї сполуки за п. 1. 18. Сполука за п. 1, яка відрізняється тим, що 28. Спосіб лікування болю, включаючи скелетний вибрана з групи, яка включає: біль, викликаний метастазом пухлин або остеоар{2-циклогекс-1-еніл-4-[1-(2-метиламіно-ацетил)тритом, або вісцеральний, запальний та нейрогенпіперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-2ний біль, у ссавця, який включає введення ссавцю, карбонової кислоти, що потребує такого лікування, терапевтично ефе[1'-(2-диметиламіно-ацетил)-6-(4,4-диметилктивної кількості, принаймні, однієї сполуки за п. 1. циклогекс-1-еніл)-1’,2',3',4',5',6'-гексагідро29. Спосіб лікування остеопорозу, хвороби Пагета [2,4']біпіридиніл-5-іл]-амід 4-ціано-1H-імідазол-2та інших хвороб, в яких ресорбція кістки опосередкарбонової кислоти сіль трифтороцтової кислоти, ковує захворюваність, включаючи артрит, пошкота дження протезу, остеолітичну саркому, мієлому та [6-(4,4-диметил-циклогекс-1-еніл)-1’-(2метастаз пухлини в кістки, який включає введення метансульфоніл-етил)-1’,2',3',4',5',6'-гексагідроссавцю, що потребує такого лікування, терапевти[2,4']біпіридиніл-5-іл]-амід 4-ціано-1Н-імідазол-2чно ефективної кількості, принаймні, однієї сполукарбонової кислоти сіль трифтороцтової кислоти, ки за п. 1. та їх сольвати, гідрати, таутомери та фармацевти30. Спосіб лікування та попередження метастазу, чно прийнятні солі. що є результатом раку яєчників, раку маткових 19. Фармацевтична композиція, яка містить сполутруб, раку молочної залози, раку товстої кишки, ку за п. 1 та фармацевтично прийнятний носій. раку шлунка, лейкозу ворсистих клітин та недріб20. Фармацевтична дозована форма, що містить ноклітинної карциноми легені, який включає ввефармацевтично прийнятний носій та від приблиздення ссавцю, що потребує такого лікування, тено 0,5 мг до приблизно 10 г, принаймні, однієї спорапевтично ефективної кількості принаймні однієї луки за п. 1. сполуки за п. 1. 21. Дозована форма за п. 20, яка відрізняється 31. Спосіб лікування аутоімунних хвороб, таких як тим, що пристосована для парентерального або системний червоний вовчак, ревматоїдний артрит, перорального введення. синдром Шегрена, розсіяний склероз або увеїт, 22. Спосіб інгібування активності протеїнтирозинякий включає введення ссавцю, що потребує такокінази, в якому піддають контактуванню кінази з го лікування, терапевтично ефективної кількості ефективною інгібуючою кількістю принаймні однієї принаймні однієї сполуки за п. 1. сполуки за п. 1. Винахід відноситься до нових сполук, що діють як інгібітори протеїн тирозин кіназ. Більш особливо, винахід відноситься до нових сполук, що діють як інгібітори c-fms кінази. Протеїн кінази являють собою ензими, що є ключовими компонентами шляхів сигнальної трансдукції за допомогою каталізу переносу кінцевого фосфату з аденозин 5'-трифосфату (АТР) до гідрокси групи залишків тирозину, серину та треоніну протеїнів. Як наслідок, інгібітори протеїн кіна зи та субстрати є цінними засобами для оцінки фізіологічних наслідків активації протеїн кінази. Було продемонстровано, що надлишкова експресія або невідповідна експресія нормальних або мутантних протеїн кіназ у ссавців відіграють істотні ролі в розвитку багатьох хвороб, включаючи рак та діабет. Протеїн кінази можуть бути поділені на два класи: протеїн кінази, які переважно фосфорилюють залишки тирозину (протеїн тирозин кінази), та 13 88648 14 протеїн кінази, які переважно фосфорилюють замолекулах. Патенти US 6,383,790; 6,346,625; лишки серину та/або треоніну (протеїн се6,235,746; 6,100,254 та міжнародні заявки PCT WO рин/треонін кінази). Протеїн тирозин кінази здійс01/47897, WO 00/27820 та WO 02/068406 описують нюють інші функції: від стимулювання росту клітин недавні спроби синтезу таких інгібіторів. та диференціювання до затримки проліферації Винахід відноситься до існуючої потреби в секлітин. Вони можуть бути класифіковані або як лективних та ефективних інгібіторах протеїн тирорецепторні протеїн тирозин кінази, або як внутрішзин кіназ, забезпечуючи ефективні інгібітори c-fms ньоклітинні протеїн тирозин кінази. Рецепторні кінази. Винахід відноситься до нових сполук Форпротеїн тирозин кінази, які мають позаклітинний мули І: ліганд-зв'язуючий домен та внутрішньоклітинний каталітичний домен з внутрішньою активністю тирозин кінази, розподілені серед 20 підсімейств. Рецепторні тирозин кінази сімейства фактора росту епідермісу ("EGF"), які включають HER-1, HER-2/neu та HER-3 рецептори, містять позаклітинний зв'язуючий домен, трансмембранний доабо їх сольвату, гідрату, таутомеру або фармен та внутрішньоклітинний цитоплазматичний мацевтично прийнятної солі, де: каталітичний домен. Зв'язування рецептора приА являє собою водить до запуску різних внутрішньоклітинних феніл або піридил, кожен з яких може бути процесів фосфорилування, що залежать від тирозаміщений одним замісником, вибраним з хлору, зин кінази, які врешті приводять до транскрипції фтору, метилу, -N3, -NH2, -NН(алкіл), -N(алкіл)2, онкогенів. З цим сімейством рецепторів були поS(алкіл), -О(алкіл) або 4-амінофенілу; в'язані рак молочної залози, колоректальний рак W являє собою та рак передміхурової залози. піроліл (включаючи 1Н-пірол-2-іл), імідазоліл, Інсуліновий рецептор ("IR") та рецептор інсу(включаючи 1Н-імідазол-2-іл), ізоксазоліл, оксазолін-подібного фактору росту І ("IGF-1R") структурліл, 1,2,4 триазоліл або фураніл (включаючи фуно та функціонально зв'язані, але вони викликають ран-2-іл), кожен з яких може бути приєднаний черізні біологічні ефекти. Надлишкова експресія IGFрез будь-який атом вуглецю, де піроліл, імідазоліл, 1R була пов'язана з раком молочної залози. ізоксазоліл, оксазоліл, 1,2,4 триазоліл або фураніл Рецептори тромбоцитарного фактора росту можуть містити один замісник, вибраний з -СІ, -CN, ("PDGF") опосередковують клітинні реакції, які -NO2, -ОМе або -CF3, приєднаний до будь-якого включають проліферацію, міграцію та виживання, і іншого вуглецю; включають PDGFR, рецептор фактора стовбурних R2 являє собою клітин (c-kit) та c-fms. Ці рецептори були пов'язані циклоалкіл (включаючи циклогексеніл, циклоз хворобами, такими як атеросклероз, фіброз та пентеніл), тіофеніл, дигідросульфонопіраніл, фепроліферативна вітреоретинопатія. ніл, фураніл, тетрагідропіридил або дигідропіраніл, Рецептори фактора росту фіброластів ("FGR") кожен з яких незалежно може бути заміщений одскладаються з чотирьох рецепторів, які відповіданим або двома замісниками, кожен з яких вибрають за продукування кровоносних судин, за виріст ний з наступного: хлор, фтор та С(1-3) алкіл (вклюкінцівок та за ріст і диференціювання численних чаючи 4,4-диметил циклогексеніл, 4-метил типів клітин. циклогексеніл, 2-метил тіофеніл, 3-метил тіофеСудинний ендотеліальний фактор росту ніл), за умови, що тетрагідропіридил приєднаний ("VEGF"), ефективний мітоген ендотеліальних клідо кільця А через вуглець-вуглецевий зв'язок; тин, продукується в підвищених кількостях багатьX являє собою ма пухлинами, включаючи карциноми яєчників. Відомі рецептори для VEGF позначені як VEGFR-1 (Flt-1), VEGFR-2 (KDR), VEGFR-3 (Flt-4). Споріднена група рецепторів, tie-1 та tie-2 кінази, була ідентифікована в клітинах судинного ендотелію та кровотворних клітинах. Рецептори VEGF були пов'язані з утворенням і розвитком судин та ангіогенезом. Внутрішньоклітинні протеїн тирозин кінази також відомі як не-рецепторні протеїн тирозин кінази. Понад 24 такі кінази були ідентифіковані та або були класифіковані в 11 підсімействах. Серин/треонін протеїн кінази, подібно до клітинних протеїн тирозин кіназ, в основному є внутрішньоклітинними. Діабет, ангіогенез, псоріаз, рестеноз, офтальмологічні хвороби, шизофренія, ревматоїдний артрит, серцево-судинне захворювання та рак є приΖ являє собою кладами патогенних станів, які були пов'язані з СН або Ν; анормальною активністю протеїн тирозин кіназ. D1 та D2 кожний являє собою Таким чином, існує потреба в селективних та ефеводень або, взяті разом, утворюють подвійний ктивних інгібіторах протеїн тирозин кіназ малих зв'язок з киснем; 15 88648 16 D3 та D4 кожний являє собою водень або, взяті разом, утворюють подвійний зв'язок з киснем; D5 являє собою водень або -СН3, де зазначений -СН3 може бути відносно орієнтований син або анти; або їх сольвату, гідрату, таутомеру або фарRa та Rb, незалежно являють собою мацевтично прийнятної сілі, де: водень, циклоалкіл, галоалкіл, арил, аралкіл, А являє собою гетероарил або гетероаралкіл; феніл або піридил, кожен з яких може бути Ε являє собою заміщений одним замісником, вибраним з хлору, N, S, О, SO або SO2, за умови, що Ε не може фтору, метилу, -N3, -NH2, -NН(алкіл), -N(алкіл)2, бути Ν, якщо одночасно мають місце наступні три S(алкіл), -О(алкіл) або 4-амінофеніл; умови: Qa є відсутнім, Qb є відсутнім, та R3 являє W являє собою собою аміно групу або циклічний аміно радикал, піроліл (включаючи 1Н-пірол-2-іл), імідазоліл, де точкою приєднання до Ε є N; (включаючи 1Н-імідазол-2-іл), ізоксазоліл, оксазоQa є ліл, 1,2,4 триазоліл або фураніл (включаючи фувідсутнім, -СН2-, -СН2СН2- або С(О); ран-2-іл), кожен з яких може бути приєднаний чеQb є рез будь-який атом вуглецю, де піроліл, імідазоліл, відсутнім, -NH-, -СН2-, -СН2СН2- або С(О), за ізоксазоліл, оксазоліл, 1,2,4 триазоліл або фураніл умови, що Qb не може бути С(О), якщо Qa являє можуть містити один замісник, вибраний з -СІ, -CN, собою С(О), та, крім того, за умови, що Qb не може -NO2, -OMe або -CF3, приєднаний до будь-якого бути -NH-, якщо Ε являє собою N та Qa відсутній, іншого вуглецю; крім того, за умови, що Qb не може бути -NH-, якR2 являє собою що R являє собою аміно групу або циклічний аміно циклоалкіл (включаючи циклогексеніл, циклорадикал, де точкою приєднання до Qb є N; пентеніл), тіофеніл, дигідросульфонопіраніл, феR3 являє собою ніл, фураніл, тетрагідропіридил або дигідропіраніл, водень, феніл, гідроксіалкіламіно (включаючи кожен з яких незалежно може бути заміщений од2-гідроксі етиламіно), (гідроксіалкіл)2аміно, гідроним або двома замісниками, кожен з яких вибраксіалкіл(алкіл)аміно (включаючи 1-гідроксіет-2ний з наступного: хлор, фтор та С(1-3)алкіл (вклюил(метил)аміно), алкіламіно (включаючи метилчаючи 4,4-диметил циклогексеніл, 4-метил аміно), аміноалкіл (включаючи 2-аміно ізопропіл), циклогексеніл, 2-метил тіофеніл, 3-метил тіофедигідроксіалкіл (включаючи 1,3-дигідроксі ізопроніл), за умови, що тетрагідропіридил приєднаний піл, 1,2-дигідроксі етил), алкокси (включаючи медо кільця А через вуглець-вуглецевий зв'язок; токси), діалкіламіно (включаючи диметиламіно), X являє собою гідроксіалкіл (включаючи 1-гідроксі ет-2-ил), СООН, -CONH2, -CN, -SO2-алкіл-R4 (включаючи SO2CH3), -NH2 або 5 чи 6 членне кільце, яке містить, принаймні, один гетероатом N, та може необов'язково містити додатковий гетерокомпонент, вибраний з S, SO2. N та О, та 5 або 6 членне кільце може бути насиченим, частково ненасиченим або ароматичним (включаючи піперидиніл, морфолініл, імідазоліл та піридил), де ароматичний азот в 5 або 6 членному кільці може бути присутній у формі N-оксиду (включаючи піридил N-оксид), та або 5 або 6 членне кільце необов'язково може бути заміщене метилом, галогеном, алкіламіно або алкокси (включаючи 1-метил імідазоліл); R3 також може бути відсутнім, за умови, що R3 не відсутній, коли Ε являє собою азот; R4 являє собою водень, -ОН, алкокси, карбокси, карбоксамідо Ζ являє собою або карбамоіл. СН або Ν; Сполуки Формули І є ефективними інгібітораD1 та D2 кожний являє собою ми c-fms протеїн тирозин кінази водень або, взяті разом, утворюють подвійний Винахід також відноситься до способів інгібузв'язок з киснем; вання активності протеїн тирозин кіназ у ссавця за D3 та D4 кожний являє собою допомогою введення терапевтично ефективної водень або, взяті разом, утворюють подвійний кількості, принаймні, однієї сполуки Формули І зв'язок з киснем; Винахід відноситься до нових сполук Формули D3 являє собою І: водень або -СН3, де зазначений -СН3 може бути відносно орієнтований син або анти; Ra та Rb незалежно являють собою водень, циклоалкіл, галоалкіл, арил, аралкіл, гетероарил або гетероаралкіл; Ε являє собою 17 88648 18 N, S, О, SO або SO2, за умови, що Ε не може 3Н-2-імідазоліл-4-карбонітрил або 5-ціано-1Нбути Ν, якщо одночасно мають місце наступні три пірол-2-іл; умови: Qa є відсутнім, Qb є відсутнім, та R3 являє f) W являє собою 3Н-2-імідазоліл-4собою аміно групу або циклічний аміно радикал, карбонітрил; де точкою приєднання до Ε є N; g) R2 являє собою Qa є циклоалкіл (включаючи циклогексеніл, цикловідсутнім, -СН2-, -СН2СН2- або С(О); пентеніл), тіофеніл, дигідросульфонопіраніл, феQb є ніл, фураніл, тетрагідропіридил або дигідропіраніл, відсутнім, -NH-, -CH2-, -CH2CH2- або С(O), за кожен з яких незалежно може бути заміщений одумови, що Qb не може бути С(О), якщо Qa являє ним або двома замісниками, кожен з яких вибрасобою С(О), та, крім того, за умови, що Qb не може ний з наступного: хлор, фтор та С(1-3)алкіл (вклюбути -NH-, якщо Ε являє собою N та Qa відсутній, чаючи 4,4-диметил циклогексеніл, 4-метил крім того, за умови, що Qb не може бути -NH-, якциклогексеніл, 2-метил тіофеніл, 3-метил тіофещо R3 являє собою аміно групу або циклічний амініл), за умови, що тетрагідропіридил приєднаний но радикал, де точкою приєднання до Qb є N, до кільця А через вуглець-вуглецевий зв'язок; R3 являє собою h) R2 являє собою водень, феніл, гідроксіалкіламіно (включаючи циклоалкіл (включаючи циклогексеніл, цикло2-гідроксі етиламіно), (гідроксіалкіл)2аміно, гідропентеніл), який може бути заміщений одним або ксіалкіл(алкіл)аміно (включаючи 1-гідроксіет-2двома С(1-3)алкілами (включаючи 4,4-диметил цикил(метил)аміно), алкіламіно (включаючи метиллогексеніл. 4-метил циклогексеніл); аміно), аміноалкіл (включаючи 2-аміно ізопропіл), і) R2 являє собою дигідроксіалкіл (включаючи 1,3-дигідроксі ізопроциклогексеніл, який може бути заміщений одпіл, 1,2-дигідроксі етил), алкокси (включаючи меним або двома С(1-3)алкілами, токси), діалкіламіно (включаючи диметиламіно), j) R2 являє собою гідроксіалкіл (включаючи 1-гідроксі ет-2-ил), циклогексеніл, 4,4-диметил циклогексеніл або СООН, -CONH2, -CN, -SO2-алкіл-R4 (включаючи 4-метил циклогексеніл, SО2СН3), -NH2 або 5 чи 6 членне кільце, яке місk) R2 являє собою тить, принаймні, один гетероатом N, та може нециклогексеніл; обов'язково містити додатковий гетерокомпонент, 1) X являє собою вибраний з S, SO2, N та О, та 5 або 6 членне кільце може бути насиченим, частково ненасиченим або ароматичним (включаючи піперидиніл, морфолініл, імідазоліл та піридил), де ароматичний азот в 5 або 6 членному кільці може бути присутній у формі N-оксиду (включаючи піридил N-оксид), та 5 або 6 членне кільце необов'язково може бути заміщене метилом, галогеном, алкіламіно або алкокси (включаючи 1-метил імідазоліл); R3 також може бути відсутнім, за умови, що R3 не відсутній, або коли Ε являє собою азот; R4 являє собою водень, -ОН, алкокси, карбокси, карбоксамідо або карбамоїл. Втілення даного винаходу включають сполуку Формули І, в якій: a) А являє собою m) X являє собою феніл або піридил, кожен з яких може бути заміщений одним замісником, вибраним з хлору, фтору, метилу, -N3, -ΝΗ2, -NH(алкіл), -N(алкіл)2, S(алкіл), -О(алкіл) або 4-амінофеніл; b) А являє собою феніл; c) W являє собою піроліл (включаючи 1Н-пірол-2-іл), імідазоліл, (включаючи 1Н-імідазол-2-іл). ізоксазоліл, оксазоліл, 1,2,4 триазоліл або фураніл (включаючи фуран-2-іл), кожен з яких може бути приєднаний через будь-який атом вуглецю, де піроліл, імідазоліл, ізоксазоліл, оксазоліл, 1,2,4 триазоліл або фураніл n) Χ являє собою можуть містити один замісник, вибраний з -СІ, -CN, -NO2, -OMe або -CF3, приєднаний до будь-якого іншого вуглецю, d) W являє собою фуран-2-іл, 1Н-пірол-2-іл або 1Н-імідазол-2-іл, кожен з яких може бути заміщений при 4 або 5 вуглеці -CN; e) W являє собою о) Ζ являє собою СН або Ν; 19 88648 20 вибраний з S, SO2, N та О, та 5 або 6 членне кільρ) Ζ являє собою це може бути насиченим, частково ненасиченим СН; або ароматичним (включаючи піперидиніл, морq) D1 та D2 кожен являє собою фолініл, імідазоліл та піридил), де ароматичний водень або, взяті разом, утворюють подвійний азот в 5 або 6 членному кільці може бути присутній зв'язок з киснем; у формі N-оксиду (включаючи піридил N-оксид), та r) D1 та D2 кожен являє собою 5 або 6 членне кільце необов'язково може бути водень; заміщене метилом, галогеном, алкіламіно або алs) D3 та D4 кожен являє собою кокси (включаючи 1-метил імідазоліл); R3 також водень або, взяті разом, утворюють подвійний може бути відсутнім, за умови, що R3 не відсутній, зв'язок з киснем; 3 4 коли Ε являє собою азот; t) D та D кожен являє собою gg) R3 являє собою водень; водень, феніл, 2-гідроксі етиламіно, 1u) D3 являє собою гідроксіет-2-ил(метил)аміно, метиламіно, 2-аміно водень або -СН3, де зазначений -СН3 може буізопропіл, 1,3-дигідроксі ізопропіл, 1,2-дигідроксі ти відносно орієнтований сип або анти; етил, метокси, диметиламіно, 1-гідроксі ет-2-ил, v) Ra та Rb незалежно являють собою СООН, -CONH2, -CN, -SO2-, -SO2CH3, -NH2, піпериводень, циклоалкіл, галоалкіл, арил, аралкіл, диніл, морфолініл, імідазоліл, піридил, піридил Nгетероарил або гетероаралкіл; оксид або 1-метил імідазоліл; w) E являє собою hh) R3 являє собою N, S, О, SO або SO2, за умови, що Ε не може алкіламіно (включаючи метиламіно), діалкілабути Ν, якщо одночасно мають місце наступні три міно (включаючи диметиламіно), або -SO2-алкіл-R4 умови: Qa є відсутнім, Qb є відсутнім, та R3 являє (включаючи -SO2CH3); собою аміно групу або циклічний аміно радикал, іі) R3 являє собою де точкою приєднання до Ε є N; метиламіно, диметиламіно або -SО2СН3; x) Ε являє собою jj) R3 являє собою Ν, за умови, що Ε не може бути Ν, якщо однодиметиламіно; часно мають місце наступні три умови: Qa є відсуkk) R4 являє собою тнім, Qb є відсутнім, та R3 являє собою аміно групу водень, -ОН, алкокси, карбокси, карбоксамідо або циклічний аміно радикал, де точкою приєдабо карбамоїл; та нання до Ε є N; 11) R4 являє собою У) Qa є водень; відсутнім, -СН2-, -СН2СН2- або С(О); та всі комбінації від а) до ll), включно, зазначеz) Qa є ні в даній заявці вище. відсутнім, -СН2СН2- або С(О); Переважними сполуками Формули І є сполуки, аа) Qa є в яких відсутнім або С(О); W заміщений одним -CN. bb) Qa є Іншими переважними сполуками Формули І є С(О); сполуки, в яких: сс) Qb є А являє собою відсутнім, -NH-, -СН2-, -СН2СН2- або С(О), за піридил, який може бути заміщений одним заумови, що Qb не може бути С(О), якщо Qa являє місником, вибраним з хлору, фтору, метилу, -N3, собою С(О), та, крім того, за умови, що Qb не може NH2, -NН(алкіл), -N(алкіл)2, -S(алкіл), -О(алкіл) або бути -NH-, якщо Ε являє собою N та Qa відсутній, 4-амінофеніл, крім того, за умови, що Qb не може бути -NH-, якW являє собою що R3 являє собою аміно групу або циклічний аміімідазоліл, (включаючи 1Н-імідазол-2-іл), який но радикал, де точкою приєднання до Qb є N; може містити один -CN; та dd) Qb є R2 являє собою відсутнім, -СН2СН2- або С(О), за умови, що Qb не може бути С(О), якщо Qa являє собою С(О); циклоалкіл. ее) Qb є Ще іншими переважними сполуками Формули І відсутнім або С(О), за умови, що Qb не може є сполуки, в яких: бути С(О), якщо Qa являє собою С(О); А являє собою ff) R являє собою феніл, який може бути заміщений одним заміводень, феніл, гідроксіалкіламіно (включаючи сником, вибраним з хлору, фтору або метилу; 2-гідроксі етиламіно), (гідроксіалкіл)2аміно, гідроX являє собою ксіалкіл(алкіл)аміно (включаючи 1-гідроксіет-2ил(метил)аміно), алкіламіно (включаючи метиламіно), аміноалкіл (включаючи 2-аміно ізопропіл), та приєднаний до фенільнодигідроксіалкіл (включаючи 1,3-дигідроксі ізопрого кільця А в пара-положенні відносно азотного піл, 1,2-дигідроксі етил), алкокси (включаючи мезаміснику, як зображено у формулі II; токси), діалкіламіно (включаючи диметиламіно), гідроксіалкіл (включаючи 1-гідроксі ет-2-ил), СООН, -CONH2, -CN, -SО2-алкіл-R4 (включаючи SО2СН3), -NH2 або 5 чи 6 членне кільце, яке містить, принаймні, один гетероатом N, та може необов'язково містити додатковий гетерокомпонент, 21 88648 22 ний С(1-3)алкілом, крім того, включаючи 4-метил циклогексеніл), циклоалкіл, заміщений С(13)діалкілом (включаючи 4,4-диметил циклогексеніл), тіофеніл (включаючи тіофеніл, заміщений С(13)алкілом, крім того, включаючи 2-метил тіофеніл та 3-метил тіофеніл), феніл, заміщений С(1D3 та D4 являють собою водні; 3)алкілом (включаючи метил феніл), дигідропіраніл та 1,1-діоксо-тетрагідротіопіраніл; Ε являє собою X являє собою N або SO2, за умови, що Ε не може бути Ν, якщо одночасно мають місце наступні три умови: Qa є відсутнім, Qb є відсутнім, та R3 являє собою аміно групу або циклічний аміно радикал, де точкою приєднання до Ε є N; та R3 являє собою водень, піперидиніл, алкіламіно, діалкіламіно, або гідроксіалкіламіно, (гідроксіалкіл)2аміно, імідазоліл, 1-метил імідазоліл, піридил, піридил N-оксид, гідроксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, морфолініл; R3 також може бути відсутнім, за умови, що R3 не відсутній, коли Ε являє собою азот. Більш переважними сполуками Формули І є сполуки, в яких: Ε являє собою А являє собою N або SO2, за умови, що Ε не може бути Ν, феніл; якщо одночасно мають місце наступні три умови: W являє собою Qa є відсутнім, Qb є відсутнім, та R3 являє собою фуран-2-іл, 1Н-пірол-2-іл або 1Н-імідазол-2-іл, аміно групу або циклічний аміно радикал, де точкожен з яких може бути заміщений при 4 або 5 кою приєднання до Ε є N; та вуглеці -CN; R3 являє собою R2 являє собою водень, феніл, гідроксіалкіламіно (включаючи циклоалкіл, дигідросульфонопіраніл, феніл, 2-гідроксі етиламіно), гідроксіалкіл(алкіл)аміно фураніл, тетрагідропіридил або дигідропіраніл, (включаючи 1-гідроксіет-2-ил(метил)аміно), алкікожен з яких може бути незалежно заміщений одламіно (включаючи метиламіно), аміноалкіл ним або двома замісниками, кожен з яких вибра(включаючи 2-аміно ізопропіл), дигідроксіалкіл ний з групи, що включає хлор, фтор та С(1-3)алкіл, (включаючи 1,3-дигідроксі ізопропіл, 1,2-дигідроксі за умови, що тетрагідропіридил повинен бути приетил), алкокси (включаючи метокси), діалкіламіно єднаний до кільця А через вуглець-вуглецевий (включаючи диметиламіно), гідроксіалкіл (включазв'язок. ючи 1-гідроксі ет-2-ил), -СООН, -CONH2, -CN, Навіть більш переважними сполуками ФормуSO2CH3, -ΝΗ2, або 5 чи 6 членне кільце, вибране з ли І є сполуки, в яких: групи, що включає: піперидиніл, морфолініл, імідаW являє собою золіл та піридил, де 5 або 6 членне кільце необо3Н-2-імідазоліл-4-карбонітрил або 5-ціано-1Нв'язково може бути заміщене метилом, галогеном, пірол-2-іл; алкіламіно або алкокси (включаючи 1-метил іміда2 R являє собою золіл), R3 також може бути відсутнім, за умови, що циклогексеніл або циклопентеніл, кожен з яких R3 не відсутній, коли Ε являє собою азот. може бути заміщений хлором, фтором або однією Найбільш переважними сполуками Формули І чи двома С(1-3)алкільними групами; є сполуки, в яких: Ε являє собою W являє собою Ν, за умови, що Ε не може бути Ν, якщо одно3Н-2-імідазоліл-4-карбонітрил; часно мають місце наступні три умови: Qa є відсуQa являє собою CO; тнім, Qb є відсутнім, та R3 являє собою аміно групу R3 являє собою або циклічний аміно радикал, де точкою приєдводень, піперидиніл, гідроксіалкіламіно (гідронання до Ε є N; ксіалкіл)2аміно, алкіламіно, діалкіламіно, імідазоΖ являє собою СН. ліл, 1-метил імідазоліл, піридил, піридил N-оксид, Особливо переважними сполуками Формули І гідроксіалкіл, -СООН, -CONH2, -CN, -SO2CH3, -NH2, є сполуки, в яких: морфолініл. W являє собою Сполуки Формули І є особливо ефективними імідазоліл, (включаючи 1Н-імідазол-2-іл), 1,2,4 інгібіторами c-fms протеїн тирозин кінази. триазоліл або фураніл (включаючи фуран-2-іл), Винахід також відноситься до способів інгібукожен з яких може бути приєднаний через будьвання активності протеїн тирозин кіназ у ссавця за який атом вуглецю, де імідазоліл, 1,2,4 триазоліл допомогою введення терапевтично ефективної або фураніл можуть містити один -СІ або -CN, кількості, принаймні, однієї сполуки Формули І. приєднаний до будь-якого іншого вуглецю; Прикладами сполук Формули І є: 2 R являє собою [4-(4-метил-піперазин-1-іл)-2-(3-метил-тіофенциклоалкіл (включаючи циклоалкіл, заміщений 2-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кисС(1-3)алкілом, крім того, включаючи циклопентеніл, лоти або заміщений С(1-3)алкілом, та циклогексеніл, заміще 23 88648 24 [4-(4-метил-піперазин-1-іл)-2-(2-метил-тіофен{2-циклопент-1-еніл-4-[1-(1-метил-1Н-імідазол3-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кис2-ілметил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нлоти, імідазол-2-карбонової кислоти, та їх сольвати, гідрати, таутомери та фарма(2-циклопент-1-еніл-4-піперидин-4-іл-феніл)цевтично прийнятні солі амід 4-ціано-1Н-імідазол-2-карбонової кислоти, Більш переважними прикладами сполук Фор(2-циклогекс-1-єні л-4-піперидин-4-іл-феніл)мули І є: амід 4-ціано-1Н-пірол-2-карбонової кислоти, [4-(1-ацетил-піперидин-4-іл)-2-(1,2,5,6[2-циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Нтетрагідро-тридин-3-іл)-феніл]-амід 4-ціано-1Н[1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1Німідазол-2-карбонової кислоти, імідазол-2-карбонової кислоти або [2-циклогекс-1-еніл-4-(1,1-діоксо-гексагідро[4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1еніл-феніл]-амід 4-ціано-1Н-пірол-2-карбонової 1lб-тіопіран-4-іл)-феніл]-амід 4-ціано-1Н-імідазолкислоти, 2-карбонової кислоти, та їх сольвати, гідрати, таутомери та фарма[2-циклогекс-1-еніл-4-(4-метил-піперазин-1-іл)цевтично прийнятні солі. феніл]-амід 5-ціано-фуран-2-карбонової кислоти, Найбільш переважними прикладами сполук [2-(3,6-дигідро-2Н-піран-4-іл)-4-(4-метилФормули І є. піперазин-1-іл)-феніл]-амід 5-ціано-фуран-2{2-циклогекс-1-еніл-4-[1-(1-окси-гаридин-3карбонової кислоти, карбоніл)-піпериди-4-іл]-феніл}-амід 4-ціано-1Н[2-(1,1-діоксо-1,2,3,6-тетрагідро-1l6-тіопіран-4імідазол-2-карбонової кислоти, іл)-4-піперидин-4-іл-феніл]-амід 4-ціано-1Н{2-циклогекс-1-еніл-4-[1-(1-окси-піридин-4імідазол-2-карбоновоі кислоти, карбоніл)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н[4-(1-ацетил-піперидин-4-іл)-2-(1,1-діоксоімідазол-2-карбонової кислоти, 1,2,3,6-тетрагідро-1l6-тіопіран-4-іл)-феніл]-амід 4{2-циклогекс-1-еніл-4-[1-(3-морфолін-4-ілціано-1Н-імідазол-2-карбонової кислоти, пропіоніл-)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н[2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2імідазол-2-карбонової кислоти, іл]-амід 5-ціано-фуран-2-карбонової кислоти або амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)[2'-фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1іл]-амід 5-ціано-фуран-2-карбоновоі кислоти, карбонової кислоти, та їх сольвати, гідрати, таутомери та фарма{2-циклогекс-1-еніл-4-[1-(піридин-3-карбоніл)цевтично прийнятні-солі. піперидин-4-іл]-феніл}-амід4-ціано-1Н-імідазол-2Навіть більш переважними прикладами сполук карбонової кислоти, Формули І є(2-гідроксі-етил)-амід 4-{4-[(4-ціано-1Н(4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)-аміно]імідазол-2-карбоніл)-аміно]-3-циклогекс-1-еніл3-циклогекс-1-eніл-феніл}-піперидин-1-іл)-оцтова феніл}-піперидин-1-карбонової кислоти, кислота, {2-циклогекс-1-еніл-4-[1-(2-3Н-імідазол-4-іл[4-(1-карбамоїлметил-піперидин-4-іл)-2ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нциклогекс-1-еніл-феніл]-амід 4-ціано-1Н-імідазолімідазол-2-карбонової кислоти, 2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-тридин-4-іл[2-(4-метил-циклогекс-1-еніл)-4-піперидин-4-ілацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нфеніл]-амід 4-ціано-1Н-імідазол-2-карбонової кисімідазол-2-карбонової кислоти, лоти, (2-циклогекс-1-еніл-4-{1-[2-(1-метил-1Н{2-циклогекс-1-еніл-4-[1-(2-гідроксі-етил)імідазол-4-іл)-ацетил]-піперидин-4-іл}-феніл)-амід піперидин-4-іл]-феніл}-амід 4-ціано-1Н-імідазол-24-ціано-1Н-імідазол-2-карбонової кислоти, карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-піридин-3-іл[2-(4-метил-циклогекс-1-еніл)-4-(1-піридин-2ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Німідазол-2-карбонової кислоти, імідазол-2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-метансульфоніл{2-циклогекс-1-еніл-4-[1-(2-гідрокси-1ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нгідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4імідазол-2-карбонової кислоти, ціано-1Н-імідазол-2-карбонової кислоти, {2-циклогекс-1-еніл-4-[1-(2-піридин-2-іл{4-[1-(2-ціано-етил)-піперидин-4-іл]-2ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нциклогекс-1-еніл-феніл}-амід 4-ціано-1Н-імідазолімідазол-2-карбонової кислоти або 2-карбонової кислоти, [4-(1-ацетил-піперидин-4-іл)-2-циклогекс-1{2-циклогекс-1-еніл-4-[1-(2-морфолін-4-іленіл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нкислоти, імідазол-2-карбонової кислоти, та їх сольвати, гідрати, таутомери та фарма(2-циклогекс- 1-еніл-4-піперидин-4-іл-феніл)цевтично прийнятні солі. амід 4-ціано-1Н-імідазол-2-карбонової кислоти, Іншою найбільш переважною сполукою Фор{2-циклогекс-1-еніл-4-[1-(2-метансульфонілмули І є: етил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н[2-циклогекс-1-еніл-4-(1-{2-[(2-гідроксі-етил)імідазол-2-карбонової кислоти, метил-аміно]-ацетил}-піперидин-4-іл)-феніл]-амід [2-циклогекс-1-еніл-4-(1-піридин-2-ілметил4-ціано-1Н-імідазол-2-карбонової кислоти, піперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2та його сольвати, гідрати, таутомери та фаркарбонової кислоти, мацевтично прийнятні солі. 25 88648 26 Додатковою найбільш переважною сполукою [2,4']біпіридиніл-5-іл]-амід4-ціано-1Н-імідазол-2Формули І є: карбонової кислоти сіль трифтороцтової кислоти, {2-циклогекс-1-еніл-4-[1-(2-диметиламінота їх сольвати, гідрати, таутомери та фармаацетил)-гаперидин-4-іл]-феніл}-амід 4-ціано-1Нцевтично прийнятні солі імідазол-2-карбонової кислоти, Винахід також відноситься до способів інгібута його сольвати, гідрати, таутомери та фарвання активності протеїн тирозин кіназ у ссавця за мацевтично прийнятні солі. допомогою введення терапевтично ефективної Ще однією найбільш переважною сполукою кількості, принаймні, однієї сполуки Формули І. Формули І є. Переважною тирозин кіназою є c-fms. {2-циклогекс-1-еніл-4-[1-(2-морфолін-4-ілВважають, що винахід включає енантіомерні, ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Ндіастереомерні та таутомерні форми всіх сполук імідазол-2-карбонової кислоти, Формули І, а також і їх рацемічні суміші. Крім того, та його сольвати, гідрати, таутомери та фардеякі зі сполук, представлених Формулою І, момацевтично прийнятні солі. жуть бути проліками, тобто, похідними діючих ліків, Ще іншими переважними сполуками формули які мають вищі здатності до доставки та терапевІ є: тичне значення в порівнянні з діючими ліками. {4-[1-(3-аміно-3-метил-бутирил)-піперидин-4Проліки перетворюються на активні ліки за допоіл]-2-циклогекс-1-еніл-феніл}-амід 4-ціано-1Нмогою ферментних або хімічних процесів in vivo. імідазол-2-карбонової кислоти сіль трифтороцтоІ. Визначення вої кислоти, Термін "алкіл" відноситься до радикалів, як з (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)лінійним, так і з розгалуженим ланцюгом, що місамід 4Н-[1,2,4]-триазол-3-карбонової кислоти сіль тять до 12 атомів вуглецю, переважно до 6 атомів біс трифтороцтової кислоти, вуглецю, якщо не вказано інше, та включає, але не (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)обмежується, метил, етил, пропіл, ізопропіл, буамід 5-хлор-4Н-[1,2,4]-триазол-3-карбонової кистил, ізобутил, втор-бутил, трет-бутил, пентил, ізолоти сіль трифтороцтової кислоти, пентил, гексил, ізогексил, гептил, октил, 2,2,4[2-циклогекс-1-еніл-4-(цис-2,6-диметилтриметилпентил, ноніл, децил, ундецил та додепіперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2цил. карбонової кислоти сіль біс трифтороцтової кислоТермін "гідроксіалкіл" відноситься до радикати, лів, як з лінійним, так і з розгалуженим ланцюгом, [2-циклогекс-1-еніл-4-(транс-2,6-диметилщо містять до 6 атомів вуглецю, в яких один атом піперидин-4-іл)-феніл]-амід 5-ціано-1Н-імідазол-2водню замінений на ОН групу. карбонової кислоти сіль біс трифтороцтової кислоТермін "гідроксіалкіламіно" відноситься до гідти, роксіалкільної групи, в якій один атом водню у вуг{2-циклогекс-1-еніл-4-[1-(R)-(+)-(2,3-дигідроксилецевому ланцюзі замінений на аміно групу, де пропіоніл-)-піперидин-4-іл]-феніл}-амід 5-ціано-1Назот є точкою приєднання до залишку молекули. імідазол-2-карбонової кислоти, Термін "циклоалкіл" відноситься до насиченого [2-циклогекс-1-еніл-4-(1-метокси-піперидин-4або частково ненасиченого кільця, що містить від іл)-феніл]-амід 5-ціано-1Н-імідазол-2-карбонової 3 до 8 атомів вуглецю. В кільці необов'язково мокислоти сіль трифтороцтової кислоти, жуть бути присутні до чотирьох алкільних замісни[6-(4,4-диметил-циклогекс-1-еніл)ків. Приклади включають циклопропіл, 1,11',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5-іл]-амід диметил циклобутил, 1,2,3-триметилциклопентил, 4-ціано-1Н-імідазол-2-карбонової кислоти сіль циклогексил, циклопентеніл, циклогексеніл та 4,4трифтороцтової кислоти, диметил циклогексеніл. {4-[1-(2-аміно-2-метил-пропіоніл-)-піперидин-4Термін "дигідросульфонопіраніл" відноситься іл]-2-циклогекс-1-еніл-феніл}-амід 5-ціано-1Німідазол-2-карбонової кислоти сіль трифтороцтоТермін "гідродо наступного радикалу: вої кислоти та ксіалкіл" відноситься до, принаймні, однієї гідро[6-циклогекс-1-еніл-1'-(2-метансульфонілксильної групи. зв'язаної з будь-яким атомом вугетил)-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-5лецю в алкільному ланцюзі. іл]-амід 5-ціано-1Н-імідазол-2-карбонової кислоти, Термін "аміноалкіл" відноситься до, принаймні, та їх сольвати, гідрати, таутомери та фармаоднієї первинної або вторинної аміно групи, зв'яцевтично прийнятні солі. заної з будь-яким атомом вуглецю в алкільному Додатковими переважними сполуками Формуланцюзі, де алкільна група є точкою приєднання ли І є: до залишку молекули. {2-циклогекс-1-еніл-4-[1-(2-метиламіноТермін "алкіламіно" відноситься до аміно з одацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Нним алкільним замісником, де аміно група є точімідазол-2-карбонової кислоти, кою приєднання до залишку молекули. [1'-(2-диметиламіно-ацетил)-6-(4,4-диметилТермін "діалкіламіно" відноситься до аміно з циклогекс-1-еніл)-1',2',3',4',5',6'-гексагідродвома алкільними замісниками, де аміно група є [2,4']біпіридиніл-5-іл]-амід 4-ціано-1Н-імідазол-2точкою приєднання до залишку молекули. карбонової кислоти сіль трифтороцтової кислоти Термін "гетероароматичний" або "гетероарил" та відноситься до 5 - 7-членних моно-або до 8 - 10[6-(4,4-диметил-циклогекс-1-еніл)-1'-(2членних біциклічних ароматичних кільцевих сисметансульфоніл-етил)-1',2',3',4',5',6'-гексагідротем, в якій будь-яке кільце може містити від одного до чотирьох гетероатомів, вибраних з Ν, Ο або S, 27 88648 28 де атоми азоту та сірки можуть існувати в будьвна кількість, принаймні, однієї сполуки Формули І якому дозволеному окисненому стані. Приклади вводять в комбінації з ефективною кількістю хіміовключають бензимідазоліл, бензотіазоліл, бензотітерапевтичного засобу. єніл, бензоксазоліл, фурил, імідазоліл, ізотіазоліл, Винахід, крім того, забезпечує способи лікуізоксазоліл, оксазоліл, піразиніл, піразоліл, піривання та попередження метастазу, що є результадил, піримідиніл, піроліл, хінолініл, тіазоліл та тієтом раку, який включають, але не обмежуються, ніл. рак яєчників, рак маткових труб, рак молочної заТермін " гетероатом" відноситься до атома лози, рак товстої кишки, рак шлунку, лейкоз ворсиазоту, атома кисню або атома сірки, де атоми азостих клітин та недрібноклітинну карциному легені. ту та сірки можуть існувати в будь-яких дозволеВинахід, крім того, забезпечує способи лікуних окиснених станах. вання остеопорозу, хвороби Пагета та інших хвоТермін "алкокси" відноситься до радикалів з роб, в яких ресорбція кістки опосередковує захвопрямим або розгалуженим ланцюгом, що містять рюваність, включаючи артрит, пошкодження до 12 атомів вуглецю, якщо не вказано інше, зв'япротезу, остеолітичну саркому, мієлому та метазаних з атомом кисню. Приклади включають метостаз пухлини в кістки, який часто відбувається при кси, етокси, пропокси, ізопропокси та бутокси. раку, включаючи, але не обмежуючись, рак молоТермін "арил" відноситься до моноциклічних чної залози, рак передміхурової залози та рак товабо біциклічних ароматичних кільцевих систем, що стої кишки. містять від 6 до 12 вуглеців в кільці. В кільці неВинахід також забезпечує способи лікування обов'язково можуть бути присутні алкільні замісниболю, зокрема скелетного болю, викликаного меки. Приклади включають бензол, біфеніл та нафтастазом пухлин або остеоартритом, а також вісталін. церального, запального га нейрогенного болю. Термін "аралкіл" відноситься до С1-6алкільної Винахід також забезпечує способи лікування групи, що містить арильний замісник. Приклади серцево-судинних, запальних та аутоімунних хвовключають бензил, фенілетил або 2-нафтилметил. роб у ссавців, включаючи людей, які включають Термін "сульфоніл" відноситься до групи введення терапевтично ефективної кількості фарS(O)2Ra, де Ra являє собою водень, алкіл, циклоамацевтично прийнятної форми, принаймні, однієї лкіл, галоалкіл, арил, аралкіл, гетероарил та гетезі сполук Формули І. Приклади хвороб із запальроаралкіл. "Сульфонілюючий агент" вводить групу ним компонентом включають гломерулонефрит, -S(O)2Ra в молекулу. запальне захворювання кишки, пошкодження проII. Терапевтичні використання тезу, саркоїдоз, застійну обструктивну легеневу Сполуки Формули І представляють нові ефекхворобу, астму, панкреатит, ВІЛ інфекцію, псоріаз, тивні інгібітори протеїн тирозин кіназ, як наприклад діабет, ангіогенез, пов'язаний з пухлиною, макуляc-fms, та можуть бути корисними при попередженрну дегенерацію, пов'язану з віком, діабетичну ні та лікуванні розладів, що є наслідком дій цих ретинопатію, рестеноз, шизофренію або хворобу кіназ. Альцгеймера. Ці хвороби можна ефективно лікуВинахід також забезпечує способи інгібування вати за допомогою сполук за даним винаходом. протеїн тирозин кінази, який включає контактуванІнші хвороби, які можна ефективно лікувати, вклюня протеїн тирозин кінази з ефективною інгібуючають, але не обмежуються, атеросклероз та гічою кількістю, принаймні, однієї зі сполук Формули пертрофію серця. Також за допомогою сполук за І. Переважної тирозин кіназою є c-fms. Сполуки за даним винаходом можна лікувати аутоімунні хводаним винаходом також є інгібіторами активності роби, такі як системний червоний вовчак, ревматоFLT3 тирозин кінази. В одному втіленні інгібування їдний артрит, синдром Шегрена, розсіяний склероз протеїн тирозин кінази, принаймні одну зі сполук або увеїт. Формули І об'єднують з відомим інгібітором тироКоли сполуки за винаходом використовують як зин кінази. інгібітори протеїн тирозин кінази, вони можуть бути В різних втіленнях винаходу, протеїн тирозин введені в ефективній кількості в межах діапазону кінази, які інгібують за допомогою сполук Формули дозування від приблизно 0,5мг до приблизно 10г, І, знаходяться в клітинах, в ссавці або in vitro. У переважно від приблизно 0,5мг до приблизно 5г, в випадку ссавців, які включають людей, вводять єдиній або розділених щоденних дозах. На введетерапевтично ефективну кількість фармацевтично не дозування будуть впливати чинники, такі як прийнятної форми, принаймні, однієї зі сполук Фошлях введення, стан здоров'я, вага та вік реципієрмули І. нту, частота лікування та наявність супутнього та Винахід, крім того, забезпечує способи лікунепов'язаного лікувань. вання раку у ссавців, включаючи людей, які вклюСполуки Формули І можуть бути виготовлені у чають введення терапевтично ефективної кількосфармацевтичних композиціях, що містять будь-які ті фармацевтично прийнятної композиції, що відомі фармацевтично прийнятні носії, приклади містить, принаймні, одну сполуку Формули І. Приносіїв включають, але не обмежуються, будь-які клади раку включають, але не обмежуються, гостприйнятні розчинники, дисперсні середовища, пору мієлоїдну лейкемію, гостру лімфоцитарну лейкриття, антибактеріальні і протигрибкові засоби та кемію, рак яєчників, рак маткових труб, рак ізотонічні агенти. Приклади наповнювачів, які тамолочної залози, рак товстої кишки, рак шлунку, кож можуть бути компонентами препарату, вклюлейкоз ворсистих клітин та не дрібноклітинну карчають заповнювачі, зв'язуючі речовини, агенти циному легені. Винахід також забезпечує способи дезинтеграції та змазуючі речовини. лікування певних передракових станів, включаючи Фармацевтично прийнятні солі сполук Формумієлофіброз. В одному втіленні винаходу, ефектили І включають традиційні нетоксичні солі або чет 29 88648 30 вертинні солі амонію, які утворені з неорганічними Крім того, сполуки за даним винаходом можуть чи органічними кислотами або основами. Прикламати одну або більше поліморфних або аморфних ди таких кислотно-адитивних солей включають кристалічних форм, та, мається на увазі, що вони, ацетат, адипат, бензоат, бензолсульфонат, цитяк такі, включені в межі даного винаходу. Крім торат, камфорат, додецилсульфат, гідрохлорид, го, сполуки можуть утворювати сольвати, напригідробромід, лактат, малеат, метансульфонат, клад з водою (тобто, гідрати) або звичайними орнітрат, оксалат, півалат, пропіонат, сукцинат, суганічними розчинниками. Як використовується в льфат та тартрат. Основні солі включають солі даній заявці, термін "сольват" означає фізичну амонію, солі лужних металів, такі як солі натрію та асоціацію сполук за даним винаходом з однією або калію, солі лужноземельних металів, такі як солі більше молекулами розчиннику. Ця фізична асоцікальцію та магнію, солі з органічними основами, ація залучає різні ступені іонного та ковалентного такі як дициклогексиламіно солі, та солі з амінокизв'язку, включаючи водневий зв'язок. В певних слотами, такими як аргінін. Також, основні групи, прикладах сольват можна виділити, наприклад, що містять азот, можуть бути кватернізовані з, коли одна або більше молекул розчинника вклюнаприклад, алкіл галогенідами. чені в кристалічну гратку кристалічної твердої реФармацевтичні композиції за винаходом мочовини. Мається на увазі, що термін "сольват" жуть бути введені за допомогою будь-яких засобів, включає, як сольвати, що знаходяться у розчині, які досягають вказаної мети. Приклади включають так і здатні до виділення сольвати. Необмежуючі введення парентеральним, підшкірним, внутрішприклади прийнятних сольватів включають етаноньовенним, внутрішньом'язовим, внутрішньочерелати, метанолати та подібні. вним, транс дермальним, букальним або окулярМається на увазі, що даний винахід включає в ним шляхом. Альтернативно або супутньо, свої межі сольвати сполук за даним винаходом. введення може бути пероральним. Прийнятні преТаким чином, в способах лікування за даним винапарати для парентерального введення включають ходом, термін "введення" повинен включати засоводні розчини активних сполук в розчинній у воді би для лікування, полегшення або попередження формі, наприклад, розчинні у воді солі, кислотні синдрому, розладу або хвороби, описаних в даній розчини, лужні розчини, розчини в декстрозі-воді, заявці, сполуками за даним винаходом або їх соізотонічні розчини вуглеводів та комплекси з вклюльватом, які очевидно будуть включені в межі виченням циклодекстрину. находу, хоча вони конкретно не розкриті. Поліморфи та сольвати III. Способи одержання Схема 1 ілюструє загальну методику одержання сполук Формули І. Сполуки Формули 1-2 можуть бути одержані за допомогою орто-галогенування, переважно бромування, аміно сполук Формули 1-1, з наступними реакціями сполучення, що каталізовані металом, з бороновими кислотами або боронатними ефірами (реакції Сузукі, де R2M являє собою R2B(OH)2 або бороновий ефір) або реагентами на основі олова (реакції Стіла, де R2M являє собою R2Sn(алкіл)3) [для огляду, див. N. Міуаша. А. Suzuki, Chem. Rev., 95:2457 (1995), J. К. Stille, Angew. Chem, Int. Ed. Engl, 25:508024 (1986) та A. Suzuki in MetalCatalyzed Coupling Reactions, F. Deiderich, P. Stang, Eds, Wiley-VCH, Weinheim (1988)]. Сполуки формули 1-1 можуть бути комерційно доступні, або для одержання сполук Формули 1-1, виходячи з вихідної речовини 1-0, можуть бути використані описані вище реакції перехресного сполучення, опосередковані паладієм. Переважними умовами для бромування 1-1 є N-бромсукцинімід (NBS) у прийнятному розчиннику, такому як Ν,Ν-диметилформамід (DMF), дихлорметан (DCM) або ацетонітрил. Сполучення, каталізовані металом, переважно реакції Сузукі, можуть бути проведені відповідно до стандартної методики, переважно в присутності каталізатору на основі паладію, такого як тетракіс(трифенілфосфін)палпдій (0) (Pd(PPh3)4), водної основи, такої як водн. Na2CO3, та прийнятного розчиннику, такого як толуол, етанол, диметоксіетан (DME) або DMF. Сполуки Формули 1 можуть бути одержані за допомогою реакції сполук Формули 1-2 з карбоновими кислотами WCOOH відповідно до стандартних методик утворення амідного зв'язку [для огляду, див.: М. Bodansky and A. Bodansky, The 31 88648 32 Practice of Peptide Synthesis, Springer-Verlag, NY первісно присутня у вихідній речовині, або приєд(1984)] або за допомогою реакції з хлорангідриданана за допомогою реакції нітрування. Крім того, ми кислот WCOC1 або активованими ефірами аміно група може бути одержана за допомогою WCO2Rq (де Rq являє собою групу, що відходить, відновлення азидної групи, яка може бути присуттаку як пентафторфеніл або N-сукцинімід). Переня у вихідній речовині, або може бути одержана в важними умовами реакцій для сполучення з результаті нуклеофільного ароматичного заміWCOOH є: коли W являє собою фуран, оксаліл щення активованого галогеніду аніоном азиду, як хлорид в DCM з DMF, як каталізатором, з одерзгадано вище. Аміно група також може бути одержанням хлорангідриду кислоти WCOC1 та потім жана в результаті нуклеофільного ароматичного сполучення в присутності триалкіламіну, такого як заміщення активованого галогеніду (в, наприклад DIEA; коли W являє собою пірол, гідрохлорид 1-(3нітрогало сполуці) аміаком або аніоном еквівалендиметиламінопропіл)-3-етилкарбодііміду (EDCI) та та захищеного аміаку, наприклад, трет-бутил кар1-гідроксибензотриазол-6-сульфонамідометил баматом. Якщо амін вводять в захищеній формі, гідрохлорид (HOBt); та коли W являє собою імідазахист може бути знятий відповідно до стандартзол, переважними умовами є гексафторфосфат них способів, описаних в літературі. [Для приклабромтрипіролідинофосфонію (РуВrOР) та діізопдів амінозахисних груп та способів зняття захисту ропілетиламін (DIEА) в DCM. див.: Theodora W. Greene and Peter G. Μ. Wuts, Розуміють, що необов'язкове заміщення, приJohn Wiley and Sons, Inc., NY (1991)]. Реакція сутнє в кільці А у Формулі І, може бути присутнім у утворення кільця включає обробку анілінової аміно вихідних речовинах 1-1 або 1-3 та, в таких випадгрупи прийнятним необов'язково заміщеним діелеках, воно буде існувати для синтезу, наведеного ктрофілом, переважно дигалогенідом або дикарна Схемі 1. Альтернативно різні замісники в сполубонільною сполукою, що приводить до двох заміках Формули І можуть бути введені різними шлящень в аміно групі з одержанням необов'язково хами, описаними нижче, з одержанням необов'яззаміщеного гетероциклу. У випадку дигалогенідів кового заміщення, наведеного для Формули І. може бути додана будь-яка з прийнятних основ, як Група, що відходить. "L1", присутня в кільці А у поглинач кислоти, така як наприклад карбонат Формулі 1-0 або 1-3, може бути заміщена до або калію, гідроксид натрію, або триалкіламін, такий як на будь-якій стадії Схеми 1. Коли такі групи, що триетиламін. Таким чином, обробка біс(2відходять, (переважно фтор або хлор) активуютьгалоетил)аміном, таким як біс(2-хлоретил)амін або ся нітро групою Формули 1-3 для нуклеофільної біс(2-брометил)амін, буде надавати піперазинове атаки, вони можуть бути піддані прямому нуклеокільце [див., наприклад, J. Med. Chem., 29: 640-4 фільному ароматичному заміщенню за допомогою (1986) та Med. Сhem., 46. 2837 (2003)]. Необов'язаміаку та аніону азиду або за допомогою амінів, кове заміщення на азоті аміну в реагенті буде ввоспиртів, тіолів та інших нуклеофілів в присутності дити необов'язкове заміщення на кінцевому аміні прийнятної основи, такої як K2СО3, Ν,Νпіперазину. Наприклад, обробка N,N-біс(2діізопропілетиламін (DIEА) або Net3. Коли група, хлоретил)аніліном буде надавати Nщо відходить, прийнятна для сполучень, каталізофенілпіперазино групу. Обробка біс(2ваних металом, (переважно бром або трифтормегалоетил)ефіром або біс(2-галоетил)тіоефіром тансульфонілокси), може бути проведений цілий буде надавати морфолінове або тіоморфолінове ряд реакцій перехресного сполучення (як наприкільце, відповідно. клад реакції Сузукі або Стілу, які описані вище, Інший альтернативний спосіб прямого замідля введення R2) Інші реакції сполучення, каталіщення для введення гетероциклічних замісників в зовані металом, які можуть бути використані, кільце А полягає в утворенні гетероциклу з альдевключають ароматичне та гетероароматичне амігіду (тобто з формільної групи в кільці А). Формінування та амідування [для огляду, див.. S. L. льна група може бути первісно присутня у вихідній Buchwald, et al, Top. Curr. Chem., 219:131-209 речовині в захищеній чи незахищеній формі або (2001) та J. F. Hartwig in "Orgcmopalladmm може бути одержана в результаті будь-якої з реаChemistry for Organic Synthesis," Wiley Interscience, кцій формілювання, відомих з літератури, включаNY (2002)]. Додаткові реакції перехресного сполуючи реакцію Вільсмеєра-Хаака [для огляду хімії чення, каталізовані металом, з 2,4,6-триметилформілювання, див.: G. A. Olah, et al, Chem Rev., циклотрибороксаном можуть бути використані, 87: (1987)] або за допомогою пара-формілювання якщо L1 являє собою бром, йод або хлор, активонітроароматиків [див.: A. Katritsky and L. Хіе, ваний нітро, з одержанням необов'язкового заміTetrahedron Lett., 37:347-50 (1996)]. щення метилом [див. М. Gray, et al, Tetrahedron Остаточно розуміють, що сполуки Формули І Lett, 41:6237-40(2000)]. можуть бути додатково дериватизовані. Захисні В деяких випадках, початкові замісники могрупи в сполуках Формули І можуть бути видалені жуть бути додатково дериватизовані, як описано відповідно до стандартним методик синтезу нижче, з одержанням кінцевого заміщення ФормуTheodora W. Greene and Peter G. Μ. VVuts, John ли І. Wiley and Sons, Inc., NY (1991)] та потім можуть Альтернативний спосіб введення гетероциклібути піддані подальшій дериватизації. Приклади чних замісників, що містять азот, в кільце А поляподальшої дериватизації сполук Формули І вклюгає в утворенні гетероциклу з аміно групи в кільці чають, але не обмежуюся: коли сполуки Формули І А. Аміно група може бути первісно присутня у вимістять первинний або вторинний амін, амін може хідній речовині в захищеній або незахищеній форбути підданий реакції з альдегідами або кетонами мі або може бути одержана в результаті відновв присутності відновника, такого як триацетоксилення нітро групи, яка також може бути або боргідрид натрію [див. Abdel-Magid J. Org. Chem. 33 88648 34 61, pp. 3849-3862, (1996)], для відновного алкілувана до амідів або кислот в кислих або основних вання; з хлорангідридами кислоти або карбоновиумовах. Основні аміни можуть бути окиснені до Nми кислотами та реагентом, що утворює амідний оксидів та навпаки N-оксиди можуть бути відновзв'язок, як описано вище, з одержанням амідів; з лені до основних амінів. Коли сполуки Формули І сульфоніл хлоридами з одержанням сульфонамімістять сульфід, ациклічний або циклічний, сульдів; з ізоціанатами з одержанням сечовин; з арилфід додатково може бути окиснений до відповідабо гетероарил-галогенідами в присутності каталіних сульфоксидів або сульфонів. Сульфоксиди затора на основі паладію, як описано вище (див. можуть бути отримані за допомогою окиснення, посилання на Бухвальда та Хартвіга, наведені використовуючи прийнятний окисник, такий як вище), з одержанням арил та гетероариламінів. один еквівалент (мета-хлорпербензойної кислоти) Крім того, коли сполуки Формули І містять арил МСРВА, або за допомогою обробки NaIO4 [див., галогенід або гетероарил галогенід, ці сполуки наприклад, J. Regan, et al, J. Med. Chem., 46: 4676можуть бути піддані реакціям, що каналізуються 86 (2003)] та сульфони можуть бути одержані, виметалом, з бороновими кислотами (наприклад, користовуючи два еквіваленти МСРВА, або за досполучення Сузукі або Стіла, як описано вище) помогою обробки N-оксидом 4-метилморфоліну та або амінами чи спиртами (сполучення типу Бухвакаталітичним тетрооксидом осмію [див, наприклад, льда або Хартвіга, див посилання на Бухвальда та заявку PCTWO 01/47919]. Хартвіга, наведені вище). Коли сполуки-Формули І містять ціано групу, ця група може бути гідролізо Схема 2а ілюструє одержання сполук Формули І. F являє собою -NQaQbR3-, -О-, S, SO або SO2, та АА являє собою -NH2 або -NO2. D1 та D2 наведені лише з метою ілюстрації; фахівець в даній галузі техніки визнає, що D5, D6, D7, D8 також можуть бути присутні. Кетони формули 2-1 можуть бути перетворені на вініл трифлат формули 2-2 за допомогою обробки ненуклеофільною основою, такою як LDA, та потім поглинання одержаного еноляту трифторметансульфонатним реагентом, таким як трифторметансульфоновий ангідрид або переважно N-фенілтрифторметансульфонімід. Сполучення Сузукі боронових кислот або боронатних ефірів формули 2-3 з вініл трифлатами формули 2-2 може забезпечити сполуки формули 2-4, в яких Ζ=С [Synthesis, 993 (1991)]. Для сполук формули 2-4 обробка Pd/C може відновлювати олефін (та нітро, якщо АА=NO2) з одержанням Ζ=СН , АА=ΝΗ 2. Сполуки формули 24, в яких F представляє -SO2, можуть бути одержані зі сполук формули 2-4, в яких АА=-NO2 та F являє собою сульфід (F=-S-), за допомогою окис нення МСРВА або іншими способами, описаними на Схемі 1. Нітро група потім може бути відновлена Pd/C з відновленням, як нітро, так і олефіну. Сполуки формули 2-4 (АА=NH2) потім перетворюють на сполуки Формули 2-5 (які також представляють сполуки Формули І, якщо не потрібно ніяких подальших модифікацій), як описано на Схемі 1. Сполуки формули 2-5 можуть, крім того, бути модифіковані з одержанням додаткових сполук Формули І. Наприклад, у випадках, коли F являє собою -NQaQbR3-, QaQb=прямий зв'язок та R3 представляє ВОС захисну групу (СО2tВu), ВОС група може бути видалена відповідно до стандартної методики, як наприклад трифтороцтова кислота (TFA) в DCM (Greene and Wuts, ibid), з одержанням вторинного аміну, який потім може бути додатково дериватизований з одержанням сполук Формули І. Подальша дериватизація включає, але не обмежується: реакції з альдегідами або кетонами в присутності відновника, такого як триацетоксиборгідрид натрію, з одержанням сполук Форму 35 88648 36 ли II, в яких F=-NCH2R3 (A. F. Abdel-Magid, ibid.); з щення, що каталізуються металами, як наведено хлорангідридами кислоти або з карбоновими кисна Схемі 1, з одержанням сполук Формули І, в яких лотами та реагентом, що утворює амідний зв'язок F=-NR'. (S. L. Buchwald, et al, ibid.; J. Η. Hartwig, (як описано на Схемі 1), з одержанням сполук фоibid). Для зазначеного вище прикладу, Ra та Rb рмули II, в яких F=-NCOR3; з сульфоніл хлоридами незалежно являють собою водень, алкіл, циклоал(як описано на Схемі 1) з одержанням сполук Фокіл, галоалкіл, арил, аралкіл, гетероарил та гетермули І, в яких F=-NSO2Ra; з ізоціанатами (як опироаралкіл. сано на Схемі 1) з одержанням сполук Формули II, в яких F=-NCONRaRb; або піддані реакціям замі Схема 2b ілюструє модифікацію Схеми 2а для синтезу частково ненасичених сполук Формули І. Ε являє собою -NQaQbR3-, -О- (D1=D2 ), -SН = (D1=D2=Н), -SO- (D1=D2=Н) або -SO2- (D1=D2=Η), та RAA представляє -NH2 або -NO2 Сполуки формули 2-4 одержують, як показано на Схемі 2. Якщо RAA=-NO2, нітро група повинна бути відновлена за допомогою способу, який не відновлює олефіни, таким як залізо та хлорид амонію. Якщо RAA У фо рмулі 2-4 являє собою аміно групу, тоді не потрібно жодної стадії, та сполуки формули 2-4 також є сполуками формули 2-7. Для одержання сполук формули 2-7, в яких Ε=-SO2- або -SO-, повинне бути проведене окиснення сульфіду в сполуці 2-4, в якій RAA=-NO2, як описано вище, з наступним відновленням нітро. III. Способи одержання Схема 3 ілюструє одержання проміжних сполук для синтезу сполук Формули І, в яких кільце А являє собою піридил, та R5 є необов'язковим заміщенням на кільці А або одним з гетероциклічних замісників, як визначено у Формулі І. K=NH2 або інші функціональні групи, такі як NO2, COOH або COOR, які в підсумку можуть бути перетворені на аміно групу за допомогою відомих з літератури способів, таких як відновлення для NO2 (як описано для Схеми 1) або перегрупування Курціуса для СООН [для огляду, див. Organic Reactions, 3: 337 (1947)]. L3 та L4 являють собою галогени (K=СООН також може бути одержаний з K=COOR за допомогою простого гідролізу, каталізованого основою або кислотою). Взагалі, селективність та порядок введення R2 та R5 можуть бути досягнуті за допомогою віднос ної реактивності галогенів L3 та L4, вибраних в сполуці (3-1), внутрішньої селективності гетероциклу та/або використаних умов реакції. Приклад використання відносної реактивності галогенів L3 та L4 в селективному введенні R2 та R5 буде включати ситуацію, коли, в сполуках Формули 3-1, в яких L являє собою фторогрупу та L являє собою бромогрупу, селективне заміщення фторогрупи на нуклеофіл може бути досягнуте після заміщення залишкової бромогрупи за допомогою хімії заміщення, що каталізується металом (як наприклад реакції перехресного сполучення Сузукі або Стіла, як додатково описано нижче). Так само в сполуках Формули 3-1, в яких один з L3 та L4 являє собою йодогрупу та інший являє собою бромо або хлорогрупу, хімія селективного заміщення, що каталізується металом (як наприклад реакції перехресного 37 88648 38 сполучення Сузукі або Стіла чи амінування Бухвачено вище, як описано на Схемі 1, може забезпельда/Хартвіга, як додатково описано нижче) на чувати сполуки Формул 3-2 або 3-3. йодогрупі може бути досягнута після заміщення Сполука 3-2 потім може бути перетворена на залишкової бромо або хлорогрупи за допомогою сполуку 3-4 за допомогою сполучення по Сузукі іншої реакції заміщення, що каталізується метаабо Стілу, що каталізується металом, як викладелом. но вище. L в сполуці 3-3 також потім може бути Як проілюстровано на Схемі 3, група, що відзаміщений R5 з одержанням сполук Формули 3-4, ходить, L3 у Формулі 3-1 спочатку може бути замізнову, за допомогою прямого нуклеофільного защена з отриманням сполук Формули 3-3 або група, міщення або реакції, що каталізується металом, з що відходить, L4 спочатку може бути заміщена з нуклеофілом або за допомогою подібної реакції отриманням сполуки Формули 3-2. Сполуки 3-2 перехресного сполучення, що каталізується метаабо 3-3 потім можуть бути піддані реакції, щоб лом, як викладено вище. Коли R5 у формулах (3-2, замінити L3 або L4, з одержанням сполуки Форму3-3 або 3-4) являє собою захищений амін та K не є ли 3-4. аміно групою, захист може бути знятий, щоб демаТаким чином, пряме нуклеофільне заміщення скувати аміно функціональність. Ця аміно функціабо амінування, що каталізується металом, сполуональність потім може бути додатково дериватики Формули 3-1 вторинним аміном, аміаком або зована, як описано на Схемі 1. Коли група K у захищеним аміном, таким як трет-бутил карбамат Формулі 3-4 не є аміно групою (як наприклад фун[для огляду, див. Modern Animation Methods: Ricci, кціональність, описана вище), вона може бути пеΑ., Ed.; Wiley-VCH: Weinheim, 2000], можуть бути ретворена на аміно групу за допомогою відомих з використані для введення R3 у Формули 3-2 або 3літератури способів [див., наприклад 3, де R5 являє собою первинний або вторинний Comprehensive Organic Transformations: Larock, амін, аміно групу (NH2) та еквівалент аміну або R.S.; Wiley and Sons Inc., USA, 1999] та одержаний захищену аміно групу. Сполучення, каталізоване амін 3-5 може бути використаний в реакціях утвометалом, сполуки 3-1 з бороновими кислотами або рення амідного зв'язку, як описано на Схемі (1), з боронатними ефірами (реакція Сузукі, Μ=група отриманням сполук Формулі І. Коли K у Формулі 3боронової кислоти або група боронатного ефіру) 4 являє собою аміно групу, вона може бути викоабо з оловоорганічною сполукою (реакція Стіла, ристана безпосередньо в амідному сполученні, як Μ=SnR3, де R3=алкіл та інші замісники, як визнавикладено вище. Схеми 4а та 4b ілюструють одержання проміжних сполук для подальшої модифікації відповідно до Схемі 3, виходячи з моногало-заміщеної сполуки Формул 4-1 та 4-5, за допомогою введення другої групи, що відходить, після того, як заміна першої групи була завершена. Ці сполуки також можуть бути використані для синтезу сполук Формули І, в яких кільце А являє собою піридин та R5 є або необов'язковим заміщенням в кільці А, або одним з гетероциклічних замісників. Як на Схемі 3, залишкові положення в піридиновому кільці можуть бути заміщені, як описано у Формулі 1. K=NH2 або інші функціональні групи, такі як NO2, СООН або COOR, які у підсумку можуть бути перетворені на аміно групу за допомогою відомих з літератури способів, таких як відновлення або перегрупуван ня Курціуса, як описано на Схемі 3. L та L являють собою галогени. В цих сполуках, Τ являє собою або Н, або функціональну групу, таку як ОН, яка може бути перетворена на групи, що відходять, L3 або L4, такі як галоген, трифлат або мезилат, за допомогою відомих з літератури способів [див., наприклад, Nicolai, Ε , et al., J. Heterocyclic Chemistry, 31. (73), (1994)]. Заміна L3 в сполуці Формули 4-1 або L4 у Формулі 4-5 за допомогою способів, описаних на Схемі 3, може надавати сполуки Формул 4-2 та 4-6. У цей момент, замісник Τ сполук 4-2 або 4-6 може бути перетворений на групу, що відходить, L4 або L3 (переважно галоген) за допомогою стандартних способів з одержанням сполук Формул 4-3 та 4-5. Наприклад, коли Τ=ОН, переважними реагентами протягом проведення 39 88648 40 цього перетворення є тіоніл хлорид, РСk5. РОСl3 або РВr3 [див., протягом прикладів, Kolder, den Hertog., Reel Tray. Chim. Pays-Bas, 285, (1953). та Iddon, B, et. al., J. Chem. Soc. Perkm Trans. 1., 1370, (1980)]. Коли Τ=Η, він може бути безпосередньо галогенований (переважно бромований) з В колбу поміщали імідазол-4-карбонітрил (0,5г, одержанням сполук Формул 4-3 або 4-7 [див., на5,2ммоль) (Synthesis, 677, 2003), 2приклад, Canibano, V. et al., Synthesis, 14, 2175, (триметилсиліл)етоксиметил хлорид (SEMC1) (2001)]. Переважними умовами протягом брому(0,95мл, 5,3ммоль), K2СО3 (1,40г, 10,4ммоль) та вання є NBS у прийнятному розчиннику, такому як ацетон (5мл) і перемішували протягом 10год при DC M або ацетонітрил. RT. Суміш розбавляли EtOAc (20мл) та промивали Сполуки Формул 4-3 або 4-7 можуть бути певодою (20мл) та сольовим розчином (20мл) та ретворені на сполуки Формул 4-4 або 4-8 шляхом органічний шар сушили над MgSO4. Неочищений введення залишкових груп R2 або R5, відповідно, продукт елюювали з 20г SPE картриджу (силіказа допомогою способів, описаних вище, та потім гель) 30 % ЕtOАс/гексан, одержуючи 0,80г (70%) на сполуки Формули І, за допомогою способів, зазначеної у заголовку сполуки у вигляді безбарвописаних на Схемі 3 протягом перетворення споного масла. Мас-спектр (СІ (СН4). m/z): Розрах. лук Формул 3-4 та 3-5 на сполуки Формули І. для C10H17N3OSi, 224,1 (М+Н), знайдено 224,1. Приклад 1 b) 2-Бром-1-(2-триметилсилант-етоксиметил)5-Ціано-фуран-2-карбонова кислота 1Н-імідазол-4-карбонітрил До колби з мішалкою та колонкою Vigreaux під Ar додавали 2-форміл-5-фуранкарбонову кислоту (2,8г, 20ммоль), гідрохлорид гідроксиламіну (2,7г, 40ммоль) та сухий піридин (50мл). Суміш нагрівали до 85°С, додавали оцтовий ангідрид (40мл) та суміш перемішували протягом 3год. Після охолодження до 60°С додавали воду (250мл) та суміш перемішували при RT протягом 70год. Суміш підкисляли до рН=2 концентрованою соляною кислотою та екстрагували 3:1 дихлорметан-ізопропанол (8x100мл). Об'єднані органічні шари промивали водою (100мл), сольовим розчином (100мл), сушили над безводним сульфатом натрію та концентрували у вакуумі, одержуючи зазначену у заголовку сполуку у вигляді жовто-коричневої твердої речовини (1,26г, 46 %). 1Н - ЯМP (CD3OD; 400МГц): d 14,05 (br s, 1H), 7,74 (d, 1H, J=3,8Гц), 7,42 (d, 1H, J=3,8Гц). Приклад 2 4-Ціано-1Н-пірол-2-карбонова кислота Зазначена у заголовку сполука була одержана відповідно до описаної в літературі методики [Loader and Anderson, Canadian J. Chem. 59: 2673 (1981)]. 1Н - ЯМP (CDCl3; 400МГц): d 12,70 (br s, 1Н), 7,78 (s, 1H), 7,13 (s, 1H) Приклад 3 4-Ціано-1-(2-триметилсиланіл-етоксиметил)1Н-імідазол-2-карбоксилат сіль калію a) 1-(2-Триметилсиланіл-етоксиметил)-1Німідазол-4-карбонітрил До розчину 1-(2-триметилсиланілетоксиметил)-1Н-імідазол-4-карбонітрилу (0,70г, 3,1ммоль) (який був одержаний на попередній стадії) в ССl4 (10мл) додавали NBS (0,61г, 3,4ммоль) та ΑΙΒΝ (кат), та суміш нагрівали при 60°С протягом 4год. Реакційну суміш розбавляли EtOAc (30мл) та промивали NaHCO3 (2x30мл) і сольовим розчином (30мл) та органічний шар сушили над Na2SO4 та потім концентрували. Зазначену у заголовку сполуку елюювали з 20-г SPE картриджу (силікагель) 30% EtOАс/гексан, одержуючи 0,73г (77%) жовтої твердої речовини. Масспектр (СІ (СН4), m/z): Розрах. для C10H16BrN3OSi, 302,0/304,0 (М+Н), знайдено 302,1/304,1. c) Етиловий ефір 4-ціано-1-(2триметилсиланіл-етоксиметил)-1Н-імідазол-2карбонової кислоти До розчину 2-бром-1-(2-триметилсиланілетоксиметил)-1Н-імідазол-4-карбонітрилу (0,55г, 1,8ммоль) (який був одержаний на попередній стадії) в THF (6мл) при -40°С по краплям додавали 2Μ розчин i-PrMgCl в THF (1мл). Реакційну суміш залишали перемішуватися протягом 10хв при 40°С та потім охолоджували до -78°С, та додавали етил ціаноформіат (0,3г, 3,0ммоль). Температурі реакційної суміші дозволяли досягти RT та реакційну суміш перемішували протягом 1год. Реакцію гасили насиченим водним NH4Cl, розбавляли EtOAc (20мл) та промивали сольовим розчином (2x20мл), та органічний шар сушили над Na2SO4 та потім концентрували. Зазначену у заголовку сполуку елюювали з 20-г SPE картриджу (силікагель) 41 88648 42 c) 1-Метил-4-[3-(3-метил-тіофен-2-іл)-4-нітро30% EtOAc/гексан, одержуючи 0,4г (74%) безбарвфеніл]-піперазин ного масла Мас-спектр (ESI, m/z): Розрах. для До колби, що містить 1-(3-бром-4-нітро-феніл)C13H21N3O3Si, 296,1 (М+Н), знайдено 296,1. 4-метил-піперазин (68мг, 0,2ммоль, який був одеd) 4-Ціано-1-(2-триметилсилант-етоксиметил)ржаний в Прикладі 4, стадія (а)), 4,4,5,51Н-імідазол-2-карбоксилат сіль калію тетраметил-2-(3-метил-тіофен-2-іл)До розчину етилового ефіру 4-ціано-1-(2[1,3,2]діоксаборолан (61мг, 0,27ммоль, який був триметилсиланіл-етоксиметил)-1Н-імідазол-2одержаний на попередній стадії) та Pd(PPh3)4 карбонової кислоти (0,4г, 1,3ммоль) (який був оде(14мг, 6мол%) поміщали толуол (3мл), етанол ржаний на попередній стадії) в етанолі (3мл) до(3мл) та 2Μ Na2CO3 (4мл). Одержану суміш нагрідавали 6Μ розчин KОН (0,2мл) та реакційну суміш вали при 80°С протягом 2год та потім виливали в перемішували протягом 10хв та потім концентруEtOAc (25мл). Органічний шар відокремлювали, вали, одержуючи 0,40г (100%) зазначеної у загосушили (Na2SO4) та концентрували у вакуумі. ловку сполуки у вигляді жовтої твердої речовини. 1 Очищенням за допомогою препаративної тонкоН - ЯМP (400МГц, CD3OD) d 7,98 (s, 1Н), 5,92 (s, шарової хроматографії на силікагелі (EtOAc) оде2H), 3,62 (m, 2H), 0,94 (m, 2Н), 0,00 (s, 9H). Масржували 40мг (63%) зазначеної у заголовку сполуспектр (ESI-нег, m/z): Розрах. для C11H17N3O3Si, ки у вигляді світло-жовтої твердої речовини. Мас266,1 (М-Н), знайдено 266,0. спектр (ESI, m/z): Розрах. для C16H19N3O2S, 318,1 Приклад 4 (М+Н), знайдено 318,2 [4-(4-Метил-піперазин-1-іл)-2-(3-метил-тіофенd) [4-(4-Метил-піперазии-1-іл)-2-(3-метил2-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кистіофен-2-іл)-феніл]-амід 5-ціано-фуран-2лоти карбонової кислоти 1-Метил-4-[3-(3-метил-тіофен-2-іл)-4-нітрофеніл]-піперазин (60мг, 0,18ммоль, який був одержаний на попередній стадії) перемішували з 40мг 5% Pd-C в МеОН (5мл) під Н2 (1атм) протягом 2год. Реакційну суміш фільтрували через целіт та концентрували у вакуумі, одержуючи 40мг (72%) 4(4-метил-піперазин-1-іл)-2-(3-метил-тіофен-2-іл)феніламіну у вигляді коричневої твердої речовини, a) 1-(3-Бром-4-нітро-феніл)-4-метил-піперазин яку негайно використовували без додаткового 2-Бром-4-фторнітробензол (949мг, 4,31ммоль) очищення. Використовуючи методику, подібну до двома порціями додавали до нерозбавленого NПрикладу 9, стадія (с), 4-(4-метил-піперазин-1-іл)метилпіперазину (8мл) при 0°С та залишали нагрі2-(3-метил-тіофен-2-іл)-феніламін (40мг, ватися до кімнатної температури. Реакційну суміш 0,13ммоль) піддавали реакції з 5-ціано-фуран-2нагрівали до 60°С протягом 1год, та потім її розкарбоніл хлоридом (30мг, 0,19ммоль, який був бавляли 50мл EtOAc та виливали в Н2О (50мл). одержаний в Прикладі 9, стадія (с)) в присутності Шари відокремлювали та органічний шар промиDIEA (61мкл, 0,34ммоль), одержуючи 18,9мг (36%) вали насиченим водним NaHCO3, сушили зазначеної у заголовку сполуки у вигляді жовтої (Na2SO4), та концентрували у вакуумі, одержуючи твердої речовини. 1Н - ЯМP (CDCl3; 400МГц): d 580мг (45%) зазначеної у заголовку сполуки у ви2,13 (s, 3Н), 2,38 (s, 3Н), 2,59-2,62 (m, 4H), 3,24гляді жовтої твердої речовини. Мас-спектр (ESI, 3,27 (m, 4H), 6,92 (d, 1Н, J=2,8Гц), 7,06 (d, 1Н, m/z): Розрах. для C11H14BrN3O2, 300,0 (М+Н), знайJ=5,1Гц), 7,15 (d, 1Н, J=3,7Гц), 7,19 (d, 1Н, дено 300,1. J=3,7Гц), 7,02 (dd, 1H, J=2,8, 9,0Гц), 7,42 (d, 1H, b) 4,4,5,5-Тетраметил-2-(3-метил-тіофен-2-іл)J=5,1Гц), 8,11 (s, 1Н), 8,34 (d, 1H, J=9,0Гц); Мас[1,3,2]діоксаборолан спектр (ESI, m/z): Розрах. для C22H22N4O2S, 407,1 До перемішаного розчину 2-бром-3(М+Н), знайдено 407,1. метилтіофену (337мг, 1,9ммоль) в 8мл THF при Приклад 5 40°С додавали n-BuLi (0,8мл, 2,5М/гексани), та [4-(4-Метил-піперазин-1-іл)-2-(4-метил-тіофенреакційну суміш залишали перемішуватися протя3-іл)-феніл]-амід 5-ціано-фуран-2-карбонової кисгом 30хв. В цей час додавали 2-ізопропоксилоти 4,4,5,5-тетраметил-[1,3,2]діоксаборолан (775мкл, 3,8ммоль) та реакційну суміш залишали нагріватися до температури навколишнього середовища, та перемішування продовжували протягом 1год. Реакційну суміш потім охолоджували до 0°С та гасили насиченим водним NaHCO3 (10мл). Суміш виливали в EtOAc (100мл), промивали Н2О (2x50мл), сушили (Na2SO4) та концентрували у вакуумі. Очищенням залишку за допомогою препаративної тонкошарової хроматографії на силікагелі (20% а) 4,4,5,5-Тетраметил-2-(2-метил-тіофен-3-іл)EtOAc-гексани) одержували 224мг (53%) зазначе[1,3,2]діоксаборолан ної у заголовку сполуки у вигляді масла. 1Н - ЯМP Використовуючи методику, подібну до При(CDCl3; 400МГц): d 1,36 (s, 12Н), 2,5 (s, 3Н), 6,99 (d, кладу 4, стадія (b), 3-бром-4-метилтіофен (571мг, 1Н, J=4,8Гц), 7,50 (d, 1H, J=4,8Гц). 3,2ммоль) обробляли н-BuLi (1,41мл, 2,5М/гексани) та потім піддавали реакції з 2 43 88648 44 ізопропокси-4,4,5,5-тетраметилa) {2-Циклогекс-1-еніл-4-[1-(2,2-диметил[1,3,2]діоксабороланом (775мкл. 3,8ммоль), одер[1,3]діоксан-5-іл)-піперидин-4-іл]-феніл}-амід 4жуючи 189мг (26%) зазначеної у заголовку сполуки ціано-1Н-імідазол-2-карбонової кислоти у вигляді безбарвного масла. 1Н - ЯМP (CDCl3; До суспензії (2-циклогекс-1-еніл-4-піперидин-4іл-феніл)у-аміду 4-ціано-1Н-імідазол-2-карбонової 400МГц): d 1,32 (s, 12H), 2,42 (s, 3Н), 6,90-6,91 (m, кислоти солі трифтороцтової кислоти (81мг, 1H), 7,84 (d, 1Н, J=2,9Гц). 0,16ммоль, яка була одержана в Прикладі 14, стаb) 1-Метил-4-[3-(4-метил-тіофен-3-іл)-4-нітродія (b)) в СН2Сl2 (3мл) додавали NEt3 (33мкл, феніл]-піперазин 0,24ммоль). Розчин потім обробляли 2,2-диметилВикористовуючи методику, подібну до При[1,3]діоксан-5-оном (31мг, 0,24ммоль) та реакційну кладу 4, стадія (с), 1-(3-бром-4-нітро-феніл)-4суміш залишали перемішуватися протягом 3год. В метил-піперазин (162мг, 0,54ммоль), 4,4,5,5цей час однією порцією додавали NaBH(OAc)3 тетраметил-2-(2-метил-тіофен-3-іл)(51мг, 0,24ммоль) та реакційну суміш залишали [1,3,2]діоксаборолан (145мг, 0,64ммоль) та перемішуватися протягом додаткових 4год. РеакPd(PPh3)4 (37мг, 6мол%) піддавали реакції, одерційну суміш розбавляли Н2О (10мл) та екстрагуважуючи 108мг (71%) зазначеної у заголовку сполуки ли EtOАс (2x25мл). Органічні екстракти сушили у вигляді жовтої твердої речовини. 1Н - ЯМР (Na2SO4) та концентрували у вакуумі. Очищенням (CDCl3; 400МГц): d 2,02 (s, 3Н), 2,37 (s, 3Н), 2,55за допомогою препаративної тонкошарової хрома2,57 (m, 4H), 3,42-3,45 (m, 4H), 6,66 (d, 1Н, тографії на силікагелі (10% МеОН-СНСІ3) одержуJ=2,8Гц), 6,87 (s, 1H), 6,99-7,00 (m, 1H), 7,09 (d, 1H, вали 22мг (28%) зазначеної у заголовку сполуки у J=3,2Гц), 8,13 (d, 1H, J=9,2Гц). вигляді не зовсім білої напівтвердої речовини. c) 4-(4-Метил-піперазин-1-іл)-2-(4-метилМас-спектр (ESI, m/z): Розрах. для С28Н35N5O3, тіофен-3-іл)-феніламін 490,2 (М+Н), знайдено 490,6. Використовуючи методику, подібну до Приb) {2-Циклогекс-1-еніл-4-[1-(2-гідрокси-1кладу 4, стадія (d), 1-метил-4-[3-(4-метил-тіофен-3гідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4іл)-4-нітро-феніл]-піперазин (100мг, 0,32ммоль) ціано-1Н-імідазол-2-карбонової кислоти сіль триперемішували з 80мг 5% Pd-C під Н2, одержуючи фтороцтової кислоти 82мг (89%) зазначеної у заголовку сполуки у виДо розчину {2-циклогекс-1-еніл-4-[1-(2,2гляді темного масла, яке негайно використовували диметил-[1,3]діоксан-5-іл)-піперидин-4-іл]-феніл}без додаткового очищення (ESI, m/z): Розрах. для аміду 4-ціано-1Н-імідазол-2-карбонової кислоти C16H21N3S, 288,15 (М+Н), знайдено 288,1. (22мг, 0,04ммоль, який був одержаний на попереd) [4-(4-метил-піперазин-1-іл)-2-(4-метилдній стадії) в THF-H2O (1мл, 4:1 об/об) додавали тіофен-3-іл)-феніл]-амід 5-ціано-фуран-2TFA (0,4мл), та реакційну суміш залишали перекарбонової кислоти мішуватися протягом 1год. Розчинник видаляли Використовуючи методику, подібну до Припід вакуумом, одержуючи 14мг (60%) зазначеної у кладу 9, стадія (с), 5-ціано-фуран-2-карбоніл хлозаголовку сполуки у вигляді бурштинової піни. 1Н рид (64мг, 0,41ммоль, який був одержаний в ПриЯМP (CD3OD, 400МГц): d 1,78-1,90 (m, 4H), 2,03кладі 9, стадія (с)) піддавали реакції з 4-(4-метил2,16 (m, 3Н), 2,29 (br s, 4H), 2,88-2,96 (m, 1H), 3,37піперазин-1-іл)-2-(4-метил-тіофен-3-іл)3,40 (m, 1Н), 3,46-3,53 (m, 2H), 3,74-3,78 (m, 3H), феніламіном (80мг, 0,27ммоль, який був одержа5,83 (s, 1H), 7,13 (d, 1H, J=2,0Гц), 7,22 (dd, 1H, ний на попередній стадії) в присутності DIEA J=2,0, 8,4Гц), 8,03 (s, 1Н), 8.17 (d, 1Н, J=8,4Гц); (0,10мл, 0,59ммоль), одержуючи 25,8мг (24%) заМас-спектр (ESI, m/z): Розрах. для C25H31N5O3, значеної у заголовку сполуки у вигляді жовтої тве450,2 (М+Н), знайдено 450,2. рдої речовини. 1Н - ЯМP (CDCl3; 400МГц): d 2,09 Приклад 7 (s, 3Н), 2,37 (s, 3Н), 2,59-2,60 (m, 4H), 3,24-3,26 (m, {2-Циклогекс-1-еніл-4-[1-(2-морфолін-4-іл4H), 6,83 (d, 1Н, J=2,9Гц), 6,98-7,06 (m, 2H), 7,14ацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н7,21 (m, 3H), 7,96 (s, 1H), 8,32 (d, 1H, J=9,0Гц). імідазол-2-карбонової кислоти Мас-спектр (ESI, m/z): Розрах. для C22H22N4O2S, 407,1 (М+Н), знайдено 407,1. Приклад 6 {2-Циклогекс-1-еніл-4-[1-(2-гідрокси-1гідроксиметил-етил)-піперидин-4-іл]-феніл}-амід 4ціано-1Н-імідизол-2-карбонової кислоти сіль трифтороцтової кислоти До розчину етилового ефіру морфолін-4-ілоцтової кислоти (117мг, 0,67ммоль) в етанолі (4мл) через шприц додавали 6N KOH (110мкл, 0,67ммоль) та перемішування продовжували протягом 3год. Концентруванням у вакуумі одержували 122мг (100%) калієвої солі морфолін-4-ілоцтової кислоти. До суміш калієвої солі морфолін4-іл-оцтової кислоти (29мг, 0,15ммоль), (2 45 88648 46 циклогекс-1-еніл-4-піперидин-4-іл-феніл)-амід 4ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти (65,1мг, 0,13ммоль, яка була одержана в Прикладі 14, стадія (b)) та РуВrоР (93мг, 0,19ммоль) в СН2Сl2 (4мл) додавали DIEA (51мкл, 0,29ммоль) та реакційну суміш залишали перемішуватися протягом ночі. Реакційну суміш розбавляли СН2Сl2 (50мл), промивали Н2О (2x25мл), сушили (Na2SO4) та концентрували у вакуумі. Очищенням неочищеного продукту за а) 1-(3-Бром-4-нітро-феніл)-4-метил-піперазин допомогою препаративної ТШХ на силікагелі одержували 8,1мг (12%) зазначеної у заголовку сполуки у вигляді білої твердої речовини. 1Н - ЯМP (CDCl3; 400МГц): d 1,68-2,04 (m, 5H), 2,20-2,29 (m, 4H), 2,53-2,78 (m, 5H), 3,09-3,23 (m, 6H), 3,35-3,40 (m, 1Н), 3,72 (br s, 4H), 4,16-4,22 (m, 1Н), 4,73-4,77 (m, 1Н), 5,82 (s, 1Н), 7,00 (s, 1H), 7,12 (dd, 1H, J=0,6, 8,0Гц), 7,73 (s, 1Н), 8,27 (d, 1Н, J=8,1Гц), До охолодженого (0°С) розчину 1,00г 9,48 (s, 1H); Мас-спектр (ESI, m/z): Розрах. для (4,55ммоль) 2-бром-4-фторнітробензолу C28H34N6O3, 503,27 (M+H), знайдено 503,1. (Oakwood) в 12мл EtOH додавали 1,52мл Приклад 8 (13,7ммоль) піперидину. Розчин перемішували при {2-Циклогекс-1-еніл-4-[1-(3-морфолін-4-іл0°С протягом 0,5год та потім при 60°С протягом пропіоніл-)-піперидин-4-іл]-феніл}-амід 4-ціано-1Н4год. Суміш концентрували у вакуумі, розчиняли в імідазол-2-карбонової кислоти EtOАс (60мл), промивали водою (3x100мл) та сольовим розчином (100мл), та сушили (Na2SO4). Концентруванням у вакуумі та хроматографуванням на 50-г SPE колонці з силікагелем 1-3% МеОН-дихлорметан одержували 1,06г (77%) зазначеної у заголовку сполуки у вигляді жовтокоричневатої твердої речовини. Мас-спектр (ESI, m/z): Розрах. для С11Н14ВrN3O2, 300,0 (М+Н, 79Вr), знайдено 300,1. b) 1-Метил-4-(2'-метил-6-нітро-біфеніл-3-іл)піперазин До колби, що містить калієву сіль 3-морфолін4-іл-пропіонової кислоти (94мг, 0,47ммоль, одержаної з етилового ефіру 3-морфолін-4-ілпропіонової кислоти точно, як описано в Прикладі 7), (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти (179мг, 0,36ммоль, яка була одержана в Прикладі 14 (b)), EDCI (83мг, 0,43ммоль) та НОВТ (68мг, 0,5ммоль), додавали DMF (4мл). До перемішаної суспензії додавали DIEA (157мкл, 0,9ммоль) та реакційну суміш залишали перемішуватися протягом ночі. Реакційну суміш розбавляли Н2О (10мл) та екстрагували EtOАс (2x25мл). Об'єднані органічні екстракти сушили (Na2SO4), концентрували у вакуумі та неочищений продукт очищали за допомогою препаративної ТШХ на силікагелі, одержуючи 10,4мг (6%) зазначеної у заголовку сполуки у вигляді білої твердої речовини. 1Н - ЯМP (CDCl3; 400МГц): d 1,49-1,93 (m, 5H), 2,22-2,31 (m, 3Н), 2,52 (br s, 4H), 2,58-2,63 (m, 3H), 2,74-2,76 (m, 4H), 3,10-3,17 (m , 2H), 3,72 (br s, 4H), 3,97-4,02 (m, 2H), 4,76-4,81 (m ,2H), 5,81-5,82 (m, 1H), 6,81-6,82 (m, 1H), 6,99-7,00 (m, 1H), 7,09-7,13 (m, 1H), 7,70 (s, 1Н), 8,26 (d, 1Н, J=8,2Гц), 9,51 (s, 1H); Мас-спектр (ESI, m/z): Розрах. для C29H36N6O3, 517,28 M+H), знайдено 517,3. Приклад 9 [2'-метил-5-(4-метил-піперазин-1-іл)-біфеніл-2іл]-амід 5-ціано-фуран-2-карбонової кислоти До суміші 200мг (0,666ммоль) 1-(3-бром-4нітро-феніл)-4-метил-піперазину (який був одержаний на попередній стадії), 136мг (0,999ммоль) та 77,0мг (0,0666ммоль) тетракіс(трифенілфосфін)паладію (0) під Ar додавали 4,0мл дегазованого диметоксіетану (DME) та 400мкл (0,799ммоль) 2,0Μ водного Na2CO3. Суміш нагрівали з перемішуванням під Ar при 80°С протягом 14год. Охолоджену (RT) суміш концентрували та хроматографували на 10-г SPE колонці з силікагелем 1-5% МеОН в дихлорметан-гексан (1:1). Фракції продукту обробляли 80мг знебарвлюючого вугілля, фільтрували, концентрували та потім повторно хроматографували на такій же колонці 1-3% EtOH-дихлорметан, одержуючи 265мг зазначеної у заголовку сполуки у вигляді жовтої смоли (75% чистоти, визначено за допомогою 1НЯМР, у вигляді суміші з трифенілфосфіном), яку використовували в наступній реакції без додаткового очищення: Мас-спектр (ESI, m/z): Розрах. для C11H21N3O3, 312,2 (М+Н), знайдено 312,2. 47 88648 с) [2'-Метил-5-(4-метил-піперазин-1-іл)біфеніл-2-іл]-амід 5-ціано-фуран-2-карбонової кислоти 48 a) 1-(2'-Фтор-6-нітро-біфеніл-3-іл)-4-метилпіперазин Суміш 140мг (0,337ммоль, базуючись на чистоті 75%) 1-метил-4-(2'-метил-6-нітро-біфеніл-3-іл)піперазину (який був одержаний на попередній стадії) та 70мг 10 % паладію на вугіллі (Degussa type E101-NE/W, Aldrich, 50% на масу води) в 5мл THF енергійно перемішували під воднем (балон) протягом 1год. Суміш фільтрували (целіт). промивали дихлорметаном (2x2мл) та розчин одержаного аніліну поміщали під Ar та негайно використовували в наступній реакції. Одночасно з наведеним вище відновленням, 55,4мг (0,404ммоль) 5-ціанофуран-2-карбонової кислоти (яка була одержана в Прикладі 1) в 2,5мл безводного дихлорметану в пробірці, яку сушили під CaSO4, обробляли 52,9мкл (0,606ммоль) оксаліл хлориду, потім 10мкл безводного DMF. Розчин перемішували протягом 25хв та швидко концентрували у вакуумі при 20-25°С. Одержаний 5-ціанофуран-2-карбоніл хлорид поміщали у високий вакуум на 2-3хв та потім негайно поміщали під Ar, охолоджували до 0°С на льодяній бані та обробляли розчином аніліну, одержаним вище, потім обробляли 141мкл (0,808ммоль) Ν,Νдіізопропілетиламіну (DIEA). Після перемішування протягом 30хв при RT, суміш концентрували у вакуумі та отриманий залишок хроматографували на 20-г SPE колонці з силікагелем з 2-10% EtOHдихлорметан, одержуючи жовту смолу (яку кристалізували з EtOAc-гексан), одержуючи 17,2мг (13 %) чистої зазначеної у заголовку сполуки у вигляді жовтої твердої речовини разом з 70,3мг неочищеної зазначеної у заголовку сполуки. Неочищену фракцію розчиняли в 50мл EtOАс, промивали насиченим водним NaHCO3-1Μ K2СО3 (11, 2x20мл) та сольовим розчином (20мл), сушили (Na2SO4) та концентрували, одержуючи додаткові 43,4мг (32 %) зазначеної у заголовку сполуки у вигляді кристалічної жовтої твердої речовини (загальний вихід 45%). 1Н - ЯМP (CDCl3; 400МГц): d 8,32 (d. 1H, J=9,0Гц), 7,73 (br s, 1H), 7,34-7,54 (m, 3H), 7,25 (d, 1H, J=7,7Гц), 7,12, 7,14 (AB q, 2H, J=3,7Гц), 7,01 (dd, 1H, J=9,0, 2,8Гц), 3,25-3,27 (m, 4H), 2,59-2,62 (m, 4H), 2,38 (s, 3H) та 2,15 (s, 3H). Мас-спектр (ESI, m/z): Розрах. для C21H24N4O3, 401,2 (M+H), знайдено 401,1. Приклад 10 [2'-Фтор-5-(4-метил-піперазин-1-іл)-біфеніл-2іл]-амід 5-ціано-фуран-2-карбонової кислоти Слідували методиці Прикладу 9, стадія (b), використовуючи 75,0мг (0,250ммоль) 1-(3-бром-4нітро-феніл)-4-метил-піперазину (який був одержаний в Прикладі 9, стадія (а)), 136мг (0,999ммоль) 2-фторфенілборонову кислоту, 26,8мг (0,0232ммоль) тетракіс(трифенілфосфін)паладію (0) та 400мкл (0,799ммоль) 2,0Μ водного Na2CO3 в DME, за винятком того, що суміш нагрівали протягом 22год. Хроматографією на 5-г SPE колонці з силікагелем 1-5% МеОН в дихлорметан-гексан (1:1) одержували 95,0мг зазначеної у заголовку сполуки (76% чистоти, визначено за допомогою 1Н-ЯМР, у вигляді суміші з трифенілфосфіном) у вигляді жовтої смоли, яку використовували в наступній реакції без додаткового очищення. Мас-спектр (ESI, m/z): Розрах для C17H18FN3O3, 316,1 (М+Н), знайдено 316,2. b) [2'-Фтор-5-(4-метил-піперазин-1-іл)-біфеніл2-іл]-амід 5-ціано-фуран-2-карбонової кислоти Слідували методиці Прикладу 9, стадія (с), використовуючи 93,2мг (0,225ммоль, базуючись на чистоті 76%) 1-(2'-фтор-6-нітро-біфеніл-3-іл)-4метил-піперазину (який був одержаний на попередній стадії), 46мг 10% паладію на вугіллі, 37,0мг (0,270ммоль) 5-ціанофуран-2-карбонової кислоти (яка була одержана в Прикладі 1), 35,3мкл (0,405ммоль) оксаліл хлориду, 5,0мкл безводного DMF та 94,1мкл (0,540ммоль) DIEA. Хроматографією на 5-г SPE колонці з силікагелем 1-4% МеОН-дихлорметан одержували 69,8мг (77%) зазначеної у заголовку сполуки у вигляді жовтої смоли. 1 Н - ЯМP (CDCl3; 400МГц): d 8,04 (d, 1H, J=9,0Гц), 7,93 (br s, 1H), 7,434-7,48 (m, 1H), 7,37 (td, 1H, J=7,5, 1,8Гц), 7,22-7,31 (m, 2H), 7,13, 7,18 (AB q, 2H, J=3,7Гц), 7,02 (dd, 1H, J=9,0, 2,9Гц), 6,88 (d, 1H, J=2,9Гц), 3,24-3,27 (m, 4H), 2,57-2,60 (m, 4H) та 49 88648 50 2,36 (s, 3H). Мас-спектр (ESI, m/z): Розрах. для додаткових 83,8мг (1,50ммоль) порошкоподібного C23H21FN4O2, 405,2 (M+H), знайдено 405,2. заліза та суміш кип'ятили зі зворотним холодильПриклад 11 ником протягом 1год. Суміш виливали в EtOАс [2-Циклогекс-1-еніл-4-(4-метил-піперазип-1-іл)(12мл), фільтрували (целіт), промивали EtOАс феніл]-амід 5-ціано-фуран-2-карбонової кислоти (2x4мл), концентрували у вакуумі та розчиняли в безводному THF (4,0мл). Одержаний розчин аніліну поміщали під Ar та негайно використовували в наступній реакції. 61,6мг (0,449ммоль) 5-ціанофуран-2карбонової кислоти (яка була одержана в Прикладі 1) в 2,5мл безводного дихлорметану в пробірці, яку сушили CaSO4, обробляли 60,0мкл (0,688ммоль) оксаліл хлориду, потім 10мкл безводного DMF. Розчин перемішували протягом 25хв та швидко концентрували у вакуумі при 20-25°С. а) 1-(3-Циклогекс-1-еніл-4-нітро-феніл)-4Залишок помішали під високий вакуум на 2-3хв та метил-піперазин потім негайно поміщали під Ar, охолоджували до 0°С на льодяній бані та обробляли розчином аніліну, який був одержаний вище, потім обробляли 104мкл (0,598ммоль) DIEA. Після перемішування протягом 30хв при RT, суміш концентрували у вакуумі, розчиняли EtOAc (20мл), промивали 1Μ K2СО3 (2x10мл) та сольовим розчином (10мл), сушили (Na2SO4) та концентрували у вакуумі. Одержаний залишок хроматографували на 10-г SPE колонці з силікагелем 1-4% МеОНСуміш 102мг (0,340ммоль) 1-(3-бром-4-нітродихлорметан, одержуючи жовту смолу, яку потім феніл)-4-метил-піперазину (який був одержаний в кристалізували з Еt2О-гексан, одержуючи 84,7мг Прикладі 9, стадія (а)), 59,7 циклогексен-1(72%) зазначеної у заголовку сполуки у вигляді ілборонової кислоти мг (0,474ммоль), 43,8мг кристалічної жовтої твердої речовини. 1Н - ЯМP (0,0379ммоль) тетракіс(трифенілфосфін)паладію (CDCl3; 400МГц): d 8,57 (br s, 1Н), 8,26 (d, 1H, (0) під Ar обробляли 206мкл (0,412ммоль) 2,0Μ J=9,0Гц), 7,20, 7,23 (AB q, 2H, J=3,7Гц), 6,86 (dd, дегазованого водного Na2CO3, 0,6мл дегазованого 1H, J=9,0, 2,9Гц), 6,74 (d, 1H, J=2,9Гц), 5,84-5,85 безводного толуолу та 0,2мл дегазованого безво(m, 1H), 3,20-3,22 (m, 4H), 2,57-2,59 (m, 4H), 2.36 дного EtOH та суміш нагрівали при 100°С протягом (s, 3Н), 2,23-2,30 (m, 4H) та 1,79-1,84 (m, 4H). Мас21год. Після охолодження до RT, суміш виливали спектр (ESI, m/z): Розрах. для C23H26N4O2, 391,2 в EtOАс (10мл), промивали сольовим розчином (M+H), знайдено 391,2. (10мл), сушили (Na2SO4) та концентрували у вакуПриклад 12 умі. Хроматографією на 5-г SPE колонці з силіка[2-(3,6-Дигідро-2Н-піран-4-іл)-4-(4-метилгелем 1-3% EtOH в дихлорметані одержували піперазин-1-іл)-феніл-амід 5-ціано-фуран-2126мг зазначеної у заголовку сполуки (чистота карбонової кислоти 74%, визначено за допомогою ОФ-ВЕРХ (колонка С18), у вигляді суміші з трифенілфосфіном) у вигляді жовтого масла, яке використовували в наступній реакції без додаткового очищення. Масспектр (ESI, m/z): Розрах. для C17H23N3O3, 302,2 (М+Н), знайдено 302,2. b) [2-Циклогекс-1-еніл-4-(4-метил-піперазин-1іл)-феніл]-амід 5-ціано-фуран-2-карбонової кислоти а) 1-[3-(3,6-Дигідро-2Н-піран-4-іл)-4-нітрофеніл]-4-метил-піперазин До 122мг (0,299ммоль, базуючись на чистоті 74%) 1-(3-циклогекс-1-еніл-4-нітро-феніл)-4-метилпіперазину (який був одержаний на попередній стадії) в 5,0мл EtOH-вода (2:1) додавали 83,8мг (1,50ммоль) порошкоподібного заліза та 160мг (2,99ммоль) NH4Cl та суміш кип'ятили зі зворотним холодильником під Ar протягом 12год. Додавали 1-(3-Бром-4-нітро-феніл)-4-метил-піперазин (який був одержаний в Прикладі 9, стадія (а)) (225,1мг, 0,79ммоль), K2СО3 (310,9мг, 2,25ммоль) та 4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл) 51 88648 52 3,6-дигідро-2Н-піран [Murata, Μ., et al, Synthesis, 778, (2000)] (157мг, 0,75ммоль) в діоксані (5мл) нагрівали при 80°С протягом ночі під Ar. Реакційну суміш залишали охолоджуватися до RT, концентрували та одержаний залишок хроматографували на силікагелі (10% EtOАс/гексан - 20% МеОН/EtOAc), одержуючи зазначену у заголовку сполуку (82мг, 36%). 1Н - ЯМP (CDCl3; 400МГц): d 8,04 (d, 1H, J=9,4Гц), 6,78 (dd, 1H, J=9,4, 2,6Гц), 6,58 (m, 1H, J=2,6Гц), 5,58 (m, 1H), 4,34 (m, 2H), 3,95 (t, 2H, Зазначену у заголовку сполуку одержували J=5,3Гц), 3,46 (m, 4H), 2,57 (m, 4H), 2.38 (s, 3H), сполученням Сузукі 4-(4,4,5,5-тетраметил2,30 (m, 2H) [1,3,2]діоксаборолан-2-іл)-феніламіну з третb) [2-(3,6-Дигідро-2Н-піран-4-іл)-4-(4-метилбутиловим ефіром 4-трифторметансульфонілоксипіперазип-1-іл)-феніл-амід 5-ціано-фуран-23,6-дигідро-2Н-піридин-1-карбонової кислоти карбонової кислоти [Synthesis, 993, (1991)] відповідно до методики, наведеної в Прикладі 35, стадія (b). Мас-спектр (ES1, m/z): Розрах. для С16Н22N2О2, 275,2 (М+Н), знайдено 275,1. b) трет-Бутиловий ефір 4-(4-аміно-феніл)піперидин-1-карбонової кислоти 1-[3-(3,6-Дигідро-2Н-піран-4-іл)-4-нітро-феніл]4-метил-піперазин (який був одержаний на попередній стадії) (80мг, 0,26ммоль) перетворювали на відповідний амін, використовуючи методику, подібну до Прикладу 4, стадія (d), та піддавали сполученю з 5-ціано-фуран-2-карбоніл хлоридом, який був одержаний в Прикладі 9, стадія (с) (отриманий з 137мг, 1,00ммоль 5-ціано-фуран-2-карбонової кислоти, яка була одержана в Прикладі 1) в СН2Сl2 (2мл) при 0°С. Продукт виділяли за допомогою флеш хроматографії на силікагелі (50% EtOAc/гексан - 10% МеОН/EtOAc), одержуючи зазначену у заголовку сполуку (62,2мг, 60%) 1Н ЯМP (CDCl3; 400МГц): d 8,35 (br s, 1H), 8,12 (d, 1H each, J=8,76Гц), 7,24 (d, 1H, J=5,08Гц), 7,19 (d, 1H, J=5,08Гц), 6,88 (dd, 1H, J=8,76, 2,7Гц), 6,73 (d, 1H, J=2,7Гц), 5,88 (br s, 1H), 4,34 (m, 2H), 3,94 (t, 2H, J=5,3Гц), 3,23 (m, 4H), 2,59 (m, 4H), 2,38 (br s, 5H). PX-MC (ESI, m/z): Розрах. для C22H24N4O3, 393,1 (M+H), знайдено 393,2. Приклад 13 (2-Циклогекс-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-пірол-2-карбонової кислоти сіль трифтороцтової кислоти а) трет-Бутиловий ефір 4-(4-аміно-феніл)-3,6дигідро-2Н-піридин-1-карбонової кислоти Розчин трет-бутилового ефіру 4-(4-амінофеніл)-3,6-дигідро-2Н-піридин-1-карбонової кислоти (0,35г, 1,2ммоль) (який був одержаний на попередній стадії) в метанолі гідрогенізували понад 10% Pd/C при 20фунт/дюйм2 протягом 1год. Розчин фільтрували та концентрували, одержуючи 0,35г (100%) зазначеної у заголовку сполуки у вигляді жовтої твердої речовини: Мас-спектр (ESI, m/z): Розрах. для C16H24N2O2, 277,2 (М+Н), знайдено 277,1. c) трет-Бутиловий ефір 4-(4-аміно-3-бромфеніл)-піперидин-1-карбонової кислоти До розчину трет-бутилового ефіру 4-(4-амінофеніл)-піперидин-1-карбонової кислоти (0,20г, 0,71ммоль) (який був одержаний на попередній стадії) в DCM (3мл) додавали N-бромсукцинімід (NBS) (0,13г, 0,71ммоль) та реакційну суміш перемішували при RT протягом 10год. Реакційну суміш розбавляли EtOAc (10мл) та промивали NaHCO4 (2x10мл) та сольовим розчином (10мл). Концентруванням органічного шару одержували 0,26г (100%) зазначеної у заголовку сполуки у вигляді 53 88648 жовтої піни Мас-спектр (ESI, m/z): Розрах. для C16H23BrN2O2, 355,1 (М+Н), знайдено 355,1. d) трет-Бутиловий ефір 4-(4-аміно-3-циклогекс1-еніл-феніл)-піперидин-1-карбонової кислоти 54 а) трет-Бутиловий ефір 4-(4-{[4-ціано-1-(2триметилсиланіл-етоксиметил)-1Н-імідазол-2карбоніл]-аміно}-3-циклогекс-1-еніл-феніл)піперидин-1-карбонової кислоти В колбу поміщали трет-бутиловий ефір 4-(4аміно-3-бром-феніл)-піперидин-1-карбонової кислоти (0,13г, 0,36ммоль) (який був одержаний на попередній стадії), циклогекс-1-енілборонову кислоту (0,060г, 0,48ммоль), Pd(PPh3)4 (0,04г, 10мол%), водний 2Μ Na2CO3 (1,5мл), етанол (1,5мл) та толуол (3мл) та нагрівали при 80°С протягом 3год. Реакційну суміш розбавляли EtOАс (10мл), промивали NaHCO3 (2x10мл) та сольовим розчином (10мл), та органічний шар сушили над Na2SO4 та потім концентрували. Зазначену у заголовку сполуку елюювали з 20-г SPE картриджу (силікагель) 30% EtOАс/гексан, одержуючи 0,10г (85%) зазначеної у заголовку сполуки у вигляді жовтого масла. Мас-спектр (ESI, m/z): Розрах. для С22Н32N2О2, 357,2 (М+Н), знайдено 357,1. e) (2-Циклогекс-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-пірол-2-карбонової кислоти сіль трифтороцтової кислоти В колбу поміщали трет-бутиловий ефір 4-(4аміно-3-циклогекс-1-еніл-феніл)-піперидин-1карбонової кислоти (0,050г, 0,14ммоль) (який був одержаний на попередній стадії), 4-ціано-1Н-пірол2-карбонову кислоту (0,019г, 0,14ммоль) (яка була одержана в Прикладі 2), EDCI (0,040г, 0,21ммоль), HOBt (0,019г, 0,14ммоль), DIEA (0,073мл, 0,42ммоль) та DCM (0,5мл) та перемішували при 25°С протягом 10год. Реакційну суміш завантажували безпосередньо на 10-г картридж (силікагель) для твердо-фазової екстракції (SPE) та одержану проміжну сполуку елюювали 30% EtOAc/гексан. Цю сполуку перемішували при RT протягом 1год в 50% TFA/DCM (2мл) та потім концентрували та очищали за допомогою ОФ-ВЕРХ (С18), елююючи 30-50% CH3CN в 0,1% TFA/Н2О протягом 12хв, одержуючи зазначену у заголовку сполуку (0,052г, 77%). 1Н - ЯМP (400МГц, CD3OD): d 7,59 (s, 1H), 7,50 (d, 1H), 7,22 (d, 1H), 7,16 (m, 2H), 5,74 (m, 1Н), 3,54, (m, 2H), 3,16 (m. 2H), 2,94 (m, 1H), 2,29 (m, 2H), 2,15 (m, 4H), 1,92 (m, 2H), 1,72 (m, 4H). Масспектр (ESI, m/z): Розрах. для C23H26N4O, 375,2 (М+Н), знайдено 375,1. Приклад 14 (2-Циклогекс-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти До розчину калієвої солі 4-ціано-1-(2триметилсиланіл-етоксиметил)-1Н-імідазол-2карбоксилату (3,34г, 10,9ммоль) (який був одержаний в Прикладі 3, стадія (d)) в 20мл DCM додавали DIEA (3,8мл, 21,8ммоль) та PyBroP (5,6г, 12,0ммоль) та реакційну суміш перемішували при 25°С протягом 15хв. Додавали розчин третбутилового ефіру 4-(4-аміно-3-циклогекс-1-енілфеніл)-піперидин-1-карбонової кислоти (3,9г, 10,9ммоль) (який був одержаний в Прикладі 13, стадія (d)) в 10мл DCM та реакційну суміш перемішували протягом 8год при 25°С. Реакційну суміш розбавляли EtOАс (60мл) та промивали NaHCO3 (2x60мл) та сольовим розчином (100мл) та органічний шар сушили над Na2SO4 і потім концентрували. Зазначену у заголовку сполуку очищали за допомогою флеш хроматографії (силікагель, 2% EtOAc/DCM), одержуючи 5,5г (85%) зазначеної у заголовку сполуки у вигляді жовтого масла. Мас-спектр (ESI, m/z): Розрах для C33H47N5O4Si, 606,2 (М+Н), знайдено 606,2. b) (2-Циклогекс-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти До розчину трет-бутилового ефіру 4-(4-{[4ціано-1-(2-триметилсиланіл-етоксиметил)-1Німідазол-2-карбоніл]-аміно}-3-циклогекс-1-енілфеніл)-піперидин-1-карбонової кислоти (1,5г, 2,5ммоль) (який був одержаний на попередній стадії) в 10мл DCM та 0,3мл EtOH додавали 3мл TFA та розчин перемішували протягом 3год при 25°С. Реакційну суміш розбавляли 5мл EtOH та потім концентрували. Залишок кристалізували з метанолу та етилового ефіру, одержуючи 0,85г (70%) зазначеної у заголовку сполуки у вигляді білої твердої речовини. 1Н - ЯМP (400МГц, CD3OD) d 8,18 (d, 1H), 8,04 (s, 1H), 7,22 (dd, 1H), 7,12 (d, 1H), 5,76 (m, 1H), 3,54, (m, 2H), 3,16 (m, 2H), 2,92 (m, 1H), 2,30 (m, 4H), 2,10 (m, 2H), 1,75 (m, 6H). 55 88648 Мас-спектр (ESI, m/z): Розрах. для C22H25N5O, 376.2 (M+H), знайдено 376,2. Приклад 15 [4-(1-Ацетил-піперидин-4-іл)-2-циклогекс-1еніл-феніл]-амід 4-ціано-1Н-пірол-2-карбонової кислоти Зазначена у заголовку сполука була одержана з (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-аміду 4-ціано-1Н-пірол-2-карбонової кислоти солі трифтороцтової кислоти (яка була одержана в Прикладі 13, стадія (e)) відповідно до методики, наведеної в Прикладі 37. 1Н - ЯМP (400МГц, CDCl3) d 10,82 (s, 1Н), 8,28 (d, 1Н), 8,18 (s, 1Н), 7,48 (d, 1H), 7,16 (dd, 1H), 7,02 (s, 1H), 6,72 (s, 1H), 5,88 (m, 1H), 4,82 (m, 1H), 3,98. (m, 1H), 3,20 (m, 1H), 2,70 (m, 2H), 2,29 (m, 4H), 2,18 (s, 3H), 1,80 (m, 8Η). Масспектр (ESI, m/z): Розрах. для C25H28N4O2, 417,2 (M+H), знайдено 417,1. Приклад 16 [4-(1-Ацетил-піперидин-4-іл)-2-циклогекс-1еніл-феніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти Зазначена у заголовку сполука була одержана з (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-аміду 4-ціано-1Н-імідазол-2-карбонової кислоти солі трифтороцтової кислоти (яка була одержана в Прикладі 13, стадія (b)) відповідно до методики, наведеної в Прикладі 37: 1Н - ЯМP (400МГц, CDCl3) d 13,12 (br s, 1H), 9,58 (s, 1H), 8,34 (d, 1H), 7,76 (s, 1H), 7,21 (dd, 1Н), 7,05 (d, 1H), 5,86 (s, 1H), 4,84 (m, 2H), 4,00 (m, 1Н), 3,22 (m, 1H), 2,72 (m, 2H), 2,30 (m, 4H), 2,21 (s, 3H), 1,80 (m, 8H). Масспектр (ESI, m/z): Розрах. для C24H27N5O2, 418,2 (M+H), знайдено 418,1. Приклад 17 [2-(4-Метил-циклогекс-1-еніл)-4-піперидин-4-ілфеніл]-амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти 56 Зазначена у заголовку сполука була одержана з калієвої солі 4-ціано-1-(2-триметилсиланілетоксиметил)-1Н-імідазол-2-карбоксилату (яка була одержана в Прикладі 3, стадія (d)) та третбутилового ефіру 4-[4-аміно-3-(4-метил-циклогекс1-еніл)-феніл]-піперидин-1-карбонової кислоти (одержаного відповідно до методики, наведеної в Прикладі 13, стадія (d), замінюючи циклогекс-1енілборонову кислоту на 4-метил-1-циклогекс-1енілборонову кислоту) відповідно до методики для Прикладу 14: 1Н - ЯМP (400МГц, CD3OD): d 8,18 (d, 1Н), 8,04 (s, 1H), 7,22 (dd, 1H), 7,12 (d, 1H), 5,80 (m, 1H), 3,54 (m, 2H), 3,18 (m, 2H), 2,94 (m, 1H), 2,30 (m, 3H), 2,12 (m, 2H), 1,92 (m, 5H), 1,54 (m, 1H), 1,12 (d, 3H). Мас-спектр (ESI, m/z): Розрах. для C23H27N5O, 390,2 (M+H), знайдено 390,2. Приклад 18 (2-Циклопент-1-еніл-4-піперидин-4-іл-феніл)амід 4-ціано-1Н-імідазол-2-карбонової кислоти сіль трифтороцтової кислоти Зазначена у заголовку сполука була одержана з калієвої солі 4-ціано-1-(2-триметилсиланілетоксиметил)-1Н-імідазол-2-карбоксилату (який був одержаний в Прикладі 3, стадія (d)) та третбутилового ефіру 4-(4-аміно-3-циклопент-1-енілфеніл)-піперидин-1-карбонової кислоти (одержаного відповідно до методики, наведеної в Прикладі 13, стадія (d), замінюючи циклогекс-1енілборонову кислоту на циклопентен-1ілборонову кислоту) відповідно до методики для Прикладу 14. 1Н - ЯМP (400МГц, DMSO-d6) d 14,25 (br s, 1H), 10,00 (s, 1H), 8,36 (s, 1Н), 7,72 (d, 1Н), 7,18 (m, 2H), 6,06 (s, 1H), 4,12 (m, 1Н), 3,42 (m, 2H). 3,18 (m, 2H), 3,00 (m, 3H), 2,80 (m, 2H), 1,92 (m, 5Н). Мас-спектр (ESI, m/z): Розрах. для С21Н23N5O, 362,2 (M+H), знайдено 362,2. Приклад 19 Альтернативний спосіб синтезу проміжної сполуки, описаного в Прикладі 1, описаний нижче. 5-Ціано-фуран-2-карбонова кислота 57 250-мл тригорлу круглодонну колбу, постачену механічною мішалкою, кожухом нагрівання та конденсатором, наповнювали 5-форміл-2фуранкарбоновою кислотою (9,18г, 65,6ммоль) та піридином (60мл). Додавали гідрохлорид гідроксиламіну (5,01г, 72,2ммоль) та суміш нагрівали до 85°С. Додавали оцтовий ангідрид (40мл) та реакційну суміш перемішували при 85°С протягом 3год, після чого розчинник випарювали при 40°С під зниженим тиском. Залишок розчиняли у воді, підлужували 2,0N розчином NaOH до рН 9 та екстрагували 41 дихлорметан/2-пропанол, поки піридин не буде повністю видалений (5x200мл) Водний розчин потім підкислювали 2,0N розчином НCl до рН 2, насичували твердим NaCl та екстрагували 4:1 дихлорметан/2-пропанол (5x200мл). Об'єднані органічні екстракти сушили над Na2SO4 та концентрували у вакуумі насухо. Залишок кристалізували з дихлорметану, одержуючи 6,80г зазначеної у заголовку сполуки у вигляді білої твердої речовини (76%). Мас-спектр (ESl-нег, m/z): Розрах. для С6Н3NО3, 136,0 (М-Н), знайдено 136,1. Спектр 1Η ЯМР узгоджувався з встановленою структурою. Приклад 20 {2-Циклогекс-1-еніл-4-{1-(2-метансульфонілацетил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Німідазол-2-карбонової кислоти В колбу помішали метансульфоніл-оцтову кислоту (14мг, 0,10ммоль), EDCl (30мг, 0,15ммоль), HOBt (14мг, 0,10ммоль), DIEA (36мкл, 0,20ммоль) та 0,5мл DCM та перемішували при 25°С. Через 10хв додавали розчин, що містить (2-циклогекс-1еніл-4-піперидин-4-іл-феніл)-амід 4-ціано-1Німідазол-2-карбонової кислоти сіль TFA (40мг, 0,08ммоль) (яка була одержана в Прикладі 20, стадія (b)) та NEt3 (14мкл, 0,09ммоль) в 0,5мл DCM та реакційну суміш витримували протягом 10год при 25°С. Реакційну суміш завантажували на 5-г SPE картридж (силікагель) та зазначену у заголовку сполуку елюювали 10% EtOH/EtOAc, одержуючи 10мг (25%) білої твердої речовини. 1Н - ЯМP (400МГц, CDCl3): d 11,60 (br s, 1H), 9,52 (s, 1H), 8,30 (d, 1H), 7,74 (s, 1H), 7,60 (dd, 1H), 7,03 (d, 1H), 5,86 (m, 1Н), 4,84 (m, 1H), 4,18 (s, 2H), 4,12 (m, 1H), 3,32 (m, 1H), 3,20 (s, 3H), 2,82 (m, 2H), 2,30 (m, 4H), 1,98 (m, 2H), 1,84 (m, 5H), 1,72 (m, 1H). Мас-спектр (ESI, m/z): Розрах. для C25H29N5O4S, 496,2 (M+H), знайдено 496,2. Приклад 21 [2-Циклогекс-1-еніл-4-(1-піридин-2-ілметилпіперидин-4-іл)-феніл]-амід 4-ціано-1Н-імідазол-2карбонової кислоти сіль трифтороцтової кислоти 88648 58 В колбу поміщали (2-циклогекс-1-еніл-4піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2карбоновоі кислоти сіль TFA (88мг, 0,18ммоль) (яка була одержана в Прикладі 14, стадія (b)), піридин-2-карбальдегід (17мкл, 0,21ммоль), Net3 (30мкл, 0,21ммоль), триацетоксиборгідрид натрію (56мг, 0,25ммоль) та 0,8мл 1,2-дихлоретану та перемішували протягом 10год при 25°С. Розчинник випарювали та зазначену у заголовку сполуку очищали за допомогою ОФ-ВЕРХ (С18), елююючи 30-50% CH3CN в 0,1% TFA/Н2О протягом 20хв, одержуючи 81мг (78%) білої твердої речовини. 1Н ЯМP (400МГц, DMSO-d6) d 14,25 (br s, 1H), 9,90 (br s, 1Н), 9,79 (s, 1H), 8,72 (s, 1H). 8,36 (s, 1H), 7,98 (m, 1H), 7,88 (dd, 1H), 7,58 (d, 1H), 7,52 (m, 1H), 7,20 (m, 1Н), 7,12 (d, 1H), 5,76 (m, 1Н), 4,56 (s, 2H), 3,40 (m, 2H), 3,18 (m, 2H), 2,88 (m, 1Н), 2,20 (m, 4H), 2,00 (m, 4H), 1,72 (m, 4H). Мас-спектр (ESI m/z): Розрах для C28H30N6O, 467,2 (M+H), знайдено 467,2 Приклад 22 [2-(4-Метил-циклогекс-1-еніл)-4-(1-піридин-2ілметил-піперидин-4-іл)-феніл]-амід 4-ціано-1Німідазол-2-карбонової кислоти сіль трифтороцтової кислоти Ця сполука була одержана відповідно до методики, наведеної в Прикладі 21 з [2-(4-метилциклогекс-1-еніл)-4-піперидин-4-іл-феніл]-аміду 4ціано-1Н-імідазол-2-карбоновоі кислоти (який був одержаний в Прикладі 17) та піридин-2карбальдегіду 1Н - ЯМP (400МГц, DMSO-d6): d 14,25 (br s, 1H), 9,90 (br s, 1H), 9,79 (s, 1H), 8,72 (s, 1H), 8,36 (s, 1H), 7,98 (m, 1H), 7,86 (dd, 1H), 7,54 (d, 1H), 7,52 (m, 1Н), 7,20 (m, 1H), 7,12 (d, 1H), 5,74 (m, 1H), 4,56 (s, 2H), 3,40 (m, 2H), 3,18 (m, 2H), 2,88 (m, 1H), 2,48-2,22 (m, 3Η), 2,18-2,06 (m, 4H), 1,98-1,82 (m, 3H), 1,52 (m, 1H), 1,02 (s, 3H). Мас-спектр (ESI, m/z): Розрах. для C28H32N6O, 481,2 (M+H), знайдено 481,2. 59 88648 60 Приклад 23 імідазол-2-карбонової кислоти сіль трифтороцто{2-Циклопент-1-еніл-4-[1-(1-метил-1Н-імідазолвої кислоти 2-ілметил)-піперидин-4-іл]-феніл}-амід 4-ціано-1Німідазол-2-карбонової кислоти сіль трифтороцтової кислоти Ця сполука була одержана з (2-циклопент-1еніл-4-піперидин-4-іл-феніл)-аміду 4-ціано-1Німідазол-2-карбонової кислоти солі TFA (яка була одержана в Прикладі 18) та 1-метил-1Н-імідазол2-карбальдегіду відповідно до методики в Прикладу 21. 1Н - ЯМP (400МГц, CD3OD): d 8,03 (m, 2H), 7,50 (d, 1Н), 7,42 (s, 1Н), 7,20 (m, 2H), 6,02 (m, 1Н), 4,22 (s, 2H), 3,96 (s, 3H), 3,30 (m, 2H), 2,82-2,40 (m, 7H), 2,13-1,84 (m, 6H). Мас-спектр (ESI, m/z): Розрах. для C26H29N7O, 456,2 (M+H), знайдено 456,2. Приклад 24 Амід 4-{4-[(4-ціано-1Н-імідазол-2-карбоніл)аміно]-3-циклогекс-1-еніл-феніл}-піперидин-1карбонової кислоти В колбу поміщали (2-циклогекс-1-еніл-4піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2карбонової кислоти сіль TFA (51мг, 0,10ммоль) (яка була одержана в Прикладі 14, стадія (b)), NEt3 (22мкл, 0,15ммоль), триметилсиліл ізоціанат (16мкл, 0,11ммоль) та 1,0мл DCM та перемішували протягом 10год при 25°С. Розчинник випарювали та зазначену у заголовку сполуку очищали за допомогою ОФ-ВЕРХ (С18), елююючи 35-60% CH,CN в 0,1% TFA/Н2О протягом 11хв, одержуючи 30мг (70%) білої твердої речовини. 1Н - ЯМP (400МГц, DMSO-d6): d 14,28 (br s, 1H), 9,76 (s, 1H), 8,34 (s, 1H), 7,84 (d, 1H), 7,18 (dd, 1Н), 7,08 (d, 1Н), 6,00 (br s, 2H), 5,72 (m, 1Н), 4,18 (m, 2H), 2,80-2,60 (m, 3H), 2,24-2,10 (m, 4H), 1,80-1,60 (m, 6H), 1,50 (m, 2H). Мас-спектр (ESI, m/z): Розрах. для C23H26N6O, 419,2 (M+H), знайдено 419,0. Приклад 25 [2-Циклогекс-1-еніл-4-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-феніл]-амід 4-ціано-1Н В колбу поміщали (2-циклогекс-1-еніл-4піперидин-4-іл-феніл)-амід 4-ціано-1Н-імідазол-2карбонової кислоти сіль TFA (75мг, 0,15ммоль) (яка була одержана в Прикладі 14, стадія (b)), K2СО3 (84мг, 0,60ммоль), 2-фторпіридин (27мкл, 0,30ммоль) та 0,3мл Ν,Ν-диметилацетаміду та перемішували протягом 8год при 120°С. Реакційну суміш розбавляли 3мл Н2О та зазначену у заголовку сполуку очищали за допомогою ОФ-ВЕРХ (С18), елююючи 30-50% CH3CN в 0,1% TFA/Н2О протягом 9хв, одержуючи 50мг (75%) білої твердої речовини 1Н - ЯМP (400МГц, CD3OD) d 8,18 (d, 1Н), 8,06 (m, 1Н), 8,02 (s, 1Н), 7,94 (dd, 1Н), 7,48 (d, 2H), 7,22 (dd, 1Н), 7,12 (d, 1Н), 6,98 (t, 1Н), 5,82 (m, 1Н), 4,32 (m, 2H), 3,46 (m, 2H), 3,00 (m, 1Н), 2,30 (m, 4H), 2,18 (m, 2H), 1,96-1,74 (m, 6H). Мас-спектр (ESI, m/z): Розрах. для C27H28N6O, 453,2 (M+H). знайдено 453,2. Приклад 26 {2-Циклогекс-1-еніл-4-[1-(2-гідроксі-етил)піперидин-4-іл]-феніл}амід 4-ціано-1H-імідазол-2карбоіювої кислоти сіль трифтороцтової кислоти Зазначена у заголовку сполука була одержана з (2-циклогекс-1-еніл-4-піперидин-4-іл-феніл)-аміду 4-ціано-1Н-імідазол-2-карбонової кислоти солі TFA (яка була одержана в Прикладі 14, стадія (b)) та гідроксі-ацетальдегіду відповідно до методики в Прикладі 21. 1Н - ЯМP (400МГц, CD3OD): d 8,18 (d, 1H), 8,02 (s, 1H), 7,22 (dd, 1Н), 7,14 (d, 2H), 5,82 (m, 1H), 3,94 (m, 2H), 3,74 (m, 2H), 3,30 (m, 2H), 3,18 (t, 2H), 2,92 (m, 1H), 2,30 (m, 4H). 2,20-1,98 (m, 4H), 1,96-1,74 (m, 4H). Мас-спектр (ESI, m/z): Розрах. для C24H29N5O2, 420,2 (M+H), знайдено 420,2. Приклад 27 {4-[1-(2-Ціано-етил)-піперидин-4-іл]-2циклогекс-1-еніл-феніл}-амід 4-ціано-1H-імідазол2-карбонової кислоти сіль трифтороцтової кислоти
ДивитисяДодаткова інформація
Назва патенту англійськоюInhibitors of c-fms kinase
Автори англійськоюIllig Carl R., Ballentine Shelley K., Chen Jinsheng, Meegalla Sanath, Rudolph M., Wall Mark, Wilson Ken, Desjarlais Renee, Molloy Christopher, Manthey Carl, Flores Christopher
Назва патенту російськоюИнгибиторы c-fms киназы
Автори російськоюИллиг Карл, Баллентайн Шелли К., Чен Джиншенг, Меегалла Санат, Рудольф М., Уолл Марк, Уилсон Кен, Десжарле Рене, Моллой Кристофер, Менти Карл, Флорес Кристофер
МПК / Мітки
МПК: A61K 31/445, A61K 31/4439, C07D 401/00, C07D 403/00, A61K 31/44, C07D 405/00, A61K 31/497
Мітки: інгібітори, кінази, c-fms
Код посилання
<a href="https://ua.patents.su/60-88648-ingibitori-c-fms-kinazi.html" target="_blank" rel="follow" title="База патентів України">Інгібітори c-fms кінази</a>
Попередній патент: C-арилглікозидні інгібітори sglt2 і процес лікування з їх використанням
Наступний патент: Спосіб одержання бензину з низьким вмістом сірки та олефінів
Випадковий патент: Таблетований харчовий продукт для лікувально-профілактичного харчування людей із порушеннями білково-мінерального обміну речовин












