Сполуки триазолу, придатні для використання в терапії
Номер патенту: 79674
Опубліковано: 10.07.2007
Автори: Стоубі Алан, Джонсон Патрік Стівен, Вейман Крістофер Пітер, Расселл Рейчел Джейн, Браянс Джастін Стівен, Рікманс Томас
Формула / Реферат
1. Сполука формули (І)
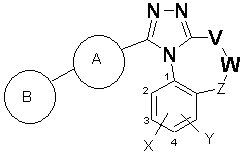 (I)
(I)
або її фармацевтично прийнятна похідна, де
V представляє (СН2)d(О)е-, -СО- або -СН(С1-6 алкіл)-;
W означає -О-,-S(О)а- або -N(R1)-;
R1 представляє Н, С1-6 алкіл, (СН2)bСОR, СО(СН2)bNR2R3, SО2R2, (СН2)cОR2, (СН2)cNR2R3 або (СН2)bhet1;
hеt1 представляє насичений або ненасичений гетероцикл з 3-8 атомами, що містять один або більшу кількість гетероатомів, вибраних з О, N або S, необов’язково заміщений С1-6 алкілом;
X і Y незалежно представляють Н, С1-6 алкіл, галоген, ОН, СF3, ОСF3, ОR4;
Z представляє -(СН2)f(О)g-, -СО- або -С(С1-6 алкіл)-;
кільце А представляє 4-7-членний, насичений N-вмісний гетероцикл, необов’язково заміщений ОН, в якому, необов’язково, принаймні один кільцевий атом N заміщений О;
кільце В представляє феніл або 4-7-членний ненасичений N-вмісний гетероцикл, необов’язково заміщений ОН, галогеном, СN, СОNН2, СFз, ОСF3, в якому, необов’язково, принаймні один кільцевий атом N заміщений О;
R2 і R3 незалежно представляють Н, С1-6 алкіл [необов’язково заміщений ОН, галогеном, N(С1-6 алкіл)2 або С1-6 алкілокси], С1-6 алкілокси, N(C1-6 алкіл)2 або [С3-8 циклоалкіл];
або R2 і R3, разом з атомом азоту, до якого вони приєднані, незалежно представляють гетероцикл з 3-8 атомами, необов’язково заміщений С1-6 алкілом;
R4 представляє лінійний або розгалужений С1-6 алкіл,
а і с незалежно представляють 0, 1 або 2;
b, e і g незалежно представляють 0 або 1; і
d і f незалежно представляють 1 або 2.
2. Сполука за п. 1, де W представляє NR1.
3. Сполука за п. 1 або п. 2, де R1 представляє Н, С1-6 алкіл, -(СН2)bСОR2 або SО2R2.
4. Сполука за будь-яким з пп. 1-3, де R1 є метилом.
5. Сполука за пп. 1 або 2, де R2 є морфолінілом або піримідинілом
(необов’язково заміщеним С1-6 алкілом [необов’язково заміщеним ОН, галогеном, N(C1-6 алкіл)2 або С1-6 алкілокси] або NМе2).
6. Сполука за будь-яким з попередніх пунктів, де X є Н.
7. Сполука за будь-яким з попередніх пунктів, де Y знаходиться в 4 положенні феніленового кільця (згідно з нумерацією формули (І)), до якого він приєднаний.
8. Сполука за п. 7, де Y є хлором.
9. Сполука за будь-яким з попередніх пунктів, де кільце А є приєднаним до кільця В через атом азоту у кільці А.
10. Сполука за будь-яким з попередніх пунктів, де кільце А представляє піперидиніл (необов’язково заміщений ОН і необов’язково принаймні один атом N заміщений О).
11. Сполука за будь-яким з попередніх пунктів, де кільце В представляє піридиніл або піримідиніл (необов’язково заміщений ОН, галогеном, СN, СОNН2, СFз, ОСFз, і необов’язково принаймні один кільцевий атом N заміщений О).
12. Сполука за п. 11, де кільце В представляє піридиніл.
13. Сполука за будь-яким з попередніх пунктів, де V представляє -СН2-.
14. Сполука за будь-яким з попередніх пунктів, де Z представляє -СН2-.
15. Сполука за будь-яким з пп. 1-3, де, коли R2 і R3 разом з азотом, до якого вони приєднані, являють собою гетероцикл, гетероцикл вибирають з піперазинілу, піролідинілу, піперидинілу, піримідинілу, тетрагідропіранілу або морфолінілу, необов’язково заміщеного С1-6 алкілом.
16. Сполука за п. 1, вибрана з:
8-хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену тригідрохлориду;
8-хлор-5-ізопропіл-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену тригідрохлориду;
1-[8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-іл]етанону дигідрохлориду;
8-хлор-5-метансульфоніл-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену;
8-хлор-5-метил-1-(1-піримідин-2-іл-піперидиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену;
8-хлор-5-метансульфоніл-1-(1-піримідин-2-іл-піперидиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену;
13-хлор-8-метил-3-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-2,4,5,8-тетраазатрицикло[9,4,0,0*2,6*]пентадека-1(11),3,5,12,14-пентаєну;
13-хлор-3-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-8-окса-2,4,5-триазатрицикло[9,4,0,0*2,6*]пентадека-1(11),3,5,12,14-пентаєну;
1-[8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-іл]-2-диметиламіноетанону;
[8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-іл]морфолін-4-іл-метанону;
(+) або (-) 8-хлор-5-(4-метилморфолін-2-ілметил)-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену;
8-хлор-5-піримідин-2-іл-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену;
8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-сульфонової кислоти диметиламіду;
8-хлор-1-(1-піримідин-2-іл-піперидиніл-4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-сульфонової кислоти диметиламіду;
13-хлор-9-метил-3-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-2,4,5,9-тетраазатрицикло[9,4,0,0*2,6*]пентадека-1(11),3,5,12,14-пентаєну;
13-хлор-8-метил-3-(1-піримідин-2-іл-піперидиніл-4-іл)-2,4,5,8-тетраазатрицикло[9,4,0,0*2,6*]пентадека-1(11),3,5,12,14-пентаєну; або її фармацевтично прийнятних похідних.
17. Сполука за п. 1, яка є 8-хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азуленом.
18. 8-хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену дибезилат.
19. Застосування сполуки за будь-яким з пп. 1-18 як лікарського засобу.
20. Спосіб лікування тривоги, серцево-судинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, зупинку серця, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передекламсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно, який включає призначення терапевтично ефективної кількості сполуки за будь-яким з пп. 1-18 пацієнтові, що страждає від такого розладу.
21. Спосіб за п. 20, де розладом є тривога.
22. Спосіб за п. 20, де розладом є дисменорея (первинна або вторинна).
23. Застосування сполуки за будь-яким з пп. 1-18 при одержанні лікарського засобу для лікування тривоги, гіпернатріємії, дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передекламсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно.
24. Застосування за п. 23 для лікування тривоги.
25. Застосування за п. 23 для лікування дисменореї (первинної або вторинної).
26. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-18, разом з фармацевтично прийнятним ексципієнтом, розчинником або носієм.
27. Проміжні сполуки формул (II), (III), (X) і (XV):
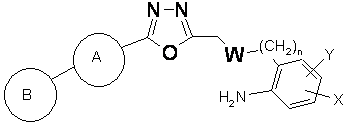 , (II)
, (II)
 , (III)
, (III)
 , (X)
, (X)
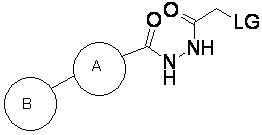 , (XV)
, (XV)
де V, W, X, Y, Z, кільця А і В і n мають значення, як визначено у пункті 1, і LG представляє собою придатну відхідну групу.
28. Спосіб одержання сполуки формули (І) за п. 1 або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (II) з кислотним каталізатором
 , (II)
, (II)
де кільця А і В і групи V, W, X, Y і n мають значення, як визначено вище.
29. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (III)
 (III)
(III)
з сполукою формули (IV)
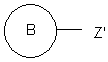 , (IV)
, (IV)
де кільця А і В і групи W, X, Y і n мають значення, як визначено у пункті 1, і Z' представляє собою відхідну групу, таку як галоген.
30. Спосіб одержання сполуки формули (І), як визначено у пункті 1, де W представляє собою NR1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (V)
 (V)
(V)
з сполукою формули (VI)
![]() , (VI)
, (VI)
де кільця А і В і групи R1, X, Y і n мають значення, як визначено у пункті 1, і Z" представляє собою відхідну групу, таку як галоген.
31. Спосіб одержання сполуки формули (І), як визначено у пункті 1, де W представляє собою NR1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (V)
 (V)
(V)
з сполукою формули (VII)
![]() , (VII)
, (VII)
де кільця А і В і групи R1, X, Y і n мають значення, як визначено у пункті 1.
32. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає взаємодію сполуки формули (XIII)
 (XIII)
(XIII)
з сполукою формули (XXIV)
 , (XXIV)
, (XXIV)
де кільця А і В і групи V, W, X, Y і Z мають значення як визначено у пункті 1.
33. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає взаємодію сполуки формули (XIII)
 (XIII)
(XIII)
з сполукою формули (XXV)
 , (XXV)
, (XXV)
де кільця А і В і групи V, W, X, Y і Z мають значення, як визначено у пункті 1.
Текст
1. Сполука формули (І) Y або її фармацевтично прийнятна похідна, де V представляє (СН2)d(О)е-, -СО- або -СН(С1-6 алкіл)-; W означає -О-,-S(О)а- або -N(R1)-; R1 представляє Н, С1-6 алкіл, (СН2)bСОR, СО(СН2)bNR2R3, SО2R 2, (СН2)cОR2 , (СН2)cNR2R3 або (СН2)bhet1; hеt1 представляє насичений або ненасичений гетероцикл з 3-8 атомами, що містять один або бі UA (21) a200508142 (22) 09.02.2004 (24) 10.07.2007 (86) PCT/IB2004/000432, 09.02.2004 (31) 0303852.8 (32) 19.02.2003 (33) GB (31) 0317227.7 (32) 23.07.2003 (33) GB (46) 10.07.2007, Бюл. № 10, 2007 р. (72) Браянс Джастін Стівен, GB, Джонсон Патрік Стівен, GB, Рікманс Томас , BE, Стоубі Алан , GB, Расселл Рейчел Джейн, GB, Вейман Крістофер Пітер, GB (73) ПФАЙЗЕР ІНК., US (56) WO 02 083678 A 24.10.2002 WO 00 43398 A 27.07.2000 WO 98 20011 A 14.05.1998 BRESLIN, HENRY J. ET AL: "Synthesis and anti-HIV activity of 1,3,4,5-tetrah ydro-2H-1,4-benzodiazepin2-one (TBO) derivatives. Truncated 4,5,6,7tetrahydro-5methylimidazoA4,5,1jkUA1,4Ubenzodiazepin2(1,H)-ones (TIBO) analogues" BIOORGANIC & MEDICIN AL CHEMISTR Y , CODEN: BMECEP; ISSN: 0968-0896, vol. 7, no. 11, 1999 ASHWOOD, MICHAEL S. ET AL: "Synthesis of 5,6dihydro-4H-imidazoA1,5-aUA4,1Ubenzoxa z epin-6ones and their transformation into 5,6-dihydro-4HimidazoA1,5-aUA1,4Ubenzodia zepin6-ones" JOURNAL OF THE CHEMICAL SOCIETY, PERKIN TRANSACTIONS 1: ORGANIC AND BIO-ORGANIC 2 (19) 1 3 79674 льшу кількість гетероатомів, вибраних з О, N або S, необов’язково заміщений С1-6 алкілом; X і Y незалежно представляють Н, С1-6 алкіл, галоген, ОН, СF3 , ОСF3, ОR4; Z представляє -(СН2)f(О)g -, -СО- або -С(С1-6 алкіл)-; кільце А представляє 4-7-членний, насичений Nвмісний гетероцикл, необов’язково заміщений ОН, в якому, необов’язково, принаймні один кільцевий атом N заміщений О; кільце В представляє феніл або 4-7-членний ненасичений N-вмісний гетероцикл, необов’язково заміщений ОН, галогеном, СN, СОNН2, СFз, ОСF3, в якому, необов’язково, принаймні один кільцевий атом N заміщений О; R2 і R3 незалежно представляють Н, С1-6 алкіл [необов’язково заміщений ОН, галогеном, N(С1-6 алкіл)2 або С1-6 алкілокси], С1-6 алкілокси, N(C1-6 алкіл)2 або [С3-8 циклоалкіл]; або R2 і R3, разом з атомом азоту, до якого вони приєднані, незалежно представляють гетероцикл з 3-8 атомами, необов’язково заміщений С 1-6 алкілом; R4 представляє лінійний або розгалужений С 1-6 алкіл, а і с незалежно представляють 0, 1 або 2; b, e і g незалежно представляють 0 або 1; і d і f незалежно представляють 1 або 2. 2. Сполука за п. 1, де W представляє NR1. 3. Сполука за п. 1 або п. 2, де R1 представляє Н, С1-6 алкіл, -(СН2)bСОR2 або SО2R2. 4. Сполука за будь-яким з пп. 1-3, де R1 є метилом. 5. Сполука за пп. 1 або 2, де R 2 є морфолінілом або піримідинілом (необов’язково заміщеним С 1-6 алкілом [необов’язково заміщеним ОН, галогеном, N(C1-6 алкіл)2 або С1-6 алкілокси] або NМе2). 6. Сполука за будь-яким з попередніх пунктів, де X є Н. 7. Сполука за будь-яким з попередніх пунктів, де Y знаходиться в 4 положенні феніленового кільця (згідно з нумерацією формули (І)), до якого він приєднаний. 8. Сполука за п. 7, де Y є хлором. 9. Сполука за будь-яким з попередніх пунктів, де кільце А є приєднаним до кільця В через атом азоту у кільці А. 10. Сполука за будь-яким з попередніх пунктів, де кільце А представляє піперидиніл (необов’язково заміщений ОН і необов’язково принаймні один атом N заміщений О). 11. Сполука за будь-яким з попередніх пунктів, де кільце В представляє піридиніл або піримідиніл (необов’язково заміщений ОН, галогеном, СN, СОNН2, СFз, ОСFз, і необов’язково принаймні один кільцевий атом N заміщений О). 12. Сполука за п. 11, де кільце В представляє піридиніл. 13. Сполука за будь-яким з попередніх пунктів, де V представляє -СН2-. 14. Сполука за будь-яким з попередніх пунктів, де Z представляє -СН2-. 15. Сполука за будь-яким з пп. 1-3, де, коли R2 і R3 разом з азотом, до якого вони приєднані, являють собою гетероцикл, гетероцикл вибирають з піперазинілу, піролідинілу, піперидинілу, піримідинілу, 4 тетрагідропіранілу або морфолінілу, необов’язково заміщеного С1-6 алкілом. 16. Сполука за п. 1, вибрана з: 8-хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену тригідрохлориду; 8-хлор-5-ізопропіл-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену тригідрохлориду; 1-[8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5іл]етанону дигідрохлориду; 8-хлор-5-метансульфоніл-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену; 8-хлор-5-метил-1-(1-піримідин-2-іл-піперидиніл-4іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену; 8-хлор-5-метансульфоніл-1-(1-піримідин-2-ілпіперидиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену; 13-хлор-8-метил-3-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-2,4,5,8тетраазатрицикло[9,4,0,0*2,6*]пентадека1(11),3,5,12,14-пентаєну; 13-хлор-3-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4іл)-8-окса-2,4,5триазатрицикло[9,4,0,0*2,6*]пентадека1(11),3,5,12,14-пентаєну; 1-[8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл4-іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5-іл]2-диметиламіноетанону; [8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5іл]морфолін-4-іл-метанону; (+) або (-) 8-хлор-5-(4-метилморфолін-2-ілметил)1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6дигідро-4Н-2,3,5,10b-тетраазабензо[е]азулену; 8-хлор-5-піримідин-2-іл-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену; 8-хлор-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4іл)-4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5сульфонової кислоти диметиламіду; 8-хлор-1-(1-піримідин-2-іл-піперидиніл-4-іл)-4Н,6Н2,3,5,10b-тетраазабензо[е]азулен-5-сульфонової кислоти диметиламіду; 13-хлор-9-метил-3-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-2,4,5,9тетраазатрицикло[9,4,0,0*2,6*]пентадека1(11),3,5,12,14-пентаєну; 13-хлор-8-метил-3-(1-піримідин-2-іл-піперидиніл-4іл)-2,4,5,8тетраазатрицикло[9,4,0,0*2,6*]пентадека1(11),3,5,12,14-пентаєну; або її фармацевтично прийнятних похідних. 17. Сполука за п. 1, яка є 8-хлор-5-метил-1(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6дигідро-4Н-2,3,5,10b-тетраазабензо[е]азуленом. 18. 8-хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену дибезилат. 19. Застосування сполуки за будь-яким з пп. 1-18 як лікарського засобу. 5 79674 20. Спосіб лікування тривоги, серцево-судинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, зупинку серця, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передекламсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно, який включає призначення терапевтично ефективної кількості сполуки за будь-яким з пп. 1-18 пацієнтові, що страждає від такого розладу. 21. Спосіб за п. 20, де розладом є тривога. 22. Спосіб за п. 20, де розладом є дисменорея (первинна або вторинна). 23. Застосування сполуки за будь-яким з пп. 1-18 при одержанні лікарського засобу для лікування тривоги, гіпернатріємії, дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передекламсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно. 24. Застосування за п. 23 для лікування тривоги. 25. Застосування за п. 23 для лікування дисменореї (первинної або вторинної). 26. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-18, разом з фармацевтично прийнятним ексципієнтом, розчинником або носієм. 27. Проміжні сполуки формул (II), (III), (X) і (XV): N N O A (CH2)n W B H 2N Y (II) X , N N H N W (III) Y , N N A N N O LG (X) B B N H X (XV) , X Y з сполукою формули (IV) B (IV) Z' , де кільця А і В і групи W, X, Y і n мають значення, як визначено у пункті 1, і Z' представляє собою відхідну гр упу, таку як галоген. 30. Спосіб одержання сполуки формули (І), як визначено у пункті 1, де W представляє собою NR1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (V) N N V N A NH (V) B z Y з сполукою формули (VI) Z'' (VI) R1 , 1 де кільця А і В і групи R , X, Y і n мають значення, як визначено у пункті 1, і Z" представляє собою відхідну гр упу, таку як галоген. 31. Спосіб одержання сполуки формули (І), як визначено у пункті 1, де W представляє собою NR1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (V) N B B (II) N N LG NH Y , де кільця А і В і групи V, W, X, Y і n мають значення, як визначено вище. 29. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (III) N N V N A N W (III) H z A A W Z H 2N , OO V O A X z X де V, W, X, Y, Z, кільця А і В і n мають значення, як визначено у пункті 1, і LG представляє собою придатну відхідн у гр упу. 28. Спосіб одержання сполуки формули (І) за п. 1 або її фармацевтично прийнятної похідної, що включає: взаємодію сполуки формули (II) з кислотним каталізатором V N A 6 V NH z X (V) Y з сполукою формули (VII) O R1 , (VII) 7 79674 де кільця А і В і групи R1, X, Y і n мають значення, як визначено у пункті 1. 32. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає взаємодію сполуки формули (XIII) O A B NH NH2 33. Спосіб одержання сполуки формули (І), як визначено у пункті 1, або її фармацевтично прийнятної похідної, що включає взаємодію сполуки формули (XIII) O A B (XIII) N V W (XIII) S S z NH NH 2 з сполукою формули (XXV) з сполукою формули (XXIV) HN 8 V W (XXV) z (XXIV) X Y , де кільця А і В і групи V, W, X, Y і Z мають значення як визначено у пункті 1. Даний винахід стосується нових композицій, придатних для використання в терапії і способів їх одержання, проміжних сполук, що використовуються в лікувальних засобах, композицій, що їх містять і застосування таких похідних. [Японська патентна заявка №09328484] описує триазольні хіноксаліни, придатні для використання як антиалергійні і протизапальні агенти. [Японська патентна заявка №09132576] описує триазольні хіноксаліни, придатні для використання як антиалергійні і протизапальні агенти. [Японська патентна заявка №06135965] описує триазольні хіноксаліни, придатні для використання для лікування і запобігання алергій, запалення і PAFасоційованих захворювань. [Японська патентна заявка №06128262] описує триазольні хіноксаліни, що використовують для проміжних сполук лікувальних засобів і агрохімічних засобів. В публікації [міжнародної патентної заявки WO 02/083678] описуються похідні бензодіазепіну, придатні для використання при лікування, в числі інших захворювань, тривоги, серцевосудинних захворювань та дисменореї. Було знайдено, що сполуки представленого винаходу, мають придатні для використання фармацевтичні властивості. Вони можуть використовуватися, для лікування агресивності, хвороби Альцгеймера, нервової анорексії, тривоги, тривожного розладу, астми, атеросклерозу, аутизму, серцево-судинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), катаракти, захворювання центральної нервової системи, цереброваскулярної ішемії, цирозу, когнітивного розладу, хвороби Кушінга, депресії, цукрового діабету, дисменореї (первинної та вторинної), блювоти (включаючи нудоту, що виникає при їзді), ендометріозу, шлунково-кишкового захворювання, глау X Y , де кільця А і В і групи V, W, X, Y і Z мають значення, як визначено у пункті 1. коми, гінекологічного захворювання, серцевого захворювання, затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), ішемії, ішемічного захворюванння серця, пухлини легень, розладу сечовипускання, міжменструального болю, новоутворення, ниркової токсичності, не-інсулін залежного діабету, ожиріння, обсесивно/компульсивного розладу, окулярної гіпертонії, передеклампсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів, легеневих захворювань, хвороби Рейно, захворювання нирок, ниркової недостатності, чоловічої або жіночої статевої дисфункції, септичного шоку, розладу сну, ушкодження спинного мозку, тромбозу, інфекції сечостатевого тракту або сечокаменевого захворювання. Особливо представляють інтерес наступні захворювання або розлади: тривога, серцевосудинне захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменорея (первинна і вторинна), ендометріоз, блювота (включаючи нудоту, що виникає при їзді), затримка внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструальний біль, передеклампсія, передчасна еякуляція, передчасні (недоношена вагітність) пологи і хвороба Рейно. Зокрема вони показують антагоністичну дію вазопресину і можуть використовуватися в лікуванні дисменореї (первинної і вторинної). Існує висока незадоволена потреба в області менструальних розладів і оцінено, що до 90% всіх жінок, що мають менструацію, в деякій мірі страждають від цих розладів. До 42% жінок пропускають роботу або інші види діяльності через менструальний біль і було оцінено, що в США в результаті цього втрачається приблизно 600 мільйонів годин 9 79674 роботи на рік (що коштує приблизно 2 мільярда у втраченій продуктивності). Менструальний біль у нижній частині черевної порожнини викликається міометріальною гіперфункцією і зниженим матковим кровотоком. Ці патофізіологічні зміни призводять до болю в животі, що поширюється на спину і ноги. Це може призводити до відчуття нудоти у жінок, головних болів і страждання від безсоння. Цей стан називають дисменореєю і він може бути класифікований або як первинна, або як вторинна дисменорея. Первинну дисменорею діагностують, коли не можна ідентифікувати ніякого відхилення, що викликає такий стан. Від цього страждає до 50% населення жіночої статі. Де є присутнім основний гінекологічний розлад, такий як ендометріоз, тазове запальне захворювання (PID), фіброзні пухлини або ракові утворення, буде діагностуватися вторинна дисменорея. Вторинна дисменорея діагностується тільки приблизно у 25% жінок, що страждають від дисменореї. Дисменорея може проходити сумісно з менорагією, що пояснює приблизно до 12% звернень до гінекологічних амбулаторних закладів. В даний час, жінок, що страждають від первинної дисменореї лікують, використовуючи нестероїдні протизапальні засоби (NSALD's) або оральні контрацептичні пігулки. У випадках вторинної дисменореї можуть бути вжиті хірургічні заходи для усунення основного гінекологічного розладу. Жінки, що страждають від дисменореї мають циркуляторні рівні вазопресину, що є більше ніж ті, що спостерігалися у здорових жінок у той же самий час менструального циклу. Інгібуванням фармакологічних дій вазопресину в матковому рецепторі вазопресину можна запобігати дисменореї. Згідно з представленим винаходом забезпечується сполука формули (І), або її фармацевтично прийнятна похідна, в якій V представляє собою -(CH2)d(O) e-, -CO- або СН(С1-6 алкіл)-; W означає -О-, -S(O)a- або -N(R1)R1 представляє собою Н, С1-6 алкіл, (CH2)bCOR2, CO(CH2)bNR2R3, SO2R2, (CH2)COR2, (CH2)CNR2R3 або (CH 2)bhet1; het1 представляє насичений або ненасичений гетероцикл з 3-8 атомами, що містять один або більшу кількість гетероатомів вибраних з О, N або S, необов'язково заміщений С1-6 алкілом; X і Υ незалежно представляють собою Н, С1-6 алкіл, галоген, ОН, CF3, OCF3, OR4; Ζ представляє собою -(CH2)f(O)g -, -CO- або СН(С1-6 алкіл)-; 10 Кільце А представляє собою 4-7 членний, насичений N-вмісний гетероцикл, необов'язково заміщений ОН і в якому необов'язково принаймні один атом N кільця є заміщений О; Кільце В представляє собою феніл або 4-7 членний ненасичений N-вмісний гетероцикл, необов'язково заміщений ОН, галогеном, CN, CONH2, CF3, OCF 3 і в якому, необов'язково принаймні один кільцевий атом N є заміщений О; R2 і R3 незалежно представляють собою Н, С1алкіл [необов'язково заміщений ОН, галогеном, 6 N(С1-6 алкіл)2 або С1-6 алкілокси], С1-6 алкілокси, N(С1-6алкіл)2 або [С3-8 циклоалкіл]; або R2 i R3, разом з атомом азоту, до якого вони приєднані незалежно, представляють собою гетероцикл з 3-8 атомами, необов'язково заміщений С1-6 алкілом; R4 представляє собою лінійний або розгалужений С1-6 алкіл, а і с незалежно представляють собою 0,1 або 2; b, e і g незалежно представляють собою 0 або 1; d і f незалежно представляють собою 1 або 2. У вищезгаданих визначеннях, галоген означає фтор, хлор, бром або йод. Алкільні групи, що містять необхідну кількість атомів вуглецю, крім де позначено, можуть бути нерозгалуженим або розгалуженим ланцюгом. Приклади включають метил, етил, н-пропіл, і-пропіл, н-бутил, і-бутил, втор.бутил і т-бутил. Приклади цикпоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил. Приклади алкілокси включають метокси, етокси, н-пропілокси, і-пропілокси, нбутилокси, і-бутилокси, втор.-бутилокси і тбутилокси. Гетероцикли влючені в визначення "гетероцикл" означають піроліл, імідазоліл, триазоліл, тієніл, фурил, тіазоліл, оксазоліл, тіадіазоліл, оксадіазоліл, піридиніл, піримідиніл, піридазиніл, піразиніл, індоліл, ізоіндоліл, хінолініл, ізохінолініл, бензімідазоліл, хіназолініл, фталазиніл, бензоксазоліл і хіноксалініл, разом з частково або повністю насиченими їх варіантами також як азетидиніл, піролідиніл, піперидиніл, піперазиніл, гомопіперазиніл, оксазепаніл і морфолініл. Переважними групами сполук є ті, в яких застосовується будь яка одна або більша кількість наступних: (і) W означає NR1; (іі) R1 означає С1-6 алкіл і більш переважно метил, і-пропіл або н-бутил; (ііі) R1 означає Н; (iv) R1 означає (CH2)bhet1; (ν) het1 представляє собою піролідиніл, піперидиніл, морфолініл, азетидиніл, оксазепаніл, піримідиніл, піридиніл, тіазоліл або імідазоліл, (необов'язково заміщений С1-6 алкілом) (vi) R1 означає CO(CH 2)bNR2R3; (vii) R2 означає морфолініл або піримідиніл (необов'язково заміщений С 1-6 алкілом [необов'язково заміщений ОН, галогеном, N(С1-6алкіл)2 або С1-6алкілокси] або NMe2). (viii) R2 і R3 разом з атомом азоту, до якого вони приєднані, представляють морфолініл, піролідиніл, піперазиніл, азетидиніл, тетрагідропіраніл, 11 79674 піримідиніл або піперидиніл (необов'язково заміщений С1-6 алкілом) (іх) V означає -(CH2)d(O)e-; (x) Ζ означає -(CH2)f(O)g -; (хі) d означає 1; (хіі) e означає 0; (хііі) f означає 1; (xi v) g означає 0; (xv) X означає Н; (xvi) Υ знаходиться в 4 положенні феніленового кільця (відповідно до нумерації формули (І)) до якого він приєднаний; (xvii) Y означає галоген, переважно хлор; (xviii) Y означає алкілокси, переважно метокси; (хі х) Υ означає алкіл, переважно метил; (хх) Υ означає CF3 або OCF3; (ххі) Ζ означає (CH2)d(O)e; (ххіі) e є 0; (ххііі) d є 1; (xxi v) кільце А є приєднаним до кільця В через атом азоту у кільці А; (xxv) кільце А є піперидинілом (необов'язково заміщеним ОН і необов'язково принаймні один атом N є заміщений О); (xxvi) кільце В є піридинілом (необов'язково заміщеним одним або більшою кількістю груп, вибраних з ОН, галогену, CN, CONH2, CF3 , OCF 3 і необов'язково принаймні один кільцевий атом N є заміщений О), переважно це 2-піридиніл; (xxvii) кільце В є піримідиніл (необов'язково заміщений однією або більшою кількістю груп, вибраних з ОН, галогену, CN, CONH2, CF3 , OCF 3 і необов'язково принаймні один кільцевий атом N є заміщений О), переважно це 2-піримідиніл; (xxviii) n є 1; (ххі х) n є 2. Переважними сполуками згідно з представленим винаходом є наступні: 8-Хлор-5-метил-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену тригідрохлорид; 8-Хлор-5-ізопропіл-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулену тригідрохлорид; 1-[8-Хлор-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10bтетраазабензо[е]азулен-5іл]етанонудигідрохлорид; 8-Хлор-5-метансульфоніл-1-(3,4,5,6тетрагідро-2Н-[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н2,3,5,10b-тетраазабензо[е]азулен; 8-Хлор-5-метил-1-(1-піримідин-2-іл-піперидин4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулен; 8-Хлор-5-метансульфоніл-1-(1-піримідин-2-ілпіперидин-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулен; 13-Хлор-8-метил-3-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-2,4,5,8тетраазатрицикло[9.4.0.0*2,6*]пентадека1(11),3,5,12,14-пентаєн; 13-Хлор-3-метил-3-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-8-окса-2,4,5триазатрицикло[9.4.0.0*2,6*]пентадека1(11),3,5,12,14-пентаєн; 12 1-[8-Хлор-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10bтетраазабензо[е]азулен-5-іл]-2диметиламіноетанон; [8-Хлор-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10bтетраазабензо[е]азулен-5-іл]морфолін-4-ілметанон; (+) або (-) 8-Хлор-5-(4-метилморфолін-2ілметил)-1-(3,4,5,6-тетрагідро-2Н-[1,2']біпіридиніл4-іл)-5,6дигідро-4Н-2,3,5,10bтетраазабензо[е]азулен; 8-Хлор-5-піримідин-2-iл-1-(-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-5,6-дигідро-4Н-2,3,5,10bтетраазабензо[е]азулен; 8-Хлор-1-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-4Н,6Н-2,3,5,10bтетраазабензо[е]азулен-5-сульфонової кислоти диметиламід; 8-Хлор-1-(1-піримідин-2-іл-піперидин-4-іл)4Н,6Н-2,3,5,10b-тетраазабензо[е]азулен-5сульфонової кислоти диметиламід; 13-Хлор-9-метил-3-(3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл-4-іл)-2,4,5,9тетраазатрицикло[9.4.0.0*2,6*]пентадека-1 (11),3,5,12,14-пентаєн; і 13-Хлор-8-метил-3-(1-піримідин-2-ілпіперидиніл-4-іл)-2,4,5,8тетраазатрицикло[9.4.0.0*2,6*]пентадека1(11),3,5,12,14-пентаєн. Альтернативно забезпечується сполука формулу (І*), W означає О, S, або NR1 R1 представляє собою Н, С1-6 алкіл, -(СН2)а[С3-8 циклоалкіл], феніл, бензил, піридил, піримідил, -COR2, -CO2R2, -CO-(CH2)a-NR2R3, -SO2R2 , (CH2)b-OR2, -(CH2)b-NR2R3 або насичений гетероцикл з 3-8 атомами, що містить один або більшу кількість гетероатомів вибраних з О, N і S; X і Υ незалежно представляють собою Н, галоген, ОН, CF3, OCF3 , R4, -(CH2) d-CONR4R5, -(CH2)dCN, -(CH2)d-SO2NR4R5, -(CH2)d-NR4SO 2 Me, -(CH2)dCOR4, -(CH2)d-OCOR 4 , -(CH2)d-NHCOR4, -(CH2)dNR4COR5, -(CH2)d-OR6 або -(CH2)d-CO2R6; Кільце А представляє собою піперидинільну, піперазинільну, піролідинільну або азетидинільну груп у; Кільце В представляє собою фенільну, піридинільну або піримідинільну групу (необов'язково заміщену однією або більшою кількістю груп, незалежно вибраних з галогену, CN, CONH2, CF3, OCF3, R 7 і -(CH2)f-OR8); R2, R3, R4, R5 і R7 незалежно представляють собою Н, лінійний або розгалужений С 1-6 алкіл, 13 79674 (СН2)с-[С3-8 циклоалкіл], феніл, бензил, піридил або піримідил; або R2 і R3, або R4 і R5 разом з атомом азоту, до якого вони приєднані, незалежно представляють собою гетероцикл з 3-8 атомами; R6 і R8 незалежно представляють собою Н, лінійний або розгалужений С 1-6 алкіл, -(СН2)с-[С3-8 циклоалкіл], -(CH2)e-NR4R5, -(CH2)e-OR4, феніл, бензил, піридил або піримідил; n=0, 1 або 2; а, с, d і f всі незалежно вибирають з 0, 1, 2 або 3; b і e незалежно вибирають з 2 або 3. Фармацевтично прийнятні похідні сполук формули (І), згідно з винаходом, включають солі, сольвати, комплекси, поліморфн, пролікарські форми, стереоізомери, геометричні ізомери, таутомерні форми і ізотопні варіації сполук формули (І). Переважно, фармацевтично прийнятні похідні сполук формули (І) включають солі, сольвати, естери й аміди сполук формули (І). Більш переважно, фармацевтично прийнятні похідні сполук формули (І) є солями і сольватами. Фармацевтично прийнятні солі сполук формули (І) включають їх кислотноадитивні й основні солі. Придатні кислотноадитивні солі одержують з кислот, що утворюють нетоксичні солі. Приклади включають ацетатні, аспартатні, бензоатні, бесилатні, бікарбонат/карбонатні, бісульфатні, боратні, камсилатні, цитратні, едизилатні, езилатні, форміатні, фумаратні, глуцептатні, глюконатні, глюкуронатні, гексафторфосфатні, хібензатні, гідрохлорид/хлоридні, гідробромід/бромідні, гідройодид/йодидні, ізотіонатні, D- та L-лактатні, малатні, малеатні, малонатні, мезилатні, метилсульфатні, нафтилатні, 2-напсилатні, нікотинатні, нітратні, оротатні, оксалатні, пальмітатні, пальмоатні, фосфатні, гідрофосфатні, дигідрофосфатні, сахаратні, стеаратні, сукцинатні, сульфатні, D- та L-тартратні, тозилатні і трифторацетатні солі. Особливо прийнятною сіллю є похідна бесилату сполук представленого винаходу. Придатні основні солі утворюються з основ, що утворюють нетоксичні солі. Приклади включають алюмінієві, аргінінові, бензатинові, кальцієві, холінові, діетиламінові, діоламінові, гліцинові, лізинові, магнієві, меглумінові, оламінові, калієві, натрієві, трометамінові та цинкові солі. Для огляду придатних солей дивіться [Stahl і Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection and Use (Довідник з фармацевтичних солей: властивості, вибір та застосування), Wiley-VCH, Weinheim, Germany (2002)]. Фармацевтично придатна сіль сполуки формули (І) може бути легко одержана, шляхом змішування разом розчинів сполуки формули (І) і бажаної кислоти або основи, відповідно. Сіль може осаджуватися з розчину і бути зібраною шляхом фільтрування або може бути відновлена шляхом випаровування розчинника. Ступінь іонізації в солі може змінюватися від цілком іонізованого до майже не-іонізованого. Сполуки згідно з винаходом можуть існувати в несольватованих формах, а також в сольватова 14 них формах. Термін "сольват" в даному контексті використовується для опису молекулярного комплексу, що включає сполуку винаходу й одну або більше молекул фармацевтично прийнятного розчинника, наприклад, етанолу. Термін "гідрат" в даному контексті використовується, коли згаданий розчинник є водою. Включені в межах винаходу комплекси такі як клатрати, комплекси включення типу лікарська речовина-"хазяїн", в яких на відміну від вищезгаданих сольватів, лікарська речовина та "хазяїн" присутні в сте хіометричній або не-стехіометричній кількостях. Також включені комплекси є комплексами лікарська речовина, що містить два або більше органічних і/або неорганічних компонентів, що можуть бути в стехіометричних або нестехіометричних кількостях. Кінцеві комплекси, можуть бути іонізовані, частково іонізовані або неіонізовані. Для огляду таких комплексів, дивіться [J. Pharm. Sci, 64 (8), 1269-1288, Haleblian (серпень 1975)]. Надалі всі посилання на сполуки формули (І) і фармацевтично прийнятні похідні включають посилання на солі, сольвати і їх комплекси і на сольвати і комплекси їх солей. Сполуки винаходу включають сполуки формули (І), як визначено вище, поліморфи, пролікарські засоби та їх ізомери (включаючи оптичні, геометричні і таутомерні ізомери), як визначено надалі та мічені ізотопами сполуки формули (І). Як заявляється, винахід включає всі поліморфи сполук формули (І), як визначено вище. Також у межах винаходу знаходяться так звані "проліки" сполук формули (І). Таким чином, певні похідні сполук формули (І), що можуть мати невелику або ніяку фармакологічну дію, якщо вводяться в організм або на тіло, можуть бути перетворені на сполуки формули (І), що мають бажану дію, наприклад, за допомогою гідролізного розщеплення. Такі похідні відносяться до "проліків". Подальша інформація щодо використання проліків може бути знайдена у ["Prodrugs as Novel Delivery System, Vol.14, ACS Symposium Series (T Higuchi і W Stella) та "Bioreversible Carriers in Drug Design", Pergamon Press, 1987 (ред. Ε Β Roche, Американська Фармацевтична Асоціація)]. Проліки згідно з винаходом можуть, наприклад, бути одержані, заміною відповідних функціональних груп присутніх у сполуках формули (І) певними фрагментами, відомими фахівцям цієї галузі як "про-фрагменти" як описано, наприклад, в ["Design of Prodrugs" by Η. Bundgaard (Elsevier) 1985]. Деякі приклади проліків згідно з винаходом включають: (і) коли сполука формули (І) містить карбоксильну групу (-СООН), її естер, наприклад, заміна водню (С1-8) алкілом; (іі) коли сполука формули (І) містить спиртову груп у (-ОН), її е тер, наприклад, заміна водню (С16)алканоїлоксиметилом; і (ііі) коли сполука формули (І) містить первинні або вторинні аміногрупи (-NH2 або -NHR, де R¹Η), її амід, наприклад, заміна одного або обох атомів водню (С1-10)алканоїлом. 15 79674 Подальші приклади замінних груп відповідно до. попередніх прикладів і прикладів інших типів проліків можуть бути знайдені у вищезгаданих цитуваннях, що включені в заявку як посилання. Нарешті, певні сполуки формули (І) можуть самостійно діяти як проліки інших сполук формули (І). Також у межах винаходу представлені метаболіти сполук формули (І) коли одержані in vivo. Сполуки формули (І), що містять один або більшу кількість асиметричних атомів вуглецю можуть існувати як два або більша кількість стереоізомерів. У випадках, коли сполука формули (І) містить алкенільну або алкеніленову груп у, можливі геометричні цис/транс (або Z/E) ізомери і, коли сполука містить, наприклад, кето- або оксимгруп у або ароматичний залишок, може існувати таутомерна ізомерія ("таутомерія"). З вищевикладеного випливає, що окрема сполука може існувати в формі більше ніж одного типу ізомерії. Включені в межах представленого винаходу всі сполуки є стереоізомерами, геометричними ізомерами і таутомерними формами сполук формули (І), включаючи сполуки, що існують в формі більше ніж одного типу ізомерії і сумішей одного або більшої їх кількості. Включені також кислотноадитивні або основні солі, де протиіон є оптично активним, наприклад, D-лактат або L-лізин, або рацемічним, наприклад, DL-тартрат або DL-аргінін. Цис/транс ізомери можуть бути виділені за допомогою стандартних методик, добре відомих фахівцям даної галузі, наприклад, за допомогою фракційної кристалізації та хроматографії. Стандартні методики для одержання/виділення індивідуальних енантіомерів включають хіральний синтез з прийнятного оптично чистого прекурсора або розділення рацемата (або рацемата солі або похідного) використовуючи, наприклад, хіральну рідинну хроматографію високого тиску (ВЕРХ). Альтернативно, рацемат (або рацемічний прекурсор) можна піддавати реакції з прийнятною оптично активною сполукою, наприклад, спиртом, або у разі, коли сполука формули (І) містить кислий або основний залишок, кислоту або основу, такі як винна кислота або 1-фенілетиламін. Одержана діастереомерна суміш може бути виділена за допомогою хроматографії і/або фракційної кристалізації й один або обидва з діастереоізомерів, перетворюються на відповідний чистий енантіомер(и) за допомогою засобів, добре відомих фа хівцям даної галузі. Хіральні сполуки винаходу (і їх хіральні прекурсори) можуть бути отримані в енантіомернозбагаченій формі, використовуючи хроматографію, типово ВЕРХ, на асиметричній смолі з мобільною фазою, що складається з вуглеводню, зазвичай гептану або гексану, що містить від 0 до 50% ізопропанолу, зазвичай від 2 до 20% і від 0 до 5% алкіламіну, зазвичай 0,1% діетиламіну. Концентруванням елюату одержують збагачену суміш. Стереоізомерні конгломерати можуть бути виділені за допомогою стандартних методик, добре відомих фа хівцям цієї галузі - дивиться, напри 16 клад, ["Стереохімію Органічних сполук" Ε L Eliel (Wiley, Нью-Йорк, 1994)]. Представлений винахід також включає всі придатні ізотопні варіації сполуки формули (І), в яких один або більше атомів замінені атомами, що мають той же самий атомний номер, але атомну масу, відмінну від природної атомної маси. Приклади ізотопів, що придатні для включення в сполуки винаходу включають ізотопи водню такі як 2Н і 3Н, вуглецю такі як 11С, 13С і 14С, азоту такі як 13N і 15N, кисню такі як 15O, 17 О і 18О, фосфору такі як 32Р, сірки такі як 35S, фтор у такі як 18F, йоду такі як 123І і 125І і хлору такі як 36СІ. Певні мічені ізотопами сполуки формули (І), наприклад, ті в які включені радіоактивні ізотопи, є корисними в ліках і/або в дослідженнях по розподіленню субстрату у тканинах. Радіоактивні ізотопи тритію, тобто 3Н і вуглецю-14, тобто 14С є особливо корисними завдяки легкості їх одержання та здатності для виявлення. Заміщення важкими ізотопами, такими як, дейтерій, тобто, 2Н, може мати певні терапевтичні переваги внаслідок їх більшої метаболічної стабільності, наприклад, підвищеного часу напівжиття in vivo або зменшених вимог до дозування і, отже, може бути бажаним в деяких обставинах. Заміщення ізотопами, що випускаються позитроном, такими як 11С, 18F, 15 О та 13N, може бути корисним в Positron Emission Topography (PET) дослідженнях для вивчення інтенсивності зв'язування рецептора з субстратом. Мічені ізотопами сполуки формули (І) можуть взагалі бути одержані за допомогою стандатних методик, відомих фа хівцям даної галузі, або процесів, аналогічних тим, що описані у супровідних Прикладах та Препаративних прикладах, заміщенням легко доступного міченого ізотопом реагента на не мічений ізотопом реагент. Фармацевтично прийнятні сольвати відповідно до винаходу включають ті, в яких розчинник кристалізації може бути заміщений ізотопами, наприклад, D2O, d6-ацетон, d6-ДМСО. Згідно з представленим винаходом також забезпечується спосіб одержання сполуки формули (І), що включає: a) реакцію сполуки формули (II) з кислотним каталізатором, де кільця А і В i групи V, W, Χ, Υ, Ζ і n є такими як визначено вище; b) реакцію сполуки формули (III) 17 79674 18 з сполукою формули (IV) де кільця А і В і групи V, W, Χ, Υ, Ζ і n є такими як визначено вище і Ζ' представляє собою відхідну груп у таку як галоген; c) коли W у сполуці (І) представляє собою NR1, реакцію сполуки формули (V) з сполукою формули (VI) де кільця А і В і групи V, W, Χ, Υ і Ζ є такі як визначено вище; f) реакцію сполуки формули (XIII) з сполукою формули (XXV) де кільця А і В і гр упи R1, V, Χ, Υ, Ζ і n є такими як визначено вище і Ζ" представляє собою відхідну гр уп у таку як галоген; або d) коли W у сполуці (І) представляє собою NR1, реакцію сполуки формули (V) з сполукою формули (VII) де кільця А і В і групи R 1, V, Χ, Υ, Ζ і n є такі як визначено вище; e) реакцію сполуки формули (XIII) з сполукою формули (XXIV) де кільця А і В і гр упи V, W, Χ, Υ і Ζ є такими як визначено вище. Якщо інакше не зазначено: WSCDI означає гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду; DCC означає Ν,Ν'-дициклогексилкарбодіімід; НОАТ означає 1-гідрокси-7-азабензотриазол; НОВТ означає 1-гідроксибензотриазолу гідрат; РуВОРÒ означає Бензотриазол-1ілокситріс(піролідин)фосфонійгексафторфосфат; РуВrOРÒ означає бром-тріспіролідинфосфонійгексафторфосфат; HBTU означає гексафторфосфат ОБензотриазол-1-іл-N,N,N',N'-тетраметилуронію. Реагент Мукаями означає 2-хлор-1метилпіридиніййодид; KHMDS означає біс(триметилсиліл)амід калію; основа Хюніга означає N-етилдіізопропіламін; Et3N означає триетиламін; NMM означає N-метилморфолін; HMDS означає гексаметилдисилазан BINAP означає 2,2'-біс(дифенілфосфін)-1,1'бінафтил; Dba означає дибензиліденацетон; Вос означає трет-бутоксикарбоніл; CBz означає бензилоксикарбоніл; p-TSA означає п-толуолсульфонову кислоту TBAF означає тетра-бутиламонійфторид МеОН означає метанол, EtOH означає етанол і EtOAc означає етилацетат; ТГФ означає тетрагідрофуран, ДМСО означає диметилсульфоксид і DCM означає дихлорметан, 19 79674 DMF означає Ν,Ν-диметилформамід, NMP означає N-метил-2-піролідинон; АсОН означає оцтову кислоту, TFA означає трифтороцтову кислоту; Me означає метил, Et означає етил; СІ означає хлор; і ОН означає гідрокси. Наступні схеми ілюструють одержання сполук формули (І), в ти х випадках, де кільця А і В і групи V, W, Χ, Υ і n мають значення ті як визначено вище, якщо інакше не заявлено. (I') представляє (І), коли W означає NR1. Стадія (а): Оксадіазол (II) піддавали реакції з кислотним каталізатором, одержуючи сполуку формули (І). Типово реакцію виконують шляхом нагрівання вихідних матеріалів до підвищених температур таких як 50-150°С, протягом від 1 до 48 годин з придатним кислотним каталізатором таким як p-TSA, трифтороцтова кислота або кислотним каталізатором Льюіса таким як хлорид магнію, необов'язково з використанням розчинника такий як ксилол, толуол або тетрагідрофуран. Переважними умовами є: амін (II) і P-TSA каталізатор, у ксилолі при 140°С протягом 48 годин; або амін (II), трифтороцтова кислота в тетрагідрофурані при 60°С протягом 24 годин. Коли W=NR1, тоді: Z' є ОН або галогеном, типово СІ Сполуки придатні для використання як сполука (VI) є наявними в продажу або є відомими з літератури. Стадія (b): реакція аміну (V) з сполукою (VI) може бути виконана за допомогою стандартних методів. Коли R1=(CH2)bCOR2, CO(CH2)bNR2R3, SO2R2 тоді, типово, конденсування може бути розпочато, з використанням: (і) ацил/сульфоніл/хлориду (VI)+амін (V) з надлишком акцептора кислоти у придатному розчиннику; або (іі) кислоти (VI) зі звичайним конденсувальним агентом+амін (V), необов'язково в присутності ка 20 талізатора, з надлишком акцептора кислоти в придатному розчиннику; і (ііі) коли R1 представляє собою арильну групу, арилгалоїду (VI)+амін (V), необов'язково в присутності каталізатора з надлишком акцептора кислоти в придатному розчиннику. Типово умови є наступними: Ацилювання/Сульфонілування. Z'=СІ (і) надлишок ацил/сульфонілхлориду (VI) (одержаний in-situ), 1екв. аміну (V), необов'язково з надлишком 30 аміну такого як Et3N, основи Хюніга або NMM, у DCM або ТГФ, без нагрівання протягом від 1 до 24 годин. Переважними умовами є: Амін (V), 1,1-3,0екв. кислота/сульфонілхлориду (VI), 1,5-3екв. NMM, Et 3N або піридин у DCM при кімнатній температурі протягом 1-16 годин. Одержання амідного зв'язку. Z'=ОН (іі) Надлишок кислоти (VI), WSCDI/DCC і НОВТ/НОАТ, 1екв. аміну (V) з надлишком NMM, Et3N, основи Хюніга в ТГФ, DCM або EtOAc, при кімнатній температурі протягом від 4 до 48 годин; або надлишок кислоти (VI), РУВОРÒ /РуВrOРÒ /реагент Мукаями/HBTU, 1екв. аміну (V) з надлишком NMM, Et3N, основа Хюніга в ТГФ, DCM або EtOAc, при кімнатній температурі протягом від 4 до 24 годин. Переважними умовами є: амін (V), 2екв. HBTU, 2екв. кислоти (R1OH) у DCM при кімнатній температурі протягом 18 годин; або амін (V) НОВТ, WSCDI, Et 3N у DCM при кімнатній температурі протягом 18 годин. Арилування Арил = (R1 , гетероарил). Z'=галоген, (ііі) Арилування сполуки (V) може бути виконане реакцією перехресного конденсування з використанням паладію як каталізатора, з використанням придатної основи (t-BuONa), каталітичної кількості придатної добавки такої як 2,2'біс(дифенілфосфін)-1,1'-бінафтил і придатного паладієвого каталізатора в толуолі при підвищених температурах протягом від 1 до 24 годин в атмосфері інертного газу, з одержанням сполуки (l'). Альтернативно сполука (I') може бути одержана за допомогою реакції аміну (V) з сполукою (VI) шляхом нагрівання при підвищеній температурі, такій як 50°С-140°С, у придатному розчиннику такому як DMF, N MP або 1,4-діоксан протягом приблизно 1-48 годин з основою такою як карбонат калію, гідрокарбонат натрію або основи Хюніга. Переважними умовами є: 1-2,5екв. галоїду (VI), 1-2екв. карбонату калію у Ν,Ν-диметилформаміді при 50-95°С протягом 418 годин; або 1-2,5екв. галоїду (VI), 2-3екв. основи Хюніга у 1,4-діоксані або ΝΜΡ при кипінні протягом 18-48 годин; або 1екв. галоїду (VI), 3,5екв. NaOt-Bu, 0,08екв. BINAP, 0,4екв. Pd(dba)2, у толуолі протягом 8 годин при 70°С. Алкілування (R1=заміщений алкіл ). Z'=галоген, переважно Вr або СІ 21 79674 Алкілування сполуки (V) може бути виконане за допомогою реакції з придатним алкілувальним агентом, R1Z' в присутності придатного третинного аміну (NMM, Et 3N або основи Хюніга) або основи лужного металу (K2СО3, Cs 2CO3) у придатному розчиннику (MeCN, DMF), приблизно при кімнатній температурі. Переважними умовами є: амін (V) R1Z', надлишок K2СО3 або основи Хюніга в DMF протягом 18 годин при кімнатній температурі. Альтернативно, сполуки (I') можуть бути одержані технологією, показаною нижче в Сполуки придатні для використання як сполука (VII) є наявними в продажу або є відомими з літератури. Стадія (с): Амін (V) реагує з надлишком альдегід/кетону (VII) у присутності відновлювального агента такого як триацетоксиборогідрид натрію або ціаноборогідрид натрію, з одержанням сполуки формули (I'). Ця реакція може бути виконана шляхом: перемішування вихідних матеріалів при температурах таких як 20°С-80°С протягом від 1 до 48 годин у придатному розчиннику такому як дихлорметан або нагрівання аміну (V) з надлишком сполуки (VII) з каталізом придатною кислотою Льюіса такою як тетрахлорид титану або тетраізопропоксид титану при температурах таких як 50°С-100°С у придатному розчиннику такому як дихлоретан або етанол протягом 1-18 годин, після того, шляхом відновлення проміжної сполуки імін/різновиди іміну з придатним відновлювальним агентом таким як борогідрид натрію або гідрогенолізом в присутності придатного каталізатора такого як оксид платини або паладій на вуглеці. Переважними умовами є: амін (V), 1-1,5екв. альдегід/кетону (VII), 12,0екв. триацетоксиборогідриду натрію в дихлорметані, необов'язково в присутності АсОН при кімнатній температурі протягом 2 годин. Коли кільце В є приєднаним до кільця через атом N і W представляє собою О або S тоді: 22 Prot представляє собою придатну захисну гр упу для азоту, наприклад Вос, CBz або алілкарбамат. Для захисних груп азоту використовується стандартна методологія, що наведена в посібниках [наприклад, "Захисні групи в органічному синтезі" Т. W. Greene і P. Wutz]. Z" представляє собою відхідну гр упу таку як галоген. Сполуки придатні для використання як сполука (IV) є наявними в продажу або відомі з літератури. Арилування сполуки (III) може бути виконане як описано в Стадії (b) наведеній вище. Переважними умовами є: 1-2,5екв. галоїду (IV), 1-2екв. карбонату калію у Ν,Ν-диметилформаміді при 50°С протягом 4-18 годин; або 1-2,5екв. галоїду (IV), 2-3екв. основи Хюніга, у 1,4-діоксані або NMP при кипінні протягом 18-48 годин; або 1екв. галоїду (IV), 3,5екв. NaOt-Bu, 0,08екв. BINAP, 0,4екв. Pd(dba)2, у толуолі протягом 8 годин при 70°С. Стадія (d): Зняття захисту з сполуки (IX) розпочинають, використовуючи стандартну методологію, як описано в ["За хисні групи в органічному синтезі" T.W. Greene і P. Wutz"]. Коли Prot є Вос, переважними способами є: хлороводень у придатному розчиннику такому як 1,4-діоксан при кімнатній температурі протягом 1-16 годин; або розчин трифтороцтової кислоти в дихлорметані протягом 1-2 годин. Коли Prot є CBz, переважним способом є гідрогеноліз з використанням придатного паладієвого каталізатора в розчиннику такому як етанол. Коли Prot є алілкарбаматом, переважними умовами є тіобензойна кислота і придатний паладієвий каталізатор такий як Pd2(Dba)3 з придатною фосфіновою добавкою такою як 1,4біс(дифенілфосфін)бутан у те трагідрофурані протягом 20 хвилин. Коли кільце В є приєднаним до кільця А через атом N і W представляє собою NR1 тоді: Prot представляє собою придатну захисну гр упу для азоту, наприклад Вос, CBz або алілкарба 23 79674 мат. Для захисних груп азоту використовується стандартна методологія, така як наведена в посібниках, [наприклад, "Захисні гр упи в органічному синтезі" Т.W. Greene і P. Wutz]. Ζ' представляє собою відхідну гр упу (типово СІ або ОН). Ζ" представляє собою галоген (типово СІ). Сполуки придатні для використання як сполука (IV) є наявними в продажу або є відомими з літератури. Сполука (IX") типово може бути одержана з сполуки (IX') використовуючи методологію, описану в Стадії (b) і Стадії (с), наведених вище. Сполука (III') типово може бути одержана з сполуки (IX"), використовуючи методологію, описану в С тадії (d), наведеній вище. Сполуки (l') типово можуть бути одержані шляхом арилування сполук (ІІl'), використовуючи методологію, описану в Стадії (b), наведеній вище. Сполуки придатні для використання як сполуки (II) і (VIII) є відомими з літератури або можуть бути одержані як показано в Схемах 3.1, 3.2 і 3.3, наведених нижче. Коли кільця А і В є приєднаними через атом N, тоді: Сполуки придатні для використання як сполуки (XI) є відомими з літератури або можуть бути одержані, використовуючи стандартну методологію: наприклад, відновлення бензойних кислот (дивіться препаративний приклад 7, наведений нижче) або бензонітрили (дивіться препаративний приклад 10, наведений нижче) або нітробензоли (препаративні приклади 57 і 58). Коли W представляє собою NR1: Стадія (e): Сполука (Х)/(ХІІ) реагує з надлишком сполуки (XI), з одержанням сполуки (II)/(VIII) 24 відповідно, необов'язково в присутності надлишку основи такої як триетиламін, основи Хюніга або NMM або карбонату калію як акцептора протонів, необов'язково в присутності каталізатора (наприклад Nal) в придатному розчиннику з високою температурою кипіння такому як ТГФ, толуолі або DMF при температурах від 50°С до 100°С протягом від 1 до 48 годин. Переважними умовами є: 2,5екв. сполуки (XI) у ТГФ при 50°С протягом 48 годин; або 1,1екв. сполуки (XI) 1,1екв. NMM або K2СО3, 0,5екв. Nal у ТГФ при 50°С. Коли W представляє собою О або S: Стадія (e): Сполука (Х)/(ХІІ) реагує з надлишком сполуки (XI) у присутності основи такої як гідрид натрію, гексаметилдисилазид, нбутиллітій або ізопропілмагнійхлорид, у придатному розчиннику такому як ТГФ, толуол або NMP при температурах від 0°С до 50°С протягом від 1 до 24 годин, з одержанням сполуки (II)/(VIII) відповідно. Переважними умовами є: 1,1-3екв. сполуки (XI) і 1,1-2,5екв. Na у ТГФ при 20°С протягом 2 годин. Коли W=NR1 і Ζ=CO, тоді Стадія (і): Амін (XX) може бути одержаний шляхом амінування сполуки (X) з аміном R1NH2 у розчиннику такому як етанол або тетрагідрофуран при 25-75°С протягом 5-72 годин. Переважними умовами є: Сполука (X), надлишок R1NH2 в етанолі і ТГФ при кімнатній температурі протягом приблизно 72 годин. Сполука (II) може бути одержана шляхом конденсування аміну (XX) з кислотою (XXI) відповідно до процедури, описаної попередньо в стадії (b). Сполуки придатні для використання як сполуки (X) і (XII) є відомими з літератури або можуть бути одержані як показано в Схемах 4.1 і 4.2. 25 79674 X' представляє собою ОН або галоген і переважно представляє СІ. LG представляє собою відхідну груп у, типово галоген і переважно хлор або бром. Коли кільця А і В є приєднаними через атом N, тоді: X' представляє собою ОН або галоген і переважно представляє собою СІ. LG є відхідною групою, типово галогеном і переважно хлором або бромом. Сполука (XIV) є або наявною у продажу або відомою з літератури. Стадія (f): реакція гідразиду (ХІІІ/ХІІl') з сполукою (XIV) може бути виконана стандартними методами. Конденсування може бути розпочате, використовуючи також: (і) ацилхлорид (XIV)+гідразид (ХІІІ/ХІІl') з надлишком акцептора кислоти в придатному розчиннику; або (іі) кислоту (XIV) зі звичайним конденсувальним агентом+гідразид (ХІІІ/ХІІl'), необов'язково в присутності каталізатора, з надлишком акцептора кислоти в придатному розчиннику. Типово умови є наступними: (і) хлорид кислоти (XIV) (одержаний in situ), надлишок гідразиду (ХІІІ/ХІІl'), необов'язково з надлишком 30 аміну такого як Et3N, основи Хюніга або NMM, у DC M або ТГФ, без нагрівання протягом від 1 до 24 годин; або (іі) кислота (XIV), WSCDI/DCC і НОВТ/НОАТ, надлишок гідразиду (ХІІІ/ХІІl'), з надлишком NMM, Et3N, основи Хюніга в ТГФ, DCM або EtOAc, при кімнатній температурі протягом від 4 до 48 годин; або (іі) кислота (XIV), РУВОРÒ /РуВrOРÒ /реагент Мукаями, надлишок гідразиду (ХІІІ/ХІІl'), з надлишком NMM, Et 3N, основи Хюніга в ТГФ, DC M або EtOAc, при кімнатній температурі протягом від 4 до 24 годин. Переважними умовами є: Гідразид (ХІІІ/ХІІl'), 1,5екв. хлорацетилхлориду (XIV), 1,5екв. NMM у DC M при кімнатній температурі протягом 16 годин. Стадія (g): Циклізацію сполуки (XV/XV) виконують при прийнятних умовах дегідратації при підвищених температурах протягом до 18 годин. 26 Як правило, дегідратуючі агенти такі як поліфосфорна кислота, оксихлорид фосфору, ангідрид трифторметансульфонової кислоти використовуються при температурах від 20 до 120°С протягом від 5 хвилин до 12 годин. При необхідності реакція може бути виконана в присутності основи такої як піридин і придатних розчинників таких як дихлорметан і ацетонітрил. Альтернативно, оксадіазол (ХІІ/Х) може бути одержаний згідно з способом, описаним в [Rigo і інш. Synth. Commun. 16 (13), 1665, 1986]. Переважними умовами є: оксихлорид фосфору при 100°С протягом 8 годин, або 2,5екв. ангідриду трифторметансульфонової кислоти в ацетонітрилі при 20°С протягом 5 годин. Сполуки придатні для використання як сполуки (ХІІІ/ХІІl') є відомими з літератури або можуть бути одержані як показано в Схемах 5.1 і 5.2. Коли кільця А і В є приєднаними через атом N, тоді: Сполуки (XVI)/(XVI') і захи щений гідразин є або наявними у продажу або відомими з стандартної методології такої як гідроліз відповідного естеру. Карбонова кислота (XVI)/(XVl') і захи щений гідразин, де prot* є типово Вос, можуть бути конденсовані з одержанням сполуки (XVIl/XVII') відповідно, використовуючи умови, описані вище для 27 79674 одержання (XV/XV') і потім prot* видаляють, використовуючи стандартну методологію, як описано вище в Стадії (d), одержуючи (ХІІІ/ХІІl'). Альтернативні шляхи одержання сполуки (ХІІІ/ХІІІ1) показані нижче в Схемах 6.1 і 6.2: Коли кільця А і В є приєднаними через атом N, тоді: Стадія (h): естер (XVIII/XVIII') може бути підданий реакції з гідразином у придатному розчиннику, такому як метанол при підвищеній температурі для одержання гідразиду (XVII/XVII'). Переважні умови: 3екв. гідразину в метанолі, при кипінні протягом 18 годин. Альтернативно, сполуки формули (І) можуть бути одержані згідно з Схемою 7.0, наведеною нижче. Коли R=Н, Сполуки формули (XXIII) можуть бути одержані інтрамолекулярною взаємодією амінокислоти (XXII), згідно з процедурою, попередньо описаною в стадії (b). Переважно сполуку (XXII) обробляють 1,4екв. HBTU, 4,5екв. ΝΜΜ у DCM при кімнатній температурі протягом приблизно 18 годин. Коли R=C1-C4 алкіл: Сполуки формули (XXIII) можуть бути одержані циклізацією амінного естеру (XXII), в умовах основного каталізу, що типово виконується при кімнатній температурі або нижче її протягом 1-5 годин. 28 Як правило, основи такі як трет-бутоксид калію, етоксид натрію або ізопропілмагнійхлорид використовуються при або нижче 20°С у придатному розчиннику такому як тетрагідрофуран або етанол протягом 1-5 годин. Переважно сполуку (XXII) обробляють 1,1екв. трет-бутоксид калію у ТГФ при 20°С протягом приблизно 2 годин. Стадія (j): Одержання тіоаміду Тіонування аміду (XXIII), з використанням придатного тіонувального агента (наприклад реагент Лавессона, P4S10) і необов'язково в присутності основи (наприклад Na2CO3) у придатному розчиннику (наприклад ТГФ) при температурах в діапазоні між 0°С і кімнатною температурою. Переважними умовами є: 1екв. P4S10, 1екв. Na2CO3, 1екв. аміду (XXIII) у ТГФ при температурах між 3-25°С протягом 18-72 годин Стадія (k): Одержання тіоімідату Обробкою тіоаміду (XXIV) сильною основою такою як KОtВu або LDA, у придатному розчиннику такому як ТГФ або етер, з наступною обробкою аніона, одержаного за допомогою придатного джерела метилу (наприклад Mel, Me п-тозилат) одержують тіоімідат (XXV). Переважними умовами є: 1екв. тіоаміду (XXIV), оброблений 1екв. KОtВu, 1екв. Me п-тозилату у ТГФ. Одержання триазолу: Стадія (І): Тіоімідат (XXV) обробляли гідразидом (XIII) у придатному розчиннику, типово в етанолі при підвищеній температурі, одержуючи сполуку формули (І), необов'язково в присутності кислотного каталізатора такого як TFA, p-TSA. Переважними умовами є: 1екв. тіоімідату (XXV), 1екв. гідразиду (XIII), в етанолі при кипінні протягом 2 годин. Стадія (m): тіоамід (XXIV) обробляли гідразидом (XIII) у придатному розчиннику, типово у нБутан-1-олі при підвищеній температурі, одержуючи сполуку формули (І), необов'язково в присутності кислотного каталізатора такого як TFA, p-TSA. Переважними умовами є: 1екв. Тіоаміду (XXIV), 1екв. гідразиду (XIII), у нбутан-1-олі при кипінні протягом 18 годин. Сполуки, придатні для використання як сполуки (XXII), є відомими з літератури або можуть бути одержані, використовуючи стандартну методологію, наприклад дивіться [С. Apfel і інш., J. Med. Chem. 44(12), 1847-1852, 2001, С. Р. Lang і інш., W02002008228, F.lshikawa, J. Med. Chem. 28 (10), 1387-93, 1985 або Uskokovic, M. І інш., Журнал Органічної хімії (1965), 30(9), 3111-14]. Для фахівців цієї галузі буде очевидним, що чутливі функціональні групи можуть бути захищені і піддані зняттю захисту протягом синтезу сполуки формули (І). Це може бути досягнуто звичайними методиками, наприклад, як описано в ["Захисні групи в органічному синтезі" T. W. Greene і P. Wutz, John Wiley і Sons Inc. 1991, проілюструвано прикладами 42-49 і 55-58]. Певні сполуки формули (І) можуть бути перетворені на альтернативні сполуки формули (І), 29 79674 використовуючи стандартні хімічні перетворення. Приклади їх проілюстровані нижче: Амінування (наприклад, приклади 40 і 41) Коли R1 містить відхідну груп у, таку як замісник хлору, він може реагувати з придатним аміном HNR2R3 у присутності придатної третинної амінної основи (Et3N, NMM або основи Хюніга) або основи лужного металу (K2СО3, Cs 2CO3) у придатному розчиннику (наприклад DMF, MeCN), необов'язково при підвищеній температурі. Переважно сполуку хлору обробляють надлишком HNR2R3, у присутності надлишку K2СО3 у D MF при 70°С. Відновлення (наприклад, приклади 50-54, 64 і 65) Сполуки, що містять карбонільну функціональну груп у можуть бути відновлені, використовуючи придатний відновлювальний агент такий як DIBAL або боран у придатному розчиннику такому як етер або ТГФ при або між кімнатною температурою і температурою кипіння реакційної суміші. Переважно, сполуку аміду обробляють за допомогою 10екв. борану у ТГФ при кипінні, з наступною обробкою надлишком НСІ при кипінні. Відновне амінування (наприклад, приклади 6981 і 84-90) Сполуки формули (І), що містять хімічноактивний атом N, можуть реагувати з альдегідом або кетоном, згідно з способами, описаними в стадії (с). Переважно, амін формули (І) обробляють надлишком суміші альдегід/кетон і 2екв. Na(OAc)3BH у DCM, необов'язково в присутності надлишку Et3N і оцтової кислоти, при кімнатній температурі протягом до 18 годин. Оксидування (наприклад, коли W=S) Сполуки формули (І), що містять атом сірки можуть бути оксидовані, використовуючи придатний оксидувальний агент такий як пероксид водню або мета-хлорпербензойну кислоту в придатному розчиннику такому як трифтороцтова кислота або 1,1,1,3,3,3-Гексафторпропан-2-ол в діапазоні температур 0-25°С. При оксидуванні до одержання сульфоксиду (W=S(O)1), переважно сульфід формули (І) обробляють за допомогою 1-1,2екв. 30% водного розчину пероксиду водню в 1,1,1,3,3,3Гексафторпропан-2-олі при кімнатній температурі протягом до 1 години. При оксидуванні до одержання сульфону (W=S(O)2), переважно сульфід формули (І) обробляють за допомогою 2-3екв. 30% водного розчину пероксиду водню в трифтороцтовій кислоті протягом періоду до 1 години. (Альтернативно, сульфоксид (W=S(O)1), наведений вище може бути оксидований з одержанням сульфону (W=S(O)2), використовуючи 1-2екв. 30% водного розчину пероксиду водню в три фтороцтовій кислоті протягом до 1 години). Згідно з представленим винаходом, надалі забезпечується проміжна сполука формули (II): 30 проміжна сполука формули (III): проміжна сполука формули (X): проміжна сполука формули (XV): проміжна сполука формули (XXIV): проміжна сполука формули (XXV): де V, W, X, Υ, Ζ, кільця А і В, LG і n мають значення такі як визначено вище. Сполуки представленого винаходу є придатними для використання, тому що вони мають фармакологічну дію у тварин. Особливо вони корисні в лікуванні ряду станів, що включають агресивність, хворобу Альцгеймера, нервову анорексію, тривогу, тривожний розлад, астму, атеросклероз, аутизм, серцевосудинне захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріемію), катаракту, захворювання центральної нервової системи, цереброваскулярну ішемію, цироз, когнітивний роз 31 79674 лад, хворобу Кушінга, депресію, цукровий діабет, дисменорею (первинну та вторинну), блювоту (включаючи нудоту, що виникає при їзді), ендометріоз, шлунково-кишкове захворювання, глаукому, гінекологічне захворювання, серцеве захворювання, затримку внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), ішемію, ішемічне захворювання серця, пухлини легень, розлад сечовипускання, міжменструальний біль, новоутворення, ниркову токсичність, не-інсулін залежний діабет, ожиріння, обсесивно/компульсивний розлад, окулярну гіпертонію, передеклампсію, передчасну еякуляцію, передчасні (недоношену вагітність) пологи, легеневі захворювання, хворобу Рейно, захворювання нирок, ниркову недостатність, чоловічу або жіночу статеву дисфункцію, септичний шок, розлад сну, ушкодження спинного мозку, тромбоз, інфекції сечостатевого тракту або сечокаменеве захворювання. Особливий інтерес представляє дисменорея (первинна або вторинна), більш особливо, первинна дисменорея. Таким чином, відповідно до іншого аспекту винаходу, забезпечується спосіб лікування дисменореї, що включає призначення терапевтично ефективної кількості сполуки, згідно з винаходом, пацієнтові, що страждає від тривоги, серцевосудинного захворюваня (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передеклампсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно. Застосування сполук як лікарського засобу і застосування сполук представленого винаходу у виробництві лікарського засобу для лікування тривоги, серцевосудинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювоти (включаючи нудоту, що виникає при їзді), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передеклампсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів або хвороби Рейно, особливо дисменореї, також забезпечуються. Сполуки згідно з винаходом, що призначені для фармацевтичного застосування можуть призначатися у вигляді кристалічного або аморфного продуктів. Вони можуть бути о тримані, наприклад, у вигляді твердих тампонів, порошків або плівок за допомогою способів, таких як осаджування, кристалізація, сублімаційна сушка, сушка розпиленням або випаровуванням. Для цієї цілі може використовуватися мікрохвильове або радіочастотне висушування. Вони можуть призначатися поодинці або в комбінації з одним або більшою кількістю інших лікарських засобів (або у вигляд] будь-якої їх комбінації). Наприклад, сполуки представленого вина 32 ходу можуть призначатися в комбінації з оральним контрацептичним засобом. Альтернативно, вони можуть призначатися в комбінації з PDE5 інгібітором. Вони можуть також призначатися в комбінації з NO донором. Альтернативно, вони можуть призначатися в комбінації з L-аргініном або у вигляді солі аргініну. Сполуки представленого винаходу можуть також застосовуватися в комбінації з СОХ інгібітором. Взагалі вони будуть призначатися як композиція у сполученні з одним або більшою кількістю відповідного фармацевтично прийнятного ексціпієнтів. Термін "ексціпієнт", використовуваний тут, описує будь-який інгредієнт, відмінний від сполуки винаходу. Вибір ексціпієнта у значній мірі буде залежати від специфічного способу введення, впливу ексціпієнта на розчинність і стабільность і характеру дозованої форми. Фармацевтичні композиції, прийнятні для доставки сполук представленого винаходу та способи їх одержання будуть очевидні для фахівців даної галузі. Такі композиції та способи їх одержання можуть бути знайдені, наприклад, в ["Remington's Pharmaceutical Sciences", 19-е Видання (Mack Publishing Company, 1995)]. Таким чином, згідно з іншим аспектом представленого винаходу, забезпечується фармацевтична композиція, що включає сполуку формули (І) у комбінації з фармацевтично прийнятним ад'ювантом, розчинником або носієм. Сполуки згідно з винаходом можуть вводитися оральним шляхом. Оральне введення може включати ковтання, внаслідок чого сполука потрапляє в шлунково-кишковий тракт, або може застосовуватися букальне або сублінгвальне введення для того, щоб сполука потрапляла в кров безпосередньо з рота. Рецептури, прийнятні для орального введення включають тверді композиції, такі як таблетки, капсули, що містять частинки, розчини або порошки, лозенги (включаючи, рідинонаповнені), жувальні гумки, мульти- та наночастинки, гелі, твердий розчин, ліпосоми, плівки (включаючи, мукоадгезиви), овули, спреї і рідкі композиції. Рідкі рецептури включають суспензії, розчини, сиропи й еліксири. Такі рецептури можуть застосовува тися як наповнювачі в м'яких або твердих капсулах і зазвичай включати носій, наприклад, воду, етанол, поліетиленгліколь, пропіленгліколь, метилцелюлозу або придатне масло та один або більшу кількість емульсифікаторів і/або супендувальних агентів. Рідкі рецептури можуть також бути одержані відтворенням твердої речовини, наприклад, з саше. Сполуки згідно з винаходом можуть також прийматися у вигляді швидкорозчинних дозованих форм, дозованих форм, що швидко розпадаються, як це описано в [Досвідченій Думці в Терапевтичних Патентах, 11 (6), 981-986 Liang і Chen (2001)]. Для дозованих форм у ви гляді таблеток, у залежності від дози, лікарській засіб може складати від 1ваг.% до 80ваг.% дозованої форми, більш типово від 5ваг.% до 60ваг.% дозованої форми. На додаток до лікарського, засобу, таблетки, як правило, містять дезінтегрант. Приклади дезінтегран 33 79674 тів включають крохмальгліколят натрію, натрійкарбоксиметилцелюлозу, кальційкарбоксиметилцелюлозу, натрійкроскармелозу, кросповідон, полівінілпіролідон, метилцеллюлозу, мікрокристалічну целюлозу, заміщену нижчим алкілом гідроксипропілцелюлозу, крохмаль, прежелатинізований крохмаль та альгінат натрію. Як правило, дезінтегрант буде включати від 1ваг.% до 25ваг.%, переважно від 5ваг.% до 20ваг.% дозованої форми. Зв'язувальні агенти в основному використовуються для надання зв'язувальних властивостей таблетованій формі. Прийнятні зв'язувальні агенти включають мікрокристалічну целюлозу, желатин, цукри, поліетиленгліколь, природні і синтетичні смоли, полівінілпіролідон, прежелатинізований крохмаль, гідроксипропілцелюлозу і гідроксипропілметилцелюлозу. Таблетки можуть також містити розчинники, такі як лактозу (моногідрат, моногідрат висушений розпиленням, безводний і т.п.), маніт, ксиліт, декстрозу, сахарозу, сорбіт, мікрокристалічну целюлозу, крохмаль і двоосновний фосфорнокислий кальцій. Таблетки можуть також необов'язково включати поверхнево-активні агенти, такі як лаурилсульфат натрію та полісорбат 80 та агенти для покращення ковзання, такі як діоксид кремнію та тальк. Якщо агенти присутні, поверхневі активні агенти можуть складати від 0,2ваг.% до 5ваг.% таблетки та агенти для покращення ковзання можуть складати від 0,2ваг.% до 1ваг.% таблетки. Таблетки також, як правило, містять змащувальні агенти, такі як стеарат магнію, стеарат кальцію, стеарат цинку, стеарилфумарат натрію і суміші стеарату магнію з лаурилсульфатом натрію. Змащувальні агенти, як правило, складають від 0,25ваг.% до 10ваг.%, переважно від 0,5ваг.% до 3ваг.% таблетки. Інші можливі інгредієнти включають антиоксиданти, фарбувальні агенти, ароматизатори, консерванти і смакові агенти. Типові таблетки містять приблизно до 80% лікарської речовини, приблизно від 10ваг.% до приблизно 90ваг.% зв'язувального агента, приблизно від 0ваг.% до приблизно 85ваг.% розчинника, приблизно від 2ваг.% до приблизно 10ваг.% дезінтегранту та приблизно від 0,25ваг.% до приблизно 10ваг.% змащувального агента. Таблеткові суміші можуть бути вироблені безпосереднім пресуванням або за допомогою валика, для формування таблеток. Таблеткові суміші або порції сумішей можуть бути альтернативно одержані вологим-, сухим- або гранулюванням з розплаву, твердінням розплаву або екструзією, перед таблетуванням. Кінцева композиція може включати один або декілька шарів і може бути з покриттям або без покриття; може бути навіть інкапсульована. Склад таблеток обговорений у ["Pharmaceutical Dosage Forms: Tablets, Vol.1", Η. Lieberman і L. Lachman, Marcel Dekker, N. Y., N. Y., 1980 (ISBN 0-8247-6918-Х)]. Тверді композиції для орального прийому, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, 34 контрольоване-, цільове та запрограмоване вивільнення. Прийнятні композиції модифікованого вивільнення для цілей винаходу описані в [патенті США №6,106, 864]. Деталі інших придатних методик вивільнення таких форм як високоенергетична дисперсія або у вигляді осмотичної дозованої форми і у вигляді покритих частинок, описані в [Verma та інш., Pharmaceutical Technology On-line, 25 (2), 1-14 (2001)]. Застосування жувальної гумки для досягнення контрольованого вивільнення описано в [WO 00/35298]. Сполуки згідно з винаходом можуть також вводитися безпосередньо в кровоток, у м'яз або у внутрішній орган. Прийнятні засоби для парентерального введення включають внутрішньовенні, внутрішньоартеріальні, інтраперитонеальні, інтратекальні, інтравентрикулярні, інтрауретральні, інтрастернапьні, інтракраніальні, внутрішньом'язові і підшкірні. Прийнятні пристрої для парентерального введення включають голкові (включаючи мікроголкові) інжектори, безголкові інжектори і засоби для введення шляхом вливання. Композиції для патентерального введення типово представляють собою водні розчини, що можуть містити ексціпієнти такі як солі, вуглеводи і буферні агенти (переважно до рН від 3 до 9), але, для деяких застосувань, вони можуть бути більш відповідно сформовані у вигляді стерильного неводного розчину або у вигляді сухої форми, яку необхідно застосовувати в комбінації з придатним розчинником таким як стерильна, апірогенна вода. Одержання придатних парентеральних композицій в стерильних умовах, наприклад, ліофілізацією, легко здійснюють за стандартними фармацевтичними методиками, добре відомими фа хівцям цієї галузі. Здатність до розчинності сполуки формули (І), використовувана при одержанні розчинів для парентерального введення може бути підвищена за допомогою відповідної технології, наприклад, використання високоенергетичних висушених розпиленням дисперсій [дивіться WO 01/47495] і/або за допомогою відповідних методик складання рецептур, таких як додавання агентів, здатних підвищувати розчинність. Композиції для парентерального введення можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, контрольоване-, цільове та запрограмоване вивільнення. Таким чином, сполуки згідно з винаходом можуть бути сформовані у вигляді твердої речовини, напівтвердої речовини або тіксотропної рідини для введення як імплантованого депо, що забезпечує модифіковане вивільнення активної сполуки. Приклади таких композицій включають покриті лікарським засобом стенти і мікросфери з полі(DL-)-молочно-когліколевої кислоти (PGLA). Сполуки згідно з винаходом можуть також призначатися місцево на шкіру, слизову оболонку, тобто, дермально або трансдермально. Типові композиції призначені для цієї цілі включають гелі, гідрогелі, лосьйони, розчини, креми, мазі, присип 35 79674 ки, пов'язки, піни, плівки, шкірні пластирі, пластинки, імплантати, тампони, волокна, бандажі та мікроемульсії. Можуть також використовуватися ліпосоми. Типові носії включають спирт, воду, мінеральне масло, рідкий вазелин, білий вазелин, гліцерин, поліетиленгліколь і пропіленгліколь. Можуть використовуватися підсилювачі проникнення - дивіться, наприклад, [J. Pharm. Sci., 88 (10), 955958 Finnin та Morgan (жовтень 1999)]. Інші засоби місцевого введення включають доставку з використанням іонтофорезу, електропорації, фонофорезу, сонофорезу і мікроголковою або безголковоюі ін'єкцією (наприклад, PowderjecÔ , BiojectÔ і т.д.). Композиції для місцевого введення можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, контрольоване-, цільове і запрограмоване вивільнення. Сполуки представленого винаходу можуть вводитися інтраназально або інгаляцією, типово в формі сухого порошку (або окремо, або у вигляді суміші, наприклад, сухої суміші з лактозою або частинок компоненту, змішаних, наприклад, з фосфоліпідами, такими як фосфатідилхолін) за допомогою інгалятору сухого порошку або у вигляді аерозольного спрею з контейнеру під тиском, помпи, аерозольного балону, пульверизатора (переважно, пульверизатора з використанням електрогідродинамічних елементів для одержання тонкодисперсного пилу) або розпилювача з або без використання придатного пропеленту такого як 1,1,1,2-тетрафторетан або 1,1,1,2,3,3,3гептафторпропан. Для інтраназального використання порошок може містити біоадгезийний агент, наприклад, хітозан або циклодекстрин. Контейнер під тиском, помпа, аерозольний балон, пульверизатор або розпилювач містять розчин або суспензію сполук згідно з винаходом, що містять, наприклад, етанол, водний розчин етанолу або придатний альтернативний агент для диспергування, розчинення або затриманого вивільнення активної речовини, пропелент(и), як розчинник, який може додатково містити довільну поверхнево-активну речовину, наприклад, триолеат сорбіту, олеїнову кислоту або олігомолочну кислоту. Перед використанням в композиції сухого порошку або в суспензії для інгаляції лікарську речовину мікронізують до розмірів, придатних для доставки інгаляцією (зазвичай вважається менше, ніж 5 мікронів). Мікронізація може досягатися за допомогою будь-якого з відповідних способів подрібнення, наприклад, змелюванням за допомогою гвинтового реактивного млина, змелюванням в реактивному млині з псевдозрідженим шаром, використанням надкритичної рідинної кристалізації з утворенням наночастинок, гомогенезацією високим тиском або сушкою розпилюванням. Капсули (зроблені, наприклад, з желатину або ГПМЦ), блістери та картриджі для використання в інгаляторі або інсуфляторі можуть містити порошкову суміш сполуки винаходу, придатну порошкову 36 основу, таку як лактоза або крохмаль та модифікатор ефективності, такий як 1-лейцин, маніт або стеарат магнію. Лактоза може бути у безводній формі або у формі моногідрату, переважно у формі останнього. Інші придатні ексціпієнти включають декстран, глюкозу, мальтозу, сорбіт, ксиліт, фруктозу, са харозу і трегалозу. Придатна композиція розчину для використання в розпилювачі із застосуванням електрогідродинамічних елементів для одержання тонкодисперсного пилу може містити від 1мкг до 20мг сполуки згідно з винаходом на запуск і об'єм такого запуску може змінюватися від 1мкл до 100мкл. Звичайна композиція може містити сполуку формули (І), пропіленгліколь, стерильну воду, етанол та хлорид натрію. Замість пропіленгліколю можуть використовуватися альтернативні розчинники, наприклад, гліцерин або поліетиленгліколь. Придатні ароматизатори, такі як ментол та левоментол або підсолоджувачі, такі як сахарин або сахарин натрію, можуть бути додані до тих композицій винаходу, що призначені для інгаляційного/інтраназального введення. Композиції для інгаляційного/інтраназального введення можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення, наприклад, полі-(DL)-молочно-когліколева кислота (PGLA). Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, контрольоване-, цільове і запрограмоване вивільнення. Сполуки згідно з винаходом можуть вводитися ректальним або вагінальним шляхом, наприклад, у формі супозиторіїв, песарій або клізми. Масло какао є традиційною основою супозиторіїв, але можуть використовуватися різні відповідні альтернативні ексціпієнти. Композиції для введення ректальним/вагінальним шляхом можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне, контрольоване-, цільове і запрограмоване вивільнення. Композиції для ректального/вагінального введення можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, контрольоване-, цільове і запрограмоване вивільнення. Сполуки винаходу можуть також вводитися безпосередньо до ока або до вуха, зазвичай у вигляді крапель мікронізованої суспензії в ізотонічному, рН доведеному, стерильному розчині солі. Інші сполуки, що прийнятні для введення очним шляхом та до вуха включають мазі, імплантати, що піддаються біодеструкції (наприклад, гемостатичні губки, колаген) або не піддаються біодеструкції (наприклад, силікон), пластинки, лінзи або доставлятися через партикулярні або везикулярні системи, такі як ніосоми або ліпосоми. Полімер, такий як поперечнозшита поліакрилова кислота, полівініловий спирт, гіалуронова кислота, полімер целюлози, наприклад, гідроксипропілметилцелюлоза, гідроксиетилцелюлоза або метилцелюлоза, 37 79674 або гетерополісахаридний полімер, наприклад, гелеподібна камедь може додаватись в поєднанні з консервантом, таким як хлорид бензалконію. Такі композиції можуть доставлятися з використанням іонтофорезу. Композиції для введення до ока/вуха можуть бути сформовані, для забезпечення негайного і/або модифікованого вивільнення. Композиції модифікованого вивільнення включають затримане-, тривале-, імпульсне-, контрольоване-, цільове і запрограмоване вивільнення. Сполуки згідно з винаходом можуть також бути об'єднані із здатними до розчинності високомолекулярними речовинами, такими як циклодекстрин або поліетиленгліколь-вмісними полімерами для поліпшення їх здатності до розчинності, швидкості розчинення, смаку, біодоступності і/або стабільності для використання в будь-якому з вищезгаданих способів введення. Комплекси лікарська речовина-циклодекстрин, наприклад, загалом є корисними для більшості дозованих форм та шля хів введення. Можуть використовуватися комплекси включення і комплекси невключення. Як альтернатива безпосередньому комплексоутворенню з лікарською речовиною, циклодекстрин може використовуватися як допоміжна добавка, тобто, як носій, розбавник або солюбілізатор. Зазвичай, найбільш використовуваними є альфа-, бета- та гама-циклодекстрини і приклади яких описані в [міжнародних патентних заявках WO-A-91/11172, WO-A-94/02518 та WO-A98/55148]. По мірі того, як це може бути бажаним призначати комбінацію активних сполук, наприклад, для цілей лікування специфічного захворювання або стану, в межах представленого винаходу, дві або більша кількість фармацевтичних композицій, принаймні, одна з яких містить сполуку згідно з винаходом, можуть бути легко об'єднані у формі набору, придатного для сумісного призначення композицій. Таким чином, набір винаходу включає дві або більше окремих фармацевтичні композиції, принаймні одна з яких містить сполуку формули (І) відповідно до винаходу і засоби для окремого збереження згаданих композицій, такі як контейнер, розділена пляшка або розділена упаковка з фольги. Прикладом такого набору є відома блістер упаковка, використовувана для упакування таблеток, капсул і т.п.. Набір винаходу є особливо прийнятним для введення різних дозованих форм, наприклад, оральним і перентеральним шляхом, для введення окремими композиціями з різними інтервалами дозування або для титрування окремих композицій для порівняння однієї з іншою. Для дотримання стандартів, набір типово включає інструкції по призначенню і може забезпечуватися так званою пам'яткою. Для введення людині, повна добова доза сполук згідно з винаходом буде типово знаходитися в діапазоні від приблизно 0,01 до приблизно 15мг/кг ваги тіла в залежності від способу введення. Повна добова доза може призначатися в одиничній дозі або розділених доз протягом дня. Дозування 38 засновані для введення людині середнього віку, що має вагу від приблизно 65кг до 70кг. Лікар може легко визначити дози для суб'єктів, вага яких виходить за межі цього діапазону, таких як дитина та людина похилого віку. Терміни "лікування" і "лікувати", що використовуються в контексті даної заявки, означають полегшення симптомів, усунення причинної обумовленості або на тимчасовій або постійній підставі, або попередження, або зниження появлення симптомів. Термін "лікування" (treatment) включає полегшення, усунення причинної обумовленості (або на тимчасовій або постійній основі) або попередження симптомів і розладів асоційованих з первинною і/або вторинною дисменореєю. Лікування (treatment) може бути попереджувальною, також як терапією на початку появлення симптомів. Сполуки представленого винаходу можуть бути перевірені в наборі аналізів, викладених нижче: 1.0 Фільтрувальний аналіз зв'язування V1A 1.1 Одержання мембрани Дослідження зв'язування рецептора виконували на клітинних мембранах, одержаних з СНО клітин, що стабільно експресують людський V1-A рецептор, (CHO-hV1-A). CHO-hVIA клітинна лінія люб'язно забезпечувалася згідно з умовами ліцензійного договору Marc Thibonnier, Департамент Медицини, Case Western Reserve University School of Medicine, Кливленда, Штату Огайо. CHO-hVIA клітини звичайно підтримувалися при 37°С у зволоженій атмосфері з 5% вмістом СО2 у DMEM/Hams F12 живильна суміш, доповнена 10% фетальною бичачою сироваткою, 2мМ L-глутаміну, 15мМ HEPES і 400мкг/мл G418. Для одержання в великих кількостях клітинних осадів, прикріплені CHO-hV| A клітини виростали до конфлуентності 90100% у 850см 2 циліндричних пляшках, що містять середовище DMEM/Hams F12 живильної суміші доповнене 10% фетальною бичачою сироваткою, 2мМ L-глутаміну і 15мм HEPES. Конфлуентні клітини CHO-hV1A промивали фосфатно забуференим сольовим розчином (PBS), збирали в охолодженому льодом PBS і центрифуговали при 1,000об/хвилину. Клітинні осади до використання зберігали при -80°С. Клітинні осади розморожували на льоді і гомогенізували в буфері для одержання мембран, що містить 50мМ Tris-HCI, pH 7,4, 5мМ МgСІ2 і доповнювали сумішшю інгібіторів протеаз, (Roche). Клітинний гомогенат центрифугували при 1000об/хвилину, протягом 10 хвилин, при 4°С і супернатант видаляли і зберігали на льоду. Осад, що залишився гомогенізували і ще раз центрифугували. Супернатанти об'єднували і центрифугували при 25,000 обертів на хвилину протягом 30 хвилин при 4°С. Осад ресуспендували у заморожувальному буфері, що складається з 50мМ Tris-HCI, pH 7,4, 5мМ МgСІ2 і 20% гліцерину і зберігали до використання у маленьких аліквотах при -80°С. Концентрацію білку визначали, використовуючи реагент Bradford і BSA як стандарт. 1.2 V1A Фільтрувальне зв'язування Лінійність білку, що витікає з дослідження зв'язування насичення виконували для кожної нової партії мембран. Концентрацію мембран вибирали таким чином, щоб вона забезпечувала специфічне 39 79674 зв'язування на лінійній частині кривої. Дослідження зв'язування насичення виконували, використовуючи різні концентрації [3Н]-аргінін вазопресину, [3H]-AVP (0,05нМ-100нМ) і визначали Kd і Вmах. Сполуки перевірені на їх дії на [3H]-AVP зв'язування з CHO-hVlA мембранами, (3Н-AVP; специфічна активність 65,5° Ku/ммол; NEN Life Sciences). Сполуки розчиняли у диметилсульфоксиді (DMSO) і розводили до робочої концентрації 10% ДМСО з буфером для аналізу, що містить 50мМ Tris-HCL, pH 7,4, 5мМ МgСІ2 і 0,05% BSA. 25мкл сполуки і 25мкл [3H]-AVP, (кінцева концентрація при або нижче Kd, визначеного для партії мембран, типово при 0,5нМ-0,6нМ) додавали до 96-лункового з круглим дном поліпропіленового планшету. Реакцію зв'язування ініціалізували за допомогою додавання 200мкл мембран і планшети обережно струшували протягом 60 хвилин при кімнатній температурі. Реакцію завершували шляхом швидкого фільтрування, використовуючи Filtermate Cell Harvester (Packard Instruments) через 96-лунковий GF/B UniFilter Планшет, який для попередження склеювання пептидів попередньо замочували в 0,5% поліетиленіміні. Фільтри промивали три рази, використовуючи 1мл охолодженого льодом промивочного буферу, що містить 50мМ Tris-HCL, рН 7,4 і 5мМ МgСІ2 . Планшети сушили .і до кожної лунки додавали 50мкл Microscint-0 (Packard Instuments). Планшети герметизували і підраховували на TopCount Microplate Сцинтиляційному лічильнику (Packard Instruments). Неспецифічне зв'язування (NSB) визначали, використовуючи 1мкМ неміченого d(CH2)5Tyr(Me)AVP ([b-меркаптоb,b-циклопентаметиленпропіоніл, 0-Ме-Туr2 , Аrg8]вазопресин) (bΜCΡVΡ), (Sigma). Дані радіолігандного зв'язування аналізували, використовуючи логістичне рівняння з чотирма параметрами з мінімумом, що наближається до 0%. Нахил був довільно установлений і падав при значеннях в діапазоні між -0,75 і -1,25 для наявних кривих. Специфічне зв'язування розраховували відніманням середньої NSB кількості імпульсів у хвилину від загальної кількості імпульсів у хвилину. Для досліджуваних сполук кількість зв'язків ліганда з рецептором була виражена як % зв'язок=(кількість імпульсів у хвилину зразку-означає NSB кількість імпульсів у хвилину)/специфічне зв'язування кількість імпульсів у хвилину х100. % зв'язків був нанесений як концентрація досліджуваної сполуки і сигмоїдна крива була пристосована. Константу дисоціації інгібування (Кi) розраховували, використовуючи рівняння Cheng-Prusoff: Ki=IC50/(1+[L]/Kd), де [L] означає концентрацію ліганда присутнього в лунці і Kd означає константу дисоціації радіоліганда, отриманого з Scatchard графічного аналізу. 2.0 V1-A Функціональний аналіз: Інгібування AVP/V1-A - R опосередковане Са2+ мобілізацією за допомогою FLIPR (зчитувач Флуоресцентного зображення планшетів) (Молекулярні Пристрої) Внутрішньоклітинне вивільнення кальцію вимірювали у CHO-hVIA клітинах, використовуючи FLIPR, що забезпечує швидке виявлення кальцію після активації рецептора. CHO-hVIA клітинна лінія люб'язно забезпечувалася згідно з умовами ліцензійного договору Marc Thibonnier, Департамент 40 Медицини, Case Western Reserve University School of Medicine, Кливленда, Штату Огайо. CHO-hVIA клітини звичайно підтримувалися при 37°С у зволоженій атмосфері з 5% вмістом СО2 у DMEM/Hams F12 живильній суміші, доповненої 10% фетальною бичачою сироваткою, 2мМ Lглутаміну, 15мМ HEPES і 400мкг/мл G418. Опівдні перед дослідженням, клітини висаджували у планшет з щільністю 20,000 клітин на лунку в чорні стерильні 96-лункові планшети з прозорим дном, для забезпечення огляду клітин і флуоресцентних вимірювань з дна кожної лунки. Промивочний буфер, що містить фосфатно забуферений сольовий розчин Дюльбекко (DPBS) і 2,5мМ пробенециду і барвник, що вводять, складається з культурального клітинного середовища, що містить 4мкМ Fluo3-AM (розчиненого у ДМСО і плюронієвій кислоті), (Молекулярні зонди) і 2,5мМ пробенециду, був одержаний свіжий у день проведення досліджень. Сполуки розчиняли у ДМСО і розводили в буфері для аналізу, що складається з DPBS, що містить 1% ДМСО, 0,1% BSA і 2,5мМ пробенециду. Клітини інкубували з 100мкл введеного барвника у кожну лунку протягом 1 години при 37°С у зволоженій атмосфері з 5% вмістом СО2. Після введення барвника клітини три рази промивали за допомогою 100мкл промивочного буферу, використовуючи пристрій Denley для промивання для планшетів. 100мкл промивочного буферу залишили в кожній лунці. Внутрішньоклітинну флуоресценцію виміряли, використовуючи FLIPR. Флуоресцентні зчитування отримували через 2 секундні інтервали з додаванням через 30 секунд 50мкл досліджуваної сполуки. Додаткові 155 вимірів через 2 секундні інтервали були потім взяті для виявлення, будьякої сполуки, що володіє агоністичною активністю. Потім додавали 50мкл аргінін вазопресину (AVP) таким чином, щоб кінцевий досліджуваний об'єм складав 200мкл. Подальші флуоресцентні зчитування збирали через 1 секундні інтервали протягом 120 секунд. Відповіді обмірювали як піки флуоресцентної інтенсивності (FI). Для фармакологічної характеристики віднімався базальний FI від кожної флуоресцентної відповіді. Для кривих залежності відповіді від дози AVP кожне значення відповіді було виражене як % відповіді на максимальну концентрацію AVP цього ряду. Для визначення значень ІС 50, кожне значення відповіді було виражене як % відповіді на значення AVP. Значення ІС50 було перетворене на модифіковану величину Kb, використовуючи ChengPrusoff рівняння, що бере до уваги агоністичну концентрацію, [А], агоніст ЕС 50 і нахил: Kb=ІС50 /(2+[А]/А50 ]n) 1/n-1, де [А] означає концентрацію AVP, А50 означає ЕС 50 AVP з кривої залежності відповіді від дози і n = нахил AVP кривої залежності відповіді від дози. Сполуки згідно з винаходом, можуть мати перевагу, як більш сильні, що мають більш довготривалу дію, мають більш широкий діапазон дії, більш стабільні, мають меншу кількість побічних ефектів або є більш селективними, або мають інші більш корисні властивості, ніж сполуки згідно з попереднім рівнем техніки. Таким чином винахід забезпечує: 41 79674 (і) сполукуформули (І) або її фармацевтично прийнятну похідну; (іі) спосіб одержання сполуки формули (І) або її фармацевтично прийнятної похідної; (ііі) фармацевтичну композицію, що включає сполуку формули (І) або її фармацевтично прийнятну похідну, разом з фармацевтично прийнятними ексціпієнтами, розчинником або носієм; (iv) сполуку формули (І) або її фармацевтично прийнятну похідну, для застосування як лікарського засобу; (ν) застосування сполуки формули (І) або її фармацевтично прийнятної похідної або їх композиції, для одержання лікарського засобу для лікування агресивності, хвороби Альцгеймера, нервової анорексії, тривоги, тривожного розладу, астми, атеросклерозу, аутизму, серцевосудинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), катаракти, захворювання центральної нервової системи, цереброваскулярної ішемії, цирозу, когнітивного розладу, хвороби Кушінга, депресії, цукрового діабету, дисменореї (первинної та вторинної), блювоти (включаючи нудоту, що виникає при їзді), ендометріозу, шлунковокишкового захворювання, глаукоми, гінекологічного захворювання, серцевого захворювання, затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), ішемії, ішемічного захворювання серця, пухлини легень, розладу сечовипускання, міжменструального болю, новоутворення, ниркової токсичності, не-інсулін залежного діабету, ожиріння, обсесивно/компульсивного розладу, окулярної гіпертонії, передеклампсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів, легеневих захворювань, хвороби Рейно, захворювання нирок, ниркової недостатності, чоловічої або жіночої статевої дисфункції, септичного шоку, розладу сну, ушкодження спинного мозку, тромбозу, інфекції сечостатевого тракту або сечокаменевого захворювання; (vi) застосування як у (ν), де захворюванням або розладом є тривога, серцевосудинне захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменорея (первинна і вторинна), ендометріоз, блювота (включаючи нудоту, що виникає при їзді), затримка внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструальний біль, передеклампсія, передчасна еякуляція, передчасні (недоношена вагітність) пологи або хвороба Рейно; (vii) застосування як у (ν), де захворюванням або розладом є дисменорея (первинна і вторинна); (viii) спосіб лікування ссавця, для лікування агресивності, хвороби Альцгеймера, нервової анорексії, тривоги, тривожного розладу, астми, атеросклерозу, аутизму, серцевосудинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), катаракти, захворювання центральної нервової системи, цереброваскулярної ішемії, цирозу, когнітивного розладу, хвороби 42 Кушінга, депресії, цукрового діабету, дисменореї (первинної та вторинної), блювоти (включаючи нудоту, що виникає при їзді), ендометріозу, шлунково-кишкового захворювання, глаукоми, гінекологічного захворювання, серцевого захворювання, затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), ішемії, ішемічного захворюванння серця, пухлини легень, розладу сечовипускання, міжменструального болю, новоутворення, ниркової токсичності, неінсулін залежного діабету, ожиріння, обсесивно/компульсивного розладу, окулярної гіпертонії, передеклампсії, передчасної еякуляції, передчасних (недоношеної вагітності) пологів, легеневих захворювань, хвороби Рейно, захворювання нирок, ниркової недостатності, чоловічої або жіночої статевої дисфункції, септичного шоку, розладу сну, ушкодження спинного мозку, тромбозу, інфекції сечостатевого тракту або сечокаменевого захворювання, що включає лікування згаданого ссавця ефективною кількістю сполуки формули (І) або її фармацевтично прийнятної похідної або її композицією; (іх) спосіб як у (vii), де захворюванням або розладом є тривога, серцево-судинне захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменорея (первинна і вторинна), ендометріоз, блювота (включаючи нудоту, що виникає при їзді), затримка внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструальний біль, передеклампсія, передчасна еякуляція, передчасні (недоношена вагітність) пологи або хвороба Рейно; (х) спосіб як у (vii), де захворюванням або розладом є дисменорея (первинна і вторинна); (хі) проміжні сполуки формул (II), (III), (X), (XV), (XXIV) і (XXV); (хіі) застосування комбінації сполуки формули (І) з оральним контрацептичним засобом для лікування дисменореї (первинної і/або вторинної); (хііі) застосування комбінації сполуки формули (І) з PDE5 інгібітором для лікування дисменореї (первинної і/або вторинної); (xi v) застосування комбінації сполуки формули (І) з NO донором для лікування дисменореї (первинної і/або вторинної); (xv) застосування комбінації сполуки формули (І) з L-аргініном для лікування дисменореї (первинної і/або вторинної); (xvi) застосування комбінації сполуки формули (І) з СОХ інгібітором для лікування дисменореї (первинної і/або вторинної). Винахід проілюстрований наступними препаративними прикладами і прикладами: Препаративний приклад 1: гідразид 3,4,5,6Тетрагідро-2Н-[1,2']біпіридиніл-4-карбонової кислоти 43 79674 Етиловий естер 3,4,5,6-Тетрагідро-2Н[1,2']біпіридиніл-4-карбонової кислоти (1г, 4,3ммол) [дивіться, посилання Farmaco, 1993, 48(10), 1439] розчиняли у метанолі (20мл), що містить гідрат гідразину (620мкл, 20ммол) і нагрівали при кипінні протягом 18 годин. Суміш охолоджували до кімнатної температури і випаровували під зниженим тиском. Одержану тверду речовину розтирали з пропан-2-олом, одержуючи вказану в заголовку сполуку у вигляді твердої речовини білого кольору (493мг). XIAT MC m/z 221 [M+H]+ Препаративний приклад 1b: Етиловий естер 3,4,5,6-Тетрагідро-2Н-[1,2']біпіридиніл-4карбонової кислоти Карбонат калію (52,5г, 0,379мол) завантажували у перемішуваний розчин 2-Бромпіридину (60г, 0,379мол) і Етилізоніпекотату (59,7г, 0,379мол) при температурі навколишнього середовища перед нагріванням до 120°С протягом 24 годин. Суміш охолоджували до кімнатної температури і у розчин завантажували пропан-2-ол. Реакційну суміш потім відфільтровували і використовували у препаративному прикладі 1с. Препаративний приклад 1с: гідразид 3,4,5,6Тетрагідро-2Н-[1,2']біпіридиніл-4-карбонової кислоти Гідрат гідразину (61,4мл, 1,265мол) завантажували до пропан-2-олового розчину етилового естеру 3,4,5,6-Тетрагідро-2Н-[1,2']біпіридиніл-4карбонової кислоти (0,253мол, 5мл/г) [дивіться посилання у Farmaco, 1993, 48(10), 1439], перед нагріванням при кипінні протягом 18 годин. Суміш охолоджували до кімнатної температури і потім до 10°С і продукт у вигляді твердої речовини білого кольору збирали за допомогою фільтрування (44,5г). XIAT MC m/z 221 [M+H]+ Препаративний приклад 2: гідразид 1Піримідин-2-іл-піперидин-4-карбонової кислоти Вказана в заголовку сполука була одержана з етилового естеру 1-Піримідин-2-іл-піперидин-4карбонової кислоти [дивіться Farmaco, 1993, 48(10), 1439] з 91% виходом, після процедури, описаної в препаративному прикладі 1. XIAT MC m/z 222 [M+H]+ 44 Препаративний приклад 3: 3,4,5,6-Тетрагідро2Н-[1,2']біпіридиніл-4-карбонової кислоти N'-(2хлорацетил)гідразид Гідразид, одержаний в Препаративному прикладі 1 (23,6г, 0,11мол) суспендували у ди хлорметані (500мл) і додавали 4-метилморфолін (17,7мл, 0,16мол). Суміш охолоджували, використовуючи ванну з льодом і додавали краплями хлорацетилхлорид (12,8мл, 0,16мол). Реакційну суміш нагрівали до кімнатної температури і перемішували протягом 3 годин. Одержану тверду речовину виділяли за допомогою фільтрування, промивали дихлорметаном і діетиловим етером і сушили під вакуумом, одержуючи вказану в заголовку сполуку (20,4г). РХМС: m/z ES+ 297 [М+Н]+ Препаративний приклад 3b: 3,4,5,6-Тетрагідро2Н-[1,2']біпіридиніл-4-карбонової кислоти N'-(2хлорацетил)гідразид Гідразид, одержаний в Препаративному прикладі 1с (5,0г, 23ммол) суспендували у дихлорметані (100мл) i додавали 4-метилморфолін (3,75мл, 34ммол). Суміш охолоджували, використовуючи ванну з льодом і додавали краплями хлорацетилхлорид (1,9мл, 24ммол). Реакційну суміш нагрівали до кімнатної температури і перемішували протягом 3 годин. Одержану тверду речовину виділяли фільтруванням, промивали дихлорметаном і сушили під вакуумом, одержуючи вказану в заголовку сполуку (2,2г). РХМС: m/z ES+ 297 [М+Н]+ Препаративний приклад 4: 1-Піримідин-2-ілпіперидин-4-карбонової кислоти N'-(2хлорацетил)гідразид Вказану в заголовку сполуку одержували з гідразиду одержаного в препаративному прикладі 2 і хлорацетилхлориду, з 96% виходом, використовуючи процедуру, описану в препаративному прикладі 3. ХІАТ МС m/z 298 [М+Н]+ Препаративний приклад 5: 4-(5-Хлорметил[1,3,4]оксадіазол-2-іл)-3,4,5,6-тетрагідро-2H[1,2']біпіридиніл 45 79674 Гідразид, одержаний в Препаративному прикладі 3 (20,4г, 69ммол), суспендували у оксихлориді фосфору (150мл) при 100°С протягом 4 годин. Суміш охолоджували і розчинник випаровували при зниженому тиску. Залишок розчиняли в етилацетаті і додавали до води. Водний шар підлуговували додаванням твердого гідрокарбонату натрію і фази відділяли. Водну фазу екстрагували за допомогою етилацетату (х2) і об'єднані органічні шари сушили над сульфатом магнію і випаровували при зниженому тиску. Виділений матеріал розтирали з діетиловим етером, одержуючи вказану в заголовку сполуку у вигляді твердої речовини бежевого кольору (15г). 1 Н ЯМР (400МГц, CD3OD): d 1,91 (м, 2Н), 2,19 (м, 2Н), 3,14 (м, 2Н), 3,30 (м, 1Н), 4,29 (м, 2Н), 4,86 (С, 2Н), 6,69 (м, 1Н), 6,89 (д, 1Н), 7,58 (м, 1Н), 8,08 (д, 1Н) Препаративний приклад 5b: 4-(5-Хлорметил[1,3,4]оксадіазол-2-іл)-3,4,5,6-тетрагідро-2Н[1,2']біпіридиніл Гідразид, одержаний в Препаративному прикладі 3 (50,0г, 169ммол), суспендували в ацетонітрилі (250мл) і охолоджували, використовуючи ванну з льодом. Додавали краплями ангідрид трифторметансульфонової кислоти (29,9мл, 177ммол) при Τ
ДивитисяДодаткова інформація
Назва патенту англійськоюTriazol compounds suitable for use in therapeutics
Автори англійськоюBryans Justin Stephen, Johnson Patrick Stephen, Ryckmans Thomas, Stobie Alan
Назва патенту російськоюСоединения триазола, пригодные для использования в терапии
Автори російськоюБраянс Джастин Стивен, Джонсон Патрик Стивен, Рикманс Томас, Стоуби Алан
МПК / Мітки
МПК: C07D 243/00, A61P 29/00, A61K 31/55, C07D 249/00, C07D 267/00, C07D 487/04, C07D 513/04, C07D 401/04, A61K 31/501, C07D 413/14, C07D 498/04, A61K 31/4427
Мітки: терапії, триазолу, придатні, сполуки, використання
Код посилання
<a href="https://ua.patents.su/62-79674-spoluki-triazolu-pridatni-dlya-vikoristannya-v-terapi.html" target="_blank" rel="follow" title="База патентів України">Сполуки триазолу, придатні для використання в терапії</a>
Попередній патент: Пристрій для геофізичної розвідки
Наступний патент: Пачка з шарнірною кришкою для стрижнеподібних курильних виробів і заготовка для пачки
Випадковий патент: Розхилюючий робочий орган












