7-аміноалкіліденілгетероциклічні хінолони та нафтиридони
Номер патенту: 93672
Опубліковано: 10.03.2011
Автори: Вейднер-Уеллс Мішель Енн, Грант Юджин Б., III, Су Сяодонг, Масілаг Марк Дж., Су Сяокін, Пейджет Стівен Девід
Формула / Реферат
1. Сполука Формули І:
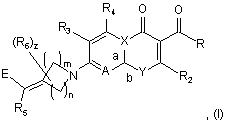
де:
n означає ціле число від 1 до 3;
m означає ціле число від 1 до 3;
z означає ціле число від 0 до 3;
R вибраний з водню, гідрокси та алкокси;
R2 являє собою водень;
R3 та R4 незалежно вибрані з водню, галогену, аміно, гідрокси, алкокси, алкілтіо, алкілу, алкенілу та алкінілу;
R5 вибраний з водню, гідрокси, галогену, алкілу, арилу, алкокси, ціано, CO2R13 та алкілтіо;
R6 незалежно вибраний з алкілу, гідрокси, алкокси, алкілтіо, алкенілу, алкінілу, арилу, алкоксііміно та галогену; або R5 та R6 сполучені разом, утворюючи 4-7-членне карбоциклічне кільце, в якому кожний кільцевий атом вуглецю може бути необов'язково заміщений R12, де R12 вибраний з групи, що включає галоген, аміно, гідрокси, алкокси, алкілтіо, алкіл, алкеніл, алкініл, оксо, алкоксііміно та гідроксііміно;
R13 являє собою водень, алкіл, арил або захисну групу карбонової кислоти;
Е вибраний з групи, що включає:
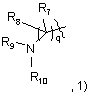
де
q означає ціле число від 1 до 3;
R7 та R8 кожний незалежно вибраний з водню та алкілу, або R7 та R8 сполучені разом, утворюючи 3-6-членне карбоциклічне кільце, або
R7 чи R8 можуть бути приєднані незалежно або до R9, або до R10, утворюючи гетероциклічне кільце, що містить атом азоту, до якого приєднані R9 або R10, де
R9 та R10 кожний незалежно вибраний з водню, алкілу, арилу, арилалкілу, ацилу, алкоксикарбонілу або сульфонілу, або альтернативно R9 та R10 сполучені разом, утворюючи гетероциклічне кільце, що містить атом азоту, до якого вони приєднані;
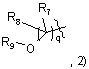
де
q є таким, як визначено вище;
R7 та R8 кожний незалежно вибраний з водню та алкілу, або R7 та R8 сполучені разом, утворюючи 3-6-членне карбоциклічне кільце, та R9 вибраний з водню, алкілу, ацилу, алкоксикарбонілу або сульфонілу; та
3) алкеніл;
А вибраний з N та C(R11), де R11 вибраний з водню, алкілу, галогену, гідрокси, алкокси, алкілтіо та ціано;
X вибраний з С та N, де, якщо X являє собою С, а являє собою подвійний зв'язок та b являє собою простий зв'язок, та, якщо X являє собою N, а являє собою простий зв'язок та b являє собою подвійний зв'язок; та
Y вибраний з N(R1) та C(R1), за умови, що, коли Y являє собою N(R1), X являє собою С, та, коли Y являє собою C(R1), X являє собою N, де R1 вибраний з С3-С6циклоалкілу, С4-С6гетероциклоалкілу, алкілу, алкену, 6-членного арилу та 6-членного гетероарилу; за умови, що
якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), тоді R11 та R1 можуть бути сполучені, утворюючи 6-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами;
якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), тоді R2 та R1 можуть бути сполучені, утворюючи моноциклічне або біциклічне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами; або
якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), потім R2 та R можуть бути сполучені, утворюючи 5-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами;
або її оптичний ізомер, діастереомер або енантіомер; її фармацевтично прийнятна сіль, гідрат або проліки.
2. Сполука за п. 1, в якій А являє собою С(ОСН3), C(OCHF2), СН, ССl або N.
3. Сполука за п. 1, в якій А являє собою C(R11), X являє собою С, Y являє собою N(R11) та R11 і R1 можуть бути сполучені, утворюючи 6-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами.
4. Сполука за п. 1, в якій Y являє собою N(R1) та R1 вибраний з С3-С6циклоалкілу або 6-членного гетероциклічного кільця.
5. Сполука за п. 1, в якій Е являє собою
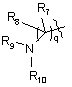 .
.
6. Сполука за п. 1, в якій m означає 1 та n означає 1, m означає 2 та n означає 2 або m означає 1 та n означає 3.
7. Сполука за п. 1, в якій z означає 0 або R6 являє собою метил та z означає 1.
8. Сполука за п. 4, в якій R7 та R8 являють собою водень.
9. Сполука за п. 7, в якій q означає 1.
10. Сполука за п. 8, в якій R9 являє собою водень, метил або етил та R10 являє собою водень.
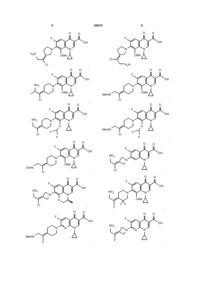
11. Сполука за п. 1, вибрана з групи, що включає:
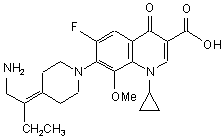 ,
,
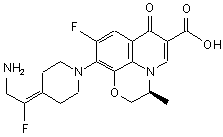 ,
,
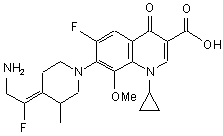 ,
,
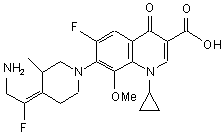 ,
,
 ,
,
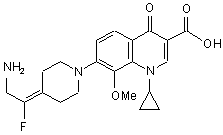 ,
,
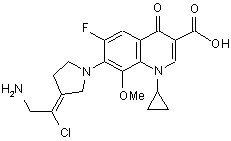 ,
,
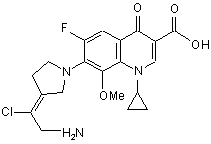 ,
,
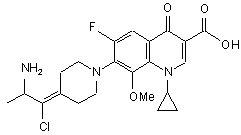 ,
,
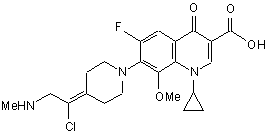 ,
,
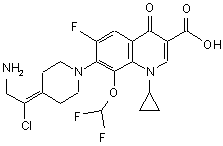 ,
,
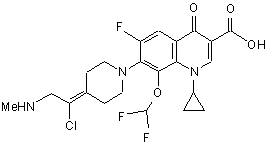 ,
,
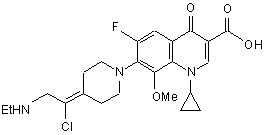 ,
,
 ,
,
 ,
,
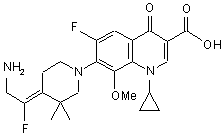 ,
,
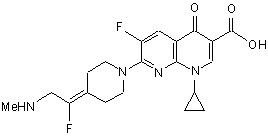 ,
,
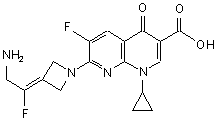 ,
,
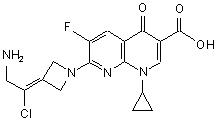 ,
,
 ,
,
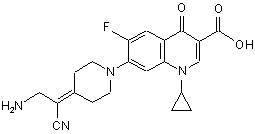 .
.
12. Сполука за п. 1, що має формулу:
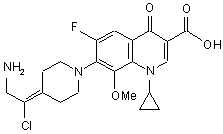 .
.
13. Сполука за п. 1, що має формулу:
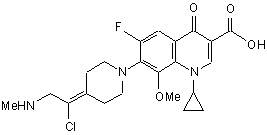 .
.
14. Сполука за п. 1, що має формулу:
 .
.
15. Спосіб лікування суб'єкта зі станом, який викликаний або якому сприяє бактеріальна інфекція, який включає введення зазначеному ссавцю терапевтично ефективної кількості сполуки за п. 1.
16. Спосіб попередження стану, який викликаний або якому сприяє бактеріальна інфекція, у суб'єкта, що цього потребує, який включає введення суб'єкту профілактично ефективної дози фармацевтичної композиції сполуки за п. 1.
Текст
1. Сполука Формули І: R4 O O R3 X (R6)z R a m A E N R2 b Y 2 3 93672 3) алкеніл; А вибраний з N та C(R11), де R11 вибраний з водню, алкілу, галогену, гідрокси, алкокси, алкілтіо та ціано; X вибраний з С та N, де, якщо X являє собою С, а являє собою подвійний зв'язок та b являє собою простий зв'язок, та, якщо X являє собою N, а являє собою простий зв'язок та b являє собою подвійний зв'язок; та Y вибраний з N(R1) та C(R1), за умови, що, коли Y являє собою N(R1), X являє собою С, та, коли Y являє собою C(R1), X являє собою N, де R1 вибраний з С3-С6циклоалкілу, С4-С6гетероциклоалкілу, алкілу, алкену, 6-членного арилу та 6-членного гетероарилу; за умови, що якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), тоді R11 та R1 можуть бути сполучені, утворюючи 6-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами; якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), тоді R2 та R1 можуть бути сполучені, утворюючи моноциклічне або біциклічне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами; або якщо А являє собою C(R11), X являє собою С та Y являє собою N(R1), потім R2 та R можуть бути сполучені, утворюючи 5-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами; O 4 або її оптичний ізомер, діастереомер або енантіомер; її фармацевтично прийнятна сіль, гідрат або проліки. 2. Сполука за п. 1, в якій А являє собою С(ОСН3), C(OCHF2), СН, ССl або N. 3. Сполука за п. 1, в якій А являє собою C(R11), X являє собою С, Y являє собою N(R11) та R11 і R1 можуть бути сполучені, утворюючи 6-членне гетероциклічне кільце, необов'язково заміщене однією або більше алкільними групами. 4. Сполука за п. 1, в якій Y являє собою N(R1) та R1 вибраний з С3-С6циклоалкілу або 6-членного гетероциклічного кільця. 5. Сполука за п. 1, в якій Е являє собою R7 R8 R9 q N R10 . 6. Сполука за п. 1, в якій m означає 1 та n означає 1, m означає 2 та n означає 2 або m означає 1 та n означає 3. 7. Сполука за п. 1, в якій z означає 0 або R6 являє собою метил та z означає 1. 8. Сполука за п. 4, в якій R7 та R8 являють собою водень. 9. Сполука за п. 7, в якій q означає 1. 10. Сполука за п. 8, в якій R9 являє собою водень, метил або етил та R10 являє собою водень. 11. Сполука за п. 1, вибрана з групи, що включає: O O F O F OH NH2 OH NH2 N N N N O OMe CH2CH3 , O F , O O F O F OH NH2 OH NH2 N N N N OMe OMe F , O F , O O O F OH NH2 OH NH2 N N O CH3 N N OMe , F , 5 93672 O 6 O O O F F OH OH N N N N H2N OMe OMe Cl Cl H2 N , O , O O F O F OH NH2 OH N N N N OMe OMe MeHN Cl Cl , O , O O F O F OH NH2 OH N N N N O O MeHN F Cl F Cl F F , O O O F O F OH OH NH2 N N , N N OMe EtHN Cl , O Cl , O O O F F OH OH NH2 NH2 N N OMe O Cl , O F O O F OH N , O F N N N OH NH2 N N N N MeHN F F , , 7 93672 O 8 O O O F F OH OH NH2 N NH2 N N Cl N N CN , O N , O F OH N N H2 N CN . 12. Сполука за п. 1, що має формулу: O O F OH NH2 O OH NH2 N N N N O OMe Cl Cl 13. Сполука за п. 1, що має формулу: O O F OH N N OMe Cl F F . 15. Спосіб лікування суб'єкта зі станом, який викликаний або якому сприяє бактеріальна інфекція, який включає введення зазначеному ссавцю терапевтично ефективної кількості сполуки за п. 1. 16. Спосіб попередження стану, який викликаний або якому сприяє бактеріальна інфекція, у суб'єкта, що цього потребує, який включає введення суб'єкту профілактично ефективної дози фармацевтичної композиції сполуки за п. 1. . MeHN O F . 14. Сполука за п. 1, що має формулу: Дана заявка є частковим продовженням заявки №10/937238, поданої 9 вересня 2004 року. Даний винахід відноситься до нових антимікробних сполук, композицій на їх основі та їх застосування. В хімічній та медичній літературі описані сполуки, які, як зазначено, є антимікробними, тобто, здатними до знищення або придушення росту або розмноження мікроорганізмів, таких як бактерії. Наприклад, такі антибактеріальні агенти описані в Antibiotics, Chemotherapeutics, and Antibacterial Agents for Disease Control (M. Greyson, editor, 1982), E. Gale et al., The Molecular Basis of Antibiotic Action 2d edition (1981), Recent Research Developments in Antimicrobial Agents & Chemotherapy (S. G. Pandalai, Editor, 2001), Quinolone Antimicrobial Agents (John S Wolfson., David С Hooper, Editors, 1989), та F. O'Grady, H. P. Lambert, R. G. Finch, D. Greenwood, Martin Dedicoat, "Antibiotic and Chemotherapy, 7th edn." (1997). Механізми дії цих антибактеріальних агентів відрізняються. Проте, загалом вважають, що вони діють за одним або більше способом: шляхом інгібування синтезу або відновлення оболонки клітин; шляхом зміни проникності оболонки клітин; шляхом інгібування синтезу протеїну; або шляхом інгібування синтезу нуклеїнових кислот. Наприклад, бета-лактамні антибактеріальні агенти діють шляхом інгібування основних пеніцилінзв'язуючих протеїнів (PBPs) в бактеріях, які відповідальні за синтез оболонки клітин. Як інший приклад, хінолони 9 діють, принаймні, частково шляхом інгібування синтезу ДНК, таким чином, перешкоджаючи відтворенню клітини. Фармакологічні характеристики антимікробних агентів та їх придатність для будь-якого наданого клінічного використання відрізняються. Наприклад, класи антимікробних агентів (та члени цих класів) можуть відрізнятися за 1) їх відносною ефективністю проти різних видів мікроорганізмів, 2) їх сприйнятливістю до розвитку резистентності мікроорганізмів та 3) їх фармакологічними характеристиками, такими як їх біодоступність та біорозподілення. Відповідно, вибір відповідного антимікробного агента в наданій клінічній ситуації вимагає аналізу багатьох чинників, включаючи вид залученого організму, бажаний спосіб введення, місце інфекції, яке лікують, та інші чинники. Проте, багато таких спроб щодо одержання поліпшених антимікробних агентів надають двозначні результати. Насправді, одержано декілька антимікробних агентів, які є дійсно клінічно прийнятними, виходячи з їх спектру антимікробної активності, усунення резистентності мікроорганізмів та фармакології. Таким чином, продовжує залишатися потреба в антимікробних агентах з широким спектром дії, які ефективні проти стійких мікробів. З рівня техніки відомо, що деякі 1,4дигідрохінолонові, нафтиридинові або споріднені гетероциклічні компоненти мають антимікробну активність та описані в наступних посиланнях: R. Albrecht Prog. Drug Research, Vol.21, p.9 (1977); J. Wolfson et al., "The Fluoroquinolones: Structures, Mechanisms of Action and Resistance, and Spectra of Activity In Vitro", Antimicrob. Agents and Chemother., Vol.28, p.581 (1985); G. Klopman et al. Antimicrob. Agents and Chemother., Vol.31, p.1831 (1987); M. P. Wentland et al., Ann. Rep. Med. Chem., Vol.20, p.145 (1986); J. B. Cornett et al., Ann. Rep. Med. Chem., Vol.21, p.139 (1986); P. B. Fernandes et al. Ann. Rep. Med. Chem., Vol.22, p.117 (1987); A. Koga, et al. "Structure-Activity Relationships of Antibacterial 6,7 - and 7,8-Disubstituted l-alkyl-l,4dihydro-4-oxoquinoline-3-carboxylic Acids" J. Med. Chem. Vol.23, pp.1358-1363 (1980); J. Μ. Domagala etal., J. Med. Chem. Vol.31, p.991 (1988); T. Rosen et al., J. Med. Chem. Vol.31, p.1598 (1988); B. Ledoussal et al., "Non 6-Fluoro Substituted Quinolone Antibacterials: Structure and Activity". J. Med. Chem. Vol.35, p.198-200 (1992); U. S. Patent 6329391; A. M. Emmerson et al., "The quinolones: Decades of development and use", J. Antimicrob. Chemother., Vol.51, pp.13-20 (2003); J. Ruiz, "Mechanisms of resistance to quinolones: target alterations, decreased accumulation and DNA gyrase protection" J. Antimicrob. Chemother. Vol.51, pp.1109-1117 (2003); Y. Kuramoto et al., "A Novel Antibacterial 8Chloroquinolone with a Distorted Orientation of the N1-(5-Amino-2,4-difluorophenyl) Group" J. Med. Chem. Vol.46, pp.1905-1917 (2003); публікація японської патентної заявки 06263754; публікація європейської патентної заявки 487030; публікація міжнародної патентної заявки WO 0248138; публікація міжнародної патентної заявки WO 9914214; публікація патенту США 2002/0049192; публікація 93672 10 міжнародної патентної заявки WO 02085886; публікація європейської патентної заявки 572259; публікація міжнародної патентної заявки WO 0136408; патент США 5677456; публікація європейської патентної заявки 362759; патент США 5688791; патент США 4894458; публікація європейської патентної заявки 677522; патент США 4822801; патент США 5256662; патент США 5017581; публікація європейської патентної заявки 304087; публікація міжнародної патентної заявки WO 0136408; публікація міжнародної патентної заявки WO 02085886; публікація японської патентної заявки 01090184; публікація міжнародної патентної заявки WO 9209579; публікація міжнародної патентної заявки WO 0185728; публікація європейської патентної заявки 343524; публікація японської патентної заявки 10130241; публікація європейської патентної заявки 413455; публікація міжнародної патентної заявки WO 0209758; публікація міжнародної патентної заявки WO 0350107; публікація міжнародної патентної заявки WO 9415933; публікація міжнародної патентної заявки WO 9222550; публікація японської патентної заявки 07300472; публікація міжнародної патентної заявки WO 0314108; публікація міжнародної патентної заявки WO 0071541; публікація міжнародної патентної заявки WO 0031062; та патент США 5869670. В WO 03050107 описані групи дигідрохінолонових, нафтиридинових та споріднених гетероциклічних антибактеріальних агентів. На особливу увагу заслуговує розкриття сполук формули де R8 та R8, являють собою водень, алкіл, заміщений алкіл, алкіламіно або арилалкіл, R9 являє собою водень, алкіл, алкіламіно, діалкіламіно, арил, арилалкіл або тригалогеналкіл, та X являє собою гідрокси, алкокси, ацилокси, аміно або заміщений аміно. В публікації європейського патенту 362759 описано 1,4-дигідрохінолонові та нафтиридинові антибактеріальні агенти формули в якому W являє собою С1-3 алкіліден та R5 і R6 являють собою водень або алкіл. Публікація міжнародної патентної заявки WO 99/14214 та патент США 6329391 розкривають хінолонові антибактеріальні агенти із замісниками С7-піперидиніл, С7-азетидиніл або С7-піролідиніл формули 11 Особливий інтерес представляють сполуки, в яких R7 являє собою аміно, аміноалкіл або заміщений аміноалкіл та R9 вибраний з водню, С1-С4 алкілу, С2-С6 алкенілу, С2-С6 алкінілу або С3-С6 конденсованого або спіроциклічного алкільного кільця. Для сполук із заміщеним піперидином в 7положенні хінолонкарбонової кислоти переважні замісники включають 3-аміно-4-метил, 3-аміно-4,4диметил, 3-аміно-4-спіроциклопропіл, 3-аміно-6циклопропіл, 3-амінометил, 4-амінометил та 3метиламіно. Для сполук із заміщеним піролідином в 7-положенні ядра хінолонкарбонової кислоти переважні замісники включають 3-(1-аміноетил), 3амінометил, 4-(1-аміноетил)-2,2-диметил та 2амінометил. Для сполук з азетидиновим замісником в 7-положенні хінолонкарбонової кислоти переважними прикладами є сполуки, що мають замісники, вибрані з 3-аміно, 3-амінометилу та 3-(1аміно-1-метил)етилу. В публікації європейського патенту 241206 А2 розкрито сполуки формули де В являє собою -СН2-, -(СН2)2- або -(СН2)з-, R4 являє собою водень, C1-С3 алкіл, гідрокси або C1-С3 алкокси, W являє собою гідрокси, C1-С3 алкокси або групу формули R5R6N-(CH2)n-, в якій п означає 0 або 1, та R5 і R6 є однаковими або різними та кожний являє собою атом водню, C1-С3 алкільну групу або арилалкільну групу, та m означає 1 або 2. Кожний символ є таким, як визначено в описі зазначеної вище публікації. Для піперидинового заміснику в 7-положенні хінолонкарбонової кислоти, переважними прикладами є сполуки, що мають замісники, вибрані з 4-аміно-3-метилу, 4метиламіно-З-метилу, 4-гідрокси-3-метилу. В публікації європейського патенту 0394553 В1 розкрито анти-вірусні сполуки формули 93672 12 де R21, R22 та R23 кожний незалежно являє собою атом водню, атом галогену, аміно, C1-С6 алкіл, C1-С8 алкокси або аміно C1-С8 алкіл та двоє з них можуть бути об'єднані один з одним, утворюючи спірокільце, та п означає 1 або 2. В публікації європейського патенту 0572259 Α1 розкрито анти-вірусні сполуки формули де R6 та R7 можуть бути однаковими або різними та кожний являє собою атом водню або нижчу алкільну групу, m означає 0 або 1, n' означає 1 або 2, n" означає 1, 2, 3 або 4, та R9 являє собою атом водню, нижчу алкільну групу, гідрокси групу або нижчу алкокси групу. В публікації міжнародної патентної заявки WO 9324479 розкрито сполуки формули де Ζ являє собою аміно радикал, R1 являє собою водень, (необов'язково гідроксильований нижчий алкільний) радикал, ацильний радикал, отриманий з карбонової кислоти, алкілвуглекислоти або арилсульфонової кислоти або ариламіно карбонільний радикал, R2 являє собою атом кисню, та n означає 0 або 1. Приклади бактеріальних інфекцій, резистентних до терапії антибіотиками, відомі з рівня техніки; на даний час вони є істотною загрозою охорони здоров'я для країн, що розвиваються. Розвиток резистентності мікроорганізмів (можливо в результаті інтенсивного використання антибактеріальних агентів протягом тривалих періодів часу) є зростаючою проблемою в медичній науці. "Резистентність" може бути визначена як існування організмів, в межах популяції певних видів мікроорганізмів, які менш сприйнятливі до дії наданого антимікробного агента. Ця резистентність є виключною проблемою в середовищах, таких як лікарні та будинки престарілих, де звичайно існують відносно високі ступені зараження та інтенсивне використання антибактеріальних агентів. Див., наприклад, W. Sanders, Jr. et al., "Inducible Betalactamases: Clinical and Epidemiologic Implications for the Use of Newer Cephalosporins", Review of Infectious Diseases, p.830 (1988). Відомо, що патогенні бактерії набувають резистентність за допомогою декількох визначених 13 механізмів, включаючи інактивацію антибіотика бактеріальними ферментами (наприклад, βлактамази, що гідролізують пеніцилін та цефалоспорини); видалення антибіотика, використовуючи насоси викачування; модифікацію мішені антибіотика шляхом мутації та генетичної рекомбінації (наприклад, резистентність до пеніциліну в Neiserria gonorrhoeae); та набуття легко переносимого гена із зовнішнього джерела для створення резистентної мішені (наприклад, резистентність до метициліну в Staphylococcus aureus). Існують певні грам-позитивні патогени, такі як резистентні до ванкоміцину Enterococcus faecium, які стійкі фактично до всіх комерційно доступних антибіотиків. Отже, існуючі антибактеріальні агенти мають обмежену здатність при подоланні загрози резистентності. Таким чином, буде корисним забезпечення нових антибактеріальних агентів, які можуть використовуватися проти стійких мікробів. Заявники знайшли нові групи хінолонів та споріднених сполук, які є ефективними проти резистентних мікробів та забезпечують істотні переваги активності відносно рівня техніки. Зокрема, винахід відноситься до сполук, що мають структуру Формули (І) в якій: n означає ціле число від 1 до 3; m означає ціле число від 1 до 3; z означає ціле число від 0 до 3; R вибраний з водню, гідрокси та алкокси; R2 являє собою водень; R3 та R4 незалежно вибрані з водню, галогену, аміно, гідрокси, алкокси, алкілтіо, алкілу, алкенілу та алкінілу; R5 вибраний з водню, галогену, алкілу, арилу, алкокси та алкілтіо; R6 незалежно вибраний з алкілу, гідрокси, алкокси, алкілтіо, алкенілу, алкінілу, арилу, алкоксііміно та галогену; або R5 та R6 сполучені разом, утворюючи 4-7-членне карбоциклічне кільце, в якому кожний кільцевий атом вуглецю може бути необов'язково заміщений R12, де R12 вибраний з групи, що включає галоген, аміно, гідрокси, алкокси, алкілтіо, алкіл, алкеніл, алкініл, оксо, алкоксііміно та гідроксііміно; Ε вибраний з групи, що включає: де q означає ціле число від 1 до 3; 93672 14 R7 та R8 кожний незалежно вибраний з водню та алкілу, або R7 та R8 сполучені разом, утворюючи 3-6-членне карбоциклічне кільце, або R7 чи R8 можуть бути приєднані незалежно або до R9, або до R10, утворюючи гетероциклічне кільце, що містить атом азоту, до якого приєднані R9 або R10, де R9 та R10 кожний незалежно вибраний з водню, алкілу, ацилу, алкоксикарбонілу або сульфонілу, або альтернативно R9 та R10 сполучені разом, утворюючи гетероциклічне кільце, що містить атом азоту, до якого приєднані; де q є таким, як визначено вище; R7 та R8 кожний незалежно вибраний з водню та алкілу, або R7 та R8 сполучені разом, утворюючи 3-6-членне карбоциклічне кільце, та R9 вибраний з водню, алкілу, ацилу, алкоксикарбонілу або сульфонілу; та 3) алкеніл; А вибраний з N та C(R11), де R11 вибраний з водню, алкілу, галогену, гідрокси, алкокси, алкілтіо та ціано; X вибраний з С та N, де, якщо X являє собою С, а являє собою подвійний зв'язок та b являє собою простий зв'язок, та якщо X являє собою N, а являє собою простий зв'язок та b являє собою подвійний зв'язок; та Υ вибраний з N(R1) та C(R1), за умови, що коли Υ являє собою N(R1), X являє собою С, та коли Υ являє собою C(R1), X являє собою N, де R1 вибраний з С3-С6 циклоалкілу, С4С6 гетероциклоалкілу, алкіл, алкену, 6-членного арилу та 6-членного гетероарилу; за умови, що якщо А являє собою C(R11), X являє собою С та Υ являє собою N(R1), тоді R11 та R1 можуть бути сполучені, утворюючи 6-членне гетероциклічне кільце, або якщо А являє собою C(R11), X являє собою С та Υ являє собою N(R1), тоді R2 та R] можуть бути сполучені, утворюючи моноциклічне або біциклічне гетероциклічне кільце, або якщо А являє собою C(R11), X являє собою С та Υ являє собою N(R1), тоді R2 та R можуть бути сполучені, утворюючи 5-членне гетероциклічне кільце; або їх оптичного ізомеру, діастереомеру або енантіомеру; їх фармацевтично прийнятної солі, гідрату або проліків. Крім того, в даному винаході також розглядаються способи використання сполук за винаходом як вихідних речовин. Було знайдено, що сполуки за даним винаходом та композиції, що містять ці сполуки, є ефективними антимікробними агентами проти широкого ряду патогенних мікроорганізмів з перевагами активності проти резистентних мікробів. Відповідно, даний винахід також відноситься до способу лікування суб'єкта зі станом, який викликаний або якому сприяє бактеріальна інфекція, який включає введення зазначеному ссавцю терапевтично ефективної кількості сполуки Формули 1. 15 Даний винахід, крім того, відноситься до способу попередження стану, який викликаний або якому сприяє бактеріальна інфекція, у суб'єкта, що цього потребує, який включає введення суб'єкту профілактично ефективної дози фармацевтичної композиції сполуки Формули 1. Даний винахід забезпечує сполуки Формули (І) Формула І де: а, b, n, m, z, R, R2, R3, R4, R5, R6, Α, Ε, X та Υ є такими, як визначено вище в Короткому описі суті винаходу. Щодо зазначеного вище опису, застосовують певні визначення, які вказано нижче. Якщо не зазначено інше, згідно зі стандартною номенклатурою, що використовується в цьому описі, спочатку описується кінцева частина описуваного бічного ланцюга, а потім суміжна з нею функціональність в напрямку до точки приєднання. Якщо не вказано інше, терміни "алкіл", "алкеніл" та "алкініл", які використовуються самі по собі або як частина заміщуючої групи, відносяться до прямих та розгалужених ланцюгів, що містять 1-8 атомів вуглецю або будь-яку кількість в межах цього діапазону. Термін "алкіл" відноситься до вуглеводнів з прямим або розгалуженим ланцюгом. "Алкеніл" відноситься до вуглеводню з прямим або розгалуженим ланцюгом з, принаймні, одним вуглець-вуглецевим подвійним зв'язком. "Алкініл" відноситься вуглеводню з прямим або розгалуженим ланцюгом з, принаймні, одним вуглецьвуглецевим потрійним зв'язком. Наприклад, алкільні радикали включають метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, третбутил, н-пентил, 3-(2-метил)бутил, 2-пентил, 2метилбутил, неопентил, н-гексил, 2-гексил та 2метилпентил. "Алкокси" радикали являють собою кисневі ефіри, утворені з описаних вище алкільних груп з прямим або розгалуженим ланцюгом. "Циклоалкільні" групи містять 3-8 кільцеві вуглеці та переважно 5-7 кільцеві вуглеці. Алкільна, алкенільна, алкінільна, циклоалкільна групи та алкокси групи можуть бути незалежно заміщені від одного або більше членами, вибраними з групи, що включає, але не обмежується, гідроксііміно, галоген, алкіл, алкеніл, алкініл, циклоалкіл, алкокси, оксо, алкоксііміно, арил, гетероарил, гетероцикло, CN, нітро, -OCORn, -OR13, -SR13, -SOR13, -SO2R13, COOR13, -NR13R14, -CONR13R14, -OCONR13R14, NHCOR13, -NHCOOR13 та -NHCONR13R14, де R13 та R14 незалежно вибрані з водню, алкілу, алкенілу, алкінілу, циклоалкілу, арилу, гетероарилу, гетероцикло, арилалкілу, гетероарилалкілу та гетероциклоалкілу, або альтернативно R14 та R15 можуть бути сполучені разом, утворюючи гетероциклічне кільце, що містить атом азоту, до якого вони приєднані. 93672 16 Термін "ацил", як використовується в даній заявці, який використовується сам по собі або як частина заміщуючої групи, означає органічний радикал, що містить від 2 до 6 атомів вуглецю (з прямим або розгалуженим ланцюгом), отримані з органічної кислоти видаленням гідроксильної групи. Термін "Ас", як використовується в даній заявці, який використовується сам по собі або як частина заміщуючої групи, означає ацетил. Термін "гало" або "галоген" означає фтор, хлор, бром або йод. (Моно-, ди-, три- та пер)галоалкіл являє собою алкільний радикал, заміщений шляхом незалежної заміни атомів водню на галоген. "Арил" або "Аr," який використовується сам по собі або як частина заміщуючої групи, означає карбоциклічний ароматичний радикал, включаючи, але не обмежуючись, феніл, 1- або 2-нафтил та подібні. Карбоциклічний ароматичний радикал може бути заміщений шляхом незалежної заміни 1-3 атомів водню на ньому на арил, гетероарил, галоген, ОН, CN, меркапто, нітро, аміно, С1-С8 алкіл, С2-С8-алкеніл, С1-С8-алкоксил, С1-С8-алкілтіо, С1-С8-алкіл-аміно, ді(С1-С8-алкіл)аміно, (моно-, ди-, три- та пер-)галоалкіл, форміл, карбокси, алкоксикарбоніл, С1-С8-алкіл-СО-О-, С1-С8-алкіл-CO-NHабо карбоксамід. Приклади арильних радикалів включають, наприклад, феніл, нафтил, біфеніл, фторфеніл, дифторфеніл, бензил, бензоїлоксифеніл, карбоетоксифеніл, ацетилфеніл, етоксифеніл, феноксифеніл, гідроксифеніл, карбоксифеніл, трифторметилфеніл, метоксіетилфеніл, ацетамідофеніл, толіл, ксиліл, диметилкарбамілфеніл та подібні. "Ph" або "РН" означає феніл. "Bz" означає бензоїл. "Гетероарил", який використовується сам по собі або як частина заміщуючої групи, відноситься до циклічного, повністю ненасиченого радикалу, що містить від п'яти до десяти атомів у кільці, з яких один кільцевий атом вибраний з S, О та N; 02 кільцеві атоми являють собою додаткові гетероатоми, незалежно вибрані з S, О та N; та інші кільцеві атоми являють собою вуглець. Радикал може бути приєднаний до залишку молекули через будь-який кільцевий атом. Приклади гетероарильних груп включають, наприклад, піридиніл, піразиніл, піримідиніл, піридазиніл, піроліл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, тіадіазоліл, триазоліл, триазиніл, оксадіазоліл, тієніл, фураніл, хінолініл, ізохінолініл, індоліл, ізотіазоліл, N-oкco-піридил, 1,1-діоксотієніл, бензотіазоліл, бензоксазоліл, бензотієніл, хінолініл-N-оксид, бензимідазоліл, бензопіраніл, бензизотіазоліл, бензизоксаоліл, бензодіазиніл, бензофуразаніл, індазоліл, індолізиніл, бензофурил, цинолініл, хіноксалініл, піролопіридиніл, фуропіридиніл (такий як фуро[2,3-с]піридиніл, фуро[3,2-b]піридиніл або фуро[2,3-b]піридиніл), імідазопіридиніл (такий як імідазо[4,5-b]піридиніл або імідазо[4,5с]піридиніл), нафтиридиніл, фталазиніл, пуриніл, піридопіридил, хіназолініл, тієнофурил, тієнопіридил та тієнотієніл. Гетероарильна група може бути заміщена шляхом незалежної заміни 1-3 атомів водню на ній на арил, гетероарил, галоген, ОН, CN, меркапто, нітро, аміно, С1-С8-алкіл, С1-С8 17 алкоксил, С1-С8-алкілтіо, С1-С8-алкіл-аміно, ді(С1С8-алкіл)аміно, (моно-, ди-, три- та пер-)галоалкіл, форміл, карбокси, алкоксикарбоніл, С1-С8-алкілСО-О-, С1-С8-алкіл-СО-NН- або карбоксамід. Гетероарил може бути заміщений моно-оксо з одержанням, наприклад, 4-оксо-1Н-хіноліну. Терміни "гетероцикл", "гетероциклічний" та "гетероцикло" відносяться до необов'язково заміщеної, повністю насиченої, частково насиченої або неароматичної циклічної групи, яка є, наприклад, 4-7-членною моноциклічною, 7-11-членною біциклічною або 10-15-членною трициклічною кільцевою системою, яка містить, принаймні, один гетероатом в, принаймні, одному кільці, що містить атоми вуглецю. Кожне кільце гетероциклічної групи, що містить гетероатом, може містити 1, 2 або 3 гетероатоми, вибрані з атомів азоту, атомів кисню та атомів сірки, де гетероатоми азоту та сірки також можуть бути необов'язково окиснені. Атоми азоту необов'язково можуть бути кватернізовані. Гетероциклічна група може бути приєднана через будь-який гетероатом або атом вуглецю. Гетероциклічна група може бути заміщена шляхом незалежної заміни 1-3 атомів водню на ній на арил, гетероарил, галоген, ОН, CN, меркапто, нітро, аміно, С1-С8-алкіл, С1-С8-алкоксил, С1-С8-алкілтіо, С1С8-алкіл-аміно, ді(С1-С8-алкіл)аміно, (моно-, ди-, три- та пер-)галоалкіл, форміл, карбокси, алкоксикарбоніл, С1-С8-алкіл-СО-О-, С1-С8-алкіл-CO-NHабо карбоксамід. Приклади моноцикл ічних гетероциклічних груп включають піролідиніл; оксетаніл; піразолініл; імідазолініл; імідазолідиніл; оксазолініл; оксазолідиніл; ізоксазолініл; тіазолідиніл; ізотіазолідиніл; тетрагідрофурил; піперидиніл; піперазиніл; 2оксопіперазиніл; 2-оксопіперидиніл; 2оксопіролідиніл; 4-піперидоніл; тетрагідропіраніл; тетрагідротіопіраніл; тетрагідротіопіраніл сульфон; морфолініл; тіоморфолініл; тіоморфолініл сульфоксид; тіоморфолініл сульфон; 1,3-діоксолан; діоксаніл; тієтаніл; тіїраніл; 2-оксазепініл; азепініл та подібні. Приклади біциклічних гетероциклічних груп включають хінуклідиніл; тетрагідроізохінолініл; дигідроізоіндоліл; дигідрохіназолініл (такий як 3,4-дигідро-4-оксо-хіназолініл); дигідробензофурил; дигідробензотієніл; бензотіопіраніл; дигідробензотіопіраніл; дигідробензотіопіраніл сульфон; бензопіраніл; дигідробензопіраніл; індолініл; хромоніл; кумариніл; ізохроманіл; ізоіндолініл; піпероніл; тетрагідрохінолініл; та подібні. Термін "карбоциклічний" відноситься до насиченого або ненасиченого, неароматичного, моноциклічного, вуглеводневого кільця з 3-7 атомами вуглецю. Заміщений арил, заміщений гетероарил та заміщений гетероцикл можуть також бути заміщені другим заміщеним арилом, другий заміщеним гетероарилом або другим заміщеним гетероциклом з одержанням, наприклад, 4-піразол-1-іл-фенілу або 4-піридин-2-іл-фенілу. Вказані кількості атомів вуглецю (наприклад, C1-C8 або C1-8) мають незалежно відноситися до кількості атомів вуглецю в алкільному або циклоалкільному фрагменті або в алкільній частині біль 93672 18 шого замісника, у префіксі якого буде зазначений алкіл. Якщо не вказано інше, мається на увазі, що визначення будь-якого замісника або змінної в конкретному положенні молекули є незалежним від їх визначень в будь-якому іншому положенні цієї самої молекули. Розуміють, що замісники та приклади заміщення в сполуках за даним винаходом можуть бути вибрані фахівцем в даній галузі техніки, щоб одержати сполуки, які є хімічно стійкими та які дійсно можуть бути синтезовані способами, що відомі з рівня техніки, а також тими способами, що наведено в даній заявці. Термін "гідроксизахисна група" відноситься до груп, відомих для цієї мети з рівня техніки. Гідроксизахисні групи, що звичайно використовуються, розкриті, наприклад, в Т. Н. Greene and P. G. M. Wuts, Protective Groups in Organic Synthesis, 2nd edition, John Wiley & Sons, New York (1991), який включений в дану заявку як посилання. Приклади гідроксизахисних груп включають, але не обмежуються, тетрагідропіраніл; бензил; метилтіометил; етилтіометил; півалоїл; фенілсульфоніл; трифенілметил; тризаміщений силіл, такий як триметилсиліл, триетилсиліл, трибутилсиліл, триізопропілсиліл, трет-бутилдиметилсиліл, три-третбутилсиліл, метилдифенілсиліл, етилдифенілсиліл, трет-бутилдифенілсиліл; ацил та ароїл, такі як ацетил, бензоїл, півалоїлбензоїл, 4метоксибензоїл, 4-нітробензоїл та арилацил. Коли сполуки за даним винаходом мають, принаймні, один стереогенний центр, вони відповідно можуть існувати як енантіомери. Коли сполуки мають два або більше стереогенних центрів, вони додатково можуть існувати як діастереомери. Крім того, деякі з кристалічних форм сполук можуть існувати як поліморфи, та, як такі, мається на увазі, включені в межі даного винаходу. Крім того, деякі зі сполук можуть утворювати сольвати з водою (тобто, гідрати) або звичайними органічними розчинниками, та також мається на увазі, що такі сольвати включені в межі даного винаходу. Деякі зі сполук за даним винаходом можуть мати транс та цис ізомери. Крім того, якщо способи одержання сполук за даним винаходом дають суміш стереоізомерів, ці ізомери можуть бути розділені традиційними способами, такими як препаративна хроматографія. Сполуки можуть бути одержані у вигляді окремих стереоізомерів або у рацемічній формі у вигляді суміші декількох можливих стереоізомерів. Нерацемічні форми можуть бути одержані або за допомогою синтезу або розділенням. Сполуки, наприклад, можуть бути розділені на їх складові енантіомери стандартними способами, такими як утворення діастереомерних пар шляхом утворення солі. Сполуки також можуть бути розділені за допомогою ковалентного сполучення з хіральною допоміжною речовиною, з наступним хроматографічним розділенням та/або кристалографічним розділенням, та видаленням хіральної допоміжної речовини. Альтернативно, сполуки можуть бути розділені, використовуючи хіральну хроматографію. Фраза "фармацевтично прийнятна сіль" означає одну або більше солей вільної основи або ві 19 льної кислоти, яка має бажану фармакологічну активність вільної основи або вільної кислоти, відповідно, та яка не є біологічно чи іншим чином неприйнятною. Ці солі можуть бути одержані з неорганічних або органічних кислот. Приклади неорганічних кислот включають соляну кислоту, азотну кислоту, бромистоводневу кислоту, сірчану кислота або фосфорну кислоту. Приклади органічних кислот включають оцтову кислоту, пропіонову кислоту, гліколеву кислоту, молочну кислоту, піровиноградну кислоту, малонову кислоту, бурштинову кислоту, яблучну кислоту, малеїнову кислоту, фумарову кислоту, винну кислоту, лимонну кислоту, бензойну кислоту, коричну кислоту, мигдальну кислоту, метансульфонову кислоту, етансульфонову кислоту, р-толуолсульфонову кислоту, бензолсульфонову кислоту, саліцилову кислоту та подібні. Прийнятні солі, крім того, є солями неорганічних або органічних основ, таких як КОН, NaOH, Ca(OH)2, Аl(OН)3, піперидин, морфолін, етиламін, триетиламін та подібні. В межі даного винаходу включені гідратовані форми сполук, які містять різні кількості води, наприклад, гідратні, гемігідратні та сесквігідратні форми. Даний винахід також включає в свої межі 93672 20 проліки сполук за даним винаходом. Взагалі, такі проліки будуть функціональними похідними сполук, які легко перетворюються in vivo на бажану сполуку. Таким чином, в способах лікування за даним винаходом термін "введення" включає лікування різних описаних розладів конкретно розкритою сполукою або сполукою, яка може не бути розкрита конкретно, але перетворюється на описану сполуку in vivo після введення пацієнту. Традиційні процедури виділення та одержання прийнятних пролікарських похідних описані, наприклад, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985. Термін "суб'єкт" включає, без обмеження, будь-яку тварину або генетично модифіковану тварину. Як конкретне втілення, суб'єктом є людина. Термін "резистентний до ліків " або "резистентність до ліків" відноситься до характеристик мікроба, який продовжує існувати в присутності доступного на даний час антимікробного агента, такого як антибіотик при його стандартній ефективній концентрації. В Таблиці 1 наведено необмежуючий перелік переважних сполук Формули І. 21 93672 22 23 93672 24 25 Загальна схема реакції одержання сполук При одержанні сполук за винаходом, порядок стадій реакцій може бути змінений, щоб збільшити вихід бажаного продукту. Крім того, фахівець в даній галузі техніки також визнає, що доцільний вибір реакцій, розчинників та температур є важливим компонентом для успішного синтезу. Хоча визначення оптимальних умов та т.п. є загальноприйнятою практикою, слід розуміти, що різні сполуки можуть бути одержані за допомогою подібних способів, використовуючи схеми, наведені нижче. Вихідні речовини, що використовуються при одержанні сполук за винаходом, є відомими, їх одержують за допомогою опублікованих способів синтезу або вони доступні у комерційних виробників. Вважають, що фахівець в галузі органічної хімії може легко здійснювати стандартні процедури з органічними сполуками без додаткової вказівки; тобто, здійснення таких процедур знаходиться в межах можливостей та практики фахівця в даній галузі техніки. Ці процедури включають, але не обмежуються, відновлення карбонільних сполук до їх відповідних спиртів, окиснення, ацилювання, ароматичні заміщення, як електрофільні, так і нуклеофільні, етерифікації, естерифікацію та омилення, тощо. Приклади цих процедур описані в стан 93672 26 дартних підручниках, таких як March, Advanced Organic Chemistry (Wiley), Carey and Sundberg, Advanced Organic Chemistry (Vol.2), Feiser & Feiser, Reagents for Organic Synthesis (16 volumes), L. Paquette, Encyclopedia of Reagents for Organic Synthesis (8 volumes), Frost & Fleming, Comprehensive Organic Synthesis (9 volumes) та подібні. Фахівець в даній галузі техніки прийме до уваги, що певні реакції краще всього проводити, коли інша функціональна група в молекулі замаскована або захищена, таким чином уникаючи будь-яких небажаних побічних реакцій та/або збільшуючи вихід реакції. Часто фахівець в даній галузі використовує захисні групи, щоб досягти таких збільшених виходів або уникнути небажаних реакцій. Приклади цих процедур можуть бути знайдені наприклад в Т. Greene, Protecting Groups in Organic Synthesis. Загальні методики одержання гетероциклічних циклів, які використовуються при одержанні сполук за винаходом, описані в наступних посиланнях, які всі включені в дану заявку (включаючи статті, наведені в посиланнях): патент США 6329391, публікація європейської патентної заявки 342849, публікація міжнародної патентної 27 Р"=захисна група У випадку, коли Е являє союбою та як R9, так і R10 являють собою водень, селективне алкілування бічного ланцюга аміну LXI також може бути проведене за допомогою захисту аміну стандартною захисною групою, такою як Вос, використовуючи реагенти та умови, очевидні фахівцю в даній галузі техніки, з отриманням LXII (Схема XXXVI). Захищений амін (LXII) потім обробляють надлишком (>2 еквівалентів) основи, такої як, без обмеження, гідрид натрію, у відповідному інертному розчиннику, такому як диметилформамід або тетрагідрофуран, з наступною обробкою відповідним алкілуючим агентом R9X, з одержанням Вос-захищеного вторинного аміну, як відповідного ефіру LXIII. Звичайно, реакцію проводять при температурах в діапазоні від -20°С до 60°С протягом від 1 до 48 годин залежно від реакційної здатності алкілуючого агента. Типові алкілуючі агенти включають алкіл йодиди (такі як метил йодид), алкіл броміди та алкіл сульфонати. Ефір LXIII може бути гідролізований при заявки WO 9711068, публікація європейської патентної заявки 195316, публікація європейської патентної заявки 1031569, патент US 6025370, публікація європейської патентної заявки 153828, публікація євро 93672 28 пейської патентної заявки 191451, публікація європейської патентної заявки 153163, публікація європейської патентної заявки 230053, публікація європейської патентної заявки 976749, публікація міжнародної патентної заявки WO 0118005, публікація міжнародної патентної заявки WO 9407873, патент патентної заявки США 4777253, публікація європейської патентної заявки 421668, публікація міжнародної патентної заявки WO 0248138, публікація європейської патентної заявки 230295, публікація міжнародної патентної заявки WO 9914214, публікація патентної заявки США 20020049223, публікація міжнародної патентної заявки WO 9921849, публікація міжнародної патентної заявки WO 9729102, публікація міжнародної патентної заявки WO 0334980, публікація міжнародної патентної заявки WO 0209758, публікація міжнародної патентної заявки WO 9619472, публікація німецької патентної заявки DE 3142854, публікація міжнародної патентної заявки WO 0334980, публікація міжнародної патентної заявки WO 0328665, публікація європейської патентної заявки 47005, публікація міжнародної патентної заявки WO 0311450 та публікація європейської патентної заявки 688772. Сполуки за даним винаходом можуть бути одержані за допомогою декількох способів. Різні методології для одержання сполук за винаходом показані на Схемі І нижче, де L являє собою групу, що відходить, таку як фтор або хлор: 29 У випадку, коли Е являє собою та, принаймні, один з R9 та R10 являють собою водень, може бути необхідним захистити термінальний азот, щоб провести селективне перетворення на бажаний продукт (Схема II). В цьому випадку, щоб замаскувати термінальний амін, як в сполуці V, можуть бути використані стандартні амінозахисні групи, відомі фахівцю в даній галузі Р"=захисна група 93672 30 техніки, такі як трет-бутоксикарбоніл (Вос), бензилоксикарбоніл (Cbz), бензил (Вn), 9флуоренілметоксикарбоніл (Fmoc), алілоксикарбоніл (Alloc), 2-триметилсилілетоксикарбоніл (Теос), N-форміл, N-ацетил, N-бензоїл або фталімід. Після приєднання бічного ланцюга, захисна група може бути видалена при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням бажаного продукту VII. VII потім може бути перетворений, наприклад за допомогою алкілування, на інші сполуки за винаходом VIII. Методики одержання сполук за винаходом, де X являє собою Η та Υ являє собою C(R]), наведені на Схемі III нижче: 31 Як і вище, коли Ε являє собою та, принаймні, один з R9 та R10 являють собою водень, може бути необхідним захистити термінальний азот, щоб провести селективне перетворення на бажаний продукт (Схема IV). В цьому випадку, щоб замаскувати термінальний амін, як в сполуці V, можуть бути використані стандартні амінозахисні групи, відомі фахівцю в даній галузі P” = захисна група У випадку, коли Е являє собою 93672 32 техніки, такі як трет-бутоксикарбоніл (Вос), бензилоксикарбоніл (Cbz), бензил (Вn), 9флуоренілметоксикарбоніл (Fmoc), алілоксикарбоніл (Alloc), 2-триметилсилілетоксикарбоніл (Теос), N-форміл, N-ацетил, N-бензоїл або фталімід. Після приєднання бічного ланцюга, захисна група може бути видалена при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням бажаного продукту XIII. XIII потім може бути перетворений, наприклад за допомогою алкілування, на інші сполуки за винаходом XIV. 33 93672 34 та як R9, так являють собою водень, селективне алкілування бічного ланцюга аміну LX1 також може бути проведене за допомогою захисту аміну стандартною захисною групою, такою як Вoc. використовуючи реагенти та умови, очевидні фахівцю в даній галузі техніки. і отриманням LXII (Схема XXXVI). Захищений амін (LXll) потім обробляють надлишком (>2 еквівалентів) основи, такої як, без обмеження, гідрид натрію, у відповідному інертному розчиннику, такому як диметилформамід або тетрагідрофуран, і наступною обробкою відповіданим алкілуючим агентом R9X, з одержанням Вoc шхищеного вторинного аміну, як відповідного ефіру LXllІ. Звичайно, реакцію проводять при температурах в діапазоні від -20°С до 60°С протягом від 1 до 48 годин залежно від реакційної здатності алкілуючого агента. Типові алкілуючі агенти включають алкіл йодиди (такі як метил йодид), алкіл броміди та алкіл сульфонатиі. Ефір LXIII може бути гідролізований при основних умовах з одержанням відповідної карбонової кислоти LXIV. Гідроліз ефіру може бути проведений за допомогою способів, відомих фахівцю в даній галузі техніки, зокрема, використовуючи основу, таку як гідроксид лужного металу (наприклад, гідроксид натрію) або карбонат лужного металу у прийнятному розчиннику, такому як вода, метанол, етанол або водні суміші спиртів, при температурі в діапазоні від 20°С до 100°С протягом від 1 до 48 годин. Видалення амінозахисної групи при умовах, відомих фахівцю в даній галузі техніки, надає вторинний амін LXV. У випадку, коли захисна група являє собою Вос, для захисту можуть бути використані, наприклад, реагенти, як наприклад з трифтороцтовою кислотою необов'язково з метилен хлоридом як співрозчинником або з соляною кислотою в діоксані. Р"=захисна група Інколи, аміни з бічними ланцюгами є недостатньо реакційноздатними, щоб приєднатися до гетероциклічного ядра (II або X), при умовах, які проілюстровані на Схемах І-IV, особливо, коли А являє собою C(R11), де R11 являє собою алкокси. Ядро може бути активоване для нуклеофільної атаки додаванням кислоти Льюїса, такої як, без обмеження, трифторид бору, триацетоксиборат та хлорид літію. Переважний спосіб активації описа ний в патенті США 5,157,117. Хінолонове ядро обробляють триацетоксиборатом, одержаним in situ, в розчиннику, такому як, без обмеження, оцтова кислота або пропіонова кислота, та нагрівали протягом 1-24год. при температурі між 60°С та 120°С. Діацил хінолінілборат (XV) виділяють фільтруванням після видалення розчинника. На Схемі V проілюстровано цей переважний спосіб активації. 35 93672 36 Інший переважний спосіб активації гетероциклічного ядра для нуклеофільної атаки, проілюстрований на Схемі XXXVII. В цьому способі, хінолон карбонову кислоту або ефірне похідне (тобто, сполуку II, де R являє собою водень або нижчий алкіл та L являє собою групу, що відходить) обробляють ефіратом трифториду бору, переважно в прийнятному розчиннику, такому як THF, протягом від 1 години до 48 годин при температурах в діапазоні від 0°С до 60°С. Після охолодження продукт LXVI може бути осаджений з реакційної суміші шляхом додавання прийнятного розчиннику, такого як діетиловий ефір, та хелат виділяють фільтруванням одержаної твердої речовини. Одержання попередника - аміну з бічним ланцюгом III На Схемі VI проілюстровано синтез аміну з бічним ланцюгом III, в якому Ε являє собою та заміна групи, що відходить, на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом 1-24год. при температурі між 0°С та 120°С перетворює спирт XVIII на амін XX. Видалення захисної групи, Р, при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, в якому Ε являє собою R7 та R8 являють собою водень, та q означає 1. Тризаміщені або тетразаміщені алкілідени XX можуть бути одержані за допомогою олефінізації Петерсона, Вітига або Вадсворта-Норнера-Емонса відповідно заміщений кетон (XVI) в розчиннику, такому як, без обмеження, тетрагідрофуран, диметилсульфоксид або метилен хлорид, протягом 1 24год. при температурі від -78°С до 120°С в присутності основи, такої як, без обмеження, трет-бутил літій, гідрид натрію або карбонат калію. Одержаний ефір (XVII) може бути відновлений відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію, в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом 1-24год. при температурі між 0°С та 120°С, з одержанням відповідного спирту XVIII, де q=1. Перетворення спирту XVIII на групу, що відходить, XIX, таку як, без обмеження, хлорид, бромід, мезилат або тозилат, при стандартних умовах R7 та R8 являють собою водень, та q означає 1. Альтернативно, безпосереднє заміщення спирту XVIII може бути проведене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом з одержанням XXI. Депротектування фталіміду (XXI) гідразином в розчиннику, такому як метанол або етанол, надає амін (XX), в якому R9 та R10 являють собою водень. Альтернативні способи депротектування включають обробку метиламіном в метанолі або 6N соляною кислотою. Захисна група, Р, може бути видалена з XXI при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, в якому R7 та R8 являють собою водень та R9 та Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу. 37 L - група, що відходить Р - захисна група Фахівцю в даній галузі техніки буде очевидно, що перетворення кетону XVI на олефін XVII, може привести до геометричних ізомерів (Схема VI), особливо у випадку, коли XVI є асиметричним (тобто, значення m не дорівнює п). В такому випадку, геометричні ізомери можуть бути розділені цілим рядом способів, відомих фахівцю в даній галузі техніки, включаючи селективну перекристалізацію, флеш хроматографію, високоефективну рідинну хроматографію та подібні. Також буде очевидним, що розділення може бути здійснене на різних стадіях процесу синтезу, включаючи стадії синтезу проміжних сполук XVII, XVIII, XIX або XXI, або альтернативно на кінцевій стадії синтезу продукту XX. На Схемі XXXVIII проілюстровано синтез аміну з бічним ланцюгом LXX, в якому Ε являє собою R5 являє собою ціано, R7 та R8 являють собою водень, та q означає 1. Тетразаміщені алкілідени LXVII можуть бути одержані за допомогою олефінізації Вадсворта-Норнера-Емонса відповідно заміщеного кетону (XVI) в розчиннику, такому як, без 93672 38 обмеження, тетрагідрофуран, диметилсульфоксид або метилен хлорид, протягом від 1 до 24год. при температурі між -78°С до 120°С в присутності основи, такої як, без обмеження, н-бутил літій, гідрид натрію або карбонат калію. Ціано-заміщені алкеніл броміди можуть бути піддані обміну бром-магній з ізо-PrMgBr в інертному розчиннику, такому як THF, при температурах в діапазоні від -78°С до -20°С. Одержані магнійорганічні сполуки, у вигляді розчину у прийнятному розчиннику, такому як THF, можуть бути оброблені електрофілом, таким як формальдегід, необов'язково стабілізований біс(2,6-дифенілфеноксид)метилалюмінієм, у прийнятному розчиннику, такому як метилен хлорид, протягом від 1 до 24 годин при температурах в діапазоні від -20°С до 37°С з одержанням спирту LXVIII. Безпосереднє заміщення спирту LXVIII може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом з отриманням LXIX. Депротектування фталіміду (LXIX) гідразином в розчиннику, такому як метанол або етанол, надає амін (LXX), в якому R9 та R10 являють собою водень. Альтернативні способи депротектування включають обробку метиламіном в метанолі або нагрівання з 6N соляною кислотою. Захисна група, Р, може бути видалена з LXX при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, в якому R5 являє собою ціано, R7 та R8 являють собою водень 39 93672 40 та R9 і Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу. P - захисна група Ціаногрупа в сполуці LXIX також може бути перетворена на альтернативні функціональні групи, такі як карбокси або алкоксикарбоніл, з одержанням амінів LXXI або LXXII (Схема XXXIX). Наприклад, основний гідроліз нітрилу LXIX гідроксидом лужного металу, таким як гідроксид калію, у прийнятному розчиннику, такому як вода, метанол, етанол або водні суміші спиртів, при температурі в діапазоні від 20°С до 100°С протягом від 1 до 48 годин, з наступним кислотним гідролізом фталамідогрупи, наприклад, 6 N соляною кислотою при температурі в діапазоні від 60°С до 100°С протягом від 1 до 48 годин, надає відповідне похідне амінокислоти LXXI, де R9 та R10 являють собою водень. Альтернативно, кислотний гід роліз нітрилу LXIX мінеральною кислотою в присутності спирту при температурі в діапазоні від 20°С до 200°С протягом від 30 хвилин до 48 годин, необов'язково під мікрохвильовим опроміненням, забезпечує відповідне аміно ефірне похідне LXXII, де R9 та R10 являють собою водень. Прийнятні мінеральні кислоти включають, але не обмежуються, сірчану кислоту. Прийнятні спирти включають, але не обмежуються, етанол. Хоча на Схемі XXXIX проілюстровано перетворення нітрилу LXIX на похідне амінокислоти LXXI та аміно ефірне похідне LXXII з кільцевим азотом, приєднаним до захисної групи, кільцевий азот також може бути зв'язаний з хінолоновим або нафтиридиновим циклом, як в сполуці VIII, поки здійснюють зазначені вище перетворення. Ρ - захисна група На Схемі XXII проілюстровано перетворення спиртів формули XVIII на сполуки формули III, в яких Ε являє собою алкеніл (LVIII). Крім того, на Схемі описано синтез сполук формули III, в яких Ε являє собою сниками, такими як періодинан Дес-Мартіна, реагент Корі-Кіма або реагент Сверна, надає відповідний альдегід (LVI). Альдегід може бути підданий реакції олефінізації, каталізуємої основою, такій як, без обмеження, реакція Вітига, з одержанням LVII, де Rс являє собою водень або алкіл. Видалення захисної групи, Р, з LVII при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, в якому Ε являє собою алкеніл (LVIII). На схемі XX також проілюстровано перетворення спиртів формули XVIII на сполуки формули III, де Ε являє собою R7 та R8 являють собою водень та R9 являє собою ацил, алкоксикарбоніл, або сульфоніл (LX). Окиснення спирту XVIII різними прийнятними оки 41 R7 та R8 являють собою водень, та R9 являє собою ацил, алкоксикарбоніл, або сульфоніл (LX). Реакція спирту XVIII з алкілуючим агентом в присутності амінної основи, такої як піридин, в інертному розчиннику, такому як дихлорметан, тетрагідрофуран або толуол, при температурах в діапазоні від -20°С до 60°С протягом 1-48 годин, забезпечує сполуки формули III, в яких Ε являє собою R7 та R8 являють собою водень та R9 являє собою ацил (LIX). Ацилюючі агенти включають галогенангідриди кислот, ангідриди кислот та кислоти в присутності агента активізації, такого як дициклогексилкарбодіімід, EDCI, BOP-C1, ВОР, РуВОР та подібні. Спирти формули XVIII можуть бути перетворені на сполуки формули III, в яких Ε являє собою R7 та R8 являють собою водень та R9 являє собою алкоксикарбоніл (LIX), за допомогою реакції Р - захисна група На Схемі VII проілюстровано безпосереднє перетворення кетону XVI на олефін XX, використовуючи реакцію олефінізації, каталізуєму основою, таку як, без обмеження, методики олефінізації Вітига, Вадсворта-Норнера-Емонса або Петерсона. Альтернативно, амін XX може бути одержаний за допомогою методики реакції олефі 93672 42 з карбонілюючим агентом в присутності амінної основи, такої як піридин, в інертному розчиннику, такому як дихлорметан, тетрагідрофуран або толуол, при температурах в діапазоні від -20°С до 60°С протягом 1-48 годин. Карбонілюючі агенти включають хлорформіати, фторформіати, азидоформіати та пірокарбонати. Спирти формули XVIII можуть бути перетворені на сполуки формули III, в яких Ε являє собою R7 та R8 являють собою водень та R9 являє собою сульфоніл (LIX), за допомогою реакції з сульфоніл хлоридом або сульфоновим ангідридом в присутності амінної основи, такої як піридин, в інертному розчиннику, такому як дихлорметан, тетрагідрофуран або толуол, при температурах в діапазоні від -20°С до 60°С протягом 1-48 годин. Видалення захисної групи, Р, з LIX при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, в якому Ε являє собою R7 та R8 являють собою водень, та R9 являє собою ацил, алкоксикарбоніл, або сульфоніл (LX). нового обміну з термінального олефіну XXII, використовуючи відповідно заміщений амін XXIII. Видалення захисної групи, Р, з XX при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, де Ε являє собою 43 та R7 і R8 являють собою водень. Р - захисна група На Схемі VIII проілюстровано гідроксилювання XXIV діоксидом селену з одержанням алільного спирту XXV. Перетворення проводять в розчиннику, такому як, без обмеження, метилен хлорид, толуол або тетрагідрофуран, при температурі між 25°С та 150°С, необов'язково в присутності співокисника, такого як трет-бутил гідропероксид. Видалення захисної групи, Р, з XXV при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін НІ, в якому Ε являє собою 93672 44 дики олефінізації Петерсона, Вітига або Вадсворта-Норнера-Емонса відповідно заміщеного кетону (XVI) в розчиннику, такому як, без обмеження, тетрагідрофуран, диметилсульфоксид або метилен хлорид, протягом від 1 до 24год. при температурі від -78°С до 120°С в присутності основи, такої як, без обмеження, н-бутил літій, гідрид натрію або карбонат калію. Одержана карбонільна сполука (XXVI) може бути відновлена відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію, в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С з одержанням відповідного спирту XXVII. Альтернативно, карбонільна сполука може бути піддана нуклеофільному приєднанню з відповідно заміщеним металорганічним агентом (R8M, де Μ являє собою метал), таким як різні літійорганічні реагенти або реактив Гріньяра, з одержанням відповідного спирту XXVII, де R8 являє собою алкіл. Прийнятні розчинники для останнього перетворення включають, діетиловий ефір, тетрагідрофуран або толуол, при температурах в діапазоні від -78°С до 20°С протягом від 30 хвилин до 48 годин. Коли один з R7 або R8 являє собою водень, перетворення спиртової функціональної групи в XXVII на групу, що відходить, таку як, без обмеження, бромід, мезилат або тозилат, як в XXVIII, при стандартних умовах та заміна групи, що відходить, на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С перетворює спирт XXVII на амін XXX. Видалення захисної групи, Р, з XXX при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, в якому Ε являє собою та один з R6 являє собою гідрокси. Р - захисна група На Схемі IX проілюстровано одержання α,βненасиченої карбонільної сполуки XXVI, в якій R7 є таким, як визначено вище, використовуючи мето та один з R7 та R8 являє собою водень. Альтернативно, коли один з R7 або R8 являє собою водень, безпосереднє заміщення спирту XXVII може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом, з наступним депротектуванням фталіміду гідразином в розчиннику, такому як метанол або етанол, з одержанням аміну XXX. Захисна група, Р, може бути видалена з XXIX при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, в якому R8 являє собою водень та R9 та Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу. 45 L - група, що відходить Р - захисна група На Схемі X наведено одержання XXXVI, де R5 являє собою галоген. Алкілідени XXXI, в яких R5 являє собою водень, можуть бути галогеновані відповідним галогенуючим агентом, таким як, без обмеження, 1-бром-2,5-піролідиндіон, 1,1,1трис(ацетилокси)-1,1-дигідро-2-бензіодоксол3(1Н)-он та бромід тетраалкіламонію або тіоніл хлорид, з одержанням XXXII. Алкіліден XXXII може бути відновлений відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію, в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С, з одержанням відповідного спирту XXXIII. Альтернативно, карбонільна сполука може бути піддана нуклеофільному приєднанню з відповідно заміщеним металорганічним агентом, таким як різні літійорганічні реагенти або реактив Гріньяра, з одержанням відповідного спирту XXXIII, в якому R8 являє собою алкіл. Прийнятні розчинники для останнього перетворення включають, діетиловий ефір, тетрагідрофуран або толуол, при температурах в діапазоні від 78°С до 20°С протягом від 30 хвилин до 48 годин. Коли один з R7 або R8 являє собою водень, перет 93672 46 ворення спиртової функціональної групи в XXXIII на групу, що відходить, таку як, без обмеження, бромід, мезилат або тозилат, як в XXXIV, при стандартних умовах та заміна групи, що відходить, на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С перетворює XXXIV на амін XXXVI. Видалення захисної групи, Р, з XXXVI при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, де Ε являє собою та один з R7 та R8 являє собою водень. Альтернативно, коли один з R7 або R8 являє собою водень, безпосереднє заміщення спирту XXXIII може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом, з наступним депротектуванням фталіміду гідразином в розчиннику, такому як метанол або етанол, з одержанням аміну XXXVI. Захисна група, Р, може бути 47 93672 48 видалена з XXXV при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, в якому R8 являє собою водень та R9 і Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу. L - група, що відходить Р - захисна група На Схемі XI проілюстровано синтез аміну з бічним ланцюгом III, в якому Ε являє собою новником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію, в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом від 1 до 24год. при температурі від 0°С та 120°С, з одержанням відповідного спирту XXXVIII, де Ra являє собою водень або алкіл, один з Rb являє собою водень, та інший Rb являє собою гідроксил. Альтернативно, карбонільна сполука XXXVII, в якій Ra являє собою алкіл, може бути піддана нуклеофільному приєднанню з відповідно заміщеним металорганічним агентом, таким як різні літійорганічні реагенти або реактив Гріньяра, з одержанням відповідного спирту XXXVIII, в якому Ra являє собою алкіл, один з Rb являє собою алкіл, та інший Rb являє собою гідроксил. Остаточно, карбонільна сполука XXXVII, в якій Ra являє собою R7 та R8 являють собою водень та R5 заміщений або розгалужений алкіл. На Схемі XI, галогеновану карбонільну сполуку XXXVII, в якій Ra являє собою водень або алкіл, може бути одержана за допомогою способу, подібного до способу одержання галогенованої карбонільної сполуки XXXII. Карбонільна сполука XXXVII, в якій Ra являє собою водень або алкіл, може бути відновлена від 49 водень або алкіл, або спирт XXXVIII, в якому Ra являє собою водень або алкіл, один з Rb являє собою водень, та інший Rb являє собою гідроксил, може бути фторована, використовуючи нуклеофільний фторуючий реагент, такий як, без обмеження, (N-етилетанамінато)трифторсірка (DAST) або трифторид біс(2-метоксіетил)аміносірки (Deoxofluor), у прийнятному розчиннику, такому як метилен хлорид, протягом від 1 до 24год. при температурі між 0°С та 60°С, з одержанням XXXVIII, де у випадку карбонільної сполуки XXXVII як субстрату, Ra являє собою водень або алкіл, та Rb являє собою фтор, та де у випадку спирту XXXVIII як субстрату, Ra являє собою водень або алкіл, один з Rb являє собою водень, та інший Rb являє собою фтор. Галогенований алкіліден XXXVIII може бути карбонільований в присутності каталізатора на основі перехідного металу, такого як, без обмеження, ацетат паладію, дикарбонілбіс(трифенілфосфін)нікелю або тетракіс(трифенілфосфін)паладію, під атмосферою моноксиду вуглецю в присутності другого допоміжного засобу, такого як метанол, необов'язково як розчиннику, або в розчиннику, такому як, без обмеження, диметилсульфоксид або тетрагідрофуран, протягом 1-24год. при температурі між 0°С та 120°С, з одержанням ефіру XXXIX. XXXIX може бути відновлений відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом 1 -24год. при 93672 50 температурі між 0°С та 120°С, з одержанням відповідного спирту XL, в якому q=1. Перетворення спирту XL на групу, що відходить, XLI, таку як, без обмеження, бромід, мезилат або тозилат, при стандартних умовах та заміна групи, що відходить на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С перетворює спирт XL на амін XLIII. Видалення захисної групи, Р, з XLIII при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, в якому Ε являє собою R7 та R8 являють собою водень, та R5 являє собою CRaRaRb. Альтернативно, безпосереднє заміщення спирту XL може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом з одержанням XLII. Депротектування фталіміду XLII гідразином в розчиннику, такому як метанол або етанол, надає амін XLIII. Захисна група, Р, може бути видалена з XLII при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, де R7 та R8 являють собою водень, R9 та Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу, та R5 являє собою CRaRaRb. 51 L - група, що відходить Р - захисна група На Схемі XII проілюстровано синтез аміну з бічним ланцюгом III, в якому Ε являє собою один з R7 або R8 являє собою водень та інший являє собою алкіл, R5 являє собою заміщений або розгалужений алкіл, та q означає 1. Сполука XXXVIII, одержана, як викладено вище, може бути карбонільована в присутності каталізатора на основі перехідного металу, такого як, без обмеження, ацетат паладію, дикарбонілбіс(трифенілфосфін)нікелю або тетракіс(трифенілфосфін)паладію, під атмосферою моноксиду вуглецю в присутності металорганічного реагенту R7M, де R7 є таким, як визначено вище, та включає реагенти, такі як гідрид трибутилолова або агенти алкіліндію (Organic Letters 2003, 5(7), 1103-1106), в розчиннику, такому як, без обмеження, метанол, диметилсульфоксид або тетрагідрофуран, протягом 1-24год. при температурі між 0°С та 120°С, з одержанням XLIV, де R7 є таким, як визначено вище. Карбонільна сполука XLIV може бути відновлена відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С, з одержанням відповідного спирту XLV. Альтернативно, карбоні 93672 52 льна сполука може бути піддана нуклеофільному приєднанню з відповідно заміщеним металорганічним реагентом, таким як різні літійорганічні реагенти або реактив Гріньяра, з одержанням відповідного спирту XLV, в якому R8 являє собою алкіл. Прийнятні розчинники для останнього перетворення включають, діетиловий ефір, тетрагідрофуран або толуол, при температурах в діапазоні від 78°С до 20°С протягом від 30 хвилин до 48 годин. Коли один з R7 або R8 являє собою водень, перетворення спиртової функціональної групи в XLV на групу, що відходить, таку як, без обмеження, бромід, мезилат або тозилат, як в XLVI при стандартних умовах та заміна групи, що відходить, на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С перетворює спирт XLV на амін XLVIII. Видалення захисної групи, Р, з XLVIII при стандартних умовах, відомих фахівцю в даній галузі техніки, надає амін III, де Ε являє собою один з R7 та R8 являє собою водень та інший являє собою алкіл, R5 являє собою заміщений або розгалужений алкіл, та q означає 1. Альтернативно, коли один з R7 або R8 являє собою водень, безпосереднє заміщення спирту XLV може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом, з наступ 53 93672 54 ним депротектуванням фталіміду гідразином в розчиннику, такому як метанол або етанол, з одержанням аміну XLVIII. Захисна група, Р, може бути видалена з XLVIII при стандартних умовах, відомих фахівцю в даній галузі техніки, з одержанням аміну V, в якому один з R7 та R8 являє собою водень та інший являє собою алкіл, R9 та Р" разом з азотом, до якого вони приєднані, утворюють фталімідну групу, R5 являє собою заміщений або розгалужений алкіл, та q означає 1. L - група, що відходить Ρ - захисна група На Схемі XIII проілюстровано перетворення кетону XVIa на олефін LIII, використовуючи каталізуєме основою анелування вінілсилану СторкаЮнга по Робінсону (Tetrahedron Letters, 2001, 42, 9123). Конденсація кетон XVIa з аліл йодидом XLIX, де Rc являє собою алкільну групу та Р' являє собою гідроксизахисну групу, (Tetrahedron Letters, 2001, 42, 9123) надає алкілований кетон L. Епоксидування кетону L епоксидуючими агентами, такими як, без обмеження, диметил діоксиран або мхлорпербензойна кислота, надає оксиран LI. Протодесилілування LI агентами, такими як, без обмеження, фторид тетра-н-бутиламонію або по лі(фторид водню)піридинію та водна кислота, з супутнім розкриттям епоксидного кільця надає кетон LII. Анелування кільця LII може бути проведене за допомогою обробки LII основою, такою як, без обмеження, метоксид натрію, з одержанням LIII. α,β-Ненасичений кетон LIII може бути відновлений відновником, таким як, без обмеження, гідрид діізобутилалюмінію, триетилборгідрид літію або боргідрид натрію, в розчиннику, такому як, без обмеження, толуол, метилен хлорид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С з одержанням, після видалення гідроксизахисної групи, відповідного спирту LIV, в якому один з R12 являє собою водень та інший R12 являє собою гідрокси. Альтернативно, LIII може 55 93672 56 бути піддана нуклеофільному приєднанню з відповідно заміщеним металорганічним агентом, таким як різні літійорганічні реагенти або реактив Гріньяра, з одержанням, після видалення гідроксизахисної групи, відповідного спирту LIV, в якому один з R12 являє собою алкіл та інший R12 являє собою гідрокси. Прийнятні розчинники для останнього перетворення включають, діетиловий ефір, тетрагідрофуран або толуол, при температурах в діапазоні від -78°С до 20°С протягом від 30 хвилин до 48 годин. Остаточно, карбонільна сполука LIII, може бути фторована, використовуючи нуклеофільний фторуючий реагент, такий як, без обмеження, (N-етилетанамінато)трифторсірка (DAST) або трифторид біс(2-метоксіетил)аміносірки (Deoxofluor), у прийнятному розчиннику, такому як метилен хлорид, протягом від 1 до 24год. при температурі між 0°С та 60°С, з одержанням, після видалення гідроксизахисної групи, спирту LIV, в якому R12 являє собою фтор. Р - захисна група Спирт LIV може бути перетворений на групу, що відходить, таку як, без обмеження, бромід, мезилат або тозилат, при стандартних умовах. Заміна групи, що відходить, на відповідно заміщений амін в розчиннику, такому як, без обмеження, диметилформамід, диметилсульфоксид або тетрагідрофуран, протягом від 1 до 24год. при температурі між 0°С та 120°С перетворює LIV на амін LV. Видалення захисної групи, Р, з LV при стандартних умовах, відомих фахівцю в даній галузі техніки, надає відповідний вторинний амін III, в якому Ε являє собою Альтернативно, безпосереднє заміщення гідроксильної групи спирту LIV може бути здійснене за допомогою реакції Мітцунобу з фталімідом та діалкіл азодикарбоксилатом, з наступним депротектуванням фталіміду гідразином в розчиннику, такому як метанол або етанол, з одержанням аміну LV, в якому R9 та R10 являють собою водень. Експериментальна частина Одержання попередника - гетероциклічних циклів Всі гетероцикличні цикли, такі як 1циклопропіл-1,4-дигідро-6,7-дифтор-8-метокси-4оксо-хінолін-3-карбонова кислота, 7-хлор-1циклопропіл-6-фтор-4-оксо-1,4-дигідронафтпіридин-3-карбонова кислота, 9,10-дифтор2,3-дигідро-3-метил-7-оксо-7Н-піридо[1,2,3-dе]-1,4бензоксазин-6-карбонова кислота, 1-циклопропіл1,4-дигідро-6,7-дифтор-4-оксо-хінолін-3-карбонова кислота, 7-хлор-1-(2,4-дифторфеніл)-6-фтор-4оксо-1,4-дигідро-нафтиридин-3-карбонова кислота, 1-циклопропіл-1,4-дигідро-6,7-дифтор-5-метил-4 R7 та R8 являють собою водень, та R5 та R6 сполучені разом, утворюючи 6-членне карбоциклічне кільце, та q означає 1. 57 93672 58 оксо-хінолін-карбонова кислота, 1-[(1R,2S)-2фторциклопропіл]-1,4-дигідро-6,7-дифтор-5-метил4-оксо-хінолін карбонова кислота, 1-(6-'аміно-3,5дифтор-2-піридиніл)-8-хлор-6,7-дифтор-1,4дигідро-4-оксо-хінолін-3-карбонова кислота та 1циклопропіл-1,4-дигідро-7-фтор-8-метокси-4-оксохінолін-3-карбонова кислота, були одержані відповідно до відомих з літератури способів (див. наведений вище опис загальних методик одержання гетероциклічних циклів) або були придбані з комерційних джерел. Одержання попередника А - одержання діацил хінолініл боратів Сполука 19 (Формула XV: L=F, А=С-ОМе, R1=циклопропіл, R2=Η, R3=F, R4=H) Діацил хінолініл борати одержували за допомогою методики, розкритої в патенті США 5,157,117. Суміш борної кислоти (2,4г, 38,7ммоль), оцтового ангідриду (13,8мл, 146ммоль) та хлориду цинку (52мг, 0,38ммоль) нагрівали до 110°С протягом 1,5год., обробляли оцтовою кислотою (51мл) та залишали перемішуватися протягом додаткової години при 110°С. Одержану суміш залишали охолоджуватися до 60°С, обробляли 1-циклопропіл1,4-дигідро-6,7-дифтор-8-метокси-4-оксо-хінолін-3карбоновою кислотою (18) (7,3г, 25,9ммоль) та оцтовою кислотою (26мл). Одержаний розчин нагрівали до 60°С протягом 5год., охолоджували до кімнатної температури та концентрували у вакуумі. Залишок обробляли водою (50мл) та тверду речовину збирали фільтруванням. Одержану тверду речовину промивали водою (3×50мл) та сушили, одержуючи зазначену у заголовку сполуку у вигляді білої твердої речовини, яку використовували, як таку, в наступній реакції. Методику, подібну до описаної вище, використовували для перетворення кожної з відповідних гетероциклічних карбонових кислот, наведених в Таблиці 2, на відповідне діацилборатне похідне (17, 21, 23 та 83). Одержання попередника С - одержання дифтор хінолініл боратів 223 Дифторборатний ефір 1-циклопропіл-1,4дигідро-6,7-дифтор-8-метокси-4-оксо-хінолін-3карбонової кислоти (223). 1-Циклопропіл-1,4-дигідро-6,7-дифтор-8метокси-4-оксо-хінолін-3-карбонову кислоту (18) (10,08г; 34,14ммоль) та ефірат трифториду бору (30мл; 236ммоль) в безводному THF (150мл) нагрівали при температурі кипіння зі зворотним холодильником під атмосферою азоту протягом 36 годин. Після охолодження додавали ефір (250мл). Одержану білу тверду речовину збирали фільтруванням, промивали ефіром та сушили, одержуючи дифторборатний ефір 1-циклопропіл-1,4-дигідро6,7-дифтор-8-метокси-4-оксо-хінолін-3-карбонової кислоти (223) у вигляді білої твердої речовини (7,29г; вихід 63%). MS 344 (Μ+Η). Дифторборатний ефір 1-циклопропіл-1,4дигідро-6,7-дифтор-5-метил-4-оксо-хінолін карбонової кислоти (224). Вказану у заголовку сполуку одержували за допомогою способу, аналогічного до способу одержання дифторборатного ефіру 1-циклопропіл-1,4дигідро-6,7-дифтор-8-метокси-4-оксо-хінолін-3карбонової кислоти (223), але виходячи з 1циклопропіл-1,4-дигідро-6,7-дифтор-5-метил-4 59 93672 60 оксо-хінолін карбонової кислоти (одержаної, як описано в Bioorganic та Medicinal Chemistry 1995, 3, 1699), одержуючи (224) у вигляді білого порошку (58%). MS 328 (Μ+Η). Дифторборатний ефір 1-[1R,2S)-2фторциклопропіл]-1,4-дигідро-6,7-дифтор-8метокси-4-оксо-хінолін-3-карбонової кислоти (225). Вказану у заголовку сполуку одержували за допомогою способу, аналогічного до способу одержання дифторборатного ефіру 1-циклопропіл-1,4дигідро-6,7-дифтор-8-метокси-4-оксо-хінолін-3карбонової кислоти (223), але виходячи з 1[(1R,2S)-2-фторциклопропіл]-1,4-дигідро-6,7дифтор-5-метил-4-оксо-хінолін карбонової кислоти (одержаної, як описано в WO 01/072738), одержуючи (225) у вигляді сірої твердої речовини (49%). MS 362 (Μ+Η). Одержання попередника В - бічного ланцюга III Сполука 27 зі Схеми XIV: трет-Бутил 4-(2-етокси-2оксоетиліден)піперидиніл-1-карбоксилат (24) був одержаний відповідно до методики описаної в Sato et al. Heterocycles, 2001, 54, 747. трет-Бутил 4-(2-гідроксіетиліден)піперидиніл1-карбоксилат (25) був одержаний відповідно до методики описаної в Sato et. al Heterocycles, 2001, 54, 747. трет-Бутил 4-[2-(1,3-дигідро-1,3-діоксо-2Нізоіндол-2-іл)етиліден]-піперидиніл-1-карбоксилат (26) був одержаний за допомогою методики, адаптованої з Synthesis 1995, 756. Розчин 25 (250мг, 1,10ммоль), фталіміду (208мг, 1,40ммоль) та трифеніл фосфіну (366мг, 1,40ммоль) в сухому THF (10мл) обробляли дієтил азодикарбоксилатом (0,25мл, 1,40ммоль) додавали через шприц в темряві під азотом. Через 5год. реакційну суміш обробляли водою (10мл), розбавляли етил ацетатом (50мл), промивали 10% водним бікарбонатом на трію (2×25мл) та сушили (MgSO4). Очищенням за допомогою флеш хроматографії (0-30% етил ацетату/гексани) одержували зазначену у заголовку сполуку (389мг, 78%) у вигляді білої піни. MS 357 (Μ+Η). 4-[2-(1,3-Дигідро-1,3-діоксо-2Н-ізоіндол2іл)етиліден]-1-піперидин трифторацетат (27). Розчин 26 (380мг, 1,03ммоль) розчиняли в СН2С12 (50мл) та обробляли трифтороцтовою кислотою (1мл) при кімнатній температурі. Через 1год. реакційну суміш концентрували у вакуумі, одержуючи зазначену у заголовку сполуку 27 (363мг, 100%) у вигляді масла. MS 257 (Μ+Η). 1-(трет-Бутоксикарбоніл)-4-піперидинон піддавали реакції з кожним з відповідних фосфоноацетатів, наведених в Таблиці 3, та продукт піддавали аналогічній методиці, як описано в синтезі 27, одержуючи відповідні спирти (28-30, 84) та похідні аміни (31-33,85).
ДивитисяДодаткова інформація
Назва патенту англійською7-amino alkylidenyl-heterocyclic quinolones and naphthyridones
Автори англійськоюGrant Iii Eugene B., Macielag Mark J., Paget Steven David, Weidner-Wells Michele Ann, Xu Xiaoqing, Xu Xiaodong
Назва патенту російською7-аминоалкилиденилгетероциклические хинолоны и нафтиридоны
Автори російськоюГрант Юджин Б., III, Масилаг Марк Дж., Пейджет Стивен Девид, Вейднер-Уэллс Мишель Энн, Су Сяокин, Су Сяодонг
МПК / Мітки
МПК: C07D 498/06, A61P 31/04, C07D 401/04, A61K 31/47, C07D 471/04, A61K 31/435
Мітки: хінолони, 7-аміноалкіліденілгетероциклічні, нафтиридони
Код посилання
<a href="https://ua.patents.su/65-93672-7-aminoalkilidenilgeterociklichni-khinoloni-ta-naftiridoni.html" target="_blank" rel="follow" title="База патентів України">7-аміноалкіліденілгетероциклічні хінолони та нафтиридони</a>
Попередній патент: Композиція для виготовлення хеку гарячого коптіння
Наступний патент: Фармацевтична композиція, яка містить омега-карбоксіарилзаміщену дифенілсечовину, для лікування раку
Випадковий патент: Спосіб одержання комплексу біологічно активних речовин з антиоксидантною та протизапальною дією