Дизаміщені фенілпіролідини як модулятори кортикальної катехоламінергічної нейротрансмісії
Номер патенту: 98783
Опубліковано: 25.06.2012
Автори: Свансон Ларс, Петтерссон Фредрік, Вотерс Ніколас, Вотерс Сюзанна, Сонессон Клас
Формула / Реферат
1. Сполука формули (2):
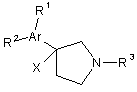 , (2)
, (2)
де:
Аr вибрано з групи, яку складають феніл, тіофеніл, фураніл, 2-піримідиніл, оксазоїл і тіазоліл;
R1 вибрано з групи, яку складають F і Сl;
R2 вибрано з групи, яку складають F і Сl;
R3 вибрано з групи, яку складають Н, Me, Et, n-Pr, i-Pr, n-Bu, i-Bu, s-Bu, t-Bu, циклопропілметил, CFH2CH2CH2-, CF2HCH2CH2-, CF3CH2CH2-, аліл і СН3ОСН2СН2-; і
X вибрано з групи, яку складають F або ОН; за умови, що, коли X - ОН, R3 не є Н;
буд-які її стереоізомери або будь-яка суміш її стереоізомерів, її N-оксид або фармацевтично прийнятна сіль.
2. Сполука за п. 1, яка відрізняється тим, що Аr - феніл.
3. Сполука за будь-яким з пп. 1-2, яка відрізняється тим, що має формулу (3):
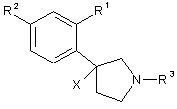 (3)
(3)
або формулу (4):
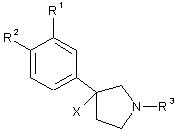 , (4)
, (4)
або формулу (5):
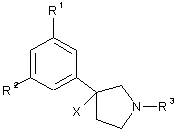 , (5)
, (5)
або формулу (6):
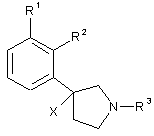 , (6)
, (6)
де R1, R2, R3 і X визначено у п. 1;
і її фармацевтично прийнятні солі.
4. Сполука за будь-яким з пп. 1-3, яка відрізняється тим, що R1 - F.
5. Сполука за будь-яким з пп. 1-4, яка відрізняється тим, що R2 - F і R3 - Н або Me.
6. Сполука за будь-яким з пп. 1-4, яка відрізняється тим, що R3 - Et або n-Рr.
7. Сполука за будь-яким з пп. 1-5, яка відрізняється тим, що R3 - Me.
8. Сполука за будь-яким з пп. 1-7, яка відрізняється тим, що має (+)-енантіомерну форму.
9. Сполука за будь-яким з пп. 1-7, яка відрізняється тим, що має (-)-енантіомерну форму.
10. Сполука за п. 1, яка відрізняється тим, що вибрана з групи, яку складають
(-)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол;
(+)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол;
3-(3-хлор-4-флуорфеніл)-1-етилпіролідин-3-ол;
3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол;
3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол;
3-(3,5-дихлорфеніл)-1-етилпіролідин-3-ол;
3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол;
3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол;
3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол;
3-(3,4-дихлорфеніл)-1-етилпіролідин-3-ол;
3-(3,5-дифлуорфеніл)-3-флуор-1-метилпіролідин;
3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол;
3-(3,5-дифлуорфеніл)-3-флуорпіролідин;
3-(3,5-дихлорфеніл)-3-флуорпіролідин;
3-(2,4-дифлуорфеніл)-1-метилпіролідин-3-ол;
3-(3,4-дифлуорфеніл)-1-метилпіролідин-3-ол;
3-(2,3-дихлорфеніл)-1-етилпіролідин-3-ол;
3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол;
3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол;
3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол;
3-(3-хлор-4-флуорфеніл)-1-пропілпіролідин-3-ол;
3-(3-хлор-5-флуорфеніл)-1-пропілпіролідин-3-ол;
3-(2,3-дифлуорфеніл)-3-флуорпіролідин;
(+)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол;
(-)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол;
3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол;
(+)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(-)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(+)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(-)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(-)-3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол;
(+)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол;
(-)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол;
(-)-1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол;
(-)-1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-(2-метоксіетил)піролідин-3-ол;
(-)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол;
(-)-1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол;
(-)-3-(3,5-дифлуорфеніл)-1-(2-метоксіетил)піролідин-3-ол;
(-)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол;
(-)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол;
(-)-3-(2,3-дифлуорфеніл)-1-(3,3,3-трифлуорпропіл)піролідин-3-ол;
(-)-1-(цикпопропілметил)-3-(2,3-дифлуорфеніл)піролідин-3-ол;
3-(3,4-дифлуорфеніл)-1-ізопропілпіролідин-3-ол;
(+)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол;
(+)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол;
(+)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол;
(+)-3-(3,5-дифлуорфеніл)-1-(2-метоксіетил)піролідин-3-ол;
(+)-1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол;
(+)-3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол;
(-)-3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол;
(+)-1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-(2-метоксіетил)піролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол;
(+)-1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол;
(+)-3-(2,3-дифлуорфеніл)-1-(3,3,3-трифлуорпропіл)піролідин-3-ол;
(+)-1-(циклопропілметил)-3-(2,3-дифлуорфеніл)піролідин-3-ол;
(-)-3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол;
(+)-3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол;
(+)-3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол
і їх фармацевтично прийнятні солі.
11. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-10, будь-якого з її стереоізомерів або будь-якої суміші її стереоізомерів, або її N-оксиду, або її фармацевтично прийнятної солі разом з одним або більше фармацевтично прийнятними носіями або розріджувачами.
12. Застосування сполуки за будь-яким з пп. 1-10, будь-якого з її стереоізомерів або будь-якої суміші її стереоізомерів, або її N-оксиду, або її фармацевтично прийнятної солі у виготовленні медикаменту.
13. Застосування за п. 12, яке відрізняється тим, що включає виготовлення фармацевтичної композиції для лікування, профілактики або полегшення хвороби або розладу центральної нервової системи у ссавця, включаючи людину.
14. Застосування за п. 13, яке відрізняється тим, що розладом центральної нервової системи є когнітивний розлад, нейродегенеративний розлад, деменція, вікові когнітивні порушення, розлад розвитку, розлад спектра аутизму, ADHD, церебральний параліч, синдром Туретта, когнітивний розлад, що виникає як центральні симптоми шизофренії, шизофренія, шизофреніформний розлад, афективний розлад, депресія, біполярний розлад, тривожний розлад, узагальнений тривожний розлад (GAD), специфічна фобія, панічний розлад (PD) або розлад сну.
15. Спосіб лікування, профілактики або полегшення розладу центральної нервової системи тіла живої тварини, включаючи людину,
який включає операцію введення у таке тіло живої тварини, що потребує цього, терапевтично ефективної кількості сполуки за будь-яким з пп. 1-10, будь-якого з її стереоізомерів або будь-якої суміші її стереоізомерів, або її N-оксиду, або її фармацевтично прийнятної солі.
16. Сполука за будь-яким з пп. 1-10, будь-який з її стереоізомерів або будь-яка суміші її стереоізомерів, або її N-оксид, або її фармацевтично прийнятна сіль, призначені для використання як медикаменту.
17. Сполука за будь-яким з пп. 1-10, будь-який з її стереоізомерів або будь-яка суміші її стереоізомерів, або її N-оксид, або її фармацевтично прийнятна сіль, призначені для використання у лікуванні, профілактиці або полегшенні хвороби або розладу, або стану ссавця, включаючи людину, на які впливає модуляція допамінергічної функції у центральній нервовій системі.
Текст
Реферат: Винахід стосується використання сполуки, яка підвищує позаклітинні рівні катехоламінів, допаміну і норепінефрину в церебральних кортикальних зонах мозку ссавця і, зокрема, використання 3-дизаміщених феніл-1-піролідинолів для лікування розладів центральної нервової системи. UA 98783 C2 (12) UA 98783 C2 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 Винахід стосується нових дизаміщених фенілпіролідинів і використання цих сполук, які підвищують позаклітинні рівні катехоламінів, допаміну і норепінефрину у церебральних кортикальних зонах мозку ссавця, зокрема, використання 3-дизаміщених арилом піролідинолів для лікування розладів центральної нервової системи (ЦНС). Церебральна кора містить декілька головних регіонів, які беруть участь у вищих функціях, наприклад, мисленні, почуттях, пам'яті і плануванні (Principles of Neural Science, 2nd Edition, ElseBier Science Publishing Co., Inc. 1985, pp 671-687). Біогенні аміни, тобто допамін, норепінефрин і серотонін є важливими кортикальних функцій ссавців. Висхідні шляхи допаміну і норепінефрину іннервують кору. Серотонергічні нейрони ЦНС проектуються на практично всі регіони мозку, включаючи церебральну кору (Fundamental Neuroscience, Academic press 1999, pp 207-212). Первинна або вторинна дисфункції активності цих шляхів призводять до розрегулювання активності на рецепторах допаміну, норепінефрину і серотоніну у цих зонах мозку і, як наслідок, до маніфестацій психіатричних і нейрологічних симптомів. Біогенні аміни кори модулюють декілька аспектів кортикальних функцій, контролюючи афект, тривожність, мотивацію, розпізнавання, увагу, збудження і пильність (Neuropsychopharmacology, 5th generation of Progress, Lippincott, Williams and Wilkins 2002, Chapter 34). Отже, катехоламіни допамін і норепінефрин сильно впливають на префронтальні кортикальні зони, працездатність яких є суттєвою для так званих виконавчих когнітивних функцій, пов'язаних, наприклад, з увагою, плануванням дій і контролем імпульсів (роль катехоламінів у цьому розглянуто у Arnsten and Li, 2005, Biol Psychiatry; 57; 1377-1384). Норепінефрин є головним фактором у ланцюгу регулювання тривожності і страху який, як вважають, зазнає розрегулювання у тривожних розладах, наприклад, панічних розладах, узагальненому тривожному розладі (GAD) і специфічних фобіях (Sullivan et al. 1999, Biol Psychiatry; 46:1205-121). Сполуки, що сприяють функціям настрою і афективності, зокрема, нейротрансмітери норепінефрин і серотонін у лікуванні депресії і тривожності, як вважають, беруть участь у регулюванні афективних функцій (Goodman & Gilman's Pharmacological Basis of Therapeutics, Tenth Edition, McGraw-Hill, 2001). Взагалі сполуки, що специфічно впливають на трансмісію біогенних амінів, а саме, моноамінів, норепінефрину, допаміну і серотоніну, успішно використовуються для полегшення афективних, когнітивних або пов'язаних з увагою симптомів у пацієнтів, що страждають від, наприклад, депресії, тривожності і розладу з дефіцитом уваги і гіперактивністю (ADHD). Крім того, моноамінні системи у корі, як відомо, безпосередньо або непрямо пов'язані з корінними симптомами шизофренії. Базуючись на відкриттях у біохімічному синтезі і генетиці, а також на нейропсихологічних спостереженнях, які вказують на дисфункцію певних кортикальних зон при шизофренії, можна припустити, що цей розлад виникає як різні патологічні етології, спрямовані на кортикальну функцію, і призводить до розрегулювання кортикального мікроланцюга, з клінічною маніфестацією у вигляді симптомів шизофренії (Harrison, Weinberger, 2005, Molecular Psychiatry; 10:40-68). Цей кортикальний мікроланцюг регулюється декількома нейротрансмітерами, включаючи глютамат, GABA і допамін. Сполуки, що належать до класу заміщених 3-феніл-піролідинів, були відкриті недавно. Серед цих сполук деякі є неактивними у ЦНС, деякі виявляють серотонергічні або змішані серотонергічні/допамінні фармакологічні профілі, а деякі є повними або частковими агоністами або антагоністами рецептора допаміну з високою спорідненістю до рецепторів допаміну. Ці сполуки були описані як інтермедіати синтезу у WO 00/05225 і у Haglid et al. як аналоги нікотину (Acta Chemica Scandinavica, 1963, 17 (6), 1743-50). 3-хлор-феніл-3-піролідин був описаний як інтермедіат синтезу у WO 2006/117669 і WO 2006/112685. 4-хлор-феніл-3-піролідин описано у J. Med. Chem. (2002), 45(17) 3721-3738, Bioorganic & Medicinal Chemistry Letters (1999), 9(10), 1379-1384 і Journal of Medicinal Chemistry (1989), 32(6). 3-флуор-феніл-3-піролідин описано у US 5 128 362 і ЕР 325963. 4-флуор-феніл-3піролідин описано у WO 2006/117669, Bioorganic & Medicinal Chemistry Letters (1999), 9(10), 1379-1384 і US 5 128 362. 4-бром-феніл-3-піролідин описано у WO 2006/117669, Bioorganic & Medicinal Chemistry Letters (1999), 9(10), 1379-1384, US 5 128 362 і WO 01/16136. 1 UA 98783 C2 3,4-дифлуор-феніл-3-піролідин описано як інтермедіат синтезу у WO 2005/028438. 5 10 15 20 Піролідиноли з вторинними амінами, зображені вище, описано у Wu et al., 3-заміщені-3піролідиноли - у US 3 118 907), Gould et al., J. Med. Chem. 1964, 7, 60-7), Lunsford et al., US 2 878 264), Hesley et al., DE 2017255), Lunsford et al.; GB 1202747), Ablordeppey et al.; WO 00/70531), Ablordeppey et al., Bioorg. Med. Chem. Lett. 2006, 16, 3219-3223), Ablordeppey et al.; US 2006052363), Luly et al., US 2002-0169155 і US 2005-0070549), Kato et al., WO 97/24325), Ablordeppey et al., Medicinal Chemistry Research 1993, 7, 459-67) і Wu et al., J. Medicinal & Фармацевтичн Chemistry 1962, 5, 762-69). Наведені вище піролідиноли описано у Lunsford et al. як блокери для симпатичної нервової системи, адренергічні блокувальні агенти і модулятори кров'яного тиску (DE1144279B1 (1958); US 2 878 264 (1959)) Було відзначено, що сполуки формули 1 (WO 92/18475) мають допамінергічні стабілізуючі властивості. Формула 1: З сполук формули 1 (Sonesson et al. (J. Med. Chem. 1994, 37, 2735-2753)) були отримані декілька фенілпіперидинів з переважними властивостями антагоністів ауторецептора. Автори виявили, що ці сполуки підвищують рівні DOPAC смугастого тіла при 100 мкмоль/кг, що є ознакою антагоністів допаміну D2. Деякі приклади наведено нижче. Приклади з J. Med. Chem. 1994, 37, 2735-2753; 2 UA 98783 C2 Наведені далі структури є відомими як інтермедіати синтезу у WO 01/46146. WO 2005/121092 стосується піперидинових сполук: 5 10 15 20 25 деякі з яких наведено у табл. 1 нижче. Крім того, Sonesson et al. (Bioorg. Med. Chem. Lett. 1997, 7, 241-246) відзначили, що 3-фенілпіролідини, заміщені електронами груп у мета-позиції фенільного кільця, мають властивості антагоніста ауторецептора допаміну. Прикладом є Відомо, що 3-феніл-піперидинам і 3-феніл-піролідинам (J. Med. Chem. 1994, 37, 2735 або Bioorg. Med. Chem. Lett. 1997, 7, 241-246) властива потужна специфічна дія на метаболізм допаміну, виміряна як зростання вмісту DOPAC (3,4-дигідроксифенілоцтова кислота) у тканині смугастого тіла (табл. 1). Ця дія на субкортикальний допаміновий метаболізм не є об'єктом винаходу. Крім того, з використанням техніки мікродіалізу було показано, що сполуки з J. Med. Chem. 1994, 37, 2735-2753 підвищують позаклітиннні рівні моноамінів (допаміну, норепінефрину і серотоніну) з однаковою дією як у смугастому тілі, так і у церебральних кортикальних зонах мозку ссавця (див. фіг. 1-10). Інакше кажучи, регіональна селективність сполуки винаходу між смугастим тілом і церебральними кортикальними зонами є не відомою. Отже, у WO 92/18475, WO 2005/121092, J. Med. Chem. 1994, 37, 2735 або Bioorg. Med. Chem. Lett. 1997, 7, 241-246, не показано, як отримати сполуки, які підвищують норепінефринну і допамінну нейротрансмісію переважно для фронтальної кори. Задачею винаходу є отримання нових сполук для терапевтичного використання, а саме, сполук, здатних до модуляції допамінної і норепінефринної нейротрансмісії у мозку ссавця, включаючи мозок людини. Іншою задачею винаходу є отримання сполук з терапевтичною дією при пероральному введенні. Ще одною задачею є отримання сполуки з більш оптимальними 3 UA 98783 C2 5 10 15 20 25 30 35 40 фармакодинімічними властивостями, наприклад, кінетичною поведінкою, біозасвоюваністю, розчинністю або ефективністю. Винахід ґрунтується на несподіваному виявленні фармакологічної діє сполуки винаходу на моноаміни у церебральній корі і можливості використання сполуки винаходу у лікуванні деяких розладів ЦНС. Фармакологічні випробування на щурах in vivo показали, що сполуки винаходу викликають регіонально селективне підвищення рівнів катехоламіну у фронтальній корі. Внаслідок специфічної модуляторної дії катехоламінів на кортикальні функції, пов'язані з розпізнаванням, увагою і афектом сполуки винаходу можуть бути використані у лікуванні розладів, що характеризуються дисфункціями у цих зонах. Отже, ці сполуки можуть бути використані у лікуванні когнітивних розладів, ADHD, депресії і тривожності. Ці сполуки можуть також бути використані у лікуванні шизофренії, яка характеризується дисфункціями церебральної кори, що виявляють себе у когнітивних розладах і психозі. Абревіатури: NA: норепінефрин, NM: норметанефрин; DA: допамін, DOPAC: 3,4-дигідроксифенілоцтова кислота; 3-МТ: 3-метокситирамін; 5-НТ: серотонін (5-гідрокситриптамін). Винахід стосується нових 4-(дизаміщених арилом)-піролідинолів, зокрема, 4-(орто, парадизаміщених фенілом)-1-піролідинолів, 4-(мета, пара-дизаміщених фенілом)-1-піролідинолів, 4(мета, мета-дизаміщених фенілом)-1-піролідинолів і 4-(орто, мета-дизаміщених фенілом)-1піролідинолів у формі вільної основи або їх фармацевтично прийнятних солей, фармацевтичних композицій, що містять зазначені сполуки, і використання зазначених сполук у терапії. Зокрема, винахід стосується сполуки формули (2): (2), де: Аr вибрано з групи, яку складають феніл, тіофеніл, фураніл, 2-піримідиніл, оксазоїл і тіазоліл; 1 R вибрано з групи, яку складають F і Сl; 2 R вибрано з групи, яку складають F і Сl; 3 R вибрано з групи, яку складають Н, Me, Et, n-Pr, i-Pr, n-Bu, i-Bu, s-Bu, t-Bu, циклопропілметил, CFH2CH2CH2-, CF2HCH2CH2-, CF3CH2CH2-, аліл і СН3ОСН2СН2-, і 3 X вибрано з групи, яку складають F або ОН; за умови, що, коли X - ОН, R не є Н; і будь-яких її стереоізомерів або будь-якої суміші її стереоізомерів, або її N-оксиду, або її фармацевтично прийнятної солі. У першому втіленні винахід стосується сполуки формули (2), в якій: Аr вибрано з групи, яку складають феніл, тіофеніл, фураніл, 2-піримідиніл, оксазоїл і тіазоліл; 1 R вибрано з групи, яку складають F і Сl; 2 R вибрано з групи, яку складають F і Сl; 3 R вибрано з групи, яку складають Н, Me, Et, n-Pr, n-Bu, i-Bu, аліл і СН3ОСН2СН2-, і 3 X вибрано з групи, яку складають F або ОН; за умови, що, коли X - ОН, R не є Н; будь-яких її стереоізомерів або будь-якої суміші її стереоізомерів, або її N-оксиду, або її фармацевтично прийнятної солі. В одному з втілень Аr - 2-тіофеніл, 2-фураніл, 2-оксазоїл або 2-тіазоліл. Придатним Аr є феніл. В іншому втіленні сполукою винаходу є сполука формули (3): (3), 45 або формули (4): 4 UA 98783 C2 (4), або формули (5): (5), або формули (6): 5 10 15 20 25 30 35 (6), 1 2 3 де R , R , R і Х визначено вище, або її фармацевтично прийнятна сіль. 1 1 2 В одному з втілень R - F. В іншому втіленні R - Сl. У ще одному втіленні R - F. В одному з 2 1 2 1 2 втілень R - Сl. В іншому втіленні R - F і R - F. У ще одному втіленні R - Сl і R - Сl. В іншому 1 2 1 2 втіленні R - Сl і R - F. В одному з втілень R - F і R - Сl. 3 3 3 У ще одному з втілень R - Et або n-Рr. В іншому втіленні R - n-Рr. У ще одному з втілень R 3 3 Et. В одному з втілень R - бутил, наприклад, n-Bu або і-Bu. В іншому втіленні, R - пропіл, 3 3 2 наприклад, n-Рr або і-Pr. У ще одному втіленні R - Н. В іншому з втілень R -Н або Me і R -F. У 3 3 3 ще одному втіленні R -Me. В іншому втіленні R - аліл. У ще одному з втілень R - СН3ОСН2СН2-. 3 3 В іншому втіленні R - циклопропілметил. У ще одному втіленні R -CF3CH2CH2-. Одним з втілень 3 винаходу є піролідиноли, тобто X - ОН. Коли X - ОН, в одному з втілень R - n-Рr. Іншим 3 втіленням винаходу є флуор-піролідини, тобто X-F. Коли X-F, в одному з втілень бажаною R є Me. Втілення формули (3): В одному з втілень сполуки формули (3), X - ОН. В іншому втіленні, 1 2 1 2 3 R - F. У ще одному втіленні R - F. У бажаному втіленні R і R є F. В іншому втіленні R - Me. 1 Втілення формули (4): В одному з втілень сполуки формули (4), X - ОН. В іншому втіленні R 1 2 2 - F. У ще одному втіленні R - Сl. В іншому втіленні R - F. У ще одному втіленні R - Сl. У 1 2 1 2 1 бажаному втіленні обидві R і R є F. В іншому втіленні R - Сl і R - F. У ще одному втіленні R і 2 3 3 3 R є Сl. В іншому втіленні R - Me. У ще одному втіленні R - Et. В іншому втіленні R - n-Рr. У ще 3 одному втіленні R - і-Рr. Втілення формули (5): В одному з втілень сполуки формули (5) X - ОН. В іншому втіленні X 1 1 2 F. У ще одному втіленні R - F. В іншому втіленні R - Сl. У ще одному втіленні R - F. В іншому 2 1 2 1 2 втіленні R - Сl. У бажаному втіленні обидві R і R є F. В іншому втіленні R - Сl і R - F. У ще 1 2 3 3 одному втіленні обидві R і R є Сl. В іншому втіленні R - Н. У ще одному втіленні R - Me. В 3 3 3 іншому втіленні R - Et. У ще одному втіленні R - n-Рr. В іншому втіленні R - n-Bu. У ще одному 3 3 3 втіленні R - і-Вu. В іншому втіленні R - аліл. В іншому втіленні R - СН3ОСН2СН2-. Втілення формули (6): В одному з втілень сполуки формули (6) X - ОН. В іншому втіленні X 1 1 2 F. У ще одному втіленні R - F. В іншому втіленні R - Сl. У ще одному втіленні R - F. В іншому 2 1 2 1 2 втіленні R - Сl. У бажаному втіленні R і R є F. В іншому втіленні R - Сl і R - F. У ще одному 1 2 3 3 втіленні обидві R і R є Сl. В іншому втіленні R - Н. У ще одному втіленні R - Me. В іншому 3 3 3 втіленні R - Et. У ще одному втіленні R - n-Рr. В іншому втіленні R - n-Bu. У ще одному втіленні 3 3 3 R - і-Bu. В іншому втіленні R - аліл. В іншому втіленні R - СН3ОСН2СН2-. У ще одному втіленні 3 3 R - циклопропілметил. В іншому втіленні R - CF3CH2CH2-. Було виявлено, що сполуки формул 2-6 підвищують позаклітинні рівні норепінефрину і допаміну переважно у фронтальній корі з суттєво меншою (або відсутньою) дією у смугастому 5 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 тілі, як це було визначено з застосуванням мікродіалізу. Безпрецедентне зростання кортикального норепінефрину і допаміну ілюструється фіг. 1-10. Сполуками згідно з винаходом є: 3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(2,4-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(3,4-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(3,5-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-етилпіролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(2,3-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(2,4-дихлорфеніл)-1-метилпіролідин-3-ол; 3-(2,4-дихлорфеніл)-1-ізобутилпіролідин-3-ол; 3-(2,4-дихлорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(2,4-дихлорфеніл)піролідин-3-ол; 3-(2,4-дихлорфеніл)-1-пропілпіролідин-3-ол; 3-(2,4-дихлорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2,4-дихлорфеніл)піролідин-3-ол; 3-(2,4-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(2,4-дифлуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(2,4-дифлуорфеніл)піролідин-3-ол; 3-(2,4-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(2,4-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2,4-дифлуорфеніл)піролідин-3-ол; 3-(2-хлор-4-флуорфеніл)-1-метилпіролідин-3-ол; 3-(2-хлор-4-флуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(2-хлор-4-флуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(2-хлор-4-флуорфеніл)піролідин-3-ол; 3-(2-хлор-4-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(2-хлор-4-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2-хлор-4-флуорфеніл)піролідин-3-ол; 3-(4-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол; 3-(4-хлор-2-флуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(4-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(4-хлор-2-флуорфеніл)піролідин-3-ол; 3-(4-хлор-2-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(4-хлор-2-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(4-хлор-2-флуорфеніл)піролідин-3-ол; 3-(2,3-дихлорфеніл)-1-метилпіролідин-3-ол; 3-(2,3-дихлорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(2,3-дихлорфеніл)піролідин-3-ол; 3-(2,3-дихлорфеніл)-1-пропілпіролідин-3-ол; 3-(2,3-дихлорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2,3-дихлорфеніл)піролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(3-хлор-2-флуорфеніл)піролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 6 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 1-бутил-3-(3-хлор-2-флуорфеніл)піролідин-3-ол; 3-(2-хлор-3-флуорфеніл)-1-метилпіролідин-3-ол; 3-(2-хлор-3-флуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(2-хлор-3-флуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(2-хлор-3-флуорфеніл)піролідин-3-ол; 3-(2-хлор-3-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(2-хлор-3-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(2-хлор-3-флуорфеніл)піролідин-3-ол; 1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-метилпіролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3-хлор-4-флуорфеніл)піролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(3-хлор-4-флуорфеніл)піролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3,4-дифлуорфеніл)піролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(3,4-дифлуорфеніл)піролідин-3-ол; 3-(4-хлор-3-флуорфеніл)-1-метилпіролідин-3-ол; 3-(4-хлор-3-флуорфеніл)-1-ізобутилпіролідин-3-ол; 3-(4-хлор-3-флуорфеніл)-1-етилпіролідин-3-ол; 1-аліл-3-(4-хлор-3-флуорфеніл)піролідин-3-ол; 3-(4-хлор-3-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(4-хлор-3-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(4-хлор-3-флуорфеніл)піролідин-3-ол; 3-(3,4-дихлорфеніл)-1-метилпіролідин-3-ол; 3-(3,4-дихлорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3,4-дихлорфеніл)піролідин-3-ол; 3-(3,4-дихлорфеніл)-1-пропілпіролідин-3-ол; 3-(3,4-дихлорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(3,4-дихлорфеніл)піролідин-3-ол; 3-(3,5-дихлорфеніл)-1-метилпіролідин-3-ол; 3-(3,5-дихлорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3,5-дихлорфеніл)піролідин-3-ол; 3-(3,5-дихлорфеніл)-1-пропілпіролідин-3-ол; 3-(3,5-дихлорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 1-бутил-3-(3,5-дихлорфеніл)піролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол; 1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-ізобутилпіролідин-3-ол; 1-аліл-3-(3-хлор-5-флуорфеніл)піролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; і 1-бутил-3-(3-хлор-5-флуорфеніл)піролідин-3-ол. Сполуками згідно з винаходом, в яких X-F, є: 3-(3,5-дифлуорфеніл)-3-флуорпіролідин; 3-(3,5-дифлуорфеніл)-3-флуор-1-метилпіролідин; 3-(3,5-дихлорфеніл)-3-флуорпіролідин; 3-(3-хлор-2-флуорфеніл)-3-флуорпіролідин; 3-(3-хлор-2-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(2-хлор-3-флуорфеніл)-3-флуорпіролідин; 3-(2-хлор-3-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(2,3-дихлорфеніл)-3-флуорпіролідин; 3-(2,3-дихлорфеніл)-3-флуор-1-метилпіролідин; 3-(2,3-дифлуорфеніл)-3-флуорпіролідин; 3-(2,3-дифлуорфеніл)-3-флуор-1-метилпіролідин; 7 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 3-(4-хлор-2-флуорфеніл)-3-флуорпіролідин; 3-(4-хлор-2-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(2-хлор-4-флуорфеніл)-3-флуорпіролідин; 3-(2-хлор-4-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(2,4-дихлорфеніл)-3-флуорпіролідин; 3-(2,4-дихлорфеніл)-3-флуор-1-метилпіролідин; 3-(2,4-дифлуорфеніл)-3-флуорпіролідин; 3-(2,4-дифлуорфеніл)-3-флуор-1-метилпіролідин; 3-(4-хлор-3-флуорфеніл)-3-флуорпіролідин; 3-(4-хлор-3-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(3-хлор-4-флуорфеніл)-3-флуорпіролідин; 3-(3-хлор-4-флуорфеніл)-3-флуор-1-метилпіролідин; 3-(3,4-дихлорфеніл)-3-флуорпіролідин; 3-(3,4-дихлорфеніл)-3-флуор-1-метилпіролідин; 3-(3,4-дифлуорфеніл)-3-флуорпіролідин; 3-(3,4-дифлуорфеніл)-3-флуор-1-метилпіролідин; 3-(3-хлор-5-флуорфеніл)-3-флуорпіролідин; 3-(3-хлор-5-флуорфеніл)-3-флуор-1-метилпіролідин; і 3-(3,5-дихлорфеніл)-3-флуор-1-метилпіролідин. У бажаному втіленні сполуками згідно з винаходом є: (-)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол; (+)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-етилпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол; 3-(3,4-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-3-флуор-1-метилпіролідин; 3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-3-флуорпіролідин; 3-(3,5-дихлорфеніл)-3-флуорпіролідин; 3-(2,4-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(2,3-дихлорфеніл)-1-етилпіролідин-3-ол; 3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол; 3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-4-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-пропілпіролідин-3-ол; 3-(2,3-дифлуорфеніл)-3-флуорпіролідин; (+)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол; (-)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол; 3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол; (+)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол; (-)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол; (+)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол; (-)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол; (-)-3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол; (+)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол; (-)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол; (-)-1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол; 8 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 (-)-1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; (-)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол; (-)-1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол; (-)-3-(3,5-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; (-)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; (-)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол; (-)-3-(2,3-дифлуорфеніл)-1-(3,3,3-трифлуорпропіл)піролідин-3-ол; (-)-1-(циклопропілметил)-3-(2,3-дифлуорфеніл)піролідин-3-ол; 3-(3,4-дифлуорфеніл)-1-ізопропілпіролідин-3-ол; (+)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол; (+)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол; (+)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; (+)-3-(3,5-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; (+)-1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол; (+)-3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол; (-)-3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол; (+)-1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол; (+)-1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол; (+)-3-(2,3-дифлуорфеніл)-1-(3,3,3-трифлуорпропіл)піролідин-3-ол; (+)-1-(циклопропілметил)-3-(2,3-дифлуорфеніл)піролідин-3-ол; (-)-3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол; (+)-3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол; (+)-3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол; або їх фармацевтично прийнятні солі. Будь-яка комбінація двох або більше втілень, описаних вище, входить в об'єм винаходу. Фармацевтично прийнятні солі Хімічну сполуку згідно з винаходом можна застосовувати будь-якій формі, придатній для введення пацієнту. Придатні форми включають фармацевтично (тобто фізіологічно) прийнятні солі і пре- або пролікові форми сполуки винаходу. Приклади фармацевтично прийнятних адитивних солей включають (без обмеження) нетоксичні неорганічні і органічні кислото-адитивні солі, наприклад, гідрохлорид, гідробромід, нітрат, перхлорат, фосфат, сульфат, формат, ацетат, асонат, аскорбат, бензолсу-льфонат, бензоат, цинамат, цитрат, ембонат, енантат, фумарат, глютамат, гліколат, лактат, малеат, малонат, манделат, метансульфонат, нафталін-2-сульфонат, фталат, саліцилат, сорбат, стеарат, сукцинат, тартрат, толуол-р-сульфонат тощо. Такі солі отримують добре відомими способами. Інші кислоти, наприклад, оксалілова кислота, яка може вважатись фармацевтично прийнятною, може бути використана у приготуванні солей-інтермедіатів для отримання хімічних сполук винаходу і їх фармацевтично прийнятних кислото-адитивних солей. Приклади фармацевтично прийнятних катіонних солей хімічної сполуки винаходу включають (без обмеження) солі натрію, калію, кальцію, магнію, цинку, алюмінію, літію, холіну, лізинію, амонію тощо хімічної сполуки винаходу, яка містить аніонну групу. Такі катіонні солі отримують добре відомими способами. Тут "онійні солі" N-вмісних сполук також вважаються фармацевтично прийнятними. Бажані "онійні солі" включають алкіл-онійні солі, циклоалкіл-онійні солі і циклоалкілалкіл-онійні солі. Приклади пре- або пролікових форм хімічної сполуки винаходу включають сполуки, модифіковані в одній або більше реактивних або дериватизаційних груп первісної сполуки. Найбільш поширеними є сполуки модифіковані у карбоксильній групі, гідроксильній групі або аміногрупі. Прикладами придатних похідних є естери або аміди. Прикладами проліків сполуки винаходу є N-оксиди і такі N-гідрокси-похідні: 3-(3-хлор-2-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(2-хлор-3-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(2,3-дихлорфеніл)-3-флуорпіролідин-1-ол; 3-(2,3-дифлуорфеніл)-3-флуорпіролідин-1-ол; 3-(4-хлор-2-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(2-хлор-4-флуорфеніл)-3-флуорпіролідин-1-ол; 9 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 3-(2,4-дихлорфеніл)-3-флуорпіролідин-1-ол; 3-(2,4-дифлуорфеніл)-3-флуорпіролідин-1-ол; 3-(4-хлор-3-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(3-хлор-4-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(3,4-дихлорфеніл)-3-флуорпіролідин-1-ол; 3-(3,4-дифлуорфеніл)-3-флуорпіролідин-1-ол; 3-(3-хлор-5-флуорфеніл)-3-флуорпіролідин-1-ол; 3-(3,5-дихлорфеніл)-3-флуорпіролідин-1-ол; 3-(3,5-дифлуорфеніл)-3-флуорпіролідин-1-ол. Хімічна сполука винаходу може бути розчинною або нерозчинною. Фармацевтично прийнятними розчинниками є, наприклад, вода, етанол тощо. Розчинні форми можуть також включати гідратовані форми, наприклад, моногідрат, дигідрат, гемігідрат, тригідрат, тетрагідрат тощо. Взагалі розчинні форми вважаються еквівалентними нерозчинним. Стеричні ізомери Сполуки винаходу можуть існувати у різних стереоізомерних формах. Винахід включає всі такі ізомере і будь-які їх суміші, включаючи рацемічні. Рацемічні форми можуть бути розрізнені на оптичні антиподи відомими способами. Одним з них є розділення енантіомерних сполук (включаючи енантіомерни інтермедіати) у випадку, коли сполука є хіральною кислотою - використовуючи оптично активний амін і вивільняючи діастереомери обробкою кислотою. Інший спосіб розрізнення рацематів на оптичні антиподи базується на хроматографії на оптично активній матриці. Рацемічні сполуки винаходу можуть, таким чином, бути розрізнені на їх оптичні антиподи, наприклад, фракційною кристалізацією Dабо L-солей (наприклад, тартратів, манделатів або камфорсульфонатів). Хімічні сполуки винаходу можуть також бути розрізнені з утворенням діастереомерних амідів реакцією хімічних сполук винаходу з оптично активною карбоновою кислотою, наприклад, отриманою з (+) або (-) фенілаланіну, (+) або (-) фенілгліцину, (+) або (-) камфанової кислоти або з утворенням діастереомерних карбаматів реакцією хімічної сполуки винаходу з оптично активним хлорформатом тощо. Інші способи розрізнення оптичних ізомерів описано у Jaques J, Collet A, & Wilen S. у "Enantiomers, Racemates and Resolutions", John Wiley and Sons, New York (1981). Оптично активні сполуки можуть також бути приготовлені з оптично активних вихідних матеріалів. N-оксиди N-оксидами є оксидні похідні третинного аміну, які включать атом нітрогену ароматичної Nгетероциклічної сполуки, неароматичних N-гетероциклічних сполук, тріалкіламіну і тріалкеніламіну. Наприклад, N-оксидом сполуки, що містить піридил, може бути похідна 1-оксипіридин-2,-3 або -4-ілу. N-оксиди сполуки винаходу можуть бути приготовлені окисленням відповідного нітрогену звичайним окислювачем, наприклад, гідрогенпероксидом у присутності кислоти, наприклад, оцтової, при підвищеній температурі, або реакцією з перкислотою, наприклад, пероцтовою, у придатному розчиннику, наприклад, ДХМ, етилацетаті або метилацетаті, або у хлороформі, або у ДХМ з 3-хлорпероксибензойною кислотою. Наведені нижче N-оксиди можуть бути проліками сполук винаходу. Формула (7): (7), де: Аr вибрано з групи, яку складають феніл, тіофеніл, фураніл, 2-піримідиніл, оксазоїл і тіазоліл; 1 R вибрано з групи, яку складають F і Сl; 2 R вибрано з групи, яку складають F і Сl; 3 R вибрано з групи, яку складають Н, Me, Et, n-Pr, n-Bu, i-Bu, аліл і СН3ОСН2СН2-; 3 X вибрано з групи, яку складають F або ОН; за умови, що, коли X - ОН, R не є Н; і її фармацевтично прийнятні солі. Цінними є проліки формули (8): 10 UA 98783 C2 (8), або формули (9): (9), або формули (10): (10), 5 або формули (11): 10 15 20 25 30 (11); 1 2 3 де R , R , R і Х визначено вище, і їх фармацевтично прийнятні солі. 1 3 3 2 Придатною R є F. R може бути Et або n-Рr, бажано, n-Рr. Коли R - Н або Me, R може бути 3 F. В одному з втілень, R - Me. Іншим втіленням винаходу ї піролідиноли, тобто Х-ОН. N-оксиди згідно з винаходом включають: 3-(3-хлор-2-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2,3-дихлорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2-хлор-3-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2,3-дифлуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2,4-дихлорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(4-хлор-2-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2-хлор-4-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(2,4-дифлуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(4-хлор-3-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3,4-дифлуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3,4-дихлорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3-хлор-4-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3-хлор-5-флуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3,5-дихлорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3,5-дифлуорфеніл)-3-флуор-1-метилпіролідин 1-оксид; 3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол 1-оксид; і 3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол 1-оксид. Мічені сполуки Сполуки винаходу можуть бути використані як мічені або немічені. Мічена сполука має один або більше атомів, заміщених атом, що має атомну масу або масовий номер, відмінний від 11 UA 98783 C2 5 10 15 20 25 30 35 атомної маси або масового номера, які звичайно зустрічаються у природі. Мічення дозволяє легко кількісно виявляти зазначену сполуку. Мічені сполуки винаходу можуть бути корисними як діагностичні інструменти, радіо-мітки або агенти моніторингу у різних діагностичних процедурах і для виявлення рецептора in vivo. Мічений ізомер винаходу, бажано, містить щонайменше один радіонуклід. Випромінюючі 2 позитрон радіонукліди є кандидатами для використання. Радіонукліди бажано вибирати з Н 3 11 13 14 13 125 123 18 (дейтерій), Н (тритій), С, С, С, 1ом ом І і F. Фізичними способами виявлення міченого ізомеру винаходу можуть бути Позитронна томографія (PET), Однофотонна комп'ютерна томографія (SPECT), Магнітно-резонансна спектроскопія (MRS), Магнітно-резонансна візуалізація (MRI) і Обчислювальна аксіальна рентгенівська томографія (CAT) або їх комбінації. Біологічна активність Сполуки згідно з винаходом можуть здійснювати модулювання норепінефрину, до-паміну і до деякої міри серотоніну і тому вони і їх фармацевтичні композиції можуть бути використані у лікуванні багатьох розладів центральної нервової системи, включаючи психіатричні розлади. Зокрема, сполуки і їх фармацевтичні композиції використовують у лікуванні розладів ЦНС, в яких порушено функції кортикальних моноаміненгічних систем внаслідок прямих або непрямих причин. Сполуки і композиції згідно з винаходом можуть бути використані у лікуванні когнітивних розладів, включаючи нейродегенеративні (наприклад, деменційні і вікові когнітивні порушення) і розлади розвитку, наприклад, розлади аутичного спектру, ADHD, церебральний параліч, синдром Туретта, а також когнітивні розлади, які є частиною корінних симптомів шизофренії. Сполуки і композиції згідно з винаходом можуть бути використані у лікуванні афективних розладів, включаючи депресію і біполярний розлад. Вони можуть також бути використані у лікуванні шизофренії і шизофренічних розладів. Сполуки і композиції згідно з винаходом можуть бути використані у лікуванні тривожних розладів, включаючи узагальнений тривожний розлад (GAD), специфічні фобії і панічний розлад (PD). Вони також можуть бути використані у лікуванні розладів сну. Було показано, що сполуки згідно з винаходом підвищують у церебральній корі позаклітинні рівні допаміну і норепінефрину і, у деяких випадках, також серотоніну. Однак, сполуки винаходу не впливають на метаболізм допаміну у смугастому тілі, що є характерним для фармакологічної діє існуючих сполук. Отже, сполуки винаходу мають несподівану і виразну фармакологію (див. табл. 1). Таблиця 1: підвищення у DOPAC рівнів (3,4-дигідроксифенілоцтової кислоти) у смугастому тілі щура після системного введення випробуваної сполуки (100 мкмоль/кг підшкірно), експресоване як підвищення (%) відносно контрольного значення. Відповідний спосіб розглянуто в описі. Таблиця 1 Порівняльні Приклади Приклад 10 посилання 1 Приклад 16 посилання 1 Приклад 26 посилання 1 Приклад 27 посилання 1 Приклад 9d посилання 2 Приклад 11d посилання 2 Приклад 1 WO2005/121092 Приклад 3 WO2005/121092 Приклад 4 WO2005/121092 Приклад 5 WO2005/121092 Приклад 8 WO2005/121092 Приклад 2 WO2005/121092 підвищення (%) DOPAC + 2622 + 1502 + 672 + 742 + 633 + 1973 + 217 + 144 + 107 + 185 + 121 + 169 Приклади DOPAC підвищення (%) 0 -16 -28 -10 Приклад 1 Приклад 2 Приклад 3 Приклад 4 12 UA 98783 C2 Продовження таблиці 1 Приклад 5 Приклад 6 Приклад 7 Приклад 8 Приклад 9 Приклад 10 Приклад 11 Приклад 12 Приклад 32 Приклад 36 5 10 15 20 25 30 35 40 45 -26 -10 0 -24 -5 -26 -4 -19 +8 -15 1. Порівняльні Приклади існуючих препаратів; Посилання 1: J. Med. Chem. 1994, 37, 2735; Посилання 2: Bioorg. Med. Chem. Lett. 1997, 7, 241-246. Посилання 3; WO 2005/121092. 2. Дані з Таблиці 2 у Посиланні 1. 3. Дані з Таблиці 2 у Посиланні 2. Дані з цього посилання накопичення DOPA, а не DOPAC. DOPAC і DOPA обидва є непрямими показниками зміни концентрації допаміну у мозку експериментальних тварин. Підвищення рівнів DOPAC і DOPA означають підвищення синтезу і обігу допаміну у системі. Накопичення DOPA є мірою концентрації 3,4-дигідроксифенілаланіну у смугастому тілі мозку. DOPAC визначає концентрацію 3,4-дигідроксифенілоцтової кислоти у смугастому тілі. Існує сильний зв'язок між DOPA і DOPAC. Можна бачити, що введення сполук, описаних у WO 2005/121092, J. Med. Chem. 1994, 37, 2735 і Bioorg. Med. Chem. Lett. 1997, викликає значне підвищення у смугастому тілі рівнів DOPAC. На відміну від цього, як було показано, сполуки винаходу несподіавано слабо діють на рівні DOPAC у смугастому тілі. З іншого боку, суттєвою характеристикою сполуки винаходу є підвищення кортикальних рівнів катехоламінів, виміряних як позаклітинні рівні допаміну і норепінефрину з застосуванням мікродіалізу, і дуже слабка дія на субкортикальні катехоламінив (фіг. 1-10). Опис тваринних моделей, використаних у винаході Вимірювання вмісту DOPAC у тканині проводили під час досліджень, починаючи з 1960-х р.р. Самцям щура Sprague-Dawely вводили випробувану сполуку за 60 хвил. перед відділенням голови. Мозок швидко виймали і розсікали. Смугасте тіло швидко заморожували і кількісно аналізували на вміст DOPAC за допомогою РХВТ і електрохімічним виявленням. Тварин використовували для кожного тесту сполуки/носія у 4 групах. Мікродіаліз (Ungerstedt, Herrera-Marschitz et al. 1982) є добре відомим способом вимірювання позаклітинних рівнів нейротрансмітерів (Ungerstedt 1991). Мікродіаліз використовують для вимірювання дії ліків на моноамінні трансмітери. Наведені графіки (фіг. 20 і 21) показують дію одного з відомих антидепресантів (міртазапіну) на моноаміни у смугастому тілі і фронтальній корі, а також дію сполук згідно з винаходом (фіг. 1-10). Кількість тварин (п), використаних для кожної випробуваної сполуки наведено на фіг. Дія на допамін і норепінефрин у кортикальних регіонах Розпізнавання Кортикальний ланцюг, що відповідає за когнітивні функції, включаючи пам'ять, увагу і робочу пам'ять, включає мережу глютаматних і GABA-нейронів, інервованих висхідними допаміненгічними і норепінефринергічними проектуваннями (Harrison, Weinberger, 2005, Arnsten, Li, 2005). Допамін, діючи через рецептори DA D1, поліпшує когнітивні функції, а гіпофункція кортикальної DA трансмісії викликає специфічні когнітивні дефіцити (розглянуті у Goldman-Rakic, 2004). Подібним чином, норепінефрин має поліпшувати когнітивні функції, ймовірно, залежно від стимуляції пост-синаптичних альфа-2 рецепторів у преф-ронтальній корі (Arnsten, 2004). Клінічними прикладами дії браку кортикального DA і NE є когнітивні розлади у шизофренії і ADHD. У шизофренії, брак кортикального DA розглядається як головна особливість когнітивних дисфункцій (Perlman et al., 2004, Goldman-Rakic, 2004). Одним з механізмів, що викликає появу такої кортикальної DA гіпофункці, вважають добре описану точкову мутацію СОМТ, що кодує ген і призводить до надмірної активності СОМТ і, отже, підвищенню швидкості усунення DA і зниженню рівнів DA, зокрема, у корі (Harrison, Weinberger, 2005, Perlman et al., 2004). Ця мутація СОМТ генетично пов'язана з шизофренією і корелює з когнітивними функціями у здорових осіб. Вважають, що окрім аномалій СОМТ, ряд інших патогенних шляхів призводять до функціонально подібного стану кортикальної дисфункці при шизофренії, маніфестацією чого є характерні аб-нормальності когнітивних функцій у шизофренічних 13 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 пацієнтів (Harrison, Weinberger, 2005). Наприклад, ряд генів вразливості, як вважають, впливають на опосередковану рецептором NMDA глютаматну трансмісію. Завдяки сприятливій дії на когнітивні функції підсиленою стимуляцією рецептора D1 DA підсилення кортикальної DA трансмісії може нормалізувати кортикальну активність і поліпшити когнітивні функції при шизофренії і інших станах (Goldman-Rakic, 2004). Крім того, оскільки абнормальності у кортикальному мікролан-цюгу вважаються головною причиною клінічного синдрому, відновлення цього мікролан-цюга поліпшенням DA трансмісії иає не тільки поліпшити когнітивні функції у шизофренії, але й послабити психотичні симптоми. Отже, нормалізація кортикальної DA трансмісії вторинною дією викликає нормалізацію субкортикальної DA трансмісії і, таким чином, послаблює симптоми, пов'язані з субкортикальною гіпердопамінергією (Goldman-Rakic, 2004, Perlman et al., 2004). Крім того, спільною ознакою атипових антипсихотичних препаратів, які, як вважають, зумовлюють їх високу ефективність і незначні побічні явища порівняно з іншими антипсихотичними сполуками, є їх здатність підвищувати кортикальний допамін (Moghaddam, Bunney, 1990, Deutch et al., 1991). Слід відзначити, що описані тут принципи винаходу, спрямовані на поліпшення когнітивності і антипсихотичних явищ, залежать від регіонально селективного кортикального підвищення у DA і NE, але не спрямовані на підвищення субкортикального DA (у смугастому тілі). Отже, сполуки згідно з винаходом підвищують кортикальну, але не субкортикальну DA трансмісію, поліпшуючи когнітивні функції і знижуючи психотичні симптоми у шизофренії. Іншими клінічними прикладами ролі DA і NE у когнітивних функціях є клінічні результати у ADHD, включаючи режим використання сполуки для полегшення симптомів цього розладу. Головними рисами ADHD є втрата уваги, тривалий брак фокусування на задачі, імпульсивність і гіперактивність (Biederman 2005, Arnsten, Li 2005). У нейропсихологічних тестах пацієнти ADHD показали погані результати тестів на специфічне оцінювання пре-фронтальних кортикальних функцій (Arnsten, Li, 2005). Структура кортикального ланцюга, відповідального за ці функції, дозволяє припустити, що недостатність DA і NE трансмісії може викликати специфічні нейропсихологічні дефіцити, що спостерігаються при ADHD. Дослідження етології ADHD вказують на розрегулювання DA і NE, зокрема, у кортикальних регіонах. Фармакологічними наявними засобами є, головним чином, психостимулятори, включаючи дексамфетамін і метилфенідат, які підвищують DA і NE у більшості зон мозку. Останнім досягненням у лікуванні ADHD є сполука атомоксетин (US 5 658 590), яка забезпечує регіонально селективну підвищення у кортикальних DA і NE, полегшуючи основні симптоми без побічної дії, пов'язані з підвищенням субкортикальної DA трансмісії, і даючи підстави вважати, що кортикальна, а не субкортикальна дія на катехоламіни є суттєвою у клінічній ефективності ліків проти ADHD (Pliszka, 2005). Все це дає суттєві свідчення того, що поліпшена кортикальна DA і NE трансмісія полегшує симптоми ADHD, а також поліпшення когнітивності. Крім того, роль кортикальних DA і NE у когнітивних функціях вказує, що поліпшення кортикальної DA трансмісії також поліпшує когнітивні функції при когнітивних розладах у випадках, не пов'язаних з шизофренією або ADHD, а також у здорових осіб. Це підтверджується кореляцією між активністю СОМТ і когнітивною здатністю у здорових осіб (Perlman et al., 2004) і численними дослідженнями на гризунах, приматах і людях впливу кортикальних DA і NE на когнітивні функції у нормальному стані, а також на різні розлади (Arnsten, 2004, Goldman-Rakic, 2004). Отже, сполуки згідно з винаходом можуть бути використані у лікуванні симптомів ADHD, a також когнітивних розладів, взагалі завдяки їх здатності регіонально селективно підвищувати рівень кортикальних DA і NE. Дія як транквілізаторів і антидепресантів Спільною особливістю всіх клінічно ефективних класів антидепресантів є підвищення рівнів допаміну і норепінефрину у корі (Tanda, Carboni et al. 1994; Millan, Lejeune et al. 2000). Наприклад, було показано, що клінічно ефективний антидепресант міртазапін (ре-мерон) підвищує переважно позаклітинні рівні норепінефрину і допаміну у корі (див. фіг. 21 і DeBoto, Flore et al. 2004). Оскільки сполуки згідно з винаходом підвищують рівні допаміну і норепінефрину у корі, це означає, що вони функціонують як антидепресанти (див. фіг. 1-10). Крім того, норепінефрин бере значну участь у нейронних шляхах, включаючи locus ceruleus, амігладалу і церебральну кору, контролюючи страх і тривожність, і тому модуляція кортикальної норепінефринної трансмісії модулює стани тривожності (Sullivan et al. 1999, Biol Psychiatry; 46:1205-121). Відповідно, сполуки, що змінюють кортикальну норепінефринну трансмісію, згідно з повідомленнями, є ефективними у лікуванні тривожних розладів. Зокрема, сполуки, що модулюють NE, наприклад, міртазапін (Remeron), який забезпечує помітне зростання рівнів кортикального NE через механізм, відмінний від пригніченні повторного поглинання NE (фіг. 21) і венлафаксин, який підвищує рівень кортикального NE пригніченням повторного поглинання 14 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 норепінефрину, має транквілізаторі властивості згідно з клінічними дослідженнями (Neuropsychopharmacology, 5th Generation of Progress, Lippincott, Williams, Wilkins, 2002, pp 967980). Базуючись на фактах, що вказують на сприятливу дію поліпшення кортикальної норепінефринної трансмісії на тривожні розлади, разом нейробіологічними даними, що вказують на вирішальну роль норепінефрину у контролі тривожності, можна дійти висновку, що сполуки винаходу, які забезпечують помітне зростанні рівня кортикального NE мають бути ефективними у лікуванні тривожних розладів. Приклади згідно з винаходом (фіг. 1-10) Фіг. 1. Приклад 1, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни Приклад 1 вводять підшкірно у момент 0. Значення, показані на фіг. 1 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 2. Приклад 1, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 1 вводять підшкірно у момент 0. Значення, показані на фіг. 2 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 3. Приклад 2, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни Приклад 2 вводять підшкірно у момент 0. Значення, показані на фіг. 3 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 4. Приклад 2, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 2 вводять підшкірно у момент 0. Значення, показані на фіг. 4 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 5: Приклад 9, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни Приклад 9 вводять підшкірно у момент 0. Значення, показані на фіг. 5 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 6. Приклад 9, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 9 вводять підшкірно у момент 0. Значення, показані на фіг. 6 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 7: Приклад 11, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни Приклад 11 вводять підшкірно у момент 0. Значення, показані на фіг. 7 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у не сплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 8. Приклад 11, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 11 вводять підшкірно у момент 0. Значення, показані на фіг. 8 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 9. Приклад 12, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 12 вводять підшкірно у момент 0. Значення, показані на фіг. 9 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Фіг. 10. Приклад 12, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни Приклад 12 вводять підшкірно у момент 0. Значення, показані на фіг. 10 репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки - SEM. 15 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 Порівняльні Приклади (фіг. 11-21) фіг. 11. (S)-(-)-3-[3-метилсульфоніл)феніл]-1-пропілпіперидин (Приклад 16 у J. Med. Chem. 1994, 37, 2735), 50 мкмоль/кг підшкірно, смугасте тіло (S)-(-)-3-[3-метилсульфоніл)феніл]-1-пропілпіперидин вводять підшкірно у момент 0. Значення, показані на фіг. 11, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 12. (S)-(-)-3-[3-метилсульфоніл)феніл]-1-пропілпіперидин (Приклад 16 у J. Med. Chem. 1994, 37, 2735), 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни, кора (S)-(-)-3-[3-метилсульфоніл)феніл]-1-пропіл піперидин вводять підшкірно у момент0. Значення, показані на фіг. 12, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін -DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 13. 4-(4-хлор-3-трифлуорметил-феніл)-1-пропіл-піперидин (Приклад 9 у WO01/46146), 50 мкмоль/кг підшкірно, смугасте тіло 4-(4-хлор-3-трифлуорметил-феніл)-1-пропіл-піперидин вводять підшкірно у момент 0. Значення, показані на фіг. 13, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 14. Приклад 3 з WO 2005/121092, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 3 WO 2005/121092 вводять підшкірно у момент 0. Значення, показані на фіг. 14, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 15. Приклад 3 з W0 2005/121092, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни, кора 4-(4-флуор-3-трифлуорметил-феніл)-1-етил-піперидин вводять підшкірно у момент 0. Значення, показані на фіг. 15, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 16. Приклад 8 з WO 2005/121092, 50 мкмоль/кг підшкірно, аміни смугастого тіла 4-(4-флуор-3-трифлуорметил-феніл)-1-етил-піперидин вводять підшкірно у момент 0. Значення, показані на фіг. 16, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 17. Приклад 8 3 WO 2005/121092, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни, кора Приклад 8 WO 2005/121092 вводять підшкірно у момент 0. Значення, показані на фіг. 17, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 18. Приклад 2 з WO 2005/121092, 50 мкмоль/кг підшкірно, аміни смугастого тіла Приклад 2 WO 2005/121092 вводять підшкірно у момент 0. Значення, показані на фіг. 18, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 19. Приклад 2 з WO 2005/121092, 50 мкмоль/кг підшкірно, перфузією, кортикальні аміни, кора Приклад 2 WO 2005/121092 вводять підшкірно у момент 0. Значення, показані на фіг. 19, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 20. Міртазапін (Remeron) 10 мг/кг підшкірно, перфузією, смугасте тіло Remeron вводять підшкірно у момент 0. Значення, показані на фіг. 20, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. фіг. 21. Міртазапін (Remeron) 10 мг/кг підшкірно, перфузією, кора Remeron вводять підшкірно у момент 0. Значення, показані на фіг. 21, репрезентують % контролю відносно базових значень. Мікродіаліз проводять на щурах у несплячому стані з 16 UA 98783 C2 5 10 15 20 25 30 35 40 45 можливістю вільно рухатись. Допамін = DA; Норепінефрин = NA; Серотонін = 5-НТ; Межі помилки = SEM. Посилання: Arnsten A.F.T. and Li В. (2005) Neurobiology of executive functions: Cathecholаmін influences on prefrontal cortical functions BIOL PSYCHIATRY 2005; 57:1377-1384 Biederman, J. Attention-Deficit/Hyperactivity Disorder: A selective overview BIOL PSYCHIATRY 2005; 57:1215-1220. Harrison, P.J. and Weinberger, D.R. (2005) Schizophrenia genes, gene expression and neuropathology. on the matter of their convergence. Molecular Psychiatry 10: 40-68. Moghaddam, B. and Bunney, B. S. (1990) Acute effects of typical and atypical antipsychotic drugs на the release of dopаmine from prefrontal cortex, nucleus accumbens, and striatum of the rat: an in vivo microdialysis study. J. Neurochem 54, 5:1755-1759. Deutch AY, Moghaddam B, Innis RB, Krystal JH, Aghajanian GK, Bunney BS, Chamey DS. (1991) Mechanisms of action of atypical antipsychotic drugs. Implications for novel therapeutic strategies for schizophrenia. Schizophr Res. Mar-Apr; 4(2):121-56. Pliszka, S.R. (2005) The neuropsychopharmacology of attention-deficit/hyperactivity disorder. Biol Psychiatry. 2005 Jun 1;57(11):1385-90. ReBiew. Ungerstedt, U. (1991). "Microdialysis-principles and applications for studies in animals and man." J. Int. Med. 230: 365-373. Ungerstedt, U., M. Herrera-Marschitz, U. Jungnelius, L. Stahle, U. Tossman and T. Zetterström (1982). Dopamine Synaptic Mechanisms Reflected in Studies Combining Behavioural Recordings and Brain Dіаlіz. Advances in Dopamine Research. M. Kohksa. Oxford, Perganon Press. 37: 219-231. DeBoto, P., G. Flore, L. Pira, G. Longu and G. L. Gessa (2004). "Mirtazapine-induced corelease of dopamine and norepinephrine from noradrenergic neurons in the medial prefrontal and occipital cortex." Eur J Pharmacol 487(1-3): 105-11. Millan, M. J., F. Lejeune and A. Gobert (2000). "Reciprocal autoreceptor and heteroreceptor control of serotonergic, dopаminergic and noradrenergic transmission in the frontal cortex: relevance to the actions of antidepressant agents." J Psychopharmacol 14(2): 114-38. Tanda, G., E. Carboni, R. Frau and G. Di Chiara (1994). "Increase of extracellular dopаmine in the prefrontal cortex: a trait of drugs with antidepressant potential?" Psychopharmacology (Berl) 115(1-2): 285-8. Goldman-Rakic, P. et al. (2004) Targeting the dopаmine D1 receptor in schizophrenia: insights for cognitive dysfunction. Psychopharmacology 174:3-16. Arnsten, A. (2004) Adrenergic targets for the treatment of cognitive deficits in schizophrenia. Psychopharmacology 174:25-31. Способи приготування Сполуки винаходу можуть бути приготовлені згідно з Схемою 1. Однак, винахід не обмежується цими способами. Ці сполуки можуть також бути приготовлені, як описано для існуючих структурно подібних сполук. Реакції можуть бути проведені згідно з стандартними процедурами (див., наприклад, Comprehensive Organic Transformation: Guide to Functional Group Preparations Richard С. Larock, 22 October, 1999 Wiley-VCH, ISBN: 0471190314; або March's Advanced organic Chemistry: Reactions, Mechanisms and Structure, 5th Edition. Michael B. Smith, Jerry March, January 15, 2001 Wiley-lnterscience, ISBN: 0471585890), або як це описано у прикладах. Вихідні матеріал для описаних процесів є відомими або можуть бути легко приготовлені відомими способами з комерційно доступних хімікатів. Фахівцю зрозуміло, що при отриманні сполук винаходу індивідуальні операції можуть бути виконані в іншому, більш зручному порядку і/або індивідуальні реакції можуть бути проведені на різних стадіях синтезу (тобто хімічні перетворення можуть бути проведені з інтермедіатами, відмінними від використаних у конкретних реакціях). 50 17 UA 98783 C2 Синтез сполуки винаходу визначено Схемою 1. Схема 1 1 5 10 15 20 25 2 3 Замісники у Схемі 1: Z - відщеплювана група, алкіл або захисна група, Аr, R , R і R визначено вище. Окислення (III) до (IV) можна здійснити за стандартною процедурою окислення (див. Handbook of Reagents for Organic Synthesis-Oxidising and Reducing Agents. S.D. Burke, R.L. Danheiser (Eds.); John. Wiley & Sons, ChichecTep, 1999, ISBN 0-471-97926-0). Сполуки винаходу можуть бути ізольовані з будь-яким рівнем чистоти стандартними способами і очищення може бути проведене звичайними відомими засобами, наприклад, дистиляцією, рекристалізацією і хроматографією. Фармацевтичні композиції В іншому аспекті винахід включає нові фармацевтичні композиції, які містять терапевтично ефективну кількість хімічної сполуки винаходу. Винахід стосується фармацевтичних композицій, що містять сполуки винаходу, і їх використання у лікуванні розладів ЦНС. Як органічні, так і неорганічні кислоти можуть бути використані для отримання нетоксичних фармацевтично прийнятних кислото-адитивних солей сполуки згідно з винаходом. Придатні кислото-адитивні солі сполуки винаходу включають ті, що утворюються фармацевтично прийнятними солями, наприклад, описані вище. Фармацевтична композиція, що включає сполуку згідно з винаходом, може також включати речовини, які допомагають приготуванню або введенню препарату. Такі речовини є добре відомими і можуть, наприклад, бути фармацевтично прийнятними ад'ювантами, носіями і консервантами. У клінічній практиці сполуки згідно з винаходом звичайно можна вводити перорально, ректально, назально або ін'єкцією, у формі фармацевтичної рецептури, яка включає активний інгредієнт як вільну основу або як фармацевтично прийнятну нетоксичну кислото-адитивну сіль, наприклад, гідрохлорид, лактат, ацетат або сульфамат, разом з фармацевтично прийнятним носієм. Носій може бути твердим, напівтвердим або рідким препаратом. Звичайно активна 18 UA 98783 C2 5 10 15 20 речовина становить 0,1-99 % рецептури, зокрема, 0,5-20 % рецептури, призначеної для ін'єкцій і 0,2-50 % (за масою) рецептури, придатної для перорального введення. Для виготовлення фармацевтичної рецептури, що містить сполуку згідно з винаходом, у формі дозованих одиниць для перорального застосування вибрана сполука може бути змішана з твердим ексципієнтом, наприклад, лактозою, сахарозою, сорбітолом, манітолом, крохмалем, наприклад, картопляним або кукурудзяним, або аьілопектином, похідними целюлози, зв'язуючими, наприклад, желатином або полівініл-піролідином, і змащувачем, наприклад, стеаратом магнію, стеаратом кальцію, поліетиленгліколем, воском, парафіном тощо, з подальшим пресуванням у таблетки. Якщо потрібно виготовити покриту таблетку, серцевина (приготовлена, як описано вище) може бути покрита концентрованим розчином цукру, який може містити, наприклад, гуміарабік, желатин, тальк, діоксид титану тощо. В іншому варіанті таблетка може бути покрита полімером, який розчиняють готовому леткому органічному розчиннику або суміші органічних розчинників. До таких покриттів можуть бути додані барвники, для полегшення розрізняння таблеток з різними активними речовинами або з різними кількостями активної сполуки. Для приготування м'яких желатинових капсул активну речовинузмішують з, наприклад, рослинною олією або поліетиленгліколем. Жорсткі желатинові капсули можуть містити гранули активної речовини і згадані вище ексципієнти для таблеток, наприклад, лактозу, сахарозу, сорбітол, манітол, крохмаль (наприклад, картопляний крохмаль, кукурудзяний крохмаль або амілопектин), похідні целюлози або желатин. Жорсткі желатинові капсули можуть містити також рідкі або напіврідкі ліки. Далі наведено приклади таблеток і капсул, придатних для перорального введення. Таблетка 1 мг/таблетка Сполука 100 Лактоза (Ph.Eur) 182,75 Кроскармелозний натрій 12,0 Паста з кукурудзяного крохмалю (5 % (маса/об'єм)) 2,25 Стеарат магнію 3,0 Таблетка II Сполука Лактоза (Ph.Eur) Кроскармелозний натрій Кукурудзяний крохмаль Полівінілпіролідон (5 % (маса/об'єм)) Стеарат магнію мг/таблетка 50 223,75 6,0 15,0 Таблетка III Сполука Лактоза (Ph.Eur) Кроскармелозний натрій Паста з кукурудзяного крохмалю (5 % (маса/об'єм)) Стеарат магнію мг/таблетка 1,0 93,25 4,0 2,25 3,0 0,75 1,0 25 30 Капсула мг/капсула Сполука 10 Лактоза (Ph.Eur) 488,5 Магній 1,5 Дозовані одиниці для ректального застосування можуть бути розчинами або суспензіями або можуть бути приготовлені у формі супозиторіїв, що включають активну речовину у суміші з нейтральною жировою основою або желатином. Ректальні капсули включають активну речовину у суміші з рослинною олією або парафіновим маслом. Рідкі препарати перорального застосування можуть мати форму сиропів або суспензій, наприклад, розчинів, що містять від приблизно 0,2 % до приблизно 20 % (за масою) активної речовини, цукор і суміш етанолу, води, гліцеролу і пропіленгліколю. Такі рідкі препарати можуть містити забарвлювачі, смакові добавки, сахарин і карбоксиметилцелюлозу, як загущувача або інші відомі ексципієнти. 19 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 Розчини для парентерального введення ін'єкцією можуть бути приготовлені у водному розчині водорозчинної фармацевтично прийнятної солі активної речовини, бажано, у концентрації приблизно 0,5-10 % за масою. Ці розчини можуть також містити стабілізатори і/або буферні агенти і можуть бути приготовлені у різних дозованих одиницях в ампулах. їх використання і введення пацієнту є легкою операцією для фахівця. Для інтраназального введення або введення інгаляцією сполуки винаходу можуть бути введені у формі розчину, сухого порошку або суспензії. Введення можна здійснювати через насосний розпилювач, який стискається пацієнтом, або через розпилювач аерозолю з контейнеру підтиском або розприскувач, з використанням придатного пропеленту, наприклад, дихлордифлуорметану, трихлорфлуорметану, дихлортетрафлуоретану, діоксиду карбон або іншого придатного газу. Сполуки винаходу можна також вводити через інгалятор сухого порошку, тонко подрібненого у комбінації з носієм (наприклад, сахарином) або мікросфер. Інгалятор, насосний розпилювач або розпилювач аерозолю може бути одно- або баготодозовим. Дозування може бути контрольоване клапаном, який подає відміряну кількість активної сполуки. Сполуки винаходу можна також вводити з контрольованим вивільненням рецептури. Сполуки вивільняються з бажаною швидкістю для підтримання постійної фармакологічної активності протягом бажаного часу. Такі дозовані форми забезпечують введення ліків у тіло протягом заздалегідь визначеного часу і підтримують рівень ліків у терапевтичних межах протягом довшого часу порівняно з звичайними неконтрольованими рецептурами. Сполуки можуть також бути приготовлені як рецептури з контрольованим вивільненням, в яких вивільнення активної сполуки є націленим. Наприклад, вивільнення сполуки може бути обмежене певним регіоном системи травлення рецептурою, чутливою до рН. Такі рецептури є добре відомими. Детальну інформацію стосовно рецептур і їх введення можна знайти в останньому виданні Remington's Pharmaceutical Sciences (Maack Publishing Co., Easton, PA). Залежно від розладу і пацієнта, що потребує лікування, і способу введення, композиції можна вводити у різних дозах. Дозування також залежить від потужності ліків, їх біозасвоюваності і частоти і способу введення. Такі дози можна вводити один, два або три або більше разів на день. Сполуки згідно з винаходом можна вводити пацієнту у дозах від 0,01 мг до 500 мг на кг маси тіла на день, хоча можливими є відхилення, які залежать від маси, статі і стану пацієнта, хвороби, що підлягає лікуванню, і вибраного способу введення. Бажаними для людини є дози від 0,1 мг до 10 мг на кг маси тіла на день, з одноразовим або багаторазовим введенням. В іншому варіанті вибирають дозу, яка забезпечує концентрацію у сироватці між 0,1 нМ до 10 мкМ сполуки. Винахід ілюструється наведеними далі прикладами, не обмежуючими об'єм винаходу. Приклад 1: (-)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,17 г, 0,85 ммоль), ацетонітрил (4 мл), карбонат натрію (0,11 г, 2,12 ммоль) і йодетан (0,13 г, 0,85 ммоль) перемішують при зовнішній температурі 72 год. Додають воду (30 мл) і водну фазу є кстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу сушать (MgSO 4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:1) дає названу сполуку (0,11 г). [ ]D = -21,4° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру. Точка плавл. 111-112 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 19), 212 (15), 141 (15), 127 (15), 71 (bр). Приклад 2: (+)-3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш енантіомеру Е1 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,14 г, 0,70 ммоль), ацетонітрил (4 мл), карбонат калію (0,09 г, 1,75 ммоль) і йодетан (0,12 г, 0,77 ммоль) нагрівають мікрохвильовим опромінюванням при 100 °C протягом 5 хвил. Додають воду (30 мл) і водну фаз екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу сушать (MgSO 4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 2:1 до 1:1) дає названу сполуку (0,11 г). [ ]D = +18,7° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру. Точка плавл. 137-139 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 19), 212 (15), 141 (15), 127(15), 71 (bр). Приклад 3: 3-(3-хлор-4-флуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 2. 3-(3-хлор-4-флуорфеніл)піролідин-3-ол (0,31 г, 1,46 ммоль), ацетонітрил (3 мл), карбонат калію (0,20 г, 1,46 ммоль), йодетан (0,12 мл, 1,5 ммоль). 20 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 Мікрохвильове опромінювання при 100 °C 20 хвил. Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 55:45). Вихід: 0,19 г. Амін перетворюють у сіль фумарової кислоти і рекристалізують з етанол/діетилетер/діізопропіл-етеру. Точка плавл. 157-158 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 9), 228 (9), 157 (13), 129 (10), 71 (bр). Приклад 4: 3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 2: 3-(2,3-дифлуорфеніл)піролідин-3-ол (0,30 г, 1,50 ммоль), ацетонітрил (3 мл), карбонат калію (0,21 г, 1,50 ммоль), йодетан (0,12 мл, 1,50 ммоль). Мікрохвильове опромінювання при 100 °C 20 хвил. Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 1:1). Амін перетворюють у сіль фумарової кислоти і рекристалізують з етанол/діетилетер/діізопропіл-етеру. Точка плавл. 119-120 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 14), 212(11), 141 (14), 127(11), 71 (bр). Приклад 5: 3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 8: 3-(3-хлор-5-флуорфеніл)піролідин-3-ол (0,30 г, 1,4 ммоль), ацетонітрил (20 мл), карбонат натрію (0,19 г, 3,5 ммоль), йодетан (0,22 г, 1,4 ммоль). Вихід: 0,17 г. Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетер/діізопропіл-етеру. Точка плавл. 169-170 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 8), 228 (7), 157 (7), 129 (7), 72 (30), 71 (bр). Приклад 6: 3-(3,5-дихлорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 8: 3-(3,5-дихлорфеніл)піролідин-3-ол (0,34 г, 1,46 ммоль), ацетонітрил (24 мл), карбонат натрію (0,20 г, 3,65 ммоль), йодетан (0,23 г, 1,46 ммоль). Нагрівають під зворотним холодильником протягом 15 хвил. Вихід: 0,24 г. Амін перетворюють у сіль фумарової кислоти і випарюють до твердого залишку. МС m/z (відносна інтенсивність 70 еВ) 259 (М+, 5), 244 (5), 173 (4), 145 (44), 71 (bр). Приклад 7: 3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 1: 3-(3,5-дифлуорфеніл)піролідин-3-ол (0,34 г, 1,7 ммоль), ацетонітрил (5 мл), карбонат натрію (0,33 г, 2,4 ммоль), йодпропан (0,17 мл, 1,7 ммоль). Перемішують 3 год. при зовнішній температурі. Очищення на Biotage Isolute SCX-3 SPE column (промивають метанолом і елююють метанол/тріетиламіном, 4:1). Вихід: 0,15 г. Амін перетворюють у сіль оксалінової кислоти і р екристалізують з метанол/діетилетеру. Точка плавл. 131-132 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 9), 212 (bр), 182 (34), 141 (19), 84 (93). Приклад 8: 3-(3,5-дифлуорфеніл)-1-етилпіролідин-3-ол До суміші 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,50 г, 2,5 ммоль) в ацетонітрилі (25 мл) додають карбонат натрію (0,34 г, 6. 25 ммоль) і йодетан (0,39 г, 2,5 ммоль) і суміш витримують під зворотним холодильником протягом 1 год. Додають воду (50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу сушать (MgSO 4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:1) дає названу сполуку (0,12 г). Амін перетворюють у сіль фумарової кислоти і ліофілізують з водою. МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 19), 212 (15), 141 (15), 127 (15), 71 (bр). Приклад 9: 3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 8: 3-(3,5-дифлуорфеніл)піролідин-3-ол (0,54 г, 2,7 ммоль), ацетонітрил (30 мл), карбонат натрію (0,38 г, 6. 75 ммоль), йодпропан (0,26 мл, 2,7 ммоль). Вихід: 0,22 г. Амін перетворюють у сіль фумарової кислоти: Точка плавл. 136-137 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 8), 213 (13), 212 (bр), 182 (34), 84 (60). Приклад 10: 3-(3,4-дихлорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 2: 3-(3,4-дифлуорфеніл)піролідин-3-ол (0,34 г, 1,46 ммоль), ацетонітрил (3 мл), крапля метанолу, карбонат натрію (0,20 г, 1,46 ммоль), йодетан (0,12 мл, 1,46 ммоль). Вихід: 0,18 г. Амін перетворюють у сіль фумарової кислоти і рекристалізують з етанол/діетилетер/діізопропіл-етеру. Точка плавл. 184-185 °C; МС m/z (відносна інтенсивність 70 еВ) 259 (М+, 7), 244 (6), 239 (8), 173 (7), 71 (bр). 21 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 11: 3-(3,5-дифлуорфеніл)-3-флуор-1-метилпіролідин Суміш 3-(3,5-дифлуорфеніл)-3-флуорпіролідину (0,17 г, 0,85 ммоль) у мурашиній кислоті (2,45 мл) і водного формальдегіду (40 %, 2,2 мл) нагрівають при 85 °C 1 год. (100 мл) і додають діетилетер, фази розділяють і водну фазу підлужують доданням водного гідроксиду натрію (5М, 20 мл). Водну фазу екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу сушать (MgSO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1) дає названу сполуку (0,12 г). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 128-129 °C; МС m/z (відносна інтенсивність 70 еВ) 215 (М+, bр), 194 (29), 193 (36), 151 (33), 57(92). Приклад 12: 3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 8: 3-(3,4-дифлуорфеніл)піролідин-3-ол (0,38 г, 1,9 ммоль), ацетонітрил (20 мл), карбонат натрію (0,26 г, 4,75 ммоль), йодетан (0,29 г, 1,9 ммоль). Витримують під зворотним холодильником 2 год., очищають РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 35:65 до 50:50). Вихід: 0,26 г. Амін перетворюють у сіль фумарової кислоти і рекристалізують з 2-пропанол/діізопропіл-етеру. Точка плавл. 157-158 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 26), 212 (18), 141 (30), 127 (23), 113(22), 71 (bр). Приклад 13: 3-(3,5-дифлуорфеніл)-3-флуорпіролідин Суміш 1-бензил-3-(3,5-дифлуорфеніл)-3-флуорпіролідину (0,65 г, 2,2 ммоль) і форміату амонію (1,4 г, 22 ммоль) у метанолі (50 мл) очищають нітрогеном і додають паладій на карбоні (65 мг). Суміш витримують під зворотним холодильником протягом 8 год. і додають паладій на карбоні (30 мг) на 4 год., 6 год. і на 7 год. відповідно. Суміш охолоджують до зовнішньої температури і фільтрують через подушку целіту. Фільтрат випарюють, додають водний карбонат натрію (10 %, 50 мл) і водну фазу екстрагують ДХМ (2 × 50 мл). Очищення колонною флеш-хроматографією на силікагелі (етилацетат/метанол, 1:1 до 0:1) дає названу сполуку (0,14 г). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетеру. Точка плавл. 176-177 °C; МС m/z (відносна інтенсивність 70 еВ) 201 (М+, bр), 181 (20), 180 (29), 158 (21), 151 (53). Приклад 14: 3-(3,5-дихлорфеніл)-3-флуорпіролідин Приготовляють згідно з Приготуваням 2: трет-бутил 3-(3,5-дихлорфеніл)-3-флуорпіролідин1-карбоксилат (0,45 г, 1,34 ммоль), ДХМ (2 мл), трифлуороцтова кислота (2 мл). Перемішують 4 год. при зовнішній температурі. Очищення на Biotage Isolute SCX-3 SPE column (промивають метанолом і елююють метанол/тріетиламіном, 4:1) і потім РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 60:40) і флеш-хроматографують на силікагелі (етилацетат/метанол, 1:0 до 1:1). Вихід: 0,15 г. Амін перетворюють у сіль гідрохлорної кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 201-202 °C; МС m/z (відносна інтенсивність 70 еВ) 235 (М+, 64), 233 (М+, bр), 213 (28), 133 (49), 120 (32). Приклад 15: 3-(2,4-дифлуорфеніл)-1-мЕТИЛпіролідин-3-ол Приготовляють згідно з Прикладом 26: 3-(2,4-дифлуорфеніл)-3-піролідин-3-ол (0,44 г, 2,21 ммоль), мурашина кислота (6,41 мл), водний формальдегід (40 %, 5,75 мл). 85 °C протягом 3 год. Вихід: 0,395 г. Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/етанол/діетилетеру. Точка плавл. 117-119 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 27), 194 (38), 127 (19), 58 (41), 57 (bр). Приклад 16: 3-(3,4-дифлуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 26: 3-(3,4-дифлуорфеніл)-піролідин-3-ол (1,32 г, 6,63 ммоль), мурашина кислота (19,2 мл), водний формальдегід (40 %, 17,2 мл). 60 °C протягом 24 год. Вихід: 0,83 г. Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 164-166 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 7), 141 (10), 113 (10), 58 (43), 57 (bр). Приклад 17: 3-(2,3-дихлорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш 3-(2,3-дихлорфеніл)піролідин-3-олу (0,35 г, 1,51 ммоль), ацетонітрилу (20 мл), карбонату калію (0,019 г, 3,77 ммоль) і йодетану (0,24 г, 1,51 ммоль) перемішують при зовнішній температурі протягом ночі, додають йодетан (0,02 мл) і отриману суміш перемішують протягом ночі. Додають воду (50 мл), водну фазу екстрагують трет-бутил 22 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 метилетером (2 × 50 мл) і об'єднану органічну фазу сушать (MgSO 4) і випарюють. Очищення колонною флеш-хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1) дає названу сполуку (0,13 г). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/етанол/діетилетеру. Точка плавл. 206-207 °C; МС m/z (відносна інтенсивність 70 еВ) 259 (М+, 5), 173 (7), 145 (6), 72 (23), 71 (bр). Приклад 18: 3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 11: 3-(3,5-дифлуорфеніл)піролідин-3-ол (0,125 г, 0,628 ммоль), мурашина кислота (1,82 мл), водний формальдегід (40 %, 1,63 мл). 65 °C протягом ночі. Амін перетворюють у сіль оксалінової кислоти і рекристалізують з мета-нол/діетилетеру (0,126 г). Точка плавл. 159-162 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 27), 141 (13), 113 (15), 58 (32), 57 (bр). Приклад 19: 3-(3-хлор-2-флуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 26: 3-(3-хлор-2-флуорфеніл)-піролідин-3-ол (0,6 г, 2,78 ммоль), мурашина кислота (8,1 мл), водний формальдегід (40 %, 7,2 мл). Очищення флешхроматографією на силікагелі (етилацетат/метанол, 2:8 до 3:8) і РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 100:0). Вихід; 0,3 г. Амін перетворюють у сіль фумарової кислоти і випарюють до двердого залишку: МС m/z (відносна інтенсивність 70 еВ) 229 (М+, 10), 157 (8), 129 (5), 58 (28), 57 (bр). Приклад 20: 3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш 3-(3-хлор-2-флуорфеніл)піролідин-3-олу (0,5 г, 2,32 ммоль), ацетонітрилу (3 мл), карбонату калію (0,48 г, 3,48 ммоль) і йодетану (0,36 г, 2,32 ммоль) нагрівають мікрохвильовим опромінюванням при 120 °C 20 хвил. Додають водний карбонат натрію (10 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл). Об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 50:50) дає названу сполуку. Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру (0,249 г). Точка плавл. 142-145,5 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 24), 228 (19), 157(15), 72(27), 71 (bр). Приклад 21: 3-(3-хлор-4-флуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 22: 3-(3-хлор-4-флуорфеніл)піролідин-3-ол (0,8 г, 3,72 ммоль), карбонат калію (1,03 г, 7,45 ммоль), йодпропан (0,83 мг, 4,86 ммоль), ацетонітрил (20 мл). Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:1 до 0:1). Вихід: 520 мг. Амін перетворюють у сіль фумарової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 157,9 °C; МС m/z (відносна інтенсивність 70 еВ) 257 (М+, 8), 228 (bр), 198 (30), 157 (15), 84 (88). Приклад 22: 3-(3-хлор-5-флуорфеніл)-1-пропілпіролідин-3-ол Суміш 3-(3-хлор-5-флуорфеніл)піролідин-3-олу (1,10 г, 5 ммоль), ацетонітрилу (20 мл), карбонату калію (1,4 г, 10,1 ммоль) і йодпропану (1,13 мг, 6,65 ммоль) перемішують при зовнішній температурі 2 год. Температуру на корткий час піднімають до 40 °C двічі протягом цього періоду. Додають воду і водну фаз екстрагують етилацетатом, об'єднану органічну фазу сушать (MgSO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1) дає названу сполуку (0,57 г). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру. Точка плавл. 157,2 °C; МС m/z (відносна інтенсивність 70 еВ) 257 (М+, 8), 228 (bр), 198 (46), 129 (36), 84 (59). Приклад 23: 3-(2,3-дифлуорфеніл)-3-флуорпіролідин До розчину 1-бензил-3-(2,3-дифлуорфеніл)-3-флуорпіролідину (1,6 г, 5,5 ммоль) у сухому 1,2-дихлоретані (10 мл) під нітрогеном додають 1-хлоретилхлорформат (600 мкл, 5,5 ммоль). Суміш перемішують при зовнішній температурі 7 год., потім додають метанол і суміш випарюють. Додають метанол (10 мл) і суміш нагрівають під зворотним холодильником протягом 4 год. Суміш випарюють і очищають колонною хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1), отримуючи названу сполуку (214 мг). Амін перетворюють у сіль гідрохлорної кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 136 °C; МС m/z (відносна інтенсивність 70 еВ) 201 (М+, 35), 151 (bр), 158 (69), 138 (45), 133 (42). 23 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 24: (+)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш енантіомеру Е1 3-(3,4-дифлуорфеніл)піролідин-3-олу (0,26 г, 1,3 ммоль), ацетонітрилу (3 мл), карбонату калію (0,269 г, 1,95 ммоль) і йодетану (0,20 г, 1,3 ммоль) нагрівають мікрохвильовим опромінюванням при 80 °C 25 хвил. Додають водний карбонат натрію (10 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу промивають розсолом, сушать (Na2SO4) і випарюють. Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 35:65 до 50:50) дає названу сполуку (0,117 г).[ ]D = +19,4° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 136-137 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 10), 207, (19), 141 (20), 72 (42), 71 (bр). Приклад 25: (-)-3-(3,4-дифлуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 24: енантіомер Е2 3-(3,4-дифлуорфеніл)-піролідин-3-олу (0,27 г, 1,35 ммоль), ацетонітрил (3 мл), карбонат калію (0,279 г, 2,02 ммоль) і йодетан (0,21 г, 1,35 ммоль). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH 3, 35:65 до 50:50). Вихід 0,14 г. [ ]D = -18,8° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 136-137 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 11), 141, (20), 113 (17), 72 (43), 71 (bр). Приклад 26: 3-(3-хлор-5-флуорфеніл)-1-метилпіролідин-3-ол Суміш 3-(3-хлор-5-флуорфеніл)піролідин-3-олу (0,4 г, 1,85 ммоль) у мурашиній кислоті (5,4 мл) і водного формальдегіду (40 %, 4,8 мл) нагрівають при 85 °C 2,5 год. Додають водний карбонат натрію (10 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 70 мл), об'єднану органічну фазу сушать (MgSO4) і випарюють. Очищення РХВТ на Waters OBD С18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 100:0) дає названу сполуку (0,131 г). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 129131 °C; МС m/z (відносна інтенсивність 70 еВ) 229 (М+, 7), 157 (5), 129(6), 58(30), 57 (bр). Приклад 27: (+)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 24: енантіомер Е1 3-(3,4-дифлуорфеніл)-піролідин-3-олу (0,26 г, 1,3 ммоль), ацетонітрил (3 мл), карбонат калію (0,269 г, 1,95 ммоль) і йодпропан (0,22 г, 1,3 ммоль). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH 3, 45:55 до 60:40). Вихід: 0,156 г. [ ]D = +19,0° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з м етанол/діетил-етер/діізопропіл-етеру. Точка плавл. 127-129 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 9), 212, (bр), 182 (32), 141 (17), 84 (58). Приклад 28: (-)-3-(3,4-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 24: енантіомер Е2 3-(3,4-дифлуорфеніл)-піролідин-3-олу (0,27 г, 1,35 ммоль), ацетонітрил (3 мл), карбонат калію (0,279 г, 2,02 ммоль) і йодпропан (137 мкл, 1,35 ммоль). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH 3, 45:55 до 60:40). Вихід: 0,125 г. [ ]D = -21,1° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з м етанол/діетил-етер/діізопропіл-етеру. Точка плавл. 128-129 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 9), 212, (bр), 182 (32), 141 (17), 84 (62). Приклад 29: (+)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 24: енантіомер Е1 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,53 г, 2,66 ммоль), ацетонітрил (3 мл), карбонат калію (0,55 г, 3,99 ммоль) і йодпропан (260 мкл, 2,66 ммоль). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 40:60 до 60:40). Вихід: 0,274 г. [ ]D = +21,2° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетеру. Точка плавл. 117-118 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 8), 212, (bр), 182 (35), 127 (12), 84 (45). Приклад 30: (-)-3-(3,5-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 24: енантіомер Е2 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,53 г, 2,66 ммоль), ацетонітрил (3 мл), карбонат калію (0,55 г, 3,99 ммоль) і йодпропан (260 мкл, 2,66 ммоль). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH 3, 40:60 до 60:40). Вихід: 0,295 г. [ ]D = -22,7° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетеру. Точка плавл. 118-119 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 9), 213, (12), 212 (bр), 182 (32), 84 (36). 24 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 31: (-)-3-(3-хлор-5-флуорфеніл)-1-етилпіролідин-3-ол Суміш (-)-1-бензил-3-(3-хлор-5-флуорфеніл)піролідин-3-олу (0,66 г, 2,16 ммоль) і йодетану (4 мл, 50,2 ммоль) витримують під зворотним холодильником протягом 4 год. Суміш випарюють і додають трет-бутил метилетер (20 мл). Розчинник зливають, додають морфолін (5 мл) і суміш нагрівають мікрохвильовим опромінюванням при 120 °C 30 хвил. Суміш випарюють і очищають двічі флеш-хроматографією на силікагелі (метанол/етилацетат, 7:3 до 3:7 і ізократно 1:1), отримуючи названу сполуку (0,26 г). [ ]D = -21,4° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетер/діізопропіл-етеру. Точка плавл. 117118 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 23), 157, (78), 130 (82), 129 (95), 71 (bр). Приклад 32: (-)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш (-)-1-бензил-3-(2,3-дифлуорфеніл-3-ол-піролідину (0,3 г, 1,04 ммоль) і йодетану (3 мл, 30,6 ммоль) нагрівають мікрохвильовим опромінюванням при 70 °C 4 год. Отриману суміш випарюють, додають морфолін (2 мл) і ацетонітрил (2 мл) і суміш нагрівають мікрохвильовим опромінюванням при 130 °C 30 хвил. Суміш випарюють і очищають РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 45:55), отримуючи названу сполуку: [ ]D = -18,7° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетеру. Точка плавл. 118-120 °C; МС m/z (відносна інтенсивність 70 еВ) 227 (М+, 15), 141, (17), 127 (15), 72 (26), 71 (bр). Приклад 33: (-)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол Приготовляють згідно з Прикладом 34: (-)-1-бензил-3-(2,3-дифлуорфеніл)піролідин-3-ол (0,40 г, 1,38 ммоль), диметил формамід (3 мл), йодпропан (1,35 мл, 13,8 ммоль) і морфолін (2 мл). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH 3, 40:60 до 60:40). Вихід: 0,174 г. [ ]D = -22,1° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 97-100 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 10), 212, (bр), 182 (34), 84 (53), 57 (14). Приклад 34: (+)-3-(2,3-дифлуорфеніл)-1-пропілпіролідин-3-ол У герметичний колбі суміш (+)-1-бензил-3-(2,3-дифлуорфеніл)піролідин-3-олу (0,40 г, 1,38 ммоль), диметил формаміду (3 мл) і йодпропану (1,35 мл, 13,8 ммоль) нагрівають мікрохвильовим опромінюванням при 80 °C 45 хвил. Отриману суміш випарюють, додають морфолін (2 мл) і суміш нагрівають мікрохвильовим опромінюванням при 130 °C 30 хвил. Додають водний карбонат натрію (10 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу промивають водним LiCl (5 %, 50 мл), сушать (Na2SO4) і випарюють. Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 40:60 до 60:40) дає названу сполуку (0,115 г). [ ]D = +22,8° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 95-98 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 8), 212, (bр), 182 (41), 84 (88), 57 (24). Приклад 35: (+)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш (+)-1-бензил-3-(3-хлор-2-флуорфеніл)піролідин-3-олу (0,31 г, 1,01 ммоль), диметил формаміду (3 мл) і йодетану (0,16 мл, 2,02 ммоль) нагрівають мікрохвильовим опромінюванням при 80 °C протягом 2 × 15 хвил. Отриману суміш випарюють, додають морфолін (2 мл) і суміш нагрівають мікрохвильовим опромінюванням при 130 °C 30 хвил. Додають водний LiCl (5 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл, сушать (Na2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1) дає названу сполуку (0,131 г). [ ]D = +27,2° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 7174 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 13), 228, (10), 157 (12), 72 (26), 71 (bр). Приклад 36: (+)-3-(2,3-дифлуорфеніл)-1-етилпіролідин-3-ол Приготовляють згідно з Прикладом 34: (+)-1-бензил-3-(2,3-дифлуорфеніл)піролідин-3-ол (0,40 г, 1,38 ммоль), диметилформамід (3 мл), йодетан (1,1 мл, 13,8 ммоль) і морфолін (2 мл). Очищення РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 45:55). Вихід: 0,11 г. [ ]D = +19,8° (метанол). Амін перетворюють у сіль фумарової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 118-120 °C; МС m/z (відносна інтенсивність 70 еВ) 228 (М+, 14), 141, (16), 127 (14), 72 (26), 71 (bр). 60 25 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 37: (-)-3-(3-хлор-2-флуорфеніл)-1-етилпіролідин-3-ол У герметичний колбі суміш (-)-1-бензил-3-(2-флуор-3-хлорфеніл-3-ол-піролідину (0,31 г, 1,01 ммоль), диметил формаміду (3 мл) і йодетану (1,35 мл, 13,8 ммоль) нагрівають мікрохвильовим опромінюванням при 80 °C 45 хвил. Отриману суміш випарюють, додають морфолін (2 мл) і суміш нагрівають мікрохвильовим опромінюванням при 130 °C 30 хвил. Додають водний LiCl (5 %, 50 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл), сушать (Na 2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 1:0 до 1:1) дає названу сполуку (0,128 г). [ ]D = -27,8° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діетилетер/діізопропіл-етеру. Точка плавл. 72-74 °C; МС m/z (відносна інтенсивність 70 еВ) 243 (М+, 11), 228, (9), 157 (12), 72 (27), 71 (bр). Приклад 38: (-)-1-бутил-3-(2,3-дифлуорфеніл)піролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(2,3-дифлуорфеніл)піролідин-3-олу (0,5 г, 2,5 ммоль), ацетонітрилу (20 мл), карбонату калію (0,69 г, 5 ммоль) і n-бутилброміду (0,25 мл, 2,6 ммоль) перемішують при зовнішній температурі 30 хвил., потім додають n-бутилбромід (0,12 мл, 1,25 ммоль) і суміш перемішують ще 1 год. Додають воду і водну фазу екстрагують етилацетатлм. Об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення флешхроматографією на силікагелі (етилацетат/метанол, 1:1) дає названу сполуку (0,35 г). [ ]D = -26° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 155,3 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+, 8), 182 (30), 98 (25), 57 (16), 212 (bр). Приклад 39: (-)-3-(2,3-дифлуорфеніл)-1-ізобутилпіролідин-3-ол Приготовляють згідно з Прикладом 38: енантіомер Е2 3-(2,3-дифлуорфеніл)піролідин-3-олу (0,5 г, 2,5 ммоль), ацетонітрил (20 мл), карбонат калію (0,69 г, 5 ммоль), 1-бром-2-метилпропан (0,32 мл, 2,97 ммоль). Перемішують 4 год. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 2:1). Вихід: 0,16 г. [ ]D = -16,1° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 176 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+ 3), 182 (45), 213 (12), 127 (6) 212 (bр). Приклад 40: (-)-3-(2,3-дифлуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 11: енантіомер Е2 3-(2,3-дифлуорфеніл)піролідин-3-олу (0,5 г, 2,5 ммоль) у мурашиній кислоті (7,2 мл) і водному формальдегіді (40 %, 6,5 мл). 65 °C протягом 5 год. Додають воду (50 мл) і суміш промивають діетилетером. Водну фазу підлужують NaOH (5M), екстрагують етилацетатом, сушать (MgSO4) і випарюють. Сиру сполуку обробляють такою ж кількістю мурашиної кислоти і водного формальдегіду протягом 5 год. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 4:1 до 2:1). Вихід: 0,7 г. [ ]D = -21,5° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 134,3 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 20), 58 (27), 141 (16), 127 (11), 57 (bр). Приклад41: (-)-1-аліл-3-(2,3-дифлуорфеніл)піролідин-3-ол Приготовляють згідно з Прикладом 8: енантіомер Е2 3-(2,3-дифлуорфеніл)піролідин-3-олу (0,5 г, 2,5 ммоль), ацетонітрил (20 мл), карбонат калію (0,69 г, 5 ммоль) і 3-бром-1-пропен (0,23 мл, 2,78 ммоль). Під зворотним холодильником 2 год. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 5:1). Вихід: 0,33 г. [ ]D = -26,6° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діізопропіл-етеру. Точка плавл. 120 °C; МС m/z (відносна інтенсивність 70 еВ) (239 (М+, 25), 198 (48), 141 (35), 127 (23), 83 (bр). Приклад 42: (-)-3-(2,3-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол Приготовляють згідно з Прикладом 43: енантіомер Е2 3-(2,3-дифлуорфеніл)-піролідин-3-олу (0,5 г, 2,5 ммоль), ацетонітрил (20 мл), карбонат калію (0,69 г, 5 ммоль), 1-бром-2-метоксиетан (0,255 мл, 2,7 ммоль). Перемішують 1 год. при зовнішній температурі. Додають 1-бром-2метоксиетан (0,05 мл, 0,53 ммоль), перемішують при 40 °C 2 хвил. Очищення флешхроматографією на силікагелі (етилацетат/метанол, 4:1). Вихід: 0,32 г. [ ]D = -20,8° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діізопропіл-етеру. Точка плавл. 146,7 °C; МС m/z (відносна інтенсивність 70 еВ) 257 (М+, 2), 212 (bр), 182 (56), 141 (9), 127 (12). 60 26 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 43: (-)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,29 г, 1,45 ммоль), ацетонітрилу (15 мл), карбонату калію (0,4 г, 2,9 ммоль) і n-бутилброміду (0,15 мл, 1,59 ммоль) перемішують при зовнішній температурі 5 год. і ще при 60 °C 2 год. Додають водний карбонат натрію (10 %, 5 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл). Об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 7:1) дає названу сполуку (0,175 г). [ ]D = -19,8° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діізопропіл-етеру. Точка плавл. 146-147 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+, 6), 212 (bр), 98 (46), 182 (35), 57 (29), 127 (13). Приклад 44: (-)-1-аліл-3-(3,5-дифлуорфеніл)піролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,29 г, 1,45 ммоль), ацетонітрилу (15 мл), карбонату калію (0,4 г, 2,9 ммоль) і алілброміду (0,13 мл, 1,59 ммоль) нагрівають при 60 °C 2 год. Додають водний карбонат натрію (10 %, 5 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл). Об'єднану органічну фазу сушать (Na 2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 7:1) дає названу сполуку (0,08 г). [ ]D = -20,3° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру. Точка плавл. 102-103 °C; МС m/z (відносна інтенсивність 70 еВ) 239 (М+, 22), 83 (bр), 198 (52), 82 (33), 84 (29), 113 (27). Приклад 45: (-)-3-(3,5-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,29 г, 1,45 ммоль), ацетонітрилу (15 мл), карбонату калію (0,4 г, 2,9 ммоль) і 2-брометилметилетеру (0,145 мл, 1,55 ммоль) перемішують при зовнішній температурі 4 год. і потім при 80 °C 1 год. Додають водний карбонат натрію (10 %, 5 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл). Об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 10:1) дає названу сполуку (0,157 г). [ ]D = -18,9° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру. Точка плавл. 130-131 °C; МС m/z (відносна інтенсивність 70 еВ) 257 (М+, 2), 212 (bр), 182 (52), 127 (12), 213 (12), 58 (8). Приклад 46: (-)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол У герметичний колбі суміш енантіомеру Е2 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,28 г, 1,45 ммоль), ацетонітрилу (15 мл), карбонату калію (0,4 г, 2,9 ммоль) і 1-бром-2-метилпропану (0,15 мл, 1,59 ммоль) перемішують при зовнішній температурі 5 год. і потім при 60 °C 2 год. Додають водний карбонат натрію (10 %, 5 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл). Об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 10:1) дає названу сполуку (0,193 г). [ ]D = -22,9° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діізопропіл-етеру: Точка плавл. 162-163 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+, 2), 212 (bр), 182 (46), 213 (13), 57 (10), 127 (10). Приклад 47: (-)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 11: енантіомер Е2 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,29 г, 1,45 ммоль), мурашина кислота (3,8 мл), водний формальдегід (40 %, 3,4 мл). 65 °C протягом 5 год. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 10:1). Вихід: 0,19 г. [ ]D = -22,8° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетер/діізопропілетеру. Точка плавл. 134-135 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 15), 57,1 (bр), 58,1 (31), 113 (13), 127(11), 141 (11). Приклад 48: (-)-3-(2,3-дифлуорфеніл)-1-(3,3,3-трифлуорпропіл)піролідин-3-ол Приготовляють згідно з Прикладом 43: енантіомер Е2 3-(2,3-дифлуорфеніл)-піролідин-3-олу (0,5 г, 2,5 ммоль), ацетонітрил (20 мл), карбонат калію (0,69 г, 5 ммоль), 1,1,1-трифлуор-3йодпропан (0,32 мл, 3,1 ммоль). Перемішують 2 год. при зовнішній температурі і 2 × 5 хвил. при 40 °C; Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 4:1). Вихід: 0,2 г. [ ]D = -14,6° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 144 °C; МС m/z (відносна інтенсивність 70 еВ) 295 (М+, 24), 212 (31), 182 (12), 139 (bp), 127 (20). 27 UA 98783 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 49: (-)-1-(циклопропілметил)-3-(2,3-дифлуорфеніл)піролідин-3-ол Приготовляють згідно з Прикладом 43: енантіомер Е2 3-(2,3-дифлуорфеніл)-піролідин-3-олу (0,58 г, 2,9 ммоль), ацетонітрил (20 мл), карбонат калію (0,69 г, 5 ммоль), циклопропілметил бромід (0,308 мл, 3,18 ммоль). Перемішують 2 год. при зовнішній температурі 2 × 5 хвил. при 40 °C. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 4:1) Вихід: 0,28 г. [ ]D = -14,3° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетеру. Точка плавл. 172,8 °C; МС m/z (відносна інтенсивність 70 еВ) 253 (М+, 4) 55 (50), 141 (18), 127 (14), 96 (bp). Приклад 50: 3-(3,4-дифлуорфеніл)-1-ізопропілпіролідин-3-ол У герметичний колбі суміш 3-(3,4-дифлуорфеніл)піролідин-3-олу (0,192 г, 0,963 ммоль), ацетонітрилу (3 мл), карбонату калію (0,133 г, 0,963 ммоль) і ізопропілброміду (0,118 г, 0,963 ммоль) нагрівають мікрохвильовим опромінюванням при 120 °C 25 хвил. Суміш фільтрують і випарюють. Очищення флеш-хроматографією на силікагелі (етилацетат/метанол, 4:1 до 1:1) і РХВТ на Waters OBD C18, 5 мкм (МеОН/33 мМ NH3, 20:80 до 55:45) дає названу сполуку (0,092 г). Амін перетворюють у сіль фумарової кислоти і рекристалізують з етанол/діетилетер/діізопропілетеру. Точка плавл. 143-147 °C; МС m/z (відносна інтенсивність 70 еВ) 241 (М+, 11), 226 (bр), 182 (46), 85 (53), 84 (31). Приклад 51: (+)-1-бутил-3-(3,5-дифлуорфеніл)піролідин-3-ол У герметичний колбі суміш енантіомеру Е1 3-(3,5-дифлуорфеніл)піролідин-3-олу (0,18 г, 0,92 ммоль), ацетонітрилу (5 мл), карбонату калію (0,25 г, 1,84 ммоль) і n-бутилброміду (0,1 мл, 1,01 ммоль) нагрівають мікрохвильовим опромінюванням при 120 °C 45 хвил. Додають водний карбонат натрію (10 %, 5 мл) і водну фазу екстрагують етилацетатом (2 × 50 мл), об'єднану органічну фазу сушать (Na2SO4) і випарюють. Очищення на Biotage Isolute SCX-3 SPE column (промивають метанолом і елююють метанол/тріетиламіном, 4:1) і флеш-хроматографією на силікагелі (етилацетат/метанол, 7:1), дає названу сполуку (0,13 г). [ ]D = +21,9° (метанол). Амін перетворюють у сіль оксаліно-вої кислоти і рекристалізують з метанол/діізопропілетеру: Точка плавл. 146-147 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+, 5), 212 (bр), 98 (66), 57 (51), 182 (39), 127 (18). Приклад 52: (+)-3-(3,5-дифлуорфеніл)-1-метилпіролідин-3-ол Приготовляють згідно з Прикладом 11: енантіомер Е1 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,18 г, 0,92 ммоль), мурашина кислота (2,6 мл), водний формальдегід (40 %, 2,45 мл). Очищення на Biotage Isolute SCX-3 SPE column (промивають метанолом і елююють метанол/тріетиламіном, 4:1) і флеш-хроматографією на силікагелі (етилацетат/метанол, 10:1). Вихід: 0,125 г. [ ]D = +19,8° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з етанол/діетилетер/діізопропілетеру. Точка плавл. 150 °C; МС m/z (відносна інтенсивність 70 еВ) 213 (М+, 14), 57 (bр), 58 (31), 113 (13), 127 (11), 141 (10). Приклад 53: (+)-3-(3,5-дифлуорфеніл)-1-ізобутилпіролідин-3-ол Приготовляють згідно з Прикладом 51. енантіомер Е1 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,18 г, 0,92 ммоль), ацетонітрил (6 мл), карбонат калію (0,25 г, 1,84 ммоль), 1-бром-2метилпропан (0,1 мл, 0,92 ммоль). Флеш-хроматографія на силікагелі (етилацетат/метанол, 9:1). Вихід: 0,18 г. [ ]D = +22,6° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діізопропілетеру. Точка плавл. 164-165 °C; МС m/z (відносна інтенсивність 70 еВ) 255 (М+, 2), 212 (bр), 182 (46), 213 (12), 127 (8), 98 (6) 1-бром-2метилпропан. Приклад 54: (+)-3-(3,5-дифлуорфеніл)-1-(2-метоксиетил)піролідин-3-ол Приготовляють згідно з Прикладом 51: енантіомер Е1 3-(3,5-дифлуорфеніл)-піролідин-3-олу (0,18 г, 0,92 ммоль), ацетонітрил (6 мл), карбонат калію (0,25 г, 1,84 ммоль) і 2брометилметилетер (0,09 мл, 0,92 ммоль). Флеш-хроматографія на силікагелі (етилацетат/метанол, 10:1). Вихід: 0,118 г. [ ]D = +22,3° (метанол). Амін перетворюють у сіль оксалінової кислоти і рекристалізують з метанол/діізопропілетеру. Точка плавл. 131-132 °C; МС m/z (відносна інтенсивність 70 еВ) 257 (М+, 2), 212 (bр), 182 (52), 213 (13), 127 (13), 58 (9). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюDisubstituted phenylpyrrolidines as modulators of cortical catecholaminergic neurotransmission
Автори англійськоюSonesson, Clas, Swanson, Lars, Pettersson, Fredrik, Waters, Nicholas, Waters, Susanna
Назва патенту російськоюДизамещенные фенилпирролидины как модуляторы кортикальной катехоламинэргической нейротрансмиссии
Автори російськоюСонессон Класс, Свансон Ларс, Петтерссон Фредрик, Вотерс Николас, Вотерс Сюзанна
МПК / Мітки
МПК: A61K 31/40, C07D 207/12, A61P 25/00
Мітки: кортикальної, нейротрансмісії, модулятори, катехоламінергічної, дизаміщені, фенілпіролідини
Код посилання
<a href="https://ua.patents.su/65-98783-dizamishheni-fenilpirolidini-yak-modulyatori-kortikalno-katekholaminergichno-nejjrotransmisi.html" target="_blank" rel="follow" title="База патентів України">Дизаміщені фенілпіролідини як модулятори кортикальної катехоламінергічної нейротрансмісії</a>
Попередній патент: Способи виготовлення полімермодифікованого поліолу, полімер-модифікований поліол, спосіб виготовлення поліуретанового пінопласту та еластичний поліуретановий пінопласт
Наступний патент: Хімічні сполуки, що є інгібіторами ненуклеозидної зворотної транскриптази
Випадковий патент: Фенілізо(тіо)ціанати і проміжні сполуки, способи їх одержання












