3,5-дизаміщені фенілпіперидини як модулятори нейротрансмісії допаміну
Формула / Реферат
1. Сполука загальної формули 1:
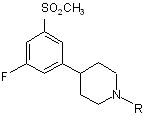 , (1)
, (1)
де R вибрано з групи: С1-С3-алкіл та аліл;
або її фармацевтично прийнятні солі.
2. Сполука за п. 1, де R вибрано з групи: н-пропіл та етил.
3. Сполука за будь-яким з пп. 1, 2, вибрана з групи:
1-етил-4-[3-флуор-5-(метилсульфоніл)феніл]піперидин;
4-[3-флуор-5-(метилсульфоніл)феніл]-1-пропілпіперидин;
1-аліл-4-[3-флуор-5-(метилсульфоніл)феніл]піперидин
або їх фармацевтично прийнятні солі.
4. Сполука за п. 1, яка є 1-етил-4-[3-флуор-5-(метилсульфоніл)феніл]піперидином, або її фармацевтично прийнятна сіль.
5. Сполука за п. 1, яка є гідрохлоридною сіллю 1-етил-4-[3-флуор-5-(метилсульфоніл)феніл]піперидину.
6. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 та один або більше фармацевтично прийнятних носіїв або розріджувачів.
7. Фармацевтична композиція за п. 6 для лікування розладу центральної нервової системи.
8. Фармацевтична композиція за п. 6 для лікування розладів руху, вибраних з групи, яка складається з нижченаведеного, хвороба Паркінсона, паркінсонізм, дискінезії (охоплюючи індуковані L-DOPA дискінезії), дистонії, судоми, тремор та хвороба Хантінгтона.
9. Фармацевтична композиція за п. 6 для лікування стану, вибраного з групи: ятрогенні та неятрогенні психози та галюцинації.
10. Фармацевтична композиція за п. 6 для лікування стану, вибраного з групи: шизофренія та шизофреноподібні розлади та біполярний розлад.
11. Фармацевтична композиція за п. 6 для лікування стану, вибраного з групи: розлади настрою та розлади з компонентом тривоги, депресія та обсесивно-компульсивна хвороба.
12. Фармацевтична композиція за п. 6 для лікування нейроеволюційних розладів, вибраних з групи: розлади різновидів аутизму, розлад з дефіцитом уваги і гіперактивністю, мозковий параліч, синдром Жиля де ла Туретта та нейродегенеративні розлади, вибрані з групи: деменція та споріднене з віком когнітивне погіршення.
13. Фармацевтична композиція за п. 6 для лікування стану, вибраного з групи: розлади сну, сексуальні розлади, розлади споживання їжі, ожиріння та головний біль і інший біль у станах, охарактеризованих збільшеним тонусом м'язів.
14. Фармацевтична композиція за п. 6 для поліпшення моторних функцій, когнітивних функцій і споріднених емоційних порушень та після пошкодження мозку, викликаного травматичними, запальними, інфекційними, неопластичними, судинними, гіпоксичними або метаболічними чинниками, або пошкодження мозку, викликаного токсичними реакціями на екзогенні хімічні сполуки, де екзогенні хімічні сполуки є вибраними з групи: речовини, якими зловживають, фармацевтичні сполуки, токсини оточуючого середовища.
15. Фармацевтична композиція за п. 6 для лікування розладу, пов'язаного зі зловживанням речовинами.
16. Фармацевтична композиція за п. 6 для лікування хвороби Альцгеймера або пов'язаних з деменцією розладів.
Текст
1. Сполука загальної формули 1: 2 (19) 1 3 93380 4 15. Фармацевтична композиція за п.6 для лікування розладу, пов'язаного зі зловживанням речовинами. 16. Фармацевтична композиція за п.6 для лікування хвороби Альцгеймера або пов'язаних з деменцією розладів. Заявлений винахід стосується нових модулятори нейротрансмісії допаміну, а більш конкретно, нових дизаміщених феніл-піперидинів та їх застосування. Допамін є нейротрансмітером у мозку. Оскільки це виявлено у 1950-х, функція допаміну у мозку добре досліджено. Зараз, добре встановлено, що допамін є незамінним у кількох аспектах функції мозку, охоплюючи моторні, когнітивні, сенсорні, емоційні та вегетативні функції (наприклад, регулювання апетиту, температур тіла, сон). Таким чином, модуляція допамінергічної функції може бути благотворною у лікуванні широких меж розладів, що вражають функції мозку. Фактично, ліки, що діють, безпосередньо або опосередковано, на центральні рецептори допаміну, звичайно застосовують у лікуванні неврологічних та психіатричних розладів, наприклад, хвороби Паркінсона та шизофренії. Однак, поточно наявні допамінергічні фармацевтичні засоби можуть мати сувору побічну дію. Наприклад, антагоністи допаміну є відомими стосовно індукування моторної (екстрапірамідальної побічної дії; EPS) та психічної побічної дії (наприклад, ангедонії, дисфорії, та погіршення пізнавальної здатності), та допамінергічні агоністи є відомими для індукування дискінезій та психозів (Goodman та Gilman's Pharmacological Basis of Therapeutics, 9th ed./McGraw-Hill, USA. Chapter 18, p.407 - 416, Chapter 22, p.509-512, p.515-516). Вибраний багатьма дослідниками підхід поліпшення ефективності та зменшення побічної дії допамінергічних фармацевтичних засобів полягає у розробці нових лігандів рецептору допаміну із селективністю стосовно конкретних підтипів рецептору допаміну або із регіональною селективністю. Ще одним класом сполук, діючих через допамінові системи мозку, є допамінергічні стабілізатори, котрі показані як корисні у лікуванні неврологічних та психіатричних розладів (A. Ekesbo, PhD Thesis, Uppsala University, Sweden: Functional consequences of dopaminergic degeneration; clinical and experimental studies using a novel stabilizer of dopaminergic systems: Ekesbo et al, (-)-OSU6162 inhibits levodopa-induced dyskinesias in a monkey model of Parkinson's disease, Neuroreport, 8, 2567, 1997; Tedroff et al. Long- lasting improvement in motor function following (-)-OSU6162 in a patient with Huntington's disease. Neurology, 22;53:1605-6, 1999; Gefvert O. et al, (-)-OSU6162 induces a rapid onset of antipsychotic effect after a single dose. A doubleblind placebo-controlled pilot study. Scandinavian Society for Psychopharmacology, 41st Annual Meeting, Copenhagen Denmark Nordic Journal of Psychiatry 54/2 93-94, April 2000. Carlsson et al, Annu. Rev. Pharmacol. Toxicol., 41, 237, 2001; Carlsson et al. Current Medicinal Chemistry, 11, 267, 20044). Ще одна допамінергічна сполука, котру позначено як стабілізатор допамін-серотонінової системи, а також частковий DA D2 агоніст рецептору є останнім часом запущеною антипсихотичною сполукою арипіпразол (Burns et al, Pharm. Exp. Ther, vol. 302, 381, 2002.). Крім того, сполуки, позначені як допамінергічні стабілізатори, описані у WO01/46145, WO01/46146, Pettersson et al. The development of ACR16. A new class of dopaminergic stabilizers. Society for Neuroscience 32nd Annual Meeting, Abstract 2002, Vol. 28 part 1 1028, Orlando USA 2002; and Nyberg et al Efficacy and tolerability of the new dopamine stabiliser ACR16 a randomised placebo-controlled add-on study in patients with schizophrenia 12th BIENNIAL WINTER WORKSHOP ON SCHIZOPHRENIA, 7-13 February 2004, Davos, Switzerland. Звичайна фармакологіча дія, що є характерною для допамінергічних стабілізаторів, як описано у WO01/46145, WO01/46146 та Pettersson et al. 2002, може бути узагальнена як: 1) Збільшене перетворення допаміну у термінальних зонах збільшуваного допамінергічного проектування мозку ссавців; 2) Відсутність або тільки слабкі поведінкові ефекти у в інших відношеннях нелікованих щурів; та 3) Інгібування поведінкових ефектів, індукованих психостимуляторами або психотоміметичними сполуками у щурів. У заявленому винаході це є позначено як профіль допамінергічного стабілізатору. Відомо, що певні фармацевтично активні сполуки, котрі застосовують у лікуванні неврологічних та психіатричних розладів (особливо антипсихотичні та антидепресантні сполуки), можуть мати небажану дію на ті серцеві калієві канали, котрі відомі, як такі, що беруть участь в електричній реполяризації серцевих клітин, звичайно позначених як hERG-канали (пов'язаний з кодованим геном етер-a-go-go потенціал-залежний калієвий канал людини) або канали ІКr (швидко активуючі затриманий вентиль струму калію). Ліки, котрі блокують ці канали, можуть індукувати шлуночкову аритмію (Torsade de Pointes, TdP), призводячи до раптової загибелі у здорових в інших відношеннях суб'єктів. Вказівки, що ліки могли б мати небажану дію на серцеву реполяризацію спостерігають через пролонгування - QT-інтервалу електрокардіограми, котрий розглядають як сурогатний маркер стосовно ризику TdP. Ряд ліків відкликано з продажу внаслідок неприйнятної побічної дії відносно серцевої аритмії (J. Cardiovasc. Electrophysiol. 15, 475, 2004.; Eur. J. Pharm., 450, 37, 2002.; Cardiovascular Research, 58, 32, 2003) Заявлений винахід стосується лікування ссавців, що потерпають від розладів центральної нервової системи, у котрих симптомами можуть бути 5 приписані допамінергічній функції, де лікування полягає у призначенні вказаному ссавцю кількості сполуки нового типу з профілем допамінергічного стабілізатору. На додаток, сполуки виявляють низьку афінність стосовно серцевих калієвих каналів, зменшуючи ризик серйозної серцевої побічної дії. Сполуки, що належать до класу заміщених 4(феніл)-N-алкіл-піперидинів представлені раніше. Серед цих сполуки, деякі є неактивними у центральній нервовій системі, деякі виявляють серотонінергічні або змішані серотонінергічні/допамінергічні фармакологічні профілі, у той час як деякі є повними або частковими агоністами або антагоністами рецепторів допаміну з високою афінністю стосовно рецепторів допаміну. Ряд похідних 4-фенілпіперидину є відомими. ЕР0369887 розкриває заміщені 4-(метатрифлуорметилфеніл)-1,2,3,6-тетрагідропіридини для лікування тривожності. WO00/03713 розкриває спосіб лікування шизофренії та інших дисфункцій допамінової системи застосуванням заміщених 1метил-4-феніл-1,2,3,6-тетрагідропіридинів. Glennon et al. (Патент США №6,057,371) заявляють спосіб лікування асоційованого з сигмарецептором розладу центральної нервової системи, який полягає у призначенні ариламінів, охоплюючи арилпіперидини, котрі є незаміщеними або моно-заміщеними на арильному кільці. Сполуки виявляють високу афінність стосовно зв'язування відносно сигма-рецептору. WO 91/095954 свідчить, що термін "висока афінність" є призначеним до середньої сполуки, котра виявляє ІК50 менше, ніж 100нМ у випробуванні проти 3H-DTG, описаному у Weber et al. Proc. Natl. Acad. Sci. (USA) 83: 87848788). Специфічно, WO 91/095954 розкриває композиції відносно "відкриття, що певні похідні фенілалкіл-амінів, амінотетралінів, піперазинів, піперидинів та споріднені похідні мають висок зв'язування до сигма-рецептору та неочікувано низьке зв'язування з рецепторами РСР та DA" (дивись сторінку 11, рядки 33-36). WO 91/095954 та WO 93/00313 вимагають, щоб сполуки мали високу афінність стосовно зв'язування до сигма-рецептору та не розкривають, що сполуки є фармакологічно активними у відсутності сигма-рецепторної афінності. На додаток, клінічні дослідження властивостей лігандів сигмарецептору у шизофреніків не дали свідоцтв ні стосовно антипсихотичної активності, ані активності у будь-якому іншому розладі центральної нервової системи. Два з найбільш екстенсивно досліджених селективних антагоністи сигма-рецепторів, BW234U (Рітсагол) та BMY14802, потерпіли невдачу у клінічних дослідженнях у шизофреніків (Borison et al, 1991, PsychoPharmacol Bull 27(2): 103-106; Gewirtz et al, 1994, Neuropsychopharmacology 10:37-40). WO97/23216 розкриває 4-заміщені піперидинові аналоги формули: 93380 6 у котрих R5 може бути вибраним з ОН, та Аr1 може бути заміщеним. Такі сполуки застосовують для лікування травм центральної нервової системи, психозу та нейродегенеративних розладів, серед іншого, через селективну блокаду підтипів рецептору NMDA. Патент США 4485109 розкриває сполуки формули: котрі застосовують як психотерапевтичні засоби, особливо як антідепресанти. ЕР 1177792 розкриває, серед іншого, сполуки із структурою: що мають допамінергічну активність - особливо як ліганди рецептору D4 - та корисні для лікування нових знайдених розладів. WO98/51668 розкриває заміщені похідні піперидину загальної формули: котрі мають властивості як нейротрансмітер моноаміну, тобто допаміну, серотоніну, норадреналіну, інгібіторів перепоглинання. Сполуки показані як корисні у лікуванні паркінсонізму, депресії, псевдодеменції, ожиріння, нарколепсії, наркоманії, та/або зловживання ліками, розладів з дефіцитом уваги та гіперактивністю, сенільної деменції або дисфункцій пам'яті. На додаток, відомо, що сполуки формули II (WO01/46145) та III (WO01/46146) мають властивості допамінергічного стабілізатору. 7 У формулі І; X, зокрема, - СН, R1 вибрано з групи: OSO2CF3, OSO2CH3, SOR3, SO2R3, COR3, CN, NO2, CONHR3, CF3 (за умови, що X - СН або С) F, СІ, Br, I (де R3 визначено нижче); R2 вибрано з групи: С1-С4-алкіл, аліл, CH2SCH3, CH2CH2OCH3, CH2CH2CH2F, CH2CF3, 3,3,3-трифлуорпропіл, 4,4,4-трифлуорбутил, або (CH2)-R4 (де R4 визначено нижче); R3 вибрано з групи: С1-С3-алкіл, CF3, або N(R2)2; R4 вибрано з групи: С3-С6-циклоалкіл, 2тетрагідрофуран, 3-тетра-гідрофуран. У формулі II; X, зокрема, - СН, R1 вибрано з групи: OSO2CF3, OSO2CH3, SOR7, SO2R7, COR7, CN, NO2, CONHR3, CF3, F, Cl, Br, І (де R3 визначено нижче), 3-тіофен, 2-тіофен, 3-фуран, 2-фуран; R2 вибрано з групи: F, СІ, Br, I, CN, CF3, CH3, OCH3, OH, NH2 R3 та R4, незалежно, -Н або С1-С4-алкіл R5 вибрано з групи: С1-С4-алкіл, аліл, CH2SCH3, CH2CH2OCH3, CH2CH2CH2F, CH2CF3, 3,3,3-трифлуорпропіл, 4,4,4-трифлуорбутил, або -(CH2)-R6; R6 вибрано з групи: С3-С6-циклоалкіл, 2тетрагідрофуран, 3-тетра-гідрофуран. R7 вибрано з групи: С1-С3-алкіл, CF3 або N(R4)2 Однак, жодний з WO01/46145 (Формул І) та WO01/46146 (Формул II) не розкривають фармакологічних даних для 3,5 дизаміщення у фенільному кільці, розкритому у заявленому винаході. Наступні структури є відомими як приклад синтезу у WO01/46146 (Приклад 44 4-[3-флуор-5(трифлуорметил)феніл-]1-пропілпіперидин). На додаток, не існує вказівок у WO01/46145 (Формула І) та WO01/46146 (Формула II) стосовно отримання потужних допамінергічних стабілізаторів. Залишається необхідність у нових фармацевтично активних сполуках, особливо корисних у лікуванні розладів у центральній нервовій системі, що мають збільшену потужність як допамінергічні стабілізатори. Також бажано, щоб будь-яка така 93380 8 фармацевтично активна сполука мала зменшену схильність до побічної дії, особливо стосовно серцевої аритмії. Об'єктом заявленого винаходу є отримання нових фармацевтично активних сполук, особливо корисних у лікуванні розладів у центральній нервовій системі, що мають збільшену потужність як допамінергічні стабілізатори (дивись таблицю 1, колонку 1) із низькою схильністю до блокування каналу hERG (дивись таблицю 1, колонку 2). Ці сполуки мають особливі переваги відносно зменшеної побічної дії, особливо серцевої побічної дії. 3,5-дизаміщення у заявленому винаході несподівано поліпшує потужність та ефективність порівняно з альтернативним заміщенням (наприклад, 3,4-дизаміщенням, у котрому у 4-положенні є галоген) або монозаміщенням (3-положення). На додаток сполуки заявленого винаходу виявляють нижчу афінність стосовно каналу hERG порівняно зі сполуками з попереднього рівня техніки. Речовини згідно із заявленим винаходом біологічно тестовані на щурах, де вони виявили дію переважно на допамінергічні системи у мозку. Вони мають вплив, на біохімічні індекси у мозку з характеристичними особливостями антагоністів допаміну. Однак, речовини згідно з винаходом не показують інгібіторної дії на спонтанну локомоцію у широких межах доз. Далі, речовини згідно з винаходом можуть індукувати слабку поведінкову активацію, зокрема, коли базова локомоторна активність є низькою. Однак, речовини у заявленому винаході інгібують поведінкову активацію, індуковану психостимуляторами та психотоміметиками. Речовини згідно із заявленим винаходом виявляють низьку потужність при інгібуванні каналу hERG, як виміряно за допомогою ІК50 у швидкому випробуванні ICE (стосовно деталей дивись експериментальний розділ), вказуючи на низький ризик стосовно пролонгування інтервалу QT та аритмії у людини. Заявлений винахід стосується нових піперидинів у формі вільної основи або її фармацевтично прийнятних солей, фармацевтичних композицій, що містять вказані сполуки та застосування вказаних сполук у виробництві фармацевтичних засобів, які є нейротрансмітерами допаміну та терапії. Більш конкретно, заявлений винахід стосується піперидинових сполук загальної формули 1: де R вибрано з групи: С1-С3-алкіли та аліл; та їх фармацевтично прийнятних солей. У певних втіленнях R вибрано з групи: нпропіл та етил. Згідно з наступним аспектом винахід стосується способу лікування розладів центральної нервової системи застосуванням терапевтично активної кількості сполуки загальної формули 1 або її фар 9 мацевтично прийнятної солі до ссавця, охоплюючи людину, що потерпає від розладу центральної нервової системи. Додатково, заявлений винахід стосується способу лікування будь-якого з перерахованих тут розладів застосуванням терапевтично активної кількості сполуки загальної формули 1 або її фармацевтично прийнятної солі до ссавця, охоплюючи людину, що потерпає від вказаного розладу. Уведення двох замісників на арильне кільце таких сполук - один у 3-положення (мета 1), а інший у 5-положення (мета 2) - збільшує їх потужність у тому, що модулює нейротрансмісію допаміну. Безпрецедентне збільшення потужності цих 93380 10 3,5-дизаміщених сполук порівняно з монозаміщеними або 3,4-дизаміщеними сполуками є ілюстрованим у таблиці 1. На додаток, 3,5 дизаміщення у заявленому винаході є виявленим стосовно зменшення побічної дії відносно серцевої аритмії, яку виміряно за допомогою впливу цих сполуки на калієвий канал hERG (Швидкий ICE). Безпрецедентне зменшення побічної дії таких заміщених сполук є ілюстрованим у таблиці 1. Порівняльні приклади з попереднього рівня техніки уведені також. Стосовно способів та статистичних розрахунків дивись вставлені тести. Таблиця 1 Вплив сполук заявленого винаходу на зменшення амфетамін-індукованої гіпер-локомоції (оцінені значення ED50) та афінності стосовно іонного каналу hERG (значення ІК50) Важливим спостереженням є те, що присутність замісників F та SO2CH3 у мета 1 та мета 2 положеннях у фенільному кільці поліпшує ефективність та потужність допамінергічного стабілізатору порівняно з моно або 3,4 дизаміщенням (напри клад, Приклад 6 WO01/46145 та Приклад 9 WO01/46146), але також зменшує афінність стосовно каналу hERG. Такий результат не було передбачено як загальне правило 11 Одною метою заявленого винаходу є отримання нових сполук для терапевтичного застосування, а більш точно, сполук для модуляції допамінергічних систем у мозку ссавців, охоплюючи мозок людини. Переважно такі сполуки мають знижену побічну дію відносно інгібування серцевого калієвого каналу. Ще одною метою винаходу є отримання сполук із терапевтичною дією після перорального призначення. Кращими заміщеними структурами є 1-етил-4-[3-флуор-5(метилсульфоніл)феніл]піперидин 4-[3-флуор-5-(метилсульфоніл)феніл]-1пропілпіперидин 1-аліл-4-[3-флуор-5(метилсульфоніл)феніл]піперидин Сполуки та композиції згідно із заявленим винаходом мають допамін-модулювальні властивості та є корисними у лікуванні ряду розладів центральної нервової системи, охоплюючи психіатричні та неврологічні розлади. Особливо, сполуки та їх фармацевтичні композиції можна застосовувати у лікуванні розладів центральної нервової системи, де допамінергічна система є дисфункціональною внаслідок безпосереднього або опосередкованого чиннику. Сполуки та композиції згідно з винаходом можна застосовувати для поліпшення усіх форм психозу, охоплюючи шизофренію та шизофреноподібні розлади, а також індуковані ліками психотичні розлади та біполярний розлад. Їх можна також застосовувати у лікуванні стану, вибраного з групи: ятрогенні та неятрогенні психози та галюцинації. Розлади настрою та розлади з компонентом тривоги, охоплюючи депресію та обсесивнокомпульсивну хворобу можна також лікувати сполуками та композиціями згідно з винаходом. Сполуки з модулювальною дією на допамінергічні системи можна також застосовувати для поліпшення когнітивних функцій та у лікуванні емоційних порушень, споріднених зі старінням, нейродегенеративних порушень (наприклад, деменції та споріднених з віком когнітивних погіршень) та еволюційних порушень (як-то розлади спектру аутизму, розлади з дефіцитом уваги і гіперактивністю, мозковий параліч, синдром Жилля де ла Туре), а також після поранення мозку. Такі поранення мозку можуть бути індукованими травматичними, запальними, інфекційними, неопластичними, судинними, гіпоксичними або метаболічними чинниками або токсичними реакціями на екзогенні хімічні продукти, де екзогенні хімічні продукти є вибраними з групи: речовини, якими зловживають, фармацевтичні сполуки та токсини оточуючого середовища. Сполуки та їх фармацевтичні композиції є корисними для лікування стану, вибраного з групи: розлади сну, сексуальні розлади, розлади споживання їжі, ожиріння та головний біль та інші види болю у станах, охарактеризованих збільшеним тонусом м'язів. їх можна також застосовувати у лікуванні хвороби Альцгеймера або споріднених з деменцією розладів. 93380 12 Сполуки та композиції згідно з винаходом можна також застосовувати при поведінкових розладах, звичайно спершу діагнозованих у ранньому дитинстві, дитинстві, або юнацтві, а також у розладах контролю збудження. Їх можна також застосовувати для лікування розладів зловживання речовинами, а також розладів, охарактеризованих зловживанням їжею. Неврологічні показання охоплюють застосування сполук та їх композицій для поліпшення психічних та моторних функцій при хворобі Паркінсона, дискінезії (охоплюючи індуковані L-DOPA дискінезії), та при синдромах, споріднених з хворобою Паркінсона. їх можна також застосовувати для поліпшення тику та тремору відмінного походження. Більш того, їх можна застосовувати для полегшення болю у станах, охарактеризованих збільшеним тонусом м'язів. Їх можна також застосовувати у лікуванні хвороби Хантингтона та інших розладах рухомості, а також розладах рухомості, індукованих ліками. Синдром втомлених ніг та споріднені розлади, а також нарколепсія можуть також бути лікованими сполуками згідно з винаходом. Заявлений винахід також стосується застосування сполуки загальної формули 1, яку визначено вище, де R вибрано з групи: С1-С3-алкіли та аліл, або її фармацевтично прийнятної солі у виробництві фармацевтично активних препаратів для лікування розладу центральної нервової системи. Розлад центральної нервової системи може бути одним або більше з описаних вище розладів. У певних втіленнях застосування, R вибрано з групи: н-пропіл та етил. Сполуки згідно із заявленим винаходом показані як такі, що виявляють профіль допамінергічного стабілізатору із поліпшеною потужність (Таблиця 1). Вони мають вплив на біохімічні індекси у мозку із характеристичними особливостями антагоністів допаміну, наприклад тими, що виявляють збільшення концентрації метаболітів допаміну. У щурах у прикладі 1 3,4 дигідроксифенілоцтова кислота (DOPAC) підвищується у стріатумі до 318% контролю при 100мкмоль/кг підшкірно. Приклад 2 збільшує DOPAC до 292% при 100мкмоль/кг підшкірно. Сполуки заявленого винаходу не показують ефекти на спонтанну локомоцію у широких межах доз (1-100мкмоль/кг підшкірно). У деяких випадках, зокрема, коли базова активність є низькою, вони можуть індукувати слабку поведінкову активацію. Поведінкова активація є обмеженою, не досягаючи сильного збільшення активності, індукованої безпосередніми або опосередкованими допамінергічними агоністами. З іншого боку кращі речовини зменшують збільшення активності, індукованої безпосередніми або опосередкованими допамінергічними агоністами, тобто d-амфетаміном та наближеними засобами (Таблиця 1). Таким чином, сполуки заявленого винаходу показують профіль допамінергічного стабілізатору з поліпшеною або підтримуваною потужністю (Таблиця 1) порівняно зі сполуками загальної формули І та II. На додаток, картина специфічного 13 заміщення зменшувала потужність при інгібуванні каналу HERG. Внаслідок втягання допаміну у велику кількість функцій центральної нервової системи та нестачі зараз доступних клінічних даних стосовно фармацевтичної дії на допамінові системи, новий клас допамінергічних модуляторів представлених у заявленому винаході, може виявитися набагато кращім за зараз відомі допамінергічні сполуки у лікуванні кількох розладів, споріднених з дисфункціями центральної нервової системи, у термінах ефективності, а також зменшеної побічної дії. Сполуки заявленого винаходу також показані як такі, що виявляють високу метаболічну стабільність у мікросомах печінки щурів, виміряну як перетворення протягом 15 хвилин (Приклад 1 5%, Приклад 2 0%,), та високу пероральну біозасвоюваність у щурів, показану у прикладі 2 (приблизно 85%). Ці сполуки є, таким чином, придатними для отримання перорально призначених фармацевтичних засобів. Не існує у попередньому рівні техніки довідок стосовно отримання сполуки з цим впливом на поведінкові та допамінові системи у мозку. Фармакологія Є наявними свідоцтва, що допамінергічна нейротрансмісія у центральній нервовій системі є порушеною при психіатричних та неврологічних хворобах. У багатьох випадках, наприклад, при шизофренії, хворобі Паркінсона, хворобі Хантингтона, біполярному розладі та при деменції, фармакотерапія на основі антагонізму або агонізму стосовно рецепторів допаміну є корисною, але не оптимальною. В останні роки багато спроб зроблено у пошуку нових та селективних сполук для підтипів рецептору допаміну (D1, D2, D3, D4, D5) з метою поліпшення ефективності та зменшення побічної дії. Заявлений винахід пропонує ще один компонент для нових терапевтичних засобів на основі взаємодій з допаміновою системою. Винахід стосується сполук, що мають як їх головну особливість стабілізувальну дію на допамінергічну систему у мозку. Опис тваринних моделей, застосованих у винаході Сполуки згідно з винаходом мають вплив на нейрохімію мозку, подібну до впливу антагоністів рецепторів допаміну D2 (тобто залежне від дози збільшення метаболіту допаміну DOPAC, у кортикальних, стріарних та лімбічних регіонах мозку). Сполуки згідно з винаходом не показують або показують тільки обмежену інгібіторну дію на спонтанну локомоцію. У певних умовах вони можуть індукувати поведінкову активацію. Поведінкова 93380 14 активація є обмеженою, не досягаючи сильного збільшення активності, індукованої безпосередніми або опосередкованими агоністами рецепторів допаміну. Однак, кращі речовини зменшують збільшення активності, індукованої опосередкованим допамінергічним агоністом d-амфетамін. Збільшення активності після лікування d-амфетаміном є стандартною моделлю гіпердопамінергії (Таблиця 1). У цій моделі, допамінергічна нейротрансмісія збільшується системним застосуванням dамфетаміну у дозі, що є достатньо високою для отримання великого збільшення локомоторної активності. Здатність сполуки до протидії цій пперактивності відбиває анті-допамінерпчні властивості, котрі є частиною профілю допамінерпчного стабілізатору Більш того, антагонізм індукованої dамфетаміном пперактивності є широко застосованим як стандартне випробування антипсихотичної активності (дивись Psychopharmacology 4th Generation of progress Chapter 68, p.793-795) Ще одна тваринна модель антипсихотичної активності є на основі застосування антагоністу глутамату МК-801 Антагоністи глутамату (тобто антагоністи NMDA), можуть індукувати психози у людини (дивись Psychopharmacology, 4th Generation of progress Chapter 101, p.1205 та 1207) та індукують поведінкові аберації у тварин Таким чином, здатність ліків впливати на шизофренію та психотичні стани може бути виміряною, застосовуючи поведінкові моделі на основі експериментально індукованих ппоглутаматерпчних станів У цьому дослідженні антагоніст NMDA МК-801 (0,7мг/кг інтраперитонеально) було застосовано для створення ппоглутаматерпчного стану, де щури виявляють анормальну, пперактивну поведінку Сполуки у заявленому винаході залежно від дози обертають поведінкову аберацію, індуковану МК801 (дивись таблицю 2) Відомо, що допамінерпчні системи мозку сильно взаємодіють із іншими трансмітерними системами (дивись Psychopharmacology, 4th Generation of progress, Chapter 101, сторінки 12081209) Такі взаємодії можуть пояснити потужну дію допамінерпчних стабілізаторів на поведінкові аберації, індуковані антагоністом глутамату МК-801 хоча ці аберації не мають перед усім основою або чинником зміни у допамінерпчній трансмісії. Дія сполук заявленого винаходу на локомоторну активність у попередньо лікованих МК-801 щурів (0,7мг/кг інтраперитонеально 90 хвилин перед тест-сполукою). Тварини були розміщеними у вимірювачі рухомості безпосередньо після застосування тест-сполук та локомоторну активність було зареєстровано між 30 та 60 хвилинами після застосування (імпульсів/30 хвилин ± SEM) 15 93380 16 Таблиця 2 Заявлений винахід стосується сполук, що мають як їх головну особливість, стабілізувальну дію на допамінергічну систему у мозку. Ці сполуки є корисними для лікування розладів центральної нервової системи, у котрій симптоми можуть бути під впливом допамінергічних функцій. На підтримку цього ствердження, дивись наступні посилання: ку* На підтримку шизофренії та психозу, заявники посилаються на Psychopharmacology 4th Generation of progress Chapter 26, p. 295-301); * Хвороба Паркінсона (Psychopharmacology 4th Generation of progress Chapter 26, p.295, Chapter 1479-1482); * Розлади з компонентом тривоги (Psychopharmacology 4th Generation of progress Chapter 21, p.227 та 237, Chapter 111, p.1317-1318 та 1320); * Розлади настрою (Psychopharmacology 4th Generation of progress Chapter 80, p.921-928;та * Зловживання речовинами (Psychopharmacology 4th Generation of progress Chapter 25, p.283 and 292, Chapter 66, p.759-760, Chapter 147, p.1725 (диваись також Nisell et al, "Systemic Nicotine-Induced Dopamine Release in the Rat Nucleus Accumbens is Regulated by Nicotinic receptors in the Ventral Tegmental Area; Synapse (1994) 16: 36-44). Chapter 149, p.1745-1747 and 1751-1752). Drugs abused by humans preferentially increase synaptic dopamine concentrations in the mesolimbic system of freely moving rats Di Chiara et al Proc Natl Acad Sci USA 85, 521 A, 1988. Drug addiction as a disorder of associative learning. Role of nucleus accumbens shell/extended amygdala dopamine Ann N.Y. Acad Sci 877,461, 1999. Як показано у цих посиланнях, заявлені стани є визнаними у попередньому рівні техніки як хвороби, котрі стосуються допамінергічної нейротрансмісії. Більш того, фармакологічна взаємодія із допамінергічною нейротрансмісією, як широко вважають, є корисною у лікуванні кількох розладів центральної нервової системи, котрі не вважають взагалі безпосередньо викликаними розладами у допамінергічній нейротрансмісії. Наприклад, симптоми хвороби Хантингтона та інших розладів рухомості можуть бути лікованими допамінергічними засобами внаслідок втягування допаміну у моторні функції (дивись Psychopharmacology 4th Generation of progress, Chapter 26, p. 295-301). Подібно, відомо, що когнітивні розлади (дивись Psychopharmacology 4th Generation of progress Chapters 25, p.292, Chapter 120, p.1417 та 1420, Chapter 123, p.1447 та 1452 та 1455-1457) аутизм (дивись Psychopharmacology 4th Generation of progress Chapter 142, p.1653 та 1661), розлади з дефіцитом уваги та гіперактивністю (дивись Psychopharmacology 4th Generation of progress Chapter 141, p. 1643 та 1649-1650), сексуальні розлади (дивись Psychopharmacology 4th Generation of progress Chapters 65, p.743-746 та Chapter 22, p.245 та 254) та розлади споживання їжі (дивись Psychopharmacology 4th Generation of progress Chapters 137, p.1600, Chapter 138, p.1609-1610 та 1612) можна лікувати засобами інтенсифікації допамінергічної трансмісії. Таким чином, вищенаведені посилання підтримують аргумент, що сполуки винаходу могли б бути корисними у лікуванні таких хвороб. * На підтримку шизофренії та психозу, заявники посилаються на Psychopharmacology 4th Generation of progress Chapter 26, p.295-301); * Хвороба Паркінсона (Psychopharmacology 4th Generation of progress Chapter 26, p.295, Chapter 1479-1482); * Розлади з компонентом тривоги (Psychopharmacology 4th Generation of progress Chapter 21, p.227 та 237, Chapter 111, p.1317-1318 та 1320); * Розлади настрою (Psychopharmacology 4th Generation of progress Chapter 80, p.921-928;та * Зловживання речовинами (Psychopharmacology 4th Generation of progress 17 Chapter 25, p.283 and 292, Chapter 66, p.759-760, Chapter 147, p.1725 (дивись також Nisell et al, "Systemic Nicotine-Induced Dopamine Release in the Rat Nucleus Accumbens is Regulated by Nicotinic receptors in the Ventral Tegmental Area; Synapse (1994) 16: 36-44). Chapter 149, p.1745-1747 and 1751-1752). Drugs abused by humans preferentially increase synaptic dopamine concentrations in the mesolimbic system of freely moving rats Di Chiara et al Proc Natl Acad Sci USA 85, 5274, 1988. Drug addiction as a disorder of associative learning. Role of nucleus accumbens shell/extended amygdala dopamine Ann N.Y. Acad Sci 877,461, 1999. Як показано у цих посиланнях, заявлені стани є визнаними у попередньому рівні техніки як хвороби, котрі стосуються допамінергічної нейротрансмісії. Більш того, фармакологічна взаємодія із допамінергічною нейротрансмісією, як широко вважають, є корисною у лікуванні кількох розладів центральної нервової системи, котрі не вважають взагалі безпосередньо викликаними розладами у допамінергічній нейротрансмісії. Наприклад, симптоми хвороби Хантингтона та інших розладів рухомості можуть бути лікованими допамінергічними засобами внаслідок втягування допаміну у моторні функції (дивись Psychopharmacology 4th Generation of progress, Chapter 26, p. 295-301). Подібно, відомо, що когнітивні розлади (дивись Psychopharmacology 4th Generation of progress Chapters 25, p.292, Chapter 120, p.1417 та 1420, Chapter 123, p.1447 та 1452 та 1455-1457) аутизм (дивись Psychopharmacology 4th Generation of progress Chapter 142, p.1653 та 1661), розлади з дефіцитом уваги та гіперактивністю (дивись Psychopharmacology 4th Generation of progress Chapter 141, p.1643 та 1649-1650), сексуальні розлади (дивись Psychopharmacology 4th Generation of progress Chapters 65, p.743-746 та Chapter 22, p.245 та 254) та розлади споживання їжі (дивись 93380 18 Psychopharmacology 4th Generation of progress Chapters 137, p. 1600, Chapter 138, p. 1609-1610 та 1612) можна лікувати засобами інтенсифікації допамінергічної трансмісії. Таким чином, вищенаведені посилання підтримують аргумент, що сполуки винаходу могли б бути корисними у лікуванні таких хвороб. Широко визнано, що інгібування каналу HERG може індукувати сувору серцеву побічну дію, охоплюючи летальну аритмію (J. Cardiovasc. Electrophysiol. 15, 475, 2004.; Eur. J. Pharm., 450, 37, 2002.; Cardiovascular Research, 58, 32, 2003). Таким чином, у розробці нових фармацевтичних засобів для центральної нервової системи є потрібними сполуки із мінімальною афінністю стосовно каналу HERG, призводячи до широких меж безпечності. Способи отримання Сполуки винаходу можна отримувати як показано нижче у схемі 1. Однак, винахід не є обмеженим цими способами. Сполуки можуть також бути отриманими, як описано для структурно споріднених сполук у попередньому рівні техніки. Реакції можна здійснювати стандартними способами1,2, або як описано у прикладах. Вихідні матеріали для способів, описаних у цій заявці є відомими або їх можна легко отримати звичайними способами з комерційно доступних хімічних продуктів. Спеціалісти повинні розуміти, що для отримання сполуки винаходу альтернативним, а у деяких випадках, більш зручним способом, індивідуальні етапи процесу можуть бути проведеними у відмінному порядку, та/або індивідуальні реакції можуть бути проведеними на відмінних етапах загального шляху (тобто хімічні перетворення можуть бути проведеними з відмінними проміжними сполуками, ніж ті, що асоційовані вище з конкретною реакцією). 19 Посилання 1. Comprehensive Organic Transformations: A Guide to Functional Group Preparations Richard С Larock, 22 October, 1999 Wiley-VCH ISBN: 0471190314 2. March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 5th Edition. Michael B. Smith, Jerry March, January 15, 2001 Wiley-lnterscience ISBN: 0471585890 Як застосовано тут, термін С1-С3-алкіл стосується алкілу, що містить 1-3 атоми карбону у будьякій ізомерній формі. Різні карбонові частини визначають таким чином: Алкіл стосується аліфатичного вуглеводневого радикалу та охоплює нерозгалужені форми, як-то метил, етил, н-пропіл,. Термін "аліл" стосується групи -СН2-СН=СН2. Термін "пацієнт", застосований тут, стосується індивіду, якому необхідне лікування згідно з винаходом. Термін "лікування", застосований тут, стосується як лікування для зцілення або полегшення хвороби або стану, так і лікування для попередження розвитку хвороби або стану. Лікування може бути проведеним гострим або хронічним шляхом. Органічні та неорганічні кислоти можуть бути застосовуваними для утворення нетоксичних фармацевтично прийнятних кислотно-адитивних солей сполук згідно з винаходом. Придатні кислотноадитивні солі сполук заявленого винаходу охоплюють фармацевтично прийнятні солі, як-то толуолсульфонат, метансульфонат, фумарат, гідрохлорид, гідробромід, гідройодид, нітрат, ацетат, лактат, цитрат, кислот цитрат, тартрат, бітартрат, аліфатичні, аліциклічні, ароматичні або гетероциклічні карбоксилати, сукцинат, малеат, фумарат, глюконат, гліколат, сахарат, аскорбат, ацетат, пропіонат, бензоат, піруват, памоат [тобто, 1,1'метилен-біс-(2-гідрокси-3-нафтоат)], фосфат, кислий фосфат, сульфат або бісульфат. Ці солі легко отримати способами, відомими у попередньому рівні техніки. Також зрозуміло, що сполуки заявленого винаходу можуть існувати у сольватованій, а також несольватованій формах, як-то, наприклад, гідратованих формах. Фармацевтичні композиції, що містять сполуку згідно з винаходом можуть також містити речовини, застосовувані для полегшення вироблення фармацевтичних препаратів або застосування препаратів. Такі речовини добре відомі спеціалістам та можуть, наприклад, бути фармацевтично прийнятними імуностимуляторами, носіями та консервантами. У клінічній практиці сполуки, застосовані згідно із заявленим винаходом, треба звичайно призначати перорально, ректально, назально або ін'єкцією, у формі фармацевтичних препаратів, які містять активний інгредієнт як вільну основу або як фармацевтично прийнятну нетоксичну, кислотноадитивну сіль, як-то гідрохлорид, лактат, ацетат, сульфамат, в асоціації з фармацевтично прийнятним носієм. Носій може бути твердим, напівтвердим або рідким препаратом. Звичайно активна речовина повинна складати між 0,1 та 99мас.% 93380 20 препарату, більш конкретно між 0,5 та 20мас.% для препаратів, призначених для ін'єкцій та між 0,2 та 50мас.% для препаратів, придатних для перорального призначення. Для виготовлення фармацевтичних препаратів, що містять сполуку згідно з винаходом у формі окремої дози для перорального застосування, вибрана сполука може бути змішаною з твердим наповнювачем, як-то лактоза, сахароза, сорбітол, манітол, крохмалі, як-то картопляний крохмаль, кукурудзяний крохмаль або амілопектин, похідні целюлози, зв'язувальний засіб, як-то желатин або полівініл-піролідин, та мастильний засіб, як-то магній стеарат, кальцій стеарат, поліетиленгліколь, воски, парафін, тощо, та тоді спресованою у таблетки. Якщо є потрібними покриті таблетки, серцевини, отримані, як описано вище, можуть бути покритими концентрованим розчином цукру, котрий може містити, наприклад, гуміарабік, желатин, тальк, титан діоксид, тощо. Альтернативно, таблетка може бути покритою полімером, відомим спеціалістам, розчиненим у легко летючому органічному розчиннику або суміші органічних розчинників. Барвники можуть бути доданими до цих покриттів для мети легко відрізняти таблетки, що містять відмінні активні речовини або відмінні кількості активної сполуки. Для отримання м'яких желатинових капсул, активна речовина може бути змішаною, наприклад, з рослинною олією або поліетиленгліколем. Тверді желатинові капсули можуть містити гранули активної речовини, застосовуючи згадані наповнювачі для таблетки, як-то лактоза, сахароза, сорбітол, манітол, крохмалі (наприклад, картопляний крохмаль, кукурудзяний крохмаль або амілопектин), похідні целюлози або желатин. Також рідкими або напівтвердими лікам можуть бути заповнені тверді желатинові капсули. Приклади композицій таблеток та капсул, придатних для перорального призначення, надані нижче: Таблетка І мг/таблетк Сполука 100 Лактоза Ph.Eur 182,75 Натрій-кроскармелоза 12,0 Кукурудзяний крохмаль, паста (5мас./об.% пасти) 2,25 Магній стеарат 3,0 Таблетка II мг/таблетку Сполука 50 Лактоза Ph.Eur 223,75 Натрій-кроскармелоза 6,0 Кукурудзяний крохмаль 15,0 Полівінілпіролідон (5мас./об.% пасти) 2,25 Магній стеарат 3,0 Таблетка III мг/таблетку Сполука 1,0 Лактоза Ph.Eur 93,25 Натрій-кроскармелоза 4,0 Кукурудзяний крохмаль,паста (5мас./об.% пасти) 0,75 Магній стеарат 1,0 21 Капсула Сполука Лактоза Ph.Eur Магнезія 93380 мг/капсул 10 488,5 1,5 Окремі дози для ректального застосування можуть бути розчинами або суспензіями або їх можна отримувати у формі супозиторіїв, які містять активну речовину у суміші із нейтральною жировою основою, або желатинових ректальних капсул, які містять активну речовину у суміші з рослинною олією або парафіновою оливою. Рідкі препарати для перорального застосування можуть бути у формі сиропів або суспензій, наприклад, розчинами, що містять приблизно від 0,2% до 20мас.% активної речовини, балансом є цукор та суміш етанолу, води, гліцерину та пропіленгліколю. Необов'язково такі рідкі препарати можуть містити барвники, смакові засоби, сахарин та карбоксиметилцелюлозу як загусник, або інші наповнювачі, відомі для людини у попередньому рівні техніки. Розчини для парентерального застосування ін'єкцією можна отримувати у водному розчині водорозчинної фармацевтично прийнятної солі активної речовини, переважно у концентрації приблизно від 0,5% до 10мас.%. Ці розчини можуть також містити стабілізувальні засоби та/або буферувальні засоби та можуть бути зручно запропонованими в різних ампулах для окремих доз. Застосування та призначення пацієнту, якого лікують у клініці, легко визначити спеціалістам. Для інтраназального призначення або призначення інгаляцією, сполуки заявленого винаходу можуть бути доставленими у як розчин, сухий порошок або суспензія. Застосування може бути за допомогою контейнеру з насосом для розпилення, який призводить у дію пацієнт, або за допомогою аерозольного розпилення з аерозольного балону чи розпилювачу, із" застосуванням придатного пропеленту, як-то дихлордифлуорметан, трихлорфлуорметан, дихлортетрафлуоретан, карбон діоксид або інший придатний газ. Сполуки винаходу можна також призначати за допомогою інгалятору для сухого порошку як мілко подрібнений порошок у комбінації із носієм (наприклад, сахаридом) або як мікросфери. Інгалятор, насос для розпилення або аерозольне розпилення можуть бути як одиничні або багатократні дози. Дозування можуть бути контрольованим клапаном, котрий постачає виміряну кількість активної сполуки. Сполуки винаходу можна також призначати у композиції для контрольованого вивільнення. Сполуки вивільняються з потрібною швидкістю для підтримування постійної фармакологічної активності протягом бажаного періоду часу. Такі форми дозування забезпечують подачу ліків до тіла протягом попередньо визначеного періоду часу та таким чином підтримування рівнів ліків у терапевтичних межах протягом довших періодів часу, ніж звичайні неконтрольовані композиції. Сполуки можуть також бути сформованими у композиції для контрольованого вивільнення, у котрих вивільнення активної сполуки є запланованим. Наприклад, 22 вивільнення сполуки можуть бути обмеженим специфічним регіоном травної систем через чутливість композиції до рН. Такі композиції добре відомі спеціалістам. Залежно від розладу та пацієнта, якого лікують, та шляху призначення, композиції можуть бути призначеними у різноманітних дозах. Дозування повинне також залежати від відношення потужності до поглинальної здатності та частоти і шляху призначення. Такі дози можна призначати раз, двічі або три чи більше разів на добу. Сполуки заявленого винаходу можна призначати для суб'єктів у дозах у межах від 0,01мг до 500мг/кг маси тіла на добу, хоча варіації повинні обов'язково траплятися залежно від маси, статі та стану суб'єкта, якого лікують, стану хвороби, який лікують та конкретного вибраного шляху призначення. Однак, рівні дозування, що є у межах від 0,1мг до 10мг/кг маси тіла на добу, одиничною або розділеними дозами найбільш бажано застосовувати для лікування хвороб людей. Альтернативно, рівні дозування є такими, щоб отримувати концентрацію сполуки у сироватці між 0,1нМ та 10мкМ. Будь-які хімічні формул або назви, дані тут, охоплюють усі стерео та оптичні ізомери та рацемати і їх суміші у будь-якому співвідношенні. Різні ізомери можна отримувати стандартними способами, добре відомими спеціалістам, наприклад, хроматографією або фракційною кристалізацією. Наприклад, цис/транс суміші можуть бути відокремленими на індивідуальні стереоізомери стереоселективним синтезом. Енантіомери або діастереомери можна виділяти відокремленням з їх суміші, наприклад, фракційною кристалізацією, розділенням або ВЕРХ. Альтернативно відокремлення можна досягти дериватизацією хіральним реагентом. Стереоізомери можуть бути створеними стереоселективним синтезом зі стереохімічно чистих вихідних матеріалів в умовах, котрі повинні не викликати втрат стереохімічної чистоти. Усі стереоізомери є уведеними у рамки винаходу. Сполуки заявленого винаходу можна виділяти будь-якого рівня чистоти стандартними способами та їх очистки можна досягти звичайними засобами, відомими спеціалістам, як-то перегонка, перекристалізація та хроматографія. Винахід далі ілюстровано у нижченаведених прикладах, котрі не є призначеними для обмеження рамок винаходу. Приклад 1 4-[3-ФЛУОР-5-(МЕТИЛСУЛЬФОНІЛ)ФЕНІЛ]-1ПРОПІЛПІПЕРИДИН До розчину 4-[3-флуор-5(метилсульфоніл)феніл]піперидину (0,5г, 1,94ммоль) в ацетонітрилі (5мл) було додано калій карбонат (0,53г, 3,83ммоль) та 1-йодпропан (0,189мл, 1,94ммоль) та суміш було нагріто мікрохвильовим опроміненням протягом 20 хвилин при 150 °С. Суміш було охолоджено до зовнішньої температури та було додано воду (50 мл). Водний залишок було екстраговано етилацетатом (3×50мл) та комбіновані органічні фази було висушено, концентровано та очищено флешколонковою хроматографією (етилацетат/метанол, 23 1:1), отримуючи заголовну сполуку (0,27 г, 46%). Амін було перетворено у гідрохлорид та перекристалізовано з суміші етанол/діетиловий етер: Тчк. пл 187-189°С. МС m/z (відносна інтенсивність, 70eV) 299 (М+, 3), 271 (15), 270 (р), 147 (5) 133 (5). Приклад 2: 1-ЕТИЛ-4-[3-ФЛУОР-5(МЕТИЛСУЛЬФОНІЛ)ФЕНІЛ]ПІПЕРИДИН Отримання згідно з прикладом 1: 4-[3-флуор-5(метилсульфоніл)феніл]піперидин (0,4г, 1,55ммоль), ацетонітрил (5мл), калій карбонат (0,42г, 3,0ммоль), 1-йодетан (0,147мл, 1,55ммоль). Вихід: 0,28г (63%). Амін було перетворено у гідрохлорид та перекристалізовано з суміші етанол/діетиловий етер: Тчк. пл 176-178°С. МС m/z (відносна інтенсивність, 70eV) 285 (М+, 15), 284 (16), 271 (16), 270 (bр), 84 (15). Синтез проміжних сполук, застосованих у вищенаведених прикладах, є описаним в отриманнях нижче. Отримання 1: 1-БРОМ-3-ФЛУОР-5-(МЕТИЛТІО)БЕНЗОЛ До розчину 1-бром-3,5-дифлуорбензолу (5,0г, 25,9ммоль) у диметилформаміді (40мл) було додано натрій тіометилат (1,81г, 25,9ммоль), та суміш було нагріто до 150°С протягом 10 хвилин. Реакційну суміш було доведено до зовнішньої температури, погашено насиченим водним розчином хлориду амонію (100мл) та екстраговано етилацетатом (3×100мл). Комбіновані органічні фази було висушено та концентровано у вакуумі для отримання чистої заголовної сполуки (3,84г). МС m/z (відносна інтенсивність, 70eV) 222 (М+, 100), 220 (М+, 100), 189 (49), 187 (50), 126 (75). Отримання 2: ТРЕТ-бутил 4-[3-ФЛУОР-5(МЕТИЛТІО)ФЕНІЛ]-4-ПДРОКСИПІПЕРИДИН-1КАРБОКСИЛАТ До розчину 1-бром-3-флуор-5(метилтіо)бензолу (3,7г, 16,7ммоль) у сухому діетиловому етері (100мл), в атмосфері азоту, при 78°С було додано краплями н-бутил літий (2,5М у гексані, 6,7мл, 16,7ммоль). Суміш перемішували протягом 30 хвилин при -78°С та тоді доведено до -20°С протягом 2 хвилин та охолоджено знов до 78°С. До утвореної суміші при -78°С, було додано краплями розчин 4-Вос-1-піперидону (3,3г, 16,7ммоль) у сухому діетиловому етері (50мл). Суміш перемішували при -78°С протягом 10 хвилин та тоді її було доведено до зовнішньої температури. Реакційну суміш було погашено насиченим водним розчином хлориду амонію (100 мл) та екстраговано етилацетатом (3×100мл). Комбіновані органічні фази було висушено, концентровано та очищено флеш-колонковою хроматографією (ізооктан/етилацетат 2:1), отримуючи заголовну сполуку (3,76г). МС m/z (відносна інтенсивність, 70eV) 341 (М+, 7), 285 (11), 241 (11), 196 (4), 57 (bр). Отримання 3: ТРЕТ-БУТИЛ-4-[3-ФЛУОР-5(МЕТИЛСУЛЬФОНІЛ)ФЕНІЛ]-4ГІДРОКСИПІПЕРИДИН-1-КАРБОКСИЛАТ До розчину трет-бутил 4-[3-флуор-5(метилтіо)феніл]-4-гідроксипіперидин-1-карбоксилату (3,66г, 10,6ммоль) у карбонтетрахлориді 93380 24 (13мл), ацетонітрилі (13мл) та воді (26мл), було додано натрій перйодат (6,8г, 31,8ммоль) та рутеній трихлорид (3мг, 0,05моль)%) та суміш перемішували протягом 20 хвилин при зовнішній температурі. Воду було додано та продукт було екстраговано етилацетатом (3×100мл). Комбіновані органічні фази було висушено та концентровано у вакуумі для отримання чистої заголовної сполуки (3,3г). МС m/z (відносна інтенсивність, 70eV) 373 (М+, 0), 273 (25), 255(74), 133(28), 56 (bр). Отримання 4: 4-[3-ФЛУОР-5-(МЕТИЛСУЛЬФОНІЛ)ФЕНІЛ]1,2,3,6-ТЕТРАГІДРОПІРИДИН Суміш трет-бутил 4-[3-флуор-5(метилсульфоніл)феніл]-4-гідроксипіперидин-1карбоксилату (3,3г, 8,8ммоль) та поліфосфатної кислоти (20мл) було нагріто при 120°С протягом 3 годин. Суміш було вилито на лід та було підлужено 5 М натрій гідроксидом. Суміш було екстраговано етилацетатом (3×100мл) та комбіновані органічні фази було висушено магній сульфатом, випарено та очищено флеш-колонковою хроматографією (метанол/етилацетат 1:1), отримуючи заголовну сполуку (2,02г). МС m/z (відносна інтенсивність, 70eV) 255 (М+, bр), 254 (50), 251 (87), 172 (87), 146 (53). Отримання 5: 4-[3-ФЛУОР-5(МЕТИЛСУЛЬФОНІЛ)ФЕНІЛ]ПІПЕРИДИН Суміш 4-[3-флуор-5-(метилсульфоніл)феніл]1,2,3,6-тетрагідропіридину (2,02г, 7,9ммоль), паладію на вугіллі (0,56г) та мурашиної кислоти (1,9мл) в ізопропіловому спирті (60мл) було гідрогеновано при 50фунт/кв.дюйм протягом 24 годин під воднем. Реакційну суміш було профільтровано через шар броунмілериту та фільтрат було концентровано та випарено до сухого стану, отримуючи 1,66 г сирого продукт. МС m/z (відносна інтенсивність, 70eV) 257 (М+, bр), 256 (80), 133 (21), 69 (25) 56 (99). Наступні тести були застосованими для оцінки сполук згідно з винаходом. In vivo тестування: Поведінка Поведінкову активність було виміряно, застосовуючи вісім моніторів активності Digiscan (RXYZM (16) TAO, Omnitech Electronics, Columbus, OH, USA), приєднай до аналізатору Omnitech Digiscan та комп'ютеру Apple Macintosh, оснащеному цифровою інтерфейсною платою (NB DIO-24, National Instruments, USA). Кожний монітор складався з квадратної металічної рамки (W×L 40×40см), оснащеної фотопроменевими сенсорами. Протягом вимірів поведінкової активності, щура поміщали у прозору акрилову клітку (Ш×Д×В, 40×40×30см), котру у свою чергу було розміщено у моніторіактивності. Кожний монітор активності було оснащено трьома рядами інфрачервоних фотопроменевих сенсорів, кожний ряд складався з 16 сенсорів. Два ряди були розміщеними вздовж фронту та збоку дверцят клітки, під кутом 90°, а третій ряд було розміщено на 10см вище дверцят для виміру вертикальної активності. Фотопроменеві сенсори були розділеними 2,5см нарізно. Кожний монітор активності було опоряджено іденти 25 чно послаблюючою звук та світло камерою, що мала слабке власне світло та вентилятор. Комп'ютерне програмне забезпечення створене, застосовуючи орієнтоване на об'єкт програмування (LabVIEW®, National instruments, Austin, TX, USA). Поведінкові дані від кожного монітора активності, що представляли положення тварини (горизонтальні центр ваги, а вертикальні активність) у кожний момент часу реєстрували з частотою 25Гц та збирали, застосовуючи власну програму LABView™. Дані від кожного сеансу спостереження зберігали та аналізували відносно пройденої відстані. Кожний сеанс спостереження поведінки продовжувався 60 хвилин, починаючи приблизно через 4 хвилин після ін'єкції тест-сполуки. Подібні способи реєстрування поведінки були застосовуваними для нелікованих та попередньо лікованих щурів. Щурам, попередньо лікованим dамфетаміном були дані дози 1,5мг/кг інтраперитонеально за 10 хвилин перед сеансом спостереження у моніторі активності. Щурам, попередньо лікованим МК-801 були дані дози 0,7мг/кг інтраперитонеально за 90 хвилин перед сеансом спостереження у моніторі активності. Результати є надані як число імпульсів/60 хвилин, або число імпульсів/30 хвилин, у одиницях довільної довжини. Статистичні порівняння були здійсненими, застосовуючи t-тестування Стьюдента відносно контрольної групи. У попередньо лікованих МК-801 або амфетаміном тварин статистичні порівняння були створеними відносно МК801 або d-амфетамінових контролів, відповідно. Значення ЕД50 стосовно зменшення індукованої амфетаміном гіпер-локомоції розраховують за допомогою підгонки кривих. Для більшості сполуки, оцінка є на основі 16 попередньо лікованих амфетаміном тварин у межах доз 0, 11, 33 та 100мкмоль/кг підшкірно в одному одиничному експерименті, з додатковими дозами в окремих експериментах. Розрахунки є на основі відстані протягом останніх 45 хвилин одної години виміру. Відстані нормалізують стосовно амфетамінового контролю та підганяють методом мінімізації найменших квадратів до функції "Кінець-(КінецьКонтроль)/(1+(доз/ЕД50)Нахил)". Чотири параметри підганяють з обмеженнями: ЕД50>0, 0,5
ДивитисяДодаткова інформація
Назва патенту англійською3,5-disubstituted phenyl-piperidines as modulators of dopamine neurotransmission
Автори англійськоюSonesson Clas
Назва патенту російською3,5-дизамещенные фенилпиперидины kak модуляторы нейротрансмиссии допамина
Автори російськоюСонессон Клас
МПК / Мітки
МПК: A61P 25/00, A61K 31/445, C07D 211/24
Мітки: модулятори, фенілпіперидини, допаміну, нейротрансмісії, 3,5-дизаміщені
Код посилання
<a href="https://ua.patents.su/15-93380-35-dizamishheni-fenilpiperidini-yak-modulyatori-nejjrotransmisi-dopaminu.html" target="_blank" rel="follow" title="База патентів України">3,5-дизаміщені фенілпіперидини як модулятори нейротрансмісії допаміну</a>
Попередній патент: Одношарова картонна упаковка для харчового продукту
Наступний патент: Процес та магнітний реагент для збагачення мінерального субстрату
Випадковий патент: Фармацевтична композиція, що містить гіалуронову кислоту та гліцерритинову кислоту, та її застосування












