Спосіб одержання золмітриптану
Номер патенту: 100236
Опубліковано: 10.12.2012
Автори: Затопкова Моніка, Вослар Міхал, Рідван Людек, Пекарек Томаш
Формула / Реферат
1. Спосіб одержання (S)-4-[{3-[2-(диметиламіно)етил]-1Н-індол-5-іл}метил]-2-оксазолідинону (золмітриптану) формули III
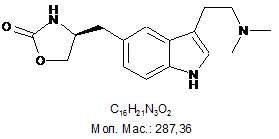 , (III)
, (III)
за наступною схемою,
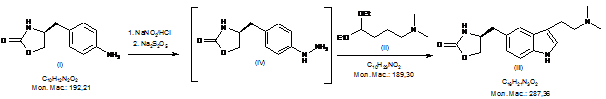 ,
,
який відрізняється тим, що відновлення солі діазонію до (S)-4-(4-гідразинобензил)-1,3-оксазолідин-2-ону формули IV здійснюють шляхом дії дисульфіту лужного металу, переважно дисульфіту натрію.
2. Спосіб за п. 1, який відрізняється тим, що продукт формули III спочатку виділяють у формі толуольного сольвату, який далі перетворюють на несольватовану форму.
3. Спосіб за п. 2, який відрізняється тим, що після завершення реакції до реакційної суміші додають толуол та основу з групи, яку складають карбонати або гідроксиди лужного металу, наприклад NaOH або К2СО3, або їх водний розчин.
4. Спосіб за п. 2, який відрізняється тим, що толуольний сольват перетворюють на несольватовану речовину шляхом сушіння при температурі 60-100 °C.
5. Спосіб за п. 2, який додатково включає десольватування та очищення толуольного сольвату золмітриптану з утворенням основи золмітриптану, який відрізняється тим, що толуольний сольват розчиняють у розбавленій кислоті, наприклад НСl, верхню незмішувану фазу толуолу відокремлюють від суміші, та потім виділяють золмітриптан з кислого водного розчину, який залишився, шляхом додавання основи з групи, яку складають карбонати або гідроксиди лужного металу, наприклад NaOH або К2СО3, або їх розчини, наприклад водні або спиртові розчини.
Текст
Реферат: При одержанні золмітриптану формули III відновлення солі діазонію до (S)-4-(4гідразинобензил)-1,3-оксазолідин-2-ону формули IV здійснюють у більш концентрованій суміші та шляхом дії дисульфіту лужного металу, переважно дисульфіту натрію. Толуольний сольват золмітриптану відрізняється вмістом толуолу 9-14 ваг. % у відповідності з результатом газової хроматографії, а також максимумом відповідної втрати маси при температурі приблизно 111°С у відповідності з результатом гравіметричного аналізу. Толуольний сольват золмітриптану показує інтенсивні смуги спектра Рамана при хвильових -1 числах 1443 та 1354 см , характерних для кристалічної решітки золмітриптану з вбудованим -1 толуолом, та додаткові виділені смуги при хвильових числах 1004 та 786 см , характерні для толуолу. H N O O (I) C10H12N2O2 Мол. Мас.: 192,21 NH2 1. NaNO2/HCl 2. Na2S2O5 H N O OB O (IV) N NH2 H BO H N O N (II) C10H23NO2 Мол. Мас.:189,30 N O (III) C12H21N3O2 Мол. Мас.: 287,36 N H UA 100236 C2 (12) UA 100236 C2 UA 100236 C2 5 10 15 20 25 30 35 40 45 50 Технічна галузь Винахід стосується способу виробництва (5)-4-[{3-[2-(диметиламіно)етил]-1Н-індол-5іл}метил]-2-оксазолідинону (золмітриптану), який належить до групи триптанів, які застосовують для лікування мігреней. Передумови винаходу Синтез золмітриптану складається з трьох загальновідомих реакцій (WO97/06162): діазотування (S)-4-(4-амінобензил)-1,3-оксазолідин-2-ону формули І нітритом у середовищі розбавленої хлорводневої кислоти, наступне відновлення одержаної солі діазонію до гідрохлориду (S)-4-(4-гідразинобензил)-1,3-оксазолідин-2-ону формули IV та, врешті-решт, його конденсування з 4,4-діетокси-N,N-диметилбутиламіном формули II, що у кислому середовищі, за Фішером, дозволяє одержати скелет індолу - у даному випадку золмітриптану формули III способом, аналогічним бензидиновому перегрупуванню. Весь синтез відбувається у водному середовищі та не потребує виділення проміжних продуктів. Як відновлювальний реагент на стадії відновлення синтезу застосовують хлорид олова або сульфіт лужного металу, наприклад, Na2SO3 (WO97/06162). Однак, застосування хлориду олова призводить до проблем з очищенням продукту та стічними водами, які містять небажані для навколишнього середовища солі олова, та тому таке застосування є непридатним в промислових масштабах. З іншого боку, Na2SO3 є порівняно слаборозчинним, що призводить або до необхідності сильнішого розбавлення відновлювальної суміші, або до системи гетерогенних реакцій (суспензії). Гетерогенні реакції можуть потім призвести до проблем з перемішуванням, зокрема, при великих об'ємах, в той час як розбавлення реакційної суміші вимагає значного збільшення часу протікання реакції. Друга стадія відновлення, яку здійснюють у кислому середовищі при 60 °C, у цьому гомогенному розбавленому розчині зазвичай триває до 18 годин (WO 97/06162), що, окрім енергії та затрат на персонал, також збільшує небажане теплове навантаження проміжного продукту та знижує вихід синтезу. Неочищений продукт зазвичай відновлюють з реакційної суміші після його обробки лугом (NaOH/вода) шляхом повторної екстракції органічним розчинником, зазвичай, етилацетатом (WO 97/06162). Після концентрування екстрактів до фракцій з початковим об'ємом, одержують кристалічний неочищений золмітриптан у формі сольвату з етилацетатом, який очищують шляхом перекристалізації з суміші етанол-етилацетату та в подальшому десольватують шляхом перемішування у водному ацетоні. Продукт - основу золмітриптану - врешті решт, видаляють шляхом фільтрування та промивають етилацетатом. Однак, з урахуванням порівняно низької розчинності золмітриптану в етилацетаті, вищеописаний екстракційний спосіб виділення потребує значних об'ємів екстракційного агенту (приблизно 25-кратний від об'єму кінцевого продукту) та його подальшого випарювання. Не кажучи нічого про енергетичні та часові потреби такого способу, під час концентрування у великих об'ємах продукт також піддають значному тепловому навантаженню, яке, з урахуванням підвищеної температури та характеру розчинника, навіть посилюється внаслідок взаємної реакційної здатності продукту (основного аміну) з розчинником (естером), а також гідролізу продукту та розчинника, викликаного водним лужним середовищем в процесі екстракцій. З цієї причини, проводились пошуки умов, які б змогли виключити або мінімізувати зазначені вище негативні аспекти до сих пір відомих способів синтезу золмітриптану. Розкриття винаходу Винахід полягає в покращеному способі виробництва (S)-4-[{3-[2-(диметиламіно)етил]-1Ніндол-5-іл}метил]-2-оксазолідинону (золмітриптану), який базується, з одного боку, на оптимізації умов реакції на стадії відновлення, коли сіль, наприклад, хлорид, (S)-4-(4бензилдіазоній)-1,3-оксазолідин-2-ону відновлюють у водному розчині до (S)-4-(4-гідразинобензил)-1,3-оксазолідин-2-ону шляхом дії дисульфіту лужного металу, та, з іншого боку, на новому способі виділення кінцевого продукту (золмітриптану формули III), який полягає у виділенні неочищеного толуольного сольвату золмітриптану як проміжного продукту, його очищенні та десольватуванні. 1 UA 100236 C2 5 10 15 20 25 30 35 40 45 50 55 60 Інший аспект винаходу включає одержання до сих пір не описаного сольвату золмітриптану з толуолом, який переважно можна застосувати для виділення неочищеного золмітриптану з реакційної суміші, та його наступне очищення. Опис винаходу Експериментально було винайдено, що дисульфіт лужного металу, найбільш переважно Na2S2O5, є придатним відновлювальним агентом для відновлення солі діазонію до (S)-4-(4гідразинобензил)-1,3-оксазолідин-2-ону, оскільки він є значно більш розчинним у воді та у той же час дешевшим, ніж Na2SO3. У той же час придатним є регулювання рН розчину відновлювального агента меншою кількістю гідроксиду лужного металу (наприклад, NaOH) - ¼ ½ застосованого Na2S2O5, виходячи з молярних співвідношень. Кількість води, необхідна для утворення стійкого гомогенного розчину при температурах близько 0 °C є лише 2,5-3-кратною по відношенню до застосованого Na2S2O5, та час, необхідний для кислотної стадії реакції при 60 °C та рН ~0 (НСІ) становить лише 5-6 годин, тобто лише третину часу, необхідного при стандартному більш високому розведенні. Крім того, склад зразків, одержаних із суміші під час реакції, яку регулюють за допомогою ВЕРХ та РХ-МС, показує, що при застосуванні дисульфіту механізм реакції відновлення відрізняється від очікуваного у випадку відновлення сульфітом. Перед кінцевим синтезом Фішера реакційну суміш розбавляють водою (приблизно половина об'єму відносно реакційної суміші), додають 4,4-діетокси-N,N-диметилбутиламін формули II та суміш кип'ятять зі зворотнім холодильником при рН = 0,6-1 та температурі приблизно 98 °C протягом 2,5 годин. Це означає, що всю послідовність реакцій можна здійснити при трьохзмінній роботі впродовж одного дня. Інший аспект винаходу включає повністю новий спосіб виділення золмітриптану у формі до сих пір неописаного толуольного сольвату. Він базується на спостереженні, що з водної реакційної суміші після реакції Фішера, до якої додають невелику кількість толуолу та емульгують, під час повільної обробки лугом з водним розчином карбонату або гідроксиду лужного металу, наприклад, NaOH або K2СО3, кристалізується твердий золмітриптан. Кристалічний неочищений продукт, одержаний в такий спосіб, містить 9-14 ваг. % толуолу, визначеного у відповідності з газовою хроматографією. Цей результат відповідає запису, одержаному за допомогою термогравіметричного аналізу (фіг. 1), який фіксує швидку втрату приблизно 10 % маси при температурі близько 111 °C, яка відповідає точці кипіння толуолу при нормальному тиску. Встановлений вміст толуолу, таким чином, відповідає вірогідному молярному вмісту толуолу у кристалічній решітці 1:2 (13,8 ваг. %). Нова кристалічна форма золмітриптану з толуолом, включеним в його кристалічну решітку, чітко характеризується інтенсивними смугами спектру Рамана при хвильових числах 1354 та -1 -1 1443 см разом з характеристичними смугами толуолу (при 786 та 1014 см ) у спектрі Рамана сольвату (фіг. 2). Для ясності, спектр Рамана неочищеного сольвату золмітриптану (чорна пунктирна лінія) порівнюється тут зі спектрами чистого золмітриптану (чорна суцільна лінія) та вільного толуолу (суцільна сіра лінія). Неочищений толуольний сольват золмітриптану може бути очищений шляхом перекристалізації зі звичайних розчинників, наприклад, спиртів, ацетону, етилацетату та подібних, або їх сумішей, або сумішей з толуолом. Перекристалізацію з розчинників, які не містять толуол, можна також використати для десольватування продукту. Десольватування також можна здійснити при застосуванні тривалого сушіння за умов зниженого тиску та температурі 60-100 °C. Десольватування та, у той же час, повторне очищення неочищеного продукту можна успішно здійснити шляхом розчинення сольвату золмітриптану у розбавленому водному розчині кислоти, наприклад, НСІ, з наступним відокремленням незмішуваної органічної фази (толуолу). Водний розчин солі золмітриптану, що залишився, потім перетворюють на вільну основу шляхом поступового додавання карбонату або гідроксиду лужного металу, наприклад, K2СО3 або NaOH, тощо, у твердому стані або у розчині. Нерозчинну у воді основу потім відфільтровують та промивають водним спиртом та водою. Вільну основу золмітриптану (форма А) можна очистити шляхом перекристалізації із суміші етанолу та води. Одержаний білий або майже білий продукт (ВЕРХ -100,0 %) відповідає, згідно з Рентгенографічним аналізом, формі А, такій же, яку можна одержати способом у відповідності із заявкою на патент № WO 97/06162. Переваги вищеописаного способу виділення та очищення включають швидкість, низьку вартість вхідних матеріалів, високий вихід та якість одержаного продукту, а також, головним чином, мінімальний вплив на довкілля, оскільки, за винятком малих об'ємів толуолу та етанолу, у всьому способі не застосовано жодних органічних розчинників. Спосіб виділення неочищеного золмітриптану з реакційної суміші у відповідності з винаходом надає можливість повністю 2 UA 100236 C2 5 10 15 20 25 30 35 40 45 50 55 усунути всі зазначені вище проблеми, які у промислових масштабах супроводжують спосіб виділення, що базується на виділенні етилацетатом, який застосовувався до сих пір. Короткий опис креслень Фігура 1 показує результат термогравіметричного аналізу (ТГА) неочищеного толуольного сольвату золмітриптану, одержаного у відповідності з Прикладом 4 -залежність втрати ваги зразка у % від температури, яка показує максимальну втрату при температурі близько 111 °C (суцільна лінія) та відповідну першу похідну (пунктирна лінія). Фігура 2 показує спектр Рамана неочищеного толуольного сольвату золмітриптану, одержаного у відповідності з Прикладом 4 (пунктирна чорна лінія), у порівнянні зі спектром чистого несольватованого золмітриптану (суцільна чорна лінія) та вільного толуолу (суцільна сіра лінія). Приклади Приклад 1 - Діазотування (S)-4-(4-амінобензил)-1,3-оксазолідин-2-ону формули (І) 2,4 літра концентрованої НСІ додають до 7,0 літрів води у реакторі з охолоджувальним контуром. У такій розбавленій НСІ перемішують 1,75 кг (S)-4-(4-амінобензил)-1,3-оксазолідине2-ону формули (І) та суміш охолоджують до 0 °C при перемішуванні. Під час охолодження водний розчин NaNO2 (0,64 кг NaNO2 / 1,4 літрів води) готують до діазотування. При температурі приблизно 0 °C до розчину вихідної речовини (І) повільно додають розчин NaNO2 / Н2О при інтенсивному перемішуванні та охолодженні. Після додавання всього нітриту суміш додатково перемішують при приблизно 0 °C протягом приблизно 30 хв. Приклад 2 - Відновлення солі діазонію Зважені 0,28 кг NaOH розчиняють у 7,0 літрах води та додають 2,66 кг дисульфіту натрію при перемішуванні. Після розчинення суміш охолоджують до приблизно 2 °C. Розчин солі діазонію повільно додають до охолодженого розчину дисульфіту при інтенсивному перемішуванні та температурі 2-5 °C. Потім суміш перемішують при приблизно 5 °C впродовж додаткових 30 хвилин. Потім її нагрівають до приблизно 25 °C та перемішують при цій температурі протягом 45 хвилин. Далі її нагрівають зі зворотнім холодильником до приблизно 60 °C при перемішуванні. Після нагрівання до реакційної суміші додають 900 мл концентрованої НСІ та суміш перемішують зі зворотнім холодильником ще протягом 5 годин. Потім суміш розбавляють 14 літрами води. Приклад 3 - Індольна реакція Фішера Розбавлену реакційну суміш нагрівають до приблизно 90 °C. Зважують 1,75 кг 4,4-діетоксиN,N-диметилбутиламіну формули II. Зважений ацеталь (II) додають до реакційної суміші, яку потім подають на помірне нагрівання зі зворотнім холодильником (при приблизно 98 °C), та, перемішуючи, її залишають реагувати протягом приблизно 2,5 годин. Через 2,5 години від початку кип'ятіння, нагрівання суміші припиняють та реакційну суміш охолоджують до кімнатної температури. Приклад 4 - Виділення неочищеного толуольного сольвату ЗОЛМІТРИПТАНУ При кімнатній температурі та перемішуванні, охолоджену суміш нейтралізують приблизно 20 % водним розчином NaOH. Додають приблизно 4 літри толуолу та суміш перемішують для одержання емульсії. Потім повільно додають водний розчин NaOH при перемішуванні до досягнення рН приблизно 9,5. Через приблизно 30 хвилин перемішування твердий продукт відфільтровують та промивають водою. Його сушать при температурі приблизно 30 °C до досягнення постійної ваги (приблизно 10 годин). Приклад 5 - Десольватування та очищення толуольного сольвату ЗОЛМІТРИПТАНУ шляхом перетворення на сіль Перемішаний при кімнатній температурі толуольний сольват золмітриптану розчиняють у 12 літрах 2 % водного розчину НСІ. Після розчинення твердої фази суміш залишають для відокремлення на приблизно 15 хвилин - толуол утворює верхній шар. Нижній водний розчин солі продукту відокремлюють та перемішують з приблизно 2,5 літрами етанолу. Суміш додатково перемішують та при температурі приблизно 25 °C додають загалом 1,0 кг карбонату калію декількома приблизно рівними порціями. Через 30 хв після останнього додавання, суспензію продукту охолоджують до приблизно 15 °C при перемішуванні, та приблизно через 1 годину перемішування основу відфільтровують. Відфільтрований осад промивають приблизно 2 літрами очищеної води та залишають сушитись при нормальному тиску та температурі приблизно 45 °C до досягнення постійної ваги. 60 3 UA 100236 C2 ФОРМУЛА ВИНАХОДУ 1. Спосіб одержання (S)-4-[{3-[2-(диметиламіно)етил]-1Н-індол-5-іл}метил]-2-оксазолідинону (золмітриптану) формули III H N O N O N H C16H21N3O2 Мол. Мас.: 287,36 5 , (III) за наступною схемою, H N 1. NaNO2/HCl 2. Na2S2O5 O O NH2 (I) OEt H N O O (IV) N H C10H12N2O2 Мол. Мас.: 192,21 10 15 20 25 NH2 (II) C10H23NO2 Мол. Мас.: 189,30 N H N N EtO O O (III) N H C16H21N3O2 Мол. Мас.: 287,36 , який відрізняється тим, що відновлення солі діазонію до (S)-4-(4-гідразинобензил)-1,3оксазолідин-2-ону формули IV здійснюють шляхом дії дисульфіту лужного металу, переважно дисульфіту натрію. 2. Спосіб за п. 1, який відрізняється тим, що продукт формули III спочатку виділяють у формі толуольного сольвату, який далі перетворюють на несольватовану форму. 3. Спосіб за п. 2, який відрізняється тим, що після завершення реакції до реакційної суміші додають толуол та основу з групи, яку складають карбонати або гідроксиди лужного металу, наприклад NaOH або K2СО3, або їх водний розчин. 4. Спосіб за п. 2, який відрізняється тим, що толуольний сольват перетворюють на несольватовану речовину шляхом сушіння при температурі 60-100 °C. 5. Спосіб за п. 2, який додатково включає десольватування та очищення толуольного сольвату золмітриптану з утворенням основи золмітриптану, який відрізняється тим, що толуольний сольват розчиняють у розбавленій кислоті, наприклад НСl, верхню незмішувану фазу толуолу відокремлюють від суміші, та потім виділяють золмітриптан з кислого водного розчину, який залишився, шляхом додавання основи з групи, яку складають карбонати або гідроксиди лужного металу, наприклад NaOH або K2СО3, або їх розчини, наприклад водні або спиртові розчини. 4 UA 100236 C2 Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for the preparation of zolmitriptan
Автори англійськоюVoslar, Michal, Zatopkova, Monika, Ridvan, Ludek, Pekarek, Tomas
Назва патенту російськоюСпособ получения золмитриптана
Автори російськоюВослар Михал, Затопкова Моника, Ридван Людек, Пекарек Томаш
МПК / Мітки
МПК: C07D 413/06
Мітки: спосіб, одержання, золмітриптану
Код посилання
<a href="https://ua.patents.su/7-100236-sposib-oderzhannya-zolmitriptanu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання золмітриптану</a>
Попередній патент: Спосіб і пристрій для з’єднання мобільних пристроїв зв’язку з безпровідними мережами в підземних спорудах
Наступний патент: Застосування композиції, що містить формотерол та беклометазон дипропіонат, для попередження та/або лікування загострення астми
Випадковий патент: Спосіб і установка термічної обробки сталевої рейки











