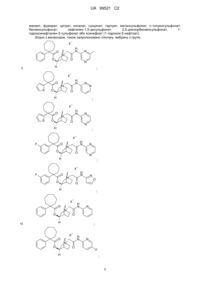
Хінуклідин-похідні як антагоністи мускаринових рецепторів м3
Номер патенту: 99521
Опубліковано: 27.08.2012
Автори: Мете Антоніо, Скідмор Елізабет Анн, Форд Ронан Лі, Булл Річард Джеймс, Метер Ендрю Найджел
Формула / Реферат
1. Сполука, вибрана з групи:
(R)-1-[(6-метилпіридин-3-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(6-метилпіразин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-[(6-трифлуорметилпіридазин-3-ілкарбамоїл)метил]-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-(бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-(піридазин-3-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-метилізоксазол-3-ілкарбамоїл)метил]-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-[(3-метилізоксазол-5-ілкарбамоїл)метил]-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(3-флуорфенілкарбамоїл)метил]-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-[(5-метилпіразин-2-ілкарбамоїл)метил]-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-(бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-(піразин-2-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-[1-(3-флуорфеніл)циклогептанкарбонілокси]-1-(піразин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-[1-(3-флуорфеніл)циклогептанкарбонілоксі]-1-(ізоксазол-3-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-флуорпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-метилпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридин-3-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2-метилпіридин-4-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-фенілкарбамоїлметил-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піримідин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2-флуорфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2,3-дифлуорфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[2-(2,3-дигідробензофуран-5-іл)етил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[2-(4-флуорфеноксі)етил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридазин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-флуорпіридин-3-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-[2-(піридин-3-ілоксі)етил]-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(6-метилпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(о-толілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(2-піразин-2-ілетил)-1-азонійбіцикло[2,2,2]октан X;
(S)-1-(3-феноксипропіл)-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-{[2-(3-флуорфеноксі)етилкарбамоїл]метил}-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(3,5-дифлуорфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[2-(4-метоксибензилоксі)етил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-(2-фенетилоксіетил)-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2,6-дифлуорфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(метилфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[3-(4-ціанофенокси)пропіл]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2,5-дифлуорфенілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[2-(4-ціанобензилоксі)етил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-[(6-трифлуорметилпіридин-2-ілкарбамоїл)метил]-1-азонійбіцикло[2,2,2]октан Х;
(R)-1-[(4-метилпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-хлорпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(п-толілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(м-толілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-(оксазол-2-ілкарбамоїлметил)-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(6-метилпіридазин-3-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піримідин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(5-ціанопіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(піримідин-5-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(3-флуорпіридин-2-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(3-флуорпіридин-4-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-{2-[(піразин-2-карбоніл)аміно]етил}-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-([1,2,4]тіадіазол-5-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-{3-[(піридин-2-карбоніл)аміно]пропіл}-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(2-метилпіримідин-4-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан X;
(R)-1-[(6-метилпіримідин-4-ілкарбамоїл)метил]-3-(1-фенілциклогептанкарбонілоксі)-1-азонійбіцикло[2,2,2]октан Х;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-{2-[(піридин-2-карбоніл)аміно]етил}-1-азонійбіцикло[2,2,2]октан X;
(R)-3-(1-фенілциклогептанкарбонілокси)-1-(3-піридин-4-ілпропіл)-1-азонійбіцикло[2,2,2]октан X;
де X - фармацевтично прийнятний аніон моно- або полівалентної кислоти.
2. Сполука за п. 1, вибрана з групи:
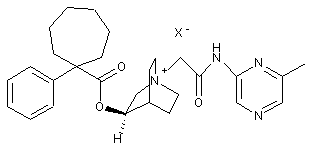 ;
;
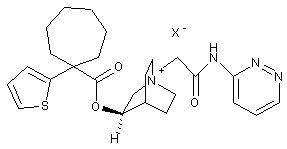 ;
;
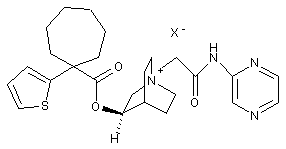 ;
;
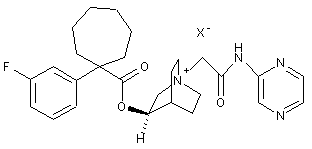 ;
;
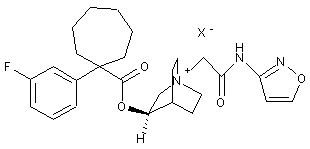 ;
;
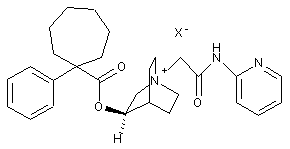 ;
;
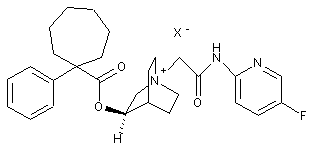 ;
;
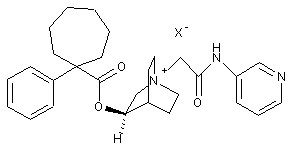 ;
;
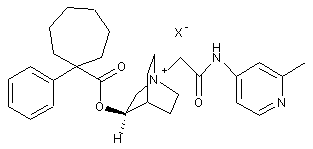 ,
,
де X - фармацевтично прийнятний аніон моно- або полівалентної кислоти.
3. Сполука за п. 1 або п. 2, якою є (R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан X, де X - фармацевтично прийнятний аніон моно- або полівалентної кислоти.
4. Сполука за будь-яким з пп. 1-3, якою є (R)-3-(1-фенілциклогептанкарбонілокси)-1-(піридин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октанбромід.
5. Фармацевтична композиція, що містить сполуку за пп. 1-4 в поєднанні з фармацевтично прийнятним ад’ювантом, розріджувачем або носієм.
6. Спосіб отримання фармацевтичної композиції за п. 5, за яким сполуку за пп. 1-4 змішують з фармацевтично прийнятним ад’ювантом, розріджувачем або носієм.
7. Сполука за пп. 1-4 для застосування у терапії.
8. Застосування сполуки за пп. 1-4 у виробництві медикаменту для застосування у лікуванні хронічної обструктивної хвороби легень.
9. Спосіб лікування хронічної обструктивної хвороби легень у теплокровної тварини, як-то людини, за яким ссавцю, що потребує такого лікування, вводять терапевтично ефективну кількість сполуки за пп. 1-4.
10. Фармацевтичний продукт, що містить, у комбінації, перший активний інгредієнт, який є сполукою за пп. 1-4, та принаймні один наступний активний інгредієнт, вибраний з нижченаведеного:
• інгібітор фосфодіестерази,
• b2 адреноміметик,
• модулятор функції рецептора хемокіну,
• інгібітор функції кінази,
• інгібітор протеази,
• агоніст рецептора стероїдного глюкокортикоїду, або
• агоніст рецептора нестероїдного глюкокортикоїду.
Текст
Реферат: Винахід стосується сполуки формули (І) R 1 R R 3 2 O R 4 O , (І) фармацевтичних композицій, що її містять, способу отримання фармацевтичних композицій та їх застосування у терапії. 1 R 2 R 3 R O O 4 R UA 99521 C2 (12) UA 99521 C2 UA 99521 C2 5 10 15 20 25 30 Заявлений винахід стосується циклоалкіл-заміщених алкіл-естерів поліциклічних аміноспиртів, способу їх отримання, фармацевтичних композицій, що їх містять, способу отримання фармацевтичних композицій, їх застосування у терапії та інтермедіатів, застосовуваних у їх отриманні. Мускаринові рецептори є родиною сполучених з G-білком рецепторів (GРСR), що має 5 членів родини М1, М2, М3, М4 та М5. З 5 мускаринових підтипів три (М1, М2 та М3), як відомо, викликають фізіологічну дію на пухлину легень людини. Парасимпатичні нерви є головним шляхом метаболізму для рефлексу бронхоконстрикції у дихальних шляхах людини та опосередковують тонус дихальних шляхів вивільненням ацетилхоліну на мускаринові рецептори. Тонус дихальних шляхів є посиленим у пацієнтів з респіраторними розладами, як-то астма та хронічна обструктивна хвороба легень (СОРD), тому антагоністи мускаринових рецепторів розроблені для застосування у лікуванні хвороб дихальних шляхів. Антагоністи мускаринових рецепторів, часто названі антіхолінергіками у клінічній практиці, набули дуже поширеного визнання, як терапія першої лінії для індивідуалів з СОРD, та їх застосування широко оглянуте у літературі (наприклад, Lее еt аl., Сurrеnt Оріnіоn іn Рhаrmасоlоgу 2001, 1, 223-229). Для лікування респіраторних розладів, антагоністи мускаринових рецепторів звичайно застосовують інгаляцією. Однак, при застосуванні інгаляцією значна частина антагоністу мускаринових рецепторів часто поглинається у великий круг кровообігу, утворюючи побічну дію, як-то сухість у роті. Крім того, більшість мускаринових антагоністів мають відносно коротку тривалість дії, що потребує їх застосування кілька разів на добу. Такий режим дозування є не тільки незручним до пацієнта, але також створює значний ризик неадекватного лікування внаслідок відсутності комплаєнса пацієнта, асоційованого із режимом частого повторення дозування. Тому залишається потреба у нових сполуках, що є здатними блокувати мускаринові рецептори. Зокрема, існує потреба у нових мускаринових антагоністах, що мають високу дієвість та зменшену системну побічну дію, при застосуванні інгаляцією. Більш того, існує потреба нових мускаринових антагоністах, що виявляють довгу тривалість дії при дозуванні інгаляцією, та котрі є придатними для дозування раз або двічі на добу. WО 98/04517 описує арилциклопропан-, арилциклобутан-, арилциклопентан- та арилциклогексан-карбокси-естери, що мають антимускаринову активність на гладенькі м'язи сечового міхура. Наша співрозглядувана заявка РСТ/GВ2007/004350 стосується сполуки формули (І): 1 R 2 R 3 R O 4 (І) R O 35 40 45 де 1 2 R та R разом з атомом карбону, до котрого вони є безпосередньо приєднаними, утворюють 7-членне аліфатичне карбоциклічне кільце, котре може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С1-6 алкокси, NН2, NН(С1-6 алкіл), N(С1-6 алкіл)2 та С1-6 алкіл, де С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген та гідроксил; 3 R – феніл або 5-6-членне гетероарильне кільце, кожне з котрих може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, нітро, 9 10 11 12 13 14 15 16 17 18 19 20 SН, S(О)0-2R , NR R , S(О)2NR R , С(О)NR R , С(О)2R , NR S(О)2R , NR С(О)R , 21 22 23 24 25 26 NR С(О)2R , NR С(О)NR R , ОR та С1-6 алкіл, де С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С1-6 алкокси, NН2, NН(С1-6 алкіл) та N(С1-6 алкіл)2; 4 R – група формули (ІІ), (ІІІа) або (ІІІb); 1 UA 99521 C2 (CH2)b Y 5 (R6)w 15 20 25 30 35 40 45 50 (CH2)a N+ R X 5 XN+ 5 R (ІІ), (ІІІа), (ІІІb), де Y – -СН2-, -СН2СН2- або -СН2СН2СН2- та заміщення на кільці у групі (ІІ) може бути у 3 або 4 позиції; а = 1 або 2; b=1 або 2; Z – -СН2-; 5 R – група формули (ІV) (Q)y 10 z X+ 5 N R 7 R (ІV), де w=0 або 1; 6 R – С1-4 алкілен, необов'язково заміщений одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С 1-6 алкокси, NН2, NН(С1-6 алкіл) та N(С1-6 алкіл)2; коли w=0, у = 0; коли w=1, у = 0 або 1; 8 8 8 8 8 Q – О, S(О)0-2, NR , -СОNR -, -SО2NR -, -NR СО-, -NR SО2-, -ОС(О)-, -С(О)О-, -НС=СН- або етинілен; 7 1 R – циклічна група Сус або С1-4 алкіл, де С1-4 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С 1-4 алкокси, 2 2 7 NН2, NН(С1-4 алкіл), N(С1-4 алкіл)2, циклічна група Сус та -ОСус ; та R може додатково бути 8 8 8 гідрогеном, коли Q – О, NR , -СОNR -, -SО2NR -, -С(О)О-, -НС=СН- або етинілен; 1 2 Сус та Сус , кожний незалежно, – арил, гетероарил, 3-8-членне аліфатичне карбоциклічне кільце або 4-8-членне аліфатичне гетероциклічне кільце, кожне з котрих може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: 9 10 11 12 13 14 15 16 17 18 галоген, ціано, нітро, SН, S(О)0-2R , NR R , S(О)2NR R , С(О)NR R , С(О)2R , NR S(О)2R , 19 20 21 22 23 24 25 26 NR С(О)R , NR С(О)2R , NR С(О)NR R , ОR , феніл та С1-6 алкіл, де феніл або С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С1-6 алкокси, NН2, NН(С1-6 алкіл) та N(С1-6 алкіл)2; 8 R – гідроген або С1-6 алкіл; 9 18 R та R , кожний незалежно, – С1-6 алкіл, де С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С1-6 алкокси, NН2, NН(С1-6 алкіл) та N(С1-6 алкіл)2; та 10 11 12 13 14 15 16 17 19 20 21 22 23 24 25 26 R , R , R , R , R , R , R , R , R , R , R , R , R , R , R та R , кожний незалежно, – гідроген або С1-6 алкіл, де С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил, С 1-6 алкокси, NН2, NН(С1-6 алкіл) 10 11 12 13 14 15 24 25 та N(С1-6 алкіл)2; або будь-що з групи: R та R , R та R , R та R або R та R , разом з атомом нітрогену, до котрого вони є приєднаними, можуть утворювати 4-8-членне аліфатичне гетероциклічне кільце, котре може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідроксил та С 1-6 алкіл, де С1-6 алкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген та гідроксил; та Х – фармацевтично прийнятний аніон моно або полівалентної кислоти. Заявлений винахід стосується сполуки що є у рамках нашої співрозглядуваної заявки РСТ/GВ2007/004350, але не є конкретно розкритою. Таким чином, заявлений винахід стосується сполуки, що має четвертинний амоній, вибрану з групи: (R)-1-[(6-Метил-піридин-3-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-[(6-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-[(6-трифлуорметил-піридазин-3-ілкарбамоїл)метил]-1-азоній-біцикло[2,2,2]октан Х; 2 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 (R)-1-(Бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-(Піридазин-3-ілкарбамоїлметил)-3-(1-тіофен-2-іл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(5-Метил-ізоксазол-3-ілкарбамоїл)-метил]-3-(1-тіофен-2-іл-циклогептанкарбонілокси)1-азоній-біцикло[2,2,2]октан Х; (R)-1-[(3-Метил-ізоксазол-5-ілкарбамоїл)-метил]-3-(1-тіофен-2-іл-циклогептанкарбонілокси)1-азоній-біцикло[2,2,2]октан Х; (R)-1-[(3-Флуор-фенілкарбамоїл)-метил]-3-(1-тіофен-2-іл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(5-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-тіофен-2-іл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-(Бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-тіофен-2-іл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-(Піразин-2-ілкарбамоїлметил)-3-(1-тіофен-2-іл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(піразин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(ізоксазол-3-ілкарбамоїлметил)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піридин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піридин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(5-Флуор-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-[(5-Метил-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піридин-3-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(2-Метил-піридин-4-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-Фенілкарбамоїлметил-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піримідин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(2-Флуор-фенілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(2,3-Дифлуор-фенілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[2-(2,3-Дигідро-бензофуран-5-іл)-етил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[2-(4-Флуор-фенокси)-етил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-феніл-циклогептанкарбонілокси)-1-(піридазин-4-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(5-Флуор-піридин-3-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-феніл-циклогептанкарбонілокси)-1-[2-(піридин-3-ілокси)-етил]-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(6-Метил-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(о-толілкарбамоїл-метил)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(2-піразин-2-іл-етил)-1-азоній-біцикло[2,2,2]октан Х; (S)-1-(3-Фенокси-пропіл)-3-(1-феніл-циклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан Х; (R)-1-{[2-(3-Флуор-фенокси)-етилкарбамоїл]-метил}-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; 3 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 (R)-1-[(3,5-Дифлуор-фенілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[2-(4-метокси-бензилокси)-етил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-(2-Фенетилоксіетил)-3-(1-феніл-циклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан Х; (R)-1-[(2,6-Дифлуор-фенілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(Метил-феніл-карбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[3-(4-Ціано-фенокси)-пропіл]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(2,5-Дифлуор-фенілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[2-(4-Ціано-бензилокси)-етил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-[(6-трифлуорметил-піридин-2-ілкарбамоїл)метил]-1-азоній-біцикло[2,2,2]октан Х; (R)-1-[(4-Метил-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-[(5-Хлор-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(п-толілкарбамоїл-метил)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(м-толілкарбамоїл-метил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-(Оксазол-2-ілкарбамоїлметил)-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(6-Метил-піридазин-3-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піримідин-2-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(5-Ціано-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піримідин-5-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(3-Флуор-піридин-2-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-[(3-Флуор-піридин-4-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-{2-[(піразин-2-карбоніл)-аміно]-етил}-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-([1,2,4]тіадіазол-5-ілкарбамоїлметил)-1-азонійбіцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-{3-[(піридин-2-карбоніл)-аміно]-пропіл}-1-азонійбіцикло[2,2,2]октан Х; (R)-1-[(2-Метил-піримідин-4-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-1-[(6-Метил-піримідин-4-ілкарбамоїл)-метил]-3-(1-феніл-циклогептанкарбонілокси)-1азоній-біцикло[2,2,2]октан Х; (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-{2-[(піридин-2-карбоніл)-аміно]-етил}-1-азонійбіцикло[2,2,2]октан Х; та (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(3-піридин-4-іл-пропіл)-1-азонійбіцикло[2,2,2]октан Х; де Х – фармацевтично прийнятний аніон моно або полівалентної кислоти. Сполуки формули (І), визначені вище, та сполуки заявленого винаходу містять аніон Х, асоційований з позитивним зарядом на четвертинний атом нітрогену. Аніоном Х може бути будь-який фармацевтично прийнятний аніон моно або полівалентної (наприклад, бівалентної) кислоти. У втіленні винаходу Х може бути аніоном мінеральної кислоти, як-то хлорид, бромід, йодид, сульфат, нітрат або фосфат; або аніоном придатної органічної кислоти, як-то ацетат, 4 UA 99521 C2 малеат, фумарат, цитрат, оксалат, сукцинат, тартрат, метансульфонат, п-толуєнсульфонат, бензенсульфонат, нафтален-1,5-дисульфонат, 2,5-дихлорбензенсульфонат, 1гідроксинафтален-2-сульфонат або ксинафоат (1-гідрокси-2-нафтоат). Згідно з винаходом, також запропоновано сполуку, вибрану з групи: X O H N + N N O O N H 5 ; X O H N + N S O N N O H ; X O H N + N S O N O N H ; X O F H N + N O N O N H ; X O F H N + N N O O O H ; X O + H N N N O O H 10 ; X O H N + N N O O H F ; 5 UA 99521 C2 X O H N + N O N O H ; та X O H N + N O 5 10 15 20 25 30 35 40 45 O N H де Х – фармацевтично прийнятний аніон моно або полівалентної кислоти. Зрозуміло, що певні сполуки заявленого винаходу можуть існувати у сольватованій, наприклад, гідратованій, а також несольватованій формах. Зрозуміло, що заявлений винахід стосується усіх таких сольватованих форм. Певні сполуки заявленого винаходу можуть існувати, як таутомери. Таутомери та їх суміші також утворюють аспект заявленого винаходу. Сполуки заявленого винаходу виявляють корисні фармацевтичні властивості. Наприклад, сполуки винаходу виявляють активності антагоністів мускаринових рецепторів, особливо мускаринових рецепторів М3. Більш того, сполуки також виявляють бажані властивості зв'язування білку плазми. Зв'язування білку плазми може бути сприятливою властивістю для сполук, застосовуваних інгаляцією, оскільки це може зменшувати дію будь-якої системної дії сполук. Сполуки винаходу мають активність, як фармацевтичні, зокрема, як антихолінергічні агенти, у тому числі антагоністи мускаринових рецепторів (М1, М2, та М3), зокрема антагоністи М3. Хвороби та стани, котрі можна лікувати сполуками охоплюють: 1. респіраторний тракт: обструктивні хвороби дихальних шляхів, охоплюючи вибране з групи: астма, у тому числі бронхіальна, алергічна, притаманна, непритаманна, індукована вправами, індукована ліками (охоплюючи аспірин та NSАІD) та індукована пилом астма, переривчаста та стійка будь-якої суворості, та інші причини дихальних шляхів гіперчутливості; хронічна обструктивна хвороба легень (СОРD); бронхіт, у тому числі інфекційний та еозинофільний бронхіт; емфізема; бронхоектаз; кістозний фіброз; саркоїдоз; легені фермера та пов'язані хвороби; пневмоніт з гіперчутливістю; фіброз легень, у тому числі криптогенний фіброзувальний альвеоліт, ідіопатичні інтерстиціальні пневмонії, фіброзне ускладнення антінеопластичної терапії та хронічна інфекція, у тому числі туберкульоз і аспергілез та інші грибкові інфекції; ускладнення при трансплантації легень; васкулітичні та тромботичні розлади судинної системи легень, та гіпертензія легень; протикашльова активність, у тому числі лікування хронічного кашлю, асоційованого з запальними та секреторними стани дихальних шляхів, та ятрогенного кашлю; гострий та хронічний риніт, у тому числі медикаментозний риніт, та вазомоторний риніт; цілорічний та сезонний алергічний риніт, у тому числі поліноз; назальний поліпоз; гостра інфекція, у тому числі звичайна застуда, та інфекція респіраторним синцитіальним вірусом, грипом, коронавірусом (охоплюючи SАRS) та аденовірусом; 2. кістки та суглоби: артритиди, асоційовані з остеоартритом/остеоартрозом, первинним та вторинним стосовно, наприклад, уродженої дисплазії стегна; цервікальний та поперековий спондиліт, та поперековий та шийний біль; ревматоїдний артрит та хвороба Стилла; серонегативні спондилоартропатії, у тому числі анкілозувальний спондиліт, псоріатичний артрит, реактивний артрит та недиференційована спондартропатія; септичний артрит та інші пов'язані з інфекцією артроопатії та розлади кісток, як-то туберкульоз, у тому числі хвороба Потта та синдром Понсе; гострий та хронічний індукований кристалами синовіт, у тому числі уратна подагра, хвороба відкладання кальцію пірофосфату, та пов'язане з кальцію апатитом запалення синовіально-сумкового сухожилля; хвороба Бехчета; первинний та вторинний синдром Шегрена; системний склероз та обмежена склеродерма; системний червоний вовчак, змішана хвороба сполучних тканин та недиференційована хвороба сполучних тканин; запальні міопатії, у тому числі дерматоміозит та поліміозит; ревматична полімалгія; юнацький артрит, у тому числі ідіопатичні запальні артритиди будь-якого суглобового розподілення та асоційовані синдроми, та ревматична лихоманка та системні ускладнення; васкулітиди, у тому числі артеріїт 6 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 гігантських клітин, артеріїт Такаясу, синдром Чарга-Штрауса, нодозний поліартерііт, мікроскопічний поліартерит, та васкулітиди, асоційовані з вірусною інфекцією, реакції гіперчутливості, кріоглобуліни, та парапротеїни; поперековий біль; родинна середньоморська лихоманка, синдром Мукла-Велса, та родинна ірландська лихоманка, хвороба Кікуші; індуковані ліками артралгії, тендонітиди та міопатії; 3. біль та, корекція сполучних тканин м'язоскелетних розладів внаслідок поранення або хвороби: артритид (наприклад, ревматоїдний артрит, остеоартрит, подагра або кристалартропатія), інша хвороба суглобів (як-то дегенерація міжхребцевих дисків або дегенерація скроне-щелепного суглобу), хвороба корекції кісток (як-то остеопороз, хвороба Паджета або остеонекроз), поліхондрит, склеродерма, змішаний розлад сполучних тканин, спондилоартропатії або періодонтальна хвороба (як-то періодонтит); 4. шкіра: псоріаз, атопічний дерматит, контактний дерматит або інші екзематозні дерматози та реакції гіперчутливості затриманого типу; фіто- та фотодерматит; себорейний дерматит, червоний плоский лишай, гангренозна піодермія, саркоїд шкіри, дискоїдний червоний вовчак, пемфігус, пемфігоїд, булезний епідермоліз, кропивниця, гігантська кропивниця, васкулітиди, токсичні еритеми, шкірні еозинофілії, осередкова плішивість, плішивість типу чоловіків, синдром Світа, синдром Вебера-Христіана, багатоформна еритема; целюліт, інфекційний та неінфекційний; панікулит; шкірні лімфоми, немеланомний рак шкіри та інші диспластичні ураження; індуковані ліками розлади, у тому числі висип; 5. очі: блефарит, кон'юнктивіт; у тому числі цілорічний та весняний алергічний кон'юнктивіт; ірит; передній та задній увеїт; хороїдит; автоімунні; дегенеративні або запальні розлади, що вражають сітчатку; офтальміт, у тому числі симпатетичний офтальміт; саркоїдоз; інфекції, у тому числі вірусні, грибкові та бактеріальні; 6. шлунково-кишковий тракт: глосит, гінгівіт, періодонтит; запалення стравоходу, у тому числі рефлюкс; еозинофільний гастро-ентерит, мастоцитоз, хвороба Крона, коліт, у тому числі виразковий коліт, проктит, свербіж заднього проходу; хронічна кишкова хвороба дітей, синдром подразненого кишечнику, та пов'язані з їжею алергії, котрі можуть мати дію, віддалену від кишечнику (наприклад, мігрень, риніт або екзема); 7. черевні: гепатит, у тому числі автоімунний, алкогольний та вірусний; фіброз та цироз печінки; холецистит; панкреатит, гострий та хронічний; 8. сечостатеві: нефрит, у тому числі інтерстиціальний та гломерулонефрит; нефротичний синдром; цистит, у тому числі гострий та хронічний (інтерстиціальний) цистит та виразка Ханнера; гострий та хронічний уретртит, простатит, епідидиміт, оофорит та сальпінгіт; вульвовагініт; хвороба Пейроне; еректильна дисфункція (самців та самиць); 9. відторгнення алотрансплантату: гостре та хронічне після, наприклад, трансплантації нирок, серця, печінки, легень, кісткового мозку, шкіри або роговиці, чи після переливання крові; або хронічна хвороба трансплантат проти хазяїна; 10. центральна нервова система: хвороба Альцгеймера та інші дементні розлади, у тому числі СJD та nvСJD; амілоїдоз; розсіяний склероз та інші синдроми демієлінування; церебральний атеросклероз та васкуліт; темпоральний артеріїт; бульбоспінальний параліч; гострий та хронічний біль (гострий, переривчастий або стійкий, чи центрального або периферійного походження), у тому числі вісцеральний біль, головний біль, мігрень, тригемінальна невралгія, атиповий лицевий біль, біль суглобів та кісток, біль від раку та інвазії пухлин, синдроми невропатичного біль., у тому числі діабетичні, постгерпетичні та асоційовані з ВІЛ невропатії; нейросаркоїдоз; ускладнення центральної та периферійної нервової системи від злоякісних, інфекційних або автоімунних процесів; 11. інші автоімунні та алергічні розлади, у тому числі тироїдит Хашимото, хвороба Граве, хвороба Аддісона, цукровий діабет, ідіопатична тромбоцитопенічна пурпура, еозинофільний фасцит, гіпер-ІgЕ-синдром, антіфосфоліпідний синдром; 12. інші розлади із запальним або імунологічним компонентом; у тому числі синдром набутого імунодефіциту (СНІД), проказа, синдром Сезарі, та паранеопластичні синдроми; 13. серцево-судинні: атеросклероз, що вражає коронарний та периферійний круг кровообігу; перикардит; міокардит, запальні та автоімунні кардіоміопатії, у тому числі міокардіальний саркоїд; ішемічні реперфузійні пошкодження; ендокардит, вальвуліт та аортит, у тому числі інфекційний (наприклад, сифілітичний); васкулітиди; розлади проксимальних та периферійних вен, у тому числі флебіт та тромбоз, у тому числі глибокий тромбоз вен та ускладнення варикозних вен; 14. онкологія: лікування звичайних типів раку, у тому числі пухлин простати, грудної залози, легень, яєчнику, підшлункової залози, травного т1ракту та ободової кишки, шлунка, шкіри та мозку та злоякісні утворення, що вражають кістковий мозок (охоплюючи лейкемії) та 7 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 лімфопроліферативні системи, як-то лімфома Ходжкіна та лімфома неХоджкіна; у тому числі відвернення та лікування метастазної хвороби та рецидиву пухлин, та паранеопластичні синдроми; та, 15. шлунково-кишковий тракт: хронічна кишкова хвороба дітей, проктит, еозинофільний гастро-ентерит, мастоцитоз, хвороба Крона, виразковий коліт, мікроскопічний коліт, недетермінантний коліт, розлад подразненого кишечнику, синдром подразненого кишечнику, незапальна діарея, пов'язані з їжею алергії, що мають дію, віддалену від кишечнику, наприклад, мігрень, риніт та екзема. Відповідно, заявлений винахід крім того стосується сполуки заявленого винаходу, що визначено вище, для застосування у терапії. У ще одному аспекті, винахід стосується застосування сполуки заявленого винаходу, що визначено вище, у виробництві медикаменту для застосування у терапії. У контексті опису термін "терапія" також охоплює "профілактику", якщо не визначене інше. Терміни "терапевтичний" та "терапевтично" є відповідними. Ще один аспект винаходу стосується способу лікування стану хвороби у ссавця, який потерпає від вказаної хвороби або при її ризику, що полягає у застосуванні до ссавця при потребі такого лікування терапевтично ефективної кількості сполуки заявленого винаходу, що визначено вище. Заявлений винахід також стосується сполуки заявленого винаходу, що визначено вище, для лікування хронічної обструктивної хвороби легень (СОРD) (як-то необоротна СОРD). Заявлений винахід також стосується сполуки заявленого винаходу, що визначено вище, для лікування астми. Заявлений винахід також стосується застосування сполуки заявленого винаходу, що визначено вище, у лікуванні хронічної обструктивної хвороби легень (СОРD) (як-то необоротна СОРD). Заявлений винахід також стосується застосування сполуки заявленого винаходу, що визначено вище, у лікуванні астми. Заявлений винахід також стосується застосування сполуки заявленого винаходу, що визначено вище, у виробництві медикаменту для застосування у лікуванні хронічної обструктивної хвороби легень (СОРD) (як-то необоротна СОРD). Заявлений винахід також стосується застосування сполуки заявленого винаходу, що визначено вище, у виробництві медикаменту для застосування у лікуванні астми. Заявлений винахід крім того стосується способу лікування хронічної обструктивної хвороби легень (СОРD) (як-то необоротна СОРD), у теплокровної тварини, як-то людини, що полягає у застосуванні до ссавця при потребі такого лікування терапевтично ефективної кількості сполуки заявленого винаходу, що визначено вище. Заявлений винахід крім того стосується способу лікування астми у теплокровної тварини, якто людини, що полягає у застосуванні до ссавця при потребі такого лікування терапевтично ефективної кількості сполуки заявленого винаходу, що визначено вище. Для застосування сполуки винаходу для терапевтичного лікування теплокровної тварини, як-то людини, вказаний інгредієнт звичайно формують стандартними способами як фармацевтичну композицію. Тому у ще одному аспекті заявлений винахід стосується фармацевтичної композиції, що містить сполуку винаходу, що визначено вище, та фармацевтично прийнятний ад'ювант, розріджувач або носій. У ще одному аспекті заявлений винахід стосується способу отримання вказаної композиції, що полягає у змішуванні активного інгредієнту з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. Залежно від режиму застосування, фармацевтичні композиції, наприклад, містять від 0,05 до 99 мас%, як-то від 0,05 до 80 мас%, наприклад, від 0,10 до 70 мас%, як-то від 0,10 до 50 мас%, активного інгредієнту, усі проценти є на основі загальної композиції. Фармацевтичні композиції цього винаходу можна застосовувати стандартним способом, що є потрібним для лікування, наприклад, місцево (як-то до легень та/або дихальних шляхів або до шкіри), перорально, ректально або парентерально. Для цього сполуки цього винаходу можна формувати у форму, наприклад, аерозолів, сухих порошків, таблеток, капсул, сиропів, гранул, водних або олійних розчинів або суспензій, (ліпідних) емульсій, дисперсивних порошків, супозиторієв, мазей, кремів, крапель та стерильних ін'єкційних водних або олійних або суспензій. Придатною фармацевтичною композицією цього винаходу є придатна для перорального застосування в одиничній дозованій формі, наприклад, таблетка або капсула, котра містить між 0,1 мг та 1 г активного інгредієнту. 8 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 У ще одному аспекті фармацевтичною композицією винаходу є придатна для внутрішньовенної, підшкірної або внутрішньом'язової ін'єкції. Кожний пацієнт може отримувати, наприклад, внутрішньовенну, підшкірну або внутрішньом'язову дозу 0,01 мг/кг – 100 мг/кг сполуки, наприклад, у межах 0,1 мг/кг – 20 мг/кг композиції цього винаходу, застосовуваної 1-4 рази на добу. Внутрішньовенну, підшкірну або внутрішньом'язову дозу можна давати засобами болюсної ін'єкції. Альтернативно внутрішньовенну дозу можна давати безперервним вливанням. Альтернативно кожний пацієнт може отримувати добову пероральну дозу, що є приблизно еквівалентною добовій парентеральній дозі композиції, застосовуваній 1-4 рази на добу Ще одною придатною фармацевтичною композицією цього винаходу є придатна для застосування інгаляцією, інгаляція є особливо корисним способом застосування сполуки винаходу, при лікуванні респіраторних хвороб, як-то хронічна обструктивна хвороба легень (СОРD) або астма. При застосуванні інгаляцією сполуки заявленого винаходу можна застосовувати ефективно у дозах у мкг, наприклад, 0,1-500 мкг, 0,1-50 мкг, 0,1-40 мкг, 0,1-30 мкг, 0,1-20 мкг, 0,1-10 мкг, 5-10 мкг, 5-50 мкг, 5-40 мкг, 5-30 мкг, 5-20 мкг, 5-10 мкг, 10-50 мкг, 1040 мкг 10-30 мкг, або 10-20 мкг активного інгредієнту. У втіленні винаходу запропоновано фармацевтичну композицію, що містить сполуку винаходу, що визначено вище, в асоціації з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм, що формують для застосування інгаляцією. При застосуванні інгаляцією, інгалятори з виміряною дозою можна застосовувати для застосування активного інгредієнту, диспергованого у придатному пропеленті та з додатковими наповнювачами або без, як-то етанол, ПАР, лубриканти або стабілізатори. Придатні пропеленти охоплюють вуглеводні, хлорфлуоркарбон та гідрофлуоралкан (наприклад, гептафлуоралкан), або їх суміші. Кращими пропелентами є Р134а та Р227, кожний з котрих можна застосовувати поодинці або у комбінації з іншими пропелентами та/або ПАР та/або іншими наповнювачами. Розпилені водні суспензії або, переважно, розчини, можна також застосовувати, з регуляторами рН та/або тонічності або без, як одиничну дозу або багато-дозову рецептуру. Інгалятори сухого порошку можна застосовувати для застосування активного інгредієнту поодинці або у комбінації з фармацевтично прийнятним носієм, в останньому випадку, як тонко подрібнений порошок або як упорядковану суміш. Інгалятор сухого порошку може бути одинично-дозовим або багато-дозовим та може застосовувати сухий порошок або капсул, що містить порошок. Інгалятор з виміряною дозою, розпилювач та інгалятори сухого порошку є добре відомими та багато таких пристроїв є доступними. Заявлений винахід крім того стосується комбінаційної терапії, де сполуку винаходу або фармацевтичну композицію або рецептуру, що містить сполуку винаходу, застосовують одночасно або послідовно, або як комбінований препарат з ще одним терапевтичним агентом або агентами для лікування одного або більше перелічених станів. Зокрема, для лікування запальних хвороб, як-то (але без обмежень) ревматоїдний артрит, остеоартрит, астма, алергічний риніт, хронічна обструктивна хвороба легень (СОРD), псоріаз, та запальна хвороба кишечнику, сполуки винаходу можна поєднувати з агентами, переліченими нижче. Нестероїдні анті-запальні агенти (далі NSАІD), у тому числі неселективні інгібітори циклооксигеназ СОХ-1 / СОХ-2, застосовувані місцево або системно (як-то піроксикам, диклофенак, пропіонові кислоти, як-то напроксен, флурбіпрофен, фенопрофен, кетопрофен та ібупрофен, фенамати, як-то мефенамінова кислота, індометацин, суліндак, азапропазон, піразолони, як-то фенілбутазон, саліцилати, як-то аспірин); селективні інгібітори СОХ-2 (як-то мелоксикам, целекоксиб, рофекоксиб, валдекоксиб, лумарококсиб, парекоксиб та еторикоксиб); циклооксигеназа, що інгібує донори нітроген оксиду (СІNОD); глюкокортикостероїди (місцеві, пероральні, внутрішньом'язові, внутрішньовенні, або інтраартикулярні); метотрексат; лефлуномід; гідроксихлорхін; d-пеніциламін; ауронафін або інші парентеральні або пероральні препарати золота; аналгетики; діацереїн; інтраартикулярні терапії, як-то похідні гіалуронової кислоти; та харчові добавки, як-то глюкозамін. Заявлений винахід крім того стосується комбінації сполуки винаходу з цитокіном або агоністом або антагоністом функції цитокіну (охоплюючи агенти, що діють на шляхи передачі сигналів метаболізму цитокіну, як-то модулятори системи SОСS), у тому числі альфа-, бета-, та гамма-інтерферони; інсуліноподібний фактор росту типу І (ІGF-1); інтерлейкіни (ІL), у тому числі ІL1-17, та антагоністи або інгібітори інтерлейкінів, як-то анакінра; інгібітори фактору некрозу пухлин альфа (ТNF-α), як-то анті-ТNF моноклональні антитіла (наприклад, інфлуксимаб; 9 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 адалімумаб, та СDР-870) та антагоністи рецепторів ТNF, у тому числі молекули імуноглобуліну (як-то етанерцепт) та агенти низької молекулярної маси, як-то пентоксифілін. На додаток заявлений винахід стосується комбінації сполуки винаходу із В-лімфоцитами націлювання моноклональних антитіл (як-то СD20 (ритуксимаб), МRА-аІLl6R та Т-лімфоцитами, СТLА4-Іg, НuМах Іl-15). Заявлений винахід крім того стосується комбінації сполуки винаходу із модулятор функції рецептору хемокіну, як-то антагоніст ССR1, ССR2, ССR2А, ССR2В, ССR3, ССR4, ССR5, ССR6, ССR7, ССR8, ССR9, ССR10 та ССR11 (для родини С-С); СХСR1, СХСR2, СХСR3, СХСR4 та СХСR5 (для родини С-Х-С) та СХ3СR1 для родини С-Х3-С. Заявлений винахід крім того стосується комбінації сполуки винаходу з інгібітором матриксних металопротеаз (ММР), як-то, стромелізини, колагенази, та желатинази, а також агреканаз; особливо колагенази-1 (ММР-1), колагенази-2 (ММР-8), колагенази-3 (ММР-13), стромелізину-1 (ММР-3), стромелізину-2 (ММР-10), та стромелізину-3 (ММР-11) та ММР-9 та ММР-12, у тому числі агентів, як-то доксициклін. Заявлений винахід крім того стосується комбінації сполуки винаходу та інгібітору біосинтезу лейкотриєну, інгібітору 5-ліпоксигенази (5-LО) або антагоністу активувального білку 5ліпоксигенази (FLАР), як-то; зилейтон; АВТ-761; фенлейтон; тепоксалін; Аbbоtt-79175; Аbbоtt85761; N-(5-заміщений)-тіофен-2-алкілсульфонамід; 2,6-ді-трет-бутилфенолгідразони; метокситетрагідропірани, як-то Zеnеса ZD-2138; сполука SВ-210661; піридиніл-заміщена сполука 2-ціанонафталенц, як-то L-739,010; сполука 2-ціанохінолін, як-то L-746,530; або сполук індолу або хіноліну, як-то МК-591, МК-886, та ВАY х 1005. Заявлений винахід крім того стосується комбінації сполуки винаходу та антагоніст рецептору для лейкотриєнів (LТ) В4, LТС4, LТD4, та LТЕ4, вибраний з групи: фенотіазин-3-1s, як-то L-651,392; амідино-сполуки, як-то СGS-25019с; бензоксаламіни, як-то ортазоласт; бензенкарбоксимідаміди, як-то ВІІL 284/260; та сполуки, як-то зафірлукаст, аблукаст, монтелукаст, пранлукаст, верлукаст (МК-679), RG-12525, Rо-245913, іралукаст (СGР 45715А), та ВАY х 7195. Заявлений винахід крім того стосується комбінації сполуки винаходу та інгібітору фосфодіестерази (РDЕ), як-то метилксантанін, у тому числі теофілін та амінофілін; селективного інгібітору ізоферменту РDЕ, у тому числі інгібітор РDЕ4 інгібітор ізоформи РDЕ4D, або інгібітор РDЕ5. Заявлений винахід крім того стосується комбінації сполуки винаходу та антагоністу рецептору гістаміну типу 1, як-то цетиризин, лоратадин, деслоратадин, фексофенадин, акривастин, терфенадин, астемізол, азеластин, левокабастин, хлорфенірамін, прометазин, циклізин, або мізоластин; застосовувані перорально, місцево або парентерально. Заявлений винахід крім того стосується комбінації сполуки винаходу та інгібітору протонного насосу (як-то омепразол) або шлункозахисного антагоністу рецептору гістаміну типу 2. Заявлений винахід крім того стосується комбінації сполуки винаходу та антагоністу рецептору гістаміну типу 4. Заявлений винахід крім того стосується комбінації сполуки винаходу та вазоконстрикторний симпатоміметичний агент агоністу адреноміметику альфа-1/альфа-2, як-то пропілгекседрин, фенілефрин, фенілпропаноламін, ефедрин, псевдоефедрин, нафазолін гідрохлорид, оксиметазолін гідрохлорид, тетрагідрозолін гідрохлорид, ксилометазолін гідрохлорид, трамазолін гідрохлорид або етилнорепінефрин гідрохлорид. Заявлений винахід крім того стосується комбінації сполуки винаходу та бетаадреноміметику (охоплюючи підтипи бета-рецептору 1-4), як-то ізопреналін, салбутамол, формотерол, салметерол, тербуталін, орципреналін, бітолтерол мезилат, пірбутерол, або індакатерол або його хіральний енантіомер. Заявлений винахід крім того стосується комбінації сполуки винаходу та хромону, як-то натрію хромоглікат або недохроміл натрію. Заявлений винахід крім того стосується комбінації сполуки винаходу із глюкокортикоїдом, якто флунізолід, триамцинолон ацетонід, беклометазон дипропіонат, будезонід, флутиказон пропіонат, циклезонід або мометазон фуроат. Заявлений винахід крім того стосується комбінації сполуки винаходу з агентом, що модулює рецептор ядерного гормону, як-то РРАRs. Заявлений винахід крім того стосується комбінації сполуки винаходу із імуноглобуліном (Іg) або препаратом або антагоністом або антитілом Іg, що модулює функцію Іg, як-то анті-ІgЕ (наприклад, омалізумаб). 10 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 Заявлений винахід крім того стосується комбінації сполуки винаходу та ще одного системного або місцево-застосовуваного анті-запального агенту, як-то талідомід або його похідне, ретиноїд, дитранол або кальципотріол. Заявлений винахід крім того стосується комбінації сполуки винаходу та комбінації аміносаліцилатів та сульфапіридину, як-то сульфасалазин, месалазин, балсалазид, та олсалазин; та імуномодуляторні агенти, як-то тіопурини, та кортикостероїди, як-то будезонід. Заявлений винахід крім того стосується комбінації сполуки винаходу із антибактеріальним агентом, як-то похідне пеніциліну, тетрациклін, макролід, бета-лактам, флуорхінолон, метронідазол, інгаляційний аміноглікозид; антівірусний агент, у тому числі ацикловір, фамцикловір, валацикловір, ганцикловір, цидофовір, амантадин, римантадин, рибавірин, занамавір та оселтамавір; інгібітор протеази, як-то індинавір, нелфінавір, ритонавір, та заксинавір; інгібітор зворотної транскриптази нуклеозиду, як-то диданозин, ламівудин, ставудин, залцитабін або зидовудин; або інгібітор зворотної транскриптази ненуклеозиду, як-то невірапін або ефавіренз. Заявлений винахід крім того стосується комбінації сполуки винаходу та серцево-судинного агенту, як-то блокатор каналів кальцію, бета-адреноблокатор, інгібітор ферменту перетворення ангіотензину (АСЕ), антагоніст рецептору ангіотензину-2; агент зниження ліпідів, як-то статин або фібрат; модулятор морфології клітин кров, як-то пентоксифілін; тромболітик, або антикоагулянт, як-то інгібітор агрегації тромбоцитів. Заявлений винахід крім того стосується комбінації сполуки винаходу та ЦНС-агенту, як-то антідепресант (як-то сертралін), ліки проти паркинсонизму (як-то депреніл, L-допа, ропінірол, праміпексол, інгібітор МАОВ, як-то селегін та разагілін, інгібітор соmР, як-то тасмар, інгібітор А2, інгібітор перепоглинання допаміну, антагоніст NМDА, агоніст нікотину, агоніст допаміну або інгібітор нейронної нітроген-оксид-синтази), або ліки проти хвороби Альцгеймера, як-то донепезил, ривастигмін, такрин, інгібітор СОХ-2, пропентофілін або метрифонат. Заявлений винахід крім того стосується комбінації сполуки винаходу та агенту для лікування гострого або хронічного болю, як-то центрально або периферійно діючий аналгетик (наприклад, опіоїд або його похідне), карбамазепін, фенітоїн, натрію валпроат, амітриптилін або інший антидепресант, парацетамол, або нестероїдний протизапальний агент. Заявлений винахід крім того стосується комбінації сполуки винаходу із парентерально або місцево-застосовуваним (охоплюючи інгаляційний) анестетик, як-то лігнокаїн або його похідне. Сполуку заявленого винаходу можна також застосовувати у комбінації з агентом проти остеопорозу, у тому числі гормональним агентом, як-то ралоксифен, або біфосфонат, як-то аленронат. Заявлений винахід крім того стосується комбінації сполуки винаходу з нижченаведеним: (і) інгібітор триптази; (іі) антагоніст активувального фактору тромбоцитів (РАF); (ііі) інгібітор ферменту перетворення інтерлейкіну (ІСЕ); (іv) інгібітор ІМРDН; (v) інгібітори адгезії молекул, у тому числі антагоніст VLА-4; (vі) катепсин; (vіі) інгібітор кінази, як-то інгібітор тирозин-кінази (якто Вtk, Іtk, Jаk3 або МАР, наприклад, гефітиніб або Іматиніб мезилат), серин/треонін-кінази (якто інгібітор МАР-кінази, як-то р38, JNК, білкової кінази А, В або С, або ІКК), або кінази, задіяної у регулюванні клітинного циклу (як-то цилін-залежна кіназа); (vііі) інгібітор глюкоза-6-фосфатдегідрогенази; (іх) антагоніст рецептору кінін-В1. - або В2. -; (х) агент проти подагри, наприклад, колхіцин; (хі) інгібітор ксантин-оксидази, наприклад, алопуринол; (хіі) урикозуричний агент, наприклад, пробенецид, сульфінпіразон або бензбромарон; (хііі) стимулятор секреції гормону росту; (хіv) фактор трансформування росту (ТGFβ); (хv) похідний від тромбоцитів фактор росту (РDGF); (хvі) фактор росту фібробластів, наприклад, основний фактор росту фібробластів (bFGF); (хvіі) фактор стимулювання колоній макрофагів-гранулоцитів (GМ-СSF); (хvііі) капсаїциновий крем; (хіх) антагоніст рецептору тахікініну NК1 або NК3, як-то NКР-608С, SВ233412 (талнетант) або D-4418; (хх) інгібітор еластази, як-то UТ-77 або ZD-0892; (ххі) інгібітор ферменту перетворення ТNF-альфа (ТАСЕ); (ххіі) інгібітор індукованої нітроген-оксид-синтази (іNОS); (ххііі) хемоатрактант рецептор-гомологічної молекули, експресованої клітинами ТН2, (якто антагоніст СRТН2); (ххіv) інгібітор Р38; (ххv) агент, що модулює функцію Толл-подібних рецепторів (ТLR), (ххvі) агент, що модулює активність пуринергічних рецепторів, як-то Р2 × 7; або (ххvіі) інгібітор фактору активування транскрипції, як-то NFkВ, АРІ, або SТАТS. Сполуку винаходу можна також застосовувати у комбінації з існуючим терапевтичним агентом для лікування раку, наприклад, придатні агенти охоплюють: (і) антипроліферативні/антінеопластичні ліки або їх комбінацію, як застосовувано у медичній онкології, як-то алкілувальний агент (наприклад, цис-платин, карбоплатин, циклофосфамід, азотистий іприт, мелфалан, хлорамбуцил, бусульфан або нітрозосечовина); антиметаболіт (наприклад, антифолат, як-то флуорпіримідин типу 5-флуорурацилу або тегафур, ралтитрексед, 11 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 метотрексат, цитозин арабінозид, гідроксисечовина, гемцитабін або паклітаксел); антіпухлинний антибіотик (наприклад, антрациклін, як-то адріаміцин, блеоміцин, доксорубіцин, дауноміцин, епірубіцин, ідарубіцин, мітоміцин-С, дактиноміцин або мітраміцин); антимітотичний агент (наприклад, алкалоїд вінка, як-то вінкристин, вінбластин, віндезин або віноребін, або таксоїд, якто таксол або таксотер); або інгібітор топоізомерази (наприклад, епіподофілотоксин, як-то етопозид, теніпозид, амсакрин, топотекан або камптототецин); (іі) цитостатичний агент, як-то антіестроген (наприклад, тамоксифен, тореміфен, ралоксифен, дролоксифен або йодоксифен), даун-регулятор рецептор естрогену (наприклад, фулвестрант), антіандроген (наприклад, бікалутамід, флутамід, нілутамід або ципротерон ацетат), антагоніст LНRН або агоніст LНRН (наприклад, госерелін, лейпрорелін або бусерелін), прогестоген (наприклад, мегестрол ацетат), інгібітор ароматази (наприклад, анастрозол, летрозол, воразол або екземестан) або інгібітор 5-редуктази, як-то фінастерид; (ііі) агент, що інгібує інвазію ракових клітин (наприклад, інгібітор металопротеїнази типу маримастат або інгібітор функції рецептору активатору плазміногену урокінази); (іv) інгібітор функції фактору росту, наприклад: фактор росту антитіл (наприклад, антитіл анти-еrbb2 трастузумаб, або антитіл анти-еrbb1 цетуксимаб [С225]), інгібітор фарнезилтрансферази, інгібітор треонін-кінази або інгібітор серин/треонін-кінази, інгібітор родини епідермального фактору росту (наприклад, інгібітор родини треонін-кінази ЕGFR, як-то N-(3хлор-4-флуорфеніл)-7-метокси-6-(3-морфолінопропокси)-хіназолін-4-амін (гефітиніб, АZD1839), N-(3-етинілфеніл)-6,7-біс(2-метоксіетокси)-хіназолін-4-амін (ерлотиніб, ОSІ-774) або 6акриламідо-N-(3-хлор-4-флуорфеніл)-7-(3-морфолінопропокси)хіназолін-4-амін (СІ 1033)), інгібітор похідної від тромбоцитів родини фактору росту, або інгібітор родини фактору росту гепатоцитів; (v) антіангіогенний агент, як-то агент, що інгібує дію судинного ендотеліального фактору росту (наприклад, антитіло анти-судинного ендотеліального фактору росту клітин бевацизумаб, сполука, розкрита у WО 97/22596, WО 97/30035, WО 97/32856 або WО 98/13354), або сполука, що працює за ще одним механізмом (як-то ліномід, інгібітор функції інтегрину αvβ3 або ангіостатин); (vі) агент пошкодження судин, як-то комбретастатин А4, або сполука, розкрита у WО 99/02166, WО 00/40529, WО 00/41669, WО 01/92224, WО 02/04434 або WО 02/08213; (vіі) агент для антисенсової терапії, наприклад, агент, спрямований проти одної з цілей, перелічених вище, як-то ІSІS 2503, анти-рас антисенс; (vііі) агент для генної терапії, наприклад, для заміщення аберантних генів, як-то аберантний р53 або аберантний ВRСА1 або ВRСА2, GDЕРТ (ген-спрямована ферментна терапія), як-то застосовуючи цитозин деаміназу, тимідин-кіназу або бактеріальний фермент нітроредуктазу та для посилення толерантності пацієнта до хіміотерапії або радіотерапії, як-то генна терапія багато-лікової резистентності; або (іх) імунотерапевтичний агент, наприклад, для посилення ех-vіvо та іn-vіvо імуногенності клітини пухлин пацієнта, як-то трансфекція цитокінами, як-то інтерлейкін 2, інтерлейкін 4 або фактор стимулювання колоній макрофагів-гранулоцитів, для зменшення анергії Т-клітин, із застосуванням трансфектованих імунних клітин, як-то цитокін-трансфектовані дендритні клітини, підходи, застосовуючи цитокін-трансфектовані пухлин лінії клітин та із застосуванням анти-ідіотипових антитіл. У ще одному втіленні заявлений винахід стосується фармацевтичного продукту, що містить, у комбінації, перший активний інгредієнт, що є сполукою заявленого винаходу, як вище описано, та принаймні один наступний активний інгредієнт, вибраний з нижченаведеного: - інгібітор фосфодіестерази, - β2. адреноміметик, - модулятор функції рецептору хемокіну, - інгібітор функції кінази, - інгібітор протеази, - стероїдний агоніст рецептору глюкокортикоїду, та - нестероїдний агоніст рецептору глюкокортикоїду. Фармацевтичний продукт у цьому втіленні може, наприклад, бути фармацевтичною композицією, що містить перший та наступні активні інгредієнти у суміші. Альтернативно, фармацевтичний продукт може, наприклад, містити перший та наступні активні інгредієнти в окремих фармацевтичних препаратах, придатних для одночасного, послідовного або окремого застосування до пацієнта при потребі цього. Фармацевтичний продукт у цьому втіленні має особливе застосування у лікуванні респіраторних хвороб, як-то астма, СОРD або риніт. 12 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклади інгібітору фосфодіестерази, що можна застосовувати у фармацевтичному продукті у цьому втіленні, інгібітор охоплюють РDЕ4, як-то інгібітор ізоформи РDЕ4D, інгібітор РDЕ3 та інгібітор РDЕ5. Приклади охоплюють сполуки (Z)-3-(3,5-дихлор-4-піридил)-2-[4-(2-інданілокси-5-метокси-2-піридил]пропеннітрил, N-[9-аміно-4-оксо-1-феніл-3,4,6,7-тетрагідропіроло[3,2,1-jk][1,4]бензодіазепін-3(R)-іл]піридин3-карбоксамід (СІ-1044) 3-(бензилокси)-1-(4-флуорбензил)-N-[3-(метилсульфоніл)феніл]-1Н-індол-2-карбоксамід, (1S-екзо)-5-[3-(біцикло[2,2,1]гепт-2-ілокси)-4-метоксифеніл]тетрагідро-2(1Н)-піримідинон (Аtіzоrаm), N-(3,5,дихлор-4-піридиніл)-2-[1-(4-флуорбензил)-5-гідрокси-1Н-індол-3-іл]-2-оксоацетамід (АWD-12-281), β-[3-(циклопентилокси)-4-метоксифеніл]-1,3-дигідро-1,3-діоксо-2Н-ізоіндол-2-пропанамід (СDС-801), N-[9-метил-4-оксо-1-феніл-3,4,6,7-тетрагідропіроло[3,2,1-jk][1,4]бензодіазепін-3(R)іл]піридин-4-карбоксамід (СІ-1018), цис-[4-ціано-4-(3-циклопентилокси-4-метоксифеніл)циклогексан-1-карбонова кислота (циломіласт) 8-аміно-1,3-біс(циклопропілметил)ксантин (ципамфілін) N-(2,5-дихлор-3-піридиніл)-8-метокси-5-хінолінкарбоксамід (D-4418), 5-(3,5-ді-трет-бутил-4-гідроксибензиліден)-2-імінотіазолідин-4-он (дарбуфелон), 2-метил-1-[2-(1-метилетил)піразоло[1,5-а]піридин-3-іл]-1-пропанон (ібудиласт), 2-(2,4-дихлорфенілкарбоніл)-3-уреїдобензофуран-6-іл метансульфонат (ліриміласт), (-)-(R)-5-(4-метокси-3-пропоксифеніл)-5-метилоксазоліdіn-2-он (мезопрам), (-)-цис-9-етокси-8-метокси-2-метил-1,2,3,4,4а, 10b-гексагідро-6-(4діізопропіламінокарбонілфеніл)-бензо[с][1,6]нафтиридин (пумафентрин), 3-(циклопропілметокси)-N-(3,5-дихлор-4-піридил)-4-(дифлуорметокси)бензамід (рофлуміласт), N-оксид рофлуміласту, 5,6-діетоксибензо[b]тіофен-2-карбонова кислота (тибенеласт) 2,3,6,7-тетрагідро-2-(мезитиліміно)-9,10-диметокси-3-метил-4Н-піримідо[6,1-а]ізохінолін-4-он (трехінзин) та 3-[[3-(циклопентилокси)-4-метоксифеніл]-метил]-N-етил-8-(1-метилетил)-3Н-пурин-6-амін (V11294А). Приклади β2-адреноміметику, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють метапротеренол, ізопротеренол, ізопреналін, албутерол, салбутамол (наприклад, як сульфат), формотерол (наприклад, як фумарат), салметерол (наприклад, як ксинафоат), тербуталін, оркіпреналін, бітолтерол (наприклад, як мезилат), пірбутерол або індакатерол. β2-адреноміметиком у цьому втіленні можуть бути довгодіючі β2агоністи, наприклад, салметерол (наприклад, як ксинафоат), формотерол (наприклад, як фумарат), бамбутерол (наприклад, як гідрохлорид), кармотерол (ТА 2005, хімічно ідентифікований як 2(1Н)-Хінолон, 8-гідрокси-5-[1-гідрокси-2-[[2-(4-метокси-феніл)-1-метилетил]аміно]етил]-моногідрохлорид, [R-(R*,R*)] також ідентифікований у Сhеmісаl Аbstrасt Sеrvісе Rеgіstrу № 137888-11-0 та розкритий U.S. Раtеnt Nо 4,579,854), індакатерол (САS № 312753-063; QАВ-149), похідні форманіліду, наприклад, 3-(4-{[6-({(2R)-2-[3-(форміламіно)-4-гідроксифеніл]2-гідроксіетил}аміно)гексил]окси}-бутил)-бензенсульфонамід, як розкрито у WО 2002/76933, похідні бензенсульфонаміду, наприклад, 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)-гексил]окси}бутил)бензенсульфонамід, як розкрито у WО 2002/88167, агоністи рецепторів ариланіліну, як розкрито у WО 2003/042164 та WО 2005/025555, похідні індолу, як розкрито у WО 2004/032921 та US 2005/222144, та сполуки GSК 159797, GSК 159802, GSК 597901, GSК 642444 та GSК 678007. Приклади модулятору функції рецептору хемокіну, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють антагоніст рецептору ССR1. Приклади інгібітору функції кінази, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють інгібітор кінази р38 та інгібітор ІКК. Приклади інгібітору протеази, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють інгібітор нейтрофіл-еластази або інгібітор ММР12. Приклади агоністу рецептору стероїдного глюкокортикоїду, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють будезонід, флутиказон (наприклад, як пропіонат естер), мометазон (наприклад, як фуроат естер), беклометазон (наприклад, як 17пропіонат або 17,21-дипропіонат естери), циклезонід, лотепреднол (як, наприклад, етабонат), 13 UA 99521 C2 5 10 15 20 25 30 35 40 45 50 55 60 етипреднол (як, наприклад, диклоацетат), триамцинолон (наприклад, як ацетонід), флунізолід, зотиказон, флумоксонід, рофлепонід, бутиксокорт (наприклад, як пропіонат естер), преднізолон, преднізон, типредан, стероїдні естери, наприклад, 6α,9α-дифлуор-17α-[(2фуранілкарбоніл)окси]-11β-гідрокси-16α-метил-3-оксо-андроста-1,4-дієн-17β-карботіонової кислот S-флуорметил-естер, 6α,9α-дифлуор-11β-гідрокси-16α-метил-3-оксо-17α-пропіонілоксиандроста-1,4-дієн-17β-карботіонової кислот S-(2-оксо-тетрагідро-фуран-3S-іл) естер та 6α,9αдифлуор-11β-гідрокси-16α-метил-17α-[(4-метил-1,3-тіазол-5-карбоніл)окси]-3-оксо-андроста-1,4дієн-17β-карботіонової кислот S-флуорметил-естер, стероїдні естери згідно із DЕ 4129535, стероїди згідно із WО 2002/00679, WО 2005/041980, або стероїди GSК 870086, GSК 685698 та GSК 799943. Приклади модулятору агоністу рецептору нестероїдного глюкокортикоїду, що можна застосовувати у фармацевтичному продукті у цьому втіленні, охоплюють описані у WО2006/046916. Винахід ілюстровано нижченаведеними прикладами. У прикладах є нижченаведені Фіг. фіг.: Фіг. 1: Рентгенодифрактограма порошку форми А прикладу 14. Фіг. 2: Рентгенодифрактограма порошку форми А прикладу 15. У прикладах ЯМР-спектри вимірювали на спектрометрі Vаrіаn Unіtу Іnоvа при частоті протону 300 або 400 або 500 МГц, або на спектрометрі Вrukеr DRХ при частоті протону 400 або 500 МГц, або на спектрометрі Вrukеr Аvаnсе при частоті протону 600 МГц або на спектрометрі Вrukеr Аvаnсе DРХ 300 при частоті протону 300 МГц. МС-спектри вимірювали на спектрометрі Аgіlеnt 1100 МSD G1946D або спектрометрі Неwlеtt Расkаrd НР1100 МSD G1946А або спектрометрі Wаtеrs Місrоміs ZQ2000. Назви створювали, застосовуючи програму Аutоnоm 2000 (варіант 4,01,305). РДП-дані збирали, застосовуючи прилад РАNаlуtісаl СubіХ РRО або прилад РАNаlуtісаl ХРеrt. РАNаlуtісаl СubіХ РRО Дані збирали з приладу РАNаlуtісаl СubіХ РRО у конфігурації θ - θ у межах сканування 2° – 40° 2θ з експозицією 100 с на інкремент 0,02°. Рентгенопромені створювали довгофокусною мідною трубкою при 45 кВ та 40 мА. Довжина хвилі рентгенопроменів була 1,5418 Å. Дані збирали на оправах з нульовим фоном, на котрих розміщали ~ 2 мг сполуки. Оправу робили з одиничного кристалу силіцію, розрізаного вздовж недифрактувальної площини, та тоді полірували до оптично матової поверхні. Рентгенопромені від цієї поверхні зводили нанівець гасінням Брегга. РАNаlуtісаl Х-Реrt Дані збирали, застосовуючи прилад РАNаlуtісаl Х-Реrt у конфігурації 2θ - θ у межах сканування 2° до 40° 2θ з експозицією 100 с на інкремент 0,02°. Рентгенопромені створювали довгофокусною мідною трубкою при 45 кВ та 40 мА. Довжина хвилі рентгенопроменів була1,5418Å. Тhе Дані збирали на оправах з нульовим фоном, на котрих ~ 2 мг сполуки розміщали. Оправу робили з одиничного кристалу силіцію, розрізаного вздовж недифрактувальної площини, та тоді полірували до оптично матової поверхні. Рентгенопромені від цієї поверхні зводили нанівець гасінням Брегга. ДСК-термограми вимірювали, застосовуючи калориметр ТА Q1000 диференційного сканування, з піддонами з алюмінію та проколеними кришками. Маси зразків були 0,5-5 мг. Спосіб проводили під потоком азоту (50 мл/хвил) та температурі 25-300 °C при постійній швидкості підвищення температури 10 °C за хвилину. ТГА-термограми вимірювали, застосовуючи термогравіметричнй аналізатор ТА Q500 з піддонами з платини. Маси зразків м 1 та 5 мг. Спосіб проводили під потоком азоту (60 мл/хвил) та температурі 25-300 °C при постійній швидкості підвищення температури 10 °C за хвилину. ГСП-профілі вимірювали, застосовуючи прилад динамічної сорбції пари DVS-1. Твердий зразок приблизно 1-5 мг розміщали у скляну посудину та масу зразку реєстрували способом подвійного циклу (40-90-0-90-0 % відносної вологості (ВВ), на етапах 10 % ВВ). Скорчення: ДХЕ = 1,2-дихлоретан ДХМ = дихлорметан ДМФ = диметилформамід ДМСО = Диметилсульфоксид ЕtОАс = етилацетат ЕtОН = етанол ГСП = гравіметрична сорбція пари НАТU = О-(7-Азабензотриазол-1-іл)-N, N,N",N’-тетраметилуронію гексафлуорфосфат 14 UA 99521 C2 5 10 МеСN - Ацетонітрил МеОН = метанол Rt = час утримування ТГФ = тетрагідрофуран ДСК = Диференційна сканувальна калориметрія ТГА = Термогравіметричний аналіз РДП = рентгенодифракція порошку Приклад 1: (R)-1-[(6-Метил-піридин-3-ілкарбамоїл)-метил]-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан хлорид а) 1-Феніл-циклогептанол OH 15 20 До магнію (1,2 г) у безводному тетрагідрофурані (60 мл) під азотом додавали кристал йоду, а потім бромбензен (7,85 г) при такій швидкості, щоб реакційна суміш мала стійке кипіння під зворотним холодильником. Реакційну суміш перемішували протягом 20 хвилин і додавали циклогептанон (4,48 г). Після перемішування протягом 10 хвилин додавали насичений водний амонію хлорид (10 мл) та реакційну суміш розподіляли між водою (100 мл) та ізогексаном (100 мл). Органічний шар сушили (МgSО4) та випарювали, отримуючи підзаголовну сполуку (7,6 г) як оливу. 1 Н ЯМР (300 МГц, СDСl3) 7,53-7,47 (m, 2Н), 7,36-7,29 (m, 2Н), 7,26-7,19 (m, 1Н), 2,07 (ddd, 2Н), 1,97-1,50 (m, 11Н). b) 1-Метокси-1-феніл-циклогептан O 25 30 1-Феніл-циклогептанол (Приклад 1а) (7,6 г) розчиняли у тетрагідрофурані (100 мл) та додавали натрію гідрид (60 % в оливі, 2,0 г). Реакційну суміш перемішували при 60С протягом 5 хвилин та додавали йодметан (7,1 г). Суміш тримали при 60С протягом ночі та тоді додавали наступну кількість натрію гідриду (60 % в оливі, 2,0 г) та йодметану (7,1 г) та реакційну суміш гріли при кипінні під зворотним холодильником протягом 70 годин. Реакційну суміш розподіляли між водою (100 мл) та ізогексаном (100 мл) та органічний шар відокремлювали, сушили (МgSО4) та випарювали, отримуючи підзаголовну сполуку (11,31 г). 1 Н ЯМР (300 МГц, СDСl3) 7,43-7,37 (m, 2Н), 7,37-7,30 (m, 2Н), 7,24-7,19 (m, 1Н), 2,98 (s, 3Н), 2,12-1,88 (m, 4Н), 1,88-1,45 (m, 8Н). с) 1-Феніл-циклогептанкарбонова кислота O OH 35 40 Калій (2,62 г) та натрій (0,52 г) нагрівали разом при 120С у мінеральній оливі під азотом протягом 30 хвилин та тоді охолоджували до кімнатної температури. Оливу видаляли та заміщали етером (100 мл) та додавали 1-метокси-1-феніл-циклогептан (Приклад 1b) (4,9 г) та реакційну суміш перемішували під азотом протягом ночі при кімнатній температурі. Реакційну суміш охолоджували до -78С та додавали при перемішуванні твердий карбон діоксид (~20 г). Реакційній суміші давали нагрітися до кімнатної температури та додавали обережно воду (150 мл) під азотом. Водний шар відокремлювали, нейтралізували концентрованою хлоридною 15 UA 99521 C2 5 кислотою та екстрагували діетил-етером (150 мл). Органічний шар сушили (МgSО 4) та випарювали, отримуючи підзаголовну сполуку (4,15 г) як оливу. 1 Н ЯМР (300 МГц, СDСl3) 7,40-7,20 (m, 5Н), 2,49-2,35 (m, 2Н), 2,16-2,03 (m, 2Н), 1,76-1,47 (m, 8Н). d) 1-Феніл-циклогептанкарбонової кислоти метил-естер O O 10 1-Феніл-циклогептанкарбонову кислоту (Приклад 1с) (4,15 г) гріли при кипінні під зворотним холодильником у метанолі (150 мл) та концентрованій хлоридній кислоті (5 мл) протягом 24 годин. Розчинник випарювали та залишок розчиняли в етері (100 мл), що промивали водою (100 мл), насиченим натрію гідрогенкарбонатом (50 мл) та водою (100 мл), сушили (МgSО 4) та випарювали, отримуючи підзаголовну сполуку (3,5 г) як оливу. 1 Н ЯМР (300 МГц, СDСl3) 7,37-7,18 (m, 5Н), 3,63 (s, 3Н), 2,47-2,35 (m, 2Н), 2,08-1,97 (m, 2Н), 1,70-1,48 (m, 8Н). е) 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер O N O 15 20 25 H 1-Феніл-циклогептанкарбонової кислоти метил-естер (Приклад 1d) (1,0 г) та (R)-хінуклідин-3ол (0,39 г) гріли при кипінні під зворотним холодильником у гептані (50 мл), що містить натрій (~5 мг) в апараті Дина-Старка протягом 24 годин. Гептан (20 мл) заміщали толуєном (20 мл) та гріли при кипінні під зворотним холодильником протягом 3 доби. Реакційну суміш розподіляли між водою (50 мл) та етером (50 мл) та етерний шар відокремлювали, сушили (МgSО 4) та випарювали. Сирий продукт очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / триетиламін (99/1), отримуючи заголовну сполуку як оливу (0,83 г). + m/е 328 [М+Н] 1 Н ЯМР (300 МГц, СDСl3) 7,35-7,27 (m, 4Н), 7,23-7,16 (m, 1Н), 4,78-4,71 (m, 1Н), 3,12 (ddd, 1Н), 2,79-2,32 (m, 7Н), 2,16-1,98 (m, 2Н), 1,91-1,80 (m, 1Н), 1,70-1,34 (m, 12Н). f) 2-Хлор-N-(6-метил-піридин-3-іл)-ацетамід H N Cl O 30 35 N Суміш 6-метилпіридин-3-аміну (1 г) та триетиламіну (2,2 мл) у сухому ТГФ (20 мл) перемішували та охолоджували до -60 °C. 2-Хлорацетилхлорид (1,567 г) додавали через шприц і перемішували суміш з утворенням жовтої суспензії. Суміш перемішували при -60 °C, доки аналіз не показав повного зникнення вихідного матеріалу. Реакційну суспензію виливали у воду та продукти екстрагували етилацетатом (2 × 150 мл). Комбіновані органічні екстракти сушили безводним магнію сульфатом та концентрували до сухого стану. Сирий коричневий твердий матеріал перекристалізовували з етеру, отримуючи підзаголовну сполуку (700 мг). 1 Н ЯМР (400 МГц, ДМСО-D6) 10,40 (1Н, s), 8,60 (1Н, d), 7,91 (1Н, dd), 7,22 (1Н, d), 4,27 (2Н, s), 2,42 (3Н, s). Приклад 1: (R)-1-[(6-Метил-піридин-3-ілкарбамоїл)-метил]-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан хлорид 16 UA 99521 C2 ClO H N + N O O N H 5 10 15 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 1е) (52 мг) розчиняли в ацетонітрилі (2 мл) та додавали 2-хлор-N-(6-метилпіридин-3-іл)ацетамід (Приклад 1f) (29 мг). Реакційну суміш перемішували протягом 10 діб та розбавляли етилацетатом (4 мл) та ізогексаном (14 мл). Суміш залишали стояти протягом 5 діб, утворені кристали відокремлювали та промивали діетил-етером (0,5 мл), отримуючи заголовну сполуку як твердий матеріал (36 мг). + m/е 476 [М] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,33 (s, 1Н), 8,70 (d, 1Н), 7,91 (dd, 1Н), 7,38-7,30 (m, 4Н), 7,27 (d, 1Н), 7,28-7,20 (m, 1Н), 5,16-5,07 (m, 1Н), 4,36 (d, 1Н), 4,31 (d, 1Н), 4,16-4,07 (m, 1Н), 3,72-3,54 (m, 4Н), 3,44-3,34 (m, 2Н), 2,44 (s, 3Н), 2,42-2,28 (m, 2Н), 2,22-2,10 (m, 2Н), 2,01-1,86 (m, 3Н), 1,83-1,71 (m, 1Н), 1,69-1,41 (m, 8Н). Приклад 2: (R)-1-[(6-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(6-метил-піразин-2-іл)-ацетамід H N Br N O 20 25 N 6-Метил-піразин-2-іламін (150 мг) та калію карбонат (571 мг) додавали до дихлорметану (25 мл). 2-Бромацетилбромід (0,120 мл) додавали до суспензії при перемішуванні. Реакційну суміш перемішували протягом ночі і перемішуючи додавали воду (0,1 мл). Наступну кількість калію карбонату (571 мг), 2-бромацетилброміду (0,120 мл) та води (0,1 мл) додавали протягом 2 годин, доки не настало завершення реакції. Реакційну суміш розбавляли водою (100 мл), обережно підкислювали хлоридною кислотою та екстрагували дихлорметаном (2 × 50 мл), сушили та випарювали, отримуючи підзаголовну сполуку, що застосовували сирою (365 мг). 1 Н ЯМР (400 МГц, СDСl3) 9,45 (s, 1Н), 9,37 (s, 1Н), 8,33 (s, 1Н), 4,05 (s, 2Н), 2,51 (s, 3Н). Приклад 2: (R)-1-[(6-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N N O O N H 30 35 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 1е) (70 мг) та 2-бром-N-(6-метилпіразин-2-іл)ацетамід (Приклад 2а) (49,2 мг) розчиняли в ацетонітрилі (1 мл) та залишали на ніч. Кристали відокремлювалися при стоянні та їх фільтрували та промивали ацетонітрилом (2 × 1 мл), етилацетатом (2 × 3 мл) та діетил-етером (2 × 3 мл) та сушили, отримуючи заголовну сполуку (24 мг). + m/е 477 [М] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,33 (s, 1Н), 9,09 (s, 1Н), 8,37 (s, 1Н), 7,38-7,31 (m, 4Н), 7,277,22 (m, 1Н), 5,15-5,09 (m, 1Н), 4,36-4,25 (m, 2Н), 4,16-4,07 (m, 1Н), 3,68-3,56 (m, 4Н), 3,46-3,33 (m, 1Н), 2,47 (s, 3Н), 2,42-2,29 (m, 2Н), 2,24-2,11 (m, 2Н), 2,04-1,87 (m, 3Н), 1,83-1,73 (m, 1Н), 1,68-1,45 (m, 9Н). 17 UA 99521 C2 Приклад 3: (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-[(6-трифлуорметил-піридазин-3ілкарбамоїл)-метил]-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(6-трифлуорметил-піридазин-3-іл)-ацетамід H N Br N N O 5 10 15 CF3 6-Трифлуорметил-піридазин-3-іламін (0,042 г) (отримувано способом, подібним описаному у WО2007048779) розчиняли у дихлорметані (40 мл) та перемішували з калію карбонатом (0,214 г). 2-Бромацетилбромід (0,12 мл) додавали та перемішування продовжували протягом 1,5 годин. Воду (0,24 мл) додавали та реакційну суміш перемішували протягом 1,5 годин, після чого вод (40 мл) додавали та реакційну суміш перемішували протягом ще 1,5 годин. Дихлорметан відокремлювали, сушили (МgSО4) та випарювали, отримуючи підзаголовну сполуку як білий твердий матеріал (0,053 г). + m/е 284/286 [М+Н] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,04 (s, 1Н), 8,79 (d, 1Н), 7,91 (d, 1Н), 4,31 (s, 2Н). Приклад 3: (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-[(6-трифлуорметил-піридазин-3ілкарбамоїл)-метил]-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N O N N O CF3 H 20 25 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 1е) (61,1 мг) та 2-бром-N-(6-трифлуорметил-піридазин-3-іл)-ацетамід (Приклад 3а) (53,0 мг) розчиняли в ацетонітрилі (2 мл) та залишали протягом ночі. Розчинник випарювали та продукт очищали хроматографією на колонці на силікагелі, елюючи сумішшю 10 % метанолу у дихлорметані, отримуючи заголовну сполуку (107 мг). + m/е 531 [М] 1 Н ЯМР (400 МГц, ДМСО-D6) 12,17 (s, 1Н), 8,50 (d, 1Н), 8,36 (d, 1Н), 7,40-7,32 (m, 4Н), 7,287,23 (m, 1Н), 5,17-5,10 (m, 1Н), 4,57-4,42 (m, 2Н), 4,22-4,14 (m, 1Н), 3,76-3,61 (m, 4Н), 3,47 (dd, 1Н), 2,43-2,30 (m, 2Н), 2,25-2,12 (m, 2Н), 2,07-1,88 (m, 3Н), 1,86-1,73 (m, 1Н), 1,72-1,44 (m, 9Н). Приклад 4: (R)-1-(Бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) N-Бензо[d]ізоксазол-3-іл-2-хлор-ацетамід H N Cl O 30 35 N O До суміші бензо[d]ізоксазол-3-іламіну (1 г) та цезію карбонату (2,42 г) у сухому ДМФ (20 мл), перемішували при кімнатній температурі, додавали бромацетилхлорид (0,62 мл) додаванням краплями. Після перемішування суміш протягом 8 годин, реакційну суміш виливали у воду (100 мл) та продукти екстрагували в етер (2 × 200 мл). Комбіновані екстракти сушили безводним магнію сульфатом та концентрували до сухого стану. Сирий продукт очищали на силікагелі, застосовуючи суміш етер / ізогексан (4 / 6), отримуючи підзаголовну сполуку як безбарвний твердий матеріал (0,5 г). + m/е 210 [М+Н] Приклад 4: (R)-1-(Бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-фенілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан хлорид 18 UA 99521 C2 ClO H N + N O O N O H 5 10 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 1е) (114 мг) та N-бензо[d]ізоксазол-3-іл-2-хлор-ацетамід (Приклад 4а) (89 мг) розчиняли в ацетонітрилі (10 мл) та залишали на один тиждень. Утворені кристали відфільтровували та промивали діетил-етером (3 × 10 мл), отримуючи заголовну сполуку як твердий матеріал (120 мг). + m/е 502 [М] 1 Н ЯМР (400 МГц, ДМСО-D6) 12,15 (s, 1Н), 8,16 (d, 1Н), 7,74 (d, 1Н), 7,72-7,67 (m, 1Н), 7,447,39 (m, 1Н), 7,38-7,30 (m, 4Н), 7,27-7,19 (m, 1Н), 5,18-5,11 (m, 1Н), 4,63-4,46 (m, 2Н), 4,17 (ddd, 1Н), 3,76-3,61 (m, 4Н), 3,49 (dd, 1Н), 2,43-2,29 (m, 2Н), 2,24-2,12 (m, 2Н), 2,03-1,89 (m, 3Н), 1,861,74 (m, 1Н), 1,70-1,44 (m, 9Н). Приклад 5: (R)-1-(Піридазин-3-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бут-3-еніл-2-тіофен-2-іл-гекс-5-єнової кислоти етил-естер O S 15 20 25 30 O Етил 2-(тіофен-2-іл)ацетат (2,35 г) розчиняли у тетрагідрофурані (30 мл) та охолоджували до -78 °C. Літію біс(триметилсиліл)амід (2,31 г) у ТГФ (1М розчин, 13,8 мл) додавали та розчин перемішували протягом 30 хвилин. 4-Бром-бут-1-ен (1,4 мл) додавали та реакційній суміші давали нагрітися до кімнатної температури та перемішували протягом 1 години. Реакційну суміш знов охолоджували до -78 °C та додавали літію біс(триметилсиліл)амід (2,31 г) у ТГФ (1М розчин, 13,8 мл) та розчин перемішували протягом 30 хвилин. 4-Бром-бут-1-ен (1,4 мл) додавали та реакційній суміші давали нагрітися до кімнатної температури та тримали протягом ночі. ВЕРХ-МС-аналіз визначав, що реакція була незавершеною і реакційну суміш знов охолоджували до -78 °C та ще додавали аліквоти літію біс(триметилсиліл)аміду (1М розчин, 10 мл) та 4-бром-бут-1-ену (1,0 мл) способом, описаним вище. Після перемішування протягом ще 2 годин, воду (30 мл) додавали та реакційну суміш екстрагували діетил-етером (2 × 60 мл). Комбіновані органічні екстракти сушили (МgSО 4) та випарювали. Утворену оливу очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / ізогексан (1/99), отримуючи підзаголовну сполуку (3,18 г). 1 Н ЯМР (400 МГц, ДМСО-D6) 7,21 (dd, 1Н), 6,97-6,94 (m, 2Н), 5,79 (ddt, 2Н), 5,01 (dq, 2Н), 4,95 (dq, 2Н), 4,17 (q, 2Н), 2,22-2,08 (m, 4Н), 2,00-1,85 (m, 4Н), 1,24 (t, 3Н). b) 1-Тіофен-2-іл-циклогепт-4-енкарбонової кислоти етил-естер O S 35 O До 2-бут-3-еніл-2-тіофен-2-іл-гекс-5-єнової кислоти етил-естеру (Приклад 5а) (3,18 г) у дихлорметані (100 мл) додавали каталізатор Грабса (2nd Gеnеrаtіоn, Sіgmа-Аldrісh Соmраnу Ltd) (0,100 г). Суміш нагрівали при кипінні під зворотним холодильником під азотом. Через 20 годин суміші давали охолонути до кімнатної температури та випарювали до оливи. Очистка 19 UA 99521 C2 5 хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / ізогексан (10:90), отримуючи підзаголовну сполуку (2,60 г) як забарвлену оливу. 1 Н ЯМР (400 МГц, ДМСО-D6) 7,19 (dd, 1Н), 6,98-6,92 (m, 2Н), 5,72 (t, 2Н), 4,15 (q, 2Н), 2,662,59 (m, 2Н), 2,25-2,14 (m, 6Н), 1,21 (t, 3Н). с) 1-Тіофен-2-іл-циклогептанкарбонової кислоти етил-естер O O S 10 15 1-Тіофен-2-іл-циклогепт-4-енкарбонової кислоти етил-естер (Приклад 5b) (2,86 г) розчиняли в етанолі (30 мл) та трис(трифенілфосфін)родій(І) хлорид (0,100 г) додавали. Реакційну суміш перемішували швидко при 5 атмосферах водню протягом ночі. Ще додавали трис(трифенілфосфін)родій(І) хлорид (0,050 г) та реакційну суміш перемішували при 5 атмосферах водню протягом 3 доби. Робили третє додавання трис(трифенілфосфін)родій(І) хлориду (0,050 г) та реакційну суміш перемішували при 3 атмосферах водню протягом ночі. Вміст випарювали до сухого стану та очищали на силікагелі, елюючи сумішшю етилацетат / ізогексан (5 / 95), отримуючи підзаголовну сполуку (2,500 г), як прозору майже безбарвну оливу. + m/е 253 [М+Н ] 1 Н ЯМР (400 МГц, ДМСО-D6) 7,17 (dd, 1Н), 6,95-6,91 (m, 2Н), 4,13 (q, 2Н), 2,53 (dd, 2Н), 2,14-2,03 (m, 2Н), 1,70-1,50 (m, 8Н), 1,20 (t, 3Н). d) 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер O N O S H 20 25 30 1-Тіофен-2-іл-циклогептанкарбонової кислоти етил-естер (Приклад 5с) (2,5 г) та (R)хінуклідин-3-ол (2,08 г) розчиняли у толуєні (350 мл) та додавали під азотом натрію гідрид (0,1 г). Суміш нагрівали при кипінні під зворотним холодильником протягом 20 годин, після чого толуєн обережно відганяли, отримуючи ~100 мл, що охолоджували та промивали водою (100 мл), сушили (МgSО4) та випарювали. Сирий продукт очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / триетиламін (99/1), отримуючи підзаголовну сполуку (2,84 г). + m/е 334 [М+Н ] 1 Н ЯМР (400 МГц, СDСl3) 7,18 (t, 1Н), 6,95-6,92 (m, 2Н), 4,77-4,72 (m, 1Н), 3,14 (ddd, 1Н), 2,83-2,64 (m, 4Н), 2,59-2,50 (m, 3Н), 2,18-2,08 (m, 2Н), 1,95-1,90 (m, 1Н), 1,71-1,44 (m, 11Н), 1,341,23 (m, 1Н). е) 2-Бром-N-піридазин-3-іл-ацетамід H N Br N N O 35 До суспензії піридазин-3-іламіну (2,7 г) та діізопропілетиламіну (6,3 мл) у дихлорметані (100 мл) при 0 °C додавали краплями бромоцтовий ангідрид (9,0 г) у дихлорметані (10 мл). Суміш перемішували при 0 °C протягом 0,5 годин та тоді їй давали нагрітися до кімнатної температури. Утворену суспензію фільтрували, промивали дихлорметаном та сушили, отримуючи підзаголовну сполуку як твердий матеріал (2,0 г). 1 Н ЯМР (400 МГц, ДМСО-D6) 11,51 (s, 1Н), 9,00 (dd, 1Н), 8,28 (dd, 1Н), 7,74-7,68 (m, 1Н), 4,15 (s, 2Н). 20 UA 99521 C2 Приклад 5: (R)-1-(Піридазин-3-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N O S N N O H 5 10 15 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (80 мг) та 2-бром-N-піридазин-3-іл-ацетамід (Приклад 5е) (52 мг) розчиняли в ацетонітрилі (3 мл) та перемішували протягом ночі. Етилацетат (9 мл) та ізогексан (4 мл) додавали та перемішували протягом ночі. Утворені кристали відфільтровували та тоді розтирали у порошок з етилацетатом, отримуючи заголовну сполуку (14 мг). + m/е 469 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,68 (s, 1Н), 9,05 (dd, 1Н), 8,25 (d, 1Н), 7,79 (dd, 1Н), 7,44 (dd, 1Н), 7,03 (dd, 1Н), 6,99 (dd, 1Н), 5,14-5,09 (m, 1Н), 4,37 (s, 2Н), 4,17-4,08 (m, 1Н), 3,76-3,57 (m, 4Н), 3,57-3,46 (m, 1Н), 2,48-2,42 (m, 1Н), 2,29-2,22 (m, 1Н), 2,21-2,11 (m, 1Н), 2,07-1,90 (m, 4Н), 1,90-1,80 (m, 1Н), 1,78-1,68 (m, 1Н), 1,66-1,46 (m, 8Н). Приклад 6: (R)-1-[(5-Метил-ізоксазол-3-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(5-метил-ізоксазол-3-іл)-ацетамід H N Br N O O 20 25 При перемішуванні до суспензії натрію гідрогенкарбонату (1,242 г) та 5-метил-ізоксазол-3іламіну (1,45 г) у дихлорметані (50 мл) додавали краплями 2-бромацетилбромід (1,28 мл). Реакційну суміш перемішували протягом ночі та тоді промивали водою (2 × 50 мл). Органічну фракцію відокремлювали, сушили магнію сульфатом та випарювали, отримуючи підзаголовну сполуку (279 мг). 1 Н ЯМР (400 МГц, ДМСО-D6) 11,32 (s, 1Н), 6,62 (s, 1Н), 4,06 (s, 2Н), 2,38 (s, 3Н). Приклад 6: (R)-1-[(5-Метил-ізоксазол-3-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N S O N O O H 30 35 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (68 мг) та 2-бром-N-(5-метил-ізоксазол-3-іл)-ацетамід (Приклад 6а) (45 мг) розчиняли в ацетонітрилі (2 мл) та перемішували протягом ночі. Етилацетат (10 мл) та ізогексан (9 мл) додавали та перемішували протягом ночі. Утворені кристали відфільтровували та промивали етилацетатом, отримуючи заголовну сполуку (82 мг). + m/е 472 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,55 (s, 1Н), 7,44 (dd, 1Н), 7,03 (dd, 1Н), 6,99 (dd, 1Н), 6,61 (s, 1Н), 5,13-5,08 (m, 1Н), 4,31 (d, 1Н), 4,26 (d, 1Н), 4,14-4,05 (m, 1Н), 3,72-3,55 (m, 4Н), 3,53-3,43 (m, 1Н), 2,54-2,42 (m, 1Н), 2,41 (d, 3Н), 2,27-2,22 (m, 1Н), 2,19-2,13 (m, 1Н), 2,07-1,90 (m, 4Н), 1,891,77 (m, 1Н), 1,77-1,65 (m, 1Н), 1,63-1,48 (m, 8Н). 21 UA 99521 C2 Приклад 7: (R)-1-[(3-Метил-ізоксазол-5-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(3-метил-ізоксазол-5-іл)-ацетамід H N Br O N O 5 10 15 3-Метил-ізоксазол-5-іламін (2,9 г) та калію карбонат (9,8 г) суспендували у дихлорметані (100 мл) при кімнатній температурі та додавали краплями2-бромацетилбромід (6 г). Суміш перемішували протягом ночі. Воду (0,3 мл) додавали разом з калію карбонатом (3 г) та реакційну суміш перемішували протягом ще 30 хвилин. Реакційну суміш виливали у воду (100 мл) та екстрагували дихлорметаном (2 × 50 мл). Комбіновані органічні екстракти сушили безводним магнію сульфатом та тоді випарювали у вакуумі. Сирий продукт очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / ізогексан (50:50), отримуючи підзаголовну сполуку (4,8 г). 1 Н ЯМР (300 МГц, СDСl3) 11,97 (s, 1Н), 6,16 (s, 1Н), 4,09 (s, 2Н), 2,19 (s, 3Н). Приклад 7: (R)-1-[(3-Метил-ізоксазол-5-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N O S O N O H 20 25 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (50 мг) та 2-бром-N-(3-метилізоксазол-5-іл)ацетамід (Приклад 7а) (32 мг) розчиняли в ацетонітрилі (2 мл) та залишали протягом ночі. Етилацетат (10 мл) та ізогексан (10 мл) додавали та кристали відфільтровували, промивали етилацетатом та сушили, отримуючи заголовну сполуку (37 мг). + m/е 472 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 12,21 (s, 1Н), 7,44 (dd, 1Н), 7,03 (dd, 1Н), 6,99 (dd, 1Н), 6,18 (s, 1Н), 5,15-5,07 (m, 1Н), 4,35 (d, 1Н), 4,30 (d, 1Н), 4,14-4,05 (m, 1Н), 3,73-3,54 (m, 4Н), 3,54-3,43 (m, 1Н), 3,17 (d, 1Н), 2,47-2,42 (m, 1Н), 2,27-2,20 (m, 1Н), 2,21 (s, 3Н), 2,19-2,12 (m, 1Н), 2,08-1,77 (m, 4Н), 1,77-1,65 (m, 1Н), 1,65-1,46 (m, 8Н). Приклад 8: (R)-1-[(3-Флуор-фенілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(3-флуор-феніл)-ацетамід H N Br F O 30 35 До суспензії натрію гідрогенкарбонату (1 г) та 3-флуораніліну (0,46 г) у дихлорметані (100 мл) додавали краплями 2-бромацетилбромід (0,36 мл). Після перемішування протягом ночі реакційну суміш промивали водою, сушили магнію сульфатом та випарювали, отримуючи підзаголовну сполуку (1,07 г). + m/е 232 [М+Н ] 1 Н ЯМР (300 МГц, СDСl3) 8,14 (s, 1Н), 7,50 (dt, 1Н), 7,31 (td, 1Н), 7,18 (ddd, 1Н), 6,87 (tdd, 1Н), 4,03 (s, 2Н). Приклад 8: (R)-1-[(3-Флуор-фенілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід 22 UA 99521 C2 BrO H N + N O S F O H 5 10 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (96 мг) та 2-бром-N-(3-флуор-феніл)-ацетамід (Приклад 8а) (67 мг) розчиняли в ацетонітрилі (2 мл) та залишали протягом ночі. Діетил-етер (10 мл) та ізогексан (8 мл) додавали та суміш залишали протягом ночі. Утворені кристали відфільтровували та промивали діетилетером, отримуючи заголовну сполуку (90 мг). + m/е 485 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 10,84 (s, 1Н), 7,58 (dt, 1Н), 7,46-7,39 (m, 2Н), 7,33-7,29 (m, 1Н), 7,04 (dd, 1Н), 7,02-6,96 (m, 2Н), 5,15-5,10 (m, 1Н), 4,33-4,24 (m, 2Н), 4,17-4,07 (m, 1Н), 3,77-3,58 (m, 4Н), 3,51 (dd, 1Н), 2,56-2,44 (m, 1Н), 2,28-2,22 (m, 1Н), 2,21-2,12 (m, 1Н), 2,08-1,70 (m, 6Н), 1,66-1,47 (m, 8Н). Приклад 9: (R)-1-[(5-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-(5-метил-піразин-2-іл)-ацетамід H N Br N O 15 20 N До суміші 5-метил-піразин-2-іламіну та цезію карбонату (11,2 г) у сухому ДМФ (30 мл) додавали краплями бромацетилбромід (2,89 г) та суміш перемішували при кімнатній температурі протягом 2 годин. Воду (200 мл) додавали та суміш екстрагували етилацетатом (2 × 100 мл) та сушили безводним магнію сульфатом. Концентрація екстракту до ~50 мл та додавання ізогексану (100 мл) дали підзаголовну сполуку як твердий матеріал (1,64 г). 1 Н ЯМР (400 МГц, ДМСО-D6) 11,06 (1Н, s), 9,17 (1Н, s), 8,31 (1Н, d), 4,16 (2Н, s), 2,46 (3Н, s). Приклад 9: (R)-1-[(5-Метил-піразин-2-ілкарбамоїл)-метил]-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан бромід BrO H N + N S 25 30 35 O O N N H 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (48 мг) розчиняли в ацетонітрилі (2 мл) та додавали 2-бром-N-(5-метил-піразин-2іл)-ацетамід (Приклад 9а) (33 мг). Після перемішування протягом 1 тижня додавали діетил-етер (8 мл) та ізогексан (5 мл). Кристали збирали фільтруванням, промивали етилацетатом (2 × 4 мл) та сушили, отримуючи заголовну сполуку (26 мг). + m/е 483 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 11,26 (s, 1Н), 9,15 (s, 1Н), 8,36 (s, 1Н), 7,44 (dd, 1Н), 7,04 (dd, 1Н), 6,99 (dd, 1Н), 5,15-5,08 (m, 1Н), 4,33 (s, 2Н), 4,13 (ddd, 1Н), 3,75-3,57 (m, 4Н), 3,56-3,46 (m, 1Н), 2,48 (s, 3Н), 2,50-2,44 (m, 1Н), 2,28-2,22 (m, 1Н), 2,20-2,11 (m, 1Н), 2,08-1,90 (m, 4Н), 1,901,80 (m, 1Н), 1,79-1,69 (m, 1Н), 1,64-1,48 (m, 8Н). Приклад 10: (R)-1-(Бензо[d]ізоксазол-3-ілкарбамоїлметил)-3-(1-тіофен-2-ілциклогептанкарбонілокси)-1-азоній-біцикло[2,2,2]октан хлорид 23 UA 99521 C2 ClO H N + N O S N O O H 5 10 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (71 мг) та N-бензо[d]ізоксазол-3-іл-2-хлор-ацетамід (Приклад 4а) (54 мг) розчиняли в ацетонітрилі (10 мл) та залишали на 6 діб. Утворені кристали відфільтровували та промивали діетил-етером (3 × 10 мл), отримуючи заголовну сполуку (82 мг). + m/е 509 [М ] 1 Н ЯМР (400 МГц, ДМСО-D6) 12,16 (s, 1Н), 8,17 (d, 1Н), 7,74 (d, 1Н), 7,72-7,67 (m, 1Н), 7,447,39 (m, 2Н), 7,04 (dd, 1Н), 6,98 (dd, 1Н), 5,16-5,11 (m, 1Н), 4,64-4,50 (m, 2Н), 4,21-4,13 (m, 1Н), 3,82-3,64 (m, 4Н), 3,59 (dd, 1Н), 2,56-2,44 (m, 2Н), 2,29-2,22 (m, 1Н), 2,22-2,13 (m, 1Н), 2,08-1,89 (m, 3Н), 1,89-1,81 (m, 1Н), 1,80-1,69 (m, 1Н), 1,64-1,47 (m, 8Н). Приклад 11: (R)-1-(Піразин-2-ілкарбамоїлметил)-3-(1-тіофен-2-іл-циклогептанкарбонілокси)1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-піразин-2-іл-ацетамід H N Br N O 15 20 N При перемішуванні до суспензії піразин-2-іламіну (1,87 г) та калію карбонату (8,19 г) у дихлорметані (25 мл) додавали краплями 2-бромацетилбромід (1,72 мл). Реакційну суміш перемішували протягом ночі та тоді промивали водою (2 × 50 мл). Органічну фазу відокремлювали, сушили магнію сульфатом та випарювали, отримуючи підзаголовну сполуку (0,70 г). 1 Н ЯМР (400 МГц, СDСl3) 9,51 (d, 1Н), 8,63 (s, 1Н), 8,42 (d, 1Н), 8,30 (dd, 1Н), 4,06 (s, 2Н). Приклад 11: (R)-1-(Піразин-2-ілкарбамоїлметил)-3-(1-тіофен-2-іл-циклогептанкарбонілокси)1-азоній-біцикло[2,2,2]октан бромід BrO H N + N S O O N N H 25 30 35 1-Тіофен-2-іл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 5d) (116 мг) та 2-бром-N-піразин-2-іл-ацетамід (Приклад 11а) (75 мг) розчиняли в ацетонітрилі (2 мл) та залишали протягом ночі. Діетил-етер (10 мл) та ізогексан (8 мл) додавали та суміш залишали на ніч. Утворені кристали відфільтровували та промивали діетил-етером, отримуючи заголовну сполуку (117 мг). + m/е 469 [М ] 1Н ЯМР (400 МГц, ДМСО-D6) 11,38 (s, 1Н), 9,28 (s, 1Н), 8,50-8,45 (m, 2Н), 7,44 (dd, 1Н), 7,04 (dd, 1Н), 6,99 (dd, 1Н), 5,15-5,09 (m, 1Н), 4,36 (s, 2Н), 4,18-4,08 (m, 1Н), 3,76-3,58 (m, 4Н), 3,583,46 (m, 1Н), 3,33-3,29 (m, 1Н), 2,55-2,43 (m, 1Н), 2,29-2,22 (m, 1Н), 2,21-2,12 (m, 1Н), 2,08-1,88 (m, 3Н), 1,88-1,79 (m, 1Н), 1,79-1,72 (m, 1Н), 1,64-1,48 (m, 8Н). Приклад 12: (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(піразин-2ілкарбамоїлметил)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бут-3-еніл-2-(3-флуор-феніл)-гекс-5-єнової кислоти метил-естер 24 UA 99521 C2 O F O 5 10 15 (3-Флуор-феніл)-оцтової кислоти метил-естер (4,30 г) розчиняли у тетрагідрофурані (20 мл) та охолоджували до -78 °C. Літію біс(триметилсиліл)амід (25,6 мл, 1М ТГФ розчин) додавали та розчин перемішували протягом 30 хвилин. 4-Бром-бут-1-ен (2,60 мл) додавали та реакційній суміші давали нагрітися до кімнатної температури та перемішували протягом години. Реакційну суміш знов охолоджували до -78 °C. Літію біс(триметилсиліл)амід (25,6 мл, 1М ТГФ розчин) додавали та розчин перемішували протягом 30 хвилин. 4-Бром-1-бутен (2,60 мл) додавали та реакційній суміші давали нагрітися до кімнатної температури та перемішували протягом години. Вміст знов охолоджували до -78 °C та наступні аліквоти літію біс(триметилсиліл)аміду (25,6 мл, 1М ТГФ розчин) та 4-бром-1-бутену (2,60 мл) додавали способом, описаним вище. Після перемішування протягом ночі додавали воду (20 мл) та реакційну суміш екстрагували діетилетером (2 × 60 мл). Комбіновані органічні екстракти сушили магнію сульфатом та випарювали. Утворену рідину очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / ізогексан (1 / 99), отримуючи підзаголовну сполуку (5,0 г). + m/е 277 [М+Н] b) 1-(3-Флуор-феніл)-циклогепт-4-енкарбонової кислоти метил-естер O F O 20 25 До 2-бут-3-еніл-2-(3-флуор-феніл)-гекс-5-єнової кислоти метил-естеру (Приклад 12а) (5,0 г) у дихлорметані (100 мл) додавали каталізатор Грабса (2nd Gеnеrаtіоn, Sіgmа-Аldrісh Соmраnу Ltd) (0,05 г). Суміш нагрівали при кипінні під зворотним холодильником під азотом. Через 20 годин реакційну суміш охолоджували до кімнатної температури, випарювали до оливи та очищали хроматографією на колонці на силікагелі, елюючи сумішшю етилацетат / ізогексан (5 / 95), отримуючи оливу. Аналіз продукту показував, що значні кількості вихідного матеріалу були у суміші, і суміш піддавали повторно реакції та очистці, як вище, отримуючи підзаголовну сполуку як забарвлену оливу (3,60 г). + m/е 249 [М+Н] с) 1-(3-Флуор-феніл)-циклогептанкарбонової кислоти метил-естер O F O 30 1-(3-Флуор-феніл)-циклогепт-4-енкарбонової кислоти метил-естер (Приклад 12b) (1,09 г) розчиняли у метанолі (20 мл), додавали паладій на вугіллі (50 мг) та суміш перемішували під 4 атм водню протягом ночі. Розчин фільтрували та випарювали, отримуючи підзаголовну сполуку (1,09 г). + m/е 251 [М+Н] d) 1-(3-Флуор-феніл)-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер 25 UA 99521 C2 O F N O H 5 10 15 1-(3-Флуор-феніл)-циклогептанкарбонової кислоти метил-естер (Приклад 12с) (0,280 г) розчиняли у толуєні (100 мл) та додавали (R)-хінуклідин-3-ол (0,320 г). Толуєн (10 мл) відганяли в апараті Дина-Старка та після охолодження додавали натрію гідрид (10 мг). Реакційну суміш гріли при кипінні під зворотним холодильником в апараті Дина-Старка протягом 4 годин, після чого додавали натрію гідрид (10 мг) та реакційну суміш нагрівали при кипінні під зворотним холодильником протягом ще 4 годин. Після охолодження до кімнатної температури, толуєн промивали водою, сушили (МgSО4) та випарювали. Залишок очищали хроматографією на колонці, елюючи сумішшю етилацетат / ізогексан / триетиламін (50 / 50 / 1), тоді етилацетат / триетиламін (99 / 1), отримуючи підзаголовну сполуку (0,200 г). + m/е 346 [М+Н] 1 Н ЯМР (399,824 МГц, СDСl3) 7,26 (td, 1Н), 7,10-7,07 (m, 1Н), 7,04 (dd, 1Н), 6,90 (ddd, 1Н), 4,78-4,73 (m, 1Н), 3,14 (ddd, 1Н), 2,79-2,66 (m, 3Н), 2,66-2,56 (m, 1Н), 2,53-2,46 (m, 1Н), 2,46-2,36 (m, 2Н), 2,13-1,99 (m, 2Н), 1,90-1,85 (m, 1Н), 1,73-1,40 (m, 11Н), 1,29-1,18 (m, 1Н). Приклад 12: (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(піразин-2ілкарбамоїлметил)-1-азоній-біцикло[2,2,2]октан бромід BrO F H N + N O O N N H 20 25 30 1-(3-Флуор-феніл)-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 12d) (0,100 г) розчиняли в ацетонітрилі (8 мл) та додавали 2-бром-N-піразин-2-ілацетамід (Приклад 11а) (0,05 г). Реакційну суміш перемішували протягом 3 діб, розбавляли діетил-етером (8 мл), перемішували ще 10 хвилин, утворений твердий матеріал фільтрували та промивали діетил-етером (3 × 8 мл), отримуючи твердий матеріал, що перекристалізовували з гарячого бутанону (8 мл), отримуючи заголовну сполуку як твердий матеріал (0,081 г). + m/е 481 [М ] 1 Н ЯМР (399,826 МГц, ДМСО-D6) 11,42 (s, 1Н), 9,28 (s, 1Н), 8,49-8,45 (m, 2Н), 7,40 (td, 1Н), 7,19-7,12 (m, 2Н), 7,09 (td, 1Н), 5,17-5,10 (m, 1Н), 4,40-4,30 (m, 2Н), 4,16-4,07 (m, 1Н), 3,71-3,57 (m, 4Н), 3,52-3,41 (m, 1Н), 2,43-2,27 (m, 2Н), 2,26-2,19 (m, 1Н), 2,19-2,09 (m, 1Н), 2,05-1,87 (m, 3Н), 1,86-1,76 (m, 1Н), 1,71-1,46 (m, 9Н). Приклад 13: (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(ізоксазол-3ілкарбамоїлметил)-1-азоній-біцикло[2,2,2]октан бромід а) 2-Бром-N-ізоксазол-3-іл-ацетамід H N Br N O O 35 Ізоксазол-3-іламін (1,14 г) розчиняли у дихлорметані (50 мл) та додавали калію карбонат (3,74 г). Бромацетилхлорид (1,12 мл) додавали повільно при перемішуванні та суспензію перемішували протягом ночі. Реакційну суміш промивали водою (2 × 50 мл), сушили та випарювали. Продукт перекристалізовували з суміші дихлорметан / ізогексан, отримуючи підзаголовну сполуку (2,3 г). 1 Н ЯМР (299,946 МГц, СDСl3) 8,94 (s, 1Н), 8,34 (s, 1Н), 7,06 (s, 1Н), 4,03 (s, 2Н). 26 UA 99521 C2 Приклад 13: (R)-3-[1-(3-Флуор-феніл)-циклогептанкарбонілокси]-1-(ізоксазол-3ілкарбамоїлметил)-1-азоній-біцикло[2,2,2]октан бромід BrO F H N + N O N O O H 5 10 15 1-(3-Флуор-феніл)-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер (Приклад 12d) (50 мг) та 2-бром-N-ізоксазол-3-іл-ацетамід (Приклад 13а) (30 мг) розчиняли в ацетонітрилі (4 мл) та перемішували протягом ночі. Розчин розбавляли діетил-етером (12 мл) та перемішували протягом ночі. Утворені кристали відфільтровували, промивали етером (3 × 10 мл) та сушили, отримуючи заголовну сполуку як твердий матеріал (48 мг). + m/е 470 [М ] 1 Н ЯМР (399,826 МГц, ДМСО-D6) 11,69 (s, 1Н), 8,90 (d, 1Н), 7,40 (td, 1Н), 7,18-7,07 (m, 3Н), 6,91 (d, 1Н), 5,16-5,10 (m, 1Н), 4,31 (d, 1Н), 4,25 (d, 1Н), 4,09 (ddd, 1Н), 3,68-3,53 (m, 4Н), 3,43 (dd, 1Н), 2,42-2,27 (m, 2Н), 2,25-2,19 (m, 1Н), 2,18-2,09 (m, 1Н), 2,04-1,88 (m, 3Н), 1,85-1,75 (m, 1Н), 1,69-1,51 (m, 9Н). Приклад 14: (R)-3-(1-Феніл-циклогептанкарбонілокси)-1-(піридин-2-ілкарбамоїлметил)-1азоній-біцикло[2,2,2]октан хлорид а) Циклогептил-феніл-метанон O 20 25 30 35 Фенілмагнію бромід (3,0М розчин у діетил-етері) (271 мл), додавали краплями при перемішуванні до розчину циклогептанкарбонітрилу (50 г) у 229 мл діетил-етеру під азотом при такій швидкості, щоб було обережне кипіння під зворотним холодильником. Реакційну суміш тоді нагрівали при кипінні під зворотним холодильником протягом 3 годин. ТШХ показала відсутність вихідного матеріалу у реакційній суміші. Реакційній суміші давали охолонути до кімнатної температури та тримали під азотом протягом ночі. Реакційну суміш охолоджували до 0 °C та обробляли краплями 102 мл 4 Н НСl(водн.), тримаючи температуру нижче 20 °C. 4 Н сульфатну кислоту (203 мл) додавали краплями спочатку швидко та тоді більш повільно. Льодяну баню видаляли та діетил-етер відганяли. Реакційну суміш нагрівали при 80-90 °C протягом 3,5 годин і давали охолонути до кімнатної температури та тримали протягом ночі. Суміш розбавляли етером (приблизно 450 мл) та водою (100 мл). Шари відокремлювали та водний шар екстрагували етером (2 × 400 мл). Органічні шари поєднували та промивали насиченим водним натрію гідрогенкарбонатом (600 мл) та розсолом (600 мл), сушили безводним магнію сульфатом, фільтрували та випарювали, отримуючи підзаголовну сполуку як оранжеву рідину (86,5 г). 1 Н ЯМР (300 МГц, СDСl3) δ 7,96-7,91 (d, 2Н), 7,54-7,49 (m, 1Н), 7,48-7,40 (t, 2Н), 3,48-3,37 (m, 1Н), 1,98-1,88 (m, 2Н), 1,85-1,44 (m, 10Н). b) (1-Хлор-циклогептил)-феніл-метанон Cl O Сульфурилхлорид (210 мл) додавали краплями до нерозбавленого циклогептил-фенілметанону (Приклад 14а) (86,5 г) при 0 °C протягом приблизно 1 години. Виділення газу та екзотерм спостерігали. Внутрішню температуру тримали нижче 15 °C при додаванні та газ 27 UA 99521 C2 5 10 промивали пропусканням через 10,2М водний розчин NаОН. Реакційну суміш нагрівали при кипінні під зворотним холодильником протягом ночі. Реакційну суміш охолоджували до 0 °C та виливали повільно на лід (1 л) при перемішуванні. Шари відокремлювали та водний шар екстрагували етером (2 × 400 мл). Комбіновані органічні шари промивали водою (600 мл), насиченим водним натрію гідрогенкарбонатом (600 мл), та розсолом (600 мл), сушили безводним магнію сульфатом, фільтрували та випарювали, отримуючи підзаголовну сполуку як коричневу оливу (100 г). 1 Н ЯМР (400 МГц, СDСl3) δ 8,10-8,06 (d, 2Н), 7,52-7,46 (t, 1Н), 7,44-7,36 (t, 2Н), 2,50 (ddd, 2Н), 2,29 (ddd, 2Н), 1,84-1,73 (m, 2Н), 1,68-1,58 (m, 2Н), 1,58-1,43 (m, 4Н). с) 1-Феніл-циклогептанкарбонов кислота OH O 15 20 25 Розчин (1-хлор-циклогептил)-феніл-метанону (Приклад 14b) (100 г) у 750 мл діоксану було швидко оброблено краплями мутним розчином аргентум нітрату (137 г) у воді (85 мл), спричинюючи утворення осаду. Реакційну суміш нагрівали до 75 °C протягом 4,5 годин. Реакційну суміш охолоджували до кімнатної температури і фільтрували та концентрували до приблизно 200 мл. Воду (200 мл) та етер (300 мл) додавали та шари відокремлювали. Водний шар екстрагували етером (2 × 250 мл). Комбіновані органічні шари екстрагували 10 % водним натрію карбонатом (3 × 250 мл). Комбіновані основні екстракти нагрівали до 90 °C протягом 40 хвилин та тоді охолоджували до кімнатної температури та підкислювали концентрованою НСl (водн). Утворений коричневий твердий матеріал відфільтровували, промивали водою (х2) та сушили під вакуумом при 50 °C. Кристалізація з гарячого етанолу (40 мл) дала підзаголовну сполуку як блідо-коричневі кристали (9,83 г). 1 Н ЯМР (400 МГц, СD3ОD) δ 7,36-7,26 (m, 4Н), 7,21-7,15 (m, 1Н), 2,43-2,35 (m, 2Н), 2,07-1,98 (m, 2Н), 1,70-1,53 (m, 8Н). d) 1-Феніл-циклогептанкарбонової кислоти метил-естер O O 30 35 2,0 М розчин триметилсиліл діазометану (29,2 мл) додавали краплями до розчину 1-фенілциклогептанкарбонової кислоти (Приклад 14с) (9,8 г) у метанолі (85 мл) та толуєні (300 мл) під азотом. Через 45 хвилин реакційну суміш концентрували під вакуумом та сирий продукт очищали хроматографією на колонці, елюючи сумішшю 0-10 % етилацетат / циклогексан, отримуючи продукт як блідо-жовту оливу (9,25 г). 1 Н ЯМР (300 МГц, СD3ОD) δ 7,32-7,24 (m, 4Н), 7,21-7,12 (m, 1Н), 3,60 (s, 3Н), 2,43-2,32 (m, 2Н), 2,07-1,96 (m, 2Н), 1,65-1,58 (m, 8Н). е) 1-Феніл-циклогептанкарбонової кислоти (R)-(1-аза-біцикло[2,2,2]окт-3-іл)-естер 28
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinuclidine derivatives as m3 muscarinic receptor antagonists
Автори англійськоюFord, Rhonan, Lee, Mather, Andrew, Nigel, Mete, Antonio, Bull Richard James, Skidmore, Elizabeth, Anne
Назва патенту російськоюХинуклидин-производные как антагонисты мускариновых рецепторов м3
Автори російськоюФорд Ронан Ли, Метер Эндрю Найджел, Мете Антонио, Булл Ричард Джеймс, Скидмор Элизабет Анн
МПК / Мітки
МПК: A61K 31/439, C07D 453/02, A61P 11/00
Мітки: мускаринових, рецепторів, хінуклідин-похідні, антагоністи
Код посилання
<a href="https://ua.patents.su/71-99521-khinuklidin-pokhidni-yak-antagonisti-muskarinovikh-receptoriv-m3.html" target="_blank" rel="follow" title="База патентів України">Хінуклідин-похідні як антагоністи мускаринових рецепторів м3</a>
Попередній патент: Циркуляційний клапан
Наступний патент: Пристрій і спосіб передачі тепла
Випадковий патент: Спосіб одержання вафельного виробу під кондитерський продукт, що містить жир