Похідні бензоімідазолу, що використовуються як антипроліферативний засіб, фармацевтична композиція на їх основі
Номер патенту: 75055
Опубліковано: 15.03.2006
Автори: Луцціо Майкл Джозеф, Барт Уейн Ернест, Ліссікатос Джозеф Петер
Формула / Реферат
1. Сполука формули I
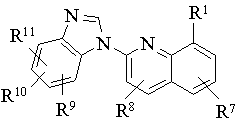
і її фармацевтично прийнятна сіль, проліки або сольват, де:
Χ означає СН або Ν;
R1 вибраний з: -(CR4R5)tC(O)OR3, -(CR4R5)tC(O)NR3R4, -(CR4R5)tOR3, (CR4R5)tC(O)(С3-С10циклоалкіл), -(CR4R5)C(O)(С6-С10арил), -(CR4R5)tC(O)(4-10-членний гетероциклічний радикал), -(CR4R5)t(С3-С10циклоалкіл), -(CR4R5)t(C6-C10арил) і -(CR4R5)t(4-10-членний гетероциклічний радикал), де кожний t незалежно означає ціле число від 0 до 5; вказані циклоалкільні, арильні і гетероциклічні R1 групи необов’язково конденсовані з бензольним кільцем, С5-С8циклоалкільною групою або 4-10-членною гетероциклічною групою; -(CR4R5)t фрагменти вказаних вище R1 груп необов’язково включають подвійний вуглець-вуглецевий або потрійний зв’язок, де t означає ціле число між 2 і 5; кожна з вказаних вище R1 груп необов’язково заміщена 1 або 2 групами, незалежно вибраними з: -NR3R4, -OR3, С1-C10алкілу, С2-С10алкенілу і С2-С10алкінілу, де вказані алкільні, алкенільні і алкінільні групи заміщені 1 або 2 групами, незалежно вибраними з -NR3R4 і -OR3; і вказані вище R1 групи необов’язково заміщені 1-3 R2 групами;
кожний R2 незалежно вибраний з: Н, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, оксо, галогену, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -OR3, -C(О)R3, -C(O)OR3, -NR4C(O)OR6, -OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR3R4, -S(О)j(СR4R5)m(С6-С10арил), -S(O)j(C1-C6алкіл), де j означає ціле число від 0 до 2, -(СR4R5)m(С6-С10арил), -O(СR4R5)m(С6-С10арил), -NR4(СR4R5)m(С6-С10арил), -O(СR4R5)m(4-10-члeнний гетероцикл), -NR4(СR4R5)m(4-10-членний гетероцикл), -(СR4R5)m(4-10-члeнний гетероциклічний радикал) і -(СR4R5)m(С3-С10циклоалкіл), де кожний m незалежно означає ціле число від 0 до 4; вказані алкільні, алкенільні і алкінільні групи необов’язково містять 1 або 2 гетерогрупи, вибрані з О, -S(O)j-, де j означає ціле число від 0 до 2, і -N(R3)-, за умови, що два атоми О, два атоми S або атом О і атом S не сполучені безпосередньо один з одним і, за умови, що атом О, атом S або атом N не сполучені безпосередньо з потрійним зв’язком або неароматичним подвійним зв’язком; вказані циклоалкільні, арильні і гетероциклічні R2 групи необов’язково конденсовані з С6-С10 арильною групою, C5-C8 циклоалкільною групою або 4-10-членною гетероциклічною групою; і вказані алкільні, циклоалкільні, арильні і гетероциклічні R2 групи необов’язково заміщені 1-5 замісниками, незалежно вибраними з: оксо (=O), галогену, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -С(O)NR3R4, -NR3R4, -OR3, С1-С10алкілу, -(СR4R5)m(С6-С10арил) і -(СR4R5)m(4-10-членний гетероциклічний радикал), де кожний m незалежно означає ціле число в межах від 0 до 4;
кожний R3 незалежно вибраний з: Н, С1-С10алкілу, -(СR4R5)m(С6-С10арил) і -(СR4R5)m(4-10-членний гетероциклічний радикал), де кожний m незалежно означає ціле число від 0 до 4; вказана алкільна група необов’язково включає 1 або 2 гетерогрупи, вибрані з: О, -S(O)j-, де j означає ціле число в межах від 0 до 2, і -N(R4)-, за умови, що два атоми О, два атоми S або атом О і атом S не сполучені безпосередньо один з одним; вказані циклоалкільні, арильні і гетероциклічні R3 групи необов’язково конденсовані з С6-С10арильною групою, C5-C8циклоалкільною групою або 4-10-членною гетероциклічною групою; і вказані вище R3 замісники, за винятком Н, необов’язково заміщені 1-5 замісниками, незалежно вибраними з: оксо, галогену, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -C(O)R4, -C(O)OR4, -OC(O)R4, -NR4C(O)R5, -C(О)NR4R5, -NR4R5, гідрокси, С1-С6алкілу і С1-С6алкокси;
кожний R4 і R5 незалежно означає Н або С1-С6алкіл;
або, коли R4 і R5 приєднані до одного і того ж атома вуглецю або азоту, R4 і R5 разом з вказаним вуглецем або азотом можуть утворювати 4-10-членний цикл, який може бути карбоциклічним або гетероциклічним;
кожний R6 вибраний із замісників, вказаних у визначенні R3, за тим винятком, що R6 не означає Н;
кожний R7, R8, R9, R10 і R11 незалежно вибраний із замісників, вказаних у визначенні R2.
2. Сполука за п. 1, де R1 означає С6-С10арил або 4-10-членний гетероциклічний радикал, де кожна з вказаних вище R1 груп заміщена 1 або 2 групами, незалежно вибраними з: - NR3R4, -OR3 і С1-С3алкілу, де вказані алкільні групи заміщені 1 або 2 групами, незалежно вибраними з: -NR3R4 і -OR3; і вказані вище R1 групи необов’язково заміщені 1-3 R2 групами;
кожний R2 незалежно вибраний з: Н, С1-С10алкілу, С3-С10циклоалкілу, оксо (=O), -OR3, -C(O)R3, -C(O)OR3, -NR4C(O)R3, -С(O)NR3R4, -NR3R4, -NR4SО2R6, -SO2NR3R4, -(СR4R5)m(4-10-членний гетероциклічний радикал) і (СR4R5)m(С3-С10циклоалкіл); і вказані алкільні групи необов’язково містять 1 або 2 гетерогрупи, вибрані з О, -S(O)j-, де j означає ціле число від 0 до 2, і -N(R3)-, за умови, що два атоми О, два атоми S або атом О і атом S не сполучені безпосередньо один з одним; і вказані алкільні і циклоалкільні R2 групи необов'язково заміщені 1-5 замісниками, незалежно вибраними з: оксо, ціано, трифторметилу, трифторметокси, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -OR3 і С1-С10алкілу, де кожний m незалежно означає ціле число в межах від 0 до 4.
3. Сполука за п. 1, де R1 означає піперидиніл, піперазиніл або феніл, де вказані R1 групи заміщені -NR3R4, оксо (=O), -OR3 і С1-С3алкілом, де вказані алкільні групи заміщені 1 або 2 групами, вибраними з -NR3R4 і -OR3; і вказані вище R1 групи необов’язково заміщені 1-3 R2 групами.
4. Сполука за п. 2, де вказані R1 групи заміщені -NR3R4, оксо (=O), OR3 або С1-С3алкілом, де вказані алкільні групи необов’язково заміщені -NR3R4.
5. Сполука за п. 1, де вказаний R1 означає феніл, заміщений піролідин-1-ілом, де вказаний піролідин-1-іл необов’язково заміщений 1-3 замісниками, незалежно вибраними з: оксо, ціано, трифторметилу, трифторметокси, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -NR4C(O)OR6, -NR4C(O)R3, -С(O)NR3R4, -NR3R4, -OR3 і C1-С10алкілу; і R11 означає -OR3.
6. Сполука за п. 5, де R1 означає 4-піролідин-1-ілметилфеніл, необов’язково заміщений 1-3 замісниками, незалежно вибраними з: оксо, ціано, трифторметилу, трифторметокси, -NR4SO2R6, SO2NR3R4, -C(O)R3, -С(O)OR3, -NR4C(O)OR6, -NR4С(O)R3, -C(O)NR3R4, -NR3R4, -OR3 і С1-С10алкілу; і R11 означає -OR3.
7. Сполука за п. 6, де R11 приєднаний в положенні 5 бензимідазольного фрагмента сполуки формули I і означає -OR3.
8. Сполука за п. 7, де R11 приєднаний в положенні 5 бензимідазольного фрагмента сполуки формули I і означає 2-метоксіетокси.
9. Сполука за п. 1, де R1 означає піролідин-1-іл або піперидин-1-іл, вказаний R1 необов’язково заміщений 1-3 замісниками, незалежно вибраними з: оксо, ціано, трифторметилу, трифторметокси, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -OR3 і С1-С10алкілу.
10. Сполука за п. 9, де R1 означає піролідин-1-іл або піперидин-1-іл, заміщений –NR3R4 і необов’язково заміщений 1-2 замісниками, незалежно вибраними з: оксо, ціано, трифторметилу, трифторметокси, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -OR3 і С1-С10алкілу; і R11 означає -OR3.
11. Сполука за п. 9 або п. 10, де R11 приєднаний в положенні 5 бензимідазольного фрагмента сполуки формули I і означає -OR3, і R9 і R10 обидва означають Н.
12. Сполука за п. 9 або п. 10, де R11 приєднаний в положенні 5 бензимідазольного фрагмента сполуки формули I і означає 2-метоксіетокси, і R9 і R10 обидва означають Н.
13. Сполука за п. 1, де R9 означає -C(O)R3, де R3 означає піролідин-1-іл або азетидин-1-іл, де вказані R3 групи необов'язково заміщені 1-3 замісниками, незалежно вибраними з: оксо, галогену, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -C(O)R4, -C(O)OR4, -OC(O)R4, -NR4C(O)R5, -С(O)NR4R5, -NR4R5, гідрокси, С1-С6 алкілу і С1-С6 алкокси.
14. Сполука за п. 1, вибрана з групи, що включає:
(1) [1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(2) 1-[8-(4-амінопінеридин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-ол;
(3) 1-{2-[5-(піридин-2-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(4) {1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(5) {4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}метиламін;
(6) {4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}диметиламін;
(7) циклопропіл-{4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}амін;
(8) трет-бутил-{4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}амін;
(9) 4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензиламін;
(10) 1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(11) {1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(12) 1-[2-(5-трифторметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(13) {4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}метиламін;
(14) циклопропіл-{4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}амін;
(15) трет-бутил-{4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}амін;
(16) (4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}диметиламін;
(17) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-он;
(18) 1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-он;
(19) 1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(20) трет-бутил-{1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}амін;
(21) {1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}метиламін;
(22) 2-(5-метоксибензоімідазол-1-іл)-8-(1-окса-6-аза-спіро[2.5]окт-6-ил)хінолін;
(23) 4-диметиламінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(24) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]-4-метиламінометилпіперидин-4-ол;
(25) 4-амінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(26) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піролідин-3-іламін;
(27) 1-(2-бензоімідазол-1-ілхінолін-8-іл)піперидин-4-іламін;
(28) 1-(2-імідазо[4,5-b]піридин-3-ілхінолін-8-іл)піперидин-4-іламін;
(29) 1-{2-[5-(4-метоксифеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(30) 1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(31) 1-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(32) 1-{2-[5-(3-амінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(33) 1-{2-[5-(2-диметиламіноетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(34) 1-{2-[5-(піридин-4-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(35) 1-[2-(5-бензилоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(36) 1-{2-[5-(піридин-3-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(37) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(38) етиловий ефір 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-карбонової кислоти;
(39) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-карбонова кислота;
(40) 4-диметиламінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(41) N-{1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}ацетамід;
(42) N-{1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}ацетамід;
(43) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ол;
(44) {1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}сечовина;
(45) 4-амінометил-1-{2-[5-(піридин-2-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ол;
(46) циклопропіл-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)амін;
(47) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)диметиламін;
(48) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метиламін;
(49) (1-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)диметиламін;
(50) {1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}метиламін;
(51) {1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(52) 2-аміно-N-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)ацетамід;
(53) (S)-2-аміно-N-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)пропіонамід;
(54) (R)-2-аміно-N-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)пропіонамід;
(55) 2-аміно-N-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)ізобутирамід;
(56) 1-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламіно)-2- метилпропан-2-ол;
(57) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)піридин-2-ілметиламін;
(58) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)піридин-3-ілметиламін;
(59) 4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}фенол;
(60) [2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}фенокси) етил]диметиламін;
(61) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-піперазин-1-ілхінолін;
(62) [2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етил]диметиламін;
(63) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піридин-2-ілметилпіперазин-1-іл)хінолін;
(64) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піридин-3-ілметилпіперазин-1-іл)хінолін;
(65) 2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)-2-метилпропан-1-он;
(66) (S)-2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)пропан-1-он;
(67) (R)-2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)пропан-1-он;
(68) 2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етанон;
(69) (1-аміноциклопропіл)-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)метанон;
(70) 2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етиламін;
(71) (R)-2-аміно-3-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)пропан-1-ол;
(72) 3-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}-3-азабіцикло[3.1.0]гекс-6-иламін;
(73) (S)-1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піролідин-3-іламін;
(74) (R)-1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піролідин-3-іламін;
(75) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-піридин-3-ілхінолін;
(76) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(6-метоксипіридин-3-іл)хінолін;
(77) метиловий ефір 4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензойної кислоти;
(78) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}-4-метилпіперидин-4-іламін;
(79) 1-[2-(6,7-дигідро-5,8-діокса-1,3-діазациклопента[b]нафталін-1-іл)хінолін-8-іл]піперидин-4-іламін;
(80) 2-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-ілоксі}етанол;
(81) 4-циклопропіламінометил-1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ол;
(82) диметиламід 1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-сульфонової кислоти;
(83) 1-[2-(6-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(84) 1-[2-(5,6-диметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(85) 2-диметиламін-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етанон;
(86) 1-[2-(5-бензилоксибензоімідазол-1-іл)хінолін-8-іл]-4-метилпіперидин-4-ол;
(87) (4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)диметиламін;
(88) (4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)метиламін;
(89) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-морфолін-4-ілметилфеніл)хінолін;
(90) 2-{4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензиламіно)етанол;
(91)4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензиламін;
(92) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(93) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(94) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(95) 1-{4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)цис-піролідин-3,4-діол;
(96) R,R-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)транс-піролідин-3,4-діол);
(97) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол;
(98) R-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол);
(99) 5-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол);
(100) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)азетидин-3-ол;
(101) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-[4-(4-метилпіперазин-1-ілметил)феніл]хінолін;
(102) трет-бутиловий ефір 4-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піперазин-1-карбонової кислоти;
(103) трет-бутиловий ефір [1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піперидин-4-іл]карбамінової кислоти;
(104) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піперидин-4-іламін;
(105) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метанол;
(106) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ілметил)метиламін;
(107) 2-[5-(2-етоксіетокси)бензоімідазол-1-іл]-8-[4-(4-метилпіперазин-1-ілметил)піперидин-1-іл]хінолін;
(108) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ілметил)диметиламін;
(109) 1-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піпериин-4-ілметил)піролідин-3-ол;
(110) С-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метиламін;
(111) 1-{2-[5-(2-диметиламіноетокси)бензоімідазол-1-іл]хінолін-8-іл}-4-метилпіперидин-4-ол;
(112) 1-{2-[5-(2-диметиламіноетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ол;
(113) S,S-(1-(4-{2-[5-(2-метоксіетоксибензоімідазол-1-іл]хінолін-8-іл}бензил)транс-піролідин-3,4-діол);
(114) 4-{2-[5-(3-амінопропокси)бензоімідазол-1-іл]хінолін-8-іл}фенол;
(115) 4-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}фенол;
(116) 1-[2-(5-фенілбензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(117) 1-[2-(5-піридин-4-ілбензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(118) 1-{2-[5-(3-метоксифеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(119) 1-[2-(5-піридин-3-ілбензоімідазол-1-іл)хінолін-8-іл)піперидин-4-іламін;
(120) 1-{2-[5-(6-метоксипіридин-3-іл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(121) 1-{2-[5-(4-амінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(122) метиловий ефір 4-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-іл}бензойної кислоти;
(123) 4-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-іл}фенол;
(124) метиловий ефір 2-(5-метоксибензоімідазол-1-іл)хінолін-8-карбонової кислоти;
(125) метиловий ефір 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-карбонової кислоти;
(126) (2-диметиламіноетил)амід 2-(5-метоксибензоімідазол-1-іл)хінолін-8-карбонової кислоти;
(127) метиловий ефір 2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-карбонової кислоти;
(128) [2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піролідин-1-ілметанон;
(129) [2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]морфолін-4-ілметанон;
(130) [2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-1-ілметанон;
(131) (3-амінопіролідин-1-іл)-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]метанон;
(132) 8-алілокси-2-(5-метоксибензоімідазол-1-іл)хінолін;
(133) {2-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-ілоксі]етил}метиламін;
(134) {2-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-ілоксі]етил}диметиламін;
(135) 2-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-ілоксі]етиламін;
(136) тригідрохлорид 1-[[2-[5-(3-морфоліноетокси)-1H-бензимідазол-1-іл]хінолін-8-іл]]піперидин-4-іламіну;
(137) 1-[[2-[5-(3-морфоліноетокси)-1Н-6ензімідазол-1-іл]хінолін-8-іл]]піперидин-4-іламінтригідрохлорид;
(138) 5-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}[1,3,4]оксадіазол-2-іламін;
(139) етил-1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]бензімідазол-5-карбоксилат;
(140) 1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]бензимідазол-5-карбонова кислота;
(141) N-(4-морфоліно)етил-1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]бензимідазол-5-карбоксамід;
(142) 4-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-іл}бензальдегід;
(143) 1-{2-[5-(4-метиламінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(144) 1-{2-[5-(4-диметиламінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(145) 1-(2-{5-[2-(2-метилімідазол-1-іл)етокси]бензоімідазол-1-іл}хінолін-8-іл)піперидин-4-іламін і
(146) 1-(2-{5-(2-[1,2,4]триазол-1-іл-етокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін,
і фармацевтично прийнятні солі, проліки і сольвати вказаних вище сполук.
15. Сполука за п. 1, вибрана з групи, що включає:
(1) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(2) 1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-ол;
(3) 1-{2-[5-(піридин-2-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(4) {1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(5) {4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}метиламін;
(6) {4-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]бензил}диметиламін;
(10) 1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(11) {1-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(13) {4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}метиламін;
(16) {4-[2-(5-етоксибензоімідазол-1-іл)хінолін-8-іл]бензил}диметиламін;
(21) {1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}метиламін;
(23) 4-диметиламінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(24) 1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]-4-метиламінометилпіперидин-4-ол;
(25) 4-амінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл-3-піперидин-4-ол;
(29) 1-{2-[5-(4-метоксифеніл)бензоімідазол-1-іл]хінолін-8-іл}іперидин-4-іламін;
(30) 1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(31) 1-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(32) 1-{2-[5-(3-амінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(33) 1-{2-[5-(2-диметиламіноетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(34) 1-{2-[5-(піридин-4-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(35) 1-[2-(5-бензилоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(36) 1-{2-[5-(піридин-3-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(37) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(40) 4-диметиламінометил-1-[2-(5-метоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-ол;
(45) 4-амінометил-1-{2-[5-(піридин-2-ілметокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ол;
(47) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)диметиламін;
(48) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метиламін;
(49) (1-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)диметиламін;
(50) {1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}метиламін;
(51) {1-[2-(5-циклопропілметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іл}диметиламін;
(57) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)піридин-2-ілметиламін;
(58) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)піридин-3-ілметиламін;
(59) 4-(2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}фенол;
(60) [2-(4-{2-[5-(2- метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}феноксі)етил]диметиламін;
(61) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-піперазин-1-ілхінолін;
(62) [2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етил]диметиламін;
(65) 2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)-2-метилпропан-1-он;
(66) (S)-2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)пропан-1-он;
(67) (S)-2-аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)пропан-1-он;
(68) 2- аміно-1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етанон;
(70) 2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперазин-1-іл)етиламін;
(72) 3-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}-3-азабіцикло[3.1.0]гекс-6-иламін;
(74) 1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}-4-метилпіперидин-4-іламін;
(79) 1-[2-(6,7-дигідро-5,8-діокса-1,3-діазациклопента[b]нафталін-1-іл)хінолін-8-іл]піперидин-4-іламін;
(80) 2-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-ілоксі}етанол;
(84) 1-[2-(5,6-диметоксибензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(87) (4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)диметиламін;
(88) (4-(2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)метиламін;
{90} 2-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензиламіно)етанол;
(91) 4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензиламін;
(92) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(93) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(94) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-(4-піролідин-1-ілметилфеніл)хінолін;
(95) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)цис-піролідин-3,4-діол;
(96) R,R-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)транс-піролідин-3,4-діол);
(97) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол;
(98) R-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол);
(99) S-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піролідин-3-ол);
(100) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)азетидин-3-ол;
(101) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-[4-(4-метилпіперазин-1-ілметил)феніл]хінолін;
(103) 1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)піперидин-4-іламін;
(105) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метанол;
(106) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ілметил)метиламін;
(107) 2-[5-(2-метоксіетокси)бензоімідазол-1-іл]-8-[4-(4-метилпіперазин-1-ілметил)піперидин-1-іл]хінолін;
(108) (1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-ілметил)диметиламін;
(110) С-(1-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іл)метиламін;
(113) S,S-(1-(4-{2-[5-(2-метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл}бензил)транс-піролідин-3,4-діол);
(115) 4-{2-[5-(3-диметиламінопропокси)бензоімідазол-1-іл]хінолін-8-іл}фенол;
(116) 1-[2-(5-фенілбензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(117) 1-[2-(5-піридин-4-ілбензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(118) 1-{2-[5-(3-метоксифеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(119) 1-[2-(5-піридин-3-ілбензоімідазол-1-іл)хінолін-8-іл]піперидин-4-іламін;
(120) 1-{2-[5-(6-метоксипіридин-3-іл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(121) 1-{2-[5-(4-амінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(122) метиловий ефір 4-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-іл}бензойної кислоти;
(123) 4-{1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]-1Н-бензоімідазол-5-іл}фенол;
(136) тригідрохлорид 1-[[2-[5-(3-морфоліноетокси)-1Н-бензимідазол-1-іл]хінолін-8-іл] ]піперидин-4-іламіну;
(139) етил 1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]бензимідазол-5-карбоксилат;
(141) N-(4-морфоліно)етил-1-[8-(4-амінопіперидин-1-іл)хінолін-2-іл]бензимідазол-5-карбоксамід;
(143) 1-{2-[5-(4-метиламінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(144) 1-{2-[5-(4-диметиламінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін;
(145) 1-(2-{5-[2-(2-метилімідазол-1-іл)етокси]бензоімідазол-1-іл}хінолін-8-іл)піперидин-4-іламін і
(146) 1-{2-[5-(2-[1,2,4]триазол-1-ілетокси)бензоімідазол-1-іл]хінолін-8-іл}піперидин-4-іламін,
і фармацевтично прийнятні солі, проліки і сольвати вказаних вище сполук.
16. Спосіб лікування аномального зростання клітин у ссавців, що включає введення вказаному ссавцеві кількості сполуки за п. 1, ефективної для лікування аномального зростання клітин.
17. Спосіб за п. 16, де вказане аномальне зростання клітин означає рак.
18. Спосіб за п. 17, де вказаний рак вибраний з: раку легенів, раку кісток, раку підшлункової залози, раку шкіри, раку голови або шиї, шкіряної або внутрішньоочної меланоми, раку матки, раку яєчника, раку прямої кишки, раку анальної області, раку шлунка, раку ободової кишки, раку молочної залози, карциноми маточних труб, карциноми ендометрію, карциноми шийки матки, карциноми піхви, карциноми вульви, хвороби Ходжкіна, раку стравоходу, раку тонкої кишки, раку ендокринної системи, раку щитовидної залози, раку паращитовидної залози, раку наднирок, саркоми м’якої тканини, раку уретри, раку статевого члена, раку передміхурової залози, хронічного або гострого лейкозу, лімфоцитарних лімфом, раку сечового міхура, раку нирок або сечоводу, ниркової карциноми клітин, карциноми ниркової миски, пухлини центральної нервової системи (ЦНС), первинної лімфоми ЦНС, пухлини спинного мозку, гліоми стовбура мозку, гіпофізарної аденоми, або поєднання одного або більше вказаних видів раку.
19. Фармацевтична композиція для лікування аномального зростання клітин у ссавців, що включає сполуку за п. 1, ефективну для лікування аномального зростання клітин, і фармацевтично прийнятний носій.
20. Фармацевтична композиція за п. 19, де вказане аномальне зростання клітин означає рак.
Текст
1-{2-[5-(2-Метоксіетокси)бензоімідазол-1(4) {1-[2-(5-Метоксибензоімідазол-1-іл)хінолініл]хінолін-8-іл}піперидин-4-іл) піридин-28-іл]піперидин-4-іл} диметиламін; ілметиламін; (5) {4-[2-(5- Метоксибензоімідазол-1-іл)хінолін(58) (1-{2-[5-(2-Метоксіетокси)бензоімідазол-18-іл]бензил} метиламін; іл]хінолін-8-іл}піперидин-4-іл)піридин-3(6) {4-[2-(5- Метоксибензоімідазол-1-іл)хінолінілметиламін; 8-іл]бензил} диметиламін; (59) 4- {2-[5-(2- Метоксіетокси)бензоімідазол-1(10) 1-[2-(5- Етоксибензоімідазол-1-іл)хінолініл]хінолін-8-іл}фенол; 8-іл] піперидин-4-іламін; (60) [2-(4-{2-[5-(2-Метоксіетокси)бензоімідазол(11) {1-[2-(5- Етоксибензоімідазол-1-іл)хінолін1-іл]хінолін-8-іл}фенокси) етил]диметиламін; 8-іл] піперидин-4-іл} диметиламін; (61) 2-[5-(2-Метоксіетокси)бензоімідазол-1-іл](13) {4-[2-(5- Етоксибензоімідазол-1-іл)хінолін8- піперазин-1-ілхінолін; 8-іл]бензил} метиламін; (62) [2-(4-{2-[5-(2-Метоксіетокси)бензоімідазол(16) {4-[2-(5- Етоксибензоімідазол-1-іл)хінолін1-іл]хінолін-8-іл}піперазин-1-іл)- етил]диметиламін; 8-іл]бензил} диметиламін; (65) 2-Аміно-1-(4-{2-[5-(2(21) {1-[2-(5Метоксибензоімідазол-1метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} пііл)хінолін-8-іл]піперидин-4-іл} метиламін; перазин-1 -іл)-2- метилпропан-1 -он; (23) 4- Диметиламінометил-1-[2-(5(66) (S)-2-Аміно-1-(4-{2-[5-(2Метоксибензоімідазол-1-іл) хінолін-8-іл] піперидинметоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} пі4-ол; перазин-1 -іл)пропан-1 -он; (24) 1-[2-(5-Метоксибензоімідазол-1-іл)хінолін(67) (S)-2-Аміно-1-(4-{2-[5-(28-іл]-4- метил-амінометилпіперидин-4-ол; метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} пі(25) 4-Амінометил-1-[2-(5перазин-1 -іл)пропан-1 -он метоксибензоімідазол-1-іл)хінолін-8-іл] піперидин(68) 2-Аміно-1-(4-{2-[5-(24-ол; метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} пі(29) 1-{2-[5-(4-Метоксифеніл)бензоімідазол-1перазин-1 -іл)етанон; іл]хінолін-8-іл}піперидин-4-іламін; (70) 2-(4-{2-[5-(2-Метоксіетокси)бензоімідазол(30) 1-[2-(5- Циклопропілметоксибензоіміда1-іл]хінолін-8-іл}піперазин-1-іл)етиламін; зол-1-іл)хінолін-8-іл] піперидин-4-іламін; (72) 3-{2-[5-(2-Метоксіетокси)бензоімідазол-1(31) 1-{2-[5-(3іл]хінолін-8-іл}-3-азабіцикло[3.1.0]гекс-6-іламін; Диметиламінопропокси)бензоімідазол-1-іл]хінолін(74) 1-{2-[5-(2-Метоксіетокси)бензоімідазол-18-іл} піперидин-4-іламін; іл]хінолін-8-іл}-4-метилпіперидин-4-іламін; (32) 1-{2-[5-(3-Амінопропокси)бензоімідазол-1(79) 1-[2-(6,7-Дигідро-5,8-діокса-1,3іл]хінолін-8-іл}піперидин-4-іламін; діазациклопента[b] нафталін-1-іл)хінолін-8(33) 1-{2-[5-(2іл]піперидин-4-іламін; Диметиламіноетокси)бензоімідазол-1-іл]хінолін-8(80) 2-{1-[8-(4-Амінопіперидин-1-іл)хінолін-2іл}піперидин-4-іламін; іл]-1Н-бензо- імідазол-5-ілокси}етанол; (34) 1-{2-[5-(Піридин-4(84) 1-[2-(5,6-Диметоксибензоімідазол-1ілметокси)бензоімідазол-1-іл]хінолін-8іл)хінолін-8-іл] піперидин-4-іламін; іл}піперидин-4-іламін; (87) (4-{2-[5-(2-Метоксіетокси)бензоімідазол-1 (35) 1-[2-(5-6ензилоксибензоімідазол-1іл]хінолін-8-іл} бензил) диметиламін; іл)хінолін-8-іл] піперидин-4-іламін; (88) (4-{2-[5-(2- Метоксіетокси)бензоімідазол-1(36) 1-{2-[5-(Піридин-3іл]хінолін-8-іл} бензил) метиламін; ілметокси)бензоімідазол-1-іл]хінолін-8(90) 2-(4-{2-[5-(2- Метоксіетокси)бензоімідазоліл}піперидин-4-іламін; 1-іл]хінолін-8-іл} бензиламіно)етанол; (37) 1-{2-[5-(2- Метоксіетокси)бензоімідазол-1(91) 4-{2-[5-(2- Метоксіетокси)бензоімідазол-1іл]хінолін-8-іл}піперидин-4-іламін; іл]хінолін-8-іл} бензиламін; (40) 4-Диметиламінометил-1-[2-(5(92) 2-[5-(2- Метоксіетокси)бензоімідазол-1-іл]метоксибензоімідазол-1-іл) хінолін-8-іл]піперидин8-(4- піролідин-1-ілметилфеніл)хінолін; 4-ол; (93) 2-[5-{2- Метоксіетокси)бензоімідазол-1-іл](45) 4-Амінометил-1-{2-[5-(піридин-28-(4- піролідин-1-ілметилфеніл)хінолін; ілметокси)бензоімід-азол-1-іл]хінолін-8-іл} піпери(94) 2-[5-(2- Метоксіетокси)бензоімідазол-1-іл]дин-4-ол; 8-(4- піролідин-1-ілметилфеніл)хінолін; (47) 1-{2-[5-(2-Метоксіетокси)бензоімідазол-1(95) 1-(4-{2-[5-(2-Метоксіетокси)бензоімідазоліл]хінолін-8-іл}піперидин-4-іл)диметиламін; 1-іл]хінолін-8-іл}бензил)-цис-піролідин-3,4-діол; (48) 1-{2-[5-(2-Метоксіетокси)бензоімідазол-1(96) R, R-(1-(4-{2-[5-(2іл]хінолін-8-іл}піперидин-4-іл) метиламін; Метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} бен(49) (1-{2-[5-(3зил)транс-піролідин-3,4-діол); Диметиламінопропокси)бензоімідазол-1-іл]хінолін(97) 1-(4- {2-[5-(2-Метоксіетокси)бензоімідазол8-іл} піперидин-4-ілдиметиламін; 1-іл]хінолін-8-іл} бензил) піролідин-3-ол; 25 75055 26 (98) R-(1-(4-{2-[5-(2іл)етокси]бензоімідазол-1-іл}хінолін-8Метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} беніл)піперидин-4-іламін і зил) піролідин-3-ол); (146) 1-{2-[5-(2-[1,2,4]Тріазол-1(99) S-(1-(4-{2-[5-(2ілетокси)бензоімідазол-1-іл]хінолін-8-іл} піперидинМетоксіетокси)бензоімідазол-1-іл]хінолін-84-іламін іл}бензил) піролідин-3-ол); і фармацевтично прийнятні солі, проліки і со(100) 1-(4-{2-[5-(2Метоксіетокльвати вищезгаданих сполук. си)бензоімідазол-1-іл]хінолін-8-іл} бензил) азетиВинахід відноситься також до фармацевтичної дин-3-ол композиції для лікування гіперпроліферативного (101) 2-[5-(2-Метоксіетокси)бензоімідазол-1порушення у ссавців, яка включає терапевтично іл]-8-[4-(4-метилпіперазин-1-ілметил)феніл]хінолін; ефективну кількість сполуки формули 1 або її фа(103) 1-(4{2-[5-(2рмацевтично прийнятної солі, проліків або гідрату і Метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} бенфармацевтично прийнятний носій. зил)піперидин-4-іламін; В одному з варіантів вказана фармацевтична (105) (1-{2-[5-(2-Метоксіетокси)бензоімідазолкомпозиція призначена для лікування ракової пух1-іл]хінолін-8-іл}піперидин-4-іл) метанол; лини, такої як злоякісна пухлина головного мозку, (106) (1-{2-[5-(2-Метоксіетокси)бензоімідазоллегенів, сквамозних клітин, сечового міхура, шлун1-іл]хінолін-8-іл}піперидин-4-ілметил) метиламін; ка, підшлункової залози, молочної залози, голови, (107) 2-[5-(2-Метоксіетокси)бензоімідазол-1шиї, нирок, яєчників, передміхурової залози, товсіл]-8-[4-(4-метилпіперазин-1-ілметил)піперидин-1тої кишки, стравоходу, яєчок, жіночих статевих іл]хінолін; органів або щитовидної залози. У іншому варіанті (108) (1-{2-[5-(2-Метоксіетокси)бензоімідазолвказана фармацевтична композиція призначена 1-іл]хінолін-8-іл}піперидин-4-ілметил)диметиламін; для лікування не злоякісного гіперпроліфератив(109) С-(1-{2-[5-(2ного порушення, такого як доброякісна гіперплазія Метоксіетокси)бензоімідазол-1-іл]хінолін-8шкіри (наприклад, псоріаз), рестеноз, або лікуваніл}піперидин-4-іл)метиламін; ня простати (наприклад, доброякісної гіпертрофії (113) 8,8-(1-(4-{2-[5-(2передміхурової залози (ВРН)). Метоксіетокси)бензоімідазол-1-іл]хінолін-8-іл} бенВинахід відноситься також до фармацевтичної зил )транс-піролідин-3,4-діол); композиції для лікування панкреатиту або хвороби (115) 4-{2-[5-(3нирок (включаючи проліферативний гломерулоДиметиламінопропокси)бензоімідазол-1-іл]хіноліннефрит і хворобу нирок, викликану діабетом) у 8-іл} фенол; ссавців, яка включає терапевтично ефективну кі(116) 1-[2-(5-Фенілбензоімідазол-1-іл)хінолін-8лькість сполуки формули 1 або її фармацевтично іл]піперидин-4-іламін; прийнятної солі, проліків або гідрату і фармацев(117) 1-[2-(5-Піридин-4-іл-бензоімідазол -1тично прийнятний носій. іл)хінолін-8-іл]піперидин-4-і л амін; Винахід відноситься також до фармацевтичної (118) 1-{2-[5-(3-Метоксифеніл)бензоімідазол-1композиції для попередження імплантації бластоіл]хінолін-8-іл}піперидин-4-iламін; цитів у ссавців, яка включає терапевтично ефек(119) 1-[2-(5-Піридин-3-ілбензоімідазол-1тивну кількість сполуки формули 1 або її фармаіл)хінолін-8-іл] піперидин-4-іламін; цевтично прийнятної солі, проліків або гідрату і (120} 1-{2-[5-(6-Метоксипіридин-3фармацевтично прийнятний носій. іл)бензоімідазол-1-іл]хінолін-8-іл} піперидин-4Винахід відноситься також до фармацевтичної іламін; композиції для лікування захворювань, пов'язаних (121) 1-{2-[5-(4з утворенням і розвитком судин або розвитком Амінометилфеніл)бензоімідазол-1-іл]хінолін-8-іл} кровоносних судин у ссавців, яка включає терапепіперидин-4-іламін; втично ефективну кількість сполуки формули 1 або (122) Метиловий ефір 4-{1-[8-(4її фармацевтично прийнятної солі, проліків або амінопіперидин-1-іл)хінолін-2-іл]-1Нгідрату і фармацевтично прийнятний носій. У одбензоімідазол-5-іл} бензойної кислоти; ному з варіантів вказана фармацевтична компози(123) 4-{1-[8-(4-Амінопіперидин-1-іл)хінолін-2ція призначена для лікування хвороби, вибраної з іл]-1Н-бензо- імідазол-5-іл} фенол; групи, що включає: розвиток кровоносних судин в (136) тригідрохлорид 1-[ [2-[5-(3пухлинах, хронічне запальне захворювання, такий Морфолінозтокси)][-1Н-бензімідазол-1-іл]хінолін-8як ревматоїдний артрит, атеросклероз, шкіряні іл] ] піперидин-4-іламіну; захворювання, такий як псоріаз, екзема і склеро(139) Етил 1-[8-(4-амінопіперидин-1-іл)хіноліндермія, діабет, діабетичну ретинопатію, сетинопа2-іл] бензімідазол-5-карбоксилат; тію раннього віку, вікову дегенерацію жовтої пля(141) N(4-Морфоліно)етил-1-[8-(4ми, гемангіому, гліому, меланому, саркому Капоши амінопіперидин-1-іл) хінолін-2-іл] бензімідазол-5і оваріальну карциному, рака молочної залози, карбоксамід; легені, підшлункової залози, передміхурової зало(143) 1-{2-[5-(4зи, ободової кишки і епідермісу. Метиламінометилфеніл)бензоімідазол-1-іл]хінолінВинахід також відноситься до способу лікуван8-іл} піперидин-4-іламін; ня гіперпроліферативного порушення у ссавців, (144) 1-{2-[5-(4який включає введення вказаному ссавцеві тераДиметиламінометилфеніл)бензоімідазол-1певтично ефективної кількості сполуки формули 1 іл]хінолін-8-іл} піперидин-4-іламін; або її фармацевтично прийнятної солі, проліків (145) 1-(2-{5-[2-(2-Метилімідазол-1або гідрату. В одному з варіантів вказаний спосіб 27 75055 28 відноситься до лікування ракової пухлини, такої як логічні пухлини (наприклад, саркома матки, карцизлоякісна пухлина головного мозку, сквамозних нома маточних труб, карцинома ендометрію, карклітин, сечового міхура, шлунка, підшлункової зацинома шийки матки, карцинома піхви або карцилози, молочної залози, голови, шиї, стравоходу, нома вульви), хвороба Ходжкіна, рак стравоходу, передміхурової залози, прямої кишки, легень, нирак тонкої кишки, рак ендокринної системи (наприрок, яєчників, яєчок, жіночих статевих органів або клад, рак щитовидної залози, паращитовидної щитовидної залози. У іншому варіанті вказаний залози або наднирок), саркома м'якої тканини, рак спосіб відноситься до лікування не злоякісного уретри, рак статевого члена, рак передміхурової гіперпроліферативного порушення, такого як добзалози, хронічний або гострий лейкоз, дитячі тверроякісна гіперплазія шкіри (наприклад, псоріаз), ді пухлини, лімфоцитарні лімфоми, рак сечового рестеноз, або лікування простати (наприклад, доміхура, рак нирок або сечоводу (наприклад, ниркоброякісної гіпертрофії передміхурової залози ва карцинома клітин, карцинома ниркової миски), (ВРН)). або пухлини центральної нервової системи (наВинахід також відноситься до способу лікуванприклад, первинна лімфома ЦНС, пухлини спинноня гіперпроліферативного порушення у ссавців, го мозку, гліоми стовбура мозку або гіпофизарні який включає введення вказаному ссавцеві терааденоми). певтично ефективної кількості сполуки формули 1 Даний винахід також відноситься до фармацеабо її фармацевтично прийнятної солі, проліків втичної композиції для інгібування аномального або гідрату в поєднанні з протипухлинним засозростання клітин, яка включає деяку кількість спобом, вибраним з групи, що включає: мітотичні інгілуки формули 1 або її фармацевтично прийнятної бітори, алкілуючі засоби, антиметаболіти, інтеркасолі, або сольвату, або проліків в поєднанні з делюючі антибіотики, інгібітори факторів зростання, якою кількістю хіміотерапевтичних засобів, де заінгібітори клітинного циклу, ферменти, інгібітори гальна кількість сполуки, солі, сольвату або пролітопоізомерази, модифікатори біологічну реакцію у ків і хіміотерапевтичного засобу ефективна для відповідь, антигормони, інгібітори розвитку кровоінгібування аномального зростання клітин. Багато носних судин і антиандрогени. які хіміотерапевтичні засоби відомі в цей час з Винахід також відноситься до способу лікуванрівня техніки. В одному з варіантів хіміотерапевтиня панкреатиту або хвороби нирок у ссавців, який чний засіб вибраний з групи, що включає: мітотичні включає введення вказаному ссавцеві терапевтиінгібітори, алкілуючі засоби, антиметаболіти, інтечно ефективної кількості сполуки формули 1 або її рполюючі антибіотики, інгібітори факторів зросфармацевтично прийнятної солі, проліків або гідтання, інгібітори клітинного циклу, ферменти, інгірату. бітори топоізомерази, біологічні модифікатори Винахід також відноситься до способу запобіреакцію у відповідь, антигормони, наприклад, ангання імплантації бластоцитів у ссавців, який тиандрогени. включає введення терапевтично ефективної кільВинахід також відноситься до способу інгібукості сполуки формули 1 або її фармацевтично вання аномального зростання клітин у ссавців або прийнятної солі, проліків або гідрату. лікування гіперпроліферативного порушення, вкаВинахід також відноситься до способу лікуванзаний спосіб включає введення ссавцеві деякої ня захворювань, пов'язаних з утворенням і розвиткількості сполуки формули 1 або її фармацевтично ком судин або розвитком кровоносних судин у прийнятної солі, або сольвату, або проліків в поссавців, який включає введення вказаному ссавєднанні з променевою терапією, де кількість споцеві терапевтично ефективної кількості сполуки луки, солі, сольвату або проліків в поєднанні з формули 1 або її фармацевтично прийнятної солі, променевою терапією ефективна для інгібування проліків або гідрату. У одному з варіантів вказаний аномального зростання клітин або лікування гіперспосіб призначений для лікування захворювань, проліферативного порушення у ссавців. Способи вибраних з групи, що включає: розвиток кровоносздійснення променевої терапії відомі з рівня техніних судин в пухлинах, хронічні запальні захворюки і вказані способи можуть бути використані у вання, такий як ревматоїдний артрит, атеросклевказаній вище комплексній терапії. Введення спороз, шкіряні захворювання, такий як псоріаз, луки за винаходом при вказаній комплексній тераекзема і склеродермія, діабет, діабетичну ретинопії може бути визначене відповідно до даного опипатію, ретинопатію раннього віку, вікову дегенерасу. цію жовтої плями, гемангіому, гліому, меланому, Вважається, що сполуки формули 1 можуть саркому Капоши і оваріальну карциному, рака мододавати аномальним клітинам велику чутливість лочної залози, легені, підшлункової залози, пепри лікуванні опроміненням з метою знищення редміхурової залози, ободової кишки і епідермісу. і/або придушення зростання вказаних клітин. ОтУ число пацієнтів, яких можна лікувати сполуже, даний винахід також відноситься до способу ками формули 1 або фармацевтично прийнятними підвищення чутливості аномальних клітин ссавців солями, проліками або гідратами вказаних сполук при лікуванні опроміненням, який включає введензгідно з способами за даним винаходом, входять, ня ссавцеві деякої кількості сполуки формули 1 наприклад, пацієнти з таким діагнозом, як псоріаз, або її фармацевтично прийнятної солі, або сольрестеноз, атеросклероз, ВРН, рак легені, рак кісвату, або проліків в кількості, ефективній для підток, CMML, рак підшлункової залози, рак шкіри, вищення чутливості аномальних клітин при лікурак голови і шиї, шкіряна або внутрішньоочна меванні опроміненням. Кількість сполуки, солі або ланома, рак матки, рак яєчника, рак прямої кишки, сольвату у вказаному способі може бути визначерак анальної області, рак шлунка, рак ободової на відповідно до описаних способів встановлення кишки, рак молочної залози, тестикулярні, гінекоефективних кількостей вказаних сполук. 29 75055 30 Даний винахід відноситься також до способу 3) гідроксіамід (2R, ЗR)-1-[4-(2-хлор-4інгібування аномального зростання клітин у ссавфторбензилокси)бензолсульфоніл] -3-гідрокси-Зців і до фармацевтичної композиції для інгібування метилпіперидин-2-карбонової кислоти; аномального зростання клітин у ссавців, що вклю4) гідроксіамід 4-[4-(4чає деяку кількість сполуки формули 1, її фармафторфенокси)бензолсульфонілцевтично прийнятної солі або сольвату, проліків аміно]тетрагідропіран-4-карбонової кислоти; або міченого ізотопом похідного і деяка кількість 5) 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1однієї або більше речовини, вибрані з групи, що гідрокси-карбамоїлциклобутил) аміно]пропіонова включає засоби проти розвитку кровоносних сукислота; дин, інгібітори передачі сигналу і антипроліфера6) гідроксіамід 4-[4-(4тивні засоби. хлорфенокси)бензолсульфоніл-аміно] тетрагідроЗасоби проти розвитку кровоносних судин, такі піран-4-карбонової кислоти; як інгібітори ММР-2 (матрикс-металопротеїнази 2), 7) гідроксіамід (R)-3-[4-(4хлорфенокінгібітори ММР-9 (матрикс-металопротеїнази 9) і си)бензолсульфоніл-аміно] тетрагідропіран-3 СОХ-II (циклооксигенази II), можуть бути викорискарбонової кислоти; тані в поєднанні із сполученням формули 1 і фар8) гідроксіамід (2R, 3R)-1-[4-(4-фтор-2мацевтичними композиціями, що описуються. Приметилбензилокси)бензолсульфоніл]-3-гідрокси-3клади корисних інгібіторів СОХ-II включають метилпіперидин-2-карбонової кислоти; CELEBREXTM (алекоксиб), валдекоксиб і рофекок9) 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1сиб. Приклади корисних інгібіторів матриксгідроксикарбамоїл-1-метилетил) аміно]пропіонова металопротеїнази описані в [WO 96/33172 (опублікислота; кована 24 жовтня 1996), WO 96/27583 (опубліко10) 3-[[4-(4-фторфенокси)бензолсульфоніл]-(4вана 7 березня 1996), європейській патентній заягідрокси-карбамоїлтетрагідропіран-4вці No. 97304971.1 (подана 8 липня 1997), іл)аміно]пропіонова кислота; європейській патентній заявці No. 99308617.2 (по11) гідроксіамід 3-екзо-3-[4-(4дана 29 жовтня 1999), WO 98/07697 (опублікована хлорфенокси)бензолсульфоніл-аміно]-826 лютого 1998), WO 98/03516 (опублікована 29 оксабіцикло[3.2.1]октан-3-карбонової кислоти; січня 1998), WO 98/34918 (опублікована 13 серпня 12) гідроксіамід 3-ендо-3-[4-(41998), WO 98/34915 (опублікована 13 серпня фторфенокси)бензолсульфоніл-аміно]-81998), WO 98/33768 (опублікована 6 серпня 6 оксабіцикло[3.2.1]октан-3-карбонової кислоти і 1998), WO 98/30566 (опублікована 16 липня 1998), 13) гідроксіамід (R)-3-[4-(4європейській патентній заявці 606046 (опубліковафторфенокси)бензолсульфоніл-аміно] тетрагідна 13 липня 1994), європейській патентній заявці рофуран-3-карбонової кислоти; 931788 (опублікована 28 липня 1999), WO і фармацевтично прийнятні солі і сольвати 90/05719 (опублікована 31 травня 1990), WO вказаних сполук. 99/52910 (опублікована 21 жовтня 1999), WO Інші засоби проти розвитку кровоносних судин, 99/52889 (опублікована 21 жовтня 1999), WO включаючи інші інгібітори СОХ-II і інші інгібітори 99/29667 (опублікована 17 червня 1999), міжнароММР, також можуть бути використані за даним дній патентній заявці РСТ No. РСТ/1В98/01113 винаходом. (подана 21 липня 1998), європейській патентній Сполуки формули 1 можуть також бути викозаявці No. 99302232.1 (подана 25 березня 1999), ристані разом з інгібіторами передачі сигналу, тапатентній заявці Великобританії No 9912961.1 (покими як агенти, здатні інгібувати відповідь EGFR дана 3 червня 1999), попередній патентній заявці (рецептора епідермального фактора зростання), США No. 60/148464 (подана 12 серпня 1999), патакими як антитіла до EGFR, антитіла до EGF і тенті США 5863949 (виданий 26 січня 1999), патемолекули, що є інгібіторами EGFR; інгібіторами нті США 5861510 (виданий 19 січня 1999) і євроVEGF (васкулярного фактора ендотеліального пейській патентній заявці 780386 (опублікована 25 зростання), такими як рецептори VEGF і молекули, червня 1997), приведені в даному описі в повному які можуть інгібувати VEGF; і інгібіторами рецептооб'ємі як посилання]. Переважними інгібіторами ра еrbВ2, такими як органічні молекули або антитіММР-2 і ММР-9 є інгібітори, що мають низьку актила, зв'язуючі рецептор еrbВ2, наприклад, вність або не активні при інгібуванні ММР-1. Більш HERCEPTINTM [Genentech, Inc. of South San переважними є ті інгібітори, які селективно інгібуFrancisco, California, USA]. ють ММР-2 і/або ММР-9 відносно інших матриксІнгібітори EGFR описані, наприклад, в [WO металопротеїназ (тобто, ММР-1, ММР-3, ММР-4, 95/19970 (опублікована 27 липня 1995), WO ММР-5, ММР-6, ММР-7, ММР-8, ММР-10, ММР-11, 98/14451 (опублікована 9 квітня 1998), WO ММР-12 і ММР-13). 98/02434 (опублікована 22 січня 1998) і патенті Деякими специфічними прикладами інгібіторів США 5747498 (виданий 5 травня 1998), і вказані ММР, корисних за даним винаходом, є AG-3340, речовини можуть бути використані за даним винаRO 32-3555, RS13-O830 і сполуки, перераховані в ходом, як описано тут, EGFR-інгібуючі агенти наступному списку: включають, але не обмежуючись ними, монокло1) 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1нальні антитіла С225, анти-EGFR 22Mab [(ImClone гідрокси-карбамоїлциклопентил) аміно]пропіонова Systems Incorporated of New York, New York, USA) і кислота; АВХ-EGF (Abgenix antibody) сполуки ZD-1839 2) гідроксіамід 3-екзо-3-[4-(4(AstraZeneca), BIBX-1382 (Boehringer Ingelheim), фторфенокси)бензолсульфоніл-аміно]-8MDX-447 (Medarex Inc. of Annandale, New Jersey, оксабіцикло[3.2.1]октан-3-карбонової кислоти; USA) і OLX-103 (Merck & Co. of Whitehouse Station, 31 75055 32 New Jersey, USA), VRCTC-310 (Ventech Research) і вання аномального зростання клітин або ракової EGF злитий токсин (Seragen Inc. of Hopkinton, пухлини, що включають, але не обмежуючись ниMassachusettes)]. Вказані і інші EGFR-інгібуючі ми, агенти, здатні посилювати протипухлинні імунагенти можуть бути використані за даним винахоні реакції, такі як антитіла до CTLA4 (цитотоксичдом. ному лімфоцитарному антигену 4) і інші агенти, Інгібітори VEGF, наприклад [SU-5416 і SUздатні блокувати CTLA4; і антипроліферативні 6668 [Sugen Inc. of South San Francisco, California, агенти, такі як інгібітори фарнезилпротеїнтрансUSA], також можуть бути об'єднані із сполукою за ферази, і інгібітори ανβ3, такі як антитіло до ανβ3 даним винаходом. Інгібітори VEGF описані, наприVitaxin, і інгібітори ανβ5, і тому подібні. Специфічні клад, в WO 99/24440 (опублікована 20 травня антитіла до CTLA4, які можуть бути використані за 1999), міжнародній патентній заявці даним винаходом, включають антитіла, описані в РСТ/ІВ99/00797 (подана 3 травня 1999), в WO попередній патентній заявці США 60/113647 (по95/21613 (опублікована 17 серпня 1995), WO дана 23 грудня 1998), представлені в даному описі 99/61422 (опублікована 2 грудня 1999), патенті в повному об'ємі як посилання, однак і інші антитіСША 5834504 (виданий 10 листопада 1998), WO ла до CTLA4 можуть бути використані за даним 98/50356 (опублікована 12 листопада 1998), патевинаходом. нті США 5883113 (виданий 16 березня 1999), паСполуки формули 1 і їх фармацевтично притенті США 5886020 (виданий 23 березня 1999), йнятні солі, проліки і сольвати можуть також, кожпатенті США 5792783 (виданий 11 серпня 1998), ний незалежно, бути використані в паліативній не WO 99/10349 (опублікована 4 березня 1999), WO допоміжній/додатковій терапії для полегшення 97/32856 (опублікована 12 вересня 1997), WO симптомів, що викликаються вказаними вище хво97/22596 (опублікована 26 червня 1997), WO робами, а також симптомів, пов'язаних з аномаль98/54093 (опублікована 3 грудня 1998), WO ним зростанням клітин. Вказана терапія може бути 98/02438 (опублікована 22 січня 1998), WO монотерапією або поєднуватися з хіміотерапією 99/16755 (опублікована 8 квітня 1999) і WO і/або імунотерапією. 98/02437 (опублікована 22 січня 1998), приведених Винахід також відноситься до способу одерв даному описі в повному об'ємі як посилання. жання сполуки формули 1. Іншими прикладами деяких специфічних інгібіторів Терміни "аномальне зростання клітин" і VEGF, що використовуються за даним винаходом, "гiперпроліферативне порушення" використовує ІМ862 [Cytran Inc. of Kirkland, Washington, USA]; ються в даному описі як взаємозамінні. IMC-1C11 моноклональне антитіло, анти-VEGF "Аномальне зростання клітин", як використано моноклональне антитіло від Genentech, Inc. of в даному описі, якщо не обумовлено особливо, South San Francisco, California; і ангіозим, синтетиозначає зростання клітин, що відбувається незачний рибозим від Ribozyme (Boulder, Colorado) i лежно від нормальних регуляторних механізмів Chiron (Emeryville, California)]. Вказані і інші інгібі(наприклад, втрата контактного інгібування). Потори VEGF можуть бути використані за даним виняття включає аномальне зростання: (1) пухлиннаходом, як описано вище. них клітин (пухлин), яких проліферують шляхом Інгібітори ЕrbВ2 рецептора, такі як GW-282974 експресії мутованої тирозинкінази або понадексп(Glaxo Wellcome ріс) і моноклональні антитіла ARресії рецепторної тирозинкінази; (2) доброякісних і 209 [Aronex Pharmaceuticals Inc. of The Woodlands, злоякісних клітин інших проліферативних захвоTexas, USA], і 2В-1 (Chiron), можливо, крім того, рювань, при яких спостерігається активація абеоб'єднані із сполукою за винаходом, наприклад, рантної тирозинкінази; (4) будь-яких пухлин, яких інгібітори, вказані в [WO 98/02434 (опублікована 22 проліферують за допомогою рецепторної тирозинсічня 1998), WO 99/35146 (опублікована 15 липня кінази; (5) будь-яких пухлин, яких проліферують 1999), WO 99/35132 (опублікована 15 липня 1999), шляхом активації аберантної серин/треонінкінази; і WO 98/02437 (опублікована 22 січня 1998), WO (6) доброякісних і злоякісних клітин інших пролі97/13760 (опублікована 17 квітня 1997), WO феративних захворювань, при яких спостерігаєть95/19970 (опублікована 27 липня 1995), патенті ся активація аберантної серин/треонінкінази. США 5587458 (виданий 24 грудня 1996) і патенті Термін "лікування (в значенні піддавати вплиСША 5877305 (виданий 2 березня 1999), приведеву)", як використано в даному описі, якщо не обуні в даному описі в повному об'ємі як посилання. мовлено особливо, означає вилікування, полегІнгібітори ЕrbВ2 рецептора, що використовуються шення, придушення прогресування або за даним винаходом, описані також в попередній попередження порушення або стану, до якого вкапатентній заявці США No. 60/117341, поданої 27 заний термін застосовується, або одного або бісічня 1999, і в попередній патентній заявці США льше симптомів вказаного захворювання або стаNo. 60/117346, поданої 27 січня 1999, приведені в ну. Термін "лікування (в значенні процесу)", як даному описі в повному об'ємі як посилання. Сповикористано в даному описі, якщо не обумовлено луки, інгібуючі рецептор ЕrbВ2, і речовина, описаособливо, означає застосування лікування, де на у вказаних вище патентних заявках РСТ США, поняття "лікування" визначено безпосередньо випатентах США і попередніх патентних заявках ще. США, також як інші сполуки і речовини, які інгібуТермін "Me" означає метил, "Et" означає етил і ють рецептор ErbB2], можуть бути використані "Аса" означає ацетил. згідно з даним винаходом із сполукою за даним Термін "галоген", як використано в даному винаходом. описі, якщо не обумовлено особливо, означає Сполука за винаходом може також бути викофтор, хлор, бром або йод. Переважними галогенристана з іншими агентами, корисними для лікуними групами є фтор, хлор і бром. 33 75055 34 Термін "алкіл", як використано в даному описі, золідиніл, 3-азабіцикло[3.1.0]гексаніл, 3якщо не обумовлено особливо, включає насичеазабіцикло[4.1.0]гептаніл, азабіцикло[2.2.2] гексаних одновалентних вуглеводневих радикалів з ніл, 3Н-індоліл і хінолізиніл. Прикладами ароматилінійними, розгалуженими або циклічними складочних гетероциклічних груп є піридиніл, імідазоліл, вими (включаючи конденсовані, сполучені місточпирімідиніл, піразоліл, триазоліл, піразиніл, тетраковим зв'язком і спіроциклічні радикали) або комзоліл, фурил, тієніл, ізоксазоліл, тіазоліл, оксазобінацію вищеперелічених груп. Щоб алкільна група ліл, ізотіазоліл, піроліл, хінолініл, ізохінолініл, інмала циклічні радикали, група повинна містити, доліл, бензімідазоліл, бензофураніл, цинолініл, щонайменше, три атоми вуглецю. індазоліл, індолізиніл, фталазиніл, піридазиніл, Термін "циклоалкіл", як використано в даному триазиніл, ізоіндоліл, птеридиніл, пуриніл, оксадіаописі, якщо не обумовлено особливо, включає золіл, тиадіазоліл, фуразаніл, бензофуразаніл, циклічні алкільні радикали, де алкіл приймає вкабензотіофеніл, бензотіазоліл, бензоксазоліл, хіназані вище значення. Використання терміну "циклозолініл, хіноксалініл, нафтиридиніл і фуропіридиалкіл" не треба тлумачити як обмеження терміну ніл. Спірорадікали, які також входять в рамки об'є"алкіл" тільки нециклічними радикалами. му даного визначення, включають 1-окса-6-азаТермін "алкеніл", як використано в даному спіро[2.5]окт-6-іл. Вказані вище в описі групи, як описі, якщо не обумовлено особливо, включає похідні перераховані вище групи, можуть бути Салкільні радикали, що мають, щонайменше, один приєднаними або N-приєднаними там, де це можподвійний вуглець-вуглецевий зв'язок, де алкіл ливе. Наприклад, групою, похідною від піролу, моприймає вказані вище значення, і включає Ε і Ζ же бути пірол-1-іл (N-приєднаний) або пірол-3-іл ізомери вказаних алкенільних радикалів. (С-приєднаний). Далі, групою, похідною від імідаТермін "алкініл", як використано в даному опизолу, може бути імідазол-1-іл (N-приєднаний) або сі, якщо не обумовлено особливо, включає алкільімідазол-3-іл (С-приєднаний). Прикладом гетероні радикали, що мають, щонайменше, один потрійциклічної групи, де 2 вуглецевих атоми циклу заний вуглець-вуглецевий зв'язок, де алкіл приймає міщені оксо (=O) групами, є 1,1вказані вище значення. діоксотіоморфолініл. Термін "алкокси", як використано в даному Фраза "фармацевтично прийнятна сіль (солі)", описі, якщо не обумовлено особливо, включає Ояк використано в даному описі, якщо не обумовлеалкільні групи, де алкіл приймає вказані вище знано особливо, включає солі кислотних або основних чення. груп, які можуть бути присутніми в сполуках форТермін "арил", як використано в даному описі, мули 1. Сполуки формули 1, що є за своєю прироякщо не обумовлено особливо, включає органічдою основними, здатні утворювати широкий ряд ний радикал, одержаний з ароматичного вуглевосолей з різними неорганічними або органічними дню шляхом видалення одного водню, такий як кислотами. Кислотами, які можуть бути використафеніл або нафтил. ні для одержання фармацевтично прийнятних киТермін "4-10-членний гетероциклічний радислотно-адитивних солей вказаних основних сполук кал", як використано в даному описі, якщо не обуформули 1, є кислоти, що створюють нетоксичні мовлено особливо, включає ароматичні або неакислотно-адитивні солі, тобто, солі, що містять роматичні гетероциклічні групи, що містять від фармацевтично прийнятні аніони, такі як ацетат, одного до чотирьох гетероатомів, кожний з яких бензолсульфонат, бензоат, бікарбонат, бісульфат, вибраний з О, S і N, де кожна гетероциклічна група бітартрат, борат, бромід, едетат кальцію, камзимає 4-10 атомів в циклічній системі, і за умови, що лат, карбонат, хлорид, клавуланат, цитрат, дигідцикл вказаної групи не містить двох сусідніх атомів рохлорид, едетат, едисилат, естолат, езилат, етиО або S. лсукцинат, фумарат, глюцептат, глюконат, Неароматичні гетероциклічні групи включають глютамат, гліколіларсанілат, гексилрезорцинат, групи, що мають тільки 4 атоми в своїй циклічній гідрабамін, гідробромід, гідрохлорид, йодид, ізотісистемі, а ароматичні гетероциклічні групи повинні онат, лактат, лактобіонат, лаурат, малат, малеат, мати, щонайменше, 5 атомів в своїй циклічній сисманделат, мезилат, метилсульфат, мукат, напзитемі. Гетероциклічні групи включають бензоконделат, нітрат, олеат, оксалат, памоат (ембонат), пансовані циклічні системи. льмітат, пантофенат, фосфат/дифосфат, полігаПрикладом 4-членной гетероциклічної групи є лактуронат, саліцилат, стеарат, субацетат, азетидиніл (одержаний з азетидину). Прикладом сукцинат, танат, тартрат, теоклат, тозилат, триеті5-членної гетероциклічної групи є тіазоліл, і прикодод і валерат. Оскільки окрема сполука за даним ладом 10-членної гетероциклічної групи є хінолівинаходом може включати більше однієї кислотної нил. Прикладами неароматичних гетероциклічних або основної групи, сполуки за даним винаходом груп є: піролідиніл, тетрагідрофураніл, дигідрофуможуть містити одну, дві або три солі в одній спораніл, тетрагідротієніл, тетрагідропіраніл, дигідролуці. піраніл, тетрагідротіопіраніл, піперидино, морфоТі сполуки за даним винаходом, які є за своєю ліно, тіоморфоліно, тіоксаніл, піперазиніл, природою кислотними, здатні утворювати солі осгомопіперазиніл, азетидиніл, оксетаніл, тієтаніл, нов з різними фармацевтично прийнятними катіогомопіперидиніл, оксепаніл, тієпаніл, оксазепинил, нами. Приклади вказаних солей включають солі діазепініл, тіазепініл, 1,2,3,6-тетрагідропіридиніл, лужних металів і лужноземельних металів і, зок2-піролініл, 3-піролініл, індолініл, 2Н-піраніл, 4Нрема, солі сполук за даним винаходом з кальцієм, піраніл, діоксаніл, 1,3-діоксоланіл, піразолініл, димагнієм, натрієм і калієм. тіаніл, дитіоланіл, дигідропіраніл, дигідротієніл, У сполуках формули 1, де використовуються дигідрофураніл, піразолідиніл, імідазолініл, імідатакі терміни, як (CR4R5)m або (CR4R5)t, R4 і R5 мо 35 75055 36 жуть змінюватися з кожною ітерацією m або t вище карбонової кислоти сполук формули 1. Амінокис1. Наприклад, коли m або t дорівнює 2, терміни лотні залишки включають, але не обмежуючись (CR4R5)m або (CR4R5)t можуть дорівнювати ними, 20 поширених в природі амінокислот, що СН2СН2- або -СН(СН3)С(СН2СН3) (СН2СН2СН3)-, звичайно означаються символами з трьох букв, а або будь-якому числу подібних радикалів, що підтакож включають 4-гідроксипролін, гідроксилізин, 4 5 падають під визначення R і R . демозин, ізодемозин, 3-метилгістидин, норвалін, Деякі сполуки формули 1 можуть мати бета-аланін, гамма-аміномасляну кислоту, цитруасиметричні центри і тому існувати в різних енанлінгомоцистеїн, гомосерин, омітин і метіонінсультіомерних формах. Вважається, що всі оптичні фон. Винахід охоплює також додаткові типи проліізомери і стереоізомери сполук формули 1 і їх суків. Наприклад, можуть бути одержані похідні міші входять в об'єм даного винаходу. Відносно вільних карбоксильних груп, такі як аміди або алкісполук формули 1, винахід включає використання лові ефіри. Похідні вільних гідроксильних груп морацемату, однієї або більше енантіомерних форм, жуть бути одержані використанням груп, що вклюодну або більше діастереомерних форм, або їх чають, але не обмежуючись ними, гемісукцинати, сумішей. Сполуки формули 1 можуть також існуваскладні ефіри фосфорної кислоти, диметиламіноти у вигляді таутомерів. Даний винахід відноситься ацетати і фосфорилоксиметилоксикарбоніли, як до використання всіх подібних таутомерів і їх сустисло викладено в Advanced Drug Delivery мішей. Reviews, 1996/ 19, 115. Включаються також карбаВинахід, що розглядається, також включає міматні проліки гідроксильних і аміногруп, якими є чені ізотопами сполуки, які ідентичні сполукам, що карбонатні проліки, складні сульфонатні ефіри і описуються формулою 1, але при тому, що один складні сульфатні ефіри гідроксильних груп. або більше атомів заміщені атомом, що має атомВключаються також похідні гідроксильних груп у ну масу або масове число, яке відрізняється від вигляді простого (ацилокси)метилового і (ацилокатомної маси або масового числа звичайно існуюси)етилового ефіру, де ацильною групою може чих в природі. Приклади ізотопів, які можуть бути бути складний алкіловий ефір, необов'язково завведені в сполуку за винаходом, включають ізотоміщений групами, що включають, але не обмежупи водню, вуглецю, азоту, кисню, фосфору, фтору ючись ними, просту ефірну, аміно і карбокислотну і хлору, такі як 2Н, 3Н, 13С, 14С, 15N, 18O, 17О, 31P, функціональності, або де ацильною групою є вка32 P, 35S, 18Fi, 36C1, відповідно. Сполуки за даним заний вище ефір амінокислоти. Проліки вказаного винаходом, їх проліки і фармацевтично прийнятні типу описані в J. Med. Chem. 1996, 39, 10. Вільні солі вказаних сполук або вказаних проліків, що аміни можуть також бути перетворені в аміди, сумістять вказані вище ізотопи і/або ізотопи інших льфонаміди або фосфонаміди. Всі вказані проліатомів, входять в об'єм даного винаходу. Деякі карські фрагменти можуть включати, але не обмемічені ізотопами сполуки за даним винаходом, жуючись ними, просту ефірну, аміноі наприклад, сполуки, в які включені радіоактивні карбокислотну функціональності. ізотопи, такі як 3Н і 14С, корисні для аналізу на розподіл лікарських засобів і/або субстрату в тканинах. Тритовані, тобто 3Н, і які містять вуглець-14, тобто, 14С, ізотопи особливо переважні через легкість їх одержання і виявлення. Крім того, заміщення важкими ізотопами, такими як дейтерій, тобто Н, може дати деякі терапевтичні переваги, що виражаються в більшій метаболічній стійкості, наприклад, більшому періоді напіврозпаду in vivo, або знижених потребах в лікарському засобі, отже, може бути переважно при деяких обставинах. Мічені ізотопами сполуки формули 1 за даним винаходом і їх проліки звичайно можуть бути одержані виконанням способів, представлених на приведених нижче схемах і/або у прикладах і препаративних методиках, заміною не утримуючого ізотопну мітку реагенту на легко доступний мічений ізотопом реагент. Даний винахід також охоплює фармацевтичні композиції, що містять проліки сполук формули 1, і способи лікування проліферативних порушень або аномального зростання клітин шляхом введення проліків сполук формули 1. Сполуки формули 1, що мають вільні аміно-, амідо-, гідроксильні або карбоксильні групи, можуть бути перетворені в проліки. Проліки включають сполуки, в яких амінокислотний залишок або поліпептидний ланцюг з двох або більше (наприклад, двох, трьох або чотирьох) амінокислотних залишків ковалентно сполучені через амідний або складноефірний зв'язок з вільною аміно-, гідроксильною групою або групою 37 75055 38 39 Докладний опис винаходу Основні способи синтезу, які можуть бути вказані в зв'язку з одержанням сполук за даним винаходом, представлені в патенті США 5990146 (виданий 23 листопада 1999) (Warner-Lambert Co.) і опублікованій патентній заявці РСТ WO 99/16755 (опублікована 8 квітня 1999} (Merck & Co.). Вказані вище патент і патентна заявка представлені в даному описі в повному об'ємі як посилання. Схема 1 ілюструє синтез сполук формули 1. На стадії 1 діол формули 2 піддають взаємодії з триалкілсилілхлоридом або триалкілсилілтрифторметансульфонатом (таким як третбутилдиметилсиліл) в присутності відповідної органічної основи, такої як імідазол або піридин, в органічному розчиннику, такому як дихлорметан (ДХМ) при температурі в межах від -78°С до 45°С, переважно, при температурі навколишнього середовища, протягом 1-12 годин, одержуючи сполуку формули 3. На стадії 2 сполуку формули 3 піддають взаємодії з трифлатуючим реагентом і основою, такою як Nфенілбіс(трифторметансульфонімід) і гідрид натрію, або трифторметансульфоновий ангідрид і 2,6-диметилпіридин, в безводному органічному розчиннику, такому як тетрагідрофуран (ТГФ) або ДХМ при температурі в межах від -78°С до температури навколишнього середовища, переважно, при температурі навколишнього середовища, протягом 1-12 годин, одержуючи сполуку формули 4. 75055 40 На стадії 3 сполуку формули 4 піддають взаємодії з аміном формули 5, переважно, X=С, в присутності паладієвого каталізатора, такого як трис(дибензиліден-ацетон) дипаладій (0) або ацетат паладію(ІІ), і основи, такої як карбонат цезію або трет-бутоксид натрію, переважно, карбонат цезію, і паліадієвого ліганду, такого як 2,2' -біс (дифенілфосфіно)-1,1'-бінафтил (BINAP) або 1,2біс(дифенілфосфіно)етан (DIPHOS), в розчиннику, такому як 1,4-діоксан або толуол, переважно, толуол, при температурі в межах від температури навколишнього середовища до інтервалу 80105°С, переважно, при 105°С протягом 1-48 годин. На стадії 4, одержану сполуку формули 6 відновлюють над паладієвим каталізатором, використовуючи або 10% паладій на вугіллі, або 20% гідроксид паладію на вугіллі, в присутності джерела водню, такого як гідразин, форміат амонію або мурашина кислота, в органічному розчиннику, такому як етанол або метанол, в присутності або у відсутності співрозчинника, такого як ТГФ, при температурі в інтервалі від температури навколишнього середовища до температури кипіння флегми протягом 1-24 годин, одержуючи сполуку формули 7. На стадії 5 сполуку формули 7 піддають взаємодії з формамідинацетатом або мурашиною кислотою в органічному розчиннику, такому як 2метоксіетанол, 1-бутанол, етанол або мурашина кислота, переважно в етанолі, при температурі в інтервалі від температури навколишнього середовища до температури кипіння флегми, переважно при температурі кипіння флегми, протягом 1-48 годин, одержуючи сполуку формули 8. На стадії 6 сполуку формули 8 піддають взаємодії з трифлатуючим реагентом і основою, такою як Nфенілбіс(трифторметан-сульфонімід) і гідрид натрію або триетиламін, в безводному органічному розчиннику, такому як ТГФ, в присутності або у відсутності співрозчинника, такого як диметилформамід (ДМФ), при температурі від -78°С до температури навколишнього середовища, переважно при температурі навколишнього середовища, протягом 1-24 годин, одержуючи сполуку формули 9. На стадії 7, у разі R1 груп, які включають арильну або гетер об арильну групу (де Аr=арил або гетероарил), сполуку формули 9 піддають взаємодії над паладієвим каталізатором, таким як тетракис(трифенілфосфін)паладій(0), з відповідним органобораном (де Ζ=В(ОН)2 або В(алкіл)2), органостананом (де Ζ=Sn(алкіл)3) або органоцинком (де Ζ=Zn(гaлoгeн)). Коли Ζ=В(ОН)2, основу, таку як фосфат калію, використовують в розчиннику, такому як 1,4-діоксан або 1,2-диметоксіетан, при температурі в інтервалі від температури навколишнього середовища до температури кипіння флегми, переважно при температурі кипіння флегми, протягом 1-48 годин, одержуючи сполуку формули 1. Коли Ζ=В(алкіл)2, основу, таку як карбонат натрію, в присутності або у відсутності хлориду літію, використовують в системі розчинники, що включає етанол і воду, в присутності або у відсутності толуолу, при температурі в інтервалі від температури навколишнього середовища до температури кипіння флегми, переважно порядку 90°С, протягом 1-48 годин, одержуючи сполуку формули 41 75055 42 1. Коли Ζ=Sn(алкіл)3, в присутності або у відсутножуючи сполуку формули 4А (де V-СІ). Альтернатисті основи, такої як фосфат калію, у відповідному вно, сполуку формули 3А піддають взаємодії з органічному розчиннику,такому як толуол або 1,4бронюючим реагентом, таким як оксибромід фосдіоксан, використовуючи температуру в інтервалі фору, в органічному розчиннику, такому як ДХМ, від температури навколишнього середовища до 1,2-дихлоретан (ДХЕ) або хлороформ, при темпетемператури кипіння флегми, переважно між 80ратурі в межах від температури навколишнього 100°С, протягом 1-48 годин, одержують сполуку середовища до температури кипіння флегми, пеформули 1. Коли Ζ=Zn(гaлoгeн), відповідний оргареважно при температурі кипіння флегми, одернічний розчинник, такий як ТГФ, 1,4-діоксан або жуючи сполуку формули 4А (де V=Вr). 1,2-диметоксіетан, використовують при темпераНа стадії 3 сполуку формули 4А піддають взатурі в інтервалі від -78°С до температури кипіння ємодії з аміном формули 5, переважно X=С, в прифлегми, переважно, між 20-45°С, протягом 1-48 сутності паладієвого каталізатора, такого як годин, з одержанням сполуки формули 1. У випадтрис(дибензиліден-ацетон)дипаладій(0) або ацеку R1 з групою NR5R6, сполуку формули 9 піддають тат паладію(ІІ), і основи, такої як карбонат цезію взаємодії з аміном HNR5R6, використовуючи палаабо трет-бутоксид натрію, переважно карбонат дієвий каталізатор, такий як цезію, і паладієвого ліганду, такого як 2,2' трис(дибензиліденацетон)дипаладій(0) або ацетат біс(дифенілфосфіно)-1, 1'-бінафтил (BINAP) або паладію, і основу, таку як карбонат цезію або трет1,2-біс(дифенілфосфіно)етан (DIPHOS), в розчинбутоксид натрію, переважно карбонат цезію, і панику, такому як 1,4-діоксан або толуол, переважно, ладієвий ліганд, такий як 2,2' толуол, при температурі в межах від температури біс(дифенілфосфіно)-1, 1'-бінафтил (BINAP) або навколишнього середовища до 105°С, переважно 1,2-біс(дифенілфосфіно)етан (DIPHOS), в розчинв межах 80-105°С, протягом 1-48 годин. На стадії 4 нику, такому як 1,4-діоксан, толуол і ксилол, переодержану сполуку формули 6А відновлюють над важно, толуол, при температурі в межах від темпаладієвим каталізатором, використовуючи або ператури навколишнього середовища до 10% паладій на вугіллі, або 20% гідроксид паладії температури кипіння флегми, переважно при темна вугіллі, в присутності джерела водню, такого як пературі кипіння флегми, протягом 1-48 годин, форміат амонію, форміат триетиламонію або муодержуючи сполуку формули 1. Сполуки формули рашина кислота, переважно, форміат амонію, фо1 можуть мати захисні групи, такі як R11, R10 або рміат триетиламонію, в органічному розчиннику, R9=ОМе, які можуть бути видалені використанням такому як етанол (EtOH) або метанол (МеОН), в стандартних умов, як описано в "Protective Groups присутності або у відсутності співрозчинника, такоfor Organic Synthesis". Наприклад, R11, R10 або го як ТГФ, при температурі в інтервалі від темпе9 11 10 R =ОМе можуть бути перетворені в R , R або ратури навколишнього середовища до температуR9=ОН шляхом обробки трибромідом бору в оргари кипіння флегми, переважно між 75°С і нічному розчиннику, такому як ДХМ, при температемпературою кипіння флегми, протягом 1-24 готурі в інтервалі від -78°С до 45°С, переважно при дин, одержуючи сполуку формули 7. температурі навколишнього середовища, протягом Схема 1В ілюструє альтернативний синтез 1-24 годин. сполук формули 6А. На стадії 1 амінохінолін форСхема 1А ілюструє альтернативний синтез мули 2В піддають взаємодії з бензилхлоридом або сполук формули 7. На стадії 1 діол формули 2 підбензилбромідом, переважно бензилбромідом, в дають взаємодії з бензилхлоридом або бензилбприсутності відповідної основи, такої як гідрид наромідом, переважно, бензилбромідом, в присутнотрію або гідрид калію, в органічному розчиннику, сті відповідної основи, такої як карбонат калію, такому як ДМФ/ТГФ або 1,2-диметоксіетан, при карбонат натрію або карбонат цезію, в органічному температурі в інтервалі від -78°С до 65°С, переварозчиннику, такому як ДМФ, при температурі в жно в межах 0-25°С, протягом 1-24 годин, одерінтервалі від -78°С до 100°С, переважно в інтерважуючи сполуку формули 3В. На стадії 2 сполуку лі 60-80°С, протягом 3-24 годин, одержуючи споформули 3В піддають взаємодії з бромароматичлуку формули 3А. На стадії 2 сполуку формули 3А ною сполукою формули 5А в присутності паладієпіддають взаємодії з трифлатуючим реагентом і вого каталізатора, такого як основою, такою як N-фенілтрис(дибензиліденацетон}дипаладій(0) або ацетат біс(трифторметансульфонімід) і гідрид натрію, або паладію(П), переважно ангідрид трифторметансульфонової кислоти і 2,6трис(дибензиліденацетон)дипаладій(0), і основи, диметилпіридин, в безводному органічному розтакої як карбонат цезію або трет-бутоксид натрію, чиннику, такому як тетрагідрофуран (ТГФ) або переважно трет-бутоксид натрію, і паладієвого ДХМ при температурі в інтервалі від -78°С до темліганду, такого як 2,2' -біс(дифенілфосфіно)-1, 1'ператури навколишнього середовища, переважно бінафтил (BINAP) або 1,2при температурі навколишнього середовища, пробіс(дифенілфосфіно)етан (DIPHOS), переважно тягом 1-12 годин, одержуючи сполуку формули 4А 2,2' -біс(дифенілфосфіно)-1, 1'-бінафтил (BINAP), (де V=OTf). Альтернативно, сполуку формули 3А в розчиннику, такому як 1,4-діоксан або толуол, піддають взаємодії з хлоруючим реагентом, таким при температурі в межах від температури навкояк оксихлорид фосфору, тіонілхлорид або оксаліллишнього середовища до 105°С, переважно в мехлорид, в органічному розчиннику, такому як ДХМ, жах 80-105°С, протягом 1-48 годин, одержуючи 1,2-дихлоретан (ДХЕ) або хлороформ, при темпесполуку формули 6А. ратурі в межах від температури навколишнього Схема 2 ілюструє синтез сполук формули 11. середовища до температури кипіння флегми, пеНа стадії 1 сполуку формули 10 в стандартних реважно при температурі кипіння флегми, одерумовах алкілування обробляють електрофилом 43 75055 44 R3Y, де Υ може означати мезилат, тозилат, бром, органічному розчиннику, такому як ДХМ, при темйод і хлор, переважно бром або йод, і основою, пературі в інтервалі від -78°С до 45°С, переважно такою як гідрид натрію, гідрид калію, карбонат напри температурі навколишнього середовища, протрію, карбонат калію або карбонат цезію, переватягом 1-24 годин. Сполуки, що визначаються форжно карбонат цезію, в органічному розчиннику, мулою 13, можна також одержувати, виходячи з такому як ДМФ або ТГФ, переважно ДМФ, протявідповідної аміносполуки формули 5 за стадією 3 гом 1-48 годин, в інтервалі температур від -78°С схеми 1 або стадією 2 схеми 1А. Альтернативно, до 85°С. Сполуки, що визначаються формулою 11, сполуки, що визначаються формулою 11, можна можна також одержувати, виходячи з відповідної також одержувати, виходячи з відповідної бромааміносполуки формули 5 за стадією 3 схеми 1 або роматичної сполуки формули 5А за стадією 2 схестадії 2 схеми 1А. Альтернативно, сполуки, що ми 1В. визначаються формулою 11, можна також одерСхема 3 ілюструє синтез сполук формули 15 жувати, виходячи з відповідної бромароматичної (де W = арил або гетероцикл). На стадії 1 сполуку сполуки формули 5А за стадією 2 схеми 1В. формули 14 піддають взаємодії з аміном HNR3R4 і Схема 2 ілюструє також синтез сполук формупоновлюючим агентом, таким як ціаноборгідрид ли 13, (де Аr означає арильну або гетероарильну натрію або триацетоксиборгідрид натрію, і оцтогрупу). На стадії 2 сполуку формули 10 піддають вою кислотою в органічному розчиннику, такому як взаємодії з трифлатуючим реагентом і основою, метанол або етанол, і в присутності або у відсуттакою як N-феніл-біс(трифторметансульфонімід) і ності співрозчинника, такого як 1,2-дихлоретан, гідрид натрію або трифторметансульфоновий анпри температурі в інтервалі від 0°С до 80°С, перегідрид і піридин, в безводному органічному розважно при температурі навколишнього середовичиннику, такому як ТГФ, в присутності або у відсуща, протягом 1-24 годин. Сполуки формули 15 тності співрозчинника, такого як ДМФ, при можуть мати захисні групи, такі як R11, R10 або температурі в межах від -78°С до температури R9=ОМе, які можуть бути видалені використанням навколишнього середовища, переважно, при темстандартних умов, як описано в "Protective Groups пературі навколишнього середовища, протягом 1for Organic Synthesis". Наприклад, R11, R10 або 24 годин, одержуючи сполуку формули 12. На стаR9=ОМе можуть бути перетворені в R11, R10 або дії 2 сполуку формули 12 піддають взаємодії над R9=ОН шляхом обробки трибромідом бору в оргапаладієвим каталізатором, таким як тетранічному розчиннику, такому як ДХМ, при темперакіс(трифенілфосфїн)паладій(0), з відповідним ортурі в інтервалі від -78°С до 45°С, переважно при ганобораном (де Ζ=В(ОН)2 або В(алкіл)2), органостемпературі навколишнього середовища, протягом тананом (де Ζ=Sn(алкіл)3) або органоцинком (де 1-24 годин. Сполуки, що визначаються формулою Ζ=Zn(гaлoгeн)), Коли Ζ=В(ОН)2, основа, така як 15, можна також одержувати, виходячи з відповідфосфат калію, використовують в розчиннику, таного ArZ або аміну NR5R6 за стадією 7 схеми 1. кому як 1,4-діоксан або 1,2-диметоксіетан, при Схема 4 ілюструє синтез сполук формули 18. температурі в інтервалі від температури навколиНа стадії 1 сполуку формули 16 піддають взаємошнього середовища до температури кипіння фледії з триметилсульфоніййодидом і основою, такою гми, переважно при температурі кипіння флегми, як гідрид натрію, в органічному розчиннику, такому протягом 1-48 годин, одержуючи сполуку формули як диметилсульфоксид (ДМСО) або ТГФ, при тем13. Коли Ζ=В(алкіл)2, основу, таку як карбонат напературі в інтервалі від -78 °С до 65°С, переважно трію, в присутності або у відсутності хлориду літію, при температурі навколишнього середовища, провикористовують в системі розчинників, що включає тягом 1-24 годин. Одержану сполуку формули 17 етанол і воду, в присутності або у відсутності топіддають взаємодії за стадією 2 з аміном NR3R4 в луолу, при температурі в інтервалі від температурозчиннику, такому як ТГФ, метанол, етанол, вода, ри навколишнього середовища до температури ДМФ, ДМСО або будь-якій комбінації з них, при кипіння флегми, переважно порядку 90°С, протятемпературі в межах від 0°С до 100°С, переважно гом 1-48 годин, одержуючи сполуку формули 13. при 65°С, в запаяній трубці, протягом 1-48 годин, Коли Ζ=Sn(алкіл)з, в присутності або відсутності одержуючи сполуку формули 18. Сполуки формуоснови, такої як фосфат калію, у відповідному орли 18 можуть мати захисні групи, такі як R11, R10 ганічному розчиннику, такому як толуол або 1,4або R9=ОМе, які можуть бути видалені викорисдіоксан, і при температурі в інтервалі від температанням стандартних умов, як описано в "Protective тури навколишнього середовища до температури Groups for Organic Synthesis". Наприклад, R11, R10 кипіння флегми, переважно між 80-100°С, протяабо R3=ОМе можуть бути перетворені в R11, R10 гом 1-48 годин, одержують сполуку формули 13. або R9=ОН шляхом обробки трибромідом бору в Коли Ζ=Zn(гaлoгeн), відповідний органічний розорганічному розчиннику, такому як ДХМ, при темчинник, такий як ТГФ, 1,4-діоксан або 1,2пературі в інтервалі від -78°С до 45°С, переважно диметоксіетан, використовують при температурі в при температурі навколишнього середовища, проінтервалі від -78°С до температури кипіння флегтягом 1-24 годин. Сполуки, що визначаються форми, переважно, між 20-45°С, протягом 1-48 годин, мулою 18, можна також одержувати, виходячи з 5 6 одержуючи сполуку формули 13. Сполуки формувідповідного аміну NR R за стадією 7 схеми 1. 11 10 ли 13 можуть мати захисні групи, такі як R , R Схема 4 ілюструє також синтез з'єднання фоабо R9=ОМе, які можуть бути видалені викорисрмули 19. На стадії 1 сполуку формули 16 піддатанням стандартних умов, як описано в "Protective ють взаємодії з аміном HNR3R4 і поновлюючим Groups for Organic Synthesis". Наприклад, R11, R10 агентом, таким як ціаноборгідрид натрію або триаабо R9=ОМе можуть бути перетворені в R11, R10 цетоксиборгідрид натрію, і оцтовою кислотою в або R9=ОН шляхом обробки трибромідом бору в органічному розчиннику, такому як метанол, ета 45 75055 46 нол, і в присутності або у відсутності співрозчинникислотою в органічному розчиннику, такому як 2ка, такого як 1,2-дихлоретан (ДХЕ), при темпераметоксіетанол, 1-бутанол, етанол або мурашина турі в інтервалі від 0°С до 80°С, переважно при кислота, переважно в етанолі, при температурі в температурі навколишнього середовища, протягом інтервалі від температури навколишнього середо1-24 годин. Сполуки формули 19 можуть мати завища до температури кипіння флегми, переважно 11 10 9 хисні групи, такі як R , R або R =ОМе, які можуть при температурі кипіння флегми, протягом 1-48 бути видалені використанням стандартних умов, годин, одержуючи сполуку формули 26. На стадії як описано в "Protective Groups for Organic 4, у разі R1 груп, які включають арильну або гете11 10 9 Synthesis". Наприклад, R , R або R =ОМе мороарильну групу (де Аr=арил або гетероарил), жуть бути перетворені в R11, R10 або R9=ОН шлясполуку формули 26 піддають взаємодії над палахом обробки трибромідом бору в органічному роздієвим каталізатором, таким як тетрачиннику, такому як ДХМ, при температурі в кис(трифенілфосфін)паладій(0), з відповідним орінтервалі від -78°С до 45°С, переважно при темпеганобораном (де Ζ=В(ОН)2 або В(алкіл)2), ратурі навколишнього середовища, протягом 1-24 органостананом (де Ζ=Sn(алкіл)3) або органоцингодин. Сполуки, що визначаються формулою 19, ком (де Ζ=Ζn(галоген)). Коли Ζ=В(ОН)2, основа, можна також одержувати, виходячи з відповідного така як фосфат калію, використовують в розчинаміну NR5R6 за стадією 7 схеми 1. нику, такому як 1,4-діоксан або 1,2-диметоксіетан, Схеми 5 і 6 ілюструють альтернативну схему при температурі в інтервалі від температури насинтезу сполуки формули 1. На стадії 1 броманілін вколишнього середовища до температури кипіння 20 ацилюють цинамілхлоридом в органічному розфлегми, переважно при температурі кипіння флечиннику, такому як ДХМ або ТГФ, переважно ДХМ, гми, протягом 1-48 годин, одержуючи сполуку фов присутності органічної основи, такої як піридин рмули 1. Коли Ζ=В(алкіл)2, основу, таку як карбоабо триетиламін, переважно піридин, при темпенат натрію, в присутності або у відсутності хлориду ратурі в інтервалі від -78°С до 40°С, переважно літію, використовують в системі розчинники, що між 0°С і 25°С, протягом 1-24 годин, одержуючи включає етанол і воду, в присутності або у відсутсполуку формули 21. На стадії 2, сполуку формули ності толуолу, при температурі в інтервалі від тем21 піддають взаємодії з сильною кислотою Л'юїса, ператури навколишнього середовища до температакою як трихлорид алюмінію, в органічному розтури кипіння флегми, переважно порядку 90°С, чиннику, такому як хлорбензол, при температурі в протягом 1-48 годин, одержуючи сполуку формули інтервалі від 25°С до 120°С, переважно в інтервалі 1. Коли Ζ=Sn(алкіл)3 в присутності або у відсутносміж 90°С і 120°С, протягом 1-24 годин, одержуючи ті основи, такої як фосфат калію, у відповідному сполуку формули 22. На стадії 3 сполуку формули органічному розчиннику, такому як толуол або 1,422 піддають взаємодії з три флатуючим реагентом діоксан і при температурі в інтервалі від темпераі основою, такою як Nтури навколишнього середовища до температури фенілбіс(трифторметансульфонімід) і гідрид накипіння флегми, переважно між 80-100°С, протятрію, або трифторметансульфоновий ангідрид і гом 1-48 годин, одержують сполуку формули 1. 2,6-диметилпіридин, в безводному органічному Коли Ζ=Zn(гaлoгeн), відповідний органічний розрозчиннику, такому як ТГФ або ДХМ, при темперачинник, такий як ТГФ, 1,4-діоксан або 1,2турі в межах від -78°С до температури навколишдиметоксіетан, використовують при температурі в нього середовища, переважно, при температурі інтервалі від -78°С до температури кипіння флегнавколишнього середовища, протягом 1-24 годин, ми, переважно, між 20-45°С, протягом 1-48 годин, одержуючи сполуку формули 23. одержуючи сполуку формули 1. У випадку R1 з За схемою б сполуку формули 23, на стадії 1, групою NR5R6, сполуку формули 26 піддають взапіддають взаємодії з аміном формули 5, переважємодії з аміном HNR5R6, використовуючи паладієно, X=С, в присутності паладієвого каталізатора, вий каталізатор, такий як такого як трис(дибензиліденацетон)дипаладій(0) трис(дибензиліденацетон)дипаладій(0) або ацетат або ацетат паладію(II), і основи, такої як карбонат паладію, і основу, таку як карбонат цезію або третцезію або трет-бутоксид натрію, переважно, карбутоксид натрію, переважно карбонат цезію, і пабонат цезію, і паладієвого ліганду, такого як 2,2' ладієвий ліганд, такий як 2,2' біс(дифенілфосфіно)-1,1'-бінафтил (BINAP) або біс(дифенілфосфіно)-1, 1'-бінафтил (BINAP) або 1,2-біс(дифенілфосфіно)етан (DIPHOS), в розчин1,2-біс(дифенілфосфіно)етан (DIPHOS), в розчиннику, такому як 1,2-діоксан або толуол, переважно, нику, такому як 1,4-діоксан, толуол і ксилол, перетолуол, при температурі в межах від температури важно, толуол, коли Υ=Вr і переважно ксилол, коли навколишнього середовища до 105°С, переважно Υ=СІ, при температурі в межах від температури в межах 80-105°С, протягом 1-48 годин. На стадії навколишнього середовища до температури ки2, одержану сполуку формули 24 відновлюють піння флегми, переважно при температурі кипіння залізним порошком і хлоридом амонію в органічфлегми, протягом 1-72 годин, одержуючи сполуку ному розчиннику, такому як етанол або метанол, в формули 1. Сполуки формули 1 можуть мати заприсутності або у відсутності співрозчинника, такохисні групи, такі як R11, R10 або R9=ОМе, які можуть го як вода, при температурі в інтервалі від темпебути видалені використанням стандартних умов, ратури навколишнього середовища до температуяк описано в "Protective Groups for Organic ри кипіння флегми, переважно при температурі Synthesis7'. Наприклад, R11, R10 або R9=ОМе мокипіння флегми, протягом 1-24 годин, одержуючи жуть бути перетворені в R11, R10 або R9=ОН шлясполуку формули 25. хом обробки трибромідом бору в органічному розНа стадії 3 сполуку формули 25 піддають взачиннику, такому як ДХМ, при температурі в ємодії з формамідинацетатом або мурашиною інтервалі від -78°С до 45°С, переважно при темпе 47 75055 48 ратурі навколишнього середовища, протягом 1-24 температури кипіння флегми, одержуючи сполуку годин. формули 31. Сполуки формули 31 можуть мати Альтернативно, сполука формули 26 може бузахисні групи, такі як R11, R10 або R9=ОМе, які моти одержана із сполуки 22 в дві послідовні стадії, жуть бути видалені використанням стандартних схематично представлені на схемі 7. На стадії 1 умов, як описано в "Protective Groups for Organic 11 10 9 сполуку формули 22, де X=СІ, піддають взаємодії Synthesis". Наприклад, R , R або R =ОМе мо11 10 з оксихлоридом фосфору, тіонілхлоридом або жуть бути перетворені в R , R або R9=ОН шляоксалілхлоридом, переважно оксалілхлоридом, в хом обробки трибромідом бору в органічному розприсутності або у відсутності органічного розчинчиннику, такому як ДХМ, при температурі в ника, такого як хлороформ або ДХЕ, переважно інтервалі від -78°С до 45°С, переважно при темпеДХЕ, при температурі в межах від температури ратурі навколишнього середовища, протягом 1-24 навколишнього середовища до температури кигодин. піння флегми, переважно при температурі кипіння Сполуки за даним винаходом можуть мати флегми, протягом 1-24 годин, одержуючи сполуку асиметричні вуглецеві атоми. Діастереомерні суформули 27. Коли X=Вr, сполуку формули 22 підміші можуть бути розділені на окремі діастереомедають взаємодії з оксибромідом фосфору в присури на основі відмінностей в фізико-хімічних властності органічного розчинника, такого як хлоротивостях з використанням способів, відомих форм або ДХЕ, переважний хлороформ, при фахівцям в даній області, наприклад, шляхом температурі в межах від температури навколишхроматографії або фракціонованої кристалізації. нього середовища до температури кипіння флегЕнантіомери можуть бути розділені шляхом переми, переважно при температурі кипіння флегми, творення енантіомерних сумішей в діастереомерпротягом 1-24 годин, одержуючи сполуку формули ну суміш за рахунок взаємодії з відповідною опти27. На стадії 2 сполуку формули 27, де X=Вr або чно активною сполукою (наприклад, спиртом), СІ, піддають взаємодії із сполукою формули 28 в розділення діастереомерів і перетворень (наприорганічному розчиннику, такому як ДМФ або 1клад, гідролізом) окремих діастереомерів у відпометил-2-піролідинон, в присутності або у відсутновідні чисті енантіомери. Все вказані ізомери, вклюсті основи, такої як гідрид натрію або натрійчаючи діастереомерні суміші і чисті енантіомери, біс(триметил-силіл)амід, при температурі в межах розглядаються як частина винаходу. від температури навколишнього середовища до Сполуки формул 1, 13, 15, 18, 19, 29, 31, що є 150°С, переважно при 60-85°С, коли використовуосновними за природою, здібні до утворення шиють основу, і 150°С, коли не використовують оснорокого ряду різних солей з різноманітними неоргаву, протягом 1-24 годин, одержуючи сполуку форнічними і органічними кислотами. Незважаючи на мули 26. те, що вказані солі повинні бути фармацевтично На стадії 1 схеми 8 сполуку формули 8 піддаприйнятними для введення тваринам, практично ють взаємодії з електрофілом RY, де Υ означає часто зручніше спочатку виділяти сполуки формумезилат, тозилат, бромід, хлорид або йодид, і осли 1, 13, 15, 18, 19, 29, 31 з реакційної суміші у новою, такою як гідрид натрію, гідрид калію, карвигляді фармацевтично прийнятної солі і потім бонат калію, карбонат натрію або карбонат цезію, просто перетворювати останні зворотно в сполуки, в розчиннику, такому як ДМФ, ТГФ, ДМСО або 1,2що є вільною основою, шляхом обробки лужним диметоксіетан, при температурі в інтервалі від реагентом, і після цього перетворювати останню 78°С до 65°С, одержуючи сполуку формули 29. вільну основу в фармацевтично прийнятну кислоСполуки формули 29 можуть мати захисні групи, тно-адитивну сіль. Кислотно-адитивні солі основтакі як R11, R10 або R9=ОМе, які можуть бути виданих сполук за даним винаходом легко одержують лені використанням стандартних умов, як описано обробкою основної сполуки по суті еквівалентною в "Protective Groups for Organic Synthesis". Наприкількістю вибраної неорганічної або органічної киклад, Rn, R10 або R9=ОМе можуть бути перетвореслоти в середовищі водного розчинника або у відні в R11, R10 або R9=ОН шляхом обробки триброміповідному органічному розчиннику, такому як медом бору в органічному розчиннику, такому як танол або етанол. Необхідну тверду сіль легко ДХМ, при температурі в інтервалі від -78°С до одержують обережним випаровуванням розчинни45°С, переважно при температурі навколишнього ка. Необхідна кислотна сіль може бути також осасередовища, протягом 1-24 годин. джена з розчину вільної основи в органічному розТакож, схематично зображену на схемі 1 спочиннику додаванням до розчину відповідної луку формули 9 на стадії 1 піддають взаємодії з неорганічної або органічної кислоти. монооксидом вуглецю при тиску в інтервалі від Ті сполуки формул 1, 13, 15, 18, 19, 29, 31, які атмосферного до 50 фунт/кв. дюйм (345кПа), пемають кислотну природу, здатні утворювати солі реважно 50фунт/кв. дюйм (345кПа), в присутності основ з різними фармацевтично прийнятними каорганічної основи, такої як триетиламін, над палатіонами. Приклади вказаних солей включають солі дієвим каталізатором, таким як ацетат паладію, з лужних металів і лужноземельних металів, і, зоклігандом, таким як 1,3рема, солі натрію і калію. Всі вказані солі одержубіс(дифенілфосфіно)пропан, в розчиннику, такому ють загальноприйнятими способами. Хімічними як ДМФ, в присутності метанолу, одержуючи споосновами, що використовуються як реагенти для луку формули 30. На стадії 2 сполуку формули 30 одержання фармацевтично прийнятних основних піддають взаємодії із заздалегідь одержаним комсолей за даним винаходом, є такі основи, які утвоплексом аміну HNR3R4 (або його гідрохлориду) з рюють нетоксичні солі основ з кислотними сполутриметил алюмінієм в розчиннику, такому як ДХМ ками формул 1, 13, 15, 18, 19, 29, 31. Вказані нетоабо ДХЕ, при температурі в інтервалі від 0°С до ксичні солі основ включають солі, одержані з таких 49 75055 50 фармацевтично прийнятних катіонів, як натрій, подальшим інкубуванням протягом 25-35 хвилин калій, кальцій і магній, і т.д. Вказані солі легко мопри кімнатній температурі. Утримуючий антитіло жуть бути одержані обробкою відповідних кислотрозчин відстоюють і пластинку знову чотири рази них сполук водним розчином, що містить необхідні промивають WB. фармакологічно прийнятні катіони, і потім випаро(f) Міру взаємодії визначають, вимірюючи погвуванням одержаного розчину насухо, переважно линання світла при 450нм. Спочатку створюють при зниженому тиску. Альтернативно, вказані солі забарвлення додаванням розчину ТМВ 50мкл на можуть також бути одержані змішуванням розчинів ямку, і дають реакції протікати до досягнення в кислотних сполук в нижчих спиртах і необхідного ямці позитивних сигналів 00450 порядку 0,6-1,2 алкоголяту лужного металу, і подальшим випароодиниць. Подальший вияв забарвлення припинявуванням одержаного розчину насухо таким же ють додаванням 50мкл на ямку 0,09Μ H2SO4. Кончином, як описано вище. У обох випадках переватролями фону служать ямки без PGT, але які місжно використати стехіометричні кількості реагентів тять всі інші компоненти. Як указано вище, для упевненості в повноті проходження реакції і переважний OD сигнал відповідає звичайно обламаксимальних виходах необхідного кінцевого прості 0,6-1,2 одиниць при практичній відсутності фодукту. Оскільки окрема сполука за даним винахону. дом може включати більш, ніж одну, кислотну або Активність in vitro сполук за даним винаходом основну групи, сполуки за даним винаходом моу відношенні інгібування рецептора PDGF може жуть містити одну, дві або три солі в одному спобути визначена наступним способом. луці. Інгібування активності тирозинкінази може буАктивність сполук формул 1, 13, 15, 18, 19, 29, ти оцінено з використанням рекомбінантного фер31 може бути оцінена наступним способом. менту в аналізі за вимірюванням здатності сполук Загальний ELISA аналіз на PGT кіназу інгібувати фосфорилювання екзогенного субстраВикористані наступні реагенти і основні розчиту, поліСluТуr (PGT, SigmaTM, 4:1). Цитоплазмічний ни: домен рецептора PDGFP людини (амінокислоти аденозинтрифосфат 559-1106) [Ishikawa, F., et al. Nature 338: 557-562, Sigma, cat. #A-2383 (АТФ) 1989] експресують в Sf9 клітинах комах як глютатіальбумін бичачої сироон-3-трансфраза(СSТ)-злитого білка, використоSigma, cat. # A-3294 ватки (ВSA) вуючи бакуловірусну систему експресії. Потім біGibco-BRL, cat. #14190лок очищають від лізатів вказаних клітин, PBS Дюльбекко (dPBS) 136 використовуючи афінні колонки з глютатіонагароMaxiSorp пластинки Nunc, cat. # 439454 зои. MgCl2 Sigma, cat. #M-1028 Випробування на фермент здійснюють в 96Полі-Glu-Tyr (PGT) Sigma, cat. #. P-0275 ямкових планшетах, які покривають субстратом Kirkegaard & Perry, cat. # PGT (0,625мкг PGT на ямку). Випробувані сполуки Субстрат TMB Micowell 50-76-05 розбавляють диметилсульфоксидом (ДМСО) і поTween 20 Sigma, cat. #P-1379 тім додають в планшети з PGT так, щоб кінцева Антитіло HRP-PY54 OSI Pharmaceuticals, Inc. концентрація ДМСО в пробі становила 1,6% Фосфорилюючий буфер (PB): 50мМ HEPES, (об./об.). Рекомбінантний фермент розбавляють pH7,3, 125мМ NaCl, 24мМ MgCl2; фосфорилюючим буфером (50мМ Hepes, pH7,3, Промивний буфер (WB): dPBS+0,1% Tween 20 125мМ NaCl, 24мМ MgCl2). Реакцію ініціюють до(поліоксіетилен-сорбітан) і блокуючий буфер: 3% даванням АТФ до кінцевої концентрації 10мкМ. BSA, 0,05% Tween 20 в dPBS. Після 10-хвилинної інкубації при кімнатній темпеМетодика аналізу: ратурі, при струшуванні, реакційну суміш відстою(a) Для покриття пластинки, заповнюють пласють і планшети промивають промивним буфером тинку Nunc MaxiSorp по 100мкл на ямку Полі-Glu(PBS-вміщуючим 0,1% Tween-20). Кількісний вміст Tyr (PGT), розбавленим dPBS (різні концентрації). фосфорильованого PGT визначають шляхом інкуПластинку інкубують протягом ночі при 37°С. Побації з пероксидазою хрону (HRP), кон'югованою з тім супернатант PGT відкидають і пластинку тричі антитілом PY-54, (Transduction Labs), проявляючи промивають промивним буфером. ТМВ пероксидазою (ТМВ означає 3,3', 5,5' (b) Потім фермент PDGF розбавляють РВ до тетраметилбензидин) і проявляючи за допомогою відповідної концентрації і додають 25мкл вказанозчитуючого пристрою BioRadTM Microplate при го вихідного розчину на ямку. 450нМ. Інгібування ферментативної активності (c) Потім розбавляють АТФ (від вихідних кінази за допомогою випробуваної сполуки вияв20мМ) до необхідної концентрації (0,5нМ-2мкМ) за ляють за зниженою спектральною поминальною допомогою РВ. Реакцію фосфорилювання почиздатністю, і концентрацію сполуки, необхідну для нають додаванням 25мкл розчину АТФ в кожну 50% придушення сигналу (в умовах випробуванямку пластинки для аналізу. Інкубування продовня), приводять як IC50 значення для випробуваної жують біля 10 хвилин, струшуючи при кімнатній сполуки. температурі. Для оцінки здатності сполук інгібувати (d) Реакцію зупиняють відсмоктуванням реакPDGFR активність тирозинкінази для повнорозміційної суміші. Потім пластинку чотири рази промирного білка, існуючого в клітинному контексті, мовають WB. жуть бути використані ендотеліальні клітини аорти (e) Антитіло HRP-PY54 розбавляють до відпосвині (РАЕ), трансфіковані PDGFR людини відної концентрації блокуючим буфером. Потім [Westermark, Bengt, et. al.f PNAS 87, pp.128-132, додають по 50мкл вказаного розчину на ямку з 1990]. Клітини висівають і залишають зв'язуватися 51 75055 52 з вмістом 96-ямкових планшетів в тому ж середона ямку). Випробувані сполуки розбавляють димевищі (Ham's F12) з 10% FBS (навколоплідною ситилсульфоксидом (ДМСО) і потім додають в роваткою теляти) протягом 6-8 годин. Клітини планшети з PGT так, щоб кінцева концентрація промивають, знову вводять живильне середовиДМСО в пробі становила 1,6% (об./об.). Рекомбіще, що не містить сироватки, і залишають інкубунантний фермент розбавляють фосфорилюючим ватися протягом ночі. Безпосередньо перед дозобуфером (50мМ Hepes, pH7,3, 125мМ NaCl, 24мМ ваним введенням сполуки клітини підгодовують MgCl2). Реакцію ініціюють додаванням АТФ до кінживильним середовищем, що не містить сироватцевої концентрації 10мкМ. Після 30-хвилинної інки. Випробувані сполуки, розчинені в ДМСО, розкубації при кімнатній температурі, при струшуванбавляють живильним середовищем (кінцева конні, реакційну суміш відстоюють і планшети центрація ДМСО 0,5% (об./об.)). По закінченні 10промивають промивним буфером (PBSхвилинного інкубування, PDGF-BB (кінцева концеутримуючим 0,1% Tween-20). Кількість фосфоринтрація 100нг/мл) додають до середовища і інкульованого PGT визначають шляхом інкубації з бують протягом 8 хвилин. Клітини промивають HRP, кон'югованої (HRP означає пероксидазу хроHepes буферним сольовим розчином (HBSS) і ліну) з антитілом PY-54, (Transduction Labs), проявзують в 50мкл HNTG буферного розчину (Hepes ляючи ТМВ пероксидазою (ТМВ означає 3,3', 5,5' 20мМ, pH7,5, NaCl 150мМ, TritonTM X-100 0,2%, тетраметилбензидин), і взаємодію оцінюють кількігліцерин 10% плюс PMSF (феніметилсульфонілфсно за допомогою зчитуючого пристрою BioRadTM торид) 0,2мМ, пепстатин 1мкг/мл, лейпептин Microplate при 450нМ. Інгібування ферментативної 1мкг/мл, апротонін 1мкг/мл, пірофосфат натрію активності кінази за допомогою випробуваної про2мМ, ортованадат натрію 2мМ) і потім розбавляявляючи виявляють по зниженою спектральною ють 50мкл HG розбавляючого буфера (Нерез проглинальною здатністю, і концентрацію сполуки, 20мМ, pH7,5, гліцерин 10%, PMSF (феніметилсунеобхідну для 50% придушення сигналу (в умовах льфонілфторид) 0,2мМ, пепстатин 1мкг/мл, лейвипробування), приводять як ІС50 значення для пептин 1мкг/мл, апротонін 1мкг/мл, пірофосфат випробуваної сполуки. натрію 2мМ, ортованадат натрію 2мМ). Міру фосДля оцінки здатності сполук інгібувати активність KDR тирозинкінази для повнорозмірного білфорилювання PDGFR вимірюють, використовуюка, існуючого в клітинному контексті, можуть бути чи випробування ELISA. 96- ямкові, покриті білком використані ендотеліальні клітини аорти свині Protein А планшети, блокують Superblock (Pierce) і (РАЕ), трансфіковані KDR людини [Waltenberger et покривають 0,5мкг на ямку анти-PDGFR Р20 анal., J. Biol. Chem. 269:26988, 1994]. Клітини висіватитілом [Santa Cruz, номер за каталогом SC-339]. ють і залишають зв'язуватися з вмістом 96Всі непов'язані антитіла вимивають з планшеямкових планшетів в тому ж середовищі (Ham's тів перед тим, як додати клітинний лізат. Після F12) з 10% FBS (навколоплідний сироваткою теляінкубування протягом 2 годин при кімнатній темпети). Потім клітини промивають, знову вводять жиратурі лізатів (50мкл) з антитілом PDGFR , вильне середовище, яке не містить сироватки, що PDGFR -пов'язаний фосфотирозин визначають включає 0,1% (об./об.) альбумін бичачої сироватки кількісно, проявляючи HRP, кон'югованої з антиті(BSA), і залишають інкубуватись протягом 24 голом PY-54, і ТМВ, як описано вище. Здатність сподин. Безпосередньо перед дозованим введенням лук інгібувати при умовах, що використовуються, сполуки клітини підгодовують живильним середоPDGF-BB-стимульовану реакцію аутофосфорилювищем, що не містить сироватки, (без ВSA). Вивання на 50%, в порівнянні з PDGF-BBпробувані сполуки, розчинені в ДМСО, розбавлястимульованими контролями, приводиться як ІС50 ють живильним середовищем (кінцева значення для випробуваної сполуки. Сполуки за концентрація ДМСО 0,5% (об./об.)). По закінченні даним винаходом, включаючи перераховані ниже 2-годинного інкубування, VEGF165 (кінцева конценприклади, при використанні вищезгаданої методитрація 50нг/мл) додають до середовища і інкубуки звичайно дають значення ІС50, то знаходяться в ють протягом 8 хвилин. Клітини промивають і лінаступних межах: 1-1000нМ. зують в HNTG буферному розчині (Hepes 20мМ, Випробування на активність за інгібуванням pH7,5, NaCl 150мМ, TritonTM X-100 0,2%, гліцерин KDR/VEGF рецептора 10%, PMSF (феніметилсульфонілфторид) 0,2мМ, Активність in vitro сполук за даним винаходом пепстатин 1мкг/мл, лейпептин 1мкг/мл, апротонін за інгібуванням KDR/VEGF рецептора може бути 1мкг/мл, пірофосфат натрію 2мМ, ортованадат визначена наступним способом. натрію 2мМ). Міру фосфорилювання KDR вимірюЗдатність сполук за даним винаходом інгібувають, використовуючи випробування ELISA. 96ти активність тирозинкінази може бути оцінена з ямкові планшети покривають 1мкг на ямку козячим використанням рекомбінантного ферменту у виантитілом кролячого антитіла. Непов'язане антитіпробуванні за вимірюванням здатності сполук інгіло вимивають з планшета і дільниці, що залишибувати фосфорилювання екзогенного субстрату, TM лися, блокують Superblock буферним розчином полiGluTyr (PGT, Sigma , 4:1). Домен кіназ (Pierce) перед додаванням анти-flk-1 С-20 антитіла KDRA/EGF людини рецептора (амінокислоти 805(0,5мкг на планшет, Santa Cruz). Всі непов'язані 1350) експресують в Sf9 клітинах комах як глютаантитіла вимивають з планшетів перед тим, як тіон-3-трансфраза(GSТ)-злитого білка, використододати клітинний лізат. Після інкубування протявуючи бакуловірусну систему експресії. Білок очигом 2 годин лізатів з flk-1 антитілом, KDRщають від лізатів вказаних клітин, використовуючи пов'язаний фосфотирозин визначають кількісно, афінні колонки з глютатіонагарозою. Випробуванпроявляючи HRP, кон'югованої з антитілом PY-54, ня на фермент здійснюють в 96-ямкових планшеі ТМВ, як описано вище. Здатність сполук інгібуватах, які покривають PGT субстратом (0,625мкг PGT 53 75055 54 ти VEGF-стимульовану реакцію аутофосфорилюцевтична композиція може включати загальнопвання на 50%, в порівнянні з VEGFрийнятий фармацевтичний носій або наповнювач і стимульованими контролями, приводиться як ІС50 сполука за винаходом як активний інгредієнт, крім значення для випробуваної сполуки. того, вказана композиція може включати інші ліВведення сполук за даним винаходом (тут і карські і фармацевтичні засоби, носії, допоміжні далі "активна сполука (сполука)") може бути ефекзасоби і т.д. тивним при будь-якому способі, що дає можлиХарактерні приклади форм для парентеральвість доставки сполук до дільниці впливу. Вказані ного введення включають розчини або суспензії способи включають пероральні способи, інтрадуоактивних сполук в стерильних водних розчинах, денальні способи, парентеральну ін'єкцію (вклюнаприклад, водних розчинах пропіленгліколю або чаючи внутрішньовенну, підшкірну, внутрішньом'ядекстрози. Вказані дозовані форми можуть, якщо зову, внутрішньосудинну або вливання), місцеве і потрібно, містити буферний розчин. ректальне введення. Відповідні фармацевтичні носії включають Кількість активної сполуки, що вводиться заінертні розріджувачі або наповнювачі, воду і різні лежить від вимагаючого лікування суб'єкта, важкоорганічні розчинники. Фармацевтичні композиції сті порушення або стану, швидкості введення, роможуть, якщо потрібно, містити додаткові інгредієзподілу сполуки і приписів, що встановлюється нти, такі як коригенти, зв'язуючі речовини, наповлікуючим лікарем. Однак, ефективна доза складає нювачі і тому подібне. Так, для перорального ввев межах приблизно від 0,001 до 100мг на кг масу дення можуть бути використані таблетки, що тіла на день, переважно, порядку 1-35мг/кг/день, у містять різну наповнювачі, таку як лимонна кисловигляді разової або розділеної загальної дози. Для та, разом з різними дезінтегрантами, такими як людини масою 70кг дана кількість повинна складакрохмаль, альгінова кислота і деякі комплексні ти порядку 0,05-7г/день, переважно, порядку 0,2силікати, і зі зв'язуючими агентами, такими як са2,5г/день. У деяких випадках рівні доз нижче нижхароза, желатин і сік акації. Додатково, замаслюньої межі вищезгаданого інтервалу можуть виявивачі, такі як стеарат магнію, лаурилсульфат натрію тися більш ніж адекватними, тоді як в інших випаді тальк, часто корисні в цілях таблетування. Тверді ках можуть бути використані ще більші дози, що не композиції подібного типу можна також використавикликають небажаного побічного ефекту, за умоти в м'яких і твердих наповнених желатинових кави, що вказані підвищені дози спочатку розділені псулах. Переважні матеріали для цього включають на декілька невеликих доз для прийому протягом лактозу або молочний цукор і поліетиленгліколі дня. високої молекулярної маси. Коли для пероральноАктивна сполука може використовуватися для го введення бажані водні суспензії або еліксири, незалежної терапії або може включати один або активна сполука в них може бути об'єднана з різбільше інших протипухлинних засобів, вибраних, ними підсолоджувачами або коригентами, фарбунаприклад, з групи, що включає; мітотичні інгібітовальними речовинами або барвниками і, якщо ри, наприклад, вібрастин; алкілуючі засоби, наприпотрібно, емультуючими агентами або суспендуюклад, цис-платин, карбоплатин і циклофосфамід; чими агентами, разом з розріджувачами, такими як антиметаболіти, наприклад, 5-фторурацил, цитовода, етанол, пропіленгліколь, гліцерин або їх зинарабінозид і гідроксисечовина, або, наприклад, комбінації. один з переважних метаболітів, описаних в євроСпособи одержання різних фармацевтичних пейській патентній заявці No.239362, такий як N(5композицій з певною кількістю активної сполуки [N(3,4-дигідро-2-метил-4-оксохіназолін-6-ілметил)відомі, або очевидні, для фахівців в даній області. N-метиламіно]-2-теноїл)-L-глутамінова кислота; Наприклад, див. Remington's Pharmaceutical інгібітори фактора зростання; інгібітори клітинного Sciences, Mack Publishing Company, Easter, Pa., циклу; інтеркалюючі антибіотики, наприклад, адрі15th Edition (1975). аміцин і блеоміцин; ферменти, наприклад, інтерПриклади і препаративні методики, приведені ферон; і антигормони, наприклад, антиестрогени, нижче, служать додатковою ілюстрацією і приклатакі як NolvadexTM (тамоксифен), або, наприклад, дами сполук за даним винаходом і способів одерантиандрогени, такі як CasodexTM (4'-ціано-3-(4жання вказаних сполук. Мається на увазі, що рамфторфенілсульфоніл)-2-гідрокси-2-метил-3'ки об'єму даного винаходу ніяким чином не (трифторметил) пропіон-анілід). Вказане спільне обмежуються рамками об'єму наступних прикладів лікування може здійснюватися одночасним, посліі препаративних методик. У наступних прикладах довним або роздільним дозованим введенням молекули з одним хіральним центром, якщо не індивідуальних компонентів, що використовуються обумовлено особливо, існують у вигляді рацемічдля лікування. ної суміші. Ті молекули, в яких є два або більше Фармацевтична композиція може, наприклад, хіральних центри, якщо не обумовлено особливо, існувати в формі, відповідній для перорального існують у вигляді рацемічної суміші діастереомевведення, такій як таблетка, капсула, пілюля, порів. Окремі енантіомери/діастереомери можуть рошок, склади уповільненого вивільнення, розчин, бути одержані за методиками, відомими фахівцям суспензія, для парентеральної ін'єкції такій, як в даній області. стерильні розчини, суспензія або емульсія, для Коли в препаративних методиках і прикладах, місцевого застосування, в такій формі як мазь або приведених нижче, згадується ВЕРХ хроматогракрем, або для ректального введення у вигляді суфія, звичайно використовуваними умовами, якщо позиторію. Фармацевтична композиція може існуне обумовлено особливо, є наступні. Використовати в дозованих лікарських формах, відповідних вують колонку ZORBAXTM RXC18 (виробництво для окремого введення точно певних доз. ФармаHewlett Packard), довжина 150мм і внутрішній діа 55 75055 56 метр 4,6мм. Зразки аналізують на системі Hewlett Приклад 1В Packard-1100. Використовують спосіб градієнтного ([8-(трет-бутилдиметилсиланілокси)хінолін-2елюювання, що зазнає зміни від 100-процентного іл]-(4-метокси-2-нітрофеніл)амін. ацетату амонію/буфер з оцтовою кислотою (0,2М) 8-(трет-бутилдиметилсиланілокси)хінолін-2до 100-процентного ацетонітрилу за 10 хвилин. іловий ефір трифтор-метансульфонової кислоти Після цього система переходить на цикл проми1А (9,81г, 24,1ммоль) і 4-метокси-2-нітроанілін вання 100-процентним ацетонітрилом протягом (4,86г, 28,9ммоль) розчиняють в 100мл діоксану в 1,5 хвилин і потім 100-процентним буферним розатмосфері сухого N2. До вказаного розчину додачином протягом 3 хвилин. Об'ємна витрата протяють (11,0г, 33,7ммоль) карбонат цезію (Cs2CO3), гом вказаного періоду постійна і дорівнює 3мл/хв. (900мг, 1,45ммоль) рацемічний 2,2'У наступних прикладах і препаративних методибіс(дифенілфосфіно)-1,1'-бінафтил (BINAP) і ках, "Et" означає етил, "Ас" означає ацетил, "Me" трис(дибензиліденацетон)дипаладій (0) (883мг, означає метил і "Вu" означає бутил. 0,964ммоль) і реакційну суміш нагрівають до Експериментальні Приклади 100°С і проводять реакцію при вказаній темпераПриклад 1 турі протягом 4 годин. Потім суміш охолоджують Синтез 1-[2-(5-метоксибензоімідазол-1до температури навколишнього середовища, коніл)хінолін-8-іл]піперидин-4-іламіну. центрують у вакуумі, обробляють ДХМ, фільтрують і концентрують у вакуумі, одержуючи червону тверду речовину. Тверду речовину очищають флеш-хроматографією на силікагелі, елююючи сумішшю гексан/ДХМ (3:1), одержуючи 7,25г вказаної в заголовку сполуки 1В у вигляді червоної твердої речовини. Приклад 1С Н1-[8-(трет-бутилдиметилсиланілокси)хінолін2-іл]-4-метокси-бензол-1,2-діамін. ([8-(трет-бутилдиметилсиланілокси)хінолін-2Приклад 1А іл]-(4-метокси-2-нітрофеніл) амін 1В (21,9г, 8-(трет-бутилдиметилсиланілокси)хінолін-251,3ммоль) розчиняють в суміші 200мл етанолу іловий ефір трифтор-метансульфонової кислоти. (EtOH) і 70мл ТГФ в атмосфері сухого N2. До вка2,8- Хіноліндіол (20,0г/ 124ммоль) суспендузаного розчину додають 10% паладій на вугіллі ють в 500мл дихлорметану (ДХМ) в атмосфері (2,18г) з подальшим додаванням краплями 10мл сухого азоту (N2). До вказаного розчину додають безводного гідразину. Реакційну суміш перемішуімідазол (20,3г, 298ммоль) з подальшим додаванють при температурі навколишнього середовища ням трет-бутилдиметилсилілхлориду (20,6г, протягом 2 годин, після чого фільтрують через 137ммоль) і 4-диметиламінопіридину (1,50г, Сеlitетм і Celite промивають ДХМ. Об'єднані фільт12,4ммоль). Реакційну суміш перемішують протярати концентрують у вакуумі і одержаний залишок гом ночі при температурі навколишнього середорозподіляють між ДХМ і водним насиченим вища, після чого розподіляють між ДХМ і 1% водNaHCO3. ДХМ шар потім промивають знов насиним бісульфатом натрію (NaHSO4). ДХМ шар ченим NaHCO3 і потім насиченим розчином солі, зберігають і промивають ще два рази 1% водним сушать над Na2SO4, фільтрують і концентрують у NaHSO4, потім насиченим водним бікарбонатом вакуумі, одержуючи 18,3г жовтувато-коричневої натрію (NaHCO3) і, нарешті, насиченим розчином твердої речовини, що є вказаною в заголовку спосолі. ДХМ шар сушать над сульфатом натрію лукою 1С. (Na2SO4), фільтрують і концентрують у вакуумі, Приклад 1D одержуючи неочищений продукт (40г) у вигляді 2-(5-Метоксибензоімідазол-1-іл)хінолін-8-ол. білої твердої речовини. Тверду речовину розчиN1-[8-(трет-бутилдиметилсиланілокси)хінолінняють в 500мл безводного тетрагідрофурану (ТГФ) 2-іл]-4-метокси-бензол-1,2-діамін 1С (18,3г, в атмосфері сухого N2. До вказаного розчину до46,1ммоль) розчиняють в 40мл 2-метоксіетанолу в дають N-фенілбіс(трифторметансульфонімід) атмосфері сухого N2. До вказаного розчину дода(48,7г, 136ммоль) і розчин охолоджують до 0°С. До ють формамідинацетат (5,28г, 50,7ммоль) і реаквказаного розчину повільно додають (3,2г, ційну суміш нагрівають до 125°С і проводять реак136ммоль) гідрид натрію (60% в маслі). Після зацію при вказаній температурі протягом 1,5 годин. вершення додавання реакційну суміш нагрівають Розчинник видаляють у вакуумі і тверду речовину, до температури навколишнього середовища. Чещо залишилася, розтирають з діетиловим ефіром рез 1 годину додають додатково 1,00г гідриду на(Еt2О) r сушать у вакуумі і одержують 13,3г рожетрію (60% в маслі) і перемішують ще 30 хвилин. вої твердої речовини, що є вказаною в заголовку Суміш концентрують у вакуумі і розчиняють в сполукою 1D. ДХМ. Повільно краплями додають воду (1,0мл), Приклад 1E щоб погасити весь непрореагувавший гідрид на2-(5-Метоксибензоімідазол-1-іл)хінолін-8трію, і потім реакційну суміш двічі екстрагують іловий ефір трифтор-метансульфонової кислоти. 0,1н. водним гідроксидом натрію (NaOH) і потім 2-(5-Метоксибензоімідазол-1-іл)хінолін-8-ол 1D промивають насиченим розчином солі. ДХМ шар (13,9г, 47,8ммоль) розчиняють в 100мл безводного сушать над Na2SO4 фільтрують і концентрують у ТГФ в атмосфері сухого N2. До вказаного розчину вакуумі, одержуючи 57г неочищеного трифлату 1Α додають N-фенілбіс (трифторметансульфонімід) у вигляді жовтого масла. (20,3г, 47,8ммоль) і потім розчин охолоджують до 57 75055 58 0°С. До вказаного розчину повільно додають бензоімідазол-5-ол. (1,31г, 54,9ммоль) гідрид натрію (60% в маслі). Після завершення додавання реакційну суміш нагрівають до температури навколишнього середовища. Через 30 хвилин додають ще 500мг гідриду натрію (60% в маслі) з подальшим додаванням 3,50г N-фенілбіс (трифторметансульфоніміду) і реакційну суміш перемішують при температурі навколишнього середовища протягом 1 години. Потім розчинник видаляють у вакуумі і одержаний залишок розчиняють в ДХМ. До вказаного розчину 1-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8повільно додають 1,0мл води для розкладання іл]піперидин-4-іламін 1 (500мг, 1,10ммоль) розчинепрореагувавшого гідриду натрію. Потім суміш няють в 10мл ДХМ в атмосфері сухого N2. До вкарозподіляють між ДХМ і 0,1 н. водним NaOH. ДХМ заного розчину додають трибромід бору (300мкл, шар потім знову промивають 0,1 н. водним NaOH з 3,30ммоль) і суміш перемішують протягом ночі при подальшим промиванням насиченим розчином температурі навколишнього середовища. Потім солі і потім сушать над сульфатом магнію (MgSO4, додають додатково 200мкл триброміду бору і суфільтрують і концентрують у вакуумі, одержуючи міш перемішують протягом двох годин. Реакційну 20,7г рожевої твердої речовини, що є вказаною в суміш виливають потім на колений лід і pH розчизаголовку сполукою 1E. ну, що утворився, доводять до 9 обережним додаПриклад 1F ванням карбонату натрію (Na2СО3). Суспензію фітрет-Бутиловий ефір {1-[2-(5льтрують і тверду речовину промивають водою і метоксибензоімідазол-1-іл)хінолін-8-іл]піперидинпотім Еt2О, потім сушать у вакуумі, одержуючи 4-іл}карбамінової кислоти вказану в заголовку сполуку 2 у вигляді жовтої 2-(5-Метоксибензоімідазол-1-іл)хінолін-8твердої речовини. іловий ефір трифторметансульфонової кислоти 1E (15,0г, 35,4ммоль) і трет-бутиловий ефір піперидин-4-ілкарбамінової кислоти (14,2г, 70,9ммоль) розчиняють в 200мл діоксану в атмосфері сухого N2. До вказаного розчину додають Cs2CO3 (16,2г, 49,6ммоль), рацемічний BINAP (1,28г, 2,12ммоль) і Приклад 3 трис(дибензиліден-ацетон)дипаладій (0) (1,29г, 1-{2-[5-(Піридин-2-ілметокси)бензоімідазол-11,41ммоль) і реакційну суміш нагрівають до 100°С і іл]хінолін-8-іл}піперидин -4-іламін. проводять реакцію при вказаній температурі протягом ночі. Суміш потім охолоджують до температури навколишнього середовища, фільтрують і концентрують у вакуумі, одержуючи оранжеву піну. Піну очищають флеш-хроматографією на силікагелі з градієнтним елююванням від етилацетату (ЕtOАс)/ДХМ (1:5) до ЕtOАс/ДХМ (7:3), одержуючи 12,3г вказаної в заголовку сполуки 1F у вигляді злегка жовтуватої твердої речовини. Приклад 1G Приклад 3А 1-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8трет-Бутиловий ефір {1-[2-(5іл]піперидин-4-іламін. гідроксибензоімідазол-1-іл)xінолін-8-iл]піперидинтрет-бутиловий ефір {1-[2-(54іл}карбамінової кислоти. метоксибензоімідазол-1-іла)хінолін-8-іл]піперидин1-[8-(4-Амінопіперидин-1-іл)хінолін-2-іл]-1Н4-іл}карбамінової кислоти 1F (8,40г, 17,7ммоль) бензоімідазол-5-ол 2 (460мг, 1,30ммоль) розчинярозчиняють в 50мл трифтороцтової кислоти (ТФО) ють в 5мл безводного ДМФ в атмосфері сухого N2. в атмосфері сухого N2. Реакційну суміш переміДо вказаного розчину додають ди-третшують при температурі навколишнього середовибутилдикарбонат (279мг, 1,30ммоль) і реакційну ща протягом 15 хвилин, після чого концентрують у суміш перемішують при температурі навколишньовакуумі, одержуючи жовте масло. Масло розподіго середовища протягом ночі. ляють між ДХМ і 0,1 н. водним NaOH. ДХМ шар Потім реакційну суміш концентрують у вакуумі промивають знову ОД н. водним NaOH. ДХМ шар і розподіляють між ДХМ і водним насиченим сушать над Na2SO4, фільтрують і концентрують, NaHCO3. ДХМ шар сушать над Na2SO4, фільтруодержуючи 5,85г вказаної в заголовку сполуки 1 у ють і концентрують у вакуумі, одержуючи жовту вигляді жовтої твердої речовини. тверду речовину. Тверду речовину очищають флеш-хроматографією на силікагелі, елююючи EtOAc, одержуючи 273мг вказаної в заголовку сполуки 3А у вигляді жовтої твердої речовини. Приклад 3В трет-Бутиловий ефір (1-{2-[5-(піридин-2ілметокси)бензоімідазол-1-іл]хінолін-8Приклад 2 іл}піперидин-4-іл)карбамінової кислоти 1-[8-(4-Амінопіперидин-1-іл)хінолін-2-іл]-1Нтрет-Бутиловий ефір {1-[2-(5 59 75055 60 гідроксибензоімідазол-1-іл)хінолін-8-іл]піперидин4-іл}карбамінової кислоти 3А (73мг, 0,16ммоль) розчиняють в 1мл безводного ДМФ в атмосфері сухого N2. До вказаного розчину додають (37мг, 0,17ммоль) калійбіс(триметилсиліл)амід (95%) з Приклад 5 подальшим додаванням 2-піколілхлориду (25мкл, {4-[2-(5-Метоксибензоімідазол-1-іл)хінолін-80,17ммоль). Реакційну суміш перемішують протяіл]бензил}метиламін. гом ночі при температурі навколишнього середовища, після чого реакційну суміш концентрують у вакуумі і потім розподіляють між ДХМ і водним насиченим NaHCO3- ДХМ шар сушать над Na2SO4, фільтрують і концентрують у вакуумі, одержуючи жовтий гель. Гель очищають флешхроматографією на силікагелі з градієнтним елююванням від ДХМ до ДХМ/МеОН (98:2), одержуючи 55мг вказаної в заголовку сполуки 3В. Приклад 3С 1-{2-[5-(Піридин-2-ілметокси)бензоімідазол-1Приклад 5А іл]хінолін-8-іл}піперидин -4-іламін. 4-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8трет-Бутиловий ефір (1-{2-[5-(піридин-2іл]бензальдегід. ілметокси)бензоімід-азол-1-іл]хінолін-82-(5-Метоксибензоімідазол-1-іл)хінолін-8іл}піперидин-4-іл)карбамінової кислоти 3В (55мг, іловий ефір трифтор-метансульфонової кислоти 0,094ммоль) розчиняють в 1мл ТФО в атмосфері 1E (265мг, 0,630ммоль) розчиняють в 3мл діоксану сухого N2 і перемішують протягом 15 хвилин при в атмосфері сухого N2. До вказаного розчину дотемпературі навколишнього середовища. Реакційдають 4-формілбензолборонову кислоту (145мг, ну суміш концентрують потім у вакуумі, одержуючи 0,940ммоль), фосфат калію (267мг, 1,26ммоль) і масло, яке потім розподіляють між ОД н. водним тетракис(трифеніл-фосфін)паладій(0) (36мг, NaOH і ДХМ. ДХМ шар сушать над Na2SO4, фільт0,032ммоль). Реакційну суміш нагрівають до 105°С рують і концентрують у вакуумі, одержуючи 38,9мг і проводять реакцію при вказаній температурі прожовтої плівки, що є вказаною в заголовку сполутягом ночі. Реакційну суміш охолоджують потім до кою 3. температури навколишнього середовища, концентрують у вакуумі і розподіляють між ДХМ і насиченим водним NaНСО3. ДХМ шар промивають потім насиченим розчином солі, сушать над Na2SO4, фільтрують і концентрують у вакуумі, одержуючи жовту тверду речовину, що є вказаною в заголовку Приклад 4 сполукою 5А, яку використовують надалі без дода{1-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8ткового очищення. іл]піперидин-4-іл} диметиламін. Приклад 5В {4-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8іл]бензил}метиламін. 4-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8іл]бензальдегід 5А (120мг, 0,32ммоль) розчиняють в 2мл метанолу в атмосфері сухого N2. До вказаного розчину додають 800мкл розчину 2,0Μ метиламіну в метанолі і потім додають краплями оцтову кислоту (АсОН) до pH розчину -5. До вказаного розчину додають (42мг, 0,64ммоль) ціаноборгідрид натрію (NaCNBH3) і реакційну суміш перемішують при температурі навколишнього середовища протягом ночі. Реакційну суміш концентрують потім у 1-[2-(5-Метоксибензоімідазол-1-іл)хінолін-8вакуумі і потім розподіляють між ДХМ і 0,1 н. воділ]піперидин-4-іламін 1 (160мг, 0,43ммоль) розчиним NaOH. ДХМ шар промивають знову 0,1 н, водняють в 2мл хлороформу в атмосфері сухого N2. ним NaOH, потім сушать над MgSO4, фільтрують і До вказаного розчину додають 50мкл 37% водного концентрують у вакуумі, одержуючи 220мг зеленоформальдегіду і 100мкл мурашиної кислоти і реаго залишку. Залишок очищають флешкційну суміш потім нагрівають до 65°С і проводять хроматографією на силікагелі з градієнтним елюреакцію при вказаній температурі протягом 4 гоюванням ДХМ/МеОН (5/95)-ДХМ/МеОН (15/85)дин. Реакційну суміш потім розподіляють між ДХМ ДХМ/МеОН/МН4ОН (15/84,5/0,5), одержуючи 50мг і 0,1 н. водним NaOH. ДХМ шар сушать над білої твердої речовини, що є вказаною в заголовку Na2SO4, фільтрують і концентрують у вакуумі, сполукою 5. одержуючи оранжеву тверду речовину, що є вказаною в заголовку сполукою 4.
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzoimidazole derivatives being used as antiproliferative agent, pharmaceutical composition based thereon
Автори англійськоюLuzzio Michael Joseph
Назва патенту російськоюПроизводные бензоимидазола, которые применяются как антипролиферативное средство, фармацевтическая композиция на их основании
Автори російськоюЛуццио Майкл Джозеф
МПК / Мітки
МПК: C07D 471/04, A61P 17/00, A61K 31/496, C07D 401/04, C07D 521/00, A61P 17/06, A61P 1/18, C07D 413/14, A61P 9/10, C07D 491/04, A61K 31/5377, A61P 29/00, C07D 491/107, C07D 491/10, A61P 43/00, C07D 491/056, C07D 401/14, A61P 17/04, A61P 35/00, A61K 31/4709, A61P 27/02, A61P 13/08, A61P 13/12, A61P 3/10
Мітки: бензоімідазолу, композиція, антипроліферативний, основі, фармацевтична, засіб, похідні, використовуються
Код посилання
<a href="https://ua.patents.su/73-75055-pokhidni-benzoimidazolu-shho-vikoristovuyutsya-yak-antiproliferativnijj-zasib-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні бензоімідазолу, що використовуються як антипроліферативний засіб, фармацевтична композиція на їх основі</a>












