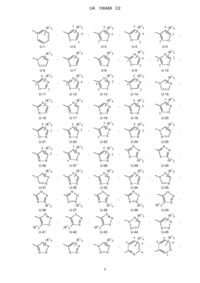
Спосіб одержання 3-трифторметильних халконів
Формула / Реферат
1. Спосіб одержання сполуки Формули 1
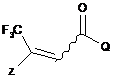 , 1
, 1
де
Z являє собою необов'язково заміщений феніл; і
Q являє собою феніл або 1-нафталеніл, кожен необов'язково заміщений;
що включає етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2:
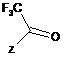 , 2
, 2
сполуку Формули 3:
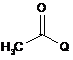 , 3
, 3
основу, яка містить щонайменше одну сполуку, вибрану з групи, що включає гідроксиди лужноземельного металу Формули 4:
М(ОН)2, 4
де М являє собою Са, Sr або Ва,
карбонати лужного металу Формули 4а:
(M1)2СО3, 4а
де М1 являє собою Li, Na або K,
1,5-діазабіцикло[4.3.0]нон-5-ен і 1,8-діазабіцикло[5.4.0]ундец-7-ен, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою.
2. Спосіб за п. 1, який відрізняється тим, що основа включає гідроксид лужноземельного металу Формули 4, та суміш додатково включає полярний апротонний розчинник.
3. Спосіб за п. 2, який відрізняється тим, що М являє собою Са.
4. Спосіб за п. 2, який відрізняється тим, що полярний апротонний розчинник включає N,N-диметилформамід.
5. Спосіб за п. 2, який відрізняється тим, що апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, включає тpeт-бутилметиловий ефір.
6. Спосіб за п. 1, який відрізняється тим, що основа включає карбонат лужного металу Формули 4а.
7. Спосіб за п. 6, який відрізняється тим, що М1 являє собою K.
8. Спосіб за п. 1, де основа включає 1,5-діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміш.
9. Спосіб за будь-яким одним з пп. 6, 7 або 8, який відрізняється тим, що апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, включає ацетонітрил.
10. Спосіб за п. 1, який відрізняється тим, що:
Z являє собою феніл, що необов'язково має до 5 замісників, незалежно вибраних з R2;
Q являє собою феніл або 1-нафталеніл, кожен необов'язково має до 4 замісників, незалежно вибраних з R3;
кожен R2 являє собою незалежно галоген, C1-С6алкіл, C1-С6галоалкіл, C1-С6алкокси, C1-С6галоалкокси, C1-С6алкілтіо, C1-С6галоалкілтіо, C1-С6алкіламіно, C2-С6діалкіламіно, -CN або -NO2;
кожен R3 являє собою незалежно галоген, C1-С6алкіл, C1-С6галоалкіл, C2-С6алкеніл, C2-С6галоалкеніл, C2-С6алкініл, C3-С6галоалкініл, C3-С6циклоалкіл, C3-С6галоциклоалкіл, C1-С6алкокси, C1-С6галоалкокси, C1-С6алкілтіо, C2-С7алкілкарбоніл, C2-С7галоалкілкарбоніл, C1-С6галоалкілтіо, C1-С6алкілсульфініл, C1-С6галоалкілсульфініл, C1-С6алкілсульфоніл, C1-С6галоалкілсульфоніл, -N(R4)R5, -C(=W)N(R4)R5, -C(=W)OR5, -CN, -OR11 або -NO2; або фенільне кільце, або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце необов'язково заміщене одним або більше замісниками, незалежно вибраними з галогену, C1-С6алкілу, C1-С6галоалкілу, C3-С6иклоалкілу, C3-С6галоциклоалкілу, C1-С6алкокси, C1-С6галоалкокси, C1-С6алкілтіо, C1-С6галоалкілтіо, C1-С6алкілсульфінілу, C1-С6галоалкілсульфінілу, C1-С6алкілсульфонілу, C1-С6галоалкілсульфонілу, -CN, -NO2, -N(R4)R5, -C(=W)N(R4)R5, -C(=O)OR5 i R7;
кожен R4 являє собою незалежно Н, C1-С6алкіл, C2-С6алкеніл, C2-С6алкініл, C3-С6циклоалкіл, C4-С7алкілциклоалкіл, C4-С7циклоалкілалкіл, C2-С7алкілкарбоніл або C2-С7алкоксикарбоніл;
кожен R5 являє собою незалежно Н; або C1-С6алкіл, C2-С6алкеніл, C2-С6алкініл, C3-С6циклоалкіл, C4-С7алкілциклоалкіл або C4-С7циклоалкілалкіл, кожен необов'язково заміщений одним або більше замісниками, незалежно вибраними з R6;
кожен R6 являє собою незалежно галоген, C1-С6алкіл, C1-С6алкокси, C1-С6алкілтіо, C1-С6алкілсульфініл, C1-С6алкілсульфоніл, C1-С6алкіламіно, C2-С8діалкіламіно, C3-С6циклоалкіламіно, C2-С7алкілкарбоніл, C2-С7алкоксикарбоніл, C2-С7алкіламінокарбоніл, C3-С9діалкіламінокарбоніл, C2-С7галоалкілкарбоніл, C2-С7галоалкоксикарбоніл, C2-С7галоалкіламінокарбоніл, C3-С9галодіалкіламінокарбоніл, -ОН, -NH2, -CN або -NO2; або Q1;
кожен R7 являє собою незалежно фенільне кільце або піридинільне кільце, кожне кільце необов'язково заміщене одним або більше замісниками, незалежно вибраними з R8;
кожен R8 являє собою незалежно галоген, C1-С6алкіл, C1-С6галоалкіл, C1-С6алкокси, C1-С6галоалкокси, C1-С6алкілтіо, C1-С6галоалкілтіо, C1-С6алкілсульфініл, C1-С6галоалкілсульфініл, C1-С6алкілсульфоніл, C1-С6галоалкілсульфоніл, C1-С6алкіламіно, C2-С6діалкіламіно, C2-С4алкілкарбоніл, C2-С4алкоксикарбоніл, C2-С7алкіламінокарбоніл, C3-С7діалкіламінокарбоніл, -ОН, -NH2, -C(=O)OH, -CN або -NO2;
кожен Q1 являє собою незалежно фенільне кільце або 5- або 6-членне насичене або ненасичене, гетероциклічне кільце, кожне кільце необов'язково заміщене одним або більше замісниками, незалежно вибраними з галогену, C1-С6алкілу, C1-С6галоалкілу, C3-С6циклоалкілу, C3-С6галоциклоалкілу, C1-С6алкокси, C1-С6галоалкокси, C1-С6алкілтіо, C1-С6галоалкілтіо, C1-С6алкілсульфінілу, C1-С6галоалкілсульфінілу, C1-С6алкілсульфонілу, C1-С6галоалкілсульфонілу, C1-С6алкіламіно, C2-С6діалкіламіно, -CN, -NO2, -C(=W)N(R9)R10 і -C(=O)OR10;
кожен R9 являє собою незалежно Н, C1-С6алкіл, C1-С6галоалкіл, C2-С6алкеніл, C2-С6алкініл, C3-С6циклоалкіл, C4-С7алкілциклоалкіл, C4-С7циклоалкілалкіл, C2-С7алкілкарбоніл або C2-С7алкоксикарбоніл;
кожен R10 являє собою незалежно Н; або C1-С6алкіл, C1-С6галоалкіл, C2-С6алкеніл, C2-С6алкініл, C3-С6циклоалкіл, C4-С7алкілциклоалкіл або C4-С7циклоалкілалкіл;
кожен R11 являє собою незалежно Н; або C2-С6алкеніл, C2-С6алкініл, C3-С6циклоалкіл, C4-С7алкілциклоалкіл, C4-С7циклоалкілалкіл, C2-С7алкілкарбоніл, C2-С7алкоксикарбоніл, C1-С6алкілсульфоніл або C1-С6галоалкілсульфоніл; і
кожен W являє собою незалежно О або S.
11. Спосіб за п. 10, який відрізняється тим, що
Z являє собою 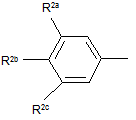 ;
;
Q являє собою 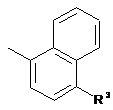 ;
;
R2a являє собою галоген, C1-С2галоалкіл або C1-С2галоалкокси;
R2b являє собою Н, галоген або ціано;
R2c являє собою Н, галоген або CF3;
R3 являє собою C(O)N(R4)R5або C(O)OR5a;
R4 являє собою Н, С2-С7алкілкарбоніл або C2-С7алкоксикарбоніл; і
R5 являє собою C1-С6алкіл або C1-С6галоалкіл, кожен заміщений одним замісником, незалежно вибраним з гідрокси, C1-С6алкокси, C1-С6алкілтіо, C1-С6алкілсульфінілу, C1-С6алкілсульфонілу, C2-С7алкіламінокарбонілу, C3-С9діалкіламінокарбонілу, C2-С7галоалкіламінокарбонілу та C3-С9галодіалкіламінокарбонілу; і
R5a являє собою C1-С6алкіл, C2-С6алкеніл або C2-С6алкініл, кожен необов'язково заміщений одним або більше замісниками, незалежно вибраними з галогену, C1-С2алкокси та фенілу, що необов'язково має до 5 замісників, вибраних з галогену та C1-С3алкілу.
12. Спосіб за п. 1, де
Z являє собою феніл, що необов'язково має до 5 замісників, незалежно вибраних з R2; і
кожен R2 являє собою незалежно F, Сl, Вr, C1-С6алкіл, C1-С6фторалкіл, C1-С6алкокси, C1-С6фторалкокси, C1-С6алкілтіо або C1-С6фторалкілтіо; додатково включає одержання сполуки Формули 2, при якому
(1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5
Z-X, 5
де X являє собою Сl, Вr або І,
приведенням у контакт сполуки Формули 5 з
(a) металевим магнієм або
(b) галогенідом алкілмагнію
у присутності ефірного розчинника; та потім
(2) приводять у контакт реакційну суміш зі сполукою Формули 6:
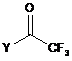 , 6
, 6
де
Y являє собою OR11 або NR12R13;
R11 являє собою C1-С5 алкіл; і
R12 і R13 являють собою незалежно C1-С2алкіл; або R12 і R13 взяті разом як -СН2СН2ОСН2СН2-.
13. Спосіб за п. 12, який відрізняється тим, що Z являє собою
 ;
;
де
R2a являє собою F, Сl, Вr, С1-С2фторалкіл або C1-С2фторалкокси;
R2b являє собою Н, F, Сl або Вr; і
R2c являє собою Н, F, Сl, Вr або CF3.
14. Спосіб за п. 1, який відрізняється тим, що основа містить щонайменше одну сполуку, вибрану з групи, що включає гідроксиди лужноземельного металу Формули 4:
М(ОН)2, 4
де М являє собою Са, Sr або Ва,
1,5-діазабіцикло[4.3.0]нон-5-ен і 1,8-діазабіцикло[5.4.0]ундец-7-ен.
Текст
Реферат: Розкритий винахід являє собою спосіб одержання сполуки Формули 1, де Q і Z є такими, як визначено у розкритті, що включає дистиляцію води із суміші, яка містить сполуку Формули 2, сполуку Формули 3, основу, що містить, щонайменше, одну сполуку, вибрану з групи, що містить гідроксиди лужноземельного металу Формули 4, де М являє собою Са, Sr або Ва, 1 карбонати лужного металу Формули 4а, де М являє собою Li, Na або K, 1,5діазабіцикло[4.3.0]нон-5-ен і 1,8-діазабіцикло[5.4.0]ундец-7-ен, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. UA 106468 C2 (12) UA 106468 C2 O F3C Q z O F3C O z 1 H3C Q 3 2 M(OH)2 (M1)2CO3 4 4a Також розкритий винахід являє собою спосіб одержання сполуки Формули 2, при якому (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий приведенням у контакт сполуки Формули 5, де X являє собою Сl, Вr або І, з металевим магнієм або галогенідом алкілмагнію в присутності ефірного розчинника, і потім (2) приводять у контакт реакційну суміш 11 12 13 11 12 13 зі сполукою Формули 6, де Y являє собою OR або NR R , і R , R і R є такими, як визначено у розкритті. O Z-X 5 Y F3C CF3 6 O z N Q 7 Додатково даний винахід розкриває спосіб одержання сполуки Формули 7, де Q і Z є такими, як визначено у розкритті, коли застосовують сполуку Формули 1, що відрізняється одержанням сполуки Формули 1 способом, розкритим вище, або застосовують сполуку Формули 1, отриману способом, розкритим вище. UA 106468 C2 5 ГАЛУЗЬ ВИНАХОДУ Даний винахід відноситься до способу одержання 3-трифторметильних халконів і трифторацетильних проміжних сполук. Даний винахід також відноситься до нових трифторацетильних і галосполук, застосовних як вихідні речовини та проміжні сполуки для раніше описаного способу. КОРОТКИЙ ОПИС ВИНАХОДУ Даний винахід забезпечує спосіб одержання сполуки Формули 1 O F3C Q Z 10 1 , де Z являє собою факультативно заміщений феніл; і Q являє собою феніл або 1-нафталеніл, кожен факультативно заміщений; що включає етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2 F3C O Z 2 , 15 сполуку Формули 3 O H3C Q 3 20 , основу, що містить, щонайменше, одну сполуку, вибрану з групи, що включає гідроксиди лужноземельного металу Формули 4 M(OH)2 4 , де M являє собою Ca, Sr або Ba, карбонати лужного металу Формули 4a (M1)2CO3 25 4a , 1 де M являє собою Li, Na або K, 1,5-діазабіцикло[4.3.0]нон-5-ен і 1,8-діазабіцикло[5.4.0]ундец-7-ен, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. Даний винахід також забезпечує спосіб одержання сполуки Формули 2, де Z являє собою факультативно заміщений феніл, що включає етапи, на яких (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5 30 Z–X 5 35 , де X являє собою Cl, Br або I, приведенням у контакт сполуки Формули 5 з (a) металевим магнієм або (b) галогенідом алкілмагнію 1 UA 106468 C2 у присутності ефірного розчинника; та потім (2) приводять у контакт реакційну суміш зі сполукою Формули 6 O Y CF3 6 5 10 15 , де 11 12 13 Y являє собою OR або NR R ; 11 R являє собою C1–C5 алкіл; і 12 13 12 13 R і R являють собою незалежно C1–C2 алкіл; або R і R взяті разом як -CH2CH2OCH2CH2-. Даний винахід також забезпечує спосіб одержання сполуки Формули 2, де Z являє собою 2 2 феніл, що факультативно має до 5 замісників, незалежно вибраних з R ; і кожен R являє собою незалежно F, Cl, Br, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1–C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо, що включає етапи, на яких (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5 Z–X 5 20 , де X являє собою I, приведенням у контакт сполуки Формули 5 з (a) металевим магнієм або (b) галогенідом алкілмагнію у присутності ефірного розчинника; та потім (2) приводять у контакт реакційну суміш зі сполукою Формули 6 O Y CF3 6 , 25 30 де 11 12 13 Y являє собою OR або NR R ; 11 R являє собою C1–C5 алкіл; і 12 13 12 13 R і R являють собою незалежно C1–C2 алкіл; або R і R взяті разом як -CH2CH2OCH2CH2-. Даний винахід також відноситься до розкритого вище способу одержання сполуки Формули 1 зі сполуки Формули 2 і сполуки Формули 3, де спосіб додатково відрізняється тим, що одержують сполуку Формули 2 зі сполук Формул 5 і 6 за допомогою способу, розкритого вище. Даний винахід також відноситься до способу одержання сполуки Формули 7 35 F 3C O Z Q 7 40 N , де Z являє собою факультативно заміщений феніл; і Q являє собою феніл або 1-нафталеніл, кожен факультативно заміщений; із застосуванням сполуки Формули 1. Спосіб відрізняється етапами, на яких (a) одержують сполуку Формули 1 за допомогою способу, розкритого вище, або (b) застосовують, як зазначену сполуку Формули 1, сполуку Формули 1, отриману за допомогою способу, розкритого вище. 2 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід також відноситься до нових сполук Формул 2 і 5, застосовних як вихідні речовини для раніше описаних способів. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Застосовувані тут вирази "включає", "що включає", "містить", "що містить", "має" "що має", "вміщує" або "що вміщує", або будь-який інший їхній варіант, призначені, щоб розглядати невиняткове включення. Наприклад, композиція, суміш, процес, спосіб, виріб або прилад, що включає перелік елементів, не обов'язково обмежується тільки тими елементами, а може включати й інші елементи, явно не перелічені або властиві такій композиції, суміші, процесу, способу, виробу або приладу. Крім того, якщо прямо не зазначене інше, "або" відноситься до або, що включає, і або, що не виключає. Наприклад, умова A або B задовольняє одному з наступного: A - істина (або є присутньою), і B - хибність (або не є присутньою), A - хибність (або не є присутньою), і B - хибність (або є присутньою), і A, і B - хибність (або є присутніми). Також, форми однини попереднього елементу або компоненту даного винаходу призначені, щоб бути необмежуючими відносно числа прикладів (тобто, подій) елементу або компоненту. Тому форму однини варто читати як таку, що включає один або, щонайменше, один, і форма однини слова елементу або компоненту також включає множину, якщо явно не мається на увазі однина. У вищевикладених перерахуваннях вираз "алкіл", застосовуваний або самостійно, або в сполученні слів, таких як "алкілтіо" або "галоалкіл", включає нерозгалужений або розгалужений алкіл, такий як метил, етил, n- пропіл, i-пропіл або різні ізомери бутилу, пентилу або гексилу. "Алкокси" включає, наприклад, метокси, етокси, n-пропілокси, ізопропілокси та різні ізомери бутокси, пентокси та гексилокси. "Алкілтіо" включає розгалужені або нерозгалужені алкілтіо частини, такі як метилтіо, етилтіо і різні ізомери пропілтіо, бутилтіо, пентилтіо та гексилтіо. "Алкілсульфініл" включає обидва енантіомери алкілсульфінільної групи. Приклади "алкілсульфінілу" включають CH3S(O)-, CH3CH2S(O)-, CH3CH2CH2S(O)-, (CH3)2CHS(O)- і різні ізомери бутилсульфінілу, пентилсульфінілу та гексилсульфінілу. Приклади "алкілсульфонілу" включають CH3S(O)2-, CH3CH2S(O)2-, CH3CH2CH2S(O)2-, (CH3)2CHS(O)2- і різні ізомери бутилсульфонілу, пентилсульфонілу та гексилсульфонілу. "Алкіламіно", "діалкіламіно" і подібне визначається аналогічно вищевикладеним прикладам. "Циклоалкіл" включає, наприклад, циклопропіл, циклобутил, циклопентил і циклогексил. Вираз "алкілциклоалкіл" означає алкільну заміну у циклоалкільній частини та включає, наприклад, етилциклопропіл, ізопропілциклобутил, 3-метилциклопентил і 4-метилциклогексил. Вираз "циклоалкілалкіл" означає циклоалкільну заміну в алкільній частини. Приклади "циклоалкілалкілу" включають циклопропілметил, циклопентилетил і інші циклоалкільні частини, зв'язані з нерозгалуженими або розгалуженими алкільними групами. Вираз "галоген", або самостійно або в сполученні слів, таких як "галоалкіл", або коли застосовують в описах, таких як "алкіл, заміщений галогеном", включає фтор, хлор, бром або йод. Додатково, коли застосовують у сполученні слів, таких як "галоалкіл", або коли застосовують в описах, таких як "алкіл, заміщений галогеном", зазначений алкіл може бути частково або повністю заміщений атомами галогенів, що можуть бути однаковими або різними. Подібним чином "фторалкіл" означає зазначений алкіл, що може бути частково або повністю заміщений атомами фтору. Приклади "галоалкілу" або "алкілу, заміщеного галогеном" включають F3C-, ClCH2-, CF3CH2- і CF3CCl2-. Вираз "галоциклоалкіл", "галоалкокси", "галоалкілтіо", "галоалкілсульфініл", "галоалкілсульфоніл" і подібне визначаються аналогічно виразу "галоалкіл". Приклади "галоалкокси" включають CF 3O-, CCl3CH2O-, HCF2CH2CH2O- і CF3CH2O-. Приклади "галоалкілтіо" включають CCl3S-, CF3S-, CCl3CH2S- і ClCH2CH2CH2S-. Приклади "галоалкілсульфінілу" включають CF 3S(O)-, CCl3S(O)-, CF3CH2S(O)- і CF3CF2S(O)-. Приклади "галоалкілсульфонілу" включають CF 3S(O)2-, CCl3S(O)2-, CF3CH2S(O)2- і CF3CF2S(O)2-. Вираз "галодіалкіламіно" означає діалкіламіно, де, щонайменше, один з аміно компонентів є заміщеним, щонайменше, одним галогеном. Приклади "галодіалкіламіно" включають CH2ClCH2N(CH3)- і (CF3CH2)2N-. "Алкілкарбоніл" означає нерозгалужені або розгалужені алкільні частини, зв'язані з C(=O) частиною. Приклади "алкілкарбонілу" включають CH 3C(=O)-, CH3CH2CH2C(=O)і (CH3)2CHC(=O)-. Приклади "алкоксикарбонілу" включають CH 3 °C(=O)-, CH3CH2 °C(=O)-, CH3CH2CH2 °C(=O)-, (CH3)2CHOC(=O)- і різні ізомери бутокси або пентоксикарбонілу. У даному розкритті та формулі винаходу, радикали "SO 2" і S(O)2" означають сульфоніл, “CN" означає ціано, “-NO2" означає нітро, та “-OH" означає гідрокси. Загальне число вуглецевих атомів у групі замісника вказується за допомогою префіксу "Ci– Cj", де i та j дорівнюють числам від 1 до 9. Наприклад, C 1–C4 алкілсульфоніл означає метилсульфоніл — бутилсульфоніл, включаючи можливі ізомери. C2 алкоксикарбоніл означає 3 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 CH3 °C(O)-; C3 алкоксикарбоніл означає CH3CH2C(O)-; і C4 алкоксикарбоніл включає (CH3)2CHC(O)- і CH3CH2CH2C(O)-. Коли сполука заміщена замісником, що містить індекс, який показує, що число зазначених замісників може перевищувати 1, зазначені замісники (коли вони перевищують 1) незалежно v вибрані з групи визначених замісників, наприклад, для (R )r у U-1 Додатку 1 r дорівнює 1, 2, 3, 4 4 5 3 або 5. Коли група включає замісник, що може бути воднем (наприклад, -NR R у визначенні R , 4 5 де R або R можуть бути воднем у варіанті здійснення 2), тоді, коли даний замісник взятий як водень, визнають, що це еквівалентно тому, коли зазначена група є незаміщеною. Коли v перемінна група, як показано, є факультативно приєднаною в положення, наприклад (R )r у U-41 Додатку 1, де r може дорівнювати 0, тоді у положенні може бути водень, навіть якщо не згаданий у визначенні перемінної групи. Коли одне або більше положень у групі зазначені як "такі, що не заміщені" або "незаміщені", тоді атоми водню приєднуються, щоб зайняти будь-як вільну валентність. Вираз "гетероциклічне кільце" або "гетероцикл" означає кільце або кільце, у якому, щонайменше, один атом, що формує основу кільця, не є вуглецем, наприклад, азот, кисень або сірка. Типово гетероциклічне кільце включає не більше ніж 4 азоту, не більше ніж 2 кисні і не більше ніж 2 сірки. Вираз "член кільця" відноситься до атома або до іншої частини (наприклад, C(=O), C(=S), S(O) або S(O)2), що формує основу кільця. Якщо не зазначене інше, то гетероциклічне кільце може бути насиченим, частково ненасиченим або повністю ненасиченим кільцем, і, крім того, ненасичене гетероциклічне кільце може бути частково ненасиченим або повністю ненасиченим. Тому перерахування "гетероциклічне кільце" не вказуючи, насичене воно або ненасичене, є синонімом перерахуванню "насичене або ненасичене гетероциклічне кільце". Коли повністю ненасичене гетероциклічне кільце задовольняє правилу Хюккеля, тоді зазначене кільце також називається "гетероароматичне кільце" або "ароматичне гетероциклічне кільце". "Ароматичне" вказує на те, що кожен з атомів кільця знаходиться в основному в одній і тій же площині та має p-орбіталь, перпендикулярну площині кільця, і що (4n+2) π електрони, де n є позитивним цілим числом, зв'язані з кільцем, підкорюючись правилу Хюккеля. Якщо не зазначене інше, гетероциклічні кільця та кільцеві системи можуть бути приєднані через будьякий доступний вуглець або азот шляхом заміщення водню на зазначений вуглець або азот. Вираз "факультативно заміщений" в поєднанні з фенілом або 1-нафталенілом у визначеннях Z і Q відноситься до груп, що є незаміщеними або мають, щонайменше, один неводневий замісник. Оскільки Z і Q є периферійними для частин молекул, що піддаються реакції в даних способах, дуже широкий діапазон як кількості, так і типів замісників відповідає даним способам. Застосовувані тут наступні визначення варто застосовувати, якщо не зазначене інше. Вираз "факультативно заміщений" застосовують взаємозамінно з фразою "заміщений або незаміщений" або з виразом “(не)заміщений". Якщо не зазначено інше, факультативно заміщена група може мати замісник у кожному положенні групи, що може заміщатися, і кожен замісник є незалежним від іншого. 3 1 Коли R або Q являє собою 5- або 6-членне азотовмісне гетероциклічне кільце, воно може бути приєднане до залишку Формули 1 через будь-який доступний вуглецевий або азотний атом 3 1 кільця, якщо не описано інше. Як відзначено у варіанті здійснення 1B, R або Q може бути (серед інших) фенілом, факультативно заміщеним одним або більше замісниками, вибраними з групи замісників, як визначено у варіанті здійснення 1B. Прикладом фенілу, факультативно v заміщеного від одного до п'яти замісниками, є кільце, проілюстроване як U-1 у Додатку 1, де R 3 1 є таким, як визначено у варіанті здійснення 1B для R або Q , і r дорівнює цілому числу від 0 до 5. 3 1 Як відзначено вище, R або Q може бути (серед інших) 5- або 6-членним гетероциклічним кільцем, що може бути насиченим або ненасиченим, факультативно заміщеним одним або більше замісниками, вибраними з групи замісників, як визначено у варіанті здійснення 2. Приклади 5- або 6-членного ненасиченого ароматичного гетероциклічного кільця, факультативно заміщеного від одного або більше замісниками, включають кільця U-2-U-61, v проілюстровані в Додатку 1, де R являє собою будь-який замісник, як визначено у варіанті 3 1 здійснення 2 для R або Q , і r дорівнює цілому числу від 0 до 4, обмежений числом доступних положень у кожній U групі. Оскільки U-29, U-30, U-36, U-37, U-38, U-39, U-40, U-41, U-42 і U-43 мають тільки одне доступне положення, для цих U груп r обмежено цілими числами 0 або 1, і r, рівне 0, означає, що U група є незаміщеною, та водень присутній у положенні, що позначено v (R )r. Додаток 1 4 UA 106468 C2 3 (Rv) r (Rv)r 4 , S U-1 , 4 (R )r , N O N 4 2 S 2 U-11 5 N 3 , 5 O N U-21 v 4 (R )r 5 N , N N U-26 (R )r N N (Rv)r U-37 S N O (R )r U-42 (Rv)r N (R )r (Rv)r U-38 N N v (R )r U-43 N N N (R )r , N N 5 (Rv)r , N N U-35 O N , N U-40 (Rv)r v N , (R )r , N S N N U-44 3 , N N U-45 4 (Rv)r 5 N , N (Rv)r (Rv)r U-39 , N N N N U-34 N S (Rv)r , (R )r U-30 , (Rv)r , N N N v v v , , , S v U-29 , , , O N N U-33 S N N , N (R )r , N N U-32 N O N (Rv)r U-36 N N N , N U-25 N N , v (R )r , N 3 O (Rv)r S N U-24 N N N N U-28 , N U-31 O N (R )r U-41 , , U-20 3 S v N , 5 , 4 (Rv)r U-27 3 (Rv)r 4 (Rv)r U-23 N 5 v v N , , N U-15 N O U-19 3 (R )r 5 N 2 4 (Rv)r 5 v N S U-22 3 (Rv)r (Rv)r , N , , O 5 U-14 N U-18 v 4 (R )r 4 (Rv)r 2 U-10 S N N U-17 5 5 (Rv)r , N U-16 , (Rv)r 4 4 (R )r U-13 , , v S (Rv)r N U-9 2 5 (R )r O 4 U-12 (Rv)r N , U-5 4 (R )r , O 2 2 v N 5 5 N N U-8 (R )r , v , v v 4 (Rv) r U-4 (Rv)r N U-7 5 O U-3 (Rv)r U-6 4 , S 2 , N 5 U-2 N N , 5 (Rv)r 3 (Rv) r 4 (Rv) r 6 4 , v 5 (R )r 6 N 2 , UA 106468 C2 U-46 U-47 v 6 (R )r 5 N , N 6 N , N 3 N N U-57 4 U-56 4 (Rv)r N N U-61 N 10 15 N , N U-54 N 5 N N (Rv)r , N N N 6 , 2 N U-55 (Rv)r , N U-58 і N N U-59 U-60 . 6 3 5 , (Rv)r , 6 (Rv)r (R )r U-53 (Rv)r 5 U-50 v N N U-52 (R )r 2 N N , v U-49 (Rv)r (R )r 2 3 U-51 U-48 v 1 Потрібно відзначити, що коли R або Q є 5- або 6- членним насиченим або ненасиченим неароматичним гетероциклічним кільцем, факультативно заміщеним одним або більше 3 1 замісниками, вибраними з групи замісників, як визначено у варіанті здійснення 2 для R або Q , один або два вуглецеві члени кільця гетероциклу можуть факультативно бути в окисленій формі карбонільної частини. Приклади 5- або 6-членного насиченого або неароматичного ненасиченого гетероциклічного кільця включають кільця G-1-G-35, як проілюстровано в Додатку 2. Потрібно відзначити, що коли точка приєднання на G групі проілюстрована як рухома, G група може бути приєднана до залишку Формули 1 через будь-який доступний вуглець або азот G групи за допомогою v заміщення атома водню. Факультативні замісники, що відповідають R , можуть бути приєднані до будь-якого доступного вуглецю або азоту за допомогою заміщення атома водню. Для даних G кілець, r типово дорівнює цілому числу від 0 до 4, обмежене числом доступних положень на кожній G групі. 3 1 2 Потрібно відзначити, що коли R або Q включають кільце, вибране з G-28 – G-35, G 2 вибрано з O, S або N. Потрібно відзначити, що коли G є N, атом азоту може повністю v заповнити свою валентність заміщенням або H, або замісниками, що відповідають R , як визначено у варіанті здійснення 1B. Додаток 2 20 (Rv)r (Rv)r , S (Rv)r , v (R )r O O (Rv)r , O , S (Rv)r , , N G-5 O G-4 (Rv)r N (Rv)r , N G-3 O G-2 G-1 O (Rv)r , N (Rv)r , , N G-6 O G-7 (Rv)r O G-8 (Rv)r , O G-11 N (Rv)r , N , S O G-12 G-13 6 O G-10 G-9 (Rv)r 2 G-14 N , O (Rv)r 2 G-15 , UA 106468 C2 v (R )r N (R )r N , S 2 G-17 (Rv)r N N O G-22 N N , 2 (Rv)r N O , N (R )r , , G2 G-31 , N (R )r O N G2 G-33 G-32 v 5 10 15 20 25 30 G G-30 v (R )r O N (Rv)r N 2 G 2 G-29 , O . G2 G-34 O , G2 v (R )r O (Rv)r (R )r O G-28 v O G-25 , N G-27 v , v , (Rv)r N , G2 O G-26 N G-20 N G-24 (R )r O N , (Rv)r v (R )r N , G-19 G-23 v (R )r (R )r N N S , v , G-18 N 2 S G-21 (R )r (Rv)r v N (Rv)r , v , O G-16 2 N v і G2 G-35 Потрібно відзначити, що коли R є H при приєднанні до атома, це рівносильно тому, якщо зазначений атом є незаміщеним. Атоми азоту, що потребують заміщення, щоб заповнити їх v v валентність, заміщаються H або R . Потрібно відзначити, що коли точка приєднання між (R )r і U v групою проілюстрована як рухома, (R )r може приєднуватися до будь-якого доступного атома вуглецю або атому азоту U групи. Потрібно відзначити, що коли точка приєднання на U групі проілюстрована як рухома, U група може бути приєднана до залишку Формули 1 через будьякий доступний вуглець або азот U групи за допомогою заміщення атома водню. Потрібно v відзначити, що деякі U групи можуть бути заміщені тільки менше ніж 4 R групами (наприклад, U-2-U-5, U-7-U-48 і U-52-U-61). Різноманітні синтетичні способи відомі в даній галузі техніки для забезпечення одержання ароматичних і неароматичних гетероциклічних кілець; на більш широкі огляди дивись восьмий том видань Comprehensive Heterocyclic Chemistry, A. R. Katritzky and C. W. Rees editors-in-chief, Pergamon Press, Oxford, 1984 і дванадцятий том видань Comprehensive Heterocyclic Chemistry II, A. R. Каtritzку, C. W. Rees and E. F. V. Scriven editors-in-chief, Pergamon Press, Oxford, 1996. У деяких випадках тут співвідношення викладені як одиночні числа, що порівнянні з числом 1; наприклад, співвідношення 4 означає 4:1. У контексті даного винаходу "декантатор" відноситься до пристрою, здатному роздільно видаляти верхню (тобто, меншої щільності) рідку фазу і/або нижню (тобто, більшої щільності) рідку фазу з рідини (наприклад, азеотропний конденсат), що містить дві рідкі фази. Пастка ДінаСтарка являє приклад одного типу декантатора. Варіанти здійснення даного винаходу включають: Варіант здійснення 1. Спосіб, описаний у короткому описі винаходу, одержання сполуки Формули 1, що включає етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу й апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. Варіант здійснення 1A. Спосіб варіанта здійснення 1, де основа являє собою гідроксид лужноземельного металу Формули 4, і суміш додатково включає полярний апротонний розчинник. Варіант здійснення 1B. Спосіб варіанта здійснення 1, де основа включає карбонат лужного металу Формули 4a. Варіант здійснення 1C. Спосіб варіанта здійснення 1, де основа включає 1,5діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміш. Варіант здійснення 1D. Спосіб, описаний у Короткому описі винаходу, одержання сполуки 7 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 Формули 7, застосовуючи сполуку Формули 1, спосіб відрізняється тим, що одержують сполуку Формули 1 способом варіанта здійснення 1. Варіант здійснення 1E. Спосіб, описаний у Короткому описі винаходу, одержання сполуки Формули 7, застосовуючи сполуку Формули 1, спосіб відрізняється тим, що одержують сполуку Формули 1 способом варіанта здійснення 1A. Варіант здійснення 1F. Спосіб, описаний у Короткому описі винаходу, одержання сполуки Формули 7, застосовуючи сполуку Формули 1, спосіб відрізняється тим, що одержують сполуку Формули 1 способом варіанта здійснення 1B. Варіант здійснення 1G. Спосіб, описаний у Короткому описі винаходу, одержання сполуки Формули 7, застосовуючи сполуку Формули 1, спосіб відрізняється тим, що одержують сполуку Формули 1 способом варіанта здійснення 1C. Варіант здійснення 2. Спосіб будь-якого одного з варіантів здійснення 1-1G, де Q являє собою феніл або 1-нафталеніл, кожен факультативно має до 4 замісників, 3 незалежно вибраних з R ; 3 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2– C6 галоалкеніл, C2–C6 алкініл, C3–C6 галоалкініл, C3–C6 циклоалкіл, C3–C6 галоциклоалкіл, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C2–C7 алкілкарбоніл, C2–C7 галоалкілкарбоніл, C1– C6 галоалкілтіо, C1–C6 алкілсульфініл, C1–C6 галоалкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 4 5 4 5 5 11 галоалкілсульфоніл, -N(R )R , -C(=W)N(R )R , -C(=W)OR , -CN, -OR або -NO2; або фенільне кільце або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце факультативно заміщено одним або більше замісниками, незалежно вибраними з галогену, C 1– C6 алкілу, C1–C6 галоалкілу, C3–C6 циклоалкілу, C3–C6 галоциклоалкілу, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфінілу, C1–C6 4 5 галоалкілсульфінілу, C1–C6 алкілсульфонілу, C1–C6 галоалкілсульфонілу, -CN, -NO2, -N(R )R , 4 5 5 7 -C(=W)N(R )R , -C(=O)OR і R ; 4 кожен R являє собою незалежно H, C1–C6 алкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; 5 кожен R являє собою незалежно H; або C 1–C6 алкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл або C4–C7 циклоалкілалкіл, кожен факультативно заміщений 6 одним або більше замісниками, незалежно вибраними з R ; 6 кожен R являє собою незалежно галоген, C 1–C6 алкіл, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 алкіламіно, C2–C8 діалкіламіно, C3–C6 циклоалкіламіно, C2–C7 алкілкарбоніл, C2–C7 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C9 діалкіламінокарбоніл, C2–C7 галоалкілкарбоніл, C2–C7 галоалкоксикарбоніл, C2–C7 1 галоалкіламінокарбоніл, C3–C9 галодіалкіламінокарбоніл, -OH, -NH2, -CN або -NO2; або Q ; 7 кожен R являє собою незалежно фенільне кільце або піридинільне кільце, кожне кільце 8 факультативно заміщене одним або більше замісниками, незалежно вибраними з R ; 8 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C1–C6 алкокси, C1– C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфініл, C1–C6 галоалкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 галоалкілсульфоніл, C1–C6 алкіламіно, C2–C6 діалкіламіно, C2–C4 алкілкарбоніл, C2–C4 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C7 діалкіламінокарбоніл, -OH, -NH2, -C(=O)OH, -CN або -NO2; 1 кожен Q являє собою незалежно фенільне кільце або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце факультативно заміщено одним або більше замісниками, незалежно вибраними з галогену, C1–C6 алкілу, C1–C6 галоалкілу, C3–C6 циклоалкілу, C3–C6 галоциклоалкілу, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфінілу, C1–C6 галоалкілсульфінілу, C1–C6 алкілсульфонілу, C1–C6 9 10 галоалкілсульфонілу, C1–C6 алкіламіно, C2–C6 діалкіламіно, -CN, -NO2, -C(=W)N(R )R і 10 C(=O)OR ; 9 кожен R являє собою незалежно H, C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; 10 кожен R являє собою незалежно H; або C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл або C4–C7 циклоалкілалкіл; 11 кожен R являє собою незалежно H; або C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл, C2–C7 алкоксикарбоніл, C1– C6 алкілсульфоніл або C1–C6 галоалкілсульфоніл; і кожен W являє собою незалежно O або S. Варіант здійснення 2A. Спосіб варіанта здійснення 2, де Q являє собою феніл, 8 UA 106468 C2 3 5 10 15 факультативно має до чотирьох замісників, незалежно вибраних з R . Варіант здійснення 2B. Спосіб варіанта здійснення 2, де Q являє собою 1-нафталеніл, 3 факультативно має до чотирьох замісників, незалежно вибраних з R . 3 Варіант здійснення 2C. Спосіб варіанта здійснення 2, де кожен R являє собою незалежно 4 5 5 галоген, C1–C6 алкіл, C1–C6 галоалкіл, -C(W)N(R )R , -C(W)OR або -CN; або фенільне кільце або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце факультативно заміщено замісниками, незалежно вибраними з галогену, C1–C6 алкілу, C1–C6 4 5 5 галоалкілу, -CN, -C(W)N(R )R і -C(O)OR . 4 Варіант здійснення 2D. Спосіб варіанта здійснення 2, де кожен R являє собою незалежно H або C1–C6 алкіл. 5 Варіант здійснення 2E. Спосіб варіанта здійснення 2, де кожен R являє собою незалежно H; 6 або C1–C6 алкіл, факультативно заміщений замісниками, незалежно вибраними з R . 6 Варіант здійснення 2F. Спосіб варіанта здійснення 2, де кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 алкокси, C1–C6 алкілтіо, C2–C7 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C9 діалкіламінокарбоніл, C2–C7 галоалкіламінокарбоніл, C3–C9 1 галодіалкіламінокарбоніл або -CN; або Q . 1 Варіант здійснення 2G. Спосіб варіанта здійснення 2, де кожен Q являє собою незалежно піридинільне кільце, факультативно заміщене до 4 галогенами. Варіант здійснення 2H. Спосіб варіанта здійснення 2B, де 20 Q являє собою ;і R3 3 25 30 35 40 45 4 5 5 R являє собою C(O)N(R )R або C(O)OR . Варіант здійснення 2I. Спосіб варіанта здійснення 2H, де 4 R являє собою H, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл. 4 Варіант здійснення 2J. Спосіб варіанта здійснення 2I, де R являє собою H. Варіант здійснення 2K. Спосіб будь-якого одного з варіантів здійснення 2H-2J, де 3 4 5 5a R являє собою C(O)N(R )R або C(O)OR ; 5 R являє собою C1–C6 алкіл або C1–C6 галоалкіл, кожен заміщений одним замісником, незалежно вибраним з гідрокси, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфінілу, C1–C6 алкілсульфонілу, C2–C7 алкіламінокарбонілу, C3–C9 діалкіламінокарбонілу, C2–C7 галоалкіламінокарбонілу і C3–C9 галодіалкіламінокарбонілу; і 5a R являє собою C1–C6 алкіл, C2–C6 алкеніл або C2–C6 алкініл, кожен факультативно заміщений одним або більше замісниками, незалежно вибраними з галогену, C 1–C2 алкокси і фенілу, що факультативно має до 5 замісників, вибраних з галогену і C1–C3 алкілу. Варіант здійснення 2L. Спосіб будь-якого одного з варіантів здійснення 2H-2K, де 5a R являє собою C1–C6 алкіл, факультативно заміщений фенілом. Варіант здійснення 2M. Спосіб будь-якого одного з варіантів здійснення 2H-2L, де 3 4 5 R являє собою C(O)N(R )R . Варіант здійснення 2N. Спосіб будь-якого одного з варіантів здійснення 2H-2J, де 3 5 R являє собою C(O)OR . Варіант здійснення 2O. Спосіб будь-якого одного з варіантів здійснення 2K-2L, де 3 5a R являє собою C(O)OR . Варіант здійснення 3. Спосіб будь-якого одного з варіантів здійснення 1-2O, де 2 Z являє собою феніл, що факультативно має до 5 замісників, незалежно вибраних з R (тобто, 3 2 5 6 4 2 (R )n , де n дорівнює 0, 1, 2, 3, 4 або 5); і 2 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C1–C6 алкокси, C1– 9 UA 106468 C2 5 10 15 C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкіламіно, C2–C6 діалкіламіно, -CN або -NO2. Варіант здійснення 3A. Спосіб варіанта здійснення 3, де Z являє собою фенільне кільце, 2 заміщене до 3 замісниками, незалежно вибраними з R , зазначені замісники приєднані в положення 3, 4 або 5 фенільного кільця. 2 Варіант здійснення 3B. Спосіб варіанта здійснення 3 або 3A, де кожен R являє собою незалежно F, Cl, Br, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1–C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо. 2 Варіант здійснення 3C. Спосіб варіанта здійснення 3 або 3A, де кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл або -CN. 2 Варіант здійснення 3D. Спосіб варіанта здійснення 3C, де кожен R являє собою незалежно галоген або C1–C6 галоалкіл. 2 Варіант здійснення 3E. Спосіб варіантаздійснення 3D, де кожен R являє собою незалежно галоген або CF3. 2 Варіант здійснення 3F. Спосіб варіанта здійснення 3E, де кожен R являє собою незалежно F, Cl або CF3. Варіант здійснення 3G. Спосіб варіанта здійснення 3A, де Z являє собою R2a R2b ; R2c 20 25 30 35 40 45 50 2a 2b R являє собою галоген, C1–C2 галоалкіл або C1–C2 галоалкокси; R являє собою H, 2с галоген або ціано; і R являє собою H, галоген або CF3. 2a Варіант здійснення 3H. Спосіб варіанта здійснення 3G, де R являє собою CF3 або галоген; 2с і R являє собою H, CF3 або галоген. 2a Варіант здійснення 3I. Спосіб варіанта здійснення 3H, де R являє собою CF3. 2b Варіант здійснення 3J. Спосіб будь-якого одного з варіантів здійснення 3G-3I, де R являє собою H. 2с Варіант здійснення 3K. Спосіб будь-якого одного з варіантів здійснення 3G-3J, де R являє собою CF3 або галоген. 2с Варіант здійснення 3L. Спосіб варіанта здійснення 3K, де R являє собою CF3, F, Cl або Br. 2с Варіант здійснення 3M. Спосіб варіанта здійснення 3L, де R являє собою F, Cl або Br. 2с Варіант здійснення 3N. Спосіб варіанта здійснення 3L, де R являє собою CF3, Cl або Br. 2с Варіант здійснення 3O. Спосіб варіанта здійснення 3N, де R являє собою Cl або Br. 2b 2с Варіант здійснення 3P. Спосіб варіанта здійснення 3O, де R являє собою H, і R являє собою Cl. 2b 2с Варіант здійснення 3Q. Спосіб варіанта здійснення 3O, де R являє собою H, і R являє собою Br. Варіант здійснення 4. Спосіб одержання сполуки Формули 2, описаний у Короткому описі винаходу, містить етапи, на яких (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5 приведенням у контакт сполуки Формули 5 з (a) металевим магнієм або (b) галогенідом алкілмагнію в присутності ефірного розчинника; і потім (2) приводять у контакт реакційну суміш зі сполукою Формули 6. Варіант здійснення 4A. Спосіб будь-якого одного з варіантів здійснення 1-2O і 3-3Q додатково відрізняється тим, що одержують сполуку Формули 2 способом варіанта здійснення 4. Варіант здійснення 4B. Спосіб варіанта здійснення 4 або 4A, де X являє собою Cl або I. Варіант здійснення 4C. Спосіб варіанта здійснення 4 або 4A, де X являє собою Br або I. Варіант здійснення 4D. Спосіб варіанта здійснення 4 або 4A, де X являє собою Cl або Br. Варіант здійснення 4E. Спосіб варіанта здійснення 4 або 4A, де X являє собою Cl. Варіант здійснення 4F. Спосіб варіанта здійснення 4 або 4A, де X являє собою Br. Варіант здійснення 4G. Спосіб варіанта здійснення 4 або 4A, де X являє собою I. Варіант здійснення 4H. Спосіб будь-якого одного з варіантів здійснення 4-4G, де 2 Z являє собою феніл, що факультативно має до 5 замісників, незалежно вибраних з R (тобто 10 UA 106468 C2 5 10 15 20 25 30 , де n дорівнює 0, 1, 2, 3, 4 або 5); і 2 кожен R являє собою незалежно F, Cl, Br, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1– C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо; 2 за умови, що коли X являє собою Cl, тоді кожен R являє собою незалежно F, Cl, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1–C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо. Варіант здійснення 4I. Спосіб варіанта здійснення 4H, при якому, коли X являє собою Br, 2 тоді кожен R являє собою незалежно F, Cl, C 1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1–C6 2 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо; і коли X являє собою Cl, тоді кожен R являє собою незалежно F, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1–C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо. Варіант здійснення 4J. Спосіб будь-якого одного з варіантів здійснення 3, 4H і 4I, де Z являє 2 собою фенільне кільце, заміщене до 3 замісниками, незалежно вибраними з R , причому зазначені замісники приєднані в 3, 4 або 5 положення фенільного кільця. Варіант здійснення 4K. Спосіб будь-якого одного з варіантів здійснення 4H, 4I і 4J, де кожен 2 R являє собою незалежно F, Cl, Br, C1–C6 алкіл або C1–C6 фторалкіл. 2 Варіант здійснення 4L. Спосіб варіанта здійснення 4K, де кожен R являє собою незалежно F, Cl, Br або C1–C6 фторалкіл. 2 Варіант здійснення 4M. Спосіб варіанта здійснення 4L, де кожен R являє собою незалежно F, Cl, Br або CF3. Варіант здійснення 4N. Спосіб будь-якого одного з варіантів здійснення 4H-4M, де Z являє 2 собою фенільне кільце, заміщене 2 замісниками, незалежно вибраними з R , причому зазначені замісники приєднані в 3 і 5 положення фенільного кільця. 2 Варіант здійснення 4O. Спосіб варіанта здійснення 4N, де кожен R являє собою незалежно F, Cl, Br або CF3. 2 Варіант здійснення 4P. Спосіб варіанта здійснення 4O, де, щонайменше, один R являє собою CF3. 2 Варіант здійснення 4Q. Спосіб варіанта здійснення 4P, де один R являє собою CF3, і інший 2 R являє собою Cl або Br. 2 Варіант здійснення 4R. Спосіб варіанта здійснення 4Q, де один R являє собою CF3, і інший 2 R являє собою Cl. Варіант здійснення 4S. Спосіб варіанта здійснення 3A або 3H, де Z являє собою 35 R2a R2b ; R2c 2a 40 45 2b R являє собою F, Cl, Br, C1–C2 фторалкіл або C1–C2 фторалкокси; R являє собою H, F, Cl 2с або Br; і R являє собою H, F, Cl, Br або CF3. 2a Варіант здійснення 4T. Спосіб варіанта здійснення 4S, де R являє собою CF3, F, Cl або Br; і 2с R являє собою H, CF3, F, Cl або Br. 2a Варіант здійснення 4U. Спосіб варіанта здійснення 4T, де R являє собою CF3. 2b Варіант здійснення 4V. Спосіб будь-якого одного з варіантів здійснення 4S-4U, де R являє собою H. 2с Варіант здійснення 4W. Спосіб будь-якого одного з варіантів здійснення 4S-4V, де R являє собою CF3, F, Cl або Br. 2с Варіант здійснення 4X. Спосіб варіанта здійснення 4W, де R являє собою F, Cl або Br. 11 UA 106468 C2 2с 5 10 Варіант здійснення 4Y. Спосіб варіанта здійснення 4W, де R являє собою CF3, Cl або Br. 2с Варіант здійснення 4Z. Спосіб варіанта здійснення 4Y, де R являє собою Cl або Br. 2b 2з Варіант здійснення 4ZA. Спосіб варіанта здійснення 4Z, де R являє собою H, і R являє собою Cl. 2b 2с Варіант здійснення 4ZB. Спосіб варіанта здійснення 4Z, де R являє собою H, і R являє собою Br. Варіант здійснення 4ZC. Спосіб будь-якого одного з варіантів здійснення 4S-4ZB, де X являє собою I. Варіант здійснення 5. Сполука Формули 2, як описано в Короткому описі винаходу, де Z являє собою R2a R2b ; R2c 2a 2с 2b R являє собою CF3; R являє собою H або галоген; і R являє собою галоген. 2b Варіант здійснення 5A. Сполука варіанта здійснення 5, де R являє собою H. 2с Варіант здійснення 5B. Сполука варіанта здійснення 5 або 5A, де R являє собою F, Cl або 15 Br. 20 25 30 35 40 45 50 2с Варіант здійснення 5C. Сполука варіанта здійснення 5B, де R являє собою Cl або Br. Варіант здійснення 5D. Сполука варіанта здійснення 5C, вибрана з групи, що містить: 1-[3-хлор-5-(трифторметил)]-2,2,2-трифторетанон; і 1-[3-бром-5-(трифторметил)]-2,2,2-трифторетанон. Варіант здійснення 5E. Сполука Формули 5, як описано в Короткому описі винаходу, являє собою 1-хлор-3-йод-5-(трифторметил)бензол. Варіант здійснення 6. Спосіб варіанта здійснення 1A або 1E, де M являє собою Ca (тобто, гідроксид лужноземельного металу являє собою гідроксид кальцію). Варіант здійснення 6A. Спосіб варіанта здійснення 1A, 1E або 6, де молярне співвідношення гідроксиду лужноземельного металу до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,1. Варіант здійснення 6A1. Спосіб варіанта здійснення 6A, де молярне співвідношення гідроксиду лужноземельного металу до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,5. Варіант здійснення 6B. Спосіб варіанта здійснення 6A1, де молярне співвідношення гідроксиду лужноземельного металу до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,8. Варіант здійснення 6C. Спосіб будь-якого одного з варіантів здійснення 1A, 1E або 6-6B, де молярне співвідношення гідроксиду лужноземельного металу до сполуки Формули 2 дорівнює не більше ніж приблизно 1. 1 Варіант здійснення 6D. Спосіб варіанта здійснення 1B або 1F, де M являє собою K (тобто карбонат лужного металу являє собою карбонат калію). Варіант здійснення 6E. Спосіб варіанта здійснення 1B, 1F або 6D, де молярне співвідношення карбонату лужного металу до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,01. Варіант здійснення 6F. Спосіб варіанта здійснення 6E, де молярне співвідношення карбонату лужного металу до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,03. Варіант здійснення 6G. Спосіб будь-якого одного з варіантів здійснення 1B, 1F або 6D-6F, де молярне співвідношення карбонату лужного металу до сполуки Формули 2 дорівнює не більше ніж приблизно 0,2. Варіант здійснення 6H. Спосіб варіанта здійснення 1C або 1G, де молярне співвідношення 1,5-діазабіцикло[4.3.0]нон-5-ена, 1,8-діазабіцикло[5.4.0]ундец-7-ена або їх суміші до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,01. Варіант здійснення 6I. Спосіб варіанта здійснення 6H, де молярне співвідношення 1,5діазабіцикло[4.3.0]нон-5-ена, 1,8-діазабіцикло[5.4.0]ундец-7-ена або їхньої суміші до сполуки Формули 2 дорівнює, щонайменше, приблизно 0,03. Варіант здійснення 6J. Спосіб будь-якого одного з варіантів здійснення 1C, 1G, 6H або 6I, де 12 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 молярне співвідношення 1,5-діазабіцикло[4.3.0]нон-5-ена, 1,8-діазабіцикло-[5.4.0]ундец-7-ена або їхньої суміші до сполуки Формули 2 дорівнює не більше ніж приблизно 0,2. Варіант здійснення 7. Спосіб варіанта здійснення 1A або 1E, де полярний апротонний розчинник включає амід або сульфоксид (включаючи їхні суміші). Варіант здійснення 7A. Спосіб варіанта здійснення 7, де полярний апротонний розчинник включає один або більше N, N-диметилформамід, N, N-диметилацетамід, N- метилпіролідинон і метилсульфоксид. Варіант здійснення 7B. Спосіб варіанта здійснення 7, де полярний апротонний розчинник включає амід. Варіант здійснення 7C. Спосіб варіанта здійснення 7B, де полярний апротонний розчинник включає один або більше N, N-диметилформамід, N, N-диметилацетамід, N- метилпіролідинон. Варіант здійснення 7D. Спосіб варіанта здійснення 7C, де полярний апротонний розчинник включає N, N-диметилформамід. Варіант здійснення 8. Спосіб варіанта здійснення 1A або 1E, де апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, включає ефір. Варіант здійснення 8A. Спосіб варіанта здійснення 8, де апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, включає трет-бутилметиловий ефір. Варіант здійснення 8B. Спосіб будь-якого одного з варіантів здійснення 1B, 1C, 1F, 1G або 6D-6J, де апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, включає ацетонітрил. Варіант здійснення 8C. Спосіб варіанта здійснення 8A, де полярний апротонний розчинник включає N, N-диметилформамід. Варіант здійснення 8D. Спосіб варіанта здійснення 8C, де трет-бутилметиловий ефір і N, Nдиметилформамід знаходяться у ваговому співвідношенні в діапазоні від приблизно 0,5 до приблизно 2. Варіант здійснення 9. Спосіб варіанта здійснення 1A або 1E, де суміш знаходиться при температурі, щонайменше, приблизно 65 °C. Варіант здійснення 9A. Спосіб варіанта здійснення 9, де суміш знаходиться при температурі, щонайменше, приблизно 70 °C. Варіант здійснення 9B. Спосіб варіанта здійснення 9A, де суміш знаходиться при температурі, щонайменше, приблизно 75 °C. Варіант здійснення 9C. Спосіб варіанта здійснення 1B, 1C, 1F або 1G, де суміш знаходиться при температурі, щонайменше, приблизно 65 °C. Варіант здійснення 9D. Спосіб варіанта здійснення 9C, де суміш знаходиться при температурі, щонайменше, приблизно 80 °C. Варіант здійснення 9E. Спосіб варіанта здійснення 9D, де суміш знаходиться при температурі, щонайменше, приблизно 85 °C. Варіант здійснення 9F. Спосіб будь-якого одного з варіантів здійснення 9-9E, де суміш знаходиться при температурі не більше ніж приблизно 110 °C. Варіант здійснення 9G. Спосіб варіанта здійснення 9F, де суміш знаходиться при температурі не більше ніж приблизно 100 °C. Варіант здійснення 9H. Спосіб варіанта здійснення 9G, де суміш знаходиться при температурі не більше ніж приблизно 90 °C. Варіант здійснення 10. Спосіб варіанта здійснення 4 або 4A, де сполуку Формули 5 приводять у контакт із металевим магнієм. Варіант здійснення 10A. Спосіб варіанта здійснення 10, де молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює, щонайменше, приблизно 1. Варіант здійснення 10B. Спосіб варіанта здійснення 10A, де молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює, щонайменше, приблизно 1,02. Варіант здійснення 10C. Спосіб варіанта здійснення 10B, де молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює, щонайменше, приблизно 1,05. Варіант здійснення 10D. Спосіб будь-якого одного з варіантів здійснення 10-10C, де молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,2. Варіант здійснення 10E. Спосіб варіанта здійснення 10D, де молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,1. Варіант здійснення 10F. Спосіб варіанта здійснення 4 або 4A, де сполуку Формули 5 приводять у контакт із галогенідом алкілмагнію. Варіант здійснення 10G. Спосіб варіанта здійснення 10F, де галогенід алкілмагнію являє собою галогенід C1–C4 алкілмагнію. 13 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 Варіант здійснення 10H. Спосіб варіанта здійснення 10F або 10G, де галогенід алкілмагнію являє собою галогенід вторинного алкілмагнію. Варіант здійснення 10I. Спосіб варіанта здійснення 10H, де галогенід алкілмагнію являє собою галогенід ізопропілмагнію. Варіант здійснення 10J. Спосіб варіанта здійснення 10I, де галогенід алкілмагнію являє собою хлорид ізопропілмагнію. Варіант здійснення 10K. Спосіб будь-якого одного з варіантів здійснення 10F-10J, де молярне співвідношення галогеніду алкілмагнію до сполуки Формули 5 дорівнює, щонайменше, приблизно 1. Варіант здійснення 10L. Спосіб варіанта здійснення 10K, де молярне співвідношення галогеніду алкілмагнію до сполуки Формули 5 дорівнює, щонайменше, приблизно 1,05. Варіант здійснення 10M. Спосіб будь-якого одного з варіантів здійснення 10F-10L, де молярне співвідношення галогеніду алкілмагнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,2. Варіант здійснення 10N. Спосіб варіанта здійснення 10M, де молярне співвідношення галогеніду ізопропілмагнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,15. Варіант здійснення 10O. Спосіб варіанта здійснення 4 або 4A, де сполука Формули 6 являє собою метилтрифторацетат або етилтрифторацетат. Варіант здійснення 11. Спосіб варіанта здійснення 4 або 4A, де ефірний розчинник включає один або більше етиловий ефір, 1,4-діоксан, тетрагідрофуран і 1,2-диметоксіетан. Варіант здійснення 11A. Спосіб варіанта здійснення 11, де ефірний розчинник включає етиловий ефір або тетрагідрофуран. Варіант здійснення 11B. Спосіб варіанта здійснення 11A, де ефірний розчинник включає тетрагідрофуран. Варіант здійснення 11C. Спосіб будь-якого одного з варіантів здійснення 4, 4A або 11-11B, де сполуку Формули 5 приводять у контакт із (a) металевим магнієм, або (b) галогенідом алкілмагнію в присутності ароматичного вуглеводневого розчинника з додаванням ефірного розчинника. Варіант здійснення 11D. Спосіб варіанта здійснення 11C, де ароматичний вуглеводневий розчинник включає один або більше бензол, толуол і ксилол. Варіант здійснення 11E. Спосіб варіанта здійснення 11D, де ароматичний вуглеводневий розчинник включає толуол. Варіанти здійснення даного винаходу, включаючи варіанти здійснення 1–11E, викладені вище, також як будь-які інші варіанти здійснення, описані тут, можуть сполучатися будь-яким способом, і описи змінних у варіантах здійснення належать не тільки до вищеописаних способів одержання сполук Формули 1, 2 і 7, але також до вихідних сполук і проміжних сполук, застосовних для одержання сполук Формули 1, 2 і 7 за допомогою даних способів. Ілюстрація сполучень варіантів здійснення 1–11E: Варіант здійснення A. Спосіб, описаний у Короткому описі винаходу, одержання сполуки Формули 1, що включає етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, де 2 Z являє собою феніл, що факультативно має до 5 замісників, незалежно вибраних з R ; Q являє собою феніл або 1-нафталеніл, кожен факультативно має до чотирьох замісників, 3 незалежно вибраних з R ; 2 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C1–C6 алкокси, C1– C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкіламіно, C2–C6 діалкіламіно, -CN або -NO2; 3 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2– C6 галоалкеніл, C2–C6 алкініл, C3–C6 галоалкініл, C3–C6 циклоалкіл, C3–C6 галоциклоалкіл, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C2–C7 алкілкарбоніл, C2–C7 галоалкілкарбоніл, C1– C6 галоалкілтіо, C1–C6 алкілсульфініл, C1–C6 галоалкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 4 5 4 5 5 11 галоалкілсульфоніл, -N(R )R , -C(=W)N(R )R , -C(=W)OR , -CN, -OR або -NO2; або фенільне кільце або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце факультативно заміщено одним або більше замісниками, незалежно вибраними з галогену, C 1– C6 алкілу, C1–C6 галоалкілу, C3–C6 циклоалкілу, C3–C6 галоциклоалкілу, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфінілу, C1–C6 4 5 галоалкілсульфінілу, C1–C6 алкілсульфонілу, C1–C6 галоалкілсульфонілу, -CN, -NO2, -N(R )R , 4 5 5 7 -C(=W)N(R )R , -C(=O)OR і R ; 4 кожен R являє собою незалежно H, C1–C6 алкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 14 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; 5 кожен R являє собою незалежно H; або C 1–C6 алкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл або C4–C7 циклоалкілалкіл, кожен факультативно заміщений 6 одним або більше замісниками, незалежно вибраними з R ; 6 кожен R являє собою незалежно галоген, C 1–C6 алкіл, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 алкіламіно, C2–C8 діалкіламіно, C3–C6 циклоалкіламіно, C2–C7 алкілкарбоніл, C2–C7 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C9 діалкіламінокарбоніл, C2–C7 галоалкілкарбоніл, C2–C7 галоалкоксикарбоніл, C2–C7 1 галоалкіламінокарбоніл, C3–C9 галодіалкіламінокарбоніл, -OH, -NH2, -CN або -NO2; або Q ; 7 кожен R являє собою незалежно фенільне кільце або піридинільне кільце, кожне кільце 8 факультативно заміщено одним або більше замісниками, незалежно вибраними з R ; 8 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, C1–C6 алкокси, C1– C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфініл, C1–C6 галоалкілсульфініл, C1–C6 алкілсульфоніл, C1–C6 галоалкілсульфоніл, C1–C6 алкіламіно, C2–C6 діалкіламіно, C2–C4 алкілкарбоніл, C2–C4 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C7 діалкіламінокарбоніл, -OH, -NH2, -C(=O)OH, -CN або -NO2; 1 кожен Q являє собою незалежно фенільне кільце або 5- або 6-членне насичене або ненасичене гетероциклічне кільце, кожне кільце факультативно заміщено одним або більше замісниками, незалежно вибраними з галогену, C1–C6 алкілу, C1–C6 галоалкілу, C3–C6 циклоалкілу, C3–C6 галоциклоалкілу, C1–C6 алкокси, C1–C6 галоалкокси, C1–C6 алкілтіо, C1–C6 галоалкілтіо, C1–C6 алкілсульфінілу, C1–C6 галоалкілсульфінілу, C1–C6 алкілсульфонілу, C1–C6 9 10 галоалкілсульфонілу, C1–C6 алкіламіно, C2–C6 діалкіламіно, -CN, -NO2, -C(=W)N(R )R і 10 C(=O)OR ; 9 кожен R являє собою незалежно H, C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; 10 кожен R являє собою незалежно H; або C1–C6 алкіл, C1–C6 галоалкіл, C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл або C4–C7 циклоалкілалкіл; 11 кожен R являє собою незалежно H; або C2–C6 алкеніл, C2–C6 алкініл, C3–C6 циклоалкіл, C4–C7 алкілциклоалкіл, C4–C7 циклоалкілалкіл, C2–C7 алкілкарбоніл, C2–C7 алкоксикарбоніл, C1– C6 алкілсульфоніл або C1–C6 галоалкілсульфоніл; і кожен W являє собою незалежно O або S. Варіант здійснення A1. Спосіб варіанта здійснення A, де основа являє собою гідроксид лужноземельного металу Формули 4, і суміш додатково включає полярний апротонний розчинник. Варіант здійснення A2. Спосіб варіанта здійснення A або A1, де Q являє собою феніл, 3 факультативно має до чотирьох замісників, незалежно вибраних з R . Варіант здійснення A3. Спосіб варіанта здійснення A або A1, де Q являє собою 13 нафталеніл, факультативно має до чотирьох замісників, незалежно вибраних з R . Варіант здійснення A4. Спосіб варіанта здійснення A, A1 або A2, де 2 кожен R являє собою незалежно галоген або C1–C6 галоалкіл; 3 4 5 кожен R являє собою незалежно галоген, C1–C6 алкіл, C1–C6 галоалкіл, -C(W)N(R )R , 5 -C(W)OR або -CN; або фенільне кільце або 5- або 6-членне гетероциклічне кільце, кожне кільце факультативно заміщено одним або більше замісниками, незалежно вибраними з галогену, C1– 4 5 5 C6 алкілу, C1–C6 галоалкілу, -CN, -C(W)N(R )R і -C(O)OR ; 4 кожен R являє собою незалежно H або C1–C6 алкіл; 5 кожен R являє собою незалежно H; або C1–C6 алкіл, факультативно заміщений одним або 6 більше замісниками, незалежно вибраними з R ; 6 кожен R являє собою незалежно галоген, C 1–C6 алкіл, C1–C6 алкокси, C1–C6 алкілтіо, C2–C7 алкоксикарбоніл, C2–C7 алкіламінокарбоніл, C3–C9 діалкіламінокарбоніл, C2–C7 1 галоалкіламінокарбоніл, C3–C9 галодіалкіламінокарбоніл або -CN; або Q ; і 1 кожен Q являє собою незалежно піридинільне кільце, факультативно заміщене до 4 галогенами. Варіант здійснення A5. Спосіб варіанта здійснення A3, де 15 UA 106468 C2 R2a Z являє собою R2b ; Q являє собою ; R3 R2c 2a 5 10 15 20 R являє собою галоген, C1–C2 галоалкіл або C1–C2 галоалкокси; 2b R являє собою H, галоген або ціано; 2с R являє собою H, галоген або CF3; 3 4 5 5a R являє собою C(O)N(R )R або C(O)OR ; 4 R являє собою H, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; і 5 R являє собою C1–C6 алкіл або C1–C6 галоалкіл, кожен заміщений одним замісником, незалежно вибраним з гідрокси, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфінілу, C1–C6 алкілсульфонілу, C2–C7 алкіламінокарбонілу, C3–C9 діалкіламінокарбонілу, C2–C7 галоалкіламінокарбонілу і C3–C9 галодіалкіламінокарбонілу; і 5a R являє собою C1–C6 алкіл, C2–C6 алкеніл або C2–C6 алкініл, кожен факультативно заміщений одним або більше замісниками, незалежно вибраними з галогену, C 1–C2 алкокси і фенілу, що факультативно має до 5 замісників, вибраними з галогену і C1–C3 алкілу. 3 4 5 Варіант здійснення A6. Спосіб варіанта здійснення A5, де R являє собою C(O)N(R )R . 3 5a Варіант здійснення A7. Спосіб варіанта здійснення A5, де R являє собою C(O)OR . Варіант здійснення B. Спосіб одержання сполуки Формули 1, описаний у короткому описі винаходу, що включає етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, де Z являє собою феніл, що факультативно має до 5 замісників, незалежно 2 вибраних з R (тобто (R2)n 25 , де n дорівнює 0, 1, 2, 3, 4 або 5); і 2 кожен R являє собою незалежно F, Cl, Br, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1– C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо; додатково включає одержання сполуки Формули 2 за допомогою етапів, на яких (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5 Z–X , 5 30 35 де X являє собою Cl, Br або I, приведенням у контакт сполуки Формули 5 з (a) металевим магнієм, або (b) галогенідом алкілмагнію у присутності ефірного розчинника; і потім (2) приводять у контакт реакційну суміш зі сполукою Формули 6 O Y CF3 , 6 40 де 11 12 13 Y являє собою OR або NR R ; 11 R являє собою C1–C5 алкіл; і 12 13 12 13 R і R являє собою незалежно C1–C2 алкіл; або R і R взяті разом як -CH2CH2OCH2CH2-. 16 UA 106468 C2 Варіант здійснення B1. Спосіб варіанта здійснення B, де основа являє собою гідроксид лужноземельного металу Формули 4, і суміш додатково включає полярний апротонний розчинник. Варіант здійснення B2. Спосіб варіанта здійснення B або B1, де Z являє собою 5 R2a R2b ; R2c 2a 10 15 R являє собою F, Cl, Br, C1–C2 фторалкіл або C1–C2 фторалкокси; 2b R являє собою H, F, Cl або Br; і 2с R являє собою H, F, Cl, Br або CF3. Варіант здійснення C. Спосіб одержання сполуки Формули 2, описаний у Короткому описі винаходу, що включає етапи, на яких (1) формують реакційну суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5, приведенням у контакт сполуки Формули 5 з (a) металевим магнієм або (b) галогенідом алкілмагнію в присутності ефірного розчинника; і потім (2) приводять у контакт реакційну суміш зі сполукою Формули 6, де X являє собою I; 2 Z являє собою феніл, що факультативно має до 5 замісників, незалежно вибраних з R (тобто (R2)n 20 , де n дорівнює 0, 1, 2, 3, 4 або 5); і 2 кожен R являє собою незалежно F, Cl, Br, C1–C6 алкіл, C1–C6 фторалкіл, C1–C6 алкокси, C1– C6 фторалкокси, C1–C6 алкілтіо або C1–C6 фторалкілтіо. Варіант здійснення C1. Спосіб варіанта здійснення C, де Z являє собою R2a R2b ; R2c 25 2a R являє собою F, Cl, Br, C1–C2 фторалкіл або C1–C2 фторалкокси; 2b R являє собою H, F, Cl або Br; і 2с R являє собою H, F, Cl, Br або CF3. Варіант здійснення D. Спосіб одержання сполуки Формули 7 30 F 3C O Z Q 7 35 N , де Z являє собою факультативно заміщений феніл; і Q являє собою феніл або 1-нафталеніл, кожен факультативно заміщений; із застосуванням сполуки Формули 1 17 UA 106468 C2 O F3C Q Z 5 1 , який відрізняється тим, що: одержують зазначену сполуку Формули 1 способом одержання сполуки Формули 1, описаним у Короткому описі винаходу, що містить етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. Варіант здійснення D1. Спосіб варіанта здійснення D, де основа являє собою гідроксид лужноземельного металу Формули 4, і суміш додатково включає полярний апротонний розчинник. Варіант здійснення D2. Спосіб варіанта здійснення D або D1, де 10 R2a Z являє собою R R4 2b Q являє собою ; ; N R R2c 5 O 2a 15 20 R являє собою галоген, C1–C2 галоалкіл або C1–C2 галоалкокси; 2b R являє собою H, галоген або ціано; 2с R являє собою H, галоген або CF3; 4 R являє собою H, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; і 5 R являє собою C1–C6 алкіл або C1–C6 галоалкіл, кожен заміщений одним замісником, незалежно вибраним з гідрокси, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфінілу, C1–C6 алкілсульфонілу, C2–C7 алкіламінокарбонілу, C3–C9 діалкіламінокарбонілу, C2–C7 галоалкіламінокарбонілу і C3–C9 галодіалкіламінокарбонілу. Варіант здійснення E. Спосіб одержання сполуки Формули 7 F 3C O N Z Q 7 25 , де Z являє собою факультативно заміщений феніл; і Q являє собою феніл або 1-нафталеніл, кожен факультативно заміщений; із застосуванням сполуки Формули 1 O F3C Q Z 30 35 1 , який відрізняється тим, що: застосовують як зазначену сполуку Формули 1 сполуку Формули 1, отриману способом, описаним у Короткому описі винаходу для одержання сполуки Формули 1, що містить етап, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. Варіант здійснення E1. Спосіб варіанта здійснення E, де основа являє собою гідроксид лужноземельного металу Формули 4, і суміш додатково включає полярний апротонний розчинник. Варіант здійснення E2. Спосіб варіанта здійснення E або E1, де 18 UA 106468 C2 R2a Z являє собою R2b ; R4 Q являє собою N R 2c ; R5 O 2a 5 10 15 R являє собою галоген, C1–C2 галоалкіл або C1–C2 галоалкокси; 2b R являє собою H, галоген або ціано; 2с R являє собою H, галоген або CF3; 4 R являє собою H, C2–C7 алкілкарбоніл або C2–C7 алкоксикарбоніл; і 5 R являє собою C1–C6 алкіл або C1–C6 галоалкіл, кожен заміщений одним замісником, незалежно вибраним з гідрокси, C1–C6 алкокси, C1–C6 алкілтіо, C1–C6 алкілсульфінілу, C1–C6 алкілсульфонілу, C2–C7 алкіламінокарбонілу, C3–C9 діалкіламінокарбонілу, C2–C7 галоалкіламінокарбонілу і C3–C9 галодіалкіламінокарбонілу. 2 3 4 5 6 7 8 9 10 11 12 13 У наступних Схемах 1–10 визначення Z, Q, R , R , R , R , R , R , R , R , R , R , R , R і W у сполуках Формули 1-7 і 11-15 є такими, як визначено вище в Короткому описі винаходу, і описі варіантів здійснення, якщо не зазначене інше. Формула 1a являє собою підмножину Формули 1. Формула 5A являє собою підмножину Формули 5. Формули 7a, 7b, 7c, 7d, 7e і 7f являють собою підмножини Формули 7. Формула 13a являє собою підмножину Формули 13. У способі даного винаходу проілюстрованому в Схемі 1, сполуку Формули 1 одержують за допомогою етапу, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу гідроксиду лужноземельного металу Формули 4, полярний апротонний розчинник, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. 20 25 30 35 40 , де M являє собою Ca, Sr або Ba. Перший етап даної реакції включає альдольну конденсацію, що формує сполуку Формули 11. Сполука Формули 11 є невиділеною, але замість цього при умовах реакції перетворюється в сполуку Формули 1. Стехіометрія даної реакції містить у собі еквімолярні кількості сполук Формули 2 і Формули 3, і застосування еквімолярних кількостей, як правило, є більш рентабельним. Проте, невеликі молярні надлишки одного з реагентів є безпечними для реакції, і якщо один з реагентів є набагато дешевшим або більш препаративно доступним, із застосуванням його невеликого надлишку (наприклад, 1,05 молярних еквівалентів), може бути бажаним забезпечити повне перетворення більш дорогого або менш препаративно доступного реагенту. Гідроксиди лужноземельного металу Формули 4 і сполуки, здатні формувати зазначені гідроксиди лужноземельного металу при контакті з водою, як було відкрито, є надзвичайно ефективним для забезпечення високих виходів сполук Формули 1. Дані основи гідроксиду лужноземельного металу включають гідроксиди кальцію, стронцію або барію, гідроксид кальцію переважний завдяки своїй низькій вартості. Гідроксиди лужноземельного металу Формули 4 можуть бути сформовані in situ зі сполук, здатних формувати гідроксиди лужноземельного металу при контакті з водою (визначених тут як "попередники гідроксиду лужноземельного металу"), такі як гідриди лужноземельного металу. Попередники гідроксиду лужноземельного металу можуть реагувати з водою, яка присутня у реакційній суміші, включаючи воду, що формується в результаті реакції, для формування відповідних гідроксидів лужноземельних металів. Гідриди лужноземельного металу є переважними як попередники, оскільки їх реакція для формування гідроксидів лужноземельного металу видаляє воду, що формується в 19 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 результаті реакції, уникаючи дистиляції. Гідрид кальцію є особливо переважним як попередник гідроксиду лужноземельного металу внаслідок його комерційної доступності та відносно низької вартості. Хоча гідрид кальцію є переважним для прямого видалення води, додавання гідроксиду кальцію для формування реакційної суміші є переважним для способу Схеми 1, у якому воду видаляють за допомогою азеотропної дистиляції, тому що гідроксид кальцію не формує газоподібний водень і є легшим для збільшення масштаб, і, власне кажучи, безпечніший при застосуванні, ніж гідрид металу у великому масштабі. Гідроксид лужноземельного металу додають для формування реакційної суміші так, щоб молярне співвідношення гідроксиду лужноземельного метала до сполуки Формули 3 знаходилося, як правило, в діапазоні від приблизно 0,1 до приблизно 1. Як правило, співвідношення в діапазоні від приблизно 0,5 до приблизно 1 забезпечує високу швидкість реакції та високі виходи продукту. У даному способі реакційна суміш включає і полярний апротонний розчинник, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. Полярний апротонний розчинник може містити суміш сполук полярного апротонного розчинника, але, як правило, являє собою окрему сполуку полярного апротонного розчинника. Як зазвичай розуміють у даній галузі техніки, апротонний розчинник означає рідку сполуку, що не має -OH або -NH частини у своїй молекулярній структурі. Також, як зазвичай розуміють у даній галузі техніки, полярний розчинник означає рідку сполуку, що має діелектричну постійну більше ніж 15. Для даного способу особливо відомі полярні апротонні розчинники є досить полярними для змішування з водою у всіх пропорціях при кімнатній температурі (наприклад, приблизно 20-25 °C). Полярний апротонний розчинник більше переважно має точку кипіння вище, ніж точка кипіння низькокиплячого азеотропу, так що полярний апротонний розчинник не видаляється з реакційної суміші. Дані властивості найкраще забезпечуються амідним і сульфоксидним розчинниками, що є комерційно доступними при відносно низькій вартості. Під амідними розчинниками мають на увазі сполуки розчинника, що містять карбоксамідну молекулярну частину. Загальними прикладами амідних розчинників є N, N-диметилформамід, N, N-диметилацетамід і N-метилпіролідинон. Сульфоксидні розчинники містять сульфоксидну молекулярну частину; загальні приклади включають диметилсульфоксид (також відомий як метилсульфоксид) і сульфолан. N, N-диметилформамід є більше переважним, оскільки він забезпечує прекрасні результати, має точку кипіння значно вище, ніж вода, але все ще може легко видалятися дистиляцією, і є комерційно доступним при відносно низькій вартості. У даному способі включення апротонного розчинника, здатного формувати низькокиплячий азеотроп з водою, сприяє видаленню за допомогою дистиляції води, що утворюється як побічний продукт. Апротонний розчинник зазвичай є окремою сполукою розчинника, але може також бути сумішшю сполук розчинника (наприклад, ізомери ксилолу). Під низькокиплячим азеотропом мається на увазі азеотроп, що має точку кипіння нижче, ніж як точка кипіння води, так і точка кипіння апротонного розчинника. За визначенням, низькокиплячі азеотропи, що містять воду, мають нормальні точки кипіння нижче, ніж 100 °C (тобто нормальна точка кипіння води). Таким чином, точка кипіння низькокиплячого азеотропа буде значно нижче, ніж точки кипіння сполук Формули 1, 2 і 3, і дані сполуки будуть залишатися в реакційній суміші протягом дистиляції. Як уже згадували, переважно, коли полярний апротонний розчинник і апротонний розчинник, здатний формувати низькокиплячий азеотроп, вибирають так, щоб полярний апротонний розчинник мав точку кипіння вище, ніж азеотроп так, щоб полярний апротонний розчинник не видалявся протягом дистиляції. Апротонні розчинники, що формують азеотропи з водою, як добре відомо в даній галузі техніки, і короткі посібники були опубліковані, представляючи їх точки кипіння (див., наприклад, Azeotropic Data, Number 6 у the Advances in Chemistry Series, American Chemical Society, Washington, D.C., 1952, зокрема, сторінки 6–12). Приклади придатних апротонних розчинників, що формують низькокиплячі азеотропи з водою, включають ефіри, такі як етилацетат, ароматичні вуглеводні, такі як бензол і толуол, і ефіри, такі як трет-бутилметиловий ефір, тетрагідрофуран і 1,4-діоксан. Переважно, азеотроп, сформований апротонним розчинником і водою, включає більший процентний вміст води, ніж є розчинним в апротонному розчиннику при кімнатній температурі (наприклад, 15–35 °C), таким чином, полегшуючи великомасштабне відділення води від конденсованого азеотропа в декантаторній пастці, і повторне застосування зневодненого апротонного розчинника до середини дистиляційної колони. Таким чином, апротонні розчинники, що не змішуються з водою, такі як етилацетат, бензол, толуол і трет-бутилметиловий ефір, є більш переважними, ніж тетрагідрофуран і 1,4-діоксан, які змішуються з водою. Трет-бутилметиловий ефір, як було відкрито, є, зокрема, застосовним у якості апротонного розчинника в даному способі. Трет-бутилметиловий ефір формує азеотроп з водою, що кипить 20 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 55 60 при 52,6 °C і утримує 4 % води і 96 % трет-бутилметилового ефіру, і тому здатний швидко переміщати воду дистиляцією з реакційної суміші. Крім того, вода є розчинною в третбутилметиловому ефірі до ступеня тільки приблизно 1 %. Тому у великомасштабних отриманнях, де кількості трет-бутилметилового ефіру в декантаторній пастці не досить для того, щоб розчинити всю воду, що утворилася в результаті реакції, конденсат у пастці буде розділятися на верхній шар, що включає трет-бутилметиловий ефір, що містить тільки приблизно 1 % води, який може бути повернутий до середини дистиляційної колони, і нижній шар, що містить переважно воду, яка може бути видалена. Крім того, відносно низькі точки кипіння трет-бутилметилового ефіру та його азеотропу з водою забезпечують вибір широкого діапазону температур реакції за допомогою регулювання пропорції трет-бутилметилового ефіру, об'єднаного з полярним апротонним розчинником, що має точку кипіння вище 100 °C, значно вище 120 °C (наприклад, N, N-диметилформамід). Наприклад, реакційні суміші, що містять значно більше трет-бутилметилового ефіру, ніж N, N-диметилформаміду (DMF), можуть кипіти при температурах резервуара не набагато вище 55 °C, у той час як реакційні суміші, що містять декілька менше трет-бутилметилового ефіру відносно DMF, можуть кипіти при температурах резервуара вище 100 °C. Як правило, трет-бутилметиловий ефір і N, Nдиметилформамід знаходяться у ваговому співвідношенні в діапазоні від приблизно 0,5 до приблизно 2. Реакція способу Схеми 1 може бути проведена в широкому діапазоні температур. Типово температура реакції дорівнює, щонайменше, приблизно 65 °C. Хоча реакція продовжується при більш низьких температурах, швидкості є нижчими, і азеотропи протонний розчинник-вода, що киплять нижче 50 °C, типово містять відносно мало води (наприклад, дихлорметан формує азеотроп, що містить 1,5 % води), що сповільнює видалення води. Більше типово, температура реакції дорівнює, щонайменше, приблизно 70 °C і найбільше типово, щонайменше, приблизно 75 °C. Хоча високі температури підвищують швидкість реакції, вони можуть також викликати побічні реакції, зменшуючи чистоту та вихід продукту. Тому типово температура реакції складає не більше ніж приблизно 110 °C, більше типово не більше ніж приблизно 100 °C, і найбільше типово не більше ніж приблизно 90 °C. Сполуки Формули 2 і 3, гідроксид лужноземельного метали Формули 4 (або попередник, такий як гідрид лужноземельного металу), полярний апротонний розчинник і апротонний розчинник, здатний формувати низькокиплячий азеотроп, можуть бути з'єднані в будь-якому придатному порядку, щоб сформувати реакційну суміш. Хід реакції може контролюватися за допомогою загальноприйнятих способів, таких як тонкошарова хроматографія, HPLC (ВЕРХ – високоефективна рідинна хроматографія) і 1H ЯМР (ядерний магнітний резонанс) аналізів аліквот. Після завершення реакції, суміш типово прохолоджують до кімнатної температури, і продукт відокремлюють за допомогою загальноприйнятих способів, таких як фільтрація, екстракція, дистиляція та кристалізація. Наприклад, гідроксиди лужного металу й інші тверді речовини, можуть бути звичайно вилучені фільтрацією. Вода може бути додана до фільтрату за сильною кислотою (такою як хлороводнева кислота), щоб нейтралізувати будь-яку основу, що залишилася, і допомогти видалити полярні розчинники, такі як DMF. Відокремлюють органічну фазу, далі промивають водою, щоб видалити полярні розчинники, такі як DMF, сушать над осушувачами, такими як сульфат магнію або молекулярні сита, і потім випаровують розчинник, залишаючи продукт, часто у вигляді кристалічної твердої речовини, що може бути перекристалізована з розчинників, таких як гексани. Для великомасштабних одержань, у яких сушіння з осушувачами є непрактичним, відділена органічна фаза може бути висушена та сконцентрована видаленням дистиляцією як води, так і апротонного розчинника, здатного формувати азеотроп з водою (далі називається тут як "реакційний азеотропний розчинник"). Залишок потім може бути розведений неполярним розчинником, що має точку кипіння вище, ніж реакційний азеотропний розчинник (наприклад, фракція гексанів, що має нормальну точку кипіння 65–70 °C, коли реакційний азеотропний розчинник являє собою трет-бутилметиловий ефір) і дистиляцію продовжили для видалення залишку реакційного азеотропного розчинника і факультативно деякої кількості неполярного розчинника. Часте охолодження суміші, що містить продукт і неполярний розчинник, призводить до кристалізації продукту. Альтернативно неполярний розчинник може бути вилучений додатковою дистиляцією або випарюванням, щоб залишити продукт. Замість виділення продукту може бути більше придатним переміщення продукту в розчинник, застосовний для подальшої реакції (наприклад, спосіб Схеми 6). Після видалення дистиляцією як води, так і реакційного азеотропного розчинника, залишок може бути розведений розчинником, застосовним у подальшій реакції (називається тут як "заміна 21 UA 106468 C2 5 10 15 20 25 30 35 40 45 50 реакційного розчинника"). Малі кількості залишку реакційного азеотропого розчинника можуть бути припустимі в подальшій реакції. Альтернативно, якщо заміна реакційного розчинника має точку кипіння вище, ніж реакційний азеотропний розчинник (наприклад, тетрагідрофуран як заміна реакційного розчинника, коли реакційний азеотропний розчинник являє собою третбутилметиловий ефір), залишок реакційного азеотропного розчинника може бути легко вилучений дистиляцією. Спосіб Схеми 1 типово забезпечує сполуку Формули 1 у вигляді суміші E і Z геометричних ізомерів (позначається хвилястою лінією у Формулі 1), у якій один ізомер може переважати. Способи очищення, такі як перекристалізація, часто забезпечують очищені продукти, що містять здебільше або винятково один геометричний ізомер. В альтернативному способі одержання сполук Формули 1, сполуки Формули 2 і 3 приводять у контакт із гідридом лужноземельного металу, таким як гідрид кальцію, у присутності полярного апротонного розчинника, такого як DMF, уникаючи необхідності включати апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою, або дистиляцію води із суміші. У даному способі гідрид лужноземельного металу слугує у якості як джерела основи, щоб каталізувати конденсацію, так і агента, що осушує, щоб видаляти воду, яка утвориться як побічний продукт. Оскільки гідрид лужного металу слугує у якості основного агента, що осушує, стехіометрія вимагає молярного співвідношення, щонайменше, 0,5 відносно сполук Формули 2 і 3. Типове співвідношення приблизно 1,3 забезпечує велику швидкість реакції та високі виходи продукту. Гідриди лужноземельного металу, як правило, мають маленьку розчинність в інертних до них розчинниках, тому маленький розмір часток покращує масове перенесення та готовність даних реагентів реагувати (наприклад, з водою). Хоча, типове молярне співвідношення гідриду лужного металу до сполуки Формули 3 не більше ніж приблизно 2 потрібно для кращих результатів (тобто високе перетворення та виходи продукту), великий розмір часток гідридів лужноземельного металу може вимагати молярного співвідношення гідриду до сполуки Формули 3 більше ніж 2 для кращих результатів. Даний процес типово проводять при температурі, щонайменше, приблизно 45 °C, більше типово, щонайменше, приблизно 55 °C, і типово не більше ніж приблизно 100 °C, більше типово не більше ніж приблизно 80 °C. У способі винаходу, проілюстрованому в Схемі 1a, сполуку Формули 1 одержують за допомогою етапу, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу карбонату лужного металу Формули 4a, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. 1 де M являє собою Li, Na або K. Перший етап даної реакції включає альдольну конденсацію, що формує сполуку Формули 11. Сполука Формули 11 є невиділеною, але замість цього при реакційних умовах перетворюється в сполуку Формули 1. Стехіометрія даної реакції містить у собі еквімолярні кількості сполук Формули 2 і Формули 3, як описано в Схемі 1. Карбонати лужного металу Формули 4a, як було виявлено, є надзвичайно ефективними для забезпечення високих виходів сполук Формули 1. Дані основи карбонату лужного металу включають карбонат літію, натрію або калію, карбонат калію переважний завдяки своєї низької вартості. Карбонат лужного металу додають для формування реакційної суміші таким чином, щоб молярне співвідношення карбонату лужного металу до сполуки Формули 3 було типово в діапазоні від приблизно 0,01 до приблизно 0,2. Типове співвідношення в діапазоні від приблизно 0,03 до приблизно 0,05 забезпечує повне перетворення сполук Формули 3 у сполуки Формули 1. Карбонат лужного металу може бути доданий у реакційну суміш маленькими порціями так, щоб можна було контролювати швидкість реакції, і швидкість утворення води в реакційній посудині може бути порівнянна зі швидкістю видалення води дистиляцією азеотропа розчинник/вода. У способі Схеми 1a, ацетонітрил, як було відкрито, є надзвичайно корисний у якості 22 UA 106468 C2 5 10 15 апротонного розчинника в даному способі. Ацетонітрил формує водний азеотроп, що кипить при 76,5 °C і утримуючий приблизно 16,3 % води і приблизно 83,7 % ацетонітрила за вагою, і тому є здатним швидко переміщати воду з реакційної суміші за допомогою дистиляції. Реакція способу Схеми 1a може бути проведена в широкому діапазоні температур. Типово температура реакції дорівнює, щонайменше, приблизно 65 °C. Хоча реакція продовжується при більш низьких температурах, швидкості стають менші, й азеотропи апротонний розчинник-вода, що киплять нижче 50 °C, типово містять відносно мало води (наприклад, дихлорметан формує азеотроп, що містить 1,5 % води), що сповільнює видалення води. Більше типово температура реакції дорівнює, щонайменше, приблизно 80 °C і більш типово, щонайменше, приблизно 85 °C. Хоча високі температури підвищують швидкість реакції, вони можуть також призводити до побічних реакцій, знижуючи чистоту та вихід продукту. Тому типово температура реакції складає не більше ніж приблизно 110 °C, більш типово не більше ніж приблизно 100 °C, і більш типово не більше ніж приблизно 90 °C. У способі винаходу, проілюстрованому в Схемі 1b, сполуку Формули 1 одержують за допомогою етапу, на якому дистилюють воду із суміші, що містить сполуку Формули 2, сполуку Формули 3, основу, вибрану з 1,5-діазабіцикло[4.3.0]нон-5-ену, 1,8-діазабіцикло[5.4.0]ундец-7ену і їх сумішей, і апротонний розчинник, здатний формувати низькокиплячий азеотроп з водою. 20 25 30 35 40 45 50 де основа являє собою 1,5-діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміш. Перший етап даної реакції включає альдольну конденсацію, що формує сполуку Формули 11. Сполука Формули 11 є невиділеною, але замість цього при реакційних умовах перетворюється в сполуку Формули 1. Стехіометрія даної реакції містить у собі еквімолярні кількості сполук Формули 2 і Формули 3, як описано Схемою 1. Як було відкрито, 1,5-діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміші є надзвичайно ефективними для забезпечення високих виходів сполук Формули 1. Як 1,5-діазабіцикло[4.3.0]нон-5-ен, так і 1,8-діазабіцикло-[5.4.0]ундец-7-ен є рідинами при 25 °C. У великому (тобто комерційному) масштабі, рідини можуть бути додані в реакційну суміш більш точно та з меншими матеріальними втратами, ніж тверді речовини. 1,5-Діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміш додають, щоб сформувати реакційну суміш так, щоб молярне співвідношення 1,5-діазабіцикло[4.3.0]нон-5-ену, 1,8-діазабіцикло[5.4.0]ундец-7-ену або їх суміші до сполуки Формули 3 знаходилося типово в діапазоні від приблизно 0,01 до приблизно 0,2. Типово, співвідношення в діапазоні від приблизно 0,03 до приблизно 0,05 забезпечує велику швидкість реакції та високі виходи продукту. 1,5-діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або їх суміш можуть бути додані в реакційну суміш маленькими порціями так, щоб швидкістю реакції можна було керувати, та швидкість утворення води в реакційній посудині може бути порівнянна зі швидкістю видалення води дистиляцією азеотропом розчинник/вода. У способі Схеми 1b ацетонітрил, як було відкрито, є надзвичайно корисним у якості апротонного розчинника в даному способі. Ацетонітрил формує водний азеотроп, що кипить при 76,5 °C і утримує 16,3 % води і 83,7 % ацетонітрила за вагою, та тому здатний швидко переміщати воду дистиляцією з реакційної суміші. Реакція способу Схеми 1b може бути проведена в широкому діапазоні температур. Типово температура реакції дорівнює, щонайменше, приблизно 65 °C. Хоча реакція продовжується при температурах нижче, швидкості стають менше, і азеотропи апротонний розчинник-вода, що киплять нижче 50 °C, типово містять відносно мало води (наприклад, дихлорметан формує азеотроп, що містить 1,5 % води), що сповільнює видалення води. Більше типово температура реакції дорівнює, щонайменше, приблизно 80 °C і більше типово, щонайменше, приблизно 85 °C. Хоча високі температури підвищують швидкість реакції, вони можуть також призводити 23 UA 106468 C2 5 10 15 до побічних реакцій, знижуючи чистоту та вихід продукту. Тому типово температура реакції дорівнює не більше ніж приблизно 110 °C, більш типово не більше ніж приблизно 100 °C, і найбільш типово не більше ніж приблизно 90 °C. Що стосується способів Схем 1, 1a і 1b, і вищеописаного альтернативного способу одержання сполук Формули 1 у їх найширших визначеннях, Z у Формулах 1 і 2 являє собою факультативно заміщений феніл, і Q у Формулах 1 і 3 являє собою феніл або 1-нафталеніл, кожен факультативно заміщений. Q і Z є придатками, що прямо не беруть участь в альдольній конденсації та дегідратації, забезпечуючи сполуки Формули 1. Реакційні умови даних способів є відносно м'якими і, таким чином, забезпечують широкий діапазон факультативних замісників у фенілі та 1-нафталенілі. Тільки функціональності, найбільш реакційно-здатні до гідроксидних основ, є сприйнятливими до того, щоб бути порушеними. Тому, визначені замісники у фенільній і 1- нафталенільній частинах Q і Z, описані у варіантах здійснення (наприклад, 1-1G, 2-2O, A-A7) і будь-де у даному розкритті, варто розглядати тільки як ілюстративні, оскільки об'єм корисності даних способів є більш загальний. У способі даного винаходу, проілюстрованого в Схемі 2, сполуку Формули 2 одержують з відповідної сполуки Формули 5, коли формують проміжну сполуку реактиву Гріньяра (описаного як Формула 12), і потім вводять у реакцію реактив Гріньяра зі сполукою Формули 6. Схема 2 O Y [Mg] Z–X 5 Z Mg X1 12 20 25 30 35 40 45 50 CF3 6 F3C O Z 2 В одному варіанті здійснення даного способу сполуку Формули 5 приводять у контакт із металевим магнієм у присутності ефірного розчинника, щоб одержати реактив Гріньяра. У контексті даного розкриття та формули винаходу, ефірний розчинник включає одну або більше органічних сполук, що включають атоми, вибрані з водню, вуглецю і кисню, і що мають, щонайменше, один ефірний зв'язок (тобто C-O-C), але без іншої функціональності. Загальні приклади ефірів включають діетиловий ефір, тетрагідрофуран, 1,4-діоксан і 1,2-диметоксіетан, але інші ефіри, такі як бутилдиглім (1,1'-[оксибіс(2,1-етандіілокси)]бісбутан) також застосовують для одержання, і застосування реактивів Гріньяра. Типово в даному варіанті здійснення ефірний розчинник включає діетиловий ефір або тетрагідрофуран. Більше типово ефірний розчинник включає тетрагідрофуран. Коли реактив Гріньяра одержують, застосовуючи 1 металевий магній, X у Схемі 2 є таким же, як X, якщо не додають інші аніонні частки в реакційну суміш. Для одержання реактивів Гріньяра з металевого магнію, метал знаходиться типово у формі стружки, ошурок або порошку, щоб забезпечити велику площу поверхні реакції. Типово металевий магній приводять у контакт зі сполукою Формули 5 при температурі, щонайменше, приблизно 0 °C, більше типово, щонайменше, приблизно 20 °C, і найбільше типово, щонайменше, приблизно 25 °C. Типово температура дорівнює не більше ніж приблизно 65 °C, більш типово не більше ніж приблизно 40 °C, і найбільш типово не більше ніж приблизно 35 °C. Оскільки стехіометрія вимагає, щонайменше, еквімолярної кількості металевого магнію відносно до сполуки Формули 5 для повного перетворення, молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює типово, щонайменше, приблизно 1, більш типово, щонайменше, приблизно 1,02 і найбільш типово, щонайменше, приблизно 1,05. Хоча великі надлишки металевого магнію можуть застосовуватися, вони дають переваги та підвищують тверді залишки. Типово молярне співвідношення металевого магнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,2, і більш типово не більше ніж приблизно 1,1. Альтернативно в іншому варіанті здійснення даного способу, реактив Гріньяра одержують приведенням у контакт сполуки Формули 5 з галогенідом алкілмагнію. Для приклада даного способу формування реактивів Гріньяра див J. L. Leazer і R. Cvetovich, Org. Syn. 2005, 82, 115– 119. Галогенід алкілмагнію є типово галогенідом вторинного алкілмагнію, що є більше реакційноздатним, ніж основний галогенід алкілмагнію. Типово галогенід алкілмагнію являє собою галогенід C1–C4 алкілмагнію. Слід зазначити галогенід алкілмагнію, що є галогенідом ізопропілмагнію, особливо хлоридом ізопропілмагнію. У даному варіанті здійснення даного 24 UA 106468 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 способу, X у Схемі 2 представляє суміш аніонів, забезпечуючи як X у сполуці Формули 5, так і галоїд галогеніду алкілмагнію. Наприклад, якщо X є I, а галогенід алкілмагнію є хлоридом 1 ізопропілмагнію, тоді X представляє суміш Cl і I (що є присутнім у виді аніонів). У даному варіанті здійснення сполуку Формули 5 приводять у контакт із галогенідом алкілмагнію в присутності ефірного розчинника. Типово сполуку Формули 5 приводять у контакт із галогенідом алкілмагнію при температурі, щонайменше, –30 °C, більш типово, щонайменше, –20 °C і найбільш типово, щонайменше, приблизно –10 °C. Типово температура дорівнює не більше ніж приблизно 40 °C, більш типово не більше ніж приблизно 20 °C, і найбільш типово не більше ніж приблизно 10 °C. Типово в даному варіанті здійснення, ефірний розчинник включає діетиловий ефір, тетрагідрофуран або їхню суміш, і більш типово ефірний розчинник включає тетрагідрофуран. Оскільки стехіометрія вимагає, щонайменше, еквімолярну кількість галогеніду алкілмагнію відносно до сполуки Формули 5 для повного перетворення, молярне співвідношення галогеніду алкілмагнію до сполуки Формули 5 дорівнює типово, щонайменше, приблизно 1, і більш типово, щонайменше, приблизно 1,05. Хоча можуть застосовуватися великі надлишки галогеніду алкілмагнію, вони можуть згодом реагувати зі сполукою Формули 6, таким чином, потрібно більше сполуки Формули 6 і виходить більше побічного продукту. Типово молярне співвідношення галогеніду алкілмагнію до сполуки Формули 5 дорівнює не більше ніж приблизно 1,2, і більш типово не більше ніж приблизно 1,15. Проте, можуть бути потрібні більші кількості галогеніду алкілмагнію, щоб компенсувати домішки води в реакційному розчиннику. Як добре відомо в даній галузі техніки, реактиви Гріньяра реагують дуже швидко з розчинниками, що містять гідроксильні групи, включаючи воду, і, таким чином, розчинники для одержання і застосування реактивів Гріньяра повинні містити настільки мало домішок води, наскільки можна, тобто бути безводними. Також, оскільки реактиви Гріньяра реагують з киснем, реакційні суміші переважно захищають від кисню, наприклад, покривають газом азотом або аргоном. Для обох варіантів здійснення даного способу, і особливо варіанта здійснення формування реактиву Гріньяра з застосуванням галогеніду алкілмагнію, спосіб може проводитися в присутності ароматичного вуглеводневого розчинника з додаванням ефірного розчинника. Вираз "ароматичний вуглеводний розчинник" у даному способі означає розчинник, що містить одну або більше ароматичних вуглеводневих сполук. Ароматичні вуглеводні сполуки містять тільки атоми вуглецю та водню, і для ароматичності містять, щонайменше, одне бензольне кільце, що може бути заміщеним вуглеводневими частинами, такими як алкільні групи. Ароматичні вуглеводневі розчинники, як правило, включають один або більше бензол, толуол і ксилол (який типово є присутнім як суміш ізомерів). Оскільки ароматичні вуглеводневі розчинники є більше висококиплячими, ніж звичайні ефірні розчинники, такі як діетиловий ефір і тетрагідрофуран, включення ароматичних вуглеводних розчинників у реакційну суміш, що формує реактив Гріньяра, поліпшує запас надійності у великомасштабному виробництві. Утворення реактивів Гріньяра, як правило, є екзотермічним, і у випадку втрати охолодження та подальшої втрати низькокиплячого ефірного розчинника, присутність більш висококиплячого ароматичного вуглеводневого розчинника зменшить реакцію. Для даного способу толуол є надзвичайно переважним у якості ароматичного вуглеводневого розчинника внаслідок своєї низької вартості, відносно низької токсичності, низької точки замерзання та помірно високій точці кипіння. Відповідно до даного способу, реакційну суміш, що містить реактив Гріньяра, сформований зі сполуки Формули 5, потім приводять у контакт зі сполукою Формули 6, щоб одержати сполуку Формули 2. Сполуку Формули 6 типово приводять у контакт із реакційною сумішшю, що містить реактив Гріньяра при температурі, щонайменше, приблизно –80 °C, більш типово, щонайменше, приблизно –25 °C, і найбільш типово, щонайменше, приблизно –5 °C. Температура дорівнює типово не більш ніж приблизно 0 °C. Типову сполуку Формули 6 додають у реакційну суміш, що містить реактив Гріньяра в розчині, і застосовують надлишок сполуки Формули 6 відносно реактиву Гріньяра, отриманого зі сполуки Формули 5. Альтернативно, реакційна суміш, що містить реактив Гріньяра, отриманий зі сполуки Формули 5, може бути додана в надлишок сполуки Формули 6. Коли реактив Гріньяра одержують з металевого магнію, молярне співвідношення сполуки Формули 6 відносно сполуки Формули 5 дорівнює типово, щонайменше, приблизно 1,05 і більш типово, щонайменше, приблизно 1,1, і типово не більше ніж приблизно 1,3 і більш типово не більше ніж приблизно 1,2. Коли реактив Гріньяра одержують з галогеніду алкілмагнію, кількість галогеніду алкілмагнію, що застосовують, є більш важливою, ніж кількість сполуки Формули 5 відносно сполуки Формули 6, тому надлишок галогеніду алкілмагнію може також реагувати зі сполукою Формули 6. У даному варіанті здійснення співвідношення сполуки Формули 6 до галогеніду алкілмагнію, що застосовують, дорівнює типово, щонайменше, 25 UA 106468 C2 5 10 15 20 25 30 35 40 приблизно 1,05 і більш типово, щонайменше, приблизно 1,1, і типово не більше ніж приблизно 1,3 і більш типово не більше ніж приблизно 1,2. Реакційну суміш типово обробляють додаванням водяної мінеральної кислоти, такої як хлороводнева кислота, і екстрагують продукт у помірно полярний органічний розчинник, що не змішується з водою, такий як діетиловий ефір, дихлорметан або толуол. Зазвичай сполуку Формули 2 одержують у суміші з його гідратним похідним і його алкілгемі-кетальним похідним (з алканольного побічного продукту, що формується зі сполуки Формули 6, коли Y являє собою 11 OR ). Будь-яка або обидві з даних похідних сполуки Формули 2 можуть бути легко перетворені в сполуку Формули 2 при обробленні (тобто приведенні в контакт) сильною кислотою, такою як органічна сульфонова кислота, наприклад, п-толуолсульфонова кислота, у присутності апротонного органічного розчинника, і видаленні води і/або алканолу, утвореного дистиляцією. Переважно апротонний органічний розчинник є таким, що не змішується з водою. Типово апротонний органічний розчинник включає один або більше розчинників, вибраних з вуглеводнів, таких як гептан або толуол, і галогенованих вуглеводнів, таких як 1,2-дихлорентан. Протягом дистиляції, реакційну суміш у посудині типово нагрівають, щонайменше, до приблизно 45 °C, більш типово, щонайменше, приблизно 80 °C, типово не більше ніж приблизно 120 °C, більш типово не більше ніж приблизно 110 °C, і більш типово не більше ніж приблизно 100 °C. Розчинники, такі як гептан, толуол і 1,2-дихлоретан і їх азеотропи з водою і алканолами, мають нормальні точки кипіння, забезпечуючи дані реакційні температури. Розчинники, такі як толуол, що формують низькокиплячі азеотропи з водою і алканолами, є переважними. Після видалення води й алканолів, дистиляція може бути продовжена для видалення розчинника, і продовжена при зниженому тиску для відокремлення сполуки продукту Формули 2. Спосіб Схеми 2 є особливо застосовним, коли X є I (тобто йод), тому це сприяє одержанню сполук Формули 2, де Z являє собою фенільне кільце, факультативно заміщене до 5 замісниками, вибраними не тільки з F, алкілу, фторалкілу, алкокси, фторалкокси, алкілтіо і фторалкілтіо, але також Cl і Br, що можуть бути більш придатними, щоб реагувати з металевим магнієм або галогенідами алкілмагнію, якщо X є Cl або Br. Хоча реактиви Гріньяра частіше одержують із хлор- або бромфенільних сполук, йодфенільні сполуки (тобто X є I), як виявлено, добре працюють при утворенні реактивів Гріньяра, і, більш того, коли X є I, фенільне кільце може бути заміщеним галогенами в інших положеннях, особливо в 3- і 5-положеннях (відносно X), що є особливо застосовним, щоб формувати інсектицидні 4,5-дигідроізоксазольні сполуки. Відомим є спосіб Схеми 2, де X є I, і Z являє собою феніл, заміщений у 3- і 5-положеннях відносно X замісниками, незалежно вибраними з Cl, Br і CF3, особливо де один замісник являє собою CF3, і інший замісник являє собою CF3, Cl або Br, більше особливо, де один замісник являє собою CF3, і інший замісник являє собою Cl або Br, і найбільш особливо, де один замісник являє собою CF3, і інший замісник являє собою Cl. Сполуки Формули 5 і 6 можуть бути отримані безліччю способів, відомих у даній галузі техніки. Багато які з даних сполук є відомими, і значне число є комерційно доступним. Вищезгаданий варіант здійснення способу Схеми 2 містить у собі сполуки Формули 5, де X являє собою I (наприклад, 1-хлор-3-йод-5-(трифторметил)бензол). Дані сполуки можуть бути отримані способом, проілюстрованим у Схемі 3. У даному способі сполуку Формули 13 діазотують, щоб одержати проміжну сполуку солі діазонію, яку потім відновлюють, щоб одержати сполуку Формули 5a (тобто Формули 5, де X є I). 45 a 50 2 де R являють собою замісники, такі як R , як визначено у варіанті здійснення 3H. У даному способі, сполуку Формули 13 приводять у контакт із натрію нітритом у присутності мінеральної кислоти, такої як хлороводнева кислота або сірчана кислота. Зазвичай для переважних результатів два або більше молярні еквіваленти мінеральної кислота потрібно 26 UA 106468 C2 5 10 15 відносно числа молів сполуки Формули 5a, що застосовують у реакції. Реакцію типово проводять у придатному розчиннику, такому як водна хлороводнева кислота або оцтова кислота. Температуру в діапазоні від приблизно –5 до приблизно 5 °C зазвичай застосовують для одержання солі діазонію. Сіль діазонію сполуки Формули 13 потім приводять у контакт з агентом, що відновлює, таким як гіпофосфорна кислота або етанол, щоб забезпечити сполуку Формули 5a. Реакцію відновлення зазвичай проводять у такому ж розчиннику, як застосовують для одержання солі діазонію при температурі від приблизно 5 до приблизно 20 °C. Продукт Формули 5a може бути відділений стандартними процедурами, такими як кристалізація, екстракція і дистиляція. Даний загальний спосіб діазотування і відновлення анілінів є добре відомим, і був розглянутий; див., наприклад, N. Kornblum, Org. Reactions 1944, 2, 262–340. 2-хлор-6-йод-4-(трифторметил)бензоламін, 4-хлор-2-йод-6-(трифторметил)бензоламін і 2хлор-4-йод-6-(трифторметил)бензоламін є особливо важливими як сполуки Формули 13 для одержання 1-хлор-3-йод-5-(трифторметил)бензолу як сполуки Формули 5a даним способом. Сполуки Формули 13 можуть бути отримані зі сполук Формули 14 йодуванням, як показано в Схемі 4. a 20 25 30 2 де R є замісники, такі як R , як визначено у варіанті здійснення 3H. У даному способі сполуку Формули 14 приводять у контакт із реагентом йодування, таким як монохлорид йоду, у придатному розчиннику, такому як вода або оцтова кислота. Факультативно хлороводнева кислота може бути включена в реакційну суміш для того, щоб підвищити розчинність сполуки Формули 14 і монохлориду йоду в реакційному середовищі. Зазвичай потрібно тільки приблизно один молярний еквівалент монохлориду йоду, щоб повністю перетворити сполуку Формули 14 у сполуку Формули 13. Великі молярні надлишки монохлориду йоду можуть застосовуватися, щоб скоротити час реакції, але підвищують вартість способу. Реакція може проводитися в температурному діапазоні від приблизно 0 до приблизно 100 °C, типово при температурі приблизно 50 °C. Продукт Формули 13 може бути відділений загальноприйнятими способами, такими як фільтрація, екстракція і дистиляція. Як проілюстровано в Схемі 5, сполуки Формули 13a, що містять, щонайменше, одну частину хлору або брому, можуть також бути отримані при введенні в контакт відповідних сполук Формули 13 із придатним агентом хлорування або бромування, таким як хлор, хлороводнева кислота/пероксид водню, або бромоводнева кислота/пероксид водню. 35 a 2 де R є замісниками, такими як R , як визначено у варіанті здійснення 3H; щонайменше, b b a один R являє собою Cl (із хлорування) або Br (із бромування) і інші приклади R є R замісниками Формули 13; і p=n + число атомів хлору або брому з хлорування або бромування, 27 UA 106468 C2 5 відповідно. Реакцію проводять у розчиннику, такому як вода або оцтова кислота. Температурний діапазон може бути від 0 до 100 °C з температурним діапазоном між 25 і 50 °C, що є переважним. В іншому аспекті даного винаходу, сполуки Формули 1, отримані способом Схеми 1, є застосовними для одержання сполук Формули 7. F 3C O Z N Q 7 10 Безліч шляхів є можливими для одержання сполук Формули 7 зі сполук Формули 1. В одному способі, як показано в Схемі 6, сполуку Формули 1 приводять у контакт із гідроксиламіном і основою, щоб одержати 5-(трифторметил)-4,5-дигідроізоксазол сполуку Формули 7. 15 20 25 30 35 40 45 Гідроксиламін може утворюватися із солі мінеральної кислоти, такої як сульфат гідроксиламіну або хлорид гідроксиламіну, при обробці основою в придатному розчиннику, або може бути отриманий комерційно у вигляді 50 % водного розчину. У даному способі перед введенням у контакт з єноном Формули 1, гідроксиламін або його сіль мінеральної кислоти типово приводять у контакт із основою. Коли застосовують сіль мінеральної кислоти та гідроксиламіна, основу приводять у контакт у кількості більшої, ніж кількість, що необхідна для перетворення гідроксиламінової солі мінеральної кислоти в гідроксиламін. Основа не витрачається в реакції Схеми 6, і, як виявляється, діє як каталізатор бажаної циклізації. Депротонування гідроксиламіну основою перед приведенням у контакт з єноном Формули 1 необхідно для того, щоб одержати гарні виходи, оскільки у відсутності основи реакція гідроксиламіну з єнонами може давати продукти, відмінні від сполук Формули 1. Таким чином, хоча часто приблизно один молярний еквівалент основи (на додаток до будь-якої основи, що застосовують для того, щоб перетворити гідроксиламінову сіль мінеральної кислоти в гідроксиламін) застосовують відносно гідроксиламіну, менше ніж один молярний еквівалент основи може давати чудові результати. Більше ніж один молярний еквівалент (наприклад, до приблизно 5 молярних еквівалентів) основи відносно гідроксиламіну можна застосовувати за умови, що надлишок основи не реагує з єноном Формули 1 або ізоксазолом Формули 7. Можна застосовувати молярний надлишок від одного до трьох еквівалентів гідроксиламіну відносно єнону Формули 1. Щоб забезпечити рентабельність, повне і швидке перетворення єнону Формули 1 у ізоксазол Формули 7, способом, що підходить для великомасштабного виробництва, найбільш придатним, як правило, є співвідношення між приблизно одним і приблизно двома молярними еквівалентами гідроксиламіну відносно єнону Формули 1. Придатні основи можуть включати, але не обмежуються, алкоксиди лужного металу, такі як метоксид натрію, карбонати лужного металу, такі як карбонат натрію або карбонат калію, гідроксиди лужного металу, такі як гідроксид натрію і гідроксид калію, і органічні основи. Переважними органічними основами є амінні основи, що мають, щонайменше, одну пару вільних електронів, доступних для протонування, такі як піридин, триетиламін або N, Nдіізопропілетиламін. Можна застосовувати більш слабкі основи, такі як піридин, але більш сильні основи, що ефективно депротонують гідроксиламін, такі як алкоксид лужного металу або гідроксид лужного металу, типово забезпечують кращі результати. Через те, що вода є особливо застосовним розчинником для депротонування гідроксиламіну, а також одержання 28
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for preparing 3-trifluoromethyl chalcones
Автори російськоюAnnis, Gary, David
МПК / Мітки
МПК: C07C 49/80, C07C 45/47, C07C 25/00, C07D 261/04, C07C 45/68
Мітки: спосіб, халконів, одержання, 3-трифторметильних
Код посилання
<a href="https://ua.patents.su/75-106468-sposib-oderzhannya-3-triftormetilnikh-khalkoniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 3-трифторметильних халконів</a>
Попередній патент: Спосіб одержання нітрильних сполук
Наступний патент: Керовані пристроями списки точок доступу в бездротовому зв’язку
Випадковий патент: Спосіб розрахунку маси хлорофілу на одиницю площі насаджень