Заміщені піперидини
Номер патенту: 107576
Опубліковано: 26.01.2015
Автори: Герікке Керстен Маттіас, Гнот Марк Жан, Хаймбах Дірк, Рьоріг Сусанне, Бендер Еккхард, Бухмюллер Аня, Циммерманн Катя, Гердес Кристоф, Єске Маріо, Канчо Гранде Йоланда
Формула / Реферат
1. Сполука формули
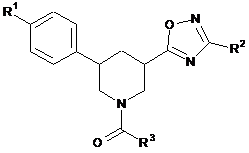 , (I)
, (I)
в якій
R1 означає трифторметил, 1,1-дифторетил, 2,2-дифторетил, 2,2,2-трифторетил, дифторметокси, трифторметокси або етил,
R2 означає 2-гідроксіет-1-ил, 2-метоксіет-1-ил, 2-етоксіет-1-ил, циклопропіл або 1-метоксициклопроп-1-іл,
R3 означає групу формули
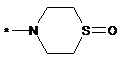 або
або 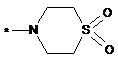 ,
,
причому
* означає місце приєднання до карбонільної групи,
або одна з її солей, її сольватів або сольватів її солей.
2. Сполука за пунктом 1, де R1 означає трифторметил, 2,2,2-трифторетил, трифторметокси або етил,
R2 означає 2-метоксіет-1-ил, циклопропіл або 1-метоксициклопроп-1-іл,
R3 означає групу формули
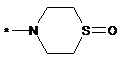 або
або 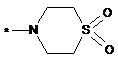 ,
,
причому
* означає місце приєднання до карбонільної групи,
або одна з її солей, її сольватів або сольватів її солей.
3. Сполука за пунктом 1 або 2, де
R1 означає трифторметокси,
R2 означає 2-метоксіет-1-ил або циклопропіл,
R3 означає групу формули
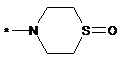 або
або 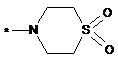 ,
,
причому
* означає місце приєднання до карбонільної групи,
або одна з її солей, її сольватів або сольватів її солей.
4. Сполука за будь-яким із пунктів 1-3, де фенільний замісник і 1,2,4-оксадіазол-5-ільний замісник, які приєднані до піперидинового кільця, знаходяться у цис-положенні один відносно одного.
5. Сполука за будь-яким із пунктів 1-4, де
R1 означає трифторметокси,
R2 означає циклопропіл,
R3 означає групу формули
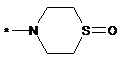 або
або 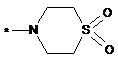 ,
,
причому
* означає місце приєднання до карбонільної групи,
або її солі.
6. Сполука за будь-яким із пунктів 1-5, де зв'язаний із фенільним замісником атом вуглецю має S-конфігурацію і атом вуглецю, зв'язаний із 1,2,4-оксадіазол-5-ілзамісником, також має S-конфігурацію.
7. Сполука формули (І) за пунктом 1, яка є {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметокси)феніл]піперидин-1-іл}(1,1-діоксидотіоморфолін-4-іл)метаноном і має наступну структурну формулу:
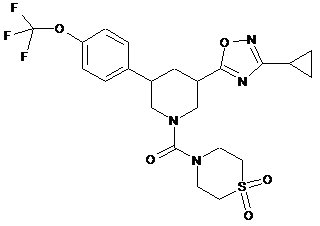 ,
,
або її солі.
8. Сполука формули (І) за пунктом 1, яка є {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметокси)феніл]піперидин-1-іл}(1,1-діоксидотіоморфолін-4-іл)метаноном і має наступну структурну формулу:
 .
.
9. Сполука формули (І) за пунктом 1, яка є {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметокси)феніл]піперидин-1-іл}(1,1-діоксидотіоморфолін-4-іл)метаноном і має наступну структурну формулу:
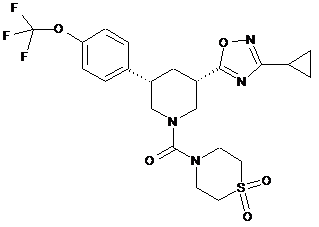 ,
,
або її солі.
10. Сполука формули (І) за пунктом 1, яка є {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметокси)феніл]піперидин-1-іл}(1,1-діоксидотіоморфолін-4-іл)метаноном і має наступну структурну формулу:
 .
.
11. Спосіб одержання сполуки формули (І) або однієї з її солей, її сольватів або сольватів її солей за пунктом 1, який відрізняється тим, що
[А] сполуку формули
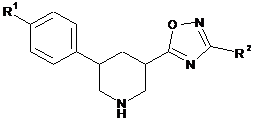 , (II)
, (II)
в якій
R1 та R2 мають вказані у пункті 1 значення,
піддають взаємодії зі сполукою формули
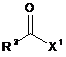 , (IIІ)
, (IIІ)
в якій
R3 має вказані у пункті 1 значення, а
X1 означає галоген, переважно бром, або хлор, або гідрокси, або 4-нітрофенокси.
12. Спосіб одержання сполуки формули (І) або однієї з її солей, її сольватів або сольватів її солей за пунктом 1, який відрізняється тим, що
[В] сполуку формули (II) на першій стадії піддають взаємодії з 4-нітрофенілхлорформіатом, а на другій стадії - зі сполукою формули
![]() , (IV)
, (IV)
в якій
R3 має вказані у пункті 1 значення.
13. Спосіб одержання сполуки формули (І) або однієї з її солей, її сольватів або сольватів її солей за пунктом 1, який відрізняється тим, що
[С] сполуку формули
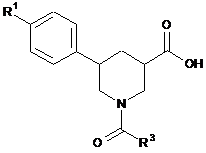 , (V)
, (V)
в якій
R1 та R3 мають вказані у пункті 1 значення,
піддають взаємодії зі сполукою формули
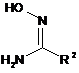 , (VI)
, (VI)
в якій
R2 має вказані у пункті 1 значення.
14. Спосіб одержання сполуки формули (І) або однієї з її солей, її сольватів або сольватів її солей за пунктом 1, який відрізняється тим, що
[D] сполуку формули
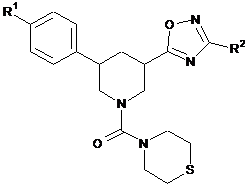 , (Ia)
, (Ia)
в якій
R1 та R2 мають вказані у пункті 1 значення,
піддають взаємодії з 0,8-1,1 еквівалентами мета-хлорпербензойної кислоти з одержанням сполуки формули
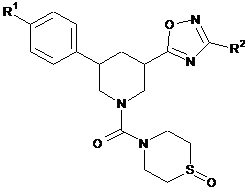 , (Ib)
, (Ib)
в якій
R1 та R2 мають вказані у пункті 1 значення.
15. Спосіб одержання сполуки формули (І) або однієї з її солей, її сольватів або сольватів її солей за пунктом 1, який відрізняється тим, що
[Е] сполуку формули (Іа) піддають взаємодії з 2,0-3,0 еквівалентами мета-хлорпербензойної кислоти з одержанням сполуки формули
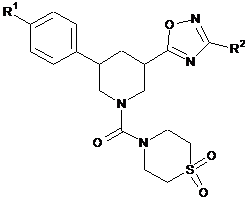 , (Ic)
, (Ic)
в якій
R1 та R2 мають вказані у пункті 1 значення.
16. Застосування сполуки за одним із пунктів 1-10 для одержання лікарського засобу для лікування та/або профілактики серцево-судинних, тромбоемболічних та/або пухлинних захворювань.
Текст
Реферат: Винахід стосується нових заміщених піперидинів R 1 O N N R 2 N O R 3 , способу їх одержання, їх застосування для лікування та/або профілактики захворювань, а також їх застосування для одержання лікарських засобів для лікування та/або профілактики захворювань, зокрема серцево-судинних та пухлинних захворювань. UA 107576 C2 (12) UA 107576 C2 R 1 O N N N O R 3 R 2 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід стосується нових заміщених піперидинів, способу їх одержання, їх застосування для лікування та/або профілактики захворювань, а також їх застосування для одержання лікарських засобів для лікування та/або профілактики захворювань, зокрема серцево-судинних та пухлинних захворювань. Тромбоцити є важливим фактором як при фізіологічній зупинці кровотечі (гемостаз), так і у випадку тромбоемболічних захворювань. Зокрема в артеріальній системі тромбоцити відіграють ключову роль у комплексній взаємодії між компонентами крові та стінками судин. Небажана активація тромбоцитів може призвести до утворення збагачених тромбоцитами тромбів та до подальшого виникнення тромбоемболічних захворювань і тромботичних ускладнень, що супроводжуються загрозливими для життя станами. Одним із найсильніших активаторів тромбоцитів є протеаза згортання крові тромбін, який утворюється на ушкоджених стінках кровоносних судин та окрім утворення фібрину призводить до активації тромбоцитів, клітин ендотелію і мезенхімальних клітин (Vu TKH, Hung DT, Wheaton VI, Coughlin SR, Cell 1991, 64, 1057-1068). На прикладі тромбоцитів in vitro та у експериментальних моделях тварин інгібітори тромбіну уповільнюють накопичення тромбоцитів або відповідно утворення збагачених тромбоцитами тромбів. В організмі людини вдається успішно запобігати або лікувати артеріальні тромбози за допомогою інгібіторів функцій тромбоцитів, а також інгібіторів тромбіну (Bhatt DL, Topol EJ, Nat. Rev. Drug Discov. 2003, 2, 1528). Тому існує висока вірогідність того, що антагоністи впливу тромбіну на тромбоцити зможуть зменшити утворення тромбів та виникнення клінічних наслідків, таких як інфаркт міокарда і апоплексія. Інші види клітинного впливу тромбіну, наприклад, на клітини ендотелію судин та клітини гладкої мускулатури судин, лейкоцити і фібробласти, ймовірно відповідають за запальні і проліферативні захворювання. Клітинні ефекти тромбіну щонайменше частково опосередковані сім'єю рецепторів, поєднаних з G-протеїнами (Protease Activated Receptors, PARs, активовані протеазами рецептори), прототип яких представляє рецептор PAR-1. PAR-1 активується шляхом зв'язування з тромбіном і протеолітичного розщеплення його позаклітинного N-кінця. В результаті протеолізу утворюється новий N-кінець з амінокислотною послідовністю SFLLRN…, який як агоніст ("прив'язаний ліганд") призводить до внутрішньомолекулярної активації рецептора та передачі внутрішньоклітинних сигналів. Пептиди, похідні від послідовності прив'язаних лігандів, можуть бути використані як агоністи рецептора, вони спричиняють активацію і накопичення тромбоцитів. Інші протеази також здатні активувати PAR-1, сюди належать, наприклад, плазмін, фактор VIIa, фактор Xa, трипсин, активований протеїн C (aPC), триптаза, катепсин G, протеїназа 3, гранзим A, еластаза і матриксна металопротеїназа 1 (MMP1). На відміну від інгібування активності протеази тромбіну прямими інгібіторами тромбіну блокада PAR-1 повинна приводити до уповільнення активації тромбоцитів, не зменшуючи при цьому здатність до згортання крові (антикоагуляція). Антитіла та інші селективні антагоністи PAR-1 уповільнюють індуковане тромбіном накопичення тромбоцитів in vitro при низьких-середніх концентраціях тромбіну (Kahn ML, Nakanishi-Matsui M, Shapiro MJ, Ishihara H, Coughlin SR, J. Clin. Invest. 1999, 103, 879-887). Ще один тромбіновий рецептор із можливим значенням для патофізіології тромботичних процесів, PAR-4, ідентифікується на тромбоцитах людини і тварини. В експериментальних моделях тромбозів тварин із подібним до людини зразком PAR-експресії антагоністи PAR-1 зменшують утворення збагачених тромбоцитами тромбів (Derian CK, Damiano BP, Addo MF, Darrow AL, D'Andrea MR, Nedelman M, Zhang H-C, Maryanoff BE, Andrade-Gordon P, J. Pharmacol. Exp. Ther. 2003, 304, 855-861). В останні роки була досліджена велика кількість речовин з огляду на їх здатність інгібувати функцію тромбоцитів, однак на практиці перевірку пройшли лише деяки з інгібіторів функції тромбінів. Тому існує потреба у лікарських засобах, які б специфічно інгібували зростаючу реакцію тромбоцитів, значно не збільшуючи ризик кровотечі і таким чином зменшуючи ризик тромбоемболічних ускладнень. Ефекти тромбіну, опосередковані рецептором PAR-1, впливають на перебігзахворювання під час або після оперативного коронарного шунтування (CABG), а також інших операцій та зокрема операцій з екстракорпоральним кровообігом (наприклад, штучне серце і легені). В ході операції передопераційне або інтраопераційне медикаментозне лікування антикоагулянтами та/або речовинами, що уповільнюють накопичення тромбоцитів, може викликати кровотечі. Тому, наприклад, лікування клопідогрелем необхідно припинити за кілька днів до CABG. Крім того, як було зазначено (наприклад, через тривалий контакт крові і штучних поверхонь при застосуванні екстракорпоральної циркуляції або при переливанні крові) може спостерігатися 1 UA 107576 C2 5 10 15 20 25 30 35 розповсюджене внутрішньосудинне згортання або коагулопатія споживання (ДВК), які можуть бути вторинними причинами кровотечі. На подальшому етапі часто виникає рестеноз накладених венозних або артеріальних шунтів (аж до повної закупорки) внаслідок тромбозу, фіброзу інтими, артеріосклерозу, стенокардії, інфаркту міокарда, серцевої недостатності, аритмії, транзиторної ішемічної атаки (TIA) та/або апоплексії. В організмі людини також інші клітини експресують рецептор PAR-1, зокрема, наприклад, клітини ендотелію, клітини гладкої мускулатури судин і пухлинні клітини. Злоякісні пухлинні захворювання (рак) характеризуються високою частотою нових випадків захворювання та загалом пов'язані з високою смертністю. За допомогою сучасних методів лікування лише у деяких пацієнтів спостерігається повна ремісія та зазвичай таке лікування пов'язане зі складними побічними ефектами. Тому існує велика потреба у більш ефективних і надійних методах лікування. Рецептор PAR-1 спричиняє виникнення, ріст, інвазивність і метастазування раку. Крім того PAR-1, експресований клітинами ендотелію, опосередковує сигнали, які викликають ріст судин ("ангіогенез"), процес, який є необхідною умовою для росту пухлини на понад 1 мм³. Ангіогенез також спричиняє виникнення або загострення інших захворювань, таких як, наприклад, гематопоетичні ракові захворювання, дегенерація жовтої плями і діабетична ретинопатія, які призводять до втрати зору, запальні захворювання, такі як ревматоїдний артрит і коліт. Сепсис (або септицемія) – це розповсюджене захворювання із високою летальністю. Початкові симптоми є зазвичай неспецифічними (наприклад, підвищена температура, погіршення самопочуття), однак надалі може спостерігатися загальна активація системи згортання крові (дисемінована внутрішньосудинна коагулопатія або "коагулопатія споживання" (ДВК)), що супроводжується мікротромбозом у різних органах і вторинними кровотечами. ДВК може також виникати незалежно від сепсису, наприклад, у рамках операцій або онкозахворювань. Лікування сепсису, з одного боку, полягає у поступовому усуненні інфекційної причини, наприклад, шляхом оперативної санації осередку ураження і антибіозу. З іншого боку, лікування полягає у тимчасовій інтенсивній медичній підтримці уражених систем органів. Способи лікування різних стадій цього захворювання описані, наприклад, у наведених нижче публікаціях (Dellinger et al., Crit. Care Med. 2004, 32, 858-873). На сьогодні, як доведено, не існує ефективних методів лікування ДВК. Тому задача даного винаходу полягала в одержанні нових антагоністів PAR-1 для лікування захворювань, таких як, наприклад, серцево-судинні захворювання та тромбоемболічні захворювання, а також пухлинні захворювання у людей і тварин. WO 2006/012226, WO 2006/020598, WO 2007/038138, WO 2007/130898, WO 2007/101270 та US 2006/0004049 описують структурно подібні піперидини як інгібітори 11-β HSD1 для лікування зокрема діабету, тромбоемболічних захворювань та апоплексії. Об'єктом даного винаходу є сполуки формули 1 R O N 2 R N (I) N 3 R O 40 45 в якій 1 R означає трифторметил, 1,1-дифторетил, 2,2-дифторетил, 2,2,2-трифторетил, дифторметокси, трифторметокси або етил, 2 R означає 2-гідроксиет-1-ил, 2-метоксиет-1-ил, 2-етоксиет-1-ил, циклопропіл або 1-метоксициклопроп-1-іл, 3 R означає групу формули O * 50 N S O або * N S O причому * означає місце приєднання до карбонільної групи, та їх солі, сольвати і сольвати їх солей. Відповідними винаходу сполуками є сполуки формули (I) та їх солі, сольвати і сольвати 2 UA 107576 C2 5 10 15 20 25 30 35 40 солей, охоплені формулою (I) сполуки наведених нижче формул та їх солі, сольвати і сольвати солей, а також охоплені формулою (I) сполуки, визначені нижче як приклади виконання, та їх солі, сольвати і сольвати солей, якщо у випадку охоплених формулою (I) наведених нижче сполук вже не мають на увазі солі, сольвати і сольвати солей. Сполуки згідно з винаходом залежно від їх структури можуть існувати у стереоізомерних формах (енантіомери, діастереомери). Тому винахід охоплює також енантіомери або діастереомери та їх відповідні суміші. Із таких сумішей енантіомерів та/або діастереомери стереоізомерні компоненти можуть бути виділені відомими способами. Якщо сполуки згідно з винаходом можуть існувати у таутомерних формах, то даний винахід охоплює всі таутомерні форми. Як солям в рамках даного винаходу перевагу надають фізіологічно прийнятним солям сполук згідно з винаходом. При цьому мають на увазі також солі, які самі непридатні для застосування у фармацевтичних цілях, однак можуть бути використані, наприклад, для виділення або очищення сполук згідно з винаходом. Фізіологічно прийнятними солями сполук згідно з винаходом є кислотно-адитивні солі мінеральних, карбонових та сульфонових кислот, наприклад, солі хлорводневої, бромводневої, сірчаної, фосфорної, метансульфонової, етансульфонової, толуолсульфонової, бензолсульфонової, нафталіндисульфонової, оцтової, трифтороцтової, пропіонової, молочної, винної, яблучної, лимонної, фумарової, малеїнової та бензойної кислоти. Фізіологічно прийнятними солями сполук згідно з винаходом є також солі звичайних основ, такі як, наприклад, і переважно солі лужних металів (наприклад, солі натрію і калію), солі лужноземельних металів (наприклад, солі кальцію і магнію) та солі амонію, похідні від аміаку або органічних амінів, що містять від 1 до 16 атомів вуглецю, як, наприклад, і переважно етиламін, діетиламін, триетиламін, етилдіізопропіламін, моноетаноламін, діетаноламін, триетаноламін, дициклогексиламін, диметиламіноетанол, прокаїн, дибензиламін, Nметилморфолін, аргінин, лізин, етилендіамін, N-метилпіперидин та холін. Під сольватами в рамках даного винаходу розуміють такі форми сполук згідно з винаходом, які у твердому або рідкому стані шляхом координації з молекулами розчинника утворюють комплекс. Гідратами є спеціальна форма сольватів, в яких координація відбувається з водою. Крім того даний винахід включає також проліки сполук згідно з винаходом. Поняття "проліки" включає сполуки, які самі можуть бути біологічно активними або неактивними, однак під час їх перебування у тілі перетворюються на сполуки згідно з винаходом (наприклад, метаболічно або гідролітично). 3 У формулі групи, яка може означати R , кінцева точка лінії, біля якої стоїть *, означає не атом вуглецю або відповідно CH2-групу, а є складовою зв'язку із атомом, до якого приєднаний 3 R. Перевагу надають сполукам формули (I), в якій 1 R означає трифторметил, 1,1-дифторетил, 2,2-дифторетил, 2,2,2-трифторетил, дифторметокси, трифторметокси або етил, 2 R означає 2-метоксиет-1-ил, циклопропіл або 1-метоксициклопроп-1-іл, 3 R означає групу формули O * 45 N S O або * N S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил, 2,2,2-трифторетил, трифторметокси або етил, 2 R означає 2-метоксиет-1-ил, циклопропіл або 1-метоксициклопроп-1-іл, 3 R означає групу формули O * 50 55 N S O або * N S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил, 2,2,2-трифторетил або трифторметокси, 2 R означає циклопропіл або 1-метоксициклопроп-1-іл, 3 UA 107576 C2 3 R означає групу формули O N * S O 5 причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил, трифторметокси або етил, 2 R означає 2-гідроксиет-1-ил, 2-метоксиет-1-ил, 2-етоксиет-1-ил або циклопропіл, 3 R означає групу формули O * 10 15 N S O або N * S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил або етил, 2 R означає 2-гідроксиет-1-ил, 2-метоксиет-1-ил або циклопропіл, 3 R означає означає групу формули O * 20 25 N S O або N * S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил або етил, 2 R означає 2-метоксиет-1-ил, 3 R означає групу формули O * 30 N S O 40 N * S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій 1 R означає трифторметил або етил, 2 R означає 2-метоксиет-1-ил, 3 R означає групу формули * 35 або N S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають сполукам формули (I), в якій 1 R означає трифторметокси, 2 R означає 2-метоксиет-1-ил або циклопропіл, 3 R означає групу формули O * 45 N S O або причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають сполукам формули (I), в якій 1 R означає трифторметокси, 2 R означає циклопропіл, 4 * N S O UA 107576 C2 3 R означає групу формули O N * 5 S O або N * S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають сполукам формули (I), в якій 1 R означає трифторметокси, 2 R означає 2-метоксиет-1-ил або циклопропіл, 3 R означає групу формули O * 10 15 20 25 S O причому * означає місце приєднання до карбонільної групи, та їх солям, сольватам і сольватам їх солей. Перевагу надають також сполукам формули (I), в якій фенільний замісник і 1,2,4-оксадіазол5-ільний замісник, які приєднані до піперидинового кільця, знаходяться у цис-положення один відносно одного. Перевагу надають також сполукам формули (I), в якій атом вуглецю, до якого приєднаний фенільний замісник, має S-конфігурацію та атом вуглецю, до якого приєднаний 1,2,4оксадіазол-5-ільний замісник, також має S-конфігурацію. 1 Перевагу надають також сполукам формули (I), в якій R означає трифторметил. 1 Перевагу надають також сполукам формули (I), в якій R означає трифторметокси. 1 Перевагу надають також сполукам формули (I), в якій R означає етил. 2 Перевагу надають також сполукам формули (I), в якій R означає 2-метоксиет-1-ил. 2 Перевагу надають також сполукам формули (I), в якій R означає циклопропіл. 2 Перевагу надають також сполукам формули (I), в якій R означає 1-метокси-циклопроп-1-іл. Перевагу надають також сполукам формули (I), в якій 3 R означає групу формули * 30 N N S O причому * означає місце приєднання до карбонільної групи. Перевагу надають також сполукам формули (I), в якій 3 R означає групу формули O * N S O 35 40 причому * означає місце приєднання до карбонільної групи. Визначення залишків, окремо зазначені у відповідних звичайних або переважних комбінаціях, незалежно від відповідних наведених комбінацій, у будь-якій формі замінюють визначеннями залишками інших комбінацій. Найбільшу перевагу надають комбінаціям двох або більше наведених вище областей переважних значень. Ще одним об'єктом даного винаходу є спосіб одержання сполук формули (I) або їх солей, сольватів або сольватів їх солей, причому [A] сполуки формули 1 R O N 2 R N N H 45 в якій 5 (II) UA 107576 C2 1 3 R та R мають вказані вище значення, піддають взаємодії зі сполуками формули O R 5 10 X в якій 3 R має вказані вище значення, а 1 X означає галоген, переважно бром або хлор, або гідрокси або 4-нітрофенокси, або [B] сполуки формули (II) на першій стадії піддають взаємодії з 4-нітрофенілхлороформатом, а на другій стадії – зі сполуками формули 3 R 15 (III) 1 3 (IV) H в якій 3 R має вказані вище значення, або [C] сполуки формули 1 R O OH (V) N 3 R O 20 в якій 1 3 R та R мають вказані вище значення, піддають взаємодії зі сполуками формули HO N (VI) R H2N 25 2 в якій 2 R має вказані вище значення, або [D] сполуки формули 1 R O N 2 R N (Ia) N O N S 30 в якій 1 2 R та R мають вказані вище значення, піддають взаємодії з 0,8-1,1 еквівалентами мета-хлорпербензойної кислоти до одержання сполук формули 6 UA 107576 C2 1 R O N 2 R N (Ib) N O N S O 5 в якій 1 2 R та R мають вказані вище значення, або [E] сполуки формули (Ia) піддають взаємодії з 2,0-3,0 еквівалентами мета-хлорпербензойної кислоти до одержання сполук формули 1 R O N 2 R N (Ic) N O N S O O 10 15 20 25 30 35 40 в якій 1 2 R та R мають вказані вище значення. Сполуки формул (Ia), (Ib) і (Ic) представляють собою підмножину сполук формули (I). 1 Якщо X означає галоген, , взаємодію за способом [A] здійснюють загалом в інертних розчинниках, необов'язково в присутності основи, переважно при температурі від -30 °C до 50 °C при нормальному тиску. Інертними розчинниками є, наприклад, тетрагідрофуран, метиленхлорид, піридин, діоксан або диметилформамід, переважно метиленхлорид. Основами є, наприклад, триетиламін, діізопропілетиламін або N-метилморфолін, перевагу надають триетиламіну або діізопропілетиламіну. 1 Якщо X означає гідрокси, взаємодію за способом [А] здійснюють загалом в інертних розчинниках, в присутності агенту дегідратації, необов'язково в присутності основи, переважно при температурі від -30 °C до 50 °C при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як дихлорметан або трихлорметан, вуглеводень, такий як бензол, нітрометан, діоксан, диметилформамід або ацетонітрил. Крім того можливо також використовувати суміші розчинників. Особливу перевагу надають дихлорметану або диметилформаміду. Як агенти дегідратації придатними є, наприклад, карбодііміди, такі як, наприклад, N, N'діетил-, N, N'-дипропіл-, N, N'-діізопропіл-, N, N'-дициклогексилкарбодіімід, N-(3диметиламіноізопропіл)-N'-етилкарбодііміду гідрохлорид (EDC), N-циклогексилкарбодіімід-N‘пропілоксиметил-полістирол (PS-карбодіімід) або карбонільні сполуки, такі як карбонілдіімідазол, або сполуки 1,2-оксазолію, такі як 2-етил-5-феніл-1,2-оксазолію 3-сульфат або 2-трет-бутил-5-метилізоксазолію перхлорат, або ациламіносполуки, такі як 2-етокси-1етоксикарбоніл-1,2-дигідрохінолін, або ангідрид пропанфосфонової кислоти, або ізобутилхлороформат, або біс-(2-оксо-3-оксазолідиніл)фосфорилхлорид або бензотриазолілокси-три(диметиламіно)фосфонію гексафторфосфат, або O-(бензотриазол-1-іл)N, N,N',N'-тетраметилуронію гексафторфосфат (HBTU), 2-(2-оксо-1-(2H)-піридил)-1,1,3,3тетраметилуронію тетрафторборат (TPTU) або O-(7-азабензо-триазол-1-іл)-N, N,N',N'тетраметилуронію гексафторфосфат (HATU), або 1-гідроксибензотриазол (HOBt), або бензотриазол-1-ілокситрис(диметиламіно)фосфонію гексафторфосфат (BOP), або Nгідроксисукцинімід, або суміші згаданих вище речовин з основами. Основами є, наприклад, карбонати лужних металів, такі як, наприклад, карбонат натрію або калію, або гідрокарбонати лужних металів, або органічні основи, такі як триалкіламіни, наприклад, триетиламін, N-метилморфолін, N-метилпіперидин, 4-диметиламінопіридин або 7 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 діізопропілетиламін. Переважно конденсацію з HATU або з EDC здійснюють в присутності HOBt. 1 Якщо X означає 4-нітрофенокси, взаємодію за способом [A] здійснюють загалом в інертних розчинниках, необов'язково в присутності основи, необов'язково у мікрохвильовій печі, переважно при температурі від 50 °C до 200 °C при тиску від нормального до 5 бар. Інертними розчинниками є, наприклад, N-метилпіролідон, діоксан або диметилформамід, переважно N-метилпіролідон. Основами є, наприклад, триетиламін, діізопропілетиламін або N-метилморфолін, переважно триетиламін або діізопропілетиламін. Сполуки формули (III) є відомими або можуть бути синтезовані відомими способами із відповідних вихідних сполук. Взаємодію на першій стадії способу [В] здійснюють загалом в інертних розчинниках, в присутності основи, переважно при температурі від 0 °C до 50 °C при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан або 1,2-дихлоретан, переважно метиленхлорид. Основами є, наприклад, органічні основи, такі як триалкіламіни, наприклад, триетиламін, N-метилморфолін, N-метилпіперидин, 4-диметиламінопіридин або діізопропілетиламін, переважно триетиламін. Взаємодію на другій стадії способу [В] здійснюють загалом в інертних розчинниках, в присутності основи, необов'язково у мікрохвильовій печі, переважно при температурі від 50 °C до 200 °C при тиску від нормального до 5 бар. Інертними розчинниками є, наприклад, диметилсульфоксид, диметилформамід або Nметилпіролідон, переважно диметилформамід. Основами є, наприклад, карбонати лужних металів, такі як, наприклад, карбонат натрію або калію, переважно карбонат калію. Сполуки формули (ІV) є відомими або можуть бути синтезовані відомими способами із відповідних вихідних сполук. Взаємодію за способом [С] здійснюють загалом в інертних розчинниках, в присутності агенту дегідратації, необов'язково в присутності основи, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан або 1,2-дихлоретан, етери, такі як діоксан, тетрагідрофуран або 1,2диметоксиетан, або інші розчинники, такі як ацетон, диметилформамід, диметилацетамід, 2бутанон або ацетонітрил. Крім того можливо також використовувати суміші розчинників. Перевагу надають диметилформаміду або суміші діоксану і диметилформаміду. Як агенти дегідратації придатними є, наприклад, карбодііміди, такі як, наприклад, N, N'діетил-, N, N'-дипропіл-, N, N'-діізопропіл-, N, N'-дициклогексилкарбодіімід, N-(3диметиламіноізопропіл)-N'-етилкарбодііміду гідрохлорид (EDC), N-циклогексилкарбодіімід-N‘пропілоксиметил-полістирол (PS-карбодіімід) або карбонільні сполуки, такі як карбонілдіімідазол, або сполуки 1,2-оксазолію, такі як 2-етил-5-феніл-1,2-оксазолію 3-сульфат або 2-трет-бутил-5-метилізоксазолію перхлорат, або ациламіносполуки, такі як 2-етокси-1етоксикарбоніл-1,2-дигідрохінолін, або ангідрид пропанфосфонової кислоти, або ізобутилхлороформат, або біс-(2-оксо-3-оксазолідиніл)фосфорилхлорид або бензотриазолілокси-три(диметиламіно)фосфонію гексафторфосфат, або O-(бензотриазол-1-іл)N, N,N',N'-тетраметилуронію гексафторфосфат (HBTU), 2-(2-оксо-1-(2H)-піридил)-1,1,3,3тетраметилуронію тетрафторборат (TPTU) або O-(7-азабензо-триазол-1-іл)-N, N,N',N'тетраметилуронію гексафторфосфат (HATU), або 1-гідроксибензотриазол (HOBt), або бензотриазол-1-ілокситрис(диметиламіно)фосфонію гексафторфосфат (BOP), або бензотриазол-1-ілокси-трис(піролідинo)фосфонію гексафторфосфат (PYBOP), або Nгідроксисукцинімід, або суміші згаданих вище речовин з основами. Основами є, наприклад, карбонати лужних металів, такі як, наприклад, карбонат натрію або калію, або гідрокарбонати лужних металів, або органічні основи, такі як триалкіламіни, наприклад, триетиламін, N-метилморфолін, N-метилпіперидин, 4-диметиламінопіридин або діізопропілетиламін, переважно діізопропілетиламін. Переважно конденсацію з HATU здійснюють в присутності діізопропілетиламіну або альтернативно лише з карбонілдіімідазолом. Сполуки формули (VІ) є відомими або можуть бути синтезовані відомими способами із відповідних вихідних сполук. Взаємодію за способом [D] здійснюють загалом в інертних розчинниках, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником при 8 UA 107576 C2 5 10 нормальному тиску. Мета-хлорпербензойну кислоту використовують переважно у кількості від 0,9 до 1,0 еквівалентів. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан або 1,2-дихлоретан. Перевагу надають метиленхлориду. Взаємодію за способом [Е] здійснюють загалом в інертних розчинниках, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником при нормальному тиску. Мета-хлорпербензойну кислоту використовують переважно у кількості від 2,3 до 2,6 еквівалентів, особливо переважно у кількості 2,5 еквівалентів. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан або 1,2-дихлоретан. Перевагу надають метиленхлориду. Сполуки формули (II) є відомими або можуть бути одержані шляхом взаємодії сполук формули 15 1 R O OH (VII) N O O H3 C 20 25 CH3 CH3 в якій 1 R має вказані вище значення, на першій стадії зі сполуками формули (VI), а на другій стадії з кислотою. Взаємодію на першій стадії здійснюють, як описано у способі [С]. Взаємодію на другій стадії здійснюють загалом в інертних розчинниках, переважно при температурі від кімнатної до 60 °C при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан або 1,2-дихлоретан, або етери, такі як тетрагідрофуран або діоксан, переважно метиленхлорид. Основами є, наприклад, трифтороцтова кислота або хлороводень у діоксані, переважно трифтороцтова кислота. Сполуки формули (VII) є відомими або можуть бути одержані шляхом взаємодії сполук формули 30 1 R O 4 R O (VIII) N H 35 40 45 в якій 1 R має вказані вище значення та 4 R означає метил або етил, на першій стадії з ди-трет-бутилдикарбоксилатом та на другій стадії з основою. Взаємодію на першій стадії здійснюють загалом в інертних розчинниках, в присутності основи, переважно при температурі від кімнатної до 50 °C при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан або 1,2-дихлоретан, переважно метиленхлорид. Основами є, наприклад, триетиламін, діізопропілетиламін або N-метилморфолін, переважно триетиламін або діізопропілетиламін. Взаємодію на другій стадії здійснюють загалом в інертних розчинниках, в присутності основи, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником при нормальному тиску. 9 UA 107576 C2 5 10 Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан або 1,2-дихлоретан, спирти, такі як метанол або етанол, етери, такі як діетиловий етер, метил-трет-бутиловий етер, 1,2-диметоксиетан, діоксан або тетрагідрофуран, або інші розчинники, такі як диметилформамід, диметилацетамід, ацетонітрил або піридин, або суміші розчинників, або суміші розчинників з водою, переважно переважно метанол або метанол з еквівалентом води або суміш тетрагідрофурану і води. Основами є, наприклад, гідроксиди лужних металів, такі як гідроксид натрію, літію або калію, або карбонати лужних металів, такі як карбонат цезію, карбонат натрію або калію, або алкоголяти, такі як трет-бутилат калію або натрію, перевагу надають гідроксиду літію або третбутилату калію. Сполуки формули (VIII) є відомими або можуть бути одержані шляхом гідрування сполук формули 1 R O 4 R O (IX) N 15 20 25 30 в якій 1 4 R та R мають вказані вище значення. Гідрування здійснюють загалом з агентом відновлення в інертних розчинниках, необов'язково при додавання кислоти, такої як мінеральні кислоти та карбонові кислоти, переважно оцтова кислота, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником та при тиску від нормального до 100 бар, переважно при нормальному тиску або при тиску від 50 до 80 бар. Як агент відновлення переважно використовують водень з паладієм на активованому вугіллі, з родієм на активованому вугіллі, з рутенієм на активованому вугіллі або суміш цих каталізаторів, або водень з паладієм на оксиді алюмінію або з родієм на оксиді алюмінію, або водень з паладієм на активованому вугіллі і оксид платини (IV), переважно водень з паладієм на активованому вугіллі, або з родієм на активованому вугіллі, або водень з паладієм на активованому вугіллі і оксид платини (IV). Однак під тиском гідрування може відбуватися лише з воднем і оксидом платини (IV). Інертними розчинниками є, наприклад, спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол або трет-бутанол, або концентрована оцтова кислота або метанол із додаванням концентрованої соляної кислоти, переважно метанол або етанол або концентрована оцтова кислота або метанол із додаванням концентрованої соляної кислоти. Сполуки формули (IX) є відомими або можуть бути одержані шляхом взаємодії сполук формули 35 O 4 Br R O (X) N в якій 4 R має вказані вище значення, та сполук формули 40 OH B 1 R або 10 OH (XI) UA 107576 C2 CH3 H3C O B (XIII) CH3 O CH3 1 R 5 10 15 20 в якій 1 R має вказані вище значення. Взаємодію здійснюють загалом в інертних розчинниках, в присутності каталізатора, необов'язково в присутності додаткового реагента, переважно при температурі від кімнатної до температури кипіння розчинника зі зворотнім холодильником при нормальному тиску. Інертними розчинниками є, наприклад, етери, такі як діоксан, тетрагідрофуран або 1,2диметоксиетан, вуглеводні, такі як бензол, ксилол або толуол, або інші розчинники, такі як нітробензол, диметилформамід, диметилацетамід, диметилсульфоксид або N-метилпіролідон, необов'язково до розчинників додають незначну кількість води. Перевагу надають толуолу з водою або суміші 1,2-диметоксиетану, диметилформаміду і води. Каталізаторами є, наприклад, паладієві каталізатори, звичайні для умов реакції Сузукі, перевагу надають таким каталізаторам, як, наприклад, дихлорбіс(трифенілфосфін)паладій, тетракістрифенілфосфінпаладій(0), ацетат паладію (II) або хлорид біс(дифенілфосфанфероценіл)паладію (II). Додатковими реагентами є, наприклад, ацетат калію, карбонат цезію, калію або натрію, гідроксид барію, трет-бутилат калію, фторид цезію, фторид калію або фосфат калію або їх суміші, переважно фторид калію або карбонат натрію або суміш фториду калію і карбонату калію. Сполуки формул (X), (XI) і (XIІІ) є відомими або можуть бути синтезовані відомими способами із відповідних вихідних сполук. Сполуки формули (V) є відомими або можуть бути одержані шляхом взаємодії сполук формули 1 R O 4 R O (XII) N O 3 R 25 30 35 40 45 в якій 1 3 R та R мають вказані вище значення, а 4 R означає метил або етил, та основи. Взаємодію здійснюють загалом в інертних розчинниках, в присутності основи, переважно при температурі від кімнатної до температури кипіння розчинників зі зворотнім холодильником при нормальному тиску. Інертними розчинниками є, наприклад, галогенвуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан або 1,2-дихлоретан, спирти, такі як метанол або етанол, етери, такі як діетиловий етер, метил-трет-бутиловий етер, 1,2-диметоксиетан, діоксан або тетрагідрофуран, або інші розчинники, такі як диметилформамід, диметилацетамід, ацетонітрил або піридин, або суміші розчинників, або суміші розчинників з водою, переважно метанол або метанол з еквівалентом води або суміш тетрагідрофурану і води. Основами є, наприклад, гідроксиди лужних металів, такі як гідроксид натрію, літію або калію, або карбонати лужних металів, такі як карбонат цезію, карбонат натрію або калію, або алкоголяти, такі як трет-бутилат калію або натрію, переважно гідроксид літію або трет-бутилат калію. Сполуки формули (XII) є відомими або можуть бути одержані шляхом взаємодії сполук формули (VIII) та сполук формули (III). Взаємодію здійснюють, як описано у способі [A]. В альтернативному способі сполуки формули (ХII) можуть бути одержані шляхом взаємодії сполук формули (VIII) на першій стадії з 4-нітрофенілхлорформатом та на другій стадії зі 11 UA 107576 C2 сполуками формули (IV). Взаємодію здійснюють, як описано у способі [B]. Процес одержання сполук формули (I) можна продемонструвати на такій схемі синтезу. Схема: OH B OH O Br O R 4 R R 1 R O R 1 O N 1 O 4 Pd/C, H2 O N R 4 N H O R R 1 O N R N 2 HO H 2N R 1 R OH 2 N 5 10 15 20 25 30 35 40 45 O R O N R O Cl 1 O O основа Base N 3 3 R 4 N R 3 O R 3 Сполуки згідно з винаходом проявляють непередбачуваний, цінний спектр фармакологічної або фармакокінетичної дії. При цьому йдеться про селективні антагоністи рецептора PAR-1, які зокрема проявляють активність інгібіторів накопичення тромбоцитів, інгібіторів активації клітин ендотелію, інгібіторів проліферації клітин гладкої мускулатури та інгібіторів росту пухлин. Для деяких із зазначений захворювань, наприклад, серцево-судинних захворювань, з високим тромбоемболічним ризиком, велике значення має постійний захист за допомогою антагонізму PAR-1 при одночасному простому медикаментозному лікуванні. Антагоністи PAR-1 за даним винаходом проявляють довготривалу дію після одноразового перорального введення, тобто дію, яка триває щонайменше 16 годин Тому вони можуть бути застосовані як лікарські засоби для лікування та/або профілактики захворювань у людей і тварин. Іншим об'єктом даного винаходу є застосування відповідних винаходу сполук для лікування та/або профілактики захворювань, переважно тромбоемболічних захворювань та/або тромбоемболічних ускладнень. До „тромбоемболічних захворювань" в рамках даного винаходу належать зокрема такі захворювання, як інфаркт міокарда з підвищення сегменту ST (STEMI) і без підвищення сегменту ST (non-STEMI), стабільна стенокардія, нестабільна стенокардія, реоклюзії та рестенози після коронарних інтервенцій, таких як ангіопластика, імплантація стенту або аортокоронарне шунтування, облітерувальний ендартеріїт, емболії легеневих артерій, глибокі венозні тромбози та тромбози ниркової вени, транзиторні ішемічні атаки, а також тромботичний та тромбоемболічний інсульт. Тому речовини є придатними також для запобігання та лікування кардіогенних тромбоемболій, таких як, наприклад, ішемії мозку, апоплексія (напад) та системні тромбоемболії і ішемії, у пацієнтів з гострими, інтермітувальними або персистувальними формами серцевої аритмії, такими як, наприклад, мерехтіння передсердь, а також такими, при яких необхідна дефібриляція серця, та у пацієнтів із захворюваннями серцевих клапанів або у пацієнтів, що мають внутрішньосудинні тіла, такі як, наприклад, штучні серцеві клапани, катетери, внутрішньоаортальна балонна контрпульсація та кардіостимулятори. Тромбоемболічні ускладнення зустрічаються також у випадку мікроангіопатичних гемолітичних анемій, екстракорпоральних кровообігів, таких як, наприклад, гемодіаліз, гемофільтрація, за наявності пристроїв для механічної підтримки шлуночків серця (ventricular assist devices) і штучного серця, а також протезів серцевого клапана. Крім того відповідні винаходу сполуки використовують також для впливу на загоєння ран, для профілактики та/або лікування атеросклеротичних уражень судин та запальних захворювань, таких як ревматичні захворювання опорно-рухомого апарату, ішемічні хвороби серця, серцевої недостатності, артеріальної гіпертонії, запальних захворювань, таких як, наприклад, астма, COPD, запальних захворювань легенів, гломерулонефриту та запальних захворювань кишечника, крім того також для профілактики та/або лікування хвороби Альцгеймера, аутоімунних захворювань, хвороби Крона та виразкового коліту. Відповідні винаходу сполуки можуть бути використані також для інгібування росту пухлин і утворення метастаз, при мікроангіопатіях, обумовлених віком дегенераціях жовтої плями, діабетичній ретинопатії, діабетичній нефропатії та інших мікросудинних захворюваннях, а також для запобігання і лікування тромбоемболічних ускладнень, таких як, наприклад, венозні тромбоемболії, у онкологічних хворих, зокрема таких, які зазнали значних хірургічних втручань 12 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 або пройшли хіміо- або радіотерапію. Крім того відповідні винаходу сполуки є придатними для лікування раку. Ракові захворювання включають зокрема такі: карциноми (серед яких рак грудної залози, гепатоцелюлярний рак, колоректальний рак, рак товстої кишки і меланома), лімфоми (наприклад, Неходжкінська лімфома і грибовидний мікоз), лейкемія, саркома, мезотеліома, рак мозку (наприклад, гліома), гермінома (наприклад, рак яєчка і рак яєчника), хоріокарцинома, рак нирок, рак підшлункової залози, рак щитовидної залози, рак голови і шиї, рак ендометрію, рак шийки матки, рак сечового міхура, рак шлунку та множинна мієлома. Крім того PAR-1, експресований клітинами ендотелію, опосередковує сигнали, які викликають ріст судин ("ангіогенез"), процес, який є необхідною умовою для росту пухлини на понад 1 мм³. Індукція ангіогенезу є суттєвою також при інших захворюваннях, серед яких захворювання ревматичної групи (наприклад, ревматоїдний артрит), легеневі захворювання (наприклад, фіброз легенів, легенева гіпертонія, зокрема легенева артеріальна гіпертензія, захворювання, які характеризуються закупорюванням легеневих судин), артеріосклероз, розрив атеросклеторичної бляшки, діабетична ретинопатія та волога дегенерація жовтої плями. Відповідні винаходу сполуки є також придатними для лікування сепсису. Сепсис (або септицемія) – це розповсюджене захворювання із високою летальністю. Початкові симптоми сепсису є зазвичай неспецифічними (наприклад, підвищена температура, погіршення самопочуття), однак надалі може спостерігатися загальна активація системи згортання крові (дисемінована внутрішньосудинна коагулопатія або "коагулопатія споживання", надалі ДВК), що супроводжується мікротромбозом у різних органах і вторинними кровотечами. Крім того це може призвести до ушкодження ендотелію та пов'язаного з цим підвищення проникності судин і виходу рідини і протеїнів у позасудинний простір. На подальшому етапі розвитку захворювання може відбуватися дисфункція або відмова органу (наприклад, відмова нирок, печінки, органів дихання, порушення функцій центральної нервової системи і серцево-судинна недостатність) аж до відмови багатьох органів відразу. При цьому може страждати принципово кожен орган, найчастіше спостерігається дисфункція і відмова легенів, нирок, серцево-судинної системи, системи згортання крові, центральної нервової системи, ендокринних залоз і печінки. Сепсис може супроводжуватися гострим респіраторним дистрес-синдромом ("Acute Respiratory Distress Syndrome", який надалі позначають як ARDS). ARDS може також виникати незалежно від сепсису. "Септичний шок" означає зниження кров'яного тиску, яке підлягає обов'язковому лікуванню та спричиняє подальше ушкодження органів і пов'язане з цим погіршення прогнозу. Збудниками захворювання можуть бути бактерії (грам-негативні і грам-позитивні), грибки, віруси та/або еукаріоти. Вхідними воротами або первинною інфекцією може бути, наприклад, пневмонія, інфекція сечових шляхів, перитоніт. Інфекція може, однак не обов'язково повинна бути пов'язана із бактеріємією. Сепсис характеризується наявністю інфекції і синдрому системної запальної відповіді (який надалі позначають як "SIRS" - "systemic inflammatory response syndrome"). SIRS виникає в рамках інфекції, а також інших станів, таких як ушкодження, опіки, шок, операції, ішемія, панкреатит, реанімація або пухлини. Згідно з визначенням Комітету погоджувальної конференції ACCP/SCCM від 1992 року (Crit. Care Med. 1992, 20, 864-874) були описані симптоми, якими характеризується "SIRS" (зокрема зміна температури тіла, підвищена частота серцевих скорочень, утруднене дихання і змінена картина крові). На більш пізній Міжнародній конференції з питань визначення сепсису SCCM/ESICM/ACCP/ATS/SIS (2001) критерії були наведені загалом, однак деталі були викладені в Levy et al., Crit. Care Med. 2003, 31, 1250-1256. ДВК і SIRS можуть спостерігатися в рамках сепсису, а також внаслідок операцій, онкозахворювань, опіків або інших ушкоджень. У випадку ДВК на поверхні ушкоджених клітин ендотелію, поверхнях чужорідних тіл або ушкоджених екстраваскулярних тканин відбувається значна активація системи згортання. Як наслідок спостерігається згортання у малих судинах різних органів, що супроводжується гіпоксією і подальшою дисфункцією органів. Вторинно відбувається використання факторів згортання (наприклад, фактору Х, протромбіну, фібриногену) і тромбоцитів, у результаті чого зменшується здатність до згортання крові та можуть спостерігатися складні кровотечі. Крім того сполуки згідно з винаходом можуть бути застосовані для запобігання коагуляції ex vivo, наприклад, для консервації продуктів крові і плазми, для очищення/попередньої обробки катетерів та інших медичних допоміжних засобів і пристроїв, включаючи пристрої для екстракорпорального кровообігу, для нанесення покриття на штучні поверхні використовуваних in vivo або ex vivo медичних допоміжних засобів і пристроїв або у випадку біологічних проб, які містять тромбоцити. Іншим об'єктом даного винаходу є застосування відповідних винаходу сполук для нанесення 13 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 на медичні інструменти і імплантати, наприклад, катетери, протези, стенти або штучні клапани серця. Сполуки згідно з винаходом можуть при цьому міцно зв'язуватися з поверхнею або через певний час вивільнятися із покриття носія у безпосереднє оточення для локальної дії. Ще одним об'єктом даного винаходу є застосування відповідних винаходу сполук для лікування та/або профілактики захворювань, зокрема зазначених вище захворювань. Ще одним об'єктом даного винаходу є застосування відповідних винаходу сполук для одержання лікарського засобу для лікування та/або профілактики захворювань, зокрема зазначених вище захворювань. Ще одним об'єктом даного винаходу є спосіб лікування та/або профілактики захворювань, зокрема зазначених вище захворювань, при застосуванні терапевтично ефективної кількості сполуки згідно з винаходом. Ще одним об'єктом даного винаходу є лікарські засоби, що містять відповідну винаходу сполуку і одну або кілька інших активних речовин, зокрема для лікування та/або профілактики зазначених вище захворювань. Придатними для комбінування активними речовинами є, наприклад, переважно такі: блокатори кальцієвих каналів, наприклад, амлодипіну бесилат (наприклад, Norvasc®), фелодипін, дилтіазем, верапаміл, нифедипін, нікардипін, нісолдипін і бепридил; іомеризин; статини, наприклад, аторвастатин, флувастатин, ловастатин, пітавастатин, правастатин, розувастатин та симвастатин; інгібітори накопичення холестерину, наприклад, езетиміб і AZD4121; інгібітори протеїну, що переносить естери холестерину ("CETP"), наприклад, торцетрапіб; низькомолекулярні гепарини, наприклад, дальтепарин натрій, ардепарин, цертопарин, еноксапарин, парнапарин, тинзапарин, ревіпарин і надропарин; інші антикоагулянти, наприклад, варфарин, маркумар, фондапаринукс; антиаритмічні засоби, наприклад, дофетилід, ібутилід, метопролол, метопрололтартрат, пропранолол, атенолол, аймалін, дизопірамід, праймалін, прокаїнамід, хінідин, спартеїн, априндин, лідокаїн, мексилетин, токамід, енкамід, флекамід, лоркамід, морицизин, пропафенон, ацебутолол, піндолол, аміодарон, бретилій-тозилат, бунафтин, соталол, аденозин, атропін і дигоксин; агоністи альфа-адренорецепторів, наприклад, доксазозин-мезилат, теразосон і празосин; блокатори бета-адренорецепторів, наприклад, карведилол, пропранолол, тимолол, надолол, атенолол, метопролол, бісопролол, небіволол, бетаксолол, ацебутолол і бісопролол; антагоністи альдостерону, наприклад, еплеренон і спіронолактон; інгібітори ангіотензин-перетворюючого ферменту ("АПФ-інгібітори"), наприклад, моексиприл, хінаприл-гідрохлорид, раміприл, лізиноприл, беназеприл-гідрохлорид, еналапирл, каптоприл, спіраприл, периндоприл, фозиноприл і трандолаприл; блокатори рецепторів ангіотензину II ("ARBs"), наприклад, олмесартан-медоксоміл, кандесартан, валсартан, телмісартан, ірбесартан, лозартан і епрозартан; антагоністи ендотеліну, наприклад, тезосентан, босентан і ситаксентан-натрій; інгібітори нейтральної ендопептидази, наприклад, кандоксатрил і екадотрил; інгібітори фосфодіестерази, наприклад, мілринон, тіофілін, вінпоцетин, EHNA (еритро-9-(2гідрокси-3-ноніл)аденін), силденафіл, варденафіл і тадалафіл; фібринолітики, наприклад, ретеплаза, альтеплаза і тенектеплаза; антагоністи GP IIb/IIIa, наприклад, інтегрилін, абциксимаб і тирофібан; прямі інгібітори тромбіну, наприклад, AZD0837, аргатробан, бівалірудин і дабігатран; непрямі інгібітори тромбіну, наприклад, одипарцил; прямі і непрямі інгібітори фактора Xa, наприклад, фондапаринукс-натрій, апіксабан, разаксабан, ривароксабан (BAY 59-7939), KFA-1982, DX-9065a, AVE3247, отаміксабан (XRP0673), AVE6324, SAR377142, ідрапаринукс, SSR126517, DB-772d, DT-831j, YM-150, 813893, LY517717 і DU-1766; прямі і непрямі інгібітори фактора Xa/Iia, наприклад, еноксапарин-натрій, AVE5026, SSR128428, SSR128429 і BIBT-986 (таногітран); модулятори ліпопротеїн-асоційованої фосфоліпази A2 ("LpPLA2"); діуретики, наприклад, хлорталідон, етакринова кислота, фуроземід, амілорид, хлоротіазид, гідрохлоротіазид, метилхтотіазид і бензтіазид; нітрати, наприклад, ізосорбід-5-мононітрат; антагоністи тромбоксану, наприклад, сератродаст, пікотамід і раматробан; інгібітори накопичення тромбоцитів, наприклад, клопідогрель, тиклопідин, цилостазол, аспірин, абциксимаб, лімапрост, ептифібатид і CT-50547; 14 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 інгібітори циклооксигенази, наприклад, мелоксикам, рофекоксиб і целекоксиб; натрійуретичний пептид типу B, наприклад, несиритид і уларитид; модулятори NV1FGF, наприклад, XRP0038; антагоністи HT1B/5-HT2A, наприклад, SL65.0472; активатори гуанілатциклази, наприклад, атацигуат (HMR1766), HMR1069, ріоцигуат і цинацигуат; енхансери транскрипції e-NOS, наприклад, AVE9488 і AVE3085; анти-атерогенні речовини, наприклад, AGI-1067; інгібітори CPU, наприклад, AZD9684; інгібітори реніну, наприклад, аліскірин і VNP489; інгібітори накопичення тромбоцитів, індукованого аденозиндифосфатом, наприклад, клопідогрель, тиклопідин, прасугрель, AZD6140, тикагрелор і еліногрель; інгібітори NHE-1, наприклад, AVE4454 і AVE4890; антибіотичне лікування: різні антибіотики або комбінації протигрибкових медикаментів використовують як завчасне лікування (до одержання результатів мікробіологічного дослідження) або як специфічне лікування; лікування рідинами, наприклад, кристалоїдами або колоїдними рідинами; вазопресори, наприклад, норепінефрин, допамін або вазопресин; інотропне лікування, наприклад, добутамін; кортикостероїди, наприклад, гідрокортизон або флудрокортизон; рекомбінантний активований протеїн С людини, ксигрис; продукти крові, наприклад, концентрати еритроцитів, концентрати тромбоцитів, еритропієтин або свіжозаморожена плазма; штучна вентиляція легенів при індукованому сепсисом гострому ушкодженні легенів (ALI-Acute Lung Injury) або гострому респіраторному дистрес-синдромі (ARDS-Acute Respiratory Distress Syndrome), наприклад, пермісивна гіперкапнія, низький дихальний об'єм; заспокоєння: наприклад, діазепам, лоразепам, мідазолам або пропофол; опіоїди: наприклад, фентаніл, гідроморфон, морфін, меперидин або реміфентаніл; NSAID (не стероїдні протизапальні препарати): наприклад, кеторолак, ібупрофен або ацетамінофен; нервово-м'язова блокада: наприклад, панкуроній; контроль рівня глюкози, наприклад, інсулін, глюкоза; способи заміни нирок, наприклад, безперервна вено-венозна гемофільтрація або періодичний гемодіаліз; допамін у низькій концентрації для ниркової протекції; антикоагулянти, наприклад, для профілактики тромбозу або при заміні нирок, наприклад, нефракціонований гепарин, гепарин з низькомолекулярною вагою, гепариноїди, гірудин, бівалірудин або аргатробан; бікарбонатна терапія; профілактика стресової виразки, наприклад, інгібітори H2рецептора, антацидні засоби; медикаменти для лікування проліферативних захворювань: урацил, хлорметил, циклофосфамід, іфосфамід, мелфалан, хлорамбуцил, піпоброман, триетиленмеламін, триетилентіофосфорамін, бусульфан, кармустин, ломустин, стрептозоцин, дакарбазин, метотрексат, 5-фторурацил, флоксуридин, цитарабін, 6-меркаптопурин, 6-тіогуанін, флударабіну фосфат, пентостатин, вінбластин, вінкристин, віндесин, блеоміцин, дактиноміцин, даунорубіцин, доксорубіцин, епірубіцин, ідарубіцин, паклітаксел, мітраміцин, деоксикоформіцин, мітоміцин-C, L-аспарагіназа, інтерферон, етопозид, теніпозид, 17.альфа.-етинілестрадіол, діетилстильбестрол, тестостерон, преднизон, флуоксиместерон, дромостанолону пропіонат, тестолактон, мегестролацетат, тамоксифен, метилпреднізолон, метилтестостерон, преднізолон, триамцинолон, хлоротрианізен, гідроксипрогестерон, аміноглютетімід, естранрустин, медроксипрогестеронацетат, леупролід, флутамід, тореміфен, госерелін, цисплатин, карбоплатин, гідроксикарбамід, амасакрин, прокарбазин, мітотан, мітоксантрон, левамізол, навельбін, анастразол, летразол, капецитабін, релоксафін, дролоксафін, гексаметилмеламін, оксаліплатин (Елоксатин®), іреса (гефмітиб, Zdl839), КСЕЛОДА® (капецитабін), Тарцева® (ерлотиніб), азацитидин (5-азацитидин; 5-AzaC), темозоломід (Темодар®), гемцитабін (наприклад, ГЕМЗАР® (гемцитабін HCl)), вазостатин або комбінація двох або більше із зазначених вище медикаментів. Ще одним об'єктом даного винаходу є спосіб запобігання згортанню крові in vitro, зокрема у випадку консервованої крові або біологічних проб, що містять тромбоцити, який відрізняється тим, що додають антикоагулянтно ефективну кількість сполуки згідно з винаходом. Сполуки згідно з винаходом можуть проявляти систематичну та/або локальну дію. Для досягнення цієї мети їх наносять відповідним чином, наприклад, перорально, парентерально, легеневим способом, назально, під язик, на язик, за щоку, ректально, дермально, трансдермально, кон'юктивально, у вухо або у вигляді імплантату чи стенту. Для таких видів застосовання сполуки згідно з винаходом можуть бути використані у відповідних формах. Для перорального застосування згідно з рівнем техніки придатними є функціонуючі лікарські 15 UA 107576 C2 5 10 15 20 25 30 35 40 45 форми, що характеризуються швидким та/або модифікованим вивільненням сполук згідно з винаходом та до складу яких ці сполуки входять у кристалічній та/або аморфній та/або розчиненій формі, такі як, наприклад, таблетки (непокриті або покриті оболонками, наприклад, оболонками, стійкими до шлункового соку, або оболонками, які повільно розчиняються або не розчиняються взагалі, що контролюють вивільнення сполуки згідно з винаходом), таблетки або плівки/облатки, плівки/ліофілізати, капсули, які швидко розчиняються у ротовій порожнині (наприклад, тверді або м'які желатинові капсули), драже, грануляти, гранули, порошки, емульсії, суспензії, аерозолі або розчини. Парентеральне застосування може відбуватися при виключенні стадії всмоктування (наприклад, внутрішньовенно, внутрішньоартеріально, внутрішньосерцево, інтраспінально або інтралюмбально) або за умови включення стадії всмоктування (наприклад, внутрішньом'язово, підшкірно, у шкіру, перкутанно або внутрішньобрюшинно). Придатними для парентерального застосування є такі форми, як ін'єкційні та інфузійні композиції у вигляді розчинів, суспензій, емульсій, ліофілізатів або стерильних порошків. Перевагу надають пероральному застосуванню. Для інших видів застосування придатними є, наприклад, лікарські засоби для інгаляції (а саме порошкові інгалятори, розпилювачі), краплі, розчини або спреї в ніс; таблетки на язик, під язик або за щоку, плівки/облатки або капсули, супозиторії, композиції для вух або очей, вагінальні капсули, водні суспензії (лосьйони, мікстури "бовтушки"), ліпофільні суспензії, мазі, креми, трансдермальні терапевтичні системи (такі як, наприклад, пластирі), молочко, пасти, піни, присипки, імплантати або стенти. Сполуки згідно з винаходом можуть бути переведені у згадані форми застосування. Це можна здійснювати відомими способами шляхом змішування з інертними, нетоксичними, фармацевтично придатними допоміжними речовинами. До таких допоміжних речовин належать зокрема носії (наприклад, мікрокристалічна целюлоза, лактоза, маніт), розчинники (наприклад, рідкі поліетиленгліколі), емульгатори та диспергатори або змочувальні агенти (наприклад, додецилсульфат натрію, олеат поліоксисорбіту), зв'язувальні агенти (наприклад, полівінілпіролідон), синтетичні та природні полімери (наприклад, альбумін), стабілізатори (наприклад, антиоксиданти, такі як аскорбінова кислота), барвники (наприклад, неорганічні пігменти, такі як оксиди заліза) та речовини, що коригують смак та/або запах. Ще одним об'єктом даного винаходу є лікарські засоби, що містять щонайменше одну сполуку згідно з винаходом, переважно у комбінації з однією або кількома інертними, нетоксичними, фармацевтично прийнятними допоміжними речовинами, а також їх застосування для зазначених вище цілей. Загалом виявили, що при парентеральному застосуванні для досягнення необхідних результатів кількість активної речовини повинна переважно становити від приблизно 5 до 250 мг кожні 24 годоини. При пероральному застосуванні кількість становить приблизно від 5 до 100 мг кожні 24 години. Крім того при необхідності можна відступати від вказаних кількостей залежно від ваги тіла, форми застосування, індивідуальної реакції на активну речовину, виду композиції та моменту або інтервалу її застосування. Показники в % у дослідженнях та прикладах, якщо не зазначено нічого іншого, означають мас. %; частини – масові частини. Співвідношення розчинників, коефіцієнти розчинення та показники концентрації розчинів рідина/рідина стосуються відповідно об'єму. Зазначення "мас./об." означає "маса/об'єм". Так, наприклад, "10 % мас./об." означає, що 100 мл розчину або суспензії містять 10 г речовини. A) Приклади Скорочення: прибл. CDI д ТШХ ПХІ дд DMAP ДМФА ДМСО DPPA приблизно карбонілдіімідазол день(дні), дублет (в ЯМР) тонкошарова хроматографія пряма хімічна іонізація (у МС) дублет дублетів (в ЯМР) 4-диметиламінопіридин N, N-диметилформамід диметилсульфоксид дифенілфосфоразидат 50 16 UA 107576 C2 прибл. DSC від теор. екв. ESI год. HATU ВЕРХ РХ-МС ЛДА м хв. МС ЯМР PYBOP кв ОФ КТ Чу с т ТГФ 5 10 15 20 25 30 приблизно дисукцинімідилкарбонат від теоретичного (виходу) еквівалент(и) іонізація при електростатичному розпилюванні (у МС) година(и) O-(7-азабензотриазол-1-іл)-N, N,N',N'тетраметилуронію гексафторфосфат високоефективна рідинна хроматографія рідинна хроматографія-мас-спектрометрія літію діізопропіламід мультиплет (в ЯМР) хвилина(и) мас-спектрометрія ядерний магнітний резонанс бензотриазол-1-ілокси-трис(піролідинo)фосфонію гексафторфосфат квартет (в ЯМР) обернена фаза (у ВЕРХ) кімнатна температура час утримання (у ВЕРХ) синглет (в ЯМР) триплет (в ЯМР) тетрагідрофуран Методи ВЕРХ: Метод 1A: прилад: HP 1100 з діодно-матричним детектором; колонка: Kromasil 100 RP-18, 60 мм x 2,1 мм, 3,5 мкм; елюент A: 5 мл хлорної кислоти (70 %-ної) / л води, елюент B: ацетонітрил; градієнт: 0 хв. 2 % B 0,5 хв. 2 % B 4,5 хв. 90 % B 6,5 хв. 90 % B 6,7 хв. 2 % B 7,5 хв. 2 % B; потік: 0,75 мл/хв.; температура колонки: 30 °C; УФ-детектування: 210 нм. РХ-МС-методи: Метод 1B: тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: HP 1100; діодно-матричний УФ-детектор; колонка: Phenomenex Gemini 3 мкм, 30 мм x 3,0 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 90 %A 2,5 хв. 30 %A 3,0 хв. 5 %A 4,5 хв. 5 %A; потік: 0,0 хв. 1 мл/хв., 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; температура термостату: 50 °C; УФ-детектування: 210 нм. Метод 2B: прилад: Micromass QuattroPremier з Waters UPLC Acquity; колонка: Thermo Hypersil GOLD 1,9 мкм, 50 мм x 1 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 90 %A 0,1 хв. 90 %A 1,5 хв. 10 %A 2,2 хв. 10 %A; температура термостату: 50 °C; потік: 0,33 мл/хв.; УФ-детектування: 210 нм. Метод 3B: тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2,5 мкм MAX-RP 100A Mercury, 20 мм x 4 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 90 %A 0,1 хв. 90 %A 3,0 хв. 5 %A 4,0 хв. 5 %A 4,01 хв. 90 %A; потік: 2 мл/хв.; температура термостату: 50 °C; УФ-детектування: 210 нм. Метод 4B: прилад: Micromass Quattro Micro МС з ВЕРХ Agilent серії 1100; колонка: Thermo Hypersil GOLD 3 мкм 20 мм x 4 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 100 %A 3,0 хв. 10 %A 4,0 хв. 10 %A 4,01 хв. 100 %A 5,00 хв. 100 %A; температура термостату: 50 °C; потік: 2 мл/хв.; УФ-детектування: 210 нм. Метод 5B: прилад: Waters ACQUITY SQD UPLC System; колонка: Waters Acquity UPLC HSS T3 1,8 мкм 50 мм x 1 мм; елюент A: 1 л води + 0,25 мл 99 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,25 мл 99 %-ної мурашиної кислоти; градієнт: 0,0 хв. 90 % A → 1,2 хв. 5 % A → 2,0 хв 5 % A температура термостату: 50 °C; потік: 0,40 мл/хв.; УФ-детектування: 210-400 нм. Метод 6B: тип приладу МС: Waters (Micromass) Quattro Micro; тип приладу ВЕРХ: Agilent 17 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 55 60 серії 1100; колонка: Thermo Hypersil GOLD 3 мкм 20 мм x 4 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 100 %A → 3,0 хв. 10 %A → 4,0 хв. 10 %A → 4,01 хв. 100 %A (потік: 2,5 мл/хв.) → 5,00 хв. 100 %A; температура термостату: 50 °C; потік: 2 мл/хв.; УФ-детектування: 210 нм. Метод 7B: прилад: Micromass Quattro LCZ з ВЕРХ Agilent серії 1100; колонка: Phenomenex Onyx Monolithic C18, 100 мм x 3 мм, елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 90 %A 2 хв. 65 %A 4,5 хв. 5 %A 6 хв. 5 %A; потік: 2 мл/хв.; температура термостату: 40 °C; УФдетектування: 208-400 нм. Метод 7B: тип приладу МС: Waters ZQ; тип приладу ВЕРХ: Agilent серії 1100; діодноматричний УФ-детектор; колонка: Thermo Hypersil GOLD 3 мкм 20 мм x 4 мм; елюент A: 1 л води + 0,5 мл 50 %-ної мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 %-ної мурашиної кислоти; градієнт: 0,0 хв. 100 % A → 3,0 хв. 10 % A → 4,0 хв. 10 % A, температура термостату: 55 °C; потік: 2 мл/хв.; УФ-детектування: 210 нм. Препаративне розділення енантіомерів: Метод 1D: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 20 мм; елюент: ізогексан/ізопропанол 25:75; потік: 15 мл/хв.; температура: 45 °C; УФ-детектування: 220 нм. Метод 2D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм, елюент: метанол/ацетонітрил 25:75; потік: 15 мл/хв.; температура: 30 °C; УФ-детектування: 220 нм. Метод 3D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм, елюент: метанол/ацетонітрил 50:50; потік: 15 мл/хв., температура: 30 °C; УФ-детектування: 220 нм. Метод 4D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм; елюент: трет-бутилметиловий етер/метанол 50:50; потік: 15 мл/хв.; температура: 30 °C; УФ-детектування: 220 нм. Метод 5D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм, елюент: метанол/ацетонітрил 25:75; потік: 15 мл/хв., температура: 30 °C; УФ-детектування: 220 нм. Метод 6D: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 20 мм, елюент: ізо-гексан/етанол 25:75; потік: 15 мл/хв., температура: 45 °C; УФ-детектування: 220 нм. Метод 7D: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 20 мм, елюент: етанол 100 %; потік: 15 мл/хв., температура: 45 °C; УФ-детектування: 220 нм. Метод 8D: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 20 мм, елюент: ізогексан/ізопропанол 30:70; потік: 15 мл/хв., температура: 45 °C; УФ-детектування: 220 нм. Метод 9D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм, елюент: ацетонітрил/метанол 70:30; потік: 15 мл/хв., температура: 30 °C; УФ-детектування: 220 нм. Метод 10D: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 20 мм, елюент: ацетонітрил/метанол 70:30; потік: 20 мл/хв., температура: 35 °C; УФ-детектування: 210 нм. Метод 11D: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 20 мм, елюент: ізо-гексан/етанол 70:30; потік: 15 мл/хв., температура: 40 °C; УФ-детектування: 220 нм. Аналітичне розділення енантіомерів:Метод 1E: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 4 мм; елюент: ізопропанол/ізогексан: 75:25; потік: 1 мл/хв.; температура: 45 °C; УФ-детектування: 220 нм. Метод 2E: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 4,6 мм; елюент: ізогексан/ізопропанол: 25:75+0,2 % трифтороцтової кислоти + 1 % води; потік: 1 мл/хв.; температура: 45 °C; УФ-детектування: 235 нм. Метод 3E: фаза: Daicel Chiralpak ІA, 5 мкм, 250 мм x 4,6 мм; елюент: ацетонітрил/метанол: 75:25; потік: 1 мл/хв.; температура: 25 °C; УФ-детектування: 220 нм. Метод 4E: фаза: Daicel Chiralpak ІA, 5 мкм, 250 мм x 4,6 мм; елюент: ацетонітрил/метанол: 50:50; потік: 1 мл/хв.; температура: 25 °C; УФ-детектування: 220 нм. Метод 5E: фаза: Daicel Chiralpak ІA, 5 мкм, 250 мм x 4,6 мм; елюент: трет-бутилметиловий естер/метанол: 50:50; потік: 1 мл/хв.; температура: 25 °C; УФ-детектування: 220 нм. Метод 6E: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 4,6 мм; елюент: етанол 100 %; потік: 1 мл/хв.; температура: 45 °C; УФ-детектування: 220 нм. Метод 7E: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 4,6 мм, елюент: ізогексан/ізопропанол 30:70; потік: 1 мл/хв., температура: 45 °C; УФ-детектування: 220 нм. Метод 8E: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 4,6 мм, елюент: ацетонітрил/метанол 70:30; потік: 15 мл/хв., температура: 25 °C; УФ-детектування: 220 нм. Метод 9E: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 4,6 мм, елюент: ацетонітрил/метанол 70:30; потік: 15 мл/хв., температура: 30 °C; УФ-детектування: 220 нм. Метод 10E: фаза: Daicel Chiralpak IA, 5 мкм, 250 мм x 4,6 мм, елюент: ацетонітрил/метанол 70:30; потік: 1 мл/хв., температура: 30 °C; УФ-детектування: 220 нм. Метод 11E: фаза: Daicel Chiralpak AD-H, 5 мкм, 250 мм x 4,6 мм, елюент: ізогексан/етанол 18 UA 107576 C2 5 10 15 20 25 30 35 40 45 50 25:75+0,2 % трифтороцтової кислоти + 1 % води; потік: 1 мл/хв., температура: 45 °C; УФдетектування: 220 нм. Методи ГХ-МС: Метод 1F: прилад: Micromass GCT, GC6890; колонка: Restek RTX-35, 15 м x 200 мкм x 0,33 мкм; постійний потік гелію: 0,88 мл/хв.; температура термостату: 70 °C; вхід: 250 °C; градієнт: 70 °C, 30 °C/хв. → 310 °C (3 хв. утримування). TM Як мікрохвильовий реактор використовують "single mode" пристрій типу Emrys Optimizer. Вихідні сполуки Загальний метод 1A: утворення N'-гідроксиімідаміду До розчину відповідного нітрилу (1,0 екв.) в етанолі (1,2 мл/ммоль) при кімнатній температурі додають хлорид гідроксиламонію (1,5 екв.) і триетиламін (1,2 екв.). Реакційну суміш протягом ночі перемішують при кімнатній температурі. Для обробки етанол видаляють у вакуумі, до реакційної суміші додають насичений водний розчин гідрокарбонату натрію та екстрагують етилацетатом. Органічну фазу сушать над сульфатом натрію та концентрують. Залишок без додаткового очищення вводять у подальшу взаємодію. Загальний метод 2A: утворення N'-гідроксиімідаміду До розчину відповідного нітрилу (1,0 екв.) у суміші етанолу (1,9 мл/ммоль) і води (0,5 мл/ммоль) при кімнатній температурі додають хлорид гідроксиламонію (1,08 екв.) і гідроксид натрію (1,12 екв.). Реакційну суміш протягом 16 годин перемішують при кімнатній температурі. Для обробки реакційну суміш концентрують у вакуумі, додають дихлорметан та фільтрують. Фільтрат концентрують у вакуумі, а залишок без додаткового очищення вводять у подальшу взаємодію. Загальний метод 3A: реакція Сузукі До суміші відповідного бромпіридину в толуолі (1,8 мл/ммоль) в атмосфері аргону при кімнатній температурі додають тетракіс-(трифенілфосфін)паладій (0,02 екв.), розчин відповідної арилборної кислоти (1,2 екв.) в етанолі (0,5 мл/ммоль) та розчин фториду калію (2,0 екв.) у воді (0,2 мл/ммоль). Реакційну суміш протягом кількох годин перемішують до завершення реакції при кипінні зі зворотнім холодильником. Після додавання етилацетату та розділення фаз органічну фазу один раз промивають водою і один раз насиченим водним розчином хлориду натрію, сушать (сульфат магнію), фільтрують та концентрують у вакуумі. Неочищений продукт очищують флеш-хроматографією (силікагель-60, елюент: суміші дихлорметан-метанол). Загальний метод 4A: гідрування піридину До розчину піридину в етанолі (9 мл/ммоль) в атмосфері аргону додають паладій на активованому вугіллі (зволожений прибл. 50 % води, 0,3 г/ммоль) та при 60 °C протягом ночі гідрують в атмосфері 50 бар водню. Після цього каталізатор відфільтровують через фільтрувальний шар та кілька разів промивають етанолом. Об'єднані фільтрати концентрують у вакуумі. Загальний метод 5A: омилення метилового естеру/епімеризація До розчину відповідного метилового естеру (1,0 екв.) в метанолі (35-40 мл/ммоль) при кімнатній температурі додають трет-бутилат калію (10 екв.). Суміш протягом ночі перемішують при 60 °C. В ході реакції додають воду (1,0 екв.) та перемішують до завершення реакції при 60 °C. Для обробки метанол видаляють у вакуумі, до залишку додають воду та підкислюють за допомогою водного розчину 1 N соляної кислоти (pH 1). Суміш екстрагують етилацетатом, органічну фазу сушать над сульфатом магнію, фільтрують та концентрують у вакуумі. Загальний метод 6A: утворення оксадіазолу До розчину відповідної піперидин-3-карбонової кислоти в диметилформаміді (10-20 мл/ммоль) в атмосфері аргону при кімнатній температурі додають HATU (1,2 екв.), N, Nдіізопропілетиламін (2,2 екв.) і відповідний N'-гідроксиімідамід (1,1 екв.). Реакційну суміш перемішують при кімнатній температурі до завершення утворення проміжної стадії, потім знову перемішують при 120 °C до утворення бажаного продукту із цієї проміжної стадії. Після цього реакційну суміш очищують препаративною ВЕРХ. Приклад 1A N'-гідрокси-3-метоксипропанімідамід N H3C 55 O OH NH2 За загальним методом 1A у взаємодію вводять 20,0 г (235,0 ммоль) 3-метоксипропіонітрилу. Вихід: 18,1 г (49 % від теор., чистота 74 %). + ВЕРХ (метод 1A): Чу = 0,35 хв.; МС (ESI-поз): m/z=119 [M+H] . Приклад 2A 19 UA 107576 C2 3-етокси-N'-гідроксипропанімідамід N H3C 5 O OH NH2 За загальним методом 2A у взаємодію вводять 5,0 г (50,4 ммоль) 3-етоксипропіонітрилу. Вихід: 0,6 г (8 % від теор., чистота 90 %). + ВЕРХ (метод 1A): Чу = 0,60 хв.; МС (ESI-поз): m/z=133 [M+H] . Приклад 3A N'-гідроксициклопропанкарбоксімідамід N OH NH 2 10 За загальним методом 2A у взаємодію вводять 7,2 г (107,3 ммоль) нітрилу циклопропан карбонової кислоти. Вихід: 4,8 г (44 % від теор.). + РХ-МС (метод 2B): Чу = 0,16 хв.; МС (ESI-поз): m/z=101 [M+H] . Приклад 4A Метиловий естер 5-(4-етилфеніл)піридин-3-карбонової кислоти H3C O O CH3 N 15 20 За загальним методом 3A 32 г (148 ммоль) метилового естеру 5-бромнікотинової кислоти піддають взаємодії з 27 г (178 ммоль, 1,2 екв.) 4-етилфенілборної кислоти. Вихід: 24 г (64 % від теор.). + РХ-МС (метод 3B): Чу = 2,03 хв.; МС (ESI-поз): m/z=242 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 9,13 (д, 1H), 9,05 (д, 1H), 8,45 (т, 1H), 7,72 (д, 2H), 7,38 (д, 2H), 3,93 (с, 3H), 2,68 (кв, 2H), 1,22 (т, 3H). Приклад 5A Метиловий естер 5-(4-етилфеніл)піперидин-3-карбонової кислоти [суміш рацемічних цис/транс-ізомерів] H 3C O O CH3 N H 25 30 За загальним методом 4A гідрують 24 г (94 ммоль) метилового етилфеніл)піридин-3-карбонової кислоти. Вихід: 20 г (77 % від теор.). + РХ-МС (метод 4B): Чу = 1,43 хв.; МС (ESI-поз): m/z=248 [M+H] . Приклад 6A Метил-5-(4-етилфеніл)-1-(тіоморфолін-4-ілкарбоніл)піперидин-3-карбоксилат рацемічних цис-/транс-ізомерів] естеру 5-(4 [суміш CH 3 O O CH 3 N O N S 35 5,00 г (12,1 ммоль) 3-метил-1-(4-нітрофеніл)-5-(4-етилфеніл)піперидин-1,3-дикарбоксилату (приклад 30A), 3,57 г (36,4 ммоль) тіоморфоліну і 5,03 г (36,4 ммоль) карбонату калію поміщають в 76 мл ДМФА та 5 порціями при 150 °C протягом 1,5 години нагрівають у Single Mode-мікрохвильовій печі (Emrys Optimizer). Для обробки реакційні розчини об'єднують, фільтрують та залишок очищують препаративною ВЕРХ. Вихід: 3,07 г (67 % від теор.) + РХ-МС (метод 5B): Чу = 1,16 і 1,18 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=377 [M+H] . Приклад 7A 20 UA 107576 C2 5-(4-етилфеніл)-1-(тіоморфолін-4-ілкарбоніл)піперидин-3-карбонова цис-ізомер] кислота [рацемічний CH 3 O OH N O N S 5 10 За загальним методом 5A 3,00 г (7,97 ммоль) сполуки з прикладу 6A піддають взаємодії з 8,94 г (79,7 ммоль) трет-бутилату калію. Реакцію здійснюють селективно до одержання цисізомеру. Вихід: 2,74 г (93 % від теор.). + РХ-МС (метод 5B): Чу = 1,04 хв.; МС (ESI-поз): m/z=363 [M+H] . Приклад 8A {3-(4-етилфеніл)-5-[3-(2-метоксиетил)-1,2,4-оксадіазол-5-іл]піперидин-1-іл}-(тіоморфолін-4іл)метанон [рацемічний цис-ізомер] O N H 3C N O CH 3 N O N S 15 За загальним методом 6A 300 мг (0,828 ммоль) сполуки з прикладу 7A піддають взаємодії з 134 мг (0,910 ммоль) N'-гідрокси-3-метоксипропанімідаміду. Вихід: 185 мг (49 % від теор.). + РХ-МС (метод 5B): Чу = 1,22 хв.; МС (ESI-поз): m/z=445 [M+H] . Приклад 9A [3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-(4-етилфеніл)піперидин-1-іл]-(тіоморфолін-4іл)метанон [рацемічний цис-ізомер] O N H 3C N N O N S 20 25 За загальним методом 6A 300 мг (0,828 ммоль) сполуки з прикладу 7A піддають взаємодії з 91 мг (0,91 ммоль) N'-гідроксициклопропанкарбоксімідаміду. Вихід: 141 мг (40 % від теор.). + РХ-МС (метод 5B): Чу = 1,32 хв.; МС (ESI-поз): m/z=427 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,22 (д, 2H), 7,15 (д, 2H), 3,92 (д, 1H), 3,52 (д, 1H), 3,44 (ш. с, 4H), 3,38-3,31 (м, 1H), 3,03-2,79 (м, 3H), 2,63-2,55 (м, 6H), 2,25 (д, 1H), 2,10 (тд, 1H), 1,91 (кв, 1H), 1,16 (т, 3H), 1,09-1,01 (м, 2H), 0,92-0,85 (м, 2H). Приклад 10A {3-(4-етилфеніл)-5-[3-(2-гідроксиетил)-1,2,4-оксадіазол-5-іл]піперидин-1-іл}-(тіоморфолін-4іл)метанон [рацемічний цис-ізомер] O N H 3C N N O N S 21 OH UA 107576 C2 5 За загальним методом 6A 300 мг (0,828 ммоль) сполуки з прикладу 7A піддають взаємодії з 112 мг (1,08 ммоль) N',3-дигідроксипропанімідаміду [Graham A. Showell et al., J. Med. Chem., 1991, 34, 1086-1094]. Вихід: 248 мг (66 % від теор.). + РХ-МС (метод 5B): Чу = 2,22 хв.; МС (ESI-поз): m/z=431 [M+H] . Приклад 11A {3-[3-(2-етоксиетил)-1,2,4-оксадіазол-5-іл]-5-(4-етилфеніл)піперидин-1-іл}-(тіоморфолін-4іл)метанон [рацемічний цис-ізомер] O N H 3C N O CH 3 N O N S 10 15 За загальним методом 6A 600 мг (1,655 ммоль) сполуки з прикладу 7A піддають взаємодії з 355 мг (прибл. 2,152 ммоль) 3-етокси-N'-гідроксипропанімідаміду. Вихід: 389 мг (49 % від теор.). + РХ-МС (метод 6B): Чу = 2,61 хв.; МС (ESI-поз): m/z=459 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,23 (д, 2H), 7,16 (д, 2H), 3,95 (д, 1H), 3,71 (т, 2H), 3,54 (д, 1H), 3,48-3,34 (м, 7H), 3,08-2,81 (м, 5H), 2,63-2,55 (м, 6H), 2,29 (д, 1H), 1,95 (кв, 1H), 1,16 (т, 3H), 1,07 (т, 3H). Приклад 12A Метиловий естер 5-[4-(трифторметил)феніл]піридин-3-карбонової кислоти F F F O O CH3 N 20 За загальним методом 3A 28 г (132 ммоль) метилового естеру 5-бромнікотинової кислоти піддають взаємодії з 30 г (158 ммоль, 1,2 екв.) 4-трифторметилфенілборної кислоти. Вихід: 32 г (85 % від теор.). + РХ-МС (метод 4B): Чу = 2,27 хв.; МС (ESI-поз): m/z=282 [M+H] . Приклад 13A Метиловий естер 5-[4-(трифторметил)феніл]піперидин-3-карбонової кислоти [суміш рацемічних цис-/транс-ізомерів] F F F O O 25 30 CH 3 N H За загальним методом 4A гідрують 32 г (112 ммоль) метилового естеру 5-[4(трифторметил)феніл]піридин-3-карбонової кислоти (приклад 12A). Вихід: 26 г (82 % від теор.). + РХ-МС (метод 1B): Чу = 1,35 і 1,41 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=288 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 9,22 (д, 1H), 9,14 (д, 1H), 8,57 (т, 1H), 8,06 (д, 2H), 7,89 (д, 2H), 3,94 (с, 3H). Приклад 14A 3-метил-1-(4-нітрофеніл)-5-[4-(трифторметил)феніл]піперидин-1,3-дикарбоксилат [суміш рацемічних цис-/транс-ізомерів] 22 UA 107576 C2 F F F O O CH 3 N O O NO2 5 10 20,0 г (69,6 ммоль) метил-5-[4-(трифторметил)феніл]піперидин-3-карбоксилату (приклад 13A) розчиняють в 1,0 л дихлорметану та при 0 °C додають 14,1 г (139 ммоль) триетиламіну. Після цього по краплях додають 14,0 г (69,6 ммоль) 4-нітрофенілхлоркарбонату. Реакційну суміш протягом 2 годин перемішують при 0 °C та після цього протягом 16 годин при кімнатній температурі. Для обробки промивають насиченим водним розчином гідрокарбонату натрію. Органічну фазу сушать над сульфатом магнію, фільтрують та концентрують у вакуумі. Одержують 31,3 г неочищеного продукту, який без додаткового очищення вводять у подальшу взаємодію. + РХ-МС (метод 3B): Чу = 2,44 хв. і 2,48 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=453 [M+H] . Приклад 15A Метил-1-(тіоморфолін-4-ілкарбоніл)-5-[4-(трифторметил)феніл]піперидин-3-карбоксилат [суміш рацемічних цис-/транс-ізомерів] F F O F O CH 3 N O N S 15 20 10,0 г (22,1 ммоль) 3-метил-1-(4-нітрофеніл)-5-[4-(трифторметил)феніл]піперидин-1,3дикарбоксилату, 6,84 г (66,3 ммоль) тіоморфоліну і 9,17 г (66,3 ммоль) карбонату калію поміщають в 150 мл ДМФА та 10 порціями при 150 °C протягом 1 години нагрівають у Single Mode-мікрохвильовій печі (Emrys Optimizer). Для обробки реакційні розчини об'єднують, фільтрують, а залишок очищують препаративною ВЕРХ. Вихід: 5,16 г (55 % від теор.). + РХ-МС (метод 5B): Чу = 1,13 і 1,16 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=417 [M+H] . Приклад 16A 1-(тіоморфолін-4-ілкарбоніл)-5-[4-(трифторметил)феніл]піперидин-3-карбонова кислота [рацемічний цис-ізомер] F F F O OH N O N S 25 30 За загальним методом 5A 5,16 г (12,4 ммоль) сполуки з прикладу 15A піддають взаємодії з 13,9 г (124 ммоль) трет-бутилат калію. Реакцію здійснюють селективно до одержання цисізомеру. Вихід: 4,90 г (98 % від теор.). + РХ-МС (метод 5B): Чу = 1,04 хв.; МС (ESI-поз): m/z=403 [M+H] . Приклад 17A {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметил)феніл]піперидин-1-іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] 23 UA 107576 C2 F F O N F N N O N S 5 10 За загальним методом 6A 600 мг (1,491 ммоль) сполуки з прикладу 16A піддають взаємодії з 164 мг (1,640 ммоль) N'-гідроксициклопропанкарбоксімідаміду. Вихід: 352 мг (47 % від теор.). + РХ-МС (метод 5B): Чу = 1,28 хв.; МС (ESI-поз): m/z=467 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,70 (д, 2H), 7,56 (д, 2H), 3,92 (д, 1H), 3,57 (д, 1H), 3,45 (ш. с, 4H), 3,40-3,34 (м, 1H), 3,08-2,95 (м, 3H), 2,59 (ш. с, 4H), 2,30 (д, 1H), 2,16-2,07 (м, 1H), 2,04-1,91 (м, 1H), 1,10-1,01 (м, 2H), 0,92-0,85 (м, 2H). Приклад 18A {3-[3-(2-метоксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметил)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] F F O N F N O CH 3 N O N S 15 20 За загальним методом 6A 600 мг (1,491 ммоль) сполуки з прикладу 16A піддають взаємодії з 242 мг (1,640 ммоль) N'-гідрокси-3-метоксипропанімідаміду. Вихід: 350 мг (46 % від теор.). + РХ-МС (метод 5B): Чу = 1,18 хв.; МС (ESI-поз): m/z=485 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,70 (д, 2H), 7,57 (д, 2H), 3,95 (д, 1H), 3,68 (т, 2H), 3,58 (д, 1H), 3,51-3,36 (м, 5H), 3,23 (с, 3H), 3,13-2,96 (м, 3H), 2,94 (т, 2H), 2,60 (ш. с, 4H), 2,33 (ш. д, 1H), 2,10-1,95 (м, 1H). Приклад 19A {3-[3-(2-етоксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметил)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] F F O N F N CH3 N O O N S 25 30 За загальним методом 6A 600 мг (1,491 ммоль) сполуки з прикладу 16A піддають взаємодії з 320 мг (прибл. 1,983 ммоль) 3-етокси-N'-гідроксипропанімідаміду. Вихід: 343 мг (46 % від теор.). + РХ-МС (метод 6B): Чу = 2,57 хв.; МС (ESI-поз): m/z=499 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,70 (д, 2H), 7,57 (д, 2H), 3,96 (д, 1H), 3,71 (т, 2H), 3,58 (д, 1H), 3,49-3,37 (м, 7H), 3,11-2,97 (м, 3H), 2,93 (т, 2H), 2,60 (ш. с, 4H), 2,34 (ш. д, 1H), 2,02 (кв, 1H), 1,07 (т, 3H). Приклад 20A {3-[3-(2-гідроксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметил)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] 24 UA 107576 C2 F F O N F N OH N O N S 5 За загальним методом 6A 600 мг (1,491 ммоль) сполуки з прикладу 16A піддають взаємодії з 201 мг (1,938 ммоль) N',3-дигідроксипропанімідаміду. Вихід: 494 мг (68 % від теор.). + РХ-МС (метод 5B): Чу = 1,04 хв.; МС (ESI-поз): m/z=471 [M+H] . Приклад 21A Метиловий естер 5-[4-(трифторметокси)феніл]піридин-3-карбонової кислоти F F O O F O CH 3 N 10 15 20 25 30 За загальним методом 3A 23 г (105 ммоль) метилового естеру 5-бромнікотинової кислоти піддають взаємодії з 26 г (126 ммоль, 1,2 екв.) 4-трифторметоксифенілборної кислоти. Вихід: 14 г (41 % від теор.). + РХ-МС (метод 1B): Чу = 2,44 хв.; МС (ESI-поз): m/z=298 [M+H] . Альтернативний синтез: До розчину 26 г (121 ммоль) метилового естеру 5-бромнікотинової кислоти в толуолі (220 мл) в атмосфері аргону при кімнатній температурі додають 2,8 г (2,4 ммоль) тетракіс(трифенілфосфін)паладію та після цього додають розчин 30 г (146 ммоль) 4трифторметоксифенілборної кислоти в етанолі (58 мл). Після додавання 14 г (243 ммоль) фторид калію у воді (58 мл) протягом ночі перемішують при кип'ятінні зі зворотнім холодильником, додають ще 0,70 г (0,61 ммоль) тетракіс(трифенілфосфін)паладію та протягом 24 годин перемішують при кип'ятінні зі зворотнім холодильником. Після нового додавання 1,4 г (1,2 ммоль) тетракіс(трифенілфосфін)паладію протягом 20 годин перемішують при кип'ятінні зі зворотнім холодильником, до реакційного розчину додають етилацетат та промивають водою і насиченим водним розчином хлориду натрію. Органічну фазу сушать над сульфатом магнію, фільтрують та концентрують у вакуумі. Залишок очищують колонковою хроматографією (силікагель, циклогексан/дихлорметан 1:1 → дихлорметан). Вихід: 31 г (86 % від теор.). + РХ-МС (метод 4B): Чу = 2,32 хв.; МС (ESI-поз): m/z=298 [M+H] ; 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 9,17 (д, 1H), 9,10 (д, 1H), 8,51 (т, 1H), 7,95 (д, 2H), 7,52 (д, 2H), 3,94 (с, 3H). Приклад 22A Метиловий естер 5-[4-(трифторметокси)феніл]піперидин-3-карбонової кислоти [суміш рацемічних цис-/транс-ізомерів] F F O O F O CH 3 N H 35 40 До 14 г (45 ммоль) метилового естеру 5-[4-(трифторметокси)феніл]піридин-3-карбонової кислоти в етанолі (500 мл) додають 17 г зволоженого каталізатору паладію на активованому вугіллі (10 % паладію, 50 % води) та після цього протягом ночі гідрують в атмосфері водню при 50 бар і 60 °C. Реакційний розчин фільтрують, залишок на фільтрі промивають етанолом, а фільтрат концентрують у вакуумі. Залишок очищують колонковою хроматографією (силікагель, дихлорметан/метанол 600:1 → 10:1). Вихід: 8 г (59 % від теор.). + РХ-МС (метод 1B): Чу = 1,29 хв. і 1,33 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=304 [M+H] ; 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,43-7,35 (м, 4H), 7,31-7,25 (м, 4H), 3,60 (с, 3H), 3,40-3,21 (м, 5H), 3,16 (д, 1H), 3,01-2,89 (м, 3H), 2,88-2,78 (м, 2H), 2,78-2,65 (м, 4H), 2,17 (д, 1H), 2,09 (д, 1H), 1,82 (тд, 1H), 1,68 (кв, 1H), суміш цис-/транс-ізомерів прибл. 1:1,3, два протони перекриті. Приклад 23A 3-метил-1-(4-нітрофеніл)-5-[4-(трифторметокси)феніл]піперидин-1,3-дикарбоксилат [суміш 25 UA 107576 C2 рацемічних цис-/транс-ізомерів] F F O O F CH3 O NO2 N O 5 10 O До 8,0 г (26,4 ммоль) метилового естеру 5-(4-(трифторметокси)феніл)піперидин-3карбонової кислоти (приклад 22A) і 5,34 г (26,3 ммоль) триетиламіну в 666 мл дихлорметану повільно при 0 °C додають 5,32 г (26,4 ммоль) 4-нітрофенілхлороформату. Суміш протягом 2 годин перемішують при кімнатній температурі. Для обробки реакційну суміш промивають спочатку насиченим водним розчином гідрокарбонату натрію, а потім водою. Органічну фазу сушать над сульфатом натрію та концентрують у вакуумі. Залишок очищують флешхроматографією на силікагелі (розчинник: циклогексан/етилацетат від 1:2 до 1:1). Вихід: 7,32 г (54 % від теор.). + РХ-МС (метод 3B): Чу = 2,47 хв.; МС (ESI-поз): m/z=469 [M+H] . Приклад 24A Метил-1-(тіоморфолін-4-ілкарбоніл)-5-[4-(трифторметокси)феніл]піперидин-3-карбоксилат [суміш рацемічних цис-/транс-ізомерів] F F O O F O CH3 N O 15 20 25 N S 12,0 г (25,1 ммоль) 3-метил-1-(4-нітрофеніл)-5-[4-(трифторметокси)феніл]-піперидин-1,3дикарбоксилату, 7,77 г (75,3 ммоль) тіоморфоліну та 10,4 г (75,3 ммоль) карбонату калію поміщають в 180 мл ДМФА та 12 порціями при 150 °C протягом 2 годин нагрівають у Single Mode-мікрохвильовій печі (Emrys Optimizer). Для обробки реакційні розчини об'єднують, фільтрують, а залишок очищують препаративною ВЕРХ. Вихід: 7,88 г (73 % від теор.). + РХ-МС (метод 5B): Чу = 1,16 і 1,18 хв. (цис-/транс-ізомери); МС (ESI-поз): m/z=433 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,46-7,39 (м, 4H), 7,32 (д, 4H), 3,84 (дд, 2H), 3,64 (с, 3H), 3,63 (с, 3H), 3,55-3,34 (м, 10H), 3,09 (дд, 1H), 3,06-2,96 (м, 1H), 2,92-2,81 (м, 6H), 2,76-2,67 (м, 1H), 2,65-2,56 (м, 7H), 2,25-2,10 (м, 2H), 1,95-1,84 (м, 1H), 1,76 (кв, 1H), суміш цис-/транс-ізомерів прибл. 1:1). Приклад 25A 1-(тіоморфолін-4-ілкарбоніл)-5-[4-(трифторметокси)феніл]піперидин-3-карбонова кислота [суміш рацемічних цис-/транс-ізомерів] F F O O F OH N O N S 30 35 До розчину 7,85 г (18,2 ммоль) сполуки з прикладу 24A в метанолі (650 мл) при кімнатній температурі додають 20,4 г (182 ммоль) трет-бутилату калію. Суміш протягом ночі перемішують при 60 °C. Для обробки метанол видаляють у вакуумі, до залишку додають воду та підкислюють водним розчином 1 n соляної кислоти (pH 1). Суміщ екстрагують етилацетатом, органічну фазу сушать сульфатом магнію, фільтрують та концентрують у вакуумі. Реакцію здійснюють до одержання суміші цис-/транс-ізомерів 85:15. Вихід: 7,70 г (99 % від теор.). РХ-МС (метод 5B): Чу = 1,03 (транс-ізомер) і 1,04 хв. (цис-ізомер); МС (ESI-поз): m/z=419 + [M+H] ; 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 12,44 (ш. с, 1H), 7,47-7,39 (м, 2H), 7,31 (д, 2H), 3,79 (д, 1H), 3,56-3,48 (м, 1H), 3,46-3,37 (м, 4H), 2,91-2,73 (м, 3H), 2,63-2,55 (м, 5H), 2,14 (д, 1H), 1,81-1,66 (м, 26 UA 107576 C2 1H). Приклад 26A {3-[3-(2-метоксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметокси)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] O F F O N F N O CH 3 N O N S 5 10 За загальним методом 6A 600 мг (1,43 ммоль) сполуки з прикладу 25A піддають взаємодії з 232 мг (1,58 ммоль) N'-гідрокси-3-метоксипропанімідаміду. Вихід: 398 мг (53 % від теор.). + РХ-МС (метод 5B): Чу = 1,21 хв.; МС (ESI-поз): m/z=501 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,47 (д, 2H), 7,33 (д, 2H), 3,95 (д, 1H), 3,68 (т, 2H), 3,56 (д, 1H), 3,50-3,35 (м, 5H), 3,23 (с, 3H), 3,08-2,86 (м, 5H), 2,60 (ш. с, 4H), 2,32 (д, 1H), 1,97 (кв, 3H). Приклад 27A {3-(3-циклопропіл-1,2,4-оксадіазол-5-іл)-5-[4-(трифторметокси)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] O F O N F F N N O N S 15 20 25 30 За загальним методом 6A 300 мг (0,717 ммоль) сполуки з прикладу 25A піддають взаємодії з 79 мг (0,789 ммоль) N'-гідроксициклопропанкарбоксімідаміду. Вихід: 135 мг (39 % від теор.). + РХ-МС (метод 2B): Чу = 1,44 хв.; МС (ESI-поз): m/z=483 [M+H] . Альтернативний синтез: До 600 мг (1,43 ммоль) сполуки з прикладу 25A в диметилформаміді (29,0 мл) при кімнатній температурі додають 654 мг (1,72 ммоль) HATU і 0,55 мл (498 мг, 3,16 ммоль) N, Nдіізопропілетиламіну та перемішують протягом 30 хвилин. Після цього додають 158 мг (1,58 ммоль) N'-гідроксициклопропанкарбоксімідаміду та протягом ночі перемішують при кімнатній температурі. Реакційний розчин нагрівають до 120 °C та при цій температурі перемішують протягом 1 години. Потім реакційний розчин очищують безпосередньо препаративною ВЕРХ. Вихід: 315 мг (45 % від теор.). + РХ-МС (метод 5B): Чу = 1,30 хв.; МС (ESI-поз): m/z=483 [M+H] ; 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,46 (д, 2H), 7,33 (д, 2H), 3,91 (д, 1H), 3,55 (д, 1H), 3,45 (ш. с, 4H), 3,39-3,32 (м, 1H), 3,05-2,91 (м, 3H), 2,59 (ш. с, 4H), 2,28 (д, 1H), 2,17-2,08 (м, 1H), 1,93 (кв, 1H), 1,10-1,02 (м, 2H), 0,92-0,84 (м, 2H). Приклад 28A {3-[3-(2-етоксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметокси)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] F F F O O N N O N O CH3 N S 35 За загальним методом 6A 600 мг (1,434 ммоль) сполуки з прикладу 25A піддають взаємодії з 307 мг (прибл. 1,864 ммоль) 3-етокси-N'-гідроксипропанімідаміду. Вихід: 403 мг (55 % від теор.). + РХ-МС (метод 6B): Чу = 2,61 хв.; МС (ESI-поз): m/z=515 [M+H] . 27 UA 107576 C2 1 5 Н-ЯМР (400 МГц, ДМСО-d6): δ = 7,47 (д, 2H), 7,33 (д, 2H), 3,95 (д, 1H), 3,71 (т, 2H), 3,56 (д, 1H), 3,50-3,35 (т, 7H), 3,10-2,88 (м, 5H), 2,60 (ш. с, 4H), 2,32 (д, 1H), 2,02-1,92 (м, 1H), 1,07 (т, 3H). Приклад 29A {3-[3-(2-гідроксиетил)-1,2,4-оксадіазол-5-іл]-5-[4-(трифторметокси)феніл]піперидин-1іл}(тіоморфолін-4-іл)метанон [рацемічний цис-ізомер] F F O O N F N OH N O N S 10 За загальним методом 6A 1,00 г (2,390 ммоль) сполуки з прикладу 25A піддають взаємодії з 323 мг (3,107 ммоль) N',3-дигідроксипропанімідаміду. Вихід: 848 мг (69 % від теор.). + РХ-МС (метод 6B): Чу = 2,26 хв.; МС (ESI-поз): m/z=487 [M+H] . Приклад 30A 3-метил-1-(4-нітрофеніл)-5-(4-етилфеніл)піперидин-1,3-дикарбоксилат [суміш рацемічних цис-/транс-ізомерів] H 3C O O CH 3 N O O NO2 15 20 3,0 г (12,1 ммоль) сполуки з прикладу 5A поміщають в 30 мл дихлорметану, охолоджують 0 °C та додають 3,4 мл (2,4 г, 12,1 ммоль) триетиламіну, а також 2,4 г (12,1 ммоль) 4нітрофенілового естеру хлормурашиної кислоти. Реакційну суміш залишать повільно нагріватися до кімнатної температури та потім протягом 16 годин перемішують при кімнатній температурі. Кілька разів промивають водою, сушать над сульфатом натрію, фільтрують та концентрують у вакуумі. Залишок очищують колонковою хроматографією на силікагелі (розчинник дихлорметан → дихлорметан/метанол 100:2). Вихід: 4,7 г (83 % від теор., чистота 89 %). + ВЕРХ (метод 1A): Чу = 4,94 хв. і 5,00 хв. (цис-/транс-ізомер); МС (ESI-поз): m/z=413 [M+H] . Приклад 31A 4-нітрофенілтіоморфолін-4-карбоксилат NO2 O O N S 25 30 35 7,7 г (74,4 ммоль) тіоморфоліну поміщають в 100 мл дихлорметану та при охолодженні на льодяній бані додають 20,7 мл (15,1 г, 148,8 ммоль) триетиламіну. Потім порціями додають 10,0 г (49,6 ммоль) 4-нітрофенілового естеру хлормурашиної кислоти. Реакційну суміш протягом однієї години перемішують при кімнатній температурі додають воду і етилацетат. Органічну фазу відокремлюють, промивають 1 N соляною кислотою, а також насиченим водним розчином хлориду натрію, сушать над сульфатом натрію, фільтрують та концентрують у вакуумі. Вихід: 13,2 г (99 % від теор.). + РХ-МС (метод 5B): Чу = 0,98 хв.; МС (ESI-поз): m/z=269 [M+H] . 1 Н-ЯМР (400 МГц, ДМСО-d6): δ = 8,28 (д, 2H), 7,46 (д, 2H), 3,86 (ш. с, 2H), 3,72 (ш. с, 2H), 2,71 (ш. д, 4H). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted piperidines
Автори англійськоюHeimbach, Dirk, Rohrig, Susanne, Cancho Grande, Yolanda, Bender, Eckhard, Zimmermann, Katja, Buchmueller, Anja, Gerdes, Christoph, Gnoth, Mark, Jean, Gericke, Kersten Matthias, Jeske, Mario
Автори російськоюХаймбах Дирк, Канчо Гранде Йоланда, Бендер Эккхард, Циммерманн Катя, Бухмюллер Аня, Гердес Кристоф, Гнот Марк Жан, Герикке Керстен Маттиас, Еске Марио
МПК / Мітки
МПК: A61K 31/541, C07D 417/14
Мітки: піперидини, заміщені
Код посилання
<a href="https://ua.patents.su/78-107576-zamishheni-piperidini.html" target="_blank" rel="follow" title="База патентів України">Заміщені піперидини</a>
Попередній патент: Біообробка
Наступний патент: Пристрій для утримання і подачі насіння
Випадковий патент: Спосіб сепарування насінин та пристрій для його реалізації