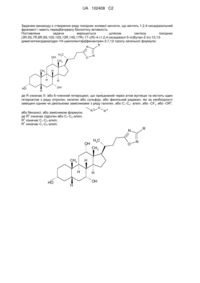
Похідні (3r,5s,7r,8r,9s,10s,12s,13r,14s,17r)-17-((r)-4(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1н-циклопента[a]фенантрен-3,7,12-тріолу
Номер патенту: 102408
Опубліковано: 10.07.2013
Автори: Коваленко Сергій Миколайович, Ніколаєнко Павло Валерійович, Заремба Олег Вікторович, Гусаров Віктор Ігорович
Формула / Реферат
Похідні (3R,5S,7R,8R,9S,10S,12S,13R,14S,l7R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Н-циклопента[а]-фенантрен-3,7,12-тріолу загальної формули:
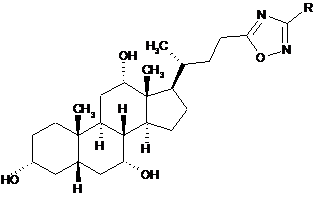 ,
,
де R означає 5- або 6-членний гетероцикл, що приєднаний через атом вуглецю та містить один гетероатом з ряду нітроген, оксиген або сульфур, або фенільний радикал, які за необхідності заміщені одним чи декількома замісниками з ряду галоген, або С1-С4-алкіл, або -CF3, або -OR, або бензоксі, або замісником формули ![]() ,
,
де R2 означає гідроген або С1-С4-алкіл,
R3 означає С1-С4-алкіл,
R4 означає С1-С4-алкіл.
Текст
Реферат: Винахід належить до органічної хімії, а саме до похідних (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13диметилгексадекагідро-1Н-циклопента[а]фенантрен-3,7,12-тріолу. UA 102408 C2 (12) UA 102408 C2 Задачею винаходу є створення ряду похідних холевої кислоти, що містять 1,2,4-оксадіазольний фрагмент і мають передбачувану біологічну активність. Поставлена задача вирішується шляхом синтезу похідних (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13диметилгексадекагідро-1Н-циклопента[а]фенантрен-3,7,12-тріолу загальної формули: R N OH H3C O CH3 CH3 H H HO N H OH H , де R означає 5- або 6-членний гетероцикл, що приєднаний через атом вуглецю та містить один гетероатом з ряду нітроген, оксиген або сульфур, або фенільний радикал, які за необхідності 2 заміщені одним чи декількома замісниками з ряду галоген, або С1-С4- алкіл, або -CF3, або -OR , R або бензоксі, або замісником формули, 2 де R означає гідроген або С1-С4-алкіл, 3 R означає С1-С4-алкіл, 4 R означає С1-С4-алкіл. 3 O R 4 R N OH H3C CH3 CH3 H H HO H H OH O N UA 102408 C2 5 Винахід належить до органічної хімії, а саме до похідних (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13диметилгексадекагідро-1Н-циклопента[а]фенантрен-3,7,12-тріолу. Відома хімічна сполука холева кислота (3,7,12-тригідрокси-5-холанова кислота, або (R)-4-((3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-3,7,12-тригідрокси-10,13-диметилгексадекагідро1Н-циклопента[а]фенантрен-17-іл)пентанова кислота загальної структурної формули (І) [1, 2], яку виділяють з жовчі великої рогатої худоби за відомою методикою [3]. OH H3C CH3 CH3 HO OH H H O H OH H (І) Відомий ряд хімічних сполук заміщених 1,2,4-оксадіазолів загальної формули (II) [4]: R N R 10 15 20 25 2 O N , (II) де R означає гідроген або алкіл, або арил, або гетероцикліл; 2 R означає гідроген або алкіл, або арил, або гетероцикліл. Серед похідних 1,2,4-оксадіазолів відомі сполуки, які виявляють протизапальну, антибактеріальну, анальгетичну, протитуберкульозну та протималярійну активність, деякі з них є ефективними антидепресантами [5], агоністами мускаринових [6] та бензадіазепінових рецепторів [8], антагоністами серотонінових рецепторів [7]. 1,2,4-Оксадіазоли виступають як біоізостерів естерів та амідів [9]. Основні методи отримання похідних 1,2,4-оксадіазолів - піроліз О-ациламідоксимів, конденсація амідоксимів з гідрохлоридами іміноетерів, реакції 1,3-диполярного циклоприєднання N-оксидів нітрилів до нітрилів [1, 10]. Задачею винаходу полягає у створенні ряду похідних холевої кислоти, що містять 1,2,4оксадіазольний фрагмент і мають передбачувану біологічну активність. Поставлена задача вирішується шляхом синтезу похідних (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13диметилгексадекагідро-1Н-циклопента[а]фенантрен-3,7,12-тріолу загальної формули (III): R N OH H3C CH3 CH3 H H HO H N O H OH , (III) де R означає 5- або 6-членний гетероцикл, що приєднаний через атом вуглецю та містить один гетероатом з ряду нітроген, оксиген або сульфур, або фенільний радикал, які за необхідності заміщені одним чи декількома замісниками з ряду галоген, або С 1-С4-алкіл, або 30 CF3, або -OR, або бензоксі, або замісником формули 2 де R означає гідроген або С1-С4-алкіл, 3 R означає С1-С4-алкіл, 4 R означає С1-С4-алкіл. 1 R 3 O 4 R , UA 102408 C2 5 Заявлені сполуки одержують наступним чином. Змішаний ангідрид холевої та мурашиної кислоти синтезують in situ в диметилформаміді (DMF) в присутності еквімолярної кількості трибутиламіну. В отриманий розчин додають відповідні заміщені амідоксими, процес взаємодії ведуть при (50-60) °С протягом 5 год. Закриття циклу проводять при додаванні 1,8діазабіцикло[5.4.0]ундец-7-ену (DBU) (при 60 °C протягом 1 год.). O O O O OH H3C CH3 HO Cl O CH3 OH O CH3 NH2 R H O HO H H R OH HO H2N H H N in situ OH N O DMF, 50'C H3C H H3C CH3 O CH3 H OH H CH3 Bu3N,DMF 50'C H H OH OH CH3 H3C H OH H I R N O OH H3C CH3 CH3 OH O R DMF, DBU, 60'C CH3 H2N H HO H H H HO OH N O H H H H3C CH3 N OH H III 10 Фрагменти ряду похідних (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Н-циклопента[а]фенантрен-3,7,12-тріолу наведені у таблиці 1. Таблиця 1 Варіанти 1 2 3 4 Хімічна назва одержаної сполуки (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-17-((R)-4-(3-(фуран-3-іл)-1,2,4R = фуран-3оксадіазол-5-іл)бутан-2-іл)-10,13іл диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-димeтил-17-((R)-4-(3R = тіофен-2(тіофен-2-іл)-1,2,4-оксадіазол-5іл іл)бутан-2-іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-диметил-17-((R)-4-(3R = піридин(піридин-2-іл)-1,2,4-оксадіазол-52-іл іл)бутан-2-іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол R = феніл (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-диметил-17-((R)-4-(3-фeнiл1,2,4-оксадіазол-5-іл)бутан-2іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол 2 Структурна формула O O N H H O O H O H O O H N S N H O N H O H O O N N H N H O H O H O O N H H O H H O N UA 102408 C2 Таблиця 1 Варіанти 5 6 7 8 9 10 Хімічна назва одержаної сполуки R = 4бромфеніл (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-17-((R)-4-(3-(4-бромфеніл)-1,2,4оксадіазол-5-іл)бутан-2-іл)-10,13диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-димeтил-17-((R)-4-(3-(мR = м-толіл толіл)-1,2,4-оксадіазол-5-іл)бутан-2іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол R = 4(трифтормет окси)феніл R = 3-фтор4метоксифені л R = 3,4,5триметоксиф еніл (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-димeтил-17-((R)-4-(3-(4(трифторметокси)феніл)-1,2,4оксадіазол-5-іл)бутан-2іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-17-((R)-4-(3-(3-фтор-4метоксифеніл)-1,2,4-оксадіазол-5іл)бутан-2-іл)-10,13диметилгексадекагідро-1Нциклопента[а]фенантрек-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R)-10,13-диметил-17-((R)-4-(3-(3,4,5тpимeтoкciфeніл)-1,2,4-оксадіазол-5іл)бутан-2-іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17 R = 4R)-17-((R)-4-(3-(4-(бензилокси)феніл)(бензокси)фе 1,2,4-оксадіазол-5-іл)бутан-2-іл)ніл 10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R R = (2)-17-((R)-4-(3-(3-(2-метоксіетил)феніл)11 метоксіетил) 1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13феніл) диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол 5 10 15 Структурна формула O O N H H O Br H O H O O H H O H O O H O F O H O H O O N O N H H O H O O H O O N N H H O H O H O O H H N N H O N N H O F F O H H O F O H O O N N H O N N H O N H O O Винахід ілюструється прикладами. Приклад 1 Сполуку 1 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-(R)-4-(3(фуран-3-іл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,50 г (4 ммоль) N'-гідроксифуран-3-карбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,49 г білих кристалів (75 % від теор.). Приклад 2 Сполуку 2 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17(R)-4-(3-(тіофен-2-іл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти 3 UA 102408 C2 5 10 15 20 25 30 35 40 45 50 55 60 холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,57 г (4 ммоль) N'-гідрокситіофен-2-карбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,58 г білих кристалів (77 % від теор.). Приклад 3 Сполуку 3 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17((R)-4-(3-(піридин-2-іл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Hциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,55 г (4 ммоль) N'-гідроксипіридин-2-карбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,68 г білих кристалів (82 % від теор.). Приклад 4 Сполуку 4 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17((R)-4-(3-феніл-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Н-циклопента[а]фенантрен3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,54 г (4 ммоль) N'-гідроксибензенкарбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,62 г білих кристалів (80 % від теор.). Приклад 5 Сполуку 5 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(3-(4бромфеніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,86 г (4 ммоль) 4-бром-N'-гідроксибензенкарбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,67 г білих кристалів (71 % від теор.). Приклад 6 Сполуку 6 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17((R)-4-(3-(м-толіл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Н-циклопента[а]фенантрен3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,60 г (4 ммоль) N'-гідрокси-3-метилбензенкарбоксімідаміду та перемішують 6 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец-7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,67 г білих кристалів (80 % від теор.). Приклад 7 Сполуку 7 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17(R)-4-(3-(4-(трифторметокси)феніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Hциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,88 г (4 ммоль) N'-гідрокси-4-(трифторметокси)бензенкарбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,78 г білих кристалів (75 % від теор.). 4 UA 102408 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 8 Сполуку 8 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(3-(3фтор-4-метоксифеніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,74 г (4 ммоль) 3-фтор-N'-гідрокси-4-метоксибензенкарбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,82 г білих кристалів (82 % від теор.). Приклад 9 Сполуку 9 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-10,13-диметил-17((R)-4-(3-(3,4,5-триметоксифеніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)гексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,90 г (4 ммоль) N'-гідрокси-3,4,5-триметоксибензенкарбоксімідаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,61 г білих кристалів (67 % від теор.). Приклад 10 Сполуку 10 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-(R)-4-(3-(4(бензилокси)феніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,97 г (4 ммоль) 4-(бензилокси)-N'-гідроксибензенкарбоксімідсаміду та перемішують 5 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,59 г білих кристалів (65 % від теор.). Приклад 11 Сполуку 11 (табл. 1), хімічна назва (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-(R)-4-(3-(3-(2метоксіетил)феніл)-1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1Нциклопента[а]фенантрен-3,7,12-тріол одержують наступним чином. 1,63 г (4 ммоль) кислоти холевої розчиняють у 10 мл диметилформаміду, додають 1 мл (4,2 ммоль) трибутиламіну. Суміш охолоджують до 10 °C та повільно додають 0,4 мл (4,2 ммоль) етилхлорформіату. Через 15 хвилин додають 0,78 г (4 ммоль) N'-гідрокси-3-(2-метоксіетил)бензенкарбоксімідаміду та перемішують 6 годин при температурі 50 °C. До розчину додають 1,8-діазабіцикло[5.4.0]ундец7-ен та нагрівають 1 годину при 60 °C. Розчин розбавляють водою. Масу, що утворилася, двічі розтирають з водою та перекристалізовують із суміші метанол/вода. Отримують 1,76 г білих кристалів (78 % від теор.). Таким чином, заявлено ряд нових похідних 3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1H-циклопента[а]фенантрен3,7,12-тріолу, які одержують шляхом однотипного синтезу за простою схемою, представляють інтерес для пошуку нових біологічно активних речовин і можуть бути рекомендовані як потенційні лікарські субстанції фармацевтичних препаратів. Джерела інформації 1. Химическая энциклопедия: В 5 т. / Гл. ред. И.Л. Кнунянц. - М.: Сов. энцикл., 1990. - Т. 2. 2. Chiang J. L. Bile acids: regulation of synthesis // J. Lipid Res. - 2009. - Vol. 50, Is. 10. - p. 19551966. 3. Лазурьевский Г.В. Практические работы по химии природних соединений. Методы выделения, разделения и идентификации / Г.В. Лазурьевский, И.В. Терентьева, А.А. Шамшурин. - М.: Высшая школа, 1961. - 192 с. 4. Joule J. A. Heterocyclic Chemistry / J. A. Joule, K. Mills. - John Wiley and Sons, 2010. - p. 569573. 5. Химическая энциклопедия: В 5 т. / Гл. ред. И.Л. Кнунянц. - М.: Сов. энцикл., 1990. - Т. 3. С. 341-342. 5 UA 102408 C2 5 10 6. Suzuki Т., Uesaka Н, Hamajima Н., Ikami. Т. Synthesis of (l-azabicyclo[3.3.0] octanyl)methylsubstituted aromatic heterocycles and their muscarinic activity // Chem. Pharm. Bull. - 1999. - Vol. 47. - p. 876-879. 7. Swain C.J., Baker R., Kneen C. et al. Novel 5-HT3 antagonists. Indole oxadiazoles//J. Med. Chem. - 1991. - Vol. 34, Is. l. - p. 140-151. 8. Watjen F., Baker R., Engelsto M. et al. Novel benzodiazepine receptor partial agonists: oxadiazolylimidazobenzodiazepines // J. Med. Chem. - 1989. - Vol. 32, Is. 10. - p. 2282-2291. 9. Diana G.D., Volkots D.L., Nitz T.J. et al. Oxadiazoles as Ester Bioisosteric Replacements in Compounds Related to Disoxaril. Antirhinovirus Activity // J. Med. Chem. - 1994. - Vol. 37, Is. 15. - p. 2421-2436. 10. Kayukova L.A. Synthesis of 1,2,4-oxadiazoles (a review) // Pharmaceutical Chemistry Journal - 2005. - Vol. 39, Is. 10. - p. 539-547. ФОРМУЛА ВИНАХОДУ 15 Похідні (3R,5S,7R,8R,9S,10S,12S,13R,14S,17R)-17-((R)-4-(1,2,4-оксадіазол-5-іл)бутан-2-іл)10,13-диметилгексадекагідро-1Н-циклопента[а]-фенантрен-3,7,12-тріолу загальної формули: R N OH H3C CH3 H H HO 20 25 H N O CH3 H OH , де R означає 5- або 6-членний гетероцикл, що приєднаний через атом вуглецю та містить один гетероатом з ряду нітроген, оксиген або сульфур, або фенільний радикал, які за необхідності заміщені одним чи декількома замісниками з ряду галоген, або С 1-С4-алкіл, або -CF3, або -OR, або бензоксі, або замісником формули 2 де R означає гідроген або С1-С4-алкіл, 3 R означає С1-С4-алкіл, 4 R означає С1-С4-алкіл. R 3 O 4 R , Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of (3r,5s,7r,8r,9s,10s,12s,13r,14s,17r)-17-((r)-4-(1,2,4-oxadiazole -5-yl)butane-2-yl)-10,13-dimethylhexadecahydro-1h-cyclopenta[a]phenanthrene -3,7,12-triol
Автори англійськоюKovalenko Serhii Mykolaiovych, Zaremba Oleh Viktorovych, Nikolaenko Pavlo Valeriiovych, Husarov Viktor Ihorovych
Назва патенту російськоюПроизводные (3r,5s,7r,8r,9s,10s,12s,13r,14s,17r)-17-((r)-4(1,2,4-оксадиазол-5-ил)бутан-2-ил)-10,13-диметилгексадекагидро-1н-циклопента[a]фенантрен-3,7,12-триола
Автори російськоюКоваленко Сергей Николаевич, Заремба Олег Викторович, Николаенко Павел Валериевич, Гусаров Виктор Игоревич
МПК / Мітки
МПК: C07D 271/06, C07C 35/00
Мітки: похідні, 3r,5s,7r,8r,9s,10s,12s,13r,14s,17r)-17-((r)-4(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1н-циклопента[a]фенантрен-3,7,12-тріолу
Код посилання
<a href="https://ua.patents.su/8-102408-pokhidni-3r5s7r8r9s10s12s13r14s17r-17-r-4124-oksadiazol-5-ilbutan-2-il-1013-dimetilgeksadekagidro-1n-ciklopentaafenantren-3712-triolu.html" target="_blank" rel="follow" title="База патентів України">Похідні (3r,5s,7r,8r,9s,10s,12s,13r,14s,17r)-17-((r)-4(1,2,4-оксадіазол-5-іл)бутан-2-іл)-10,13-диметилгексадекагідро-1н-циклопента[a]фенантрен-3,7,12-тріолу</a>
Попередній патент: Удосконалена трубна заглушка з подвійним блокуванням та спускним отвором
Наступний патент: Спосіб виготовлення броньованої і куленепробивної конструкції і броньована і куленепробивна конструкція
Випадковий патент: Система покриття підлоги