Заміщені 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-они і спосіб їх одержання
Номер патенту: 102939
Опубліковано: 27.08.2013
Автори: Афанасіаді Людмила Михайлівна, Ткаченко Володимир Володимирович, Руденко Роман Володимирович, Десенко Сергій Михайлович, Чебанов Валентин Анатолійович, Муравйова Олена Олександрівна
Формула / Реферат
1. Заміщені 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-они загальної формули
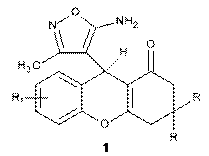 ,
,
де R=Н, СН3, 4-СlС6Н4,
R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3.
2. Спосіб одержання сполук загальної формули
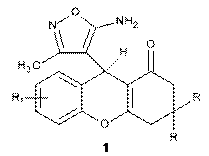 ,
,
де R=Н, СН3, 4-СlС6Н4,
R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3,
який відрізняється тим, що конденсують еквімолярні кількості 5-аміно-3-метилізоксазолу з R1-заміщеними 2-гідроксибензальдегідами і відповідними R-заміщеними циклогексан-1,3-діонами в органічному розчиннику - N,N-диметилформаміді при кипінні протягом 2-3 хвилин, після чого цільовий продукт висаджують ацетоном.
Текст
Реферат: Винахід належить до ксантен-1-онів формули заміщених 1 де R=Н, СН3, 4-СlС6Н4, R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3, , 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н UA 102939 C2 і способу їх одержання, що включає конденсацію еквімолярних кількостей 5-аміно-3метилізоксазолу з R1-заміщеними 2-гідроксибензальдегідами і R-заміщеними циклогексан-1,3діонами в органічному розчиннику - N,N-диметилформаміді при кипінні протягом 2-3 хвилин, після чого цільовий продукт висаджують ацетоном. Технічне рішення дозволяє зменшити тривалість технологічного процесу і підвищити якість сполук, забезпечує створення широкого набору заміщених тетрагідроксантенонів для медицини та препаративного органічного синтезу (флуоресцентні барвники та індикатори, активні лазерні середовища і т. ін.). 1 UA 102939 C2 Винахід стосується області хімії і являє собою нові заміщені 9-(5-аміно-3-метилізоксазол-4іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів загальної формули 1 1 5 10 15 20 25 R=Н, СН3, 4-СlС6Н4 R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3. Складні гетероциклічні сполуки, що заявляються, мають у своєму складі бензопірановий, ксантиновий і ізоксазольний цикли - фармакофорні фрагменти, що давно притягують увагу синтетиків. Наявність цих фармакофорних циклів обумовлює перспективність пошуку у низці сполук формули 1 речовин з різними видами біологічної активності. Так, ксантени і бензопірани входять до складу багатьох природних продуктів, що мають антибактеріальну [K.P. Chitre et al., Orient. J. Chem., 20, 377 (2004)], антиалергійну, протипухлинну [J. Nawrot-Modranka et al., Pharmazie, 59, 731 (2004)], антиоксидантну [Т.Т. Wei et al., Biochem. Pharm., 66, 83 (2003)], інсулін-чутливу активність [L. Tang et al., Bioorg. Med. Chem. Lett., 13, 3437 (2003)], або є активаторами калієвого каналу [R. Thompson et al., Bioorg. Med. Chem., 11, 1663 (2003)]. Крім того, ксантинові похідні мають антиплазмодіальну [F. Zelefack et al., J. Nat. Prod., 72, 954 (2009)], протизапальну активність [J.P. Poupelin et al., Eur. J. Med. Chem., 13, 67 (1978)], є антагоністами для лікарських стійких ліній лейкемії [Н.Т. Nguyen et al., J. Nat. Prod., 72, 527 (2009)]. Широко відомо застосування ксантенів як флуоресцентних барвників [А.Т. Peters et al., Dyes Pigments, 6, 349 (1985)], рН-чутливих флуоресцентних індикаторів (флуоресцеїн, еозин) [J. Lin et al., Bioorg. Med. Chem. Lett, 11, 2903 (2001)], активних лазерних середовищ [M. Ahmad et al., J. Phys. D: Appl. Phys., 35, 1473 (2002)]. Тому використання таких складних гетероциклічних сполук як біологічно активних речовин потребує постійного підвищення ступеня чистоти, простоти і доступності їх синтезу, удосконалення методів одержання. Відомий структурний аналог сполук, що заявляються, -2-(3,3-диметил-1-оксо-2,3,4,9тетрагідро-1Н-ксантен-9-іл)-5,5-диметилциклогексан-1,3-діон формули 2 і спосіб його одержання [А.N. Pyrko, Chem. Heterocycl. Сотр., 32, vol. 6, 635 (1996)]. 2 30 Автором описано лише один продукт конденсації з незаміщеним саліциловим альдегідом. Спосіб одержання відомої сполуки складається з однієї стадії і здійснюється за схемою: 2 Суміш 20 ммоль димедону, 10 ммоль саліцилового альдегіду і декількох крапель піперидину в 10 мл ізопропанолу кип'ятять 20 хвилин. Після 20-тигодинного стояння осад відфільтровують, промивають етилацетатом і одержують 2-(3,3-диметил-1-оксо-2,3,4,9-тетрагідро-1Н-ксантен-9 1 UA 102939 C2 5 10 15 іл)-5,5-диметилциклогексан-1,3-діон з виходом 93 %. Загальний час реакції - приблизно 21 година. Реакція каталізується основним або кислотним каталізатором. У разі відсутності таких сполук, як піперидин або 10 % НСl, реакція в сторону утворення заміщеного тетрагідроксантенону не проходить. Недоліком даного способу одержання сполуки формули 2 є тривалий технологічний процес, обумовлений низькою швидкістю реакції. У структурі тетрагідроксантенону можливість широкої хімічної модифікації відсутня, оскільки незаміщеними є тільки положення у фрагменті саліцилового альдегіду, але автором цю можливість модифікації не було показано, що також можна віднести до недоліків як структури молекули, так і способу її одержання. Відомий структурний аналог сполук, що заявляються, -3,8-диметил-2,3,4,9-тетрагідро-1Hксантен-1-он формули 3 і спосіб його одержання [Mahesh L. Patil, Hanumant В. Borate, J. Chem. Res., 454-456 (2005)]. 3 Недоліком структури сполуки формули 3 є відсутність хімічної модифікації у положенні 9 ксантенового фрагменту. Спосіб одержання сполуки формули 3 є двостадійним і реалізується за схемою: 50 % 40 % 20 25 30 35 40 На першій стадії перемішують суміш 5-метилциклогексан-1,3-діону (0,01 моль) і 1-метил-5метоксибензальдегіду (0.012 моль) у льодяній оцтовій кислоті (3 мл) і додають при 0 °C в атмосфері азоту 500 мг піперидину. Суміш перемішують 30 хвилин і виливають у льодяну воду, екстрагують хлороформом. Органічний шар сушать над безводним натрій сульфатом, відганяють у вакуумі розчинник і очищають на хроматографічній колонці з силікагелем (елюент 10 % етилацетат у петролейному ефірі). Одержують 2-(2-метокси-6-метилфенілметилен)-5метилциклогександіон-1,3 з виходом реакції 60 % (після перекристалізації із суміші петролейного ефіру і етилацетату). Т. пл. 95-97 °C. На другій стадії ведуть процес відновлення одержаного бензилідендіону. До розчину бензилідендіону (0,01 моль) в 20 мл безводного тетрахлорметану, який перемішують, додають триетилсилан (0,01 моль) і трифтороцтову кислоту (0,1 моль) при кімнатній температурі в атмосфері аргону. Суміш перемішують при 50-60 °C 3 години, виливають у льодяну воду, екстрагують етилацетатом. Органічний шар промивають водою і розсолом, сушать над безводним натрій сульфатом. Утворюється суміш 2-х сполук, яку розділяють на хроматографічній колонці на силікагелі (елюент - 10-15 % етилацетат у петролейному ефірі). З виходом 50 % у вигляді безбарвних кристалів одержують 3,8-диметил-2,3,4,9-тетрагідро-1Нксантен-1-он з т. пл. 141-142 °C. До недоліків способу одержання сполуки формули 3 слід віднести тривалий, двостадійний процес (приблизно 12-13 годин), застосування складних технологічних операцій (екстракція, хроматографія), використання газів - азоту і аргону - як середовище для проведення реакції, утворення суміші двох продуктів, яка потребує розділення на хроматографічній колонці, невисокий вихід реакції (50 %). Відомий структурний аналог сполук, що заявляються, -9-арил-1,2,3,4,5,6,7,8октагідроксантен-1,8-діони загальної формули 4 і спосіб їх одержання [R. J. Cremlyn, Gh. Shabbir, Phosphorus, Sulfur and Silicon, 179, 2635-2643 (2004)]. 2 UA 102939 C2 4 5 R=C6HS; 2-CH3-C6H4; 4-CH3-C6H4; 4-OCH3-C6H4; 4-Cl-C6H4; 4-Br-C6H4; 4-NO2-C6H4. Недоліком структури сполук формули 4 є обмежена варіація замісників тільки ароматичного характеру. Це значно скорочує кількість нових потенційних біологічно активних речовин. Спосіб одержання сполук формули 4 складається із 2-х стадій і реалізується за схемою: 2 10 15 20 25 30 35 40 На першій стадії 0,05 моль циклогександіону розчиняють у теплому 10 % водному етанолі (50 мл), потім додають розчин відповідного арилальдегіду (0,025 моль) в 10 мл етанолу і 3 краплі піперидину. Суміш нагрівають на водяній бані 10 хвилин. Після охолодження льодяною водою випадає 1,2-аддукт, який відфільтровують і сушать. На другій стадії одержаний продукт розчиняють в 30 мл етанолу, який містить 3 краплі концентрованої НСl, розчин нагрівають на водяній бані 30 хвилин. Після охолодження льодяною водою випадає 9-арил-1,2,3,4,5,6,7,8-октагідроксантен-1,8-діон, який сушать у вакуумексикаторі. Автори не наводять виходи реакцій. Загальний час реакції складає приблизно 2-3 години (без урахування часу для висушування проміжного і кінцевого продуктів). До недоліків відомого способу одержання сполук формули 4 слід віднести двостадійність технологічного процесу, використання основного і кислотного каталізаторів реакції. В основу винаходу поставлено задачу синтезу нових сполук ряду 9-(5-аміно-3метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів, а також розробки простого і доступного способу одержання таких сполук. Вирішення поставленої задачі забезпечується розробкою нових сполук - 9-(5-аміно-3метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів формули 1. 1 R=Н, СН3, 4-СlС6Н4, R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3. Вирішення поставленої задачі забезпечується також тим, що у способі одержання сполук формули 1, згідно винаходу, конденсують еквімолярні кількості 5-аміно-3-метилізоксазолу з R1заміщеними 2-гідроксибензальде-гідами і R-заміщеними циклогексан-1,3-діонами в органічному розчиннику - N, N-диметилформаміді при кипінні протягом 2-3 хвилин, після чого цільовий продукт висаджують ацетоном. Можливість модифікації хімічної структури сполук формули 1 варіюванням замісників R і R 1 як в альдегідній складовій, так і в циклогексан-1,3-діоні, які формують ксантеновий фрагмент, відкриває перспективи синтезу великого числа нових корисних речовин з новими особливостями і використанням. Застосування диметилформаміду як основного апротонного розчинника для реакції виключає використання як кислотного, так і основного каталізатора. Ось чому для повного проходження реакції в сторону утворення кінцевих продуктів - сполук формули 1 - достатньо лише 2-3 хвилини. Диметилформамід має температуру кипіння 153 °C, що значно вище, ніж 3 UA 102939 C2 5 10 15 20 25 30 35 40 45 50 температура кипіння ізопропанолу (82 °C) чи оцтової кислоти (118 °C). Підвищення температури, при якій проходить реакція, сприяє збільшенню швидкості реакції, що дозволяє значно скоротити тривалість технологічного процесу до 2-3 хвилин і зменшити енерговитрати. Вибір компонентів реакції і їх взаємодія у диметилформаміді дозволяє підвищити чистоту кінцевих продуктів. Використання будь-якого із компонентів реакції в більшому або меншому співвідношенні призводить до утворення суміші продуктів, що не прореагували. В однореакторному процесі, коли реакція проходить в одній хімічній колбі, одностадійним методом одержують чисті індивідуальні цільові сполуки, що не потребують перекристалізації. Крім того, спосіб дозволяє уникнути застосування каталізаторів. Однореакторність, доступність вихідних компонентів, одночасне варіювання одразу декількох фрагментів молекули, легкість автоматизації (традиційне нагрівання) - все це переваги способу одержання сполук формули 1, що заявляється. Вказаного часу проведення реакції (2-3 хвилини) достатньо для повного її проходження і утворення цільових продуктів, тому нагрівання більше 3 хвилин є недоцільним. В таблиці 1 представлено порівняльні характеристики способу, що заявляється, і способіваналогів. В таблиці 2 дано характеристики деяких сполук, що заявляються. Спосіб, що заявляється, здійснюється за схемою: Еквімолярні кількості 5-аміно-3-метилізоксазолу, відповідного R 1-заміщеного 2гідроксибензальдегіду і R-заміщеного циклогексан-1,3-діону кип'ятять у диметилформаміді протягом 2-3 хвилин. Охолоджену масу розбавляють ацетоном, відфільтровують осад, промивають ацетоном, сушать. Спосіб одержання сполук, що заявляються, ілюструється наступними прикладами. Приклад 1. Одержання 9-(5-аміно-3-метилізоксазол-4-іл)-7-нітро-2,3,4,9-тетрагідро-1Нксантен-1-ону. Суміш 0,2 г (2 ммоль) 5-аміно-3-метилізоксазолу, 0,23 г (2 ммоль) циклогександіону і 0,34 г (2 ммоль) 2-гідрокси-5-нітробензальдегіду кип'ятять у 0,1 мл диметилформаміду протягом 2 хвилин. Охолоджену до кімнатної температури масу розбавляють ацетоном. Осад, що випав, відфільтровують, промивають ацетоном, сушать. Вихід становить 0,39 г (57 %); т. пл. 214-216 °C. 1 Спектр ЯМР Н (ДМСО-d6; δ, м.ч.): 1,63 (с; 3Н), 1,87 (м; 2Н), 2,32 (м; 2Н), 2,64 (м; 2Н), 4,73 (с; 1Н), 6,52 (с; 2Н), 6,9-7.5 (м; 3Н). Приклад 2. Одержання 9-(5-аміно-3-метилізоксазол-4-іл)-7-бромо-3,3-диметил-2,3,4,9тетрагідро-1Н-ксантен-1-ону. Суміш 0,2 г (2 ммоль) 5-аміно-3-метилізоксазолу, 0.29 г (2 ммоль) циклогександіону і 0,41 г (2 ммоль) 2-гідрокси-5-бромобензальдегіду кип'ятять у 0,15 мл диметилформаміду протягом 3 хвилин. Охолоджену до кімнатної температури масу розбавляють ацетоном. Осад, що випав, відфільтровують, промивають ацетоном, сушать. Вихід становить 0,29 г (50 %); т. пл. 222-224 °C. 1 Спектр ЯМР Н (ДМСО-d6; δ, м.ч.): 1,00 (с; 3H), 1.02 (с; 3H), 1,62 (с; 3H), 2,24 (дд; 2Н), 2,58 (дд; 2Н), 4,74 (с; 1H), 6,48 (с; 2Н), 6,7-7,3 (м; 3H). Решту прикладів наведено в таблиці 2. Як видно із опису матеріалів винаходу і даних таблиць 1, 2, структура сполук, що заявляються, забезпечує одержання значного набору заміщених тетрагідроксантенонів з покращеними характеристиками - високим ступенем чистоти. Спосіб одержання сполук формули 1 дозволяє: - значно зменшити тривалість технологічного процесу; - підвищити якість сполук, що заявляються, їх виходи за рахунок проведення реакції у висококиплячому розчиннику - диметилформаміді; - широко варіювати замісники R і R1; - використовувати у синтезі доступні вихідні реагенти і розчинник, що випускаються вітчизняною промисловістю. 4 UA 102939 C2 Всі ці переваги нових сполук і способу їх одержання дають можливість їх потенційного використання як біологічно активних речовин, лікарських препаратів в медицині, флуоресцентних барвників, активних середовищ лазерів і т. ін. Спосіб, що заявляється, простий і доступний, легко відтворюється в лабораторних умовах. 5 Таблиця 1 Спосіб, що заявляється Спосіб одержання сполуки формули 2 Спосіб одержання сполуки формули 3 Спосіб одержання сполуки формули 4 Тривалість Вихід процесу реакції, % 1 стадія, 2-3 50-63 хвилини 1 стадія, ~ 21 93 година 2 стадії, ~ 12-13 ~50 годин 2 стадії, ~ 2-3 не години наведено Очищення цільового продукту Розчинник для реакції не потребується диметилформамід екстракція, хроматографія ізопропанол, каталізатор піперидин льодяна оцтова кислота, б/в ССl4 етанол, каталізатори піперидин, HCl не потребується не потребується Таблиця 2 Сполука Час реакції, хв Т. пл., °C Вихід цільового продукту, % 9-(5-аміно-3-метилізоксазол-4іл)-7-бромо-2,3,4,9-тетрагідро1Н-ксантен-1-он 3 213-215 58 9-(5-аміно-3-метилізоксазол-4іл)-5-метокси-2,3,4,9тетрагідро-1Н-ксантен-1-он 3 196-198 61 9-(5-аміно-3-метилізоксазол-4іл)-5-метокси-3,3-диметил2,3,4,9-тетрагідро-1H-ксантен1-он 3 210-212 56 9-(5-аміно-3-метилізоксазол-4іл)-7-нітро-3,3-диметил-2,3,4,9тетрагідро-1Н-ксантен-1-он 2 223-225 63 1 Спектр ЯМР Н 1,63 (с; 3H), 1,87 (м; 2Н), 2,32 (м; 2Н), 2,64 (м; 2Н), 4,73 (с; 1Н), 6,52 (с; 2Н), 6,9-7,5 (м; 3H) 1,62 (с; 3H), 1,85 (м; 2Н), 2,30 (м; 2Н), 2,63 (м; 2Н), 3,80 (с; 3H), 4,78 (с; 1Н), 6,38 (с; 2Н), 6,8-7,1 (м; 3H) 0,99 (с; 3H), 1,02 (с; 3H), 1,62 (с; 3H), 2,21 (дд; 2Н), 2,56 (дд; 2Н), 3,79 (с; 3H), 4,76 (с; 1Н), 6,36 (с; 2Н), 6,5-7,1 (м; 3H) 1,02 (с; 3H), 1,05 (с; 3H), 1,63 (с; 3H), 2,31(дд; 2Н), 2,65 (дд; 2Н), 4,90 (с; 1Н), 6,54 (с; 2Н), 7,2-7,8 (м; 3H) ФОРМУЛА ВИНАХОДУ 10 15 1. Заміщені формули 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-они 1 , де R=Н, СН3, 4-СlС6Н4, R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3. 2. Спосіб одержання сполук загальної формули 5 загальної UA 102939 C2 5 1 , де R=Н, СН3, 4-СlС6Н4, R1=Н, 7-Сl, 7-Вr, 7-NO2, 5-ОСН3, який відрізняється тим, що конденсують еквімолярні кількості 5-аміно-3-метилізоксазолу з R1заміщеними 2-гідроксибензальдегідами і відповідними R-заміщеними циклогексан-1,3-діонами в органічному розчиннику - N,N-диметилформаміді при кипінні протягом 2-3 хвилин, після чого цільовий продукт висаджують ацетоном. Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted 9-(5-amino-3-methylisoxazol-4-yl)-2,3,4,9-tetrahydro-1h- xanthen-1-ones and a process for the preparation thereof
Автори англійськоюRudenko Roman Volodymyrovych, Muraviova Olena Oleksandrivna, Chebanov Valentyn Anatoliiovych, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna, Tkachenko Volodymyr Volodymyrovych
Назва патенту російськоюЗамещенные 9-(5-амино-3-метилизоксазол-4-ил)-2,3,4,9-тетрагидро-1н-ксантен-1-оны и способ их получения
Автори російськоюРуденко Роман Владимирович, Муравьева Алена Александровна, Чебанов Валентин Анатолиевич, Десенко Сергей Михайлович, Афанасиади Людмила Михайловна, Ткаченко Владимир Владимирович
МПК / Мітки
МПК: C07D 311/82
Мітки: одержання, заміщені, спосіб, 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-они
Код посилання
<a href="https://ua.patents.su/8-102939-zamishheni-9-5-amino-3-metilizoksazol-4-il-2349-tetragidro-1n-ksanten-1-oni-i-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Заміщені 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-они і спосіб їх одержання</a>












