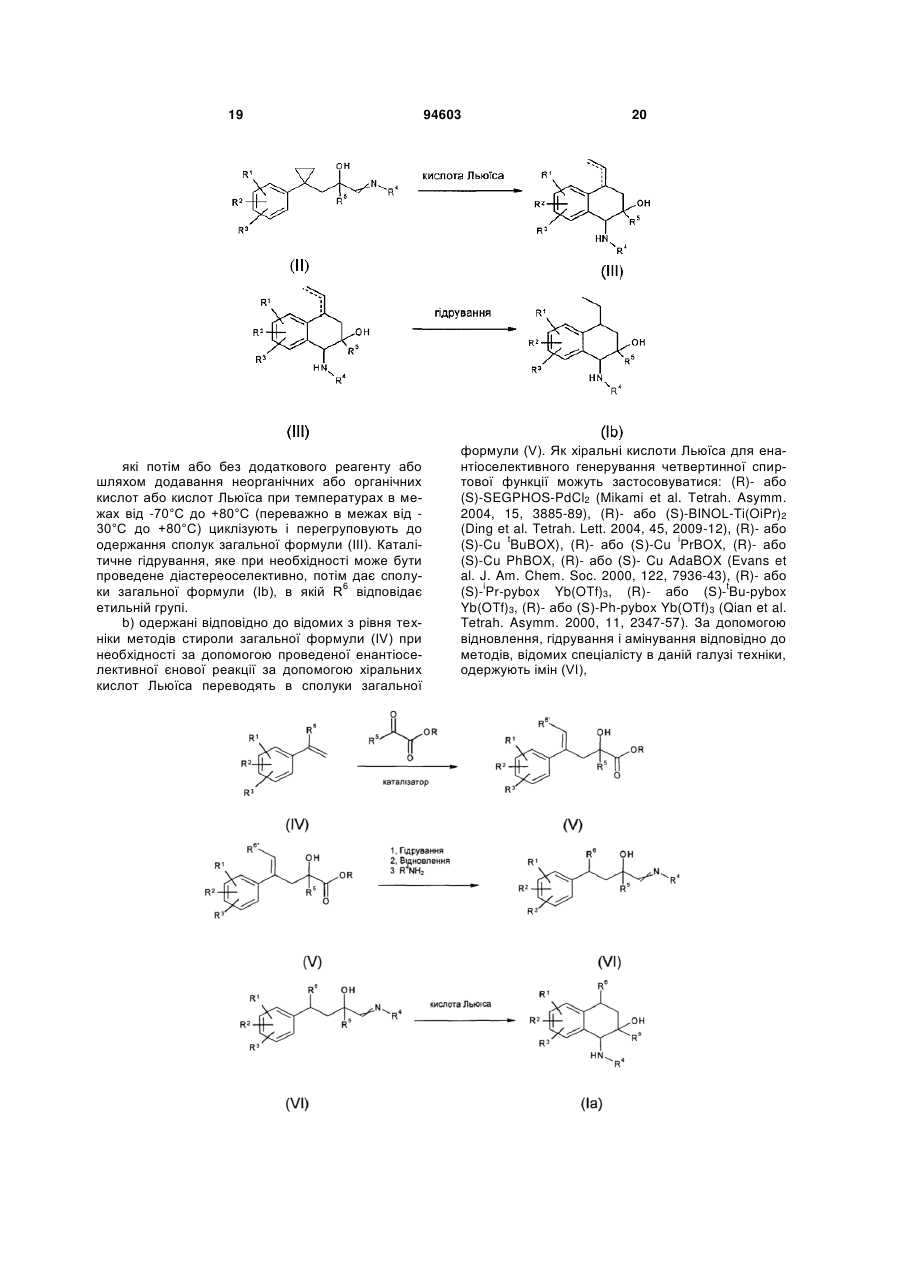
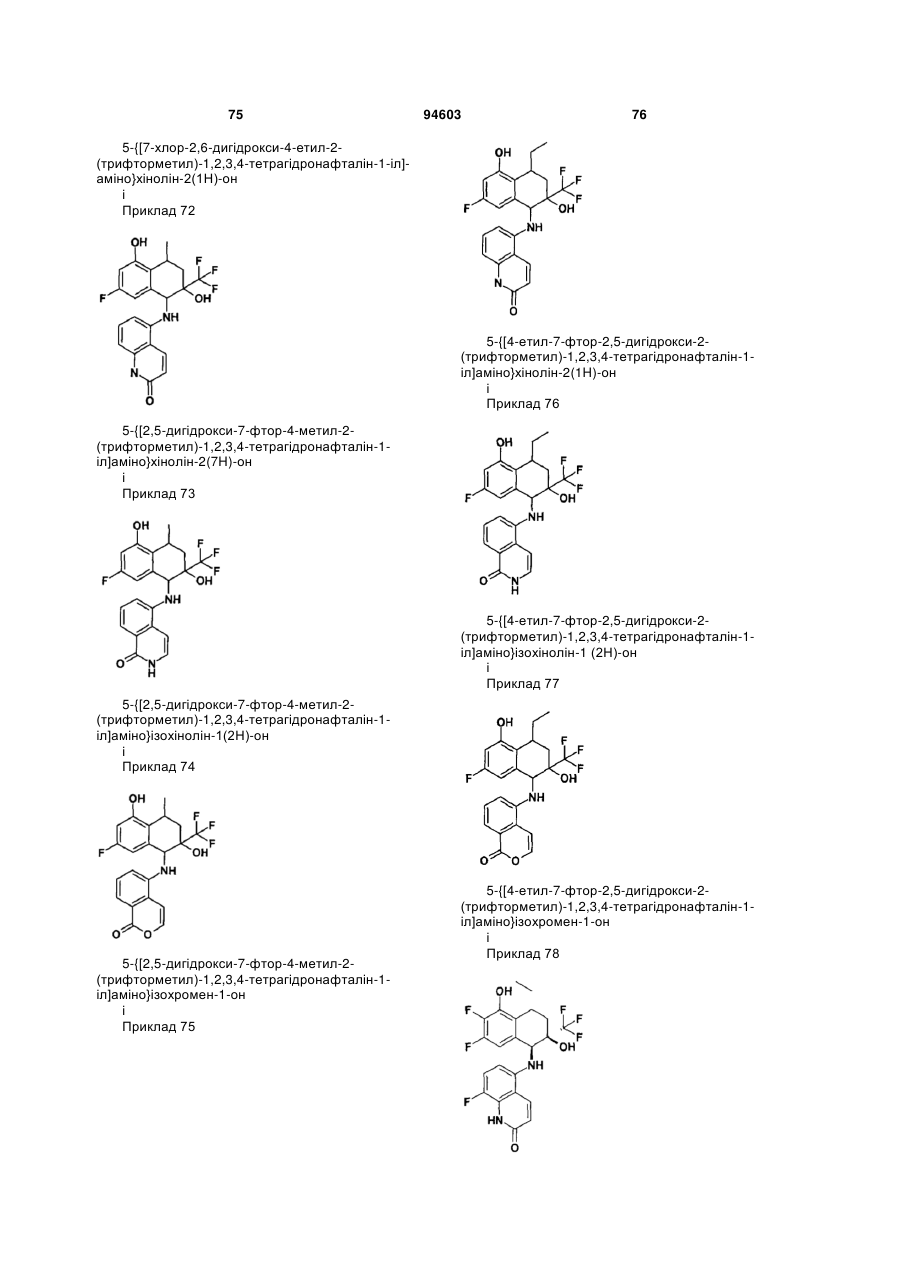
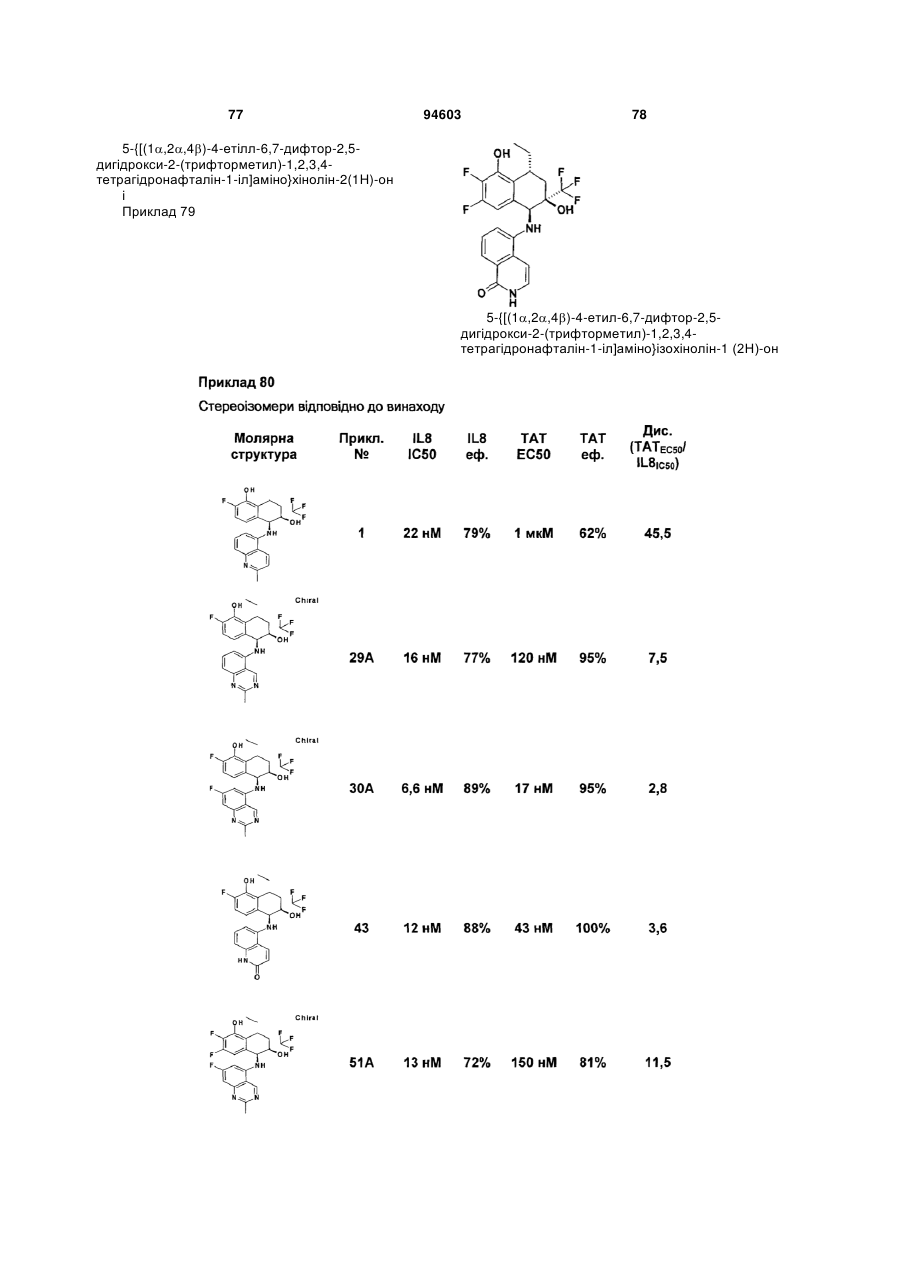
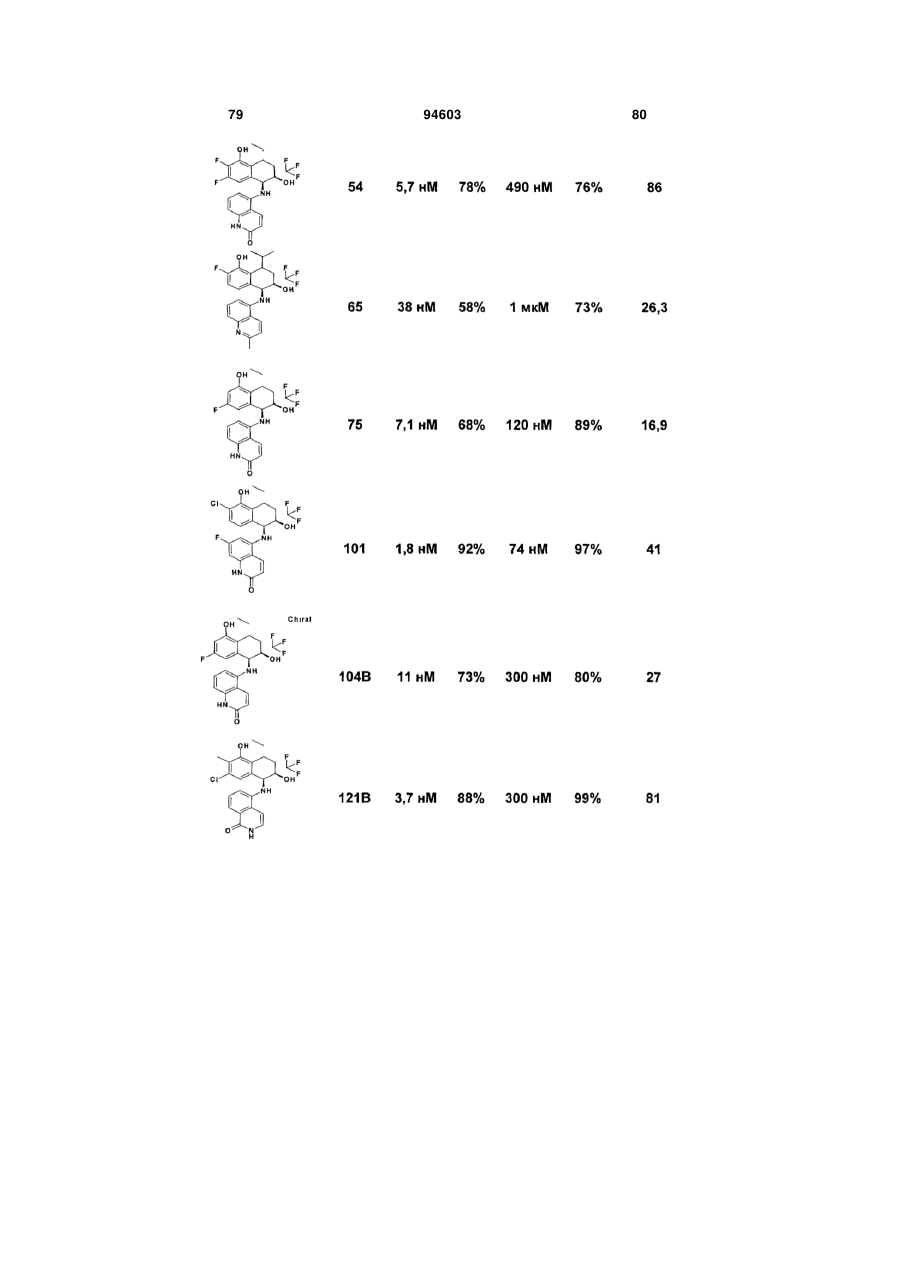
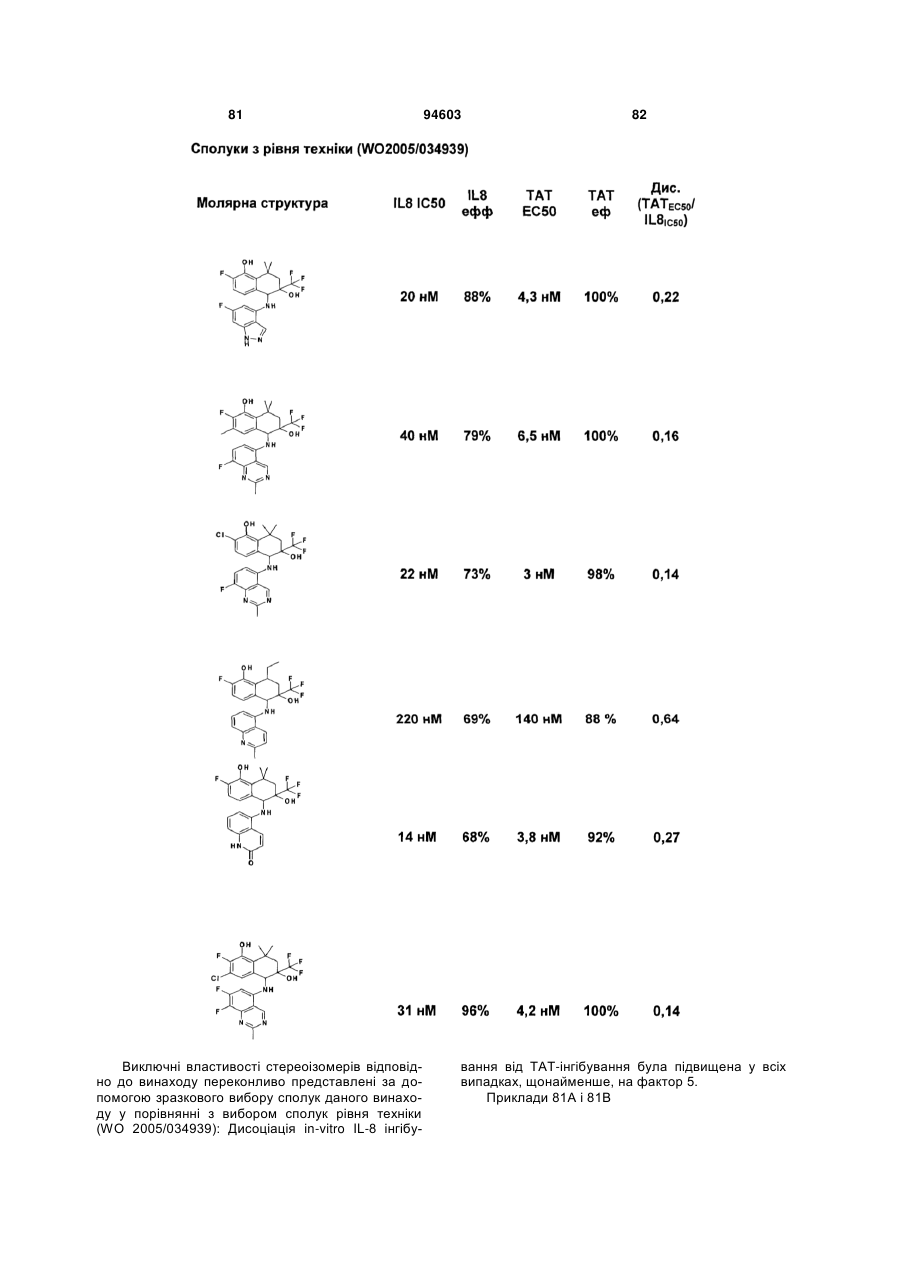
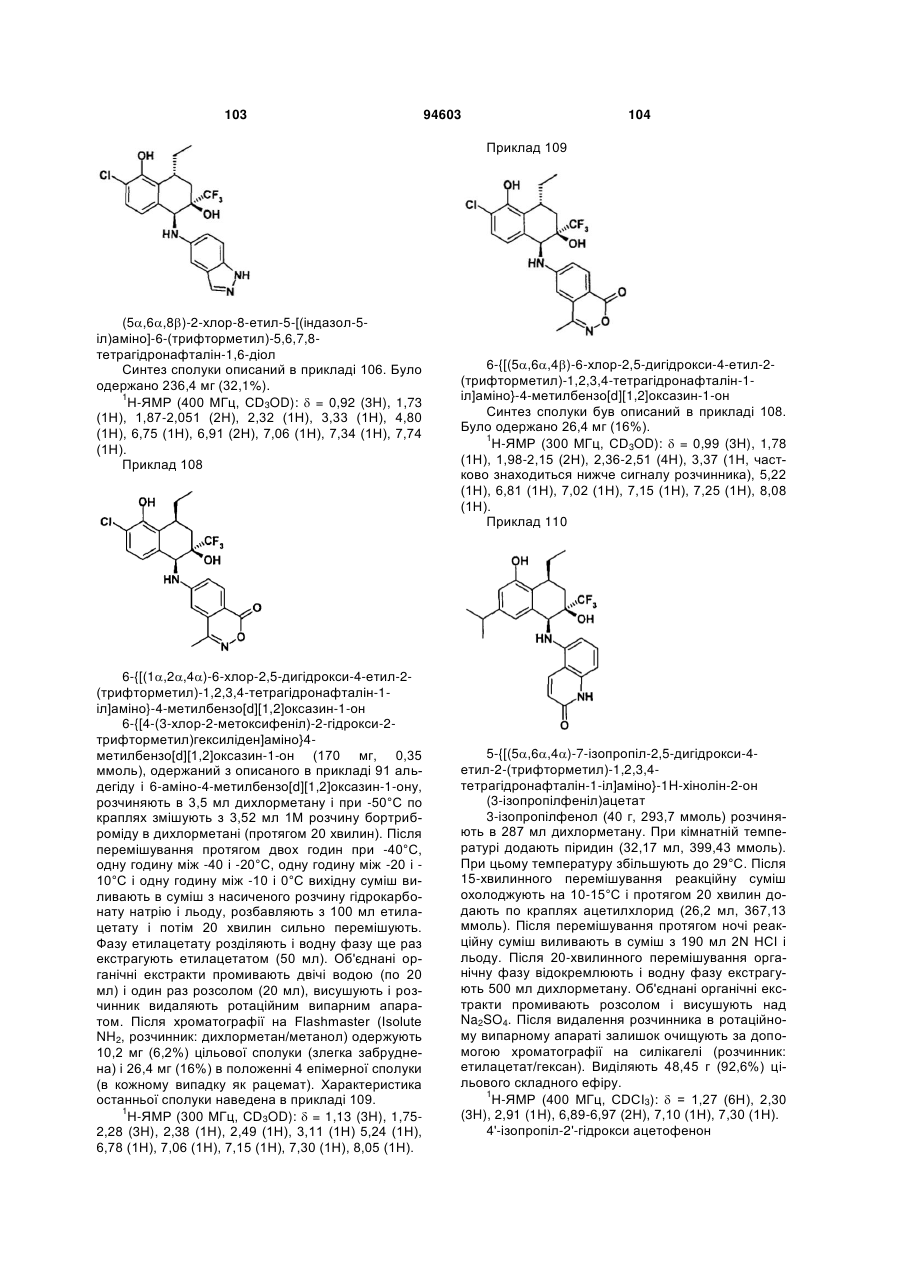
Похідні тетрагідронафталіну, спосіб їх одержання та їх застосування як інгібіторів запалення
Номер патенту: 94603
Опубліковано: 25.05.2011
Автори: Шмеес Норберт, Бойєрле Штефан, Шьокке Хайке, Ревінкель Хартмут, Бергер Маркус
Формула / Реферат
1. Сполука загальної формули (Іа)
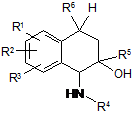 , (Іа)
, (Іа)
в якій
I) залишки R1, R2 і R3 незалежно один від іншого вибрані з -ОН, О-СН3, Сl, F, Н,
II) залишок R4 вибраний з
2-метилхінолін-5-ілу,
2-метилхіназолін-5-ілу,
2-етилхіназолін-5-ілу,
7-фтор-2-метилхіназолін-5-ілу,
8-фтор-2-метилхіназолін-5-ілу,
7,8-дифтор-2-метилхіназолін-5-ілу,
хінолін-2(1Н)он-5-ілу,
7-фторхінолін-2(1Н)он-5-ілу,
8-фторхінолін-2(1Н)он-5-ілу,
ізохромен-1-он-5-ілу,
2-метилфталазин-1-он-5-ілу,
ізохінолін-2(1Н)он-5-ілу,
III) залишок R5 означає -CF3, і
IV) залишок R6 вибраний з -СН3, -СН2-СН3, -(СН2)2-СН3 або -СН=СН2,
а також її стереоізомери або солі з фізіологічно сумісними аніонами, яка відрізняється тим, що сполуки представлені в 1α,2α,4b-конфігурації основної речовини 1-аміно-1,2,3,4-тетрагідронафталін-2-олу або сполуки представлені в 5α,6α,8b-конфігурації основної речовини 5,6,7,8-тетрагідронафталін-1,6-діолу.
2. Сполука за пунктом 1, яка відрізняється тим, що сполуки представлені у вигляді (1S,2R,4R) або (1S,2R,4S) абсолютної конфігурації основної речовини 1-аміно-(1,2,3,4)-тетрагідронафталін-2-олу або
(5S,6R,8R) або (5S,6R,8S) абсолютної конфігурації основної речовини 5,6,7,8-тетрагідронафталін-1,6-діолу.
3. Сполука за пунктом 1 або 2, вибрана з групи, що включає
(5α,6α,8b)-2-фтор-8-метил-5-[(2-метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-(5α,6α,8b)-2-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(-)-(5α,6α,8b)-2-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-2-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-5-[(7,8-дифтор-2-метилхіназолін-5-іл)аміно]-2-фтор-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-2-фтор-8-метил-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(5α,6α,8b)-1,6-дигідрокси-2-фтор-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-5-іл]аміно}хінолін-2(1Н)он,
8-фтор-5-{[(1α,2α,4b)-6-фтор-2-гідрокси-5-метокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-хінолін-2(1Н)он,
(+)-5-{[(1α,2α,4b)-6-фтор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
(-)-5-{[(1α,2α,4b)-6-фтор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
5-{[(1α,2α,4b)-6-фтор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2-метилфталазин-1-он,
(5α,6α,8b)-3-хлор-2-фтор-8-метил-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-3-хлор-2-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-1-метокси-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-6-ол,
(5α,6α,8b)-3-хлор-2-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-3-хлор-2-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-1-метокси-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-6-ол,
(5α,6α,8b)-3-хлор-2-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-3-хлор-5-[(7,8-дифтор-2-метилхіназолін-5-іл)аміно]-2-фтор-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-3-хлор-2-фтор-8-метил-5-[(2-метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-5-{[(1α,2α,4b)-7-хлор-2,5-дигідрокси-6-фтор-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]-аміно}-хінолін-2(1Н)он,
(-)-5-{[(1α,2α,4b)-7-хлор-2,5-дигідрокси-6-фтор-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]-аміно}-хінолін-2(1Н)он,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідрокси-6-фтор-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]-аміно}-8-фторхінолін-2(1Н)он,
(5α,6α,8b)-8-метил-5-[(2-метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-8-етил-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-(5α,6α,8b)-8-етил-2-фтор-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(-)-(5α,6α,8b)-8-етил-2-фтор-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-2-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-(5α,6α,8b)-8-етил-2-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(-)-(5α,6α,8b)-8-етил-2-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-5-[(7,8-дифтор-2-метилхіназолін-5-іл)аміно]-8-етил-2-фтор-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-хінолін-2(1Н)он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2-гідрокси-5-метокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
(+)-5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
(-)-5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2-метилфталазин-1-он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохінолін-(2Н)он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}ізохромен-1-он,
(5α,6α,8b)-5-[(2-етилхіназолін-5-іл)аміно]-2-фтор-8-пропіл-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-(5α,6α,8b)-8-етил-2,3-дифтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(-)-(5α,6α,8b)-8-етил-2,3-дифтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(7,8-дифтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(+)-5-{[(1α,2α,4b)-4-етил-6,7-дифтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
(-)-5-{[(1α,2α,4b)-4-етил-6,7-дифтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-4-етил-6,7-дифтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}фталазин-1-он,
(5α,6α,8b)-2-фтор-5-[(2-метилхіназолін-5-іл)аміно]-8-проп-1-іл-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5α,6α,8b)-2-фтор-5-[(7-фторо-2-метилхіназолін-5-іл)аміно]-8-проп-1-іл-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-4-етил-6,7-дифтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1H)он,
5-{[(1α,2α,4b)-4-етил-6,7-дифтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}ізохінолін-1(2Н)он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохромен-1-он,
5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохромен-1-он,
4-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2-он,
4-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2-он,
5-{[(1S,2R,4S)-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2H-хінолін-1-он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохромен-1-он,
5-{(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-4-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохромен-1-он,
4-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1 -іл]аміно}-1,3-дигідроіндол-2-он,
4-{[(1S,2R,4R)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
(5α,6α,8b)2-хлор-8-етил-5-[(індазол-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
6-{[(1α,2α,4b)-6-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-4-метилбензо[d][1,2]оксазин-1-он,
5-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
(5α,6α,8b)-8-етил-3-ізопропіл-5-[2-метилхіназолін-5-іламіно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
4-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2-он,
5-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-ізохромен-1-он,
5-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1H-хінолін-2-он,
5-{[(1α,2α,4b)-7-ізопропіл-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1H-хінолін-2-он,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-7-хлор-2,5-дигідрокси-6-метил-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2H-хінолін-1-он,
4-{[(1α,2α,4b)-7-хлор-2,5-дигідрокси-6-метил-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2-он,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1H-хінолін-2-он,
(5α,6α,8b)-3-хлор-8-етил-2-метил-5-[2-метилхіназолін-5-іламіно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1S,2R,4S)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-7-хлор-2,5-дигідроксі-4-етил-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фторхінолін-2(1Н)он,
5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}ізохінолін-1(2Н)он,
(5S,6R,8R)-8-етил-3-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-2-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-3-фтор-5-[(8-фтор-2-метилхіназолін-5-іл)аміно]-2-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1S,2R,4S)-4,6-діетил-7-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
5-{[(1S,2R,4R)-4,6-діетил-7-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
5-{[(1S,2R,4S)-4,6-діетил-7-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фторхінолін-2(1Н)он,
5-{[(1S,2R,4R)-4,6-діетил-7-фтор-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фторхінолін-2(1Н)он,
5-{[(1S,2R,4S)-4,6-діетил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-4,6-діетил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-4,6-діетил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-4,6-діетил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
(5S,6R,8S)-2,8-діетил-5-[2-метилхіназолін-5-іламіно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-7-хлор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7-фтор-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7-фтор-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фторхінолін-2(1Н)он,
5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7-фтор-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фторхінолін-2(1Н)он,
(5S,6R,8R)-2-хлор-8-етил-3-фтор-5-[(2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-2-хлор-8-етил-3-фтор-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-7-фтор-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(5S,6R,8R)-8-етил-3-фтор-1,6-дигідрокси-6-(трифторметил)-5,6,7,8-тетрагідронафталін-5-іл]аміно}-8-фторхінолін-2(1Н)он,
5-{[(1α,2α,4b)-7-фтор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-7-фтор-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-7-бром-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-7-бром-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-7-бром-2,5-дигідроксі-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-6-фтор-2,7-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
(5α,6α,8b)-8-етил-1,6-дигідроксі-5-(2-оксо-1,2-дигідрохінолін-5-іламіно)-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
(5α,6α,8b)-8-етил-1,6-дигідрокси-5-(8-фтор-2-оксо-1,2-дигідрохінолін-5-іламіно)-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
(5α,6α,8b)-8-етил-1,6-дигідроксі-5-[(1-оксо-1,2-дигідроізохінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
(5α,6α,8b)-1,6-дигідрокси-8-метил-5-[(2-оксо-2,3-дигідро-1Н-індол-4-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
(5α,6α,8b)-5-[(8-фтор-2-оксо-1,2-дигідрохінолін-5-іл)аміно]-1,6-дигідрокси-8-метил-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
5-{[(5S,6R,8R)-8-етил-1,6-дигідрокси-3-фтор-5-[(2-оксо-1,2-дигідрохінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
(5α,6α,8b)-8-етил-1,6-дигідрокси-3-фтор-5-[(8-фтор-2-оксо-1,2-дигідрохінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-2-карбонітрил,
5-{[(1S,2R,4S)-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4S)-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1S,2R,4R)-2,5-дигідрокси-4-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-4-етил-2,5-дигідрокси-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-6-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-7-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-7-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-7-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-4-етил-6-фтор-2,5-дигідрокси-7-метил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
(5α,6α,8b)-8-етил-2-фтор-3-метил-5-[2-метилхіназолін-5-іламіно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метил-1-оксихінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
5-{[(1α,2α,4b)-2,5-дигідрокси-6,7-диметил-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-2,5-дигідрокси-6,7-диметил-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін-2-он,
5-{[(1α,2α,4b)-2,5-дигідрокси-6,7-диметил-4-етил-2-(трифторметил)-1,2,3,4-тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он,
5-{[(5S,6R,8R)-2-хлор-8-етил-1,6-дигідрокси-3-фтор-2-6-(трифторметил)-5,6,7,8-тетрагідронафталін-5-іл]аміно}хінолін-2(1H)он,
5-{[(5S,6R,8R)-3-хлор-8-етил-1,6-дигідрокси-2-6-(трифторметил)-5,6,7,8-тетрагідронафталін-5-іл]аміно}-7-фторхінолін-2(1Н)он,
(5S,6R,8R)-2,3-дихлор-8-етил-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол,
(5S,6R,8R)-2-хлор-8-етил-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол
або
(5S,6R,8R)-3-хлор-8-етил-5-[(7-фтор-2-метилхіназолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6-діол.
4. Застосування сполук за одним з пунктів 1-3 для одержання лікарських засобів.
5. Застосування сполук за одним з пунктів 1-3 для одержання лікарських засобів для лікування запальних захворювань.
6. Енантіомерно чисті складні ефіри формули (VII)
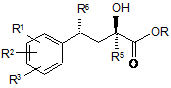 , (VII)
, (VII)
причому R1, R2, R3, R4, R5 і R6 мають значення, наведені в пункті 1, і R означає етильний залишок.
Текст
1. Сполука загальної формули (Іа) 2 3 сполуки представлені в 1α,2α,4-конфігурації основної речовини 1-аміно-1,2,3,4тетрагідронафталін-2-олу або сполуки представлені в 5α,6α,8-конфігурації основної речовини 5,6,7,8-тетрагідронафталін-1,6-діолу. 2. Сполука за пунктом 1, яка відрізняється тим, що сполуки представлені у вигляді (1S,2R,4R) або (1S,2R,4S) абсолютної конфігурації основної речовини 1-аміно-(1,2,3,4)-тетрагідронафталін-2-олу або (5S,6R,8R) або (5S,6R,8S) абсолютної конфігурації основної речовини 5,6,7,8-тетрагідронафталін-1,6діолу. 3. Сполука за пунктом 1 або 2, вибрана з групи, що включає (5α,6α,8)-2-фтор-8-метил-5-[(2-метилхінолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (+)-(5α,6α,8)-2-фтор-5-[(7-фтор-2-метилхіназолін5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (-)-(5α,6α,8)-2-фтор-5-[(7-фтор-2-метилхіназолін5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (5α,6α,8)-2-фтор-5-[(8-фтор-2-метилхіназолін-5іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (5α,6α,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-2-фтор-8-метил-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5α,6α,8)-2-фтор-8-метил-5-[(2-метилхіназолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(5α,6α,8)-1,6-дигідрокси-2-фтор-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-5іл]аміно}хінолін-2(1Н)он, 8-фтор-5-{[(1α,2α,4)-6-фтор-2-гідрокси-5-метокси4-метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-хінолін-2(1Н)он, (+)-5-{[(1α,2α,4)-6-фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1Н)он, (-)-5-{[(1α,2α,4)-6-фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1Н)он, 5-{[(1α,2α,4)-6-фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2-метилфталазин-1-он, (5α,6α,8)-3-хлор-2-фтор-8-метил-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5α,6α,8)-3-хлор-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-1-метокси-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-6-ол, (5α,6α,8)-3-хлор-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, (5α,6α,8)-3-хлор-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-1-метокси-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-6-ол, (5α,6α,8)-3-хлор-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-8-метил-6 94603 4 (трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, (5α,6α,8)-3-хлор-5-[(7,8-дифтор-2-метилхіназолін5-іл)аміно]-2-фтор-8-метил-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5α,6α,8)-3-хлор-2-фтор-8-метил-5-[(2метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (+)-5-{[(1α,2α,4)-7-хлор-2,5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-хінолін-2(1Н)он, (-)-5-{[(1α,2α,4)-7-хлор-2,5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-хінолін-2(1Н)он, 5-{[(1α,2α,4)-7-хлор-2,5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-8-фторхінолін2(1Н)он, (5α,6α,8)-8-метил-5-[(2-метилхінолін-5-іл)аміно]-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, (5α,6α,8)-8-етил-5-[(2-метилхіназолін-5-іл)аміно]6-(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, (+)-(5α,6α,8)-8-етил-2-фтор-5-[(2-метилхіназолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (-)-(5α,6α,8)-8-етил-2-фтор-5-[(2-метилхіназолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (5S,6R,8R)-8-етил-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (+)-(5α,6α,8)-8-етил-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (-)-(5α,6α,8)-8-етил-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5α,6α,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-8-етил-2-фтор-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-хінолін-2(1Н)он, 5-{[(1α,2α,4)-4-етил-6-фтор-2-гідрокси-5-метокси2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1Н)он, (+)-5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1Н)он, (-)-5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1Н)он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2-метилфталазин-1-он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохінолін-(2Н)он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}ізохромен-1-он, 5 (5α,6α,8)-5-[(2-етилхіназолін-5-іл)аміно]-2-фтор-8пропіл-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (+)-(5α,6α,8)-8-етил-2,3-дифтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (-)-(5α,6α,8)-8-етил-2,3-дифтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(7,8-дифтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (+)-5-{[(1α,2α,4)-4-етил-6,7-дифтор-2,5дигідрокси-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он, (-)-5-{[(1α,2α,4)-4-етил-6,7-дифтор-2,5-дигідрокси2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}хінолін-2(1Н)он, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метилхінолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-4-етил-6,7-дифтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}фталазин-1-он, (5α,6α,8)-2-фтор-5-[(2-метилхіназолін-5-іл)аміно]8-проп-1-іл-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, (5α,6α,8)-2-фтор-5-[(7-фторо-2-метилхіназолін-5іл)аміно]-8-проп-1-іл-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-4-етил-6,7-дифтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}хінолін-2(1H)он, 5-{[(1α,2α,4)-4-етил-6,7-дифтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}ізохінолін-1(2Н)он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2Н-хінолін-1-он, 5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2Н-хінолін-1-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохромен-1-он, 94603 6 5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохромен-1-он, 4-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1,3-дигідроіндол-2-он, 4-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1,3-дигідроіндол-2-он, 5-{[(1S,2R,4S)-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1α,2α,4)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2H-хінолін-1-он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2Н-хінолін-1-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохромен-1-он, 5-{(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-4-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохромен-1-он, 4-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1 іл]аміно}-1,3-дигідроіндол-2-он, 4-{[(1S,2R,4R)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1,3-дигідроіндол-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, (5α,6α,8)2-хлор-8-етил-5-[(індазол-5-іл)аміно]-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, 6-{[(1α,2α,4)-6-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-4-метилбензо[d][1,2]оксазин-1-он, 5-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, (5α,6α,8)-8-етил-3-ізопропіл-5-[2-метилхіназолін5-іламіно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 7 5-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2Н-хінолін-1-он, 4-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1,3-дигідроіндол-2-он, 5-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохромен-1-он, 5-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1H-хінолін-2-он, 5-{[(1α,2α,4)-7-ізопропіл-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1H-хінолін-2-он, 5-{[(1α,2α,4)-7-хлор-2,5-дигідроксі-4-етил-6-метил2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-7-хлор-2,5-дигідрокси-6-метил-4етил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-2H-хінолін-1-он, 4-{[(1α,2α,4)-7-хлор-2,5-дигідрокси-6-метил-4етил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-1,3-дигідроіндол-2он, 5-{[(1α,2α,4)-7-хлор-2,5-дигідроксі-4-етил-6-метил2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-7-хлор-2,5-дигідроксі-4-етил-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-8-фтор-1H-хінолін2-он, (5α,6α,8)-3-хлор-8-етил-2-метил-5-[2метилхіназолін-5-іламіно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, 5-{[(1S,2R,4S)-7-хлор-2,5-дигідроксі-4-етил-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін2-он, 5-{[(1α,2α,4)-7-хлор-2,5-дигідроксі-4-етил-6-метил2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-7-хлор-2,5-дигідроксі-4-етил-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін2-он, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, 5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он, 5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-7-фторхінолін2(1Н)он, 5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-8-фторхінолін2(1Н)он, 5-{[(1S,2R,4R)-4-етил-7-фтор-2,5-дигідрокси-6метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}ізохінолін-1(2Н)он, 94603 8 (5S,6R,8R)-8-етил-3-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-2-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, (5S,6R,8R)-8-етил-3-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-2-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол, 5-{[(1S,2R,4S)-4,6-діетил-7-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}хінолін-2(1Н)он, 5-{[(1S,2R,4R)-4,6-діетил-7-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}хінолін-2(1Н)он, 5-{[(1S,2R,4S)-4,6-діетил-7-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фторхінолін-2(1Н)он, 5-{[(1S,2R,4R)-4,6-діетил-7-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фторхінолін-2(1Н)он, 5-{[(1S,2R,4S)-4,6-діетил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-4,6-діетил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-4,6-діетил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-4,6-діетил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, (5S,6R,8S)-2,8-діетил-5-[2-метилхіназолін-5іламіно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-7-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1α,2α,4)-7-хлор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7фтор-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}хінолін-2(1Н)он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7фтор-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-7-фторхінолін2(1Н)он, 5-{[(1S,2R,4R)-6-хлор-4-етил-2,5-дигідрокси-7фтор-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-8-фторхінолін2(1Н)он, (5S,6R,8R)-2-хлор-8-етил-3-фтор-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5S,6R,8R)-2-хлор-8-етил-3-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-7-фтор-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(5S,6R,8R)-8-етил-3-фтор-1,6-дигідрокси-6(трифторметил)-5,6,7,8-тетрагідронафталін-5іл]аміно}-8-фторхінолін-2(1Н)он, 9 94603 10 5-{[(1α,2α,4)-7-фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-7-фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-7-бром-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-7-бром-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-7-бром-2,5-дигідроксі-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-6-фтор-2,7-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, (5α,6α,8)-8-етил-1,6-дигідроксі-5-(2-оксо-1,2дигідрохінолін-5-іламіно)-6-(трифторметил)5,6,7,8-тетрагідронафталін-2-карбонітрил, (5α,6α,8)-8-етил-1,6-дигідрокси-5-(8-фтор-2-оксо1,2-дигідрохінолін-5-іламіно)-6-(трифторметил)5,6,7,8-тетрагідронафталін-2-карбонітрил, (5α,6α,8)-8-етил-1,6-дигідроксі-5-[(1-оксо-1,2дигідроізохінолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-2-карбонітрил, (5α,6α,8)-1,6-дигідрокси-8-метил-5-[(2-оксо-2,3дигідро-1Н-індол-4-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-2-карбонітрил, (5α,6α,8)-5-[(8-фтор-2-оксо-1,2-дигідрохінолін-5іл)аміно]-1,6-дигідрокси-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-2карбонітрил, 5-{[(5S,6R,8R)-8-етил-1,6-дигідрокси-3-фтор-5-[(2оксо-1,2-дигідрохінолін-5-іл)аміно]-6(трифторметил)-5,6,7,8-тетрагідронафталін-2карбонітрил, (5α,6α,8)-8-етил-1,6-дигідрокси-3-фтор-5-[(8фтор-2-оксо-1,2-дигідрохінолін-5-іл)аміно]-6(трифторметил)-5,6,7,8-тетрагідронафталін-2карбонітрил, 5-{[(1S,2R,4S)-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-7-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4S)-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1S,2R,4R)-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-4-етил-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-6-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-7метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-1Н-хінолін-2-он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-7метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-7-фтор-1Н-хінолін2-он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-7метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-8-фтор-1Н-хінолін2-он, 5-{[(1α,2α,4)-4-етил-6-фтор-2,5-дигідрокси-7метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-2Н-хінолін-1-он, (5α,6α,8)-8-етил-2-фтор-3-метил-5-[2метилхіназолін-5-іламіно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5S,6R,8R)-8-етил-2,3-дифтор-5-[(2-метил-1оксихінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол, 5-{[(1α,2α,4)-2,5-дигідрокси-6,7-диметил-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-1Н-хінолін-2-он, 5-{[(1α,2α,4)-2,5-дигідрокси-6,7-диметил-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фтор-1Н-хінолін-2-он, 5-{[(1α,2α,4)-2,5-дигідрокси-6,7-диметил-4-етил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2Н-хінолін-1-он, 5-{[(5S,6R,8R)-2-хлор-8-етил-1,6-дигідрокси-3фтор-2-6-(трифторметил)-5,6,7,8тетрагідронафталін-5-іл]аміно}хінолін-2(1H)он, 5-{[(5S,6R,8R)-3-хлор-8-етил-1,6-дигідрокси-2-6(трифторметил)-5,6,7,8-тетрагідронафталін-5іл]аміно}-7-фторхінолін-2(1Н)он, (5S,6R,8R)-2,3-дихлор-8-етил-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол, (5S,6R,8R)-2-хлор-8-етил-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол або (5S,6R,8R)-3-хлор-8-етил-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол. 4. Застосування сполук за одним з пунктів 1-3 для одержання лікарських засобів. 5. Застосування сполук за одним з пунктів 1-3 для одержання лікарських засобів для лікування запальних захворювань. 6. Енантіомерно чисті складні ефіри формули (VII) OH R6 Дана патентна заявка заявляє пріоритет європейської патентної заявки ЕР06090031.3 (Дата подання: 15,3,2006), крім того, вона претендує на всі переваги дати подання заявки на патент США R1 R2 OR R5 O R3 , (VII) 1 2 3 4 5 6 причому R , R , R , R , R і R мають значення, наведені в пункті 1, і R означає етильний залишок. 11 60/784,441 (Дата подання: 22,3,2006, попередня заявка США). Винахід відноситься до похідних тетрагідронафталіну, способу їх одержання та їх застосування як інгібіторів запалення. З рівня техніки (WO 2005/034939) відомі циклічні інгібітори запалення загальної формули І причому ці сполуки в ході експерименту проявляють активні дисоціації між протизапальними і небажаними метаболічними діями. До того ж ці сполуки мають покращену вибірковість в порівнянні з іншими стероїдними рецепторами. Несподівано було виявлено, що сполуки формул (Іа) є особливо дисоційованими, приймаючи до уваги побічні дії, які in vitro можна виміряти у вигляді ТАТ індукції. Тому, даний винахід відноситься до стереоізомерів загальної формули (Іа), в якій 1 2 R і R незалежно один від іншого означають атом водню, гідроксигрупу, атом галогену, при необхідності заміщену (С1-С10)-алкільну групу, при необхідності заміщену (С1-С10)-алкоксигрупу, (С1С10)-алкілтіогрупу, (С1-С5)-перфторалкільну групу, 1 2 ціаногрупу, нітрогрупу, або R і R разом групу, вибрану з груп -О-(СН2)n-О-, -О-(СН2)n-СН2-, -ОСН=СН-, -(CH2)n+2-, -NH-(CH2)n+1, -N(С1-С3-алкіл)(СН2)n+1, -NH-N=CH-, причому n=1 або 2 і кінцеві атоми кисню і/або атоми вуглецю і/або атоми азоту зв'язані з безпосередньо суміжними кільцевими 8 9 8 9 атомами вуглецю, aбo NR R , причому R і R незалежно один від іншого можуть бути воднем, С1С5-алкілом або (СО)-С1-С5-алкілом, 3 R атом водню, гідроксигрупу, атом галогену, ціаногрупу, при необхідності заміщену (С1-С10)алкільну групу, (С1-С10)-алкоксигрупу, (С1-С10)алкілтіогрупу, (С1-С5)-перфторалкільну групу, 4 R С1-С10-алкільну групу, при необхідності заміщену за допомогою 1-3 гідроксигруп, атомів галогену, 1-3 (С1-С5)-алкоксигруп, при необхідності заміщену (С3-С7)-циклоалкільну групу, при необхідності заміщену гетероциклільну, при необхідно 94603 12 сті заміщену арильну групу, моно- або біциклічну гетероарильну групу при необхідності незалежно один від іншого заміщену за допомогою однієї або декількох груп, вибраних з (С1-С5)-алкільних груп (які при необхідності можуть бути заміщені 1-3 13 гідрокси або 1-3 COOR -групами), (С1-С5)8 9 алкоксигруп, атомів галогену, гідроксигруп, NR R груп, ексометиленгруп, кисню, яка при необхідності містить 1-4 атоми азоту і/або 1-2-атоми кисню і/або 1-2 атоми сірки і/або 1-2 кетогрупи, причому ця група в будь-якому положенні може бути зв'язана з аміном системи тетрагідронафталіну і при необхідності в одному або декількох місцях може бути гідрованою, 5 R (С1-С10)-алкільну групу або при необхідності частково або повністю фторовану (С1-С10)алкільну групу, (С3-С7)циклоалкільну групу, (C2С8)алкіл(С3-С7)циклоалкільну групу, (С2С8)алкеніл(С3-С7)циклоалкільну групу, гетероциклільну групу, (С1-С8)алкілгетероциклільну групу, (С2-С8)-алкенілгетероциклільну групу, арильну групу, (С1-С8)алкіларильну групу, (С2С8)алкеніларильну групу, (С2-С8)алкініларильні групи, при необхідності заміщені за допомогою 1-2 кетогруп, 1-2 (С1-С5)-алкільних груп, 1-2 (С1-С5)алкоксигруп, 1-3 атомів галогену, 1-2 ексометиленгруп, 1-3 атоми азоту і/або 1-2-атоми кисню і/або 12 атоми сірки, що містять моно- або біциклічну гетероарильну групу, (С1-С8)алкілгетероарильну групу або (С2-С8)алкенілгетероарильну групу, (С2С8)алкінілгетероарильну групу, причому ці групи в будь-якому положенні можуть бути зв'язані з тетрагідронафталіновою системою і при необхідності в одному або декількох місцях можуть бути гідрованими, 6 R метильну, етильну, пропільну, ізопропільну групу або етиленову групу і їх солі з фізіологічно сумісними аніонами, за винятком 6-фтор-1-[(2-метилхінолін-5-іл)аміно]-4етил-2-(трифторметил)-1,2,3,4тетрагідронафталін-2,5-діолу. Відома з рівня техніки (WO 2005/034939, приклад 279) сполука (6-фтор-1-[(2-метилхінолін-5іл)аміно]-4-етил-2-(трифторметил)-1,2,3,4тетрагідронафталін-2,5-діол)) категорично виключена з області захисту даної патентної заявки. Особливим об'єктом винаходу є стереоізомери загальної формули 1а, які у ароматичного кільця тетрагідронафталінової системи мають як заміс1 2 ники R і R , які незалежно один від іншого вибрані 13 8 9 з групи С1-С5-алкіл, С1-С5-алкокси, COOR , NR R , С1-С5-перфторалкіл, галоген, гідрокси, ціано, нітро, 3 і незалежно від них мають як замісники R , які вибрані з групи атоми водню, гідроксигрупи, атоми галогену, ціаногрупи, при необхідності заміщеної (С1-С3)-алкільної групи, (С1-С3)-алкоксигрупи, (С1С3)-алкілтіогрупи, (С1-С3)-перфторалкільної групи. 4 Залишок R аміном прив'язаний до тетрагідро4 нафталінової системи. Якщо залишок R має декілька положень, які можливі хімічно, щоб бути прив'язаним до кільцевої системи, тоді даний винахід охоплює всі ці варіанти. 4 Залишок R також включений в даний винахід, якщо він в одному або декількох місцях є гідрованим. 13 Як замісники моно- або біциклічних гетероа4 рильних груп (гетероциклічні групи) R , як вони були визначені вище, розташованих в хімічно прийнятних положеннях, придатні, наприклад, гідрокси, атоми галогену, особливо фтор і хлор, (С1-С5)алкільні групи (які самі при необхідності можуть бути заміщені за допомогою гідроксигруп, (С1-С5)13 13 алкоксигруп або COOR -груп, причому R означає водень або (С1-С5)-алкіл), особливо метил, (С2-С5)-алкенільні групи, повністю або частково фторовані (С1-С5)-алкільні групи, особливо CF3, CFH2, або C2F5, (С1-С5)-алкоксигрупи, особливо 8 9 метокси і етокси, NR R -групи, особливо NH2, N(СН3)2 або NH(CH3), ціаногрупи. а також кетогрупи, які утворюються з атомом вуглецю циклу гетероарильної групи і кисень, який з наявним при необхідності атомом азоту кільця утворює N-оксид. Звідси випливає як переважна група замісників до 4 гетероциклічної групи для залишку R як він визначений в пункті 1 і у всіх інших пунктах формули винаходу, група, що складається з фтору, хлору, ОН, СН3, CF3, CFH2, або C2F5, OCH3, OC2H5, NH2, N(CH3)2 і NH(CH3), ціано, кето, кисню. 5 Залишок R безпосередньо прив'язаний до те5 трагідронафталінової системи. Якщо залишок R має декілька положень, які є хімічно можливими для приєднання до кільцевої системи, то в такому випадку даний винахід охоплює всі ці варіанти. Тому, іншим об'єктом винаходу є стереоізоме5 ри загальної формули І в якій R означає (С1-С5)алкільну групу або при необхідності частково або повністю фторовану (С1-С5)-алкільну групу, (С3С7)циклоалкільну групу, (С1-С8)алкіл(С3С7)циклоалкільну групу, (С2-С8)алкеніл(С3С7)циклоалкільну групу, гетероциклільну групу, (С1-С8)алкілгетероциклільну групу, (С2С8)алкенілгетероциклільну групу, арильну групу, (С1-С8)алкіларильну групу, (С2-С8)алкеніларильну групу. Далі об'єктом винаходу є стереоізомери зага5 льної формули І, в якій R означає арильну групу, (С1-С8)алкіларильну групу, (С2-С8)алкеніларильну групу, (С3-С7)циклоалкільну групу, (С1-С8)алкіл(С3С7)циклоалкільну групу, (С2-С8)алкеніл(С3С7)циклоалкільну групу. Іншим об'єктом винаходу є стереоізомери за5 гальної формули І в яких R являє собою (С1-С10)алкільну групу або при необхідності частково або повністю фторовану (С1-С10)-алкільну групу, переважно (С1-С5)-алкільну групу або при необхідності частково або повністю фторовану (С1-С5)-алкільну групу, особливо переважно являє (С1-С3)-алкільну групу або при необхідності частково або повністю фторовану (С1-С3)-алкільну групу, особливо при необхідності являє частково або повністю фторовану (С1-С3)-алкільну групу, зовсім особливо CF3 або C2F5. Значним аспектом винаходу є ті стереоізомери відповідно до загальної формули Іа, причому 1 2 3 I) залишки R , R і R незалежно один від іншого вибрані з -ОН, С1-С4-алкокси, галогену, Н, 4 II) залишок R вибраний з хінолінової, хіназолінової або фталазинової групи, яка від нуля до двох разів заміщена метилом або етилом, а також від нуля до двох разів заміщена фтором 94603 14 5 III) залишок R означає при необхідності частково або повністю фторовану С1-С3-алкільну групу і 6 IV) залишок R вибраний з -СН3, -СН2-СН3, (СН2)2-СН3, -СН(СН3)2 або -СН=СН2. Особливо значним аспектом винаходу є ті стереоізомери відповідно до загальної формули Іа, в яких 1 2 3 I) залишки R , R і R незалежно один від іншого вибрані з -ОН, О-СН3, СІ, F, Н, 4 II) залишок R вибраний з 2-метилхінолін-5-іл 2-метилхіназолін-5-іл 2-етилхіназолін-5-іл 7-фтор-2-метилхіназолін-5-іл, 8-фтор-2-метилхіназолін-5-іл, 7,8-дифтор-2-метилхіназолін-5-іл, хінолін-2(1Н)-он-5-іл, 7-фторхінолін-2(1H)-он-5-іл, 8-фторхінолін-2(1Н)-он-5-іл, ізохромен-1-он-5-іл 2-метил-фталазин-1-он-5-іл ізохінолін-2(1H)-он-5-іл, 5 III) залишок R означає -CF3 і 6 IV) залишок R вибраний з -СН3, -СН2-СН3, (СН2)2-СН3, або -СН=СН2. Виключно важливим аспектом винаходу є ті стереоізомери відповідно до загальної формули Іа, причому енантіомерні сполуки знаходяться в 1, 2, 4-конфігурації до основної речовини 1,2,3,4-тетрагідронафталін-2-олу. Виходячи з правил номенклатури ІЮПАК при заміщені 1,6-дигідрокси тетрагідронафталіну це відповідає 5, 6, 8-конфігурації основної речовини 5,6,7,8-тетрагідронафталін-1,6-діолу (див. приклади). Особливо переважну підгрупу, як вона була розкрита для даного винаходу, являють ті залишки і всі їх підлеглі комбінації, які підтверджені прикладами. Визначення: Поняття атом галогену або галоген означає атом фтору, хлору, брому або йоду. Переважні атом фтору, хлору або брому. 1 2 4 5 С1-С10- або С1-С5-алкільні групи R , R , R , R , 6 7 11 12 13 R , R , R , R і R можуть бути з прямим ланцюгом або розгалуженими і наприклад, означають метильну, етильну, n-пропільну, ізо-пропільну, nбутил, ізо-бутил, трет.- бутильну або n-пентильну, 2,2-диметилпропільну, 2-метилбутильну або 3метилбутильну групу, а також гексильну, гептильну, нонільну, децильну групу і їх довільно розгалужені похідні. Переважною є метильна або етильна група. Наведені вище алкільні групи при необхідності можуть бути заміщені 1-5 групами незалежно один від іншого вибраними з гідрокси, ціано, нітро, 13 8 9 COOR , С1-С5-алкоксигруп, галогену, NR R , частково або повністю фторованої С1-С3-алкільної групи; одну подгрупу являють собою замісники 1-3 атомів галогену і/або 1-3 гідрокси- і/або 1-3 ціано13 і/або 1-3-СОOR -групи. Переважну підгрупу являють атом фтору, гідрокси- метокси- і/або ціаногрупи. 15 Алкильні групи при необхідності можуть бути 13 заміщені тільки 1-3 гідрокси-і/або 1-3- COOR групами. В такому випадку переважні гідроксигрупи. Для частково або повністю фторованої С1-С3алкільної групи придатні, наприклад, наступні частково або повністю фторовані групи: фторметил, дифторметил, трифторметил, фторетил, 1,1дифторетил, 1,2-дифторетил, 1,1,1-трифторетил, тетрафторетил, пентафторетил. З них переважні трифторметильна або пентафторетильна група, причому повністю фторованою групо, також називається перфторалкільна група. Реагенти, які при необхідності використовуються під час синтезу, є в продажі або опубліковані синтези відповідних реагентів відносяться до рівня техніки або можуть застосовуватися аналогічно до опублікованих синтезів. С1-С10- або С1-С5-алкоксигрупи можуть бути з прямим ланцюгом або розгалуженими і наприклад, означають метокси-, етокси-, n-пропокси-, ізопропокси-, n-бутокси, ізо-бутокси, трет.-бутоксиабо n-пентокси-, 2,2-диметилпропокси-, 2метилбутокси- або 3-метилбутоксигрупу. Переважні С1-С5-алкоксигрупи. Особливо переважною є метокси- або етоксигрупа. Наведені вище алкоксигрупи при необхідності можуть бути заміщені 1-3 групами, вибраними з галогену, особливо фтору, хлору, гідрокси і ціано. С1-С5-алкілтіогрупи можуть бути з прямим ланцюгом або розгалуженими і, наприклад, означать метилтіо-, етилтіо-, n-пропілтіо-, ізо-пропілтіо-, nбутилтіо, ізо-бутилтіо, трет.-бутилтіо- або nпентилтіо-, 2,2-диметилпропілтіо-, 2метилбутилтіо- або 3-метилбутилтіогрупу. Переважною є метилтіо- або етилтіогрупа. 8 9 Замісник NR R означає, наприклад, NH2, NH(CH3), N(CH3)2, NH(C2H5), N(C2H5)2, NH(C3H7), N(C3H7)2, NH(C4H9), N(C4H9)2, NH(C5H11), N(C5H11)2, NH(CO)CH3, NH(CO)C2H5, NH(CO)C3H7, NH(CO)C4H9, NH(CO)C5H11. Циклоалкільна група означає при необхідності заміщену за допомогою однієї або декількох груп вибраних з гідроксигруп, атомів галогену, (С1-С5)8 9 алкільних груп, (С1-С5)-алкоксигруп, NR R -груп, 13 COOR -груп, CHO, ціано насичену циклічну групу з від 3 до 7 циклічними атомами вуглецю, такими як, наприклад, циклопропіл, метилциклопропіл, циклобутил, метилциклобутил, циклопентил, метилциклопентил, циклогексил, метилциклогексил, циклогептил, метилциклогептил. Під (С1-С8)алкіл(С3-С7)циклоалкільною групою 5 R слід розуміти циклоалкільну групу, яка за допомогою нерозгалуженої або розгалуженої (С1-С8)алкільної одиниці з'єднана з циклічною системою. Під (С2-С8)алкеніл(С3-С7)циклоалкільною гру5 пою R слід розуміти циклоалкільну групу, яка за допомогою нерозгалуженої або розгалуженої (C2С8)-алкенільної одиниці з'єднана з циклічною системою. Гетероциклільна група є не ароматичною і може, наприклад, представляти собою піролідин, імідазолідин, піразолідин, піперидин. Пергідрохінолін і пергідроізохінолін також відносяться до охоплюваних гетероциклільних груп. Як замісники для гетероциклільних і гетероарильних груп при 94603 16 датні, наприклад, замісники з групи при необхідності заміщеної С1-С5-алкільної групи, гідрокси-, С18 9 13 С5-алкокси-, NR R -, галоген, ціано-, COOR -, CHO-. Замісники при необхідності можуть також бути прив'язані до атому азоту; тоді N-оксиди також включені у визначення. Арильні групи в змісті винаходу являють собою ароматичні або частково ароматичні карбоциклічні групи з від 6 до 14 атомами вуглецю, що мають один цикл, як наприклад феніл або фенілен або декілька конденсованих циклів, як наприклад нафтил або антраніл. Як приклад слід назвати феніл, нафтил, тетралініл, антраніл, індаліл і інденіл. Арильні групи можуть в кожному придатному місці, що веде до стабільного ізомеру, бути заміщені одним або декількома залишками з групи гідрокси, галоген, С1-С5-алкіл, С1-С5-алкокси, ціано, CF3, нітро, при необхідності заміщених 1-3 гід13 рокси групами, або СОOR -групами. Переважні необов'язково заміщені фенільні групи і нафтильні групи. (С1-С8)алкіларильна група являє собою арильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С1-С8)алкільної одиниці з'єднана з циклічною системою. (С2-С8)алкеніларильна група являє собою арильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С2-С8)алкенільної одиниці з'єднана з циклічною системою. (С2-С8)алкініларильна група являє собою арильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С2-С8)алкінільної одиниці з'єднана з циклічною системою. Моно- або біциклічна гетероарильна група при необхідності може бути заміщеною за допомогою одного або декількох замісників вибраних з ексометилену, галогену, С1-С5-алкільної групи, С1-С5алкоксигрупи необов'язково заміщених 1-3 гідрок13 си групами або 1-3-СОOR -групами. Замісники при необхідності можуть також бути безпосередньо прив'язаними до гетероатому. N-оксиди також включені в даний винахід. Моно- або біциклічна гетероарильна група при необхідності може містити 0-9 груп з груп атомів азоту, атомів кисню, атомів сірки або кетогруп, з чого можуть міститися максимально 4 атоми азоту, максимально 2 атоми кисню, максимально 2 атоми сірки і максимально 2 кетогрупи. Можлива кожна субкомбінація цієї групи. Гетероарильна група може бути гідрованою в одному або декількох місцях. Моноциклічні гетероарильні групи можуть представляти собою, наприклад, піридин, піразин, піримідин, піридазин, триазин, азаіндолізин, 2Н- і 4Н-піран, 2Н- і 4Н-тиопіран, фуран, тіофен, 1Н- і 4Н-піразол, 1Н- і 2Н-пірол, оксазол, тіазол, фуразан, 1Н- і 4Н-імідазол, ізоксазол, ізотіазол, оксадіазол, тріазол, тетразол, тіадіазол. Бициклічні гетероарильні групи можуть представляти собою, наприклад, фталідил-, тиофталідил-, індоліл-, ізоіндоліл-, дигідроіндоліл-, дигідроизоіндоліл-, індазоліл-, бензотіазоліл-, індолоніл-, дигідроіндолоніл-, ізоіндолоніл-, дигідроизоіндолоніл-, бензофураніл-, бензімідазоліл-, дигідроізохі 17 нолініл-, дигідрохінолініл-, бензоксазиноніл-, фталазиноніл-, дигідрофталазиноніл- хінолініл-, ізохінолініл-, хінолоніл-, ізохінолоніл-, хіназолініл-, хіноксалініл-, ціннолініл-, фталазиніл-, дигідрофталазиніл-, 1,7- або 1,8-нафтгіридиніл-. кумариніл-, ізокумариніл-, індолізиніл-, ізобензофураніл-, азаіндоліл-, азаізоіндоліл-, фуранопіридил-, фуранопіримідиніл-, фуранопіразиніл-, фуранопиридазиніл-, дигідробензофураніл-, дигідрофуранопіридил-, дигідрофуранопіримідиніл-, дигідрофуранопіразиніл-, дигідрофуранопіридазиніл-, дигідробензофураніл-, хроменіл-, ізохроменіл-, хроменоніл- або ізохроменоніл групами. Якщо гетероарильні групи частково або повністю гідровані, то до даного винаходу відносяться 3 стереоізомери формули Іа, в якій R означає тетрагідропіраніл, 2Н-піраніл, 4Н-піраніл, піперидил, тетрагідропіридил, дигідропіридил, 1Н-піридин-2оніл, 1Н-піридин-4-оніл, 4-амінопіридил, 1Нпіридин-4-іліденамініл, хроманіл, ізохроманіл, тіохроманіл, декагідрохінолініл, тетрагідрохінолініл, дигідрохінолініл, 5,6,7,8-тетрагідро-1H-хінолін-4оніл, декагідроізохінолініл, тетрагідроізохінолініл, дигідроізохінолініл, 3,4-дигідро-2Нбенз[1,4]оксазиніл, 1,2-дигідро[1,3]бензоксазин-4оніл, 3,4-дигідробенз[1,4]оксазин-4-оніл, 3,4дигідро-2Н-бензо[1,4]тіазиніл, 4Нбензо[1,4]тіазиніл, 1,2,3,4-тетрагідрохіноксалініл, 1Н-циннолін-4-оніл, 3H-хіназолін-4-оніл, 1Нхіназолін-4-оніл, 3,4-дигідро-1H-хіноксалин-2-оніл, 2,3-1,2,3,4-тетрагідро[1,5]нафтгиридинил, дигідро1H-[1,5]нафтгіридил, 1H-[1,5]нафтгірид-4-оніл, 5,6,7,8-тетрагідро-1H-нафтгиридин-4-оніл, 1,2дигідропиридо[3,2-d][1,3]оксазин-4-оніл, октагідро1H-індоліл, 2,3-дигідро-1H-індоліл, октагідро-2Низоіндоліл, 1,3-дигідро-2Н-изоіндоліл, 1,2дигідроіндазоліл, 1H-піроло[2,3-b]піридил, 2,3дигідро-1H-піроло[2,3-b]піридил, 2,2-дигідро-1Нпіроло[2,3-b]піридин-3-оніл. (С1-С8)алкілгетероарильна група являє собою гетероарильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С1С8)-алкільної одиниці з'єднана з циклічною системою. (С2-С8)алкенілгетероарильна група являє собою гетероарильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С2-С8)-алкенільної одиниці з'єднана з циклічною системою. 94603 18 (С2-С8)алкінілгетероарильна група являє собою гетероарильну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С2-С8)-алкінільної одиниці з'єднана з циклічною системою. (С1-С8)алкілгетероциклільна група являє собою гетероциклільну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С1-С8)-алкільної одиниці з'єднана з циклічною системою. (С2-С8)алкенілгетероциклільна група являє собою гетероциклільну групу, як вже описану вище, яка за допомогою нерозгалуженої або розгалуженої (С2-С8)-алкенільної одиниці з'єднана з циклічною системою. Відповідно до винаходу стереоізомери загальної формули Іа завдяки наявності центрів асиметрії можуть бути представленими як стереоізомери. Об'єктом даного винаходу є всі можливі стереоізомери (наприклад: RRR, RRS, RSR, SRR, RSS, SRS, SSR, SSS), як у вигляді рацематів, так і в енантіомерно чистому вигляді. Поняття стереоізомери також включає всі можливі діастереомери, регіоізомери і таутомери (наприклад, кето-енолтаутомери), в яких можуть перебувати стереоізомери відповідно до винаходу, які рівним чином є об'єктом винаходу. Як особливо переважні стереоізомери описаної сполуки слід назвати ті (1,2,3,4)тетрагідронафталіни, які містять (1S, 2R, 4R) або (1S, 2R, 4S) як абсолютну конфігурацію у 1-аміно1,2,3,4-тетрагідронафталін-2-ол основної речовини. Виходячи з правил номенклатури ІЮПАК при 1,6-дигідрокси заміщенні тетрагідронафталіну це відповідає (5S, 6R, 8R)-кoнфiгypaцiї основної речовини 5,6,7,8-тетрагідронафталін-1,6-діолу (див. приклади), або (5S, 6R, 8S)-конфігурації. Відповідно до винаходу стереоізомери можуть також перебувати у вигляді солей з фізіологічно сумісними аніонами, наприклад, у вигляді гідрохлориду, сульфату, нітрату, фосфату, півалату, малеату, фумарату, тартрату, бензоату, мезилату, цитрату або сукцинату. Сполуки відповідно до винаходу одержують тим, що, а) відповідно до відомих з рівня техніки методів генерують попередники з відкритим ланцюгом 1 2 3 загальної формули (II), в якій залишки R , R , R , 4 5 R , і R мають значення, наведені в пункті 1 формули винаходу, 19 які потім або без додаткового реагенту або шляхом додавання неорганічних або органічних кислот або кислот Льюїса при температурах в межах від -70°С до +80°С (переважно в межах від 30°С до +80°С) циклізують і перегруповують до одержання сполук загальної формули (III). Каталітичне гідрування, яке при необхідності може бути проведене діастереоселективно, потім дає сполу6 ки загальної формули (Іb), в якій R відповідає етильній групі. b) одержані відповідно до відомих з рівня техніки методів стироли загальної формули (IV) при необхідності за допомогою проведеної енантіоселективної єнової реакції за допомогою хіральних кислот Льюїса переводять в сполуки загальної 94603 20 формули (V). Як хіральні кислоти Льюїса для енантіоселективного генерування четвертинної спиртової функції можуть застосовуватися: (R)- або (S)-SEGPHOS-PdCl2 (Mikami et al. Tetrah. Asymm. 2004, 15, 3885-89), (R)- або (S)-BINOL-Ti(OiPr)2 (Ding et al. Tetrah. Lett. 2004, 45, 2009-12), (R)- або t i (S)-Cu BuBOX), (R)- або (S)-Cu PrBOX, (R)- або (S)-Cu PhBOX, (R)- або (S)- Cu AdaBOX (Evans et al. J. Am. Chem. Soc. 2000, 122, 7936-43), (R)- або i t (S)- Pr-pybox Yb(OTf)3, (R)- або (S)- Bu-pybox Yb(OTf)3, (R)- або (S)-Ph-pybox Yb(OTf)3 (Qian et al. Tetrah. Asymm. 2000, 11, 2347-57). За допомогою відновлення, гідрування і амінування відповідно до методів, відомих спеціалісту в даній галузі техніки, одержують імін (VI), 21 94603 22 який потім або без додаткового реагенту або за допомогою додавання неорганічних або органічних кислот або кислот Льюїса при температурах в межах від -70°С до +80°С (переважно в межах від 30°С до +80°С) циклізують до одержання сполук загальної формули (Іа). В наведених вище форму1 2 3 4 5 лах, взагалі, визначені залишки R , R , R , R , R , і 6 R мають значення, наведені в пункті 1 формули винаходу. Таким чином, об'єктом даного винаходу також є спосіб одержання стереоізомерів загальної формули (Іа), який відрізняється тим, що іміни загальної формули (VI) або (II) або без додаткового реагенту в розчиннику або концентрованих органічних кислотах або за допомогою додавання неорганічних або органічних кислот або кислот Льюїса при температурах в межах від -70°С до +80°С (переважно в межах від -30°С до +80°С) циклізують до одержання стереоізомерів загальної формули (Іа) або (III), a також їх безпосередніх попередників формули (V). Нові іміни (IV) для циклізації рівним чином є об'єктом даного винаходу, особливо ті, які розкриті за допомогою прикладів. Особливо переважним способом є метод одержання сполук загальної формули (V), в якій як каталізатори енантіоселективної єнової реакції використовують [Cu(S,S)біс(трет-бутилоксазолін] (SbF6)2 або [Cu(R,R)біс(трет-бутилоксазолін] (SbF6)2 і досягають надлишків енантіомерів до 95%, які можуть бути ще підвищені шляхом кристалізації. Енантіомерно чисті сполуки формули (V) шляхом хроматографічних методів розділення на силікагелі на стадії гідрованого альдегіду або іміну потім можуть бути переведені в енантіомерно чисті сполуки формули (VI). Альтернативно для одержання енантіомерно чистої сполуки формули (VI) можуть використатися діастереоселективні методи гідрування. Як каталізатори для зазначеного вище каталітичного гідрування придатні: 1. Палладій на вугіллі 2. Нікель Ренея 3. Родієві каталізатори з хіральними лігандами, такі як описані в нижченаведених публікаціях: - Weissenstein et al., Adv. Synth.Catal. 2003, 345, 160-164 - Imwinkelried et al., Chimia 1997, 51, 300 4. Іридієві каталізатори з хіральними лігандами, такі як описані в нижченаведених публікаціях: - Pfaltz et al., Org.Lett. 2004, 6, 2023-2026 - Blaser et al., Chimia 1999, 53, 275 5. Рутенієві каталізатори з хіральними лігандами, такі як описані в нижченаведеній публікації: - Chirality 2000, 12, 514-522 Таким чином, іншим об'єктом винаходу є енантіомерно чисті складні ефіри формули (VII), які можуть бути одержані шляхом діастереоселективних методів гідрування або розділення діастереомерів. Зв'язування речовин до глюкокортикоїдного рецептора (ГР) і інших стероїдних гормональних рецепторів (мінералкортикоїдний рецептор (МР), прогестероновий рецептор (ПР) і андрогеновий рецептор (АР) контролюється за допомогою рекомбінантно одержаних рецепторів. Препарування цитозоля Sf9 клітин, які були інфіковані рекомбінантними бакуловірусами, які кодують ГР, використовують для досліджень зв'язування. На відміну 3 від стандартної речовини [ Н]-дексаметазон речовини показують високу спорідненість до ГР. Як суттєвий, молекулярний механізм протизапальної дії глюкокортикоїдів розглядають передане за допомогою ГР інгібування транскрипції цитокинів, зчеплення молекул, ензимів і інших прозапальних факторів. Це інгібування досягається шляхом взаємодії ГР з іншими факторами транскрипції, наприклад, АР-1 і NF-каппа-В, (для огляду див. Cato ACB and Wade E, BioEssays 18, 371378 1996). Відповідно до винаходу стереоізомери загальної формули Іа інгібують викликану за допомогою ліпополісахариду (ЛПС) секрецію цитокіну IL-8 в людській моноцитарній клітинній лінії ТНР-1. Протизапальна дія стереоізомерів загальної формули Іа була випробувана в ході експерименту на тваринах за допомогою дослідження запалення, викликаного кротоновою олією, у щурів і мишей (J. Exp. Med. (1995), 182, 99-108). Для цього тваринам місцево нанесли на вуха спиртовий розчин кротонової олії. Дослідні речовини нанесли одночасно або за дві години до кротонової олії також місцево або системно. Через 16-24 годині вагу вух вимірювали як міру запального набряку, активність пероксидази як міру для дифузії гранулоцитів і активність еластази як міру для дифузії нейтрофільних гранулоцитів. Стереоізомери загальної формули Іа в цьому тесті інгібували три зазначених вище запальних параметри як після місцевого, так і після системного нанесення. Однією з самих частих небажаних дій глюкокортикоїдної терапії є так званий "стероїдний діабет" [див. Hatz, HJ, Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien, 23 Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart, 1998]. Причиною якого є стимуляція глюконеогенезу в печінці за допомогою індукції відповідальних за це ензимів і за допомогою вільних амінокислот, які утворюються з розщеплення білків (катаболічна дія глюкокортикоїдів). Ключовим ензимом катаболічного обміну речовин в печінці є тирозинамінотрансфераза (ТАТ). Активність цього ензиму може бути визначена фотометрично з печінкових гомогенатів і являє собою гарну міру для небажаних метаболічних дій глюкокортикоїдів. Для вимірювання ТАТ індукції через 8 годин після прийому дослідних речовин тварин умертвляли, виймали печінку і вимірювали активність ТАТ в гомогенаті. В цьому тесті стереоізомери загальної формули Іа в дозах, в яких вони діють протизапально, не індукували або індукували тільки в незначній мірі тирозинамінотрансферазу. Виходячи з їх протизапальної і додаткової протиалергійної, імунодепресивної і антипроліферативної дії відповідно до винаходу стереоізомери загальної формули Іа можуть застосовуватися як ліки для лікування або профілактики наступних хворобливих станів у ссавців і людей: при цьому поняття „ЗАХВОРЮВАННЯ" відноситься до нижченаведених показань: (і) захворювання легенів, що супроводжуються запальними, алергійними і/або проліферативними процесами: - хронічні обструктивні захворювання легенів будь-якого ґенезу, насамперед бронхіальна астма - бронхіт різного генезу - всі форми рестриктивних захворювань легенів, насамперед алергійний альвеоліт, - всі форми набряку легенів, насамперед токсичний набряк легенів - саркоїдози і гранулематози, особливо хвороба Бека (іі) ревматичні захворювання/автоімунні захворювання/захворювання суглобів, що супроводжуються запальними, алергійними і/або проліферативними процесами: - всі форми ревматичних захворювань, особливо ревматоїдний артрит, гостра ревматична лихоманка, ревматична поліміалгія - реактивний артрит - запальні захворювання м'яких частин тіла іншого генезу - артритичні симптоми при дегенеративних захворюваннях суглобів (артрози) - травматичні артритиди - колагенові захворювання будь-якого генезу, наприклад системна червона вовчанка, склеродермія, поліміозит, дерматоміозитний синдром Шегрена, синдром Стилла, синдром Фелті (ііі) аллергії, що супроводжуються запальними і/або проліферативними процесами: - всі види алергійних реакцій, наприклад, набряк Квінке, сінна лихоманка, укуси комах, алергійні реакції на ліки, препарати крові, контрастні речовини і т.п., анафілактичний шок, кропивниця, контактний дерматит (iv) запалення стінок суглобів (васкуліти) - вузлуватий панартериїт, артериїт темпоральний, вузлувата еритема 94603 24 (ν) дерматологічні захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - атопічний дерматит (насамперед у дітей) - псоріаз - червоний волосяний лишай - еритематозні захворювання, викликані різними шкідливими факторами, наприклад, опроміненням, хімікатами, опіками і т.п. - пузирчасті шкіряні хвороби - лихеноідні захворювання, - шкіряна сверблячка (наприклад, алергійного генезу) - себорейна екзема - розацеа - звичайна пузирчатка - багатоформна екссудативна еритема - баланіт - вульвіт - випадінняволосся, таке як колоподібне облисіння - шкіряна лімфома Τ - клітин (vi) захворювання нирок, що супроводжуються запальними, алергійними і/або проліферативними процесами: - нефротичний синдром - всі нефрити (vii) захворювання печінки, що супроводжуються запальними, алергійними і/або проліферативними процесами: - гостра дисоціація печінкових клітин - гострі гепатити різного генезу, наприклад вірусний, токсичний, викликаний прийомом ліків - хронічно агресивний і/або хронічно перемежований гепатит (viii) шлунково-кишкові захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - регіональний ентерит (хвороба Крона) - виразковий коліт - гастрит - рефлюкс-езофагіт - гастроентерити іншого генезу, наприклад ендемічний спру (іх) проктологічні захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - анальна екзема - тріщини - гемороїдальні вузли - ідиопатичний проктит (х) захворювання очей, що супроводжуються запальними, алергійними і/або проліферативними процесами: - алергійний кератит, увеїт, ірит, - кон'юнктивіт - блефарит - неврит зорового нерва - хоріодит - офтальмія симпатична (хі) захворювання вуха, горла, носа, що супроводжуються запальними, алергійними і/або проліферативними процесами: - алергійний риніт, сінна нежить 25 - зовнішній отит, наприклад викликаний контактною екземою, інфекцією і т. п. - запалення середнього вуха (хіі) неврологічні захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - набряк головного мозку, насамперед зумовлений пухлиною - розсіяний склероз - гострий енцефаломієліт - менінгіт - різні види судорожних припадків, наприклад блискавичні салаамови судороги (хііі) захворювання крові, що супроводжуються запальними, алергійними і/або проліферативними процесами: - придбана гемолітична анемія - ідіопатична тромбоцитопенія (xiv) онкологічні захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - гострий лімфалейкоз - злоякісні лімфоми - лімфогранулематози - лімфосаркоми - обширні метастазування, насамперед при раку молочної залози, бронхогенному раку і раку передміхурової залози (xv) ендокринні захворювання, що супроводжуються запальними, алергійними і/або проліферативними процесами: - ендокринна орбітопатія - тиреотоксичний криз - тиреоідит де Кервена - тиреоідит Хашимото - базедова хвороба (xvi) трансплантації органів і тканин, реакція "трансплантат проти хазяїна" (xvii) важкі шокові стани, наприклад, анафілактичний шок, синдром системної запальної відповіді (SIRS) (хvііі) блювота, що супроводжується запальними, алергійними і/або проліферативними процесами: - наприклад, в комбінації з 5-НТ3-антагоністом при цитостично зумовлених блювотах. (хіх) болі запального генезу, наприклад люмбаго (хх) замісна терапія при: - уродженій первинній недостатності наднирок, наприклад уроджений адреногенітальний синдром - придбаній первинній недостатності наднирок, наприклад, хвороба Аддісона, автоімунний адреналіт, постінфекційний, пухлини, метастази і т. п. - уродженій вторинній недостатності наднирок, наприклад, уроджений гіпопітуїтаризм - придбаній вторинній недостатності наднирок, наприклад, постінфекційній, пухлинах і т. д. Особливу ефективність проявляють лікарські засоби, що містять стереоізомери загальної формули Іа при наступних захворюваннях: 1. захворювання легенів 2. ревматичні захворювання/автоімунні захворювання 3. дерматологічні захворювання 94603 26 4. дегенеративні захворювання суглобів 5. запалення стінки суглоба 6. реакція "трансплантат проти хазяїна" 7. важкі шокові стани 8. блювоти, що супроводжуються запальними, алергійними і/або проліферативними процесами 9. біль, викликаний запаленням. Крім цього, відповідно до винаходу стереоізомери загальної формули Іа можуть використатися для терапії і профілактики інших не зазначених вище хворобливих станів, і для яких в теперішній час застосовують синтетичні глюкокортикоїди (для цього див. Hatz, HJ, Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien, Wissenschafliche Verlagsgesellschaft mbH, Stuttgart, 1998). Всі раніше названі показання від (і) до (хх) докладно описані в Hatz, HJ, Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien, Wissenschafliche Verlagsgesellschaft mbH, Stuttgart, 1998. Для терапевтичних впливів при зазначених вище хворобливих станах прийнятна доза є різною і залежить, наприклад, від сили дії сполуки загальної формули Іа, «хазяїна», способу застосування, виду і важкості станів, які лікують, а також застосування як профілактичного або терапевтичного засобу. Винахід відноситься до застосування сполук/ стереоізомерів, що заявляються, для одержання лікарських засобів. Крім того, винахід відноситься до (і) застосування одного з стереоізомерів відповідно до винаходу відповідно до формули Іа або їх сумішей для одержання ліків для лікування ЗАХВОРЮВАННЯ; (іі) способу лікування ЗАХВОРЮВАННЯ, причому спосіб включає застосування відповідно до винаходу стереоізомера формули Іа, причому кількості достатньої для пригнічення захворювання; (ііі) фармацевтичної композиції для лікування ЗАХВОРЮВАННЯ, лікування якого включає стереоізомери відповідно до винаходу або їх суміші і, щонайменше, одну фармацевтичну допоміжну речовину і/або носій. Взагалі, задовільних результатів можна очікувати у тварин, якщо добові дози містяться в межах від 1 мкг до 100,000 мкг сполуки відповідно до винаходу на кг маси тіла. Для більш великих ссавців, наприклад, людей, рекомендована добова доза знаходиться в межах від 1 мкг до 100,000 мкг на кг маси тіла. Переважною є доза від 10 до 30,000 мкг на кг маси тіла, особливо переважною є доза від 10 до 10,000 мкг на кг маси тіла. Наприклад, доцільно приймати цю дозу декілька разів на день. Для лікування гострих шокових станів (наприклад, анафілактичний шок) можуть видаватися однократні дози, які явно є вищими за зазначені дози. Приготування фармацевтичних препаратів на основі нових сполук відбувається відомим чином, при якому діючу речовину переробляють з використовуваними в галенових препаратах речовинаминосіями, наповнювачами, засобами, що впливають на розпад, зв'язувальними речовинами, стабіліза 27 торами вологості, речовинами, що надають слизькість, абсорбентами, розріджувачами, покращувачами смаку, барвниками і т.п., і переводять в бажану форму застосування. При цьому посилання робиться на Remington's Pharmaceutical Science, 15th ed. Mack Publishing Company, East Pennsylvania (1980). Для перорального застосування особливо придатні таблетки, драже, капсули, пігулки, порошки, грануляти, пастилки, суспензії, емульсії або розчини. Для парентерального застосування можливі ін'єкційні та інфузійні препарати. Для внутрішньосуглобної ін'єкції можуть застосовуватися приготовлені відповідним чином кристалічні суспензії. Для внутрішньом'язової ін'єкції можуть бути застосовними водні розчини і розчини в олії для ін'єкцій або суспензії і відповідні препарати пролонгованої дії. Для ректального застосування нові сполуки можуть застосовуватися у вигляді супозиторій, капсул, розчинів (наприклад, у вигляді клізм) і мазей, як для системної, так і для місцевої терапії. Для легеневого застосування нових сполук їх можливо застосовувати у вигляді аерозолів та інгалятів. Для місцевого застосування на очі, в зовнішній слуховий прохід, середнє вухо, носову порожнину і придаткові порожнини носа, нові сполуки можуть застосовуватися у вигляді крапель, мазей і настоянок у відповідних фармацевтичних композиціях. Для місцевого нанесення можливі препарати у вигляді гелів, мазей, жирових мазей, кремів, паст, присипок, молочка і настоянок. Дозування сполук загальної формули Іа в цих композиціях повинна складати 0,01%-20%, для того, щоб досягти необхідної фармакологічної дії. Також винахід включає сполуки загальної формули Іа відповідно до винаходу як терапевтичної діючої речовини. Далі до винаходу відносяться сполуки загальної формули Іа відповідно до винаходу як терапевтичної діючої речовини разом з фармацевтично сумісними і прийнятними допоміжними речовинами і носіями. Рівним чином винахід відноситься до фармацевтичної композиції, що містить одну з фармацевтично активних сполук відповідно до винаходу або її суміш, або її фармацевтично сумісну сіль і одну фармацевтично сумісну сіль або фармацевтично сумісні допоміжні речовини і носії. Крім того, винахід відноситься до комбінованого лікування або комбінованих композицій, в яких глюкокортикоїдний рецептор (ГР) агоніст формули (Іа) або його фармацевтично прийнятну сіль, або фармацевтичну композицію, що містить ГР агоніст формули (Іа) або їх фармацевтично прийнятну сіль, вводять або одночасно (при необхідності в ту ж саму композицію) або по черзі разом з одним або декількома лікарськими засобами для лікування одного з зазначених вище хворобливих станів. Наприклад, для лікування ревматоїдного артриту, остеоартриту, ХОЗЛ (хронічного обструктивного захворювання легенів), астми або алергійного риніту, ГР агоніст даного винаходу може бути ском 94603 28 бінований з одним або декількома лікарськими засобами для лікування такого стану. Якщо така комбінація вводиться шляхом інгаляції, то лікарський засіб, який комбінують, може бути вибраний з наступного переліку: - PDE4 інгібітор, включаючи інгібітор ізоформи PDE4D; - вибірковий агоніст .2. адренорецептора, такий як, наприклад, метапротеренол, ізопротеренол, ізопреналін, альбутерол, сальбутамол, формотерол, сальметерол, тербуталін, орципреналін, бітолтеролмезілат, пірбутерол або індакатерол; - антагоніст мускаринового рецептора (наприклад, М1, М2 або M3 антагоніст, такий як, наприклад, вибірковий M3 антагоніст), такий як, наприклад, іпратропійбромід, тіотропійбромід, окситропійбромід, пірензепін або телензепін; - модулятор функції хемокінового рецептора (як, наприклад, антагоніст CCR1 рецептора); або - інгібітор функції р38 кінази. Для іншого об'єкту даного винаходу така комбінація з ГР агоністом формули Іа або його фармацевтично прийнятною сіллю використовується для лікування ХОЗЛ, астми або алергійного риніту і може застосовуватися шляхом інгаляції або перорально в комбінації з ксантином (як, наприклад, амінофілін або теофілін), які також можуть вводитися шляхом інгаляції або перорально. Експериментальна частина Приклад 1 (5,6,8)-2-фтор-8-метил-5-[(2-метилхінолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол 4-(3-фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)пентанал: 41,8 г (639 ммоль) цинкового пилу і 874 мг (3,1 ммоль) хлориду свинцю(ІІ) суспендують в 557 мл ТГФ і при кімнатній температурі додають 39 мл (556 ммоль) дибромметану. Перемішують в наступні 30 хвилин і додають по краплях при 0°С 68,8 мл (68,8 ммоль) 1 Μ розчин хлориду титану (IV) в дихлорметані. Охолоджувальну ванну видаляють і через 30 хвилин при кімнатній температурі додають по краплях 13,6 г (80,8 ммоль) 1-(3-фтор-2метоксифеніл)етан-1-ону (Chem. Commun. 2000, 14, 1323-4) в 139 мл ТГФ. Перемішують в наступні 1,5 години при кімнатній температурі. Розбавляють простим діетиловим ефіром і реакційну суміш обережно додають в суміш з 4 Μ соляної кислоти і льоду. Фази розділяють, екстрагують простим діетиловим ефіром, промивають водою, сушать над сульфатом натрію і розчинник видаляють. Вихід 29 ний продукт очищують колонковою хроматографією на силікагелі (гексан/простий ізопропіловий ефір 0-5%) і одержують 9,5 г 2-фтор-6-(1метиленетил)анізолу. До 1,56 г (5,7 ммоль) 1,1'-бі-2-нафтолу додають 5,7 мл (2,85 ммоль) 0,5 Μ розчину тетраізопропілату титану в толуолі і червоний розчин перемішують протягом 2 годин при кімнатній температурі. Додають 9,5 г (57,2 ммоль) 2-фтор-6(1-метиленетил)анізолу і 12,5 мл (95 ммоль) етилтрифторпірувату і суміш нагрівають протягом 18 годин до 140°С. Після охолодження відразу очищують колонковою хроматографією на силікагелі (гексан/етилацетат 0-5%) і одержують 8,9 г складного етилового ефіру 4-(3-фтор-2-метоксифеніл)2-гідрокси-2-(трифторметил)пент-4-єнової кислоти. 8,9 г складного етилового ефіру (26,5 ммоль) 4-(3фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)-пент-4-єнової кислоти розчиняють в 200 мл метанолу і 2 мл оцтової кислоти і додають 890 мг палладія на вугіллі (10%-ий). Суспензію збовтують 1,5 години під атмосферою водню при нормальному тиску до поглинання водню в 560 мл. Суміш фільтрують крізь целіт, причому ретельно промивають повторно етилацетатом. Після видалення розчинника одержують 8,6 г складного етилового ефіру 4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)-пентанової кислоти. 8,6 г (25,4 ммоль) складного етилового ефіру 4-(3фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)-пентанової кислоти охолоджують в 350 мл простого діетилового ефіру до -30°С і через 15 хвилин додають порційно 1,7 г (44,7 ммоль) твердого алюмогідриду літію. Перемішують 1,5 години, причому температуру підвищують до -15°С, потім додають по краплях один за іншим етилацетат і воду і перемішують протягом наступної години, поки не утвориться добре фільтрівний осад. Суспензію фільтрують крізь целіт, причому ретельно повторно промивають етилацетатом. Фази фільтрату розділяють і ще раз екстрагують етилацетатом. Промивають насиченим розчином хлориду натрію, сушать над сульфатом натрію, і розчинник видаляють в вакуумі. Розділення за допомогою колонкової хроматографії на силікагелі (гексан/простий диізопропіловий ефір 0-15%) дає 3,1 г (2R*,4R*)-4-(3-фтор-2-метокси-феніл)-2гідрокси-2-(трифторметил)-пентаналу. 1 Н-ЯМР (300 МГц, CDCI3); = 1,13 (d, 3H), 2,25 (dd, 1H), 2,58 (dd, 1H), 3,33 (qdd, 1H), 3,92 (s, 3H), 3,98 (s, 1H), 6,92-6,99 (m, 3H), 9,12 (s, 1H), 0,72 г (2R*,4S*)-4-(3-фтор-2-метокси-феніл)-2-гідрокси-21 (трифторметил)-пентаналу Н-ЯМР (300 МГц, CDCI3); = 1,21 (d, 3H), 2,33 (dd, 1H), 2,39 (dd, 1H), 3,30 (qdd, 1H), 3,74 (s, 1H) 3,94 (s, 3H), 6,90-6,99 (m, 3H), 9,71 (s, 1H) і 2,0 г спирту. 175 мг (0,60 ммоль) (2R*,4R*)-4-(3-фтор-2метокси-феніл)-2-гідрокси-2-(трифторметил)пентаналу, 103 мг (0,63 ммоль) 5-аміно-2метилхіноліну і 0,3 мл тетраетилату титану перемішують в 20 мл толуолу 2 год. при 100°С. Після охолодження виливають на воду і енергійно перемішують. Суспензію фільтрують крізь целіт, причому ретельно повторно промивають етилацетатом. Фази фільтрату розділяють і ще раз 94603 30 екстрагують етилацетатом. Сушать над сульфатом натрію і розчинник видаляють в вакуумі і одержують 230 мг (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-1-[(2-метилхінолін-5ил)іміно]-2(трифторметил)пентан-2-олу у вигляді вихідного продукту. До 230 мг сирого іміну в 12 мл СН2СІ2 додають по краплях при -30°C 6 мл (6 ммоль) 1 Μ розчину бортриброміду. Залишають нагріватися до кімнатної температури і перемішують 2 години. Вихідну суміш змішують з нас. розчином NaHCO3, фази розділяють, водну фазу екстрагують за допомогою СН2СІ2, об'єднані органічні фази висушують (Na2SO4) і концентрують в вакуумі. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 145 мг продукту. 1 Н-ЯМР (300 МГц, CDCI3); = 1,39 (d, 3H), 1,82 (dd, 1H), 2,39 (dd, 1H), 2,64 (s, 3H), 3,40 (m, 1H), 4,95 (s, 1H), 6,60 (s, 1H), 6,75 (m, 2H), 7,17 (d, 1H), 7,29 (d, 1H), 7,45 (t, 1H), 8,20 (d, 1H). Приклад 2 (5,6,8)-2-фтор-5-[(7-фтор-2-метилхіназолін5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 250 мг (0,85 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 185 мг (1,05 ммоль) 5-аміно-7-фтор-2-метилхіназоліну і 0,4 мл тетраетилату титану до одержання (2R*,4R*)-4-(3-фтор-2-метокси-феніл)-1-[(7-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)пентан-2-олу. 430 мг одержаного таким чином сирого іміну циклізують аналогічно прикладу 1 при 30°С за допомогою 8 мл (8 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 67 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,44 (d, 3H), 1,88 (dd, 1H), 2,43 (dd, 1H), 2,74 (s, 3H), 3,40 (qdd, 1H), 5,25 (s, 1H), 6,69 (d, 1H), 6,70 (dd, 1H), 6,74 (d, 1H), 6,85 (dd, 1H), 9,49 (s, 1H). Приклад 2А/2В (5,6,8)-2-фтор-5-[(7-фтор-2-метилхіназолін5-іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол відщеплюють за допомогою препаративної хіральної ВЕРХ (Chiracel OD 5мк) в енантіомерно чисті сполуки: (+)-енантіомер: аналітична ВЕРХ: Rt=5,5 хв. (Chiralcel OD 5мк, 250x4,6 мм, гексан/етанол 5=>50%(20'), 1 мл/хв. плинність) 31 (-)-енантіомер: аналітична ВЕРХ: Rt=8,7 хв. (Chiralcel OD 5мк, 250x4,6 мм, гексан/етанол 5=>50%(20'), 1 мл/хв. плинність) Приклад 3 (5,6,8)-2-фтор-5-[(8-фтор-2-метилхіназолін5-іл)аміно]8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 150 мг (0,5 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 90 мг (0,5 ммоль) 5-аміно-8-фтор-2-метилхіназоліну і 0,2 мл тетраетилату титану до одержання (2R*,4R*)-4-(3-фтор-2-метокси-феніл)-1-[(8-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)пентан-2-олу. 230 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -30°С з 4 мл (4 ммоль) 1 Μ розчину бортриброміду циклізують до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) дає 42 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,42 (d, 3H), 1,85 (dd, 1H), 2,42 (dd, 1H), 2,80 (s, 3H), 3,41 (qdd, 1H), 5,16 (s, 1H), 6,73-6,80 (m, 1H), 6,83 (dd, 1H), 7,50 (dd, 1H), 9,58 (s, 1H). Приклад 4 (5,6,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-2-фтор-8-метил-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 150 мг (0,5 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 100 мг (0,51 ммоль) 5-аміно-7,8-дифтор-2метилхіназоліну і 0,2 мл тетраетилату титану до одержання (2R*,4R*)-1-[(7,8-дифтор-2метилхіназолін-5ил)іміно]-4-(3-фтор-2-метоксифеніл)-2-(трифторметил)-пентан-2-олу. 240 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -30°С з 4 мл (4 ммоль) 1 Μ розчину бортриброміду циклізують до одержання цільового 94603 32 продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) дає 30 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,44 (d, 3H), 1,87 (dd, 1H), 2,43 (dd, 1H), 2,79 25 (s, 3H), 3,40 (qdd, 1H), 5,20 (s, 1H), 6,71 (dd, 1H), 6,77 (dd, 1H), 6,85 (dd, 1H), 9,52 (s, 1H). Приклад 5 (5,6,8)-2-фтор-8-метил-5-[-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 135 мг (0,46 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 100 мг (0,63 ммоль) 5-аміно-2-метилхіназолін і 0,23 мл тетраетилат титану до одержання (2R*,4R*)-4-(3фтор-2-метокси-феніл)-1-[(2-метилхіназолін5ил)іміно]-2-(трифторметил)пентан-2-олу. 260 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -30°С з 5 мл (5 ммоль) 1 Μ розчину бортриброміду циклізують до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 56 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,44 (d, 3H), 1,87 (dd, 1H), 2,44 (dd, 1H), 2,77 (s, 3H), 3,41 (qdd, 1H), 5,23 (s, 1H),6,73 (dd, 1H), 6,83 (dd, 1H), 6,87 (d, 1H), 7,14 (d, 1H), 7,74 (t, 1H), 9,56 (8, 1H). Приклад 6 5-{[(5,6,8)-1,6-дигідрокси-2-фтор-8-метил6-(трифторметил)-5,6,7,8-тетрагідронафталін-5іл]аміно}хінолін-2(1H)-он Аналогічно прикладу 1 піддають взаємодії 250 мг (0,46 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 132 мг (0,63 ммоль) 5-амінохінолону і 0,4 мл тетраетилату титану до одержання 5-{[(2R*,4R*)-4-(3-фтор2-метоксифеніл)-2-гідрокси-2(трифторметил)пентиліден]аміно}хінолін-2(1H) 33 ону. 64 мг очищеного колонковою хроматографією іміну (силікагель, гексан/складний ефір оцтової кислоти 0-75%) циклізують аналогічно прикладу 1 при -30°С з 1,5 мл (1,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 52 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,42 (d, 3H), 1,84 (dd, 1H), 2,42 (dd, 1H), 3,40 (qdd, 1H), 5,08 (s, 1H), 6,47 (d, 1H), 6,54 (d, 1H), 6,65 (d, 1H), 6,71 (dd, 1H), 6,83 (dd, 1H), 7,32 (t, 1H), 8,17 (d, 1H). Приклад 7 8-фтор-5-{[(1,2,4)-6-фтор-2-гід рокси-5метокси-4-метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-хінолін-2(1H)-он 5-аміно-8-фторхінолін-2(1Н)-он: 5,8-дифторхінолін-2(1Н)-ону і 1,18 г (8,2 ммоль) Cu2О домішують в 620 мл етиленгліколю під 8 бар з газоподібн. NH3. Реакційну суміш протягом 19 год. нагрівають до 190°С. Після охолодження реакційної суміші і видалення розчинника вихідний продукт очищують колонковою хроматографією (силікагель, гексан; СН2СІ2/МеОН 0-5%). Одержують 1,03 г 5-аміно-8-фторхінолін-2(7Н)-ону у вигляді світло-жовтої твердої речовини. 1 Н-ЯМР (300 МГц, ДМСО-d6); = 5,58 (s, 2H), 6,23 (dd, 1H), 6,31 (d, 1H), 7,03 (dd, 1H), 8,05 (dd, 1H), 11,28 (s, 1H). Аналогічно прикладу 1 піддають взаємодії 300 мг (1,01 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 180 мг (1,01 ммоль) 5-аміно-8-фторхінолону і 0,48 мл тетраізопропілату титану в 9 мл ксилолу до одержання 8-фтор-5-{[(2R*,4R*)-4-(3-фтор-2метоксифеніл)-2-гідрокси-2-(трифторметил)пентиліден]аміно}хінолін-2(1Н)-он. 80 мг очищеного колонковою хроматографією іміну (силікагель, гексан; СН2СІ2/і-РrОН 0-5%) циклізують аналогічно прикладу 1 при -40°С з 1,7 мл (1,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту і до розщепленого простого ефіру прикладу 8. 1 Н-ЯМР (300 МГц, CD3OD); = 1,38 (d, 3H), 1,85 (dd, 1H), 2,39 (dd, 1H), 3,38 (m, 1H), 3,88 (s, 3H), 5,03 (s, 1H), 6,43 (dd, 1H), 6,51 (d, 1H), 6,80 7,05 (m, 2H), 7,15 (dd, 1H), 8,14 (dd, 1H). Приклад 8 94603 34 5-{[(1,2,4)-6-Фтор-2,5-дигідрокси-4-метил-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он одержують після хроматографічного очищення з прикладу 7. 1 Н-ЯМР (300 МГц, CD3OD); = 1,40 (d, 3H), 1,83 (dd, 1H), 2,40 (dd, 1H), 3,38 (m, 1H), 5,03 (s, 1H), 6,45 (dd, 1H), 6,48 (d, 1H) 6,49 (dd, 1H), 6,70 (dd, 1H), 6,82 (t, 1H), 7,07 (dd, 1H), 7,17 (dd, 1H), 8,13 (dd, 1H). Приклад 8А/8В 5-{[(1,2,4)-6-фтор-2,5-дигідрокси-4-метил2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiracel OD 20мк) в енантіомерно чисті сполуки: (-)-енантіомер: аналітична ВЕРХ: Rt=7,71 хв. (Chirapak AD-H 5мк, 150x4,6 мм, гексан/етанол 5%50% (20'), 1 мл/хв. плинність, 25°С). (+)-енантіомер (ZK 376768): аналітична ВЕРХ: Rt=9,53 хв. [Chirapak AD-H 5мк, 150x4,6 мм, гексан/етанол 5%50% (20'), 1 мл/хв. плинність, 25°С). Приклад 9 5-{[(1,2,4)-6-фтор-2,5-дигідрокси-4-метил2-(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2-метилфталазин-1-он Аналогічно прикладу 1 піддають взаємодії 295 мг (1,0 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 217 мг (1,0 ммоль) 5-аміно-2-метилфталазин-1-ону і 0,53 мл тетраетилату титану до одержання 5{[(2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси2-(трифторметил)пентиліден]аміно}-2метилфталазин-1-ону. 590 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при 30°С циклізують з 10 мл (10 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-60%) дає 204 мг продукту. 35 Н-ЯМР (300 МГц, CD3OD); = 1,43 (d, 3H), 1,86 (dd, 1H), 2,43 (dd, 1H), 3,40 (qdd, 1H), 3,79 (s, 3H), 5,18 (s, 1H), 6,71 (dd, 1H), 6,84 (dd, 1H), 7,16 (d, 1H), 7,59 (t, 1H), 7,60 (d, 1H), 8,50 (s, 1H). Приклад 10 1 (5,6,8)-2-фтор-8-метил-5-[(2-метилхінолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 175 мг (0,60 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 103 мг (0,63 ммоль) 5-аміно-2-метилхіноліну і 0,3 мл тетраетилату титану до одержання (2R*,4S*)-4-(3фтор-2-метокси-феніл)-1-[(2-метилхінолін-5іл)іміно]-2-(трифторметил)пентан-2-олу. 230 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -30°С циклізують з 5 мл (5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 135 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,60 (d, 3H), 2,21 (d, 1H), 2,33 (dd, 1H), 2,70 (s, 3H), 3,43 (qd, 1H), 5,16 (s, 1H), 6,76-6,87 (m, 3H), 7,30 (d, 1H), 7,33 (d, 1H), 7,55 (t, 1H), 8,44 (d, 1H). Приклад 11 (5,6,8)-2-фтор-5-[(2-метилхіназолін-5іл)аміно]-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 135 мг (0,46 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-пентаналу, 100 мг (0,63 ммоль) 5-аміно-2-метилхіназоліну і 0,23 мл тетраетилату титану до одержання (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-1-[(2метилхіназолін-5-іл)іміно]-2(трифторметил)пентан-2-олу. 260 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -30°С циклізують з 5 мл (5 ммоль) 1 Μ розчину 94603 36 бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 56 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,58 (d, 3H), 2,20 (dd, 1H), 2,44 (dd, 1H), 2,77 (s, 3H), 3,41 (qdd, 1H), 5,16 (s, 1H), 6,73-6,87 (m, 3H), 7,14 (d, 1H), 7,74 (t, 1H), 9,56 (s, 1H). Приклад 12 (5,6,8)-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно] 8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 170 мг (0,58 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 124 мг (0,70 ммоль) 5-аміно-8-фтор-2-метилхіназоліну і 0,31 мл тетраетилату титану до одержання (2R*,4S*)-4-(3-фтор-2-метокси-феніл)-1-[(8-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)пентан-2-олу. 295 мг одержаного таким чином сирого іміну аналогічно прикладу 1 при -20°С циклізують з 2,6 мл (2,6 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) дає 25 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,55 (d, 3H), 2,16 (dd, 1H), 2,29 (dd, 1H), 2,79 (s, 3H), 3,38 (qdd, 1H), 5,15 (s, 1H), 6,74 (dd, 1H)6,81-6,87 (m, 2H), 7,52 (dd, 1H), 9,62 (s, 1H). Приклад 13 (5,6,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-2-фтор-8-метил-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 170 мг (0,58 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 124 мг (0,60 ммоль) 5-аміно-7,8-дифтор-2 37 метилхіназоліну і 0,31 мл тетраетилату титану до одержання (2R*,4S*)-1-[(7,8-дифтор-2метилхіназолін-5ил)іміно]-4-(3-фтор-2метоксифеніл)-2-(трифторметил)пентан-2-олу. 85 мг очищеного колонковою хроматографією іміну (силікагель, гексан/складний ефір оцтової кислоти 0-30%) циклізують аналогічно прикладу 1 при 20°С з 0,72 мл (0,72 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Препаративна тонкошарова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) дає 15 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,55 (d, 3H), 2,15 (dd, 1H), 2,30 (dd, 1H), 2,78 (s, 3H), 3,37 (qdd, 1H), 5,16 (s, 1H), 6,72 (dd, 1H)6,83 (dd, 2H), 6,86 (dd, 1H), 9,58 (s, 1H). Приклад 14 (5,6,8)-3-хлор-2-фтор-8-метил-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол 4-(4-хлор-3-фтор-2-метоксифеніл)-2-гідрокси2-(трифторметил)пентанал: До 10 г (68,2 ммоль) 3-хлор-2-фторфенолу в 68 мл дихлорметану і 7,7 мл (98,5 ммоль) піридину додають по краплях при 0°С мл 5,1 мл (71,6 ммоль) ацетилхлориду. Суміш перемішують протягом години і додають 100 мл 1 Μ соляної кислоти. Екстрагують за допомогою дихлорметану і промивають водою. Після висушування над сульфатом натрію і видалення розчинника в вакуумі кількісно одержують 13 г складного ефіру 3-хлор2-фторфеніл-оцтової кислоти. 13 г (68,2 ммоль) складного ефіру 3-хлор-2-фторфеніл-оцтової кислоти в 6,9 мл 1,2-дихлорбензолу додають по краплях при охолодженні льодом до одержання 9,2 г (68,9 ммоль) трихлориду алюмінію в 6,9 мл 1,2дихлорбензолу і по закінченні суміш перемішують протягом 6 годин при 100°С. Залишають охолоджуватися, розбавляють дихлорметаном і обережно виливають в суміш з 4 Μ соляної кислоти і льоду. Фази розділяють, екстрагують за допомогою дихлорметану, промивають насиченим розчином хлориду натрію і сушать над сульфатом натрію. Вихідний продукт очищують колонковою хроматографією на силікагелі (гексан/етилацетат 10-50%) і одержують 11,4 г 1-(4-хлор-3-фтор-2гідроксифеніл)етан-1-ону і 0,74 г 1-(2-хлор-3-фтор4-гідроксифеніл)етан-1-ону. 11,4 г (60,4 ммоль) 1(4-хлор-3-фтор-2-гідроксифеніл)етан-1-он в розчиняють 120 мл ацетону і додають 15,5 г (112 ммоль) карбонату калію і 6,9 мл (110 ммоль) метилйодіду. Суміш перемішують 7 годин при 70°С і по закін 94603 38 ченні розчинник в значній мірі видаляють. Залишок виливають в воду і екстрагують простим метил-tбутиловим ефіром. Промивають насиченим розчином хлориду амонію, сушать над сульфатом натрію і після видалення розчинника в вакуумі одержують 11,3 г 1-(4-хлор-3-фтор-2метоксифеніл)етан-1-ону. 27,1 г (415 ммоль) цинкового пилу і 640 мг (2,3 ммоль) хлориду свинцю (II) суспендують в 400 мл ТГФ і при кімнатній температурі додають 26 мл (230 ммоль) дибромметану. Перемішують в наступні 30 хвилин і додають по краплях при охолодженні крижаною ванною 46,1 мл (46,1 ммоль) 1 Μ розчину хлориду титану (IV) в дихлорметані. Через 30 хвилин при 5-10°С додають по краплях 9,3 г (46,1 ммоль) 1-(4-хлор-3фтор-2-метоксифеніл)етан-1-ону в 92 мл ТГФ при 5°С. Перемішують в наступні 15 годин при кімнатній температурі. Розбавляють простим діетиловим ефіром і реакційну суміш обережно додають в суміш з 4 Μ соляної кислоти і льоду. Фази розділяють, екстрагують простим діетиловим ефіром, промивають водою, сушать над сульфатом натрію і розчинник видаляють. Вихідний продукт очищують колонковою хроматографією на силікагелі (гексан/етилацетат 10-40%) і одержують 2,68 г 3хлор-2-фтор-6-(1-метиленетил)-анізол. До 760 мг (2,67 ммоль) 1,1'-бі-2-нафтолу додають 2,68 мл (1,34 ммоль) 0,5 Μ розчину тетраізопропілату титану в толуолі і червоний розчин перемішують протягом години при кімнатній температурі. 5,07 г (28,1 ммоль) 3-хлор-2-фтор-6-(1-метиленетил)анізолу і 3,25 мл (26,7 ммоль) етилтрифторпірувату додають і суміш нагрівають протягом 17 годин до 140°С. Після охолодження відразу очищують колонковою хроматографією на силікагелі (пентан/простий діетиловий ефір 25-40%) і одержують 1,47 г складного етилового ефіру 4-(4-хлор-3фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)-пент-4-єнової кислоти. 1,47 г (3,97 ммоль) складного етилового ефіру 4-(4-хлор-3фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)-пент-4-єнової кислоти охолоджують в 40 мл простого діетилового ефіру до -15°С і через 10 хвилин порційно додають 300 мг (7,9 ммоль) твердого алюмогідриду літію. Перемішують 1 годину, причому суміш нагрівають до 0°С і виливають в насичений розчин хлориду амонію. Додають насичений розчин винної кислоти і перемішують 30 хвилин. Фази розділяють і багаторазово екстрагують етилацетатом. Промивають насиченим розчином хлориду натрію, сушать над сульфатом натрію, і розчинник видаляють в вакуумі. Розділення за допомогою колонкової хроматографії на силікагелі (гексан/етилацетат 0-50%) дає 0,38 г 4-(4-хлор-3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)-пент-4-еналу і 0,15 г спирту. 0,27 г 4-(4-хлор-3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)-пент-4-енал розчиняють в 14 мл метанолу і додають 0,3 мл оцтової кислоти і 27 мг палладія на вугіллі (10%-ий). Суспензію збовтують 2 години під атмосферою водню при нормальному тиску до поглинання водню в 46 мл. Суміш фільтрують крізь целіт, причому ретельно промивають повторно етилацетатом. Після видалення розчинника одержують 0,27 г 4-(4-хлор 39 3-фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)пентанал у вигляді суміші діастереомерів. 1 Н-ЯМР (300 МГц, CDCI3); = 1,18 (d, 1,5Н), 1,29 (d, 1,5Н), 2,23 (dd, 0,5Н), 2,30 (dd, 0,5Н), 2,38 (dd, 0,5Н), 2,55 (dd, 0,5Н), 3,24 (m, 1H), 3,95 (s, 3H), 6,84 (dd, 1H), 7,05 (dd, 1H), 9,18 (s, 0,5Н), 9,73 (s, 0,5Н). 100 мг (0,3 ммоль) 4-(4-хлор-3-фтор-2метокси-феніл)-2-гідрокси-2-(трифторметил)пентаналу, 48 мг (0,3 ммоль) 5-аміно-2метилхіназоліну і 0,1 мл тетраетилату титану перемішують в 9 мл толуолу 2 год. при 100°C. Після охолодження виливають на воду і енергійно перемішують. Суспензію фільтрують крізь целіт, причому ретельно повторно промивають етилацетатом. Фази фільтрату розділяють і ще раз екстрагують етилацетатом. Сушать над сульфатом натрію і розчинник видаляють в вакуумі і одержують 130 мг 4-(3-фтор-2-метокси-феніл)-1-[(2метилхінолін-5ил)іміно]-2-(трифторметил)-пентан2-олу у вигляді вихідного продукту. До 130 мг сирого іміну в 6 мл СН2СІ2 при -30°C додають по краплях 3 мл (3 ммоль) 1 Μ розчину бортриброміду. Залишають нагріватися протягом З годин до 5°С. Вихідну суміш змішують з нас. розчином NaHCO3, фази розділяють, водну фазу екстрагують етилацетатом, об'єднані органічні фази висушують (Na2SO4) і концентрують в вакуумі. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 0-75%) дає 30 мг у вигляді суміші сполуки зазначеної в заголовку і (5,6,8)3-хлор-2-фтор-8-метил-5-[(2-метилхіназолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол (прикл.23). Препаративна тонкошарова хроматографія на амінофазі (Merck) з етилацетат/метанол/триетиламін 25:3:1 дає 5 мг продукту. 1 Н-ЯМР (300 МГц, CDCI3); = 1,43 (d, 3H), 1,79 (dd, 1H), 2,42 (dd, 1H), 2,82 (s, 3H), 3,44 (qdd, 1H), 5,02 (d, 1H), 6,62 (d, 1H), 6,71 (d, 1H), 6,87 (d, 1H), 7,14 (d, 1H), 7,72 (t, 1H), 9,55 (s, 1H). Приклад 15 (5,6,8)-3-хлор-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-1-метокси-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-6-ол Аналогічно прикладу 14 піддають взаємодії 100 мг (0,3 ммоль) 4-(4-хлор-3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)пентаналу, 54 мг (0,3 ммоль) 5-аміно-7-фтор-2-метилхіназоліну і 0,1 мл тетраетилату титану до одержання 4-(4хлор-3-фтор-2-метокси-феніл)-1-[(7-фтор-2 94603 40 метилхіназолін-5ил)іміно]-2-(трифторметил)пентан-2-олу. 150 мг сирого іміну циклізують аналогічно прикладу 14 при -30°С з 2,5 мл (2,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на амінофазі (Merck) з етилацетат/метанол/триетиламін 25:3:1 дає 3,4 мг продукту і 3 мг дигідрокси сполуки прикл. 16. 1 Н-ЯМР (300 МГц, CDCI3); = 1,41 (d, 3H), 1.94 (dd, 1H), 2,45 (dd, 1H), 2,85 (s, 3H), 3,45 (ddq, 1H), 4,01 (s, 3H), 4,91 (d, 1H), 6,45 (d, 1H), 6,54 (br, 1H), 6,95 (d,1H), 7,01 (d, 1H), 9,62 (s, 1H). Приклад 16 (5,6,8)-3-хлор-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол У вигляді продукту з прикл. 15 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CDCI3); = 1,44 (d, 3H), 1,81 (dd, 1H), 2,49 (dd, 1H), 2,87 (s, 3H), 3,42 (qdd, 1H), 4,94 (d, 1H), 6,48 (d, 1H), 6,82 (d, 1H), 6,95 (d, 1H), 9,90 (s, 1H). Приклад 17 (5,6,8)-3-хлор-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно] 1-метокси-8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-6-ол Аналогічно прикладу 14 піддають взаємодії 100 мг (0,3 ммоль) 4-(4-хлор-3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-пентаналу, 53 мг (0,3 ммоль) 5-аміно-8-фтор-2-метилхіназоліну і 0,1 мл тетраетилату титану до одержання 4-(4хлор-3-фтор-2-метокси-феніл)-1-[(8-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)пентан-2-олу. 140 мг сирого іміну циклізують аналогічно прикладу 14 при -30°С с 2,5 мл (2,5 ммоль) 41 94603 42 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на амінофазі (Merck) с етилацетат/метанол/триетиламін 25:3:1 дає 3 мг продукту і 16 мг дигідрокси сполуки прикл. 18. 1 Н-ЯМР (300 МГц, CDCI3); = 1,40 (d, 3H), 1,96 (dd, 1H), 2,42 (dd, 1H), 2,93 (s, 3H), 3,45 (ddq, 1H), 4,01 (s, 3H), 5,92 (br, 1H), 6,59 (dd, 1H), 7,10 (d, 1H), 7,50 (dd, 1H), 9,60 (s, 1H). Приклад 18 (5,6,8)-3-хлор-2-фтор-8-метил-5-[-2метилхінолін-5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Приклад 21 (5,6,8)-3-хлор-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно] 8-метил-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол У вигляді продукту з прикл. 17 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CD3OD); = 1,35 (d, 3H), 1,78 (dd, 1H), 2,36 (dd, 1H), 2,75 (s, 3H), 3,28 (qdd, 1H), 5,10 (s, 1H), 6,70 (dd, 1H), 6,71 (d, 1H), 7,46 (dd, 1H), 9,52 (s, 1H). Аналогічно можуть бути одержані: Приклад 19 (5,6,8)-3-хлор-5-[(7,8-дифтор-2метилхіназолін-5-іл)аміно]-2-фтор-8-метил-6(трифторметил)-5,6,7,8-тетрагідронафталін-1,6діол і Приклад 20 5-{[(1,2,4)-7-хлор-2.5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-хінолін-2(1H)-он Аналогічно прикладу 14 піддають взаємодії 100 мг (0,3 ммоль) 4-(4-хлор-3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-пентаналу, 48 мг (0,3 ммоль) 5-амінохінолону і 0,1 мл тетраетилату титану до одержання 5-{[4-(4-хлор-3-фтор-2метокси-феніл)-2-гідрокси-2(трифторметил)пентиліден]аміно}хінолін-2(1Н)ону. 130 мг сирого іміну циклізують аналогічно прикладу 14 при -30°С з 2,5 мл (2,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на амінофазі (Merck) з етилацетат/метанол/триетиламін 25:3:1 і препаративна ВЕРХ дає 11 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,38 (d, 3H), 1,84 (dd, 1H), 2,42 (dd, 1H), 3,36 (qdd, 1H), 5,09 (s, 1H), 6,48 (d, 1H), 6,54 (d, 1H), 6,68 (d, 1H), 6,70 (d, 1H), 7,34 (t, 1H), 8,19 (d, 1H). Приклад 21А/21В 5-{[(1,2,4)-7-хлор-2,5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-хінолін-2(1H)-он розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiracel OD 20мк) в енантіомерно чисті сполуки: енантіомер 1: аналітична ВЕРХ: Rt=8,5 хв. (Chiralpak AD 5 мк, 250x4,6 мм, гексан/етанол 5%=>95% в 20 хв, 1 мл/хв. плинність) енантіомер 2: аналітична ВЕРХ: Rt=9,6 хв. (Chiralpak AD 5мк, 250x4,6 мм, 10 гексан/етанол 5%=>95% в 20 хв, 1 мл/хв. плинність) 43 Аналогічно може бути одержаний: Приклад 22 5-{[(1,2,4)-7-хлор-2,5-дигідрокси-6-фтор-4метил-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]-аміно}-8-фторхінолін2(1Н)-он Приклад 23 (5,6,8)-3-хлор-2-фтор-8-метил-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Препаративна тонкошарова хроматографія суміші діастереомерів з прикл. 14 на амінофазі (Merck) з етилацетат/метанол/триетиламін 25:3:1 дає 3 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,54 (d, 3H), 2,17 (dd, 1H), 2,30 (dd, 1H), 2,77 (s, 3H), 3,35 (m, 1H), 5,21 (s, 1H), 6,81 (d, 1H), 6,92 (d, 1H), 7,16 (d, 1H), 7,76 (t, 1H), 9,60 (s, 1H). Приклад 24 (5,6,8)-8-метил-5-[-2-метилхінолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол 2-гідрокси-4-(2-метоксифеніл)-2(трифторметил)пентанал: складний етиловий ефір 4-(3-хлор-2метоксифеніл)-2-гідрокси-2-(трифторметил)пент-4 94603 44 єнової кислоти може бути одержаний аналогічно прикладу 14 з ацетилхлориду і 2-хлорфенолу. Послідовність реакції з воднем над палладієм на вугіллі і алюмогідрид літію аналогічно прикладу 14 дає в цьому випадку суміш з 2-гідрокси-4-(2метоксифеніл)-2-(трифторметил)пентаналу і 4-(3хлор-2-метоксифеніл)-2-гідрокси-2(трифторметил)пентаналу, яка не була розділеною. Аналогічно прикладу 1 піддають взаємодії 160 мг суміші з 4-(3-хлор-2-метокси-феніл)-2гідрокси-2-(трифторметил)пентаналу і 2-гідрокси4-(2-метоксифеніл)-2-(трифторметил)пентаналу, 86 мг (0,55 ммоль) 5-аміно-2-метилхіноліну і 0,3 мл тетраетилату титану до одержання відповідних імінів. 230 мг сирого іміну циклізують аналогічно прикладу 1 при -30°С з 4 мл (4 ммоль) 1 Μ розчину бортриброміду до одержання цільових продуктів. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на силікагелі з гексан/2-пропанол 17% дозволяє розділення окремих продуктів. 1 Н-ЯМР (300 МГц, CDCI3); = 1,61 (d, 3H), 2,24 (dd, 1H), 2,33 (dd, 1H), 2,74 (s, 3H), 3,43 (qdd, 1H), 4,68 (br, 1H), 5,17 (br, 1H), 6,70 (d, 1H), 6,76 (d, 1H), 6,95 (m, 2H), 7,24 (d, 1H), 7,55 (m, 2H), 8,07 (d, 1H). Приклад 25 ZK 350663 (5,6,8)-8-метил-5-[-2-метилхінолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол У вигляді продукту з прикл. 24 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CDCI3); = 1,51 (d, 3H), 1,98 (dd, 1H), 2,48 (dd, 1H), 2,77 (s, 3H), 3,47 (m, 1H), 4,69 (d, 1H), 5,17 (d, 1H), 6,71 (d, 1H), 6,74 (d, 1H), 6,94 (m, 2H), 7,25 (d, 1H), 7,56 (m, 2H), 8,12 (d, 1H). Приклад 26 ZK 350661 45 94603 46 (5,6,8)-8-метил-5-[-2-метилхінолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол У вигляді продукту з прикл. 24 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CDCI3); 1,47 (d, 3H), 2,00 (dd, 1H), 2,47 (dd, 1H), 2,73 (s, 3H), 3,45 (m, 1H), 5,03 (d, 1H), 5,82 (br, 1H), 6,70 (d, 1H), 6,90 (d, 1H), 7,13 (d, 1H), 7,22 (d, 1H), 7,45 (d, 1H), 7,55 (t, 1H), 8,06 (d, 1H). Приклад 27 (5,6,8)-8-метил-5-[-2-метилхінолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 1 піддають взаємодії 100 мг суміші з 4-(3-хлор-2-метокси-феніл)-2-гідрокси2-(трифторметил)пентаналу і 2-гідрокси-4-(2метоксифеніл)-2-(трифторметил)пентаналу, 80 мг (0,42 ммоль) 5-аміно-7,8-дифтор-2метилхіназоліну і 0,3 мл тетраетилату титану до одержання відповідних імінів. 180 мг сирого іміну циклізують аналогічно прикладу 1 при -30°С з 4 мл (3 ммоль) 1 Μ розчину бортриброміду до одержання цільових продуктів. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на силікагелі з гексан/2пропанол 17% дає 7 мг продукту. 1 Н-ЯМР (300 МГц, CDCI3); 1,45 (d, 3H), 1,94 (dd, 1H), 2,45 (dd, 1H), 2,91 (s, 3H), 3,46 (m, 1H), 4,85 (d, 1H), 5,70 (d, 1H), 6,48 (dd, 1H), 6,83 (d, 1H), 7,09 (d, 1H), 9,23 (s, 1H). Аналогічно може бути одержаний: Приклад 28 (5,6,8)-8-етил-5-[2-метилхіназолін-5іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Приклад 29 (5,6,8)-8-етил-2-фтор-5-[(2-метилхіназолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол 4-(3-фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)гексанал: 29,04 г (3-фтор-2-метокси-феніл)-борної кислоти, 25 г 2-бром-1-бутен і тетракіс (трифенілфосфін) палладій розчиняють в 174 мл толуолу і 17,4 мл 1-пропанолу. Суміш нагрівають протягом 5 годин в закритій ємності до 120°С і після охолодження додають в воду. Водну фазу тричі екстрагують простим діетиловим ефіром, об'єднані органічні фази промивають насиченим розчином хлориду натрію і висушують над Na2SO4. Після обережно видаленого розчинника залишок очищують колонковою хроматографією на силікагелі (гексан/простий діетиловий ефір). Одержують 16,6 г (49,7%) 6-(бут-1-ен-2-іл)-2-фтороанізол. До 4,0 г (22,2 ммоль) 6-(бут-1-ен-2-іл)-2-фтороанізолу і 2,8 г молекулярного сита в 5,85 мл (44,4 ммоль) етилтрифторпірувату додають по краплях при 0°С протягом 30 хвилин 1005 мг (1,1 ммоль) [Cu(S,S)бисфеніл-оксазолін)(Н2О)2]((SbF6)2, в 56 мл дихлорметану. Перемішують реакційну суміш 16 годин при 0°С і реакційну суміш очищують за допомогою колонкової хроматографії на силікагелі (гексан/етилацетат). Одержують 7,2 г (92,6%) енантіомерно збагаченого складного етилового ефіру (R)-4-(3-фтор-2-метокси-феніл)-2-гідрокси-2(трифторметил)-гекс-4-єнової кислоти у вигляді E/Z суміші (E/Z співвідношення 2:1, Ε : прибл. 9%е, Ζ : прибл. 58%ее). 9,3 г (26,6 ммоль) складного етилового ефіру (Ε/Ζ)-4-(3-фтор-2-метокси-феніл)2-гідрокси-2-(трифторметил)-гекс-4-єнової кислоти розчиняють в 300 мл простого діетилового ефіру під аргоном і охолоджують до -15°С. 2,02 г алюмогідриду літію додають порційно за 30 хвилин у вигляді твердої речовини і перемішують протягом наступної години, причому температуру підвищують до -5°С. Після наступних 30 хвилин при -5°С додають по краплях 4 мл етилацетату і суміш перемішують ще 10 хвилин. Виливають в суміш з льоду і насиченого розчину хлориду амонію і енергійно перемішують. Фази розділяють і екстрагують багаторазово етилацетатом і простим діетиловим ефіром. Об'єднані органічні екстракти промивають насиченим розчином хлориду натрію і висушують над Na2SO4. Розчинник відганяють, і залишок очищують колонковою хроматографією на силікагелі (гексан/етилацетат). Одержують 5,9 г (72,6%) (Ε/Ζ)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2трифторметил-гекс-4-еналу і 2,0 г (Ε/Ζ)-4-(3-фтор2-метокси-феніл)-2-трифторметил-гекс-4-ен-1,2 47 діолу. 1,51 г (4,9 ммоль) (Е/Z)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)гекс-4-еналу розчиняють в 40 мл метанолу і 1,2 мл оцтової кислоти і додають 80 мг палладія на вугіллі (10%-ий). Суспензію збовтують під атмосферою водню при нормальному тиску до повної взаємодії. Суміш фільтрують крізь целіт, причому ретельно промивають повторно етилацетатом. Після видалення розчинника і розділення колонковою хроматографією на силікагелі (гексан/простий диізопропіловий ефір 10-25%) одержують 530 мг енантіомерно збагаченого (2R*,4R*)-4-(3-фтор-2-метокси-феніл)2-гідрокси-2-(трифторметил)гексаналу. 1 Н-ЯМР (300 МГц, CDCI3); = 0,77 (d, 3H), 1,65 (m, 2H), 2,32 (dd, 1H), 2,55 (dd, 1H), 3,14 (m, 1H), 3,91 (s, 3H), 3,97 (s, 1H), 6,86 (dd,1H),6,95-6,99 (m, 2H), 8,99 (s, 1H) і 620 мг енантіомерно збагаченого (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)гексаналу 1 Н-ЯМР (300 МГц, CDCI3); = 0,73 (d, 3H), 1,60 (m, 2H), 2,35 (dd, 1H), 2,43 (dd, 1H), 2,96 (m, 1H), 3,63 (s, 1H), 3,92 (s, 3H), 6,84 (dd,1H),6,93-6,99 (m, 2H), 9,67 (s, 1H). 113мг (0,37 ммоль) (2R*,4R*)-4-(3-фтор-2метоксифеніл)-2-гідрокси-2(трифторметил)гексаналу, 103 мг (0,37 ммоль) 5аміно-2-метилхіназоліну і 0,2 мл тетраетилату титану перемішують в 15 мл толуолу 1,5 год. при 100°C. Після охолодження виливають на воду і енергійно перемішують. Суспензію фільтрують крізь целіт, причому ретельно повторно промивають етилацетатом. Фази фільтрату розділяють і ще раз екстрагують етилацетатом. Сушать над сульфатом натрію і розчинник видаляють в вакуумі і одержують 178 мг (2R*,4R*)-4-(3-фтор-2метокси-феніл)-1-[(2-метилхіназолін-5ил)іміно]-2(трифторметил)гексан-2-олу у вигляді вихідного продукту. До 178 мг сирого іміну в 20 мл СН2СІ2 додають по краплях при -20°C 1,6 мл (1,6 ммоль) 1 Μ розчину бортриброміду. Залишають нагріватися до кімнатної температури і перемішують 1,5 години. Виливають в нас. розчин NaHCO3, фази розділяють, водну фазу екстрагують за допомогою СН2СІ2, об'єднані органічні фази висушують (Na2SO4) і концентрують в вакуумі. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) дає 20 мг продукту. 1 Н-ЯМР (300MHz, CD3OD); = 0,99 (t, 3H), 1,81 (ddq, 1H), 2,04 (m, 2H), 2,43 (dd, 1Н), 2,82 (s, 3H), 3,43 (dddd, 1H), 5,14 (s, 1H), 6,73 (dd,1H), 6,82 (m, 2H), 7,20 (d, 1H), 7,77 (t, 1H), 9,63 (s, 1H). Приклад 29А/29B (5,6,8)-8-етил-2-фтор-5-[(2-метилхіназолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiralpak AD 5мк) в енантіомерно чисті сполуки: (-)-енантіомер: аналітична ВЕРХ: Rt=2,58 хв. (Chiralpak AD 5мк, 250x4,6 мм, гексан/етанол 25%, 1 мл/хв. плинність) (+)-енантіомер: аналітична ВЕРХ: Rt=5,53 хв. (Chiralpak AD 5мк, 250x4,6 мм, гексан/етанол 25%, 1 мл/хв. плинність) Приклад 30А 94603 48 (5S,6R,8R)-8-етил-2-фтор-5-[(7-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол (R,R)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)гексанал: До 4,0 г (22,2 ммоль) 6-(бут-1-ен-2-іл)-2фторанізолу і 2,8 г молекулярного сита в 5,85 мл (44,4 ммоль) етилтрифторпірувату додають по краплях при 0°С за 30 хвилин 1005 мг (1,1 ммоль) [Cu(R,R)-2,2-біс(4,5-дигідро-4-трет-бутилоксазолін2-іл)пропану (H2O)2]((SbF6)2, комплекс (J. Org. Chem. 1998, 63, 4541-4544) в 56 мл дихлорметану. Перемішують реакційну суміш 16 годин при 0°С і реакційну суміш очищують за допомогою колонкової хроматографії на силікагелі (гексан/етилацетат). Одержують 7,2 г (%) складного етилового ефіру (R)-4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)-гекс-4-єнової кислоти з надлишком енантіомерів більше 90% у вигляді E/Z суміші. Аналогічно прикладу 29 одержаний таким чином ненасичений складний ефір за допомогою алюмогідриду літію i водню під палладієвим каталізом переводять в майже енантіомерно чистий альдегід. 120 мг (0,4 ммоль) (R,R)-4-(3-фтор-2метокси-феніл)-2-гідрокси-2(трифторметил)гексанал і 75 мг (0,42 ммоль) 5аміно-7-фтор-2-метилхіназоліну розчиняють в 10 мл толуолу і додають 0,1 мл (0,42 ммоль) етилату титану. Реакційну суміш нагрівають 2 години до 100°, після охолодження виливають в воду і енергійно перемішують. Суспензію фільтрують крізь целіт, причому ретельно повторно промивають етилацетатом. Фази фільтрату розділяють і ще раз екстрагують етилацетатом. Сушать над сульфатом натрію і розчинник видаляють в вакуумі і одержують 205 мг (2R,4R)-4-(3-фтор-2-метоксифеніл)-1-[(7-фтор-2-метилхінолін-5ил)іміно]-2(трифторметил)-гексан-2-олуу вигляді вихідного продукту. Сирий імін розчиняють в 18 мл СН2СІ2 і охолоджують до -40°С. 3,4 мл (3,4 ммоль) 1М розчину ВВr3 повільно додають по краплях в дихлорметан за 5 хв. і залишають нагріватися 1 годину до 0°С, через 30 хвилин при 0°С виливають в суміш з нас. NaHCO3 і льоду. Багаторазово екстрагують етилацетатом, промивають насиченим розчином NaCI і сушать над Na2SO4. Очищення колонковою хроматографією на силікагелі (150 мл) з етилацетатом дає 37 мг продукту (аналітична ВЕРХ: Rt=9,2 хв. (Chiralcel OD 5мк, 250x4,6 мм, гексан/етанол 10%, 1 мл/хв. плинність)) у вигляді (-)1 енантіомера. Н-ЯМР (300MHz, CD3OD); = 0,96 (t, 3Н), 1,76 (ddq, 1H), 2,02 (dd, 1Н), 2,06 (ddq, 1Н), 2,41 (dd, 1Н), 2,77 (s, 3Н), 3,39 (m, 1H), 5,13 (s, 1H), 49 6,58 (d,1H), 6,73 (dd, 1H), 6,77 (d, 1H), 6,88 (dd, 1H), 9,51 (s, 1H). Приклад 30В (5R,6S,8S)-8-етил-2-фтор-5-[(7-фторо-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол складний етиловий ефір 3-[1-(3-фтор-2метоксифеніл)-циклопропіл]-2-оксопропіонової кислоти: До 26 г (180 ммоль) 2,6-дифторанізолу і 14,6 мл (198 ммоль) циклопропілцианіду в 500 мл толуолу при 0°С за 40 хв. додають по краплях 396 мл 0,5 молярного (198 ммоль) розчину біс(триметилсилил)-аміду калію в толуолі. Перемішують 18 годин при кімнатній температурі і змішують при охолодженні льодом з водою і 1М сірчаної кислоти. Органічну фазу відокремлюють і водну фазу багаторазово екстрагують етилацетатом. Промивають розсолом, висушують за допомогою сульфату натрію і концентрують в вакуумі. Після хроматографічного очищення на силікагелі (гексан/етилацетат 10%-20%) одержують 12,7 г 1-(3фтор-2-метоксифеніл)-циклопропілнітрилу. 12,7 г (66,1 ммоль) нітрилу повільно змішують в толуол при -78°С з 82,7 мл (99,2 ммоль) розчин (20% в толуолі) гідриду діізобутилалюмінію і через 3 год. при -78°С додають по краплях 11,1 мл ізопропанолу. Залишають нагріватися до -5°С і додають 150 мл 10%-ого водного розчину винної кислоти. Після розведення простим ефіром сильно перемішують, органічну фазу відокремлюють і водну фазу багаторазово екстрагують етилацетатом. Промивають розсолом, висушують за допомогою сульфату натрію і концентрують в вакуумі. Одержують 11,8 г альдегіду у вигляді жовтої олії. Розчин 16,3 г (60,7 ммоль) складного етилового ефіру 2діетилфосфоно-2-етоксиоцтової кислоти в 60 мл тетрагідрофурану змішують при охолодженні льодом протягом 20 хвилин з 33,4 мл (66,8 ммоль) 2 Μ розчину диізопропіламіду літію в тетрагідрофуран-гептан-толуолі і перемішують 30 хвилин при 0°C. Протягом 30 хвилин додають по краплях розчин 11,8 г (60,7 ммоль) І в 61 мл тетрагідрофурану при 0°С. Через 20 годин при КТ додають крижану воду і багаторазово екстрагують за допомогою простого ефіру і етилацетату. Промивають насиченим розчином хлориду амонію, сушать над сульфатом натрію і концентрують. Вихідний продукт омилюють з 170 мл 2 Μ натрового лугу в 170 мл етанолу протягом 15 годин при кімнатній температурі. Одержують 13,9 г кислоти, яку перемішують з 87 мл 2 N сірчаної кислоти при 90°С протягом 16 94603 50 годин. Після охолодження підлуговують карбонатом калію, промивають за допомогою простого ефіру і підкислюють соляною кислотою. Після екстракції етилацетатом, промивання насиченим розчином хлориду натрію і видалення розчинника одержують 10,2 г сирої кетокислоти. 10,2 г (40,6 ммоль) 3-[1-(3-фтор-2-метоксифеніл)циклопропіл]-2-оксопропіонової кислоти і 4,5 мл (85,3 ммоль) сірчаної кислоти (96%-на) нагрівають в 200 мл етанолу одну годину в колбі зі зворотним холодильником. Вихідну суміш концентрують в вакуумі, залишок додають в крижану воду і підлуговують насиченим розчином гідрокарбонату натрію. Багаторазово екстрагують складним ефіром оцтової кислоти, промивають насиченим розчином хлориду натрію, висушують (сульфат натрію) і концентрують в вакуумі. Після хроматографічного очищення на силікагелі (гексан/етилацетат 20%) одержують 9,6 г складного етилового ефіру 3-[1-(3фтор-2-метоксифеніл)-циклопропіл]-2оксопропіонової кислоти. 1 Н-ЯМР (CDCI3): = 0,90 (m, 4Н), 1,29 (t, 3H), 3,09 (s, 2Н), 3,99 (d, 3H), 4,20 (q, 2H), 6,87 (ddd, 1H), 6,95 (ddd, 1H), 7,07 (d, 1H). 3-[1-(3-фтор-2-метоксифеніл)-циклопропіл]-2гідрокси-2-(трифторметил)пропанал 9,6 г (34,3 ммоль) складного етилового ефіру 3-[1-(3-фтор-2-метоксифеніл)-циклопропіл]-2оксопропіонової кислоти і 34,5 мл (233 ммоль) (трифторметил)-триметилсилану в 343 мл ДМФ змішують з 46,9 г карбонату цезію при 0°С. Перемішують 2 год. при 0°С і потім реакційну суміш додають в воду. Багаторазово екстрагують складним ефіром оцтової кислоти, промивають насиченим розчином хлориду натрію, висушують за допомогою сульфату натрію і концентрують в вакуумі. Після хроматографічного очищення на силікагелі (гексан/етилацетат 10%-40%) одержують 10,4 г складного етилового ефіру 3-[1-(3-фтор2-метоксифеніл)-циклопропіл]-2-гідрокси-2(трифторметил)-пропанової кислоти у вигляді жовтої олії. Цю олію змішують в 297 мл простого діетилового ефіру при 0°С з 2,25 г (59,4 ммоль) алюмогідриду літію і ще 1 годину перемішують при КТ. До вихідної суміші при 0°С обережно додають 20 мл насиченого розчину хлориду амонію і 15 хвилин сильно перемішують. Багаторазово екстрагують простим діетиловим ефіром, промивають насиченим розчином хлориду натрію, висушують за допомогою сульфату натрію і концентрують в вакуумі. Після хроматографічного очищення на силікагелі (гексан/етилацетат 10%-50%) одержують 5,6 г 3-[1-(3-фтор-2-метоксифеніл)-циклопропіл]-2(трифторметил)-пропан-1,2-діолу. До 5,6 г (18,1 ммоль) діолу в 100 мл дихлорметану і 61 мл ДМСО додають 12,4 мл (89 ммоль) триетиламіну і порційно за 10 хв. 11 г (70 ммоль) піридинового SO3 комплексу. Перемішують протягом 3 годин і додають насичений розчин хлориду амонію. Суміш перемішують наступні 15 хв., фази розділяють і екстрагують за допомогою дихлорметану. Промивають водою і сушать над сульфатом натрію. Розчинник видаляють в вакуумі і після хроматографічного очищення на силікагелі (гексан/етилацетат, 0-50%) одержують 5,9 г продукту. 51 Н-ЯМР (CDCI3): = 0,68-0,76 (m, 2H), 0,901,02 (m, 2H), 2,03 (d, 1H), 2,91 (d, 1Н), 3,85 (s, 1Н), 4,03 (s, 3H), 6,80 (d, 1H), 6,87 (ddd, 1H), 6,98 (dd, 1H), 9,26 (s, 1H). Аналогічно прикладу 29 з 800 мг (2,61 ммоль) 3-[1-(3-фтор-2-метоксифеніл)-циклопропіл]-2гідрокси-2-(трифторметил)пропаналу і 500 мг (2,82 ммоль) 5-аміно-7-фтор-2-метилхіназоліну одержують кількісно 1-[(7-фтор-2-метил-хиназол-5іл)іміно]-3-[1-(3-фтор-2-метоксифеніл)циклопропіл]-2-(трифторметил)пропан-2-ол. Обробка за допомогою 24 мл (24 ммоль) розчину ВBr3 і наступна дефлегмація протягом 14 годин дає 55 мг (1R,2S,Ζ) 4-етилен 6-фтор-1-[(7-фтор-2метилхіназолін-5-іл)аміно]-2-(трифторметил)1,2,3,4-тетрагідронафталін-2,5-діолу після хроматографії на силікагелі (гексан/етилацетат від 25 до 50%) і препаративної хіральної ВЕРХ на Chiracel OD-H 5мк (аналітична ВЕРХ: Rt=10,4 хв. (Chiralcel OD 10 мк, 250x4,6 мм, гексан /етанол 7%, 1 мл/хв. плинність) у вигляді (+)-енантіомера. 1 Н-ЯМР (300MHz, CD3OD); = 1,77 (d, 3H), 2,57 (d, 1H), 2,80 (s, 3H), 3,14 (d, 1Н), 4,64 (s, 1Н), 5,86 (q, 1H), 6,26 (dd, 1H), 6,77-6,97 (m, 2H), 7,02 (dd, 1H), 9,57 (s, 1H). 20 мг (1R,2S,Z) 4-етиліден-6-фтор-1-[(7-фтор2-метилхіназолін-5-іл)аміно]--2-(трифторметил)1,2,3,4-тетрагідронафталін-2,5-діол розчиняють при КТ під N2 в 1 мл етилацетату і 0,07 мл Et3N і змішують з 2 мг Pd-C (10%). Суміш збовтують 2 год. під атмосферою водню; (Н2-поглинання: 17 мл) і реакційну суміш фільтрують крізь целіт, причому ретельно піддають наступному промиванню за допомогою ЕА. Концентрують до прибл. 4 мл і перемішують 3 години з 40 мг активованого МnО2. реакційну суміш фільтрують крізь целіт, піддають наступному промиванню етилацетатом і концентрують. Препаративна тонкошарова хроматографія на силікагелі (гексан/2-пропанол 15%) дає 2 мг цільового продукту у вигляді жовтої олії. 1 Н-ЯМР (300MHz, CD3OD); = 0,96 (t, 3H), 1,76 (ddq, 1H), 2,02 (dd, 1H), 2,06 (ddq, 1Н), 2,41 (dd, 1Н), 2,77 (s, 3H), 3,39 (m, 1H), 5,13 (s, 1H), 6,58 (d,1H), 6,73 (dd, 1H), 6,77 (d, 1H), 6,88 (dd, 1H), 9,51 (s, 1H) і 1 мг іншого діастереомера. Приклад 31 1 (5,6,8)-8-етил-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Аналогічно прикладу 29 піддають взаємодії 123 мг (0,40 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)гексаналу, 72 94603 52 мг (0,60 ммоль) 5-аміно-8-фтор-2-метилхіназоліну і 0,22 мл тетраетилату титану до одержання (2R*,4R*)-4-(3-фтор-2-метокси-феніл)-1-[(8-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)гексан2-олу. 170 мг сирого іміну циклізують аналогічно прикладу 29 при -30°С з 2,8 мл (2,8 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Після хроматографічного очищення на силікагелі (дихлорметан/етилацетат 0-40%) одержують 21 мг продукту. 1 Н-ЯМР (300MHz, CD3OD); = 0,97 (t, 3H), 1,77 (m, 1H), 2,03 (dd, 1H), 2,04 (m, 1H), 2,42 (dd, 1H), 2,84 (s, 3H), 3,42 (dddd, 1H), 5,10 (s, 1H), 6,71 (dd,1H), 6,78 (dd, 1H), 6,90 (dd, 1H), 7,56 (dd, 1H), 9,63 (s, 1H). Приклад 31А/31В (5,6,8)-8-етил-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiralcel OD-Н 5мк) в енантіомерно чисті сполуки: (+)-енантіомер: аналітична ВЕРХ: Rt=4,13 хв. (Chiralcel OD-H 5мк, 250x4,6 мм, гексан/етанол 10%, 1 мл/хв. плинність) (-)-енантіомер: аналітична ВЕРХ: Rt=10,28 хв. (Chiralcel OD-H 5мк, 250x4,6 мм, гексан/етанол 10%, 1 мл/хв. плинність) Приклад 32 (5,6,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-8-етил-2-фтор-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 29 піддають взаємодії 138 мг (0,45 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-гекстаналу, 89 мг (0,45 ммоль) 5-аміно-7,8-дифтор-2метилхіназоліну і 0,24 мл тетраетилату титану до одержання (2R*,4S*)-1-[(7,8-дифтор-2метилхіназолін-5ил)іміно]-4-(3-фтор-2метоксифеніл)-2-(трифторметил)-пентан-2-олу. 210 мг сирого іміну циклізують аналогічно прикладу 29 при -30°С з 3,5 мл (3,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Після хроматографічного очищення на силікагелі (дихлорметан/етилацетат 0-40%) одержують 21 мг продукту. 1 Н-ЯМР (300MHz, CD3OD); = 0,97 (t, 3H), 1,78 (m, 1H), 2,04 (dd, 1H), 2,06 (m, 1Н), 2,42 (dd, 1Н), 2,84 (s, 3H), 3,39 (m, 1H), 5,13 (s, 1H), 6,72 (dd, 1H), 6,76 (dd, 1H), 6,90 (dd, 1H), 9,56 (s, 1H). Приклад 33 53 94603 54 1H), 3,65 (m, 1H), 3,90 (s, 3H), 4,94 (s, 1H), 6,33 (dd, 1H), 6,54 (d, 1H), 6,90-7,00 (m, 2H), 7,17 (dd, 1H), 8,17 (d, 1H). Приклад 35 5-{[1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-хінолін-2(1H)-он Аналогічно прикладу 29 піддають взаємодії 300 мг (0,97 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-гекстаналу, 132 мг (0,97 ммоль) 5-аміно-хінол-2(Н1)-ону і 0,44 мл тетраетилату титану до одержання 5{[(2R*,4S*)-4-(3-фтор-2-метокси-феніл)-2-гідрокси2-(трифторметил)гексиліден]аміно}хінолін-2(1H)ону. 250 мг сирого іміну циклізують аналогічно прикладу 29 при -20°С з 2 мл (2 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Препаративна тонкошарова хроматографія на силікагелі (гексан/2-пропанол 17%) дає 11,5 мг цільового продукту 1 Н-ЯМР (300 МГц, CD3OD); = 0,97 (t, 3H), 1,78 (m, 1H), 1,96-2,15 (m, 2H), 2,40 (dd, 1H), 3,42 (dddd, 1H), 5,03 (s, 1H), 6,49 (d, 1H), 6,53 (d, 1H), 6,70 (d, 1H), 6,75 (dd, 1H), 6,88 (dd, 1H), 7,36 (t, 1H), 8,23 (d, 1H). Приклад 34 5-{[(1,2,4)-4-етил-6-фтор-2-гідрокси-5метокси-2-(трифторметил)-1,2,3,4тетрагідронафталін-1-іл]аміно}-8-фторхінолін2(1Н)-он Аналогічно прикладу 29 конденсують 4-(3фтор-2-метоксифеніл)-2-гідрокси-2(трифторметил)гексанал і 5-аміно-8-фторхінолін2(1Н)-он до одержання 8-фтор-5-{[4-(3-фтор-2метоксифеніл)-2-гідрокси-2(трифторметил)гексиліден]аміно}хінолін-2(1H)-ону. Взаємодія з 1 Μ розчину бортриброміду після колонкової хроматографії на силікагелі (гексан/етилацетат 33-100%) і препаративної ВЕРХ дає як цільовий продукт, так і прості метилові ефіри розщеплених сполук прикладу 35 і 44. 1 Н-ЯМР (400 МГц, CD3OD); = 0,92 (t, 3H), 1,70 (m, 1H), 1,86 (m, 1H), 2,02 (dd, 1H), 2,32 (dd, 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он Як продукт з прикл. 34 після хроматографічного розділення одержують: 1 Н-ЯМР(400МГц, CD3OD); = 0,93 (t, 3H), 1,73 (m, 1H), 1,90-2,02 (m, 2H), 2,85 (dd, 1H), 3,60 (m, 1H), 4,92 (s, 1H), 6,34 (dd, 1H), 6,53 (d, 1H), 6,70 (dd, 1Η), 6,84 (dd, 1H), 7,17 (dd, 1H), 8,17 (dd, 1H). Приклад 35А/35В 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiralcel OD-H 5мк) в енантіомерно чисті сполуки: (-)-енантіомер: аналітична ВЕРХ: Rt=7,29 хв. (Chiralpak AD-H 5мк, 250x4,6 мм, гексан/етанол 5=>50% (20'), 1 мл/хв плинність) (+)-енантіомер: аналітична ВЕРХ: Rt=8,90 хв. (Chiralpak AD-H 5мк, 250x4,6 мм, гексан/етанол і 5=>50% (20 ), 1 мл/хв. плинність) Приклад 36 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2-метилфталазин-1-он Аналогічно прикладу 29 піддають взаємодії 265 мг (0,86 ммоль) 4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)гексанал, 150 мг (0,86 ммоль) 5-аміно-2-метилфталазин-1-он і 0,42 мл тетраетилату титану до одержання 5-{[4-(3-фтор2-метокси-феніл)-2-гідрокси-2(трифторметил)гексиліден]аміно}-2метилфталазин-1-ону. 410 мг сирого іміну циклізують аналогічно прикладу 29 при -20°С з 3,5 мл 55 (3,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Колонкова хроматографія на силікагелі (гексан/складний ефір оцтової кислоти 50%) і наступна препаративна тонкошарова хроматографія на силікагелі з дихлорметан/метанол 9:1 дає 10 мг продукту і 8,6 мг 8 сполуки (приклад 45). 1 Н-ЯМР (300 МГц, CD3OD); = 0,85 (t, 3H), 1,66 (m, 1H), 1,90 (dd, 1H), 1,91 (m, 1H), 2,29 (dd, 1H), 3,29 (dddd, 1H), 3,72 (s,3H), 4,89 (s, 1H), 6,63 (dd, 1H), 6,77 (dd, 1H), 6,98 (t, 1H), 7,51 (m, 2H), 8,43 (s, 1H). Аналогічно можуть бути одержані: Приклад 37 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохінолін-(2Н)-он і Приклад 38 94603 56 Одержують аналогічно прикладу 29 з відповідного (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)гексаналу. 1 Н-ЯМР (300 МГц, CD3OD); = 1,14 (t, 3H), 2,00 (m, 1H), 2,13 (m, 1H), 2,15 (dd, 1H), 2,45 (dd, 1H), 2,80 (s, 3H), 3,11 (m, 1H), 5,28 (s, 1H), 6,78 (dd, 1H), 6,89 (dd, 1H), 6,98 (d, 1H), 7,18 (d, 1H), 7,79 (t, 1H), 9,63 (s, 1H). Приклад 40 (5,6,8)-8-етил-2-фтор-5-[(7-фторо-2метилхіназолін-5-іл)аміно]-6--(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Одержують аналогічно прикладу 30 з відповідного (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)гексаналу. 1 Н-ЯМР (300 МГц, CD3SOCD3); = 1,05 (t, 3H), 1,92-1,99 (m, 2H), 2,15 (dd, 1Н), 2,25 (dd, 1Н), 2,69 (s, 3H), 2,95 (m, 1H), 5,43 (d, 1H), 6,16 (s, 1H), 6,67 (dd, 1H), 6,76 (d, 1H), 6,80 (d, 1H), 6,99 (dd, 1H), 7,23 (d, 1H), 9,61 (s, 1H), 9,69 (s, 1H). Приклад 41 5-{[(1,2,4)-4-етил-6-Фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}ізохромен-1-он Приклад 39 (5,6,8)-8-етил-2-фтор-5-[(2-метилхіназолін5-іл)аміно]-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол (5,6,8)-8-етил-2-фтор-5-[(8-фтор-2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол Аналогічно прикладу 31 піддають взаємодії 123 мг (0,40 ммоль) (2R*,4R*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)гексаналу, 72 мг (0,60 ммоль) 5-аміно-8-фтор-2-метилхіназоліну і 0,22 мл тетраетилату титану до одержання (2R*,4S*)-4-(3-фтор-2-метокси-феніл)-1-[(8-фтор-2метилхіназолін-5ил)іміно]-2-(трифторметил)гексан2-олу. 170 мг сирого іміну циклізують аналогічно прикладу 31 при -30°С з 2,8 мл (2,8 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Після хроматографічного очищення на силікагелі (дихлорметан/етилацетат 0-40%) одержують 68 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,14 (t, 3H), 1,98 (m, 1H), 2,09 - 2,15 (m, 2H), 2,43 (dd, 1Н), 2,83 57 (s, 3H), 3,10 (m, 1H), 5,21 (s, 1H), 6,77 (dd, 1H), 6,88 (dd, 1Н), 6,89 (dd, 1H), 7,57 (dd, 1H), 9,67 (s, 1H). Приклад 42 (5,6,8)-5-[(7,8-дифтор-2-метилхіназолін-5іл)аміно]-8-етил-2-фтор-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 32 піддають взаємодії 138 мг (0,45 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-гекстаналу, 89 мг (0,45 ммоль) 5-аміно-7,8-дифтор-2метилхіназоліну і 0,24 мл тетраетилату титану до одержання (2R*,4S*)-1-[(7,8-дифтор-2метилхіназолін-5ил)іміно]-4-(3-фтор-2метоксифеніл)-2-(трифторметил)-пентан-2-олу. 210 мг сирого іміну циклізують аналогічно прикладу 32 при -30°С з 3,5 мл (3,5 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Після хроматографічного очищення на силікагелі (дихлорметан/етилацетат 0-40%) одержують 41 мг продукту. 1 Н-ЯМР (300 МГц, CD3OD); = 1,14 (t, 3H), 1,96 (m, 1H), 2,09 - 2,20 (m, 2H), 2,42 (dd, 1H), 2,83 (s, 3H), 3,10 (m, 1H), 5,22 (s, 1H), 6,76 (dd, 1H), 6,86 (dd, 1H), 6,92 (dd, 1H), 9,62 (s, 1H). Приклад 43 5-{[(1,2,4)-4-етил-6-фтор-2.5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}хінолін-2(1H)-он Аналогічно прикладу 29 піддають взаємодії 300 мг (0,97 ммоль) (2R*,4S*)-4-(3-фтор-2-метоксифеніл)-2-гідрокси-2-(трифторметил)-гекстаналу, 132 мг (0,97 ммоль) 5-аміно-хінол-2(Н1)-ону і 0,44 мл тетраетилату титану до одержання 5{[(2R*,4S*)-4-(3-фтор-2-метокси-феніл)-2-гідрокси2-(трифторметил)гексиліден]аміно}хінолін-2(1Н)ону. 250 мг сирого іміну циклізують аналогічно прикладу 29 при -20°С з 2 мл (2 ммоль) 1 Μ розчину бортриброміду до одержання цільового продук 94603 58 ту. Препаративна тонкошарова хроматографія на силікагелі (гексан/2-пропанол 17%) дає 15,4 мг цільового продукту 1 Н-ЯМР (300 МГц, CD3OD); = 1,13 (t, 3H), 1,97 (m, 1H), 2,08-2,15 (m, 2H), 2,43 (dd, 1H), 3,09 (m, 1H), 5,13 (s, 1H), 6,50 (d, 1H), 6,67 (d, 1H), 6,71 (d, 1H), 6,76 (dd, 1H), 6,88 (dd, 1H), 7,38 (t, 1H), 8,23 (d, 1H). Приклад 44 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он Як продукт з прикл. 34 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CD3OD); = 1,07 (t, 3H), 1,90 (m, 1H), 2,00-2,13 (m, 2H), 2,17 (s, 1H), 2,37 (dd, 1H), 3,04 (m, 1H), 4,99 (s, 1H), 6,50 (d, 1H), 6,55 (dd, 1H), 6,68 (dd, 1H), 6,85 (dd, 1H), 7,18 (dd, 1H), 7,43 (d, 1H), 8,15 (dd, 1H). Приклад 44А/44В 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-8-фторхінолін-2(1H)-он розщеплюється за допомогою препаративної хіральної ВЕРХ (Chiralcel OD-H 5мк) в енантіомерно чисті сполуки: (-)-енантіомер: аналітична ВЕРХ: Rt=7,53 хв. (Chiralpak AD-H 5мк, 250x4,6 мм, гексан/етанол 5=>50% (20'), 1 мл/хв. плинність) (+)-енантіомер: аналітична ВЕРХ: Rt=10,10 хв. (Chiralpak AD-H 5мк, 250x4,6 мм, гексан/етанол 5=>50% (20'), 1 мл/хв. плинність) Приклад 45 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-2-метилфталазин-1-он Як продукт з прикл. 36 після хроматографічного розділення одержують: 59 Н-ЯМР (300 МГц, CD3OD); = 1,01 (t, 3H), 1,83 (m, 1H), 2,00 (m, 1H), 2,02 (dd, 1H), 2,30 (dd, 1H), 2,97 (m, 1H), 3,70 (s, 3H), 5,08 (s, 1H), 6,63 (dd, 1H), 6,77 (dd, 1H), 7,15 (dd, 1H), 7,51 (d, 1H), 7,52 (d, 1H), 8,44 (s, 1H). Аналогічно можуть бути одержані: Приклад 46 1 94603 60 мл (2,4 ммоль) 1 Μ розчину бортриброміду до одержання цільового продукту. Після хроматографічного очищення на силікагелі (етилацетат) одержують 4 мг цільового продукту і 11 мг 8 сполуки (приклад 49). 1 Н-ЯМР (300 МГц, CD3OD); = 0,99 (t, 3H), 1,46 (t,3H), 1,80 (m, 1H), 2,04 (dd, 1H), 2,05 (m, 1H), 2,43 (dd, 1H), 3,08 (q, 2H), 3,42 (dddd, 1H), 5,17 (s, 1H), 6,77 (dd, 1H), 6,81 (d, 1H), 6,89 (dd, 1H), 7,22 (d, 1H), 7,78 (t, 1H), 9,64 (s, 1H). Приклад 49 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}-ізохінолін-(2Н)-он і Приклад 47 (5,6,8)-5-[(2-етилхіназолін-5-іл)аміно]-2фтор-8-пропіл-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Як продукт з прикл. 36 після хроматографічного розділення одержують: 1 Н-ЯМР (300 МГц, CD3OD); = 0,14 (t, 3H), 1,45 (t,3H), 2,00 (m, 1H), 2,13 (, 1H), 2,15 (dd, 1H), 2,46 (dd, 1H), 3,07 (q, 2H), 3,10 (m, 1H), 5,28 (s, 1H), 6,78 (dd, 1H), 6,89 (dd, 1H), 6,98 (d, 1H), 7,21 (d, 1H), 7,79 (t, 1H), 9,66 (s, 1H). Приклад 50 5-{[(1,2,4)-4-етил-6-фтор-2,5-дигідрокси-2(трифторметил)-1,2,3,4-тетрагідронафталін-1іл]аміно}ізохромен-1-он Приклад 48 (5,6,8)-5-[(2-етилхіназолін-5-іл)аміно]-2фтор-8-пропіл-6-(трифторметил)-5,6,7,8тетрагідронафталін-1,6-діол Аналогічно прикладу 31 піддають взаємодії 112 мг (0,37 ммоль) (4-(3-фтор-2-метоксифеніл)-2гідрокси-2-(трифторметил)гексаналу, 60 мг (0,37 ммоль) 5-аміно-2-етилхіназоліну і 0,2 мл тетраетилату титану до одержання 1-[(2-етилхіназолін5ил)іміно]-4-(3-фтор-2-метоксифеніл)-2(трифторметил)гексан-2-олу. 280 мг сирого іміну циклізують аналогічно прикладу 31 при -20°С з 2,4 (5S,6R,8R)-8-етил-2,3-дифтор-5-[(2метилхіназолін-5-іл)аміно]-6-(трифторметил)5,6,7,8-тетрагідронафталін-1,6-діол 4-(3,4-дифтор-2-метокси-феніл)-2-гідрокси-2(трифторметил)-гексанал: До 20 г (153,7 ммоль) 2,3-дифторфенолу в 150 мл дихлорметану і 17,5 мл піридину при 0°С додають по краплях 14 мл (161 ммоль) хлориду пропіонової кислоти. Перемішують суміш протягом двох годин і додають 100 мл 2Μ соляної кислоти. Екстрагують за допомогою дихлорметану і промивають водою. Після висушування над сульфатом натрію і видалення розчинника в вакуумі одержують 30,1 г 2,3-дифторфенілового складного ефіру пропіонової кислоти. 30,1 г (161 ммоль) 2,3дифторфенілового складного ефіру пропіонової
ДивитисяДодаткова інформація
Назва патенту англійськоюTetrahydronaphthaline derivatives, methods for the production and use thereof as anti-inflammatory agents
Автори англійськоюBerger Markus, Schmees Norbert, Schaecke Heike, Baeurle Stefan, Rehwinkel Hartnut
Назва патенту російськоюПроизводные тетрагидронафталина, способ их получения и их применения в качестве ингибиторов воспаления
Автори російськоюБергер Маркус, Ревинкель Хартмут, Шьокке Хайке, Бойерле Штефан, Шмеес Норберт
МПК / Мітки
МПК: A61K 31/47, C07D 215/38, A61K 31/517, C07D 265/02, A61K 31/502, C07D 237/32, C07D 311/76, C07D 215/60, A61P 29/00, C07D 209/34, C07D 231/56, C07D 217/24, C07D 239/74, C07D 215/22
Мітки: застосування, одержання, похідні, спосіб, інгібіторів, тетрагідронафталіну, запалення
Код посилання
<a href="https://ua.patents.su/86-94603-pokhidni-tetragidronaftalinu-sposib-kh-oderzhannya-ta-kh-zastosuvannya-yak-ingibitoriv-zapalennya.html" target="_blank" rel="follow" title="База патентів України">Похідні тетрагідронафталіну, спосіб їх одержання та їх застосування як інгібіторів запалення</a>
Попередній патент: Інгібітори вірусної полімерази
Наступний патент: Нейрозахисна сполука dlhw та її застосування
Випадковий патент: Біологічно активна фітодобавка "наркомед"