Противірусні сполуки проти rsv
Номер патенту: 114531
Опубліковано: 26.06.2017
Автори: Вендевілль Сандрін Марі Елен, Демен Самюель Домінік, Коіманс Людвіг Поль, Тахрі Абделлах, Рабуассон П'єр Жан-Марі Бернар, Йонкерс Тім Хьюго Марія, Ху Лілі
Формула / Реферат
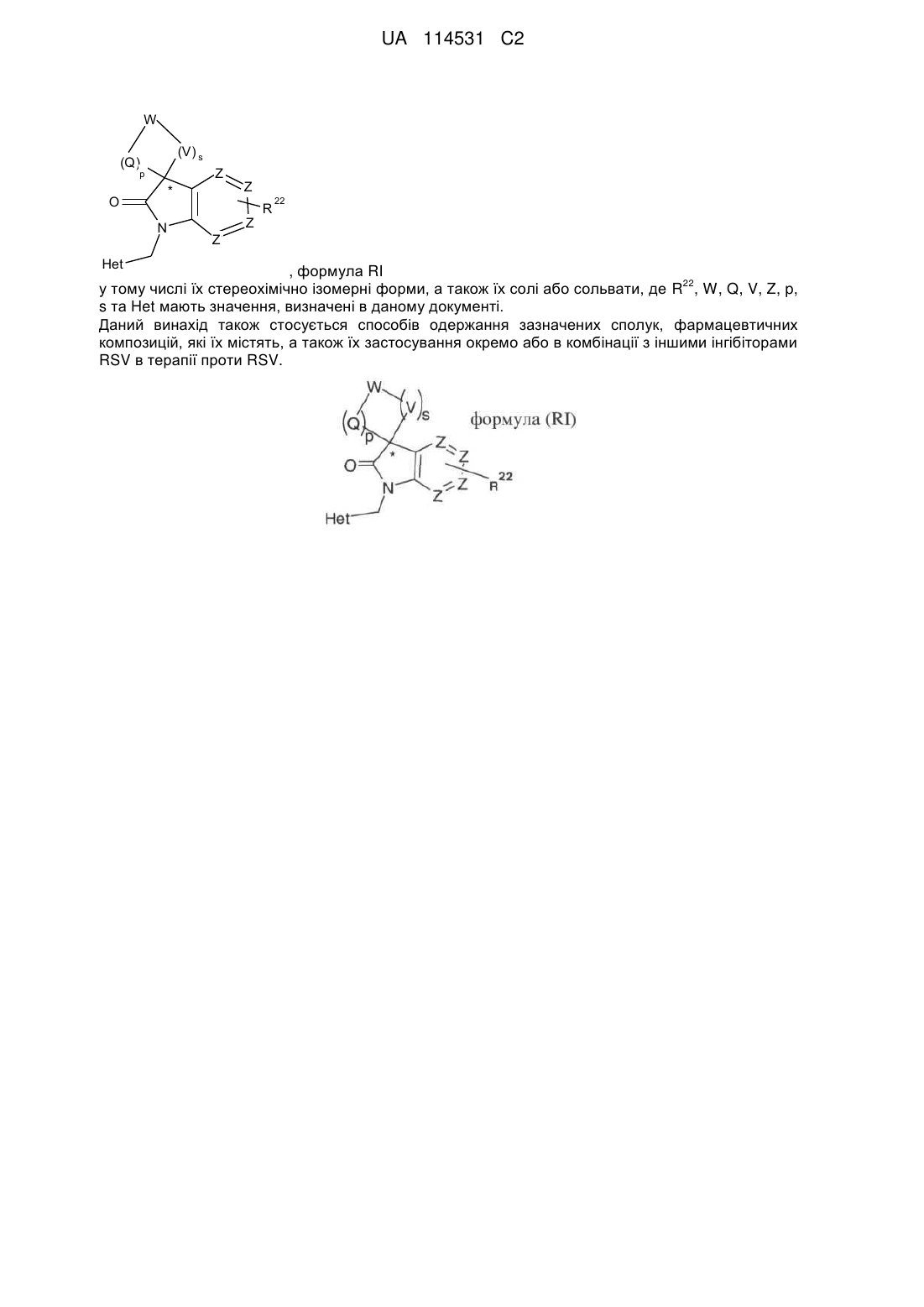
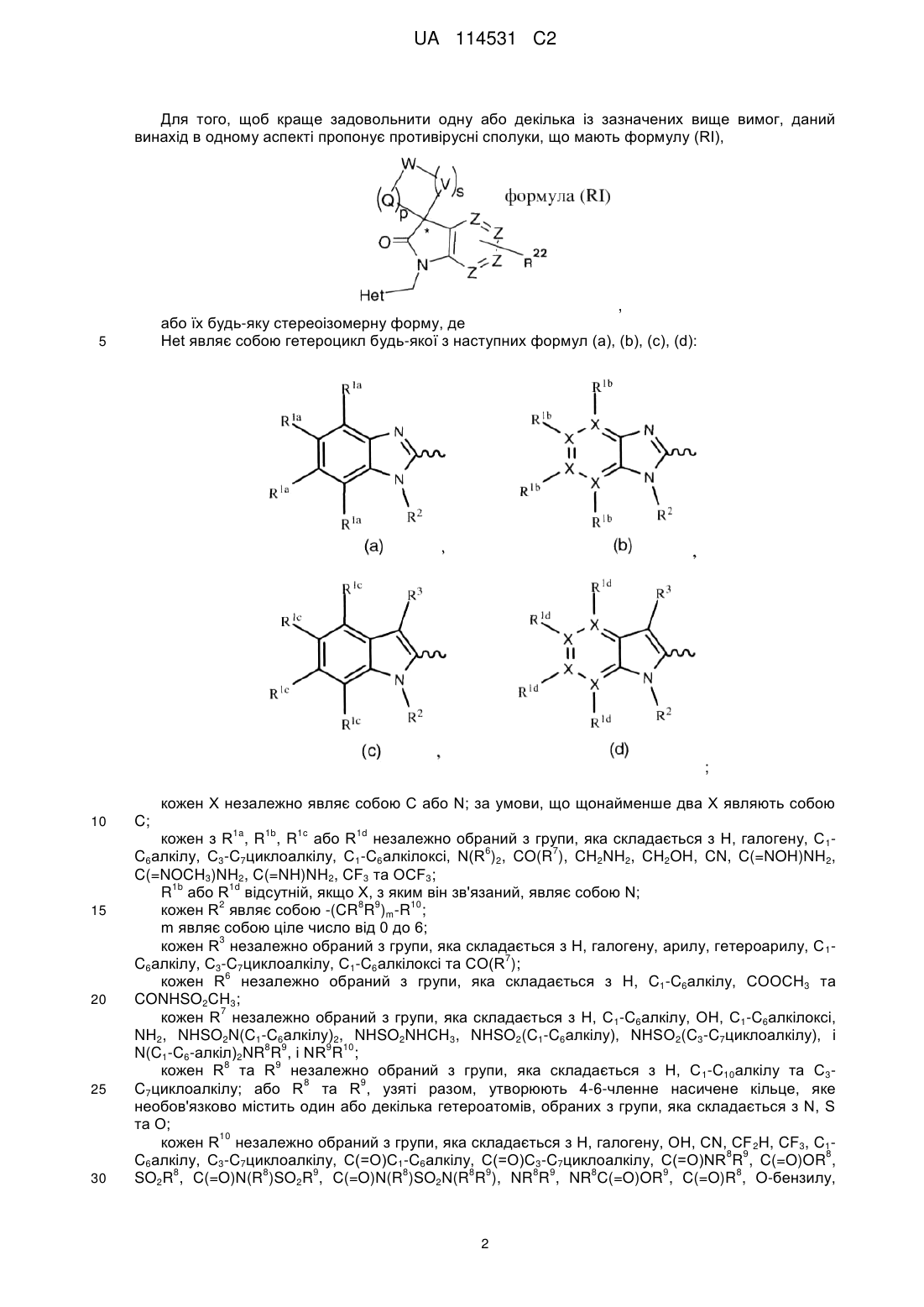
1. Сполука формули (RI)
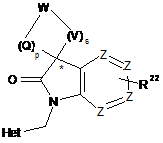 формула RI
формула RI
або її будь-яка стереоізомерна форма, де
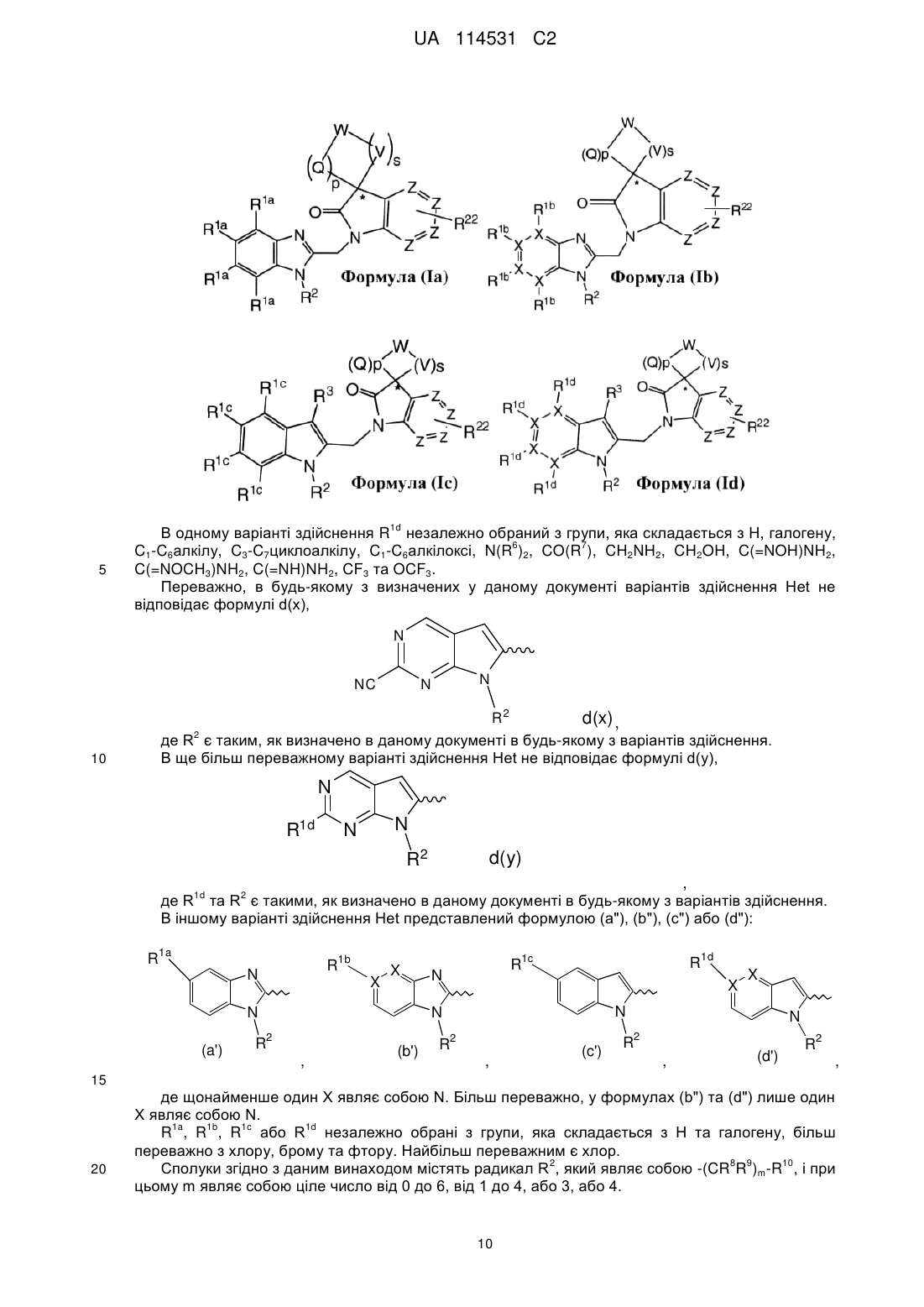
Het являє собою гетероцикл будь-якої з наступних формул (a), (b), (c), (d):

кожен X незалежно являє собою С або N, за умови, що щонайменше два X являють собою С;
кожен з R1a, R1b, R1c або R1d незалежно вибраний з групи, яка складається з Н, галогену, С1-С6алкілу, С3-С7циклоалкілу, С1-С6алкілокси, N(R6)2, CO(R7), CH2NH2, СН2ОН, CN, C(=NOH)NH2, C(=NOCH3)NH2, C(=NH)NH2, CF3 та OCF3;
R1b або R1d відсутній, якщо Х, з яким він зв'язаний, являє собою N;
кожен R2 являє собою -(CR8R9)m-R10;
m являє собою ціле число від 0 до 6;
кожен R3 незалежно вибраний з групи, яка складається з Н, галогену, арилу, гетероарилу, С1-С6алкілу, С3-С7циклоалкілу, С1-С6алкілокси та CO(R7);
кожен R6 незалежно вибраний з групи, яка складається з Н, С1-С6алкілу, СООСН3 та CONHSO2CH3;
кожен R7 незалежно вибраний з групи, яка складається з Н, С1-С6алкілу, ОН, С1-С6алкілокси, NH2, NHSO2N(С1-С6алкілу)2, NHSO2NHCH3, NНSО2(С1-С6алкілу), NHSO2(С3-С7циклоалкілу), N(C1-C6aлкiл)2NR8R9 і NR9R10;
кожен R8 та R9 незалежно вибраний з групи, яка складається з Н, С1-С10алкілу та С3-С7циклоалкілу; або R8 та R9, узяті разом, утворюють 4-6-членне насичене кільце, яке необов'язково містить один або декілька гетероатомів, вибраних з групи, яка складається з N, S та О;
кожен R10 незалежно вибраний з групи, яка складається з Н, галогену, ОН, CN, CF2H, CF3, С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, C(=O)NR8R9, C(=O)OR8, SO2R8, C(=O)N(R8)SO2R9, C(=O)N(R8)SO2N(R8R9), NR8R9, NR8C(=O)OR9, OC(=O)R8, О-бензилу, NR8SO2R9, SO2NR8R9, SO2R8, OC(=O)NR8R9, OC(=O)NR8R12, N(R8)C(=O)N(R8R9), R11, N(R8)C(=O)OR12, OR11, C(=O)R11 та 4-6-членного насиченого кільця, яке містить один атом кисню;
R11 являє собою феніл, піридиніл або піразоліл, кожен з яких може бути необов'язково заміщений одним або декількома замісниками, кожен з яких незалежно вибраний з групи, яка складається з CF3, СН3, ОСН3, OCF3 та галогену;
R12 являє собою С1-С6алкіл або С3-С7циклоалкіл; кожен з яких заміщений одним або декількома замісниками, кожен з яких незалежно вибраний з групи, яка складається з CF3, CH3, ОСН3, OCF3 та галогену;
кожен Z незалежно являє собою С або N, за умови, що щонайменше два Z являють собою С;
кожен з Q та V незалежно являє собою С=О, SO2 або CR20R21;
р та s незалежно являють собою ціле число від 0 до 3, де сума р та s повинна дорівнювати щонайменше 2, і, якщо р=0 або s=0, тоді атом вуглецю, позначений *, безпосередньо зв'язаний з W;
R20 та R21 незалежно вибрані з групи, яка складається з водню, гідроксилу, С1-С3алкілу, С3-С7циклоалкілу, CF3, ОСН3, OCF3 та галогену;
R22 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, С3-С7циклоалкілу, СF3, ОСН3, OCF3 та галогену;
W вибраний з групи, яка складається з SO, SO2, S, С, О та N, де такий С або N необов'язково заміщений одним або декількома R23;
R23 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, С3-С7циклоалкілу, С1-С6алкіл-R24, SO2R24, SO2N(R24)2, арилу, гетероарилу, C(=O)OR24, OR24, C(=O)R24, C(=O)N(R24)2, OC(=O)N(R24)2, P(=O)-(O-C1-C6алкілу)2, N(R24)2, NR25C(=O)OR24, NR25C(=O)N(R24)2, NR25SO2R24 та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-С6алкілу, С3-С7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, ОН, CN, ОСН3;
R24 вибраний з групи водню, ОН, галогену, С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, CF3, OH, CN, ОСН3, ОС(=О)СН3 та С1-С3алкілу, заміщеного щонайменше одним CN;
R25 вибраний з групи, яка складається з водню та С1-С3алкілу;
арил являє собою феніл або нафталініл;
гетероарил являє собою моноциклічний 5-6-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно вибраний з групи, яка складається з О, S та N; або біциклічний 8-12-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно вибраний з групи, яка складається з О, S та N;
за умови, що Het не відповідає формулі d(x)
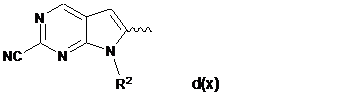
або її фармацевтично прийнятна сіль приєднання або сольват.
2. Сполука формули (RI) за п. 1 або її будь-яка стереоізомерна форма, де
Het являє собою гетероцикл будь-якої з наступних формул (a), (b), (c), (d):

кожен X незалежно являє собою С або N, за умови, що щонайменше два X являють собою С;
кожен з R1a, R1b, R1c або R1d незалежно вибраний з групи, яка складається з Н, галогену, С1-С6алкілу, С1-С6алкілокси, CF3 та OCF3;
R1b або R1d відсутній, якщо X, з яким він зв'язаний, являє собою N;
кожен R2 являє собою -(CR8R9)m-R10;
m являє собою ціле число від 2 до 6;
кожен R3 являє собою Н, галоген або С1-С6алкіл;
кожен R8 та R9 незалежно вибраний з групи, яка складається з H та С1-С10алкілу;
кожен R10 незалежно вибраний з групи, яка складається з Н, галогену, ОН, CN, CF2H, CF3, С1-С6алкілу, С3-С7циклоалкілу, C(=O)NR8R9, C(=O)OR8 та SO2R8;
кожен Z незалежно являє собою С або N, за умови, що щонайменше два Z являють собою С;
кожен з Q та V незалежно являє собою CR20R21;
р та s незалежно являють собою ціле число від 0 до 3, де сума р та s повинна дорівнювати щонайменше 2, і, якщо р=0 або s=0, тоді атом вуглецю, позначений *, безпосередньо зв'язаний з W;
R20 та R21 являють собою водень;
R22 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, CF3, ОСН3, OCF3 та галогену;
W вибраний з групи, яка складається з SO2, С, О та N, де такий С або N необов'язково заміщений одним або декількома R23;
R23 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, С3-С7циклоалкілу, С1-С6алкіл-R24, SO2R24, SO2N(R24)2, арилу, гетероарилу, C(=O)OR24, OR24, C(=O)R24, C(=O)N(R24)2, OC(=O)N(R24)2, P(=O)-(O-C1-C6алкілу)2, N(R24)2, NR25C(=O)OR24, NR25C(=O)N(R24)2, NR25SO2R24 та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких С1-С6алкілу, С3-С7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, ОН, CN, ОСН3;
R24 вибраний з групи водню, ОН, галогену, С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, CF3, OH, CN, ОСН3, ОС(=О)СН3 та С1-С3алкілу, заміщеного щонайменше одним CN;
R25 вибраний з групи, яка складається з водню та С1-С3алкілу;
арил являє собою феніл або нафталініл;
гетероарил являє собою фураніл, тіофеніл, піридиніл, піридазиніл, піримідиніл, піразиніл, хіноксалініл або бензімідазоліл;
або її фармацевтично прийнятна сіль приєднання або сольват.
3. Сполука за п. 2, де R23 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, С3-С7циклоалкілу, С1-С6алкіл-R24, SO2R24, SO2N(R24)2, арилу, гетероарилу, C(=O)OR24, OR24, C(=O)R24, C(=O)N(R24)2, OC(=O)N(R24)2 та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких С1-С6алкілу, С3-С7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, ОН, CN, ОСН3;
R24 вибраний з групиводню, ОН, галогену, С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких С1-С6алкілу, С3-С7циклоалкілу, С(=О)С1-С6алкілу, С(=О)С3-С7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, вибраними з групи, яка складається з галогену, CF3, OH, CN, ОСН3 та ОС(=О)СН3.
4. Сполука формули (RI) за п. 1, де Het представлений формулою (а'), (b'), (с') або (d'):
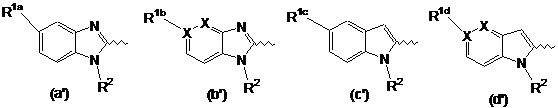
де щонайменше один X являє собою N;
a R1a, R1b, R1c, R1d та R2 визначені у п. 1.
5. Сполука за будь-яким з попередніх пунктів, де у формулах (b') та (d') один X являє собою N.
6. Сполука за будь-яким з попередніх пунктів, де кожен з R1a, R1b, R1c або R1d незалежно вибраний з групи, яка складається з Н та галогену.
7. Сполука за будь-яким з попередніх пунктів, де кожен з R1a, R1b, R1c або R1d незалежно вибраний з групи, яка складається з хлору, брому та фтору.
8. Сполука за п. 4, де кожен з R1a, R1b, R1c або R1d являє собою хлор.
9. Сполука за будь-яким з попередніх пунктів, де R2 являє собою -(CR8R9)m-R10, і де m являє собою ціле число від 1 до 4, а кожен R8 та R9 незалежно вибраний з Н або С1-С6алкілу.
10. Сполука за будь-яким з попередніх пунктів, де R2 являє собою С1-С6алкіл-R10.
11. Сполука за будь-яким з попередніх пунктів, де R10 вибраний з групи, яка складається з С1-С3алкілу, Н, ОН, CN, F, CF2H, CF3, SО2-С1-С3алкілу та SO2C3-С6циклоалкілу.
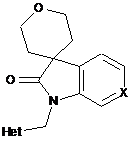
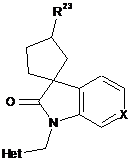
12. Сполука за будь-яким з попередніх пунктів, де сполука характеризується формулою RII, RIII, RIV, RV, RVI або RVII:
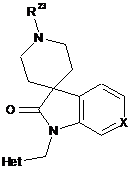 ,
,
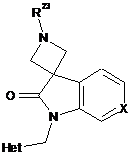 ,
,
 ,
,
формула RII
формула RIII
формула RIV
 ,
,
 ,
,
 ,
,
формула RV
формула RVI
формула RVII
або її будь-яка стереоізомерна форма, де Het, X та R23 визначені в будь-якому з попередніх пунктів.
13. Сполука за п. 12, де R23 вибраний з групи, яка складається з водню, гідроксилу, С1-С6алкілу, С1-С3алкіл-R24, SO2R24, O-R24, фенілу, піридинілу, піримідилу, піразолілу, C(=O)OR24, C(=O)R24, при цьому будь-який з таких С1-С6алкілу, фенілу, піридинілу, піримідилу, піразолілу необов'язково заміщений одним або декількома з наступних замісників: ОСН3, галоген, ОН або CN.
14. Сполука за п. 1, де сполука являє собою
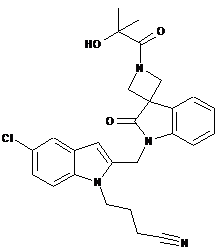 ,
,
або її фармацевтично прийнятна сіль приєднання або сольват.
15. Сполука за будь-яким з пп. 1-14 для застосування як лікарського засобу.
16. Фармацевтична композиція, яка містить фармацевтично прийнятний носій і терапевтично ефективну кількість сполуки за будь-яким з пп. 1-14 як активний інгредієнт.
17. Сполука за будь-яким з пп. 1-14 або фармацевтична композиція за п. 16 для застосування в лікуванні інфекції, спричинюваної респіраторним синцитіальним вірусом.
18. Спосіб лікування вірусних RSV-інфекцій у суб'єкта, що потребує цього, який включає введення зазначеному суб'єкту ефективної кількості сполуки за будь-яким з пп. 1-14.
Текст
Реферат: Інгібітори реплікації RSV формули RI (72) Винахідник(и): Тахрі Абделлах (BE), Вендевілль Сандрін Марі Елен (BE), Йонкерс Тім Х'юго Марія (BE), Рабуассон П'єр Жан-Марі Бернар (BE), Ху Лілі (BE), Демен Самюель Домінік (BE), Коіманс Людвіг Поль (BE) (73) Власник(и): ЯНССЕН САЙЄНСІЗ АЙРЛЕНД ЮСі, Eastgate Village, Eastgate, Little Island, Co Cork, Ireland (IE) (74) Представник: Мошинська Ніна Миколаївна, реєстр. №115 (56) Перелік документів, взятих до уваги експертизою: WO 2012/080449 A1, 21.06.2012 COMBRINK ET AL, "Respiratory syncytial virus fusion inhibitors. Part 6: An examination of the effect of structural variation of the benzimidazol-2-one heterocycle moiety", BIOORGANIC & MEDICINAL CHEMISTRY LETTERS, PERGAMON, ELSEVIER SCIENCE, GB, (2007-08-04), vol. 17, no. 17, pages 4784-4790 UA 114531 C2 МІНІСТЕРСТВО ЕКОНОМІЧНОГО РОЗВИТКУ І ТОРГІВЛІ УКРАЇНИ UA 114531 C2 W (V) s (Q) Z p * O N Het Z Z R 22 Z , формула RI 22 у тому числі їх стереохімічно ізомерні форми, а також їх солі або сольвати, де R , W, Q, V, Z, p, s та Het мають значення, визначені в даному документі. Даний винахід також стосується способів одержання зазначених сполук, фармацевтичних композицій, які їх містять, а також їх застосування окремо або в комбінації з іншими інгібіторами RSV в терапії проти RSV. UA 114531 C2 5 10 15 20 25 30 35 40 45 50 55 Галузь винаходу Даний винахід стосується нових спіросполук, які мають противірусну активність, зокрема, які мають інгібіторну активність стосовно реплікації респіраторного синцитіального вірусу (RSV). Даний винахід додатково стосується одержання таких нових сполук, композицій, які містять дані сполуки, а також сполук для застосування у лікуванні інфекції, спричинюваної респіраторним синцитіальним вірусом. Рівень техніки RSV людини, або респіраторний синцитіальний вірус, являє собою великий РНК-вмісний вірус, що входить до родини Paramyxoviridae, підродини Pneumoviridae, разом з респіраторним синцитіальним вірусом великої рогатої худоби. RSV людини спричиняє ряд захворювань дихальних шляхів у людей будь-якого віку в усьому світі. Він є основною причиною захворювань нижніх дихальних шляхів у немовлячому віці та дитинстві. Більше половини всіх немовлят стикаються з RSV у свій перший рік життя та майже всі протягом своїх перших двох років. Інфекція у маленьких дітей може призводити до ушкодження легень, яке зберігається роками та може сприяти розвитку хронічного захворювання легень у подальшому житті (хронічна бронхолегенева обструкція, астма). Підлітки та дорослі часто страждають на (сильний) нежить під час RSV-інфекції. У старості схильність знову зростає, та RSV був залучений у багато спалахів пневмонії у літніх людей, що призводило до істотної смертності. Інфікування вірусом з даної підгрупи не захищає від подальшого інфікування ізолятом RSV з тієї ж підгрупи у наступний зимовий період. Повторне інфікування RSV, таким чином, є поширеним, незважаючи на існування лише двох підтипів, A та B. На даний момент були схвалені лише три лікарські препарати для застосування проти RSVінфекції. Першим є рибавірин, нуклеозидний аналог, що забезпечує аерозольний спосіб лікування важкої RSV-інфекції у шпиталізованих дітей. Аерозольний шлях введення, токсичність (ризик тератогенного впливу), вартість та вкрай мінлива ефективність обмежують його застосування. Інші два лікарські препарати, RespiGam® (RSV-IG) та Synagis® (палівізумаб), імуностимулятори на основі поліклональних та моноклональних антитіл, призначені для профілактичного застосування. Обидва є дуже дорогими та потребують парентерального введення. Інші спроби створення безпечної та ефективної вакцини проти RSV до цього часу зазнавали невдачі. Інактивовані вакцини були не здатні захистити від захворювання та фактично у деяких випадках ускладнювали перебіг захворювання в умовах подальшого інфікування. Живі ослаблені вакцини були апробовані з обмеженим успіхом. Очевидно, що існує потреба у ефективному, нетоксичному та простому в застосуванні лікарському препараті, що пригнічує реплікацію RSV. Буде особливо переважним одержати лікарські препарати, що пригнічують реплікацію RSV, які можуть бути введені перорально. Літературним джерелом щодо залежності активності від структури у 5-заміщених сполук бензімідазолу стосовно інгібування RSV є X.A. Wang et al., Bioorganic and Medicinal Chemistry Letters 17 (2007) 4592-4598. Сполуки, що проявляють активність проти RSV, розкриті у WO 2012/080446, WO 2012/080447, WO 2012/080449, WO 2012/080450 та WO 2012/080451. У WO-2004/069256 розкриті 2-ціанопіролопіримідини, а у WO-2004/076455 розкриті спірозаміщені 2-ціанопіролопіримідини як інгібітори катепсину K або S, що застосовуються у лікуванні різних больових розладів. Teno N. et al. у Bioorganic & Medicinal Chemistry Letters, vol. 17, 6096-6100 (2007) та Teno N. et al. у J. Med. Chem., vol. 51, 5459-5462 (2008) розкривають 2ціанопіролопіримідини як інгібітори катепсину K. Потенційними проблемами, з якими можна стикатись у разі використання противірусних препаратів проти RSV, є токсичність, мутагенність, недостатня селективність, слабка ефективність, слабка біодоступність та складність синтезу. Бажано одержати нові сполуки, що мають противірусну активність. Зокрема, бажано було б одержати нові лікарські препарати, що мають інгібіторну активність стосовно реплікації RSV. Крім того, бажано було б знайти структури сполук, що дозволяють одержання засобів з противірусними біологічними активностями такого порядку величини, як відомо для найбільш релевантних галузей техніки, та переважно на рівні приблизно найактивніших сполук, розкритих у рівні техніки, більш переважно навіть із сильнішою активністю, ніж у них. Також бажано знайти сполуки, що мають противірусну активність у випадку перорального застосування. Існує потреба у додаткових інгібіторах RSV, які можуть долати щонайменше один з цих недоліків або мати один з бажаних ефектів. Короткий опис винаходу 1 UA 114531 C2 Для того, щоб краще задовольнити одну або декілька із зазначених вище вимог, даний винахід в одному аспекті пропонує противірусні сполуки, що мають формулу (RI), , або їх будь-яку стереоізомерну форму, де Het являє собою гетероцикл будь-якої з наступних формул (a), (b), (c), (d): 5 ; кожен X незалежно являє собою C або N; за умови, що щонайменше два X являють собою 10 15 20 25 30 C; 1a 1b 1c 1d кожен з R , R , R або R незалежно обраний з групи, яка складається з H, галогену, C 16 7 C6алкілу, C3-C7циклоалкілу, C1-C6алкілоксі, N(R )2, CO(R ), CH2NH2, CH2OH, CN, C(=NOH)NH2, C(=NOCH3)NH2, C(=NH)NH2, CF3 та OCF3; 1b 1d R або R відсутній, якщо X, з яким він зв'язаний, являє собою N; 2 8 9 10 кожен R являє собою -(CR R )m-R ; m являє собою ціле число від 0 до 6; 3 кожен R незалежно обраний з групи, яка складається з H, галогену, арилу, гетероарилу, C 17 C6алкілу, C3-C7циклоалкілу, C1-C6алкілоксі та CO(R ); 6 кожен R незалежно обраний з групи, яка складається з H, C1-C6алкілу, COOCH3 та CONHSO2CH3; 7 кожен R незалежно обраний з групи, яка складається з H, C1-C6алкілу, OH, C1-C6алкілоксі, NH2, NHSO2N(C1-C6алкілу)2, NHSO2NHCH3, NHSO2(C1-C6алкілу), NHSO2(C3-C7циклоалкілу), і 8 9 9 10 N(C1-C6-алкіл)2NR R , і NR R ; 8 9 кожен R та R незалежно обраний з групи, яка складається з H, C 1-C10алкілу та C38 9 C7циклоалкілу; або R та R , узяті разом, утворюють 4-6-членне насичене кільце, яке необов'язково містить один або декілька гетероатомів, обраних з групи, яка складається з N, S та O; 10 кожен R незалежно обраний з групи, яка складається з H, галогену, OH, CN, CF 2H, CF3, C18 9 8 C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, C(=O)NR R , C(=O)OR , 8 8 9 8 8 9 8 9 8 9 8 SO2R , C(=O)N(R )SO2R , C(=O)N(R )SO2N(R R ), NR R , NR C(=O)OR , C(=O)R , O-бензилу, 2 UA 114531 C2 8 5 10 15 20 25 30 35 40 9 8 9 8 8 9 8 12 8 8 9 11 NR SO2R , SO2NR R , SO2R , C(=O)NR R , C(=O)NR R , N(R )C(=O)N(R R ), R , 8 12 11 11 N(R )C(=O)OR , OR , C(=O)R та 4-6-членного насиченого кільця, яке містить один атом кисню; 11 R являє собою феніл, піридиніл або піразоліл; кожен з яких може бути необов'язково заміщеним одним або декількома замісниками, кожен з яких незалежно обраний з групи, яка складається з CF3, CH3, OCH3, OCF3 та галогену; 12 R являє собою C1-C6алкіл або C3-C7циклоалкіл; кожен з яких заміщений одним або декількома замісниками, кожен з яких незалежно обраний з групи, яка складається з CF 3, CH3, OCH3, OCF3 та галогену; кожен Z незалежно являє собою C або N, за умови, що щонайменше два Z являють собою C; 20 21 кожен з Q та V незалежно являє собою C=O, SO2 або CR R ; p та s незалежно являють собою ціле число від 0 до 3, де сума p та s повинна дорівнювати щонайменше 2, і якщо p=0 або s=0, тоді атом вуглецю, позначений *, безпосередньо зв'язаний з W; 20 21 R та R незалежно обрані з групи, яка складається з водню, гідроксилу, C 1-C3алкілу, C3C7циклоалкілу, CF3, OCH3, OCF3 та галогену; 22 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C3-C7циклоалкілу, CF3, OCH3, OCF3 та галогену; W обраний з групи, яка складається з SO, SO 2, S, C, O та N, де такий C або N необов'язково 23 заміщений одним або декількома R ; 23 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C3-C7циклоалкілу, C124 24 24 24 24 24 C6алкіл-R , SO2R , SO2N(R )2, арилу, гетероарилу, C(=O)OR , OR , C(=O)R , 24 24 24 25 24 25 24 C(=O)N(R )2, °C(=O)N(R )2, P(=O)-(O-C1-C6-алкілу)2, N(R )2, NR C(=O)OR , NR C(=O)N(R )2, 25 24 NR SO2R та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, OH, CN, OCH3; 24 R обраний з групи водню, OH, галогену, C 1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, CF 3, OH, CN, OCH3, °C(=O)CH3 та C1-C3алкілу, заміщеного щонайменше одним CN; 25 R обраний з групи, яка складається з водню та C1-C3алкілу; арил являє собою феніл або нафталініл; гетероарил являє собою моноциклічний 5-6-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N; або біциклічний 8-12-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N; за умови, що Het не відповідає формулі d(x), N NC N N R2 45 50 d(x) , або їх фармацевтично прийнятні сіль приєднання або сольват. 23 Переважно, R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C324 24 24 24 24 C7циклоалкілу, C1-C6алкіл-R , SO2R , SO2N(R )2, арилу, гетероарилу, C(=O)OR , OR , 24 24 24 C(=O)R , C(=O)N(R )2, C(=O)N(R )2 та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, OH, CN, OCH3; 24 R обраний з групи водню, OH, галогену, C 1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, CF 3, OH, CN, OCH3 та OC(=O)CH3. 3 UA 114531 C2 5 10 15 20 25 30 35 40 45 50 55 В іншому аспекті даний винахід стосується зазначених вище сполук для застосування у лікуванні RSV-інфекцій у теплокровних тварин, переважно в людей. У ще одному аспекті даний винахід представляє спосіб лікування вірусних RSV-інфекцій у суб'єкта, що потребує цього, який включає введення зазначеному суб'єкту ефективної кількості сполуки, яка визначена вище. У ще одному аспекті даний винахід стосується застосування сполуки, яка визначена вище, для виробництва медикаменту для лікування RSV-інфекції. У додатковому аспекті даний винахід стосується фармацевтичної композиції, яка містить сполуку, яка визначена вище, та фармацевтично прийнятний наповнювач. У ще одному аспекті даний винахід стосується способів одержання сполук, визначених вище. Докладний опис винаходу Даний винахід в широкому сенсі базується на розумному визнанні того, що сполуки формули (RI), як правило, мають інгібіторну активність стосовно RSV, яка становить інтерес. Даний винахід далі буде описано з посиланням на конкретні варіанти здійснення та з посиланням на деякі приклади, але даний винахід ними не обмежений, а обмежений лише формулою винаходу. Якщо в даному описі та формулі винаходу застосовують вираз "який містить", то він не виключає інші елементи або стадії. Форми однини застосовуються у даному документі для позначення іменника як в однині, так і у множині, якщо конкретно не зазначено будь-що інше. У випадках застосування виразу "заміщений" у даному винаході це означає, якщо не зазначено або чітко не випливає з контексту інше, що один або декілька атомів водню, зокрема, від 1 до 4 атомів водню, переважно від 1 до 3 атомів водню, більш переважно 1 атом водню на атомі або радикалі, позначеному виразом з використанням "заміщений", заміщені обраним із зазначеної групи, за умови, що не перевищується нормальна валентність і що заміщення дає хімічно стабільну сполуку, тобто сполуку, яка достатньо стійка, щоб витримати виділення до придатного ступеня чистоти з реакційної суміші та складання у терапевтичний засіб. Застосовуваний у даному документі "C1-C6алкіл" як група або частина групи означає насичені вуглеводневі радикали з прямим або розгалуженим ланцюгом, які містять від 1 до 6 (1, 2, 3, 4, 5 або 6) атомів вуглецю, такі як метил, етил, пропіл, 1-метилетил, бутил, пентил, гексил, 2-метилбутил тощо. "C1-C10алкіл" як група або частина групи означає насичені вуглеводневі радикали з прямим або розгалуженим ланцюгом, які містять від 1 до 10 атомів вуглецю, такі як групи, визначені як C1-C6алкіл та гептил, октил, ноніл, 2-метилгексил, 2-метилгептил, децил, 2-метилноніл тощо. "C1-C4алкілоксі" або "C1-C4алкоксі" як група або частина групи означає O-C1-C4алкільний радикал, у якому C1-C4алкіл незалежно має зазначене вище значення. "C1-C6алкілоксі" або "C1-C6алкоксі" як група або частина групи означає O-C1-C6алкільний радикал, у якому C1-C6алкіл незалежно має зазначене вище значення. Вираз "C3-C7циклоалкіл" окремо або в комбінації означає циклічний насичений вуглеводневий радикал, який містить від 3 до 7 атомів вуглецю. Необмежувальні приклади придатних C3-C7циклоалкілів включають циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. 8 9 Вираз "-(CR R )m-", що застосовується в даному документі, означає m повторювань підгрупи 8 9 CR R , де кожна з цих підгруп визначена незалежно. Вираз "галогено" або "галоген" як група або частина групи є загальним для фтору, хлору, брому, йоду, якщо не зазначено або не випливає з контексту інше. Вираз у формі NRCOOR є ідентичним N(R)COOR. Переважними прикладами 4-6-членного аліфатичного кільця, яке необов'язково містить один або декілька гетероатомів, обраних з групи, яка складається з N, S та O, є циклобутил, циклопентил, циклогексил, піперидиніл, оксетаніл, тетрагідрофураніл, тетрагідропіраніл, піперидиніл, азетидиніл, тіоланіл, піперазиніл та піролідиніл. Гетероарил являє собою моноциклічний 5-6-членний ароматичний гетероцикл, який містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N; або біциклічний 8-12-членний ароматичний гетероцикл, який містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N. Прикладами такого гетероарилу є фураніл, тіофеніл, піридиніл, піридазиніл, піримідиніл, піразиніл, хіноксалініл та бензімідазоліл. Варто відзначити, що положення радикалів у будь-якому фрагменті молекули, що застосовуються у визначеннях, можуть бути у будь-якому місці такого фрагмента, за умови, що він зберігає хімічну стабільність. 4 UA 114531 C2 5 10 15 20 25 30 35 40 45 50 55 Радикали, що застосовуються у визначеннях змінних, включають всі можливі ізомери, якщо не зазначено інше. Наприклад, пентил включає 1-пентил, 2-пентил та 3-пентил. Якщо будь-яка змінна трапляється більше одного разу в будь-якому складнику, кожна визначається незалежно. Вище та нижче у даному документі передбачають включення у вираз "сполука формули (RI)" або "сполуки формули (RI)" їх таутомерів та стереоізомерних форм, а також їх фармацевтично прийнятних солей приєднання та сольватів. Вирази "стереоізомери", "стереоізомерні форми" або "стереохімічно ізомерні форми" вище або нижче у даному документі застосовуються взаємозамінно. Вираз "стереохімічно ізомерні форми", що застосовується у даному документі, означає всі можливі сполуки, які складені з одних і тих же атомів, зв'язаних однією і тією ж послідовністю зв'язків, але мають різні тривимірні структури, які не є взаємозамінними та які можуть мати сполуки формули (RI). Слід мати на увазі, що деякі зі сполук формули (RI) можуть містити один або декілька центрів хіральності та існувати як стереохімічно ізомерні форми. Даний винахід включає всі стереоізомери сполуки формули (RI) та його таутомери або у формі чистого стереоізомеру, або у формі суміші двох або більше стереоізомерів. Енантіомери є стереоізомерами, які являють собою дзеркальні відображення один одного, що не збігаються під час накладання. Суміш 1:1 пари енантіомерів являє собою рацемат або рацемічну суміш. Діастереомери (або діaстереоізомери) являють собою стереоізомери, які не є енантіомерами, тобто вони не співвідносяться як дзеркальні відображення. Якщо сполука містить подвійний зв'язок, замісники можуть перебувати у E- або Z-конфігурації. Замісники у бівалентних циклічних (частково) насичених радикалах можуть перебувати або у цис-, або у транс-конфігурації; наприклад, якщо сполука містить двозаміщену циклоалкільну групу, то замісники можуть бути у цис- або транс-конфігурації. Таким чином, даний винахід включає енантіомери, діaстереомери, рацемати, E-ізомери, Z-ізомери, цис-ізомери, транс-ізомери та їх суміші у всіх випадках, коли це можливо з хімічної точки зору. Абсолютна конфігурація визначається згідно з системою Кана-Інгольда-Прелога. Конфігурація асиметричного атома позначається або R, або S. Розчинні сполуки, абсолютна конфігурація яких невідома, можуть бути позначені (+) або (-) залежно від напрямку, у якому вони обертають плоскополяризоване світло. Якщо зазначено конкретний стереоізомер, це означає, що зазначений стереоізомер є практично чистим, тобто зв'язаний з менше 50 %, переважно з менше 20 %, більш переважно з менше 10 %, ще більш переважно з менше 5 %, зокрема, з менше 2 % та найбільш переважно з менше 1 % інших ізомерів. Таким чином, якщо сполука формули (RI), наприклад, зазначена як (R), то це означає, що сполука практично вільна від ізомеру (S); якщо сполука формули (RI), наприклад, зазначена як E, то це означає, що сполука практично вільна від ізомеру Z; якщо сполука формули (RI), наприклад, зазначена як цис, то це означає, що сполука практично вільна від транс-ізомеру. Деякі сполуки формули (RI) можуть також існувати в їх таутомерній формі. Мається на увазі, що такі форми, хоча вони явно і не зазначені у наведеній вище формулі, включені в обсяг даного винаходу. Якщо не згадано або не зазначено інше, хімічне позначення сполуки охоплює суміш усіх можливих стереохімічно ізомерних форм, які може мати зазначена сполука. Зазначена суміш може містити усі діастереомери та/або енантіомери з основною молекулярною структурою зазначеної сполуки. Мається на увазі, що всі стереохімічно ізомерні форми сполук згідно з даним винаходом як у чистій формі, так і в суміші одна з одною включені в обсяг даного винаходу. Чисті стереоізомерні форми сполук та проміжні сполуки згідно з даним винаходом можна одержувати шляхом застосування методик, відомих з рівня техніки. Діастереомерні рацемати формули (RI) можна одержувати окремо за допомогою традиційних способів. Для деяких сполук формули (RI), їх таутомерів та стереоізомерних форм, а також їх фармацевтично прийнятних солей приєднання та сольватів; та проміжних сполук, застосовуваних для їх одержання, абсолютну стереохімічну конфігурацію експериментально не визначали. Фахівець у даній галузі зможе визначити абсолютну конфігурацію таких сполук, застосовуючи відомі з рівня техніки способи, такі як, наприклад, дифракція рентгенівських променів. Мається на увазі, що даний винахід також включає всі ізотопи атомів, які трапляються у сполуках згідно з даним винаходом. Ізотопи включають атоми, які мають однакове атомне 5 UA 114531 C2 5 10 15 20 25 30 35 40 45 50 55 число, але різні масові числа. Як загальний приклад і без обмеження, ізотопи водню включають тритій та дейтерій. Ізотопи вуглецю включають C-13 та C-14. Сполука згідно з даним винаходом, таким чином, за своєю природою включає в себе сполуку з одним або декількома ізотопами одного або декількох елементів та їх сумішами, в тому числі радіоактивну сполуку, яку також називають міченою радіоактивним ізотопом сполукою, в якій один або декілька нерадіоактивних атомів замінені одним з їх радіоактивних ізотопів. Під виразом "мічена радіоактивним ізотопом сполука" розуміють будь-яку сполуку формули (RI), яка містить щонайменше один радіоактивний атом. Наприклад, сполука може бути мічена позитронно- або гамма-активними радіоактивними ізотопами. Для методів 3 125 радіолігандного зв'язування переважним атомом для заміни є атом H або атом I. Для візуалізації найчастіше використовуваними позитронно-активними (PET) радіоактивними 11 18 15 13 ізотопами є C, F, O та N, всі з яких створені за допомогою прискорювача та мають періоди напіврозпаду 20, 100, 2 та 10 хвилин (хв.), відповідно. Оскільки періоди напіврозпаду цих радіоактивних ізотопів настільки короткі, їх використання можливо лише в закладах, в яких є прискорювач частинок в місці їх одержання, що, таким чином, обмежує їх застосування. 18 99m 201 123 Найбільш широко використовуваними серед них є F, Tc, Tl та I. Обробка цих радіоактивних ізотопів, їх одержання, виділення та вбудовування в молекулу відомі фахівцю в даній галузі. Зокрема, радіоактивний атом обраний з групи водню, вуглецю, азоту, сірки, кисню та 3 11 18 122 123 125 131 75 76 галогену. Зокрема, радіоактивний ізотоп обраний з групи H, C, F, I, I, I, I, Br, Br, 77 82 Br та Br. Для терапевтичного застосування солі сполуки формули (RI) є такими, що їх протиіон є фармацевтично прийнятним. Однак солі кислот та основ, що не є фармацевтично прийнятними, також можуть знайти застосування, наприклад, в одержанні або очищенні фармацевтично прийнятної сполуки. Усі солі, незалежно від того, чи є вони фармацевтично прийнятними, включені в обсяг даного винаходу. Фармацевтично прийнятні солі приєднання кислоти та основи, як зазначалось у даному документі вище, розуміють як ті, що включають терапевтично активні нетоксичні форми солей приєднання кислоти та основи, що можуть бути утворені із сполук формули (RI). Фармацевтично прийнятні солі приєднання кислоти традиційно можна одержати шляхом обробки основної форми такою відповідною кислотою. Придатні кислоти включають, наприклад, неорганічні кислоти, такі як галогеноводневі кислоти, наприклад, хлороводневу або бромоводневу кислоту, сірчану, азотну, фосфорну та подібні кислоти; або органічні кислоти, такі як, наприклад, оцтова, пропанова, гідроксіоцтова, молочна, піровиноградна, щавелева (тобто етандіова), малонова, бурштинова (тобто бутандіова кислота), малеїнова, фумарова, яблучна (тобто гідроксибутандіова кислота), винна, лимонна, метансульфонова, етансульфонова, бензенсульфонова, п-толуенсульфонова, цикламова, саліцилова, п-аміносаліцилова, памова та подібні кислоти. І навпаки, зазначені сольові форми можна перетворити шляхом обробки відповідною основою на форму вільної основи. Сполуки формули (RI), які містять кислотний протон, також можна перетворити на форми їх нетоксичних солей приєднання металів або амінів шляхом обробки відповідними органічними та неорганічними основами. Прийнятні форми основних солей включають в себе, наприклад, амонієві солі, солі лужних та лужноземельних металів, наприклад, солі літію, натрію, калію, магнію, кальцію тощо, солі органічних основ, наприклад, бензатинову, N-метил-D-глюкамінову, гідрабамінову солі, та солі амінокислот, такими як, наприклад, аргінін, лізин тощо. Вираз "сольват" включає гідрати та форми приєднання розчинника, у формі яких можуть бути утворені сполуки формули (RI), а також їх солі. Прикладами таких форм є, наприклад, гідрати, алкоголяти тощо. Без відступу від загального обсягу даного винаходу деякі варіанти здійснення обговорюються детальніше нижче. Описані вище та інші вирази, що застосовуються в даному описі, добре зрозумілі фахівцям у даній галузі. Далі будуть викладені переважні ознаки сполук згідно з даним винаходом. Даний винахід стосується нових сполук формули (RI), 6 UA 114531 C2 , або їх будь-якої стереоізомерної форми, де Het являє собою гетероцикл будь-якої з наступних формул (a), (b), (c), (d): R1b R1b R1a R1a N 1a R 1a R N R1b R1b X XN X X N R1a R1a N X X XN R1b R1b X 2 R1a R1a R (a) (a) 1c 1c R R1c R1c R R3 R2 , 1d R R3 N 2 R1cR R1c (c) (c) R2 R1b R1b R (b) (b) R1d N N 2 R1c R1c N R1d R2 R R3 R3 R1d X X X X X X XN R1d X R1d (d) , , 1d N 2 R1dR (d) R2 ; 5 кожен X незалежно являє собою C або N; за умови, що щонайменше два X являють собою C; 10 15 20 25 30 1a 1b 1c 1d кожен з R , R , R або R незалежно обраний з групи, яка складається з H, галогену, C16 7 C6алкілу, C3-C7циклоалкілу, C1-C6алкілоксі, N(R )2, CO(R ), CH2NH2, CH2OH, CN, C(=NOH)NH2, C(=NOCH3)NH2, C(=NH)NH2, CF3 та OCF3; 1b 1d R або R відсутній, якщо X, з яким він зв'язаний, являє собою N; 2 8 9 10 кожен R являє собою -(CR R )m-R ; m являє собою ціле число від 0 до 6; 3 кожен R незалежно обраний з групи, яка складається з H, галогену, арилу, гетероарилу, C 17 C6алкілу, C3-C7циклоалкілу, C1-C6алкілоксі та CO(R ); 6 кожен R незалежно обраний з групи, яка складається з H, C 1-C6алкілу, COOCH3 та CONHSO2CH3; 7 кожен R незалежно обраний з групи, яка складається з H, C1-C6алкілу, OH, C1-C6алкілоксі, NH2, NHSO2N(C1-C6алкілу)2, NHSO2NHCH3, NHSO2(C1-C6алкілу), NHSO2(C3-C7циклоалкілу), і 8 9 9 10 N(C1-C6-алкіл)2NR R , і NR R ; 8 9 кожен R та R незалежно обраний з групи, яка складається з H, C 1-C10алкілу та C38 9 C7циклоалкілу; або R та R , узяті разом, утворюють 4-6-членне насичене кільце, яке необов'язково містить один або декілька гетероатомів, обраних з групи, яка складається з N, S та O; 10 кожен R незалежно обраний з групи, яка складається з H, галогену, OH, CN, CF 2H, CF3, C18 9 8 C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, C(=O)NR R , C(=O)OR , 8 8 9 8 8 9 8 9 8 9 8 SO2R , C(=O)N(R )SO2R , C(=O)N(R )SO2N(R R ), NR R , NR C(=O)OR , C(=O)R , O-бензилу, 8 9 8 9 8 8 9 8 12 8 8 9 11 NR SO2R , SO2NR R , SO2R , C(=O)NR R , °C(=O)NR R , N(R )C(=O)N(R R ), R , 8 12 11 11 N(R )C(=O)OR , OR , C(=O)R та 4-6-членного насиченого кільця, яке містить один атом кисню; 11 R являє собою феніл, піридиніл або піразоліл; кожен з яких може бути необов'язково заміщеним одним або декількома замісниками, кожен з яких незалежно обраний з групи, яка складається з CF3, CH3, OCH3, OCF3 та галогену; 7 UA 114531 C2 12 5 10 15 20 25 30 R являє собою C1-C6алкіл або C3-C7циклоалкіл; кожен з яких заміщений одним або декількома замісниками, кожен з яких незалежно обраний з групи, яка складається з CF3, CH3, OCH3, OCF3 та галогену; кожен Z незалежно являє собою C або N, за умови, що щонайменше два Z являють собою C; 20 21 кожен з Q та V незалежно являє собою C=O, SO2 або CR R ; p та s незалежно являють собою ціле число від 0 до 3, де сума p та s повинна дорівнювати щонайменше 2, і якщо p=0 або s=0, тоді атом вуглецю, позначений *, безпосередньо зв'язаний з W; 20 21 R та R незалежно обрані з групи, яка складається з водню, гідроксилу, C 1-C3алкілу, C3C7циклоалкілу, CF3, OCH3, OCF3 та галогену; 22 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C3-C7циклоалкілу, 22 CF3, OCH3, OCF3 та галогену; R приєднаний до одного Z, який не являє собою N; W обраний з групи, яка складається з SO, SO 2, S, C, O та N, де такий C або N необов'язково 23 заміщений одним або декількома R ; 23 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C3-C7циклоалкілу, C124 24 24 24 24 24 24 C6алкіл-R , SO2R , SO2N(R )2, арилу, гетероарилу, C(=O)OR , OR , C(=O)R , C(=O)N(R )2, 24 24 25 24 25 24 25 24 C(=O)N(R )2, P(=O)-(O-C1-C6-алкілу)2, N(R )2, NR C(=O)OR , NR C(=O)N(R )2, NR SO2R та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, OH, CN, OCH 3; 24 R обраний з групи водню, OH, галогену, C 1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, CF3, OH, CN, OCH3, C(=O)CH3 та C1-C3алкілу, заміщеного щонайменше одним CN; 25 R обраний з групи, яка складається з водню та C1-C3алкілу; арил являє собою феніл або нафталініл; гетероарил являє собою моноциклічний 5-6-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N; або біциклічний 8-12-членний ароматичний гетероцикл, що містить один або декілька гетероатомів, кожен з яких незалежно обраний з групи, яка складається з O, S та N; за умови, що Het не відповідає формулі d(x), N NC N N R2 d(x) , 35 або їх фармацевтично прийнятної солі приєднання або сольвату. У варіанті здійснення даний винахід стосується сполук формули (RI), 40 , або їх будь-якої стереоізомерної форми, де Het являє собою гетероцикл будь-якої з наступних формул (a), (b), (c), (d): 8 UA 114531 C2 1b 1b 1a 1a R R R R R1a 1a R N N N N N N 1a 1a R R R1b 1b X X R X X X X R1b 1b X X R N N 1a 1a R2 R2 R R (a)(a) 1c 1c R R 2 2 R1b 1b R R R (b)(b) , , R1dR1d R3 R3 R3 R3 1c 1c R1dR1d X X X X R R X X R1dR1d X X N N N N R1cR1c 1c 1c 2 2 R R R R (c) (c) 2 2 R1dR1d R R (d) (d) ; , кожен X незалежно являє собою C або N; за умови, що щонайменше два X являють собою C; 5 10 15 20 25 30 35 40 1a 1b 1c 1d кожен з R , R , R або R незалежно обраний з групи, яка складається з H, галогену, C 1C6алкілу, C1-C6алкілоксі, CF3 та OCF3; 1b 1d R або R відсутній, якщо X, з яким він зв'язаний, являє собою N; 2 8 9 10 кожен R являє собою -(CR R )m-R ; m являє собою ціле число від 2 до 6; 3 кожен R являє собою H, галоген або C1-C6алкіл; 8 9 кожен R та R незалежно обраний з групи, яка складається з H та C1-C10алкілу; 10 кожен R незалежно обраний з групи, яка складається з H, галогену, OH, CN, CF 2H, CF3, C18 9 8 8 C6алкілу, C3-C7циклоалкілу, C(=O)NR R , C(=O)OR та SO2R ; кожен Z незалежно являє собою C або N, за умови, що щонайменше два Z являють собою C; 20 21 кожен з Q та V незалежно являє собою CR R ; p та s незалежно являють собою ціле число від 0 до 3, де сума p та s повинна дорівнювати щонайменше 2, і якщо p=0 або s=0, тоді атом вуглецю, позначений *, безпосередньо зв'язаний з W; 20 21 R та R являють собою водень; 22 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, CF3, OCH3, OCF3 та галогену; W обраний з групи, яка складається з SO2, C, O та N, де такий C або N необов'язково 23 заміщений одним або декількома R ; 23 R обраний з групи, яка складається з водню, гідроксилу, C 1-C6алкілу, C3-C7циклоалкілу, C124 24 24 24 24 24 24 C6алкіл-R , SO2R , SO2N(R )2, арилу, гетероарилу, C(=O)OR , OR , C(=O)R , C(=O)N(R )2, 24 24 25 24 25 24 25 24 C(=O)N(R )2, P(=O)-(O-C1-C6-алкілу)2, N(R )2, NR C(=O)OR , NR C(=O)N(R )2, NR SO2R та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, арилу або гетероарилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, OH, CN, OCH3; 24 R обраний з групи водню, OH, галогену, C 1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу та 4-6-членного насиченого кільця, яке містить один атом кисню, де будь-який з таких C1-C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, арилу, гетероарилу, бензилу необов'язково заміщений одним або декількома замісниками, обраними з групи, яка складається з галогену, CF 3, OH, CN, OCH3, C(=O)CH3 та C1-C3алкілу, заміщеного щонайменше одним CN; 25 R обраний з групи, яка складається з водню та C1-C3алкілу; арил являє собою феніл або нафталініл; гетероарил являє собою фураніл, тіофеніл, піридиніл, піридазиніл, піримідиніл, піразиніл, хіноксалініл або бензімідазоліл; або їх фармацевтично прийнятної солі приєднання або сольвату. Згідно з даним винаходом варіанти здійснення сполук RI представлені формулами Ia, Ib, Ic та Id, відповідно. 9 UA 114531 C2 1d 5 В одному варіанті здійснення R незалежно обраний з групи, яка складається з H, галогену, 6 7 C1-C6алкілу, C3-C7циклоалкілу, C1-C6алкілоксі, N(R )2, CO(R ), CH2NH2, CH2OH, C(=NOH)NH2, C(=NOCH3)NH2, C(=NH)NH2, CF3 та OCF3. Переважно, в будь-якому з визначених у даному документі варіантів здійснення Het не відповідає формулі d(x), N NC N N R2 2 10 d(x) , де R є таким, як визначено в даному документі в будь-якому з варіантів здійснення. В ще більш переважному варіанті здійснення Het не відповідає формулі d(y), N R1d N N R2 d(y) , 1d 2 де R та R є такими, як визначено в даному документі в будь-якому з варіантів здійснення. В іншому варіанті здійснення Het представлений формулою (a"), (b"), (c") або (d"): R1a 1a R1a R R1a 1d 1d 1d 1d 1c 1c 1c 1c N N N N 1b 1b 1b 1b R R RR R R RR X X XX X X XX N N NN N N N N 2 2 R R (a')(a') (a') R R (a') , 2 2 2 22 (b')(b') R R RR (b') (b') X X XX X X XX N N NN N N NN 22 R R RR , 2 N N NN 22 R R RR (c')(c')(c') (c') , 2 R2 R2 RR2 (d') (d') (d') (d') , 15 20 де щонайменше один X являє собою N. Більш переважно, у формулах (b") та (d") лише один X являє собою N. 1a 1b 1c 1d R , R , R або R незалежно обрані з групи, яка складається з H та галогену, більш переважно з хлору, брому та фтору. Найбільш переважним є хлор. 2 8 9 10 Сполуки згідно з даним винаходом містять радикал R , який являє собою -(CR R )m-R , і при цьому m являє собою ціле число від 0 до 6, від 1 до 4, або 3, або 4. 10 UA 114531 C2 8 5 10 9 Переважно, кожен R та R незалежно обраний з H або C1-C6алкілу. У конкретному варіанті 2 10 2 здійснення R являє собою C1-C6алкіл-R . У підваріанті здійснення R являє собою C3-C4алкіл10 R . 10 Кожен R незалежно обраний з групи, яка складається з H, галогену, OH, CN, CF 2H, CF3, C18 9 8 C6алкілу, C3-C7циклоалкілу, C(=O)C1-C6алкілу, C(=O)C3-C7циклоалкілу, C(=O)NR R , C(=O)OR , 8 8 9 8 8 9 8 9 8 9 8 SO2R , C(=O)N(R )SO2R , C(=O)N(R )SO2N(R R ), NR R , NR C(=O)OR , °C(=O)R , O-бензилу, 8 9 8 9 8 8 9 8 12 8 8 9 11 NR SO2R , SO2NR R , SO2R , C(=O)NR R , °C(=O)NR R , N(R )C(=O)N(R R ), R , 8 12 11 11 N(R )C(=O)OR , OR , C(=O)R та 4-6-членного насиченого кільця, яке містить один атом кисню. 10 В конкретному варіанті здійснення R обраний з групи, яка складається з C1-C3алкілу, H, OH, CN, F, CF2H, CF3, SO2-C1-C3алкілу, SO2C3-C6циклоалкілу. Конкретний варіант здійснення даного винаходу стосується сполук з формулою RII, RIII, RIV, RV, RVI або RVII; 15 23 20 25 30 35 або їх будь-якої стереоізомерної форми, де Het, X та R визначені в будь-якому з описаних варіантів здійснення. 23 В іншому варіанті здійснення сполук формули RI, RII, RIII, RIV, RV або RVI R обраний з 24 24 24 групи, яка складається з водню, гідроксилу, C1-C6алкілу, C1-C3алкіл-R , SO2R , O-R , фенілу, 24 24 піридинілу, піримідилу, піразолілу, C(=O)OR , C(=O)R , де будь-який з таких C1-C6алкілу, фенілу, піридинілу, піримідилу, піразолілу необов'язково заміщений одним або декількома з наступних замісників: OCH3, галоген, OH та CN. Загальні схеми синтезу Сполуки формули RI або їх фармацевтично прийнятні солі можна одержувати відповідно до схем реакцій, розглянутих у даному документі нижче, із застосуванням способів синтезу, відомих у галузі органічної хімії, або модифікацій та варіантів, що знайомі фахівцям у даній галузі. Вихідні речовини, що застосовуються у даному документі, є комерційно доступними або їх можна одержувати за допомогою звичайних способів, відомих з рівня техніки, наприклад, таких способів, які описані у стандартних довідниках. Переважні способи включають, без обмеження, описані нижче. Протягом будь-якої з наступних послідовностей синтезу може бути необхідним та/або бажаним захист чутливих або реакційноздатних груп у будь-якій з розглянутих молекул. Цього можна досягнути за допомогою звичайних захисних груп, таких як описані у T. W. Greene and P. G. M. Wuts, Protective Groups in Organic Chemistry, John Wiley & Sons, 1999, який включений у даний документ за допомогою посилання. Якщо не зазначено інше, замісники у схемах визначені вище. Виділення та очищення продуктів здійснюють за допомогою стандартних процедур, відомих фахівцю-хіміку. 11 UA 114531 C2 5 Наступні схеми є прикладами способів одержання сполук формули RI. На схемах, наведених нижче, використовуються цифри включно з цифрами від I до XXVIII, що застосовуються для зручності позначення формул на схемах. Сполуки формули (Ia) можна синтезувати, наприклад, із застосуванням одного зі способів, наведених на схемі 1. Як правило, фрагмент A або B вводять у реакцію сполучення з фрагментом C з одержанням похідних формули (Ia). 10 15 20 Схема 1. Загальний синтез сполук формули (Ia) У способі 1 прикладом придатних "умов сполучення" для реакції фрагмента A з фрагментом C з утворенням сполук типу формули (Ia) є реакція Міцунобу. Придатним розчинником для даного типу реакції є THF (тетрагідрофуран). Альтернативно (без обмеження), сполука типу фрагмента B, де LG являє собою відхідну групу, таку як галогенід, переважно хлор, або сульфонат, можна вводити у реакцію зі сполукою типу фрагмента C за допомогою реакції сполучення, опосередкованої основою (Спосіб 2). Можливі основи для здійснення цієї реакції (без обмеження) являють собою K 2CO3, Cs2CO3, триетиламін, гідрид натрію. Придатним розчинником (без обмеження) для даного типу реакції сполучення, опосередкованої основою, є DMF (диметилформамід) або THF (тетрагідрофуран). Сполуки типу фрагмента A загалом можна одержати, як представлено на схемі 2. 12 UA 114531 C2 Схема 2. Загальний синтез сполук типу фрагмента A Як правило, сполуки типу фрагмента B можна одержувати зі сполук типу фрагмента A за допомогою реакції з такими реагентами, як (без обмеження) SOCl2, PBr3, п-TsCl, MsCl. 5 10 15 20 25 Схема 3. Загальний синтез сполук типу фрагмента B Проміжні сполуки типу фрагмента C формули (VI) можна одержувати, як представлено на схемі 4. Схема 4. Загальний синтез сполук типу фрагмента C (VI) Синтез похідних спіро-2-оксоіндолу та похідних спіро-2-оксоазаіндолу наведений на схемі 4. Проміжні сполуки формули VI можуть бути синтезовані із застосуванням процедури, наведеної на схемі 4. Заміщення (U), який являє собою галогенід, переважно фтор, або алкілоксигрупу, переважно метоксі, у нітропіридині або нітроарилі формули I трет-бутилетилмалонатом у придатному розчиннику, такому як THF або DMF, за присутності основи, такої як гідрид натрію або карбонат калію, зумовлює одержання проміжної сполуки формули (II). Обробка проміжної сполуки II кислотою, такою як трифтороцтова кислота або суха хлороводнева кислота, зумовлює одержання проміжної сполуки III. Остання може бути перетворена на проміжну сполуку V шляхом конденсації з дигалогеновмісною сполукою IV, яка переважно є бромовмісною, за присутності придатної основи, такої як карбонат калію, карбонат натрію, гідрид натрію тощо, у придатному розчиннику, такому як DMF, THF тощо. Відновлення нітрогрупи проміжної сполуки V, коли його виконують стехіометричним способом із застосуванням заліза за присутності хлориду амонію або хлориду олова, за присутності концентрованої хлороводневої кислоти, зумовлює безпосереднє одержання сполуки VI. 13 UA 114531 C2 5 10 Альтернативно, проміжна сполука формули III може бути спочатку відновлена каталітичним способом із застосуванням водню за присутності каталізатора, такого як паладій або платина, у придатному розчиннику, такому як метанол, з одержанням проміжної сполуки VII. Остання може бути перетворена на проміжну сполуку VIII за присутності кислоти з застосуванням хлороводневої кислоти тощо у придатних розчинниках, таких як спирти, наприклад, ізопропанол. Конденсацію проміжної сполуки VIII з дигалогеновмісною сполукою IV, яка переважно є хлоровмісною або бромовмісною, здійснюють за присутності придатної неорганічної основи, такої як карбонат калію, карбонат натрію, гідрид натрію тощо, у придатному розчиннику, такому як DMF, THF тощо, або з застосуванням органічної основи, такої як гексаметилдисилазид натрію (NaHMDS) або основ у формі алкіллітієвих сполук, наприклад, н-BuLi, у придатних розчинниках, таких як THF або ефір, з одержанням проміжної сполуки VI. 15 20 25 30 35 40 Схема 5. Загальний синтез сполук типу фрагмента C (VI) Альтернативно, сполуки формули VI можна одержувати, без обмеження, за допомогою загальних процедур, проілюстрованих на схемі 5. Вихідна речовина IX може бути комерційно доступною або одержаною із застосуванням процедур, відомих з рівня техніки. Кислота X може бути активована у формі аміду Вайнреба із застосуванням стандартних процедур синтезу пептидів шляхом сполучення, наприклад, EDCI/HOBT, HATU, DCC і т. д. Відразу після активації кислоти у формі складного ефіру або аміду Вайнреба можна додавати анілін IX для перетворення його на проміжну сполуку XI. Реакція проміжної сполуки XI з PG, де PG являє собою захисну групу, таку як параметоксибензил, бензил, трет-бутоксикарбоніл, мезил або тозил, за присутності придатної основи, такої як карбонат калію, карбонат цезію або гідрид натрію, у придатному розчиннику, такому як DMF або THF, зумовлює одержання проміжної сполуки XIII. Проміжну сполуку XIV одержували відповідно до процедури, описаної у Lee, S. and J. F. Hartwig (2001). J. Org. Chem. 66(10): 3402-3415. Заміщення (U), який являє собою галоген, переважно бром, із застосуванням ацетату паладію (II) як каталізатора за присутності основи, такої як трет-бутоксид калію, та ліганду, такого як трициклогексилфосфін, у розчиннику, такому як 1,4-діоксан, зумовлює одержання проміжної сполуки XIV. Видалення захисної групи у проміжній сполуці XIV можна виконати із застосуванням умов, описаних у Green and Wurts, Protecting groups in Organic rd Synthesis 3 Edition, з одержанням проміжної сполуки VI. 1b 2 22 На схемі 6 проілюстрований спосіб одержання сполук формули Ib, де R , R , R , Q, V, W, X та Z визначені вище. Як видно зі схеми 6, сполука формули Ib може бути синтезована шляхом сполучення 2гідроксиметиленімідазопіридинів XV-a зі спірооксоіндолом або спірооксоазаіндолом VI за допомогою відомого з рівня техніки способу, такого як реакція Міцунобу, в якій застосовують, наприклад, азадіізопропілдикарбоксилат та трифенілфосфін, у придатному розчиннику, такому як DMF або THF. Альтернативно, сполука формули Ib може бути одержана шляхом заміщення (LG), де (LG) являє собою відхідну групу, яка являє собою галогенід, переважно хлор XV-b, або сульфонат, такий як мезилат XV-c, за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF. 14 UA 114531 C2 Схема 6 5 10 15 20 25 30 35 Одержання сполуки XV-b та XV-c Обробка спирту XV-a тіонілхлоридом зумовлює утворення 2-хлорметилімідазопіридинів XVb. Альтернативно, спирт XV-a може бути перетворений на проміжну сполуку XV-c шляхом реакції з метансульфонілхлоридом за присутності органічної основи, такої як триетиламін або діізопропілетиламін, у придатному розчиннику, такому як дихлорметан (схема 7). Схема 7 Одержання сполуки XV-a Сполуки формули XV-a або є комерційно доступними, або можуть бути одержані, без 1b 2 обмеження, за допомогою загальних процедур, проілюстрованих на схемі 8, де R , R , X визначені вище. Як видно зі схеми 8 нижче, галогенгетероарили XVI, де (U) являє собою галогенід, переважно фтор, можуть бути оброблені за допомогою первинних амінів формули XVII за присутності придатної основи, такої як карбонат калію тощо, у придатному розчиннику, такому як етанол або дихлорметан, за температури реакції в діапазоні від кімнатної температури до 100 °C з одержанням сполук формули XVIII. Гідрування нітрогрупи із застосуванням стандартних умов, таких як застосування Pd/C або іншого каталізатора в атмосфері водню або Fe/EtOH/CaCl2, зумовлює одержання діаміну формули XIX. Альтернативно, гідрування нітрогрупи сполуки XX із застосуванням стандартних умов, таких як застосування Pd/C або іншого каталізатора в атмосфері водню або Fe/EtOH/CaCl 2, зумовлює одержання діаміну формули XXI. Він може бути оброблений альдегідами формули XXII за присутності придатних відновників, таких як NaBH(OAc)3 або Na(CN)BH3, у розчинниках, таких як метиленхлорид, DMF або THF, за температури, що приблизно дорівнює кімнатній, з одержанням сполук формули XIX. Імідазольне кільце може бути утворене за допомогою обробки діамінів XIX гліколевою кислотою або складним ефіром, таким як XXV, за присутності сильної кислоти, такої як водна хлороводнева кислота, за підвищеної температури, наприклад, із нагріванням зі зворотним холодильником, з одержанням спиртів формули XV-a. Альтернативно, діаміни XIX можна конденсувати з діалкоксіацетатом формули XXIV за присутності оцтової кислоти у придатному розчиннику, такому як метанол, що зумовлює одержання ацеталю XV-e. Ацеталь сполук XV-e може бути видалений за допомогою кислот, таких як хлороводнева кислота, з одержанням альдегідів формули XV-f. Одержані альдегіди формули XV-f можуть бути відновлені до спиртів із застосуванням придатного відновника, такого як NaBH4 або LiAlH4, у придатному розчиннику, такому як етанол або THF, з одержанням необхідних спиртів формули XV-a. На додаток, діаміни XIX можна циклізувати з 15 UA 114531 C2 5 10 діалкілоксалатом формули XXIII у придатному розчиннику, такому як етанол, за підвищеної температури з нагріванням під впливом мікрохвильового випромінювання або без нього з одержанням імідазолів формули XV-d. Альтернативно, сполуки формули XV-d можуть бути одержані протягом двох стадій синтезу, починаючи з діамінів XIX. По-перше, діамін XIX може бути підданий реакції з алкілтригалогенацетімідатом, переважно метил-2,2,2трихлорацетімідатом, за присутності кислоти, переважно оцтової кислоти, за температури в діапазоні від 25 °C до 50 °C з одержанням сполуки формули XV-g. По-друге, реакція сполук формули XV-g з карбонатом металу, переважно карбонатом натрію, у придатному розчиннику, такому як метанол, зумовлює одержання сполук формули XV-d. Сполуки XV-d можуть бути згодом відновлені до необхідних спиртів формули XV-a із застосуванням придатного відновника, такого як NaBH4 або LiAlH4, у придатному розчиннику, такому як етанол або THF. Схема 8 15 20 25 Альтернативний шлях одержання сполук типу XV-a наведений на схемі 9. Діамін XXI спочатку може бути введений у реакцію сполучення з алкілгліколевою кислотою або складним ефіром, таким як XXV, за присутності сильної кислоти, такої як водна хлороводнева кислота, за підвищеної температури, наприклад, із нагріванням зі зворотним холодильником, з одержанням спиртів формули XXVI. Цей спирт може бути захищений за допомогою PG, де PG являє собою захисну групу, таку як, без обмеження, тритил, що в результаті зумовлює утворення сполуки XXVII. Придатним розчинником для даного типу реакцій може бути, без обмеження, дихлорметан. Обробка сполуки XXVII сполукою XXVIII, де LG являє собою відхідну групу, таку як галогенід, переважно бром, або сульфонат, за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF, зумовлює одержання сполуки XV-h. Видалення PG у сполуці XV-h можна здійснювати за присутності кислоти, такої як хлороводнева кислота, за присутності розчинника, такого як, без обмеження, діоксан, з одержанням сполуки XV-a. Схема 9 30 16 UA 114531 C2 5 10 15 20 25 Сполуки формули Ic або їх фармацевтично прийнятні солі можуть бути одержані відповідно до схем реакції, розглянутих у даному документі нижче. Якщо не зазначено інше, замісники у схемах визначені вище. Виділення та очищення продуктів здійснюють за допомогою стандартних процедур, відомих фахівцю-хіміку. 1c 2 3 22 Як видно зі схеми 10, сполука формули Ic, де R , R , R , R , Q, V, W та Z визначені вище, може бути синтезована шляхом сполучення 2-гідроксиметиленіндолу (XV-i) з (VI) за допомогою відомого з рівня техніки способу, такого як реакція Міцунобу, в якій застосовують азадіізопропілдикарбоксилат та трифенілфосфін, у придатному розчиннику, такому як DMF або THF. Альтернативно, сполука формули Ic може бути одержана шляхом заміщення LG (відхідної групи), що являє собою галогенід, переважно хлор (XV-j), або сульфонат, такий як мезилат (XVk), за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF. Схема 10 Одержання сполуки XV-i Вихідні речовини XXIX, що застосовуються у даному винаході, є комерційно доступними або можуть бути синтезовані, без обмеження, за допомогою відомих з рівня техніки способів, таких 2 як синтез Райссерта або синтез Фішера, при цьому реакція таких індолів з R -LG, де LG являє собою відхідну групу, таку як галогенід, переважно бром, або сульфонат, за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF, зумовлює одержання сполуки XXX (схема 11). Перетворення алкілового складного ефіру сполуки XXX на спирт XV-i може здійснюватися за допомогою гідриду металу, такого як алюмогідрид літію або борогідрид натрію, у придатному розчиннику, такому як THF, метанол або етанол. Схема 11 30 17 UA 114531 C2 5 Обробка спирту XV-i тіонілхлоридом зумовлює утворення 2-хлорметиліндолу XV-j. Альтернативно, спирт XV-i може бути перетворений на проміжну сполуку XV-k шляхом реакції з метансульфонілхлоридом за присутності органічної основи, такої як триетиламін або діізопропілетиламін, у придатному розчиннику, такому як дихлорметан (схема 12). Схема 12 10 1d 2 3 22 На схемі 13 проілюстрований спосіб одержання сполук формули (Id), де R , R , R , R , Q, V, W, X та Z визначені вище. 15 20 Схема 13. Загальний синтез сполук формули (Id) Сполука формули Id може бути синтезована шляхом сполучення 2гідроксиметиленазаіндолу XV-I зі спірооксоіндолом або спірооксоазаіндолом VI за допомогою відомого з рівня техніки способу, такого як реакція Міцунобу, в якій застосовують азадіізопропілдикарбоксилат (DIAD) та трифенілфосфін, у придатному розчиннику, такому як DMF або THF. Альтернативно, сполуки формули Id можуть бути одержані шляхом заміщення LG, де LG являє собою відхідну групу, яка являє собою галогенід, переважно хлор XV-m, або сульфонат, такий як мезилат XV-n, за присутності основи, такої як, без обмеження, гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF. 25 18 UA 114531 C2 5 10 15 20 25 Схема 14. Загальний синтез сполук типу XV-I Сполуку XV-I одержують відповідно до способів, наведених на схемі 14. Вихідні речовини XXXI, що застосовуються у даному винаході, відповідно до способу 1 є комерційно доступними або можуть бути синтезовані, без обмеження, за допомогою способів, відомих з рівня техніки, таких як синтез Райссерта або синтез Фішера. Реакція такої сполуки з 2 R -LG, де LG являє собою відхідну групу, таку як галогенід, переважно бром, або сульфонат, за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF, зумовлює одержання сполуки XXXII. Перетворення алкілового складного ефіру сполуки XXXII на спирт XV-l можна здійснювати за допомогою гідриду металу, такого як алюмогідрид літію або борогідрид натрію, у придатному розчиннику, такому як THF або метанол. Альтернативно, сполука типу XV-l також може бути синтезована за допомогою способу 2, наведеного на схемі 14. Комерційно доступну вихідну речовину XXXIII захищають за допомогою PG, де PG являє собою захисну групу, таку як, без обмеження, тозил, що в результаті зумовлює утворення сполуки XXXIV. Придатним розчинником для даного типу реакцій може бути, без обмеження, толуен. Металування сполуки XXXIV з наступною обробкою сполукою XXXV, де галогенід переважно являє собою хлор, у придатному розчиннику, такому як, без обмеження, THF, зумовлює одержання сполуки XXXVI. Видалення PG у сполуці XXXVI може здійснюватися за присутності основи, такої як карбонат калію або карбонат цезію, у придатному розчиннику, 2 такому як THF та метанол, з одержанням індолу XXXVII. Реакція індолів XXXVII з R -LG, де LG являє собою відхідну групу, таку як галогенід, переважно бром, або сульфонат, за присутності основи, такої як гідрид натрію, карбонат калію або карбонат цезію, у придатному розчиннику, такому як DMF або THF, зумовлює одержання сполуки XXXVIII. Перетворення алкілового складного ефіру сполуки XXXVIII на спирт XV-l можна здійснювати за допомогою гідриду металу, такого як алюмогідрид літію або борогідрид натрію, у придатному розчиннику, такому як THF або етанол. 30 19 UA 114531 C2 5 10 15 20 25 30 35 40 45 50 Схема 15. Загальний синтез сполук типу XV-m та XV-n Обробка спирту XV-I реагентами, такими як, без обмеження, SOCl2, PBr3, п-TsCl, MsCl, зумовлює утворення 2-хлорметиліндолу XV-m або таких сполук, як XV-n. Сполуки формули (RI) можна перетворити на відповідні форми N-оксидів, дотримуючись відомих з рівня техніки процедур для перетворення тривалентного азоту на його форму Nоксиду. Описану реакцію N-окиснення, як правило, можна виконувати шляхом здійснення реакції вихідної речовини формули (RI) з відповідним органічним або неорганічним пероксидом. Відповідні неорганічні пероксиди включають, наприклад, пероксид водню, пероксиди лужних металів або лужноземельних металів, наприклад, пероксид натрію, пероксид калію; відповідні органічні пероксиди можуть включати надкислоти, такі як, наприклад, бензенкарбопероксова кислота або галогензаміщена бензенкарбопероксова кислота, наприклад, 3хлорбензенкарбопероксова кислота, пероксoалканові кислоти, наприклад, пероксoоцтова кислота, алкілгідропероксиди, наприклад, трет-бутилгідропероксид. Придатними розчинниками є, наприклад, вода, нижчі спирти, наприклад, етанол тощо, вуглеводні, наприклад, толуен, кетони, наприклад, 2-бутанон, галогензаміщені вуглеводні, наприклад, дихлорметан, та суміші таких розчинників. Всі вихідні речовини можуть бути придбані комерційним шляхом або можуть бути одержані фахівцями у даній галузі. Чисті стереохімічно ізомерні форми сполук формули (RI) можна одержувати шляхом застосування процедур, відомих з рівня техніки. Діастереомери можуть бути розділені за допомогою фізичних способів, таких як селективна кристалізація, та хроматографічних методів, наприклад, протитечійного розподілу, рідинної хроматографії тощо. Придатними способами фізичного розділення, які можна переважно використовувати, є, наприклад, селективна кристалізація та хроматографія, наприклад, колонкова хроматографія. Сполуки формули (RI), які одержують за допомогою способів, описаних у даному документі вище, як правило, являють собою рацемічні суміші енантіомерів, що можуть бути відділені один від одного згідно з процедурами розділення, відомими з рівня техніки. Рацемічні сполуки формули (RI), що є достатньо основними або кислими, можуть бути перетворені на відповідні форми діастереомерних солей за допомогою реакції з придатною хіральною кислотою і, відповідно, хіральною основою. Зазначені діастереомерні сольові форми згодом розділяють, наприклад, шляхом селективної або фракційної кристалізації, а енантіомери виділяють з них за допомогою лугу або кислоти. Альтернативний спосіб розділення енантіомерних форм сполук формули (RI) включає рідинну хроматографію, зокрема, рідинну хроматографію із застосуванням хіральної нерухомої фази. Зазначені чисті стереохімічно ізомерні форми також можна одержати з відповідних чистих стереохімічно ізомерних форм придатних вихідних речовин за умови, що реакція проходить стереоспецифічно. Якщо необхідний певний стереоізомер, переважно, щоб зазначена сполука була синтезована за допомогою стереоспецифічних способів одержання. В цих способах переважно будуть використовуватися енантіомерно чисті вихідні речовини. В додатковому аспекті даний винахід стосується фармацевтичної композиції, яка містить терапевтично ефективну кількість сполуки формули (RI), визначеної в даному документі, або сполуки згідно з будь-яким з варіантів здійснення сполук формули (RI), визначеної в даному документі, та фармацевтично прийнятний носій. Терапевтично ефективна кількість у зазначеному контексті являє собою кількість, достатню для профілактичної дії проти вірусної інфекції, для її стабілізації або для її послаблення, та, зокрема, вірусної інфекції, спричинюваної RSV, у інфікованих суб'єктів або суб'єктів, що зазнають ризику бути інфікованими. У ще одному аспекті даний винахід стосується способу одержання фармацевтичної композиції, визначеної в даному документі, який включає ретельне перемішування фармацевтично прийнятного носія з терапевтично ефективною кількістю сполуки формули (RI), визначеної в даному документі, або 20 UA 114531 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуки за будь-яким з варіантів здійснення сполук формули (RI), визначеної в даному документі. Таким чином, сполуки згідно з даним винаходом або будь-який їх варіант здійснення можна скласти в різні фармацевтичні форми відповідно до цілей введення. Як придатні композиції можуть бути згадані всі композиції, що зазвичай використовують для системного введення лікарських препаратів. Для одержання фармацевтичних композицій за даним винаходом ефективну кількість конкретної сполуки, необов'язково у формі солі приєднання, як активний інгредієнт об'єднують у однорідну суміш з фармацевтично прийнятним носієм, при цьому носій може набувати широкого різноманіття форм залежно від форми препарату, необхідного для введення. Ці фармацевтичні композиції є бажаними у одиничній лікарській формі, придатній, зокрема, для перорального, ректального, черезшкірного введення або введення шляхом парентеральної ін'єкції. Переважним є пероральне введення. Наприклад, під час одержання композицій у формі пероральної лікарської форми можна застосовувати будь-яке загальноприйняте фармацевтичне середовище, таке як, наприклад, вода, гліколі, олії, спирти тощо, у випадку пероральних рідких препаратів, таких як суспензії, сиропи, міцні настої, емульсії та розчини; або тверді носії, такі як крохмалі, цукри, каолін, змащувальні речовини, зв'язувальні речовини, розпушувачі тощо, у випадку порошків, пігулок, капсул та таблеток. Завдяки простоті їх введення таблетки і капсули являють собою найбільш переважні пероральні форми одиниць дозування, у випадку яких, зрозуміло, застосовуються тверді фармацевтичні носії. У випадку композицій для парентерального введення носій буде, як правило, щонайменше значною мірою містити стерильну воду, хоча може включати й інші інгредієнти, наприклад, для поліпшення розчинності. Наприклад, можуть бути одержані розчини для ін'єкцій, в яких носій включає фізіологічний розчин, розчин глюкози або суміш фізіологічного розчину та розчину глюкози. Також можуть бути одержані суспензії для ін'єкцій, у випадку яких можна використовувати придатні рідкі носії, суспендувальні засоби тощо. Також включені препарати у твердій формі, які, згідно з інструкцією, необхідно перетворювати, безпосередньо перед застосуванням, на препарати в рідкій формі. В композиціях, придатних для підшкірного введення, носій необов'язково включає речовину, що сприяє проникненню, та/або придатний змочувальний засіб, необов'язково в комбінації з придатними добавками будь-якої природи в мінімальних пропорціях, при цьому добавки не чинять значного шкідливого впливу на шкіру. Сполуки згідно з даним винаходом можна також вводити шляхом пероральної інгаляції або інсуфляції за допомогою способів і препаратів, застосовуваних у даній галузі техніки для введення таким шляхом. Таким чином, сполуки згідно з даним винаходом у цілому можна вводити в легені у формі розчину, суспензії або сухого порошку, при цьому розчин є переважним. Будь-яка система, розроблена для доставки розчинів, суспензій або сухих порошків шляхом пероральної інгаляції або інсуфляції, є придатною для введення сполук згідно зданим винаходом. Таким чином, даний винахід також стосується фармацевтичної композиції, яка містить сполуку формули (RI) та фармацевтично прийнятний носій, пристосованої для введення шляхом інгаляції або інсуфляції через рот. Сполуки згідно з даним винаходом переважно вводять шляхом інгаляції розчину в розпилюваних або аерозольованих дозах. Особливо переважним є складання вищезазначених фармацевтичних композицій у формі одиничної лікарської форми для простоти введення і рівномірності дозування. Одинична лікарська форма, застосовувана в даному документі, стосується фізично окремих одиниць, що є придатними як одиничні дози, при цьому кожна одиниця містить попередньо встановлену кількість активного інгредієнта, розраховану для одержання необхідного терапевтичного ефекту, у поєднанні з необхідним фармацевтичним носієм. Прикладами таких одиничних лікарських форм є таблетки (у тому числі подільні таблетки або вкриті таблетки), капсули, пігулки, супозиторії, пакетики з порошком, пластинки, розчини або суспензії для ін'єкцій тощо, а також їх окремі множини. Сполуки формули (RI) демонструють противірусні властивості. Вірусні інфекції, які можна лікувати шляхом застосування сполук та способів згідно з даним винаходом, включають інфекції, спричинювані орто- та параміксовірусами та, зокрема, респіраторним синцитіальним вірусом (RSV) людини та великої рогатої худоби. Низка сполук згідно з даним винаходом, крім того, є активними проти мутантних штамів RSV. Крім того, багато зі сполук згідно з даним винаходом демонструють сприятливий фармакокінетичний профіль та характеризуються привабливими властивостями щодо біодоступності, включаючи прийнятний період напіввиведення, AUC та пікові значення, а також відсутність несприятливих явищ, таких як недостатньо швидкий початок дії та затримка у тканинах. 21 UA 114531 C2 5 10 15 20 25 30 35 40 45 Противірусну активність сполук згідно з даним винаходом проти RSV in vitro випробовували за допомогою тесту, що описаний у експериментальній частині опису, та її також можна продемонструвати із застосуванням аналізу зі зниженням врожаю вірусу. Противірусна активність сполук згідно з даним винаходом проти RSV in vivo може бути продемонстрована у тестовій моделі з застосуванням бавовняних хом'яків, як описано у Wyde et al. (Antiviral Research (1998), 38, 31-42). Завдяки противірусним властивостям, зокрема, своїм властивостям, спрямованим проти RSV, сполуки формули (RI) або будь-який з їх варіантів здійснення, їх таутомери та стереоізомерні форми, а також їх фармацевтично прийнятні солі приєднання та сольвати можна застосовувати у лікуванні індивідуумів з вірусною інфекцією, зокрема, з RSV-інфекцією, та для профілактики зазначених інфекцій. Загалом, сполуки згідно з даним винаходом можуть бути придатними у лікуванні теплокровних тварин, інфікованих вірусами, зокрема, респіраторним синцитіальним вірусом. Тому сполуки згідно з даним винаходом або будь-який їх варіант здійснення можна застосовувати в якості лікарських засобів. Зазначене застосування в якості лікарського засобу або спосіб лікування включають системне введення суб'єктам, інфікованим вірусом, або суб'єктам, сприйнятливим до вірусних інфекцій, кількості, ефективної для боротьби зі станами, асоційованими з вірусною інфекцією, зокрема, з RSV-інфекцією. Даний винахід також стосується застосування сполук згідно з даним винаходом або будьякого з їх варіантів здійснення у виготовленні медикаменту для лікування або профілактики вірусних інфекцій, зокрема, RSV-інфекції. Даний винахід також стосується способу лікування теплокровної тварини, інфікованої вірусом або яка піддається ризику інфікування вірусом, зокрема, RSV, при цьому зазначений спосіб включає введення ефективної кількості противірусної сполуки формули (RI), яка визначена у даному документі, або сполуки за будь-яким з варіантів здійснення сполук формули (RI), визначеної в даному документі. Точне дозування та частота введення залежать від конкретної застосовуваної сполуки формули (RI), конкретного стану, який підлягає лікуванню, тяжкості стану, який підлягає лікуванню, віку, ваги, статі, ступеня розладу та загального фізичного стану конкретного пацієнта, а також від іншого медикаментозного лікування, що індивідуум може отримувати, яке добре відомо фахівцям у даній галузі. Більш того, є очевидним, що зазначену ефективну добову кількість можна зменшувати або збільшувати залежно від реакції суб'єкта, що піддається лікуванню, та/або залежно від оцінювання лікарем, який призначає сполуки згідно з даним винаходом. Діапазони ефективної добової кількості, наведені далі у даному документі, є лише рекомендаційними. Крім того, в якості лікарського засобу можна застосовувати комбінацію іншого противірусного засобу та сполуки формули (RI). Таким чином, даний винахід також стосується продукту, що містить (a) сполуку формули (RI) та (b) іншу противірусну сполуку, як комбінованого препарату для одночасного, роздільного або послідовного застосування в противірусній терапії. Різні лікарські препарати можна поєднувати в один препарат разом з фармацевтично прийнятними носіями. Наприклад, сполуки згідно з даним винаходом можна поєднувати з інтерфероном-бета або фактором некрозу пухлин-альфа для лікування або попередження RSV-інфекції. Даний винахід далі в даному документі буде проілюстровано з посиланням на наступні необмежувальні приклади. Експериментальна частина Синтез проміжних сполук Проміжна сполука 1b. Синтез 2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону Спосіб 1 50 Br O N H O O Br O TMEDA, n-BuLi, THF, -78oC-25oC 1a N H 1b н-BuLi (108 мл, 216 ммоль, 2 M у THF) додавали до розчину оксіндолу 1a (номер CAS: 59-483, 11 г, 82,6 ммоль) при -78 °C у THF (1000 мл). Після завершення додавання додавали TMEDA 22 UA 114531 C2 5 (25 г, 214,76 ммоль), підтримуючи внутрішню температуру < -70 °C. Через 1 годину при -78 °C додавали біс(2-бромметиловий) ефір (номер CAS: 5414-19-7, 57,5 г, 247,8 ммоль), і реакційну суміш нагрівали до кімнатної температури. Через 48 годин реакційну суміш гасили за допомогою H2O, і суміш розділяли між EtOAc та H2O. Водний розчин екстрагували за допомогою EtOAc, і об'єднані органічні шари промивали за допомогою сольового розчину, сушили над Na2SO4, фільтрували та концентрували у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі з елююванням з градієнтом CH2Cl2:MeOH=100:0-97:3, одержуючи 8 % 2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 1b. Спосіб 2 10 Br O O Br O N H 1a 15 20 O LiHMDS, THF, -78oC-25oC N H 1b Оксіндол 1a (номер CAS: 59-48-3, 40 г, 264,659 ммоль) додавали до розчину LiHMDS (800 мл, 800 ммоль) при -78 °C. Суміш перемішували протягом 1 години при -78 °C. Згодом додавали біс(2-бромметиловий) ефір (номер CAS: 5414-19-7, 61,378 г, 264,659 ммоль), підтримуючи внутрішню температуру < -50 °C. Реакційну суміш нагрівали до кімнатної температури. Через 18 годин реакційну суміш гасили за допомогою H2O, і суміш розділяли між EtOAc та H2O. Водний розчин екстрагували за допомогою EtOAc, і об'єднані органічні шари промивали за допомогою сольового розчину, сушили над Na2SO4, фільтрували та концентрували у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі з елююванням з градієнтом петролейний ефір:етилацетат = 3:1, одержуючи 10,187 г (17 %) 2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2ону 1b. Проміжна сполука 2c. Синтез трет-бутил-2-оксоспіро[індолін-3,4'-піперидин]-1'-карбоксилату 25 30 35 40 45 Стадія 1 1'-Бензилспіро[індолін-3,4'-піперидин]-2-он 2a синтезували з виходом 59 % (52 г) згідно зі способом 2, який застосовують для синтезу 2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 1b із застосуванням N, N-біс(2-хлоретил)бензенметанаміну (номер CAS: 55-51-6, 70 г, 302 ммоль) замість біс(2-бромметилового) ефіру. Стадія 2 Розчин 1'-бензилспіро[індолін-3,4'-піперидин]-2-ону 2a (5 г, 17,10 ммоль, 1 екв.) в метанолі (100 мл) гідрогенізували за RT з 10 % Pd/C (0,18 г) як каталізатором протягом 15 годин. Каталізатор відфільтровували, і розчинник випарювали у вакуумі. Згодом залишок перекристалізовували з DIPE/ацетонітрилу з одержанням 2,7 г (вихід 78 %) спіро[індолін-3,4'піперидин]-2-ону 2b. Стадія 3 До розчину спіро[індолін-3,4'-піперидин]-2-ону 2b (2,73 г, 11,42 ммоль, 1 екв.) у THF (100 мл) додавали Boc2O (2,74 г, 12,57 ммоль) та триетиламін (2,38 мл, 17,135 ммоль) за RT. Суміш перемішували за кімнатної температури протягом 4 годин. Згодом розчинник випарювали у вакуумі, і залишок обробляли сумішшю води та DCM. Водний шар екстрагували за допомогою DCM (3x), і органічні шари об'єднували, сушили над Na 2SO4, фільтрували та концентрували з одержанням трет-бутил-2-оксоспіро[індолін-3,4'-піперидин]-1'-карбоксилату 2c (кількісний вихід 1 4,02 г) у формі білої піни. H-ЯМР (400 МГЦ, DMSO-d6) δ ppm 1,44 (s, 9 H), 1,56 – 1,73 (m, 4 H), 23 UA 114531 C2 3,55 – 3,79 (m, 4 H), 6,86 (dd, J=7,70, 0,40 Гц, 1 H), 6,95 (td, J=7,59, 1,10 Гц, 1 H), 7,19 (td, J=7,70, + 1,10 Гц, 1 H), 7,43 (dd, J=6,80, 0,70 Гц, 1 H), 10,41 (br. s., 1 H); маса/заряд = 303,05 (M+H) . Проміжна сполука 3f. Синтез трет-бутил-2'-оксоспіро[азетидин-3,3'-індолін]-1-карбоксилату 5 10 15 20 25 30 35 40 Стадія 1 До перемішаного розчину 2-броманіліну (150 г, 872 ммоль, 1 екв.) та DMAP (138,5 г, 1133 ммоль, 1,3 екв.) у CH2Cl2 (2500 мл) додавали N-(трет-бутоксикарбоніл)азетидин-3-карбонову кислоту (номер CAS: 142253-55-2, 176 г, 872 ммоль, 1 екв.) однією порцією з наступним додаванням EDCI (217 г, 1133 ммоль, 1,3 екв.) однією порцією за кімнатної температури. Одержану суміш перемішували за кімнатної температури протягом ночі. Згодом її послідовно промивали за допомогою 10 % водного розчину лимонної кислоти, води, насиченого водного розчину Na2CO3 та сольового розчину й сушили над Na2SO4. Після фільтрації розчинник видаляли у вакуумі з одержанням трет-бутил-3-((2-бромфеніл)карбамоїл)азетидин-1карбоксилату 3b (вихід 85 %, 328 г). Стадія 2 Суміш трет-бутил-3-((2-бромфеніл)карбамоїл)азетидин-1-карбоксилату 3b (307 г, 864 ммоль, 1 екв.), 4-метоксибензилхлориду (203 г, 1296 ммоль, 1,5 екв.) та K 2CO3 (358 г, 2593 ммоль, 3 екв.) у CH3CN (3000 мл) нагрівали зі зворотним холодильником протягом ночі. Згодом розчин фільтрували, і тверду речовину промивали за допомогою CH 3CN (1000 мл). Фільтрат концентрували у вакуумі, і неочищений продукт розтирали у суміші петролейний ефір/етилацетат (30:1) з одержанням трет-бутил-3-((2-бромфеніл)(4метоксибензил)карбамоїл)азетидин-1-карбоксилату 3c (вихід 90 %, 380 г). Стадія 3 Pd(OAc)2 (2,25 г, 10 ммоль, 0,025 екв.) та PCy3 (2,8 г, 10 ммоль, 0,025 екв.) додавали до розчину трет-бутил-3-((2-бромфеніл)(4-метоксибензил)карбамоїл)азетидин-1-карбоксилату 3c (190 г, 400 ммоль, 1 екв.) та трет-BuONa (57,6 г, 600 ммоль, 1,5 екв.) в діоксані (960 мл) в атмосфері N2. Реакційну суміш перемішували при 90 °C протягом ночі в атмосфері N2. Згодом розчин фільтрували та концентрували у вакуумі. Залишок розчиняли у CH 2Cl2, промивали задопомогою NH4Cl, сольового розчину та сушили над Na2SO4. Розчинник видаляли у вакуумі з одержанням 158 г (кількісний вихід) трет-бутил-1'-(4-метоксибензил)-2'-оксоспіро[азетидин-3,3'індолін]-1-карбоксилату 3d. Стадія 4 CF3SO3H (119 мл, 1350 ммоль, 3 екв.) додавали до суміші трет-бутил-1'-(4-метоксибензил)2'-оксоспіро[азетидин-3,3'-індолін]-1-карбоксилату 3d (178 г, 450 ммоль, 1 екв. неочищеного продукту) у TFA (750 мл). Суміш перемішували протягом ночі при 25 °C. Розчинник згодом видаляли у вакуумі, і залишок (78,4 г) використовували безпосередньо на наступній стадії. Стадія 5 Розчин спіро[азетидин-3,3'-індолін]-2'-ону 3e (78,4 г, 450 ммоль, 1 екв. неочищеного продукту) у CH2Cl2 (1500 мл) виливали у суміш K2CO3 (186,6 г, 1350 ммоль, 3 екв.) у крижаній 24 UA 114531 C2 5 воді (1500 мл). Водний шар відділяли та промивали за допомогою CH 2Cl2 (3*500 мл). Водний шар розводили у THF (1500 мл) та додавали (Boc) 2O (98,2 г, 450 ммоль, 1 екв.). Розчин перемішували протягом ночі. 500 мл розчину аміаку в MeOH (7M) згодом додавали краплинами до згаданого вище розчину. Органічний розчинник випарювали у вакуумі. Водний розчин екстрагували за допомогою CH 2Cl2 (800 мл*3), промивали за допомогою сольового розчину, сушили над Na2SO4, фільтрували та згодом концентрували у вакуумі. Одержаний залишок промивали за допомогою трет-бутилметилового ефіру з одержанням чистого продукту третбутил-2'-оксоспіро[азетидин-3,3'-індолін]-1-карбоксилату 3f (вихід 37 %, 44 г). Проміжні сполуки 4c та 4d. Синтез (3S) та (3R)-гідроксиспіро[циклобутан-1,3'-індолін]-2'-ону 10 15 20 25 30 35 40 45 Стадія 1 Суміш, що складається з бензилброміду (62,43 г, 365,03 ммоль, 1 екв.), 2(бромметил)оксирану (50 г, 365,03 ммоль, 1 екв.) та HgCl2 (100 мг), нагрівали з перемішуванням при 155 °C протягом 16 годин у колбі, обладнаній зворотним холодильником. Продукт виділяли за допомогою вакуумної перегонки за допомогою зворотного холодильника Vigreux (110-115, 0,5 мм рт. ст.) на 30 см з одержанням безбарвної рідини. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: дихлорметан) з одержанням 65 г (((1,3дибромпропан-2-іл)окси)метил)бензену 4a. Стадія 2 Оксіндол 1a (20 г, 150,210 ммоль, 1 екв.) розчиняли в THF (400 мл) та HMPA (40 мл). Реакційну суміш охолоджували до -78 °C, згодом додавали n-BuLi (132,185 мл, 330,462 ммоль, 2,2 екв.). Реакційну суміш перемішували при -78 °C протягом 1 години. Згодом додавали (((1,3дибромпропан-2-іл)окси)метил)бензен 4a (46,27 г, 150,210 ммоль, 1 екв.). Суміш послідовно перемішували за кімнатної температури протягом 14 годин, гасили за допомогою води та екстрагували за допомогою дихлорметану. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: петролейний ефір:етилацетат 10:1). Фракції продукту збирали, і розчинник випарювали з одержанням 15 г необхідного продукту 3(бензилокси)спіро[циклобутан-1,3'-індолін]-2'-ону 4b. Стадія 3 Суміш 3-(бензилокси)спіро[циклобутан-1,3'-індолін]-2'-ону 4b (15 г, 53,699 ммоль, 1 екв.) та Pd/C (1,5 г) в метанолі (150 мл) гідрогенізували під тиском 30 фунтів/кв. дюйм протягом 15 годин. Реакційну суміш фільтрували крізь прокладку з целіту, яку промивали декілька разів за допомогою CH3OH. Об'єднані фільтрати випарювали до сухого стану. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: петролейний ефір:етилацетат = 3:1) з одержанням рацемічної суміші (3)-гідроксиспіро[циклобутан-1,3'-індолін]-2'-ону, енантіомери якого 4c та 4d розділяли за допомогою високоефективної рідинної хроматографії (умови HPLC: колонка: SYNERGI 250*50 10 мкм, швидкість потоку: 80 мл/хвилина, рухома фаза A: очищена вода (яка містить 0,075 % TFA), рухома фаза B: ацетонітрил, градієнт: 5-30 % (% B)). Необхідні фракції збирали, випарювали з видаленням CH 3CN у вакуумі та підлужували за допомогою насиченого розчину NaHCO3. Водний розчин екстрагували за допомогою CH2Cl2. Органічні шари сушили, фільтрували, і розчинник випарювали з одержанням 4,59 г (3S)гідроксиспіро[циклобутан-1,3'-індолін]-2'-ону 4c та 0,89 г (3R)-гідроксиспіро[циклобутан-1,3'індолін]-2'-ону 4d. Проміжна сполука 5c. Синтез трет-бутил-5-фтор-2-оксоспіро[індолін-3,4'-піперидин]-1'карбоксилату 25 UA 114531 C2 5 10 15 20 25 30 5-Фторіндолін-2-он 5a (35 г, 231,576 ммоль, 1 екв.) додавали до розчину LiHMDS (700 мл, 700 ммоль, 3 екв.) при -78 °C. Суміш перемішували протягом 1 години при -78 °C, згодом додавали трет-бутил-біс(2-хлоретил)карбамат 5b (56,075 г, 231,576 ммоль, 1 екв.), підтримуючи внутрішню температуру < -50 °C. Реакційну суміш згодом нагрівали до кімнатної температури протягом 2 годин, і реакційну суміш нагрівали зі зворотним холодильником протягом ночі. Суміш гасили за допомогою H2O, і суміш розділяли між EtOAc та H2O. Водний розчин екстрагували за допомогою EtOAc, і об'єднані органічні шари промивали за допомогою сольового розчину, сушили над Na2SO4, фільтрували та концентрували у вакуумі. Одержаний залишок очищали за допомогою високоефективної рідинної хроматографії (умови HPLC: колонка: Synergi-10 мкм, 250×50 мм I.D., швидкість потоку: 80 мл/хвилина, рухома фаза A: очищена вода (яка містить 0,1 % TFA), рухома фаза B: ацетонітрил, градієнт: 35-65 % (% B)) з одержанням 5,003 г (7 % вихід) трет-бутил-5-фтор-2-оксоспіро[індолін-3,4'-піперидин]-1'-карбоксилату 5c. Проміжна сполука 6a. Синтез 5-фтор-2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 5-Фторіндолін-2-он 5a (30 г, 198,49 ммоль, 1,0 екв.) додавали до LiHMDS (1 M у THF, 595,48 мл, 595,48 ммоль, 3,0 екв.) при -78 °C. Суміш перемішували при -78 °C протягом 10 хвилин та нагрівали до 0 °C. Суміш перемішували при 0 °C протягом 30 хвилин, згодом додавали біс(2бромметиловий) ефір (номер CAS: 5414-19-7, 46,03 г, 198,49 ммоль, 1,0 екв.). Суміш перемішували за кімнатної температури протягом ночі. Додавали воду (300 мл) у реакційну суміш. Одержаний осад відфільтровували та промивали за допомогою води з одержанням 5фтор-2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 6a (вихід 13 %, 12 г). Проміжна сполука 7b. Синтез 4-фтор-2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 4-Фторіндолін-2-он 7a (9,5 г, 62,856 ммоль, 1,0 екв.) додавали до LiHMDS (1 M у THF, 188,568 мл, 188,568 ммоль, 3,0 екв.) при -78 °C. Суміш перемішували при -78 °C протягом 10 26 UA 114531 C2 5 10 15 20 25 30 35 40 хвилин та нагрівали до 0 °C. Суміш перемішували при 0 °C протягом 30 хвилин, згодом додавали біс(2-бромметиловий) ефір (14,577 г, 62,856 ммоль, 1,0 екв.). Суміш перемішували за кімнатної температури протягом ночі. Додавали воду (300 мл) у реакційну суміш. Одержану тверду речовину відфільтровували та промивали за допомогою води з одержанням 4-фтор2',3',5',6'-тетрагідроспіро[індолін-3,4'-піран]-2-ону 7b (вихід 12 %, 1,61 г). Проміжна сполука 8d. Синтез спіро[циклопентан-1,3'-піроло[2,3-c]піридин]-2'(1'H)-ону Стадія 1 До розчину трет-бутилетилмалонату (160 г, 850 ммоль) у THF (1600 мл) додавали порціями NaH (80 г, 2118 ммоль) при 0 °C. Суміш перемішували протягом 1 години при 15 °C, згодом додавали порціями 4-хлор-3-нітропіридин (112 г, 706 ммоль) при 0 °C. Суміш перемішували протягом 1 години при 15 °C. Реакційну суміш гасили за допомогою води, і додавали 1 н. HCl до досягнення рН=5. Суміш двічі екстрагували за допомогою етилацетату. Органічні шари промивали за допомогою сольового розчину, сушили та випарювали у вакуумі з одержанням 1(трет-бутил)-3-етил-2-(3-нітропіридин-4-іл)малонату 8a (250 г), який використовували без додаткового очищення на наступній стадії. Стадія 2 До розчину 1-(трет-бутил)-3-етил-2-(3-нітропіридин-4-іл)малонату 8a (неочищений продукт, 250 г, 706 ммоль) у CH2Cl2 (1500 мл) додавали TFA (250 мл). Через 14 годин перемішування при 60 °C суміш випарювали. Згодом додавали 10 % водний розчин NaHCO3, і суміш двічі екстрагували за допомогою етилацетату. Органічні шари промивали за допомогою сольового розчину, сушили та випарювали у вакуумі з одержанням етил-2-(3-нітропіридин-4-іл)ацетату 8b (180 г), який використовували без додаткового очищення на наступній стадії. Стадія 3 Етил-2-(3-нітропіридин-4-іл)ацетат 8b (50 г, 238 ммоль), 1,4-дибромбутан (50 г, 238 ммоль), K2CO3 (100 г, 714 ммоль) та молекулярне сито 4A (50 г) в DMF (500 мл) перемішували протягом 14 годин при 80 °C. Згодом додавали 1 н. HCl, і суміш двічі екстрагували за допомогою CH 2Cl2. Органічні шари промивали за допомогою 10 % водного розчину NaHCO3 (2x), сольового розчину (2x), сушили та випарювали у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: CH2Cl2/етилацетат = 10/1) з одержанням 8,4 г (вихід 15 % в цілому для трьох стадій) етил-1-(3-нітропіридин-4-іл)циклопентан-1-карбоксилату 8c. Стадія 4 Етил-1-(3-нітропіридин-4-іл)циклопентан-1-карбоксилат 8c (8,4 г, 31,8 ммоль), Fe (7 г, 127 ммоль) та NH4Cl (7 г, 127 ммоль) у CH3OH (80 мл), THF (80 мл) та H2O (80 мл) перемішували та нагрівали зі зворотним холодильником протягом 3 годин. Згодом суміш відфільтровували, і розчинник випарювали у вакуумі. Додавали 10 % водний розчин NaHCO3, і суміш екстрагували за допомогою етилацетату (3x). Об'єднані органічні шари промивали за допомогою сольового розчину, сушили та випарювали у вакуумі. Залишок промивали за допомогою CH3CN (2x), і тверду речовину збирали та сушили з одержанням 4 г (вихід 67 %) спіро[циклопентан-1,3'піроло[2,3-c]піридин]-2'(1'H)-ону 8d. Проміжна сполука 9c. Синтез 2,3,5,6-тетрагідроспіро[піран-4,3'-піроло[2,3-c]піридин]-2'(1'H)ону 27 UA 114531 C2 5 10 15 20 25 30 Стадія 1. Синтез етил-2-(3-амінопіридин-4-іл)ацетату (проміжної сполуки 9a) Суміш етил-2-(3-нітропіридин-4-іл)ацетату 8b (65 г, 309 ммоль, чистота 90 %, 1 екв.) в метанолі (1500 мл) гідрогенізували при 20 °C (атмосферний тиск) за допомогою 10 % Pd/C (6,5 г) як каталізатора протягом 16 годин. Після поглинання H 2 (3 еквів.) каталізатор відфільтровували, а фільтрат випарювали у вакуумі з одержанням 50 г (вихід: 90 %) етил-2-(3амінопіридин-4-іл)ацетату9a, який використовували без додаткового очищення на наступній стадії. Стадія 2. Синтез 1,3-дигідро-2H-піроло[2,3-c]піридин-2-ону (проміжної сполуки 9b) Етил-2-(3-амінопіридин-4-іл)ацетат 9a (34 г, 189 ммоль, 1 екв.) розчиняли у 1,4 н. HCl (1000 мл) та діізопропіловому ефірі (1000 мл). Суміш перемішували за кімнатної температури протягом ночі. Відділюваний органічний шар відділяли та промивали за допомогою H 2O. Об'єднані водні шари промивали за допомогою CH 2Cl2 та випарювали майже насухо. Одержаний осад відфільтровували та сушили (вакуум, 60 °C, 2 години) з одержанням 26 г (вихід: 94 %) 1,3-дигідро-2H-піроло[2,3-c]піридин-2-ону 9b у формі солі хлороводневої кислоти. Стадія 3. Синтез 2,3,5,6-тетрагідроспіро[піран-4,3'-піроло[2,3-c]піридин]-2'(1'H)-ону (проміжної сполуки 9c) 1,3-Дигідро-2H-піроло[2,3-c]піридин-2-он 9b (12 г, 70,34 ммоль, 1,05 екв.) додавали до розчину 1 M LiHMDS у THF (281 мл, 281 ммоль, 4 екв.) при -78 °C. Суміш перемішували при 78 °C протягом 10 хвилин та нагрівали до 0 °C природним шляхом. Після перемішування при 0 °C протягом 0,5 години додавали 1-бром-2-(2-брометоксі)етан (15,54 г, 66,99 ммоль, 1 екв.). Суміш нагрівали до 20 °C та перемішували при 20 °C протягом 0,5 години, згодом нагрівали зі зворотним холодильником протягом ночі. Після охолодження до кімнатної температури реакційну суміш послідовно гасили за допомогою 10 % розчину NH4Cl (300 мл) та екстрагували за допомогою етилацетату (2*300 мл). Об'єднані органічні шари промивали за допомогою сольового розчину, сушили (Na2SO4), фільтрували, і розчинник випарювали у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: CH 2Cl2:метанол від 1:0 до 20:1) з одержанням 1,735 г (вихід 12 %) 2,3,5,6-тетрагідроспіро[піран-4,3'-піроло[2,3c]піридин]-2'(1'H)-ону 9c. Проміжна сполука 10c. Синтез трет-бутил-2'-оксо-1',2'-дигідроспіро[піперидин-4,3'-піроло[2,3c]піридин]-1-карбоксилату 28
ДивитисяДодаткова інформація
Назва патенту англійськоюRsv antiviral compounds
Автори англійськоюTahri, Abdellah, Vendeville, Sandrine, Marie, Helene, Jonckers, Tim Hugo Maria, Raboisson, Pierre Jean-Marie Bernard, Hu, Lili, Demin, Samuel Dominique, Cooymans, Ludwig Paul
Автори російськоюТахри Абделлах, Вендевилль Сандрин Мари Элен, Йонкерс Тим Хьюго Мария, Рабуассон Пьер Жан-Мари Бернар, Ху Лили, Демен Самюель Доминик, Коиманс Людвиг Поль
МПК / Мітки
МПК: C07D 487/10, C07D 403/14, C07D 471/04, A61K 31/4184, C07D 491/107, C07D 495/20, C07D 471/10, A61K 31/498, A61K 31/435, C07D 471/20, C07D 519/00, C07D 403/06, C07D 491/20, A61K 31/501
Мітки: сполуки, противірусні
Код посилання
<a href="https://ua.patents.su/90-114531-protivirusni-spoluki-proti-rsv.html" target="_blank" rel="follow" title="База патентів України">Противірусні сполуки проти rsv</a>
Попередній патент: Вдосконалений спосіб одержання металів
Наступний патент: Корпус пневматичного дозатора насіння з запобіганням насіннєвому проходу
Випадковий патент: Спосіб лікування епілепсії у дітей і підлітків