Похідні азабіфеніламінобензойної кислоти як інгібітори dhodh
Номер патенту: 99734
Опубліковано: 25.09.2012
Автори: Кастро Паломіно Ларія Хуліо Сезар, Наварро Ромеро Елоіза, Фонкерна Поу Сільвія, Лосоя Торібіо Марія Естрелла, Террікабрас Беларт Емма, Кардус Фігуерас Арансасу, Ерра Сола Монтсеррат
Формула / Реферат
1. Сполука формули (І) для застосування для лікування або профілактики патологічного стану або захворювання, чутливого до полегшення шляхом інгібування дегідрооротатдегідрогенази:
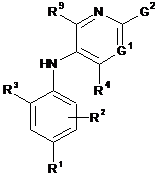 ,
,
де:
R1 вибраний із групи, яка складається із атомів водню, атомів галогену, С1-4алкілу, С3-4циклоалкілу, -CF3 та -OCF3,
R2 вибраний із групи, яка складається із атомів водню, атомів галогену та С1-4алкільної групи,
R3 вибраний із групи, яка складається із -COOR5, -CONHR5, тетразолілу, груп SO2NHR5 та -CONHSO2R5, де R5 вибраний із групи, яка складається із атома водню та лінійних або розгалужених C1-4алкільних груп,
R4 вибраний із групи, яка складається із атома водню та C1-4алкільної групи;
R9 вибраний із групи, яка складається із атома водню та фенільної групи,
G1 являє собою групу, вибрану із N та CR6, де R6 вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4алкілу, С3-4циклоалкілу, C1-4алкокси, -CF3, -OCF3, моноциклічних N-вмісних С5-7гетероарильних, моноциклічних N-вмісних С3-7гетероциклільних груп та С6-10арильної групи, яка необов'язково заміщена одним або декількома замісниками, вибраними із атомів галогену та C1-4алкільної групи,
G2 являє собою групу, вибрану із:
атома водню, гідроксигрупи, атома галогену, С3-4циклоалкільної групи, C1-4алкоксигрупи та -NRaRb, де
Ra являє собою C1-4алкільну групу, та Rb вибраний із групи, яка складається із C1-4алкільної групи та C1-4алкоксі-C1-4алкільної групи, або
Ra та Rb разом з атомом азоту, до якого вони приєднані, утворюють насичене 6-8-членне гетероциклічне кільце, яке необов'язково містить один атом кисню як додатковий гетероатом,
моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить один або декілька атомів азоту, яке необов'язково заміщене одним або декількома замісниками, вибраними із атомів галогену, C1-4алкілу, C1-4алкокси, С3-4циклоалкілу, С3-4циклоалкокси, -CF3, -OCF3 та -CONR7R8, де R7 та R8 незалежно вибрані із атома водню, лінійної або розгалуженої C1-4алкільної групи, С3-7циклоалкільної групи, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
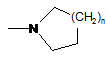 ,
,
де n має значення від 0 до 3, та
фенільної групи, яка необов'язково заміщена одним або декількома замісниками, вибраними із атомів галогену, C1-4алкілу, гідрокси, C1-4алкокси, С3-4циклоалкілу, С3-4циклоалкокси, ціано, -CF3, -OCF3, CONR7R8, оксадіазолільних, триазолільних, піразолільних та імідазолільних груп, де оксадіазолільні, триазолільні, піразолільні та імідазолільні групи необов'язково заміщені C1-4алкільною або С3-7циклоалкільною групою, та де R7 та R8 незалежно вибрані із атома водню, лінійної або розгалуженої C1-4алкільної групи, С3-7циклоалкільної групи, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
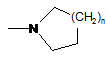 ,
,
де n має значення від 0 до 3;
або G2 разом з R6 утворює неароматичну С5-10карбоциклічну групу або С6-10арильну групу, і її фармацевтично прийнятні солі та N-оксиди.
2. Сполука за п. 1, де патологічний стан або захворювання вибрано із ревматоїдного артриту, псоріатичного артриту, анкілозуючого спондиліту, розсіяного склерозу, гранулематозу Вегенера, системного червоного вовчака, псоріазу та саркоїдозу.
3. Сполука за п. 1 або п. 2, де R1 вибраний із групи, яка складається із атомів водню, атомів фтору, атомів хлору, атомів брому, C1-4алкілу, С3-4циклоалкілу та груп -CF3.
4. Сполука за будь-яким із попередніх пунктів, де R2 вибраний із групи, яка складається із атома водню, атома галогену та метильної групи.
5. Сполука за будь-яким із попередніх пунктів, де G1 вибраний із групи, яка складається із атома азоту, груп ССl, CF, СН, С(СН3), С(циклопропіл), С(феніл) та C(CF3).
6. Сполука за будь-яким із попередніх пунктів, де G2 являє собою групу, вибрану із:
атома водню, атома галогену, С3-4циклоалкільної групи, С1-2алкоксигрупи та -NRaRb, де
Ra являє собою С1-2алкільну групу, та Rb вибраний із групи, яка складається із С1-2алкільних груп та С1-2алкоксі-С1-2алкільних груп, або
Ra та Rb разом з атомом азоту, до якого вони приєднані, утворюють насичене 6- або 7-членне гетероциклічне кільце, яке необов'язково містить один атом кисню як додатковий гетероатом,
моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить один або два атома азоту, яке необов'язково заміщене одним або декількома замісниками, вибраними із атомів галогену та C1-4алкільних груп, та
фенільної групи, яка необов'язково заміщена одним, двома або трьома замісниками, вибраними із атомів галогену, C1-4алкілу, гідроксилу, C1-4алкокси, С3-4циклоалкілу, С3-4циклоалкокси, ціано, -CF3, -OCF3, -CONR7R8 та оксадіазолільних груп, де оксадіазолільна група необов'язково заміщена C1-4алкільною або С3-7циклоалкільною групою, та де R7 та R8 незалежно вибрані із атомів водню, лінійних або розгалужених C1-4алкільних груп, С3-4циклоалкільних груп, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
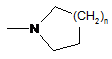 ,
,
де n означає 1 або 2,
або G2 разом з R6 утворює неароматичну С6карбоциклічну групу або фенільну групу.
7. Сполука за будь-яким із попередніх пунктів, де G2 являє собою групу, вибрану із:
атома водню, атома фтору, циклопропільної групи, метоксигрупи, NMeEt, -NEt2, -N(Me)-(CH2)2-O-CH3, 6-морфолінілу, азепан-1-ілу та піперидин-1-ілу,
піридинільного, піримідинільного, хінолінільного або піразинільного кільця, необов'язково заміщеного одним або двома замісниками, вибраними із Me та F,
та
фенільної групи, яка необов'язково заміщена одним, двома або трьома замісниками, вибраними із фтору, хлору, метилу, гідрокси, метокси, етокси, ізопропілокси, циклопропілу, циклопропілокси, ціано, -CF3, -OCF3, оксадіазолілу та груп -CONR7R8, де оксадіазолільна група необов'язково заміщена метильною групою, та де R7 та R8 незалежно вибрані із атома водню, метильної групи, ізопропільної групи, циклопропільної групи, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
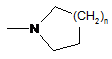 ,
,
де n означає 1,
або G2 разом з R6 утворюють неароматичну С6карбоциклічну групу або фенільну групу.
8. Сполука за будь-яким із попередніх пунктів, де G2 являє собою групу, вибрану із метоксигрупи, циклопропільної групи та необов'язково заміщених фенільної, піридильної, хінолінільної, піримідинільної та піразинільної груп.
9. Сполука за п. 1 або п. 2, де:
R1 вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4алкілу, С3-4циклоалкілу, -CF3 та -OCF3,
R2 вибраний із групи, яка складається із атомів водню, атомів галогену та C1-4алкільної групи,
R3 вибраний із групи, яка складається із -COOR5, -CONHR5, тетразолілу, груп SO2NHR5 та -CONHSO2R5, де R5 вибраний із групи, яка складається із атома водню та лінійних або розгалужених C1-4алкільних груп,
R4 вибраний із групи, яка складається із атома водню та C1-4алкільної групи,
R9 являє собою атом водню,
G1 являє собою групу, вибрану із N та CR6, де R6 вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4алкілу, С3-4циклоалкілу, C1-4алкокси, -CF3, -OCF3, моноциклічних N-вмісних С5-7гетероарильних, моноциклічних N-вмісних С3-7гетероциклільних груп та С6-10арильної групи, яка необов'язково заміщена одним або декількома замісниками, вибраними із атомів галогену та C1-4алкільної групи,
G2 являє собою групу, вибрану із:
моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить атом азоту, який необов'язково заміщений одним або декількома замісниками, вибраними із атомів галогену, C1-4алкілу, C1-4алкокси, С3-4циклоалкілу, С3-4циклоалкокси, -CF3, -OCF3 та CONR7R8, де R7 та R8 незалежно вибрані із атома водню, лінійної або розгалуженої C1-4алкільної групи, С3-7циклоалкільної групи, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
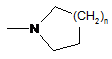 ,
,
де n має значення від 0 до 3, та
фенільної групи, яка необов'язково заміщена одним або декількома замісниками, вибраними із атомів галогену, C1-4алкілу, C1-4алкокси, С3-4циклоалкілу, С3-4циклоалкокси, -CF3, -OCF3, -CONR7R8, оксадіазолільних, триазолільних, піразолільних та імідазолільних груп, де оксадіазолільні, триазолільні, піразолільні та імідазолільні групи необов'язково заміщені C1-4алкільною або С3-7циклоалкільною групою, та де R7 та R8 незалежно вибрані із атома водню, лінійної або розгалуженої C1-4алкільної групи, С3-7циклоалкільної групи, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
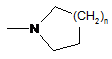 ,
,
де n має значення від 0 до 3.
10. Сполука за будь-яким із попередніх пунктів, де R1 вибраний із групи, яка складається із C1-4алкілу, С3-4циклоалкілу та груп -CF3.
11. Сполука за будь-яким із попередніх пунктів, де R1 вибраний із групи, яка складається із метильних та циклопропільних груп.
12. Сполука за будь-яким із попередніх пунктів, де R1 являє собою циклопропільну групу.
13. Сполука за будь-яким із попередніх пунктів, де R2 вибраний із атома водню або галогену.
14. Сполука за будь-яким із попередніх пунктів, де R2 являє собою атом водню.
15. Сполука за будь-яким із попередніх пунктів, де R3 вибраний із групи, яка складається із COOR5, -CONHR5та тетразолільних груп.
16. Сполука за будь-яким із попередніх пунктів, де R3 являє собою групу -СООН.
17. Сполука за будь-яким із попередніх пунктів, де R4 являє собою атом водню або метильну групу.
18. Сполука за будь-яким із попередніх пунктів, де R9 являє собою атом водню.
19. Сполука за будь-яким із попередніх пунктів, де G1 вибраний із групи, яка складається із атомів азоту та груп СН, С(СН3), С(циклопропіл), С(феніл) та C(CF3).
20. Сполука за будь-яким із попередніх пунктів, де G2 являє собою групу, вибрану із необов'язково заміщених фенільної, піридильної, хінолінільної, піримідинільної та піразинільної груп.
21. Сполука за будь-яким із попередніх пунктів, де G2 являє собою групу, вибрану із групи, яка складається із необов'язково заміщених фенільної, 4-піридильної, 5-хінолінільної та 2-піразинільної груп.
22. Сполука за п. 1 або п. 2, де R1 вибраний із метильної або циклопропільної групи, R2 являє собою атом водню, R3 являє собою групу СООН, R4 являє собою атом водню або метильну групу, G1 вибраний із атомів азоту та груп СН, С(СН3), С(циклопропіл), С(феніл) та C(CF3), та G2 являє собою групу, вибрану із групи, яка складається із необов'язково заміщених фенільних, 4-піридильних, 5-хінолінільних та 2-піразинільних груп.
23. Сполука за п. 22, де R9 являє собою атом водню.
24. Сполука за п. 1 або п. 2, де R1 вибраний із метильної або циклопропільної групи, R2 являє собою атом водню, R3 являє собою групу СООН, R4 являє собою атом водню, G1 вибраний із атомів азоту та груп СН, С(СН3) та C(CF3), та G2 являє собою фенільну групу, необов'язково заміщену одним або двома замісниками, вибраними із хлору, фтору, метокси, етокси, ізопропокси, трифторметокси та -CONR7R8, де R7 являє собою водень та R8 являє собою циклопропіл, або R7 та R8 разом з атомом азоту, до якого вони приєднані, утворюють групу формули:
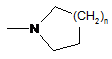 ,
,
де n означає 1.
25. Сполука за п. 1 або п. 2, яка вибрана з групи наступних сполук:
5-циклопропіл-2-(2-фенілпіримідин-5-іламіно)бензойна кислота,
2-(6-циклопропіл-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
1-оксид 5-(2-карбокси-4-циклопропілфеніламіно)-3-метил-2-фенілпіридину,
5-метил-2-(6-(3-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота,
5-циклопропіл-2-(6-гідрокси-5-фенілпіридин-3-іламіно)бензойна кислота,
5-циклопропіл-2-(2-(2,6-дифтор-4-гідроксифеніл)піримідин-5-іламіно)бензойна кислота,
5-циклопропіл-2-(6-метокси-5-фенілпіридин-3-іламіно)бензойна кислота,
2-(5-фтор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(етил(метил)аміно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
5-циклопропіл-2-(3'-фтор-2,4'-біпіридин-5-іламіно)бензойна кислота,
2-(6-(діетиламіно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-((2-метоксіетил)(метил)аміно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(5-хлор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота,
5-циклопропіл-2-(2-(2-циклопропілфеніл)піримідин-5-іламіно)бензойна кислота,
5-циклопропіл-2-(5-фенілпіридин-3-іламіно)бензойна кислота,
5-метил-2-(хінолін-3-іламіно)бензойна кислота,
5-метил-2-(5,6,7,8-тетрагідрохінолін-3-іламіно)бензойна кислота,
2-(5-хлор-2-фенілпіридин-3-іламіно)-5-метилбензойна кислота,
5-циклопропіл-2-(5,6-дифенілпіридин-3-іламіно)бензойна кислота,
5-циклопропіл-2-(2-(2,6-дифторфеніл)піримідин-5-іламіно)бензойна кислота,
5-циклопропіл-2-(5-метилпіридин-3-іламіно)бензойна кислота,
2-(2-(3-циклопропоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
5-метил-2-(6-морфолінопіридин-3-іламіно)бензойна кислота,
5-метил-2-(5-метил-6-морфолінопіридин-3-іламіно)бензойна кислота,
5-циклопропіл-2-(6-циклопропіл-5-фенілпіридин-3-іламіно)бензойна кислота,
2-(6-(2-циклопропілфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2-ціанофеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(2-(3-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
5-метил-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота,
5-метил-2-(5-метил-6-(піперидин-1-іл)піридин-3-іламіно)бензойна кислота,
2-(6-(азепан-1-іл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензойна кислота,
2-(2,3'-біпіридин-5-іламіно)-5-циклопропілбензойна кислота,
2-(3'-хлор-2,4'-біпіридин-5-іламіно)-5-метилбензойна кислота,
5-метил-2-(3-метил-2,2'-біпіридин-5-іламіно)бензойна кислота,
2-(5,6-дифторпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-метоксифеніл)піридин-3-іламіно)бензойна кислота,
2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота,
2-(6-(3-етоксифеніл)піридин-3-іламіно)-5-фторбензойна кислота,
2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота,
2-(6-(3-етоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-етокси-2-фторфеніл)піридин-3-іламіно)бензойна кислота,
2-(6-(3-етоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-етоксифеніл)-4-метилпіридин-3-іламіно)бензойна кислота,
5-бром-2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота,
5-хлор-2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота,
2-(6-(5-етокси-2-фторфеніл)піридин-3-іламіно)бензойна кислота,
2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)-5-(трифторметил)бензойна кислота,
2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-5-(трифторметил)бензойна кислота,
2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-6-метилбензойна кислота,
5-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота,
2-(6-(5-етокси-2-фторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2-фтор-5-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(2-фтор-5-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(2-фторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензойна кислота,
(і) етил-2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензоат,
5-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота,
(іі) етил-5-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат,
5-метил-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензойна кислота,
етил-5-метил-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензоат,
2-(5-циклопропіл-6-(3-метоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(5-циклопропіл-6-(3-метоксифеніл)піридин-3-іламіно)-5-метилбензоат,
2-(6-(2-фтор-5-ізопропоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(3-циклопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
(ііі) тpeт-бутил-2-(6-(3-циклопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(2-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
тpeт-бутил-2-(6-(2-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(3-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(3-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(2-фтор-5-метоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(2-фтор-5-метоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)-5-метилбензоат,
2-(6-(3-(диметилкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(3-(диметилкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-3-метилбензойна кислота,
тpeт-бутил-2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-3-метилбензоат,
3-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота,
тpeт-бутил-3-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат,
2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-метилбензоат,
3-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота,
тpeт-бутил-3-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензоат,
5-циклопропіл-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензойна кислота,
етил-5-циклопропіл-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензоат,
5-циклопропіл-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота,
етил-5-циклопропіл-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат,
5-метил-2-(5-метил-6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота,
трет-бутил-5-метил-2-(5-метил-6-(2-(трифторметил)феніл)піридин-3-іламіно)бензоат,
2-(6-(3-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(6-(3-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
2-(6-(2-фторфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(6-(2-фторфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат,
5-метил-2-(5-метил-6-(хінолін-5-іл)піридин-3-іламіно)бензойна кислота,
трет-бутил-5-метил-2-(5-метил-6-(хінолін-5-іл)піридин-3-іламіно)бензоат,
2-(3'-фтор-3-метил-2,4'-біпіридин-5-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(3'-фтор-3-метил-2,4'-біпіридин-5-іламіно)-5-метилбензоат,
5-метил-2-(5-метил-6-(піразин-2-іл)піридин-3-іламіно)бензойна кислота,
трет-бутил-5-метил-2-(5-метил-6-(піразин-2-іл)піридин-3-іламіно)бензоат,
5-циклопропіл-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота,
етил-5-циклопропіл-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензоат,
5-циклопропіл-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)бензойна кислота,
етил-5-циклопропіл-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)бензоат,
5-хлор-2-(6-(2-фторфеніл)піридин-3-іламіно)бензойна кислота,
5-хлор-2-(6-(2-хлорфеніл)піридин-3-іламіно)бензойна кислота,
5-хлор-2-(6-(хінолін-5-іл)піридин-3-іламіно)бензойна кислота,
2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-циклопропілбензойна кислота,
етил-2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-циклопропілбензоат,
5-хлор-2-(6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота,
5-фтор-2-(6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота,
2-(3'-фтор-2,4'-біпіридин-5-іламіно)-5-метилбензойна кислота,
2-(2-(2-фторфеніл)піримідин-5-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(2-(2-фторфеніл)піримідин-5-іламіно)-5-метилбензоат,
2-(6-(2,6-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
етил-2-(6-(2,6-дифторфеніл)піридин-3-іламіно)-5-метилбензоат,
2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
метил-2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензоат,
2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-метилбензойна кислота,
трет-бутил-2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-метилбензоат,
5-метил-2-(5-метил-6-(3-(піролідин-1-карбоніл)феніл)піридин-3-іламіно)бензойна кислота,
2-(6-(3-(циклопропілкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
5-циклопропіл-2-(2-(2-фторфеніл)піримідин-5-іламіно)бензойна кислота,
2-(2-(2-трифторметилфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-о-толілпіримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-(2-циклопропоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-(2,5-дифторфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-(2,3-дифторфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-(2-фтор-5-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(2-(2-трифторметилфеніл)піримідин-5-іламіно)-5-метилбензойна кислота,
2-(2-(2-фтор-5-трифторметоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота,
2-(6-(2-трифторметилфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-фенілпіридин-3-іламіно)-5-циклопропілбензойна кислота,
2-(6-(2-фторфеніл)піридин-3-іламіно)-5-циклопропілбензойна кислота,
2-(6-(3,5-дифторпіридин-4-іл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-циклопропілкарбамоїлфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2,4-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2,5-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2-фторфеніл)піридин-3-іламіно)-5-циклопропіл-3-фторбензойна кислота,
2-(6-(2,3,6-трифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(3-(5-метил-1,3,4-оксадіазол-2-іл)феніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(5-метил-6-(піримідин-5-іл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(2,3-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(5-фтор-2-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота,
2-(6-(4-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота;
і її фармацевтично прийнятні солі та N-оксиди.
26. Сполука формули (І):
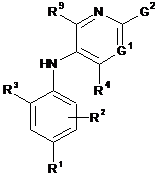 ,
,
де R1,R2,R3,R4,R9,G1 та G2 мають значення, наведені в будь-якому одному із попередніх пунктів, при умові, що коли G2 являє собою атом водню або хлору, метокси- або бутоксигрупу або разом з R6 утворює фенільну групу, тоді R1 не являє собою атом водню або атом хлору.
27. Сполука за п. 26 для застосування для лікування людини або тварини.
28. Фармацевтична композиція, яка містить сполуку за п. 26 в суміші з фармацевтично прийнятним розріджувачем або носієм.
29. Застосування сполуки за будь-яким із пп. 1-25 для виготовлення лікарського засобу для лікування патологічного стану або захворювання, визначеного в п. 1 або п. 2.
30. Спосіб лікування суб'єкта, який страждає патологічним станом або захворюванням, визначеним в п. 1 або п. 2, який включає введення зазначеному суб'єкту ефективної кількості сполуки за будь-яким із пп. 1-25.
31. Комбінація продукту, яка містить (і) сполуку за будь-яким із пп. 1-26 та (іі) другу сполуку, вибрану із наступних сполук:
(а) aнти-TNF-альфа моноклональні антитіла, такі як інфліксимаб, цертолізумаб pegol, голімумаб, адалімумаб та АМЕ-527 від Applied Molecular Evolution,
(б) антагоністи TNF-альфа, такі як етанерцепт, ленерцепт, онерцепт та пегсунерцепт,
(в) інгібітори кальциневрину (РР-2В)/інгібітори експресії INS, такі як циклоспорин А, такролімус та ISA-247 від Isotechnika,
(г) антагоністи рецептора IL-1, такі як анакінра та AMG-719 від Amgen,
(д) анти-СD20 моноклональні антитіла, такі як ритуксимаб, офатумумаб, окрелізумаб, велтузумаб та TRU-015 від Trubion Pharmaceuticals,
(e) інгібітори р38, такі як AMG-548 (від Amgen), ARRY-797 (від Array Biopharma), хлорметіазолу едисилат, дорамапімод, PS-540446,BMS-582949 (від ВМS), SB-203580, SB-242235, SB-235699, SB-281832, SB-681323, SB-856553 (всі від GlaxoSmithKline), KС-706 (від Kemia), LEO-1606, LEO-15520 (всі від Leo), SC-80036, SD-06, РН-797804 (всі від Pfizer), RWJ-67657 (від R.W.Johnson), RO-3201195, RO-4402257 (всі від Roche), AVE-9940 (від Aventis), SCIO-323, SCIO-469 (всі від Scios), TA-5493 (від Tanabe Seiyaku) та VX-745, VX-702 (всі від Vertex),
(ж) інгібітори активації NF-каппаВ (NFKB), такі як сульфазалазин та ігуратимод, та
(з) інгібітори дигідрофолатредуктази (DHFR), такі як метотрексат, аміноптерин та СН-1504 від Chelsea.
Текст
Реферат: Описані нові похідні азабіфеніламінобензойної кислоти, що мають хімічну структуру формули (І); а також спосіб їх одержання, фармацевтичні композиції, що їх містять, та їх застосування для лікування як інгібіторів дегідрооротатдигідрогенази (DHODH). UA 99734 C2 (12) UA 99734 C2 R 9 N G G HN R 3 R R R 2 1 4 2 1 Формула (I) UA 99734 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід стосується нових інгібіторів дигідрооротатдегідрогенази (DHODH). Ці сполуки корисні для лікування, профілактики або пригнічення захворювань та порушень, які, як відомо, чутливі до поліпшення інгібування дигідрооротатдегідрогенази, таких як аутоімунні захворювання, імунні та запальні захворювання, деструктивні кісткові порушення, злоякісні неопластичні захворювання, ангіогенні порушення, вірусні захворювання та інфекційні захворювання. Фермент дигідрооротатдегідрогенази (DHODH) є ферментом, який каталізує четверту стадію в біосинтезі піримідину, а саме, перетворення дигідрооротату на оротат, що супроводжується перенесенням електрону до убіхінону (кофактор Q) через флавінову мононуклеотидну проміжну сполуку (стаття Loffler та інші., Моля Cell Biochem, 1997). На противагу паразитам (Plasmodium falciparum) (стаття McRobert та інші, Моля Biochem Parasitol, 2002) та бактеріям (E.coli), які включають винятково цей de novo шлях як джерел піримідинів, клітини ссавця мають додатковий запасний шлях. В процесі гомеостатичної проліферації, запасний шлях, який не залежить від DHODH, як виявляється, є достатнім для клітинної підтримки піримідиновими основами. Але клітини з високим оборотом та особливо T та B лімфоцити нуждаються в шляху de novo для проліферації. В цих клітинах інгібування DHODH зупиняє прогресію клітинного циклу, пригнічуючи синтез ДНК, та отже, клітинну проліферацію (стаття Breedveld FC та інші., Ann Rheum Dis, 2000). Отже, інгібітори DHODH показують благоприємні імунодепресантні та антипроліферативні дії при захворюваннях людини, які характеризуються порушеною та неконтрольованою клітинної проліферацією, викликаною хронічним запаленям та руйнуванням тканини. На додаток до цього, скасовані інгібітори проліферації лімфоцитів DHODH (тобто терифлуномід, маритимус (FK778) та брехінар) мають протизапальну дію шляхом інгібування продукції цитокінів та передачі сигналу ядерного фактора (NF)-kB-, міграції моноцитів та підвищеної продукції трансформуючого фактора росту бета-1, та індукують зсув диференціації субпопуляції від T-хелперних клітин типу 1 (Th1) до типу 2 (Th2) (статті Manna та інші, J Immunol, 2000, Dimitrova та інші, J. Immunol, 2002). Крім того, диференціація остеокласту, опосередкована RANKL, знижується при інгібуванні DHODH (стаття Urushibara та інші, Arthrititis Rheum, 2004). В експериментах з співкристалізацією з двома інгібіторами DHODH, які включені в клінічні випробування, брехінар (стаття Dexter D.L. та інші; Cancer Res. 1985) та терифлуномід (A771726), як було виявлено, обидва сполучаються в загальному сайті, який, як вважають, також є сполучним сайтом для кофактора убіхінону (стаття Liu та інші; Struc. Fold. Des., 2000). Лефлуномід, який випускається під товарним знаком Arava (EP 0 780 128, WO 97/34600), був першим інгібітором DHODH, выпущеним на ринок. Лефлуномід є проліком терифлуноміду, який є активным метаболітом, що інгібує DHODH людини з помірною активністю (стаття Fox та інші, J. Rheumatol. Suppl., 1998). Лефлуномід є DMARD (який модифікує захворювання протиревматичним лікарським препаратом) від Aventis, який був дозволений FDA для лікування ревматоїдного артриту в 1998, та EMEA для лікування псоріатичного артриту в 2004. В даний час лефлуномід знаходиться в активній розробці для лікування системного червоного вовчака, грануломатозу Вегенера (стаття Metzler та інші; Rheumatology, 2004; 43(3), сс. 315-320) та ВІЛ-інфекції. Більш того, терифлуномід, його активний метаболіт, є ефективним при розсіяному склерозі, та зараз проходить фазу III клінічних випробувань (стаття O’Connor та інші, Neurology, 2006). Інші дані випливають із інших тісно зв'язаних захворювань, таких як анкілозуючий спондиліт (стаття Haibel та інші; Ann. Rheum. Dis., 2005), юнацький ідіопатичний поліартрит (стаття Silverman та інші; Артрит Rheum., 2005) та саркоїдоз (стаття Baughman та інші; Sarcoidosis Vasc. Diffuse Lung Dis., 2004). Крім того, лефлуномід та FK778 показали та відмінну противірусну активність відносно цитомегаловірусу. Лефлуномід в даний час показаний для вторинної терапії захворювання, зв'язаногоз цитомегаловірусом, після трансплантації органу (стаття John та інші, Transplantation, 2004). Додатково, лефлуномід знижує реплікацію ВІЛ на близько 75% в концентрації, яка може бути одержана при звичайному дозуванні (стаття Schlapfer E та інші, AIDS, 2003). Через фізіологічні дії, опосередковані інгібуванням дегідрооротатдегідрогенази, деякі інгібітори DHODH нещодавно були описані для лікування або профілактики аутоімунних захворювань, імунних та запальних захворювань, деструктивних кісткових порушень, злоякісних неопластичних захворювань, ангіогенних порушень, вірусних захворювань та інфекційних захворювань. Див., наприклад, міжнародні заявки на патент WO 06/044741; WO 06/022442; WO 06/001961, WO 04/056747, WO 04/056746, WO 03/006425, WO 02/080897 та WO 99/45926. 1 UA 99734 C2 5 10 15 20 25 30 35 40 45 Захворювання або порушення, при яких віддіграє роль інгібування DHODH, включаютьь, без обмеження, аутоімунні захворювання, імунні та запальні захворювання, деструктивні кісткові порушення, злоякісні неопластичні захворювання, ангіогенні порушення, вірусні захворювання та інфекційні захворювання. Аутоімунні захворювання, які можна запобігти або вилікувати, включаютьь, але не обмежуються ними, ревматоїдний артрит, псоріатичний артрит, системний червоний вовчак, розсіяний склероз, псоріаз, анкілозуючий спондиліт, грануломатоз Вегенера, юнацький ідіопатичний поліартрит, запальне кишкове захворювання, таке як виразковий коліт та хворобу Крона, синдром Рейтера, фіброміалгію та діабет 1 типу. Імунні та запальні захворювання, які можна запобігти або вилікувати, включають, але не обмежуються ними, астму, ХОЗЛ, респіраторний дистрес-синдром, гострий або хронічний панкреатит, хворобу «трансплантат проти хазяїна», хронічний саркоїдоз, відторгнення трансплантата, контактний дерматит, атопічний дерматит, алергічний риніт, алергічний кон’юнктивіт, синдром Бехета, запаленням очей, такі як кон’юнктивіт та ювеїт. Деструктивні кісткові порушення, які можна запобігти або вилікувати, включають, але не обмежуються ними, остеопороз, остеоартрит та множинне зв’язане з мієломою кісткове порушення. Злоякісні неопластичні захворювання, які можна запобігти або вилікувати, включають, але не обмежуються ними, рак простати, яєчників та головного мозку. Зв’язані з ангіогенезом порушення, які можна запобігти або вилікувати, включають, але не обмежуються ними, гемангіомы, неоваскуляризацію ока, дегенерацію жовтої плями або діабетичну ретинопатію. Вірусні захворювання, які можна запобігти або вилікувати, включають, але не обмежуються ними, ВІЛ-інфекцію, гепатит та цитомегаловірусну інфекцію. Інфекційні захворювання, які можна запобігти або вилікувати, включають, але не обмежуються ними, сепсис, септичний шок, ендотоксичний шок, грамнегативний сепсис, синдром токсичного шоку, бактеріальну дизентерію та інші протозойні зараження, такі як малярію. Було встановлено, що деякі похідні азабіфеніламінобензойної кислоти є новими потужними інгібіторами DHODH, та отже, можуть використовуватися для лікування або профілактики цих захворювань. Іншими цілями даного винаходу є забезпечення способу одержання зазначених сполук; фармацевтичні композиції, які містять ефективну кількість зазначених сполук; застосування сполук для виготовлення лікарського засобу для лікування патологічних станів або захворювань, сприйнятливих до поліпшення шляхом інгібування DHODH, де патологічний стан або захворювання вибране із ревматоїдного артриту, псоріатичного артриту, анкілозуючого спондиліту, розсіяного склерозу, грануломатозу Вегенера, системного червоного вовчака, псоріазу та саркоїдозу, та спосіб лікування патологічних станів або захворювань, сприйнятливих до поліпшення шляхом інгібування DHODH, де патологічний стан або захворювання вибране із ревматоїдного артриту, псоріатичного артриту, анкілозуючого спондиліту, розсіяного склерозу, грануломатозу Вегенера, системного червоного вовчака, псоріазу та саркоїдозу, який включає введення сполук за винаходом суб’єкту, який потребує такого лікування. Так, даний винахід стосується сполук формули (I) для застосування для лікування або профілактики патологічного стану або захворювання, сприйнятливого до поліпшення шляхом інгібування дегідрооротатдегідрогенази: R9 G2 N G1 HN R3 R4 R2 R1 50 де: 1 R вибраний із групи, яка складається із атомів водню, атомів галогену, C 1-4 алкілу, C3-4 циклоалкілу, -CF3 та -OCF3, 2 R вибраний із групи, яка складається із атомів водню, атомів галогену та C1-4 алкільної групи, 2 UA 99734 C2 3 5 10 15 20 5 N 25 30 35 45 50 5 (CH2)n де n має значення від 0 до 3, та - фенільної групи, яка необов’язково заміщена одним або декількома замісниками, вибраними із атомів галогену, C1-4 алкілу, гідроксі, C1-4 алкокси, C3-4циклоалкілу, C3-4 7 8 циклоалкокси, ціано, -CF3, -OCF3, CONR R , оксадіазолільних, триазолільних, піразолільних та імідазолільних груп, де оксадіазолільні, триазолільні, піразолільні та імідазолільні групи 7 8 необов’язково заміщені C1-4 алкільною або C3-7 циклоалкільною групою, та де R та R незалежно вибрані із атома водню, лінійної або розгалуженої C1-4 алкільної групи, C3-7 7 8 циклоалкільної групи, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: (CH2)n N 40 5 R вибраний із групи, яка складається із –COOR , -CONHR , тетразолілу, груп SO2NHR та 5 5 CONHSO2R , де R вибраний із групи, яка складається із атома водню та лінійних або розгалужених C1-4 алкільних груп, 4 R вибраний із групи, яка складається із атома водню та C1-4 алкільної групи, 9 R вибраний із групи, яка складається із атома водню та фенільної групи, 1 6 6 G являє собою групу, вибрану із N та CR , де R вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4 алкілу, C3-4 циклоалкілу, C1-4 алкокси, -CF3, -OCF3, моноциклічного N-вмісного C5-7 гетероарилу, моноциклічних N-вмісних C3-7 гетероциклільних груп та C6-10 арильної групи, яка необов’язково заміщена одним або декількома замісниками, вибраними із атомів галогену та C1-4 алкільної групи, 2 G являє собою групу, вибрану із: - атома водню, гідроксигрупи, атоми галогену, C3-4 циклоалкільної групи, C1-4 алкоксигрупи та a b –NR R , де a b R являє собою C1-4 алкільну групу, та R вибраний із групи, яка складається із C1-4 алкільної групи та C1-4 алкоксі-C1-4 алкільної групи, або a b R та R разом з атомом азоту, до якого вони приєднані, утворюють насичене 6-8-членне гетероциклічне кільце, яке необов’язково містить один атом кисню як додатковий гетероатом; - моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить один або декілька атомів азоту, які необов’язково заміщені одним або декількома замісниками, вибраними із атомів галогену, C1-4 алкілу, C1-4 алкокси, C3-4 циклоалкілу, C3-4 циклоалкокси, -CF3, 7 8 7 8 -OCF3 та –CONR R , де R та R незалежно вибрані із атома водню, лінійної або розгалуженої 7 8 C1-4 алкільної групи, C3-7 циклоалкільної групи, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: де n має значення від 0 до 3; 2 6 або G разом з R утворюють неароматичну C5-10 карбоциклічну групу або C6-10 арильну групу, і їх фармацевтично прийнятних солей та N-оксидів. Як тут використовується, термін алкіл включає необов’язково заміщені лінійні або розгалужені вуглеводневі радикали, які містять від 1 до 4 атомів вуглецю. Кращими замісниками для алкільних груп є атоми галогену та гідроксигрупи. Приклади включають метил, етил, н-пропіл, ізо-пропіл, н-бутил, втор-бутил та трет-бутильні радикали. Як тут використовується, термін алкокси включає необов’язково заміщені лінійні або розгалужені кисневмісні радикали, кожний із яких містить 1-4 атоми вуглецю. Кращими замісниками для алкоксигруп є атоми галогену та гідроксигрупи. Приклади включають метокси, етокси, н-пропокси, ізо-пропокси, н-бутокси, втор-бутокси та трет-бутоксирадикали. Як тут використовується, термін циклоалкіл включає необов’язково заміщені насичені карбоциклічні радикали і, якщо не зазначено інше, циклоалкільний радикал звичайно містить від 3 до 7 атомів вуглецю, краще 3 або 4 атоми вуглецю. 3 UA 99734 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклади включають циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. Коли циклоалкільний радикал має 2 або більше замісників, замісники можуть бути однаковими або різними. Кращими замісниками для циклоалкільних груп є атоми галогену та гідроксигрупи. Як тут використовується, термін циклоалкокси включає насичені оксивмісні карбоциклічні радикали і, якщо не зазначено інше, циклоалкоксирадикал звичайно містить від 3 до 8 атомів вуглецю, краще 3 або 4 атоми вуглецю. Приклади включають циклопропілокси, циклобутилокси, циклопентилокси, циклогексилокси та циклогептилокси. Коли циклоалкоксирадикал містить 2 або більше замісників, замісники можуть бути однаковими або різними. Кращими замісниками для циклоалкоксигруп є атоми галогену та гідроксигрупи. Як тут використовується, термін арильний радикал включає звичайно необов’язково заміщений C6-C10 моноциклічний або полициклічний арильний радикал, такий як феніл, нафтил, антраніл та фенантрил. Феніл є кращим. Зазначений необов’язково заміщений арильний радикал звичайно є незаміщеним або заміщений 1, 2 або 3 замісниками, які можуть бути однаковими або різними. Замісники краще вибрані із атомів галогену, краще атомів фтору, гідроксигруп, алкоксикарбонільних груп, в яких алкільна група містить від 1 до 4 атомів вуглецю, гідроксикарбонільних груп, карбамоїльних груп, нітрогруп, ціаногруп, C1-C4 алкільних груп, C1-C4 алкоксигруп та C1-C4 гідроксіалкільних груп. Коли арильний радикал містить 2 або більше замісників, замісники можуть бути однаковими або різними. Якщо не зазначено інше, замісники для арильної групи самі звичайно є незаміщеними. Як тут використовується, терміни гетероарильне та гетероароматичне кільце використовуються взаємозамінно, та звичайно включають 5-14-членну циклічну систему, краще 5-10-членну циклічну систему, яка містить принаймні одне гетероароматичне кільце, та яка містить принаймні один гетероатом, вибраний із O, S та N. Гетероарильний радикал може містити одне кільце (моноциклічний) або два або більше конденсованих кілець (поліциклічний), де принаймні одне кільце містить гетероатом. Як тут використовується, термін гетероциклільний радикал включає звичайно неароматичну насичену або ненасичену C3-C10 карбоциклічну кільцеву систему, таку як 5, 6 або 7-членний радикал, в якомуодин або декілька, наприклад, 1, 2, 3 або 4 атоми вуглецю, краще 1 або 2 атоми вуглецю заміщені гетероатомом, вибраним із N, O та S. Насичені гетероциклільні радикали є кращими. Як тут використовується, термін атом галогену включає атоми хлору, фтору, брому або йоду, звичайно атом фтору, хлору або брому. Термін гало, використовуваний як префікси, має теж саме значення. Як тут використовується, деякі із атомів, радикалів, груп, ланцюгів або циклів, які присутні в загальних структурах за винаходом, є “необов’язково заміщеними”. Це означає, що ці атоми, радикали, групи, ланцюги або цикли можуть бути або незаміщеними, або заміщеними в будьякому положені одним або декількома, наприклад, 1, 2, 3 або 4 замісниками, де атома водню, зв’язані з незаміщеними атомами, радикалами, групами, ланцюгами або циклами, заміщені хімічними прийнятними атомами, радикалами, групами, ланцюгами або циклами. Коли присутні два або більше замісників, кожний замісник може бути однаковим або різним. Як тут використовується, термін фармацевтично прийнятна сіль включає солі з фармацевтично прийнятною кислотою або основою. Фармацевтично прийнятні кислоти включають неорганічні кислоти, наприклад, хлористоводнева, сірчана, фосфорна, дифосфорна, бромистоводнева, йодистоводнева та азотна кислота, та органічні кислоти, наприклад, лимонна, фумарова, малеїнова, яблучна, мигдальна, аскорбінова, щавлева, бурштинова, винна, бензойна, оцтова, метансульфонова, етансульфонова, бензолсульфонова, циклогексилсульфамінова (цикламінова) або п-толуолсульфонова кислота. Фармацевтично прийнятні основи включають гідроксиди лужного металу (наприклад, натрію або калію) та лужноземельного металу (наприклад, кальцію або магнію) та органічні основи, наприклад, алкіламіни, арилалкаламіни гетероциклічні аміни. Іншими кращими солями відповідно до винаходу є четвертинні амонієві сполуки, де еквівалент аніона (X ) зв'язаний з позитивно зарядженим атомом N. X може являти собою аніон різних мінеральних кислот, таких як, наприклад, хлорид, бромід, йодид, сульфат, нітрат, фосфат, або аніон органічної кислоти, такої як, наприклад, ацетат, малеат, фумарат, цитрат, оксалат, сукцинат, тартрат, малат, манделат, трифторацетат, метансульфонат та птолуолсульфонат. X краще являє собою аніон, вибраний із хлориду, броміду, йодиду, сульфату, нітрату, ацетату, малеату, оксалату, сукцинату або трифторацетату. Більш краще X являє собою хлорид, бромід, трифторацетат або метансульфонат 4 UA 99734 C2 3 5 10 15 20 25 30 У конкретному випадку, коли R являє собою COOH групу, вона переважно містить солі, одержані з відповідною карбоновою кислотою заміщенням атома водню карбонової групи катіоном, одержаним з фармацевтично прийнятною основою, як описано вище. Як тут використовується, N-оксид утворений із третинних основних амінів або імінів, які присутні в молекулі, використовуючи звичайний оисний агент. Переважно, патологічний стан або захворювання вибране із ревматоїдного артриту, псоріатичного артриту, анкілозуючого спондиліту, розсіяного склерозу, грануломатозу Вегенера, системного червоного вовчака, псоріазу та саркоїдозу. 1 Звичайно R вибраний із групи, яка складається із атомів водню, атомів фтору, атомів хлору, атомів брому, C1-4 алкільних, C3-4 циклоалкільних та -CF3 груп. 2 Звичайно R вибраний із групи, яка складається із водню, атома галогену та метильної групи. 1 Звичайно G вибраний із групи, яка складається із атомів азоту, CCl, CF, CH, C(CH 3), C(циклопропіл), C(феніл) та C(CF3) груп. 2 Звичайно G являє собою групу, вибрану із: a b - атома водню, атома галогену, C3-4 циклоалкільної групи, C1-2 алкоксигрупи та –NR R , де a b R являє собою C1-2 алкільну групу, та R вибраний із групи, яка складається із C1-2 алкільних груп та C1-2 алкоксі-C1-2 алкільних груп, або a b R та R разом з атомом азоту, до якого вони приєднані, утворюють насичене 6- або 7членне гетероциклічне кільце, яке необов’язково містить один атом кисню як додатковий гетероатом, - моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить один або два атома азоту, які необов’язково заміщені одним або декількома замісниками, вибраними із атомів галогену та C1-4 алкільних груп, та - фенільної групи, яка необов’язково заміщена одним, двома або трьома замісниками, вибраними із атомів галогену, C1-4 алкілу, гідроксилу, C1-4 алкокси, C3-4циклоалкілу, C3-4 7 8 циклоалкокси, ціано, -CF3, -OCF3, –CONR R та оксадіазолільних груп, де оксадіазолільна група 7 8 необов’язково заміщена C1-4 алкільною або C3-7 циклоалкільною групою, та де R та R незалежно вибрані із атомів водню, лінійних або розгалужених C 1-4 алкільних груп, C3-4 7 8 циклоалкільних груп, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: N 35 40 45 де n має значення 1 або 2, 2 6 або G разом з R утворюють неароматичну C6 карбоциклічну групу або фенільну групу. 2 Більш конкретно, G являє собою групу, вибрану із: - атома водню, атома фтору, циклопропільної групи, метоксигрупи, NMeEt, -NEt2, -N(Me)(CH2)2-O-CH3, 6-морфолінілу, азепан-1-ілу та піперидин-1-ілу, - піридинільного, піримідинільного, хінолінільного або піразинільного кільця, необов’язково заміщеного одним або двома замісниками, вибраними із Me та F, и - фенільної групи, яка необов’язково заміщена одним, двома або трьома замісниками, вибраними із фтору, хлору, метилу, гідрокси, метокси, етокси, ізопропілокси, циклопропілу, 7 8 циклопропілокси, ціано, -CF3, -OCF3, CONR R та оксадіазолільних груп, де оксадіазолільна 7 8 група необов’язково заміщена метильною групою, та де R та R незалежно вибрані із атома 7 8 водню, метильної групи, ізопропільної групи, циклопропільної групи, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: N 50 (CH2)n (CH2)n где n означає 1, 2 6 або G разом з R утворює неароматичну C6 карбоциклічну групу або фенільну групу. 1 В одному варіанті здійснення даного винаходу, R вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4 алкілу, C3-4 циклоалкілу, -CF3 та -OCF3, 5 UA 99734 C2 2 5 10 15 R вибраний із групи, яка складається із атомів водню, атомів галогену та C1-4 алкільної групи, 3 5 5 5 R вибраний із групи, яка складається із –COOR , -CONHR , тетразолілу, SO2NHR та 5 5 CONHSO2R груп, де R вибраний із групи, яка складається із атома водню та лінійних або розгалужених C1-4 алкільних груп, 4 R вибраний із групи, яка складається із атома водню та C1-4 алкільної групи, 9 R являє собою атом водню, 1 6 6 G являє собою групу, вибрану із N та CR , де R вибраний із групи, яка складається із атомів водню, атомів галогену, C1-4 алкілу, C3-4 циклоалкілу, C1-4 алкокси, -CF3, -OCF3, моноциклічних N-вмісних C5-7 гетероарильних, моноциклічних N-вмісних C3-7 гетероциклільних груп та C6-10 арильної групи, яка необов’язково заміщена одним або декількома замісниками, вибраними із атомів галогену та a C1-4 алкільної групи, 2 G являє собою групу, вибрану із: - моноциклічного або біциклічного 5-10-членного гетероароматичного кільця, яке містить атом азоту, який необов’язково заміщений одним або декількома замісниками, вибраними із атомів галогену, C1-4 алкілу, C1-4 алкокси, C3-4 циклоалкілу, C3-4 циклоалкокси, -CF3, OCF3 та – 7 8 7 8 CONR R , де R та R незалежно вибрані із атома водню, лінійної або розгалуженої C1-4 7 8 алкільної групи, C3-7 циклоалкільної групи, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: 20 N 25 30 де n має значення від 0 до 3, та - фенільної групи, яка необов’язково заміщена одним або декількома замісниками, вибраними із атомів галогену, C1-4 алкілу, C1-4 алкокси, C3-4циклоалкілу, C3-4 циклоалкокси, -CF3, 7 8 OCF3, –CONR R , оксадіазолільних, триазолільних, піразолільних та імідазолільних груп, де оксадіазолільні, триазолільні, піразолільні та імідазолільні групи необов’язково заміщені C 1-4 7 8 алкільною або C3-7 циклоалкільною групою, та де R та R незалежно вибрані із атома водню, 7 8 лінійної або розгалуженої C1-4 алкільної групи, C3-7 циклоалкільної групи, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: N 35 40 45 50 (CH2)n (CH2)n де n має значення від 0 до 3, і їх фармацевтично прийнятні солі та N-оксиди. 1 Звичайно R вибраний із групи, яка складається із C1-4 алкілу, C3-4 циклоалкілу та -CF3, краще метильної та циклопропільної групи, більш краще циклопропільної групи. 2 Звичайно R вибраний із атома водню або галогену, краще атома водню. 3 5 5 3 Звичайно R вибраний із COOR , -CONHR та тетразолільної групи; краще R являє собою COOH групу. 4 Звичайно R являє собою атом водню або метильну групу, краще атом водню. 9 Звичайно R являє собою атом водню. 1 Звичайно G являє собою групу, вибрану із N, CH, C(CH3), C(циклопропіл), C(феніл) або C(CF3) групи. 2 Звичайно G вибраний із групи, яка складається із метоксигрупи, циклопропільної групи та необов’язково заміщених фенільних, піридильних, хінолінільних, піримідинільних та 2 піразинільних груп, більш краще, G вибраний із групи, яка складається із необов’язково заміщених фенільних, піридильних, хінолінільних, піримідинільних та піразинільних груп, наибільш краще необов’язково заміщених фенільних, 4-піридильних, 5-хінолінільних та 2піразинільних груп. 1 В іншому варіанті здійснення даного винаходу R вибраний із метильної або 2 3 4 циклопропільної групи, R являє собою атом водню, R являє собою COOH групу, R являє 1 собою атом водню або метильну групу, G вибраний із N, CH, C(CH3), C(циклопропіл), C(феніл) 2 та C(CF3) груп, та G являє собою групу, вибрану із групи, яка складається із необов’язково 6 UA 99734 C2 9 5 заміщених фенільних, 4-піридильних, 5-хінолінільних та 2-піразинільних груп, більш краще R являє собою групу водню. 1 В іншому варіанті здійснення даного винаходу R вибраний із метильної або 2 3 4 циклопропільної групи, R являє собою атом водню, R являє собою COOH групу, R являє 1 2 собою атом водню, G вибраний із атома азоту та CH, C(CH3) та C(CF3) груп, та G являє собою фенільну групу, необов’язково заміщену одним або двома замісниками, вибраними із хлору, 7 8 7 фтору, метокси, етокси, ізопропокси, трифторметокси та CONR R , де R являє собою водень та 8 7 8 R являє собою циклопропіл, або R та R разом з атомом азоту, до якого вони приєднані, утворюють групу формули: 10 N 15 20 25 30 35 40 45 50 55 (CH2)n де n означає 1. Конкретні індивідуальні сполуки за винаходом включають наступні сполуки: 5-циклопропіл-2-(2-фенілпіримідин-5-іламіно)бензойна кислота, 2-(6-циклопропіл-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 1-оксид 5-(2-карбокси-4-циклопропілфеніламіно)-3-метил-2-фенілпіридину, 5-метил-2-(6-(3-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(6-гідрокси-5-фенілпіридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(2-(2,6-дифтор-4-гідроксифеніл)піримідин-5-іламіно)бензойна кислота, 5-циклопропіл-2-(6-метокси-5-фенілпіридин-3-іламіно)бензойна кислота, 2-(5-фтор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(етил(метил)аміно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(3'-фтор-2,4'-біпіридин-5-іламіно)бензойна кислота, 2-(6-(діетиламіно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-((2-метоксіетил)(метил)аміно)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(5-хлор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(2-(2-циклопропілфеніл)піримідин-5-іламіно)бензойна кислота, 5-циклопропіл-2-(5-фенілпіридин-3-іламіно)бензойна кислота, 5-метил-2-(хінолін-3-іламіно)бензойна кислота, 5-метил-2-(5,6,7,8-тетрагідрохінолін-3-іламіно)бензойна кислота, 2-(5-хлор-2-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(5,6-дифенілпіридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(2-(2,6-дифторфеніл)піримідин-5-іламіно)бензойна кислота, 5-циклопропіл-2-(5-метилпіридин-3-іламіно)бензойна кислота, 2-(2-(3-циклопропоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 5-метил-2-(6-морфолінoпіридин-3-іламіно)бензойна кислота, 5-метил-2-(5-метил-6-морфолінoпіридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(6-циклопропіл-5-фенілпіридин-3-іламіно)бензойна кислота, 2-(6-(2-циклопропілфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2-ціанофеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(2-(3-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 5-метил-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота, 5-метил-2-(5-метил-6-(піперидин-1-іл)піридин-3-іламіно)бензойна кислота, 2-(6-(азепан-1-іл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 2-(2,3'-біпіридин-5-іламіно)-5-циклопропілбензойна кислота, 2-(3'-хлор-2,4'-біпіридин-5-іламіно)-5-метилбензойна кислота, 5-метил-2-(3-метил-2,2'-біпіридин-5-іламіно)бензойна кислота, 2-(5,6-дифторпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-метоксифеніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)піридин-3-іламіно)-5-фторбензойна кислота, 2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-етокси-2-фторфеніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензойна кислота, 7 UA 99734 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-(6-(3-етоксифеніл)-4-метилпіридин-3-іламіно)бензойна кислота, 5-бром-2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота, 5-хлор-2-(6-(3-етоксифеніл)піридин-3-іламіно)бензойна кислота, 2-(6-(5-етокси-2-фторфеніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)-5-(трифторметил)бензойна кислота, 2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-5-(трифторметил)бензойна кислота, 2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-6-метилбензойна кислота, 5-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота, 2-(6-(5-етокси-2-фторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2-фтор-5-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(2-фтор-5-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(2-фторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(3-метоксифеніл)-5-фенілпіридин-3-іламіно)-5-метилбензоат, 5-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота, етил 5-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат, 5-метил-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензойна кислота, етил 5-метил-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензоат, 2-(5-циклопропіл-6-(3-метоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота, етил 2-(5-циклопропіл-6-(3-метоксифеніл)піридин-3-іламіно)-5-метилбензоат, 2-(6-(2-фтор-5-ізопропоксифеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(3-циклопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, трет-бутил 2-(6-(3-циклопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(2-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, трет-бутил 2-(6-(2-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(3-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(3-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(2-фтор-5-метоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(2-фтор-5-метоксифеніл)-4-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)-5-метилбензоат, 2-(6-(3-(диметилкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(3-(диметилкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-3-метилбензойна кислота, трет-бутил 2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-3-метилбензоат, 3-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота, трет-бутил 3-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат, 2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-метилбензойна кислота, трет-бутил 2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-метилбензоат, 3-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензойна кислота, трет-бутил 3-фтор-2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)бензоат, 5-циклопропіл-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензойна кислота, етил 5-циклопропіл-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензоат, 5-циклопропіл-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота, етил 5-циклопропіл-2-(5-метил-6-фенілпіридин-3-іламіно)бензоат, 5-метил-2-(5-метил-6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота, трет-бутил 5-метил-2-(5-метил-6-(2-(трифторметил)феніл)піридин-3-іламіно)бензоат, 2-(6-(3-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, трет-бутил 2-(6-(3-хлорфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 2-(6-(2-фторфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, трет-бутил 2-(6-(2-фторфеніл)-5-метилпіридин-3-іламіно)-5-метилбензоат, 5-метил-2-(5-метил-6-(хінолін-5-іл)піридин-3-іламіно)бензойна кислота, трет-бутил 5-метил-2-(5-метил-6-(хінолін-5-іл)піридин-3-іламіно)бензоат, 2-(3’-фтор-3-метил-2,4’-біпіридин-5-іламіно)-5-метилбензойна кислота, трет-бутил 2-(3’-фтор-3-метил-2,4’-біпіридин-5-іламіно)-5-метилбензоат, 5-метил-2-(5-метил-6-(піразин-2-іл)піридин-3-іламіно)бензойна кислота, трет-бутил 5-метил-2-(5-метил-6-(піразин-2-іл)піридин-3-іламіно)бензоат, 8 UA 99734 C2 5 10 15 20 25 30 35 40 45 50 55 60 5-циклопропіл-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота, етил 5-циклопропіл-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензоат, 5-циклопропіл-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)бензойна кислота, етил 5-циклопропіл-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)бензоат, 5-хлор-2-(6-(2-фторфеніл)піридин-3-іламіно)бензойна кислота, 5-хлор-2-(6-(2-хлорфеніл)піридин-3-іламіно)бензойна кислота, 5-хлор-2-(6-(хінолін-5-іл)піридин-3-іламіно)бензойна кислота, 2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-циклопропілбензойна кислота, етил 2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-циклопропілбензоат, 5-хлор-2-(6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота, 5-фтор-2-(6-(2-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота, 2-(3’-фтор-2,4’-біпіридин-5-іламіно)-5-метилбензойна кислота, 2-(2-(2-фторфеніл)піримідин-5-іламіно)-5-метилбензойна кислота, трет-бутил 2-(2-(2-фторфеніл)піримідин-5-іламіно)-5-метилбензоат, 2-(6-(2,6-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, етил 2-(6-(2,6-дифторфеніл)піридин-3-іламіно)-5-метилбензоат, 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, метил 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензоат, 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-метилбензойна кислота, трет-бутил 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-метилбензоат, 5-метил-2-(5-метил-6-(3-(піролідин-1-карбоніл)феніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-(циклопропілкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(2-(2-фторфеніл)піримідин-5-іламіно)бензойна кислота, 2-(2-(2-трифторметилфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-o-толілпіримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2-циклопропоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2,5-дифторфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2,3-дифторфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2-фтор-5-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2-трифторметилфеніл)піримідин-5-іламіно)-5-метилбензойна кислота, 2-(2-(2-фтор-5-трифторметоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(6-(2-трифторметилфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-фенілпіридин-3-іламіно)-5-циклопропілбензойна кислота, 2-(6-(2-фторфеніл)піридин-3-іламіно)-5-циклопропілбензойна кислота, 2-(6-(3,5-дифторпіридин-4-іл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-циклопропілкарбамоїлфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2,4-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2,5-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2-фторфеніл)піридин-3-іламіно)-5-циклопропіл-3-фторбензойна кислота, 2-(6-(2,3,6-трифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-(5-метил-1,3,4-оксадіазол-2-іл)феніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(5-метил-6-(піримідин-5-іл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2,3-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(5-фтор-2-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота и 2-(6-(4-карбамоїлфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, і їх фармацевтично прийнятні солі та N-оксиди. окремий інтерес являють сполуки: 5-циклопропіл-2-(2-фенілпіримідин-5-іламіно)бензойна кислота, 1-оксид 5-(2-карбокси-4-циклопропілфеніламіно)-3-метил-2-фенілпіридину, 5-метил-2-(6-(3-(трифторметил)феніл)піридин-3-іламіно)бензойна кислота, 2-(5-фтор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(3'-фтор-2,4'-біпіридин-5-іламіно)бензойна кислота, 2-(5-хлор-6-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(2-(2-циклопропілфеніл)піримідин-5-іламіно)бензойна кислота, 5-циклопропіл-2-(5-фенілпіридин-3-іламіно) бензойна кислота, 2-(5-хлор-2-фенілпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(5,6-дифенілпіридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(2-(2,6-дифторфеніл)піримідин-5-іламіно)бензойна кислота, 2-(2-(3-циклопропоксифеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 5-метил-2-(6-морфолінoпіридин-3-іламіно)бензойна кислота, 9 UA 99734 C2 5 10 15 20 25 30 5-метил-2-(5-метил-6-морфолінoпіридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(6-циклопропіл-5-фенілпіридин-3-іламіно)бензойна кислота, 2-(6-(2-циклопропілфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(2-ціанофеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(2-(3-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 5-метил-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота, 5-метил-2-(5-метил-6-(піперидин-1-іл)піридин-3-іламіно)бензойна кислота, 2-(6-(азепан-1-іл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(2,3'-біпіридин-5-іламіно)-5-циклопропілбензойна кислота, 2-(3'-хлор-2,4'-біпіридин-5-іламіно)-5-метилбензойна кислота, 5-метил-2-(3-метил-2,2'-біпіридин-5-іламіно)бензойна кислота, 2-(6-(3-етоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 2-(6-(3-метоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-метил-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота, 2-(6-(3-ізопропоксифеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(5-метил-6-(3-(трифторметокси)феніл)піридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(5-метил-6-фенілпіридин-3-іламіно)бензойна кислота, 2-(6-(2-фторфеніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(6-феніл-5-(трифторметил)піридин-3-іламіно)бензойна кислота, 5-циклопропіл-2-(6-(3-метоксифеніл)-5-(трифторметил)піридин-3-іламіно)бензойна кислота, 2-(6-(2-хлорфеніл)піридин-3-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-циклопропілбензойна кислота, 2-(2-(2-хлорфеніл)піримідин-5-іламіно)-5-метилбензойна кислота, 2-(6-(2,6-дифторфеніл)піридин-3-іламіно)-5-метилбензойна кислота, 5-метил-2-(5-метил-6-(3-(піролідин-1-карбоніл)феніл)піридин-3-іламіно)бензойна кислота, 2-(6-(3-(циклопропілкарбамоїл)феніл)-5-метилпіридин-3-іламіно)-5-метилбензойна кислота, 5-циклопропіл-2-(2-(2-фторфеніл)піримідин-5-іламіно)бензойна кислота, і їх фармацевтично прийнятні солі та N-оксиди 2 Сполуки формули (I) є новими, при умові, що коли G являє собою атом водню або хлору, 6 1 метокси або бутоксигрупу, або разом з R утворює фенільну групу, тоді R не являє собою атом водню або атом хлору. Так, даний винахід також стосується сполук формули (I): R9 G2 N G1 HN R3 R4 R2 R1 35 40 1 2 3 4 9 1 2 2 де R , R , R , R , R , G та G є такими, як визначено вище, при умові, що коли G являє 6 собою атом водню або хлору, метокси або бутоксигрупу, або разом з R утворює фенільну 1 групу, тоді R не являє собою атом водню або атом хлору. Сполуки загальної формули (I) можуть бути одержані відповідно до наступної схеми синтезу, наведеної на фігурі 1. 10 UA 99734 C2 Фігура 1 R9 H2N R O2N O2N N R9 9 R4 N N G1 X1 R G1 OH R4 G1 IX R9 VII XI 4 Z-G2 H2N X1 Z-G2 VIII N R9 N VII R4 G1 R4 O2N G1 G2 III R3 G2 X2 X R1 R3 H N R1 R4 R2 R2 R9 II N G1 G2 I 1 5 10 15 20 25 30 35 Сполуки загальної формули (I) можуть бути одержані реакцією проміжних сполук (II), де R , 3 2 R та R є такими, як описано вище, та X являє собою атом хлору або брому, з проміжними 4 9 1 2 сполуками (III), де R , R , G та G є такими, як описано вище. Реакція може проводитися в інертній атмосфері над паладієвим каталізатором, таким як Pd(OAc) 2 або трис(дибензиліденацетон)дипаладій(0) (Pd2(dba)3), використовуючи фосфіновий ліганд, такий як рац-2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (BINAP) або ксантфос, в присутності основи, такої трет як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може проводитися в мікрохвильовій печі при температурі в діапазоні від 100ºC до 160ºC протягом від 0,5 до 15 годин. Альтернативно, реакція може проводитися з мідним каталізатором, таким як суміш Cu та Cu2O, використовуючи основу, таку як Cs2CO3, K2CO3 або Na2CO3, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може проводитися в мікрохвильовій печі при температурі в діапазоні від 100ºC до 160ºC протягом від 0,5 до 15 годин. Проміжні сполуки загальної формули (III) можуть бути одержані із проміжних сполук (X) відновленням нітрогрупи, використовуючи водень та каталізатор, такий як Pd/C, Pt/C, PtO 2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. Альтернативно, проміжні сполуки загальної формули (III) також можуть бути одержані 1 реакцією проміжних сполук (XI), де X являє собою атом хлору або брому, з проміжними сполуками (VII), де Z являє собою борну кислоту, боронат, триалкілстанан або похідну цинкату. Реакція може проводитися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або [1,1'-біс(дифенілфосфіно)-фероцен]дихлорпаладій(II) (PdCl2(dppf)ДХМ), використовуючи фосфіновий ліганд, такий як BINAP, трициклогексилфосфін (P(Cy)3) або ксантфос при необхідності, в присутності основи, такої як Cs 2CO3, K2CO3 або трет NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. Проміжні сполуки загальної формули (X) можуть бути одержані реакцією проміжних сполук 1 (IX), де X являє собою атом хлору або брому, з проміжними сполуками (VII), де Z являє собою борну кислоту, боронат, триалкілстанан або похідну цинкату. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf), використовуючи фосфіновий ліганд, такий як BINAP, P(Cy) 3 або 2 11 UA 99734 C2 трет 5 10 15 ксантфос при необхідності, в присутності основи, такої як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. Проміжні сполуки формули (XI) є комерційно доступними або можуть бути одержані із проміжних сполук формули (IX) відновленням нітрогрупи за допомогою водню та каталізатора, такого як Pd/C, Pt/C, PtO2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. Проміжні сполуки формули (IX) є комерційно доступними або можуть бути одержані із проміжних сполук формули (VIII). Реакція може здійснюватися в присутності POCl3 або POBr3 з PCl5 або PBr3 в діапазоні температур від 70ºC до 140ºC протягом від 15 хвилин до 24 годин. 6 В конкретному випадку, коли R являє собою групу, вибрану із C3-4 циклоалкілу, C6-10 арилу, C3-7 гетероциклілу або C5-7 гетероарилу, проміжні сполуки загальної формули (IIIb) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 2. Фігура 2 R9 H2N R9 O2N R R9 N 4 Z Br Br G VII 2 O2N N G2 R4 Br N R9 H2N N 2 Z R 6 R O2N IXb G2 R4 R9 Br Xa VIIa R6 IIIa G R4 Z 6 N VIIa IIIb R G2 4 R6 Xb 20 4 25 30 35 40 45 9 2 Проміжні сполуки (IIIb), де R , R та G є такими, як описано вище, можуть бути одержані реакцією проміжних сполук (IIIa) з проміжними сполуками (VIIa), де Z являє собою борну кислоту, боронатний ефір, триалкілстанан або похідну цинкату. Реакція може проводитися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy) 3 трет або ксантфос, при необхідності в присутності основи, такої як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. Альтернативно, проміжні сполуки загальної формули (IIIb) можуть бути одержані із проміжних сполук загальної формули (Xb) відновленням нітрогрупи за допомогою водню та каталізатора, такого як Pd/C, Pt/C, PtO2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. 4 2 Проміжні сполуки загальної формули (IIIa), де R та G є такими, як описано вище, можуть бути одержані із проміжних сполук загальної формули (Xa) відновленням нітрогрупи, використовуючи водень та каталізатор, такий як Pd/C, Pt/C, PtO 2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. Проміжні сполуки загальної формули (Xb) можуть бути одержані реакцією проміжних сполук 4 2 загальної формули (Xa), де R та G є такими, як описано вище, з проміжними сполуками (VIIa), де Z являє собою борну кислоту, боронатний ефір, триалкілстанан або похідну цинкату. Реакція 12 UA 99734 C2 5 10 15 20 25 може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy)3 або ксантфос при необхідності, в присутності основи, такої як Cs 2CO3, трет K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою триалкілстанан, CuI додають як співкаталізатор. Проміжні сполуки загальної формули (Xa) можуть бути одержані реакцією проміжних сполук (IXb) з проміжними сполуками (VII), де Z являє собою борну кислоту, боронатний ефір, триалкілстанан або похідну цинкату. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy) 3 або ксантфос при трет необхідності, в присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. Проміжні сполуки загальної формули (IXb) є комерційно доступними або можуть бути одержані аналогічно способу, показаному для одержання проміжних сполук формули (IX) на фігурі 1. В альтернативній методиці сполуки загальної формули (I) можуть бути одержані відповідно до схеми синтезу, показаної на фігурі 3. Фігура 3 R9 R9 X4 X4 N R4 G1 R4 X3 XIV N G2 Z + G1 G2 V VII R3 NH2 R3 H N R1 R R4 2 R9 R1 N G1 G2 R2 IV I 1 30 35 40 2 Сполуки загальної формули (I) можуть бути одержані реакцією проміжних сполук (IV), де R , R 3 4 9 1 2 та R є такими, як описано вище, з проміжними сполуками (V), де R , R , G та G є такими, 4 як описано вище, та X являє собою атом брому або йоду або похідну триалкілстанану. 4 Коли X являє собою атом брому або йоду, реакція може здійснюватися з паладієвим каталізатором, таким як Pd(OAc)2 або Pd2(dba)3, використовуючи фосфіновий ліганд, такий трет як BINAP або ксантфос, в присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. 4 Коли X являє собою похідну триалкілстанану, мідьвмісний каталізатор, такий як Cu(OAc) 2, вмкористовується в присутності основи, такої як триетиламін, 1,2-лутидин, CsF або фторид тетра-н-бутиламонію (TBAF), в розчиннику, такому як ацетонітрил, толуол, дихлорметан або ТГФ, в діапазоні температур від 25ºC до 90ºC. Проміжні сполуки загальної формули (V) можуть бути одержані реакцією проміжних сполук 3 (XIV), де X являє собою атом брому або хлору, з проміжними сполуками (VII), де Z являє собою борну кислоту, боронат, триалкілстанан або похідну цинкату. Реакція може 13 UA 99734 C2 5 10 здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy)3 або ксантфос при необхідності, в присутності основи, такої як трет Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Коли Z являє собою триалкілстанан, CuI додають як співкаталізатор. В іншій альтернативній методиці сполуки загальної формули (I) можуть бути одержані відповідно до схеми синтезу, показаної на фігурі 4. Фігура 4 R9 R3 I NH2 N + R1 3 R X2 1 R2 II R3 H2N R R1 9 4 G1 VI X5 R9 H N R2 R N + R Br XV IV R G1 R4 R2 R3 Z G2 N 4 G1 X5 VII R1 R2 H N R4 R9 N G1 G2 I XVI 1 Сполуки загальної формули (I) можуть бути одержані реакцією проміжних сполук (VI), де R , 3 4 9 1 5 R , R , R , R та G є такими, як описано вище, та X являє собою атом хлору або брому, з 2 проміжними сполуками (VII), де G є таким, як описано вище, та Z вибраний із борної кислоти, боронату, триалкілстанану та похідної цинкату. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy) 3 або ксантфос трет при необхідності, в присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Альтернативно, реакція може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. Проміжні сполуки загальної формули (VI) можуть бути одержані реакцією проміжних сполук 1 2 3 2 4 1 5 (II), де R , R , R та X є такими, як описано вище, з проміжними сполуками (XVI), де R , G та X є такими, як описано вище. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2 або Pd2(dba)3, використовуючи фосфіновий ліганд, такий як трет BINAP або ксантфос, в присутності основи, такої як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Альтернативно, реакція може здійснюватися з мідним каталізатором, таким як Cu або Cu 2O, використовуючи основу, таку як Cs2CO3, K2CO3 або Na2CO3, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Проміжні сполуки загальної формули (VI) також можуть бути одержані реакцією проміжних 1 2 3 4 9 сполук (IV), де R , R та R є такими, як описано вище, проміжними сполуками (XV), де R , R та 1 G є такими, як описано вище. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2 або Pd2(dba)3, використовуючи фосфіновий ліганд, такий як трет BINAP або ксантфос, в присутності основи, такої як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. 2 В конкретному випадку, коли де G являє собою атом водню або алкоксигрупу, проміжні сполуки формул (IIIc) та (IIId) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 5. 2 15 20 25 30 35 40 45 14 UA 99734 C2 Фігура 5 R9 O2 N R4 R9 H2N N G 1 Cl N G1 R4 IXc IIIc R9 O2 N R4 O2N N G1 Br 10 15 20 R4 G1 OR' IIId R9 O2N I XII O O S F OH R9 O N N R4 35 R4 OR' Проміжні сполуки загальної формули (IIIc) можуть бути одержані відновленням проміжних сполук загальної формули (IXc) за допомогою водню та каталізатора, такого як Pd/C, Pt/C, PtO 2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2 або SnCl2.H2O або Fe-HCl, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. ’ З іншого боку, проміжні сполуки загальної формули (IIId), де R являє собою метильну групу, можуть бути одержані відновленням проміжних сполук загальної формули (Xd) за допомогою водню та каталізатора, такого як Pd/C, Pt/C, PtO2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2 або SnCl2.H2O або Fe-HCl, в розчиннику, такому як EtOAc. Проміжні сполуки загальної формули (Xd) можуть бути одержані із проміжної сполуки формули (IXd) нагріванням в присутності метанолу при 100ºC. Проміжні сполуки загальної формули (IXc) та (IXd) є комерційно доступними або можуть бути одержані аналогічно способу, наведенному для одержання проміжних сполук формули (IX) на фігурі 1. 6 6 В конкретному випадку, коли G1 являє собою CR , де R являє собою -CF3, проміжні сполуки загальної формули (IXa) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 6. Фігура 6 O2N 30 G1 N Xd R9 25 H2N N IXd 5 R9 R9 X1 R4 F F O2N N O X1 R4 I CF3 XIII IXa Проміжні сполуки загальної формули (IXa) можуть бути одержані із проміжних сполук формули (XIII) в присутності метил 2,2-дифтор-2-(фторсульфоніл)ацетату в розчиннику, такому як ДМФА або толуол, в діапазоні температур від 40ºC до 130ºC протягом від 1 до 48 годин. Проміжні сполуки формули (XIII) можуть бути одержані із проміжних сполук загальної формули (XII). Реакція може здійснюватися в присутності POCl3 або POBr3 з PCl5 або PBr3 в діапазоні температур від 70ºC до 140ºC протягом від 15 хвилин до 24 годин. Звичайно, проміжні сполуки формули (II) та (IV) є комерційно доступними. Однак в 1 конкретному випадку, коли R являє собою циклопропільну групу, зазначена проміжна сполука може бути одержана відповідно до схеми синтезу, показаної на фігурі 7. Фігура 7 15 UA 99734 C2 R3 R3 Cl + Br Cl Z R2 R2 XVII XVIII IIa R3 R3 NH2 NH2 Z + X6 R2 R2 XIX 5 10 XVII IVa Проміжні сполуки формули (IIa) та (IVa) можуть бути одержані реакцією проміжних сполук 6 (XVIII) та (XIX) відповідно, де X являє собою атом брому або хлору, з проміжною сполукою (XVII), де Z являє собою борну кислоту або боронатну похідну. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або PdCl2(dppf)ДХМ, використовуючи фосфіновий ліганд, такий як BINAP, P(Cy) 3 трет або ксантфос при необхідності, основу, таку як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода, діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. 2 В конкретному випадку, коли G являє собою гідроксигрупу, сполуки формули (Id) можуть бути одержані відповідно до схеми, наведеної на фігурі 8. Фігура 8 R9 O2N O2N N R4 R O I O2N Z-G 1 N R4 OH R9 9 9 R R4 Ph H2N N G1 O R4 Ph I G1 O Ph IIId XXVI XXV XII N R3 X2 R3 4 R 15 20 25 R9 H N R2 R 3 R N 4 1 G R4 OH R H N 9 R4 N 4 R2 R G1 R2 II O Ph XXIX Id Сполуки загальної формули (Id) можуть бути одержані із проміжних сполук загальної формули (XXIX) обробкою трифтороцтовою кислотою при температурі від 25ºC до 60ºC протягом від 30 хвилин до 24 годин. Проміжні сполуки загальної формули (XXIX) можуть бути одержані реакцією проміжних сполук загальної формули (IIId) з проміжними сполуками загальної формули (II). Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або [1,1'-біс(дифенілфосфіно)фероцен]дихлорпаладій(II) (PdCl2(dppf)ДХМ), використовуючи фосфіновий ліганд, такий як BINAP, трициклогексилфосфін (P(Cy)3) або ксантфос при необхідності, в присутності основи, такої як Cs2CO3, K2CO3 або трет NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може 16 UA 99734 C2 5 10 15 20 25 здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Проміжні сполуки загальної формули (IIId) можуть бути одержані відновленням проміжних сполук загальної формули (XXVI) за допомогою водню та каталізатора, такого як Pd/C, Pt/C, PtO2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2 або SnCl2.H2O або Fe-HCl, в розчиннику, такому як EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин. Проміжні сполуки загальної формули (XXVI) можуть бути одержані реакцією проміжних 1 сполук загальної формули (XXV) з Z-G , де Z являє собою борну кислоту, боронат, триалкілстанан або похідну цинкату. Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або [1,1'біс(дифенілфосфіно)фероцен]дихлорпаладій(II) (PdCl2(dppf)ДХМ), використовуючи фосфіновий ліганд, такий як BINAP, трициклогексилфосфін (P(Cy) 3) або ксантфос при необхідності, в трет присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. В конкретному випадку, коли Z являє собою похідну триалкілстанану, CuI додають як співкаталізатор. В конкретному випадку, коли Z являє собою похідну цинкату, реакцію здійснюють in situ з відповідною арильною похідною. Проміжні сполуки загальної формули (XXV) можуть бути одержані реакцією проміжних сполук загальної формули (XII) з бензилбромідом в присутності основи, такої як Cs 2CO3, K2CO3 або Ag2CO3, в розчиннику, такому як толуол, бензол або ДМФА, при температурі від 60ºC до 120ºC протягом від 5 до 24 годин. 3 В альтернативній методиці сполуки даного винаходу формули (Ib), де R являє собою карбоновую кислоту, також можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 9. Фігура 9 R9 O OH H2 N OR5 O N 2 X R1 X2 R2 IIb IIc OR5 O R9 H N OH O O R O NH2 R G2 III R1 R2 G1 R4 5 R1 NH2 R2 R9 1 R2 R1 X4 R2 IVb IVc R4 R O H N N 4 G1 G2 R1 R2 Ia R4 R9 N G1 G2 Ib N G1 OH G2 V R9 X OH O O H N R2 IVd 30 O H N CF3 O R1 O R1 R2 R4 NH2 NaBH4 R1 R2 IVe N O CF3 O 4 IVf G1 G2 O O H N V R1 R2 R4 R9 N G1 G2 Ic Сполуки загальної формули (Ib) можуть бути одержані гідролізом сполук формули (Ia) або 1 2 4 9 1 2 5 (Ic), де R , R , R , R , G та G є такими, як описано вище, та R являє собою C1-4 алкільну групу. 5 Коли R являє собою метильну або етильну групу, водний розчин гідроксиду натрію або літію 17 UA 99734 C2 5 10 15 20 25 30 використовується в розчиннику, такому як етанол або ТГФ, в діапазоні температур від 20ºC до 5 70ºC протягом від 1 до 16 годин. Коли R являє собою трет-бутильну групу, гідроліз сполуки формули (Ic) може здійснюватися в кислих умовах, використовуючи трифтороцтову кислоту або хлорид водню в розчиннику, такому як дихлорметан, ТГФ або діоксан, в діапазоні температур від 20ºC до 80ºC протягом від 30 хвилин до 16 годин. Сполуки загальної формули (Ia) можуть бути одержані реакцією проміжної сполуки (IIc), де 2 X є таким, як описано вище, з проміжною сполукою (III), аналогічно до методики, наведеної на фігурі 1 для одержання сполук формули (I) із проміжних сполук (II) та (III). Альтернативно, сполуки загальної формули (Ia) також можуть бути одержані реакцією проміжної сполуки (IVc) з проміжною сполукою (V) аналогічно до методики, наведеної на фігурі 3 для одержання сполук формули (I) із проміжних сполук (IV) та (V). Проміжні сполуки формул (IIc) та (IVc) можуть бути одержані із проміжних сполук (IIb) та (IVb) відповідно, в присутності кислоти, такої як HCl або H2SO4, в розчиннику, такому як метанол, етанол або діоксан, в діапазоні температур від 25ºC до 110ºC протягом від 1 до 48 годин. Сполуки загальної формули (Ic) можуть бути одержані реакцією проміжної сполуки (IVf) з проміжною сполукою (V), аналогічно до методики, описаної на фігурі 3 для одержання сполук формули (I) із проміжних сполук (IV) та (V). Проміжні сполуки загальної формули (IVf) можуть бути одержані із проміжних сполук (IVe) в присутності NaBH4 в розчиннику, такому як метанол або етанол, в діапазоні температур від 0ºC до кімнатної температури. Проміжні сполуки загальної формули (IVe) можуть бути одержані із проміжної сполуки (IVd) в присутності ди-трет-бутилкарбонату або 1,1-дитрет-бутокси-N,N-диметилметанаміну в розчиннику, такому як етанол, толуол, дихлорметан або ДМФА, в діапазоні температур від 25ºC до 100ºC протягом від 2 до 24 годин. Проміжні сполуки загальної формули (IVd) можуть бути одержані із проміжних сполук загальної формули (IVb) в присутності трифтороцтової кислоти або ангідриду трифтороцтової кислоти в діапазоні температур від 25ºC до 70ºC протягом від 1 до 24 годин. 1 В конкретному випадку, коли R являє собою –CF3, проміжні сполуки загальної формули (IVc) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 10. Фігура 10 NH2 F3C R2 XX HO H N F3C O COOR5 O NH2 H N O O R 2 F3C O R XXI F3C R2 2 IVg XXII 35 40 45 Проміжні сполуки загальної формули (IVg) можуть бути одержані із проміжних сполук формули (XXII) в присутності неорганічної кислоти, такої як HCl або H 2SO4, в спиртовому розчиннику, такому як етанол або метанол, в діапазоні температур від 70ºC до 120ºC протягом від 8 до 24 годин. Проміжні сполуки загальної формули (XXII) можуть бути одержані із проміжних сполук загальної формули (XXI). Реакція може здійснюватися в присутності н-бутиллітію та триметилетилендіаміну, та пропускаючи CO2 протягом від 0,5 до 3 годин, в розчиннику, такому як етиловий ефір або ТГФ, в діапазоні температур від -78ºC до -40º. Проміжні сполуки загальної формули (XXI) можуть бути одержані із проміжних сполук загальної формули (XX). Реакція може здійснюватися в присутності ди-трет-бутилкарбонату та водного розчину NaOH при кімнатній температурі протягом від 6 до 48 годин. 3 В конкретному випадку, коли R являє собою тетразолільну групу, сполуки формули (Ie) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 11. 18 UA 99734 C2 Фігура 11 R9 CN H2N X N 2 G1 R4 R1 R2 G2 N III R9 CN XXIII N N NH H N R9 H N N N R1 CN NH2 R2 R9 R 4 G1 G2 R1 R2 XXV R G1 G2 Ie 4 X 1 R4 N R2 R4 XXIV G1 G2 V 5 10 15 20 Сполуки загальної формули (Ie) можуть бути одержані із проміжних сполук загальної формули (XXV). Реакція може здійснюватися в присутності N 3SnMe3 або азиду натрію з NH4Cl або Bu3SnCl при кип’ятінні розчинника, такого як ДМФА або ксилол, в діапазоні температур від 100ºC до 150ºC протягом від 20 до 120 годин. Проміжні сполуки загальної формули (XXXV) можуть бути одержані реакцією проміжних 1 2 2 сполук загальної формули (XXIII), де R , R та X є такими, як описано вище, з проміжними сполуками (III) відповідно до методики, наведеної на фігурі 1 для одержання сполук загальної формули (I) із проміжних сполук (II) та (III). Альтернативно, проміжні сполуки загальної формули 1 2 (XXXV) можуть бути одержані реакцією проміжних сполук загальної формули (XXIV), де R та R є такими, як описано вище, з проміжними сполуками (V), відповідно до методики, наведеної на фігурі 3 для одержання сполук загальної формули (I) із проміжних сполук (V) та (IV). 2 Проміжні сполуки загальної формули (VII), де Z та G є такими, як описано вище, є 2 комерційно доступними. Однако, в конкретному випадку, коли G являє собою циклопропоксифенільну групу, зазначена проміжна сполука може бути одержана відповідно до схеми синтезу, наведеної на фігурі 12. Фігура 12 O Br Br OH + XXXIII 25 30 O O B O Br XXVII XXVIII VIIb Проміжна сполука (VIIb) може бути одержана із 1-бром-3-циклопропоксибензолу (XXVIII) в присутності 4,4,4',4',5,5,5',5'-октаметил-2,2'-біс(1,3,2-діоксаборолану), PdCl2dppf.ДХМ та основи, такої як KAcO, при кип’ятінні розчинника, такого як ДМФА або ДМСО, в діапазоні температур від 130ºC до 180ºC протягом від 45 хвилин до 24 годин. Альтернативно, реакція може здійснюватися в мікрохвильовій печі. 1-Бром-3-циклопропоксибензол (XXVIII) може бути одержаний із 3-бромфенолу (XXXIII) та бромциклопропану (XXVII) в присутності основи, такої як Cs2CO3 або K2CO3, при кип’ятінні 19 UA 99734 C2 5 розчинника, такого як ДМФА або ДМСО, в діапазоні температур від 130ºC до 180ºC протягом від 6 до 24 годин. Альтернативно, реакція може здійснюватися в мікрохвильовій печі. 2 a b В конкретному випадку, коли G являє собою –NR R групу, сполуки формули (If) можуть бути одержані відповідно до схеми синтезу, наведеної на фігурі 13, реакцією проміжних сполук 5 загальної формули (VI), де X являє собою атом брому, та проміжних сполук загальної формули (XXX). Фігура 13 R3 R9 Ra H N Rb N R9 R3 N H H N N XXX R1 R2 G1 R4 X5 R1 R R2 VI 10 15 20 G1 4 Ra N Rb If Реакція може здійснюватися в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc)2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або [1,1'біс(дифенілфосфіно)фероцен]дихлорпаладій(II) (PdCl2(dppf)ДХМ), використовуючи хлорид 1,3трет біс(2,6-діізопропілфеніл)імідазолію, в присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може проводитися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. 1 2 В конкретному випадку, коли G -G являє собою тетрагідрохінолініламіногрупу, сполуки 1 2 формули (Ik) можуть бути одержані відновленням сполук загальної формули (I), де G -G являє собою хінолініламіногрупу (Ij), використовуючи водень та каталізатор, такий як Pd/C, Pt/C, PtO 2, Pd(OH)2 або Ni-Ренея, необов’язково в присутності ZnBr2 або SnCl2.H2O або Fe-HCl, в розчиннику, такому як трифтороцтова кислота, оцтова кислота, EtOAc, MeOH, ТГФ або EtOH, при кімнатній температурі протягом від 1 до 24 годин, як показано на фігурі 14. Фігура 14 25 R3 R1 R9 H N R3 H N N R1 4 R2 R R9 N R4 Ik Ij В конкретному випадку сполук загальної формули (Ih) та (Ig), вони можуть бути одержані із проміжних сполук загальної формули (XXIa) та (XXIb) відповідно, як показано на фігурі 15. 20 UA 99734 C2 Фігура 15 R3 NH2 + R R1 R2 IV R3 ON + Cl 4 Cl XXXVII R 1 H N N + R3 O R4 R1 H N 20 25 30 35 40 N XXIb R3 N R1 Cl Br R4 Cl Ph R4 Ih 15 R 1 Cl XXIa R1 10 H N N + R4 Cl XXXVI R3 5 R3 Br H N H N N Ph R4 Ig Cl Реакція сполук формули (Ih) та (Ig) може здійснюватися реакцією фенілборної кислоти в інертній атмосфері з паладієвим каталізатором, таким як Pd(OAc) 2, Pd2(dba)3, Pd(PPh3)4, PdCl2(PPh3)2 або [1,1'-біс(дифенілфосфіно)фероцен]дихлорпаладій(II) (PdCl2(dppf)ДХМ), використовуючи фосфіновий ліганд, такий як BINAP, трициклогексилфосфін (P(Cy) 3) або трет ксантфос при необхідності, в присутності основи, такої як Cs 2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан або ТГФ, в діапазоні температур від 40ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Проміжні сполуки загальної формули (XXIa) та (XXIb) можуть бути одержані із проміжної сполуки загальної формули (XXXVI) обробкою POBr3 в дихлорметані при кип’ятінні з оберненим холодильником протягом від 2 до 3 годин. Проміжні сполуки загальної формули (XXIV) можуть бути одержані реакцією проміжних сполук загальної формули (IV) та проміжних сполук загальної формули (XXXVII). Реакція може здійснюватися з паладієвим каталізатором, таким як Pd(OAc)2 або Pd2(dba)3, використовуючи фосфіновий ліганд, такий як BINAP або ксантфос, в трет присутності основи, такої як Cs2CO3, K2CO3 або NaO Bu, при кип’ятінні розчинника, такого як толуол, ксилол, ДМФА, вода або діоксан, в діапазоні температур від 80ºC до 160ºC протягом від 0,5 до 24 годин. Реакція також може здійснюватися в мікрохвильовій печі в діапазоні температур від 100ºC до 160ºC протягом від 0,5 до 15 годин. Сполуки загальної формули (II), (IV), (VII), (VIIa), (VIII), (XII), (IXb), (XIV), (XV), (XVI), (XVII), (XVIII), (XIX), (XX), (IIb), (IVb), (XXIII), (XXIV), (XXV), (XXVI), (XXVII), (XXXIII) та (XXXVII) є комерційно доступними або можуть бути одержані відповідно до звичайних методів синтезу, відомих із попереднього рівня техніки. Синтези сполук за винаходом та проміжних сполук для використання тут наведені в наступних прикладах (1-118), включаючи приклади одержання (проміжні сполуки 1-74), які ніяким чином не обмежують обсяг винаходу. 1 Спектры H ядерного магнітного резонансу записували на спектрометрі Varian Mercury 200. Мас-спектри низького розрізнення (m/z) записували на мас-спектрометрі Micromass ZMD, використовуючи іонізацію ESI. Хроматографічні розділення проводили, використовуючи систему Waters 2690, оснащену колонкою Symmetry C18 (2,1 x 10 мм, 3,5 мM). Рухомою фазою була мурашина кислота (0,4 мл), аміак (0,1 мл), метанол (500 мл) та ацетонітрил (500 мл) (Б) та мурашина кислота (0,46 мл), аміак (0,115 мл) та вода (1000 мл) (A): спочатку 0,5 хв з 0% Б, потім від 0% до 95% Б протягом 6,5 хв, та потім 1 хв 95% Б. Час врівноважування між двома введеннями становив 1 хв. Швидкість потоку становила 0,4 мл/хв. Об’єм ін’єкції становив 5 мкл. Діодні хроматограми збирали при 210 нM. Приклади одержання Синтез проміжних сполук Проміжна сполука 1 H2N N CF3 6-Феніл-5-(трифторметил)піридин-3-амін 21 UA 99734 C2 5 10 15 20 25 30 35 40 45 A. 2-Хлор-3-йод-5-нітропіридин Суміш 3-йод-5-нітропіридин-2-олу (37,60 ммоль, 10 г), POCl3 (86,47 ммоль, 7,94 мл) та PCl5 (48,87 ммоль, 10,2 г) нагрівали при 140ºC протягом 45 хвилин в атмосфері аргону. Суміш охолоджували до кімнатної температури, виливали повільно у льодяну воду та екстрагували дихлорметаном. Органічну фазу промивали водою, водним розчином NaHCO 3 та насиченим розчином хлориду натрію. Розчинник упарювали, та сиру суміш очищали хроматографією на SiO2, елююючи сумішшю гексан/ДХМ з одержанням 7,32 г (вихід 69%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 8,90 (s, 1H), 9,19 (s, 1H). Б. 2-Хлор-5-нітро-3-(трифторметил)піридин В колбі Шленка суміш 2-хлор-3-йод-5-нітропіридину (17,58 ммоль, 5,00 г), метил 2,2-дифтор2-(фторсульфоніл)ацетату (8,79 ммоль, 1,12 мл) та CuI (2,64 ммоль, 0,5 г) в ДМФА (30 мл) нагрівали при 70ºC протягом 3 годин в атмосфері аргону. Добавляли метил 2,2-дифтор-2(фторсульфоніл)ацетат (4,40 ммоль, 0,6 мл), та суміш нагрівали при 70ºC протягом 16 годин. Розчинник упарювали, та сиру суміш екстрагували етилацетатом та водою. Сиру суміш очищали хроматографією на SiO2, елююючи сумішшю гексан/ДХМ, одержуючи 1,19 г (вихід 30%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 8,82 (s, 1H), 9,41 (s, 1H). В. 6-Хлор-5-(трифторметил)піридин-3-амін Суміш 2-хлор-5-нітро-3-(трифторметил)піридину (5,25 ммоль, 1,19 г), ZnBr 2 (1,05 ммоль, 0,200 г) та 5% Pt (C) (1,58 ммоль, 0,31 г) в етилацетаті (50 мл) перемішували протягом 20 годин в атмосфері водню. Каталізатор відфільтровували, та тверду речовину промивали теплим етанолом. Розчинник упарювали з одержанням цільового продукту (0,95 г, вихід 92%). 1 H ЯМР (300 МГц, ДМСО-d6) ppm: 5,59 (bs, 1H), 7,37 (s, 1H), 7,92 (s, 1H). Г. N-(5-Бром-3-(трифторметил)піридин-2-іл)ацетамід Суміш 6-хлор-5-(трифторметил)піридин-3-аміну (2,95 ммоль, 0,58 г) та 30% HBr в оцтовій кислоті (6 мл) в закритій колбі нагрівали при 100ºC протягом ночі. Сиру суміш виливали у льодяну воду, значення pH доводили до 10 за допомогою 2N водного розчину NaOH та екстрагували CHCl3. Розчинник вилучали при зниженому тиску з одержанням 0,680 г (вихід 82%) цільового продукту. ESI/MS (m/e, %): 281,96 (100,0%), 283,96 (97,3%). Д. N-(6-Феніл-5-(трифторметил)піридин-3-іл)ацетамід В колбі Шленка суміш N-(5-бром-3-(трифторметил)піридин-2-іл)ацетаміду (2,40 ммоль, 0,680 г), фенілборної кислоти (3,22 ммоль, 0,392 г), карбонату цезію (6,87 ммоль, 2,238 г) та PdCl2dppf.CH2Cl2 (0,24 ммоль, 0,196 г) в суміші діоксан/вода 3:1 (20 мл) нагрівали при 110ºC протягом ночі в атмосфері аргону. Розчинник упарювали, та сиру суміш очищали на SiO2, елююючи сумішшю CH2Cl2/MeOH з одержанням 0,478 г (вихід 71%) цільової сполуки. ESI/MS (m/e, %): 280 (100,0%). Е. 6-Феніл-5-(трифторметил)піридин-3-амін До розчину N-(6-феніл-5-(трифторметил)піридин-3-іл)ацетаміду (1,68 ммоль, 0,280 г) в етанолі (6 мл) добавляли 2N водний розчин NaOH (5 мл). Суміш нагрівали при 110ºC протягом 3 годин. Розчинник вилучали, значення pH доводили до 8 та екстрагували CHCl 3. Розчинник вилучали з одержанням 0,394 г (вихід 98%) цільового продукту. ESI/MS (m/e, %): 238 (100,0%). Проміжна сполука 2 N H2N 50 55 A. 3-Метил-5-нітро-2-фенілпіридин В колбі Шленка суміш 2-бром-3-метил-5-нітропіридину (4,6 ммоль, 1,0 г), фенілборної кислоти (4,6 ммоль, 0,560 г), PdCl2dppf.ДХМ (0,47 ммоль, 0,4 г), Cs2CO3 (13,8 ммоль, 4,5 г) в суміші діоксан/вода 4:1 (18 мл) нагрівали при 100ºC протягом 14 годин в атмосфері аргону. Розчинник упарювали, та сиру суміш екстрагували водою та етилацетатом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 3метил-5-нітро-2-фенілпіридину (0,95 г, вихід 97%) у вигляді основного продукту. + ESI/MS (m/e, %): 215 [(M+1) , 100]. Б. 5-Метил-6-фенілпіридин-3-амін Суміш 3-метил-5-нітро-2-фенілпіридину (4,43 ммоль, 0,95 г) та Pd/C 10% (0,1 г) в етанолі (40 мл) перемішували протягом 16 годин в атмосфері водню. Каталізатор відфільтровували, та 22 UA 99734 C2 5 тверду речовину обережно промивали теплим етанолом. Фільтрат упарювали, та сирий продукт очищали хроматографією на SiO2, елююючи сумішшю ДХМ/метанол та одержуючи 0,65 г (вихід 80%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 2,29 (s, 3H), 6,90 (m, 1H), 7,30- 7,50 (m, 5H), 8,04 (m, 1H). + ESI/MS (m/e, %): 185 [(M+1) , 100]. Проміжна сполука 3 H2N N O 10 15 20 25 30 35 40 6-Метокси-5-фенілпіридин-3-амін A. 5-Нітро-3-фенілпіридин-2-ол В колбі Шленка суміш 3-йод-5-нітропіридин-2-олу (7,52 ммоль, 2 г), фенілборної кислоти (8,28 ммоль, 1,01 г), PdCl2dppf.ДХМ (0,75 ммоль, 0,6 г), Cs2CO3 (22,56 ммоль, 7,4 г) в суміші діоксан/вода 4:1 (26 мл) нагрівали при 100ºC протягом 4 годин в атмосфері аргону. Розчинник упарювали, та сиру суміш екстрагували водою та етилацетатом. Органічну фазу упарювали, та сирий продукт суспендували в метанолі з одержанням твердої речовини, яку відфільтровували та сушили в вакуумі протягом ночі з одержанням 1,2 г (вихід 74%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm:: 7,31 - 7,54 (m, 3H), 7,61 - 7,76 (m, 2H), 8,26 (d, 1H), 8,44 (s, 1H). ESI/MS (m/e, %): 215 [(M-1) , 100]. Б. 2-Бром-5-нітро-3-фенілпіридин Суміш 5-нітро-3-фенілпіридин-2-олу (4,63 ммоль, 1 г), POBr3 (4,74 ммоль, 0,45 мл) та PBr3 (4,71 ммоль, 1,4 г) нагрівали при 120ºC протягом 3,5 годин. Сиру суміш виливали в суміш льоду та води та екстрагували ДХМ. Органічну фазу сушили та упарювали з одержанням 0,8 г (вихід 62%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 7,38 - 7,61 (m, 5H), 8,39 (d, J=2,20 Гц, 1H), 9,19 (d, J=2,20 Гц, 1H). В. 2-Метокси-5-нітро-3-фенілпіридин Суміш 2-бром-5-нітро-3-фенілпіридину (0,72 ммоль, 0,2 г), 2-циклопропіл-4,4,5,5-тетраметил1,3,2-діоксаборолану (0,86 ммоль, 0,16 мл), Pd(PPh3)4 (0,04 ммоль, 0,05 г), K2CO3 (2 ммоль, 0,28 г) в суміші толуол/метанол 4:1 (10 мл) нагрівали при 100ºC протягом 30 хвилин при мікрохвильовому випромінюванні в атмосфері аргону. Розчинник упарювали, та сиру суміш екстрагували водою та етилацетатом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 2-метокси-5-нітро-3-фенілпіридину (0,1 г, вихід 55%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 4,11 (s, 3H) 7,41 - 7,54 (m, 3H) 7,54 - 7,64 (m, 2H) 8,41 (d, J=2,75 Гц, 1H) 9,07 (d, J=2,75 Гц, 1H). Г. 6-Метокси-5-фенілпіридин-3-амін Суміш 2-метокси-5-нітро-3-фенілпіридину (0,43 ммоль, 0,1 г) та Pd/C 10% (0,14 ммоль, 0,015 г) в етанолі (2 мл) перемішували протягом 16 годин в атмосфері водню. Каталізатор відфільтровували, та тверду речовину обережно промивали теплим етанолом. Фільтрат упарювали з одержанням 0,085 г (вихід 98%) цільового продукту. + ESI/MS (m/e, %): 201 [(M+1) , 100]. Проміжна сполука 4 H2N 45 N A. 2-Хлор-3-йод-5-нітропіридин Суміш 3-йод-5-нітропіридин-2-олу (37,6 ммоль, 10 г), POCl3 (86,47 ммоль, 7,94 мл) та PCl5 (48,87 ммоль, 10,2 г) нагрівали при 140ºC протягом 1 год в атмосфері аргону. Сиру суміш виливали в суміш льоду та води та екстрагували ДХМ. Твердий залишок очищали 23 UA 99734 C2 5 10 15 20 хроматографією на SiO2, елююючи сумішшю гексан/дихлорметан з одержанням 2-хлор-3-йод-5нітропіридину (7,32 г, вихід 69%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 8,91 (d, J=2,47 Гц, 1H) 9,19 (d, J=2,47 Гц, 1H). Б. 2-Хлор-5-нітро-3-фенілпіридин В колбі Шленка суміш 2-хлор-3-йод-5-нітропіридину (1,76 ммоль, 0,5 г), фенілборної кислоти (1,94 ммоль, 0,24 г), PdCl2dppf.ДХМ (0,18 ммоль, 0,1 г), Cs2CO3 (5,28 ммоль, 1,7 г) в суміші діоксан/вода 4:1 (6,5 мл) нагрівали при 120ºC протягом 4 годин в атмосфері аргону. Розчинник упарювали, та сиру суміш екстрагували водою та етилацетатом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю гексан/дихлорметан з одержанням 2-хлор-5-нітро3-фенілпіридину (0,23 г, вихід 55%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 7,36 - 7,67 (m, 5H) 8,47 (d, J=2,75 Гц, 1H) 9,23 (d, J=2,75 Гц, 1H). В. 5-Фенілпіридин-3-амін Суміш 2-хлор-5-нітро-3-фенілпіридину (0,43 ммоль, 0,1 г), KOAc (0,43 ммоль, 0,042 г) та Pd/C 10% (0,03 г) в етанолі (4 мл) перемішували протягом 24 годин в атмосфері водню. Каталізатор відфільтровували, та тверду речовину обережно промивали теплим етанолом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю дихлорметан/метанол з одержанням 5-фенілпіридин-3-аміну (0,05 г, вихід 69%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 7,15 - 7,23 (m, 1H), 7,37 - 7,51 (m, 3H), 7,52 - 7,63 (m, 2 H), 8,09 (d, 1H), 8,27 (d, 1H). + ESI/MS (m/e, %): 171 [(M+1) , 100]. Проміжна сполука 5 H2N 25 30 35 40 45 50 N 5,6-Дифенілпіридин-3-амін A. 3-Бром-5-нітропіридин-2-ол До розчину 5-нітропіридин-2-олу (0,06 моль, 8,6 г) в 400 мл води при 40º, добавляли 3,7 мл Br2. Суміш перемішували при 40ºC протягом 2,5 год, та потім суміш перемішували при кімнатній температурі протягом ночі. Тверду речовину відфільтровували, промивали водою та сушили в вакуумі протягом ночі з одержанням 12,5 г (вихід 93%) цільового продукту. 1 H ЯМР (300 МГц, ДМСО-d6) ppm: 8,57 (d, 1H) 8,74 (s, 2H). Б. 2,3-Дибром-5-нітропіридин Одержували (2,23 г, вихід 87%) відповідно до методики, описаної для проміжної сполуки 2 (стадія Б), виходячи із 3-бром-5-нітропіридин-2-олу (9,13 ммоль, 2 г). 1 H ЯМР (300 МГц, CDCl3) ppm: 8,48 - 8,84 (m, 1 H) 8,94 - 9,31 (m, 1 H) ESI/MS (m/e, %): 267 [(M-1) , 100]. В. 5-Нітро-2,3-дифенілпіридин Одержували у вигляді мінорного продукту (0,2 г) відповідно до методики, описаної для проміжної сполуки 2 (стадія A), виходячи із 2,3-дибром-5-нітропіридину (3,55 ммоль, 1 г). 1 H ЯМР (300 МГц, CDCl3) ppm: 7,03 - 7,65 (m, 10H), 8,52 (d, J=2,47 Гц, 1H), 9,49 (d, J=2,47 Гц, 1H). + ESI/MS (m/e, %): 277 [(M+1) , 100]. Г. 5,6-Дифенілпіридин-3-амін Суміш 5-нітро-2,3-дифенілпіридину (0,74 ммоль, 0,21 г) та Pd/C 10% (0,02 г) в метанолі (5 мл) перемішували протягом 16 годин в атмосфері водню. Каталізатор відфільтровували, та тверду речовину обережно промивали метанолом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 0,14 г (вихід 74%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 3,79 (s, 2H), 7,04 (d, J=2,75 Гц, 1H), 7,11 - 7,36 (m, 10H), 8,20 (d, J=2,75 Гц, 1H). + ESI/MS (m/e, %): 247 [(M+1) , 100]. Проміжна сполука 6 24 UA 99734 C2 H 2N 5 10 15 20 N 6-Циклопропіл-5-фенілпіридин-3-амін A. 2-Циклопропіл-5-нітро-3-фенілпіридин В колбі Шленка суміш 2-хлор-5-нітро-3-фенілпіридину (описанного для проміжної сполуки 3 (стадія Б)) (1,43 ммоль, 0,4 г), 2-циклопропіл-4,4,5,5-тетраметил-1,3,2-діоксаборолану (1,59 ммоль, 0,29 мл), PdCl2dppf.ДХМ (0,14 ммоль, 0,12 г), Cs2CO3 (4,3 ммоль, 1,4 г) в суміші діоксан/вода 4:1 (6,5 мл) нагрівали при 100ºC протягом 16 годин в атмосфері аргону. Розчинник упарювали, та сиру суміш екстрагували водою та етилацетатом. Твердий залишок очищали хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 2-циклопропіл-5нітро-3-фенілпіридину (0,06 г, вихід 17%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 0,45 - 0,55 (m, 2H), 0,56 - 0,70 (m, 2H), 2,10 - 2,30 (m, 1H), 7,42 - 7,57 (m, 5H), 8,23 - 8,30 (m, 1H), 9,21 - 9,29 (m, 1H). + ESI/MS (m/e, %): 241 [(M+1) , 100]. Б. 6-Циклопропіл-5-фенілпіридин-3-амін Суміш 2-циклопропіл-5-нітро-3-фенілпіридину (0,25 ммоль, 0,06 г) та SnCl2.H2O (0,89 ммоль, 0,2 г) в етанолі (2 мл) нагрівали при 80ºC протягом 1 години. Розчинник упарювали, та сирий залишок розчиняли у воді. Розчин нейтралізували 6N водним розчином NaOH та екстрагували дихлорметаном. Твердий залишок очищали хроматографією на SiO 2, елююючи сумішшю дихлорметан/метанол з одержанням 6-циклопропіл-5-фенілпіридин-3-аміну (0,03 г, вихід 57%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 0,61 - 0,92 (m, 2H), 0,89 - 1,10 (m, 2H), 1,78 - 2,12 (m, 1H), 3,56 (s, 2H), 6,87 (d, J=2,75 Гц, 1H), 7,31 - 7,57 (m, 5H), 7,78 - 8,15 (m, J=2,75 Гц, 1H). + ESI/MS (m/e, %): 211 [(M+1) , 100]. Проміжна сполука 7 (процес 1) H2N N O 25 30 35 40 6-(3-Метоксифеніл)-5-фенілпіридин-3-амін A. 3-Бром-2-(3-метоксифеніл)-5-нітропіридин Одержували (1,15 г, вихід 39%) відповідно до методики, описаної для проміжної сполуки 2 (стадія A), виходячи із 2,3-дибром-5-нітропіридину (описанного как проміжна сполука 5 (стадія Б) (9,33 ммоль, 2,630 г) та 3-метоксифенілборної кислоти (9,33 ммоль, 1,42 г). + + ESI/MS (m/e, %): 309 [(M+1) , 100], 311 [(M+1) , 80] Б. 2-(3-Метоксифеніл)-5-нітро-3-фенілпіридин Одержували (0,257 г, вихід 87%) відповідно до методики, описаної для проміжної сполуки 2 (стадія A), виходячи із 3-бром-2-(3-метоксифеніл)-5-нітропіридину (0,97 ммоль, 0,300 г) та фенілборної кислоти (1,07 ммоль, 0,130 г). + ESI/MS (m/e, %): 307 [(M+1) , 100]. В. 6-(3-Метоксифеніл)-5-фенілпіридин-3-амін Одержували (0,160 г, вихід 69%) відповідно до методики, описаної для проміжної сполуки 5 (стадія Г), виходячи із 2-(3-метоксифеніл)-5-нітро-3-фенілпіридину (0,84 ммоль, 0,257 г). 1 H ЯМР (300 МГц, ДМСО-d6) ppm: 3,60 (s, 3H), 6,73-6,76 (m, 1H), 6,80-6,83 (m, 1H), 6,856,88 (m, 1H), 7,07-7,16 (m, 1H), 7,17-7,20 (m, 2H), 7,25-7,29 (m, 3H), 8,18-8,20 (m, 1H). + ESI/MS (m/e, %): 277 [(M+1) , 100]. Проміжна сполука 7 (процес 2) OMe N H2N Ph 45 6-(3-Метоксифеніл)-5-фенілпіридин-3-амін A. 2,3-Дибром-5-нітропіридин 25 UA 99734 C2 5 10 15 20 25 Суміш 3-бром-5-нітропіридин-2-олу, POBr3 та PBr3 нагрівали при 120ºC протягом 3,5 год. Сиру суміш виливали в суміш льоду та води та екстрагували ДХМ. Сиру суміш очищали прискореною хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 2,63 г (вихід 73%) цільового продукту. 1 H ЯМР (300 МГц, ДМСО-d6): 8,95 (s, 1H), 9,18 (s, 1H) Б. 3-Бром-2-(3-метоксифеніл)-5-нітропіридин Одержували (1,15 г, вихід 40%) відповідно до методики, описаної для проміжної сполуки 27, виходячи із 2,3-дибром-5-нітропіридину (9,33 ммоль, 2,63 г), 3-метоксифенілборної кислоти (9,33 ммоль, 1,42 г). 1 H ЯМР (300 МГц, ДМСО-d6): 3,80 (s, 3H), 7,09-7,12 (d, 1H), 7,21-7,26 (m, 2H), 7,42-7,47 (t, 1H), 8,95 (s, 1H), 9,40 (s, 1H). + + ESI/MS (m/e, %): 309 [(M+1) , 100], 311[(M+1) , 98]. В. 2-(3-Метоксифеніл)-5-нітро-3-фенілпіридин Одержували (0,258 г, вихід 87%) відповідно до методики, описаної для проміжної сполуки 27, виходячи із 3-бром-2-(3-метоксифеніл)-5-нітропіридину (0,97 ммоль, 0,300 г), фенілборної кислоти (1,07 ммоль, 0,130 г). 1 H ЯМР (300 МГц, CDCl3): 3,64 (s, 3H), 6,89-6,99 (m, 3H), 7,21-7,24 (m, 3H), 7,32-7,37 (m, 4H), 8,50 (s, 1H), 9,47 (s, 1H). + ESI/MS (m/e, %): 307 [(M+1) , 100]. Г. 6-(3-Метоксифеніл)-5-фенілпіридин-3-амін Суміш 2-(3-метоксифеніл)-5-нітро-3-фенілпіридину (0,84 ммоль, 0,257 г) та Pd/C 10% (0,08 ммоль, 0,009 г) в етанолі (5 мл) перемішували протягом 16 годин в атмосфері водню. Каталізатор відфільтровували, та тверду речовину обережно промивали теплим етанолом. Фільтрат упарювали, та сирий продукт очищали хроматографією на SiO 2, елююючи сумішшю ДХМ/метанол з одержанням 0,160 г (вихід 69%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3): 3,60 (s, 3H), 3,91 (bs, 2H), 6,73-6,80 (m, 1H), 6,81-6,83 (t, 1H), 6,85-6,88 (m, 1H), 7,01 (s, 1H), 7,07-7,12 (t, 1H), 7,15-7,19 (m, 2H), 7,22-7,29 (m, 4H), 8,18 (s, 1H). + ESI/MS (m/e, %): 277 [(M+1) , 100]. Проміжна сполука 8 HO O NH2 30 35 40 45 2-Аміно-5-циклопропілбензойна кислота A. Метил 2-аміно-5-циклопропілбензоат В колбі Шленка суміш метил 2-аміно-5-бромбензоату(43,47 ммоль, 10 г), циклопропілборної кислоти (112,92 ммоль, 9,700 г), K3PO4 (144,16 ммоль, 30,6 г), Pd(AcO)2 (3,47 ммоль, 0,780 г), P(Cy)3 (7,85 ммоль, 2,2 г) в толуолі (170 мл) та воді (10 мл) нагрівали протягом 2 годин при 100ºC в атмосфері азоту. Реакційну суміш відфільтровували через целіт, та органічну фазу відокремлювали та упарювали з одержанням 7,34 г (вихід 77%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 0,48 - 0,66 (m, 2H) 0,75 - 0,95 (m, 2H), 1,80 (s, 1H), 3,86 (s, 3H), 5,56 (s, 2H), 6,59 (d, J=8,50 Гц, 1H), 7,03 (dd, J=8,50, 2,15 Гц, 1H), 7,60 (s, 1H). + ESI/MS (m/e, %): 192 [(M+1) , 87]. Б. 2-Аміно-5-циклопропілбензойна кислота До розчину проміжної сполуки 36 (24,58 ммоль, 4,70 г) в суміші MeOH/ТГФ 8:1 (225 мл) добавляли (150 ммоль, 75 мл) 2N водного розчину NaOH, та суміш нагрівали при 60ºC протягом 15 годин. Органічний розчинник упарювали, водну фазу підкисляли до значення pH 5 та екстрагували етилацетатом. Розчинник упарювали з одержанням 3,93 г (вихід 83%) цільового продукту. + ESI/MS (m/e, %): 178 [(M+1) , 100]. Проміжна сполука 9 O OEt 50 Cl Етил 2-хлор-5-циклопропілбензоат 26 UA 99734 C2 5 10 В колбі Шленка суміш етил 5-бром-2-хлорбензоату(7,60 ммоль, 2 г), 2-циклопропіл-4,4,5,5тетраметил-1,3,2-діоксаборолану (7,59 ммоль, 1,3 г), Cs2CO3 (18,97 ммоль, 6,18 г), PdCl2dppf.CH2Cl2 (0,76 ммоль, 0,620 г) в діоксані (70 мл) та воді (15 мл) нагрівали протягом 2 годин при 110ºC в атмосфері аргону. Розчинник упарювали, та суміш екстрагували етилацетатом та водою. Сиру суміш очищали хроматографією на SiO2, елююючи сумішшю гексан/етилацетат з одержанням 1,5 г (вихід 92%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) δ ppm: 0,67-0,71 (t, 3H), 0,97-1,01 (m, 2H), 1,38-1,43 (t, 3H), 1,851,91 (m, 1H), 4,36-4,43 (q, 2H), 7,07-7,10 (d, 1H), 7,26-7,32 (m, 1H), 7,49 (s, 1H). ESI/MS (m/e, %): 225 [(M+1)+, 100]. Проміжна сполука 10 O OEt Cl 15 20 Етил 2-хлор-5-метилбензоат До розчину 2-хлор-5-метилбензойної кислоти (7,62 ммоль, 1,30 г) в етанолі (16 мл) добавляли H2SO4 (35 ммоль, 1,82 мл), та суміш кип’ятили з оберненим холодильником протягом 20 годин. Розчинник упарювали, та сирий залишок розчиняли у воді. Розчин нейтралізували 6N водним розчином NaOH та екстрагували CHCl3. Органічну фазу упарювали з одержанням 1,46 г (вихід 96%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 1,41 (t, 3H), 2,35 (s, 3H), 4,40 (q, 2H), 7,21 (d, 1H), 7,32 (d, 1H), 7,61 (s, 1H). + ESI/MS (m/e, %): 199 [(M+1) , 100]. Проміжна сполука 11 O O NH2 25 30 35 40 45 50 трет-Бутил 2-аміно-5-метилбензоат A. 5-Метил-2-(2,2,2-трифторуцетамідо)бензойна кислота В тригорлу круглодонну колбу з ангідридом трифтороцтової кислоти (283,0 ммоль, 40 мл) добавляли 2-аміно-5-метилбензойну кислоту (39,69 ммоль, 6 г) порціями при температурі від 20ºC до 30ºC. Суміш перемішували при кімнатній температурі протягом 2 годин, та повільно добавляли воду при температурі нижче 30ºC, охолоджуючи колбу зовні льодом. Одержану тверду речовину відфільтровували та сушили в вакуумі протягом ночі з одержанням 9,51 г (вихід 91%). 1 H ЯМР (300 МГц, CDCl3) ppm: 2,41 (s, 2H), 7,50-7,53 (d, 1H), 8,01 (s, 1H), 8,57-8,60 (d, 1H), 11,89 (bs, 1H). Б. трет-Бутил 5-метил-2-(2,2,2-трифторуцетамідо)бензоат До розчину 5-метил-2-(2,2,2-трифторуцетамідо)бензойної кислоти (20,23 ммоль, 5,0 г) в толуолі (40 мл) по каплях добавляли 1,1-ди-трет-бутокси-N,N-диметилметанумін (80,92 ммоль, 19,40 мл). Суміш перемішували при 80ºC протягом 6 годин, та розчинник упарювали. Сиру суміш очищали хроматографією на SiO2, елююючи сумішшю ДХМ/MeOH з одержанням 6,01 г (вихід 98%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 1,63 (s, 9H), 2,37 (s, 3H), 7,38-7,41 (d, 1H), 7,81 (s, 1H), 8,518,54 (d, 1H), 12,36 (bs, 1H). + ESI/MS (m/e, %): 304 [(M+1) , 100]. В. трет-Бутил 2-аміно-5-метилбензоат До суспензії трет-бутил 5-метил-2-(2,2,2-трифторуцетамідо)бензоату(19,78 ммоль, 6,0 г) в етанолі (19 мл), охолодженої в бані вода-лід, добавляли порціями NaBH4 (39,57 ммоль, 1,50 г), та суміш перемішували при кімнатній температурі протягом 3 годин. Повільно добавляли воду (40 мл) та упарювали. Твердий продукт розчиняли в CHCl3 та промивали водою та насиченим розчином хлориду натрію. Органічну фазу упарювали з одержанням 3,73 г (вихід 91%) цільового продукту. 1 H ЯМР (300 МГц, CDCl3) ppm: 1,59 (s, 9H), 2,23 (s, 3H), 5,52 (bs, 2H), 6,56-6,59 (d, 1H), 7,05-7,08 (d, 1H), 7,60 (s, 1H). + ESI/MS (m/e, %): 208 [(M+1) , 100]. Проміжна сполука 12 27 UA 99734 C2 HO O Cl 5 2-Хлор-5-циклопропілбензойна кислота Одержували (9,6 г, вихід 91%) відповідно до методики, описаної для проміжної сполуки 8 (стадія Б), виходячи із проміжної сполуки 9 (50 ммоль, 16,4 г). + ESI/MS (m/e, %): 197 [(M+1) , 100]. Проміжна сполука 13 O OH H N N Cl 10 15 2-(6-Хлорпіридин-3-іламіно)-5-метилбензойна кислота Суміш 6-хлорпіридин-3-аміну (11,67 ммоль, 1,5 г) та 2-бром-5-метилбензойної кислоти (23,34 ммоль, 5,02 г), Cu (1,17 ммоль, 0,1 г), Cu 2O (0,58 ммоль, 0,1 г) та K2CO3 (23,34 ммоль, 3,2 г) в 1,2-диметоксіетані (15 мл) нагрівали при 130ºC протягом 16 годин в атмосфері аргону. Добавляли воду, та суміш відфільтровували через целіт. Добавляли 2N водний розчин HCl до значення pH 6, та одержану тверду речовину відфільтровували. Сирий продукт очищали хроматографією, елююючи сумішшю ДХМ/MeOH з одержанням 1,40 г (вихід 46%). 1 H ЯМР (ДМСО-d6) ppm: 2,24 (s, 3H), 7,16-7,19 (d, 1H), 7,25-7,27 (d, 1H), 7,38-7,41 (d, 1H), 7,67-7,73 (m, 2H), 8,28 (s, 1H), 9,45 (bs, 1H). + ESI/MS (m/e, %): 263 [(M+1) , 100]. Проміжна сполука 14 HO O H N N Br 20 25 2-(6-Бромпіридин-3-іламіно)-5-циклопропілбензойна кислота Одержували (0,680 г, вихід 6%) відповідно до методики, описаної для проміжної сполуки 13, виходячи із 6-бромпіридин-3-аміну (28,90 ммоль, 5 г) та проміжної сполуки 12 (34,68 ммоль, 6,82 г). + + ESI/MS (m/e, %): 333 [(M+1) , 100], 335[(M+1) , 97]. Проміжна сполука 15 O O H N N Br 30 35 трет-Бутил 2-(6-бромпіридин-3-іламіно)-5-метилбензоат В колбі Шленка суміш трет-бутил 2-аміно-5-метилбензоату(2,89 ммоль, 0,600 г), 2-бром-5йодпіридину (2,89 ммоль, 0,822 г), BINAP (0,29 ммоль, 0,096 г), Pd2(dba)3 (0,14 ммоль, 0,132 г) та трет NaO Bu (5,79 ммоль, 0,556 г) в толуолі (15 мл) нагрівали при 120ºC протягом 3 годин. До сирої реакційної суміші добавляли воду та етилацетат. Водну фазу екстрагували знову етилацетатом. Органічну фазу промивали водою та насиченим розчином хлориду натрію, сушили, відфільтровували та концентрували в вакуумі. Сиру суміш очищали хроматографією (Biotage 40S, SiO2, гексан:етилацетат від 0% до 10%) з одержанням 0,422 г (вихід 40%) цільового продукту. 1 H ЯМР (200 МГц, CDCl3) ppm: 1,61 (s, 9H), 2,29 (s, 3H), 7,11-7,16 (m, 2H), 7,35-7,43 (m, 2H), 7,73 (s, 1H), 8,28 (s, 1H), 9,44 (s, 1H). + ESI/MS (m/e, %): 363 [(M+1) , 100]. Проміжна сполука 16 28
ДивитисяДодаткова інформація
Назва патенту англійськоюAzabiphenylaminobenzoic acid derivatives as dhodh inhibitors
Автори англійськоюCastro Palomino Laria, Julio, Cesar, Terricabras Belart, Emma, Erra Sola, Montserrat, Navarro Romero, Eloisa, Fonkerna Pou Sil'viya, Cardus Figueras, Aranzazu, Lozoya Toribio, Maria, Estrella
Назва патенту російськоюПроизводные азабифениламинобензойной кислоты как ингибиторы dhodh
Автори російськоюКастро Паломино Лария Хулио Сезар, Террикабрас Беларт Эмма, Эрра Сола Монтсеррат, Наварро Ромеро Элоиза, Фонкерна Поу Сильвия, Кардус Фигуэрас Арансасу, Лосоя Торибио Мария Эстрелла
МПК / Мітки
МПК: C07D 413/10, C07D 401/10, A61P 19/00, A61P 35/00, A61P 37/00, C07D 239/42, C07D 401/04, A61K 31/44, A61P 31/00, A61K 31/506, C07D 213/74, A61P 17/00
Мітки: інгібітори, dhodh, азабіфеніламінобензойної, кислоти, похідні
Код посилання
<a href="https://ua.patents.su/95-99734-pokhidni-azabifenilaminobenzojjno-kisloti-yak-ingibitori-dhodh.html" target="_blank" rel="follow" title="База патентів України">Похідні азабіфеніламінобензойної кислоти як інгібітори dhodh</a>
Попередній патент: Ін’єкційний пристрій з механізмом фіксації для оправи шприца та спосіб зняття ковпачка з ін’єкційного пристрою
Наступний патент: Конденсовані біциклічні піримідини
Випадковий патент: Ферозондовий пристрій












