Сполуки тіадіазину, спосіб їх одержання і фармацевтична композиція, яка їх містить
Номер патенту: 80046
Опубліковано: 10.08.2007
Автори: Грандорж Еманюель, Франкотт П'єр, Бовері Стефан, деТюльйо Паскаль, Лєстаж П'єр, Данобер Лоранс, Піротт Бернар, Кеньяр Даніель-Енрі, Ренар Пьєр
Формула / Реферат
1. Сполуки формули (І):
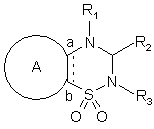 , (І)
, (І)
де:
А, з двома атомами вуглецю, які до нього приєднані, утворює тієнільну, фурильну або піролільну групу, вибрану з груп А1, А2, А3:
 ,
, 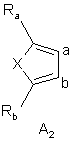 ,
, 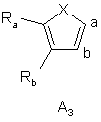 ,
,
де Х в кожному випадку являє собою атом сірки, кисню або азоту, і Ra і Rb, які можуть бути однаковими або відрізнятись, кожний незалежно від іншого являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну групу (необов'язково заміщену одним або більше атомами фтору), лінійну або розгалужену (С1-С6)алкоксигрупу, атом галогену, гідроксигрупу, аміногрупу, необов'язково заміщену лінійною або розгалуженою (С1-С6)алкілкарбонільною групою, однією або двома лінійними або розгалуженими (С1-С6)алкільними групами, карбоксильну групу або лінійну або розгалужену (С1-С6)алкоксикарбонільну групу, оксатіольну групу, вибрану з груп А4, А5, А6, А7:
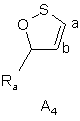 ,
, 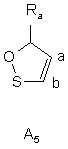 ,
, 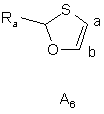 ,
, 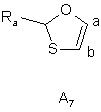 ,
,
де Ra є таким же, як визначено вище, тіазольну групу, вибрану з груп A8, A9:
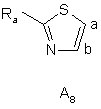 ,
, 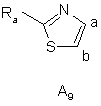 ,
,
де Ra є таким же, як визначено вище, ізотіазольну групу, вибрану з груп А10, A11:
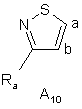 ,
, 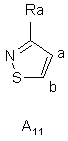 ,
,
де Ra є таким же, як визначено вище, оксазольну групу, вибрану з груп А12, А13, А14, А15:
 ,
,  ,
, 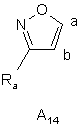 ,
, 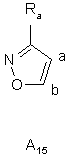 ,
,
де Ra є таким же, як визначено вище, або імідазольну групу формули А16:
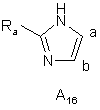 ,
,
де Ra є таким же, як визначено вище,
![]() являє собою одинарний зв'язок або подвійний зв'язок,
являє собою одинарний зв'язок або подвійний зв'язок,
R1 являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, які відрізняються від фтору, або (С1-С6)алкоксі-(С1-С6)алкільну групу, в якій кожна алкільна частина може бути лінійною або розгалуженою,
R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, які відрізняються від фтору,
R3 являє собою атом водню або групу, вибрану з лінійного або розгалуженого (С1-С6)алкілу, CONHR' і SO2NHR’, де R' являє собою лінійну або розгалужену (С1-С6)алкільну групу,
їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
2. Сполуки формули (І) за п. 1, які відрізняються тим, що А являє собою тієнільну групу, яку вибирають з груп A1, А2 і А3, де Х являє собою атом сірки, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
3. Сполуки формули (І) за п. 1 або 2, які відрізняються тим, що А являє собою тієнільну групу, яку вибирають з груп A1 і А2, де Х являє собою атом сірки, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
4. Сполуки формули (І) за п. 2 або 3, які відрізняються тим, що Ra і Rb кожний являє собою незалежно один від одного атом водню або атом хлору, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
5. Сполуки формули (І) за п. 1, які відрізняються тим, що R1 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, переважно метильну, етильну або ізопропільну групу, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
6. Сполуки формули (І) за п. 1, які відрізняються тим, що R2 являє собою атом водню, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
7. Сполуки формули (І) за п. 1, які відрізняються тим, що R3 являє собою атом водню або CONHR', де R' є таким же, як визначено для формули (І), їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою.
8. Сполуки формули (І) за п. 1, які являють собою:
6-хлор-4-етил-3,4-дигідро-2Н-тієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид,
6-хлор-4-ізопропіл-3,4-дигідро-2Н-тієно [3,2-е][1,2,4]тіадіазин 1,1-діоксид,
5,7-дихлор-4-метил-3,4-дигідро-2Н-тієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид.
9. Спосіб одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II):
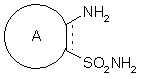 , (II)
, (II)
в якій А і ![]() є такими ж, як визначено для формули (І), сполуку формули (II) циклізують у присутності сполуки формули (ІІІ):
є такими ж, як визначено для формули (І), сполуку формули (II) циклізують у присутності сполуки формули (ІІІ):
R2 - С(ОМе)3, (III)
в якій R2 є таким же, як визначено для формули (І), з одержанням сполуки формули (IV):
 , (IV)
, (IV)
в якій A, R2 і ![]() є такими ж, як визначено вище, сполуку формули (IV)
є такими ж, як визначено вище, сполуку формули (IV)
або піддають реакції з відновлювальним агентом з одержанням сполуки формули (І/а), яка являє собою окремий випадок сполук формули (І):
 , (I/a)
, (I/a)
в якій A, R2 і ![]() є такими ж, як визначено вище,
є такими ж, як визначено вище,
сполуку формули (І/а) необов'язково піддають реакції з ди(трет-бутил)-дикарбонатом з одержанням сполуки формули (V):
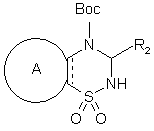 , (V)
, (V)
в якій Вос являє собою групу трет-бутоксикарбонілу, і в якій A, R2 і ![]() є такими ж, як визначено вище, сполуку формули (V) піддають реакції зі сполукою формули (VI):
є такими ж, як визначено вище, сполуку формули (V) піддають реакції зі сполукою формули (VI):
R'3-Y3 (VI),
в якій R'3 являє собою лінійну або розгалужену (С1-С6)алкільну групу або CONHR', або SO2NHR' групу, в якій R' є таким же, як визначено для формули (І), і Y3 являє собою відхідну групу, з одержанням, після зняття захисту, сполуки формули (І/b), яка являє собою окремий випадок сполук формули (І):
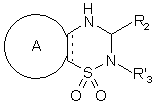 , (I/b)
, (I/b)
в якій A, R2, R'3 і ![]() є такими ж, як визначено вище,
є такими ж, як визначено вище,
або піддають реакції, в основному середовищі, зі сполукою формули (VII):
R'1 – Y1 (VII)
в якій R'1 являє собою лінійну або розгалужену (С1-С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, і Y1 являє собою відхідну групу, з одержанням сполуки формули (VIII):
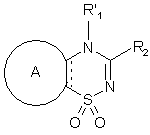 , (VIII)
, (VIII)
в якій A, R'1, R2 і ![]() є такими ж, як визначено вище, сполуку формули (VIII) піддають реакції з відновлювальним агентом з одержанням сполуки формули (І/с), яка являє собою окремий випадок сполук формули (І):
є такими ж, як визначено вище, сполуку формули (VIII) піддають реакції з відновлювальним агентом з одержанням сполуки формули (І/с), яка являє собою окремий випадок сполук формули (І):
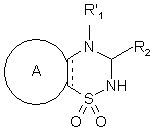 , (I/c)
, (I/c)
в якій A, R'1,R2 і ![]() є такими ж, як визначено вище,
є такими ж, як визначено вище,
сполуку формули (І/с) необов'язково піддають реакції зі сполукою формули (VI), як визначено вище, з одержанням сполуки формули (I/d), яка являє собою окремий випадок сполук формули (І):
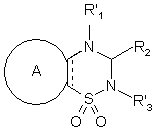 , (I/d)
, (I/d)
в якій A, R'1, R2, R'3 і ![]() є такими ж, як визначено вище, сполуки формул (І/а) - (I/d) утворюють сукупність сполук формули (І), які очищують, якщо необхідно, відповідно до звичайної техніки очищення, розділяють, якщо бажано, на їх енантіомери або діастереоізомери, відповідно до звичайної техніки розділення, і перетворюють, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою.
є такими ж, як визначено вище, сполуки формул (І/а) - (I/d) утворюють сукупність сполук формули (І), які очищують, якщо необхідно, відповідно до звичайної техніки очищення, розділяють, якщо бажано, на їх енантіомери або діастереоізомери, відповідно до звичайної техніки розділення, і перетворюють, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою.
10. Фармацевтична композиція, яка містить як активний інгредієнт сполуку за будь-яким з пп. 1-8, одну або в поєднанні з одним або більше інертним, нетоксичним, фармацевтично прийнятним носієм.
11. Фармацевтична композиція за п. 10 для застосування у виробництві лікарських засобів для лікування захворювань, які вимагають модуляторів АМРА.
12. Фармацевтична композиція за п. 11 для застосування як лікарських засобів як таких, що сприяють процесам запам'ятовування і пізнання.
13. Фармацевтична композиція за п. 11 для застосування як лікарський засіб у лікуванні шизофренії.
Текст
1. Сполуки формули (І): 3 80046 R6 N S b Ra a N S a b A11 , , де Ra є таким же, як визначено вище, оксазольну груп у, вибрану з груп А12 , А13, А14 , А15: A10 O Ra N N Ra a O b A12 a b A13 , , Ra N O a a N b O b Ra A14 , A1 5 , де Ra є таким же, як визначено вище, або імідазольну груп у формули А16: H N Ra a N b A16 , де Ra є таким же, як визначено вище, являє собою одинарний зв'язок або подвійний зв'язок, R1 являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, які відрізняються від фтору, або (С1-С6)алкоксі-(С1-С6)алкільну групу, в якій кожна алкільна частина може бути лінійною або розгалуженою, R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, які відрізняються від фтор у, R3 являє собою атом водню або групу, вибрану з лінійного або розгалуженого (С1-С6)алкілу, CONHR' і SO2NHR’, де R' являє собою лінійну або розгалужену (С1-С6)алкільну гр упу, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 2. Сполуки формули (І) за п. 1, які відрізняються тим, що А являє собою тієнільну групу, яку вибирають з груп A1, А2 і А3, де Х являє собою атом сірки, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 4 3. Сполуки формули (І) за п. 1 або 2, які відрізняються тим, що А являє собою тієнільну гр упу, яку вибирають з груп A1 і А2 , де Х являє собою атом сірки, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 4. Сполуки формули (І) за п. 2 або 3, які відрізняються тим, що Ra і Rb кожний являє собою незалежно один від одного атом водню або атом хлору, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 5. Сполуки формули (І) за п. 1, які відрізняються тим, що R1 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну груп у, переважно метильну, етильну або ізопропільну групу, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 6. Сполуки формули (І) за п. 1, які відрізняються тим, що R2 являє собою атом водню, їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 7. Сполуки формули (І) за п. 1, які відрізняються тим, що R3 являє собою атом водню або CONHR', де R' є таким же, як визначено для формули (І), їх енантіомери і діастереоізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою або основою. 8. Сполуки формули (І) за п. 1, які являють собою: 6-хлор-4-етил-3,4-дигідро-2Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид, 6-хлор-4-ізопропіл-3,4-дигідро-2Н-тієно [3,2е][1,2,4]тіадіазин 1,1-діоксид, 5,7-дихлор-4-метил-3,4-дигідро-2Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид. 9. Спосіб одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): NH 2 A (II) SO2NH2 , в якій А і є такими ж, як визначено для формули (І), сполуку формули (II) циклізують у присутності сполуки формули (ІІІ): R2 - С(ОМе)3, (III) в якій R2 є таким же, як визначено для формули (І), з одержанням сполуки формули (IV): H N A S R2 (IV) N O O , в якій A, R2 і є такими ж, як визначено вище, сполуку формули (IV) або піддають реакції з відновлювальним агентом з одержанням сполуки формули (І/а), яка являє собою окремий випадок сполук формули (І): 5 H N 80046 R2 A (I/a) NH S O O , в якій A, R2 і є такими ж, як визначено вище, сполуку формули (І/а) необов'язково піддають реакції з ди(трет-бутил)-дикарбонатом з одержанням сполуки формули (V): 6 в якій A, R'1, R2 і є такими ж, як визначено вище, сполуку формули (VIII) піддають реакції з відновлювальним агентом з одержанням сполуки формули (І/с), яка являє собою окремий випадок сполук формули (І): R'1 A S R2 O O в якій (V) NH , являє Вос собою групу трет бутоксикарбонілу, і в якій A, R2 і є такими ж, як визначено вище, сполуку формули (V) піддають реакції зі сполукою формули (VI): R'3-Y3 (VI), в якій R'3 являє собою лінійну або розгалужену (С1С6)алкільну груп у або CONHR', або SO2NHR' гр упу, в якій R' є таким же, як визначено для формули (І), і Y3 являє собою відхідну гр уп у, з одержанням, після зняття захисту, сполуки формули (І/b), яка являє собою окремий випадок сполук формули (І): H N R2 A N S (I/b) R'3 O O , в якій A, R2, R'3 і є такими ж, як визначено вище, або піддають реакції, в основному середовищі, зі сполукою формули (VII): R'1 – Y1 (VII) в якій R'1 являє собою лінійну або розгалужену (С1С6)алкільну групу, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, і Y1 являє собою відхідну груп у, з одержанням сполуки формули (VIII): R'1 N A R2 (VIII) N S O O (I/c) NH S O O Вос N R2 N A , в якій A, R'1,R2 і є такими ж, як визначено вище, сполуку формули (І/с) необов'язково піддають реакції зі сполукою формули (VI), як визначено вище, з одержанням сполуки формули (I/d), яка являє собою окремий випадок сполук формули (І): R'1 N A R2 N S O O (I/d) R'3 , в якій A, R'1 , R2, R'3 і є такими ж, як визначено вище, сполуки формул (І/а) - (I/d) утворюють сукупність сполук формули (І), які очищують, якщо необхідно, відповідно до звичайної техніки очищення, розділяють, якщо бажано, на їх енантіомери або діастереоізомери, відповідно до звичайної техніки розділення, і перетворюють, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою. 10. Фармацевтична композиція, яка містить як активний інгредієнт сполуку за будь-яким з пп. 1-8, одну або в поєднанні з одним або більше інертним, нетоксичним, фармацевтично прийнятним носієм. 11. Фармацевтична композиція за п. 10 для застосування у виробництві лікарських засобів для лікування захворювань, які вимагають модуляторів АМРА. 12. Фармацевтична композиція за п. 11 для застосування як лікарських засобів як таких, що сприяють процесам запам'ятовування і пізнання. 13. Фармацевтична композиція за п. 11 для застосування як лікарський засіб у лікуванні шизофренії. , Даний винахід відноситься до нових сполук тіадіазину, до способу їх одержання і фармацевтичних композицій, які їх містять. На сьогоднішній день визнано, що збуджувальні амінокислоти, особливо глутамат, відіграють вирішальну роль у фізіологічних процесах нейронної пластичності і в механізмах, що лежать в основі навчання і запам'ятовування. Патофізіологічні дослідження чітко продемонстрували, що дефіцит у глутаматергічній нейротрансмісії тісно пов'язаний з розвитком хвороби Альцгеймера [Neuroscience and Biobehavioral reviews, 1992, 16, 13-24; Progress in Neurobiology, 1992, 39, 517-545]. Крім того, деякі роботи за останні роки продемонстрували існування підтипів рецепторів збуджувальних амінокислот і їх функціональних взає 7 80046 модій [Molecular Neuropharmacology, 1992, 2, 1531]. Серед рецепторів, рецептори АМРА (a-аміно3-гідрокси-5-метил-4-ізоксазол-пропіонова кислота), очевидно, залучені найбільшим чином у явища фізіологічної нейронної збудливості і, особливо, в ті явища, які залучені до процесів запам'ятовування. Наприклад, було виявлено, що навчання пов'язане зі зростанням у зв'язуванні АМРА з його рецептором в гіпокампусі, одній з ділянок мозку, суттєви х для процесів запам'ятовування і пізнавання. Також, ноотропні агенти, такі як анірацетам, нещодавно були описані як такі, що модулюють АМРА рецептори нейронних клітин позитивним чином [Journal of Neurochemistry, 1992, 58, 1199-1204]. В літературі, сполуки, які мають структур у бензаміду, були описані як такі, що володіють тим же механізмом дії і покращують процес запам'ятовування [Synapse, 1993, 15, 326-329). Сполука ΒΑ 74, зокрема, являє собою найбільш активний з нових фармакологічних агентів. Нарешті, опис [патенту ЕР 692484] розкриває сполуку бензотіадіазину, яка володіє полегшувальною активністю відносно струму АМРА, і [патентна заявка WO 99/42456] описує серед інших конкретні сполуки бензотіадіазину як модулятори АМРА рецепторів. Сполуки тіадіазину, до яких відноситься даний винахід, окрім того, що вони є новими, несподівано проявляють особливо цінну фармакологічну активність на АМРА стр ум, яка є очевидно кращою у порівнянні з активністю сполук, що мають подібні структури, які розкриті у попередньому рівні техніки. Вони с корисними як АМРА модулятори для лікування або запобігання розладам запам'ятовування і пізнавання, які пов'язані з віком, синдромами тривоги або депресії, прогресуючими нейродегенеративними захворюваннями, хворобою Альцгеймера, хворобою Піка, хореєю Хантінгтона, шизофренією, наслідками гострих нейродегенеративних захворювань, наслідками ішемії і наслідками епілепсії. Більш конкретно, даний винахід відноситься до сполук формули (І): 8 , де X в кожному випадку являє собою атом сірки, кисню або азоту і Ra і Rb, які можуть бути однаковими або відрізнятись, кожний незалежно від іншого являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну гр упу (необов'язково заміщену одним або більше атомами фтору), лінійну або розгалужену (С1-С6)алкоксигрупу, атом галогену, гідрокигрупу, аміногрупу, необов'язково заміщену лінійною або розгалуженою (С1С6)алкілкарбонільною групою, однією або двома лінійними або розгалуженими (С1-С6)алкільними групами, карбоксильну груп у або лінійну або розгалужену (С1-С6)алкоксикарбонільну груп у, оксатіольну групу, вибрану з груп А4, А5, А6, А7: , де Ra є таким же, як визначено вище, тіазольну гр уп у, вибрану з груп А8, А9: , де Ra є таким же, як визначено вище, ізотіазольну груп у, вибрану з гр уп А10 , А11: , де: - А, з двома атомами вуглецю, які несуть його, утворює тієнільну, фурильну або піролільну гр упу, вибрану з груп А1 , А2, А3: де Ra є таким же, як визначено вище, оксазольну групу, вибрану з груп А12 , А13 , A14 , А15: 9 80046 де Ra є таким же, як визначено вище, або імідазольну груп у формули А16: де Ra є таким же, як визначено вище, - ------ являє собою одинарний зв'язок або подвійний зв'язок, - R1 являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну груп у, необов'язково заміщену одним або більше атомами фтору, або множиною атомів галогену, які відрізняються від фтор у, або (С1-С6)алкоксі-(С1-С6)алкільну групу, в якій кожна алкільна частина може бути лінійною або розгалуженою, - R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну гр упу, необов'язково заміщену одним або більше атомами фтору, або множиною атомів галогену, які відрізняються від фтор у, - R3 являє собою атом водню або групу, вибрану з лінійного або розгалуженого (С1-С6)алкілу, CONHR' і SO2NHR', де R' являє собою лінійну або розгалужену (С1-С6)алкільну гр упу, до їх енантіомерів і діастереоізомерів, а також до їх адитивних солей з фармацевтично прийнятною кислотою або основою. Серед фармацевтично прийнятних кислот можуть бути згадані, без будь-якого обмеження, хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, фосфорна кислота, оцтова кислота, трифтороцтова кислота, молочна кислота, піровиноградна кислота, малонова кислота, янтарна кислота, глутарова кислота, фумарова кислота, винна кислота, малеїнова кислота, лимонна кислота, аскорбінова кислота, метансульфонова кислота, камфорна кислота і т.д. Серед фармацевтично прийнятних основ можуть бути згадані, без будь-якого обмеження, гідроксид натрію, гідроксид калію, триетиламін, третбутиламін і т.д. Група А, якій віддається перевага, являє собою тієнільну груп у, вибрану з гр уп А2 і А3 , де X являє собою атом сірки. Навіть більш переважно, група А, якій віддається перевага, являє собою тієнільну групу, вибрану з груп А1 і А2 , де X являє собою атом сірки. Групи Ra і Rb, яким віддається перевага, незалежно одна від одної, являють собою атом водню і атом хлору. Група R1, якій віддається перевага, являє собою атом водню лінійну або розгалужену (С1С6)алкільну групу, переважно метальну, етильну або ізопропільну гр упу. 10 Група R2, якій віддається перевага, являє собою атом водню. Група R3, якій віддається перевага, являє собою атом водню або CONHR' групу, в якій R' є таким же, як визначено для формули (І). Сполуки, яким віддається перевага за даним винаходом, являють собою наступні: 6-хлор-4-етил-3,4-дигідро-2Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид, - 6-хлор-4-ізопропіл-3,4-дигідро-2Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид, - 5,7-дихлор-4-метил-3,4-дигідро-2Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид. Винахід відноситься також до способу одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): , в якій А і ------ є такими ж, як визначено для формули (І), сполуку формули (II) циклізують у присутності сполуки формули (lll): R2-C(OMe)3 (lll) в якій R2 є таким же, як визначено для формули (І), з тим, щоб одержати сполуку формули (IV): , в якій A, R2 і ------ є такими ж, як визначено вище, сполуку формули (IV): - або піддають реакції з відновлювальним агентом з тим, щоб одержати сполуку формули (І/а), яка являє собою конкретний випадок сполук формули (І): , в якій A, R2 і ------ є такими ж, як визначено вище, сполуку формули (І/а) необов'язково піддають реакції з ди(трет-бутил)-дикарбонатом з тим, щоб одержати сполуку формули (V): 11 80046 12 вище, з тим, щоб одержати сполуку формули (I/d), яка являє собою конкретний випадок сполук формули (І): , в якій Вос являє собою групу третбутоксикарбонілу і в якій A, R2 і ------ є такими ж, як визначено вище, сполуку формули (V) піддають реакції зі сполукою формули (VI): R'3-Y3 (VI) в якій R'3 являє собою лінійну або розгалужену (С1-С6)алкільну групу або CONHR' або SO2NHR' груп у, в якій R' є таким же, як визначено для формули (І), і Y3 являє собою відхідн у гр упу, з тим, щоб одержати, після зняття захисту, сполуку формули (І/b), яка являє собою конкретний випадок сполук формули (І): , в якій A, R2, R'3 і ------ є такими ж, як визначено вище, - або піддають реакції, в основному середовищі, зі сполукою формули (VII): R'1-Y1 (VII) в якій R'1 являє собою лінійну або розгалужену (С1-С6)алкільну груп у, необов'язково заміщену одним або більше атомами фтору або множиною атомів галогену, і Y1 являє собою відхідну гр упу, з тим, щоб одержати сполуку формули (VIII): , в якій A, R'1, R2 і ------ є такими ж, як визначено вище, сполуку формули (VIII) піддають реакції з відновлювальним агентом з тим, щоб одержати сполуку формули (І/с), яка являє собою конкретний випадок сполук формули (І): , в якій A, R'1, R2 і ------ є такими ж, як визначено вище, сполуку формули (І/с) необов'язково піддають реакції зі сполукою формули (VI), як визначено , в якій A, R'1, R2, R'3 і ------ є такими ж, як визначено вище, сполуки формул (І/а)-(I/d) утворюють сукупність сполук формули (І), які очищують, якщо необхідно, відповідно до звичайної техніки очищення, розділяють, якщо бажано, на їх енантіомери або діастереоізомери відповідно до звичайної техніки розділення і перетворюють, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою. Сполуки за даним винаходом, окрім того, що вони є новими, володіють АМРА-рецепторактивуючими властивостями, які роблять їх корисними у лікуванні розладів пізнавальної здатності, пов'язаних з церебральним старінням і з нейродегенеративними патологіями, такими як хвороба Альцгеймера, хвороба Паркінсона, алкогольний параліч, лобна і субкортикоїдальна деменції, а також у лікуванні шизофренії. Винахід також відноситься до фармацевтичних композицій, які містять як активний інгредієнт сполуку формули (І) разом з одним або більше прийнятними інертними, нетоксичними ексципієнтами. Серед фармацевтичних композицій відповідно до даного винаходу можуть бути згадані більш конкретно ті, які прийнятні для орального, парентерального (внутрішньовенного або підшкірного) або назального введення, таблетки, драже, під'язикові таблетки, желатинові капсули, коржики, супозиторії, креми, мазі, дермальні гелі, ін'єктовані препарати, питні суспензії і т.д. Корисне дозування може бути пристосоване в залежності від природи і тяжкості захворювання, шляху введення, віку і ваги пацієнта. Дозування знаходиться в діапазоні від 1 до 500мг на день за одне або більше введень. Наступні приклади демонструють даний винахід і жодним чином не обмежують його об'єму. Як вихідні матеріали використовують продукти, які відомі або виготовляються відповідно до відомих способів приготування. Структури сполук, описані у Прикладах, були визначені відповідно до звичайної спектрофотометричної техніки (інфрачервоне випромінювання, ЯМР, мас-спектрометрія...). Приготування 1: 6-Хлор-4Н-тієно[3,2с][1,2,4]тіадіазин 1,1-діоксид 250мг 3-аміно-5-хлор-2-тіофенсульфонамід гідрохлориду [J. Med. Chem., 2002, 4171-4187] вміщують в 2,5мл триетил о-форміату. Розчин нагрівають при близько 60°С протягом 30 хвилин. Утворюється гранульований жовтий осад, і його 13 80046 збирають фільтруванням, промивають діетиловим ефіром і потім висушують. Точка плавлення: 260-262°С ІЧ (KВr): 3214, 3103, 3061, 2926, 1602, 1569, 1515, 1446, 1378, 1366, 1287, 1220, 1177, 1147, 978, 840, 824, 750, 628, см-1 Приготування 2: 5,7-Дихлор-4Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 2,5-Ди хлор-4-нітро-3тіофенсульфоніл хлорид Суміш 30мл сірчаної кислоти і 30мл азотної кислоти, що димить, охолоджують за допомогою просоченої сіллю льодяної бані. 10г 2,5-дихлор-3тіофенсульфоніл хлориду повільно додають до суміші. Розчин перемішують при температурі навколишнього середовища протягом 3 годин. Розчин потім виливають на лід. Жовтуватий осад, який утворюється, збирають фільтруванням, промивають водою і висушують. ІЧ (KВr): 3525, 3410, 2917, 1673, 1552, 1442, 1388, 1176, 1085 см -1 Стадія В: 2,5-Дихлор-4-нітро-3тіофенсульфонамід 11г сполуки вищезазначеної Стадії А розчиняють в 150мл діоксану. Цей розчин додають краплями до 300мл 10% розчину гідроксиду амонію. Через одну годину, аміак і діоксан випаровують під зниженим тиском. Білий осад, який утворюється, збирають фільтруванням, промивають водою і висушують. Точка плавлення: 125-126°С ІЧ (KВr): 3390, 3291, 1541, 1505, 1440,1369, 1170, 1090 см-1 Стадія С: 4-Аміно-2,5-дихлор-3тіофенсульфонамід 7,25г сполуки вищезазначеної стадії В вміщують в 375мл 1:1 суміші етанол/вода. Розчин нагрівають доти, доки продукт не розчинитися. Потім додають 4,5г хлориду амонію, з наступними 15г порошкоподібного заліза. Через 10 хвилин нагрівання зі зворотним холодильником, реакцію завершують. Нерозчинний матеріал видаляють фільтруванням і промивають невеликою кількістю гарячого етанолу. Фільтрат випаровують під зниженим тиском. Бежевий осад, який утворюється, збирають фільтруванням, промивають водою і потім висушують. Точка плавлення: розкладення при близько 120°С ІЧ (KВr): 3440, 3412, 3354, 3290, 1600, 1557, 1336, 1318, 1166, 1125 см -1 Стадія D: 5,7-Дихлор-4Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид 250мг сполуки вищезазначеної стадії С розчиняють в 2,5мл триметил ортоформіату. Розчин доводять докипіння у відкритій посудині. Через 1,5 годин реакцію завершують. Розчину дають охолонути, одержуючи бежевий осад, який збирають фільтруванням, промивають діетиловим ефіром і висушують. Точка плавлення: 200-203°С Приклад 1: 6-Хлор-3,4-дигідро-2Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид 196мг сполуки Приготування 1 вміщують в 4мл води. Повільно додають 500мг NaBH4. Через 15 14 хвилин реакцію завершують. рН розчину потім доводять до 5-6 і продукт екстрагують, використовуючи дихлорметан. Органічну фазу висушують над сульфатом магнію і потім випаровують під зниженим тиском. Залишок додають в мінімальну кількість метанолу, і воду додають з тим, щоб спричинити випадіння продукту в осад. Продукт збирають фільтруванням, промивають водою і потім висушують. Точка плавлення: 154-156°С Приклад 2: 6-Хлор-4-метил-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 6-Хлор-4-метил-4Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид 250мг сполуки Приготування 1 вміщують в 5мл ацетонітрилу і 0,5мл диметилформаміду. Додають 500мг карбонату калію, також як і 0,3мл метил йодиду. Розчин нагрівають при близько 55°С протягом близько 7 годин. В кінці реакції розчинник видаляють під зниженим тиском і залишок додають у воду. Нерозчинний матеріал швидко збирають фільтруванням, промивають водою і потім висушують. Точка плавлення: 252-254°С ІЧ (KВr): 3091, 2943, 1607, 1519, 1485, 1434, 1390, 1297, 1150, 1107, 1059, 1015, 835, 778, 754, 570, 541 см -1 Стадія В: 6-Хл ор-4-метил-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид 100мг сполуки вищезазначеної Стадії А розчиняють в 5мл ізопропанолу. Розчин нагрівають при близько 60°С, і додають 400мг NaBH4. Через 20 хвилин розчинник видаляють під зниженим тиском і залишок додають у воду. рН доводять до близько 5-6 і продукт екстрагують 3x10мл хлороформу. Органічну фазу потім висушують над сульфатом магнію, фільтрують і потім концентрують під зниженим тиском. Залишок додають в мінімальну кількість хлороформу і потім продукт осаджують шляхом додавання гексану. Продукт потім збирають фільтруванням і промивають гексаном і висушують. Точка плавлення: 174-176°С ІЧ: 3236, 3089, 2923, 2867, 2807, 1562, 1419, 1407, 1358, 1322, 1284, 1154, 1077, 1002, 814, 742, 680, 569, 504 см -1 Приклад 3: 6-Хлор-4-етил-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 6-Хлор-4-етил-4Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид Цю сполуку одержують відповідно до способу, описаного на Стадії А Прикладу 2, використовуючи брометан замість метил йодиду. Точка плавлення: 189-190°С ІЧ (KВr): 3098, 2982, 2943, 2878, 1609, 1518, 1480, 1464, 1437, 1400, 1300, 1255, 1173, 1161, 1121, 1015, 973, 943, 805, 766, 740, 567, 542 см-1 Стадія В: 6-Хлор-4-етил-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид Цю сполуку одержують відповідно до способу, описаного на Стадії В Прикладу 2, використовуючи сполуку ви щезазначеної Стадії А. Точка плавлення: 119-120°С 15 80046 ІЧ (KВr): 3235, 2980, 2931, 2872, 1558, 1462, 1448, 1407, 1360, 1324, 1154, 1082, 1010, 798, 742, 678, 570, 501 см -1 Приклад 4: 6-Хлор-4-ізопропіл-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 6-Хлор-4-ізопропіл-4Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид 400мг сполуки Приготування 1 розчиняють в 8мл ацетонітрилу і декількох каплях диметилформаміду. Потім додають 800мг карбонату калію, з наступними 0,6мл 2-йодпропану. С уміш нагрівають до близько 55°С. Через 8 годин додають наступні 0,6мл 2-йодпропану і реакційну суміш перемішують протягом ночі. Розчинник випаровують під зниженим тиском і залишок додають у воду. Нерозчинний матеріал, який одержують, швидко збирають фільтруванням, промивають водою і розчиняють в мінімальній кількості гарячого метанолу. Охолодження дає білі кристали, які збирають фільтруванням, промивають метанолом і потім висушують. Точка плавлення: 149-150°С ІЧ (KВr): 3112, 2983, 1605, 1515, 1458, 1442, 1407, 1392, 1306, 1284, 1170, 1141, 1095, 1010, 805, 778, 717, 696, 670, 565, 538 см -1 Стадія В: 6-Хлор-4-ізопропіл-3,4-дигідро-2Нтієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид Цю сполуку одержують відповідно до способу, описаного на Стадії В Прикладу 2, використовуючи сполуку ви щезазначеної Стадії А. Точка плавлення: 100-102°С ІЧ (KВr): 3267, 3241, 2970, 2954, 1545, 1460, 1445, 1409, 1332, 1301, 1156, 1123, 1025, 786. 742, 692, 678, 566, 502 см-1 Приклад 5: 5,7-Дихлор-3,4-дигідро-2Нтієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид 800мг сполуки Приготування 2 суспендують в 15мл води, і туди повільно додають 2г дрібно подрібненого NaBH4. Після 10-хвилинного перемішування при температурі навколишнього середовища, реакційну суміш доводять до рН 6, використовуючи 6N хлористоводневу кислоту, і екстрагують двічі дихлорметаном. Органічну фазу висушують над сульфатом магнію і розчинник видаляють під зниженим тиском. Залишок розчиняють в мінімальній кількості метанолу і обробляють активованим вугіллям, і потім додають воду доти, доки не завершиться осаджування. Осад потім збирають фільтруванням і очищують двічі розчиненням в мінімальній кількості метанолу і додаванням води. Точка плавлення: 125-130°С Приклад 6: 5,7-Дихлор-4~метил-3,4-дигідро2Н-тієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 5,7-Ди хлор-4-метил-4Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид 200мг сполуки Приготування 2 розчиняють в 2мл нітроетану і 2мл диметилформаміду. Розчин нагрівають до 60°С. Потім додають 0,2г карбонату калію, з наступними 0,2мл йодметану. Розчин перемішують протягом 2 годин. Розчинники потім видаляють під зниженим тиском. Залишок додають у воду. Нерозчинний матеріал швидко збирають фільтруванням, промивають водою і висушують. 16 Точка плавлення: 202-207°С ІЧ (KВr): 3436, 3043, 2960, 1607, 1551, 1472, 1439, 1400, 1356, 1347, 1308, 1202, 1145, 1101, 1060, 862, 789, 744, 664, 573, 527 см-1 Стадія В: 5,7-Дихлор-4-метил-3,4-дигідро-2Нтієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид 500мг сполуки вищезазначеної Стадії А розчиняють в 15мл ізопропанолу при 60°С. Потім до розчину додають 1,5г дрібно подрібненого NaBH4. Через 30 хвилин ізопропанол випаровують під зниженим тиском. Залишок потім додають у воду і рН розчину доводять до 7. Розчин потім екстрагують хлороформом (3x40мл). Органічну фазу висушують над сульфатом магнію, фільтрують і потім випаровують досуха під зниженим тиском. Залишок додають в мінімальну кількість хлороформу, і повільно додають гексан для того, щоб спричинити випадіння продукту в осад. Продукт збирають фільтруванням, промивають гексаном і потім висушують. Точка плавлення: 145-155°С з розкладанням ІЧ (KВr): 3447, 3231, 2972, 2821, 1547, 1465, 1414, 1328, 1232, 1180, 1146, 1090, 1034, 1002, 975, 746, 661, 565, 556, 525 см -1 Приклад 7: 5,7-Дихлор-4-етил-3,4-дигідро-2Нтієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 5,7-Ди хлор-4-етил-4Н-тієно[3,4е][1,2,4]тіадіазин 1,1-діоксид 4г сполуки Стадії С Приготування 2 вміщують в 20мл триетил ортоформіату і нагрівають при 170°С протягом 30 хвилин у відкритій посудині. Суспензію потім охолоджують на льоді. Залишок, який утворюється, збирають фільтруванням, промивають n-гексаном і висушують. Точка плавлення: 172-175°С Стадія В: 5,7-Дихлор-4-етил-3,4-дигідро-2Нтієно[3,4-е][1,2,4]тіадіазин 1,1-діоксид 0,5г сполуки вищезазначеної Стадії А розчиняють в 20мл ізопропанолу. Розчин нагрівають до 60°С, і потім до нього додають 1,5г дрібно подрібненого NaBH4. Через 30 хвилин розчинник видаляють під зниженим тиском. Залишок потім додають у 30 мл води і суспензію нейтралізують шляхом додавання 6N хлористоводневої кислоти. Розчин двічі екстрагують хлороформ. Органічну фазу висушують над сульфатом магнію і розчинник видаляють під зниженим тиском. Залишок додають у гексан, збирають фільтруванням, промивають n-гексаном і висушують. Точка плавлення: 144-147°С Приклад 8: 6-Хлор-N,4-діетил-3,4-дигідро-2Нтієно[3,2-е][1,2,41тіадіазин-2-карбоксамід 1,1діоксид 200мг сполуки Прикладу 3 розчиняють в 1,5мл CH3CN. Потім до розчину додають 1мл етил ізоціанату і 0,2мл триетиламіну. Реакційну суміш перемішують при температурі навколишнього середовища протягом 2 годин. В кінці цього періоду розчинники видаляють у вакуумі. Залишок розчиняють у мінімальній кількості ацетону. Продукт потім осаджують шляхом послідовного додавання води. Продукт швидко збирають фільтруванням, промивають водою і потім висушують. Точка плавлення: 80-81°С 17 80046 Приклад 9: 6-Хлор-N-етил-4-ізопропіл-3,4дигідро-2Н-тієно[3,2-е][1,2,4]-тіадіазин-2карбоксамід 1,1-діоксид Цю сполуку одержують відповідно до способу Прикладу 8, використовуючи сполуку Прикладу 4 замість сполуки Прикладу 3. Точка плавлення: 72-74°С Приклад 10: 5,7-Дихлор-N-етил-4-метил-3,4дипдро-2Н-тiено[3,4-е][1,2,4]-тіадіазин-2карбоксамід 1,1-діоксид Цю сполуку одержують відповідно до способу Прикладу 8, використовуючи сполуку Прикладу 6 замість сполуки Прикладу 3. Точка плавлення: 87-88°С Приклад 11: 6-Хлор-4-(2-фторетил)-3,4дигідро-2Н-тієно[3,2-е][1,2,4]-тіадіазин 1,1-діоксид Стадія А: 6-Хлор-4-(2-фторетил)-4Н-тієно[3,2е][1,2,4]тіадіазин 1,1-діоксид 500мг сполуки Приготування 1 суспендують в 10мл ацетонітрилу. 10 крапель ДМФ, 1г карбонату калію і 0,3мл 1-фтор-2-йодетану додають до суспензії. Реакційну суміш нагрівають при 70°С протягом 35 годин, з перемішуванням. Після охолодження реакційної суміші нерозчинний матеріал видаляють фільтруванням. Розчинники видаляють випаровуванням під зниженим тиском. Твердий залишок, який одержують, додають в 10мл води і негайно збирають фільтруванням. Одержаний таким чином продукт перекристалізовують з етилацетату. Точка плавлення: 185-187°С. Стадія В: 6-Хлор-4-(2-фторетил)-3,4-дигідро2Н-тієно[3,2-е][1,2,4]тіадіазин 1,1-діоксид 100мг сполуки, одержаної на вищезазначеній Стадії А, розчиняють в 4мл ізопропанолу. Суміш нагрівають до 60°С, потім додають 200 мг боргідриду натрію. Через 10 хвилин при цій температурі розчинник випаровують під зниженим тиском.Залишок, який одержують, додають в 10мл води, охолоджують на льодяній бані і доводять до рН 4 шляхом додавання 6N хлористоводневої кислоти. Нерозчинний матеріал збирають фільтруванням і промивають водою. Продукт потім розчиняють в мінімальній кількості хлороформу і осаджують шляхом додавання n-гексану. Осад потім збирають фільтруванням. Точка плавлення: 141-144°С. Приклад 12: 4,7-Диметил-3,4-дигідро-2Нтієно[2,3-е][1,2,4]тіадіазин 1,1-діоксид Стадія А: 7-Метил-4Н-тієно[2,3е][1,2,4]тіадіазин 1,1-діоксид 200мг 2-аміно-4-метилтіофен-3-сульфонаміду, приготування якого розкрите в [патенті WO 99/03861], розчиняють в 1,5мл триметил ортоформіату. Суміш нагрівають при 90°С протягом 2 годин у відкритій посудині. Після випаровування розчинника під зниженим тиском, залишок додають в 3мл етилацетату. Нерозчинний матеріал, який одержують в результаті, збирають фільтруванням, промивають діетиловим ефіром і висушують. Точка плавлення: 195-198°С. Стадія В: 4,7-Диметил-4Н-тієно[2,3е][1,2,4]тіадіазин 1,1-діоксид 18 150мг сполуки, одержаної на вищезазначеній Стадії А, суспендують в 5мл ацетонітрилу. Туди додають 300мг карбонату калію і 0,15мл йодметану. Реакційну суміш нагрівають при 65°С протягом 30 хвилин, з перемішуванням. Після випаровування розчинників під зниженим тиском залишок додають в 5мл води і потім збирають фільтруванням, промивають водою і висушують. Точка плавлення: 265-270°С. Стадія С: 4,7-Диметил-3,4-дигідро-2Нтієно[2,3-е][1,2,4]тіадіазин 1,1-діоксид 240мг боргідриду натрію додають до 120мг сполуки, одержаної на вищезазначеній Стадії В, розчиненої у 6мл ізопропанолу. Суміш нагрівають при 50°С протягом 10 хвилин. Розчинник видаляють під зниженим тиском, потім залишок, який одержують, додають в 5мл води. рН розчину доводять до 4 шляхом додавання 6N хлористоводневої кислоти. Осад збирають фільтруванням, промивають водою і висушують. Точка плавлення: 171-173°С. Приклад 13: 6-Хлор-4-ізопропілметил-3,4дигідро-2Н-тієно[3,2-е][1,2,4]-тіадіазин 1,1-діоксид Стадія А: 6-Хлор-4-фторметил-4Н-тісно[3,2е][1,2,4]тіадіазин 1,1-діоксид 500мг сполуки Приготування 1 суспендують в 15мл ацетонітрилу. Туди додають 500мг карбонату калію і 1мл бромфторметану. Суміш вміщують в запечатаний автоклав і нагрівають при 70°С протягом 8 годин. Нерозчинний матеріал потім виділяють фільтруванням. Після випаровування розчинника, залишок додають в 20мл води і збирають на фільтрі. Одержану таким чином тверду речовину перекристалізовують з метанолу. Стадія В: 6-Хлор-4-ізопропілметил-3,4-дигідро1Н-тієно[3,2-е][1,2,4]-тіадіазин 1,1-діоксид 400мг боргідриду натрію додають до 200мг сполуки, одержаної на вищезазначеній Стадії А, суспендованої в 8мл ізопропанолу. Суміш нагрівають при 50°С протягом 10 хвилин, з перемішуванням. Нерозчинний матеріал виділяють фільтруванням. Після випаровування розчинника під зниженим тиском, залишок додають в 1мл суміші етилацетат/n-гексан (15/5) і очищують колонкового хроматографією в тій же рухомій фазі. Після випаровування розчинників, залишок розчиняють в 1мл метанолу і осаджують у воді. Одержаний таким чином твердий продукт збирають фільтруванням, промивають водою і висушують. Точка плавлення: 65-68°С. Фармакологічні дослідження сполук за даним винаходом Приклад А: Дослідження збуджувальних струмів, викликаних АМРА в ооцитах Xenopus мРНК одержують з кори головного мозку самців щурів Wistar способом гуанідин тіоціанат/фенол/хлороформ. Полі (А+) мРНК відділяють хроматографією на оліго-dT целюлозі та ін'єктують в кількості 50нг на ооцит. Ооцити інкубують протягом 2-3 днів при 18°С, щоб дозволити експресування рецепторів, і потім зберігають при 8-10°С. Проводять електрофізіологічну реєстрацію у камері Plexiglass a при 20-24°С у середовищі OR2 [J. Exp. Zool., 1973, 184, 321-334] способом "напру 19 80046 га-фіксація" з використанням двох електродів, з третім електродом, розміщеним у ванні, яка служить як зразок. Всі сполуки вводять через середовище інкубації і електричний струм вимірюють в кінці періоду введення. (S)-AMPA використовують у концентрації 10мкМ. Для кожної досліджуваної сполуки визначають концентрацію, яка подвоює (ЕС2Х) або збільшує у п'ять разів (ЕС5Х) силу стр уму, індукованого самим АМРА (від 5 до 50нА). Сполуки за даним винаходом підсилюють збуджувальні ефекти, індуковані (S)-AMPA, до дуже значних рівнів. З метою прикладів, сполуки Прикладів 4-6 мають значення ЕС2Х і ЕС5Х, зазначені в таблиці нижче: Сполука Приклад 4 Приклад 6 ЕС2Х (мкМ) 4,2±0,7 5,4±2,8 ЕС5Х (мкМ) 11±3 11,3±4,9 Приклад В: Дослідження збуджувальних постсинаптичних потенціалів (EPSP), індукованих електричною стимуляцією на ділянки гіпокампу щура. Поперечні ділянки гіпокампу (500мкМ) самців щурів Wistar готують за допомогою ножа для тканин і потім інкубують протягом 45 хвилин у вільному від кальцію середовищі, яке містить Mg2+ (10мкм Моль). Їх потім стабілізують в Krebs, доведеному до рН 7,35 і окисленому за допомогою Комп’ютерна в ерстка О. Гапоненко 20 О2/СО 2 (95%/5%) при температурі навколишнього середовища. Ділянки занурюють у воду при 30°С і збуджувальні постсинаптичні потенціали (EPSP) зчитують у дендритному полі гепариноцитів зубчастої звивини протягом стимуляції (50-100мкА, 50мксек.) кожні 30 секунд перфорантного шляху за допомогою біполярного вольфрамового електроду. EPSP одержують і аналізують за допомогою AD конвертера, TL-1 інтерфейс і програмне забезпечення "pCLAMP". Амплітуду і тривалість EPSP оцінюють на негативній хвилі відносно основного струму. Сполуки вміщують на 10 хвилин в охолоджувальну баню, яка містить MgSO4 (1мкмМоль) з тим, щоб блокувати активацію NMDA рецепторів. Для кожної сполуки вимірюють концентрацію, яка збільшує на 50% амплітуду (А50) або тривалість (D50) PSEP. Сполуки за даним винаходом значно збільшують амплітуду і тривалість збуджувальних постсинаптичних потенціалів поля, що зчитуються на ділянках гіпокамну щурів. Фармакологічна композиція Формула для приготування 1000 таблеток, кожна з яких містить 100мг сполука Приклад 1 100г гідроксипропілцелюлоза 2г пшеничний крохмаль 10г лактоза 100г стеарат магнію 3г тальк 3г Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюThiadiazine compounds, method for obtaning thereof and pharmaceutical composition containing them
Автори англійськоюLestage Pierre, Danober Laurence, Renard Pierre, Caignard Daniel-Henri
Назва патенту російськоюСоединения тиадиазина, способ их получения и фармацевтическая композиция, которая их содержит
Автори російськоюЛестаж Пьер, Данобер Лоранс, Ренар Пьер, Кеньяр Даниэль-Энри
МПК / Мітки
МПК: A61P 25/18, C07D 513/04
Мітки: одержання, яка, сполуки, фармацевтична, композиція, містить, тіадіазину, спосіб
Код посилання
<a href="https://ua.patents.su/10-80046-spoluki-tiadiazinu-sposib-kh-oderzhannya-i-farmacevtichna-kompoziciya-yaka-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">Сполуки тіадіазину, спосіб їх одержання і фармацевтична композиція, яка їх містить</a>
Попередній патент: Пристрій для транспортування і очищування коренебульбоплодів
Наступний патент: Вимірювач інтервалів часу
Випадковий патент: Панчоха, шкарпетка або подібний до них виріб та спосіб його виготовлення














