Похідні заміщеного n-феніл 2-гідрокси-2-метил-3,3,3-трифторпропанаміду, які підвищують активність піруватдегідрогенази
Формула / Реферат
1. Сполука формули (І):
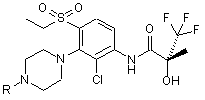 , (I)
, (I)
де R являє собою метил або мезил;
або її фармацевтично прийнятна сіль або складний ефір, який здатний гідролізуватися в умовах in vivo.
2. Сполука формули (І) за пунктом 1, в якій R являє собою метил, або її фармацевтично прийнятна сіль або складний ефір, який здатний гідролізуватися в умовах in vivo.
3. Сполука формули (І) за пунктом 1, в якій R являє собою мезил, або її фармацевтично прийнятна сіль або складний ефір, який здатний гідролізуватися в умовах in vivo.
4. Сполука формули (І) або її фармацевтично прийнятна сіль або складний ефір, який здатний гідролізуватися в умовах in vivo, як вказано у будь-якому з пунктів 1-3, для застосування як лікарського засобу.
5. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vivo, як вказано у будь-якому з пунктів 1-3, причому спосіб (де R має значення, вказані для формули (І), якщо спеціально не вказано інакше), у якому:
знімають захист з захищеної сполуки формули (II):
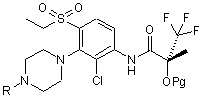 , (II)
, (II)
де Pg являє собою спиртову захисну групу;
і потім, при необхідності, одержують фармацевтично прийнятну сіль або складний ефір, який здатний гідролізуватися в умовах in vivo.
6. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль або складний ефір, який здатний гідролізуватися в умовах in vivo, як вказано в будь-якому з пунктів 1-3, у сполученні з фармацевтично прийнятним наповнювачем або носієм.
7. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vivo, як вказано у будь-якому з пунктів 1-3, для приготування лікарського засобу, який застосовують для підвищення активності ПДГ у теплокровної тварини, такої як людина.
8. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vivo, як вказано у будь-якому з пунктів 1-3, для приготування лікарського засобу, який застосовують для лікування цукрового діабету у теплокровної тварини, такої як людина.
9. Спосіб підвищення активності ПДГ у теплокровної тварини, що має потребу в такому лікуванні, у якому вказаній тварині вводять ефективну кількість сполуки формули (І) або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vivo, як вказано в будь-якому з пунктів 1-3.
10. Спосіб лікування цукрового діабету в теплокровної тварини, такої як людина, що має потребу в такому лікуванні, у якому вказаній тварині вводять ефективну кількість сполуки формули (І) або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vivo, як вказано в будь-якому з пунктів 1-3.
11. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль або складний ефір, який здатний гідролізуватися в умовах in vivo, як вказано в будь-якому з пунктів 1-3, у сполученні з фармацевтично прийнятним наповнювачем або носієм, для застосування для підвищення активності ПДГ у теплокровної тварини, такої як людина.
12. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль або складний ефір, який здатний гідролізуватися в умовах in vivo, як вказано у будь-якому з пунктів 1-3, у сполученні з фармацевтично прийнятним наповнювачем або носієм для застосування для лікування цукрового діабету у теплокровної тварини, такої як людина.
Текст
1. Сполука формули (І): 3 77967 4 ефіру, який здатний гідролізуватися в умовах in 12. Фармацевтична композиція, яка містить сполуvi vo, як вказано в будь-якому з пунктів 1-3. ку формули (І) або її фармацевтично прийнятну 11. Фармацевтична композиція, яка містить сполусіль або складний ефір, який здатний гідролізуваку формули (І) або її фармацевтично прийнятну тися в умовах in vivo, як вказано у будь-якому з сіль або складний ефір, який здатний гідролізувапунктів 1-3, у сполученні з фармацевтично прийнятися в умовах in vivo, як вказано в будь-якому з тним наповнювачем або носієм для застосування пунктів 1-3, у сполученні з фармацевтично прийнядля лікування цукрового діабету у теплокровної тним наповнювачем або носієм, для застосування тварини, такої як людина. для підвищення активності ПДГ у теплокровної тварини, такої як людина. Даний винахід стосується сполук, які підвищують активність піруватдегідрогенази (ПДГ), способів їх одержання, фармацевтичних композицій, які їх містять як активний компонент, способів лікування хворобливих станів, пов'язаних із зниженою активністю ПДГ, їх застосування як лікарських засобів та їх застосування для приготування лікарських засобів для застосування для підвищення активності ПДГ у теплокровних тварин, таких як люди. Зокрема, даний винахід стосується сполук, які корисні для лікування цукрового діабету, захворювань периферичних судин і ішемії міокарда в теплокровних тварин, таких як люди, більш переважно, застосування цих сполук для приготування лікарських засобів для застосування для лікування цукрового діабету в теплокровних тварин, таких як люди. У тканинах аденозинтрифосфат (АТФ) забезпечує енергію для синтезу складних молекул і в м'язах для їх скорочення. АТФ утворюється при розщепленні високоенергетичних субстратів, таких як глюкоза або вільні жирні кислоти з довгим ланцюгом. В окисних тканинах, таких як м'язи, більшість АТФ утворюється з ацетил СоА при його входженні в цикл лимонної кислоти, відповідно запаси ацетил СоА мають вирішальне значення для утворення АТФ в окисних тканинах. Ацетил СоА утворюється як при b-окисленні жирних кислот, так і в результаті метаболізму глюкози за гліколітичним шляхом метаболізму. Ключовим регуляторним ферментом для контролювання рівня утворення ацетил СоА із глюкози є ПДГ, яка каталізує окислення пірувату до ацетил СоА і вуглекислого газу, що супроводжується відновленням нікотинамідаденіндинуклеотиду (НАД) до НАДН. При хворобливих станах, таких як обидва типи цукрового діабету, а саме інсулін-незалежному (Тип 2) та інсулін-залежному (Тип 1) цукровому діабеті, збільшується окислення ліпідів, що супроводжується зменшенням засвоєння глюкози, що приводить до гіперглікемії. Зменшення засвоєння глюкози при діабеті 1 і 2 типів пов'язано зі зменшенням активності ПДГ. Крім того, ще одним свідченням зменшення активності ПДГ може бути те, що підвищення концентрації пірувату приводить до підвищеної приступності лактату як субстрату для глюконеогенезу в печінці. Також можна обґрунтовано очікувати, що підвищення активності ПДГ може приводити до підвищення рівня окислення глюкози й, отже, до сумарного засвоєння глюкози, зменшуючи при цьому вироблення глюкози печінкою. Іншим фактором, який вносить свій вклад у розвиток цукрового діабету, є зниження вироблен ня інсуліну, що, як було показано, пов'язано зі зменшеною активністю ПДГ у b-клітинах підшлункової залози (на генетичній моделі цукрового діабету в гризунів [Zhou і ін. (1996) Diabetes. 45. – P.580-586]. При окисленні глюкози утворюється більше АТФ на моль кисню, ніж при окисленні жирних кислот. В умовах, коли потреба в енергії може перевищува ти запаси енергії, таких як ішемія міокарда, переміжна кульгавість, ішемія головного мозку і реперфузія [Zaidan і ін. 1998 J. Neurochem. – 70. – P.233-241], зрушення рівноваги утилізації субстрату у бік метаболізму глюкози шляхом підвищення активності ПДГ може приводити, як очікується, до поліпшення можливостей для підтримання рівнів АТФ і отже, функціонування. Засіб, який здатний підвищувати активність ПДГ, також може бути корисним, як припускають, при лікуванні станів, при яких має місце надлишок циркулюючої молочної кислоти, таких як певні види сепсису. Для дихлороцтової кислоти (ДХК), яка при гострому введенні підвищує у тварин активність ПДГ [Vary і ін.1998; Circ. Shock. 24. – P.3-18), показано, що вона має передбачені дії щодо зменшення глікемії, [Stacpoole і ін 1978; N. Engl. J. Med. 298. – P.526-530], і для лікування ішемії міокарда [Bersin, Stacpoole 1997; American Heart Journal, 134. – P.841-855] і молочної ацидемії [Stacpoole і ін.1983; N. Engl. J. Med. 309. – P.390-396]. ПДГ являє собою внутрішньомітохонріальний багатоферментний комплекс, який складається з багатьох копій декількох субодиниць, які включають три активних ферменти Е1, Е2 і ЕЗ, необхідні для здійснення перетворення пірувату в ацетил CoA [Patel, Roche1990; FASEB J., 4. – P.32243233]. Е1 каталізує необоротне виділення СО2 з пірувату; Е2 утворює ацетил СоА і Е3 відновлює НАД до НАДН. Два додаткові активні ферменти зв'язані з комплексом: специфічна кіназа, яка здатна фосфорилювати Е1 за трьома залишками серину і слабко зв'язана специфічна фосфатаза, яка має протилежну до фосфорилювання дію. Фосфорилювання тільки одного з трьох залишків серину викликає інактивацію Е1. Частка ПДГ у її активному (дефосфорильованому) стані визначається рівновагою між активностями кінази і фосфатази. Активність кінази може регулюватися в умовах in vi vo за допомогою відносних концентрацій метаболічних субстратів, таких як НАД/НАДН, СоА/ацетилСоА й аденозиндифосфату (АДФ)/АТФ, а також доступністю самого пірувату. Сполука, яка підвищує активність ПДГ, потен 5 77967 6 ційно може бути ефективною при лікуванні хворо0625516] і в [GB, 2278054] і в міжнародних заявках бливих станів, пов'язаних з порушенням засвоєння [WO, 9323358; WO, 9738124; WO, 9944618; WO, глюкози, таких цукровий діабет, ожиріння [Curto і 9947508; WO, 9962506; WO, 9962873; WO, ін.,1997; Int. J. Obes. 21. – P.1137-1142], і молочна 01/17942; WO, 01/17955; WO, 01/17956]. ацидемія. Крім того, передбачається, що така споІншим об'єктом даного винаходу є спосіб оделука також може бути ефективною при захворюржання сполук формули (І) або її фармацевтично ваннях, при яких обмежені запаси високоенергеприйнятної солі або складного ефіру, який здатний тичних субстратів у тканинах, таких як гідролізуватися в умовах in vivo, при цьому спосіб захворювання периферичних судин (включаючи (де змінювані групи мають значення, вказані для переміжну кульгавість), серцеву недостатність і формули (І), якщо спеціально не вказано інакше) певні міопатії серця, м'язову слабість, гіперліпідепередбачає: мії й атеросклероз [Stacpoole і ін., 1978; N. Engl. J. (а) зняття захисту з захи щеної сполуки форMed. 298. – P.526-530]. Сполука, яка активує ПДГ, мули (II): також може бути корисною для лікування хвороби Альцгеймера (AD) [J. Neural. Transm. – 1998. – (II) 105. – P.855-870]. У європейських патентних публікаціях [EP, 617010; EP, 524781] описані сполуки, здатні виклиде: Pg - являє собою спиртову захисну гр упу; кати розслаблення гладких м'язів сечового міхура і (б) окислення сполуки формули (III): які можуть застосуватися для лікування позивів до сечовипускання. У міжнародних заявках [WO, 9944618; WO, 9947508; WO, 9962506; WO, (III) 9962873; WO, 01/17942; WO, 01/17955; WO, 01/17956] описані сполуки, які підвищують активність ПДГ. Сполуки згідно із даним винаходу конкде: а - являє собою 0 або 1; ретно не описані в жодній з вищезгаданих заявок, і (в) сполучення сполуки формули (IV): нами несподівано було виявлено, що ці сполуки мають корисні властивості у відношенні однієї або декількох їх фармацевтичних активностей (особ(IV) ливо як сполуки, які підвищують активність піруватдегідрогенази) і/або мають фармакокінетичні, діючі, метаболічні і токсикологічні профілі, які робз кислотою формули (V): лять їх особливо придатними для введення в умовах in vi vo теплокровній тварині, такій як людина. Таким чином, даний винахід стосується сполу(V) ки формули (І): (I) де: R - являє собою метил або мезил; або її фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vi vo. В одному варіанті здійснення винаходу R являє собою метил. В іншому варіанті здійснення винаходу R являє собою мезил. Інші варіанти здійснення винаходу стосується сполуки або її фармацевтично прийнятної солі. Також мається на увазі, що сполука формули (І) і її фармацевтично прийнятні солі і складні ефіри, які здатні гідролізуватися в умовах in vivo, можуть існувати у вигляді сольватів, а також у несольватованих формах, таких як, наприклад, гідратовані форми. Також мається на увазі, що під обсяг винаходу підпадають усі такі сольватовані форми, які підвищують активність ПДГ. Сполука формули (І) і її фізіологічно прийнятні солі і складні ефіри, які здатні гідролізуватися в умовах in vi vo, можуть бути отримані за допомогою будь-яких відомих способів, які придатні для одержання хімічно подібних сполук. Такі способи включають, наприклад, описані в європейських заявках на патенти [EP, 0524781; EP, 0617010; EP, де: X - являє собою ОН; (г) сполучення аніліну формули (IV) з активованим похідним кислоти формули (V); (д) реагування сполуки формули (VI): (VI) де: L - являє собою групу, яка витісняється; з 4-мезилпіперазином або 4-метилпіперазином; (e) для сполук формули (І), де R являє собою метил, метилювання сполуки формули (VII): (VII) (є) для сполук формули (І), де R являє собою мезил, мезилювання сполуки формули (VII); (ж) хлорування сполуки формули (VIII): (VIII) (з) перетворення функціональної групи на хлор для сполуки формули (IX): (IX) де: Fg - являє собою функціональну груп у; 7 77967 8 (и) приєднання металоорганічного реагенту до 3) якщо Рg являє собою ацетил: сполуки формули (X): і) слабкий водний луг, наприклад, гідроксид літію; або (X) іі) аміак або амін, такий як диметиламін. Реакцію можна проводити в придатному роз(і) приєднання металоорганічного реагенту до чиннику, такому як етанол, метанол, ацетонітрил сполуки формули (XI): або диметилсульфоксид і придатна температура для здійснення реакції знаходиться в інтервалі від -40 до 100°С. (XI) Сполуки формули (II) можуть бути отримані відповідно до схеми 1: (к) приєднання сполуки формули (V), де X явСхема 1 ляє собою NH2, до сполуки формули (XII): (XII) де: L - являє собою груп у, яка витісняється; (л) перегрупування Смайсла сполуки формули (XIII): (XІІІ) або (м) розділення суміші (R) і (S) енантіомерів сполук формули (І) для одержання (R)енантіомеру; і потім, при необхідності, одержання фармацевтично прийнятної солі або складного ефіру, який здатний гідролізуватися в умовах in vi vo. Придатними значеннями для Рg є бензильна група, силільна група (наприклад, триалкілсилільна група або алкілдифенілсилільна група) або ацетилзахисна група. Якщо формула (V) являє собою активоване похідне кислоти, прийнятними значеннями для X є галоген (наприклад, хлор або бром), ангідриди, арилокси (наприклад, 4-нітрофенокси або пентафторфенокси) або імідазол-1-іл. L являє собою групу, яка витісняється. Придатними значеннями для L є фтор, хлор, бром, нітро, метансульфонат і трифторметансульфонат. Fg являє собою функціональну груп у. Придатною функціональною групою є аміногрупа, яка може бути взаємоперетворена за допомогою діазотування і реакції солі діазонію з хлоридом у присутності мідного каталізатора. Конкретними умовами для вищевказаних реакцій є наступні: Спосіб (а) Прикладами придатних реагентів для зняття захисту зі спирту формули (II) є: 1) якщо Рg являє собою бензил: (і) водень у присутності паладієвого/вуглецевого каталізатора, тобто гідрогеноліз; або (іі) бромід водню або йодид водню; 2) якщо Рg являє собою силільну захисну гр упу: (і) фторид тетрабутиламонію; або (іі) фтористоводнева або соляна кислота; Ε являє собою карбоксизахисну групу. Придатними значеннями для Ε є (С1-С6)алкіл, такий метил і етил. Сполука формули (IIa) є комерційно доступною сполукою. Спосіб (б) Придатними окисниками є перманганат калію, ΟΧΟΝΕ™, перйодат натрію, надкислоти (такі як, наприклад, 3-хлорпероксибензойна кислота або пероцтова кислота), перекис водню, ТРАР (перутенат тетрапропіламонію) або кисень. Реакцію можна проводити в придатному розчиннику, такому як діетиловий ефір, ДХМ, метанол, етанол, вода, оцтова кислота або сумішах двох або більше цих розчинників. Реакцію звичайно здійснюють при температурі в інтервалі від -40 до 100°С. Сполуки формули (III) можуть бути отримані відповідно до схеми 2: Схема 2 9 77967 Схема 2 Сполука формули (IlIa) є комерційно доступною сполукою. Спосіб (в) Реакцію можна здійснювати в присутності придатної зв'язувальної речовини. Стандартні амідні зв'язувальні реагенти, відомі в даній галузі, можуть застосуватися як придатні зв'язувальні реагенти, наприклад, такі умови, як описані вище для сполучення (ІІІа) і (V) або (IV) і (lId), або, наприклад дициклогексил-карбодіімід, необов'язково в присутності каталізатора, такого як диметиламінопіридин або 4-піролідинопіридин, необов'язково в присутності основи, наприклад, триетиламіну, піридину, або 2,6-ди-алкіл-піридинів (таких як 2,6-лутидин або 2,6-ди-третбутилпіридин) або 2,6-дифенілпіридину. Придатними розчинниками є диметилацетамід, ДХМ, бензол, ТГФ і ДМФА. Сполучення звичайно можна здійснювати при температурі в інтервалі від -40 до 40°С. Сполуки формули (IV) можуть бути отримані відповідно до 3 схеми: Схема 3 10 Pg являє собою амінозахисну груп у, таку як описану далі. Сполуки формули (IVa) і (V) є комерційно доступними сполуками і відомі з літератури. Наприклад, розділення кислоти формули (V) може здійснюватися за допомогою будь-якого з відомих способів одержання оптично активних форм (наприклад, шляхом перекристалізації хіральної солі [наприклад, міжнародна заявка WO, 9738124], шляхом ферментативного розділення або хроматографічного розділення за допомогою хіральної нерухомої фази). Наприклад, (R)-(+) розділена кислота може бути отримана за допомогою способу відповідно до схеми 2, що описана в [опублікованій міжнародній заявці на патент WO, 9738124] для одержання (S)-(-) кислоти, тобто за допомогою стандартного способу розділення, описаного [в європейській патентній заявці ЕР, 0524781], також для одержання (S)-(-) кислоти, за винятком того, що (1S,2R)-норефедрин застосовується замість (S)-(-)-1-фенілетиламіну. Хіральна кислота також може бути отримана за допомогою способу ферментативного розділення, як описано в [Tetrahedron Asymmetry. – 1999. – 10. – P.679]. Спосіб (г) Це сполучення може здійснюватися необов'язково в присутності основи, наприклад, триетиламіну, піридину, 2,6-ди-алкіл-піридинів (таких як 2,6лутидин або 2,6-ди-трет-бутилпіридин) або 2,6дифенілпіридину. Придатними розчинниками є диметилацетамід, ДХМ, бензол, ТГФ і ДМФА. Сполучення звичайно можна здійснювати при температурі в інтервалі від -40 до 40°С. Спосіб (д) Це реакцію можна здійснювати шляхом взаємодії 1-мезилпіперазину [US, 6140351] або 1метилпіперазину (1-20 молярних еквівалентів, переважно 2-10 еквівалентів) з (VI) у розчиннику, такому як N-метил-2-піролідон або диметилацетамід, або нерозбавлених, при нагріванні до температури від 40 до 160°С. Сполуки формули (VI), у яких L являє собою фтор, можуть бути отримані відповідно до схеми 4: Схема 4 Спосіб (e) Сполука (VII) може бути метилирована за допомогою формальдегіду і відновника, такого як борогідрид натрію або триацетоксиборогідрид натрію в придатному розчиннику, такому як 1,2дихлоретан, ДХМ або ТГФ, при температурі в діапазоні від 0°С до температури флегми, переважно при кімнатній або приблизно при кімнатній температурі. Альтернативно, сполука (VII) може бути метилирована за допомогою метилювального засобу, такого як метилйодид або диметилсульфат у розчиннику, такому як або ацетон ДМФА в присутності основи, такої як бікарбонат натрію, карбонат натрію або гідроксид натрію, необов'язково при захисті гідроксильної групи. Одержання сполуки 11 77967 12 (VII) описано далі в способі 1. Схема 6 Спосіб (є) Сполука (VII) може бути мезилирована за допомогою придатного засобу, такого як хлорид метансульфонілу, у присутності основи, такої як триетиламін, у придатному розчиннику, такому як ДХМ, ТГФ, піридин або етилацетат, при температурі в діапазоні від -40°С до температури флегми, переважно при кімнатній або приблизно при кімнатній температурі. Спосіб (ж) Хлорування може здійснюватися, наприклад, за допомогою N-хлорсукциніміду в розчиннику, такому як ДХМ, ацетонітрил, ізопропанол або ДМФА при температурі в діапазоні від 0°С до температури флегми, або за допомогою хлору в приСпосіб (и) сутності каталізатора, такого як трихлорид заліза, Реакцію можна здійснювати шляхом додавану придатному розчиннику, такому як оцтова кислоня придатного реагенту, такого як CF3SiMe3 (реата, ДМФА або ацетонітрил, при температурі в діагент Рупперта (Ruppert's reagent) [Tetrahedron. – пазоні від -20°С до 40°С, переважно при кімнатній 2000. - 56(39). – P.7613], яка може відбуватися або нижчій за кімнатну температурі, з наступним асиметрично при використанні придатного каталірозділенням потрібного продукту від небажаних затора, такого як хіральний цинхоній-фторидний ізомерних домішок, якщо такі утворюються. каталізатор [Tetrahedron Lett. – 1994. – 35. – Сполуки формули (VIII) можуть бути отримані P.3137], і наступного підкислення водного робочовідповідно до схеми 5: го середовища для того, щоб викликати гідроліз Схема 5 третинного простого силільного спиртового ефіру, утвореного в реакції. Цю реакцію можна здійснювати в придатному розчиннику, такому як толуол, при температурі в діапазоні від -100°С до кімнатної температури до температури флегми, переважно від -78°С до кімнатної температури. Сполуки формули (X) можуть бути отримані за допомогою способу (в), тобто шля хом взаємодії сполуки (IV) з піровиноградною кислотою замість кислоти формули (V). Спосіб (і) Реакцію можна здійснювати шляхом додавання придатного металоорганічного реагенту, такого як CH3MgBr або СН3СеСІ2 у розчиннику, такому як простий ефір або ТГФ при температурі від -120 до Сполука (Villa) є комерційно доступною. 40°С у присутності хірального каталізатора, такого Спосіб (з) як TADDOL (тетраарилдиметилдіоксоландиДля цих взаємоперетворень функціональних метанол, наприклад, де арил являє собою феніл груп використовуються реагенти й умови реакцій, або 2-нафтил [Angew. Chem. Int. Ed. Engl. – 1992. які добре відомі в галузі хімії. – 31. – P.84-6]. Наприклад, взаємоперетворення функціонаСполуки формули (XI) можуть бути отримані льної групи (IX), де Fg являє собою NH2, у сполуку за допомогою способу (в), тобто шляхом сполуформули (І) може здійснюватися за допомогою чення сполуки (IV) із трифторпіровиноградною діазотування, наприклад із трет-бутилнітритом і кислотою [Tetrahedron Lett. – 1989. - 30(39). – т.д. у присутності каталізатора, такого як хлорид P.5243] замість кислоти формули (V). міді, у розчиннику, такому як ацетонітрил, при теСпосіб (к) мпературі в діапазоні від 0°С до температури флеРеакцію можна здійснювати за допомогою гми, переважно при кімнатній або приблизно при взаємодії сполуки формули (XII) з діаніоном, отрикімнатній температурі. Альтернативно, перетвоманим шляхом обробки сполуки формули (V), де X рення можна здійснювати шляхом діазотування з являє собою NH2, із двома молярними еквіваленнітритною сіллю в присутності кислоти, такою як тами основи, такої як гідрид натрію, у придатному НСІ або сірчана кислота, у розчиннику, такому як розчиннику, такому як ТГФ або NMP, при темперавода, оцтова кислота або суміші двох розчинників, турі в інтервалі 20-160°С. при температурі від -20 до 40°С, з наступною реаСполука формули (XII), де L являє собою СІ, кцією в такий спосіб утвореної солі діазонію з хломоже бути отримана, наприклад, шляхом діазотуридом одновалентної міді в тому ж розчиннику при вання сполуки формули (IV) відповідно до методу, температурі в інтервалі від 0°С до температури описаному у способі (з). флегми. Спосіб (л) Сполуки формули (IX) можуть бути отримані Перегрупування Смайсла можна здійснювати відповідно до схеми 6: шляхом обробки сполуки формули (XIV) основою, 13 77967 14 такою як гідрид натрію, у розчиннику, такому як пи є, наприклад, ацильна група, наприклад алкаДМФА. ноїльна група, така як ацетил, алкоксикарбонільна Сполука формули (XIV) може бути отримана із група, наприклад, метоксикарбонільна, етоксикарсполуки формули (XII), де L являє собою СІ, при бонільна або трет-бутоксикарбонільна група, ариреагуванні зі сполукою формули (V), де X являє лметоксикарбонільна група, наприклад бензилоксобою NH2, з одним молярним еквівалентом осносикарбоніл, або ароїльна група, наприклад ви, такої як гідрид натрію, у розчиннику, такому як бензоїл. Умови зняття захисту для ви щезгаданих ТГФ або NMP, при температурі в інтервалі 20захисних груп головним чином будуть залежати 160°С. від вибору захисної групи. Так, наприклад, ацильСпосіб (м) на група, така як алканоїльна або алкоксикарбоніПотрібна оптично активна форма сполуки фольна група або ароїльна група можуть бути відщермули (І) може бути отримана шляхом розділення плені, наприклад, шляхом гідролізу з придатною суміші сполуки формули (І) і її відповідного (S) основою, такою як гідроксид лужного металу, наенантіомеру при використанні звичайних методик, приклад гідроксид літію або натрію. Альтернативдобре відомих фа хівцю в даній галузі техніки, нано, ацильна група, така як тpeтприклад, кристалізацією, ферментативним роздібутоксикарбонільна група може бути відщеплена, ленням або хроматографічним розділенням енаннаприклад, шляхом обробки придатною кислотою, тіомерів. такою як соляна, сірчана або фосфорна кислота Потрібні вихідні речовини для вищеописаних або трифтороцтова кислота й арилметоксикарбометодик, якщо вони не є комерційно доступними, нільна група, така як бензилоксикарбонільна груможуть бути отримані за допомогою методик, вибпа, може бути відщеплена, наприклад, шляхом раних із стандартних технологій органічної хімії, гідрування в присутності каталізатора, такого як технологій, аналогічних до синтезу відомих струкпаладій на вугіллі або шляхом обробки кислотою турно подібних сполук, або те хнологій, аналогічних Льюіса, наприклад, трис(трифторацетатом) бору. до вищеописаних методик, або методик, описаних Придатною альтернативною захисною групою для у прикладах. первинної аміногрупи є, наприклад, фталоїльна Слід зазначити, що багато ви хідних речовин група, яка може бути відщеплена шляхом обробки для вищевказаних способів синтезу є комерційно з алкіламіном, наприклад, диметиламінопропіладоступними і/або добре описаними в науковій ліміном або 2-гідроксіетиламіном, або з гідразином. тературі, або можуть бути отримані з комерційно Захисні групи можуть бути відщеплені на будьдоступних сполук за допомогою модифікацій споякій придатній стадії синтезу за допомогою звисобів, описаних у на уковій літературі. Як основний чайних методик, добре відомих в галузі хімії, або посібник для умов здійснення реакції і реагентів вони можуть бути відщеплені на пізній стадії реакавтори посилаються на [Advanced Organic Chemisції або підготовки. try, 4-е видання, Jerry March, опублікований - John Сполука формули (І) може утворювати стабіWiley & Sons, 1992]. льні кислотні або основні солі, і в таких випадках Також слід взяти до уваги, що для деяких реавведення сполуки у вигляді солі може бути доцількцій, описаних у даному винаході, може бути необним, і фармацевтично прийнятні солі можуть бути хідним/бажаним захищати будь-які чутливі групи отримані за допомогою звичайних способів, таких сполук. Випадки, коли такий захист необхідний або як описані далі. Прикладами фармацевтично прибажаний, відомі фахівцю в даній галузі техніки, так йнятних солей є органічні кислото-адитивні солі, само як і прийнятні способи для такого захисту. утворені з кислотами, які утворюють фізіологічно Звичайні захисні групи можуть застосовуватися прийнятний аніон, наприклад, тозилат, метансувідповідно до загальноприйнятої практики (наприльфонат і α-гліцерофосфат. Придатними утвореклад, [Greene T.W. Protective Groups in Organic ними неорганічними солями також бути сульфат, Synthesis. - John Wiley & Sons, 1991]. нітрат і хлорид. Прикладами придатної захисної групи для гідФармацевтично прийнятні солі можуть бути роксильної групи є, наприклад, ацильна група, отримані за допомогою стандартних методик, вінаприклад алканоїльна група, така як ацетил, ародомих у даній галузі, наприклад шляхом реагуванїльна група, наприклад бензоїл, силільна група, ня сполуки формули (І) (і в деяких випадках склатака як триметилсиліл або арилметильна група, дного ефіру) із придатною кислотою, яка дає наприклад бензил. Умови зняття захисту для вифізіологічно прийнятний аніон. Також можливо щезгаданих захисних груп головним чином будуть одержувати солі з відповідним лужним металом залежати від вибору захисної групи. Так, напри(наприклад, натрієм, калієм або літієм) або лужноклад, ацильна група, така як алканоїльна або ароземельним металом (наприклад, кальцієм) шляїльна група, можуть бути відщеплені, наприклад, хом обробки сполуки формули (І) (і в деяких випаза допомогою гідролізу з придатною основою, тадках складного ефіру) одним еквівалентом кою як гідроксид лужного металу, наприклад гідрогідроксиду лужного металу або алкоксиду або поксид літію або натрію. Альтернативно, силільна ловиною еквівалента гідроксиду лужноземельного група, така як триметилсиліл, може бути відщепметалу або алкоксиду (наприклад, етоксиду або лена, наприклад, за допомогою фториду або аквометоксиду) у водному середовищі з наступними кислоти; або арилметильна група, така як бензизвичайними методиками очищення. льна група, може бути відщеплена, наприклад, Складний ефір сполуки формули (І), який здашляхом гідрування в присутності каталізатора, тний гідролізуватися в умовах in vivo, являє собою, такого як паладій на вугіллі. наприклад, фармацевтично прийнятний складний Придатними захисними групами для аміногруефір, який гідролізується в організмі людини або 15 77967 16 тварини з утворенням вихідної кислоти або спирту. центрифугування при 26000хg впродовж 30хв. Придатні складні ефіри сполуки формули (І), Мічений по 6-His білок видаляли із супернатанту які здатні гідролізуватися в умовах in vivo, утворені за допомогою кобальтової хелатувальної полімерз гідроксильною групою, включають неорганічні ної матриці (TALON: Clontech), яку промивали в 20мм N-[2-гідроксіетил]піперазин-N'-[2складні ефіри, такі як фосфатні складні ефіри і aетансульфонової кислоти (HEPES), 500мМ NaCI, ацилоксіалкільні ефіри. Прикладами a1% (об./об.) етиленгліколю, 0,1%(мас./об.) Pluronацилоксіалкільних ефірів є ацетоксиметокси і 2,2ics F-68 рН8,0, до поступового ступінчастого елюдиметилпропіонілокси-метокси. Іншими групами, ювання зв'язаного білка за допомогою подібного які утворюють складні ефіри, здатні гідролізуватибуфера при додаванні 100мМ імідазолу рН 8,0. ся в умовах in vi vo, для гідроксигрупи є алканоїл, Елюйовані фракції, які містять мічений по 6-His бензоїл, фенілацетил і заміщені бензоїл і фенілабілок, об'єднували, додавали етилендіамінтетраоцетил, алкоксикарбоніл (для одержання алкілкарцтову кислоту (EDTA) і дитіотретоїл (DTT) до кінбонатного складного ефіру), діалкілкарбамоїл і Nцевої концентрації 1мМ і мітку відщеплювали шля(діалкіламіноетил-N-алкілкарбамоїл (для одерхом додавання прецизійної протеази (Amersham жання карбаматів), діалкіламіноацетил і карбоксіPharmacia Biotech). Цю протеазу видаляли за доацетил. Прикладами замісників для бензоїлу є помогою глутатіон-сефарози (Amersham Pharморфоліногрупа і піперазиногрупа, зв'язані з атоmacia Biotech). Немічений білок діалізували в бумом азоту кільця за допомогою метиленової групи фері для зберігання, який складається з 20мМ в 3-му або 4-му положенні бензоїльного кільця. HEPES-Na, 150мМ хлориду натрію, 0,5мМ EDTA, Об'єктом даного винаходу є виявлення сполук, 1%(мас./об.) Pluronics F68, 1%(об./об.) етиленгліякі підвищують активність ПДГ. Такі властивості колю рН 8,0 і зберігали в аліквотах при температуможуть бути оцінені, наприклад, за допомогою рі 80°С. одного або декількох способів тестування, відомих Кожну нову партію вихідного ферменту ПДГК з літератури, наприклад, таких, які викладені в титрували в дослідженні для визначення концентміжнародній заявці [WO, 9962506], а саме дослірації, яка забезпечує приблизно 75% інгібування дження (а) - підвищення активності ПДГ в умовах ПДГ в умовах аналізу. Вихідний фермент (звичайin vitro, дослідження (b) - підвищення активності но в концентрації 20мкг/мл) залишали для зв'язуПДГ в умовах in vitro на виділених первинних клівання впродовж 24год. при температурі 4°С із ПДГ тинах і дослідження (с) - підвищення активності (ПДГ із серця свині, Sigma P7032) (0,05Од/мл) у ПДГ в умовах in vi vo і всі ці дослідження включені буфері, який містить 50мМ 3-[Nв даний винахід шля хом посилання. Альтернативморфоліно]пропансульфонової кислоти (MOPS), но, ці властивості можуть бути оцінені за допомо20мМ ортофосфату дикалію, 60мМ хлориду калію, гою наступного експерименту: 2мМ хлориду магнію, 0,4мМ етилендіамінтетраоцПідвищення активності ПДГ в умовах in vitro тової кислоти (EDTA), 0,2% Pluronic F68, 1мМ диЗа допомогою цього аналізу визначалася здатіотретоїлу (DTT), рН 7,3. тність тестованої сполуки підвищувати активність Для дослідження активності нових сполук, ПДГ. кДНК, яка кодує кіназу ПДГ, може бути отрисполуки розчиняли в 5% ДМСО і 5мкл переносили мана за допомогою полімеразної ланцюгової реав окремі лунки 384-лункових плашок для дослікції (ПЛР) і потім клонована. її можна екпресувати дження. Контрольні лунки містили 5мкл 5% ДМСО у придатній експресійній системі й одержувати замість сполуки. Для визначення максимального поліпептид, який має ПДГ-кіназну активністю. Назначення реакції ПДГ друга серія контрольних луприклад, ПДГкіназа2 людини (rPDHK2), отримана нок включала 5мкл відомого інгібітора в кінцевій при експресії рекомбінатного білка в Escherichia концентрації в кіназній реакції 10мкМ. coli (Е. Соlі), виявляє ПДГ-кіназну активність. Додавали 40мкл розчину попередньо зв'язаноrPDHK2 людини (реєстр, номер L42451.1 у баго ферменту і реакцію фосфорилювання ініціюванку генів) клонували і експресували за допомогою ли шляхом додавання 5мкл 10мкММ АТО у ви щеспособу, описаного в [Baker і ін. (2000) J. Biol. вказаному буфері. Через 45хв. при кімнатній Chem. – 275. – P.15773-15781]. У експресований температурі визначали залишкову активність ПДГ білок вводили сайт розщеплення протеазою, як шляхом додавання субстратів (2,5мМ коферменту описано в цьому посиланні. Інші відомі кінази ПДГ А, 2,5мМ пірофосфату тіаміну (кокарбоксилази), для застосування в дослідженнях можуть бути 2,5мМ пірувату натрію, 6мМ НАД) в об'ємі 40мкл і клоновані і експресовані подібним чином. Для експлашки інкубували протягом 90хв. при температурі пресії активної rPDHK2, клітини штаму Е. coli BL21 навколишнього середовища. Одержання віднов(DE3) трансформували вектором рЕТ28А, який леного НАД (НАДН) визначали шляхом вимірюмістить кДНК rPDHK2. Цей вектор включає мітку вання оптичної густини при 340нм за допомогою на 6-His у білок на його N-кінці. Клітини Е. coli виспектрофотометра для аналізу плашок. Значення рощували у ферментері до значення оптичної гусЕС50 для тестованої сполуки визначали звичайним тини, яке дорівнює 12 (550нм) при температурі шляхом на основі отриманих результатів для 12 37°С, зменшуючи температуру до 22°С доти, поки різних концентрацій сполуки. оптична густина не досягала 15, і експресію білка Відповідно до іншого варіанта здійснення, даіндукували шляхом додавання 0,5мМ ізопропілтіоний винахід забезпечує фармацевтичну композиb-галактозидази. Клітини вирощували впродовж цію, яка містить сполуку формули (І), як описано 3год. при температурі 22°С і збирали шляхом тут ви ще, або її фармацевтично прийнятну сіль центрифугування. Масу ресуспендованих клітин або складний ефір, який здатний гідролізуватися в лізували шляхом гомогенізації при високому тиску умовах in vi vo, у сполученні з фармацевтично приі нерозчинний матеріал видаляли шляхом 17 77967 18 йнятним наповнювачем або носієм. локровної тварини, такої як людина. Композиція може знаходитися у формі, яка Отже, іншим варіантом здійснення винаходу є підходить для перорального введення, наприклад застосування сполуки формули (І), або її фармау вигляді таблетки або капсули, для парантеральцевтично прийнятної солі або складного ефіру, ного введення (включаючи внутрішньовенне, підякий здатний гідролізуватися в умовах in vi vo, для шкірне, внутрішньом'язове, внутрішньосудинне приготування лікарського засобу для застосування введення або інфузію) наприклад, у вигляді стеридля лікування цукрового діабету в теплокровної льного розчину, суспензії або емульсії, для місцетварини, такої як людина. вого введення, наприклад у вигляді мазі або пасТаким чином, іншим варіантом здійснення вити, або для ректального введення, наприклад, у находу є застосування сполуки формули (І), або її вигляді супозиторію. У цілому, вищенаведені комфармацевтично прийнятної солі або складного позиції можуть бути приготовлені звичайним споефіру, який здатний гідролізуватися в умовах in собом при використанні звичайних наповнювачів. vi vo, для приготування лікарського засобу для заКомпозиції згідно із даним винаходом перевастосування для лікування цукрового діабету, зажно представлені у вигляді стандартної дозованої хворювань периферичних судин і ішемії міокарда в форми. Звичайно сполука вводиться теплокровній теплокровної тварини, такої як людина. тварині в стандартній дозі в діапазоні 5-5000мг на Відповідно до іншого варіанта здійснення, ви1м 2 поверхні тіла тварини, тобто приблизно 0,1нахід забезпечує фармацевтичну композицію, яка 100мг/кг. Стандартна доза приблизно знаходиться містить сполуку формули (І), як описано тут вище, в діапазоні, наприклад, 1-100мг/кг, переважно 1або її фармацевтично прийнятну сіль або склад50мг/кг і звичайно вона є терапевтично ефективний ефір, який здатний гідролізуватися в умовах in ною дозою. Лікарська форма, яка містить стандарvi vo, у сполученні з фармацевтично прийнятним тну дозу, така як таблетка або капсула, звичайно наповнювачем або носієм для застосування для включає, наприклад, 1-250мг активного компопідвищення активності ПДГ у теплокровної тваринента. ни, такої як людина. Відповідно до іншого варіанта здійснення, даВідповідно до іншого варіанта здійснення, виний винахід стосується сполуки формули (І) або її нахід забезпечує фармацевтичну композицію, яка фармацевтично прийнятної солі або складного містить сполуку формули (І), як описано тут вище, ефіру, який здатний гідролізуватися в умовах in або її фармацевтично прийнятну сіль або складvi vo, як визначено тут ви ще, для застосування в ний ефір, який здатний гідролізуватися в умовах in способі терапевтичного лікування людини або vi vo, у сполученні з фармацевтично прийнятним тварини. наповнювачем або носієм для застосування для Нами було виявлено, що сполуки за даним вилікування цукрового діабету в теплокровної тваринаходом підвищують активність ПДГ і, отже, предни, такої як людина. ставляють інтерес, оскільки знижують рівень глюВідповідно до іншого варіанта здійснення, викози в крові. нахід забезпечує фармацевтичну композицію, яка Іншим варіантом здійснення даного винаходу є містить сполуку формули (І), як описано тут вище, сполука формули (І) і її фармацевтично прийнятні або її фармацевтично прийнятну сіль або складсолі або складні ефіри, здатні гідролізуватися в ний ефір, який здатний гідролізуватися в умовах in умовах in vi vo, для застосування як лікарського vi vo, у сполученні з фармацевтично прийнятним засобу. наповнювачем або носієм для застосування для Таким чином, винахід стосується сполуки фолікування цукрового діабету, за хворювань перирмули (І), або її фармацевтично прийнятної солі феричних судин і ішемії міокарда в теплокровної або складного ефіру, який здатний гідролізуватися тварини, такої як людина. в умовах in vi vo, для застосування як лікарського Відповідно до іншого варіанта здійснення, визасобу для підвищення активності ПДГ у теплонахід забезпечує спосіб підвищення активності кровної тварини, такої як людина. ПДГ у теплокровної тварини, такої як людина, що Більш конкретно, винахід стосується сполуки має потребу в такому лікуванні, який передбачає формули (І), або її фармацевтично прийнятної солі введення вказаній тварині ефективної кількості або складного ефіру, який здатний гідролізуватися сполуки формули (І) або її фармацевтично прийнв умовах in vi vo, для застосування як лікарського ятної солі або складного ефіру, який здатний гідзасобу для лікування цукрового діабету в теплоролізуватися в умовах in vi vo, як описано тут ви ще. кровної тварини, такої як людина. Відповідно до іншого варіанта здійснення, виБільш переважно, винахід стосується сполуки нахід забезпечує спосіб лікування цукрового діаформули (І), або її фармацевтично прийнятної солі бету в теплокровної тварини, такої як людина, що або складного ефіру, який здатний гідролізуватися має потребу в такому лікуванні, який передбачає в умовах in vi vo, для застосування як лікарського введення вказаній тварині ефективної кількості засобу для лікування цукрового діабету, захворюсполуки формули (І) або її фармацевтично прийнвання периферичних судин і ішемії міокарда в теятної солі або складного ефіру, який здатний гідплокровної тварини, такої як людина. ролізуватися в умовах in vi vo, як описано тут ви ще. Таким чином, іншим варіантом здійснення виВідповідно до іншого варіанта здійснення, винаходу є застосування сполуки формули (І), або її нахід забезпечує спосіб лікування цукрового діафармацевтично прийнятної солі або складного бету, захворювань периферичних судин і ішемії ефіру, який здатний гідролізуватися в умовах in міокарда в теплокровної тварини, такої як людина, vi vo, для приготування лікарського засобу для защо має потребу в такому лікуванні, який передбастосування для підвищення активності ПДГ у тепчає введення вказаній тварині ефективної кількості 19 77967 20 сполуки формули (І) або її фармацевтично прийн(iv) у цілому, перебіг реакцій відслідковують за ятної солі або складного ефіру, який здатний гіддопомогою ТШХ і час реакції наведений тільки з ролізуватися в умовах in vi vo, як описано тут ви ще. метою ілюстрації; Як зазначалося вище, величина дози, необ(ν) ви ходи наведені тільки з метою ілюстрації і хідної для терапевтичного або профілактичного необов'язково, що їх можна одержати при ретельлікування конкретного хворобливого стану звичайному здійсненні способу; приготування може поно змінюється залежно від організму, який піддавторюватися, якщо необхідні додаткові речовини; ється лікуванню, шляху введення і тяжкості захво(vi) дані ЯМР, якщо вони наведені, представрювання, яке піддається лікуванню. Переважно лені у вигляді дельта-значень основних визначазастосовувана денна доза знаходиться в діапазоні льних протонів, представлених у вигляді частин на 1-50мг/кг. Однак, денна доза звичайно змінюється млн (ppm) відносно тетраметилсилану (ТМС) як залежно від організму, який піддається лікуванню, внутрішнього еталона, визначених при 300МГц особливості шляху введення і тяжкості захворю(якщо не вказано інакше) із застосуванням обробвання, яке піддається лікуванню. Отже, оптимальленого дейтерієм диметилсульфоксиду (ДМСО-d6) на доза може бути визначена лікуючим лікарем як розчинника; і піки мультиплетності представлені індивідуально для кожного пацієнта. в такий спосіб: s - синглет; d - дублет; dd - дублет Як зазначалося вище, сполуки, розкриті в дадублетів; t - триплет; tt - потрійний триплет; q ному винаході, становлять інтерес у зв'язку з їх квартет; tq - потрійний квартет; m - мультиплет; br здатністю підвищува ти активність ПДГ. Отже, спо- широкий; луки відповідно до винаходу можуть бути корис(vii) хімічні символи мають звичайні значення; ними для лікування ряду хворобливих станів, застосовуються одиниці і символи СІ; включаючи цукровий діабет, захворювання пери(viii) співвідношення розчинників представлене феричних судин (включаючи переміжну кульгау вигляді об'ємних значень, об./об.; вість), серцеву недостатність і певні міопатії серця, (іх) мас-спектрометричний аналіз (MS) здійсішемію міокарда, ішемію головного мозку і репернювали при енергії електронів 70еВ методом хіміфузію, м'язову слабість, гіперліпідемії, хворобу чної іонізації (СІ), використовуючи зонд прямого Альцгеймера і/або атеросклероз. Альтернативно, опромінення; де ЕІ - вказану іонізацію здійснювали такі сполуки відповідно до винаходу можуть бути шляхом іонізації електронним ударом, FAB - бомкорисними при багатьох хворобливих станів, бардуванням швидкими атомами, ESP - електровключаючи захворювання периферичних судин розпилювального іонізації; m/z - представлені зна(включаючи переміжну кульгавість), серцеву недочення для маси/заряду, звичайно наведені тільки статність і певні міопатії серця, ішемію міокарда, для іонів, які вказані у вихідній масі і, якщо не вкаішемію головного мозку і реперфузію, м'язову слазано інакше, значення представлені в дужках у бість, гіперліпідемії, хворобу Альцгеймера і/або вигляді (М-Н)-; атеросклероз, особливо захворювання перифери(х) використані наступні скорочення: чних судин і ішемію міокарда. NMP 1-метил-2-піролідон; Додатково до їх застосування в терапевтичній ДМФА N,N-диметилформамід; медицині, сполуки формули (І) і їх фармацевтично ТГФ тетрагідрофуран прийнятні солі і складні ефіри, які здатні гідролізуДХМ дихлорметан; ватися в умовах in vivo, також корисні як фармаEtOAc Етилацетат; цевтичні засоби для розвитку та стандартизації (хі) якщо (R) або (S) стереохімія наведена в систем дослідження в умовах in vitro і in vivo для дужках на початку найменування, то вказана стеоцінки дій речовин, які підвищують активність ПДГ реохімія стосується -NH-C(O)-C*(Me)(CF3)(OH) у лабораторних тварин, таких як коти, собаки, кроцентру, як зображено у формулі (І). лики, мавпи, щури і миші, для пошук у нових тераПриклад 1 певтичних засобів. (R)-N-[2-хлор-4-етилсульфоніл-3-(4Далі винахід ілюструється наступними прикламетилпіперазин-1-іл)феніл1-2-гідрокси-2-метилдами, які не обмежують його обсяг, у яких, якщо 3,3,3-трифторпропанамід спеціально не вказано інакше: Формальдегід (0,77г) і триацетоксиборогідрид (і) температура наведена в градусах Цельсія натрію (1,00г) додавали до перемішуваного розчи(°С); операції здійснюються при кімнатній темпену (R)-N-(2-хлор-4-етилсульфоніл-3-піперазин-1ратурі або при температурі навколишнього сереілфеніл)-2-гідрокси-2-метил-3,3,3довища, тобто при температурі в діапазоні 18-25°С трифторпропанаміду (0,467г; Спосіб 1) у 1,2і в атмосфері інертного газу, такого як аргон; дихлоретані (9мл). Реакційну суміш перемішували (іі) органічні розчини висушують над безводпри температурі навколишнього середовища проним сульфатом магнію, випаровування розчинника тягом 16год., потім додавали 1М розчин NaOH здійснюють на роторному випарнику при знижено(20мл) і продукт екстрагували з ДХМ (3x30мл). му тиску (600-4000Па; 4,5-30мм.рт.ст.) при темпеОб'єднані органічні екстракти висушували і летку ратурі бані до 60°С; речовину видаляли шляхом випаровування. За(ііі) хроматографія являє собою флешлишок перекристалізовували з EtOAc/ізогексану, хроматографію на силікагелі; де під картриджем одержуючи вказану в заголовку сполуку (0,315г) у Biotage мають на увазі картридж, який містить KPвигляді твердої речовини. ЯМР: 1,11 (3Н, t), 1,60 (3Н, s), 2,10-2,18 (2Н, SILä діоксиду кремнію, 60А, з розміром частинок 32-63мМ, який постачається Biotage, відділом m), 2,21 (3Н, s), 2,70-2,82 (4Н, m), 3,53 (2Н, q), Dyax Corp., 1500 Avon Street Extended, Charlottes3,55-3,62 (2Н, m), 7,91 (1Н, d), 8,07 (1Н, brs), 8,23 ville, VA 22902, США; (1Н, d), 9,94(1 Η, brs); m/z: 456. 21 77967 22 Приклад 2 (альтернативне одержання) (R)-N-[2-хлор-4-етилсульфоніл-3-(41-Метансульфонілпіперазин (0,370г) додавали метилпіперазин-1-іл)феніл1-2-гідрокси-2-метилдо перемішуваного розчину (R)-N-(43,3,3-трифторпропанамід (альтернативне одеретилсульфоніл-3-фтор-2-хлорфеніл)-2-гідрокси-2жання) метил-3,3,3-трифторпропанаміду (приклад 15 за1-Метилпіперазин (0,102г) додавали до переявки [WO, 01/17956}, 0,213г) у NMP (2мл). Реакціймішуваного розчину (R)-N-(4-етилсульфоніл-3ну суміш нагрівали при 150°С впродовж 48год., фтор-2-хлор феніл)-2-гідрокси-2-метил-3,3,3охолоджували і потім додавали насичений розчин трифторпропанаміду (приклад 15 заявки [WO, хлориду амонію (100мл). Продукт екстрагували з 01/17956]; 0,096г) у N MP (1мл). Реакційну суміш діетиловим ефіром (3x100мл). Органічні екстракти нагрівали при 130°С впродовж 24год. Реакційну висушували і летку речовину видаляли шляхом суміш охолоджували і потім додавали насичений випаровування. Залишок очищали шляхом хромарозчин хлориду амонію (100мл). Продукт екстрагутографії на картриджі Biotage (8г діоксиду кремвали з діетиловим ефіром (3x100мл). Органічні нію), елююючи з 50-70% EtOAc/ізогексану. Продукт екстракти висушували і летку речовину видаляли перекристалізовували з EtOAc/ізогексану, одершляхом випаровування. Залишок очищали шляжуючи вказану в заголовку сполуку (0,167г) у вихом хроматографії на картриджі Biotage (8г діоксигляді твердої речовини. ду кремнію), елююючи з 5% метанолом/ДХМ, одеЯМР (CDCI3): 1,26 (3Н, t), 1,78 (3Н, s), 2,86 (3Н, ржуючи вказану в заголовку сполуку (0,086г) у s), 3,01-3,18 (4Н, m), 3,39 (2Н, q), 3,68 (1Н, s), 3,75вигляді твердої речовини. 3,87 (4Н, m), 8,01 (1Н, d), 8,57 (1Н, d), 9,62 (1Н, ЯМР: 1,11 (3Н, t), 1,60 (3Н, s), 2,10-2,18 (2Н, brs); m/z: 520. m), 2,21 (3Н, s), 2,70-2,82 (4Н, m), 3,53 (2Н, q), Вихідна речовина 3,55-3,62 (2Н, m), 7,91 (1Н, d), 8,07 (1Н, brs), 8,23 Спосіб 1 (1Н, d), 9,94 (1Н, brs); m/z: 456. (R)-N-(2-хлор-4-етилсульфоніл-3-піперазин-1Приклад 3 ілфеніл)-2-гідрокси-2-метил-3,3,3(R)-N-[2-хлор-4-етилсульфоніл-3-(4трифторпропанамід мезилпіперазин-1-іл)феніл]-2-гідрокси-2-метилТрет-бутиловий ефір 1-піперазинкарбоксилату 3,3,3-трифторпропанамід (6,12г) додавали до перемішуваного розчину (R)Триетиламін (0,091г) і метансульфонілхлорид N-(4-етилсульфоніл-3-фтор-2-хлорфеніл)-2(0,124г) додавали до перемішуваної суспензії (R)гідрокси-2-метил-3,3,3-трифторпропанаміду (приN-(2-хлор-4-етилсульфоніл-3-піперазин-1-ілфеніл)клад 15 заявки [WO, 01/17956}, 4,14 г) у NMP 2-гідрокси-2-метил-3,3,3-трифторпропанаміду (15мл). Реакційну суміш нагрівали при 150°С (0,401г; Спосіб 1) у ДХМ (10мл). Реакційну суміш впродовж 24год., охолоджували і потім додавали перемішували при температурі навколишнього насичений розчин хлориду амонію (300мл). Просередовища впродовж 2год. і потім додавали надукт екстрагували з діетиловим ефіром (3x300мл). сичений розчин хлориду амонію (20мл) і продукт Органічні екстракти висушували і летку речовину екстрагували з ДХМ (3x30мл). Органічні екстракти видаляли шляхом випаровування. Залишок очивисушували і летку речовину видаляли шляхом щали шляхом хроматографії на картриджі Biotage випаровування. Залишок очищали шляхом хрома(90г діоксиду кремнію), елююючи з 70% тографії на картриджі Biotage (8г діоксиду кремEtOAc/ізогексану. Продукт розчиняли в трифторонію), елююючи з 50-70% EtOAc/ізогексану, одерцтової кислоті (12мл), потім перемішували при жуючи вказану в заголовку сполуку (0,215г) у температурі навколишнього середовища впродовж вигляді твердої речовини. 30хв. Реакційну суміш розчиняли в EtOAc (200мл), ЯМР (CDCI3): 1,26 (3Н, t), 1,78 (3Н, s), 2,86 (3Н, потім промивали 1М розчином NaOH (300мл). Орs), 3,01-3,18 (4Н, m), 3,39 (2H, q), 3,68 (1H, s), 3,75ганічні екстракти висушували і летку речовину ви3,87 (4H, m), 8,01 (1H, d), 8,57 (1H, d), 9,62 (1H, даляли шляхом випаровування, одержуючи вказаbrs); m/z: 520. ну в заголовку сполуку (3,52г) у вигляді твердої Приклад 4 речовини. (R)-N-[2-хлор-4-етилсульфоніл-3-(4ЯМР: 1,12 (3Н, t), 1,60 (3Н, s), 2,74-2,86 (6Н, мезилпіперазин-1-іл)феніл1-2-гідрокси-2-метилm), 3,48-3,59 (4Н, m), 7,89 (1Н, d), 8,22 (1Н, d); m/z: 3,3,3-трифторпропанамід 442. Комп’ютерна в ерстка В.Сердюк Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted of n-phenyl 2-hydroxy-2-methyl-3,3,3-trifluoropropanamide derivatives, which elevate activity of pyruvate dehydrogenase activity
Автори англійськоюButlin Roger John
Назва патенту російськоюПроизводные замещенного n-фенил 2-гидрокси-2-метил-3,3,3-трифторпропанамида, которые повышают активность пируватдегидрогеназы
Автори російськоюБатлин Роджер Джон
МПК / Мітки
МПК: A61P 9/10, A61P 3/10, C07D 295/26, C07D 295/096, A61K 31/495, C07D 295/12
Мітки: активність, похідні, заміщеного, 2-гідрокси-2-метил-3,3,3-трифторпропанаміду, піруватдегідрогенази, n-феніл, підвищують
Код посилання
<a href="https://ua.patents.su/11-77967-pokhidni-zamishhenogo-n-fenil-2-gidroksi-2-metil-333-triftorpropanamidu-yaki-pidvishhuyut-aktivnist-piruvatdegidrogenazi.html" target="_blank" rel="follow" title="База патентів України">Похідні заміщеного n-феніл 2-гідрокси-2-метил-3,3,3-трифторпропанаміду, які підвищують активність піруватдегідрогенази</a>
Попередній патент: Спосіб експрес-контролю октанових та цетанових чисел рідких нафтових палив
Наступний патент: Пристрій для кріплення закладної деталі до форми
Випадковий патент: Спосіб анестезіологічного забезпечення при оперативних втручаннях в зоні іннервації люмбосакральних сегментів спинного мозку у дітей















