Сполука тетрагідропіридину та лікарський засіб на її основі
Номер патенту: 61102
Опубліковано: 17.11.2003
Автори: Рідел Ріхард, Постіус Стефан, Сімон Вольфганг-Александер
Формула / Реферат
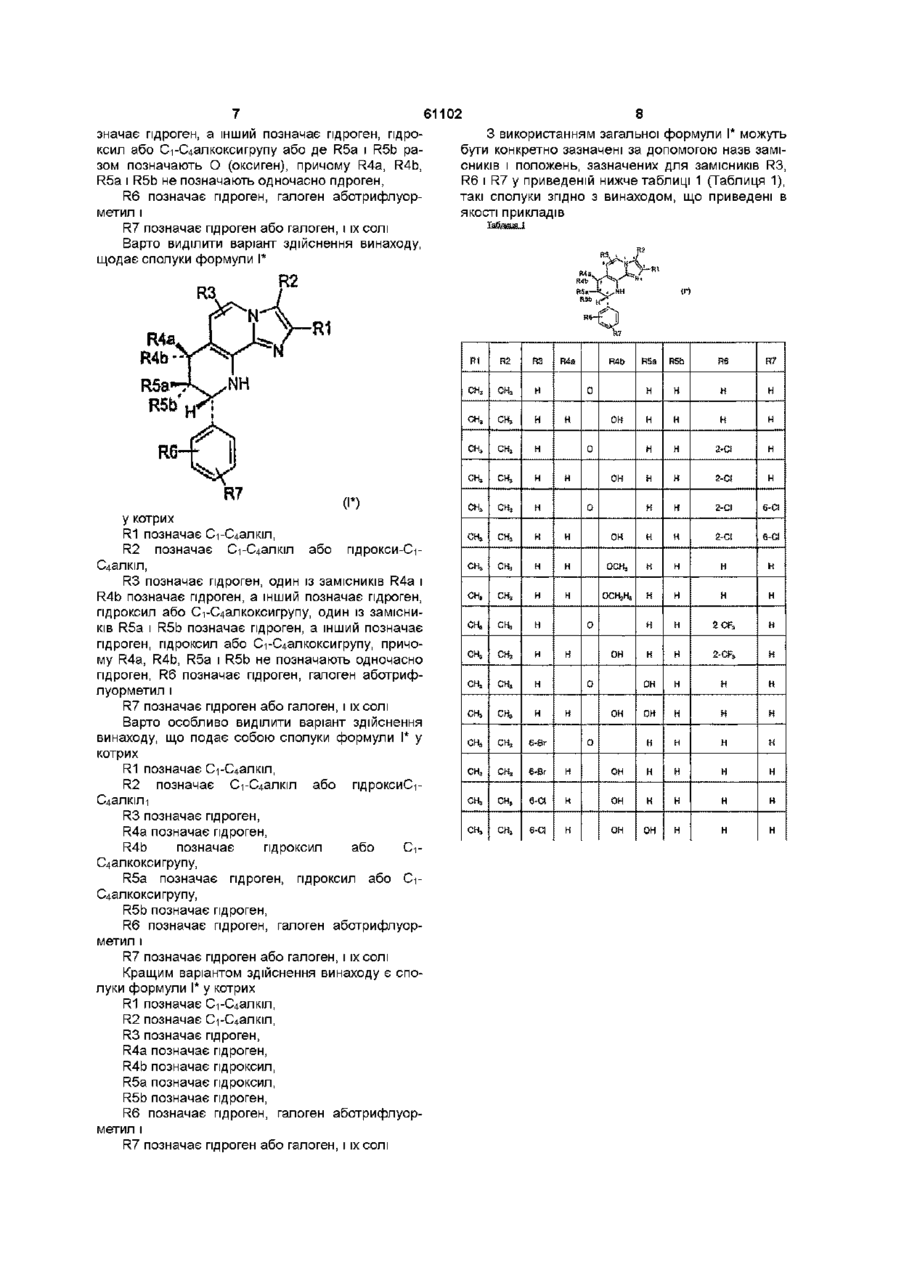
1. Сполука тетрагідропіридину формули І
, (І)
де
R1 означає С1-С4алкіл,
R2 означає С1-С4алкіл або гідроксі-С1-С4алкіл,
R3 означає гідроген або галоген,
один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил, С1-С4алкоксил, С1-С4алкоксі-С1-С4алкоксил або С1-С4алкілкарбонілоксигрупу, або де R4a і R4b разом означають О (оксиген),
один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил, С1-С4алкоксил, С1-С4алкоксі-С1-С4алкоксил або С1-С4алкілкарбонілоксигрупу, або де R5a і R5b разом означають О (оксиген),
або де
один із замісників R4a і R4b, з одного боку, і один із замісників R5a і R5b, з іншого боку, означають у кожному випадку гідроген, а інші замісники в кожному випадку разом утворюють метилендіоксигрупу (-О-СН2-О-) або етилендіоксигрупу (-O-CH2-CH2-O-), ізопропілідендіокси групу, причому R4a, R4b, R5a і R5b одночасно не означають гідроген,
R6 означає гідроген, галоген, С1-С4алкіл, С1-С4алкоксил, С1-С4алкоксикарбоніламіногрупу, С1-С4алкоксі-С1-С4алкоксикарбоніламіногрупу чи трифлуорметил, а
R7 означає гідроген, галоген, С1-С4алкіл або С1-С4алкоксигрупу,
і її солі.
2. Сполука за п.1, яка відрізняється тим, що в ній
R1 означає С1-С4алкіл,
R2 означає С1-С4алкіл або гідроксі-С1-С4алкіл,
R3 означає гідроген,
один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил або С1-С4алкоксигрупу, або в котрому R4a і R4b разом означають О (оксиген),
один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил або С1-С4алкоксигрупу, або в котрому R5a і R5b разом означають О (оксиген),
причому R4a, R4b, R5a і R5b не означають одночасно гідроген,
R6 означає гідроген, галоген або трифлуорметил і
R7 означає гідроген або галоген, і її солі.
3. Сполука за п.1, яка відрізняється тим, що має формулу І*
, (І*)
де
R1 означає С1-С4алкіл,
R2 означає С1-С4алкіл або гідроксі-С1-С4алкіл,
R3 означає гідроген,
один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил або С1-С4алкоксигрупу,
один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил або С1-С4алкоксигрупу,
причому R4a, R4b, R5a і R5b не означають одночасно гідроген,
R6 означає гідроген, галоген або трифлуорметил і
R7 означає гідроген або галоген, і її солі.
4. Сполука за п.3, яка відрізняється тим, що в ній
R1 означає С1-С4алкіл,
R2 означає С1-С4алкіл або гідрокси-С1-С4метил,
R3 означає гідроген,
R4a означає гідроген, R4b означає гідроксил або С1-С4алкоксигрупу,
R5a означає гідроген, гідроксил або С1-С4алкоксигрупу,
R5b означає гідроген,
R6 означає гідроген, галоген або трифлуорметил і
R7 означає гідроген або галоген, і її солі.
5. Сполука за п.3, яка відрізняється тим, що в ній
R1 означає С1-С4алкіл,
R2 означає С1-С4алкіл,
R3 означає гідроген,
R4a означає гідроген,
R4b означає гідроксил,
R5a означає гідроксил,
R5b означає гідроген,
R6 означає гідроген, галоген або трифлуорметил і
R7 означає гідроген або галоген,
і її солі.
6. Сполука за п.1, яка відрізняється тим, що обрана з групи, що включає
7,8-дигідрокси-2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин-7-он,
9-(2-хлорфеніл)-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h] [1,7]нафтирідин-7-он,
9-(2,6-дихлорфеніл)-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин-7-он,
9-(2-трифлуорметилфеніл)-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин-7-он,
7-гідрокси-2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
9-(2-хлорфеніл)-7-гідрокси-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
9-(2,6-дихлорфеніл)-7-гідрокси-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
9-(2-трифлуорметилфеніл)-7-гідрокси-2,3-диметил-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
8-гідрокси-2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[ 1,2-h][1,7]нафтирідин-7-он,
(7S,8R,9R)-2,3-диметил-7,8-дигідрокси-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
(8R,9R)-3-форміл-8-гідрокси-2-метил-7-оксо-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
(7R,8R,9R)-3-гідроксиметил-7,8-дигідрокси-2-метил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин і
(7S,8R,9R)-7,8-ізопропілідендіокси-2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин,
або її сіль.
7. Сполука за п.6, яка відрізняється тим, що має 9R-конфігурацію, або її сіль.
8. Сполука за п.1, яка відрізняється тим, що має хімічну назву (7R,8R,9R)-7,8-дигідрокси-2,3-диметил-9-феніл-7,8,9,10-тетрагідроімідазо[1,2-h][1,7]нафтирідин, або її сіль.
9. Сполука за п.1 і її фармакологічно прийнятна сіль, яка відрізняється тим, що використовується для виготовлення лікарських засобів, призначених для попередження і лікування шлунково-кишкових хвороб.
10. Лікарський засіб, що містить сполуку за п.1 і/або її фармакологічно прийнятну сіль разом із звичайними фармацевтичними допоміжними речовинами і/або ексципієнтами.
Текст
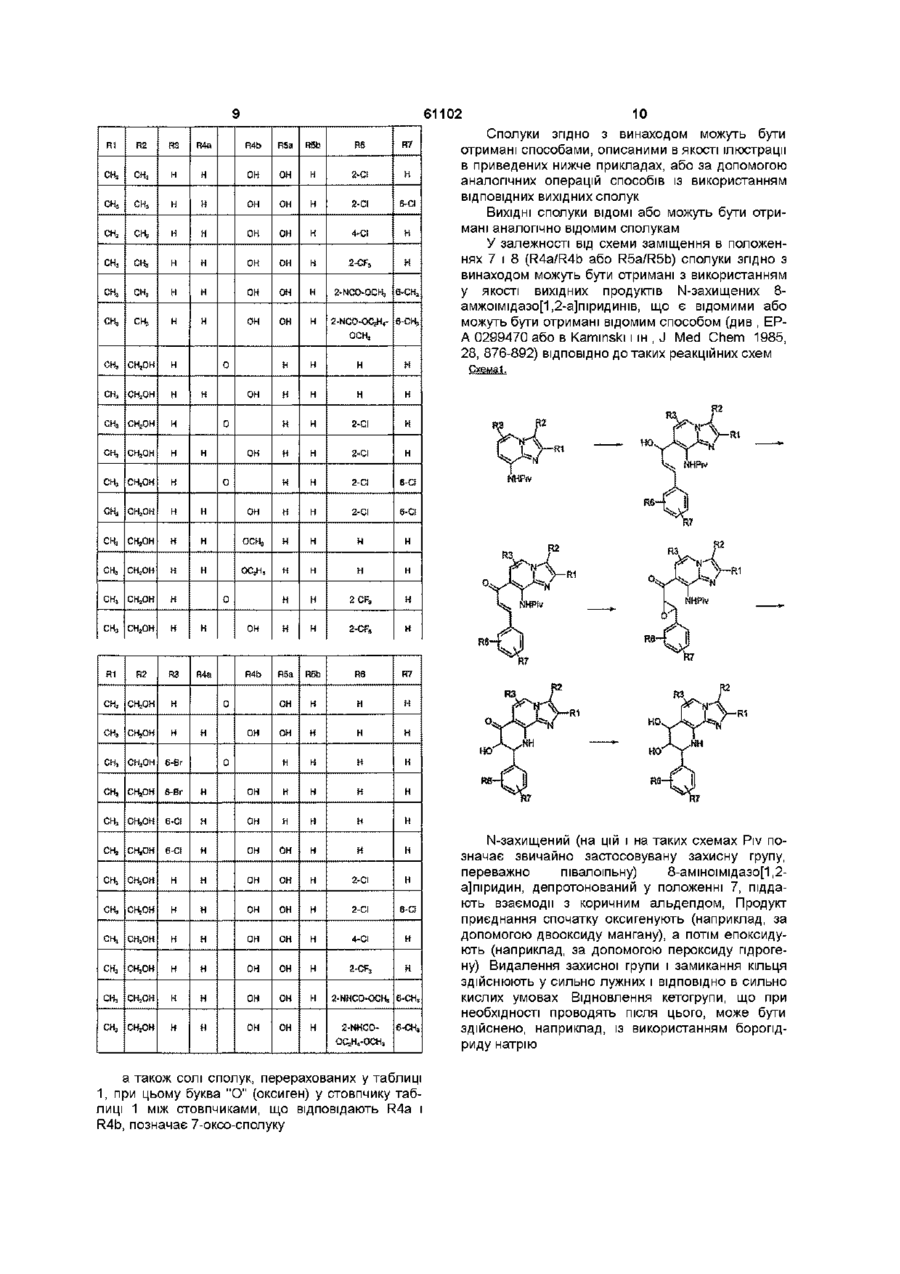
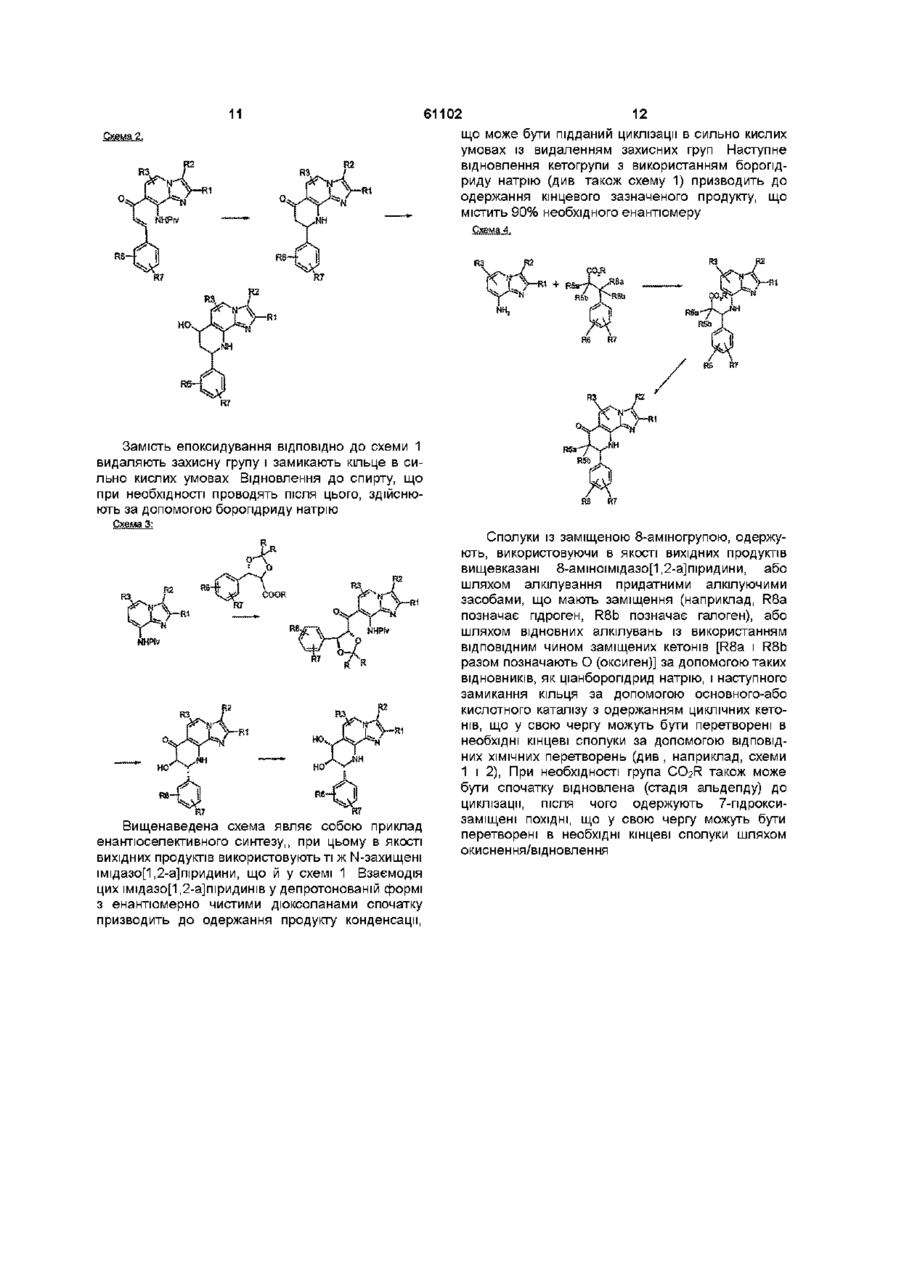
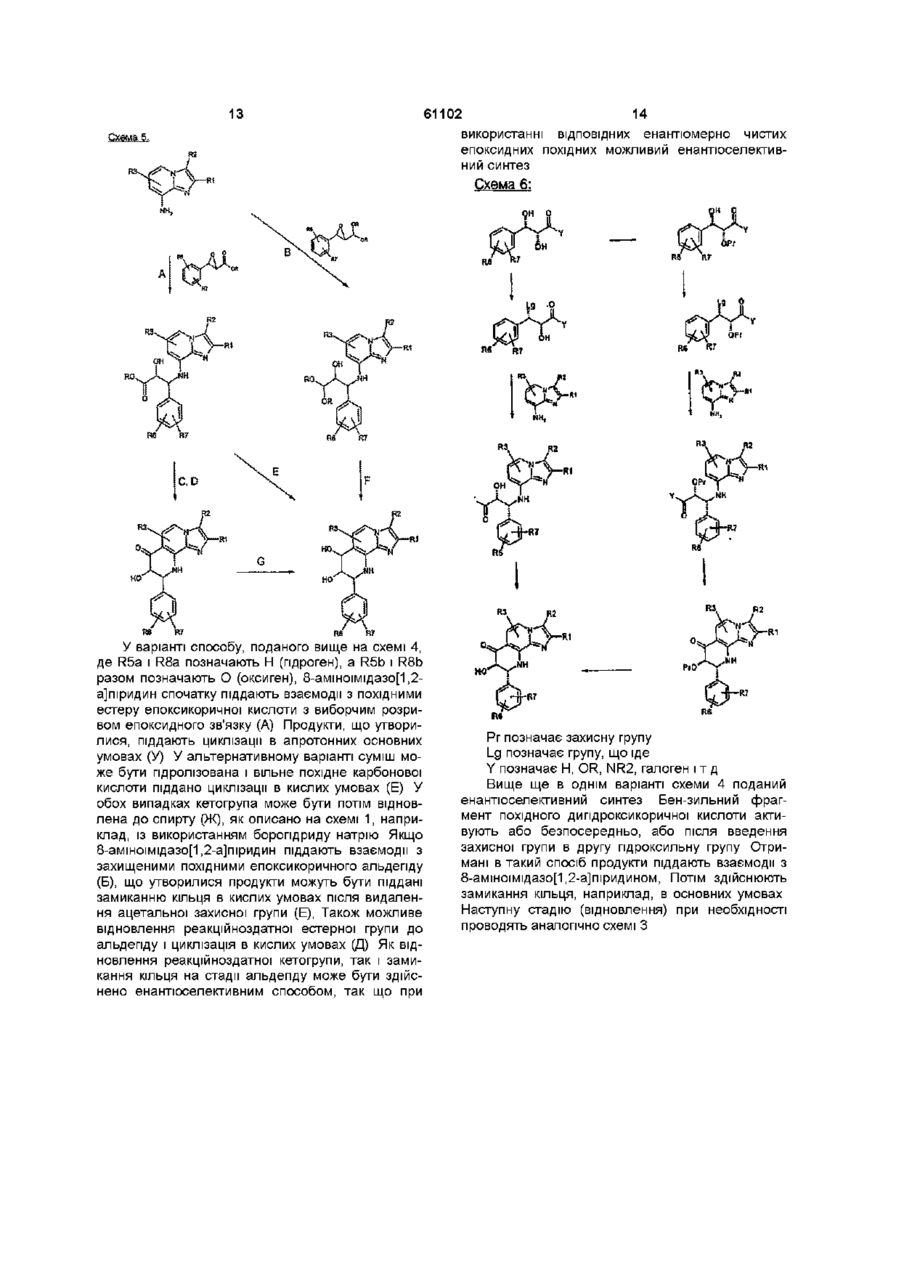
1 Сполука тетрагідропіридину формули І R2 RX .(І) Де R1 означає Сі-С4алкіл, R2 означає Сі-С4алкіл або пдроксі-Сі-С4алкіл, R3 означає гідроген або галоген, один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил, Сі-С4алкоксил, Сі-С4алкоксі-Сі-С4алкоксил або Сг С4алкілкарбонілоксигрупу, або де R4a і R4b разом означають О (оксиген), один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил, Сі-С4алкоксил, Сі-С4алкоксі-Сі-С4алкоксил або Сг С4алкілкарбонілоксигрупу, або де R5a і R5b разом означають О (оксиген), або де один із замісників R4a і R4b, з одного боку, і один із замісників R5a і R5b, з іншого боку, означають у кожному випадку гідроген, а ІНШІ замісники в кожному випадку разом утворюють метилендюксигрупу (-О-СН2-О-) або етилендюксигрупу (-О-СН2-СН2О-), ізопропілідендюкси групу, причому R4a, R4b, R5a і R5b одночасно не означають гідроген, R6 означає гідроген, галоген, Сі-С4алкіл, d С4алкоксил, Сі-С4алкоксикарбоніламіногрупу, d С4алкоксі-Сі-С4алкоксикарбоніламшогрупу чи трифлуорметил, а R7 означає гідроген, галоген, Сі-С4алкіл або С г С4алкокси групу, і її солі 2 Сполука за п 1, яка відрізняється тим, що в ній R1 означає Сі-С4алкіл, R2 означає Сі-С4алкіл або пдроксі-Сі-С4алкіл, R3 означає гідроген, один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил або Сг С4алкоксигрупу, або в котрому R4a і R4b разом означають О (оксиген), один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил або Сг С4алкоксигрупу, або в котрому R5a і R5b разом означають О (оксиген), причому R4a, R4b, R5a і R5b не означають одночасно гідроген, R6 означає гідроген, галоген або трифлуорметил і R7 означає гідроген або галоген, і її солі 3 Сполука за п 1, яка відрізняється тим, що має формулу R1 означає Сі-С4алкіл, О о (О 61102 R2 означає Сі-С4алкіл або пдроксі-Сі-С4алкіл, R3 означає гідроген, один із замісників R4a і R4b означає гідроген, а інший означає гідроген, гідроксил або d С4алкокси групу, один із замісників R5a і R5b означає гідроген, а інший означає гідроген, гідроксил або d С4алкокси групу, причому R4a, R4b, R5a і R5b не означають одночасно гідроген, R6 означає гідроген, галоген або трифлуорметил і R7 означає гідроген або галоген, і її солі 4 Сполука за п 3, яка відрізняється тим, що в ній R1 означає Сі-С4алкіл, R2 означає Сі-С4алкіл або пдрокси-С-і^метил, R3 означає гідроген, R4a означає гідроген, R4b означає гідроксил або Сі-С4алкокси групу, R5a означає гідроген, гідроксил або dС4алкокси групу, R5b означає гідроген, R6 означає гідроген, галоген або трифлуорметил і R7 означає гідроген або галоген, і її солі 5 Сполука за п 3, яка відрізняється тим, що в ній R1 означає Сі-С4алкіл, R2 означає Сі-С4алкіл, R3 означає гідроген, R4a означає гідроген, R4b означає гідроксил, R5a означає гідроксил, R5b означає гідроген, R6 означає гідроген, галоген або трифлуорметил і R7 означає гідроген або галоген, і її солі 6 Сполука за п 1, яка відрізняється тим, що обрана з групи, що включає 7,8-дипдрокси-2,3-диметил-9-феніл-7,8,9,10тетрапдроімідазо[1,2-п][1,7]нафти рідин, 2,3-диметил-9-феніл-7,8,9,10тетрапдроімідазо[1,2-п][1,7]нафтирідин-7-он, 9-(2-хлорфеніл)-2,3-диметил-7,8,9,10тетрапдроімідазо[1,2-h] [1,7]нафтирідин-7-он, 9-(2,6-дихлорфеніл)-2,3-диметил-7,8,9,10тетрапдроімідазо[1,2-h][1,7]нафтирідин-7-он, 9-(2-трифлуорметилфеніл)-2,3-диметил-7,8,9,10тетрапдроімідазо[1,2-h][1,7]нафтирідин-7-он, 7-пдрокси-2,3-диметил-9-феніл-7,8,9,10тетрапдроімідазо[1,2-h][1,7]нафти рідин, 9-(2-хлорфеніл)-7-пдрокси-2,3-диметил-7,8,9,10тетрапдроімідазо[1,2-h][1,7]нафти рідин, 9-(2,6-дихлорфеніл)-7-пдрокси-2,3-диметил7,8,9,10-тетрапдроімідазо[1,2-п][1,7]нафтирідин, 9-(2-трифлуорметилфеніл)-7-пдрокси-2,3диметил-7,8,9,10-тетрапдроімідазо[1,2п][1,7]нафтирідин, 8-пдрокси-2,3-диметил-9-феніл-7,8,9,10тетрапдроімідазо[ 1,2-п][1,7]нафтирідин-7-он, (73^^)-2,3-диметил-7,8-дипдрокси-9-феніл7,8,9,10-тетрапдроімідазо[1,2-п][1,7]нафтирідин, (8R,9R)-3^opMin-8-riflpoKCH-2-MeTHn-7-OKCo-9феніл-7,8,9,10-тетрапдроімідазо[1,2п][1,7]нафтирідин, (7R,8R,9R)-3-riflpoKCHMeTHn-7,8-flHriflpoKCH-2метил-9-феніл-7,8,9,10-тетрапдроімідазо[1,2п][1,7]нафтирідин | (7S,8R,9R)-7,8-i3onpomnifleHflioKCH-2,3-flHMeTHn-9феніл-7,8,9,10-тетрапдроімідазо[1,2п][1,7]нафтирідин, або и сіль 7 Сполука за п 6, яка відрізняється тим, що має 9R-кoнфlгypaцlю, або її сіль 8 Сполука за п 1, яка відрізняється тим, що має хімічну назву (7R,8R,9R)-7,8-flHriflpoKCH-2,3диметил-9-феніл-7,8,9,10-тетрапдроімідазо[1,2п][1,7]нафтирідин, а бо її сіль 9 Сполука за п 1 і її фармакологічно прийнятна сіль, яка відрізняється тим, що використовується для виготовлення лікарських засобів, призначених для попередження і лікування шлунково-кишкових хвороб 10 Лікарський засіб, що містить сполуку за п 1 і/або її фармакологічно прийнятну сіль разом із звичайними фармацевтичними допоміжними речовинами і/або ексципієнтами Винахід відноситься до нових сполук, що використовуються у фармацевтичній промисловості в якості діючих речовин для готування лікарських засобів R3. ВІДОМІ прототипи У патенті США 4468400 описані трициклічні імідазо[1,2-а]піридини, які мають різноманітні кільцеві системи, сконденсовані з імідазопіридинівим скелетом, і придатні для лікування пептичних виразкових хвороб Опис винаходу Винахід відноситься до сполук формули І R6 (І) у котрій R1 позначає Сі-С4алкіл, R2 позначає Сі-С4алкіл або пдроксиСг С43ЛКІЛ, R3 позначає гідроген або галоген, один із замісників R4a і R4b позначає гідроген, а інший гідроген, гідроксил, Сі-С4алкоксил, Сі-С4алкоксиСі-С4алкоксил або С1-С4алкілкарбонілоксигрупу 61102 або де R4a і R4b разом позначають О (оксиген), один із замісників R5a і R5b позначає гідроген, а інший позначає гідроген, гідроксил, СгС4алкоксил, Сі-С4алкоксиСі-С4алкоксил або С1С4алкілкарбонілоксигрупу, або де R5a і R5b разом позначають О (оксиген), або в котрій один із замісників R4a і R4b, з одного боку, і один із замісників R5a і R5b, з іншого боку, позначають у кожному випадку гідроген, а ІНШІ замісники в кожному випадку разом утворюють метилендіоксигрупу (-О-СН2О-) або етилендюксигрупу (-О-СН2-СН2-О-), причому R4a, R4b, R5a і R5b одночасно не позначають гідроген, R6 позначає гідроген, галоген, d С4алкт, Сі-С4алкоксил, dС4алкоксикарбоніламшогрупу, Сі-С4алкокси d С4алкоксикарбоніламіногрупу або трифлуорметил, a R7 позначає гідроген, галоген, Сі-С4алкіл або d С4алкоксигрупу, а також до їх солей Сі-С4алкіл позначає алкільні радикали з прямим або розгалуженим ланцюгом, що мають від 1 до 4 атомів вуглецю У якості прикладів можна відзначити бутильний радикал, ізобутильний радикал, втор-бутильний радикал, трет-бутильний радикал, пропільний радикал, ізопропільний радикал, етильний радикал і метиль-ний радикал Кращим є метильний радикал ГідроксиСі-С4алкіл позначає зазначені вище Сі-С4алкільні радикали, що заміщені пдроксигрупою У якості прикладів можна відзначити пдроксиметильний радикал, 2-пдроксіетильний радикал і 3-пдроксипропільний радикал Кращим є гідрокси метильний радикал У контексті даного опису галоген позначає бром, хлор або флуор Сі-С4алшксигрупа позначає радикали, що крім атома оксигену містять алкільний радикал із прямим чи розгалуженим ланцюгом, що має від 1 до 4 атомів вуглецю У якості прикладів можна відзначити бутоксигрупу, ізобутоксигрупу, третбутоксигрупу, пропоксигрупу, ізопропоксигрупу, а переважно етоксигрупу і метоксигрупу Сі-С4алкокси-Сі-С4алкоксигрупа позначає одну з вищевказаних Сі-С4алкоксигруп, що заміщена ще одною Сі-С4апкоксифупою У якості прикладівможна відзначити 2-(метокси)етоксигрупу (СНз-ОСН2-СН2-О) і 2-(етокси)етоксигрупу(СН3-СН2-ОСН2-СН2-О) Сі-С4алкілкарбонілоксигрупа позначає карбонілоксигрупу, приєднану до одного з вищевказаних Сі-С4алкільних радикалів Як приклад можна відзначити аце-токсигрупу (СНзСОО-), Сі-С4алкоксикарбоніл позначає карбонільну групу, до якої приєднана одна з вищевказаних d С4алкоксигруп У якості прикладів можна відзначити метоксика-рбоншьний радикал (СНзО-С(О)-) і етоксикарбонільний радикал (СНзСН2О-С(О)-) Сі-С4алкоксикарбоніламшогрупа позначає аміногрупу, заміщену одним із вищевказаних d С4алкоксикарбонільних радикалів У якості прикладів можна відзначити етоксикарбоніламіногрупу і метоксикарбоніламшогрупу Сі-С4алкокси-Сі-С4алкоксикарбоніл позначає карбонільну групу, до якої приєднана одна з вищевказаних Сі-С4алкокси-Сі-С4алкоксигруп У якості прикладів можна відзначити 2(метокси)етоксикарбонільний радикал (СНз-О СН2СН2-О-СО-) і 2-(етокси)етоксикарбонільний радикал (СН3СН2-О-СН2СН2-О-СО-) Сі-С4алкокси-Сі-С4алкоксикарбоніламшогрупа позначає аміногрупу, заміщену одним із вищевказаних Сі-С4алкокси-Сі-С4алкокси карбонільних радикалів, У якості прикладів можна відзначити 2(метокеи)етоксикарбоніламшогрупу і 2(етокси)етоксикарбоніламшогрупу Прийнятні солі сполук формули І, у залежності від заміщень, головним чином являють собою кислотно-адитивні солі Особливо слід відзначити фармакологічно прийнятні солі неорганічних і органічних кислот, звичайно застосовувані у фармації Такої прийнятні солі являють собою водорозчинні і водонерозчинні кислотно-адитивні солі таких кислот, як, наприклад, пдрохлоридна кислота, пдробромідна кислота, фосфорна кислота, нітратна кислота, сульфатна кислота, оцтова кислота, лимонна кислота, D-глюконова кислота, бензойна кислота, 2-(4-пдроксибензош)бензойна кислота, масляна кислота, сульфосаліцилова кислота, малеїнова кислота, лауринова кислота, яблучна кислота, фумарова кислота, янтарна кислота, щавлева кислота, винна кислота, ембонова кислота, стеаринова кислота, толуолсульфонова кислота, метансульфонова кислота або 3-пдрокси2-нафтойна кислота, причому при одержанні солей кислоти застосовують в еквімо-лярному або у відмінному від нього кількісному співвідношенні в залежності від того, використовується одно- або багатоосновна кислота, і від того, яку сіль потрібно одержати Фармакологічно неприйнятні солі, що можуть бути спочатку отримані в якості проміжних продуктів способу, наприклад, при одержанні сполук згідно з винаходом в промисловому масштабі, перетворюють у фармакологічно прийнятні солі способами, відомими спеціалісту в даній області ВІДПОВІДНО ДО експертних даних сполуки згідно з винаходом, а також їх солі, наприклад, коли їх можна виділити в кристалічній формі, можуть містити різну КІЛЬКІСТЬ розчинників Тому під об'єм винаходу підпадають усе сольвати і зокрема всі гідрати сполук формули І, а також усе сольвати і зокрема всі гідрати солей сполук формули І Сполуки формули І мають три хіральних центри Винахід відноситься до усіх восьми можливих стереоізомерів у будь-якому необхідному співвідношенні у суміші одного з одним, у тому числі до чистих енантюмерів, що являють собою кращий об'єкт винаходу Якщо один із замісників R4a і R4b, з одного боку, і один із замісників R5a і R5b, з іншого боку, разом утворять метилендіоксигрупу або етилендіоксигрупу, ті два замісники, що утворять метилендіоксигрупу або етилендюксигрупу, переважно знаходяться в цис-положенні щодо один одного Варто виділити ті сполуки формули І, у котрих R1 позначає Сі-С4алкіл, R2 позначає Сі-С4алкіл або пдрокси-Сг С43ЛКІТІ1 R3 позначає гідроген, один із замісників R4a і R4b позначає гідроген, а інший позначає гідроген, гідроксил або d С4алкоксигрупу, або де R4a і R4b разом позначають О (оксиген), один із замісників R5a і R5b по 61102 R3 СНз сн3 н сн3 СНз н СНз СНз н СНз СНз н (І*) у штрих R1 позначає Сі-С4алкіл, R2 позначає Сі-С4алкіл або пдрокси-Сг С43ЛКІЛ, R3 позначає гідроген, один із замісників R4a і R4b позначає гідроген, а інший позначає гідроген, гідроксил або Сі-С4алкоксигрупу, один із замісників R5a і R5b позначає гідроген, а інший позначає гідроген, гідроксил або Сі-С4алкоксигрупу, причому R4a, R4b, R5a і R5b не позначають одночасно гідроген, R6 позначає гідроген, галоген аботрифлуорметил і снэ СНз н СНз СНз н Н си, СНз н снэ СНз н CHS СНз н CHS сн3 н CHS сна н R7 позначає гідроген або галоген, і їх солі Варто особливо виділити варіант здійснення винаходу, що подає собою сполуки формули Г у котрих R1 позначає Сі-С4алкіл, R2 позначає Сі-С4алкіл або пдроксиСг сн5 СИ, н С4ЭЛК1Л1 R3 позначає гідроген, R4a позначає гідроген, R4b позначає гідроксил або Сг С4алкокси групу, R5a позначає гідроген, гідроксил або С г С4алкокси групу, R5b позначає гідроген, R6 позначає гідроген, галоген аботрифлуорметил і R7 позначає гідроген або галоген, і їх солі Кращим варіантом здійснення винаходу є сполуки формули Г у котрих R1 позначає Сі-С4алкіл, R2 позначає Сі-С4алкіл, R3 позначає гідроген, R4a позначає гідроген, R4b позначає гідроксил, R5a позначає гідроксил, R5b позначає гідроген, R6 позначає гідроген, галоген аботрифлуорметил і R7 позначає гідроген або галоген, і їх солі R 6 R7 н н н н н н н н н н 2-а н н н 2-а н н н 2-а б-С! ОН н н 2-а 6-а Н ОСН Э н н н н Н ОСНгН, н н н н н н SCF, н н н 2-CF3 н он н и н он н и и н н н н X R2 сн а В5Ь он н н н н X B1 он н н н н он он н н н В4а СНя СНз СНз СНз 6-Вг S-CI R4b 0 Н ОН 0 Н ОН 0 0 он Н 0 он Н 6-вг сн 3 I К5э X значає гідроген, а інший позначає гідроген, гідроксил або Сі-С4алкоксигрупу або де R5a і R5b разом позначають О (оксиген), причому R4a, R4b R5a і R5b не позначають одночасно гідроген, R6 позначає гідроген, галоген аботрифлуорметил і R7 позначає гідроген або галоген, і їх солі Варто виділити варіант здійснення винаходу ; щодає сполуки формули Г 8 З використанням загальної формули Г можуть бути конкретно зазначені за допомогою назв замісників і положень, зазначених для замісників R3, R6 і R7 у приведеній нижче таблиці 1 (Таблиця 1), такі сполуки згідно з винаходом, що приведені в якості прикладів 0 61102 Rl R2 R3 R4a R4b R5a R b S СИ* СНз н н он он СН3 н н он сн3 сн3 н н сн3 СНз н CHj сн3 СН. В6 R7 н 2-а H он н 2-а 6-а он он н 4-а H н он он н 2-CF5 H н н он он и 2-NCO-OCHi 6-CH3 снэ н н он он н 2-NCO-OCH,- 6-CH, OCHS ев, СНгОН н н н н H снэ СНгОН н н н н H СНэ СНгОН н н н 2-а H сн 3 сн,он н н н 2-CI H СНз сн г он н н н г-а 6-а сн, сн г он н н он н н 2-CI 6-CI СНэ СНгОН н н осн3 н н H H сн3 СН3ОН н н QQ,H5 н н H H сиэ СНгОН н н н 2CF3 и сн3 CHjOH и н он н н 2-CF3 H R1 R 2 R3 Ra 4 Rb 4 R 6 R7 СН3 СНгОН н СН, сн,он н сн3 СН,ОН 6-Вг 10 Сполуки ЗГІДНО з винаходом можуть бути отримані способами, описаними в якості ілюстрації в приведених нижче прикладах, або за допомогою аналогічних операцій способів із використанням ВІДПОВІДНИХ вихідних сполук ВИХІДНІ сполуки ВІДОМІ або можуть бути отримані аналогічно відомим сполукам У залежності від схеми заміщення в положеннях 7 і 8 (R4a/R4b або R5a/R5b) сполуки згідно з винаходом можуть бути отримані з використанням у якості вихідних продуктів N-захищених 8амжоімідазо[1,2-а]піридинів, що є відомими або можуть бути отримані відомим способом (див , ЕРА 0299470 або в Kammski і ш , J Med Chem 1985, 28, 876-892) ВІДПОВІДНО ДО таких реакційних схем О н он О н он О О 0 н R5a R b S ОН 0 н н ОН н н н н он н н н н сн, СН3ОН 6-Вг н он н н н н сн, сн,он 8-Сі н он н н н н сн, сн,он 6-а н он он н н н CHSOH н н он он н 2-а н сн, снгон н я он он н 2-а 6-а сн 3 снгон н н он он н 4-а н сна СН;ОН н н он он н 2-CF3 н сн, сн,он н и он он н сн, н н он он н R6 СНз СНгОН 2-NHCO-OCH, 6-СНз 2-NHCOОСУ-и-ОСНз 6-СНз а також солі сполук, перерахованих у таблиці 1, при цьому буква "О" (оксиген) у стовпчику таблиці 1 між стовпчиками, що відповідають R4a і R4b, позначає 7-оксо-сполуку R7 N-захищений (на цій і на таких схемах Piv позначає звичайно застосовувану захисну групу, переважно півалоіпьну) 8-амшоімідазо[1,2а]піридин, депротонований у положенні 7, піддають взаємодії з коричним альдегідом, Продукт приєднання спочатку оксигенують (наприклад, за допомогою двооксиду мангану), а потім епоксидують (наприклад, за допомогою пероксиду гідрогену) Видалення захисної групи і замикання кільця здійснюють у сильно лужних і ВІДПОВІДНО в сильно кислих умовах Відновлення кетогрупи, що при необхідності проводять після цього, може бути здійснено, наприклад, із використанням боропдриду натрію 61102 11 R 2 12 що може бути підданий циклізації в сильно кислих умовах із видаленням захисних груп Наступне відновлення кетогрупи з використанням борогідриду натрію (див також схему 1) призводить до одержання кінцевого зазначеного продукту, що містить 90% необхідного енантюмеру R 6 Замість епоксидування ВІДПОВІДНО ДО схеми 1 видаляють захисну групу і замикають кільце в сильно кислих умовах Відновлення до спирту, що при необхідності проводять після цього, здійснюють за допомогою борогідриду натрію Схема 3: RT R2 Вищенаведена схема являє собою приклад енантюселективного синтезу,, при цьому в якості вихідних продуктів використовують ті ж N-захищені імідазо[1,2-а]піридини, що й у схемі 1 Взаємодія цих імідазо[1,2-а]піридинів у депротонованій формі з енантюмерно чистими дюксоланами спочатку призводить до одержання продукту конденсації, R R 6 7 Сполуки із заміщеною 8-амшогрупою, одержують, використовуючи в якості вихідних продуктів вищевказані 8-амшоімідазо[1,2-а]піридини, або шляхом алкілування придатними алкілуючими засобами, що мають заміщення (наприклад, R8a позначає гідроген, R8b позначає галоген), або шляхом відновних алкілувань із використанням ВІДПОВІДНИМ чином заміщених кетонів [R8a і R8b разом позначають О (оксиген)] за допомогою таких ВІДНОВНИКІВ, як ціанборопдрид натрію, і наступного замикання кільця за допомогою основного-або кислотного каталізу з одержанням циклічних кетонів, що у свою чергу можуть бути перетворені в необхідні кінцеві сполуки за допомогою ВІДПОВІДНИХ ХІМІЧНИХ перетворень (див , наприклад, схеми 1 і 2), При необхідності група CO2R також може бути спочатку відновлена (стадія альдегіду) до циклізації, після чого одержують 7-пдроксизаміщені ПОХІДНІ, що у свою чергу можуть бути перетворені в необхідні кінцеві сполуки шляхом окиснення/відновлення 13 61102 14 використанні ВІДПОВІДНИХ енантюмерно чистих епоксидних похідних можливий енантюселективний синтез Схема 6: У варіанті способу, поданого вище на схемі 4, де R5a і R8a позначають Н (гідроген), a R5b і R8b разом позначають О (оксиген), 8-амшоімідазо[1,2а]піридин спочатку піддають взаємодії з похідними естеру епоксикоричної кислоти з виборчим розривом епоксидного зв'язку (А) Продукти, що утворилися, піддають циклізації в апротонних основних умовах (У) У альтернативному варіанті суміш може бути пдролізована і вільне похідне карбонової кислоти піддано циклізації в кислих умовах (Е) У обох випадках кетогрупа може бути потім відновлена до спирту (Ж), як описано на схемі 1, наприклад, із використанням боропдриду натрію Якщо 8-амшоімідазо[1,2-а]піридин піддають взаємодії з захищеними похідними епоксикоричного альдегіду (Б), що утворилися продукти можуть бути піддані замиканню кільця в кислих умовах після видалення ацетальної захисної групи (Е), Також можливе відновлення реакційноздатної естерної групи до альдегіду і циклізація в кислих умовах (Д) Як відновлення реакційноздатної кетогрупи, так і замикання кільця на стадії альдегіду може бути здійснено енантюселективним способом, так що при Рг позначає захисну групу Lg позначає групу, що іде Y позначає Н, OR, NR2, галоген і т д Вище ще в однім варіанті схеми 4 поданий енантюселективний синтез Бен-зильний фрагмент похідного дипдроксикоричної кислоти активують або безпосередньо, або після введення захисної групи в другу гідроксильну групу Отримані в такий спосіб продукти піддають взаємодії з 8-амшоімідазо[1,2-а]піридином, Потім здійснюють замикання кільця, наприклад, в основних умовах Наступну стадію (відновлення) при необхідності проводять аналогічно схемі З 15 61102 NY H I CO OR 16 лення кетогрупи до спирту як описано на схемі 1 У приведених вище схемах "R" позначає d С4алкіл У естерних групах, зазначених як приклад (-COOR або -CO2R) замість радикала -OR можуть бути присутнім ІНШІ відщеплювані групи, або замість естерної групи може також бути присутньою інша група, що має потрібну реакційну спроможність, Сполуки формули І, у котрих R4a/R4b або R5a/R5b позначають Сі-С4алкоксил, Сі-С4апкоксиСі-С4алкоксил або С1-С4алкілкарбонілоксигрупу, можуть бути отримані такими узвичаєними способами дериватизаци, що ВІДОМІ спеціалісту в даній області (наприклад, алкілуванням або ацилуванням), ВІДПОВІДНИХ сполук, у котрих R4a/R4b або R5a/R5b позначають гідроксил Сполуки формули І, у котрих R2 позначає пдрокси-Сі-С4алкіл, або ВІДПОВІДНІ ВИХІДНІ сполуки в 8-Галогенімідазо[1,2-а]піридини (X позначає галоген) піддають взаємодії з ВІДПОВІДНИМ ЧИНОМ заміщеними р-феніл-р-амшокислотами з використанням у якості каталізатора важкого металу (переважно Pd) з одержанням заміщених амінів, що у свою чергу піддають циклізації ВІДПОВІДНО ДО схеми 4 Замість COOR-групи при необхідності також може бути використана альдегідна група (як була вже зазначена на схемі 4) у формі ацеталю Y позначає Н (гідроген) або захисну групу, що може бути віддалена до або після замикання кільця При використанні в якості вихідного продукту імідазолу, що є відомим або може бути отриманий аналогічним способом, замиканню кільця, яке потрібно здійснити (необов'язково з захистом пдроксигрупи), сприяє присутність енамшо-вой групи (рівновага!) Після введення подвійного зв'язку шляхом окиснення може бути здійснене віднов схемах 1-8, можуть бути отримані з ВІДПОВІДНИХ естерів і альдегидів узвичаєним способом (див WO 94/18199) шляхом відновлення, наприклад, боропдридом натрію або алюмопдридом ЛІТІЮ При необхідності відновлення з одержанням пдрокси-Сі-С4алкільноі групи може бути здійснене одночасно з відновленням кетогрупи в положенні 8 і особливо в положенні 7 (R4a і R4b разом позначають О) Сполуки згідно з винаходом виділяють і очищають добре відомим способом, наприклад, відгонкою розчиннику у вакуумі і перекристалізовуючи отриманий залишок із придатного розчиннику або піддаючи його одному такому з узвичаєних способів очищення, як, наприклад, хроматографія на колонках із використанням придатного носія Солі одержують шляхом розчинення вільної сполуки в придатному розчиннику, наприклад, у такому хлорованому вуглеводні, як метилхлорид або хлороформ, або аліфатичний спирт із низькою молекулярною масою (етанол, ізопропанол), що містить необхідну кислоту, або до якого потім добавляють необхідну кислоту Солі одержують шляхом фільтрації, повторного осадження, осадження з осаджувачем для кислотно-адитивної солі або шляхом випарювання розчинника Отримані солі можуть бути перетворені за допомогою підлужування або підкислювання у ВІЛЬНІ сполуки, що у свою чергу можуть бути перетворені в солі Таким способом фармакологічно неприйнятні солі можуть бути перетворені у фармакологічно прийнятні солі Чисті енантюмери, зокрема, чисті енантюмери формули Г, що є кращим об'єктом винаходу, можуть бути отримані способом, відомим спеціалісту в даній області, наприклад, шляхом енантюселективного синтезу (див , наприклад, схему 3), шляхом хроматографіческого поділу на хіральних розділювальних колонках, шляхом дериватизацм з використанням хіральних допоміжних реагентів, наступного поділу діастереомерів і видалення хіральних допоміжних груп, шляхом одержання солей із хіральними кислотами, наступного розділення солей і виділення необхідної сполуки із солі, або шляхом (фракціонованої) кристалізації з придатного розчиннику Крім того, винахід відноситься до способів і проміжних продуктів способів, описаних у вищена 18 17 61102 ведених схемах, зокрема, до тих проміжних продузаголовку сполуки з Т пл 210-212°С ктів способів, поданих на схемах 1, 2, 3, 4, 5, 6 і 7, 6 9-(2-Хлорфеніл)-7-пдрокси-2 3-диметилщо можуть бути виділені до стадії кристалізації 7 8 9 10-тетрапдроімідазо[1 2-п][1 7]нафтиридин Такі приклади служать для ЦІЛІ подальшої ілюАналогічно способові, описаному в прикладі 5, страції винаходу, але не обмежують його об'єм використовуючи в якості вихідного продукту 9-(2Більш ТОГО, ІНШІ сполуки формули І, спосіб одерхлорфеніл)-2,З-диметил-7,8,9,10жання яких не описаний явно, можуть бути отритетрапдроімгдазо[1,2-п][1,7]нафтиридин-7-он, мані аналогічними способами або способами, віодержують зазначену в заголовку сполуку (вихід домими спеціалісту в даній області, із 73%) із Тпл 150-152°С використанням узвичаєних способів обробки Ско7 9-(2 6-Дихлорфеніл)-7-пдрокси-2 3-диметилрочення хв позначає хвилину(и), год позначає го7 8 9 10-Іетрапдроімідазо[1,2-п][1 7]нафтиридин дину(и), єн позначає енантюмерний надлишок Аналогічно способові, описаному в прикладі 5, Приклади Кінцеві продукти використовуючи в якості вихідного продукту 9-(2,61 2 3-Диметил-9-феніл-7 8 9 10дихлорфеніл)-2,3-диметил-7і8,9|10тетрапдроімшазо[1 2-п][1 7]нафтиридин-7-он тетрапдроімідазо[1,2-п][1,7]нафтиридин-7-он, одеРозчин, що містить 4,5г 2,3-диметил-7-(3ржують зазначену в заголовку сполуку (вихід 72%) феніл-1 -оксо-2-пропеніл)-8із Тпл 155-157°С півалоіламіноімідазо[1,2-а]піридину в ЗОмл дюкса8 9-(2-Трифлуорметилфеніл)-7-пдрокси-2 3на, обробляють 20мл конц, пдрохлоридної кислодиметил-7 8 9 10-тетрапдроімідазо[1 2ти, витримують при температурі дефлегмації проh][1 7]нафтиридин тягом 8год, доводять при охолодженні значення Аналогічно способові, описаному в прикладі 5, рН до 7,0 за допомогою 2Н розчину гідроксиду використовуючи в якості вихідного продукту 9-(2натрію і тричі екстрагують 50 мл етилацетату Об'трифлуорметилфеніл)-2,3-диметил-7,8і9,10єднані екстракти промивають водою, сушать над тетрапдроімідазо[1,2-И][1,7]нафтиридин-7-он, карбонатом калію і концентрують досуха під вакуодержують зазначену в заголовку сполуку (вихід умом Залишок у виді в'язкого масла хроматогра72%) із Тпл 145-147°С фують на силікагелі з використанням у якості елю9 8-Гідрокси-2 3-диметил-9-феніл-7 8 9 10енту суміші етилацетат/петролейний естер (1 1) тетрапдроімідазо[1 2-h][1 7]нафтиридин-7-он Одержують 2,6г зазначеної в заголовку сполуки з Розчин, що містить 500мг 2,3-диметил-7-(2,3Тпл 138-140°С епокси-1 -оксо-3-фенілпропіл)-82 9-(2-Хлорфеніл)-2 З-диметил-7 8 9 10півалоіламшоімідазо[1,2-а]піридину в 5мл безводтетрапдроімідазо[1 2-п][1 7]нафтиридин-7-он ного етанолу, обробляють при інтенсивному переАналогічно способові, описаному в прикладі 1, мішуванні 95мг гідроксиду ЛІТІЮ І ПІСЛЯ перемішувикористовуючи в якості вихідного продукту 7-[3вання протягом 2 год при кімнатній температурі (2-хлорфеніл)-1-оксо-2-пропеніл]-8-півалоіламшоохолоджують до 0°С у льодяній бані Кристали, що 2,3-диметилімідазо[1,2-а]піридин, одержують завипали, відфільтровують під вакуумом і промивазначену в заголовку сполуку (вихід 73%) із Т пл ють невеличкою КІЛЬКІСТЮ холодного етанолу Піс80-82°С ля сушіння в глибокому вакуумі твердий продукт добавляють при кімнатній температурі до 5 мл 3 9-(2 6-Дихлорфеніл)-2 З-диметил-7 8 9 10сульфатної кислоти 90%-ноі МІЦНОСТІ І перемішутетрапдроімідазо[1 2-п][1 7]нафтиридин-7-он ють протягом 1год Потім розчин при охолодженні Аналогічно способові, описаному в прикладі 1, на льоду нейтралізують за допомогою охолоджевикористовуючи в якості вихідного продукту 7-[3ного розчину гідроксиду натрію 40%-ноі МІЦНОСТІ (2,6-дихлорфеніл)-1-оксо-2-пропеніл]-8Осад, що випав при цьому, відфільтровують і супівалошамшо-2,3-диметилімідазо[1,2-а]піридин, шать у вакуумі Одержують 145мг зазначеної в одержують зазначену в заголовку сполуку (вихід заголовку сполуки з Т пл 232-234°С 41%) із Тпл 248-24°С 4 9-(2-ТриФлуорметилфеніл)-2 3-диметил10 7 8-Дипдрокси-2 З-диметил-9-феніл7 8 9 10-тетрапдроімідазо[1 2-п][1 7]нафтиридин-77 8,9 10-тетрапдроімідазоГ1,2-п][1 7]нафтиридин он 700мг 8-пдрокси-2)3-диметил-9-фенілАналогічно способові, описаному в прикладі 1, 7,8і9і10-тетрапдроімідазо[1,2-п][1,7]нафтиридинвикористовуючи в якості вихідного продукту 7-[37-ону суспендують у 15мл метанолу і добавляють (2-трифлуорметилфеніл)-1-оксо-2-пропеніл]-8порціями при кімнатній температурі при перемішупівалоіламшо-2,3-диметилімідазо[1,2-а]піридин, ванні 200мг боропдриду натрію Після перемішуодержують зазначену в заголовку сполуку (вихід вання протягом 2год суміш зливають у ЮОмл льо41%) із Тпл 184-185°С дяної води Осад, що випав, відфільтровують, швидко сушать у вакуумі і перекристалізовують із 5 7-Гідрокси-2 3-диметил-9-феніл-7 8 9 10невеличкої КІЛЬКОСТІ 2-пропанолу Одержують тетрапдроімідазо[1 2-п][1,7]нафтиридин 500мг зазначеної в заголовку сполуки з Т пл 150Суспензію, що містить 1г 2,3-диметил-9-феніл152°С 7,8,9,10-тетрапдроімідазо[1,2-п][1,7]нафтиридин-7ону в 15мл метанолу, обробляють при кімнатній 11 (8R 9R)-2 3-Диметил-8-пдрокси-9-фенілтемпературі 450мг боропдриду натрію у виді неве7 8 9 10-тетрапдроімідазо[1 2-п][1 7]нафтиридин-7личких порцій Жовтуватий розчин, що утворився, он перемішують протягом 2год і потім розбавляють 10,8г (24 ммоля) 2,3-flHMe™>7-[(2S,3R)-2,3-Oльодяною водою Осад, що випав, відфільтровуізопропілиден-З-фенілпропан-1 -он-1 -іл]-8ють під вакуумом і промивають невеличкою КІЛЬКІпівалоіламіноімідазо[1,2-а]піридину (єн > 95%, СТЮ 2-пропанола Одержують 800 мг зазначеної в ВЕРХ із використанням сорбенту типу Daicel 20 19 61102 Chiracei) добавляють протягом 4хв при охолооксо-9-феніл-7 8 9 10-тетрапдроімідазо[1 2дженні на льоду до 50мл сульфатної кислоти 70%h][1 7]нафтиридин ноі МІЦНОСТІ У процесі цього утвориться суспензія, (8R,9R)-8-riflpoKCH-2,3-flHMeTHn-7-OKCO-9що через ЗОхв перетворюється в оранжевий розфеніл-7,8,9,10-тетрапдроімідазо[1,2чин Після завершення додавання льодяну баню їі][1,7]нафтиридин (-|г) розчиняють у 20мл безводвидаляють і суміш перемішують при кімнатній теного хлороформу і добавляють 5г перманганату мпературі Через 50год реакційний розчин добавкалію Після перемішування реакційної суміші проляють до льодяної води, добавляють дихлорметягом 40 днів при кімнатній температурі відфільттан, після чого значення рН суміші доводять до 8 ровують тверді частки Фільтрат ДВІЧІ хроматограза допомогою 6Н розчину гідроксиду натрію і нафують на силікагелі (елюенти сиченого розчину гідрокарбонату натрію Відокредихлорметан/метанол, 13/1), одержуючи 0,07г замлюють органічну фазу Водну фазу ДВІЧІ екстразначеної в заголовку сполуки у виді напівтвердого гують дихлорметаном Органічні фази об'єднують і продукту промивають невеличкою КІЛЬКІСТЮ дистильованої 15 (7R 8R 9R)-3-l~iflpoKCHMe™i-7 8води Потім органічний прошарок сушать над бездипдрокси-2-метил-9-феніл-7 8 910водним сульфатом натрію, фільтрують і конценттетрапдроімідазо[1 2-h][1 7]нафтиридин рують у вакуумі на роторному випарнику Концент0,07г (8R,9R)-3^opMin-8-riflpoKCH-2-MeTHn-7рований залишок хроматографують на силікагелі оксо-9-феніл-7,8,9,10-тетрапдроімідазо[1,2(елюент дихлорметан/метанол, 1001) Основну їі][1,7]нафтиридину розчиняють у 5мл безводного фракцію концентрують і обробляють етилацетаметанолу і добавляють 0,1г боропдриду натрію том, у процесі цього кристалізується зазначена в Суміш перемішують протягом ЗОхв і концентрують заголовку сполука у виді твердої речовини жовтого у вакуумі Маслянистий залишок розподіляють між кольору Цей осад відфільтровують під вакуумом і водою і хлороформом Відокремлюють органічний сушать до постійної ваги у вакуумній сушильній прошарок, сушать над безводним сульфатом нашафі при 50°С У результаті одержують 4,22г трію і концентрують Продукт очищають експрес(57%, єн > 95%, ВЕРХ із використанням сорбенту хроматографією на силікагелі (елюент дихлорметипу Daicel Chiracei) зазначеної в заголовку сполутан/метанол, 9/1), одержуючи 0,05 г зазначеної в ки з Т пл 231-234°С заголовку сполуки у виді напівтвердого продукту 1 Н-ЯМР (CD3OH, 400МГц) d = 1,90 (s, ЗН, 212 (7R 8R 9RJ-2 З-Диметил-7 8-дипдрокси-9СНЗ), 3,87 (dd, J8,9 = 9,5Гц, J8,7 = 8,0Гц, 1Н, 8-Н), феніл-7 8 9 10-тетрапдроішдазо[1 24,45 (d, J9,8= 9,4Гц, 1Н, 9-Н), 4,79 (bs, 2Н, 3-СН2), п][1 7]нафтиридин 5,42 (d, J7 8 = 8,0Гц, 1Н, 7-Н), 7,03 (d, J6,5 = 6,9Гц, 6г (19,52 ммоля) (8R,9R)-2,3-flHMe™>81Н/6-Н), 7,35-7,42 (m, ЗН, 9-Ph), 7,55 (d, J = 7,0Гц, пдрокси-9-феніл-7,8,9,10-тетрапдроімідазо[1,22H, 9-Ph), 7,77 (d, J5,6 = 7,0Гц, 1H, 5-H) п][1,7]нафтиридин-7-ону ( є н > 90%, ВЕРХ із вико16 (7S 8R 9R)-7 8-Ізопропілидендюкси-2 3ристанням сорбенту типу Daicel Chiracei) суспендиметил-9-феніл-7 8 9 10-тетрапдроімідазо[1 2дують у 60мл метанолу і охолоджують до темпеh][1 7]нафтиридин ратури в діапазоні від -5 до ОС у бані метанол-лід При цій температурі шпателем протягом 0,5 год 0,3г (7S,8R,9R)-2,3-flHMe™>7,8-flHnflpoKCH-9добавляють боропдрид натрію (0,81г, 21,47 ммофеніл-7,8,9,10-тетрапдроімідазо[1,2ля) (виділяється газ) Після завершення додаванїі][1,7]нафтиридину розчиняють у 5мл безводного ня суміш перемішують ще протягом Юхв і потім ацетону і Юмл безводного N,Nконцентрують у вакуумі на роторному випарнику диметилформаміду Добавляють 2,2при температурі бані 40°С Отриманий маслянисдиметоксипропан (20мл) і моногідрат паратолуолтий залишок розчиняють у дистильованій воді і сульфоновой кислоти (0,68г) і суміш перемішують тричі екстрагують хлороформом Органічні фази протягом 20год при кімнатній температурі Реакоб'єднують і промивають невеличкою КІЛЬКІСТЮ ційну суміш розподіляють між водою і дихлормеводи, потім сушать із використанням безводного таном Відокремлюють органічний прошарок, просульфату натрію і фільтрують Фільтрат концентмивають водою і сушать над безводним рують у вакуумі на роторному випарнику і випасульфатом натрію Після випарювання розчинника рюють спільно з ацетоном, у процесі цього кристазалишок хроматографують на силікагелі (елюент лізується зазначена в заголовку сполука Осад етилацетат/метанол, 20/1), одержуючи 0,2г зазнавідфільтровують, промивають ацетоном і сушать ченої в заголовку сполуки у виді безбарвних голдо постійної ваги при 50°С у вакуумній сушильній частих кристалів, Т пл 231-232°С (розкл , діетилошафі Одержують 5,15г (85,3%, єн > 90%, ВЕРХ із вий етер) використанням сорбенту типу Daicel Chiracei) заВИХІДНІ продукти значеної в заголовку сполуки у виді безбарвних А 2 3-Диметил-7-(3-феніл-1 -оксо-2-пропеніл)кристалів із Тпл 206-209°С 8-півалоіламшоімідазо[1 2-а]піридин Спосіб А 13 (7S 8R 9RJ-2 З-Диметил-7 8-дипдрокси-9а) 7-Трибутилстанум-23-Диметил-8феніл-7 8 9 10-тетрапдроімідазо[1 2півалоіламшоімідазс[1,2-а]піридин h][1 7]нафтиридин Розчин, що містить 1 г 2,3-диметил-82г маточнику з прикладу 12 хроматографують півапоіламшоімідазо[1,2-а]піридину в 40мл діетина силікагелі (елюент етилацетат/метанол, 19 1), лового етеру, обробляють, додаючи краплями при одержуючи 0,35г зазначеної в заголовку сполуки у -78°С 8мл 1,5М розчину трет-бутиллітію в нвиді масла, що кристалізується після додавання гексані Суміш перемішують протягом 15хв і потім етилацетату Тпл 199-200°С (етилацетат) обробляють 3,3мл хлориду три-н-бутилстануму 14 (8R 9Р)-3-Форміл-8-пдрокси-2-метил-7 22 21 61102 Потім внутрішній температурі дають піднятися до Аналогічно способові А прикладу А і викорискімнатної температури, суміш зливають у льодяну товуючи 2-хлорцинамоілхлорид, одержують заводу і тричі екстрагують етилацетатом, об'єднані значену в заголовку сполуку (вихід 42%) у виді екстракти промивають невеличкою КІЛЬКІСТЮ ВОДИ І пдрохлориду з Т пл 158-160°С сушать над карбонатом калію, розчинник відганяВ 7-[3-(2 3-Дихлорфеиіл)-1 -оксо-2-прропеніл]ють у вакуумі й отримане масло хроматографують 8-півалоіламшо-2,3-диметилімідазо[1 2-а]піридин на силікагелі, використовуючи в якості елюента Аналогічно способові А прикладу А і викориссуміш етилацетат/петролейний естер (1 3) Одертовуючи 2,6-дихлорцинамоілхлорид, одержують жують 1,3г 7-трибутилстанум-2,3-диметил-8зазначену в заголовку сполуку (вихід 51%) у виді півапоіламшоімідазо[1,2-а]піридину у виді в'язкого пдрохлориду з Т пл 218-219°С масла М 7-[3-(2-Трифлуорметилфеніл)-1-оксо-2б) 2бЗ-Диметил-7-(3-феніл-1 -оксо-2-пропеніл)проленіл]-8-півалотамшо-2,3-диметилімідазо[1 28-півалоіламшоімідазо[1,2-а]піридин а]піридин Розчин, що містить 1г 7-трибутилстанум-2,3Аналогічно способові А прикладу А і викорисдиметил-8-півалоіламшоімідазо[1,2-а]піридину в товуючи 2-трифлуорметилцинамоілхлорид, одер15мл тетрапдрофурана, послідовно обробляють жують зазначену в заголовку сполуку (вихід 12%) у 85мг хлориду ЛІТІЮ, 60мг хлориду виді пдрохлориду з Т пл 206-208°С бис(ацетозасобрил)паладію(ІІ) і 340мг цинамоілхД 2 3-Диметил-7-(2 З-епокси-1-оксо-Злориду Суміш перемішують при 60°С протягом фенілпропіл )-8-півалоіламшоімідазо[1 2-а]піридин Згод Після охолодження до 0°С відфільтровують Суміш, що містить 4г 2,3-диметил-7-(3-фенілпід вакуумом жовтуватий осад і промивають неве1-оксо-2-пропеніл)-8-півалоіламшоімідазо[1,2личкою КІЛЬКІСТЮ тетрапдрофурану і діетилового а]піридину в 60мл ацетону і 400мг гідроксиду наетеру Після сушіння у вакуумі одержують 720мг трію в 12мл води, обробляють краплями при інтезазначеної в заголовку сполуки у виді пдрохлоринсивному перемішуванні протягом 20хв при 30°С ду з Т пл 263-265°С (розкл ) 5,6мл водного розчину пероксиду гідрогену 30%Спосіб Б ноі МІЦНОСТІ, що надходить у продаж, Після переа) 2,3-Диметил-7-(3-феніл-1-пдрокси-2мішування при 30°С ще протягом ЗОхв суміш охопропеніл)-8-півалоіламшоімідазо[1,2-а]піридин лоджують до 0°С і обробляють сумішшю, що місДо розчину, що містить 41г 8-півалоіламшотить 60мл води, 13г тіосульфату натрію і ЗОмл 2,3-диметилімідазо[1,2-а]піридину, при інтенсиветилацетату Після розділення фаз водну фазу ному перемішуванні добавляють краплями в атмоекстрагують 20 мл етилацетату Органічні фази сфері захисного газу аргону 320мл наявного в об'єднують, промивають невеличкою КІЛЬКІСТЮ продажу 1,5М розчину трет-бутиллітію в н-пентані води і сушать над карбонатом калію Після відгонтаким чином, щоб температура не перевищувала ки розчинника під вакуумом залишок у виді масла 70°С Після перемішування при -78°С протягом ще сушать у глибокому вакуумі У результаті одержу15хв краплями добавляють розчин, що містить 61г ють 4г зазначеної в заголовку сполуки у виді амокоричного альдегіду в 50мл безводного діетиловорфної маси го етеру (внутрішня температура 99,05%, півалоіламшоімідазо[1,2-а]піридину в 900мл трихВЕРХ із використанням сорбенту типу Daicel лорметану, обробляють 60г двооксиду мангану й Chiracel) у 150мл абсолютного ТГФ Потім швидко інтенсивно перемішують протягом 20год при кім(5хв) краплями добавляють КІЛЬКІСТЬ, ЩО залишинатній температурі, Потім суміш фільтрують, фільлася, при цьому відбувається підвищення темпетрат концентрують під вакуумом досуха й отримаратури до -60°С Після завершення додавання не масло обробляють невеличкою КІЛЬКІСТЮ видаляють охолоджуючу баню Після того, як внудмзопропілового етеру Кристали, що утворилися трішня температура досягає -30°С, добавляють при цьому, відфільтровують під вакуумом У ре20мл метанолу, а після того, як внутрішня темпезультаті одержують 31,5г зазначеної в заголовку ратура стане рівною 0°С, добавляють 200мл диссполуки з Тпл 108-110°С тильованої води Водну фазу відокремлюють за Б 7-[3-(2-Хлорфеніл)-1-оксо-2-пропеніл]-8допомогою ділильної лійки, органічну фазу промипівалоіламшо-2,3-диметилімідазо[1 2-а]піридин 23 вають пять разів дистильованою водою, використовуючи щораз по 100мл, потім органічну фазу тричі екстрагують сульфатною кислотою 10%-ноі МІЦНОСТІ (200мл, 50мл, 50мл) Фази, екстраговані сульфатною кислотою, об'єднують, обробляють 200мл дихлорметану і при охолодженні на льоду й інтенсивному перемішуванні доводять значення рН до 2,3 за допомогою 10Н розчину гідроксиду натрію Відокремлюють органічну фазу Водну фазу екстрагують ЗОмл дихлорметану Об'єднані дихлорметанові фази ДВІЧІ промивають невеличкою КІЛЬКІСТЮ дистильованої води Потім органічну фазу сушать над безводним сульфатом натрію і розчинник цілком відганяють під вакуумом Утвориться продукт у виді масла коричневого кольору, що обробляють 50мл діетилового етеру Після внесення затравки утворяться кристали, що відфільтровують після витримки протягом ночі і промивають діетиловим етером Після сушіння у вакуумі одержують 57,7г (вихід 52,5%, єн > 99, ВЕРХ із використанням сорбенту типу Daicel Chiracel) зазначеної в заголовку сполуки у виді порошку ясножовтого кольору з Т пл 76-80°С Практичне застосування Сполуки формули І і їх солі мають ЦІННІ фармакологічні властивості, що обумовлюють їх практичну придатність Зокрема, вони мають виражену інгібуючу дію у відношенні секреції шлункових кислот і високої захисної активності у відношенні шлунка і кишечнику теплокровних тварин, зокрема, людини У цьому контексті сполуки згідно з винаходом відрізняються високою вибірковістю дії, великою тривалістю дії, дуже гарною активністю у відношенні тонкого кишечнику, відсутністю значних побічних дій і широкого спектру терапевтичної дії У контексті даного винаходу поняття "захист шлунка і кишечнику" означає попередження і лікування шлунково-кишкових хвороб, зокрема, запальних хвороб і ушкоджень шлунково-кишкового тракту (наприклад, таких, як виразки шлунка, виразки дванадцятипалої кишки, гастрити, функціональна гастропатія, викликана підвищеною кислотністю або лікарськими засобами), що можуть бути викликані, наприклад, мікроорганізмами (наприклад, Hehcobacter pylory), бактеріальними токсинами, лікарськими засобами(наприклад, певними протизапальними і противоревматичними засобами), ХІМІЧНИМИ речовинами (наприклад, етанолом), шлунковою кислотою або стресовими ситуаціями З використанням різноманітних моделей, на яких визначали характеристики противиразкової дії і інгібування секреції, зненацька було встановлено, що завдяки своїм ВІДМІННИМ характеристикам сполуки згідно з винаходом сильно перевершують ВІДОМІ в даній області сполуки Беручи до уваги ці характеристики, сполуки формули І і їх фармакологічно прийнятні солі є надзвичайно цінними для застосування в медицині людини і ветеринари, де їх застосовують, зокрема, для лікування і/або профілактики хвороб шлунка і/або кишечнику Тому винахід також відноситься до сполук згідно з винаходом, призначених для застосування при лікуванні і/або профілактиці вищевказаних хвороб До об'єму винаходу також підпадає застосу 61102 24 вання сполук згідно з винаходом для виготовлення лікарських засобів, що застосовують при лікуванні і/або профілактиці вищевказаних хвороб, Крім того, до об'єму винаходу підпадає застосування сполук згідно з винаходом для лікування і/або профілактики вищевказаних хвороб Крім того, винахід також відноситься до лікарських засобів, що містять одну або декілька сполук формули І і/або їх фармакологічно прийнятних солей Лікарські засоби одержують добре відомими способами, що ВІДОМІ спеціалісту в даній області У якості лікарських засобів фармакологічно активні сполуки згідно з винаходом (ДІЮЧІ речовини) застосовують або індивідуально, або переважно в сполученні з придатними фармацевтичними допоміжними речовинами-або ексципієнтами у формі таблеток, таблеток із покриттям, капсул, супозиторієв, бляшок (наприклад, у виді TTS), емульсій, суспензій або розчинів, у яких вміст чинної речовини переважно знаходиться в діапазоні від 0,1 до 95%, і при цьому шляхом ВІДПОВІДНОГО вибору допоміжних речовин і ексципієнтів може бути досягнуте те, що фармацевтична форма для уведення (наприклад, форма з уповільненим вивільненням або форма, призначена для кишечнику) буде точно відповідати характеристикам діючої речовини і/або необхідному початку дії Спеціалісту в даній області на основі його практичного досвіду ВІДОМІ ДОПОМІЖНІ речовини або ексципієнти, що придатні для необхідної фармацевтичної композиції Крім розчинників, гелеутворюючих засобів, основ для супозиторієв, допоміжних речовин для таблеток і інших носив для діючої речовини можна використовувати, наприклад, антюксиданти, диспергатори, емульгатори, пеногасники, коригенти, консерванти, солюбілізатори, барвники або, зокрема, речовини, що посилюють проникаючу спроможність, і комплексоутворюючі засоби, (наприклад, циклодекстрини) ДІЮЧІ речовини можуть вводитися перрально, парентерально або підшкірна У цілому, у медицині людини для досягнення необхідного результату у випадку перорального введення переважно вводять діючу(і) речовину(и) у добовій дозі приблизно від 0,01 до приблизно 20, переважно від 0,05 до 5, зокрема, від 0,1 до 1,5мг/кг маси тіла, при необхідності у виді декількох, переважно від 1 до 4 розділених доз У випадку парентерального введення можуть бути використані аналогічні або (зокрема, у випадку внутрішньовенного введення діючих речовин), як правило, менші дози Оптимальна доза і спосіб уведення діючих речовин, необхідні в кожному випадку, легко можуть бути визначені спеціалістом у даній області на основі його практичного досвіду Якщо сполуки згідно з винаходом і/або їх солі застосовують для лікування вищевказаних хвороб, то фармацевтичні композиції також можуть містити один або декілька фармакологічно активних компонентів з інших фармацевтичних груп Прикладами, що варто згадати, є транквілізатори (наприклад, із групи бензодіа-запшів, наприклад, діазепам), спазмолітичні засоби (наприклад, біетаміверин або камілофін), антихолшерпчні засоби (наприклад, оксифенциклімін або фенкарба 26 25 61102 мід), місцеві анестетики (наприклад, тетракаш або льну активність, що варто згадати, є, наприклад, прокат) і при необхідності також ферменти, вітамезлоцилін, ампицилін, амоксицилін, цефалотин, міни або амінокислоти цефокситин, цефо-таксим, іміпенем, гентаміцин, У цьому зв'язку, зокрема, кращою є комбінація амікацин, еритроміцин, ципрофлоксацин, метронісполук згідно з винаходом з лікарськими засобами, дазол, кларитроміцин, азитроміцин і їх комбінації що інгібують секрецію кислоти, такими, як, напри(наприклад, кларитроміцин 4-метронідазол) клад, Н2-блокатори (наприклад, циметидин, раніФармакологія тидин), інгібітори Н+/К+ - АТФази (наприклад, омеНадзвичайно сильна захисна дія у відношенні празол, пантопразол), або крім того з так шлунка і інгібуюча дія у відношенні секреції шлунназиваними периферичними антихолшерпчними кових кислот сполук згідно з винаходом може бути засобами (такими, як, наприклад, пірензепін, телепоказана в експериментах на тваринах-моделях нзепін), і з антагоністами гастрину з метою адитиСполуки згідно 'з винаходом, тестовані в приведевного або зверхадитивного збільшення основної них нижче експериментах, мали номери, що відподії і/або усунення або зменшення побічних дій, або відають номерам цих сполук у прикладах крім того комбінація з речовинами, що мають анТестування інгібуючої секрецію дії за допомотибактеріальну активність (такими, як, наприклад, гою перфузм шлунка щура У приведеній нижче цефалоспорини, тетрацикліни, пеніциліни, макротаблиці А подані результати in vivo дм сполук згідліди, нітроімідазоли або в альтернативному варіано з винаходом після внутрішньовенного введення нті солі вісмуту) для боротьби з Hehcobacter pylori на стимулюєму пентагастрином секрецію кислоти Компонентами комбінації, що мають антибактеріав підданому перфузм шлунку щура Таблиця А № 5 6 10 12 13 Доза (мкмоли/кг) в в інгібування секреції кислоти (%) 3 3 3 3 3 100 100 100 100 100 Методика Черевну порожнину щурів, підданих анестезії (щур лінії CD, самка, 200-250г, уретан 1,5г/кг в м ), розкривали після трахеотомії шляхом серединного розтину верхньої частини черевної порожнини і перорально вводили і фіксували в стравоході один катетер із ПВХ, а інший уводили через воротар так, щоб КІНЦІ трубки проходили в просвіток шлунка Катетер, що виходить із воротаря, виводили назовні через бічний отвір у правій СТІНЦІ черевної порожнини Після ретельного промивання (приблизно 50ЮОмл) через шлунок безупинно пропускали теплий фізіологічний розчин NaCI при 37°С (0,5мл/хв, рН 6,8-6,9, Braun-Umta І) Для рідини, що виходить, яку у кожному випадку збирали кожні 15хв, визначали значення рН (pH-meter 632, скляний електрод Комп'ютерна верстка О В Кураєв ЕА 147, Ж = 5мм, Metrohm) і шляхом титрування свежовиготовленим 0,01Н розчином NaCI до значення рН, рівного 7 (Dosimat 665, Metrohm) визначали концентрацію НСІ Шлункову секрецію стимулювали шляхом безперервної внутрішньовенної інфузм 1мкг/кг (тобто 1,65мл/г) пентагастрину (ліва стегнова вена) приблизно через ЗОхв після закінчення операції (тобто, після аналізу двох попередніх фракцій) Теетуємі сполуки уводили внутрішньовенне у об'ємах рідини 1мл/кг через бОхв після початку безперервної інфузм пентагастрина Температуру тіла тварин підтримували на постійному рівні 37-38°С за допомогою інфрачервоного опромінення й обігрівальних подушок (автоматичний безперервний контроль за допомогою ректального датчика температури) Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюCompound of tetrahydropyridine
Назва патенту російськоюСоединение тетрагидропиридина
МПК / Мітки
МПК: C07D 471/14
Мітки: сполука, лікарський, тетрагідропіридину, засіб, основі
Код посилання
<a href="https://ua.patents.su/13-61102-spoluka-tetragidropiridinu-ta-likarskijj-zasib-na-osnovi.html" target="_blank" rel="follow" title="База патентів України">Сполука тетрагідропіридину та лікарський засіб на її основі</a>
Попередній патент: Сцинтиляційна речовина (варіанти) та сцинтиляційний хвилевідний елемент
Наступний патент: Спосіб кількісного визначення фосгену
Випадковий патент: Борона для пошарового обробітку грунту