Сполуки 5-(фенілізоксазолілетокси)-триазол-3-іл-заміщеного піридину для лікування неврологічних, психіатричних чи больових розладів
Номер патенту: 92503
Опубліковано: 10.11.2010
Автори: Мінідіс Александер, Венсбо Давід, Профір Вероніка, Арора Джалай, Ерікссон Кароліне, Сінь Тао, Берґстром Пер-Олув, Слассі Абделмалік, Айзаак Метвін, Едвардз Луїз
Формула / Реферат
1. Сполука формули II
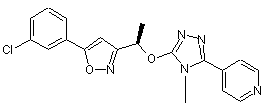 , (II)
, (II)
а також її фармацевтично прийнятні солі, гідрати та/або ізоформи.
2. Сполука за п. 1 у кристалічній формі.
3. Гідрохлорид сполуки за будь-яким з пп. 1, 2.
4. Сульфат сполуки за будь-яким з пп. 1, 2.
5. Сіль, вибрана з :
4-(5-{(1R)-1-[5-(3-хлорфеніл)ізоксазол-3-іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин гідрохлориду та
4-(5-{(1R)-1-[5-(3-хлорфеніл)ізоксазол-3-іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин сульфату.
6. Сполука за будь-яким з пп. 1-5 для застосування у терапії.
7. Фармацевтична композиція, яка містить як активний інгредієнт сполуку за будь-яким з пп. 1-5 разом із фармакологічно та фармацевтично прийнятним носієм.
8. Застосування сполуки за будь-яким з пп. 1-5 або її фармацевтично прийнятної солі, або оптичного ізомеру для виробництва медикаменту для лікування опосередкованого рецептором mGluR5 розладу.
9. Застосування за п. 8, де вказаним розладом є неврологічний розлад.
10. Застосування за п. 8, де вказаним розладом є психіатричний розлад.
11. Застосування за п. 8, де вказаним розладом є шлунково-кишковий розлад.
12. Застосування за п. 8, де вказаним розладом є будь-яка з хвороб: шлунково-стравохідний рефлюкс, хвороба подразненого кишечнику, функціональна диспепсія, кашель, ожиріння, сенільна деменція при хворобі Альцгеймера, індукована СНІД деменція, хвороба Паркінсона, бічний аміотрофічний склероз, хорея Хантингтона, мігрень, епілепсія, шизофренія, депресія, тривожність, гостра тривожність, обсесивно-компульсивний розлад, офтальмологічні розлади, як-то ретинопатії, діабетичні ретинопатії, глаукома, слухові невропатичні розлади, як-то дзвін у вухах, індуковані хемотерапією невропатії, постгерпетична невралгія та тригемінальна невралгія, толерантність, залежність, згубні звички та розлади жадання, нейроеволюційні розлади, охоплюючи уроджений стан з розумовою субнормальністю, аутизм, уроджене слабоумство, шизофренія та синдром Дауна, біль, пов'язаний з мігренню, біль при запаленні, невропатичні больові розлади, як-то діабетичні невропатії, артрит та ревматоїдні хвороби, біль унизу спини, післяоперативний біль, біль, асоційований з різними станами, охоплюючи стенокардію, ниркову коліку або коліку жовчного міхура, менструація, мігрень та подагра; інсульт, травма голови, аноксичні та ішемічні пошкодження, гіпоглікемія, серцево-судинні хвороби та епілепсія.
Текст
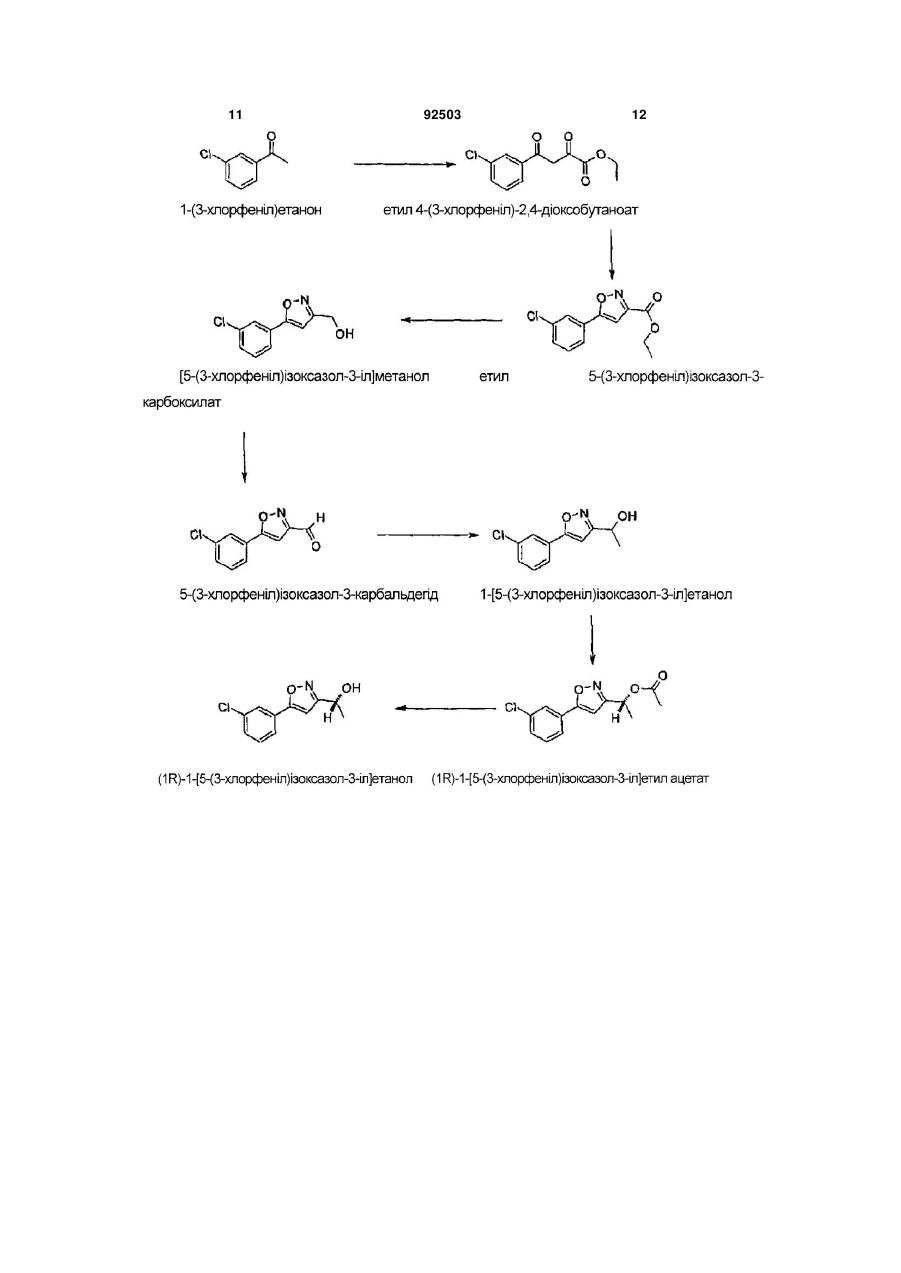
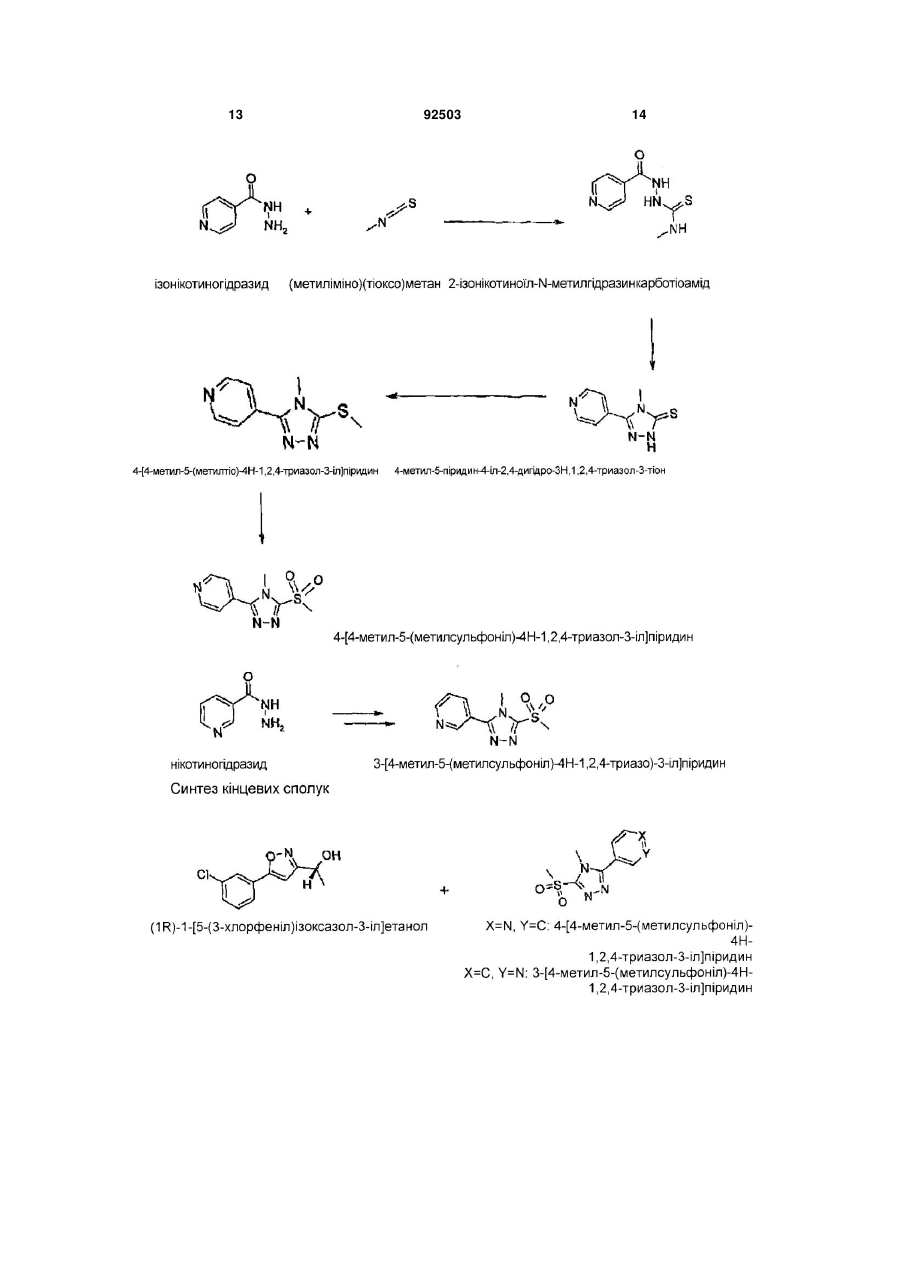
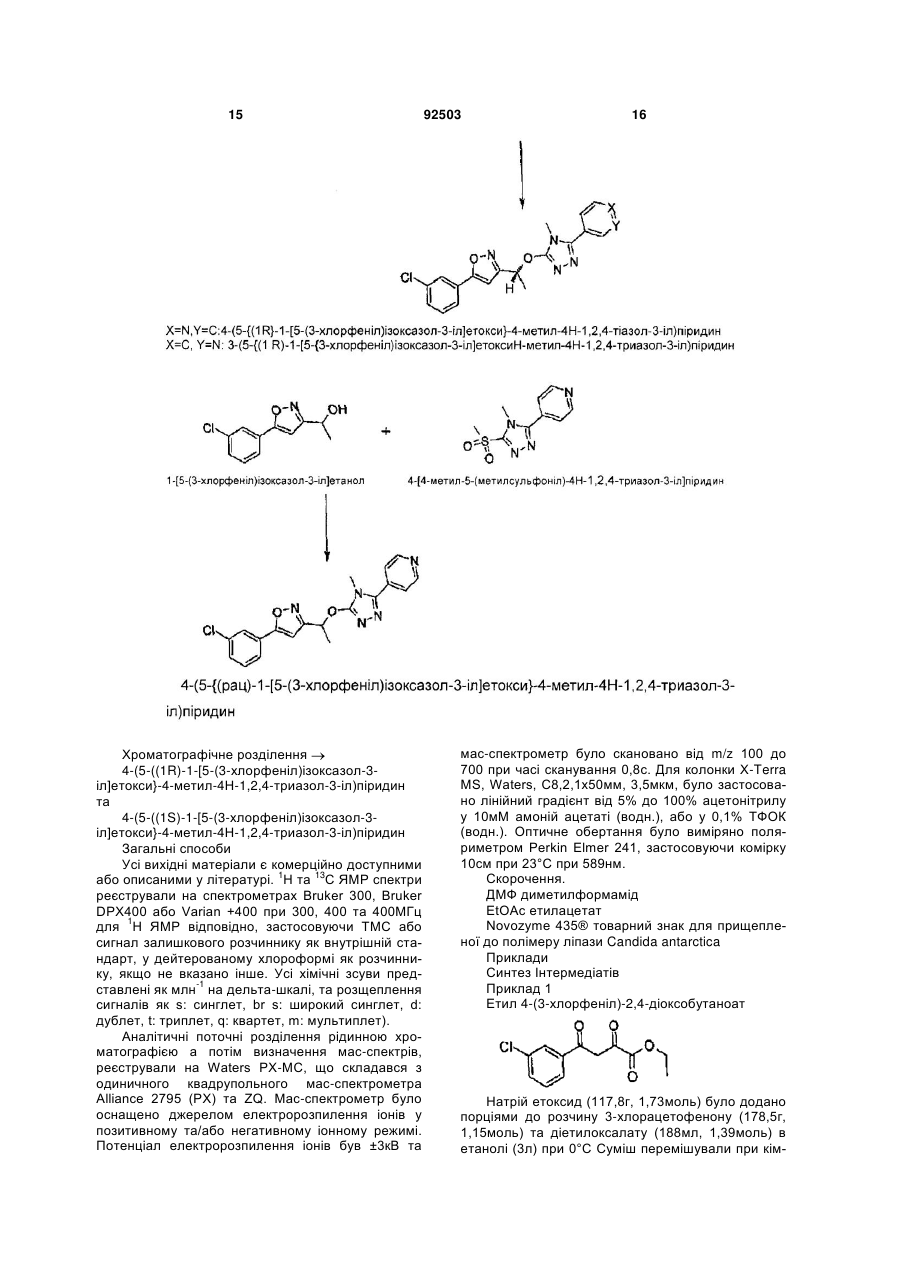
1. Сполука формули II C2 2 (19) 1 3 Заявлений винахід стосується нових сполук, їх застосування у терапії та фармацевтичних композицій, які містять вказані нові сполуки. Глутамат є головним збуджувальним нейротрансмітером у центральній нервовій системі ссавців (ЦНС). Глутамат діє на центральні нейрони приєднанням до рецепторів клітинної поверхні та таким чином їх активуванням. Ці рецептори поділені на два головні класи, іонотропічні та метаботропічні рецептори глутамату, на основі структурних особливостей рецепторних білків, засобів, котрими рецептори переносять сигнали у клітину, та фармакологічного профілю. Метаботропічні рецептори глутамату (mGluR) є сполученими з G-білком рецепторами, що активують різноманітність внутрішньоклітинних вторинних м еседжерних систем після приєднання глутамату. Активування mGluR у непошкоджених нейронах ссавців дає одну або більше з наступних реакцій: активування фосфоліпази С; збільшення гідролізу фосфоінозитид (PI); вивільнення внутрішньоклітинного кальцію; активування фосфоліпази D; активування або інгібування аденіл-циклази; збільшення або зниження утворення циклічного аденозин-монофосфату (цАМФ); активування гуаніліл-циклази; збільшення утворення циклічного гуанозин монофосфату (цГМФ); активування фосфоліпази А2; збільшення вивільнення арахідонової кислоти; та збільшення або зниження керованих потенціалом та лігандами іонних каналів. Schoepp et al, Trends Pharmacol Set 14:13 (1993), Schoepp, Neurochem. Int. 24:439 (1994), Pin et al, Neuropharmacology 34:1 (1995), Bordi та Ugolini, Prog. Neurobiol 59:55 (1999). Молекулярним клонуванням ідентифіковано вісім відмінних підтипів mGluR, названих mGluR1 mGluR8. Nakanishi, Neuron 13:1031 (1994), Pin et al, Neuropharmacology 34:1 (1995), PCMJS2006/036423 Knopfel et al, J. Med. Chem. 38:1417 (1995). Наступна відмінність рецепторів відбувається внаслідок експресії альтернативно сплайсованих форм деяких підтипів mGluR. Pin et al, PNAS 8Р:1033І (1992), Minakami et al, BBRC 199:7136 (1994), JoIy et al, J. Neurosci 75:3970 (1995). Підтипи метаботропічних рецепторів глутамату можуть бути поділеними далі на три групи, Групу І, Групу II, та Групу III mGluR, на основі гомології амінокислотної послідовності, вторинних меседжерних систем, застосовуваних рецепторами, та їх фармакологічних характеристик. Група I mGluR містить mGluR1, mGluR5 та їх альтернативно сплайсовані варіанти. Приєднання агоністів до цих рецепторів призводить до активування фосфоліпази C та наступної мобілізації внутрішньоклітинного кальцію. Неврологічні, психіатричні та больові розлади Спроби пояснення фізіологічної ролі групи I mGluR підказують, що активування цих рецепторів дає неврональне збудження. Різні дослідження продемонстрували, що група 1 агоністів mGluR може давати постсинаптичне збудження при дії на нейрони у гіпокампі, корі головного мозку, мозочку, 92503 4 та таламусі, а також інших регіонах центральної нервової системи. Дані вказують, що це збудження спрямоване на активування постсинаптичного mGluR, але цим також підказано, що відбувається активування пресинаптичного mGluR, призводячи до збільшеного вивільнення нейротрансмітерів. Baskys, Trends Pharmacol Set 15:92 (1992), Schoepp, Neurochem. Int. 24:439 (1994), Pin et al., Neuropharmacology 54:1(1995), Watkins et al, Trends Pharmacol Sci. 15:33 (1994). Метаботропічні рецептори глутамату приймають участь у ряді нормальних процесів у центральній нервовій системі ссавців. Активування mGluR, як показано, є необхідним для індукування гіпокампальної довготермінової потенціації та мозочкової довготермінової депресії. Bashir еt al., Nature 363:347 (1993), Bortolotto et al, Nature 368:740 (1994), Alba et al, Cell 79:365 (1994), Aiba et al., Cell 79:377 (1994). Також продемонстровано роль стосовно активування mGluR у ноцицепції та аналгезії, Meller et al. Neuroreport 4: 879 (1993), Bordi та Ugolini, Brain Res. 871:223 (1999). На додаток, активування mGluR, як підказано, грає модуляторну роль у різноманітності інших нормальних процесів, у тому числі синаптичної трансмісії, неврональному розвитку, апоптичної неврональної загибелі, синаптичної пластичності, просторового навчання, нюхової пам'яті, центрального контролю серцевої активності, пробудження, моторного контролю та контролю вестибулоокулярного рефлексу. Nakanishi, Neuron 73:1031 (1994), Pin et аl, Neuropharmacology 34:1, Knopfel et al, J, Med. Chem. 35:1417(1995). Далі, група І метаботропічних рецепторів глутамату та зокрема mGluR5, як підказано, грає ролі у різноманітності патофізіологічних процесів та розладів, що вражають центральну нервову систему. Це охоплює напад, травму голови, аноксичні та ішемічні пошкодження, гіпоглікемію, епілепсію, нейродегенеративні розлади, як-то хвороба Альцгеймера та біль. Schoepp et al, Trends Pharmacol Sci 14:\3 (1993), Cunningham et al., Life Sci. 54:135 (1994), Hollman et al, Ann. Rev. Neurosci. 77:31 (1994), Vin et al, Neuropharmacology 34:1 (1995), Knopfel et al, J. Med. Chem. 35:1417 (1995), Spooren et al., Trends Pharmacol. Sci. 22:331 (2001), Gasparini et al. Curr. Opin. Pharmacol. 2:43 (2002), Neugebauer Pain 98:1 (2002). Багато з патологій у цих станах, можна вважати, відбувається внаслідок надлишкового індукованого глутаматом збудження нейронів центральної нервової системи. Оскільки група I mGluR показує збільшення опосередкованого глутаматом невронального збудження шляхом постсинаптичних механізмів та посиленого пресинаптичного вивільнення глутамату, їх активування ймовірно сприяє патології. Відповідно, селективні антагоністи групи І рецепторів mGluR могли б бути терапевтично корисними, особливо як нейропротективні засоби, анальгетики або антиконвульсанти. Нещодавніми успіхами стосовно пояснення нейрофізіологічної ролі метаботропічних рецепторів глутамату загалом та групи І зокрема встанов 5 92503 6 лено, що ці рецептори є перспективними цілями для ліків у терапії гострих та хронічних неврологічних та психіатричних розладів та хронічних та гострих больових розладів. Шлунково-кишкові розлади Нижчий стравохідний сфінктер (LES) є схильним до переміжного розслаблення. Як наслідок, рідина зі шлунку може потрапляти у стравохід а також її фармацевтично прийнятних солей, оскільки механічний бар'єр є тимчасово втраченим гідратів та/або ізоформ. у цей час, це далі позначено як "рефлюкс". Ще одним втіленням є фармацевтична компоХвороба шлунково-стравохідний рефлюкс зиція, яка містить як активний інгредієнт терапев(GERD) є найпоширенішою хворобою верхнього тично ефективну кількість сполуки формул I-III, в шлунково-кишкового тракту. Сучасні цілі фармакоасоціації з одним або більше фармацевтично притерапії полягають у зменшенні секреції шлункової йнятними розріджувачами, наповнювачами та/або кислоти або нейтралізуванні кислоти у стравоході. інертними носіями. Головним механізмом рефлюксу вважають гіпотоІнші втілення, які описано більше детально нічність нижчого стравохідного сфінктера. Однак, нижче, стосуються сполук формул I-III для застонаприклад, Holloway & Dent (1990) Gastroenterol сування у терапії, у лікуванні опосередкованих Clin. N. Amer. 19, pp. 517-535, показано, що більmGluR5 розладів, у виробництві медикаменту для шість випадків рефлюксу відбуваються при тимчалікування опосередкованих mGluR5 розладів. совій релаксації нижчого стравохідного сфінктера Наступні втілення стосуються способу ліку(TLESR), тобто релаксація не ініціюється ковтками. вання опосередкованих mGluR5 розладів, який Також показано, що секреція шлункової кислоти полягає у призначенні ссавцю терапевтично ефекзвичайно є нормальною у пацієнтів з GERD. тивної кількості сполуки формул 1-ІII. Нові сполуки згідно із заявленим винаходом, У ще одному втіленні запропоновано спосіб іняк припускають, будуть корисними для інгібування гібування активування рецепторів mGluRR5, який тимчасової релаксації нижчого стравохідного сфіполягає в обробці клітин, що містять вказаний ренктера (TLESR) та таким чином для лікування розцептор, ефективною кількістю сполуки формул І-ІІІ. ладу шлунково-стравохідний рефлюкс (GERD). Сполуки заявленого винаходу є корисними у Внаслідок їх фізіологічного та патофізіологічтерапії, зокрема для лікування неврологічних, псиного значення, існує потреба у нових потужних хіатричних, больових, та шлунково-кишкових розагоністах та антагоністах mGluR, що виявляють ладів. високу селективність стосовно підтипів mGluR, Треба також розуміти спеціалістам, що деякі особливо підтипу групи І рецепторів, найбільш сполуки заявленого винаходу можуть існувати у особливо mGluR5 сольватованій, наприклад, гідратованій, а також Об'єктом заявленого винаходу є отримання несольватованій формах. Треба також розуміти, сполук, що виявляють активність стосовно метащо заявлений винахід стосується усіх таких сольботропічних рецепторів глутамату (mGluR), особватованих форм сполук формули І-ІІІ. ливо рецептору mGluR5. У рамках винаходу є також солі сполук форОдне втілення заявленого винаходу стосуєтьмули І-ІІІ. Загалом, фармацевтично прийнятні солі ся сполуки формули І: сполук заявленого винаходу отримують, застосо а також її фармацевтично прийнятних солей, гідратів, ізоформ та/або енантіомерів. В одному втіленні сполук формули І є R-енантіомер. У ще одному втіленні сполук формули І є S'-енантіомер. Наступне втілення заявленого винаходу стосується сполуки формули II: а також її фармацевтично прийнятних солей, гідратів та/або ізоформ. Ще одне втілення заявленого винаходу стосується сполуки формули III: вуючи стандартні операції, добре відомі у рівні техніки, наприклад, реакцією достатньо основної сполуки, наприклад, алкіл аміну, з придатною кислотою, наприклад, HCI або оцтовою кислотою, отримуючи сіль із фізіологічно прийнятним аніоном. Також можливо створити відповідні солі лужного металу (як-то натрій, калій, або літій) або лужно-земельного металу (як-то кальцій), обробкою сполуки заявленого винаходу, що має відповідно кислотний протон, як-то карбонова кислота або фенол, одним еквівалентом гідроксиду або алкоксиду лужного металу або лужно-земельного металу (як-то етоксид або метоксид), або відповідно основного органічного амін (як-то холін або меглумін) у водному середовищі, а потім звичайними способами очистки. На додаток, солі четвертинного амонію можуть бути отриманими додаванням алкілувальних засобів, наприклад, до нейтральних амінів. В одному втіленні заявленого винаходу, сполуку формули І-ІІІ можна перетворити у фармацевтично прийнятну сіль або сольват, особливо, кислотно-адитивну сіль, як-то гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, метансульфонат чи п 7 92503 8 толуолсульфонат. застосування можна зробити диспергуванням мілУ наступних втіленнях заявленого винаходу, ко подрібненого активного компоненту у воді располуку формули І-ІІІ можна перетворити у фарзом з в'язким матеріалом, як-то природні синтетимацевтично прийнятну сіль або сольват сульфочні камеді, смоли, метилцелюлоза, натрій нової кислоти, 1,2-етандисульфонової кислоти (як карбоксиметилцелюлоза, та інші суспендувальні 1:1 та 2:1), етансульфонової кислоти, нітратної засоби, відомі у рівні техніки фармацевтичних кислоти, 2-мезитиленсульфонової кислоти, 1,5композицій. Типові композиції для перорального нафталіндисульфонової кислоти (як 1:1 та 2:1) чи застосування можуть містити один або більше п-ксилолсульфонової кислоти. барвників, підсолоджувачів, смакових засобів Фармацевтична композиція та/або консервантів. Сполуки заявленого винаходу можна формуЗалежно від режиму застосування, фармацеввати у звичайні фармацевтичні композиції, які містична композиція повинна містити приблизно від тять сполуку формули І-ІІІ, або її фармацевтично 0,05 мас.% (мас.%) до 99 мас.%, або приблизно прийнятну сіль або сольват, в асоціації з фармавід 0,10 мас.% до 50 мас.%, сполуки винаходу, усі цевтично прийнятним носієм або наповнювачем. проценти за масою є на основі загальної маси Фармацевтично прийнятні носії можуть бути тверкомпозиції. дими або рідкими. Тверді форми препаратів охопТерапевтично ефективна кількість для практилюють, але без обмеження, порошки, таблетки, ки заявленого винаходу може бути визначеною дисперсивні гранули, капсули, облатки та супозиспеціалістом, застосовуючи відомі критерії, охопторії. люючи вік, масу та реакцію індивідуального пацієТвердим носієм може бути одна або більше нта, та інтерпретованою у контексті хвороби, яку речовин, котрі можуть також діяти як розріджувачі, лікують або попереджують. смакові засоби, солюбілізатори, змащувальні заМедичне застосування соби, суспендувальн засоби, зв'язуючі, або засоби Сполуки згідно із заявленим винаходом є корозкладання таблеток. Твердим носієм може тарисними у лікуванні станів, асоційованих із збукож бути інкапсулювальний матеріал. джувальним активуванням mGluR5 та для інгібуУ порошках носій є мілко подрібненим твервання невронального пошкодження, викликаного дим матеріалом, котрий є у суміші з мілко подрібзбуджувальним активуванням mGluR5. Сполуки неною сполукою винаходу, або активним компонеможуть бути застосовуваними для виклику інгібунтом. У таблетках активний компонент є змішаним вальної дії mGluR5 у ссавців, у тому числі людини. з носієм, що має необхідні з'єднувальні властивосГрупа І рецепторів mGluR, охоплюючи ті у придатній пропорції та це спресовують до баmGluR5, є сильно експресованими у центральній жаної форми та розміру. та периферійній нервовій системі та в інших ткаДля отримання композицій супозиторію, низьнинах. Таким чином, очікують, що сполуки винахокоплавкий віск, як-то суміш гліцеридів жирних кисду є добре придатними для лікування опосередколот та масла какао, спершу плавлять та активний ваних mGluR5 розладів, як-то гострі та хронічні інгредієнт диспергують в цьому, наприклад, переневрологічні та психіатричні розлади, шлунковомішуванням. Розплавлену гомогенну суміш тоді кишкові розлади, та хронічні та гострі больові розвиливають у форми потрібного розміру та надають лади. змоги охолонути та затверднути. Винахід стосується сполуки формули І-ІІІ, яку Придатні носії охоплюють, але без обмеження, визначено вище, для застосування у терапії. магній карбонат, магній стеарат, тальк, лактозу, Винахід стосується сполуки формули І-ІІІ, яку цукор, пектин, декстрин, крохмаль, трагакант, мевизначено вище, для застосування у лікуванні тилцелюлозу, натрій карбоксиметилцелюлозу, опосередкованих mGluR5 розладів. низькоплавкий віск, масло какао, тощо. Винахід стосується сполуки формули І-ІІІ, яку Термін композиція також охоплює композицію визначено вище, для застосування у лікуванні сеактивного компоненту з інкапсулювальним матерінільної деменції хвороби Альцгеймера, індуковаалом як носієм, що забезпечує капсулу, у котрій ної СНІД деменції, хвороби Паркінсона, бічного активний компонент (з іншими носіями або без аміотрофічного склерозу, хореї Хантингтона, мігних) є оточеним носієм, котрий є таким чином в рені, епілепсії, шизофренії, депресії, тривожності, асоціації з ним. Подібним чином уводять облатки. гострої тривожності, офтальмологічних розладів, Таблетки, порошки, облатки та капсули мояк-то ретинопатій, діабетичних р етинопатій, глаужуть бути застосовуваними як тверді дозовані фокоми, слухових невропатичних розладів, як-то рми, придатні для перорального застосування. дзвону у вухах, індукованих хемотерапією невроРідкі форми композицій охоплюють розчини, патій, постгерпетичної невралгії та тригемінальної суспензії, та емульсії. Наприклад, стерильні водні невралгії, толерантності, згубних звичок, уроджеабо водно-пропіленгліколеві розчини активних ного стану з розумовою субнормальністю, аутизсполук можуть бути рідкими препаратами, придатму, уродженого слабоумства, шизофренії та синдними для парентерального застосування. Рідкі рому Дауна. композиції можуть також бути сформованими у Винахід стосується сполуки формул І-ІІІ, яку водно-поліетиленгліколевому розчині. визначено вище, для застосування у лікуванні боВодні розчини для перорального застосування лю, пов'язаного з мігренню, запального болю, невможуть бути отриманими розчиненням активного ропатичних больових розладів, як-то діабетичні компоненту у воді та додаванням придатних барвневропатії, артрит та ревматоїдні хвороби, болю ників, смакових засобів, стабілізаторів та загусниунизу спини, післяоперативного болю та болю, ків, за потребою. Водні суспензії для перорального асоційованого з різними станами, охоплюючи рак, 9 92503 10 стенокардію, ниркову коліку або коліку жовчного ніж 3 тижні або як кашель, що продовжується доміхура, менструацію, мігрень та подагру. вше, ніж 2 місяці. Термін "гострий кашель" є також Винахід стосується сполуки формули І-ІІІ, яку визначеним згідно з вищенаведеним посиланням визначено вище, для застосування у лікуванні іняк кашель, що продовжується менше, ніж 8 тижнів. сульту, травми голови, аноксичного та ішемічного Сполуки формули І-ІІІ вище є корисними для пошкодження, гіпоглікемії, серцево-судинних хволікування або попередження ожиріння або надлироб та епілепсії. шкової ваги, (наприклад, стимулювання втрати Заявлений винахід стосується також застосуваги та підтримання втрати ваги), попередження вання сполуки формули І-ІІІ, яку визначено вище, у або скасування збільшення ваги (наприклад, пригвиробництві медикаменту для лікування опосеренічення індукованої лікуванням або викликаної дкованих групи І рецепторів mGluR5 розладів та відмовою від паління), для модуляції апетиту будь-якого розладу з перерахованих вище. та/або насичення, розлади споживання їжі (наприОдне втілення винаходу стосується застосуклад, обжерливість, втрата апетиту, булімія та вання сполуки формул І-ІІІ у лікуванні шлунковонав'язлива схильність) та жадання (до ліків, тютюкишкових розладів. ну, алкоголю, будь-якого харчувального макроеЩе одне втілення винаходу стосується застолементу, що стимулює апетит або неістотних харсування сполуки формули І-ІІІ для виробництва чових продуктів). медикаменту для інгібування тимчасової релаксаВинахід також стосується способу лікування ції нижчого стравохідного сфінктера, для лікування опосередкованих mGluR5 розладів та будь-якого GERD, для попередження шлунково-стравохідного розладу з перерахованих вище, у пацієнта, який рефлюксу, для лікування регургітації, для лікуванпотерпає від вказаного стану, або при ризику його ня астми, для лікування ларингіту, для лікування виникнення, котрий полягає у застосуванні до пахвороби легень, для терапії затримки росту, для цієнта ефективної кількості сполуки формули І-ІІІ, лікування хвороби подразненого кишечнику (IBS) яку визначено вище. та для лікування функціональної диспепсії (FD). Доза, необхідна для терапевтичного або проВираз "TLESR", тимчасова релаксація нижчого філактичного лікування конкретного розладу постравохідного сфінктера, визначено тут згідно із винна неодмінно варіювати залежно від лікованого Mittal, R.K., Holloway, R.H., Penagini, R., Blackshaw, хазяїна, шляху застосування та від суворості хвоL.A., Dent, J., 1995; Transient lower esophageal роби, яку лікують. sphincter relaxation. Gastroenterology 109, pp. 601У контексті наданого опису, термін "терапія" та 610. "лікування" охоплює попередження або профілакВираз "рефлюкс" визначено тут як здатність тик, якщо конкретно не вказано інше. Терміни "терідини зі шлунку потрапляти у стравохід, оскільки рапевтичний" та "терапевтично" слід розуміти відмеханічний бар'єр є тимчасово втраченим у цей повідно. час. У наданому описі, якщо не вказано інше, терВираз "GERD", хвороба шлунковомін "антагоніст" та "інгібітор" означають сполуку, стравохідний рефлюкс, визначено тут згідно з van що будь-яким чином, частково або повністю, блоHeerwarden, М.А., Smout A.J.P.M., 2000; Diagnosis кує шлях передачі, даючи реакцію на ліганд. of reflux disease. Bailliere's Clin. Gastroenterol. 14, Термін "розлад", якщо не вказано інше, ознаpp. 759-774. чає будь-який стан та хворобу, асоційовані з актиНаступне втілення винаходу стосується застовністю метаботропічного рецептору глутамату. сування сполуки формул І-ІІІ для виробництва Немедичне застосування медикаменту для лікування кашлю. В одному втіНа додаток до їх застосування у терапії сполуленні кашель, що треба лікувати, є хронічним каки формули І-ІІІ, а також солі та гідрати таких спошлем. У наступному втіленні кашель, що треба лук, є корисними як фармакологічні засоби у розлікувати, є гострим кашлем. Термін хронічний каробці та стандартизації in vitro та in vivo тестшель визначають згідно із Kardos P et al (The систем для оцінки дії пов'язаної з інгібіторами German Respiratory Society's Guideline for the mGluR активності у лабораторних тварин, як-то Diagnosis and Treatment of Patients with Acute and коти, собаки, кролі, мавпи, щури та миші, як частиChronic Cough Medizinische Klinik 2004;99(8):468ни дослідження нових терапевтичних засобів. 75) як кашель, що продовжується довше, ніж 8 Способи отримання тижнів. Однак, хронічний кашель може також бути Синтез інтермедіатів визначеним як кашель, що продовжується довше, 11 92503 12 13 92503 14 15 Хроматографічне розділення 4-(5-((1R)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин та 4-(5-((1S)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин Загальні cпособи Усі вихідні матеріали є комерційно доступними або описаними у літературі. 1H та 13C ЯМР спектри реєстрували на спектрометрах Bruker 300, Bruker DPX400 або Varian +400 при 300, 400 та 400МГц для 1H ЯМР відповідно, застосовуючи TMC або сигнал залишкового розчиннику як внутрішній стандарт, у дейтерованому хлороформі як розчиннику, якщо не вказано інше. Усі хімічні зсуви представлені як млн-1 на дельта-шкалі, та розщеплення сигналів як s: синглет, br s: широкий синглет, d: дублет, t: триплет, q: квартет, m: мультиплет). Аналітичні поточні розділення рідинною хроматографією а потім визначення мас-спектрів, реєстрували на Waters РХ-МС, що складався з одиничного квадрупольного мас-спектрометра Alliance 2795 (PX) та ZQ. Мас-спектрометр було оснащено джерелом електророзпилення іонів у позитивному та/або негативному іонному режимі. Потенціал електророзпилення іонів був ±3кВ та 92503 16 мас-спектрометр було скановано від m/z 100 до 700 при часі сканування 0,8с. Для колонки X-Terra MS, Waters, С8,2,1х50мм, 3,5мкм, було застосовано лінійний градієнт від 5% до 100% ацетонітрилу у 10мМ амоній ацетаті (водн.), або у 0,1% ТФОК (водн.). Оптичне обертання було виміряно поляриметром Perkin Elmer 241, застосовуючи комірку 10см при 23°С при 589нм. Скорочення. ДМФ диметилформамід EtOAc етилацетат Novozyme 435® товарний знак для прищепленої до полімеру ліпази Candida antarctica Приклади Синтез Інтермедіатів Приклад 1 Етил 4-(3-хлорфеніл)-2,4-діоксобутаноат Натрій етоксид (117,8г, 1,73моль) було додано порціями до розчину 3-хлорацетофенону (178,5г, 1,15моль) та діетилоксалату (188мл, 1,39моль) в етанолі (3л) при 0°C Суміш перемішували при кім 17 92503 18 натній температурі протягом 1 години та тоді гріли 1Н), 8,08 (br s,1H), 7,95 (m, 1Н), 7,61 (m, 3Н). MC при 70°С протягом 2 годин. Після охолодження, (М++1) = 208. суміш було підкислено 3М гідрохлоридною кислоПриклад 5 тою (рН~3). Розчинник було відігнано та до суміші 1 -[5-(3-хлорфеніл)ізооксазол-3-іл] етанол було додано EtOAc. Органічний шар було промито водою та насиченим розсолом. Розчинник було відігнано, отримуючи сирий заголовний продукт, котрий було застосовувано безпосередньо на наступному етапі. MC (M+-1) = 253. Приклад 2 MeMgBr (3М у ТГФ, 313мл, 937,2ммоль) було Етил 5-(3-хлорфеніл)ізоксазол-3-карбоксилат додано краплями при 0°С до 5-(3хлорфеніл)ізоксазол-3-карбальдегіду (177г, 252ммоль) у ТГФ (3л). Суміші було надано змоги досягти кімнатної температури, її перемішували при цій температурі протягом 3 годин та тоді її було погашено водним амоній хлоридом при 0°С та розчинник було відігнано. До залишку було доРозчин сирого етил 4-(3-хлорфеніл)-2,4дано EtOAc та профільтровано через шар броундіоксобутаноату (макс 294г, 1,16моль) та гідроксимілериту. Органічний шар було промито водою, ламін гідрохлориду (120,4г, 1,73моль) в етанолі насиченим розсолом та концентровано. Сирий (4л) гріли при 80°С протягом 4 годин. Після охолопродукт було очищено флеш-колонковою хроматодження (протягом ночі) приблизно до 5-10°С, суграфією на силікагелі, застосовуючи гептан/ЕtOАс міш було профільтровано, промито холодним ета= 80:20, отримуючи заголовну сполуку (70г, 37%) 1 нолом та висушено у вакуумі, отримуючи як біло-жовтий твердий матеріал. H ЯМР: 7,73 (m, 1 заголовну сполуку (214,5г, 74%). H ЯМР: 7,82 (s, 1H), 7,63 (m, 1Н), 7,38 (m, 2Н), 6,57 (s, 1H), 5,07 (q, 1H), 7,72 (m, 1H), 7,47 (m, 2H), 4,03 (s, 3Н), MC 1Н), 2,44 (s, 1H), 1,59 (d, 3H). (М++1) = 252. Приклад 6 Приклад 3 (1R)-1-[5-(3-хлорфеніл)ізоксазол-3[5-(3-хлорфеніл)ізоксазол-3-іл]метанол іл]етилацетат Натрій борогідрид (96,7г, 2,6моль) було повільно додано до розчину етил 5-(3хлорфеніл)ізоксазол-3-карбоксилату (214,5г, 0,85моль) у метанолі (2,5л) при 0°C. Реакційну суміш гріли при 50°С протягом 2 годин та її було погашено EtOAc при кімнатній температурі. Більшість розчиннику було відігнано та до сирого залишку було додано EtOAc. Органічний шар було промито водою, насиченим розсолом та концентровано, отримуючи заголовну сполуку, котру було застосовувано безпосередньо на наступному етапі. MC (М++1) = 210. Приклад 4 5-(3-хлорфеніл)ізоксазол-3-карбальдегід [5-(3-хлорфеніл)ізоксазол-3-іл]метанол (178,6г, 852ммоль) у дихлорметані (2л) було краплями додано до піридиній хлорхромату (400г, 1,86моль) у дихлорметані (2л). Утворену густу суспензію перемішували протягом ночі при кімнатній температурі. Густу суспензію було профільтровано через броунмілерит та фільтрат було відігнано. До залишкового розчину було додано EtOAc. Органічний шар було промито водою, насиченим розсолом та концентровано, отримуючи сиру заголовну сполуку, котру було застосовувано безпосередньо на наступному етапі. 1H ЯМР (DMSO-d6): 10,13 (s, 1-[5-(3-хлорфеніл)ізоксазол-3-іл]етанол (106,5г, 476ммоль) та Novozyme 435® (13г) переносять під Ar у сухий толуол (1,5л). Після додавання вінілацетату (66мл, 716 ммоль) реакція перебігала при кімнатній температурі протягом ночі, а потім проводили фільтрування через броунмілерит та промивання Д ХМ. Розчинник було випарено у вакуумі та сирий продукт було піддано колонковій хроматографії на силікагелі, застосовуючи суміш дихлорметан/метанол 20:1, отримуючи заголовну сполуку (50г, 47%). 1H ЯМР: 7,76 (m, 1Н), 7,65 (m, 1Н), 7,41 (m, 2Н), 6,54 (s, 1Н), 6,07 (q, 1Н), 2,13 (s, 3Н), 1,66 (d, 3Н). PX-MC (М++1) = 266. Приклад 7 (1R)-1-[5-(3-хлорфеніл)ізоксазол-3-іл]етанол (1R)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етилацетат (56г, 211ммоль) та літій гідроксид моногідрат (10,6г, 253ммоль) були змішаними з ТГФ/Вода (7/5,1,2л) та це перемішували при кімнатній температурі протягом ночі. Зменшення об'єму суміші у вакуумі до приблизно 1/2, а потім розведення розсолом, екстракція етером та тоді сушка магній сульфатом та у вакуумі концентрація дали сирий продукт. Сирий продукт було очищено флеш-колонковою хроматографією на силікагелі, застосовуючи гептан/ЕtOАс - 70:30, отримуючи 19 92503 20 заголовну сполуку (40г, 85%). 1H ЯМР: 7,73 (m, тримати температуру між 10 та 15°С. Ще одну 1Н), 7,63 (m, 1Н), 7,38 (m, 2 H), 6,57 (s, 1Н), 5,07 (q, порцію води (50мл) було тоді додано та темпера1Н), 2,44 (s, 1H), 1,59 (d, 3H). турі було надано змоги досягти 21-24°С. Після ще 2 годин ацетон було відігнано з реакційної суміші у вакуумі (водяну баню тримали при 30°С). Ще одну порцію води (750мл) було тоді додано перед охолодженням (17 до 18°С) та збиранням утвореного осаду фільтруванням. Цей твердий матеріал було тоді промито водою (2x1л) перед сушкою при 100мбар під обережним струмом повітря протягом 3 діб, отримуючи 235г заголовної сполуки як білий Приклад 8 порошок. 1H ЯМР (DMSO-d6): 2,7 (s, 3H), 3,6 (s, 2-Ізонікотиноїл-JV-метилгідразинкарботіоамід 3H), 7,7 (m, 2H), 8,8 (d, 2H). До обережно нагрітої (35°С) суспензії ізонікоПриклад 11 тиногідразиду (435г) в ізопропіловому спирті (6,0л) 4-[4-Метил-5-(метилсульфоніл)-4Н-1,2,4при механічному перемішуванні було додано (метриазол-3-іл]піридин тиліміно)(тіоксо)метан (230г) кількома невеликими порціями. Після повного додавання реакційну суміш гріли (70°С) протягом 6 годин з додатковим додаванням ізопропілового спирту (600мл) після 30 хвилин. Після охолодження (льодяна баня) реакційної При механічному перемішуванні до розчину 4суміші до 17°С, отриманий осад було відфільтро[4-метил-5-(метилтіо)-4Н-1,2,4-триазол-3вано та промито ізопропіловим спиртом (1,0л). іл]піридину (228г) з попереднього етапу у суміші Цей твердий матеріал було тоді висушено на повіводи (1,15л) та оцтової кислоти (1,15л), було дотрі протягом ночі, отримуючи 615г заголовної сподано порціями при охолодженні калій перманганат луки як білий порошок. (234г), при такій швидкості, щоб тримати темпераПриклад 9 туру 12-17°С (приблизно 45 хвилин). Реакційну 4-Метил-5-піридин-4-іл-2,4-дигідро-3Н-1,2,4суміш тоді перемішували при кімнатній температутриазол-3-тіон рі протягом 4 годин перед охолодженням на льо До суспензії 2-ізонікотиноїл-Nметилгідразинкарботіоамід (610г) у воді (5,0л) при механічному перемішуванні було додано натрій гідрокарбонат (390г) при кімнатній температурі. Реакційну суміш далі повільно гріли до 70°С протягом 2 годин, та тримали при цій температурі протягом ще 3,5 годин перед охолодженням (льодяна баня) до 17°С, а потім доводили рН до 3 повільним додаванням (протягом 90 хвилин) концентрованої гідрохлоридної кислоти (приблизно 470мл). Наступне фільтрування реакційної суміші, а потім промивання зібраного твердого матеріалу розведеною гідрохлоридною кислотою (0,1Н, 2х1,0л), дали вологий шар на фільтрі, який було висушено при 100мбар під обережним струмом повітря протягом 1,5 доби, отримуючи 544г заголовної сполуки. Приклад 10 4-[4-Метил-5-(метилтіо)-4Н-1,2,4-триазол-3іл]піридин До суспензії 4-метил-5-піридин-4-іл-2,4дигідро-3Н-1,2,4-триазол-3-тіону (267г) та метилйодиду (197,7г) при механічному перемішуванні та охолодженні (9°С) в ацетоні (2,6л), було додано розчин натрій гідроксиду (54г у 600мл води) при такій швидкості (приблизно 20мл/хвилин), щоб дяній бані протягом додавання розчину натрій гідроксиду (5H) протягом 2,5 годин до рН приблизно до 10. Dicalite® (100г) та хлороформ (1,6л) було тоді додано до реакційної суміші перед фільтруванням. Органічну фазу було відділено від фільтрату та водну фазу було екстраговано хлороформом (2x1л). Шар на фільтрі було екстраговано двічі хлороформом (2x1,5л). Комбіновані органічні фази були висушеними магній сульфатом, профільтрованими та концентрованими у вакуумі отримуючи 158г заголовної сполуки як білий порошок. Ще одну партію (78г, білий порошок) було отримано екстракцією шару на фільтрі хлороформом (2х2л) та концентрацією цього розчину у вакуумі. 'H ЯМР (DMSO-d6): 3,6 (s, 3H), 3,9 (s, 3H), 7,8 (s, 2H), 8,8 (s, 2Н). Приклад 12 3-[4-метил-5-(метилсульфоніл)-4Н-1,2,4триазол-3-іл]піридин Заголовну сполуку було отримано аналогічно 4-[4-метил-5-(метилсульфоніл)-4Н-1,2,4-триазол-3іл]піридину, як описано тут, за відповідною послідовністю з відповідних етапів, виходячи від нікотиногідразиду замість ізонікотиногідразиду. 'H ЯМР: 3,59 (s, 3Н), 3,99 (s, 3Н), 7,52 (m, 1Н), 8,02 (dt, 1Н), 8,83 (dd, 1Н), 8,91 (m, 1Н). Синтез кінцевих сполук Приклад 13 3-(5-((1R)-[5-(3-хлорфеніл)ізоксазол-3іл]стокси]-4-метил-4Н-1,2,4-триазол-3-іл)піридин (1R)-1-[5-(3-хлорфеніл)ізоксазол-3-іл]етанол 21 92503 22 (5,40г, 24,1ммоль) було розчинено у ДМФ (45мл). що елюється першим. До цього були доданими 3-[4-метил-5Спосіб 2: Заголовну сполуку було отримано (метилсульфоніл)-4Н-1,2,4-триазол-3-іл]піридин аналогічно 3-(5-((1R)-1-[5-(3-хлорфеніл)ізоксазол(5,75г, 24,1ммоль) та цезій карбонат (10,1г, 3-іл]етокси}-4-метил-4Н-1,2,4-триазол-331,4ммоль). Після перемішування протягом ночі іл)піридину сполученням (1R)4-[5-(3при 60°С, було додано воду. Суміш було екстрагохлорфеніл)ізоксазол-3-іл]етанолу з 4-[4-метил-5вано дихлорметаном, а потім органічний шар кон(метилсульфоніл)-4Н-1,2,4-триазол-3центровано у вакуумі, отримуючи сирий матеріал, іл]піридином, застосовуючи цезій карбонат у ДМФ. 1 котрий було очищено колонковою хроматографією H ЯМР (DMSO-d6)'. 8,73 (m, 2Н), 7,97 (br. s, 1Н), на силікагелі, застосовуючи дихлорметан/метанол 7,85 (m, 1Н), 7,74 (m, 2Н), 7,58 (m, 2Н), 7,39 (s, 1Н), = 98/2, отримуючи заголовну сполуку (7,10г, 77%). 6,20 (q, 1Н), 3,60 (s, 3Н), 1,81 (d, 3Н). 1 H ЯМР: 8,90 (d, 1Н), 8,72 (m, 1Н), 8,04 (dt, 1Н), [а]DRТ(5,827g/л, CDCI3) = -48,567° 7,76 (bs, 1Н), 7,66 (m, 1Н), 7,45 (m, 1Н), 7,40 (m, Приклад 16 2Н), 6,73 (s, 1Н), 6,35 (q, 1Н), 3,57 (s, 3Н), 1,93 (d, 4-(5-((15)-1-[5-(3-хлорфеніл)ізоксазол-33Н). 1H ЯМР (DMSO-d6): 8,90 (d, 1Н), 8,71 (dd, 1Н), іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин 8,13 (dt, 1Н), 7,99 (s, 1Н), 7,86 (m, 1Н), 7,58 (m, 3Н), 7,40 (s, 1Н), 6,19 (q, 1Н), 3,54 (s, 3Н), 1,81 (d, 3Н). PX-MC (М++1) = 382. [a]DRT(2,92г/л, CDCI3)= 46,575° Приклад 14 4-(5-{(рац)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин 1-[5-(3-хлорфеніл)ізоксазол-3-іл]етанол (63,4мг, 0,28ммоль), ДМФ та натрій гідрид (60% дисперсія в оливі, 15,1мг, 0,38ммоль) були змішаними під інертною атмосферою та це перемішували при кімнатній температурі протягом 1 години, а потім додавали 4-[4-метил-5-(метилсульфоніл)4Н-1,2,4-триазол-3-іл]піридин (45мг, 0,19ммоль). Після перемішування при 80°C протягом 24h, суміш було охолоджено до кімнатної температури, розведено EtOAc та промито водою та розсолом. Органічну фазу було висушено натрій сульфатом, профільтровано та концентровано у вакуумі. Сирий залишок було очищено колонковою хроматографією на силікагелі, застосовуючи 5% метанол у EtOAc для виділення заголовної сполуки (11,7мг). 'Н-ЯМР: 8,81 (bs, 2Н), 7,77 (s, 1Н), 7,67 (m, 3Н), 7,42 (m, 2Н), 6,73 (s, 1Н), 6,36 (q, 1Н), 3,62 (s, 3Н), 1,94 (d, 3Н). Приклад 15 4-(5-((1,2)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин Спосіб 1: Розділенням препаративною хіральною ВЕРХ 4-(5-{(рац)-1-[5-(3-хлорфеніл)ізоксазол3-іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин на колонці chiralpak AD з ізопропанолом як елюент, отримуючи заголовну сполук як енантіомер, Заголовну сполуку було виділено як ту, що елюється другим енантіомером у розділенні препаративною хіральною ВЕРХ, як описано у прикладі 4-(5-((1R)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридину (спосіб 1). 'Н-ЯМР: 8,81 (bs, 2H), 7,77 (s, 1Н), 7,67 (m, 3Н), 7,42 (m, 2Н), 6,73 (s, 1Н), 6,36 (q, 1Н), 3,62 (s, 3Н), 1,94 (d, 3Н). Приклад 17 4-(5-((1R)-1-[5-(3-хлорфеніл)ізоксазол-3іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин гідрохлорид Заголовну сіль було отримано додаванням 10мкл 32% водного розчину HCI двома порціями до прозорого розчину 35мг вільної основи 4-(5((1R)-1-[5-(3-xлopфeнiл)iзoкcaзoл-3-іл]етокси}-4метил-4Н-1,2,4-триазол-3-іл)піридину у 500мкл етанолу при 50°С. Густу суспензію було охолоджено до 10°С та її тримали протягом ночі з перемішуванням перед тим, як сіль було відфільтровано, промито 500мкл етанолу та висушено при кімнатній температурі під вакуумом. Сіль була кристалічною, мала чітку температуру плавлення та мала збільшене поглинання вологи при 90-95% відносної вологості. Заголовну сіль було вироблено подібним шляхом в етанолі, 2-пропанолі та етилацетаті та також у масштабі 1г в етанолі. Усі партії, продукували ту ж кристалічну модифікацію, хоча вміст аморфного матеріалу був трохи вищим у деяких партіях. Точка плавлення була від 150°C до 160°С. Сіль, вироблену у масштабі 1г з етанолу далі досліджували на її власну розчинність та порівнювали з вільною основою 4-(5-((1R)-1-[5-(3хлорфеніл)ізоксазол-3-іл]етокси}-4-метил-4Н-1,2,4триазол-3-іл)піридину. Сіль мала у 1000 разів вищу власну розчинність порівняно з вільною основою. Розчинність основи та солі були виміряними низькооб'ємним способом обертового диску. Диски були спресованими з чистої сполуки та їх центрально монтували у тримач диску із відкритою площею 0,07см2. Тримач диску обертали при 23 92503 24 500об/хвил зануреним у 50мл фосфатного буферу замінюють свіжим буфером для аналізу. FLIPRUSP з рН 6,8 при 37°С. Сполуку було проаналізоексперименти проводять, застосовуючи лазерну вано УФ-спектрофотометром із проточною кювеустановку 0,800W та частоту зйомки камерою 0,4 с тою та перистальтичним насосом з безперервною CCD з довжиною хвилі збудження та емісії 488нм циркуляцією. та 562нм, відповідно. Кожний експеримент ініціюПриклад 18 ють 160мкл буферу у кожній лунці планшету для 4-(5-((1R)-1-[5-(3-хлорфеніл)ізоксазол-3клітин. Додавання 40мкл з планшету антагоністу іл]етокси}-4-метил-4Н-1,2,4-триазол-3-іл)піридин супроводжували додаванням 50мкл з планшету сульфат агоністу. Інтервал 90с відділяє додавання антагоМаслянисту сіль було вироблено випарюванністу та агоністу. Флуоресцентний сигнал є реєстням прозорого розчину, отриманого змішуванням рують 50 разів при інтервалах 1с, а потім 3 при 500мкл води із 33мг вільної основи 4-(5-((1R)-1-[5інтервалах 5с негайно після кожного з двох дода(3-хлорфеніл)ізоксазол-3-іл]етокси}-4-метил-4Нвань. Реакції вимірюють як різницю між висотою 1,2,4-триазол-3-іл)піридину, 500мкл метанолу та піку реакції на агоніст, мінус фонову флуоресцен7мкл 98% сульфатної кислоти. Заголовну сіль буцію. Визначення IK50 роблять, застосовуючи проло вироблено перекристалізацією маслянистої граму підгонки методом найменших квадратів. солі у 500мкл етанолу. ІР3-Аналіз Заголовна сіль була кристалічною з суттєвим Додатковий функціональний аналіз mGluR5d є вмістом аморфного матеріалу, вона не мала чіткої описаним у WO97/05252 та має основою перетвоточки плавлення та переходила в рідкий стан при рення фосфатидилінозитолу. Активування рецеп60-70% відносної вологості. тору стимулює активність фосфоліпази C та призЗаголовну сіль було знов вироблено додаванводить до збільшеного утворення інозитол 1,4,5ням трьох порцій 5мкл концентрованої сульфатної трифосфату (IP3). кислоти (98%) протягом 1,5 годин до прозорого GHEK, що стабільно експресують mGluR5d розчину 66-68мг вільної основи 4-(5-((1R)-1-[5-(3людини засівають на 24-лункові покриті полi-Lхлорфеніл)ізоксазол-3-іл]етокси}-4-метил-4Н-1,2,4лізином планшети при 40x104 клітин/комірку у сетриазол-3-іл)піридину у 1мл 2-пропанолу або 1мл редовищі, що містить 1мкКi/комірку [3Н]міоетанолу при 68°C. Сіль, вироблена з етанолу, маінозитол. Клітини були інкубованими протягом ночі ла точку плавлення 128°С хоча і переходила в (16 годин), тоді промитими три рази та інкубоварідкий стан при 70-80% відносної вологості. ними протягом 1 години при 37°С у буферованому Біологічна оцінка ГЕПЕС фізіологічному розчині (146мМ NaCI, Функціональна оцінка антагонізму mGluR5 у 4,2мМ КСІ, 0,5мМ MgCI2, 0,1% глюкози, 20мМ ГЕлініях клітин, що експресують mGluR5D ПЕС, рН 7,4), доповненому 1 одиниц/мл глутаматВластивості сполук винаходу можна аналізупіруват-трансаміназ та 2мМ піруват. Клітини провати, застосовуючи стандартні аналізи на фармамивають раз у буферованому ГЕПЕС фізіологічкологічну активність. Приклади аналізів рецептору ному розчині та преінкубують протягом 10 хвилин глутамату добре відомі у рівні техніки як описано, у буферованому ГЕПЕС фізіологічному розчині, наприклад, у Aramori et al, Neuron 8:757 (1992), що містить 10мМ LiCI. Сполуки інкубують у подвоTanabe et al., Neuron 8:169 (1992), Miller et al, J. єнні при 37°С протягом 15 хвилин, тоді додають Neuroscience 15: 6103 (1995), Balazs, et al, J. глутамат (80мкМ) або DHPG (30мкМ) та інкубують Neurochemistry 69:151 (1997). Методологію, описапротягом додаткових 30 хвилин. Реакцію зупиняну у цих публікаціях уведено тут як посилання. ють додаванням 0,5мл перхлоратної кислоти (5%) Сполуки винаходу можуть бути дослідженими на льоді з інкубацією при 4°С протягом принаймні аналізом (FLIPR), що вимірює мобілізацію внутрі30 хвилин. Зразки збирають у 15мл поліпропіленошньоклітинного кальцію, [Са2+]і у клітинах, що ексві туби та інозитол-фосфат відділяють, застосовупресують mGluR5, або ще одним аналізом (IP3), ючи колонки з іонообмінною смолою (Dowex AG1що вимірює перетворення інозитол-фосфату. X8 форміат, 200-400меш, BIORAD). Розділення FLIPR-Аналіз інозитол-фосфатів було проведено елюванням спершу гліцерофосфатидил-інозитолу 8мл 30мМ Клітини, що експресують mGluR5d людини, амоній форміату. Далі, загальні інозитол-фосфати які описано у WO97/05252 засівають при густині елюють 8мл 700мМ амоній форміату /100мМ му100000 клітини на лунку на покритих колагеном 96рашиної кислоти та збирають у сцинтиляційні коміркових планшетах з прозорим дном з чорними склянки. Цей елюат тоді змішують із 8мл сцинтистінками та експерименти проводять через 24 голянту та уведення [3Н]інозитолу визначають підрадини після засівання. Усі аналізи проводять у бухунком сцинтиляції. Число імпульсів за хвилину від фері, що містить 127мМ NaCI, 5мМ КСІ, 2мМ подвоєних зразків наносять на графік та IK50 виМgСІ2, 0,7мМ NaH2PO4, 2мМ CaCI2, 0,422мг/мл значення роблять, застосовуючи програму підгонNaHCO3, 2,4мг/мл ГЕПЕС, 1,8мг/мл глюкози та ки методом найменших квадратів. 1мг/мл фракції IV альбуміну коров'ячої сироватки Скорочення (рН 7,4). Культури клітин у 96-лункові планшети BSA Альбумін коров'ячої сироватки завантажують протягом 60 хвилин у вищезгаданоCCD прилад із зарядовим зв'язком му буфері, що містить 4мкМ ацетоксиметилового CRC Крива концентрація-реакція естеру флуоресцентного кальцієвого індикатору DHPG 3,5-дигідроксифенілгліцин fluo-3 (Molecular Probes, Eugene, Oregon) у 0,01% FLIPR планшетний зчитувач флуорометричноплюронову кислоту (патентований, неіоногенний го відображення поліоловий сурфактант - CAS Number 9003-11-6). GLAST транспортер глутамату/аспартату Після завантаження fluo-3 буфер видаляють та 25 92503 26 ГЕПЕС 4-(2-гідроксіетил)-1При базовому вимірюванні без голоднечі піперазинетансульфонова кислота (буфер) отримано моторну активність шлункової/LES фази IP3 інозитол-трифосфат III, плацебо (0,9% NaCI) або тест-сполук застосоЗагалом, сполуки були активними у вищенавують внутрішньовенно 0,5мл/кг) у вену передньої веденому аналіз з величинами IK50 менше, ніж лапи. Десять хвилин внутрішньовенного застосу10000нМ. Згідно з одним аспектом винаходу, вевання, харчувальну суміш (10% пептон, 5% Dличина IK50 є менше, ніж 1мкМ. У наступному асглюкози, 5% lntralipid, рН 3,0) уводять у шлунок пекті винаходу, величина IK50 є менше, ніж 100нМ. через центральний просвіт комплекту при Скринінг активності сполуки проти TLESR 100мл/хвилин до кінцевого об'єму 30мл/кг. Інфузію Застосовують дорослих мисливських собак харчувальної суміші супроводжують інфузією повілабрадорів обох статей, привчених знаходитися у тря при швидкості 500мл/хвил, доки не отримують пов'язці Павлова. Езофаготомію слизова-шкіра внутрішньошлунковий тиск 10±1мм Hg. Тиск тоді створюють та собакам надають змоги повністю тримають на цьому рівні протягом експерименту, відновитися перед тим, як проводять будь-які ексзастосовуючи інфузійний насос для наступної інперименти. фузії повітря або для відсосу повітря зі шлунку. Вимірювання рухомості Час експерименту від початку уведення харчуванПісля голоднечі протягом приблизно 17 годин ня до кінця вдування повітря 45 хвилин. Операцію з вільним доступом до води, багатоканальний затверджено як достовірний засіб ініціювання комплект рукав/отвір (Dentsleeve, Adelaide, South TLESR. Australia) уводять через езофагостомію для виміTLESR визначають як зниження тиску нижчого рювання шлункового, нижчого стравохідного сфінстравохідного сфінктера (з посиланням на внутріктеру (LES) та стравохідного тиску. Комплект обпшньошлунковий тиск) при швидкості менше 1мм рискують водою, застосовуючи низькоподатливий Нд/с. Релаксації не повинен передувати глотковий манометричний перфузійний насос (Dentsleeve, сигнал менше 2с перед її початком, у цьому випаAdelaide, South Australia). Обприскану повітрям дку релаксацію класифікують як індуковану ковттубу уводять у пероральному напрямі для вимірюками. Різниця тисків між LES та шлунком не повання ковтків, та сурм'яним електродом вимірюють винна бути менше, ніж 2мм Hg, та тривалість рН, 3см вище LES. Усі сигнали підсилюють та збеповної релаксації довше, ніж 1с. рігають на персональному комп'ютері при 10Гц. Комп’ютерна верстка А. Крулевський Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською5-(phenylisoxazolylethoxy)-triazol-3-yl-substituted pyridine compounds for the treatment of neurological, psychiatric or pain disorders
Автори англійськоюMinidis Alexander, Wensbo David, Slassi Abdelmalik, Isaac Methvin, Ericsson Caroline, Profir Veronica, Bergstrom Per-Olov, Edwards Louise, Arora Jalaj, Xin Tao
Назва патенту російськоюСоединения 5-(фенилизоксазолилэтокси)-триазол-3-ил-замещенного пиридина для лечения неврологических, психиатрических или болевых расстройств
Автори російськоюМинидис Александер, Венсбо Давид, Сласси Абдельмалик, Айзаак Метвин, Эрикссон Каролине, Профир Вероника, Бергстром Пер-Олув, Эдвардз Луиз, Арора Джалай, Синь Тао
МПК / Мітки
МПК: A61P 25/00, A61K 31/00, A61P 1/04, C07D 413/14
Мітки: лікування, 5-(фенілізоксазолілетокси)-триазол-3-іл-заміщеного, психіатричних, розладів, больових, піридину, неврологічних, сполуки
Код посилання
<a href="https://ua.patents.su/13-92503-spoluki-5-fenilizoksazoliletoksi-triazol-3-il-zamishhenogo-piridinu-dlya-likuvannya-nevrologichnikh-psikhiatrichnikh-chi-bolovikh-rozladiv.html" target="_blank" rel="follow" title="База патентів України">Сполуки 5-(фенілізоксазолілетокси)-триазол-3-іл-заміщеного піридину для лікування неврологічних, психіатричних чи больових розладів</a>
Попередній патент: Спосіб діагностики ураження кишечнику при підпечінковій формі портальної гіпертензії у дітей
Наступний патент: Антиміостатинове моноклональне антитіло
Випадковий патент: Спосіб дренування плевральної порожнини при гідротораксі