Похідне етинілу як модулятор активності метаботропного глутаматного рецептора підтипу 5
Номер патенту: 114934
Опубліковано: 28.08.2017
Автори: Віейра Ерік, Річчі Антоніо, Ліндеманн Лотар, Єшкє Гєорг, Штадлєр Хайнц, Рюхер Даніель
Формула / Реферат
1. Сполука формули І
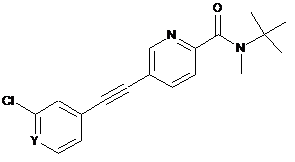 , І
, І
де
Y є N або СН
або її фармацевтично прийнятна сіль приєднання кислоти.
2. Сполука формули І за п. 1, де Y є N.
3. Сполука формули І за п. 2, що являє собою трет-бутилметиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти.
4. Сполука формули І за п. 1, де Y є СН.
5. Сполука формули І за п. 4, що являє собою трет-бутилметиламід 5-(3-хлорфенілетиніл)-піридин-2-карбонової кислоти.
6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активна речовина.
7. Спосіб отримання сполуки формули І за п. 1, що включає наступні варіанти, за якими:
а) в реакцію вводять сполуку формули
 5
5
із сполукою СН3І
з отриманням сполуки формули
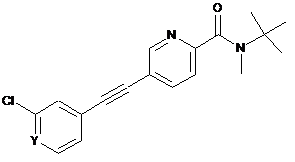 , І
, І
де замісники описані у п. 1, або
b) в реакцію вводять сполуку формули
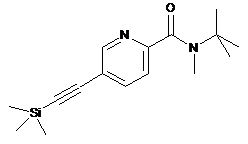 8
8
із сполукою формули
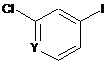 9
9
з отриманням сполуки формули
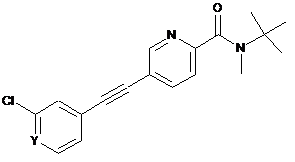 , І
, І
де замісники описані у п. 1.
8. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-5 і терапевтично інертний носій.
9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ).
10. Застосування сполуки за будь-яким з пп. 1-5 для виготовлення лікарського засобу для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ).
11. Сполука за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ).
12. Спосіб лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ), що включає введення ефективної кількості сполуки за будь-яким з пп. 1-5.
Текст
Реферат: Даний винахід належить до похідних етинілу формули І O N N Cl Y ,І або до їх фармацевтично прийнятних солей приєднання кислоти, рацемічних сумішей або відповідних енантіомерів і/або оптичних ізомерів, і/або стереоізомерів. Несподівано виявилося, UA 114934 C2 (12) UA 114934 C2 що сполуки загальної формули І є антагоністами метаботропного глутаматного рецептора (негативні алостеричні модулятори) для застосування при лікуванні тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ). UA 114934 C2 Даний винахід відноситься до похідних етинілу формули I O N N Cl Y 5 10 15 20 25 30 35 40 45 50 І, де Y є N або CH або їх фармацевтично прийнятних солей приєднання кислоти, рацемічних сумішей або відповідних енантіомерів і/або оптичних ізомерів, і/або стереоізомерів. В даний час несподівано виявили, що сполуки загальної формули I є антагоністами метаботропних глутаматних рецепторів (НАМ = негативні алостеричні модулятори). Сполуки формули I відрізняються тим, що проявляють цінні терапевтичні властивості. Їх можна застосовувати при лікуванні або профілактиці розладів, опосередкованих дією рецепторів mGluR5. Передача сигналу в центральній нервовій системі (ЦНС) здійснюється шляхом взаємодії нейропередавача, що виділяється нейроном, з нейрорецептором. Глутамат є основним збудливим нейропередавачем у мозку і відіграє унікальну роль у великій кількості функцій центральної нервової системи (ЦНС). Рецептори, що залежать від стимулювання глутаматом, поділяють на дві основні групи. Перша основна група, так звані іонотропні рецептори, утворює лігандзалежні іонні канали. Метаботропні глутаматні рецептори (mGluR) належать до другої основної групи і, більш того, належать до родини рецепторів, спряжених з G-білком (G-protein coupled receptors, GPCR). Зараз відомі вісім різних членів родини mGluR, у деяких з них є підтипи. За гомологією своєї амінокислотної послідовності, механізмами передачі сигналу і селективністю до агоністів ці вісім рецепторів можна розділити на три підгрупи: mGluR1 і mGluR5 належать до групи I, mGluR2 і mGluR3 - до групи II, а mGluR4, mGluR6, mGluR7 і mGluR8 - до групи III. Негативні алостеричні модулятори метаботропних глутаматних рецепторів, що належать першій групі, можна використовувати для лікування або профілактики гострих і/або хронічних неврологічних розладів, таких як хвороба Паркінсона, синдром ламкої Х-хромосоми, пов'язані з аутизмом розлади, когнітивні розлади і порушення пам'яті, а також хронічний і гострий біль і гастроезофагеальна рефлюксна хвороба (ГЕРХ). Іншими пов'язаними з ними показаннями для лікування є порушення роботи мозку, викликані операціями шунтування або трансплантацією, погане кровопостачання мозку, пошкодження спинного мозку і голови, викликана вагітністю гіпоксія, зупинка серця і гіпоглікемія. Крім того, до таких захворювань належать ішемія, хорея Хантінгтона, аміотропний латеральний склероз (АЛС), викликана СНІДом деменція, пошкодження очей, ретинопатія, ідіопатичний паркінсонізм або паркінсонізм, викликаний прийманням ліків, а також стани, що ведуть до розвитку функцій, пов'язаних з дефіцитом глутамату, такі як, наприклад, м'язові спазми, судоми, мігрень, нетримання сечі, нікотинова залежність, опіатна залежність, тривожність, блювання, дискінезія і депресії. Розладами, які повністю або частково опосредковуються mGluR5, наприклад, є гострі, травматичні і хронічні дегенеративні захворювання нервової системи, такі як хвороба Альцгеймера, сенільна деменція, хвороба Паркінсона, хорея Хантінгтона, аміотропний латеральний склероз і множинний склероз, психіатричні захворювання, такі як шизофренія і тривожність, депресія, біль і наркотична залежність (Expert Opin. Ther. Patents (2002), 12 (12)). Особливо корисні селективні антагоністи mGluR5 для лікування таких розладів, при яких бажано домогтися зниження активності рецепторів mGluR5, наприклад, тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ). Метою даного винаходу є сполуки формули I і їх фармацевтично прийнятні солі, вищеназвані сполуки як фармацевтично активні речовини і їх отримання. Ще однією метою винаходу є лікарські засоби, основані на сполуках за винаходом, і їх виготовлення, а також застосування сполук для контролю або профілактики захворювань, які опосредковуються рецептором mGluR5 (НАМ), таких як тривожність і біль, депресія, синдром ламкої Х-хромосоми, пов'язані з аутизмом розлади, хвороба Паркінсона і гастроезофагеальна рефлюксна хвороба 1 UA 114934 C2 5 10 15 20 25 30 35 40 45 50 55 60 (ГЕРХ), і, відповідно, для виготовлення відповідних лікарських засобів. Одним утіленням даного винаходу є сполуки формули I, де Y є N. Такою сполукою є трет-бутилметиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти. Одним утіленням даного винаходу є сполуки формули I, де Y є CH. Такою сполукою є трет-бутилметиламід 5-(3-хлорфенілетиніл)-піридин-2-карбонової кислоти. Особливе утілення винаходу складається з наступних сполук: трет-бутилметиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти трет-бутилметиламід 5-(3-хлорфенілетиніл)-піридин-2-карбонової кислоти. Сполуки, подібні до сполук за даним винаходом, були, загалом, відомі як позитивні алостеричні модулятори рецептора mGluR5. Несподівано виявилося, що замість позитивних алостеричних модуляторів mGluR5 були отримані високо-ефективні mGluR5-антагоністи, що характеризуються абсолютно іншою фармакологією у порівнянні з позитивними алостеричними модуляторами. Основна відмінність між позитивними і негативними алостеричними модуляторами представлена на фігурі 1. Позитивний алостеричний модулятор (ПАМ) mGluR5 веде до 2+ підвищення активності рецептора (мобілізації Са ) у присутності фіксованої концентрації глутамату, тоді як алостеричний антагоніст (негативний алостеричний модулятор, НАМ) веде до зменшення активації рецептора. Фігура 1 демонструє загальну поведінку НАМ і ПАМ за -7 однакових умов. Спорідненість до рецептора на фігурі 1 для ПАМ складає близько 10 M, а для -7 -8 НАМ вона знаходиться в інтервалі від 10 M до 10 M. Ці величини можна визначити в аналізі з'вязування, основаному на заміщенні радіоактивно міченого ліганда (= MPEP), див. опис аналізу. Фігура 1: Порівняння позитивного алостеричного модулятора (ПАМ) і антагоніста (негативного алостеричного модулятора = НАМ) mGluR5. Захворювання, які можна лікувати цими сполуками, розрізняються. mGluR5 НАМ корисні при захворюваннях, коли бажано понизити надмірну рецепторну активність, таких як тривожність і біль, депресія, синдром ламкої Х-хромосоми, пов'язані з аутизмом розлади, хвороба Паркінсона і гастроезофагеальна рефлюксна хвороба (ГЕРХ). З іншого боку, mGluR5 ПАМ корисні при захворюваннях, коли бажано нормалізувати знижену рецепторну активність, таких як психоз, епілепсія, шизофренія, хвороба Альцгеймера і пов'язані з нею порушення пам'яті, а також туберозний склероз. Цю відмінність можна практично продемонструвати на моделі тривожності на тваринах, такій як питний конфліктний тест Фогеля, де сполуки за винаходом демонструють анксіолітичну активність, а mGluR-ПАМи не показують активність на цій моделі. Опис і результати біологічних аналізів 2+ Аналіз внутрішньоклітинної мобілізації Ca Була отримана моноклональна клітинна лінія HEK-293, стабільно трансфікована кДНК, що кодує рецептор mGlu5a людини; для роботи з позитивними алостеричними модуляторами (ПАМ) mGlu5 була вибрана клітинна лінія з низьким рівнем експресії рецептора і низькою конститутивною активністю рецептора, це дозволило відрізняти активність речовин як агоністів від ПАМ-активності. Клітини вирощували відповідно до стандартних протоколів (Freshney, 2000) у середовищі Ігла, модифікованому за Дульбекко (DMEM), з 1 мМ глутаміну, 10 % (об/об) температурно-інактивованого бичачого сироваткого альбуміну, пеніциліном/стрептоміцином, 50 мкг/мл гігроміцину і 15 мкг/мл бластіцідіну (всі реагенти для ведення культур клітин і антибіотики виробництва "Інвітроген", Базель, Швейцарія). Приблизно за 24 години до початку експерименту у покриті полі-D-лізином 96-лункові 4 планшети з чорним/прозорим дном посіяли клітини у концентрації 5 × 10 клітин/лунку. Клітини протягом години завантажували 2,5 мкМ Fluo-4AM у завантажувальному буфері (1xHBSS, 20 мМ HEPES) при 37 °C, після чого п'ять разів промили завантажувальним буфером. Після цього клітини перенесли у систему для скринінгу Functional Drug Screening System 7000 ("Хамаматсу", Париж, Франція), додали 11 послідовних напівлогарифмічних розведень досліджуваних сполук при 37 °C, після чого 10-30 хвилин інкубували клітини, безперервно реєструючи флуоресценцію. Після закінчення цього етапу попередньої інкубації до клітин додали агоніст L-глутамат у концентрації, відповідній EC20 (зазвичай, близько 80 мкМ), безперервно реєструючи флуоресценцію. Щоб врахувати добові коливання клітинної відповіді, EC20 глутамату визначали безпосередньо перед кожним експериментом, реєструючи для глутамату повну криву дозавідповідь. Відповіді визначали як збільшення піка флуоресценції за вирахуванням базового рівня 2 UA 114934 C2 5 10 15 (тобто, флуоресценції без додавання L-глутамату), нормалізоване на максимальний стимулюючий ефект, отриманий для насичувальної концентрації L-глутамату. Графіки залежності відсотка від максимального стимулюючого ефекту будували з використанням програми апроксимації кривої по точках XLfit, яка ітеративно проводить лінію за алгоритмом Левенбурга-Марквардта. Для аналізу конкурентного інгібування за одним центром використовували рівняння у = A + ((B-A)/(1+((x/C)D))), де у є відсотком від максимального стимулюючого ефекту, А відповідає мінімальному значенню у, В - максимальному значенню у, С є EC50, x означає log10 від концентрації конкуруючої сполуки, а D відповідає нахилу кривої (коефіцієнт Хілла). На підставі цих кривих були розраховані значення EC50 (концентрація, за якої досягається напівмаксимальна стимуляція), коефіцієнт Хілла і максимальна відповідь, виражена у відсотках від максимального стимулюючого ефекту, якого досягають при насичувальній концентрації L-глутамату. Позитивні сигнали, отримані протягом попередньої інкубації з ПАМ (тобто, перед введенням L-глутаміну в концентрації, відповідній EC20), означали агоністичну активність, відсутність сигналу свідчила про відсутність такої активності. Придушення сигналу після введення Lглутаміну в концентрації, відповідній EC20, означало інгібувальну активність досліджуваної сполуки. У наступному списку представлені відповідні результати для сполук, EC50 яких не перевищує 50 нМ. 20 mGlu5 ПАМ EC50 [нМ] Ефективність [%] 16 64 17 33 37 Приклад 80 Сполука порівняння 1 O N N F Сполука порівняння 2 O N N N Cl Сполука порівняння 3 O N F N F F Cl N Приклад1 O N N Неактивна Cl N Приклад 2 O N N Неактивна Cl 3 UA 114934 C2 5 10 15 20 Аналіз зв'язування MPEP У експериментах зі зв'язування кДНК, що кодує рецептор mGlu5a людини, була тимчасово трансфікована у клітини EBNA способом, описаним у роботі Schlaeger і Christensen [Cytotechnology 15:1-13 (1998)]. Гомогенати клітинних мембран зберігали при -80 °C до дня аналізу, під час якого їх розморозили, ресуспендували і гомогенізували в буферному розчині, що складається з 15 мМ Tris-HCl, 120 мМ NaCl, 100 мМ KCl, 25 мМ CaCl2, 25 мМ MgCl2 при рН 7,4 до фінальної концентрації 20 мкг білка/лунку. Ізотерми насичення визначали, додавши до цих мембран дванадцять концентрацій 3 [ H]MPEP (0,04-100 нМ), загальний об'єм склав 200 мкл, на 1 годину при 4 °C. Експерименти з 3 конкурентного інгібування проводили з фіксованою концентрацією [ H]MPEP (2 нМ), значення IC50 досліджуваних сполук визначали за 11 концентраціями (0,3-10000 нМ). Інкубацію проводили 1 годину за температури 4 °C. Після закінчення інкубації мембрани відокремили на юніфільтрі (unifilter) (96-лункові білі мікропланшети з фільтром GF/C, заздалегідь інкубовані протягом 1 години з 0,1 % ПЕІ у промивальному буфері, компанія Packard BioScience, Меріден, штат Коннектікут) і тричі промили холодним 50 мМ буфером Tris-HCl при pH 7,4. Неспецифічне зв'язування визначали у присутності 10 мкМ MPEP. Радіоактивність фільтру зчитували (3 хвилини) на мікропланшетному сцинтиляційному лічильнику Packard Top-count з поправкою на гасіння після додавання 45 мкл розчину microscint 40 (Canberra Packard S.A., Цюріх, Швейцарія) і струшування протягом 20 хвилин. Порівняння сполук за винаходом і сполук порівняння 1 і 2 Як видно з наступної таблиці, сполуки за винаходом (НАМ) демонструють профіль, що помітно відрізняється від профілю структурно схожих сполук порівняння 1, 2 і 3 (ПАМ). EC50 (нМ) mGlu5 аналіз ПАМ Профіль активності 29 ПАМ 17 42 ПАМ 37 58 ПАМ Неактивна 28 НАМ Неактивна Структура Ki (нМ) Зв'язування MPEP 16 Приклад 15 НАМ O N Сполука порівняння 1 N F O N Сполука порівняння 2 N Cl N O N Сполука порівняння 3 F N F F Cl N O N N 1 Cl N O N N 2 Cl 25 Сполуки формули I можна виготовити способами, описаними далі, способами, наведеними у 4 UA 114934 C2 5 прикладах, або аналогічними. Умови, необхідні для проведення окремих етапів реакції, відомі фахівцям у рівні техніки. Послідовність реакцій не обмежена зображеною на схемах, залежно від початкових матеріалів і їх відповідної реактивності, послідовність етапів реакції можна вільно змінювати. Початкові матеріали або доступні комерційно, або можуть бути отримані способами, аналогічними описаним нижче, способами, викладеними в посиланнях, що наводяться в описі і прикладах, або способами, відомими у рівні техніки. Представлені сполуки формули I і їх фармацевтично прийнятні солі можуть бути отримані способами, відомими у рівні техніки, наприклад, способом, що включає наступні варіанти: a) взаємодія сполуки формули O N N H Cl Y 5 10 із сполукою CH3I з отриманням сполуки формули O N N Cl Y I 15 де замісники описані вище, або b) взаємодія сполуки формули O N N Si 8 із сполукою формули I Cl Y 9 з отриманням сполуки формули O N N Cl Y 20 I де замісники описані вище. Докладніше отримання сполуки формули I описане на схемах 1 і 2 і в прикладах 1-2. Схема 1 5 UA 114934 C2 5 10 15 20 25 Сполуку прикладу 1 можна отримати, наприклад, здійснивши реакцію між 5-бромпіридин-2карбоновою кислотою 1 і трет-бутиламіном 2 у присутності основи, такої як основа Хуніга, і пептидного реагента поєднання, такого як TBTU, у розчиннику, наприклад, діоксані. Реакція поєднання за Соногашира спільно з десилюванням in situ за участю аміду 5-бромпіридин-2карбонової кислоти 3 і арилацетилену 4 приводить до отримання необхідної етинільної сполуки 5. Алкілування етинільної сполуки 5 йодометаном і гідридом натрію у такому розчиннику, як ДМФ, приводить до отримання необхідної сполуки Прикладу 1 (схема 1). Схема 2 Сполуку прикладу 2 можна отримати, наприклад, в результаті алкілування аміду 5-бромпіридин-2-карбонової кислоти 3 йодометаном і гідридом натрію у такому розчиннику, як ДМФ, з утворенням необхідного аміду 5-бромпіридин-2-карбонової кислоти 6. Реакція поєднання за Соногашира аміду 5-бромпіридин-2-карбонової кислоти 6 з етинілтриметилсиланом 7 приводить до утворення відповідної 5-триметилсиланілетинільної похідної 8. Реакція поєднання за Соногашира спільно з десилюванням in situ за участю сполуки 8 і 1-хлор-3-йодобензолу 9 приводить до отримання необхідної сполуки Прикладу 2 (схема 2). Фармацевтично прийнятні солі сполук формули I можна легко отримати відомими методами, з урахуванням природи сполук, конвертовних у сіль. Неорганічні або органічні кислоти, такі як, наприклад, соляна, бромоводнева, сірчана, азотна, фосфорна кислота або лимонна, мурашина, фумарова, малеїнова, оцтова, бурштинова, тартарова, метансульфонова, п-толуолсульфонова кислота і подібні до них, підходять для отримання фармацевтично прийнятних солей основних сполук формули I. Сполуки, що містять лужні і лужноземельні метали, наприклад, натрій, калій, кальцій, магній і подібні до них, основні аміни або основні амінокислоти, підходять для 6 UA 114934 C2 5 10 15 20 отримання фармацевтично прийнятних солей кислотних сполук. Більш того, винахід відноситься також до лікарських препаратів, що містять одну або більше сполуку за даним винаходом і фармацевтично прийнятні ексципієнти, для лікування і профілактики захворювань, які опосередковуються рецептором mGluR5, таких як тривожність і біль, депресія, синдром ламкої Х-хромосоми, пов'язані з аутизмом розлади, хвороба Паркінсона і гастроезофагеальна рефлюксна хвороба (ГЕРХ). Винахід відноситься також до застосування сполук за даним винаходом, а також їх фармацевтично прийнятних солей, для виробництва ліків, призначених для лікування і профілактики захворювань, які опосередковуються рецептором mGluR5, описаних вище. Фармакологічну активність сполук досліджували наступним способом: кДНК, що кодує рецептор mGlu 5a людини, тимчасово трансфікували у клітини EBNA способом, описаним у роботі Schlaeger і Christensen (Cytotechnology 1998:15:1-13). Вимірювання 2+ [Ca ]i проводили на mGlu 5a-трансфікованих клітинах EBNA після їх інкубації з Fluo 3-AM (отриманим в компанії "Флука", кінцева концентрація 0,5 мкМ) протягом години при 37 °C з подальшим 4-кратним промиванням буфером для аналізу (DMEM з сіллю Ханка і 20 мМ 2+ HEPES). Виконували вимірювання [Ca ]i на флуориметричному сканувальному планшетному рідері (FLIPR, "Молекулар Девайс Корпорейшн", Ла Хойа, Каліфорнія, США). Після оцінки сполук на предмет активності як антагоністів, їх проаналізували також і як агоністів, у порівнянні з 10 мкМ глутамату. Криві інгібування (антагоністи) були побудовані за чотирьох-параметричним логістичним рівнянням, значення IC50 і коефіцієнт Хілла були отримані за допомогою програмного пакета Origin ("Майкрокал Софтваре Інк", Нортгемптон, Массачусетс, США) з ітеративної нелінійної побудови кривих. Значення Ki сполук представлені. Їх визначали за наступною формулою: Ki IC 50 = 1+ 25 30 35 40 45 50 55 [L] EC 50 де IC50 є концентраціями сполук у мкМ, при яких досягається 50 % інгібування. [L] відповідає концентрації, а значення EC50 відповідає концентрації сполук у мкМ, при яких досягається 50 % стимулювання. Сполуки за даним винаходом є антагоністами mGluR 5a рецепторів. Активність сполук формули I, виміряна під час описаного вище аналізу, відповідає Ki < 100 мкМ. Сполуки формули I і їх фармацевтично прийнятні солі можуть використовуватися як ліки, наприклад, у формі фармацевтичних препаратів. Фармацевтичні препарати можна вводити перорально, наприклад, у формі таблеток, покритих оболонкою таблеток, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Однак, введення можна здійснювати ще й ректально, наприклад, у формі супозиторіїв, або парентерально, наприклад, у формі розчинів для ін'єкцій. Для отримання лікарських препаратів, сполуки формули (I) і їх фармацевтично прийнятні солі можуть оброблятися спільно з фармацевтично інертними неорганічними або органічними носіями. Як такі носії для отримання таблеток, покритих оболонкою таблеток, драже і твердих желатинових капсул можуть використовуватися лактоза, кукурудзяний крохмаль або його похідні, тальк, стеаринова кислота або її солі і подібні до них. Для м'яких желатинових капсул підходять, наприклад, такі носії як рослинні масла, віск, жири, напівтверді і рідкі поліоли і подібні до них; проте, залежно від природи діючої речовини, зазвичай, у випадку м'яких желатинових капсул, носії не потрібні. Відповідними носіями для виготовлення розчинів і сиропів є, наприклад, вода, поліоли, цукроза, інвертований цукор, глюкоза і подібні до них. Для приготування призначених для ін'єкцій водних розчинів водорозчинних солей сполук формули (I) можуть застосовуватися такі ад'юванти, як спирти, поліоли, гліцерин, рослинні масла і подібні до них, але, як правило, необхідності у них не виникає. Відповідними носіями для приготування супозиторіїв є, наприклад, природні або гідрогенізовані масла, віск, жири, напіврідкі або рідкі поліоли і подібні до них. Крім того, фармацевтичні препарати можуть містити консерванти, солюбілізатори, стабілізатори, зволожувачі, емульсифікатори, підсолоджувачі, барвники, ароматизатори, солі для змінювання осмотичного тиску, буфери, маскувальні агенти або антиоксиданти. Вони також можуть містити й інші терапевтично цінні речовини. Як уже згадувалося, предметом даного винаходу також є лікарські засоби, що містять сполуку формули (I) або її фармацевтично прийнятні солі і терапевтично інертний носій, а також 7 UA 114934 C2 5 10 і спосіб отримання таких лікарських засобів, що включає введення однієї або більше сполук формули I або їх фармацевтично прийнятних солей і, за необхідності, однієї або більше інших терапевтично цінних речовин, у галенову лікарську форму спільно з одним або більше терапевтично інертним носієм. Дозування коливається у широких межах і, зрозуміло, підбирається з урахуванням індивідуальних потреб у кожному конкретному випадку. У загальному випадку, ефективне дозування для перорального або парентерального введення знаходиться в інтервалі від 0,01 до 20 мг/кг/день, причому для всіх описаних показань переважним є дозування 0,1-10 мг/кг/день. Добова доза для дорослої людини вагою 70 кг, відповідно, знаходиться в інтервалі від 0,7 до 1400 мг на день, переважно, від 7 до 700 мг на день. Щоб додатково прояснити суть винаходу, наводяться наступні приклади: Приклад 1 Трет-бутилметиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти O N N Cl N 15 Етап 1: трет-бутиламід 5-бромпіридин-2-карбонової кислоти O N N Br 20 25 5-бромпіколінову кислоту (200 мг, 0.99 ммоль) розчиняли у діоксані (2 мл), після чого при кімнатній температурі додавали основу Хуніга (520 мкл, 2,97 ммоль, 3 еквів.), TBTU (350 мг, 1,09 ммоль, 1,1 еквів.) і трет-бутил амін (124 мкл, 1,19 ммоль, 1,2 еквів.). Суміш 16 годин перемішували при кімнатній температурі, після чого її упарювали і екстрагували насиченим розчином NaHCO3 і ще двічі невеликою кількістю дихлорметану. Неочищений продукт очищали методом флеш-хроматографії, безпосередньо завантаживши шари дихлорметану у колонку з силікагелем і елююючи градієнтом етил ацетат:гептан 0:100-50:50. Необхідний трет-бутиламід 5-бром-піридин-2-карбонової кислоти (235 мг, вихід 92 %) отримували у вигляді безбарвного + масла, МС: m/e=257,0/259,0 (M+H ). Етап 2: трет-бутиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти O N N Cl N 30 35 Трет-бутиламід 5-бром-піридин-2-карбонової кислоти (Приклад 1, етап 1) (280 мг, 0,92 ммоль) розчиняли у ТГФ (20 мл). У атмосфері азоту у систему додавали 2-хлор-4триметилсиланілетиніл-піридин [CAS 499193-57-6] (222 мг, 1,06 ммоль, 1,15 еквів.), Et3N (1,28 мл, 9,2 ммоль, 10 еквів.), біс-(трифенілфосфін)-паладій(II)дихлорид (19 мг, 28 мкмоль, 0,03 еквів.) і йодид міді(I) (5 мг, 28 мкмоль, 0,03 еквів.), після чого суміш нагрівали до 70 °C. По краплинах протягом 20 хвилин при 70 °C додавали TBAF 1M у ТГФ (970 мкл, 0,97 ммоль, 1,05 еквів.). Реакційну суміш 2 години перемішували при 70 °C і упарили у присутності сорбенту Isolute® до сухого стану. Неочищений продукт очищали методом флеш-хроматографії на колонці з 20 г силікагелю, здійснюючи елюювання градієнтом гептан:етил ацетат 100:0 → 0:100. Потрібний трет-бутиламід 5-(2-хлор-піридин-4-ілетиніл)-піридин-2-карбонової кислоти (210 мг, + вихід 73 %) отримували у вигляді білої твердої речовини, МС: m/e=314,4/316,4 (M+H ). Етап 3: трет-бутилметиламід 5-(2-хлорпіридин-4-ілетиніл)-піридин-2-карбонової кислоти O N N Cl 40 N (180 мг, 574 мкмоль) трет-бутиламіду 5-(2-хлор-піридин-4-ілетиніл)-піридин-2-карбонової 8 UA 114934 C2 5 10 кислоти (Приклад 1, етап 2) розчиняли у ДМФ (3 мл) і охолоджували до 0-5 °C. У систему додавали йодометан (54 мкл, 860 мкмоль, 1,5 еквів.) і NaH (55 %) (41 мг, 860 мкмоль, 1,5 еквів.), після чого її перемішували 2 години без охолоджувальної бані. Реакційну суміш обробляли насиченим розчином NaHCO3 і двічі екстрагували EtOAc. Органічні шари екстрагували водою, сушили над сульфатом натрію і упарювали до сухого стану. Неочищений продукт очищали методом флеш-хроматографії на силікагелі (20 г, градієнт етил ацетат/гептан, 0:100-100:0). Потрібний трет-бутилметиламід 5-(2-хлор-піридин-4-ілетиніл)-піридин-2-карбонової кислоти (78 + мг, вихід 42 %) отримували у вигляді жовтої твердої речовини, МС: m/e=328,4/330,4 (M+H ). Приклад 2 Трет-бутилметиламід 5-(3-хлорфенілетиніл)-піридин-2-карбонової кислоти O N N Cl Етап 1: трет-бутилметиламід 5-бромпіридин-2-карбонової кислоти O N N Br 15 Вказану в заголовку сполуку отримували у вигляді білої твердої речовини, МС: + m/e=271,2/273,2 (M+H ), способом, подібним до описаного у Прикладі 1, етап 3, починаючи від трет-бутиламіду 5-бром-піридин-2-карбонової кислоти (Приклад 1, етап 1) і йодометану. Етап 2: трет-бутилметиламід 5-триметилсиланілетинілпіридин-2-карбонової кислоти O N N Si 20 Вказану у заголовку сполуку отримували у вигляді жовтої твердої речовини, МС: m/e=289,2 + (M+H ), способом, подібним до описаного у Прикладі 1, етап 2, без використання TBAF, починаючи від трет-бутилметиламіду 5-бром-піридин-2-карбонової кислоти (Приклад 2, етап 1) і етинілтриметилсилану. Етап 3: трет-бутилметиламід 5-(3-хлорфенілетиніл)-піридин-2-карбонової кислоти O N N Cl 25 Вказану у заголовку сполуку отримували у вигляді ясно-жовтого масла, МС: m/e=327,3/329,3 + (M+H ), способом, подібним до описаного у Прикладі 1, етап 2, починаючи від третбутилметиламіду 5-триметилсиланілетиніл-піридин-2-карбонової кислоти (Приклад 2, етап 2) і 1-хлор-3-йодобензолу. 9 UA 114934 C2 ФОРМУЛА ВИНАХОДУ 1. Сполука формули І O N N Cl Y 5 10 15 ,І де Y є N або СН або її фармацевтично прийнятна сіль приєднання кислоти. 2. Сполука формули І за п. 1, де Y є N. 3. Сполука формули І за п. 2, що являє собою трет-бутилметиламід 5-(2-хлорпіридин-4ілетиніл)-піридин-2-карбонової кислоти. 4. Сполука формули І за п. 1, де Y є СН. 5. Сполука формули І за п. 4, що являє собою трет-бутилметиламід 5-(3-хлорфенілетиніл)піридин-2-карбонової кислоти. 6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активна речовина. 7. Спосіб отримання сполуки формули І за п. 1, що включає наступні варіанти, за якими: а) в реакцію вводять сполуку формули O N N H Cl Y 5 20 із сполукою СН3І з отриманням сполуки формули O N N Cl Y ,І де замісники описані у п. 1, або b) в реакцію вводять сполуку формули 10 UA 114934 C2 O N N Si 8 із сполукою формули Cl I Y 9 з отриманням сполуки формули O N N Cl Y 5 10 15 20 ,І де замісники описані у п. 1. 8. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-5 і терапевтично інертний носій. 9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ). 10. Застосування сполуки за будь-яким з пп. 1-5 для виготовлення лікарського засобу для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ). 11. Сполука за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ). 12. Спосіб лікування тривожності і болю, депресії, синдрому ламкої Х-хромосоми, пов'язаних з аутизмом розладів, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (ГЕРХ), що включає введення ефективної кількості сполуки за будь-яким з пп. 1-5. 11 UA 114934 C2 Комп’ютерна верстка М. Мацело Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 12
ДивитисяДодаткова інформація
Назва патенту англійськоюEthynyl derivatives as modulators of mglur5 receptor activity
Автори англійськоюJaeschke, Georg, Lindemann, Lothar, Ricci, Antonio, Rueher, Daniel, Stadler, Heinz, Vieira, Eric
Автори російськоюЕшке Георг, Линдеманн Лотар, Риччи Антонио, Рюхер Даниель, Штадлер Хайнц, Виэйра Эрик
МПК / Мітки
МПК: C07D 213/81, A61K 31/44, A61K 31/444
Мітки: етинілу, метаботропного, похідне, активності, рецептора, глутаматного, модулятор, підтипу
Код посилання
<a href="https://ua.patents.su/14-114934-pokhidne-etinilu-yak-modulyator-aktivnosti-metabotropnogo-glutamatnogo-receptora-pidtipu-5.html" target="_blank" rel="follow" title="База патентів України">Похідне етинілу як модулятор активності метаботропного глутаматного рецептора підтипу 5</a>
Попередній патент: Попередники і способи перенесення при гідротермальному рідкофазному спіканні (hlps)
Наступний патент: Водовугільне паливо
Випадковий патент: Добавка до комбікорму для сільськогосподарської птиці












