Заміщені 6,6-гетеробіциклічні похідні, проміжні сполуки, фармацевтична композиція та спосіб лікування, попередження або інгібування розладів
Формула / Реферат
(21) 99020647
(57)
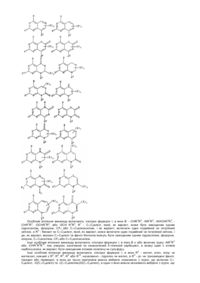
1. Заміщені 6, 6-гетеробіциклічні похідні формули
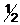 , I
, I
де пунктирна лінія означає можливі подвійні зв'язки;
А - нітроген чи CR7;
В - -NR1R2, -CR1R2R10, -C(=CR2R11)R1, -NHCR1R2R10, -OCR1R2R10, -SCR1R2R10, -CR2R10NHR1, -CR2R10OR1, -CR2R10SR1 або -COR2;
G - нітроген чи CR4, і з всіма оточуючими атомами пов'язаний простими зв'язками, або G - карбон, що зв'язаний з К подвійним зв'язком;
К - нітроген чи CR6, що зв'язаний з G чи Е подвійним зв'язком, або К - оксиген, сульфур, С=O, C=S, CR6R12 або NR8, коли з всіма оточуючими атомами пов'язаний простими зв'язками, або К - двоатомна проміжна група, в якій один чи два кільцевих атоми проміжної групи - оксиген, нітроген, сульфур, С=O, C=S, CR6R12, NR6 або CR6, а другий - CR6R12 або CR9;
D та Е, кожний незалежно один від одного - С=O, C=S, сульфур, оксиген, CR4R6 або NR8, коли з всіма оточуючими атомами пов'язані простими зв'язками, або нітроген чи CR4, коли з сусіднім атомом пов'язані подвійним зв'язком;
6- чи 7-членний цикл, що включає D, E, K та G, може містити 1-3 подвійних зв'язки, оксиген, нітроген та сульфур, та 0-2 групи С=O чи C=S, в яких атоми карбону є частиною кільця, а атоми оксигену та сульфуру - замісники в цьому кільці;
R1 - С1-С6алкіл, заміщений, як варіант, одним чи двома замісниками, що незалежно вибрані з групи, яка включає гідроксил, флуор, хлор, бром, йод, С1-С4алкоксил, СF3, -С(=O)(С1-С4алкіл), -С(=O)-O-(С1-С4)алкіл, -ОС(=O)(С1-С4алкіл), -OC(=O)N(С1-С4алкіл)(С1-С2алкіл), -NHCO(С1-С4алкіл), -СООН, -СОО(С1-С4алкіл), -СОNН(С1-С4алкіл), -СON(С1-С4алкіл)(С1-С2алкіл), -S(С1-С4алкіл), -CN, -NO2, -SO(С1-С4алкіл), -SO2(С1-С4алкіл), -SO2NН(С1-С4алкіл) і -SO2N(С1-С4алкіл)(С1-С2алкіл), де кожна з груп С1-С4 у групах R1 може, як варіант, містити один чи два подвійних або потрійних зв'язки,
R2 - С1-С12алкіл, що може, як варіант, містити один-три подвійних або потрійних зв'язки, арил або (С1-С4алкілен)арил, де вказаний арил та арильна група вказаного (С1-С4 алкілен)арилу вибрана з групи, яка включає феніл, нафтил, тієніл, бензотієніл, піридил, хіноліл, піразиніл, піримідиніл, імідазоліл, фураніл, бензофураніл, бензотіазоліл, ізотіазоліл, піразоліл, піроліл, індоліл, піролопіридил, оксазоліл та бензоксазоліл; С3-С8 циклоалкіл або (С1-С6алкілен)(С3-С8циклоалкіл), де 1-2 атоми карбону вказаного циклоалкіла та 5-8-членних циклоалкільних груп вказаного (С1-С6алкілен)(С3-С8циклоалкіла) можуть незалежно, як варіант, бути заміщеними атомами оксигену чи сульфуру або NZ, де Z - гідроген, С1-С4алкіл або бензил, і де кожна з вищеозначених груп R2 може, як варіант, бути заміщеною 1-3 замісниками, вибраними з групи, що включає хлор, флуор, гідроксил та С1-С4алкіл, або одним замісником, вибраним з групи, що включає С1-С6алкоксил, -ОС(=O)(С1-С6алкіл), -ОС(=O)N(С1-С4алкіл)(С1-С2алкіл), -S(С1-С6алкіл), аміногрупу, -NH(С1-С2алкіл), -N(С1-С2алкіл)(С1-С4алкіл), -N(С1-С4алкіл)-СО-(С1-С4алкіл), -NНСО(С1-С4алкіл), -СООН, -СОО(С1-С4алкіл), -СОNН(С1-С4алкіл), -СОN(С1-С4алкіл)(С1-С2алкіл), -SH, -CN, -NO2, -SO(С1-С4алкіл), -SO2(С1-С4алкіл), -SO2NH(С1-С4алкіл) та SO2N(С1-С4алкіл)(С1-С2алкіл);
-NR1R2 або -CR1R2R10 можуть утворювати 3-8-членне насичене кільце, 5-8-членне кільце, що як варіант, містить 1 чи 2 подвійних зв'язки, і де один чи два кільцевих атоми карбону такого 5-8-членного кільця можуть незалежно, як варіант, бути заміщеними атомами оксигену чи сульфуру або NZ2, де Z2 - гідроген, С1-С4алкіл або бензил,
R3 - гідроген, С1-С4алкіл, -O(С1-С4алкіл), хлор, флуор, бром, йод, -S(С1-С4алкіл) або -SO2(С1-С4алкіл);
кожний R8, R9 та R12 незалежно вибрані з гідрогену та С1-С4алкілу;
кожний R4 та R6, що приєднані до атому карбону, незалежно вибрані з групи, що включає гідроген, С1-С6алкіл, флуор, хлор, бром, йод, гідроксил, гідроксі(С1-С2алкіл), трифлуорметил, ціано-, аміно-, нітрогрупи, -O(С1-С4алкіл), -N(С1-С4алкіл)(С1-С2алкіл), -CH2SCH3, -S(С1-С4алкіл), -СО(С1-С4алкіл), -С(=O)Н або -С(=O)O(С1-С4алкіл), де кожна з С1-С2алкільних груп у вищеозначених групах R4 та R6 може, як варіант, містити один чи два подвійних або потрійних зв'язки, а приєднаний до атома нітрогену R6 вибирають з гідрогену та С1-С4алкілу;
R5 - заміщені феніл, нафтил, піридил або піримідил, кожний з яких заміщено 2-4 замісниками R13, до трьох з яких можна незалежно вибрати з групи, що включає хлор, С1-С6алкіл, -О(С1-С6алкіл) та -(С1-С6алкілен)О(С1-С6алкіл), а один з яких можна незалежно вибрати з групи, що включає бром, йод, форміл, трифлуорметил, ціано-, нітро-, аміногрупи, -NH(С1-С2алкіл), -N(С1-С2алкіл)(С1-С6алкіл), -С(=O)O(С1-С4алкіл), -С(=O)(С1-С4алкіл), -СООН, -SO2NН(С1-С4алкіл), -SO2N(С1-С2алкіл)(С1-С4алкіл), -SO2NH2, -NHSO2(С1-С4алкіл), -(С0-С1алкілен)-SO-(С1-С2алкіл), -(С0-С1алкілен)-SO-(С1-С2алкіл), -(С0-С1алкілен)-SO2-(С1-С2алкіл) та (С1-С4алкілен)-ОН, і де кожний С1-С4алкіл та С1-С6алкіл у вищеозначених групах R5 можуть, як варіант, бути заміщеними 1-2 замісниками, незалежно вибраними з флуору, гідроксилу, аміно-, метиламіно-, диметиламіногруп та ацетилу;
R7 - гідроген, метил, галоген (наприклад, хлор, флуор, йод або бром), гідроксил, ме-токсил, -С(=O)(С1-С2алкіл), -С(=O)O(С1-С2алкіл), гідроксиметил, трифлуорметил або форміл,
R10 - гідроген, гідроксил, метоксил або флуор; а
R11 - гідроген або С1-С4алкіл,
за умови, що в кільці, що включає D, Е, К та G, за формулою І не може бути двох сусідніх подвійних зв'язків,
а також фармацевтично прийнятна сіль такої сполуки.
2. Сполука за п.1, яка відрізняється тим, що В - -NR1R2, -NHCHR1R2 або -OCHR1R2, R1 - С1-С6алкіл, який, як варіант, може бути заміщений одним флуором або С1-С4алкоксилом, і як варіант, включати один подвійний чи потрійний зв'язок, а R2 - С1-С4алкіл або -(С1-С2алкіл)-СО-(С1-С2алкіл), який, як варіант, може включати один подвійний чи потрійний зв'язок.
3. Сполука за п. 1, яка відрізняється тим, що В - -CHR1R2, -NR1R2, -NHCHR1R2, -OCHR1R2 або -SCHR1R2, R1 - С1-С6алкіл, який, як варіант, може бути заміщений одним гідроксилом, флуорциклопропілом, СF3 або С1-С4алкоксилом, і як варіант, включати один подвійний чи потрійний зв'язок, a R2 - бензил чи С1-С6алкіл, який, як варіант, може включати один подвійний чи потрійний зв'язок, і де, як варіант, вказаний С1-С6алкіл та феніл вказаного бензилу можуть бути заміщеним одним гідроксилом, флуором, хлором, циклопропілом, С1-С2алкілом, СF3 або С1-С2алкоксилом.
4. Сполука за п.1, яка відрізняється тим, що А - N, CH або ССН3.
5. Сполука за п.1, яка відрізняється тим, що G - нітроген.
6. Сполука за п.1, яка відрізняється тим, що G - карбон, а кільце, що включає D, E, К та G, є бензокільцем.
7. Сполука за п.1, яка відрізняється тим, що G - N, D - NH чи N(метил), а ![]() -СН2-СН2, СН=СН, С(O)-СН2 або СН2-С(O).
-СН2-СН2, СН=СН, С(O)-СН2 або СН2-С(O).
8. Сполука за п.1, яка відрізняється тим, що G - N, a ![]() - С(O)-О-СH2, СН2-O-СН2, С(O)-СН2-СН2, С(O)-СН=СН, СН2-СН2-СН2, СН2-СН2-С(O), СН=СН-С(O), СН=СН-СН2, CH-CH-NH або СН=СН-NCH3.
- С(O)-О-СH2, СН2-O-СН2, С(O)-СН2-СН2, С(O)-СН=СН, СН2-СН2-СН2, СН2-СН2-С(O), СН=СН-С(O), СН=СН-СН2, CH-CH-NH або СН=СН-NCH3.
9. Сполука за п.1, яка відрізняється тим, що R3 - метил, а кожний з R4, R6, R8, R9 або R12 - гідроген.
10. Сполука за п.1, яка відрізняється тим, що R5 - ди- чи тризаміщений феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, ціаногрупу, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
11. Сполука за п.1, яка відрізняється тим, що R3 - метил, етил, хлор чи метоксил, а кожний з R4, R6, R8, R9 або R12, незалежно - гідроген чи метил.
12. Сполука за п.1, яка відрізняється тим, що R5 - ди- чи тризаміщені феніл, піридил або піримідил, в яких два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, ціаногрупу, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
13. Сполука за п.1, яка відрізняється тим, що В - -CHR1R2, -NHCHR1R2 або -OCHR1R2, а група CHR1R2, що входить у склад В, є циклопентановим кільцем, тетрагідрофурановим кільцем або тетрагідротієніловим кільцем.
14. Сполука за п.3, яка відрізняється тим, що G - карбон, а кільце, що включає D, Е, К та G, є бензокільцем.
15. Сполука за п.14, яка відрізняється тим, що R3 - метил.
16. Сполука за п.15, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
17. Сполука за п.15, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні піридил, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
18. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - С(С0-С1алкіл)-O-С(С0-С1алкіл)-(С0 -С1алкіл).
- С(С0-С1алкіл)-O-С(С0-С1алкіл)-(С0 -С1алкіл).
19. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - СН2-О-CH2.
- СН2-О-CH2.
20. Сполука за п. 19, яка відрізняється тим, що R3 - метил.
21. Сполука за п.20, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара- положенні феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
22. Сполука за п.20, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні піридил, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
23. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - O-C(С0-С1алкiл)(С0-С1алкiл)-С(С0-С1алкiл)(С0-С1алкiл), S-C(С0-С1алкiл)(С0-С1алкiл)-С(С0-С1алкiл)(С0-С1алкiл) або N(С0-С1алкiл)-C(С0-С1алкiл)(С0-С1алкiл)-C(С0-С1алкiл)(С0-С1алкiл).
- O-C(С0-С1алкiл)(С0-С1алкiл)-С(С0-С1алкiл)(С0-С1алкiл), S-C(С0-С1алкiл)(С0-С1алкiл)-С(С0-С1алкiл)(С0-С1алкiл) або N(С0-С1алкiл)-C(С0-С1алкiл)(С0-С1алкiл)-C(С0-С1алкiл)(С0-С1алкiл).
24. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - О-CH2-CH2, O-СН=СН, S-CH2-CH2 або S-CH=CH.
- О-CH2-CH2, O-СН=СН, S-CH2-CH2 або S-CH=CH.
25. Сполука за п.24, яка відрізняється тим, що R3 - метил.
26. Сполука за п.25, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
27. Сполука за п.25, яка відрізняється тим, що R5 - дизаміщений в орто- чи параположенні піридил, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
28. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - NH-СН2-СН2, N(метил)-CH2-CH2-N-R5, NH-CH=CH-N-R5 або N(метил)-СН=СН-N-R5.
- NH-СН2-СН2, N(метил)-CH2-CH2-N-R5, NH-CH=CH-N-R5 або N(метил)-СН=СН-N-R5.
29. Сполука за п.28, яка відрізняється тим, що R3 - метил.
30. Сполука за п.29, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
31. Сполука за п.29, яка відрізняється тим, що R5 - дизаміщений в орто- чи параположенні піридил, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), CF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
32. Сполука за п.3, яка відрізняється тим, що G - N, a ![]() - N=С(С0-С1алкiл)-С(=О), N(С0-С1алкiл)-С(=О)-С(С0-С1алкiл), С(=О)-N(С0-С1алкiл)-С(=О), С(С1)=N-С(=О), С(С0-С1алкiл)=N-С(=О), СН2СН2СН2, СН2-СН2-С(=О), СН2-N(С0-С1алкiл)-С(=О).
- N=С(С0-С1алкiл)-С(=О), N(С0-С1алкiл)-С(=О)-С(С0-С1алкiл), С(=О)-N(С0-С1алкiл)-С(=О), С(С1)=N-С(=О), С(С0-С1алкiл)=N-С(=О), СН2СН2СН2, СН2-СН2-С(=О), СН2-N(С0-С1алкiл)-С(=О).
33. Сполука за п.32, яка відрізняється тим, що R3 - метил.
34. Сполука за п.33, яка відрізняється тим, що R5 - ди- чи тризаміщений в орто- чи пара-положенні феніл, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
35. Сполука за п.33, яка відрізняється тим, що R5 - дизаміщений в орто- чи пара-положенні піридил, в якому два чи три замісники незалежно вибрані з групи, що включає С1-С4алкіл, циклопропіл, -O(С1-С4алкіл), -(С1-С4алкілен)-O-(С1-С4алкіл), СF3, -ОСF3, -СНО, (С1-С4алкілен)-ОН, флуор, хлор, бром, йод, де кожний вищевказаний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок.
36. Сполука за п.1, яка відрізняється тим, що нею є
4-(бутилетиламіно)-2,6-диметил-8-(2,4,6-триметилфеніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он,
8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он,
8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідропіридо[2,3-b]піразин,
8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он,
5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін,
5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1,2-дигідро-3-окса-1,8-діаза-нафталін-4-он,
8-(1-етилпропокси)-1,6-диметил-4-(2,4,б-триметилфеніл)-1,2,3,4-тетрагідропіридо[2,3-b]піразин,
(1-етилпропіл)-[2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-іл]-амін,
4-(1-етилпропокси)-2-метил-8-(2,4,6-триметилфеніл)-хінолін,
2-метил-4-(тетрагідрофуран-3-ілокси)-8-(2,4,6-триметилфеніл)-хінолін,
5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-[1,8]нафтиридин-2-он,
5-(1-етилпропіламіно)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-[1,8]нафтиридин-2-он,
5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-d]піримідин-2-он,
4-(1-етилпропокси)-2,6-диметил-8-(2,4,6-триметилфеніл)-8Н-птеридин-7-он,
5-(1-етилпропокси)-7-метил-1 -(2,4,6-триметилфеніл)-1,2,3,4-тетрагідро-[1,8]нафтиридин,
8-(1-етилпропокси)-2,6-диметил-4-(2,4,6-триметилфеніл)-4Н-піридо[2,3-b]піразин-3-он,
4-хлор-5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1Н-піридо[2,3-d]піримідин-2-он,
5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1Н-піридо[2,3-d]піримідин-2,4-діон,
1-(4-бром-2,6-диметилфеніл)-5-(1-етилпропокси)-7-метил-1,4-дигідро-2Н-3-окса-1,8-діазанафталін,
1-(4-хлор-2,6-диметилфеніл)-5-(1-етилпропокси)-7-метил-1,4-дигідро-2Н-3-окса-1,8-діазанафталін,
або фармацевтично прийнятна сіль такої сполуки.
37. Сполука за п.1, яка відрізняється тим, що вказана сполука є:
8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он,
8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідропіридо[2,3-b]піразин,
8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он,
8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідропіридо[2,3-b]піразин,
або фармацевтично прийнятна сіль такої сполуки.
38. Фармацевтична композиція для лікування, попередження чи інгібування (а) розладів, лікування яких здійснюють чи посилюють протидією ФВК, включаючи, але без обмеження, розлади, що викликані чи посилені ФВК, або (б) розлади, що вибрані з таких запальних розладів, як ревматоїдні артрити та остеоартрити, біль, астма, псоріаз та алергії, генералізований тривожний розлад, панічний розлад, фобії, примусово-нав'язливі розлади, пост-травматичний стресовий розлад, індуковані стресом розлади сну, такі больові відчутя, як фіброміалгія, такі розлади настрою, як депресія, включаючи депресивний розлад повнолітніх, епізодичну депресію, рецидивну депресію, дитячу депресію, викликану зловживанням, розлади настрою, поєднані з передменструальним синдромом, постнатальну депресію, дистимію, біполярні розлади та циклотимію, синдром хронічної втоми, індукований стресом головний біль, рак, синдром подразнення кишечнику, хвороба Крона, спазми товстої кишки, пост-оперативна кишкова непрохідність, виразка, діарея, індукована стресом лихоманка, вірусні інфекції імунодефіциту людини (ВІЛ), такі нейродегенеративні хвороби, як хвороба Альцгеймера, хвороби Паркінсона та Хантингтона, шлунково-кишкові захворювання, такі розлади харчування, як анорексія та невротична булімія, геморагічний стрес, хімічні залежності та звикання (наприклад, до алкоголю, нікотину, кокаїну, героїну, бензодіазепіну або інших ліків), симптоми відмови від ліків та алкоголю, викликані стресом психотичні напади, синдром еутиреозної слабкості, синдром несприйнятності антидіаретичного гормону (АДГ), ожиріння, безплідність, травми голови та спинного хребта, ішемічні нервові пошкодження (наприклад, така церебральна ішемія, як ішемія гіпокампа), нервове пошкодження від збудження, епілепсія, напад, імунні дисфункції, включаючи імунну дисфункцію від стресу (наприклад, синдром стресу свиней, сипний тиф корів, пароксизмальна фібриляція у коней, викликані обмеженням дисфункції у курей, стрес при стрижці баранів або викликаний спілкуванням людини з твариною стрес у собак), спазми м'язів, нетримання сечі, вікове слабоумство типу Альцгеймера, слабоумство від багатократного інфаркту, бічний аміотрофічний склероз, гіперчутливість, тахікардія, застійна серцева нестача, остеопороз, передчасні пологи та гіпоглікемія у ссавців, вказана композиція містить кількість сполуки за п.1, яка ефективна при лікуванні таких розладів, а також фармацевтично прийнятний носій.
39. Спосіб лікування, попередження чи інгібування (а) розладів, лікування яких здійснюють чи посилюють протидією ФВК, включаючи, але без обмеження, розлади, що викликані чи посилені ФВК, або (б) розлади, що вибрані з таких запальних розладів, як ревматоїдні артрити та остеоартрити, біль, астма, псоріаз та алергії, генералізований тривожний розлад, панічний розлад, фобії, примусово-нав'язливі розлади, посттравматичний стресовий розлад, індуковані стресом розлади сну, такі больові відчуття, як фіброміалгія, такі розлади настрою, як депресія, включаючи депресивний розлад повнолітніх, епізодичну депресію, рецидивну депресію, дитячу депресію, викликану зловживанням, розлади настрою, поєднані з предменструальним синдромом, постнатальну депресію, дистимію, біполярні розлади та циклотимію, синдром хронічної втоми, індукований стресом головний біль, рак, синдром подразнення кишечнику, хвороба Крона, спазми товстої кишки, постоперативна кишкова непрохідність, виразка, діарея, індукована стресом лихоманка, вірусні інфекції імунодефіциту людини (ВІЛ), такі нейродегенеративні хвороби, як хвороба Альцгеймера, хвороби Паркінсона та Хантингтона, шлунково-кишкові захворювання, такі розлади харчування, як анорексія та невротична булімія, геморагічний стрес, хімічні залежності та звикання (наприклад, до алкоголю, нікотину, кокаїну, героїну, бензодіазепіну або інших ліків), симптоми відмови від ліків та алкоголю, викликані стресом психотичні напади, синдром еутиреозної слабкості, синдром несприйнятності антидіаретичного гормону (АДГ), ожиріння, безплідність, травми голови та спинного хребта, ішемічні нервові пошкодження (наприклад, така церебральна ішемія, як ішемія гіпокампа), нервове пошкодження від збудження, епілепсія, напад, імунні дисфункції, включаючи імунну дисфункцію від стресу (наприклад, синдром стресу свиней, сипний тиф корів, пароксизмальна фібриляція у коней, викликані обмеженням дисфункції у курей, стрес при стрижці баранів або викликаний спілкуванням людини з твариною стрес у собак), спазми м'язів, нетримання сечі, вікове слабоумство типу Альцгеймера, слабоумство від багатократного інфаркту, бічний аміотрофічний склероз, гіперчутливість, тахікардія, застійна серцева нестача, остеопороз, передчасні пологи та гіпоглікемія у ссавців, який відрізняється тим, що особі, яка потребує такого лікування, вводять деяку кількість сполуки за п.1, яка ефективна при лікуванні таких розладів.
40. Спосіб лікування чи попередження розладів чи станів, лікування чи попередження яких здійснюють чи полегшують інгібуванням зв'язуючого ГВК білка у ссавців, включаючи людину, який відрізняється тим, що вказаному ссавцю вводять деяку кількість сполуки за п. 1, яка інгібуює пов'язуючий ГВК білок.
41. Фармацевтична композиція для лікування чи попередження розладів чи станів, лікування чи попередження яких здійснюють чи полегшують інгібуванням зв'язуючого ГВК білка у ссавців, включаючи людину, яка містить інгібуючу зв'язуючий ГВК білок кількість сполуки за п.1, а також фармацевтично прийнятний носій.
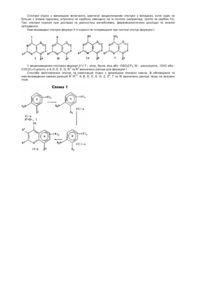
42. Проміжні сполуки формули
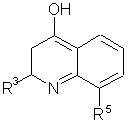 IVZ,
IVZ,
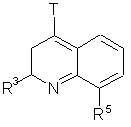 IIZ,
IIZ,
де R3 та R5 визначено за п. 1, а Т - Сl, Вr, І чи OTf.
Текст
Згідно з винаходом запропоновані деякі фармацевтично активні заміщені 6,6-гетеро-біциклічні похідні, фармацевтичні композиції, що їх містять, та спосіб застосування особами при необхідності антагоністичної активності відносно фактора вивільнення кортикотропіну. Заявлені заміщені гетероциклічні похідні виявляють активність як антагоністи фактора (гормона) вивільнення кортикотропіна ФВК (ГВК). Антагоністи ФВК згадані в патентах США 4606642 та 5063245, що відносяться до пептидів та піразолінонів, відповідно. Вони також описані в патентних заявках: РСТ/ІВ95/00439, що позначена США і подана 06.06.1995, а опублікована 14.12.1995, РСТ/ІВ95/00373, що позначена США і подана 18.05.1995, а опублікована 21.12.1995, патентній заявці США 08/448539, що подана в РСТ 12.11.1993 і вступила в національну фазу США 14.06.1995, патентній заявці РСТ WO 95/10506, що подана 12.10.1993, а опублікована 20.04.1995, патентній заявці США 08/481413, що подана в РСТ 26.11.1993 і вступила в національну фазу США 24.07.1995, патентній заявці США 08/254820, що подана 19.04.1995, попередній патентній заявці США 60/008396, що подана 08.12.1995 та попередній патентній заявці США 60/006333, що подана 08.11.1995. Всі ці патентні заявки включено як посилання в їх цілісності. Важливість антагоністів ФВК розкрито у лі тературі, наприклад, P.BIack, Scientific American SCIENCE&MEDICINE, 1995, 16-25, T.Lovenberg et al., Current Pharmaceutical Design, 1995, 1, 395-316, а також вищезгаданому патенті США 5063245. Попередні дані про активності різних антагоністів ФВК можна знайти у M.J.Owens et al., Pharm. Rev., 1991, 1, 425-473, що також включено як посилання. Згідно з дослідами, що описано в цих посиланнях, антагоністи ФВК ефективні при лікуванні широкого кола стрессзалежних хвороб, таких розладів настрою, як депресія, депресивний розлад повнолітніх, епізодична депресія, рецидивна депресія, дитяча депресія, викликана зловживанням, постнатальна депресія, дистимія, біполярні розлади та циклотимія, синдром хронічної втоми, таких розладів харчування, як анорексія та невротична булімія, генералізований тривожний розлад, фобії, примусово-нав'язливі розлади, посттравматичний стрес, таких больових відчуттів, як фіброміалгія, головний біль, шлунково-кишкові захворювання, геморагічний стрес, виразки, викликані стресом психотичні напади, лихоманки, діарея, постоперативна кишкова непрохідність, гіперчутливість товстої кишки, синдром подразнення кишечника, хвороба Крона, спазми товстої кишки, таких запальних розладів, як ревматоїдні артрити та остеоартрити, біль, астма, псоріаз, алергії, остеопороз, передчасні пологи, гіперчутливість, застійна серцева нестача, розлади сну, таких нейродегенеративних хвороб, як хвороба Альцгеймера, вікове слабоумство типу Альцгеймера, слабоумство від багатократного інфаркту, хвороби Паркінсона та Хантингтона, травма голови, ішемічне нервове пошкодження, нервове пошкодження від збудження, епілепсія, напад, травма спинного хребта, психосоціальна нерозвиненість, синдром еутиреозної слабкості, синдром несприйнятності антидіаретичного гормону, ожиріння, хімічні залежності та звикання, симптоми відмови від ліків та алкоголю, безплідність, рак, спазми м'язів, невтримання сечі, гіпоглікемія, та імунні дисфункції, включаючи імунну дисфункцію від стресу, імуносупресію та вірусні інфекції імунодефіциту людини, а також викликані стресом інфекції людини та тварин. Можна вважати, що сполуки згідно з винаходом також є інгібіторами зв'язуючого ГВК білка, а тому корисні при лікуванні розладів, лікування яких може викликати чи посилювати інгібування таких білків. Прикладами таких розладів є хвороба Альцгеймера та ожиріння. Згідно з винаходом запропоновані сполуки формули де пунктирна лінія позначає можливі подвійні зв'язки А - нітроген чи CR7, В - -NR1R2, -CR1R2R10, -C(=CR 2R11)R1, -NHCR1R2R10, -OCR 1R2R10, -SCR 1R2R10, -CR2R10NHR1, 2 10 CR R OR1, -CR 2R10SR1 або -COR 2; G - нітроген чи CR4, і з всіма оточуючими атомами пов'язаний простими зв'язками, або G - карбон, що зв'язаний з К подвійним зв'язком, К - нітроген чи CR6, що зв'язаний з G чи Е подвійним зв'язком, або К - оксиген, сульфур, С =О, C=S, 6 12 CR R , або NR8, коли з всіма оточуючими атомами пов'язаний простими зв'язками, або К - двоатомна проміжна група, в якій один чи два кільцевих атома проміжної групи - оксиген, нітроген, сульфур , С=О, C=S, CR6R12, NR6, або CR6, а другий CR6R12 або CR9, D та Е, кожний незалежно один від одного - С=О, C=S, сульфур, оксиген, CR4R6 або NR8, коли з всіма оточуючими атомами пов'язані простими зв'язками, або нітроген чи CR 4, коли з сусіднім атомом пов'язані подвійним зв'язком; 6- чи 7-членний цикл, що включає D, Е, К та G може містити 1-3 подвійних зв'язка, оксиген, нітроген та сульфур, та 0-2 групи С=О чи C=S, в яких атоми карбону є частиною кільця, а атоми оксигену та сульфуру замісники в цьому кільці; R1 - С1-С6алкіл, заміщений, як варіант, одним чи двома замісниками, що незалежно вибрано з групи, яка включає гідроксил, флуор, хлор, бром, йод, С1-С4алкоксил, CF3, -С(=О)(С1-С4алкіл), -С(=О)-О-(С1-С4)алкіл, ОС(=О)(С1-С4алкіл), -ОС(=О)N(С1-С4алкіл)(С1-С2алкіл), -NHCO(С1-С4алкіл), -СООН, -СОО(С1-С4алкіл), СОNН(С1-С4алкіл), -СОN(С1-С4алкіл)(С1-С2алкіл), -S(С1-С4алкіл), -CN, -NO2, -SO(С1-С4алкіл), -SО2(С1С4алкіл), -SО2NН(С1-С4алкіл) и -SО2N(С1-С4алкіл)(С1-С2алкіл), де кожна з груп С1-С4 у гр упах R1 може, як варіант, містити один чи два подвійних або потрійних зв'язка, R2 - С1-С12 алкіл, що може, як варіант, містити один-три подвійних або потрійних зв'язка, арил або (С1С4 алкілен)арил, де вказаний арил та арильна група вказаного (С1-С4 алкілен)арилу вибрана з групи, яка включає феніл, нафтил, тієніл, бензотієніл, піридил, хіноліл, піразиніл, піримідиніл, імідазоліл, фураніл, бензофураніл, бензотіазоліл, ізотіазоліл, піразоліл, піроліл, індоліл, піролопіридил, оксазоліл та бензоксазоліл; С3-С8 циклоалкіл або (С1-С6 алкілен)( С3-С8 циклоалкіл), де 1-2 атоми карбону вказаного циклоалкіла та 5-8-членних циклоалкільних груп вказаного (С1-С6 алкілен)(С3-С8 циклоалкіла) можуть незалежно, як варіант, бути заміщеними атомами оксигену чи сульфур у або NZ, де Z - гідроген, С1-С4алкіл або бензил, і де кожна з вищеозначених груп R 2 може, як варіант, бути заміщеною 1-3 замісниками, вибраними з групи, що включає хлор, флуор, гідроксил та С 1-С4алкіл, або одним замісником, вибраним з групи, що включає С1-С6алкоксил, -ОС(=О)(С1-С6алкіл), -ОС(=О)М(С1-С4алкіл)(С1-С2алкіл), -S(С1-С6алкіл), аміногрупу, -NН(С1-С2алкіл), -N(С1-С2алкіл)(С1-С4алкіл), -N(С1-С4алкіл)-СО-(С1-С4алкіл), -NНСО(С1-С4алкіл), -СООН, -СОО(С 1-С4алкіл), -СОNН(С1-С4алкіл), -СОN(С1-С4алкіл)(С1-С2алкіл), -SH, -CN, -NO2, -SO(С1С4алкіл), -SO2(С1-С4алкіл), -SO2NH(С1-С4алкіл) та SO2N(С1-С4алкіл)(С1-С2алкіл); -NR1R2 або -CR 1R2R10 можуть створювати 3-8-членне насичене кільце, 5-8-членне кільце, що як варіант, містить 1 чи 2 подвійних зв'язки, і де один чи два кільцевих атоми карбону такого 5-8-членного кільця можуть незалежно, як варіант, бути заміщеними атомами оксигену чи сульфуру або NZ2, де Z2 - гідроген, С1-С4алкіл або бензил, R3 - гідроген, С1-С4алкіл, -O(С1-С4алкіл), хлор, флуор, бром, йод, -S(С1-С4алкіл) або -SO2(С1-С4алкіл), кожний R8, R9 та R12 незалежно вибрано з гідрогену та С1-С2алкілу, кожний R4 та R6, що приєднано до атому карбону, незалежно вибрано з групи, що включає гідроген, С1С6алкіл, флуор, хлор, бром, йод, гідроксил, гідрокси(С1-С2алкіл), трифлуорметил, циано-, аміно-, нітрогрупи, -O(С1-С4алкіл), -N(С1-С4алкіл)(С1-С2алкіл), -CH2SCH3, -S(С1-С4алкіл), -СО(С1-С4алкіл), -С(=О)Н або С(=O)O(С1-С4алкіл), де кожна з С1-С2алкільних груп у вищеозначених групах R4 та R6 може, як варіант, містити один чи два подвійних або потрійних зв'язка, а приєднану до атому нітрогену R6 вибирають з гідрогену та С1-С4алкілу, R5 - заміщені феніл, нафтил, піридил або піримідил, кожний з яких заміщено 2-4 замісниками R13, до трьох з яких можна незалежно вибрати з групи, що включає хлор, С1-С6алкіл, -О(С1-С6алкіл) та -(С1С6алкілен)О(С 1-С6алкіл), а один з яких можна незалежно вибрати з групи, що включає бром, йод, форміл, трифлуорметил, циано-, нітро-, аміно-групи, -NН(С1-С2алкіл), -N(С1-С2алкіл)(С1-С6алкіл), -С(=О)О(С1С4алкіл), -С(=О)(С1-С4алкіл), -СООН, -SО2NH(С1-С4алкіл), -SО2N(С1-С2алкіл)(С1-С4алкіл), -SO2NH2, NHSO2(С1-С4алкіл), -(С0-С1алкілен)-SO-(С1-С2алкіл), -(С0-С1алкілен)-SO-(С1-С2алкіл), -(С0-С1алкілен)-SO2(С1-С2алкіл) та (С1-С4алкілен)-ОН, і де кожний С 1-С4алкіл та С1-С6алкіл у вищеозначених групах R5 можуть, як варіант, бути заміщеними 1-2 замісниками, незалежно вибраними з флуору, гідроксилу, аміно-, метиламіно-, диметиламіно-груп та ацетилу, R7 - гідроген, метил, галоген (наприклад, хлор, флуор, йод або бром), гідроксил, метоксил, -С(=О)(С1С2алкіл), -С(=О)О(С1-С2алкіл), гідроксиметил, трифлуорметил або форміл, R10 - гідроген, гідроксил, метоксил або флуор; а R11 - гідроген або С1-С4алкіл, за умови, що в кільці, що включає D, Е, К та G за формулою І не може бути двох сусідніх подвійних зв'язків, а також фармацевтично прийнятні солі таких сполук. В прикладах конкретніших втілень формули І, що наведено далі, де X - оксиген, сульфур або NR8, де R8 визначено вище, кожна пунктирна лінія позначає, як варіант, подвійний зв'язок, a (Rn) представляє 0-4 замісники, кожний з яких позначено вище для формули І. Особливі втілення винаходу включають сполуки формули І, в яких В - -CHR1R2, -NR1R2, -NHCHR1R2, CHR1R2, -OCHR1R2, або -SCH R1R2, R1 - С1-С6алкіл, який, як варіант, може бути заміщеним одним гідроксилом, флуором, CF3 або С1-С4алкоксилом, і як варіант, включати один подвійний чи потрійний зв'язок, a R2 - бензил чи С1-С6алкіл, який, як варіант, може включати один подвійний чи потрійний зв'язок, і де, як варіант, вказані С1-С6алкіл та феніл бензила можуть бути заміщеним одним гідроксилом, флуором, хлором, С1-С2алкілом, CF3 або С 1-С2алкоксилом. Інші особливі втілення винаходу включають сполуки формули І, в яких В є або включає групу -NR1R2 або -CHR1R2R10, яка утворює насичений чи ненасичений 5-членний карбоцикл, в якому один з атомів карбону може, як варіант, бути заміщеним атомом оксигену чи сульфур у. Інші особливі втілення винаходу включають сполуки формули І, в яких R3 - метил, етил, хлор чи метоксил, кожний з R4, R6, R8 , R9 або R12 , незалежно - гідроген чи метил, a R5 - ді- чи тризаміщені феніл, піридил або піримідил, в яких до трьох замісників можна вибрати незалежно з групи, що включає С1С4алкіл, -О(С1-С4алкіл) та -(С1-С4алкілен)О(С 1-С4алкіл), а один з яких можна незалежно вибрати з групи, що включає -(С0-С1алкілен)-S-(С1-С2алкіл), -(С0-С1алкілен)-SO-(С1-С2алкіл), -(С0-С1алкілен)-SО2-(С1-С2алкіл), флуор, хлор, бром, йод, форміл, CF3, -OCF3, -СНО, (С1-С4алкілен)-OН, ціаногрупу, і де кожний С1-С4алкіл може, як варіант, включати один подвійний чи потрійний зв'язок. Інші особливі втілення винаходу включають сполуки формули І, в яких А - N, СН або ССН 3. Інші особливі втілення винаходу включають сполуки формули І, в яких G - N. Інші особливі втілення винаходу включають сполуки формули І, в яких G - С, а кільце, що включає D, Е, К та G є бензокільцем. Інші особливі втілення винаходу включають сполуки формули І, в яких G - N, D - NH чи N(метил), а Е---К - СН2-СН2, СН=СН, С(О)-СН2 або СН 2-С(О). Інші особливі втілення винаходу включають сполуки формули І, в яких G - N, а D---E---К - С(О)-О-СН2, СН2-О-СН2, С(О)-СН=СН , С(О)-СН2-СН2, СН2-СН2-СН2, СН2-СН2-СО, СН=СН-СО, СН=СН-СН 2, CH=CH-NH або CH=CH-NCH3. Прикладами конкретних сполук згідно з винаходом є 4-(бутил-етил-аміно)-2,6-диметил-8-(2,4,6-триметил-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он, 8-(1-етил-пропокси)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-(1-етил-пропокси)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 4-(1-етил-пропокси)-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 5-(1-етил-пропокси)-7-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, 5-(1-етил-пропокси)-7-метил-1-(2,4,6-триметил-феніл)-1,2-дигідро-3-окса-1,8-діаза-нафталін-4-он, 8-(1-етил-пропокси)-1,6-диметил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, (1-етил-пропіл)-[2-метил-8-(2,4,6-триметил-феніл)-хінолін-4-іл]-амін. Іншими прикладами сполук формули І є 4-(бутил-етил-аміно)-2,6-диметил-8-(2,6-диметил-4-бром-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин7-он, 4-(бутил-етил-аміно)-2-метил-8-(2,6-диметил-4-бром-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он, 4-(1-етил-пропокси)-2-метил-8-(2,6-диметил-4-бром-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он, (бутил-етил)-(2-метил-8-(2,6-диметил-4-бром-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (пропіл-етил)-[2-метил-8-(2,6-диметил-4-бром-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]амін, (діетил)-[2-метил-8-(2,6-диметил-4-бром-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (1-етил-пропіл)-[2-метил-8-(2,6-диметил-4-бром-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]амін, (1-етил-пропокси)-2-метил-8-(2,6-диметил-4-бром-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин, 4-(бутил-етил-аміно)-2-метил-8-(2,4,6-триметил-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-oн, 4-(1-етил-пропокси)-2-метил-8-(2,4,6-триметил-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он, (бутил-етил)-[2-метил-8-(2,4,6-триметил-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (пропіл-етил)-[2-метил-8-(2,4,6-триметил-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (діетил)-[2-метил-8-(2,4,6-триметил-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (1-етил-пропіл)-[2-метил-8-(2,4,6-триметил-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин-4-іл]-амін, (1-етил-пропокси)-2-метил-8-(2,4,6-триметил-феніл)-5,6,7,8-тетрагідро-піридо[2,3-d]піримідин, 8-(1-етил-пропокси)-6-метил-4-(2,6-диметил-4-бром-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-(1-етил-пропокси)-6-метил-4-(2,6-диметил-4-бром-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 4-(1-етил-пропокси)-2-метил-8-(2,6-диметил-4-бром-феніл)-хіноліл, 5-(1-етил-пропокси)-7-метил-1-(2,6-диметил-4-бром-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, 5-(1-етил-пропокси)-7-метил-1-(2,6-диметил-4-бром-феніл)-1,2-дигідро-3-окса-1,8-діаза-нафталін-4-он, 8-(1-етил-пропокси)-1,6-диметил-4-(2,6-диметил-4-бром-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, (1-етил-пропіл)-[2-метил-8-(2,6-диметил-4-бром-феніл)-хіноліл-4-іл]-амін, 4-(бутил-етил-аміно)-2,6-диметил-8-(2,6-диметил-4-хлор-феніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7oн, 8-(1-етил-пропокси)-6-метил-4-(2,6-диметил-4-хлор-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-(1-етил-пропокси)-6-метил-4-(2,6-диметил-4-хлор-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 4-(1-етил-пропокси)-2-метил-8-(2,6-диметил-4-хлор-феніл)-хінолін; 5-(1-етил-пропокси)-7-метил-1-(2,6-диметил-4-хлор-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, 5-(1-етил-пропокси)-7-метил-1-(2,6-диметил-4-хлор-феніл)-1,2-дигідро-3-окса-1,8-діаза-нафталін-4-он, 8-(1-етил-пропокси)-1,6-диметил-4-(2,6-диметил-4-хлор-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, (1-етил-пропіл)-[2-метил-8-(2,6-диметил-4-хлор-феніл)-хінолін-4-іл]-амін, 8-(1-гідроксилметил-пропокси)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2он, 8-(1-гідроксилметил-пропіламіно)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин2-он, 8-(1-етил-пропіламіно)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-діетиламіно-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-(етил-пропіл-аміно)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он, 8-(бутил-етил-аміно)-6-метил-4-(2,4,6-триметил-феніл)-3,4-дигідро-1Н-піридо [2,3-b]піразин-2-он, 8-(1-гідроксиметил-пропокси)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 8-(1-гідроксиметил-пропіламіно)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3b]піразин, 8-(1-етил-пропіламіно)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо(2,3-b]піразин, 8-діетиламіно-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 8-(етил-пропіл-аміно)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 8-(бутил-етил-аміно)-6-метил-4-(2,4,6-триметил-феніл)-1,2,3,4-тетрагідро-піридо[2,3-b]піразин, 4-(1-гідроксиметил-пропокси)-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 4-(1-гідроксиметил-пропіламіно)-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 4-(1-етил-пропіламіно)-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 4-діетиламіно-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 4-(етил-пропіл-аміно)-2-метил-8-(2,4,6-триметил-фент)-хінолін, 4-(бутил-етил-аміно)-2-метил-8-(2,4,6-триметил-феніл)-хінолін, 5-(1-гідроксиметил-пропокси)-7-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діазанафталін, 5-(1-гідроксиметил-пропіламіно)7-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діазанафталін, 5-(1-етил-пропіламіно)-7-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, 5-діетиламіно-5-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, 5-(етил-пропіл-аміно)-7-метил-1-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін, та 8-(бутил-етил-аміно)-6-метил-4-(2,4,6-триметил-феніл)-1,4-дигідро-2Н-3-окса-1,8-діаза-нафталін. Згідно з винаходом запропоновано також фармацевтичну композицію для лікування, попередження чи інгібування (а) розладів, лікування яких може здійснюватися чи посилюватися протидією ФВК, включаючи, але без обмеження, розлади, що викликані чи посилені ФВК, або (б) розлади, що вибрані з таких запальних розладів, як ревматоїдні артрити та остеоартрити, біль, астма, псоріаз та алергії, генералізований тривожний розлад, фобії, примусово-нав'язливі розлади, пост-травматичний стрес, індуковані стресом розлади сну, такі больові відчуття, як фіброміалгія, такі розлади настрою, як депресія, включаючи депресивний розлад повнолітніх, епізодичну депресію, рецидивну депресію, дитячу депресію, викликану зловживанням, розлади настрою, поєднані з предменструальним синдромом, постнатальну депресію, дистимію, біполярні розлади та циклотимію, синдром хронічної втоми, індукований стресом головний біль, рак, синдром подразнення кишечнику, хвороба Крона, спазми товстої кишки, пост-оперативна кишкова непрохідність, виразка, діарея, індукована стресом лихоманка, вірусні інфекції імунодефіциту людини (ВІЛ), такі нейродегенеративні хвороби, як хвороба Альцгеймера, хвороби Паркінсона та Хантингтона, шлунковокишкові захворювання, такі розлади харчування, як анорексія та невротична булімія, геморагічний стрес, хімічні залежності та звикання (наприклад, звикання до алкоголю, нікотину, кокаїну, героїну, бензодіазепіну, або інших ліків), симптоми відмови від ліків та алкоголю, викликані стресом психотичні напади, синдром еутиреозної слабкості, синдром несприйнятності антидіаретичного гормону (АДГ), ожиріння, безплідність, травми голови та спинного хребта, ішемічні нервові пошкодження (наприклад, така церебральна ішемія, як ішемія гіпокампа), нервове пошкодження від збудження, епілепсія, напад, імунні дисфункції, включаючи імунну дисфункцію від стресу (наприклад, синдром стресу свиней, сипний тиф корів, пароксизмальна фібриляція у коней, викликані обмеженням дисфункції у курей, стрес при стрижці баранів або викликаний спілкуванням людини з твариною стрес у собак), спазми м'язів, невтримання сечі, вікове слабоумство типу Альцгеймера, слабоумство від багатократного інфаркту, бічний аміотрофічний склероз, гіперчутливість, тахікардія, застійна серцева нестача, остеопороз, передчасні пологи та гіпоглікемія у ссаців, включаючи людину, композиція містить кількість сполуки формули І або її фармацевтично прийнятної солі, яка ефективна при лікуванні таких розладів, а також фармацевтично прийнятний носій. Згідно з винаходом запропоновано також спосіб лікування, попередження чи інгібування (а) розладів, лікування яких може здійснюватися чи посилюватися протидією ФВК, включаючи, але без обмеження, розлади, що викликані чи посилені ФВК, або (б) розлади, що вибрані з таких запальних розладів, як ревматоїдні артрити та остеоартрити, біль, астма, псоріаз та алергії, генералізований тривожний розлад, фобії, примусово-нав'язливі розлади, пост-травматичний стрес, індуковані стресом розлади сну, такі больові відчуття, як фіброміалгія, такі розлади настрою, як депресія, включаючи депресивний розлад повнолітніх, епізодичну депресію, рецидивну депресію, дитячу депресію, викликану зловживанням, розлади настрою, поєднані з предменструальним синдромом, постнатальну депресію, дистимію, біполярні розлади та циклотимію, синдром хронічної втоми, індукований стресом головний біль, рак, синдром подразнення кишечнику, хвороба Крона, спазми товстої кишки, постоперативна кишкова непрохідність, виразка, діарея, індукована стресом лихоманка, вірусні інфекції імунодефіциту людини (ВІЛ), такі нейродегенеративні хвороби, як хвороба Альцгеймера, хвороби Паркінсона та Хантингтона, шлунково-кишкові захворювання, такі розлади харчування, як анорексія та невротична булімія, геморагічний стрес, хімічні залежності та звикання (наприклад, звикання до алкоголю, нікотину, кокаїну, героїну, бензодіазепіну, або інших ліків), симптоми відмови від ліків та алкоголю, викликані стресом психотичні напади, синдром еутиреозної слабкості, синдром несприйнятності антидіаретичного гормону (АДГ), ожиріння, безплідність, травми голови та спинного хребта, ішемічні нервові пошкодження (наприклад, така церебральна ішемія, як ішемія гіпокампа), нервове пошкодження від збудження, епілепсія, напад, імунні дисфункції, включаючи імунну дисфункцію від стресу (наприклад, синдром стресу свиней, сипний тиф корів, пароксизмальна фібриляція у коней, викликані обмеженням дисфункції у курей, стрес при стрижці баранів або викликаний спілкуванням людини з твариною стрес у собак), спазми м'язів, невтримання сечі, вікове слабоумство типу Альцгеймера, слабоумство від багатократного інфаркту, бічний аміотрофічний склероз, гіперчутливість, тахікардія, застійна серцева нестача, остеопороз, передчасні пологи та гіпоглікемія у ссавців, включаючи людину, спосіб включає вживання особою, що потребує такого лікування, кількості сполуки формули І або її фармацевтично прийнятної солі, яка ефективна при лікуванні таких розладів. Згідно з винаходом запропоновано також спосіб лікування чи попередження розладів чи станів, лікування чи попередження яких може здійснюватися чи полегшуватися інгібуванням зв'язуючого ГВК білка у ссавців, включаючи людину, застосуванням вказаним ссавцем інгібуючої зв'язуючий ГВК білок кількості сполуки формули І або її фармацевтично прийнятної солі. Згідно з винаходом запропоновано також фармацевтичну композицію для лікування чи попередження розладів чи станів, лікування чи попередження яких може здійснюватися чи полегшуватися інгібуванням зв'язуючого ГВК білка у ссавців, включаючи людину, що містить інгібуючу зв'язуючий ГВК білок кількість сполуки формули І або її фармацевтично прийнятної солі, а також фармацевтично прийнятний носій. В рамки винаходу включено всі оптичні ізомери та інші стереоізомери сполук формули І. При наявності в цих сполуках одного чи більше хіральних центрів слід розуміти, що в рамки винаходу включено рацемічні суміші, індивідуальні енантіомери та діастереомери цих сполук , а також їх суміші. Сполуки згідно з винаходом включають ідентичні вищеописаним сполуки у випадках, коли один чи більше з атомів гідрогену, нітрогену чи карбону заміщено на їх ізотопи (наприклад, тритій чи карбон-14). Такі сполуки корисні при дослідах та діагностиці метаболізму, фармакокінетичних дослідах та аналізі зв'язування. Нижченаведені сполуки формул II-V корисні як інтермедіати при синтезі сполук формули І. У вищенаведених сполуках формул II-V Т - хлор, бром, йод або -OSO2CF3, W - ціаногруппа, -СНО або СОС(С0-С4алкіл), a A, D, Е, К, G, R 3 та R5 визначено раніше для формули І. Способи виготовлення сполук та композицій згідно з винаходом описано нижче. В обговоренні та нижченаведених схемах реакцій R1-R13, А, В, D, Е, К, G, Z, Z2 , Т та W визначено раніше, якщо не вказано інше. Сполуки формули І, в яких В - -NR1R2 або -NHCR1R2R11 можна виготовити реакцією сполуки формули II, в якій Т - хлор, бром чи йод, зі сполукою формули ВН у присутності основи та з такою металоорганічною сполукою або без неї, як Сu(І)Х, де X - хлор, бром чи йод або кислота (така, як п-тозил-ОН або інший стерично утруднений фенол), або аналогічний відомий спеціалістам агент. Придатні для реакції розчинники включають ДМСО, N-МП та ТГФ. ВН у надлишку можна використовувати як реагент і як основу. Можна використовува ти також такі основи, як карбонати чи (С1-С4)алкоксиди калію та натрію, тріетиламін або гідрид натрію. Коли R7 - така електронноакцепторнa група, як -СОО(С1-С4алкіл) або CN, реакцію звичайно проводять при температурах від кімнатної до 130°С. Коли R7 - не електронноакцепторнa група, температура реакції може звичайно бути в межах 50-270°С, а тиск в межах 27-2000кПа. Можна використовува ти автоклав. Сполуки формули І також можна виготовити реакцією сполуки формули II, в якій Т - бром чи йод, з одним еквівалентом чи надлишком ВН та такою основою, як карбонати чи (С1-С4)алкоксиди калію та натрію у присутності таких паладієвих(0 чи II) каталізаторів, як Рd(ОАс)2 або Рd(РН3)4 разом з такою рацемічною або хіральною сполукою, як 2,2-біс(дифенілфосфіно)-1,1-бінафтил (БІНАФ). Інакше можна використати попередньо виготовлений Рd(ІІ)(БІНАФ) безпосередньо в прийнятному інертному (тобто інертному з огляду на конкретну реакцію) розчиннику, як-то толуол, ксилол, діоксан або сульфолан при температурах від кімнатної до 180°С, краще під зворотним холодильником. Сполуки формули І, в яких В - -OCR1R2R11, -SCR1R2R11 або -NHCR1R2R11 можна виготовити реакцією сполуки формули II, в якій Т - хлор, бром чи йод, зі сполукою формули ВН у присутності основи, що. здатна депротонувати ВН (наприклад гідрид натрію чи калію, або така металоорганічна сполука, як діізопропіламід або біс(триметилсиліл)амід натрію чи літію, (С1-С4)алкоксид натрію або н-бутиллітий) у прийнятному інертному розчиннику, як-то бензол, толуол, ксилол, тетрагідрофуран, ацетонітрил, диметилсульфоксид, ацетон, (С1-С4)спирт, хлороформ, N,N-диметилформамід (ДМФ), метиленхлорид (MX), 1-метил-2 піролідинон (N-МП) або суміш двох чи більше вищенаведених розчинників (наприклад, ДМСО та ТГФ) при температурах 0-180°С, краще 50-180°С. Сполуки формули І, в яких В - -CR1R2R11, -C(C=CR2R12)R1, -CR2R11NHR1, -CR2R11OR1 , -CR2R11SR1 або C(O)R2, можна виготовити реакцією сполуки формули III, в якій W - ціаногрупа, форміл, або карбоксил, нижченаведеними способами. Реакцією сполуки формули III, в якій W - ціаногрупа, з реактивом Грин'яра, що містить групу R2, отримують сполуку формули І, в якій В - COR2. Подальшою реакцією сполуки формули І, в якій В - COR2, з реактивом Грин'яра, що містить групу R1 , отримують відповідну сполуку формули І, в якій В - CR1R2OH. Реакцією сполуки формули III, в якій W - форміл, з реактивом Грин'яра, що містить групу R2, о тримують відповідну сполуку формули І, в якій В - CHR2OH. Прийнятним розчинником для вищенаведеної реакції Грин'яра є етерний розчинник, як-то ТГФ етер, діоксан та глім. Сполуки формули І, в яких В - -CR1R2R11 або -C(C=CR2R12)R1, можна виготовити звичайними способами. Так, реакцією сполуки формули І, в якій В - -CR1·R2·OH (де R1· та R2· визначено як R1 та R2, відповідно, за винятком випадків, коли R1· може не бути R1, a R2· може не бути R2), з такою кислотою, як концентрована сульфатна в оцтовій кислоті, або така внутрішня сіль Бургесса, як метиловий естер гідроксиду (карбоксисульфамоїл)тріетиламмонія отримують сполуку формули І, в якій В - C(=CR 2R11)R1. Гідруванням сполуки формули І, в якій В - -C(=CR2R11)R1, з використанням як каталізатору паладію на вугіллі (Pd/C) або оксиду платини в (С1-С4)спиртовому розчиннику, етилацетаті, бензолі чи ТГФ отримують сполуку формули І, в якій В - -CHR1R2. Реакцією сполуки формули І, в якій В - -CR1R2OH, з трифлуоридом диметиламіносульфур у або трифенілфосфіном/тетрахлоркарбоном у такому інертному розчиннику, як тетрахлорид карбону, отримують сполуку формули І, в якій В - -CR1R2F або -CR 1R2CI, відповідно. Відновленням сполуки формули І, в якій В - -C(O)R2, борогідридом натрію в такому прийнятному інертному розчиннику, як (С1-С4)спирт, отримують сполуку формули І, в якій В - -CHR 2OH. Алкілуванням сполуки формули І, в якій В - -CHR 2OH, алкілгалогенідом (як-то алкілйодидом) у присутності такої основи, як гідрид натрію, приблизно при кімнатній температурі в такому інертному органічному розчиннику, як ДМФ, етер, ДМСО, діоксан або ТГФ, отримують сполуку формули І, в якій В - -CHR 2OR1. Сполуки формули І, в яких В - -CR2R10NHR1 можна виготовити такими звичайними способами, як відновне амінування відповідної сполуки формули І, в якій В - -COR2, прийнятним аміном та відновником (як-то ціаноборогідридом чи тріацетокси-борогідридом натрію або алюмогідридом літію) у такому прийнятному інертному розчиннику, як (С1-С4)спирт або оцтова кислота. Перетворення сполуки формули І, в якій В - -C(O)R2, у сполук у формули І, в якій В - -C(S)R2, можна здійснити стандартними добре відомими спеціалістам способами (наприклад, використовуючи реагент Лауссона або дифосфор пентасульфід P2S5). Відновленням сполуки формули І, в якій В - -C(S)R2, таким відновником, як борогідрид натрію в (С1-С4)спирті або алюмогідрид літію в ТГФ чи етері при температурі приблизно від кімнатної до кипіння розчинника, отримують сполуку формули І, в якій В - -CHR2SH. Алкілуванням сполуки формули І, в якій В - -CHR2SH, алкілгалогенідом (як-то алкілйодидом) у присутності такої основи, як гідрид натрію, при температурі приблизно від кімнатної до кипіння розчинника в такому інертному розчиннику, як ДМФ, отримують відповідну сполуку формули І, в якій В - -CHR 2SR1. Сполуки формули II можна виготовити зі сполук формул IV та V нижченаведеними способами. Сполуки формули II, в яких Т - хлор, бром чи йод, можна виготовити реакцією сполук формули IV з одним еквівалентом чи надлишком РОТ3, де Т - хлор, бром чи йод, у присутності чи відсутності ди(С1С4алкіл)аніліну, краще діетиланіліну, у розчиннику (як-то дихлоретан, ДМФ, ДМСО або ацетамід) чи без нього, при температурі від кімнатної до приблизно 180°С, краще 100-150°С. Сполуки формули II, в яких Т хлор, бром чи йод, можна інакше виготовити реакцією відповідних сполук формули II, де Т - OSO 2CF3 , з галогенідом калію чи натрію у прийнятному інертному розчиннику, як-то сульфолан, ДМФ, ДМСО або ацетонітрил), при температурі від 60°С до приблизно 180°С. Сполуки формули II, в яких Т - OSO2CF 3, можна виготовити реакцією сполук формули IV з Tf2О у присутності такої основи, як тріетиламін чи піридин, у такому прийнятному інертному розчиннику, як ТГФ, MX, діоксан, етер чи толуол, при температурі від 0°С до приблизно 50°С, краще від 0°С до кімнатної. Сполуки формули II, в яких Т - хлор, бром чи йод, можна виготовити також реакцією сполук формули V з ди(С 1-С7алкіл)нітритом та Сu(І)T2 (де Т - хлор, бром чи йод), у такому прийнятному інертному розчиннику, як ацетонітрил, ацетон ТГФ, MX, діоксан, бензол, толуол, дихлоретан, ДМФ, ДМСО або N-МП, при температурі від кімнатної до приблизно 150°С, краще 40-100°С. Сполуки формули III, в яких W - ціаногрупа, можна виготовити реакцією відповідних сполук формули II, в яких Т - хлор, бром чи йод, з ціанідами купруму, калію, натрію чи ди(С1-С4алкіл)алюмінію, у такому прийнятному інертному розчиннику, як толуол, ксилол, ДМФ або ДМСО, при температурі від кімнатної до приблизно 180°С, краще 60-150°С у присутності Pd(ll)OAC або Pd(0)(PPh3)4 чи без них. Сполуки формули III, в яких W - -СНО чи -СООН, можна виготовити реакцією відповідних сполук формули II, в яких Т - бром чи йод, з такими літій-органічними реагентами, як т-бутиллітій, в-бутиллпгій чи н-бутиллітій, у такому прийнятному інертному розчиннику, як ТГФ, MX, діоксан, бензол або етер, при температурі від приблизно -110°С до кімнатної, краще -110° - -60°С, з наступним гасінням таким прийнятним електрофілом, як ДМФ чи СО2 (газ чи сухий лід), з отриманням сполук формули III, в яких W - СНО чи -СООН, відповідно. Зрозуміло, що в усіх випадках, коли одна з наведених послідовностей реакцій може бути зміненою, можна застосовувати загальновідомі способи органічної хімії. Зміна послідовностей реакцій базується на можливості такої конкретної реакції на конкретній стадії послідовності, як використання протектуючих гр уп на будь-якій стадії синтезу, що цього потребує, або відновлення естерної групи до відповідного С 1-С4алкілу на будь-якій зручній стадії синтезу. Сполуки формули І, в яких R 3 - бром, хлор, -СОО(С1-С4алкіл) або СООН, можна перетворити на відповідні сполуки, в яких R3 - (С1-С4алкіл), -О(С1-С4алкіл), F або S(С1С4алкіл), описаними в літературі способами. Таке перетворення не обов'язково здійснювати на останній стадії конкретного синтезу, якщо це зручніше провести на ранішній стадії. Сполуки формули І або інших описаних тут формул, в яких R3 - -О(С1-С4алкіл) або -S(С1-С4алкіл), можна виготовити реакцією відповідних сполук, в яких R3 - бром, хлор чи йод, з такими нуклеофілами, як С 1 С4алканол або С1-С4алкантіол з органічною чи неорганічною основою. Придатні для цієї реакції такі основи, як натрій та гідрид натрію. Сполуки формули І або інших описаних тут формул, в яких R3 - флуор, можна виготовити реакцією відповідних сполук, в яких R3 - хлор, з флуоридом тетрабутиламонію в такому придатному інертному розчиннику, як ТГФ, MX або ДМСО (краще ТГФ), при температурі від кімнатної приблизно до 180°С. Відновленням сполук, в яких R 3 - естерна група, за допомогою LiАІH4/АІСІ3 у такому прийнятному інертному розчиннику, як ТГФ, діоксан, або етер, при температурі від кімнатної до приблизно 180°С, отримують відповідні сполуки, де R3 - метил. Конверсію сполук, в яких В - -СООН у відповідні сполуки, яких В - -СОО(С1-С3алкіл) можна здійснити добре відомими спеціалістам способами. Відновленням сполук, в яких В - -СОО(С1-С3алкіл), стандартними описаними в літературі способами отримують сполуки, в яких R3 - одне з різних похідних (С1-С4алкілу). Сполуки формули IV-а, в яких шостичленний цикл з правого боку представлено бензольним, піридиновим, піримідиновим чи піридазиновим кільцем, (Rn) представлено 0-3 позначеними для формули IV замісниками, a R3, R5 та R7 позначено вище для формули IV, можна виготовити наведеним на схемі 1 способом, починаючи зі сполуки формули IV-а, в якій шостичленний цикл з правого боку представлено бензольним, піридиновим, піримідиновим чи піридазиновим кільцем, (Rn) представлено 0-3 позначеними для формули IV замісниками, а X1 - Вr чи І. Сполуки формули Vll-a можна виготовити сполученням Сузукі, сполученням Стилла або біарильним синтезом Ульмана, що описано в літературі (див. Tetrahedron Lett., 37, 1043-1044, 1996, Tetrahedron, 36, 3111-4, 1995, J. Chem. Soc. Chem. Commun, 2551-2553, 1995, J. Org. Chem., 49, 5237-5243, 1984, Synlett, 765-766, 1995, Synlett, 207, 1992). Приклади придатних реакційних умов включають (а) реакцію сполуки формули IV-а, в якій X1 - Вr чи І, з R5-B(OH)2 та такою основою як водні карбонат чи гідроксид натрію, Ва(ОН)2, CS2CO3, К3PO4, 10%ТІОН, (С1-С4алкоксид) натрію чи калію, у присутності каталітичної кількості (0,5-50мол.%) сполуки Pd(0) чи Pd(ll) разом з рацемічним чи хіральним фосфіновим лігандом, краще Pd(PPh3)4, у такому прийнятному інертному розчиннику, як диметоксіетан (ДМЕ), ДМФ, бензол, диметилацетамід (ДМА), такий (С1-С6алканол), як етанол, діоксан або N-МП, при температурі від приблизно 25 до приблизно 150°С, краще від кімнатної до приблизно 120°С. Сполуки формули Vll-a можна інакше виготовити описаними в літературі способами (див. Tetrahedron, 49, 49-64, 1993, 1995, Chem. Ber., 93, 2479-2484, 1960, Can. J. Chem., 38, 445, 1960, Can. J. Chem., 38, 21522158, 1960, Pol. J. Chem., 66, 801-805, 1992, Chem. Pharm. Bull., 31, 3460-3464, 1983). Сполуки формули Vll-a можна виготовити відомими способами відновлення нітрогруп до аміногруп. Кращим способом є гідрування з використанням 5-10% Pd/C при тиску від 95 до 380кПа при кімнатній температурі в такому інертному розчиннику, як етилацетат (ЕА), бензол, ТГФ або (С1-С4алканол). Сполуки формули IV-a можна виготовити нагріванням сполук формули VIІІ-а сполуки формули R3-С(О)СН(В7)-СОО(С1-С2алкіл) у присутності кислоти або кислоти Льюїса з розчинником чи без нього. Приклади придатних реакційних умов включають (а) нагрівання в поліфосфатній кислоті, (б) нагрівання в толуолі, бензолі чи ксилолі в присутності кислотного каталізатору (як-то п-TsOH, сульфатна кислота, газуватий НСІ, використовуючи пастку Дин-Старка), та (в) нагрівання в такому придатному розчиннику, як дихлоретан, Рh2О або Dowterm А у присутності такої кислоти Льюїса, як SnCI4, ZnCI2/PCI або АІСІ 3. Сполуки формул IV-b та V-а, в яких шестичленний цикл з правого боку представлено бензольним, піридиновим, піримідиновим чи піридазиновим кільцем, (Rn) представлено 0-3 позначеними для формули IV замісниками, a R3, R5 та R7 позначено вище для формули IV, можна виготовити наведеним на схемі 2 способом, починаючи зі сполуки формули VI-b, в якій шестичленний цикл з правого боку представлено бензольним, піридиновим, піримідиновим чи піридазиновим кільцем, (Rn) представлено 0-3 позначеними для формули IV замісниками, X1 - Вr чи І, a W1 - CN, -CONH2 або -СОО(С1-С2алкіл). Конверсію сполук формули Vl-b у сполуки формули VlIl-b можна здійснити аналогічними описаним раніше способами для конверсії сполук формули Vl-a у сполуки формули Vlll-a. Сполуки формул IV-b та V-а можна виготовити нагріванням сполук формули Vlll-b, в яких W 1 - -СОО(С1-С2алкіл) та CN, відповідно, з прийнятним R 3-С(О)СН2-СОО(С1-С4алкілом) у присутності такої кислоти Льюїса, як SnCI4, ZnCl2, ТiСІ3 або АІСІ3 в ди хлоретані під зворотним холодильником, що показано схемою 2. Основним гідролізом сполук формул IV-b та V-а гідроксидом натрію в воді/(С1-С4cпирті) під зворотним холодильником або гідроксидом літію в воді/ТГФ або воді/діоксані при температурі між кімнатною та кипіння під зворотним холодильником, а потім декарбоксилуванням нагріванням на масляній бані при температурі 140-180°С одержують сполуки формул IV-с та V-b, відповідно. Сполуки формули IV-d можна виготовити наведеним на схемі 3 способом реакцією сполуки формули Vlll-b, в якій W1 - -СОО(С1-С2алкіл) або -CONH2, з (R3CO)2O, R3COOH або R3С(ОС 1-С2алкіл)3 в оцтовій кислоті або в такому прийнятному інертному розчиннику, як толуол, діоксан, ацетонітрил, MX або хлороформ, при температурі від приблизно 25 до приблизно 150°С, краще - кипіння під зворотним холодильником, а потім нагріванням у 85% фосфатній кислоті або такій водній кислоті, як оцтова, гідрохлоридна або сульфатна, краще - 50-85% фосфатна. Інакше, сполуки формули IV-d отримують нагріванням сполуки формули Vlll-b, в якій W1 - -СОO(С1-С2алкіл) або -CONH2, зі сполукою R3CONH2 при температурі від приблизно 180 до приблизно 230°С. Сполуки формули V-c можна виготовити наведеним на схемі 3 способом нагріванням сполуки формули Vlll-b, в якій W1 - CN, з надлишком сполуки R3CONH2 приблизно при температурі кипіння під зворотним холодильником. Сполуки формули I-А, в яких X - О, S або NR8, можна виготовити наведеним на схемі 4 способом, починаючи зі сполуки формули IX. Сполуки формули X, в яких R4 - Н, а X - О, можна виготовити відновленням відповідної сполуки формули IX, використовуючи, наприклад, LiAIH4 або гідрид діізобутилалюмінію в ТГФ, етиловому етері чи діоксані при температурі від кімнатної до кипіння під зворотним холодильником. Сполуки формули X, в яких R4 - Н, а X - S, можна виготовити стандартними відомими з літератури способами конверсії груп -СН2ОН у відповідні групи -CH2SH. Окисненням сполук формули X, в яких R4 - Н, а X - О, хлорохроматом піридину (ХХП), використовуючи відомі з літератури способи, можна отримати відповідні сполуки, що містять форміл. Реакцією Грин'яра (використовуючи реагент формули R4MgBr) з таким формілом отримують сполуки формули X, в яких R 4 визначено раніше для формули І. Відновним амінуванням такого формілу, використовуючи стандартні відомі з літератури способи, отримують сполуки формули X, в яких R4 - Н, а X - N. Інакше, конверсією карбонової кислоти сполуки формули IX у відповідну груп у -CONR 8, а потім відновленням з використанням ВН3·ДМС або LiAIH4 отримують сполуки формули X, в яких R4 - H, a X - NR 8. Сполуки формул І-А та І-С можна виготовити наведеним на схемі 4 способом, зі сполук формул X та IX, відповідно, реакцією сполук формули X, в яких X - О, S або NR8, зі сполуками формул R6CHO або R6СН(ОС1-С2алкіл)2 та кислотним каталізатором (як-то п-TsOH, НСІ, HBr, H2SO4) у такому інертному розчиннику, як бензол, толуол чи ксилол, краще - толуол, з 9-10 еквівалентами води при температурі приблизно від 70 до 160°С, з пасткою Дина-Старка або у присутності безводного сульфату натрію. Сполуки формул І-В та I-D можна виготовити реакцією сполук формул X та IX, відповідно, з трифосгеном або з тіофосгеном та такою основою, як тріетиламін або піридин у такому інертному розчиннику, як MX, ТГФ, діоксан, етер, бензол, хлороформ, краще - MX або сухий ТГФ, при температурі приблизно від 0 до 25°С. Сполуки формул I-G, 1-Е, I-Q та I-F можна виготовити наведеним на схемі 5 способом зі сполук формули X, в яких X - ОН. Сполуки формули XI можна виготовите реакцією сполук формули X з надлишком тіонілхлориду в безводному MX при кімнатній температурі. Надлишок розчинника та тіонілхлориду потім видаляють і залишок піддають дії сполуки, що має формулу Na-, К- чи Lі-СR4(СООС 1-С4алкіл)2 або Na-, Кчи Li-CR4(CN), у такому прийнятному розчиннику, як ДМС О, ТГФ, N-МП, сульфолан або С1-С4алканол при температурі від кімнатної до приблизно 100°С, краще при кімнатній. Сполуки формули I-Q можна виготовити відомими з літератури стандартними способами амідної циклізації, які включають кислотну циклізацію (як-то нагріванням у 40-85% фосфатній кислоті при температурі приблизно від 100 до 150°С, нагріванням у водній оцтовій кислоті/НСІ, або основним гідролізом, декарбоксилуванням, а потім амідною циклізацією). Сполуки формули І-Е можна виготовити бромуванням сполук I-Q з наступним елімінуванням такою основою, як DBU чи DBN. Сполуки формул I-G та I-F можна виготовити відновленням сполук І-Е та IQ, відповідно, такими стандартними способами, як нагрівання з ВН 3·ДМС, або ВН 3 чи Li АІH4 у ТГФ. Сполуки формул І-Н—I-L, в яких (Rn) представлено такими 0-3 такими замісниками, як R4, R6, R8, R9 тa 12 R , можна виготовити наведеним на схемі 6 способом, починаючи зі сполуки формули XII, в якій X - NR8, О або S. Сполуки формули XIII можна виготовити реакцією сполук формули XII з такими алкілгалогенідами, як X1CH(R8)CPL (X1 - хлор, бром, йод, мезилат або тозилат, a L - хлор, бром чи йод) у присутності такої основи, як три(С 1-С4алкіл)амін, піридин чи заміщений піридин, у такому прийнятному розчиннику, як MX, хлороформ, ТГФ, ДМСО, діоксан, етер або ДМЕ, при температурі приблизно від 0 до 100°С, краще від кімнатної приблизно до 60°С. Сполуки формули І-Н можна виготовити реакцією сполук формули XIII з такими основами, як натрій, гідриди натрію та калію, діізопропіламід та біс(триметилсиліл)амід літію, бутиллітій, діізопропіламід натрію та карбонати натрію та калію. Алкілуванням сполук формули І-Н основами з наступним гасінням алкілгалогенідами в такому прийнятному розчиннику, як MX, бензол, толуол, ТГФ, ДМСО, діоксан, етер або ДМЕ, разом з ГМФА чи без нього, при температурі приблизно від 78°С до кімнатної, отримують сполуки формули I-J. Придатні для цього основи включають діізопропіламід та біс(триметилсиліл)амід літію, бутиллітіи та діізопропіламід натрію. Реакцією сполук формул І-Н та I-J з таким відновником, як ВН3·ДМС, ВН3, гідрид діізобутилалюмінію чи LіАІН4, отримують сполуки формул І-К та I-І, відповідно. Реакцією сполук формул I-Н та I-J з РОСІ3 чи РСІ5 , а потім з таким металоорганічним реагентом, що містить групу R6, як R63 AI чи R62Zn, о тримують сполуки формул І-К та I-І з додатковим замісником R6 при наступному за групою N-R 5 атомі. Сполуки формул I-М—І-Р можна виготовити наведеними на схемі 7 способами, що аналогічні описаним на схемі 6. Утворення подвійного зв'язку, що показано формулами I-N, I-O та І-Р, можна досягти бромуванням з наступним елімінуванням стандартними описаними в літературі способами. Інакше сполуки формул I-N, I-O та І-Р можна виготовити реакцією сполук формули I-М з основами та гасінням PhSeSePh, PhSSO2Ph, PhSSOPh, PhSSPh, або еквівалентним реагентом з наступним окисненням NalO4 та елімінуванням основою. З моноциклічними піридиновими чи піримідиновими вихідними реагенами такі сполуки формул IX, X та XIV можна отримати способами, аналогічними описаним у Патентній заявці РСТ/ІВ95/00373, США, подано 18.05.1995 та опубліковано 21.12.1995. Солі приєднання кислот до сполук формул можна виготовити звичайними способами обробкою розчину чи суспензії відповідної вільної основи одним хімічним еквівалентом фармацевтично прийнятної кислоти. Для виділення солей можна застосовувати такі звичайні способи, як концентрування та кристалізацію. Прикладами придатних кислот є оцтова, молочна, янтарна, малеїнова, винна, лимонна, глюконова, аскорбінова, бензойна, цинамова, фумарова, суль фатна, фосфатна, гідрохлоридна, гідробромідна, гідройодидна, сульфамінoва, такі сульфонові кислоти, як метан-, бензол-, п-толуолсульфонова та споріднені кислоти. Сполуки формули І та їх фармацевтично прийнятні солі (позначені далі як активні сполуки згідно з винаходом) можна застосовувати поодинці або у комбінації з фармацевтично прийнятними носіями як одиничні або багатократні дози. Придатні фармацевтичні носії включають тверді інертні розріджувачі чи наповнювачі, стерильні водні розчини, масла, наприклад, арахісове та кунжутне, і різні органічні розчинники. Фармацевтичні композиції, що створені комбінуванням сполуки формули І з фармацевтично прийнятним носієм, можна легко вживати у вигляді таких різних дозованих форм, як таблетки, порошки, пастилки, емульсії, м'які масляні гелі, сиропи, розчини для ін'єкцій тощо. За бажанням, ці фармацевтичні композиції можуть додатково включати такі інгредієнти, як смакові, зв'язуючі, наповнюючі тощо. Так, для перорального вживання такі різні наповнювачі, як цитрат натрію, карбонат та фосфат кальцію, можна застосовувати разом з такими дезинтегруючими засобами, як крохмаль, метилцелюлоза, алгінова кислота та деякі складні силікати, разом з такими зв'язувачами, як полівінілпіролідон, сахароза, желатин та гуміарабік. Крім того, для таблетування корисні такі змащувачі, як стеарат магнію, лаурилсуль фат натрію та тальк. Тверді композиції такого типу можна також застосовувати для наповнення м'яких та твердих желатинових капсул. Кращі для цього матеріали включають лактозу чи молочний цукор та високомолекулярний поліетиленгліколь. Коли для перорального вживання бажані водні суспензії чи елексири, основний активній інгредієнт можна комбінувати з різними підсолоджувачами чи смаковими засобами, барвниками та, за бажанням, емульгуючими чи суспендуючими засобами разом з такими розріджувачами, як вода, етанол, пропіленгліколь, гліцерин та їх комбінації. Для парентерального вживання можна застосовувати розчини, що містять активні сполуки згідно з винаходом в арахісовий та кунжутній олії, водному пропіленгліколі або стерильному водному розчині. Такі водні розчини треба буферувати та робити ізотонічними сіллю чи глюкозою. Такі водні розчини особливо придатні для внутрішньовенних, вн утрішньом'язових, підшкірних та інтраперитональних застосувань. Застосовані стерильні водні розчини придатні для вживання добре відомими спеціалістам стандартними способами. Ефективне дозування активних сполук згідно з винаходом залежить від шляху застосування та таких факторів, як вік та маса лікуємого пацієнта, досвіду лікаря, а також лікуємої хвороби. Наприклад, добове дозування для індукованих стресом хвороб, запальних розладів, хвороби Альцгеймера, шлунково-кишкових захворювань, анорексії на нервовому грунті, геморагічного стресу та симптомів при відмові від ліків та алкоголю знаходиться в межах приблизно 0,1-50мг/кг маси лікуємого пацієнта. Способи визначення ФВК-антагоністичної активності активних сполук згідно з винаходом описано в Endocrinology, 116, 1653-1659, (1985) та Peptides, 10, 179-188, (1985). Активність сполук формули І відносно зв'язування, яку виражено величиною ІК50, звичайно знаходиться в межах приблизно 0,5-10000нМ. Способи визначення активності сполук формули І відносно інгібування ФВК-зв'язуючого білка описано в Brain Research, 745(1,2), 248-256, (1997). Винахід ілюстровано прикладами, зрозуміло, що винахід не обмежено конкретними деталями цих прикладів. Температури плавлення не скоректовано. Спектри 1Н ЯМР та 13С ЯМР виміряно в розчинах у дейтерохлороформі (CDCI3), а положення піків виражено як млн-1 відносно тетраметилсилану (ТМС). Розщеплення піків позначено так: s - синглет, d - дублет, t - триплет, q - квартет, m - мультиплет, b широкий. У прикладах використано скорочення: Ph - феніл, іРr - ізопропіл, МСВР - мас-спектр високого розрізнення. Приклад 1 4-(бутилетиламіно)-2,6-диметил-8-(2,4,6-триметилфеніл)-5,8-дигідро-6Н-піридо[2,3d]піримідин-7-он Суміш 75мг (0,227ммоль) 4-хлор-2,6-диметил-8-(2,4,6-триметилфеніл)-5,8-дигідро-6Н-піридо[2,3d]піримідин-7-ону та 65мг (0,682ммоль) N-бутилетиламіну в 1мл ДМСО гріли на масляній бані при 135°С протягом 15 годин, потім гасили водою та екстрагували етилацетатом (ЕА). Органічний шар сушили та концентрували, одержавши 114мг сирого матеріалу, який очищали на колонці з силікагелем з 5% ЕА в гексані як елюентом, отримавши 50мг потрібної сполуки як безбарвне масло. 1 Н ЯМР (CDCI3) d 6,95(s,1H), 6,94(s,1H), 3,2-3,55(m,4H), 2,88-3,05(dd,1H), 2,70-2,85(m,1H)) 2,552,70(m,1H), 2,35(s,3H), 2,25(s,3H), 2,05(s,3H), 1,97(s,3H), 1,5-1,65(m,2H), 1,3-1,5(m,2H), 1,35(d,3H), 1,2(t,3H), 0,98(t,3H). Приклад 2 8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-он До охолодженого розчину 40мг (0,099ммоль) 2-хлор-N-[4-(1-етилпропокси)-6-метил-2-(2,4,6триметилфеніламіно)-піридин-3-іл]ацетаміду в сухому ТГФ додали при -78°С 0,3мл (0,3ммоль) 1,0М розчину бістриметилсиліламіду літію (LiN(SiMe 3)2) в ТГФ і перемішували при цій температурі протягом 1 години, потім нагрівали до кімнатної протягом 0,5 години, гасили водою та екстрагували етилацетатом (ЕА). Органічний шар сушили та концентрували, одержавши 38мг потрібної сполуки як світлокоричневі кристали, які очищали на колонці з силікагелем з 5% ЕА в гексані як елюентом, отримавши 29мг (81%) потрібної сполуки як білі кристали. Т,пл, 179-181°С, 1Н ЯМР (CDCI3) d 7,75(s,1H), 6,95(s,2H), 6,09(s,1H), 4,22(s,2H), 4,22(m,1 H), 2,32(s,3H), 2,17(s,3H), 2,16(s,6H), 1,71(m,4H), 0,97(m,6H). Приклад 3 8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідро-1Н-піридо[2,3b]піразин Суміш 13мг (0,054ммоль) 8-(1-етилпропокси)-6-метил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Нпіридо[2,3-b]піразин-2-ону та 0,044мл (0,0884ммоль) 2М розчину комплексу борану з диметилсульфідом (ВН3·ДМС) в 2мл сухого ТГФ і нагрівали під зворотним холодильником протягом 2 годин, потім гасили 0,2мл метанолу та 0 ,2мл концентрованої НСІ та перемішували при кімнатній температурі протягом 2 години, і концентрували досуха, гасили водою, нейтралізували насиченим гідрокарбонатом натрію та екстрагували етилацетатом (ЕА). Органічний шар промивали розсолом, сушили та концентрували, одержавши 14,7мг потрібної сполуки як коричневі кристали, які очищали на колонці з силікагелем з 10% ЕА в гексані як елюентом, отримавши 9мг потрібної сполуки як безбарвне масло. 1 Н ЯМР (CDCI3) d 6,93(s,2H), 6,02(s,1H), 4,18(m,1H), 3,62(m,2H), 3,44(m,2H), 2,31(s,3H), 2,12(s,9H), 1,71(m,4H), 0,98(t,6H). Приклад 4 8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин2-он До охолодженого до -78°С розчину 50мг (0,136ммоль) 8-(1-етилпропокси)-6-метил-4-(2,4,6триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-b]піразин-2-ону в 3мл сухого ТГФ додали при -78°С 0,14мл (0,14ммоль) 1,0М розчину LiN(SiMe3)2 в ТГФ і перемішували при цій температурі протягом 20 хвилин, потім нагрівали до кімнатної температури і перемішували протягом ночі, гасили водою та насиченим хлоридом амонію і екстрагували етилацетатом (ЕА). Органічний шар промивали розсолом, сушили та концентрували, одержавши 51мг золотавого масла, які очищали на колонці з силікагелем з 10% ЕА в гексані як елюентом, отримавши 41мг (79%) потрібної сполуки як золотаве масло. 1 Н ЯМР (CDCI3) d 6,9(s,2H), 6,17(s,1H), 4,30(m,1H), 4,01(s,2H), 3,47(s,3H), 2,30(s,3H), 2,20(s,3H), 2,01 (s,6H), 1,70(m,4H), 0,97(t,6H). Приклад 5 4-(1-етилпропокси)-2-метил-8-(2,4,6-триметилфеніл)-хінолін До розчину 5,8мл (52,7ммоль) 3-пентанолу в 5мл сухого ТГФ порціями протягом 10 хвилин додали гідрид натрію, а потім розчин 4,0006г (13,52ммоль) 4-хлор-2-метил-8-(2,4,6-триметилфеніл)-хіноліну в 10мл сухого ТГФ і перемішували при цій температурі протягом 10 хвилин, потім додавали 15мл сухого ДМСО і гріли на масляній бані з температурою 12°С протягом 1,5 годин. Суміш гасили водою і екстрагували етилацетатом (ЕА). Органічний шар відділяли, сушили, фільтрували та концентрували, одержавши 5,002г потрібної жовтої твердої сполуки. 1 Н ЯМР (СOСI3) d 8,19(d,1H), 7,42(m,2H), 6,96(s,2H), 6,53(s,1H), 4,41(m,1H), 2,51 (s,3H), 2,36(s,3H), 1,89(s,6H), 1,84(m,4H), 1,02(t,6H). Жовту тверду сполук у пертворювали в її гідрохлорид та концентрували досуха і розтирали з гексаном, одержавши білувату тверду речовину, яку перекристалізовували з ЕА, отримавши 4,020г (78%) білих кристалів. Т,пл, 153-156°С, 1Н ЯМР (СOСI3) d 14,05(brs,1H), 8,33(dd,1H), 7,74(m,1H), 7,66(m,1H), 7,08(s,2H), 6,97(s,1H), 4,76(m,1H), 3,13(s,3H), 2,06(s,3H), 1,8-2,0(m,4H), 1,91(s,6H), 1,06(t,6H). Приклад 6 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1,4-дигідро-2Н-3-окса-1,8-діазанафталін Суміш 79мг (0,231ммоль) [4-(1-етилпропокси)-6-метил-2-(2,4,6-триметилфеніламіно)-піридин-3іл]метанолу та 0,1мл 37% водного розчину формальдегіду та 22мг (0,116ммоль) п-TsOH в 10мл толуолу нагрівали під зворотним холодильником з пасткою Дина-Старка протягом 3 годин, потім гасили водою та екстрагували етилацетатом (ЕА). Органічний шар відділяли, сушили та концентрували, одержавши 100мг сирого матеріалу, який очищали на колонці з силікагелем з 2% метанолом у хлороформі як елюентом, отримавши 40мг (50%) потрібної сполуки як прозоре масло. 1 Н ЯМР (CDCI3) d 6,90(s,2H), 6,04(s,1H), 4,87(2 набори s, 4Н), 4,16(m,1H), 2,28(s,3H), 2,19(s,3H), 2,14(s,6H), 1,67(m,4H), 0,94(t,6H). Приклад 7 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1,2-дигідро-3-окса-1,8-діазанафталін-4он Потрібну сполуку одержали аналогічно способу з прикладу 6, виходячи з 4-(1-етилпропокси)-6-метил-2(2,4,6-триметилфеніламіно)-нікотинової кислоти, отримавши потрібну сполуку як масло. 1 Н ЯМР (CDCI3) d 6,92(s,2H), 6,18(s,1H), 5,21(s,2H), 4,30(m,1H), 2,30(s,3H), 2,25(s,3H), 2,12(s,6H), 1,80(m,4H), 30 1,02(t,6H). Приклад 8 8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідропіридо[2,3b]піразин Суміш 50мг (0,131ммоль) 8-(1-етилпропокси)-1,6-диметил-4-(2,4,6-триметилфеніл)-3,4-дигідро-1Нпіридо[2,3-b]піразин-2-ону та 0,16мл (0,32ммоль) 2М ВН3·ДМС в 3мл сухого ТГФ і нагрівали під зворотним холодильником протягом 3 годин, потім гасили 0,5мл 1Н НСІ та перемішували при кімнатній температурі протягом 20 хвилин, і концентрували досуха, гасили водою, нейтралізували насиченим гідрокарбонатом натрію та екстрагували етилацетатом (ЕА). Органічний шар промивали розсолом, сушили та концентрували, одержавши 38мг потрібної сполуки як коричневі кристали, які очищали на колонці з силікагелем з 10% ЕА в гексані як елюентом, отримавши 22мг потрібної сполуки як безбарвне масло. 1 Н ЯМР (CDCI3) d 6,91(s,2H), 6,01(s,1H), 4,19(m,1H), 3,44(m,2H), 3,16(m,2H), 2,77 (s,3H), 2,29(s,3H), 2,12(s,3H), 2,07(s,6H), 1,75(m,4H), 0,99(t,6H). Приклад 9 (1-етилпропіл)-[2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-іл]амін Суміш 130мг (0,365ммоль) 4-бром-2-метил-8-(2,4,6-триметилфеніл)-хіноліну, 0,13мл (1,095ммоль) 1етилпропіламіну, 1,7мг (0,073ммоль) Pd(OAC)2 4,55мг (0,0073ммоль) БІНАФ та 49мг (0,51ммоль) тбутоксиду натрію в 2мл толуолу нагрівали протягом 5 годин на масляній бані з температурою 130-150°С, потім гасили водою і екстрагували ізопропіловим етером Органічний шар сушили та концентрували, одержавши 160мг сирого матеріалу, який очищали на колонці з силікагелем з 5®15% метанолом у хлороформі як елюентом, отримавши 78мг (62%) потрібної сполуки як світложовте масло. 1 Н ЯМР (CDCI3) d 7,80(m,1H), 7,38(т,1Н), 7,33(т,1Н), 6,96(s,2H), 6,28(s,1H), 3,45(т,1Н), 2,42(s,3H), 2,36(s,3H), 1,90(s,6H), 1,6-1,8(m,4H), 1,20(t,6H). Відповідний гідрохлорид виготовили як світложовтий твердий продукт. 1Н Я МР (CDCI3) d 9,87(brs,1H), 9,80(s,1H), 9,62(d,1H), 7,62(1,1Н), 7,44(d,1H), 6,33(s,1H), 3,62(m,1H), 2,55(s,3H), 2,37(s,3H), 2,34(s,3H), 30 2,15(m,4H), 1,87(s,6H), 0,97(t,6H). Приклад 10 2-метил-4-(тетрагідрофуран-3-ілокси)-8-(2,4,6-триметилфеніл)-хінолін Потрібну світложовту тверду сполуку одержали аналогічно способу з прикладу 5, виходячи з 3гідрокситетрагідрофурану та 4-хлор-2-метил-8-(2,4,6-триметилфеніл)-хіноліну. 1 Н ЯМР (CDCI3) d 8,17(d,1H), 7,39-7,46(m,2H), 6,96(s,2H), 6,49(s,1H), 5,13(m,1H), 4,14(d,2H), 3,84,1(m,4H), 2,51(s,3H), 2,36(s,3H), 2,15-2,20(m,2H), 1,89(s,6H). Приклад 11 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1H-[1,8]нафтиридин-2-он Суміш 100мг (0,219ммоль) диметилового естеру 2-[4-(1-етилпропіламіно)-6-метил-2-(2,4,6триметилфеніламіно)-піридин-3-ілметил]малонової кислоти, 3мл 85% фосфатної кислоти та 3мл води нагрівали під зворотним холодильником протягом 2 годин, охолоджували до кімнатної температури, розбавляли водою та екстрагували етилацетатом (ЕА). Органічний шар промивали розсолом, сушили безводним сульфатом магнію, фільтрували та концентрували досуха, одержавши 91мг потрібної сполуки як прозоре масло, яке очищали на колонці з силікагелем з 10% метанолом в MX (СН2СІ2) як елюентом, отримавши потрібну сполуку як світлокоричневі кристали. Т,пл, 138-140°С, 1Н ЯМР (CDCI3) d 6,93(s,2H), 6,31(s,1H), 4,21(m,1H), 2,93(m,2H), 2,76(m,2H), 2,31(s,3H), 2,19(s,3H), 20 1,99(s,6H), 1,71(m,4H), 0,96(t,6H). Приклад 12 5-(1-етилпропіламіно)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-[1,8]нафтиридин-2он Потрібну світлокоричневу тверду сполуку одержали аналогічно способу з прикладу 11, виходячи з диметилового естеру 2-[4-(1-етилпропіламіно)-6-метил-2-(2,4,6-триметилфеніламіно)-піридин-3ілметил]малонової кислоти та водної фосфатної кислоти. 1 Н ЯМР (CDCI3) d 6,91(s,2H), 6,09(s,1H), 3,68(d,1H), 3,33(m,1H), 2,82(m,2H), 2,67(m,2H), 2,30(s,3H), 2,12(s,3H), 1,99(s,6H), 1,5-1,7(m,4H), 0,94(t,6H). Приклад 13 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1Н-піридо[2,3-d]піримідин2-он До суміші 100мг (0,293ммоль) 3-амінометил-4-N-(1-етилпропіл)-6-метил-2-N-(2,4,6-триметилфеніл)піридин-2,4-діаміну в сухому ТГФ додали при 0°С 34мг (0,114ммоль) трифосгену, потім залишили поступово нагріватися до кімнатної температури і перемішували протягом 1 години, гасили водою та екстрагували етилацетатом (ЕА). Органічний шар сушили та концентрували досуха, одержавши 100мг (92,5%) світло коричневого твердого матеріалу, який очищали на колонці з силікагелем з 20®40% ЕА в гексані як елюентом, отримавши 75мг (69,4%) потрібної сполуки як білі кристали. Т,пл, 258-260°С, 1Н ЯМР (CDCI3) d 6,92(s,2H), 6,24(s,1H), 5,19(s,1H), 4,48(s,2H), 4,20(m,1H), 2,30(s,3H), 2,19(s,3H), 2,07(s,6H), 1,67(m,4H), 0,94(t,6H). Приклад 14 5-(1-етилпропокси)-2,6-диметил-8-(2,4,6-триметилфеніл)-8Н-птеридин-7-он До розчину 100мг (0,305моль) 6-(1-етилпропокси)-2-метил-4-N-(2,4,6-триметилфеніл)-піримідин-4,5діаміну в 2мл сухого етанолу додали 30мг (0,335ммоль) піровиноградної кислоти, нагрівали під зворотним холодильником протягом 1 години, додали ще 60мг піровиноградної кислоти і нагрівали під зворотним холодильником протягом ночі, потім гасили водою та екстрагували хлороформом. Органічний шар промивали водою та розсолом, сушили сульфатом натрію, фільтр ували та концентрували, одержавши залишок, як масло, яке очищували на колонці з силікагелем з 0®15% ЕА в гексані як елюентом, отримавши 75мг (69,4%) жовтої твердої потрібної сполуки. 1 Н ЯМР (CDCI3) d 6,99 (s,2H), 5,39(m,1H), 2,61 (s,3H), 2,40(s,3H), 2,35(s,3H), 1,88(s,6H), 1,7-1,9(m,4H), 0,99(t,6H). Приклад 15 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-1,2,3,4-тетрагідро-[1,8]нафтиридин Потрібну сполуку одержали як прозоре масло з виходом 86% аналогічно способу з прикладу 8, виходячи з 5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл)-3,4-дигідро-1H-[1,8]нафтаридин-2-ону та ВН3·ДМС у ТГФ. 1 Н ЯМР (CDCI3) d 6,90(s,2H), 5,95(s,1H), 4,13(m,1H), 3,40(m,2H), 2,71(m,2H), 2,28(s,3H), 2,14(s,3H), 2,08(s,6H), 1,99(m,2H), 1,67(m,4H), 0,94(t,6H). Приклад 16 8-(1-етилпропокси)-2,6-диметил-4-(2,4,6-триметилфеніл)-4Н-піридо[2,3-b]піразин-3-он Суміш 250мг (0,763ммоль) 4-(1-етилпропокси)-6-метил-N-2-(2,4,6-триметилфеніл)-піридин-2,3-діаміну та 67мг (0,763ммоль) піровиноградної кислоти в 8мл сухого етанолу, нагрівали під зворотним холодильником протягом ночі, потім охолоджували і утворений блідожовтий кристалічний осад відфільтровували, одержавши 83мг потрібної сполуки з т.пл. 215-217°С. Фільтрат концентрували досуха, одержавши ще 200мг жовтої твердої потрібної сполуки. 1 Н ЯМР (CDCI3) d 6,98(s,2H), 6,53(s,1H), 4,37(m,1H), 10 2,61(s,3H), 2,34(s,3H), 1,87(s,6H), 1,8-2,0(m,4H), 1,04(t,6H). Титульні сполуки з прикладів 17 та 18 було виділено, починаючи з 4-(1-етилпропокси)-6-метил-2-(2,4,6триметилфеніламіно)-нікотинаміду та трифосгену аналогічно способу з прикладу 13. Приклад 17 4-хлор-5-(1-етилпропокси)-7-метил-1-(2,4,6-триметилфеніл-1Н-піридо[2,3-d]піримідин-2-он Білі кристали, т,пл, 125-127°С, 1Н ЯМР (CDCI3) d 6,93(s,3H), 6,56(s,1H), 4,31(m,1H), 2,35(s,3H), 2,34(s,6H), 2,30(s,3H), 1,76(m,4H), 0,97(t,6H). Титульні сполуки з прикладів 18 та 19 було виготовлено, починаючи з [2-(4-бром чи хлор-(2,6диметилфеніламіно)-4-(1-етилпропокси)-6-метилпіридин-3-іл]метанолу та 37% водного формальдегіду аналогічно способу з прикладу 6. Приклад 18 1-(4-бром-2,6-триметилфеніл)-5-(1-етилпропокси)-7-метил-1,4-дигідро-2Н-3-окса-1,8діазанафталін Потрібна сполука є прозорим маслом. 1 Н ЯМР (CDCI3) d 7,20(s,2H), 6,05(s,1H), 4,85(s,2H), 4,83(s,2H), 4,14(m,1H), 2,17(s,3H), 2,12(s,6H), 1,65(m,4H), 0,92(t,6H). Біла тверда сіль гідрохлориду, т.пл. 206-209°С. 1Н ЯМР (CDCI3) d 14,5(brs,1H), 7,31(s,2H), 6,23(s,1H), 4,84(s,2H), 4,81(s,2H), 4,34(m,1H), 2,76(s,3H), 2,20(s,6H), 1,72(m,4H), 0,94(t,6H). Приклад 19 1-(4-хлор-2,6-триметилфеніл)-5-(1-етилпропокси)-7-метил-1,4-дигідро-2Н-3-окса-1,8діазанафталін Потрібна сполука є прозорим маслом. 1 Н ЯМР (CDCI3) d 7,07(s,2H), 6,07(s,lH), 4,87(s,2H), 4,85(s,2H), 4,17(m,1H), 2,19(s,3H), 2,15(s,6H), 1,67(m,4H), 0,95(t,6H) ppm, Біла тверда сіль гідрохлориду, т, пл, 190-192°С. 1H ЯМР (CDCI3) d 14,5(brs,1H), 7,26(s,2H), 6,27(s,1H), 4,87(s,2H), 4,85(s,2H), 4,37(m,1H), 2,78(s,3H), 2,23(s,6H), 1,74(m,4H), 0,97(t,6H). Синтез A 2-ocnop-N-[4-(1-етилпропокси)-6-метил-2-(2,4,6-триметилфеніламіно)-піридин-3-іл]ацетамід До охолодженого розчину 103мг (0,315ммоль) 4-(1-етилпропокси)-6-метил-N-2-(2,4,6-триметилфеніл)піридин-2,3-діаміну в 4мл сухого ТГФ додали при 0°С 36мг (0,315ммоль) хлорацетилхлориду та 32мг (0,315ммоль) тріетиламіну в ТГФ, потім нагрівали до кімнатної температури і перемішували протягом ночі, гасили водою та екстрагували етилацетатом (ЕА). Органічний шар сушили та концентрували, одержавши 125мг коричневого залишку, який очищали на колонці з силікагелем з 10% ЕА в гексані як елюентом, отримавши 59мг світлокоричневої твердої потрібної сполуки. Т,пл, 79-82°С, 1H ЯМР (CDCI3) d 8,15(brs,1H), 6,87(s,2H), 6,78(s,1H), 6,14(s,1H), 4,20(m,1H), 4,19(s,2H), 2,28(s,3H), 2,24(s,3H), 2,16(s,6H). Синтез Б 4-хлор-216-диметил-8-(2,4,6-триметилфеніл)-5,8-дигідро-6Н-піридо[2,3-d]піримідин-7-он Суміш 173мг (0,46ммоль) етилового естеру 3-[4-хлор-2-метил-6-(2,4,6-триметилфеніламіно)-піримідин5-іл]-2-метилпропіонової кислоти та 56мг n-TsOH в 10мл толуолу нагрівали під зворотним холодильником з пасткою Дина-Старка протягом 9 годин, гасили водою та екстрагували етилацетатом (ЕА). Органічний шар промивали розсолом, сушили та концентрували досуха, одержавши 184мг сирого матеріалу, який очищали на колонці з силікагелем з 10% етилацетатом у гексані як елюентом, отримавши 95мг потрібної сполуки як білі кристали з т.пл. 136-139°С, після перекристалізації з етилового етеру. 1 Н ЯМР (CDCI3) d 6,95(s,1H), 6,94(s,1H), 3,25(dd,1H), 2,8-3,0(m,2H), 2,41(s,3H), 2,32(s,3H), 1,96(s,3H), 1,93(s,3H), 1,37(d,3H). Синтез В 2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-ол Суміш 607мг (2,88ммоль) 2',4',6'-триметилбіфеніл-2-іламіна та 607мг (5,75ммоль) метилацетилацетону в 3мл поліфосфатної кислоти нагрівали на масляній бані з температурою 170°С протягом 2,5 годин, гасили водою та двічі екстрагували хлороформом. Органічний шар промивали розсолом, сушили та концентрували, одержавши 91мг потрібної сполуки як масло, яке відкачували у вакуумі, потім розтирали в суміші етеру з гексаном, одержавши 642мг (81%) бежевої твердої потрібної сполуки, яку перекристалізовували з етилацетату отримавши бежеву тверду сполуку з т.пл. >250°С. 1Н ЯМР (CDCI3) d 8,31(d,1H), 7,9(brs,1H), 7,40(m,1H), 7,34(m,1H), 7,01(s,2H), 6,26(s,1H), 2,33(s,3H), 2,26(s,3H), 1,6(s,3H), 1,93(s,3H), 1,37(d,3H). Синтез Г 4-хлор-2-метил-8-(2,4,6-триметилфеніл)-хінолін Суміш 335мг (1,21ммоль) 2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-олу та 2,5мл РОСІ3 нагрівали на масляній бані з температурою 130°С протягом 3 годин, охолоджували, виливали у воду з льодом та екстрагували етилацетатом. Органічний шар промивали розсолом, сушили та концентрували, одержавши 350мг сирого матеріалу як коричневе масло, яке очищали на колонці з силікагелем з хлороформом як елюентом, отримавши 316мг (87%) потрібної сполуки як жовте масло. 1Н ЯМР (CDCI3) d 8,20(d,1H), 7,60(m,1H), 7,47(d,1H), 7,35(s,1H), 6,97(s,2H), 2,54(s,3H), 2,36(s,3H), 1,86(s,6H). Синтез Д Естер 2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-олу з трифлуорметансульфоновою кислотою Суміш 416мг (1,5ммоль) 2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-олу, 508мл (1,8ммоль) трифлатного ангідриду та 182мг (1,8ммоль) тріетиламіну в 5мл MX перемішували при кімнатній температурі протягом години, гасили водою та екстрагували хлороформом. Органічний шар промивали розсолом, сушили та концентрували, одержавши 587мг коричневої склоподібної потрібної сполуки, яку використовували безпосередньо в наступній реакції. 1Н ЯМР (CDCI3) d 8,02(d,1H), 7,65(t,1H), 7,55(d,1H), 7,24(s,1H), 6,97(s,2H), 2,62(s,3H), 2,37(s,3H), 1,85(s,6H). Синтез E 4-бром-2-метил-8-(2,4,6-триметилфеніл)-хінолін Суміш 426мг (1,0ммоль) естеру 2-метил-8-(2,4,6-триметилфеніл)-хінолін-4-олу з трифлуорметансульфоновою кислотою та 809мг (1,1ммоль) броміду калію в суміші 1мл ДМСО та 3мл ТГФ нагрівали на масляній бані з температурою 120°С протягом 3 годин, охолоджували, гасили водою та екстрагували етилацетатом. Органічний шар сушили та концентрували, одержавши 358мг білуватої твердої потрібної сполуки. 1 Н ЯМР (CDCI3) d 8,16 (m,1H), 7,59(m,1H), 7,56(s,1H), 7,48(m,1H), 6,97(s,1H), 2,53(s,3H), 2,37(s,3H), 1,87(,6H).
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted 6,6-hetero-bicyclic derivatives
Назва патенту російськоюЗамещенные 6,6-гетеро-бициклические производные
МПК / Мітки
МПК: A61P 15/00, A61P 1/12, A61P 25/16, A61P 31/00, A61K 31/4985, A61P 43/00, A61K 31/435, A61P 25/20, A61P 35/00, A61K 31/529, C07D 215/18, A61P 15/06, A61P 31/18, A61P 3/04, A61P 13/00, A61P 37/04, A61K 31/00, A61P 3/00, A61P 3/02, A61P 25/04, A61K 31/505, C07D 405/12, A61P 25/30, A61P 25/24, C07D 498/04, A61P 21/02, A61P 13/02, C07D 215/22, A61K 31/519, A61P 5/24, A61K 31/5365, A61K 31/4353, A61P 1/00, A61P 1/04, A61P 25/08, A61P 29/00, C07D 471/04, A61P 25/28, A61K 31/4704, A61P 25/22, A61K 31/495, A61P 15/08, C07D 215/233, A61P 5/42, A61K 31/535, A61K 31/4709, A61P 21/00, A61K 31/47, A61P 37/00, C07D 215/42, A61K 31/4375, C07D 475/00, A61P 1/14
Мітки: фармацевтична, спосіб, лікування, 6,6-гетеробіциклічні, проміжні, розладів, заміщені, інгібування, похідні, попередження, сполуки, композиція
Код посилання
<a href="https://ua.patents.su/16-66345-zamishheni-66-geterobiciklichni-pokhidni-promizhni-spoluki-farmacevtichna-kompoziciya-ta-sposib-likuvannya-poperedzhennya-abo-ingibuvannya-rozladiv.html" target="_blank" rel="follow" title="База патентів України">Заміщені 6,6-гетеробіциклічні похідні, проміжні сполуки, фармацевтична композиція та спосіб лікування, попередження або інгібування розладів</a>
Попередній патент: Похідні антрациклінону і антрацикліну як діагностичний агент та фармацевтична композиція
Наступний патент: Пристрій для навчання письму з звуковим та світловим супроводженням
Випадковий патент: Лікарський засіб для інтраспінального введення на основі 3-(1н-імідазол-4-ілметил) індан-5-олу, спосіб індукування аналгезії, спосіб лікування ссавця (варіанти)