Похідні b-карболіну, корисні як інгібітори фосфодіестерази
Формула / Реферат
1. Сполука формули (І):
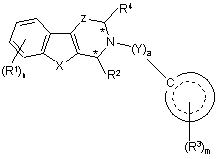 ,(I),
,(I),
де
R1 є незалежно вибраним з групи, що складається з галогену, нітрогрупи, гідроксигрупи, С1-С8алкілу, С1-С8алкоксигрупи, -NH2, -NHRА-, -N(RА)2, -O-RА, -С(О)NH2, -C(О)NHRA, -C(О)N(RA)2, -NС(O)-RA, -SO2NHRA, -SO2N(RA)2, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох);
де кожний RA є незалежно вибраним з групи, що складається з С1-С8алкілу, арилу (заміщеного, при потребі, RB у кількості від одного до трьох), С1-С8аралкілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох);
де кожний RB є незалежно вибраним з групи, що складається з галогену, гідроксигрупи, нітрогрупи, ціаногрупи, С1-С8алкілу, С1-С8алкоксигрупи, С1-С8алкілкарбонілу, карбоксиС1-С8алкілу, С1-С8алкілсульфонілу, трифторметилу, трифторметоксигрупи, аміногрупи, ацетиламіногрупи, ді(С1-С8алкіл)аміногрупи, ді(С1-С8алкіл)аміноС1-С8алкоксигрупи, ді(С1-С8алкіл) аміноацетилС1-С8алкілу, ді(С1-С8алкіл)аміноацетиламіногрупи, карбоксіС1-С8алкілкарбоніламіногрупи, гідроксіС1-С8алкіламіногрупи, NHRA, N(RA)2 та
гетероциклоалкілС1-С8алкоксигрупи;
n є цілим числом від 0 до 4;
Х є незалежно вибраним з групи, що складається з О, S та NRD;
де RD є вибраним з групи, що складається з водню, гідроксигрупи, -ORA, С1-С8алкілу, (де алкіл є, при потребі, заміщеним замісниками у кількості від одного до трьох, незалежно вибраними з галогену, карбоксигрупи, аміногрупи, С1-С8алкіламіногрупи, ді(С1-С8алкіл)аміногрупи, С1-С8алкоксикарбонілу, гетероарилу або гетероциклоалкілу), гетероарилу та гетероарилкарбонілу (де гетероарил може бути заміщеним, при потребі, фенілом або заміщеним фенілом, де замісниками фенілу є RВ у кількості від одного до трьох);
R2 є вибраним з групи, що складається з С5-С10алкілу (заміщеного, при потребі, RС у кількості від одного до трьох), арилу (заміщеного, при потребі, RВ у кількості від одного до трьох), гетероарилу (заміщеного, при потребі, RВ у кількості від одного до трьох), гетероциклоалкілу (заміщеного, при потребі, RВ у кількості від одного до трьох);
де RС є незалежно вибраним з групи, що складається з галогену, гідроксигрупи, нітрогрупи, NH2, NHRA та N(RA)2;
Z є вибраним з групи, що складається з СН2, СНОН та С(О); при умові, що коли Z є СНОН або С (О), тоді Х є NH;
R4 є вибраним з групи, що складається з водню, гідроксигрупи, карбоксигрупи, С1-С6алкілкарбонілу, С1-С6алкоксикарбонілу, ді(С1-С8алкіл)аміноалкоксикарбонілу, ді(С1-С8алкіл)аміноС1-С8алкіламінокарбонілу та –CORF;
RF є вибраним з групи, що складається з С1-С8алкілу, NH2, NHRA, NRA2, -С1-С8алкіл-NH2, -C1-C8алкіл-NHRA, -C1-C8aлкіл-NRА2 та -NH-С1-С8алкіл-NRA2;
а є 1;
Y є вибраним з групи, що складається з С(О), С(О)О, С(О)-NH та SО2;
![]() є вибраним з групи, що складається з нафтилу та гетероциклоалкілу;
є вибраним з групи, що складається з нафтилу та гетероциклоалкілу;
m є цілим числом від 1 до 2;
R3 є незалежно вибраним з групи, що складається з галогену, нітрогрупи, С1-С8алкілу, С1-С8алкоксигрупи, трифторметилу, трифторметоксигрупи, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох), фенілсульфонілу, нафтилу, С1-С8аралкілу, гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох), NH2, NHRA та N(RA)2;
при умові, що коли ![]() є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
та її фармацевтичнo прийнятні солі.
2. Сполука за п. 1, яка відрізняється тим, що
n є 0;
Х є вибраним з S або NRD, де RD є вибраним з групи, що складається з водню, галоС1-С6алкілу, ді(С1-4алкілу)аміноС1-С6алкілу, гетероарилу, гетероарилС1-С4алкілу, гетероциклоалкілС1-С4алкілу, карбоксіС1-С4алкілу, С1-С4алкоксикарбонілС1-С4алкілу та гетероарилкарбонілу; де гетероарил є додатково заміщеним, при потребі, фенілом або заміщеним фенілом, де замісники на фенілі від одного до двох є незалежно вибраними з RB;
де кожний RB є незалежно вибраними з групи, яка складається з галогену, нітрогрупи, С1-С4алкілу, С1-С4алкокси, трифторметилу, трифторметокси, аміно та ді(С1-С4алкіл)аміно;
R2 є вибраним з групи, яка складається з 3,4-метилендіоксифенілу, 3,4-(дифтор)метилендіоксифенілу, 2,3-дигідробензофурилу, 2,3-дигідробензо-[1,4]-оксин-6-ілу, піридилу, фенілу та заміщеного фенілу; де фенільними замісниками є від одного до двох замісників, незалежно вибраних з галогену, С1-С4алкілу, С1-С4алкоксигрупи, трифторметилу, ціаногрупи, нітрогрупи, С1-С4алкоксикарбонілу, ді(С1-С4алкіл)аміно або ді(С1-С4алкіл)аміноС1-С4алкоксигрупи;
R4 є вибраним з групи, яка складається з водню, карбоксигрупи, С1-С4алкоксикарбонілу, ди(С1-С4алкіл) аміноС1-С4алкоксикарбонілу та ди(С1-С4алкіл)аміноС1-С4алкіламінокарбонілу;
Y є вибраним з групи, яка складається з С(О), SO2 та CH2;
![]() є вибраним з групи, яка складається з нафтилу та гетероарилу;
є вибраним з групи, яка складається з нафтилу та гетероарилу;
R3 є незалежно вибраним з групи, яка складається з галогену, нітрогрупи, С1-С4алкілу, С1-С4алкоксигрупи, трифторметилу, С1-С4аралкілу, піразинілу, піридилу, галогензаміщеного піридилу, диметил заміщеного імідазолілу, фенілу, фенілсульфонілу та заміщеного фенілу; де замісники на фенілі є одним або більше замісниками незалежно вибраними з галогену, гідроксигрупи, С1-С4алкілу, С1-С4алкоксигрупи, трифторметилу, трифторметоксигрупи, нітрогрупи, аміногрупи, ацетиламіно, С1-С4алкілсульфонілу, карбоксіС1-С4алкілкарбоніламіногрупи, гідроксіС1-С4алкіламіногрупи, ді(С1-С4алкіл)аміноС1-С4алкоксигрупи, ді(С1-С4алкіл)аміноацетиламіногрупи або гетероциклоалкілС1-С4алкоксигрупи;
при умові, що коли ![]() є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
та її фармацевтичнo прийнятні солі.
3. Сполука за п. 2, яка відрізняється тим, що
Х є вибраним з S або NRD, де RD є вибраним з групи, яка складається з водню, ди(метил)аміноетилу, ди(метил)аміно-n-пропілу, ді(етил)аміноетилу, ді(етил)аміно-n-бутилу, N-піролідинілетилу, N-морфолінілетилу, 2-піридилметилу, 4-піридилметилу, 5-(4-метилфеніл)-2-піримідинілу, карбоксиметилу, карбоксіетилу, 4-хлор-n-бутилу, 2-(5-(3-трифторметилфеніл)фурил)карбонілу, 2-(5-(3-нітрофеніл)фурил)карбонілу, метоксикарбонілметилу, метоксикарбонілетилу та 2-бензоксазолілу;
R2 є вибраним з групи, яка складається з фенілу, 3,4-метилендіоксифенілу, 3,4-(дифтор)метилендіоксифенілу, 2,3-дигідробензофурилу, 2,3-дигідробензо-[1,4]оксин-6-ілу, 4-піридилу, 3-піридилу, 4-ціанофенілу, 3-нітрофенілу, 4-нітрофенілу, 4-трифторметилфенілу, 4-метоксифенілу, 3,4-диметилфенілу, 3,5-диметилфенілу, 3,4-диметоксифенілу, 3-трифторметил-4-хлорфенілу, 3,4-дихлорфенілу, 4-хлорфенілу, 4-метоксикарбонілфенілу, 3,4-диметоксифенілу, 4-(диметиламінo)фенілу та 4-(N-(3-диметиламіно)-n-пропокси)фенілу;
R4 є вибраним з групи, яка складається з водню, карбоксигрупи, диметиламіноетоксикарбонілу, диметиламіноетиламінокарбонілу та метоксикарбонілу;
![]() є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2-фурилу, 3-фурилу, 2-бензофурилу, 2-тієнілу, 2-бензотієнілу, 2-бензотіазолілу, 2-бензоксазолілу, 2-бензимідазолілу, 4-тіазолілу, 2-тіазолілу, 3-піразолілу, 4-піразолілу, 5-піразолілу, 3-(1,2,5-триазоліл), 4-ізоксазолілу, 2-піридилу та 3-піридилу;
є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2-фурилу, 3-фурилу, 2-бензофурилу, 2-тієнілу, 2-бензотієнілу, 2-бензотіазолілу, 2-бензоксазолілу, 2-бензимідазолілу, 4-тіазолілу, 2-тіазолілу, 3-піразолілу, 4-піразолілу, 5-піразолілу, 3-(1,2,5-триазоліл), 4-ізоксазолілу, 2-піридилу та 3-піридилу;
R3 є незалежно вибраним з групи, яка складається з хлору, брому, метилу, n-пропілу, t-бутилу, метоксигрупи, трифторметилу, нітрогрупи, фенілу, бензилу, фенілсульфонілу, 4-гідроксифенілу, 4-хлорфенілу, 4-метилфенілу, 3,4-диметоксифенілу, 3-трифторметилфенілу, 4-трифторметилфенілу, 5-трифторметилфенілу, 4-метоксифенілу, 2-нітрофенілу, 3-нітрофенілу, 4-нітрофенілу, 3-амінофенілу, 4-амінофенілу, 2-нітро-4-хлорфенілу, 2-нітро-4-метилфенілу, 2-нітро-4-метилсульфонілфенілу, 3-ацетиламінофенілу, 4-ацетиламінофенілу, 4-(3-карбокси-n-пропіл)карбоніламінофенілу, 2-хлор-5-трифторметилфенілу, 4-(4-гідрокси-n-бутил)амінофенілу, 2-(диметиламінo)ацетиламінофенілу, 4-[2-(N-піролідиніл)етокси]фенілу, 4-[2-(4-морфолініл)етокси]фенілу, 4-(2-(диметиламінo)етокси)фенілу, 4-піразинілу, 2,3-диметил-3Н-імідазолілу, 2-піридилу та 3-піридилу;
при умові, що коли ![]() є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
та її фармацевтичнo прийнятні солі.
4. Сполука за п. 3, яка відрізняється тим, що
Х є NRD, де RD є вибраним з групи, яка складається з водню, ди(метил)аміноетилу, 4-піридилметилу, 2-піридилметилу, N-морфолінілетилу, карбоксіетилу, карбоксиметилу, ді(етил)аміноетилу, N-піролідинілетилу та 5-(4-метилфеніл)-2-піримідинілу;
R2 є вибраним з групи, яка складається з 3,4-метилендіоксифенілу, 2,3-дигідробензофурилу та 2,3-дигідробензо-[1,4]-оксин-6-ілу;
R4 є воднем;
Y є вибраним з групи, яка складається з С(О) та СН2;
![]() є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2-фурилу, 2-бензофурилу, 2-тієнілу, 2-бензотієнілу, 2-бензотіазолілу, 2-бензоксазолілу, 2-тіазолілу, 4-тіазолілу та 2-піридилу;
є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2-фурилу, 2-бензофурилу, 2-тієнілу, 2-бензотієнілу, 2-бензотіазолілу, 2-бензоксазолілу, 2-тіазолілу, 4-тіазолілу та 2-піридилу;
m є цілим числом від 0 до 1;
R3 є вибраним з групи, яка складається з брому, t-бутилу, метокси, трифторметилу, нітрогрупи, фенілу, 4-хлорфенілу, 3,4-диметоксифенілу, 3-трифторметилфенілу, 4-метилфенілу, 4-метоксифенілу, 2-нітрофенілу, 3-нітрофенілу, 4-нітрофенілу, 3-амінофенілу, 2-нітро-4-хлорфенілу, 2-нітро-4-метилфенілу, 2-нітро-4-метилсульфонілфеніл, 4-(3-карбокси-n-пропіл)карбоніламінофенілу, 2-хлор-5-трифторметилфенілу, 4-(4-гідрокси-n-бутил)амінофенілу, 2-2-(диметиламінo)ацетиламінофенілу, 4-піразиніл 2-піридилу та 2,3-диметил-3Н-імідазол-4-ілу;
при умові, що коли ![]() є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
є 2-фурилом або 2-тієнілом, тоді m є цілим числом від 1 до 2;
та її фармацевтично прийнятні солі.
5. Сполука за п. 4, яка відрізняється тим, що
Х є NRD, де RD є вибраним з групи, яка складається з водню, ди(метил)аміноетилу, N-морфолінілетилу, карбоксиметилу та N-піролідинілетилу;
R2 є вибраним з групи, яка складається з 3,4-метилендіоксифенілу та 2,3-дигідробензофурилу;
Z є вибраним з групи, яка складається з СН2 та С(О); при умові, що коли Z є С(О), тоді Х є NH;
Y є С(О);
![]() є вибраним з групи, яка складається з 2-піримідинілу, 2-фурилу, 2-бензофурилу, 2-бензоксазолілу, 2-тіазолілу та 2-піридилу;
є вибраним з групи, яка складається з 2-піримідинілу, 2-фурилу, 2-бензофурилу, 2-бензоксазолілу, 2-тіазолілу та 2-піридилу;
R3 є вибраним з групи, яка складається з t-бутилу, метоксигрупи, нітрогрупи, фенілу, 4-хлорфенілу, 4-метилфенілу, 4-метоксифенілу, 3,4-диметоксифенілу, 3-трифторметилфенілу, 2-нітрофенілу, 3-нітрофенілу, 4-нітрофенілу, 3-амінофенілу, 2-нітро-4-метилсульфонілфенілу, 2-(диметиламінo)ацетиламінофенілу, 2-піридилу та 2,3-диметил-3Н-імідазол-4-ілу;
при умові, що коли ![]() є 2-фурилом, тоді m є 1;
є 2-фурилом, тоді m є 1;
та її фармацевтичнo прийнятні солі.
6. Сполука за п. 3, яка відрізняється тим, що є вибраною з групи, яка складається з:
1-(3,4-метилендіоксифеніл)-2-[(5-феніл-2-фурил)карбоніл]-2,3,4,9-тетрагідро-1Н-b- карболіну;
1-(3,4-метилендіоксифеніл)-2-[5-(2-піридил)-2-піримідиніл]-9-ди(метил)аміноетил-2,3,4,9-тетрагідро-1Н-b-карболіну;
1-(3,4-метилендіоксифеніл)-2-[5-(3,4-диметоксифеніл)-2-піримідиніл]-1,2,3,9-тетрагідро-4-оксо-4Н-b-карболіну;
1-(3,4-метилендіоксифеніл)-2-[5-(4-метилфеніл)-2-піримідиніл]-1,2,3,9-тетрагідро-4-оксо-4Н-b-карболіну;
1-(3,4-метилендіоксифеніл)-2-[5-(4-метоксифеніл)-2-піримідиніл]-1,2,3,4-тетрагідро-4-оксо-4Н-b-карболіну;
1-(3,4-метилендіоксифеніл)-2-[4-(4-метоксифеніл)-2-тіазоліл]-2,3,4,9-тетрагідро-1Н-b-карболіну;
1-(3,4-метилендіоксифеніл)-2-(4-феніл-2-тіазоліл)-2,3,4,9-тетрагідро-1Н-b-карболіну;
2-[2,3']біпіридиніл-6'-іл-1-(2,3-дигідробензофуран-5-іл)-2,3,4,9-тетрагідро-1Н-b-карболіну;
1-(2,3-дигідробензофуран-5-іл)-2-[5-(2,3-диметил-3Н-імідазол-4-іл)-2,3-2,3,49-тетрагідро-1Н-b-карболіну;
та її фармацевтичнo прийнятні солі.
7. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та сполуку за пунктом 1.
8. Спосіб лікування полової дисфункції у суб'єкта, який потребує такого лікування, що включає введення суб'єкту терапевтично ефективної кількості сполуки за пунктом 1.
9. Спосіб лікування полової дисфункції за п. 8, який відрізняється тим, що половою дисфункцією є чоловіча полова дисфункція.
10. Спосіб лікування полової дисфункції за пунктом 8, який відрізняється тим, що полову дисфункцію вибирають з групи, яка складається з чоловічої полової дисфункції, чоловічої еректильної дисфункції, імпотенції, жіночої полової дисфункції, жіночої дисфункції полового збудження та жіночої полової дисфункції, пов'язаної з кровотечею та виробленням окису азоту в тканинах піхви та клітора.
11. Спосіб підвищення концентрації cGMP у тканинах полового члена у суб'єкта чоловічої статі, який потребує цього, який включає введення суб'єкту ефективної кількості сполуки за пунктом 1.
12. Спосіб лікування стану, вибраного з групи, що складається з чоловічої еректильної дисфункції (ЕД), імпотенції, жіночої дисфункції полового збудження, жіночої полової дисфункції, пов'язаної з кровотечею та виробленням окису азоту в тканинах піхви та клітора, передчасних пологів, дисменореї, серцево-судинних захворювань, атеросклерозу, артеріальних оклюзивних захворювань, тромбозу, коронарного рестенозу, стенокардії, інфаркту міокарда, серцевого нападу, ішемічних серцевих захворювань, гіпертонії, легеневої гіпертонії, астми, синдрому переміжної кульгавості та діабетичних ускладнень у суб'єкта, який потребує такого лікування, що включає введення суб'єкту терапевтично ефективної кількості сполуки за пунктом 1.
Текст
УКРАЇНА (19) UA (11) 74826 (13) C2 (51) МПК (2006) C07D 221/00 C07D 333/50 (2006.01) C07D 495/04 (2006.01) A61K 31/4365 (2006.01) C07D 491/048 (2006.01) A61P 15/00 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ОПИС ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ДО ПАТЕНТУ НА ВИНАХІД (54) ПОХІДНІ -КАРБОЛІНУ, КОРИСНІ ЯК ІНГІБІТОРИ ФОСФОДІЕСТЕРАЗИ (R1) X n R2 (Y)a (I), C (R3)m , де R1 є незалежно вибраним з групи, що складається з галогену, нітрогрупи, гідроксигрупи, С1-С8алкілу, С1-С8алкоксигрупи, -NH2, -NHRА-, -N(RА)2, -O-RА, С(О)NH2, -C(О)NHRA, -C(О)N(RA)2, -NС(O)-RA, SO2NHRA, -SO2N(RA)2, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох); де кожний RA є незалежно вибраним з групи, що складається з С1-С8алкілу, арилу (заміщеного, при потребі, RB у кількості від одного до трьох), С1С8аралкілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох); де кожний RB є незалежно вибраним з групи, що складається з галогену, гідроксигрупи, нітрогрупи, (13) N 74826 * * (11) R4 z ціаногрупи, С1-С8алкілу, С1-С8алкоксигрупи, С1С8алкілкарбонілу, карбоксиС1-С8алкілу, С1 С8алкілсульфонілу, трифторметилу, трифторметоксигрупи, аміногрупи, ацетиламіногрупи, ді(С1С8алкіл)аміногрупи, ді(С1-С8алкіл)аміноС1С8алкоксигрупи, ді(С1-С8алкіл) аміноацетилС1С8алкілу, ді(С1-С8алкіл)аміноацетиламіногрупи, карбоксіС1-С8алкілкарбоніламіногрупи, гідроксіС1С8алкіламіногрупи, NHRA, N(RA)2 та гетероциклоалкілС1-С8алкоксигрупи; n є цілим числом від 0 до 4; Х є незалежно вибраним з групи, що складається з О, S та NRD; де RD є вибраним з групи, що складається з водню, гідроксигрупи, -ORA, С1-С8алкілу, (де алкіл є, при потребі, заміщеним замісниками у кількості від одного до трьох, незалежно вибраними з галогену, карбоксигрупи, аміногрупи, С1-С8алкіламіногрупи, ді(С1-С8алкіл)аміногрупи, С1-С8алкоксикарбонілу, гетероарилу або гетероциклоалкілу), гетероарилу та гетероарилкарбонілу (де гетероарил може бути заміщеним, при потребі, фенілом або заміщеним фенілом, де замісниками фенілу є RВ у кількості від одного до трьох); R2 є вибраним з групи, що складається з С5С10алкілу (заміщеного, при потребі, RС у кількості від одного до трьох), арилу (заміщеного, при потребі, RВ у кількості від одного до трьох), гетероарилу (заміщеного, при потребі, RВ у кількості від одного до трьох), гетероциклоалкілу (заміщеного, при потребі, RВ у кількості від одного до трьох); де RС є незалежно вибраним з групи, що складається з галогену, гідроксигрупи, нітрогрупи, NH2, NHRA та N(RA)2; Z є вибраним з групи, що складається з СН2, СНОН та С(О); при умові, що коли Z є СНОН або С (О), тоді Х є NH; R4 є вибраним з групи, що складається з водню, гідроксигрупи, карбоксигрупи, С1-С6алкілкарбонілу, С1-С6алкоксикарбонілу, ді(С1С8алкіл)аміноалкоксикарбонілу, ді(С1С8алкіл)аміноС1-С8алкіламінокарбонілу та –CORF; UA (21) 2002119179 (22) 03.05.2001 (24) 15.02.2006 (86) PCT/US01/14357, 03.05.2001 (31) 60/204,667 (32) 17.05.2000 (33) US (46) 15.02.2006, Бюл. № 2, 2006 р. (72) Суі Жіхуа, US, Мейсілаг Марк Дж., US (73) ОРТО-МАКНЕЙЛ ФАРМАЦЕВТИКАЛ, ІНК., US (56) CH.ABS.SERV.,OHIO,US,POGOSYAN, S.A. "Synthesis and biological activity ..." 1987 GRIDD,R.ET AL:"Pictet-Spengler/Palladium Catalyzed..." 2000 (57) 1. Сполука формули (І): C2 2 (19) 1 3 74826 4 RF є вибраним з групи, що складається з С1фенілі є одним або більше замісниками незалежно С8алкілу, NH2, NHRA, NRA2, -С1-С8алкіл-NH2, -C1вибраними з галогену, гідроксигрупи, С1-С4алкілу, C8алкіл-NHRA, -C1-C8aлкіл-NRА2 та -NH-С1-С8алкілС1-С4алкоксигрупи, трифторметилу, трифторметоNRA2; ксигрупи, нітрогрупи, аміногрупи, ацетиламіно, С1а є 1; С4алкілсульфонілу, карбоксіС1Y є вибраним з групи, що складається з С(О), С4алкілкарбоніламіногрупи, гідроксіС1С(О)О, С(О)-NH та SО2; С4алкіламіногрупи, ді(С1-С4алкіл)аміноС1С4алкоксигрупи, ді(С1C С4алкіл)аміноацетиламіногрупи або гетероциклоає вибраним з групи, що складається з нафлкілС1-С4алкоксигрупи; тилу та гетероциклоалкілу; C m є цілим числом від 1 до 2; 3 при умові, що коли є 2-фурилом або 2R є незалежно вибраним з групи, що складається з галогену, нітрогрупи, С1-С8алкілу, С1тієнілом, тоді m є цілим числом від 1 до 2; С8алкоксигрупи, трифторметилу, трифторметоксита її фармацевтичнo прийнятні солі. 3. Сполука за п. 2, яка відрізняється тим, що групи, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох), фенілсульфонілу, нафХ є вибраним з S або NRD, де RD є вибраним з тилу, С1-С8аралкілу, гетероарилу (заміщеного, при групи, яка складається з водню, потребі, RB у кількості від одного до трьох), NH2, ди(метил)аміноетилу, ди(метил)аміно-n-пропілу, NHRA та N(RA)2; ді(етил)аміноетилу, ді(етил)аміно-n-бутилу, Nпіролідинілетилу, N-морфолінілетилу, 2C піридилметилу, 4-піридилметилу, 5-(4при умові, що коли є 2-фурилом або 2метилфеніл)-2-піримідинілу, карбоксиметилу, картієнілом, тоді m є цілим числом від 1 до 2; боксіетилу, 4-хлор-n-бутилу, 2-(5-(3та її фармацевтичнo прийнятні солі. трифторметилфеніл)фурил)карбонілу, 2-(5-(32. Сполука за п. 1, яка відрізняється тим, що нітрофеніл)фурил)карбонілу, метоксикарбонілмеn є 0; тилу, метоксикарбонілетилу та 2-бензоксазолілу; Х є вибраним з S або NRD, де RD є вибраним з R2 є вибраним з групи, яка складається з фенілу, групи, що складається з водню, галоС1-С6алкілу, 3,4-метилендіоксифенілу, 3,4ді(С1-4алкілу)аміноС1-С6алкілу, гетероарилу, гете(дифтор)метилендіоксифенілу, 2,3роарилС1-С4алкілу, гетероциклоалкілС1-С4алкілу, дигідробензофурилу, 2,3-дигідробензо-[1,4]оксинкарбоксіС1-С4алкілу, С1-С4алкоксикарбонілС16-ілу, 4-піридилу, 3-піридилу, 4-ціанофенілу, 3С4алкілу та гетероарилкарбонілу; де гетероарил є нітрофенілу, 4-нітрофенілу, 4додатково заміщеним, при потребі, фенілом або трифторметилфенілу, 4-метоксифенілу, 3,4заміщеним фенілом, де замісники на фенілі від диметилфенілу, 3,5-диметилфенілу, 3,4одного до двох є незалежно вибраними з RB; диметоксифенілу, 3-трифторметил-4-хлорфенілу, B де кожний R є незалежно вибраними з групи, яка 3,4-дихлорфенілу, 4-хлорфенілу, 4складається з галогену, нітрогрупи, С1-С4алкілу, метоксикарбонілфенілу, 3,4-диметоксифенілу, 4С1-С4алкокси, трифторметилу, трифторметокси, (диметиламінo)фенілу та 4-(N-(3-диметиламіно)-nаміно та ді(С1-С4алкіл)аміно; пропокси)фенілу; 2 R є вибраним з групи, яка складається з 3,4R4 є вибраним з групи, яка складається з водню, метилендіоксифенілу, 3,4карбоксигрупи, диметиламіноетоксикарбонілу, (дифтор)метилендіоксифенілу, 2,3диметиламіноетиламінокарбонілу та метоксикардигідробензофурилу, 2,3-дигідробензо-[1,4]-оксинбонілу; 6-ілу, піридилу, фенілу та заміщеного фенілу; де C фенільними замісниками є від одного до двох зає вибраним з групи, яка складається з нафмісників, незалежно вибраних з галогену, С1С4алкілу, С1-С4алкоксигрупи, трифторметилу, ціатилу, 2-піримідинілу, 2-фурилу, 3-фурилу, 2ногрупи, нітрогрупи, С1-С4алкоксикарбонілу, ді(С1бензофурилу, 2-тієнілу, 2-бензотієнілу, 2С4алкіл)аміно або ді(С1-С4алкіл)аміноС1бензотіазолілу, 2-бензоксазолілу, 2С4алкоксигрупи; бензимідазолілу, 4-тіазолілу, 2-тіазолілу, 3R4 є вибраним з групи, яка складається з водню, піразолілу, 4-піразолілу, 5-піразолілу, 3-(1,2,5карбоксигрупи, С1-С4алкоксикарбонілу, ди(С1триазоліл), 4-ізоксазолілу, 2-піридилу та 3С4алкіл) аміноС1-С4алкоксикарбонілу та ди(С1піридилу; С4алкіл)аміноС1-С4алкіламінокарбонілу; R3 є незалежно вибраним з групи, яка складається Y є вибраним з групи, яка складається з С(О), SO2 з хлору, брому, метилу, n-пропілу, t-бутилу, метокта CH2; сигрупи, трифторметилу, нітрогрупи, фенілу, бензилу, фенілсульфонілу, 4-гідроксифенілу, 4C хлорфенілу, 4-метилфенілу, 3,4-диметоксифенілу, є вибраним з групи, яка складається з наф3-трифторметилфенілу, 4-трифторметилфенілу, 5тилу та гетероарилу; трифторметилфенілу, 4-метоксифенілу, 2R3 є незалежно вибраним з групи, яка складається нітрофенілу, 3-нітрофенілу, 4-нітрофенілу, 3з галогену, нітрогрупи, С1-С4алкілу, С1амінофенілу, 4-амінофенілу, 2-нітро-4-хлорфенілу, С4алкоксигрупи, трифторметилу, С1-С4аралкілу, 2-нітро-4-метилфенілу, 2-нітро-4піразинілу, піридилу, галогензаміщеного піридилу, метилсульфонілфенілу, 3-ацетиламінофенілу, 4диметил заміщеного імідазолілу, фенілу, фенілсуацетиламінофенілу, 4-(3-карбокси-nльфонілу та заміщеного фенілу; де замісники на пропіл)карбоніламінофенілу, 2-хлор-5 5 74826 6 трифторметилфенілу, 4-(4-гідрокси-nR3 є вибраним з групи, яка складається з t-бутилу, бутил)амінофенілу, 2метоксигрупи, нітрогрупи, фенілу, 4-хлорфенілу, 4(диметиламінo)ацетиламінофенілу, 4-[2-(Nметилфенілу, 4-метоксифенілу, 3,4піролідиніл)етокси]фенілу, 4-[2-(4диметоксифенілу, 3-трифторметилфенілу, 2морфолініл)етокси]фенілу, 4-(2нітрофенілу, 3-нітрофенілу, 4-нітрофенілу, 3(диметиламінo)етокси)фенілу, 4-піразинілу, 2,3амінофенілу, 2-нітро-4-метилсульфонілфенілу, 2диметил-3Н-імідазолілу, 2-піридилу та 3-піридилу; (диметиламінo)ацетиламінофенілу, 2-піридилу та 2,3-диметил-3Н-імідазол-4-ілу; C при умові, що коли є 2-фурилом або 2тієнілом, тоді m є цілим числом від 1 до 2; та її фармацевтичнo прийнятні солі. 4. Сполука за п. 3, яка відрізняється тим, що Х є NRD, де RD є вибраним з групи, яка складається з водню, ди(метил)аміноетилу, 4піридилметилу, 2-піридилметилу, Nморфолінілетилу, карбоксіетилу, карбоксиметилу, ді(етил)аміноетилу, N-піролідинілетилу та 5-(4метилфеніл)-2-піримідинілу; R2 є вибраним з групи, яка складається з 3,4метилендіоксифенілу, 2,3-дигідробензофурилу та 2,3-дигідробензо-[1,4]-оксин-6-ілу; R4 є воднем; Y є вибраним з групи, яка складається з С(О) та СН2; C є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2-фурилу, 2-бензофурилу, 2тієнілу, 2-бензотієнілу, 2-бензотіазолілу, 2бензоксазолілу, 2-тіазолілу, 4-тіазолілу та 2піридилу; m є цілим числом від 0 до 1; R3 є вибраним з групи, яка складається з брому, tбутилу, метокси, трифторметилу, нітрогрупи, фенілу, 4-хлорфенілу, 3,4-диметоксифенілу, 3трифторметилфенілу, 4-метилфенілу, 4метоксифенілу, 2-нітрофенілу, 3-нітрофенілу, 4нітрофенілу, 3-амінофенілу, 2-нітро-4-хлорфенілу, 2-нітро-4-метилфенілу, 2-нітро-4метилсульфонілфеніл, 4-(3-карбокси-nпропіл)карбоніламінофенілу, 2-хлор-5трифторметилфенілу, 4-(4-гідрокси-nбутил)амінофенілу, 2-2(диметиламінo)ацетиламінофенілу, 4-піразиніл 2піридилу та 2,3-диметил-3Н-імідазол-4-ілу; C при умові, що коли є 2-фурилом або 2тієнілом, тоді m є цілим числом від 1 до 2; та її фармацевтично прийнятні солі. 5. Сполука за п. 4, яка відрізняється тим, що Х є NRD, де RD є вибраним з групи, яка складається з водню, ди(метил)аміноетилу, Nморфолінілетилу, карбоксиметилу та Nпіролідинілетилу; R2 є вибраним з групи, яка складається з 3,4метилендіоксифенілу та 2,3-дигідробензофурилу; Z є вибраним з групи, яка складається з СН2 та С(О); при умові, що коли Z є С(О), тоді Х є NH; Y є С(О); C є вибраним з групи, яка складається з 2піримідинілу, 2-фурилу, 2-бензофурилу, 2бензоксазолілу, 2-тіазолілу та 2-піридилу; C при умові, що коли є 2-фурилом, тоді m є 1; та її фармацевтичнo прийнятні солі. 6. Сполука за п. 3, яка відрізняється тим, що є вибраною з групи, яка складається з: 1-(3,4-метилендіоксифеніл)-2-[(5-феніл-2фурил)карбоніл]-2,3,4,9-тетрагідро-1Н-- карболіну; 1-(3,4-метилендіоксифеніл)-2-[5-(2-піридил)-2піримідиніл]-9-ди(метил)аміноетил-2,3,4,9тетрагідро-1Н--карболіну; 1-(3,4-метилендіоксифеніл)-2-[5-(3,4диметоксифеніл)-2-піримідиніл]-1,2,3,9-тетрагідро4-оксо-4Н--карболіну; 1-(3,4-метилендіоксифеніл)-2-[5-(4-метилфеніл)-2піримідиніл]-1,2,3,9-тетрагідро-4-оксо-4Н-карболіну; 1-(3,4-метилендіоксифеніл)-2-[5-(4-метоксифеніл)2-піримідиніл]-1,2,3,4-тетрагідро-4-оксо-4Н-карболіну; 1-(3,4-метилендіоксифеніл)-2-[4-(4-метоксифеніл)2-тіазоліл]-2,3,4,9-тетрагідро-1Н--карболіну; 1-(3,4-метилендіоксифеніл)-2-(4-феніл-2-тіазоліл)2,3,4,9-тетрагідро-1Н--карболіну; 2-[2,3']біпіридиніл-6'-іл-1-(2,3-дигідробензофуран5-іл)-2,3,4,9-тетрагідро-1Н--карболіну; 1-(2,3-дигідробензофуран-5-іл)-2-[5-(2,3-диметил3Н-імідазол-4-іл)-2,3-2,3,49-тетрагідро-1Н-карболіну; та її фармацевтичнo прийнятні солі. 7. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та сполуку за пунктом 1. 8. Спосіб лікування полової дисфункції у суб'єкта, який потребує такого лікування, що включає введення суб'єкту терапевтично ефективної кількості сполуки за пунктом 1. 9. Спосіб лікування полової дисфункції за п. 8, який відрізняється тим, що половою дисфункцією є чоловіча полова дисфункція. 10. Спосіб лікування полової дисфункції за пунктом 8, який відрізняється тим, що полову дисфункцію вибирають з групи, яка складається з чоловічої полової дисфункції, чоловічої еректильної дисфункції, імпотенції, жіночої полової дисфункції, жіночої дисфункції полового збудження та жіночої полової дисфункції, пов'язаної з кровотечею та виробленням окису азоту в тканинах піхви та клітора. 11. Спосіб підвищення концентрації cGMP у тканинах полового члена у суб'єкта чоловічої статі, який потребує цього, який включає введення суб'єкту ефективної кількості сполуки за пунктом 1. 12. Спосіб лікування стану, вибраного з групи, що складається з чоловічої еректильної дисфункції (ЕД), імпотенції, жіночої дисфункції полового збудження, жіночої полової дисфункції, пов'язаної з 7 74826 8 кровотечею та виробленням окису азоту в тканисерцевих захворювань, гіпертонії, легеневої гіпернах піхви та клітора, передчасних пологів, дисметонії, астми, синдрому переміжної кульгавості та нореї, серцево-судинних захворювань, атероскледіабетичних ускладнень у суб'єкта, який потребує розу, артеріальних оклюзивних захворювань, такого лікування, що включає введення суб'єкту тромбозу, коронарного рестенозу, стенокардії, терапевтично ефективної кількості сполуки за пунінфаркту міокарда, серцевого нападу, ішемічних ктом 1. Даний винахід стосується нових похідних карболіну, корисних як інгібітори фосфодіестерази. Даний винахід також стосується синтезу похідних -карболіну, та проміжних сполук, які використовують в процесі їх приготування. Крім того, даний винахід стосується використання описаних похідних для лікування хвороб та станів пов'язаних з фосфодіестеразою (ФДЕ), наприклад для лікування чоловічої еректільної дисфункції. Еректільна дисфункція (ЕД) визначена як нездатність досягати або підтримувати ерекцію, досить стійку для задовільного полового акту. В даний час підраховано, що приблизно 7-8% чоловічого населення страждають від еректільної дисфункції різного ступеню, що тільки у Сполучених Штатах Америки еквівалентно, принаймні, 20 мільйонам чоловіків. Оскільки ймовірність еректільної дисфункції з віком збільшується, передбачається, що поширення цього стану в майбутньому підвищиться, тому що зростає середній вік населення. Чоловіча еректільна дисфункція може бути наслідком психогенних та/або органічних факторів. Незважаючи на те, що еректільна дисфункція є багатофакторною, певні підгрупи чоловічого населення, більш ймовірно, мають ознаки цього захворювання. Зокрема, особливо високе поширення еректільна дисфункція має серед хворих діабетом, гіпертонією, серцевою хворобою та розсіяним склерозом. Крім того, хворі, які приймають певні групи ліків, такі як антигіпотензивні засоби, антидепресанти, седативні засоби та транквілізатори, більш схильні до еректільної дисфункції. Лікування еректільної дисфункції включає ряд фармакологічних засобів, вакуумні пристрої та протези полового члена. Серед фармакологічних засобів в даний час на практиці використовуються папаверин, фентоламін та алпростадил. Ці засоби ефективно діють тільки після прямого внутрішньокавернозного або внутрішньоуретрального введення, та їх дія пов'язана з побічними ефектами, такими як пріапізм, фіброс, біль у половому члені та гематоми на місці введення. Вакуумні пристрої є нешкідливим альтернативним лікуванням еректільної дисфункції. Ці пристрої викликають ерекцію шляхом створення тиску нижче атмосферного навколо тіла полового члену, що приводить до збільшеного кровотоку у кавернозне тіло завдяки пасивній артеріальній ділатації. Незважаючи на те, що ця форма терапії часто є успішною при еректільній дисфункції, що має органічне походження, скарги включають відсутність спонтанності та необхідність витрачати час на використання механічного пристрою, та труднощі і дискомфорт пов'язані з еякуляцією. Різні напівтверді або надувні протези полового члену використовуються з деяким успіхом, особливо чоловіками з діабетом. Ці пристрої взагалі використовують, коли інші варіанти лікування зазнають невдачу, і вони пов'язані з підвищеним ризиком інфекції та ішемії. Нещодавно, інгібітор фосфодіестерази V (ФДEV), сілденафіл (Viagra), був схвалений Управлінням по санітарному нагляду за харчовими продуктами та медикаментами США, як перорально ефективний медичний засіб для лікування еректільної дисфункції. Сілденафіл, 5-[2-етокси-5-(4метилпіперазин-1-ілсульфоніл)феніл]-1-метил-3-нпропіл-6,7-дигідро-1Н-піразоло[4,3-d]піримідин-7он та ряд пов'язаних з ним аналогів, та їх використання як антистенокардитичних засобів описано в Патентах США 5,250,534 та 5,34 6,901. Використання сілденафілу та пов'язаних з ним аналогів для лікування чоловічої еректільної дисфункції описано в [Міжнародній Публікації РСТ № WO 94/28902, опублікованої 22 грудня, 1994]. У клінічних дослідженнях, цей лікарський засіб поліпшив полову функцію приблизно у 70% чоловіків, які потерпали від еректільної дисфункції психогенної або органічної етіології. Однак, цей лікарський засіб показав менш вражаючий ефект у тих хворих, які піддавалися радикальної простатектоми, з поліпшеними ерекціями у 43% пацієнтів, з тих, що приймали сілденафіл у порівнянні з 15% на плацебо. Крім того, використання сілденафілу пов'язане з декількома небажаними побічними ефектами, включаючи головний біль, гіперемію та порушення кольорового зору, які є результатом неселективних впливів на різні тканини. Незважаючи на ці недоліки, лікарський засіб розглядається хворими, як найкращий серед інших лікувань, які включають введення медичного засобу безпосередньо в половий член за допомогою ін'єкції, використання зовнішнього пристрою або хірургічної процедури. [Daugan та інш., у Патенті США №5,859,009 (Європейський Патент ЕР 0740668 В1 та Міжнародна публікація WO 9519978)] описують синтез тетрациклічних похідних сполук як інгібіторів циклічного гуанозин 3',5'-монофосфату, особливо фосфодиестерази, та їх використання при лікуванні серцево-судинних захворювань. [Daugan та інш., у Міжнародній Публікації WO 97/03675] досліджують використання тетрациклічних похідних сполук для лікування імпотенції. [Bombrun та інш., у міжнародній публікації WO 97/43287] описує серію похідних сполук карболіну, зокрема похідних 2 - (заміщений алкіл карбоніл) заміщеного карболіну та їх використання при лікуванні серцево-судинних захворювань як інгібіторів циклічного гуанозин 3',5'-монофосфату, особливо 9 74826 10 фосфодиестерази. лікування еректільної дисфункції. Внутрішньоклі[Ellis та інш., у Міжнародній публікації WO тинні рівні cGMP регулюються ферментами, що 94/28902 та Європейському Патенті ЕР0702555 пов’язані з їх формуванням та розпадом, а саме, В1] описує серію похідних сполук піразолпіримідигуанілат циклазами та циклічними нуклеотидними нону та їх використання при еректільної дисфункфосфодіестеразами (ФДЕ). Дотепер, описано, ції. [Campbell, S.F. у Міжнародній публікації WO принаймні, дев'ять груп фосфодіестераз у ссавців, 96/16657] повідомляє про використання біциклічп'ять з яких здатні до гідролізування активного них гетероциклічних сполук для лікування імпотеcGMP до неактивного GMP при фізіологічних станції (піразолопіримідонів); у той час коли [Campbell нах (ФДЕ І, II, V, VI та IX). Фосфодіестераза V є на інш., у Міжнародній публікації WO 96/16644] переважаючим ізоформом у кавернозному тілі повідомляє про використання селективних інгібілюдини. Тому інгібітори фосфодіестерази V, як торів cGMP ФДЕ для лікування еректільної дисфуочікується, підвищують концентрацію cGMP у канкції. вернозному тілі, та збільшують тривалість та час[Ohashi та інш., у Міжнародній публікації WO тоту виникання ерекції полового члену. 9745427] описує тетрациклічні похідні піридокарДодатково, селективні інгібітори фосфодіестебазолу, що мають cGMP ФДЕ інпбувальну дію. рази, як відомо, є корисними для лікування різних [Fourtillan та інш., у Міжнародній публікації WO захворювань та станів, включаючи чоловічу ерек96/08490 A1] описує серію похідних карболіну та їх тільну дисфункцію (ЕД), жіночу дисфункцію половикористання при лікуванні захворювань пов'язавого збудження, жіночу полову дисфункцію, пов'яних з порушеннями активності мелатоніну. [Ueki та зану з кровотечею та вироблянням окису азоту в інш., у Патенті США №5,126,448] описує піридин тканинах піхви та клітора, передчасні пологи, диста похідні 1,2,3,4-тетрагідропіридину корисні як менорею, серцево-судинні захворювання, атеропсихотропні лікарські засоби, що мають заспокійсклероз, артеріальні оклюзивні захворювання, ливу дію. [Atkinson та інш., у Патенті США No. тромбоз, коронарний рестеноз, стенокардію, ін3,328,412] описує похідні 1-арил- та 1-гетероарилфаркт міокарда, параліч серця, ішемічні серцеві захворювання, гіпертонію, легеневу гіпертонію, 2-ацил-1,2,3,4-тетрагідро--карболіну, що мають астму, синдром переміжної кульгавості та діабетитривалі стійкі анальгезуючі властивості. чні ускладнення. Сексуально стимульована ерекція полового Згідно з викладеним, метою даного винаходу є члена є результатом комплексної взаємодії фізіоідентифікація сполук, які підвищують концентрацію логічних процесів, які заторкають центральну нерcGMP у тканині полового члену завдяки інгібуванвову систему, периферійну нервову систему та ню фосфодіестераз, зокрема фосфодіестерази V. гладкий м'яз. Зокрема, вивільнення окису азоту з Іншою метою винаходу є ідентифікація сполук, які неадренерпйних, нехолінергійних нервів та ендоє корисними для лікування полової дисфункції, телія ініціює гуанілілову циклазу та підвищує внутзокрема еректільної дисфункції та/або імпотенції у рішньоклітинні рівні cGMP у кавернозному тілі. тварин чоловічої статі, та/або полової дисфункції у Підвищення у внутрішньоклітинному cGMP знижує тварин жіночої статі. Ще однією метою винаходу є внутрішньоклітинні рівні кальцію, що приводить до ідентифікація способів лікування полової дисфунтрабекулярної релаксації гладкого м'яза, яка, у кції, зокрема еректільної дисфункції, використовусвою чергу, приводить до фізичного розширення ючи сполуки даного винаходу. об'єму та стиску підоболонкових венул, що привоІншою метою винаходу є ідентифікація сполук, дить до ерекції полового члену. які є корисними для лікування станів захворювань, Фосфодіестераза V, знайдена у тромбоцитах опосередкованих фосфодіестеразою V, таких як людини та судинному гладкому м'язі, наводить на чоловіча еректильна дисфункція, жіноча полова думку о ролі цього ферменту в стабілізації внутрідисфункція, серцево-судинні захворювання, атешньоклітинних концентрацій cGMP у серцеворосклероз, артеріальні оклюзивні захворювання, судинній тканині. Фактично, інгібітори фосфодіестромбоз, коронарний рестеноз, стенокардія, інтерази V показали, що викликають ендотеліально фаркт міокарда, параліч серця, ішемічні серцеві - залежне розширення судин за допомогою потензахворювання, гіпертонія, легенева гіпертонія, ціючого підвищення у внутрішньоклітинному астма, синдром переміжної кульгавості та діабетиcGMP, індукованого окисом азоту. Крім того, інгібічні ускладнення. тори фосфодіестерази V вибірково знижують леЗараз ми описуємо серію похідних похідних геневий артеріальний тиск у тваринних моделях застійної серцевої недостатності і легеневої гіперкарболіну зі здатністю інгібувати фосфодіестеразу тонії. Отже, на додаток до їх корисності при еректипу V у аналізах ферменту та підвищувати контільній дисфункції, інгібітори фосдіестерази V, центрацію cGMP у кавернозній тканині у vitro. ймовірно, були б терапевтично корисними для Даний винахід спрямований на отримання ностанів, подібних до паралічу серця, легеневої гіпевих похідних сполук -карболіну, корисних як інгібіртонії та ангіни. торів фосфодіестерази (ФДЕ). Зокрема, даний Очікується, що засоби, які підвищують конценвинахід спрямований на сполуки загальної фортрацію cGMP у тканині полового члена, або завдямули (І): ки розширеному вивільненню, або зниженому розщепленню cGMP, будуть ефективними для 11 де R1 є незалежно вибраним з групи, що складається з галогену, нітро групи, гідрокси групи, С1С8алкілу, С1-С8алкокси групи, -NH2, -NHRA, -N(RA)2, -О-RА, -C(O)NH2, -C(O)NHRA, -C(O)N(RA)2, -NC(O)RA; -SO2NHRA, -SO2N(RA)2, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох); де кожний RA є незалежно вибраним з групи, що складається з С1-С8алкілу, арилу (заміщеного, при потребі, RB у кількості від одного до трьох), С1С8аралкілу (заміщеного, при потребі, RB у кількості від одного до трьох) та гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох); де кожний RB є незалежно вибраним з групи, що складається з галогену, гідрокси групи, нітро групи, ціано групи, С1-С8алкілу, С1-С8алкокси групи, С1-С8алкілкарбонілу, карбокси С1-С8алкілу, С1С8алкілсульфонілу, трифторметилу, аміно групи, ацетиламіно групи, ди(С1-С8алкіл)аміно групи, ди(С1-С8алкіл)аміноС1-С8алкокси групи, ди(С1С8алкіл)аміноацетиламіно групи, карбоксиС1С8алкілкарбоніламіно групи, гідроксиС1С8алкіламіно групи, NHRA, N(RA)2 та гетероциклоалкілС1-С8алкокси групи; n є цілим числом від 0 до 4 ; X є незалежно вибраним з групи, що складається з O, S та NRD; де RD є вибраним з групи, що складається з водню, гідрокси групи, -ORA, С1-С8алкілу, (де алкіл є, при потребі, заміщеним замісниками у кількості від одного до трьох, незалежно вибраними з галогену, карбокси групи, аміно, С1-С8алкіламіно групи, ди(С1-С8алкіл)аміно групи, С1-С8алкоксикарбонілу, гетероарилу або гетероциклоалкілу), гетероарилу та гетероарилкарбонілу (де гетероарил може бути заміщеним, при потребі, фенілом або заміщеним фенілом, де замісниками фенілу є RB у кількості від одного до трьох) ; R2 є вибраним з групи, що складається з С5С10алкілу (заміщеного, при потребі, RC у кількості від одного до трьох), арилу (заміщеного, при потребі, RB у кількості від одного до трьох), гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох), гетероциклоалкілу (заміщеного, при потребі, RB у кількості від одного до трьох); де RC є незалежно вибраним з групи, що складається з галогену, гідрокси групи, нітро групи, A A NH2, NHR та N(R )2; Ζ є вибраним з групи, що складається з СН2, СНОН та С(O); при умові, що коли Ζ є СНОН або С(O), тоді X є ΝΗ; R4 є вибраним з групи, що складається з водню, гідрокси групи, карбокси групи, С1 74826 12 С6алкілкарбонілу, С1-С6алкоксикарбонілу, ди(С1С8алкіл) аміноалкоксикарбонілу, ди(С1С8алкіл)аміноС1-С8алкіламіно карбонілу, та -CORF; RF є вибраним з групи, що складається з С1С8алкілу, NH2, NHRA, NRA2, -С1-С8алкіл-NH2, -С1A A С8aлкiл-NHR , -С1-С8aлкlЛ-NR 2 та -NH-С1-С8алкілА NR 2; а є цілим числом від 0 до 1; Υ є вибраним з групи, що складається з СН2, С(O), С(O)O, C(O)-NH та SO2; є вибраним з групи, що складається з нафтилу, гетероарилу та гетероциклоалкілу; m є цілим числом від 0 до 2; R3 є незалежно вибраним з групи, що складається з галогену, нітро групи, С1-С8алкілу, С1С8алкокси групи, трифторметилу, трифторметокси, фенілу (заміщеного, при потребі, RB у кількості від одного до трьох), фенілсульфонілу, нафтилу, С1-С8аралкілу, гетероарилу (заміщеного, при потребі, RB у кількості від одного до трьох), NH2, NHRA та N(RA)2; при умові, що коли є 2-фурилом або 2тіенілом, тоді m є цілим числом від 0 до 2 ; та її фармацевтично прийнятні солі. Ілюстрацією винаходу є фармацевтична композиція, яка включає фармацевтично прийнятний носій та будь-яку з описаних вище сполук. Ілюстрацією винаходу є фармацевтична композиція, що одержана за допомогою змішування будь-якої з описаних вище сполук з фармацевтично прийнятним носієм. Ілюстрацією винаходу є спосіб одержання фармацевтичної композиції, що включає змішування будь-якої з описаних вище сполук та фармацевтично прийнятного носія. Ілюстрацією винаходу є способи лікування станів, наприклад, чоловічої еректільної дисфункції, імпотенції, жіночої полової дисфункції, наприклад, жіночої дисфункції полового збудження, жіночої полової дисфункції пов'язаної з кровотечею та виробленням окису азоту в тканинах піхви та клітора, передчасними пологами та/або дисменореєю у суб'єкта, який потребує такого лікування, що включає введення суб'єкту ефективної кількості будь-якої з описаних вище сполук або фармацевтичних композицій. Прикладом винаходу є спосіб підвищення концентрації cGMP у тканині полового члена завдяки інгібуванню фосфодіестераз, зокрема фосфодіестерази V, у суб'єкта чоловічої статі, який потребує такого лікування, що включає введення суб'єкту ефективної кількості будь-якої з описаних вище сполук або фармацевтичних композицій. Подальшою ілюстрацією винаходу є спосіб забезпечення ендотеліалзалежного розширення судин за допомогою потенціючого підвищення у внутрішньоклітинному cGMP зниженому окисом азоту у суб'єкта, який потребує такого лікування, що включає введення суб'єкту ефективної кількості будь-якої з описаних вище сполук або фармацевтичних композицій. Ілюстрацією винаходу є спосіб лікування станів, вибраних з групи, яка складається з чоловічої 13 74826 14 еректільної дисфункції (ЕД), імпотенції, жіночої С4алкілу, С1-С4алкоксикарбонілС1-С4алкілу та геполової дисфункції, жіночої дисфункції полового тероарилкарбоніл; де гетероарил є додатково, при збудження, жіночої полової дисфункції, пов'язаної потребі, заміщеним фенілом або заміщеним феніз кровотечею та виробленням окису азоту в тканилом, де замісники на фенілі від одного до двох є нах піхви та клітора, передчасних пологів, дисменезалежно вибраними з RB; та де кожний RB є ненореї, серцево-судинних захворювань, атеросклезалежно вибраними з групи, яка складається галорозу, артеріальних оклюзивних захворювань, гену, нітро групи, С1-С4алкілу, С1-С4алкокси, тритромбозу, коронарного рестенозу, стенокардії, фторметилу, трифторметокси, аміно та ди(С1інфаркту міокарда, паралічу серця, ішемічних серС4алкіл)аміно. Переважно, X є вибраним з S та цевих захворювань, гіпертонії, легеневої гіпертонії, NRD, де RD є вибраним з групи, яка складається з астми, синдрому переміжної кульгавості та діабеводню, ди(метил)аміноетилу, тичних ускладнень у суб'єкта, який потребує такого ди(метил)аміноетилу, ди(метил)аміно-n-пропілу, лікування, що включає введення суб'єкту ефективди(етил)аміноетилу, ди(етил)аміно-n-бутилу, Nної кількості будь-якої з описаних вище сполук або пірролідинілетилу, N-морфолінілетилу, 2фармацевтичних композицій. піридилметилу, 4-піридилметилу, 5-(4Прикладом винаходу є використання будь-якої метилфеніл)-2-піримідинілу, карбоксиметилу, карз описаних вище сполук для одержання медикабоксиетилу, 4-хлоро-n-бутилу, 2-(5-(3ментів для: (а) лікування полової дисфункції, зоктрифторметилфеніл)фурил)карбоніл, 2-(5-(3рема чоловічої еректільної дисфункції, (b) лікуваннітрофеніл)фурил) карбоніл, метоксикарбонілменя імпотенції, (с) підвищення концентрації cGMP у тилу, метоксикарбонілетилу та 2-бензоксазоілу. тканині полового члена шляхом інгібування фосБажано, X є NRD, де RD є вибраним з групи, яка фодіестерази, зокрема фосфодіестерази V та/або складається з водню, ди(метил)аміноетилу, 4(d) лікування стану, вибраного з групи, що складапіридилметилу, 2-піридилметилу, Nється з передчасних пологів, дисменореї, серцевоморфолінілетилу, карбоксиетилу, карбоксиметилу, судинних захворювань, атеросклерозу, артеріальди(етил)аміноетилу, N-пірролідинілетилу та 5-(4них оклюзивних захворювань, тромбозу, коронарметилфеніл)-2-піримідинілу. Найкраще, X є NRD, ного рестенозу, стенокардії, інфаркту міокарда, де RD є вибраним з групи, яка складається з водпаралічу серця, ішемічних серцевих захворювань, ню, ди(метил)аміноетилу, N-морфолінілетилу, кагіпертонії, легеневої гіпертонії, астми, синдрому рбоксиетилу та N-пірролідинілетилу; переміжної кульгавості та діабетичних ускладнень Ζ є вибраним з групи, що складається з СН2 та у суб'єкта, який потребує такого лікування. С(О); при умові, що коли Ζ є С(О), тоді X є ΝΗ; Даний винахід спрямований на отримання ноПереважно, Υ є вибраним з групи, яка складається з С (О), SO2 та СН2; вих похідних -карболіну, корисних для лікування Бажано, Υ є вибраним з групи, яка складаєтьполової дисфункції, зокрема чоловічої еректільної ся з С(O) та СН2. Найкраще, Υ є С(O). У варіанті дисфункції (ЕД). Не зважаючи на те, що сполуки даного винаходу є корисним насамперед для лікування чоловічої полової дисфункції або еректільвиконання даного винаходу вибраним з ної дисфункції, вони можуть також бути корисними групи, яка складається з нафтилу та гетероарилу. для лікування жіночої полової дисфункції, наприклад, жіночої дисфункції полового збудження, жіночої полової дисфункції, пов'язаної з кровотечею Переважно, є вибраним з групи, яка склата виробленням окису азоту в тканині піхви та клідається з нафтилу, 2-піримідинілу, 2-фурилу, 3тора, та передчасних пологів і дисменореї. фурилу, 2-бензофурилу, 2-теінілу, 2-бензотиенілу, Більш детально, сполуки даного винаходу є 2-бензотіазолілу, 2-бензоксазолілу, 2сполуками формули (І): бензимідазолілу, 4-тіазоліл, 2-тіазолілу, 3піразолілу, 4-піразолілу, 5-піразолілу, 3-(1,2,5триазоліл), 4-ізоксазолілу, 2-піридилу та 3піридилу. Більш бажано, є вибраним з групи, яка складається з нафтилу, 2-піримідинілу, 2фурилу, 2-бензофурилу, 2-тиенілу, 2-бензотиенілу, 2-бензотіазолілу, 2-бензоксазолілу, 2-тіазолілу, 4 де усі перемінні є такими, як визначено вище. Переважно, n є 0. Переважно, m є цілим числом від 0 до 1. У варіанті виконання даного винаходу X є вибраним з S та NRD; де RD є вибраним з групи, що складається з водню, галоС1-С6алкілу, ди(С1-С4алкілу)аміноС1С6алкілу, гетероарилу, гетероарилС1-С4алкілу, гетероциклоалкілС1-С4алкілу, карбоксиС1 тіазолілу та 2-піридилу. Найкраще, є вибраним з групи, яка складається з 2-піримідинілу, 2фурилу, 2-бензофурилу, 2-бензоксазолілу, 2тіазолілу та 2-піридилу. 2 У варіанті виконання даного винаходу, R є вибраним з групи, яка складається з 3,4метилендюксифенілу, 3,(4-(дифтор) метилендюксифенілу, 2,3-дигідробензофурилу, 2,3дигідробензо-[1,4]-оксин-6-іл, піридилу, фенілу та заміщеного фенілу; де фенільні замісники є від одного до двух замісників незалежно обраних з 15 74826 16 галогену, С1-С4алкілу, С1-С4алкокси групи, триКраще, R3 є вибраним з групи, яка складається з фторметилу, ціано групи, нітро групи, С1бромо, t-бутилу, метокси групи, трифторметилу, С4алкоксикарбонілу, ди(С1-С4алкіл)аміно або нітро групи, фенілу, 4-хлорфенілу, 3,4ди(С1-С4алкіл)аміноС1-С4алкокси групи. Переваждиметоксифенілу, 3-трифторметилфенілу, 4но, R2 є вибраним з групи, яка складається з феніметилфенілу, 4-метоксифенілу, 2-нітрофенілу, 3лу, 3,4-метилендюксифенілу, 3,4нітрофенілу, 4-нітрофенілу, 3-амінофенілу, 2(дифтор)метилендюксифенілу, 2,3нітро-4-хлорфенілу, 2-нітро-4-метилфеніл, 2-нітродигідробензофурилу, 2,3-дигідробензо-[1,4]-оксин4-метилсульфонілфенілу, 4-(3-карбокси-n6-ілу, 4-піридилу, 3-піридилу, 4-ціанофенілу, 3пропіл)карбоніламінофенілу, 2-хлор-5нітрофенілу, 4-нітрофенілу, 4трифторметилфенілу, 4-(4-гідрокси-n-бутил) амітрифторметилфенілу, 4-метоксифенілу, 3,4нофенілу, 2-2-(диметиламіно)ацетиламінофенілу, диметилфенілу, 3,5-диметилфенілу, 3,44-піразиніл-2-піридилу та 2,3-диметил-3Н-імідазолдиметоксифенілу, 3-трифторметил-4-хлорфеніл, 4-ілу. Найкраще, R3 є вибраним з групи, яка скла3,4-дихлорфенілу, 4-хлорфенілу, 4дається з t-бутилу, метокси групи, нітро групи, феметоксикарбонілфенілу, 3,4-диметоксифенілу, 4нілу, 4-хлорфенілу, 4-метилфенілу, 4(диметиламіно)феніл та 4-(N-(3-диметиламіно)-nметоксифенілу, 3,4-диметоксифенілу, 3пропокси)фенілу. Більш бажано, R2 є вибраним з трифторметилфенілу, 2-нітрофенілу, 3групи, яка складається з 3,4-метилендюксифенілу, нітрофенілу, 4-нітрофенілу, 3-амінофенілу, 22,3-дигідробензофурилу та 2,3-дигідробензо-[1,4]нітро-4-метилсульфонілфенілу, 2оксин-6-ілу. Найкраще, R2 є вибраним з групи, яка (диметиламіно)ацетиламінофенілу, 2-піридилу та складається з 3,4-метилендюксифенілу та 2, 32,3-диметил-3Н-імідазол-4-ілу. дигідробензофурилу. Бажано, R4 є вибраним з Для використання у медицині солі сполук дагрупи, яка складається з водню, карбокси групи, ного винаходу відносяться до нетоксичних "фарС1-С4алкоксикарбонілу, ди(С1-С4алкіл)аміноС1мацевтично прийнятних солей". Проте інші солі С4алкоксикарбонілу та ди(С1-С4алкіл)аміноС1можуть бути корисними у виготовленні сполук згіС4алкіламінокарбонілу. Краще, R4 є вибраним з дно з даним винаходом або їх фармацевтично групи, яка складається з водню, карбокси групи, прийнятних солей. Відповідні фармацевтично придиметиламіноетоксикарбонілу, диметиламіноетийнятні солі сполук включають кислотно-адитивні ламінокарбонілу та метоксикарбонілу. Найкраще, солі, які можуть бути сформованими, наприклад, R4 є воднем. шляхом змішування розчину сполуки з розчином У варіанті виконання даного винаходу, R3 є нефармацевтично прийнятної кислоти, такої як созалежно вибраним з групи, яка складається з галоляна кислота, сірчана кислота, фумарова кислота, гену, нітро групи, С1-С4алкілу, С1-С4алкокси групи, малеїнова кислота, бурштинова кислота, оцтова трифторметилу, С1-С4аралкілу, піразинілу, піридикислота, бензойна кислота, лимонна кислота, винлу, галоген заміщеного піридилу, диметил заміщена кислота, вугільна кислота або фосфорна кислоного імідазолілу, фенілу, фенілсульфоніл та заміта. Крім того, там, де сполуки винаходу несуть щеного фенілу; де замісники на фенілі є одним кислотну складову, їх відповідні фармацевтично або більше замісниками незалежно обраними з прийнятні солі можуть включати солі лужного мегалогену, гідрокси групи, С1-С4алкілу, С1-С4алкокси талу, наприклад, солі натрію або калію; лужні солі групи, трифторметилу, трифторметокси групи, лужноземельного металу, наприклад, солі кальцію нітро групи, аміно групи, ацетиламіно, С1або магнію; та солі сформовані відповідними оргаС4алкілсульфонілу, карбоксиС1нічними лігандами, наприклад, солі четвертинного С4алкілкарбоніламіно групи, гідроксиС1амонію. Таким чином, зразки фармацевтично приС4алкіламіно групи, ди(С1-С4алкіл)аміноС1йнятних солей включають наступні: С4алкокси групи, ди(С1-С4алкіл)аміноацетиламіно ацетат, бензолсульфонат, бензоат, бікарбогрупи або гетероциклоалкілС1-С4алкокси групи. нат, бісульфат, бітартрат, борат, бромід, едетат Переважно, R3 є незалежно вибраним з групи, яка кальцію, камсілат, карбонат, хлорид, клавуланат, складається з хлору, бромо, метилу, n-пропілу, tцитрат, дихлоргідрат, едетат, едисілат, естолат, бутилу, метокси групи, трифторметилу, нітро груезилат, фумарат, глюцептат, глюконат, глютамат, пи, фенілу, бензилу, фенілсульфонілу, 4гліколіларсанілат, гексилресорцинат, гідрабамін, гідроксифенілу, 4-хлорфенілу, 4-метилфенілу, 3,4бромгідрат, хлоргідрат, гідроксинафтоат, йодид, диметоксифенілу, 3-трифторметилфенілу, 4ізетюнат, лактат, лактобюнат, лаурат, малат, матрифторметилфенілу, 5-трифторметилфенілу, 4леат, манделат, мезилат, метилбромід, метилнітметоксифенілу, 2-нітрофенілу, 3-нітрофенілу, 4рат, метилсульфат, мукат, напсілат, нітрат, сіль Nнітрофенілу, 3-амінофенілу, 4-амінофенілу, 2метилглюкамін амонію, олеат, памоат (ембонат), нітро-4-хлорфенілу, 2-нітро-4-метилфенілу, 2палмітат, пантотенат, фосфат/дифосфат, поліганітро-4-метилсульфонілфенілу, 3лактуранат, саліцилат, стеарат, сульфат, субацеацетиламінофенілу, 4-ацетиламінофенілу, 4-(3тат, сукцинат, танат, тартрат, теоклат, тозилат, карбокси-n-пропіл)карбоніламінофенілу, 2-хлор-5тритюдид та валерат. трифторметилфенілу, 4-(4-гідрокси-nДаний винахід включає у своєму обсязі пролібутил)амінофенілу, 2ки сполук даного винаходу. Взагалі, такі проліки (диметиламіно)ацетиламінофенілу, 4-[2-(Nбудуть функціональними похідними сполук, які пірролідиніл)етокси]фенілу, 4-[2-(4легко перетворюються у vivo у задану сполуку. морфолініл)етокси]фенілу, 4-(2Так, у способах лікування за даним винаходом, (диметиламіно)етокси)фенілу, 4-піразинілу, 2,3термін "введення" повинен охоплювати лікування диметил-3Н-імідазолілу, 2-піридилу та 3-піридилу. різних розладів за допомогою сполуки, що безпо 17 74826 18 середньо описана, або сполукою, що не може бути чають піридил, піразоліл, фурил, тіазоліл, тіеніл, безпосередньо розкрита, але яка перетворюється імідазоліл, ізоксазоліл, піразиніл, піримідиніл, тіав задану сполуку у vivo після введення пацієнту. золіл, бензофурил, бензотієніл, бензимідозаліл, Загальновідомі процедури для відбору та одербензотіазоліл та бензіксозаліл. жання відповідних похідних проліків описані, наТермін "циклоалкіл", що використовується у приклад, у ["Design Prodrugs", під редакцією Н. описі даного винаходу, являє собою стабільну Bundgaapd, Eisevier, 1985]. трьох- або вісьмичленну моноциклічну кільцеву У тих випадках коли сполуки згідно з даним структуру, яка складається з насичених атомів винаходом мають принаймні один хіральний вуглецю. Відповідні приклади включають циклопцентр, вони можуть відповідно існувати як енанропіл, циклобутил, циклопентил, циклогексил, циктюмери. У тих випадках коли дані сполуки мають логептил і циклооктил. два або більшу кількість хіральних центрів, вони Термін "гетероциклоалкіл" являє собою стабіможуть додатково існувати як діастереомери. Зрольну насичену або частково насичену трьох- або зуміло, що всі такі ізомери та їх суміші входять в вісьмичленну моноциклічну кільцеву структуру, що обсяг даного винаходу. Крім того, деякі кристалічні містить атоми карбону та від одного до чотирьох, форми даних сполук можуть існувати як поліморпереважно від одного до двох, гетероатомів незафні модифікації, і як такі також призначені для лежно вибраних з Ν, Ο або S; та будь-яке стабільвключення у даний винахід. Крім того, деякі сполуне насичене, частково ненасичене або частково ки можуть утворювати сольвати з водою (тобто ароматичне 9-10-членне біциклічне кільце, що гідрати) або зі звичайними органічними розчиннимістить атоми карбону та від одного до чотирьох ками, і такі сольвати також включаються в обсяг гетероатомів, незалежно вибраних з від N, O або даного винаходу. S. Гетероциклоалкіл може бути приєднаний при Термін "галоген" включає йод, бром, хлор та будь-якому атомі карбону або гетероатомі, що фтор. приводить до створення стабільної структури. ВідТермін "алкіл", який або використовується повідні приклади гетероциклоалкільних груп вклюокремо, або як частина групи замісника, позначає чають піролідиніліл, піразолідиніліл, піперидиніл, алкани з прямими або розгалуженими ланцюгами, піперазиніл, морфолініл, дитіаніл, тритіаніл, діокщо мають від 1 до 10 атомів карбону, або будь-яку соланіл, діоксаніл, тіоморфолініл, 3,4кількість у межах цього діапазону. Наприклад, раметилендіоксифеніл, 2, 3-дигідробензофурил, 2,3дикали алкілу включають метил, етил, н-пропіл, дигідробензо-[1,4]-діоксин-6-іл, 2,3-дигідроізопропіл, н-бутил, ізобутил, сек-бутил, т-бутил, нфуро[2,3-b]піридиніл, 1,2пентил, 3-(2-метил)бутил, 2-пентил, 2-метилбутил, (метилендюкси)циклогексан, інданіл, 2-оксанеопентил, н-гексил та 2-метилпентил. біцикло[2.2.1]гептаніл, та інші їм подібні. ПереважТермін "алкокси" позначає радикал, який є рані гетероциклоалкільні групи включають піролідидикалом оксигенового простого ефіру, що сфорніл, морфолініл, 3,4-метилендюксифеніл, 2,3мований з описаних вище алкільних груп з прямидигідробензофурил та 2, 3-дигідробензоми та розгалуженими ланцюгами. Наприклад, [1,4]діоксин-6-іл. алкокси радикали включають метокси групу, етокЯк використовується у описі даного винаходу, си групу, н-пропокси групу, сек-бутокси групу, третсимвол "*" позначає присутність стереогенного бутокси групу, та інші їм подібні. центра. Термін "арил" позначає ароматичну групу, таку Відповідно до стандартної номенклатури, що як феніл, нафтил, та інші їм подібні. використовується у описі даного винаходу, кінцева Термін "аралкіл" позначає алкільну групу зачастина замісника пишеться спочатку, потім наміщену арильною групою. Наприклад, бензил, феступні частини до місця приєднання. Таким чином, нілетил, та інші їм подібні. замісник "фенілС1-С6алкіламінокарбонілС1Термін "гетероарил", що використовується у С6алкіл" відноситься до групи формули: описі даного винаходу, являє собою стабільну п'яти- або шестичленну моноциклічну ароматичну кільцеву систему, яка містить гетероатоми кількістю від 1 до 3, незалежно вибраних з N, О або S; або будь-яку 9- або 10-членну біциклічну ароматичну кільцеву систему, яка містить атоми вуглецю Припускають, що визначення будь-якого заміта гетероатоми кількістю від одного до трьох, несника або змінної у конкретному місцеположенні в залежно вибраних з N, О або S. Група "гетероаримолекулі не залежить від їх визначень в інших міслу" може бути приєднаною при будь-якому гетероцеположеннях даної молекули. Зрозуміло, що заатомі або атомі карбону, з утворенням стабільної місники та схеми заміщення у сполуках даного структури. Приклади прийнятних гетероарильних винаходу можуть вибиратись звичайним фахівцем груп включають, але не обмежуються піридинілом, у даній галузі у такий спосіб, щоб забезпечити хіпіримідинілом, тієнілом, фурилом, імідазолілом, мічну стабільність даних сполук та їх легкий синтез ізоксазолілом, оксазолілом, піразолілом, піразиніз використанням як відомих способів, так і спосолом, піролілом, тіазолілом, тіадіазолілом, тріазолібів, що викладені у даному винаході. Надалі прилом, бензимідозалілом, бензофуранілом, бензотіпускають, що, коли n або m>1, відповідні замісники єнілом, бензіксозалілом, бензоксазолілом, R1 або R3 можуть бути однаковими або різними. індазолілом, індолілом, бензотіазолілом, бензотіаТермін "полова дисфункція", який використодіазолілом, бензотріазолілом, хінолінілом або ізовується у описі даного винаходу, включає чоловічу хінолінілом. Переважні гетероарильні групи вклю 19 74826 20 полову дисфункцію, чоловічу еректільну дисфункнижче. цію, імпотенцію, жіночу полову дисфункцію, жіночу Сполуки формули (І) де (Y)a є С(О), можуть дисфункцію полового збудження та жіночу полову бути одержані відповідно способу, що показано на дисфункцію, зв'язану з кровотечею та виробленСхемі 1. ням окису азоту в тканинах піхви та клітора. ' Термін "суб єкт", що використовується у описі даного винаходу, відноситься до тварин, переважно ссавців, найбільш переважно до людини, яка є об'єктом лікування, нагляду або експерименту. Термін "терапевтично ефективна кількість", що використовується у описі даного винаходу, означає кількість активної сполуки або фармацевтичного агенту, що дає біологічний або медичний відклик у тканинах системи, тварини або людини, що спостерігається дослідником, ветеринаром, медичним доктором або іншим клініцистом, включаючи полегшення симптомів хвороби або розладу, що лікується. Термін "композиція", що використовується у описі даного винаходу, відноситься до продукту, що містить точно встановлені компоненти у точно встановлених кількостях, так само як і будь-який продукт, що отримують, прямо або побічно, комбіПереважно, сполука формули (II), де X є О, S нацією точно встановлених компонентів у точно або NH, відома сполука або сполука отримана за встановлених кількостях. допомогою відомих методів, вступає у реакцію з Скорочення, які використовуються у описі даприйнятним заміщеним альдегідом формули (III), у ного винаходу, зокрема у Схемах та Прикладах, є органічному розчиннику такому як ДХМ, ТГФ, тотакими: луол тощо, у присутності кислотного каталізатора Спол. № = Ідентифікаційний номер сполуки такого як ТФО, п-толуолсульфокислота тощо, для ДЦК = 1,3-Дициклогексилкарбодімід одержання відповідної трициклічної сполуки форДХМ = Дихлорметан мули (IV). ДДХ = Дихлордиціанохінолін Сполука формули (IV) вступає у реакцію з Дік = Діізопропілкарбодимід прийнятною заміщеною сполукою формули (V), де ДІПЕА = Діізопропілетиламін А є галогеном, у присутності основи такої як триеДМФ = Ν,Ν-диметилформамід тиламін (TEA), діізопропілетиламін (ДІПЕА), карДМСО = Диметилсульфоксид бонат натрію тощо, у органічному розчиннику таДффп = 1,3-Біс(дифенілфосфіно)пропан кому як дихлорметан(ДХМ), Ν,Ν'ЕДТО = Етилєндинітрилотетраоцтова диметилформамід (ДМФ), тетрагідрофуран (ТГФ) кислота тощо; або з прийнятною заміщеною сполукою фоFmoc 9-флуоренілметоксикарбоніл рмули (V), же А є гідрокси, у присутності зв'язуваFmoc-NCS = 9-флуоренілметоксикарбоніл льної речовини такої як ДЦК, ДІК, РуВор, РуВгор ізотіоціанаτ тощо, у органічному розчиннику такому як дихлорГЕПЕС = 2-[4-(2-пдроксиетил)метан (ДХМ), Ν,Ν'-диметилформамід (ДМФ), тетпіперазиніл]-етансульфокислота рапдрофуран (ТГФ) тощо; для одержання відповіЛАГ = Алюмогідрид літію дної сполуки формули (1а). ФДЕ = Фосфодіестераза Альтернативно, сполуки формули (І), де X є О, Pd2bda3 = Трис(дибензиліден ацеS, або NH та (Y) є С(О) можуть бути отримано відтон)дипаладій (0) повідно до процесу як показано на Схемі 2. Pd(OAc)2 = Паладія (II) ацетат Pd(PPh3)4 = Паладія тетракис(трифеніл фосфін) Ph = Феніл ФМСФ = Фенілметансульфонілу фторид PPh3 = Трифенілфосфін РуВор = Фосфористий (1-гідрокси-1Нбензотриазолато-О)три-1пірролідиніл PyBrop = Фосфористий бромо-три-1пірридиніл ННП = Натрію нітропрусид TEA = Триетиламін ТФО = Трифтороцтова кислота ТГФ = Тетрапдрофуран TsOH = п-толуолсульфокислота Сполуки формули (І) можуть бути одержані відповідно до процесів, які більш детально показані 21 Зокрема, сполуки формули (II), де X є О, S або NH, вступає в реакцію з прийнятно заміщеною сполукою формули (V), wherein А є галоген або гідрокси, у органічному розчиннику такому як ДХМ, ТГФ, ДМФ, тощо, для одержання відповідної сполуки формули (VII). Сполука формули (VII) циклізується шляхом обробки РОСІ3, у органічному розчиннику такому як толуол, бензен тощо, з наступним відновленням NaBH4, у органічному розчиннику такому як етанол, ізопропанол тощо, для одержання відповідної сполуки формули (IV). Сполука формули (IV) потім вступає у реакцію з відповідно заміщеною сполукою формули (V) для одержання сполуки формули (Іа) як показано на Схемі 1. Сполуки формули (І), де X є О, S або NH та (Y)a є SО2 можуть бути отримані відповідно до процесу, який показано на Схемі 3. Відповідно, відповідно заміщена сполука формули (IV) вступає у реакцію з відповідно заміщеною сполукою формули (VIII), де А є галогеном або гідрокси, відомою сполукою або сполукою одержаною відомими методами, у органічному розчиннику такому як ДХМ, хлороформ, ДМФ, ТГФ 74826 22 тощо, для одержання відповідної сполуки формули (Іb). Сполуки формули (І), де X є O, S або NH та (Y)а є СН2 можу бути одержані відповідно до процесу як показано на Схемі 4. Відповідно, прийнятно заміщена сполука формули (1а) обробляється відновлювальною речовиною, такою як ЛАГ, дибор тощо, бажано ЛАГ, у органічному розчиннику такому як метанол, ТГФ, диетил ефір тощо, бажано при температурі в межах від приблизно -20 до 40°С, для одержання відповідної сполуки формули (Іс). Сполуки формули (І), де (Y)a є СН2 та X є NH, можуть бути альтернативно одержані відповідно до процесу як показано на Схемі 5. Відповідно, сполука формули (IVa) вступає в реакцію з відповідно заміщеною сполукою формули (IX), де Q є галогеном, О-тозилатом або Омезолат, у органічному розчиннику такому як ДХМ, ТГФ тощо, для одержання відповідної сполуки формули (Id). Сполуки формули (І), де X є О, S або NH та (Y)a є (Y)o (тобто де а є 0, тоді Υ відсутній), може бути одержаний відповідно до процесу як показано на Схемі 6. Переважно, сполука формули (IV), відома сполука або сполука одержана за допомогою відомих способів, вступає в реакцію з відповідно заміщеним галідом формули (X), відома сполука або сполука одержана за допомогою відомих ме 23 74826 тодів, у органічному розчиннику такому як толуол, ДМФ, 1-метил-2-пірролідинон тощо, бажано при температурі в межах від приблизно 80 до 250°С, для одержання відповідної сполуки формули (Іе). Сполуки формули (1), де X є NR можуть бути одержані відповідно до процесу, який показано на Схемі 7. Відповідно, сполука формули (If) вступає в реакцію зі сполукою формули (XI), де Ζ є галогеном, гідрокси, О-тоілатом або О-мезолатом та основою такою як гідрид натрію, t-бутоксид калію тощо, у розчиннику, такому як ДМФ, 1-метил-2пірролідинон тощо, для одержання відповідної сполуки формули (Ig). Сполуки формули (І), де Ζ є СН-ОН або С(О) може бути одержана відповідно до процесу як показано на Схемі 8. 24 Відповідно, прийнятно заміщена сполука формули (IVa) вступає у реакцію з Fmoc-NCS, у органічному розчиннику такому як ДХМ, ДМФ, ТГФ, тощо, переважно при кімнатній температурі, для одержання відповідної сполуки формули (XII). Сполука формули (XII) вступає в реакцію з 20% піперидин, у спирті, такому як метанол , етанол тощо, для одержання відповідного аміну формули (XIII). Амін формули (XIII) вступає в реакцію з прийнятно заміщеним -гало метил кетоном формули (XIV), у присутності органічного розчинника або суміші такої як ДМФ, етанол: діоксан тощо, у присутності основи такої як TEA, ДІПЕА тощо, бажано при температурі у приблизно 70°С, для одержання відповідної сполуки формули (Ij). Сполуки формули (І) де (Y)a є С(О)О, можуть бути одержані відповідно до процесу, який показано на Схемі 10. Переважно, сполуки формули (If) обробляють окислювачем таким як ДДХ, хлораніл тощо, у розчиннику, такому як ТГФ, метанол, вода тощо, переважно при температурі у межах від приблизно 78 до приблизно 30°С, для одержання суміші відповідних сполук формули (Ih) та (Iї). Переважно, сполуки формули (Ih) та (Iї) відділяють за допомогою відомих методів, таких як рекристалізація, колонкова хроматографія тощо. Сполуки формули (І) де є 2-тіазолілом, можуть бути отрмані відповідно до процесу, який показано на Схемі 9. Переважно, сполука формули (IV) вступає в реакцію з прийнятно заміщеним хлорформатом формули (XV) або ангідридом формули (XVI) у органічному розчиннику такому як ДХМ, ДМФ, ТГФ тощо, для одержання відповідної сполуки форму 25 74826 26 ли (Ik). Таким чином, даний винахід забезпечує спосіб Сполуки формули (І) де (Y)a є C(O)-NH можуть лікування полової дисфункції у суб'єкта, який має бути одержані відповідно до процесу, який показав цьому потребу, що включає введення будь-якої но на Схемі 11. зі сполук, визначених у даному описі, у кількості, ефективної для лікування еректільної дисфункції. Сполука може бути введена пацієнту за допомогою будь-якого загальновідомого способу введення, включаючи, але не обмежуючись тільки внутрішньовенним, пероральним, підшкірним, внутришньом'язовим, інтрадермальним та парентеральним. Кількість сполуки, що є ефективною для лікування еректільної дисфункції встановлюється у межах від 0,1 до 20мг на кілограм ваги тіла суб'єкта. Даний винахід також призначений для створення фармацевтичних композицій, що включають одну або більшу кількість сполук даного винаходу у поєднанні з фармацевтично прийнятним носієм. Переважно ці композиції знаходяться у одиницях форми дозування, таких як таблетки, пігулки, капсули, порошки, гранули, стерильні парентеральні розчини або суспензії, дозовані аерозолі або рідкі розпилювачі, краплі, ампули, автоінжектори або Відповідно, сполука формули (IV) вступає в супозиторії; для орального, парентерального, інреакцію з прийнятно заміщеною сполукою формутраназального, під'язичного або ректального ввели (XVII), у органічному розчиннику такому як ДХМ, дення, або для введення при інгаляції або інсуфДМФ, ТГФ, тощо, для одержання відповідної споляції. Альтернативно, композиція може бути луки формули (Im). представлена у формі, що відповідає щотижневоКоли способи отримання сполук згідно з даним му або щомісячному введенню; наприклад, нерозвинаходом дають суміші стереоізомерів, ці ізомери чинна сіль активної сполуки, така як сіль деканоаможуть бути розділені за допомогою звичайних ту, може адаптованою для одержання складу для способів, таких як препаративна хроматографія. внутришньом'язової ін'єкції. Для одержання тверДані сполуки можуть бути одержані у рацемічній дих композицій, таких як таблетки, основний актиформі, або за допомогою енантіоспецифічного вний інгредієнт змішують з фармацевтичним носісинтезу чи шляхом розщеплення можуть бути єм, наприклад, загальновідомими наповнювачами одержані окремі енантюмери. Дані сполуки модля таблеток, такими як кукурудзяний крохмаль, жуть, наприклад, бути розщеплені на окремі енанлактоза, сахароза, сорбіт, тальк, стеаринова кистюмери за допомогою стандартних методів, таких лота, стеарат магнію, дикальцію фосфат або смояк утворення діастереомерних пар шляхом солеула, та інших фармацевтичних розчинників, напритворення з оптично активною кислотою, такою як (клад, вода, щоб сформувати попередній твердий )-ди-р-толуол-d-винна кислота та / або (+)-ди-рсклад композиції, який містить гомогенну суміш толуол-1-винна кислота після часткової кристалісполуки даного винаходу або її фармацевтично зації та регенерації вільної основи. Дані сполуки прийнятної солі. Коли зазначені попередні компоможуть бути також розкладені шляхом утворенням зиції називають гомогенними, мають на увазі, що діастереомерних ефірів або амідів з наступним активний інгредієнт є рівномірно диспергованим по хроматографічним розділенням та вилученням всій даній композиції, так що дана композиція мопобічної хіральної речовини. Як альтернатива, же бути легко розділена на однаково ефективні дані сполуки можуть бути розкладені використоформи дозування, такі як таблетки, пілюлі та капвуючи рідинну хроматографію високого тиску з сули. Потім дану попередню тверду композицію використанням хіральної HPLC колонки. розділяють на одиничні форми дозування, такі як Під час будь-якого способу отримання сполук описано вище, що містять від приблизно 1мг до даного винаходу може виникнути потреба та/або приблизно 1000мг активного інгредієнту даного бажання захистити чутливі або реакційні групи на винаходу. Таблетки або пілюлі, що містять нові будь-якій із відповідних молекул. Це може бути композиції, можуть бути покритими іншими сполудосягнуто за допомогою звичайних захисних груп, ками, що дає перевагу пролонгованої дії. Напритаких як описані у роботах [Protective Groups у клад, таблетка або пілюля може включати внутріOrganic Chemistry, ed. by J.F.W. McOmie, Plenum шній дозовий компонент та зовнішній дозовий Press, 1973, та T.W. Greene & P.G.M. Wuts, компонент, останній у формі оболонки навколо Protective Groups у Organic Synthesis, John Wiley & першого. Зазначені компоненти можуть бути розSons, 1991]. Дані захисні групи можуть бути вилуділені ентеральним шаром, який захищає від розчені на будь-якій зручній наступній стадії з викорищеплення у шлунку та дозволяє внутрішньому станням відомих у цій галузі способів. компоненту проходити неушкодженим до дванадКорисність сполук для лікування полової дисцятипалої кишки або забезпечує затримку його функції може бути визначена у відповідності до виділення. Для таких ентеральних шарів або покпроцедур, описаних у Прикладі 10, 11 та 12 даного рить можуть використовуватися різні матеріали, опису. такі матеріали включають ряд полімерних кислот з 27 74826 28 такими матеріалами як шелак, цетиловий спирт та рид натрію та інші їм подібні. Дезінтегратори ацетилцелюлоза. включають, без обмеження, крохмаль, метилцелРідкі форми, в які можуть бути включені нові люлозу, агар, бентоніт, ксантанову смолу та інші композиції даного винаходу, для перорального їм подібні. введення або для ін'єкцій, включають, але не обДо рідких форм можна додавати смакові домежуються тільки ними, водні розчини, відповідбавки, суспендувальні або диспергуючі агенти, такі ним чином ароматизовані сиропи, водні або олійні як синтетичні та натуральні гуми, наприклад, трасуспензії та ароматизовані емульсії з їстівними гакант, гуміараік, метилцелюлоза та інші їм подіболіями, такими як бавовняна олія, кунжутна олія, ні. Для парентерального призначення, бажаними є кокосова або арахісова олія, так само як і еліксири стерильні суспензії та розчини. Ізотонічні препарата подібні їм фармацевтичні наповнювачі. Прийняти звичайно містять консерванти та застосовуютьтні суспендуючі агенти для водних суспензій вклюся, коли бажаним є внутрішньовенне введення. чають синтетичні та природні смоли, такі як трагаСполуки даного винаходу можуть також ввокант, гуміарабик, альгінат, декстран, дитися у вигляді ліпосомальних систем доставки, карбоксиметилцелюлоза натрію, метилцелюлоза, таких як маленькі уніламелярні бульбашки, великі полівініл-піролідон або желатин. уніламелярні бульбашки та мультиламелярні буМетод лікування полової дисфункції, зокрема льбашки. Ліпосоми можуть бути утворені з великої чоловічої еректільної дисфункції, описаний в дакількості фосфоліпідів, таких як холестерол, стеаному винаході, може також бути виконано, викоририламін і фосфатидилхолін. стовуючи фармацевтичну композицію, яка вклюСполуки даного винаходу можуть також досчає будь-яку із сполук, визначених у даному описі тавлятися шляхом використання моноклональних та фармацевтично прийнятний носій. Фармацевантитіл як індивідуальних носив, з якими сполучені тична композиція може вміщувати приблизно від 1 молекули сполуки. Сполуки даного винаходу також до 1000мг, переважно приблизно від 10 до 500мг, можуть сполучатися з розчинними полімерами, як сполуки, і може бути складеною у будь-якій формі, носіями ліків. Такі полімери включають полівінілпіщо відповідає обраному способу введення. Носії ролідон, пірановий кополімер, полігідроксипропілвключають необхідні та інертні фармацевтичні метакріламідофенол, полігідроксиетилнаповнювачі, включаючи, але не обмежуючись аспартамідофенол або поліетилен-оксидполілізин, тільки ними, в'яжучі агенти, суспендувальні композаміщений пальмітоіловим залишком. Крім того, ненти, мастило, ароматизатори, підсолоджувачі, сполуки даного винаходу також можуть сполучатистабілізатори, барвники та покривні агенти. Компося з класом полімерів, що біоруйнуються, що є зиції, прийнятні для перорального прийому вклюкорисним для керованого вивільнення ліків, напричають тверді форми, такі як пігулки, таблетки, капклад, полімолочна кислота, полі-епсилонлети, капсули (кожна включаючи склади капролактам, полігідроксибутанова кислота, полібезпосереднього вивільнення, встановленого виортоестери, поліацеталі, полідигідропірани, полівільнення, вивільнення, що підтримується), грануціанакрілати та перекресні та амфіпатичні блоксоли та порошки, та рідкі форми, такі як розчини, полімери пдрогелів. сиропи, еліксири, емульсії та суспензії. Форми, Сполуки даного винаходу можуть вводитися в корисні для парентерального введення, включабудь-якій з нижченаведених композицій відповідно ють стерильні розчини, емульсії та суспензії. до встановленого режиму дозування, що встановПереважно, сполуки даного винаходу можуть лений фахівцями, для лікування полової дисфунквводитися як одинична добова доза, або повна ції, зокрема чоловічої еректільної дисфункції, де щоденна доза може вводитися в розділених дозах таке лікування необхідне. два, три або чотири рази на день. Крім того, споДоза продуктів може змінюватися у широких луки даного винаходу можуть вводитися у інтранамежах, від 1мг до 1000мг на дорослу людину на зальній формі шляхом топічного застосування день. Для перорального введення, композиції певідповідних інтраназальних носив, або через зовреважно застосовуються у вигляді таблеток, що нішні частини тіла, які добре відомі звичайним фамістять приблизно 5,0, 10,0, 15,0, 25,0, 50,0, 100, хівцям у цій галузі. При введенні у трансдермаль250 і 500мг активного компоненту для симптоманій формі доставки, перевагу має безперервний тичного регулювання дози для пацієнту, якого лірежим введення дози у порівнянні з переривчаскують. Ефективна кількість ліків звичайно досягатим режимом дозування. ється при дозуванні від приблизно 0,1мг/кг до Наприклад, для перорального введення у виприблизно 20мг/кг маси тіла на день. Переважним гляді таблетки або капсули, активний лікарського є дозування від приблизно 0,2мг/кг до приблизно засіб може бути об'єднаним з оральним, нетоксич10мг/кг маси тіла на день, головним чином, від ним фармацевтично прийнятним інертним носієм, приблизно 0,5мг/кг до приблизно 10мг/кг маси тіла таким як етиловий спирт, гліцерин, вода та інші їм на день. Сполуки можуть бути введені у режимі від подібні. Крім того, при бажанні або необхідності 1 до 4 разів на день. суміш також може включати прийнятні в'яжучі агеОптимальні дозування для введення можуть нти, любриканти та барвники. Відповідні в'яжучі бути легко визначені фахівцем у цій галузі, та моагенти включають, без обмеження, крохмаль, жежуть змінюватися в залежності від вибраної сполулатин, природний цукор, такий як глюкоза або беки, сили препарату, режиму введення, та розвитку та-лактоза, цукристі речовини з кукурудзи, приростану хвороби. Також певну роль можуть відіградні та синтетичні смоли, такі як гуміарабик, вати фактори, що залежать від конкретного пацієтрагаканта або олеат натрію, стеарат натрію, стента, наприклад його вік, вага, дієта або час призарата магнію, бензоат натрію, ацетат натрію, хлоначення, що обумовлюють необхідність корекції 29 74826 30 дозування. ла отримана шляхом додавання 1,0 еквівалента Наступні Приклади наводяться для полегшенметансульфонової кислоти до розчину сполуки, ня розуміння винаходу, та не призначені і не пояка наведена у заголовку прикладу у ДХМ для винні розглядатися як обмеження винаходу, який отримання продукта для біологічного дослідження, розкривається у наведеній нижче формулі. тп: 122-124°С. 1 Якщо інакше не зазначено, Н ЯМР виконуваПриклад 3 ли на пристрої Брукера АС-300. 1-(3,4-Метилендіоксифеніл)-2-[5-(3,4Приклад 1 диметоксифеніл)піримідин-2-іл]-2,3,4,9-тетрагідро1-(3,4-метилендіоксифеніл)-2-[5-(31Н--карболін (№7) трифторметилфеніл)фуроїл]-2,3,4,9тетрапдро-1НРозчин 1-(3,4-метилендюксифеніл)-2,3,4,9-карболін (№58) тетрагідро-1Н--карболін (3,73г, 12,8ммоль) [який До суспензії 5-(3отримано відповідно до способу, що описано у трифторметилфеніл)фуранкарбонової кислоти Міжнародній публікації WO 97/43287, Проміжна (256мг, 1ммоль) у ДХМ (20мл, безводний) додавасполука 7, сторінка 24] та 2-хлор-5-(3,4ли хлорангідрид щавлевої кислоти (165мг, диметоксифеніл)піримідин (1,6г, 6,4ммоль) у ДМФ 1,3ммоль), з наступним додаванням двох капели (50мл, безводний) нагрівали при температурі ДМФ. Суміш перемішували при кімнатній темпера120°С при перемішуванні протягом 16 годин. Реатурі протягом 1 години. Додавали розчин 1-(3,4кційну суміш охолодили NH4CІ та екстрагували метилендіоксифеніл)-2,3,4,9-тетрагідро-1Н-етил ацетатом. Органічну фазу промили соляним карболіну (292мг, 1ммоль) [який отримано відповірозчином (2Х) та висушили MgSO4. Колонкова дно до способу, що описано у Міжнародній публіхроматографія (силікагель, етил ацетат:гексани = кації WO 97/43287, Проміжна сполука 7, сторінка 2:3) дала білу тверду речовину, тп: 173-175°С. 24] та триетиламін (0,4мл) у ДХМ (10мл, безводMS (m/z): 507 (МН+) 1 ний) та суміш перемішували при кімнатній темпеН - ЯМР (CDCІ3) 2,91 (д, J=9Гц, 1Η), 3,02 ратурі протягом 16 годин, послідовно промили (тд, J=9,1Гц, 1Η), 3,39 (тд, J=9,1Гц, 1Η), 3,92 (с, водним NaHCO3, соляним розчином (2Х), 1N НСІ 3Η), 3,94 (с, 3Η), 5,02 (д, J=9,1Гц, 1Η), 5,92 (с, 2Η), та соляним розчином (2Х) та висушили MgSO4. 6,72 (д, J=8Гц, 1Η), 6,87-7,03 (м, 4Η), 7,11-7,17 (м, Після випарювання розчинника, була отримана 3Η), 7,31 (д, J=8Гц, 1Η), 7,56 (д, J=8Гц, 1Η), 7,80 (с, біла тверда речовина. 1Η), 8,56 (с, 2Η). тп: 126-129°С Приклад 4 MS (m/z): 531 (MH+); 1-(3,4-Метилендюксифеніл)-2-[5-(3,41 Н - ЯМР (CDCІ3) 2,96 (д, J=8Гц, 1 Η), 3,24 (м, диметоксифеніл)піримідин-2-іл]-91 Η), 3,56 (м, 1 Η), 4,60 (д, J=8Гц, 1 Η), 5,90 (с, 2 Η), диметиламіноетил-2,3,4-тригідро-1Н--карболін 6,70 (д, J=8Гц, 1 Η), 6,83-6,99 (м, 4Η), 7,13-7,34 (м, (№5) 4Η), 7,55 (м, 3Η), 7,87 (д, J=7Гц, 1Η), 7,95 (с, 1Η), Дотримуючись процедури, що описана у При8,23 (с, 1Η). кладі 2, 1-(3,4-метилендюксифеніл)-2-[5-(3,4Приклад 2 диметоксифеніл)піримідин-2-іл]-2,3,4,9-тетрагідро9-[2-(Пірролідин-1-іл)-етил]-1-(3,41Н--карболін (який отримано як описано у Прикметилендіоксифеніл)-2-[5-(3ладі 3) (1,0г, 1,97ммоль), 2-хлор-Ν,Νтрифторметилфеніл)фуроїл]-2,3,4-тригідро-1Η-диметилетиламін гідрохлорид (0,342г, 2,37ммоль), карболін (№75) гідрид натрію (60%, 0,190г, 4,74ммоль) та 15-краун До розчину 1-(3,4-метилендюксифеніл)-2-[5-(3ефір-5 вступили в реакцію, що дало продукт у витрифторметилфеніл)фуроїл]-2,3,4,9-тетрапдрогляді трохи жовту тверду речовину (після колонко1Н--карболіну (який отримано як описано у Приквої хроматографії з силікагелем, етил ацетатом). ладі 1) (600мг, 1,14ммоль) у ДМФ (15мл, безводMS (m/z): 578 (МН+) 1 ний) додавали гідрид натрію (60%, 105мг, Н - ЯМР (CDCІ3) 2,21 (с, 6Η), 2,22 (м, 1Η), 2,6ммоль) при кімнатній температурі. Суміш пере2,61 (м, 1Η), 2,89 (дд, J=13,4Гц, 1 Η), 3,03 (тд, мішували при кімнатній температурі протягом 30 J=13,4Гц, 1Η), 3,35 (тд, J=13,4Гц, 1Η), 3,91 (м, 1Η), хвилин. Додавали N-хлоретилпірролідин пдрохло3,92 (с, 3Η), 3,95 (с, 3Η), 4,06 (м, 1Η), 4,96 (дд, рид (214мг, 1,26ммоль) та 15-краун ефір-5 (1 краJ=13,4Гц, 1Η), 5,93 (с, 2Η), 6,72 (д, J=8Гц, 1Η), 6,83 пля). Суміш перемішували при кімнатній темпера(д, 1Η), 6,85-6,98 (м, 4Η), 7,12 (д, J=8Гц, 1Η), 7,21 турі протягом 16 годин, охолодили NH4CІ, (д, J=8Гц, 1Η), 7,31 (д, J=8Гц, 1Η), 7,34 (с, 1Η), 7,58 екстрагували етил ацетатом та висушили MgSO4. (д, J=8Гц, 1Η), 8,56 (с, 2Η). Після випарювання розчинника, залишок очистили Приклад 5 за допомогою колонкової хроматографії (силіка1-(3,4-Метилендіоксифеніл)-2-[5-(4гель, етил ацетат:гексани = 3:1), що дало білу твеметоксифеніл)-піримідин-2-іл]-4-оксо-2,3,4,9рду речовину. тетрагідро-1Н--карболін (№157) та 1-(3,4MS (m/z): 628 (МН+) Метилендіокси-феніл)-2-[5-(4-метоксифеніл)1 Н - ЯМР (CDCІ3) 1,26 (м, 4Н), 2,64 (м, 4Н), піримідин-2-іл]-4-гідрокси-2,3,4,9-тетрагідро-1Н-2,89 (м, 2Η) , 3,05 (д, J=8Гц, 1Η), 3,28 (т, J = 8 Гц, карболін (№158) 1Η), 3,59 (т, J=8Гц, 1Η), 3,96 (м, 1Η), 4,16 (м, 1Η), До суміші ДДХ (113,5мг, 0,5ммоль) та 1-(3,44,58 (д, J=8Гц, 1Η), 5,96 (с, 2Η), 6,75 (д, J=8Гц, 1Η), метилендіоксифеніл)-2-[5-(3,46,84(м, 2Η), 7,02 (д, J=8Гц, 1Η), 7,15-7,29 (м, 4Η), диметоксифеніл)піримідин-2-іл]-2,3,4,9-тетрагідро7,43 (с, 1Η), 7,59 (м, 3Η), 7,89 (д, J=7Гц, 1Η), 7,96 1Н--карболін (який отримано як описано у Прик(с, 1Η). ладі 3) (51мг, 0,1ммоль) додали змішений розчинВідповідна сіль метансульфонової кислоти бу 31 74826 32 ник ТГФ:вода (9:1) при температурі -78°С. Суміш карболін перемішували при температурі 0°С та потім доДо розчину тюсечовини з Частини В (223мг, зволили нагрітися до кімнатної температурі протя0,63ммоль) у суміші (1:1) діоксан:етанол (5мл) догом 15 годин. Колонкова хроматографія (силікадавали 4-метоксифеніл-2'-бромоацетофенон гель, гексани:етил ацетат = 1:1), що відповідно (175мг, 0,76ммоль) та триетиламін (0,40мл). Суміш дало -оксо- та -гідрокси похідні, у вигляді білих нагрівали до температури 70°С протягом 3 годин, твердих речовин. охолоджували до кімнатної температури та конце№157: нтрували в обертальному випарнику. Залишок MS (m/z) 521 (МН+), 519 (M-1) очищували за допомогою флеш-хроматографи 1 (SiO2, 0-10% метанол у дихлорметане), що дало Н ЯМР (CDCІ3) 3,90 (д, J=18Гц, 1Η), 3,89 (с, на виході безбарвну тверду речовину. 3Η), 3,91 (с, 3Η), 5,43 (д, J=18Гц, 1Η), 5,84 (с, 2Η), MS (m/z): 482 (МН+) 6,62 (д, J=8Гц, 1Η), 6,71 (д, J=8Гц, 1Η), 6,88-7,00 1 Н-ЯМР (CDCІ3) 2,86-3,07 (серія м, 2Н), 3,61(м, 4Η), 7,29-7,43 (м, 3Η), 7,53 (с, 1Η), 8,25 (м, 1Η), 8,51 (с, 2Η); 9,55 (с, 1Η). 3,71 (м, 1Н) 3,78 (с, 3Н), 3,91-4,02 (м, 1Н), 5,99 (д, №158: J=3,3Гц, 2Н), 6,58 (с, 1Н), 6,80-7,11 (серія м, 8Н), MS (m/z) 523 (MH+), 521 (M-1) 7,31 (д, J=7,8Гц, 1Н), 7,48 (д, J=7,6Гц, 1H), 7,82 (д, 1 J=8,7Гц, 2Н), 10,93 (с, 1Н). Н ЯМР (CDCІ3) 3,30 (т, J=6Гц, 1Η), 3,69 (д, Приклад 7 J=6Гц, 1Η), 3,92 (с, 3Η), 3,94 (с, 3Η), 5,97 (с, 2Η), 1-(3,4-Метилендюксифеніл)-2-[4-фенілтіазол6,11 (с, 1Η), 6,71 (д, J=8Гц, 1Η), 6,93-7,05 (m, 4Η), 7,18 (д, J=8Гц, 1Η), 7,23 (д, J=8Гц, 1Η), 7,40 (т, 2-іл]-2,3,4,9-тетрапдро-1Н--карболін (№170) J=6Гц, 1Η), 7,49 (д, J=8Гц, 1Η), 7,82 (д, J=8Гц, 1Η), Α. 1-(3,4-Метилендюксифеніл)-2-[38,43 (с, 2Η); 9,15 (с, 1Η). (фторенілметилоксикарбоніл)тіо-карбомоіл]Приклад 6 2,3,4,9-тетрагідро-1Н--карболін 1-(3,4-Метилендіоксифеніл)-2-[4-(4Суміш 1-(3,4-метилендюксифеніл)-2,3,4,9метоксифеніл)тіазол-2-іл]-2,3,4,9-тетрагідро-1Η-тетрагідро-1Н--карболіну (2,66г, 9,08ммоль) [одекарболін (№169) ржаного відповідно до способу, який розкрито у А. 1-(3,4-Метилендіоксифеніл)-2-[3Міжнародній Публікації WO 97/43287, проміжна (флуоренілметилоксікарбоніл)тіокарбамоіл]сполука 7, сторінка 24] та Fmoc-ізотіоціанату 2,3,4,9-тетрагідро-1Н--карболін (2,82г, 10,14ммоль) розчинювали у сухому дихлоСуміш 1-(3,4-метилендіоксифеніл)-2,3,4,9рметане (50мл). Суміш перемішували протягом 16 годин при температурі навколишнього середовитетрагідро-1Н--карболін (2,66г, 9,08ммоль) [який ща, а потім концентрували у вакуумі. Очищення за отримано відповідно до способу, що описано у допомогою флеш-хроматографи (0-10% метанол у Міжнародній публікації WО 97/43287, Проміжна дихлорметане) дало захищену тіосечовину у висполука 7, сторінка 24] та Fmoc-ізотіоціанат (2,82г, гляді твердої речовини блідо-жовтого кольору. 10,14ммоль) була розчинена у сухому дихлормеMS (m/z): 574 (МН+) тані (50мл). Суміш перемішували протягом 16 го1 дин при температурі навколишнього середовища, Н - ЯМР (CDCІ3) 2,86 (дд, J=12,9, 5,1Гц, 1Η), та потім концентрували у вакуумі. Очищення за 3,09 (дт, J=17,1, 6,9Гц, 1Η), 3,56 (дт, J=12,9, 5,1Гц, допомогою флеш-хроматографії (0-10% метанола 1Η), 4,19 (т, J=6,9Гц, 1Η), 4,43-4,53 (м, 2Η), 5,91 (с, у дихлорметані) дало захищену тіосечовину у ви2Η), 6,70 (д, J=8Гц, 1Η), 6,90 (шир. д, J=7,6Гц, 1Η), гляді твердої речовини блідо-жовтого кольору. 6,97 (шир. с, 1Η), 7,11-7,78 (серія м, 17Η). MS (m/z): 574 (МН+) В. 1-(3,4-Метилендюксифеніл)-21 Н - ЯМР (CDCІ3) 2,86 (дд, J=12,9, 5,1Гц, 1Η), (тіокарбомоіл)-2,3,4,9-тетрагідро-1Н--карболін 3,09 (дт, J=17,1, 6,9Гц, 1Η), 3,56 (дт, J=12,9, 5,1Гц, Розчин захищеної тіосечовини з Частини А 1Η), 4,19 (т, J=6,9Гц, 1Η), 4,43-4,53 (м, 2Η), 5,91 (с, (4,78г, 8,33ммоль) у 20% (за масою) піперидині у 2Η), 6,70 (д, J=8Гц, 1Η), 6,90 (шир. д, J=7,6Гц, 1Η), метанолі нагрівали з оберненим охолодженням 6,97 (шир.с, 1Η), 7,11-7,78 (серія м, 17Η). протягом 5 годин. Суміш концентрували у вакуумі, В. 1-(3,4-Метилендюксифеніл)-2що дало неочищений залишок, який очищували за допомогою флеш-хроматографи (SiO2, 0-10% ме(тіокарбамоіл)-2,3,4,9-тетрапдро-1Н--карболін танол у дихлорметане), що дало на виході тверду Розчин захищеної тіосечовини з Частини А речовину жовтого кольору. (4,78г, 8,33ммоль) у 20% (за масою) піперидина у MS (m/z): 352 (МН+) метанолі нагрівали з оберненим охолодженням 1 Н - ЯМР (CDCІ3) 2,69-2,87 (серія м, 2Н), протягом 5 годин. Суміш концентрували у вакуумі, що дало неочищений залишок, який очищували за 3,10-3,19 (м, 1Н), 4,24 (шир. с, 1Н), 6,00 (д, допомогою флеш-хроматографи (SiO2, 0-10% меJ=3,3Гц, 2Η), 6,72 (д, J=8,0Гц, 1Η), 6,87 (д, J=8,0Гц, танол у дихлорметані), що дало на виході тверду 1Η), 7,00-7,11 (серія м, 3Η), 7,30 (д, J=8,0Гц, 1Η), речовину жовтого кольору. 7,46 (д, J=7,7Гц, 1Η), 7,74 (шир. с, 3Η), 11, 06 (с, MS (m/z): 352 (МН+) 1Η). 1 С. 1-(3,4-Метилендіоксифеніл)-2-[4Н-ЯМР (CDCІ3) 2,69-2,87 (серія м, 2Н), 3,103,19 (м, 1Н), 4,24 (шир.с, 1Н), 6,00 (д, J=3,3Гц, 2Η), фенілтіазол-2-іл]-2,3,4,9-тетрагідро-1Н--карболін 6,72 (д, J=8,0Гц, 1Η), 6,87 (д, J=8,0Гц, 1Η), 7,00(№170) 7,11 (серія м, 3Н), 7,30 (д, J=8,0Гц, 1Η), 7,46 (д, До розчину тіосечовини з Частини В (227мг, J=7,7Гц, 1Η), 7,74 (шир.с, 3Н), 11,06 (с, 1Η)/ 0,65ммоль) додавали бромацетофенон (159мг, С. 1-(3,4-Метилендюксифеніл)-2-[4-(40,80ммоль) та триетиламін (0,40мл). Цю суміш нагрівали до температури 70°С протягом 3 годин, метоксифеніл)тіазол-2-іл]-2,3,4,9-тетрапдро-1Н- 33 74826 34 охолодили до кімнатної температури та концент88°С протягом 24 годин. Реакційну суміш фільтрурували у роторному випарнику. Залишок очищували крізь тампон з целіту з СН2Сl2, а потім концевали за допомогою флеш-хроматографи (SiO2, 0нтрували до малого об'єму. Препаративна TLC 10% метанол у дихлорметан), що дало на виході (3:7 етилацетат/гексан; потім 5% СН3ОН/СН2СІ2) тверду речовину блідо-жовтого кольору. дала продукт у вигляді твердої речовини жовтого + MS (m/z): 452 (МН ) кольору. 1 1 Н - ЯМР (CDCІ3) 2,87-2-3,06 (серія м, 2Н), Н ЯМР (CDCІ3) 2,82 (м, 1Н), 3,10 (м, 3Н), 3,63-3,73 (м, 1Н), 3,93-3,99 (м, 1Н), 5,99 (д, 3,58 (м, 1Н), 4,31 (м, 1Н), 4,53 (т, 2Н, J=9,5Гц), 6,71 J=3,3Гц, 2Н), 6,59 (с, 1Н), 6,81-7,11 (серія м, 5Н), (д, 1Н, J=7,6Гц), 6,85 (д, 1Н, J=7,6Гц). 7,25-7,69 (серія м, 6Н), 7,89 (д, J=7,4Гц, 2Н), 10,95 MS (m/z) 445 (МН+), 443 (ΜΗ) (с, 1Н). Дотримуючись процедур, які описані у цьому Приклад 8 описі, були отримані сполуки, що описані у Табли1-(2,3-дигідро-бензофуран-5-іл)-2-[5-(2,3цях 1-6. диметил-3Н-імідазол-4-іл)-піримідин-2-іл]-2,3,4,9тетрагідро-1Н--карболін (№190) 2-(5-бром-2-піримідиніл)-1-(2,3-дигідро-5бензофураніл)-2,3,4,9-тетрагідро-1Н--карболін (0,45г, 1,00ммоль), 1,2-диметил-1Н-імідазол (0,18г, 1,87ммоль), Pd(OAc)2 (12мг, 0,05ммоль), PPh3 (26мг, 0,1ммоль) та К2СО3 (0,28г, 2ммоль) перемішували у 3,5мл ДМФ при температурі 140°С протягом 14 годин. Суміш виділи у водний 10% розчин NaOH (50мл). Отриманий розчин екстрагували СН2СІ2 (350мл) та висушили над Na2SO4. Очищення за допомогою препаративної TLC дало продукт у заголовку прикладу у вигляді жовтого порошку. 1 Н ЯМР 300МГц (CDCІ3) 2,21 (с, 3Н) , 2,35 (с, 3Н) , 2,90 (м, 2Н), 3,10 (т, 2Η, J=8,8Гц), 3,35 (м, 1 Н), 4,52 (т, 2Η, J=8,8Гц), 4,91 (м, 1Н), 6,68-7,61 (м, 10Н). MS (m/z) 463 (МН+), 461 (ΜΗ). Приклад 9 2-[2,3']біпіридиніл-6'-іл-1-(2,3-дигідробензофуран-5-іл)-2,3,4,9-тетрагідро-1Н--карболін (№191) А: 2-(5-бром-піридин-2-іл)-1-(2,3-дигідробензофуран-5-іл)-2,3,4,9-тетрагідро-1Н--карболін 1-(2,3-дигідро-5-бензофураніл)-2,3,4,9тетрагідро-1Н--карболін (11,6г, 40ммоль), 2,5дибромпіридин (10,42г, 44ммоль), Pd2dba3 (1,465г, 1,6ммоль), Дффп (1,32г, 3,2ммоль) та NaOtBu (5,38г, 56ммоль) перемішували у 60мл ДМФ при температурі 80°С протягом 3 днів. Реакційну суміш фільтрували крізь тампоні з целіту з СН2СІ2. Потім реакційну суміш концентрували, потім неочищену суміш завантажували в колонку Фоксі (110г силікагелю), та елюювали сумішшю етилацетат/гексан (3:7). Продукт викристалізовувався в пробірках. Продукт концентрували і потім перекристалізували з ТГФ, що дало на виході продукт у вигляді кристалів жовтого кольору. 1 Η ЯМР 400МГц (ТГФ-d8) 0,91 (м, 1Н), 1,15 (м, 1Н), 1,25 (т, 2Н, J=9,5Гц), 1,60 (м, 1Н), 2,31 (м, 1Н), 2,60 (т, 2Η, J=9,5Гц), 4,75 (д, 1Н, J=7,6Η), 5,02 (д, 1Н, J=7,6Гц), 5,10-5,28 (м, 4Η), 5,380 (м, 2Н), 5,58 (м, 1Н), 5,72 (м, 1Н), 6,28 (с, 1Н), 8,12 (с, 1Н). MS (m/z) 446, 448 (MH+), 444, 446 (ΜΗ). В: 2-[2,3’]біпіридиніл-6'-іл-1-(2,3дигідробензофуран-5-іл)-2,3,4,9-тетрагідро-1Н-карболін Продукт, отриманий на етапі А, (0,4г, 0,896ммоль), 2-трибутилстананіл-піридин (0,8г, 2,17ммоль) та Рd(РРh3)4 (0,12г, 0,104ммоль) перемішували в 1,4-діоксані (5мл) при температурі 35 74826 36 37 74826 38 39 74826 40 41 74826 42 Приклад 10 In vitro дослідження Аналіз Циклічної Фосфодіестерази Нуклеотиду (ФДЕ) Виділення ФДЕУ ФДЕУ була виділена із тканин кролика та людини відповідно до протоколу, що описано [Boolell et at. [Boolell, Μ., Allen, Μ.J., Ballard, S.Α., GejoAttee, S., Muirhead, G.J., Naylor, Α. Μ., Osterloh, I.H., та Gingell, С] у Міжнародному Журналі Дослідження Імпотенції 1996 8, 47-52 з незначними модифікаціями]. У декількох словах, тканини кролика або людини були гомогенізовані у крижаному буферному розчині, що містив 20мМ ГЕПЕС (pH 7,2), 0,25Μ сахарози, 1мМ EDTO, та 1мМ фенілметилсульфоніл фториду (ФМСФ). Гомогенати центрифугували при 100,000g протягом 60 хвилин при температурі 4 С. Надосадочну рідину фільтрували через 0,2мкМ фільтр та завантажили в аніонітну колонку Pharmacia Mono Q (об'єм шару - 1мл), яка була урівноважена 20мМ ГЕПЕС, 1мМ EDTO та 0,5мМ ФМСФ. Після вимивання незв'язаних протеїнів, ферменти були елюйовані NaCl з лінійним градієнтом 100-600мМ у тому ж самому буфері (загальна кількість від 35 до 50мл, у залежності від тканини. Ферменти з кістякового м'яза, печерового тіла, сітківки, серця та тромбоцити були елюйовані 35, 40, 45, 50, і 50мл відповідно). Колонка керувалася при швидкості потоку 1мл/хвилина та фракції по 1мл булі зібрані. Фракції, що включають різні активності PDE, були об'єднані окремо і використовувалися в наступних дослідженнях. Вимір Інгібування ФДЕ Дослідження PDE були проведені, як описано [Thompson і Appleman у Біохімія 1971 10, 311-316, з незначними модифікаціями], як відзначено нижче. Дослідження були адаптовані до формату 96комірок. Фермент аналізувався в 5мМ МgСІ2, 15мМ 43 74826 44 Trie HCI (р 7,4), 0,5мг/мл альбумін сироватки велиінгібувальної активності для характерних сполук кої рогатої худоби, 1мкМ cGMP або сАМР, 0,1мкСі даного винаходу описані в Таблицях 6-7. Дані інгі[3Н]-cGMP чи [3Н] - сАМР, і 2-10мкл колонкового бування представлені як ІС50 (мкМ), як відсоток елюювання. Повний обсяг дослідження був інгібування при даній концентрації сполуки, що 100мкл. Реакційна суміш була витримана при теманалізується або як значення Кі. пературі 30°С протягом 30 хвилин. Реакція була зупинена після кипіння протягом 1 хвилини, і потім Таблиця 6 реакційну суміш охолодили на льоді. Отримані [3Н] 5'-мононуклеотиди були далі перетворені в незаСпол. %інгіб. @ 10мкМ MW MS(M+1) ряджені [3Н]-нуклеозиди, шляхом додавання 25мкл № (кролик) 1мг/мл отрути змії (Ophiophagus hannah), та ви1 288,30 289 67 тримані при температурі 30°С протягом 10 хвилин. 2 496,63 497 43 Реакція була зупинена додаванням 1мл полімер3 425,51 426 84 ної суспензії Bio-Rad AG1-X2 (1:3). Усі заряджені 4 552,08 553 94 нуклеотиди були зв'язані полімером, і тільки неза5 577,68 578 3 ряджені [ Н]-нуклеозиди залишилися в надосадоч6 547,66 548 95 ній рідині після центрифугування. Аліквота 200мкл 7 506,56 507 91 було узята та підрахована за допомогою сцинтіля8 569,60 580 89 ційної рідини. Активність ФДЕ була виражена, як 9 476,53 477 80 пмоль пдролізованого циклічного нуклеоти10 480,95 481 79 ду/хв/мл підготовки ферменту. 11 550,96 551 53 Дослідження інгібітору було проведено в бу12 516,52 517 76 фері, що досліджувався з кінцевою концентрацією 13 552,58 553 94 10% ДМСО. При цих умовах, гідроліз продукту лінійно збільшувався у залежності від часу та кон14 481,46 482 88 центрації ферменту. 15 466,49 467 90 Приклад 11 16 436,47 437 88 In Vitro Визначення Кi для Інгібіторів Фосфоді17 523,65 524 88 естерази: 18 452,53 453 87 Дослідження були адаптовані до формату 9619 758,64 759 15 комірок. 20 804,64 805 4 Фосфодіестераза аналізувалася в 5мМ МgСІ2, 21 543,48 544 32 15мМ Trie HCl (pH 7,4), 0,5мг/мол альбумінів сиро22 566,48 567 16 ватки великої рогатої худоби, 30нМ 3H-cGMP, та 23 616,59 617 30 тестовій сполуці при різних концентраціях. Кіль24 579,56 580 40 кість ферменту, що використовувався для кожної 25 602,56 603 20 реакції, було такою, що менше ніж 15% вихідного 26 621,61 622 88 субстрату були перетворені протягом періоду дослідження. Для усіх вимірів, тестова сполука була 27 621,05 622 56 розчинена та розбавлена в 100% ДМСО (2% 28 643,66 644 94 ДМСО в пробі). Повний обсяг проби був 100мкл. 29 79 602,56 601* (M-1) Реакційна суміш була витримана при температурі No M+1 ion 30°С протягом 90 хвилин. Реакція була зупинена 30 565,54 564 93 після кипіння протягом 1 хвилини, та потім негайно 31 588,54 587* (M-1) no 75 охолоджена за допомогою перенесення у ванну з M+1 ion льодом. Потім до кожної комірки було додано 33 629,68 630 88 25мкл 1мг/мл отрути змії (Ophiophagus hannah), і 33 629,68 630 63 реакційна суміш витримувалась при температурі 34 629,68 630 67 30°С протягом 10 хвилин. Реакція була зупинена 35 601,62 602 98 за допомогою додавання 1мл полімерної суспензії 36 513,63 514 97 Bio-Rad AG1-X2 (1:3). Аліквота 200мкл була узята 37 578,62 579 95 та підрахована за допомогою сцинтіляційної ріди38 578,62 579 91 ни. 39 568,07 569 93 Відсоток інгібування максимальної конверсії 40 613,07 614 78 субстрату (за допомогою ферменту при відсутності інгібітору) був розрахований для кожної концент41 578,62 579 93 рації тестової сполуки. Використовуючи аналіз 42 592,65 593 89 нелінійної регресії GraphPad Prism's (сигмоідальна 43 636,07 637 22 реакція на дозу) для визначення ІС50 використову44 615,65 616 65 вали залежність відсотку інгібування від логариф45 477,52 478 му концентрації тестової сполуки. При умовах, де 46 496,95 497 концентрація субстрату набагато менше за Км фе47 541,94 542 83 рменту (Км=концентрація субстрату, при який до48 577,59 578 60 сягається половина максимальної швидкості фер49 519,55 520 60 менту), Кi є еквівалентним значенню ІС50. 50 507,50 508 76 Дані мас-спектрографічного аналізу та ФДЕУ 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 541,94 577,59 521,53 507,50 519,55 507,50 564,95 530,50 477,52 549,62 562,62 454,40 465,30 431,40 442,51 541,94 550,50 68 69 70 71 622,63 644,65 574,51 588,54 72 588,54 73 565,54 74 75 76 77 78 79 80 81 621,61 627,66 524,55 514,00 487,48 520,94 488,50 511,50 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 529,56 506,56 531,49 508,49 464,48 487,48 486,49 561,58 546,57 513,01 461,57 502,40 493,56 461,57 477,52 480,55 535,95 458,52 45 542 578 522 508 520 508 565 531 478 550 563 455 465 432 443 542 549* (M-1) No M+1 ion 623 645 573 587* (M-1) No M+1 ion 587* (M-1) No M+1 ion 564* (M-1) No M+1 ion 622 628 525 515 488 521 489 510* (M-1) No M+1 ion 530 507 532 509 465 488 487 562 547 514 462 503 494 462 478 481 536 459 74826 76 85 81 70 76 92 89 90 86 78 83 66 23 50 35 21 46 21 15 20 84 27 58 35 37 27 18 13 27 20 26 69 34 49 69 82 39 44 19 13 57 71 38 40 46 100 101 102 103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 119 120 121 122 123 124 125 126 127 128 129 130 131 132 133 134 135 136 137 138 139 140 141 142 143 144 145 491,55 463,54 478,51 510,97 476,53 564,95 476,53 533,67 431,88 502,40 493,56 461,56 477,52 461,56 535,95 458,52 491,54 463,53 478,51 514,55 555,39 546,55 504,59 530,50 564,95 575,50 514,55 588,94 511,51 544,53 516,52 531,49 480,55 557,52 548,68 516,69 532,64 516,69 591,07 513,64 546,67 518,66 533,63 517,63 446,50 578,69 146 578,69 492 464 479 511 477 565 477 534 432 503 494 462 478 462 536 459 492 464 479 515 556 547 505 531 565 576 515 589 512 545 517 532 481 556 547 517 533 517 592 514 547 519 534 518 447 579* (M-1) No M+1 ion 579 24 48 40 55 72 40 70 15 48 31 32 35 33 29 27 30 32 32 28 28 18 10 65 56 53 54 12 13 11 46 45 12 76 1 5 8 18 -3 13 -9 8 11 -5 60 76 43 35 47 74826 Таблиця 7 Спол. № 147 148 149 150 151 152 153 154 155 156 157 158 159 160 161 162 164 166 167 168 169 170 172 174 175 176 178 179 180 182 MW 507,59 573,69 462,50 526,55 409,44 533,63 447,50 666,76 480,56 518,62 520,54 522,56 474,52 476,53 460,54 490,52 492,53 628,73 522,60 370,41 481,57 451,55 408,46 474,56 506,56 506,56 557,70 449,31 573,69 445,52 MS IC50 %інгіб. @ 10мкМ (M+1) (мкМ) (кролик) 508 5,2 52 574 4,4 66 463 0,75 80 527 4 410 0,13 95 534 1,2 80 448 0,12 95 667 0,11 97 481 9,2 57 519 0,0075 521 0,0087а 523 49 475 0,024 477 8,95 461 0,789 491 0,024а 493 82 629 58 523 1,49 371 2,15а 482 0,042 452 0,049 409 44а 475 0,150а 507 0,214 507 0,056 558 37 450 1,58 574 40 446 0,058 Комп’ютерна верстка О. Гапоненко 48 183 184 185 186 187 188 189 190 191 447,50 448 446 448 446 491 448 463 443 0,122а 0,640а 200,40а 240,10а 49,79а 642,69а 121,60а Кі=14,21нМ Кі=0,69нМ a Сполуки, які аналізувалися з використанням тканини людини. Приклад 12 Дослідження in vivo Дотримуючись процедури, розкритої [Картером та іншими, [Carter, A.J., Ballard, S.Α., and Nailor, A.M.] у Журналі Урології 1998, 160, 242246], сполуки за даним винаходом досліджували на ефективність in vivo. Приклад 13 Як особливий варіант здійснення композиції для перорального використання, 100мг сполуки Прикладу 7 поєднують з достатньою тонко роздробленою лактозою, для забезпечення загальної кількості від 580 до 590мг, достатньої для заповнення твердої желатинової капсули О формату. У той час, як вищенаведений опис спрямований на розкриття принципів даного винаходу, за допомогою прикладів, призначених для ілюстративних цілей, зрозуміло, що практичне застосування винаходу охоплює всі звичайні варіації, адаптації та/або модифікації, які знаходяться у межах наведеної нижче формули та їх еквівалентів. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюb-carboline derivatives as phosphodiesterase inhibitors
Назва патенту російськоюПроизводные b-карболина полезные как ингибиторы фосфодиэстеразы
МПК / Мітки
МПК: A61K 31/5377, A61P 43/00, A61P 9/00, A61P 11/06, C07D 471/04, A61K 31/444, A61K 31/4365, A61P 15/10, A61P 15/00, C07D 495/04, C07D 491/048, A61P 5/24, A61P 9/12, A61P 9/10, A61P 7/02, A61K 31/506, A61K 31/437, A61P 9/04
Мітки: похідні, корисні, b-карболіну, фосфодіестерази, інгібітори
Код посилання
<a href="https://ua.patents.su/24-74826-pokhidni-b-karbolinu-korisni-yak-ingibitori-fosfodiesterazi.html" target="_blank" rel="follow" title="База патентів України">Похідні b-карболіну, корисні як інгібітори фосфодіестерази</a>
Попередній патент: Пристрій для десантування з літака важких великогабаритних вантажів
Наступний патент: Похідні тетразолу, гербіцидна композиція на їх основі та проміжна сполука
Випадковий патент: Мікроелектронний сенсор для виміру магнітної індукції












