N-арилпіперидин заміщені біфенілкарбоксаміди як інгібітори аполіпопротеїну b
Номер патенту: 83510
Опубліковано: 25.07.2008
Автори: Меерпоель Лівен, Віллевойє Марсель, Ліндерс Йоаннес Теодорус Марія
Формула / Реферат
1. Сполука формули (І)
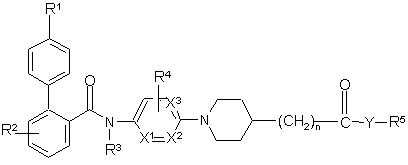 , (I)
, (I)
її N-оксиди, фармацевтично прийнятні кислотно-адитивні солі та стереохімічно ізомерні форми, де
R1 являє собою водень, С1-4алкіл, галоген або полігалогенС1-4алкіл;
R2 являє собою водень, С1-4алкіл, галоген або полігалогенС1-4алкіл;
R3 являє собою водень або С1-4алкіл;
R4 являє собою водень, С1-4алкіл або галоген;
n є цілим числом, яке дорівнює 0 або 1;
X1 являє собою атом вуглецю та X2 являє собою атом вуглецю; або X1 являє собою атом азоту та X2 являє собою атом вуглецю; або X1 являє собою атом вуглецю та X2 являє собою атом азоту;
X3 являє собою атом вуглецю або азоту;
Y являє собою О або NR6, де R6 являє собою водень або С1-4алкіл;
R5 являє собою радикал формули
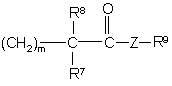 (a-1)
(a-1)
або
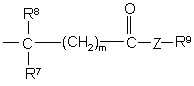 , (a-2)
, (a-2)
де
m є цілим числом, яке дорівнює 0, 1 або 2;
Z являє собою О або NH;
R7 являє собою водень;
С1-6алкіл;
С1-6алкіл, заміщений гідроксильною групою, аміно-, моно- або ді(С1-4алкіл)аміногрупою, С1-4алкілоксикарбонілом, амінокарбонілом, арилом або гетероарилом;
С1-4алкіл-О-С1-4алкіл;
С1-4алкіл-S-С1-4алкіл або арил;
R8 являє собою водень або С1-6алкіл;
R9 являє собою водень, С1-4 алкіл, арил або С1-4алкіл, заміщений арилом1;
або коли Y являє собою NR6, радикали R5 та R6 можуть бути взяті разом з атомом азоту, до якого вони приєднані, утворюючи піролідиніл, заміщений С1-4алкілоксикарбонілом та необов'язково додатково заміщений гідроксилом; або піперидиніл, заміщений С1-4алкілоксикарбонілом;
арил являє собою феніл; феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно вибраний з С1-4алкілу, С1-4алкілокси, галогену, гідроксигрупи, нітро, ціаногрупи, С1-4алкілоксикарбонілу, трифторметилу або трифторметокси; або бензо[1,3]діоксоліл;
арил1 являє собою феніл; феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно вибраний з С1-4алкілу, С1-4алкілокси, галогену, гідроксигрупи, нітро, ціаногрупи, С1-4алкілоксикарбонілу, трифторметилу або трифторметокси; та
гетероарил являє собою імідазоліл, тіазоліл, індоліл або піридил.
2. Сполука за п. 1, де X1, X2 та X3 являє собою атоми вуглецю.
3. Сполука за п. 1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, яке дорівнює 0.
4. Сполука за п. 1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, яке дорівнює 1.
5. Сполука за п. 1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-2), де n є цілим числом, яке дорівнює 1.
6. Сполука за п. 1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, та R5 та R6, разом з атомом азоту, до якого вони приєднані, утворюють піролідиніл, заміщений С1-4алкоксикарбонілом та необов'язково додатково заміщений гідроксилом, або піперидиніл, заміщений С1-4алкоксикарбонілом.
7. Фармацевтична композиція, що містить фармацевтично прийнятний носій та терапевтично активну кількість сполуки, вказаної в будь-якому з пп. 1-6.
8. Спосіб одержання фармацевтичної композиції за п. 7, в якому терапевтично активну кількість сполуки, вказаної в будь-якому з пп. 1-6, ретельно змішують з фармацевтично прийнятним носієм.
9. Сполука, вказана в будь-якому з пп. 1-6, для застосування як лікарський засіб.
10. Спосіб одержання сполуки формули (І), в якому
a) проміжну сполуку формули (II)
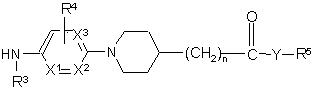 , (П)
, (П)
де R3, R4, R5, Y, n, X1, X2 та X3 мають значення, визначені в п. 1,
піддають взаємодії з біфенілкарбоновою кислотою або галогенангідридом формули (III)
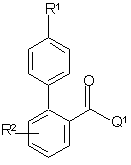 , (III)
, (III)
де R1 та R2 мають значення, визначені у формулі (І), та Q1 вибраний з гідроксигрупи та галогену, в принаймні одному реакційно-інертному розчиннику та необов'язково в присутності підходящої основи;
b) і/або сполуки формули (І) перетворюють одна в одну відповідно до відомих в даній галузі реакцій перетворення або, якщо необхідно, сполуку формули (І) перетворюють в кислотно-адитивну сіль або, навпаки, кислотно-адитивну сіль сполуки формули (І) перетворюють у форму вільної основи обробкою лугом; та, якщо необхідно, одержують їх стерехімічно ізомерні форми.
Текст
1. Сполука формули (І) 3 83510 4 гетероарил являє собою імідазоліл, тіазоліл, індоліл або піридил. 2. Сполука за п.1, де X1, X2 та X3 являє собою атоми вуглецю. 3. Сполука за п.1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, яке дорівнює 0. 4. Сполука за п.1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, яке дорівнює 1. 5. Сполука за п.1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-2), де n є цілим числом, яке дорівнює 1. 6. Сполука за п.1, де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, яке дорівнює 1; Y являє собою NR6, та R5 та R6, разом з атомом азоту, до якого вони приєднані, утворюють піролідиніл, заміщений С1-4алкоксикарбонілом та необов'язково додатково заміщений гідроксилом, або піперидиніл, заміщений С14алкоксикарбонілом. 7. Фармацевтична композиція, що містить фармацевтично прийнятний носій та терапевтично активну кількість сполуки, вказаної в будь-якому з пп.1-6. 8. Спосіб одержання фармацевтичної композиції за п.7, в якому терапевтично активну кількість сполуки, вказаної в будь-якому з пп.1-6, ретельно змішують з фармацевтично прийнятним носієм. 9. Сполука, вказана в будь-якому з пп.1-6, для застосування як лікарський засіб. 10. Спосіб одержання сполуки формули (І), в якому a) проміжну сполуку формули (II) Даний винахід відноситься до нових Nарилпіперидин заміщених біфенілкарбоксамідів, що мають інгібуючу активність у відношенні аполіпопротеїну В та супутню активність зниження вмісту ліпідів. Даний винахід відноситься також до способу одержання таких сполук, фармацевтичних композицій, що містять зазначені сполуки, а також до застосування зазначених сполук як лікарського засобу для лікування гіперліпідемії, ожиріння та діабету II типу. Ожиріння є причиною величезної кількості серйозних проблем зі здоров'ям, таких як початок розвитку цукрового діабету у дорослих та захворювання серця. Крім того, втрата ваги стає нав'язливою ідеєю серед ледачі більшої частини людського населення. В даний час широко визнаний взаємозв'язок між гіперхолестеринемією, зокрема, пов'язаною з підвищеними концентраціями в плазмі ліпопротеїнів низької густини (названих далі LDL) та ліпопротеїнів дуже низької густини (названих далі VLDL), та раннім розвитком атеросклерозу та/або серце во-судинних захворювань. Проте в даний час для лікування гіперліпідемії доступна обмежена кількість лікарських засобів. Лікарські засоби, що використовують, головним чином, для лікування ліпідемії, включають смоли, що підсилюють екскрецію жовчних кислот, такі як холестирамін та колестипол, похідні фібринової кислоти, наприклад, бензафібрат, клофібрат, фенофібрат, ципрофібрат та гемфіброзил, нікотинову кислоту та інгібітори синтезу холестерину, такі як інгібітори HMG-Co-A редуктази. Все ще зберігається потреба в ліпідознижуючих лікарських засобах з поліпшеною ефективністю та/або дією за допомогою механізмів, відмінних від механізмів дії зазначених вище лікарських засобів. Ліпопротеїни плазми являють собою водорозчинні комплекси високої молекулярної маси, що утворюються з ліпідів (холестерин, тригліцерид, фосфоліпіди) та аполіпопротеїнів. Відповідно до густини (яку вимірюють ультрацентрифугуванням) визначені п'ять основних класів ліпопротеїнів, що розрізняються за співвідношенням ліпідів та типу R4 O X3 (CH 2)n N HN X1 X2 C Y R5 R , (П) де R3, R4, R5, Y, n, X1 , X2 та X3 мають значення, визначені в п.1, піддають взаємодії з біфенілкарбоновою кислотою або галогенангідридом формули (III) 3 R1 O R2 Q1 , (III) де R1 та R2 мають значення, визначені у формулі 1 (І), та Q вибраний з гідроксигрупи та галогену, в принаймні одному реакційно-інертному розчиннику та необов'язково в присутності підходящої основи; b) і/або сполуки формули (І) перетворюють одна в одну відповідно до відомих в даній галузі реакцій перетворення або, якщо необхідно, сполуку формули (І) перетворюють в кислотно-адитивну сіль або, навпаки, кислотно-адитивну сіль сполуки формули (І) перетворюють у форму вільної основи обробкою лугом; та, якщо необхідно, одержують їх стерехімічно ізомерні форми. 5 83510 аполіпопротеїну, та які утворюються в печінці та/або кишечнику. Вони включають LDL, VLDL, ліпопротеїни середньої густини (названі далі IDL), ліпопротеїни високої густини (названі далі HDL) та хіломікрони. Ідентифіковано десять основних аполіпопротеїнів плазми людини. VLDL, що секретуються печінкою та містять аполіпопротеїн В (названий далі Аро-В), піддаються розкладанню до LDL, що переносять 60-70% загального холестерину сироватки. Аро-В є також основним білковим компонентом LDL. Підвищений вміст LDLхолестерину в сироватці крові внаслідок надлишкового синтезу або зниженого метаболізму є причиною розвитку атеросклерозу. Ліпопротеїни високої густини (названі далі HDL), що містять аполіпопротеїн А1, навпаки, мають захисну дію та зворотно пропорційно корельовані з ризиком розвитку коронарного захворювання серця. Таким чином, визначення співвідношення HDL/LDL є зручним методом оцінки атерогенного потенціалу ліпідного профілю плазми індивідуума. Дві ізоформи аполіпопротеїну (аро) В, аро В48 та аро В-100, є важливими білками в метаболізмі ліпопротеїнів людини. Аро В-48, названий так тому що він, очевидно, складає приблизно 48% розміру аро В-100 на натрійдодецилсульфатполіакриламідних гелях, в організмі людини синтезується в кишечнику. Аро В-48 необхідний для складання хіломікронів та тому відіграє важливу роль у поглинанні харчових жирів у кишечнику. Аро В-100, що в організмі людини виробляється печінкою, необхідний для синтезу та секреції VLDL. LDL, що містять приблизно 2/3 холестерину в плазмі людини, є продуктами метаболізму VLDL. Аро В-100 фактично є єдиним білковим компонентом LDL. Підвищені концентрації аро В-100 та LDL холестерину в плазмі є визнаними факторами ризику розвитку атеросклеротичної коронарної хвороби серця. Велика кількість спадкових та придбаних захворювань може призводити до гіперліпідемії. Вони можуть підрозділятися на первинні та вторинні гіперліпідемічні стани. Найбільш розповсюдженими причинами вторинних гіперліпідемій є цукровий діабет, зловживання алкоголем, наркотики, гіпотиреоз, хронічна ниркова недостатність, нефротичний синдром, холестаз та булімія. Первинні гіперліпідемії також підрозділені на загальну гіперхолестеринемію, сімейну комбіновану гіперліпідемію, сімейну гіперхолестеринемію, залишкову гіперліпідемію, синдром хіломікронемії та сімейну гіпертригліцеридемію. Білок переносу мікросомальних тригліцеридів (названий далі МТР), як відомо, каталізує транспорт тригл іцериду та складного ефіру холестерину переважно до фосфоліпідів, таких як фосфатидилхолін. В публікації [D. Sharp et al., Nature (1993) 365: 65] було показано, що де фект, який викликає абеталіпопротеїнемію, знаходиться в МТР гені. Це вказує на те, що для синтезу Аро-В-вмісних ліпопротеїнів, таких як VLDL, що є попередником LDL, потрібен МТР. Отже, інгібітор МТР повинен сповільнювати синтез VLDL та LDL, знижуючи, таким чином, рівні вмісту VLDL, LDL, холестерину та тригліцериду в людей. 6 Однієї з цілей даного винаходу є надання поліпшеного способу лікування пацієнтів, що страждають на ожиріння або атеросклероз, зокрема, коронарний атеросклероз, та, більш загально, на розлади, пов'язані з атеросклерозом, такі як ішемічна хвороба серця, периферійне судинне захворювання та церебральне судинне захворювання. Іншою метою даного винаходу є забезпечення регресії атеросклерозу та інгібування його клінічних наслідків, зокрема, поширення хвороби та смертності. Інгібітори МТР були описані в [WO-00/32582, WO-01/96327 та WO-02/20501]. Даний винахід заснований на несподіваному відкритті того, що нові N-арилпіперидин заміщені біфенілкарбоксаміди діють як селективні інгібітори МТР, тобто, здатні вибірково блокувати МТР на рівні стінки кишечнику в ссавців та, отже, є потенційними кандидатами як лікарські засоби, зокрема, для лікування гіперліпідемії. Даний винахід додатково надає декілька способів одержання таких Nарилпіперидин заміщених біфенілкарбоксамідів, а також фармацевтичних композицій, що містять такі сполуки. Крім того, винахід надає певну кількість нових сполук, що корисні як проміжні сполуки для одержання терапевтично активних Nарилпіперидин заміщених біфенілкарбоксамідів, а також способи одержання цих проміжних сполук. Та, нарешті, винахід надає спосіб лікування стану, вибраного з атеросклерозу, панкреатиту, ожиріння, гіперхолестеринемії, гіпертригліцеридемії, гіперліпідемії, діабету та діабету II типу, що включає введення ссавцю терапевтично активної кількості сполуки формули (І)· Даний винахід відноситься до сімейства нових сполук формули (І) (I) їх N-оксидів, фармацевтично прийнятних кислотно-адитивних солей та стереохімічно ізомерних форм, де R1 являє собою водень, С1-4алкіл, галоген або полігалогенС 1-4алкіл; R2 являє собою водень, С1-4алкіл, галоген або полігалогенС 1-4алкіл; R3 являє собою водень або С 1-4алкіл; R4 являє собою водень, С1-4алкіл або галоген; n є цілим числом, рівним 0 або 1; X1 являє собою атом вуглецю та X2 являє собою атом вуглецю; або X1 являє собою атом азоту та X2 являє собою атом вуглецю; або X1 являє собою атом вуглецю та X являє собою атом азоту; X3 являє собою атом вуглецю або азоту; Υ являє собою О або NR6, де R6 являє собою водень або С1-4алкіл; R5 являє собою радикал формули (а-1) 7 83510 або (а-2) де m є цілим числом, рівним 0, 1 або 2; Ζ являє собою О або ΝΗ; R7 являє собою водень; С1-6алкіл; С1-6алкіл, заміщений гідроксильною групою, аміно-, моно- або ді(С1-4алкіл)аміногрупою, С14алкілоксикарбонілом, амінокарбонілом, арилом або гетероарилом; С1-4алкіл-О-С 1-4алкіл; С1-4алкіл-S-С1-4алкіл або арил; R8 являє собою водень або С 1-6алкіл; R9 являє собою водень, С1-4алкіл, арил або С11 4алкіл, заміщений арилом ; або коли Υ являє собою NR6, радикали R5 та R6 можуть бути взяті разом з атомом азоту, до якого вони приєднані, утворюючи піролідиніл, заміщений С1-4алкілоксикарбонілом та необов'язково додатково заміщений гідроксилом; або піперидиніл, заміщений С 1-4алкілоксикарбонілом; арил являє собою феніл; феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно вибраний з С 1-4алкілу, С14алкілокси, галогену, гідроксигрупи, нітро, ціаногрупи, С1-4алкілоксикарбонілу, трифторметилу або трифторметокси; або бензо[1,3]діоксоліл; арил1 являє собою феніл; феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно вибраний з С 1-4алкілу, С14алкілокси, галогену, гідроксигрупи, нітро, ціаногрупи, С1-4алкілоксикарбонілу, трифторметилу або трифторметокси; та гетероарил являє собою імідазоліл, тіазоліл, індоліл або піридил. За винятком особливо зазначених випадків, у представлених ви ще та нижче визначеннях: - термін «галоген» є загальним для фтору, хлору, брому та йоду; - термін «С1-4алкіл» відноситься до насичених вуглеводневих радикалів з прямим або розгалуженим ланцюгом, що містить від 1 до 4 атомів вуглецю, таких як, наприклад, метил, етил, пропіл, нбутил, 1-метилетил, 2-метилпропіл, 1,1диметилетил та т.п.; - термін «С1-6алкіл» включає С1-4алкіл (який визначений вище) та його вищі гомологи, що містять 5 або 6 атомів вуглецю, такі як, наприклад, 2метилбутил, н-пентил, диметилпропіл, н-гексил, 2метилпентил, 3-метилпентил та т.п.; - термін «полігалогенС1-4алкіл» означає С14алкіл, заміщений 2-6 атомами галогену, такий як дифторметил, трифторметил, трифторетил та т.п.; - термін «С1-4алкіламіно» визначає вторинні аміногрупи, що містять від 1 до 4 атомів вуглецю, такі як, наприклад, метиламіно, етиламіно, пропіламіно, ізопропіламіно, бутиламіно, ізобутиламіно та т.п.; 8 - термін «ді(С1-4алкіл)аміно» визначає третинні аміногрупи, що містять від 1 до 4 атомів вуглецю, такі як, наприклад, диметиламіно, діетиламіно, дипропіламіно, діізопропіламіно, N-метил-Nетиламіно, N-етил-N'-пропіламіно та т.п. Термін «фармацевтично прийнятні кислотноадитивні солі», що використовується в даному описі, включає терапевтично активні нетоксичні кислотно-адитивні сольові форми, що можуть утворювати сполуки формули (І). Фармацевтично прийнятні кислотно-адитивні солі стандартно можуть бути отримані обробкою основної форми такою підходящою кислотою. Підходящі кислоти включають, наприклад, неорганічні кислоти, такі як галогенводневі кислоти, наприклад, соляна або бромистоводнева кислота, сірчана, азотна, фосфорна та подібні кислоти; або органічні кислоти, такі як, наприклад, оцтова, пропанова, оксіоцтова, молочна, піровиноградна, щавлева (тобто етандіонова), малонова, бурштинова (тобто бутандіонова кислота), малеїнова, фумарова, яблучна, винна, лимонна, метансульфонова, етансульфонова, бензолсульфонова, п-толуолсульфонова, цикламінова, саліцилова, п-аміносаліцилова, памова та подібні кислоти. Зазначені сольові форми можуть бути перетворені навпаки у форму вільної основи обробкою підходящою основою. Термін «адитивна сіль», зазначений вище, включає також сольвати, що здатні утворювати сполуки формули (І). Такими сольватами є, наприклад, гідрати, алкоголяти та т.п. N-оксидні форми сполук формули (І), що можуть бути отримані за допомогою відомих з рівня техніки способів, включають сполуки формули (І), в яких атом азоту окиснений до N-оксиду. Зокрема, зазначені N-оксидні форми являють собою сполуки формули (І), де атом азоту піперидинільної групи є окисненим. Термін «стереохімічно ізомерні форми», зазначений в описі вище, визначає всі можливі ізомерні форми, які можуть мати сполуки формули (І). За винятком особливо зазначених випадків, хімічне позначення сполуки включає суміш всіх можливих стереохімічно ізомерних форм, причому зазначені суміші містять всі діастереомери та енантіомери основної молекулярної структури. Більш особливо, стереогенні центри можуть мати R- або S-конфігурацію, замісники на двовалентних циклічних (частково) насичених радикалах можуть мати цис- або транс-конфігурацію. За винятком особливо зазначених випадків, хімічне позначення сполук означає суміш всіх можливих стереоізомерних форм, причому зазначені суміші містять всі діастереомери та енантіомери основної молекулярної структури. Це поширюється і на проміжні сполуки, описані в даній заявці, які використовуються для одержання кінцевих продуктів формули (І). Терміни «цис-» та «транс-» використовуються в описі відповідно до номенклатури Chemical Abstracts та відносяться до положення замісників на кільцевому фрагменті. Абсолютна стереохімічна конфігурація сполук формули (І) та проміжних сполук, що використовуються для їх одержання, може бути легко визна 9 83510 чена фахівцем в даній галузі техніки, використовуючи добре відомі методи, такі як, наприклад, рентгенографічна дифракція. Крім того, деякі сполуки формули (І) та деякі проміжні сполуки, що використовуються для їх одержання, можуть виявляти поліморфізм. Зрозуміло, що даний винахід включає будь-які поліморфні форми, що мають властивості, корисні для лікування станів, зазначених вище. В одному варіанті здійснення даний винахід відноситься до сполук формули (І), їх N-оксидів, фармацевтично прийнятних кислотно-адитивних солей та стереохімічно ізомерних форм, де R1 являє собою водень, С1-4алкіл, галоген або полігалогенС 1-4алкіл; R2 являє собою водень, С1-4алкіл, галоген або полігалогенС 1-4алкіл; R являє собою водень або С1-4алкіл; R4 являє собою водень, С1-4алкіл або галоген; n є цілим числом, рівним 0 або 1; X1 являє собою атом вуглецю та X2 являє собою атом вуглецю; або X1 являє собою атом азоту та X2 являє собою атом вуглецю; або X1 являє собою атом вуглецю та X2 являє собою атом азоту; X3 являє собою атом вуглецю або атом азоту; Υ являє собою О або NR6, де R6 являє собою водень або С1-4алкіл; R5 являє собою радикал формули (а-1) або (а-2) m є цілим числом, рівним 0, 1 або 2; Ζ являє собою О або ΝΗ; R7 являє собою водень; С1-6алкіл; С1-6алкіл, заміщений гідроксильною групою, аміно, моно- або ді(С1-4алкіл)аміно, С1-4алкілоксикарбонілом, амінокарбонілом, арилом або гетероарилом; С1-4алкіл-О-С 1-4а алкіл; С1-4алкіл-S-С1-4алкіл або арил; R8 являє собою водень або С 1-6алкіл; R9 являє собою С 1-4алкіл, феніл або бензил; або коли Υ являє собою NR6, радикали R5 та 6 R можуть бути взяті разом з атомом азоту, до якого вони приєднані, утворюючи піролідиніл, заміщений С1-4алкілоксикарбонілом та необов'язково додатково заміщений гідроксилом; або піперидиніл, заміщений С 1-4алкілоксикарбонілом; арил являє собою феніл; феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно вибраний з С 1-4алкілу, С14алкілокси, галогену, гідроксигрупи, нітро, ціаногрупи, С1-4алкілоксикарбонілу, трифторметилу або трифторметокси; або бензо[1,3]діоксоліл; та гетероарил являє собою імідазоліл, тіазоліл, індоліл або піридиніл. 10 В іншому варіанті здійснення даний винахід відноситься до сполук формули (І), їх Ν-оксидів, фармацевтично прийнятних кислотно-адитивних солей та стереохімічно ізомерних форм, де R1 являє собою полігалогенС1-4алкіл; R2 являє собою водень або С 1-4алкіл; R3 являє собою водень або С 1-4алкіл; R4 являє собою водень; n є цілим числом, рівним 0 або 1; X1 являє собою атом вуглецю та X2 являє собою атом вуглецю; або X1 являє собою атом азоту та X2 являє собою атом вуглецю; або X1 являє собою атом вуглецю та X2 являє собою атом азоту; X3 являє собою атом вуглецю або атом азоту; Υ являє собою О або NR6, де R6 являє собою водень або С1-4алкіл; R5 являє собою радикал формули (а-2) де m є цілим числом, рівним 0 або 1; Ζ являє собою О або ΝΗ; R7 являє собою водень; С1-6алкіл; С1-6алкіл, заміщений аміногрупою, С1-4алкілоксикарбонілом, арилом або гетероарилом; С1-4алкіл-S-С1-4алкіл або арил; R8 являє собою водень або С 1-6алкіл; R9 являє собою С 1-4алкіл; або коли Υ являє собою NR6, радикали R5 та 6 R можуть бути взяті разом з атомом азоту, до якого вони приєднані, утворюючи піролідиніл, заміщений С1-4алкілоксикарбонілом та необов'язково додатково заміщений гідроксилом; або піперидиніл, заміщений С 1-4алкілоксикарбонілом; арил являє собою феніл; феніл, заміщений гідроксилом, або бензо[1,3]діоксоліл; гетероарил являє собою імідазоліл. Група сполук, що представляють інтерес, складається зі сполук формули (І), де застосовують одне або декілька з наступних обмежень: a) R1 являє собою трет-бутил або трифторметил; b) R 2 являє собою водень або С 1-4алкіл; c) R3 являє собою водень; d) R 4 являє собою водень; e) Υ являє собою NR6, де R6 являє собою водень або метил; f) Z являє собою О; g) R 8 являє собою водень; h) R 9 являє собою С 1-4алкіл. Першу особливу гр уп у сполук складають сполуки формули (І), де X , X2 та X3 являють собою атом вуглецю. Другу особливу гр уп у сполук складають сполуки формули (І), де X1 являє собою атом вуглецю, X2 являє собою атом азоту та X3 являє собою атом вуглецю. Третю особливу групу сполук складають сполуки формули (І), де X1 являє собою атом азоту, X2 являє собою атом вуглецю та X3 являє собою атом вуглецю. 11 83510 Четверту особливу гр уп у сполук складають сполуки формули (І), де X1 являє собою атом вуглецю, X2 являє собою атом азоту та X3 являє собою атом азоту. П'яту особливу гр упу сполук складають сполуки формули (І), де n є цілим числом, рівним 1. Першу переважну груп у сполук складають сполуки формули (І), де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, рівним 1; Υ являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, рівним 0. Другу переважну групу сполук складають сполуки формули (І), де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, рівним 1; Υ являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-1), де m є цілим числом, рівним 1. Третю переважну групу сполук складають сполуки формули (І), де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X являють собою атоми вуглецю; n є цілим числом, рівним 1; Υ являє собою NR6, де R6 являє собою водень або метил; та R5 являє собою радикал формули (а-2), де m є цілим числом, рівним 1. Четверту переважну груп у сполук складають сполуки формули (І), де R1 являє собою трифторметил; R2 являє собою водень; R3 являє собою водень; R4 являє собою водень; X1, X2 та X3 являють собою атоми вуглецю; n є цілим числом, рівним 1; Υ являє собою NR6, та R5 і R6, взяті разом з атомом азоту, до якого вони приєднані, утворюють піролідиніл, заміщений С 1-4алкілоксикарбонілом та необов'язково додатково заміщений гідроксилом, або піперидиніл, заміщений С14алкілоксикарбонілом. Особливу гр упу сполук складають переважні групи сполук, де R8 являє собою водень та R9 являє собою С 1-4алкіл. Перший спосіб одержання сполук формули (І) представляє собою спосіб, в якому проміжну сполуку формули (II) (II) де R3, R4, R5, Υ, n, X1, X2 та X3 мають значення, визначені у формулі (І), піддають взаємодії з біфенілкарбоновою кислотою або галогенангідридом формули (III) (III) де R1 та R2 мають значення, визначені у формулі (І), та Q вибраний з гідроксигрупи та галогену, в, принаймні, одному реакційно-інертному розчин 12 нику та необов'язково в присутності підходящої основи, причому зазначений спосіб додатково необов'язково включає перетворення сполуки формули (І) в її адитивн у сіль та/або одержання її стереохімічно ізомерних форм. У випадку, коли Q1 являє собою гідроксигрупу, може бути прийнятним активувати бі фенілкарбонову кислоту формули (III) додаванням ефективної кількості промотору реакції. Необмежуючі приклади таких промоторів включають карбонілдіімідазол, дііміди, такі як Ν,Ν'дициклогексилкарбодіімід (DCC) або 1-етил-3-(3'диметиламінопропіл)карбодіімід (EDCI) та їх функціональні похідні. Для способів ацилювання такого типу переважно використовувати полярний апротонний розчинник, такий як, наприклад, дихлорметан. Підходящі основи для проведення даного першого способу включають третинні аміни, такі як триетиламін, триізопропіламін та подібні. Підходящі температури для проведення першого способу за даним винаходом звичайно знаходяться в інтервалі приблизно від 20°С до приблизно 140°С в залежності від конкретного розчинника, що використовують, та в більшості випадків будуть дорівнювати температурі кипіння зазначеного розчинника. Другий спосіб одержання сполуки за даним винаходом представляє собою спосіб, в якому проміжну сполуку формули (IV) (IV) де R1, R2, R3,R4 , n, X1, X2 та X3 мають значення, визначені у формулі (І), та Q2 вибраний з галогену та гідроксигрупи, піддають взаємодії з проміжною сполукою (V) формули H-NR5R6, де R5 та R6 мають значення, визначені для сполук формули (І), в, принаймні, одному реакційно-інертному розчиннику та необов'язково в присутності, принаймні, одного підходящого регенту сполучення та/або підходящої основи, причому зазначений спосіб необов'язково включає перетворення сполуки формули (І) в її кислотно-адитивну сіль та/або одержання її стереохімічно ізомерних форм. У випадку, коли Q2 являє собою гідроксигрупу, може бути прийнятним активува ти карбонову кислоту формули (IV) додаванням ефективної кількості промотору реакції. Необмежуючі приклади таких промоторів включають карбонілдіімідазол, дііміди, такі як DCC, EDCI, гідроксибензотриазол, гексафторфосфат бензотриазол-1-іл-Nокситрис(диметиламіно)фосфонію (ВОР), гексафторфосфат тетрапіролідинофосфонію, гексафторфосфат бромтрипіролідинофосфонію або їх функціональні похідні, такі як сполуки, описані в ["Solid-Phase Synthesis: A Practical Guide", ed. by Steven A. Kates and Fernando Albericio, Marcel Dekker, Inc., 2000 (ISBN: 0-8247-0359-6) на сторінках 306-319]. Третій спосіб одержання сполуки відповідно до даного винаходу представляє собою спосіб, в якому проміжну сполуку формули (VI) 13 83510 14 (VI) де R1, R2, R3 , R4, X1, X2 та X3 мають значення, визначені у формулі (І), та Q3 вибраний з галогену, В(ОН)2, алкілборонатів та їх циклічних аналогів, піддають взаємодії з реагентом формули (VII) (VII) де n, R5 та Υ мають значення, визначені у формулі (І), в, принаймні, одному реакційноінертному розчиннику та необов'язково в присутності, принаймні, одного реагенту сполучення з перехідного металу та/або, принаймні, одного підходящого ліганду, причому зазначений спосіб необов'язково включає перетворення сполуки формули (І) в її кислотно-адитивну сіль та/або одержання її стереохімічно ізомерних форм. Даний тип реакції відомий в даній галузі техніки як реакція Бухвальда (Buchwald), причому опис використовуваних реагентів сполучення з металів та/або підходящих лігандів, наприклад, сполук паладію, таких як тетра(трифенілфосфін)паладію, трис(дифеніліден)ацетондипаладію, 2,2'біс(дифенілфосфіно)-1,1'-бінафтил (BINAP) та т.п., можна знайти, наприклад, у [Tetrahedron Letters, (1996), 37(40), 7181-7184 та J. Am. Chem Soc, (1996), 118: 7216]. Якщо Q3 являє собою В(ОН)2, алкілборонат або його циклічний аналог, тоді, згідно [Tetrahedron Letters, (1998), 39: 2933-6], як реагент сполучення варто використовувати ацетат міді. Сполуки формули (1-а), визначені як сполуки формули (І), де Υ являє собою ΝΗ та R3 являє собою водень, легко можуть бути отримані з використанням методів твердофазного синтезу, як показано на Схемі 1 нижче. Звичайно твердофазний синтез включає взаємодію проміжної сполуки в синтезі з полімерним носієм. Дана проміжна сполука, нанесена на полімерний носій, може проходити через ряд стадій синтезу. Після кожної стадії домішки видаляють фільтруванням смоли та багаторазовим промиванням різними розчинниками. На кожній стадії смола може бути піддана розщепленню для взаємодії з різними проміжними сполуками на наступній стадії, надаючи можливість, таким чином, здійснювати синтез великої кількості сполук. Після останньої стадії синтезу смолу піддають обробці реагентом або процесу для відділення смоли від зразка. Більш докладне пояснення методів, що використовуються в твердофазній хімії описані, наприклад, у публікації ["Handbook of Combinatorial Chemistry: Drugs, Catalysts, Materials" ed. by K.C. Nicolaou, R. Hanko, W. Hartwig, vv.1-2, Wiley (ISBN: 3-527-30509-2)]. Схема 1 Замісники R1, R2, R4, R4, R5 . n, X1, X2 та X3 мають значення, визначені для сполук формули (І). PG являє собою захисну групу, таку як, наприклад, С1-6алкілоксикарбоніл, фенілметилоксикарбоніл, трет-бутоксикарбоніл, 9флуоренілметоксикарбоніл (Fmoc) та т.п.Використані скорочення мають наступні значення: "NMP" означає N-метил-2-піролідон, "DIPEA" означає діізопропілетиламін, "TFA" означає трифтороцтову кислоту, "TIS" означає триізопропілсилан. Сполуки формули (І-b), визначені як сполуки формули (І), де R3 являє собою водень, можуть бути отримані з використанням методу твердофазного синтезу, представленого на схемі 2. Схема 2 15 83510 Замісники R1, R2, R4, R4, R5, Υ, n, Χ1, X2 та Χ3 мають значення, визначені для сполук формули (І). Використані скорочення мають наступні значення: "ΝΜΡ" означає N-метил-2-піролідон, "DIPEA" означає діізопропілетиламін, "TFA" означає трифтороцтову кислоту, "TIS" означає триізопропілсилан, "DMAP" означає диметиламінопіридин та "ΒΙΝΑΡ" означає 2,2'-біс(дифенілфосфіно)-1,1'бінафтил. Сполуки формули (І), що отримані описаними вище способами, можуть бути синтезовані у формі рацемічних сумішей енантіомерів, що можуть бути розділені наступними відомими методами розділення. Сполуки формули (І), отримані в рацемічній формі, можуть бути перетворені у відповідні діастереомерні сольові форми взаємодією з підходящої хіральною кислотою. Зазначені діастереомерні сольові форми послідовно розділяють, наприклад, селективною або фракційною кристалізацією з наступним виділенням енантіомерів за допомогою лугу. Альтернативний спосіб розділення енантіомерних форм сполук формули (І) включає рідинну хроматографію з використанням хіральної стаціонарної фази. Зазначені стереохімічно чисті ізомерні форми також можуть бути отримані з відповідних стереохімічно чистих ізомерних форм підходящих ви хідних речовин за умови, що реакція відбувається стереоспецифічно. Переважно, якщо бажано отримати конкретний стереоізомер, зазначена сполука буде синтезована стереоспецифічними способами одержання. В даних способах переважно будуть використовуватися енантіомерно чисті вихідні речовини. Сполуки формули (І), їх N-оксидні форми, фармацевтично прийнятні солі та стереоізомерні форми мають корисну інгібуючу активність у відношенні аполіпопротеїну В та супутню активність зниження вмісту ліпідів. Отже, представлені сполуки формули (І) корисні як лікарський засіб, особливо в способі лікування пацієнтів, що страждають на гіперліпідемію, ожиріння, атеросклероз або діабет II типу. Зокрема, представлені сполуки можуть 16 застосовуватися для одержання лікарського засобу для лікування розладів, викликаних надлишком ліпопротеїнів дуже низької густини (VLDL) або ліпопротеїнів низької густини (LDL) та, особливо, розладів, викликаних холестерином, пов'язаним із зазначеними VLDL та LDL. Очевидно, основний механізм дії сполук формули (І), включає інгібування активності МТР (білка переносу мікросомальних тригліцеридів) в гепатоцитах та клітинах кишкового епітелію, що приводить до зниження продукування VLDL та хіломікронів, відповідно. Це є новим інноваційним підходом до гіперліпідемії та, як очікується, до зниження LDL-холестерину та тригліцеридів за допомогою зниження продукування VLDL печінкою та продукування хіломікронів кишечником. Велика кількість спадкових та придбаних захворювань може призводити до гіперліпідемії. Вони можуть підрозділятися на первинні та вторинні гіперлшідемічні стани. Найбільш розповсюдженими причинами вторинних гіперліпідемій є цукровий діабет, зловживання алкоголем, наркотики, гіпотиреоз, хронічна ниркова недостатність, нефротичний синдром, холестаз та булімія. Первинними гіперліпідеміями є загальна гіперхолестеринемія, сімейна загальна гіперліпідемія, сімейна гіперхолестеринемія, залишкова гіперліпідемія, синдром хіломікронемії та сімейна гіпертригліцеридемія. Сполуки за даним винаходом також можуть застосовува тися для профілактики або лікування пацієнтів, що страждають на ожиріння або атеросклероз, особливо коронарний атеросклероз, та, більш загально, на захворювання, що пов'язані з атеросклерозом, наприклад, ішемічною хворобою серця, периферійним судинним захворюванням та церебральним судинним захворюванням. Сполуки за даним винаходом можуть викликати регресію атеросклерозу та інгібувати клінічні наслідки атеросклерозу, зокрема захворюваності та смертність. Наслідком можливості такого застосування сполук формули (І) є те, що даний винахід надає також спосіб лікування теплокровних тварин, включаючи людей (у даному описі названих пацієнтами), що страждають на розлади, викликані надлишком ліпопротеїнів дуже низької густини (VLDL) або ліпопротеїнів низькою густини (LDL), та особливо розлади, викликані холестерином, пов'язаним із зазначеними VLDL та LDL. Отже, запропоновано спосіб лікування для полегшення станів пацієнтів, що страждають на, наприклад, гіперліпідемію, ожиріння, атеросклероз або діабет II типу. Аро В-48, синтезований кишечником, необхідний для складання хіломікронів та тому відіграє важливу роль у поглинанні харчових жирів у кишечнику. Даний винахід надає похідні біфенілкарбоксаміду, що діють як селективні інгібітори МРТ на рівні стінки кишечнику. Крім того, даний винахід надає фармацевтичні композиції, що містять, принаймні, один фармацевтично прийнятний носій та терапевтично ефективну кількість сполуки формули (І). Для одержання фармацевтичних композицій за даним винаходом ефективну кількість конкретної сполуки у формі вільної основи або адитивної 17 83510 солі, як активний інгредієнт, ретельно змішують з, принаймні, одним фармацевтично прийнятним носієм, що може приймати різні форми в залежності від бажаної форми препарату для введення. Дані фармацевтичні композиції бажано являють собою одиничну дозовану форму, що підходить переважно для перорального введення, ректального введення, крізьшкірного введення або парентеральної ін'єкції. Наприклад, при одержанні композиції в дозованій формі для перорального введення може застосовуватися будь-який зі звичайних рідких фармацевтичних носіїв, такий як, наприклад, вода, гліколі, олії, спирти та подібні, у випадку рідких препаратів для перорального введення, таких як суспензії, сиропи, еліксири та розчини; або будьякий з твердих фармацевтичних носіїв, таких як крохмалі, цукри, каолін, лубриканти, зв'язуючі речовини, агенти дезинтеграції та подібні, у випадку порошків, пігулок, капсул або таблеток. Через легкість введення таблетки та капсули являють собою найбільш переважну одиничну дозовану форму для перорального введення, в якій у цьому випадку використовуються тверді фармацевтичні носії. Фармацевтичний носій в композиціях для парентеральної ін'єкції буде включати, головним чином, стерильну воду, хоча можуть бути включені й інші інгредієнти для поліпшення розчинності активного інгредієнта. Розчини для ін'єкцій можуть бути отримані, наприклад, з використанням фармацевтичного носія, що включає фізіологічний розчин, розчин глюкози або їх суміш. Суспензії для ін'єкцій можуть бути о тримані з використанням підходящих рідких носіїв, суспендуючих агентів та т.п.В композиціях, що підходять для крізьшкірного введення, фармацевтичний носій може необов'язково включати добавки, що підвищують проникнення крізь шкіру, та/або прийнятний зволожуючий агент, необов'язково об'єднані з підходящими добавками, які використовуються в невеликих кількостях, що не здійснюють значного несприятливого впливу на шкіру. Зазначені добавки можуть бути вибрані для полегшення введення активного інгредієнта крізь шкіру та/або щоб сприяти одержанню бажаних композицій. Такі композиції для місцевого введення можуть бути введені різними способами, наприклад, у ви гляді трансдермального пластиру, крапковим нанесенням або у вигляді мазі. Адитивні солі сполук формули (І), внаслідок їх підви щеної розчинності в порівнянні з відповідною основною формою, мабуть, є більш підходящими для одержання водних композицій. Особливо переважно одержувати фармацевтичні композиції за даним винаходу в одиничній дозованій формі для легкості введення та однорідності дозування. Термін «одинична дозована форма», що використовується у даному описі, відноситься до фізично дискретних одиниць, що підходять для застосування як одиничні дози, причому кожна одиниця містить визначену кількість активного інгредієнта, розраховану для одержання бажаного терапевтичного ефекту, у сполученні з необхідним фармацевтичним носієм. Прикладами таких одиничних дозованих форм є таблетки (включаючи таблетки з надсічками або таблетки з 18 покриттям), капсули, пігулки, порошки в пакетах, пластини, розчини або суспензії для ін'єкцій, дози в чайних ложках, столових ложках та т.п., та їх різноманітні різновиди. Фармацевтичні композиції за даним винаходом для перорального введення можуть приймати форму твердих дозованих форм, наприклад, таблеток (для ковтання та розжовування), капсул або желатинових капсул, отриманих стандартними способами з фармацевтично прийнятними ексципієнтами та носіями, такими як зв'язуючі агенти (наприклад, попередньо желатинізований кукурудзяний крохмаль, полівінілпіролідон, гідроксипропілметилцелюлоза та т.п.), наповнювачі (наприклад, лактоза, мікрокристалічна целюлоза, фосфа т кальцію та т.п.), лубриканти (наприклад, стеарат магнію, тальк, діоксид кремнію та т.п.), агенти дезинтеграції (наприклад, картопляний крохмаль, натрійкрохмальгліколят та т.п.), зволожуючі агенти (наприклад, натрійлаурилсульфат) та т.п.Такі таблетки також можуть бути покриті оболонкою за допомогою способів, що добре відомі з рівня техніки. Рідкі препарати для перорального введення можуть приймати форму, наприклад, розчинів, сиропів або суспензій, або вони можуть бути отримані у формі сухого продукту для змішування перед застосуванням з водою та/або іншим підходящим носієм. Такі рідкі препарати можуть бути отримані стандартними способами, необов'язково з іншими фармацевтично прийнятними добавками, такими як суспендуючі агенти (наприклад, сорбітовий сироп, метилцелюлоза, гідроксипропілметилцелюлоза або гідрогенізовані харчові жири), емульгатори (наприклад, лецитин або гуміарабік), неводні носії (наприклад, мигдальне масло, маслянисті складні ефіри або етиловий спирт), підсолоджуючі речовини, ароматизатори, речовини, що маскують неприємний смак, та консерванти (наприклад, метил- або пропіл-п-гідроксибензоати або сорбінова кислота). Фармацевтично прийнятні підсолоджуючі речовини, що використовують у фармацевтичних композиціях за даним винаходом, переважно включають, принаймні, одну інтенсивну підсолоджуючу речовина, таку як аспартам, ацесульфам калію, цикламат натрію, алітам, дигідрохальконовий підсолоджувач, монелін, стевіозид сукралоза (4,1',6'-трихлор-4,1',6'-тридезоксигалактосахароза) або, переважно, сахарин, натрієва або кальцієва сіль сахарину та, необов'язково, принаймні, одну об'ємну підсолоджуючу речовину, таку як сорбіт, маніт, фр уктоза, сахароза, мальтоза, ізомальт, глюкоза, сироп гідрогенізованої глюкози, ксиліт, карамель або мед. Інтенсивні підсолоджуючі речовини звичайно застосовують з низькими концентраціями. Наприклад, у випадку натрієвої солі сахарину зазначена концентрація може знаходитися в інтервалі приблизно від 0,04% до 0,1% (мас/об.) кінцевої композиції. Об'ємна підсолоджуюча речовина може ефективно використовуватися з великими концентраціями, що знаходяться в інтервалі приблизно від 10% до приблизно 35%, переважно приблизно від 10% до 15% (мас/об.). 19 83510 Фармацевтично прийнятні ароматизатори, що можуть приховувати гіркий смак інгредієнтів в композиціях низького дозування, переважно являють собою фруктові ароматизатори, такі як ароматизатори зі смаком вишні, малини, чорної смородини або суниці. Сполучення двох ароматизаторів може приводити до дуже гарних результатів. У композиціях високого дозування можуть бути необхідними більш сильні фармацевтично прийнятні ароматизатори, такі як «карамельний шоколад», «охолоджуюча м'ята», «фантазія» та т.п.Кожний ароматизатор може бути присутній в кінцевій композиції в концентрації в інтервалі приблизно від 0,05% до 1% (мас./об.). Переважно застосовуються сполучення зазначених сильних ароматизаторів. Переважно використовують ароматизатор, що не піддається якій-небудь зміні або не втрачає смак та/або колір при введенні в композицію. Сполуки формули (І) можуть бути введені в композицію для парентерального введення за допомогою ін'єкції, зручно внутрішньовенної, внутрішньом'язової або підшкірної ін'єкції, наприклад, за допомогою болюсного вливання або безперервного внутрішньовенного вливання. Композиції для ін'єкції можуть бути представлені в одиничній дозованій формі, наприклад, в ампулах або в контейнерах з багаторазовими дозами, що включають доданий консервант. Вони можуть приймати такі форми, як суспензії, розчини або емульсії в масляних або водних носіях, та можуть містити добавки, що сприяють одержанню композиції, такі як ізотонізуючі, суспендуючі, стабілізуючі та/або диспергуючі агенти. Альтернативно, активний інгредієнт може бути присутній у формі порошку для змішування перед застосуванням з підходящим розріджувачем, наприклад, стерильною непірогенною водою. Сполуки формули (І) також можуть бути введені в композиції для ректального застосування, такі як супозиторії або затримуючі клізми, наприклад, що містять стандартну основу супозиторіїв, таку як масло какао та/або інші гліцериди. Сполуки формули (І) можуть застосовуватися в сполученні з іншими фармацевтичними лікарськими засобами, зокрема, фармацевтичні композиції за даним винаходом можуть додатково включати, принаймні, один додатковий ліпідознижуючий лікарський засіб, забезпечуючи, таким чином, так названу комбіновану терапії для зниження ліпідів. Зазначений додатковий ліпідознижуючий лікарський засіб може бути, наприклад, відомим лікарським засобом, що звичайно використовується для впливу на гіперліпідемію, таким як, наприклад, смола, що підсилює екскрецію жовчних кислот, похідне фібринової кислоти або нікотинова кислота, як зазначено вище в розділі опису попереднього рівня техніки. Підходящі додаткові ліпідознижуючі лікарські засоби включають також інші інгібітори біосинтезу холестерину та інгібітори абсорбції холестерину, зокрема, інгібітори HMG-Co редуктази та інгібітори HMG-Co синтази, інгібітори експресії гена HMG-Co редуктази, інгібітори СЕТР, інгібітори АСАТ, інгібітори скваленсинтетази та т.п. Будь-який інгібітор HMG-Co редуктази може бути використаний як друга сполука в аспекті ком 20 бінованої терапії за даним винаходом. Термін «інгібітор HMG-Co редуктази» в даному описі відноситься, за винятком особливо зазначених випадків, до сполуки, що інгібує біотрансформацію гідроксиметилглутарил-кофермента А в мевалонову кислоту, що каталізується ферментом HMGCo редуктази. Такими «інгібіторами HMG-Co редуктази» є, наприклад, ловастатин, симвастатин, флуваста тин, правастатин, ривастатин та аторвастатин. Будь-який інгібітор HMG-Co синтази може бути використаний як друга сполука у варіанті комбінованої терапії за даним винаходом. Термін «інгібітор HMG-Co синтази», що використовується в даному описі, відноситься, за винятком особливо зазначених випадків, до сполуки, що інгібує біосинтез гідроксиметилглутарил-кофермента А з ацетилу-коферменту А та ацетоацетил-кофермента А, що каталізується ферментом HMG-Co синтази. Будь-який інгібітор експресії гена HMG-Co редуктази може бути використаний як друга сполука у варіанті комбінованої терапії за даним винаходом. Ці лікарські засоби можуть являти собою інгібітори транскрипції HMG-Co редуктази, що блокують транскрипцію ДНК, або інгібітори трансляції мРНК кодування HMG-Co редуктази в білок. Такі інгібітори можуть або впливати на транскрипцію або трансляцію безпосередньо, або можуть біотрансформуватися в сполуки, що мають описані вище властивості, під дією одного або декількох ферментів у каскаді біосинтезу холестерину або можуть приводити до акумулювання метаболіту, що має зазначені вище активності. Будь-який СЕТР інгібітор може бути використаний як друга сполука у варіанті комбінованої терапії за даним винаходом. Термін «інгібітор СЕТР», що використовується в описі, відноситься, за винятком особливо зазначених випадків, до сполуки, що інгібує транспорт різних холестеринових ефірів та тригліцеридів з HDL у LDL та VLDL, опосередкований білком переносу холестеринових ефірів (СЕТР). Будь-який інгібітор АСАТ може бути використаний як друга сполука у варіанті комбінованої терапії за даним винаходом. Термін «інгібітор АС АТ», що використовується в описі, відноситься, за винятком особливо зазначених випадків, до сполуки, що інгібує вн утрішньоклітинну етерифікацією холестерину їжі ферментом ацил СоА:холестеринацилтрансферази. Будь-який інгібітор скваленсинтетази може бути використаний як друга сполука у варіанті комбінованої терапії за даним винаходом. Термін «інгібітор скваленсинтетази», що використовується в описі, відноситься, за винятком особливо зазначених випадків, до сполуки, що інгібує конденсації двох молекул фарнезилпірофосфату з утворенням сквалену, що каталізується ферментом скваленсинтетази. Фахівець в області лікування гіперліпідемії, легко визначить терапевтично ефективну кількість сполуки формули (І) з результатів досліджень, представлених нижче. Звичайно мається на увазі, що терапевтично ефективна доза буде складати приблизно від 0,001мг/кг до приблизно 0,5мг/кг 21 83510 маси тіла пацієнта, що підлягає лікуванню. Може бути прийнятним введення терапевтично ефективної дози у формі двох або більш субдоз, що вводяться через підходящі інтервали часу протягом доби. Зазначені субдози можуть бути представлені у вигляді одиничної дозованої форми, кожна з яких містить, наприклад, приблизно від 0,1мг до приблизно 350мг, більш переважно приблизно від 1 до приблизно 200мг, активного інгредієнта на одиничну дозовану форму. Точне дозування та частота введення залежать від конкретної сполуки формули (І), що використовують, конкретного стану, що підлягає лікуванню, важкості стану, що підлягає лікуванню, віку, маси тіла та загального фізичного стану конкретного пацієнта, а також іншого лікування (включаючи зазначені вище додаткові ліпідознижуючі лікарські засоби), що може мати пацієнт, що добре відомо фахівцю в даній галузі техніки. Крім того, зазначена ефективна добова кількість може бути знижена або підвищена в залежності від реакції пацієнта, що підлягає лікуванню, та/або в залежності від оцінки лікаря, що прописує біфенілкарбоксамідні похідні за даним винаходом. Тому інтервали ефективної добової кількості, зазначені вище, є лише рекомендаціями. Експериментальна частина У методиках, описаних нижче, використовували наступні скорочення: "PS-DIEA" означає N,N(діізопропіл)амінометилполістирольну смолу, доступну від Argonaut (New Road, Hengoed, Mid Glamorgan CF82 8AU, United Kingdom) під кодом продукту 800279. "PS-DCC" означає Nциклогексилкарбодіімід-N'-метилполістирольну смолу, доступну від Calbiochem-Novabiochem AG, (Weidenmattweg 4, CH-4448 Laufelfingen, Switzerland) під кодом продукту No vabiochem 0164-0211. «ТГФ» означає тетрагідрофуран. А. Синтез проміжних сполук Приклад А. 1 a) Одержання проміжної сполуки (1) 4'-(Трифторметил)-[1,1'-біфеніл]-2-карбонову кислоту (0,0069моль) розчиняють в дихлорметані (400мл) разом з оксалілхлоридом (0,069моль) та диметилформамідом (одна крапля) при 0°С. Далі невеликими порціями додають 4'-(трифторметил)[1,1'-біфеніл]-2-карбонову кислоту (0,0621моль) в потоці азоту. Додають оксалілхлорид (0,069моль) та диметилформамід (одна крапля) та реакційну суміш перемішують протягом 2 годин при 0°С. Реакційну суміш фільтрують, залишок розчиняють в дихлорметані (100мл) та отриману суміш додають по краплям при 0°С до суміші етилового ефіру 1(4-амінофеніл)-4-піперидиноцтової кислоти (0,069моль), триетиламіну (17,5мл) та дихлорметану (300мл). Реакційній суміші дають нагрітися до 22 кімнатної температури протягом 90 хвилин. Отриману реакційну суміш промивають водою, сушать та розчинник випарюють. Залишок перемішують в теплій суміші гексану та етилацетату та одержаний осад відфільтровують теплим через целіт. Фільтрат охолоджують та одержаний осад відфільтровують, промивають ефіром та сушать, одержуючи 31г проміжної сполуки (1) (т.пл. 160-162°С). b) Одержання проміжної сполуки (2) Суміш проміжної сполуки (1) (0,015моль) в розчині концентрованої НСI (50мл) кип'ятять зі зворотним холодильником при перемішуванні протягом 90 хвилин. Одержаний осад відфільтровують, промивають водою та сушать. Отриманий осад (0,008моль) розчиняють в суміші розчину NaOH (1н, 50мл) та 2-пропанолу (100мл) та перемішують протягом 1 години при 50°С. Реакційну суміш охолоджують до кімнатної температури, додають НСI (1н, 70мл) та отриману суміш двічі екстрагують дихлорметаном. Екстракти поєднують, випарюють та отриманий залишок розтирають з дихлорметаном, одержуючи 4,1г проміжної сполуки (2). Приклад А.2 а) Одержання проміжної сполуки (3) 6-Метил-4'-(трифторметил)-[1,1’-біфеніл]-2карбонову кислоту (0,0025моль) розчиняють в суміші сухого дихлорметану (140мл), етандіоїлдихлориду (2,4мл) та декількох краплях диметилформаміду при 0°С. Потім в потоці азоту невеликими порціями додають залишкову 6-метил-4(трифторметил)-[1,1’-біфеніл]-2-карбонову кислоту (0,0225моль). Реакційну суміш обережно нагрівають до 40°С та витримують при цій температурі до одержання гомогенного розчину та припинення виділення газу. Отриманій суміші дають можливість охолонути до кімнатної температури, потім її фільтрують через лійку Бюхнера. Осад на фільтрі розчиняють в дихлорметані, потім отриманий розчин по краплям додають при 0°С до розчину етилового ефіру 1-(4-амінофеніл)-4-піперидиноцтової кислоти (1екв., 0,025моль) та триетиламіну (3г) в сухому дихлорметані (140мл). Реакційній суміші дають можливість нагріватися до кімнатної температури протягом 90 хвилин. Отриманий осад відфільтровують та сушать, одержуючи 13,65г проміжної сполуки (3) (т.пл. 150-151°С). b) Одержання проміжної сполуки (4) 23 83510 Гідроксид натрію (1н, 100мл) додають до розчину проміжної сполуки (3) (0,0334моль) в метанолі (300мл), потім реакційну суміш перемішують протягом 2 годин при 50°С та протягом 20 годин при кімнатній температурі. До суміші додають воду (300мл) та отриману суміш підкисляють за допомогою 1н НСI. Додають дихлорметан (200мл) та реакційну суміш перемішують протягом 2 годин, що потім утворений осад відфільтровують, промивають водою та дихлорметаном та сушать, одержуючи 17,1г проміжної сполуки (4), виділеної у вигляді гідрохлоридної солі (1:1). Приклад А.3 а) Одержання проміжної сполуки (5) Суміш етилового ефіру 4-піперидинкарбонової кислоти (0,03моль), 1-фтору-4-нітробензолу (0,03моль) та карбонату калію (4,5г) в диметилформаміді (50мл) піддають взаємодії протягом 4 годин при 60°С, потім розчинник випарюють при зниженому тиску та отриманий залишок поміщають у воду. Отриману тверду речовину жовтого кольору відфільтровують та переносять в дихлорметан (100мл). Органічний шар суша ть та розчинник випарюють. Отримане масло кристалізують з гексану, одержуючи 7г проміжної сполуки (5) (т.пл. 70-71°С). b) Одержання проміжної сполуки (6) Суміш проміжної сполуки (5) (0,025моль) та етанолу (150мл) гідрують при підвищеному тиску (30бар=3.106Па) протягом ночі при 25°С з використанням, як каталізатору, Pd/C (10%, 0,5г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш фільтрують та розчинник випарюють при зниженому тиску, одержуючи 6г проміжної сполуки (6). c) Одержання проміжної сполуки (7) Реакцію проводять в атмосфері азоту: 0,2г 4'(трифторметил)-[1,1’-біфеніл]-2-карбонову кислоту в дихлорметані (50мл) піддають взаємодії з етандіоїлдихлоридом (0,01моль) при 0°С та потім ініціюють реакцію диметилформамідом (1 крапля). Невеликими порціями додають залишок 4'(трифторметил)-[1,1’-біфеніл]-2-карбонової кислоти (1,8г) та додають надлишкову кількість етандіоїлдихлориду. Реакційну суміш перемішують протя 24 гом 2 годин при 0°С (відсутність кислоти при аналізі зразка реакційної суміші в метанолі методом ТПІХ), потім дихлорметан та надлишкову кількість етандіоїлдихлориду випарюють при зниженому тиску. Отриманий залишок переносять в дихлорметан (50мл) та по краплям додають до суміші проміжної сполуки (6) (0,0075моль) та триетиламіну (0,0075моль) в дихлорметані (50мл) при 0°С. Отриману суміш перемішують протягом 1 години при кімнатній температурі, потім органічний шар промивають водою, суша ть та розчинник випарюють при зниженому тиску. Отриманий залишок кристалізують з метанолу, одержуючи 2.9г проміжної сполуки (7) (т.пл. 190-192°С). d) Одержання проміжної сполуки (8) Проміжну сполуку (7) (0,006моль) додають до розчину NaOH (0,018моль) в етанолі (20мл) та воді (20мл) та потім реакційну суміш нагрівають до 60°С. Отриманий розчин витримують при 60°С протягом 1 години та охолоджують. Отриману суміш підкисляють за допомогою 4н НСI та перемішують протягом 1 години, потім утворений осад відфільтровують та промивають водою, одержуючи 2,7г проміжної сполуки (8) (т.пл. 260-262°С). Приклад А.4 a) Одержання проміжної сполуки (9) Суміш гідрату натрієвої солі нітромалональдегіду (CAS 53821-72-0) (0,06моль), сульфату метилового ефіру карбамімідотіонової кислоти (2:1) (0,03моль) та етилового ефіру 4піперидинкарбонової кислоти (0,047моль) у воді (200мл) перемішують протягом 2 годин при 80°С або до припинення виділення газоподібного метантіолу, потім утворений осад відфільтровують та промивають водою. Тверді речовини змішують з мінімальною кількістю метанолу, потім знову відфільтровують та промивають ефіром, одержуючи 4,8г проміжної сполуки (9) (т.пл. 114-116°С). b) Одержання проміжної сполуки (10) Суміш проміжної сполуки (9) (0,017моль) в етанолі (100мл) гідрують протягом 4 годин при 60°С з використанням, як каталізатору, паладію на вугіллі (10%, 0,5г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш відфільтровують та розчинник випарюють. Отриманий залишок очищають за допомогою колоночної хроматографії (елюент:етилацетат/гексан 1/2). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 3г проміжної сполуки (10). c) Одержання проміжної сполуки (11) 25 83510 Реакцію проводять в атмосфері азоту: 0,3г 4'(трифторметил)-[1,1’-біфеніл]-2-карбонової кислоти в дихлорметані (50мл) піддають взаємодії з етандіоїлдихлоридом (0,01моль) при 0°С та потім ініціюють реакцію додаванням диметилформаміду (1 крапля) Залишкову 4'-(трифторметил)-[1,1’біфеніл]-2-карбонову кислоту (2,7г) додають невеликими порціями отриманий залишок поміщають у воду. Отриману тверду речовину жовтого кольору відфільтровують та переносять в дихлорметан (100мл). Органічний шар сушать та розчинник випарюють. Отримане масло кристалізують з гексану, одержуючи 7г проміжної сполуки (5) (т.пл. 7071°С). b) Одержання проміжної сполуки (6) Суміш проміжної сполуки (5) (0,025моль) та етанолу (150мл) гідрують при підвищеному тиску (30бар=3.106Па) протягом ночі при 25°С з використанням, як каталізатору, Pd/C (10%, 0,5г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш фільтрують та розчинник випарюють при зниженому тиску, одержуючи 6г проміжної сполуки (6). c) Одержання проміжної сполуки (7) Реакцію проводять в атмосфері азоту: 0,2г 4'(трифторметил)-[1,1’-біфеніл]-2-карбонову кислоту в дихлорметані (50мл) піддають взаємодії з етандіоїлдихлоридом (0,01моль) при 0°С та потім ініціюють реакцію диметилформамідом (1 крапля). Невеликими порціями додають залишок 4'(трифторметил)-[1,1’-біфеніл]-2-карбонової кислоти (1,8г) та додають надлишкову кількість етандіоїлдихлориду. Реакційну суміш перемішують протягом 2 годин при 0°С (відсутність кислоти при аналізі зразка реакційної суміші в метанолі методом ТШХ), потім дихлорметан та надлишкову кількість етандіоїлдихлориду випарюють при зниженому тиску. Отриманий залишок переносять в дихлорметан (50мл) та по краплям додають до суміші проміжної сполуки (6) (0,0075моль) та триетиламіну (0,0075моль) в дихлорметані (50мл) при 0°С. Отриману суміш перемішують протягом 1 години при кімнатній температурі, потім органічний шар промивають водою, суша ть та розчинник випарюють при зниженому тиску. Отриманий залишок кристалізують з метанолу, одержуючи 2,9г проміжної сполуки (7) (т.пл. 190-192°С). d) Одержання проміжної сполуки (8) 26 Проміжну сполуку (7) (0,006моль) додають до розчину NaOH (0,018моль) в етанолі (20мл) та воді (20мл) та потім реакційну суміш нагрівають до 60°С. Отриманий розчин витримують при 60°С протягом 1 години та охолоджують. Отриману суміш підкисляють за допомогою 4н НСI та перемішують протягом 1 години, потім утворений осад відфільтровують та промивають водою, одержуючи 2,7г проміжної сполуки(8) (т.пл. 260-262°С). Приклад А.4 a) Одержання проміжної сполуки (9) Суміш гідрату натрієвої солі нітромалональдегіду (CAS 53821-72-0) (0,06моль), сульфату метилового ефіру карбамімідотіонової кислоти (2:1) (0,03моль) та етилового ефіру 4піперидинкарбонової кислоти (0,047моль) у воді (200мл) перемішують протягом 2 годин при 80°С або до припинення виділення газоподібного метантіолу, потім утворений осад відфільтровують та промивають водою. Тверді речовини змішують з мінімальною кількістю метанолу, потім знову відфільтровують та промивають ефіром, одержуючи 4,8г проміжної сполуки (9) (т.пл. 114-116°С). b) Одержання проміжної сполуки (10) Суміш проміжної сполуки (9) (0,017моль) в етанолі (100мл) гідрують протягом 4 годин при 60°С з використанням, як каталізатору, паладію на вугіллі (10%, 0,5г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш відфільтровують та розчинник випарюють. Отриманий залишок очищають за допомогою колоночної хроматографії (елюент: етилацетат/гексан 1/2). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 3г проміжної сполуки (10). c) Одержання проміжної сполуки (11) Реакцію проводять в атмосфері азоту 0,3г 4'(трифторметил)-[1,1'-біфеніл]-2-карбонової кислоти в дихлорметані (50мл) піддають взаємодії з етандіоїлдихлоридом (0,01моль) при 0°С та погім ініціюють реакцію додаванням диметилформаміду (1 крапля). Залишкову 4'-(трифторметил)-[1,1'біфеніл]-2-карбонову кислоту (2,7г) додають невеликими порціями (відсутність кислоти при аналізі зразка реакційної суміші в метанолі методом ТШХ) та розчинник випарюють при зниженому тиску. 27 83510 Отриманий залишок переносять в дихлорметан (50мл) та по краплям додають до суміші проміжної сполуки (10) (0,011моль) та триетиламіну (0,011моль) в дихлорметані (50мл) при 0°С. Отриману суміш перемішують протягом 30 хвилин та додатково очищають за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/гексан 1/4, 1/2). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 2,9г проміжної сполуки (11) (т.пл 171-173°С). d) Одержання проміжної сполуки (12) Проміжну сполуку (11) (0,006моль) додають до розчину NaOH (0,018моль) в етанолі (20мл) та воді (20мл), потім реакційну суміш нагрівають до 60°С та витримують при даній температурі протягом 1 години, потім охолоджують та підкисляють за допомогою 4н НСI. Одержаний осад відфільтровують, промивають водою та сушать, одержуючи 2,6г проміжної сполуки (12) (т.пл. 231-233°С). Приклад А. 5 a) Одержання проміжної сполуки (13) Суміш 2-хлор-5-нітропіридину (0,0227моль), етилового ефіру 4-піперидиноцтової кислоти (0,0227моль) та карбонату натрію (0,091моль) в диметилсульфоксиді (40мл) нагрівають до 60°С та перемішують при даній температурі протягом 2 годин, потім реакційну суміш охолоджують до кімнатної температури та виливають у крижану воду. Одержаний осад відфільтровують та промивають водою. Неочищений продукт у вигляді твердої речовини очищають кристалізацією із суміші етилацетат/гексан, одержуючи 3,2г проміжної сполуки (13) (т.пл. 99-101°С). b) Одержання проміжної сполуки (14) Суміш проміжної сполуки (13) (0,0102моль) в ТГФ (50мл) гідрують протягом 30 хвилин при 50°С з використанням, як каталізатору, паладію на вугіллі (10%, 0,3г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш охолоджують та каталізатор відфільтровують, потім фільтрат випарюють, одержуючи 2,6г проміжної сполуки (14). c) Одержання проміжної сполуки (15) 28 Розчин 6-метил-4'-(трифторметил)-[1,1’біфеніл]-2-карбонової кислоти (0,005моль) в 1,4діоксані (5мл) додають до розчину проміжної сполуки (14) (0,005моль) та триетиламіну (0,005моль) в 1,4-діоксані (15мл) при 10°С, потім реакційну суміш перемішують при кімнатній температурі протягом 60 годин. Отриману суміш розбавляють водою та екстрагують етилацетатом (100мл). Отриманий продукт промивають насиченим розчином солі, сушать та розчинник випарюють. Залишок очищають за допомогою колоночної хроматографії (елюент: етилацетат/гексан 1/4). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 1,7г проміжної сполуки (15) (т.пл. 134137°С). d) Одержання проміжної сполуки (16) Розчин NaOH (0.0114моль) у воді (20мл) додають до суміші проміжної сполуки (15) (0,0038моль) в етанолі (20мл) та потім реакційну суміш перемішують протягом 2 годин при 60°С. Після охолодження до кімнатної температури отриману суміш підкисляють за допомогою конц. НСI та розчинник випарюють. Отриманий залишок перемішують в діетиловому ефірі та цільовий продукт збирають, одержуючи 2,2г проміжної сполуки (16). Приклад А.6 а) Одержання проміжної сполуки (17) Водний 37% розчин формальдегіду (0,0072моль) та паладій на вугіллі (10%, 0,15г) додають до розчину етилового ефір у 1-(4амінофеніл)-4-піперидиноцтової кислоти (0,0057моль) в етилацетаті (40мл) та потім реакційну суміш гідрують протягом 5 годин. Після завершення поглинання водню (1 еквівалент) каталізатор відфільтровують через целіт та целіт промивають етилацетатом (40мл). Фільтрат випарюють та отриманий залишок поєднують із залишком, отриманим аналогічним чином. Отриманий залишок очищають за допомогою колоночної флеш-хроматографії (елюент: етилацетат/гексан 30/70). Фракції, що містять продукт, збирають, потім розчинник випарюють та отриманий маслянистий залишок сушать, одержуючи 1,6г проміжної сполуки (17). b) Одержання проміжної сполуки (18) 29 83510 Суміш 4'-(трифторметил)-[1,1’-біфеніл]-2карбонової кислоти (0,0058моль) в дихлорметані (40мл) перемішують при 0°С в атмосфері азоту, потім додають етандіоїлдихлорид (0,0087моль) з наступним додаванням диметилформаміду (2 краплі). Отриману суміш нагрівають до 15°С та витримують при даній температурі протягом 1 години, потім до 30-35°С та витримують при зазначеній температурі протягом 1 години. Розчинник випарюють та отриманий твердий залишок жовтого кольору розчиняють в дихлорметані. Отриманий розчин додають до розчину проміжної сполуки (17) (0,0058моль) та триетиламіну (0,0087моль) в дихлорметані в атмосфері азоту та потім реакційну суміш перемішують протягом 16 годин при кімнатній температурі. Отриману суміш розбавляють етилацетатом (100мл) та промивають 1н НСI (50мл), насиченим розчином NаНСО3 (50мл) та насиченим розчином солі (50мл). Органічний шар сушать та розчинник випарюють. Отримане масло додатково очищають за допомогою колоночної флеш-хроматографії (елюент: етилацетат/гексан 30/70). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 1,6г проміжної сполуки (18). c) Одержання проміжної сполуки (19) Реакцію проводять в атмосфері азоту: проміжну сполуку (18) (0,0029моль) розчиняють в етанолі (20мл) при 20°С та потім додають розчин NaOH (0,0087моль) у воді (20мл). Отриману емульсію перемішують протягом 16 годин при 20°С та протягом 1 години при 60°С. Реакційну суміш нейтралізують за допомогою 2н НСI, одержуючи суспензію. Етанол випарюють, потім водний концентрат охолоджують до 0°С та одержані тверді речовини відфільтровують. До фільтрату додають дихлорметан та отриману емульсію розділяють на шари. І, нарешті, розчинник випарюють, одержуючи 1г проміжної сполуки (19). Приклад А. 7 а) Одержання проміжної сполуки (20) Суміш гідрохлориду етилового ефір у 4піперидиноцтової кислоти (0,025моль), 5-бром-2нітропіридину (0,03моль) та карбонату калію (0,06моль) в диметилформаміді (100мл) витримують при 60°С протягом двох днів та потім розчинник випарюють при зниженому тиску. Отриманий 30 залишок змішують з водою та фільтрують. Отриманий на фільтрі осад переносять в дихлорметан (100мл), сушать та розчинник випарюють. Залишок очищають за допомогою колоночної флешхроматографії на силікагелі (елюент: етилацетат/гексан 1/5, 1/3). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 3,3г проміжної сполуки (20). b) Одержання проміжної сполуки (21) Суміш проміжної сполуки (20) (0,01моль) в етанолі (100мл) гідрують протягом ночі в автоклаві (30бар=3.106Па) при 30°С з використанням, як каталізатору, паладію на вугіллі (10%, 0,5г). Після завершення поглинання водню (3 еквіваленти) реакційну суміш відфільтровують та фільтрат випарюють, одержуючи 2,8г проміжної сполуки (21). c) Одержання проміжної сполуки (22) Реакцію проводять при 0°С в атмосфері азоту: етандіоїлдихлорид (0,01моль) та диметилформамід (2 краплі) додають до частини 6-метил-4'(трифторметил)-[1,1’-біфеніл]-2-карбонової кислоти (0,2г) в дихлорметані-(100мл) та потім невеликими порціями додають залишкову частину 6метил-4'-(трифторметил)-[1,1’-біфеніл]-2карбонової кислоти (1,9г) (відсутність кислоти при аналізі зразка реакційної суміші в метанолі методом ТШХ). Реакційну суміш перемішують протягом 2 годин при 0°С та розчинник видаляють випарюванням. Залишок переносять в дихлорметан (25мл) та отриману суміш по краплям при перемішуванні додають до розчину проміжної сполуки (21) (0,0075мл) та триетиламіну (0,75г) в ди хлорметані (25мл). Після перемішування протягом ночі реакційну суміш промивають водою, сушать та розчинник випарюють. Залишок очищають за допомогою колоночної флеш-хроматографії (елюент: етилацетат/гексан 1/3). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 1,5г проміжної сполуки (22). d) Одержання проміжної сполуки (23) Суміш NaOH (0,008моль) у воді (20мл) додають до суміші проміжної сполуки (22) (0,003моль) в етанолі (20мл) та потім реакційну суміш перемішують протягом 2 годин при 50°С. Після охолодження отриману суміш підкисляють за допомогою концентрованої НСI, фільтрують та промивають водою. Осад на фільтрі поміщають в діетиловий 31 83510 ефір, сушать та розчинник випарюють, одержуючи 1г проміжної сполуки (23). Приклад А.8 Одержання проміжної сполуки (24) Воду (28мл) та гідроксид літію (0,7г) додають до розчину сполуки (46) (0,013моль) в ТГФ (84мл) та реакційну суміш перемішують при кімнатній температурі до завершення реакції. Отриману суміш фільтрують та потім майже сухий осад на фільтрі переносять в невелику кількість води. Отриману суміш промивають дихлорметаном та водний шар обережно підкисляють до рН7. Одержаний осад відфільтровують та сушать в ексикаторі, одержуючи 6,9г проміжної сполуки (24) (т.пл. 170-172°С). Приклад А.9 а) Одержання проміжної сполуки (25) Суміш проміжної сполуки (14) (0,008моль), водного розчину формальдегіду (37%, 0,01моль) та паладію на вугіллі (5%, 0,1г) в етилацетаті (100мл) перемішують в атмосфері водню протягом 2 годин та потім додають ще одну порцію водного розчину формальдегіду (37%, 0,01моль). Реакційну суміш перемішують протягом 24 годин та потім нагрівають протягом ночі при 40°С. Фільтрат випарюють та отриманий залишок очищають за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/гексан 1/1). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 1,7г проміжної сполуки (25). b) Одержання проміжної сполуки (26) Реакцію проводять при 0°С в атмосфері азоту: 0,18г 6-метил-4'-(трифторметил)-[1,1’-біфеніл]-2карбонової кислоти перемішують в ди хлорметані (50мл) з етандіоїлдихлоридом (0,008моль) та потім отриману суміш ініціюють диметилформамідом (1 крапля). Залишкову частину 6-метил-4'(трифторметил)-[1,1’-біфеніл]-2-карбонової кислоти (1,62г) додають невеликими порціями та отриману суміш перемішують протягом 2 годин. Дихлорметан випарюють при зниженому тиску, одержуючи залишок (І). Суміш проміжної сполуки (25) (0,0065моль) та триетиламіну в дихлорметаш (50мл) охолоджують в атмосфері азоту до 0°С та до суміші по краплям додають розчин залишку (І) в дихлорметані (20мл). Реакційну суміш перемішу 32 ють протягом 3 годин при кімнатній температурі та розбавляють водою. Органічний шар відокремлюють, промивають водою, сушать та розчинник випарюють. Отриманий залишок очищають за допомогою колоночної флеш-хроматографії (елюент: етилацетат/гексан 1/3). Фракції, що містять продукт, збирають та розчинник випарюють, одержуючи 1,2г проміжної сполуки (26). c) Одержання проміжної сполуки (27) Проміжну сполуку (26) (0,0022моль) додають до розчину гідроксиду натрію (0,0066моль) у воді (16мл) та етанолі (30мл) та потім реакційну суміш перемішують протягом 18 годин при 30°С. Розчинник випарюють при зниженому тиску та отриманий залишок підкисляють за допомогою 4н НСI. Розчинник випарюють, одержуючи 1,2г проміжної сполуки (27). Приклад А. 10 а) Одержання проміжної сполуки (28) Суміш проміжної сполуки (4) (0,0019моль) та карбонату калію (0,0053моль) в диметилформаміді (30мл) нагрівають при 45°С протягом 30 хвилин, потім додають фенілметиловий ефір бромоцтової кислоти (0,0029моль) та реакційну суміш нагрівають протягом 3 годин при 45°С. Отриману суміш виливають у воду (75мл) та дихлорметан (75мл) та перемішують, потім дихлорметановий шар відокремлюють та концентрують, одержуючи 0,9г проміжної сполуки (28). b) Одержання проміжної сполуки (29) Розчин проміжної сполуки (28) (0,0014моль) в етилацетаті (40мл) та етанолі (40мл) гідрують при атмосферному тиску та при кімнатній температурі протягом 16 годин з використанням, як каталізатору, паладію на вугіллі (10%, 0,100г). Після завершення поглинання водню (1 еквівалент) реакційну суміш фільтрують через целіт та фільтрат випарюють, одержуючи 0,600г проміжної сполуки (29). В. Одержання кінцевих сполук 33 83510 Приклад В.1 Проміжну сполуку (2) (0,0001моль) розчиняють в дихлорметані (2мл) та додають PS-DIEA (0,03г). Отриману суспензію струшують протягом ночі при кімнатній температурі та фільтрують. PS-DCC (0,08г) додають до фільтрату з попередньої стадії та 2-(етоксикарбоніл)піперидину (0,0001моль), розчиненому в диметилформаміді (2мл). Реакційну суміш перемішують протягом 20 годин при кімнатній температурі та фільтрують. Фільтрат випарюють та залишок очищають за допомогою ВЕРХ з оберненою фазою, одержуючи 0,001г сполуки (1). Приклад В.2 Моногідрохлорид N'-(етилкарбонімідоїл)-N,Nдиметил-1,3-пропандіаміну (0,0015моль) додають до суміші проміжної сполуки (8) (0,001моль), 1гідрокси-1H-бензотриазолу (0,0015моль), 4метилморфоліну (0,004моль) та гідрохлориду е тилового ефіру D-аланіну (0,001моль) в дихлорметані (50мл) та реакційну суміш перемішують протягом ночі в атмосфері азоту. Отриману суміш промивають 1н НСI (20мл), насиченим розчином NаНСО3 (20мл) та насиченим розчином солі, потім сушать та відфільтровують. Розчинник випарюють при зниженому тиску та отриманий залишок змішують з гексаном, одержуючи 0,470г сполуки (38) (т.пл. 213-215°С). Приклад В.З Проміжну сполуку (4) (0,002моль), диметилформамід (50мл) та N-етил-N-(1-метилетил)-2пропанамін (0,5мл) перемішують до повного розчинення, потім додають гексафторфосфат(і-) 3оксиду 1-[біс(диметиламіно)метилен]-1Нбензотриазолію (0,0033моль) та отриману суміш перемішують протягом 15 хвилин. До суміші додають гідрохлорид діетилового ефіру Lглутамінової кислоти (0,003моль) та реакційну суміш перемішують протягом ночі. Отриману суміш виливають у воду та екстрагують етилацетатом (
ДивитисяДодаткова інформація
Назва патенту англійськоюN-aryl piperidine substituted biphenylcarboxamides as inhibitors of apolipoprotein b
Автори англійськоюMeerpoel Lieven, Viellevoye Marcel, Linders Joannes Theodorus Maria
Назва патенту російськоюN-арилпиперидин замещенные бифенилкарбоксамиды как ингибиторы аполипопротеина b
Автори російськоюМеерпоель Ливен, Виллевойе Марсель, Линдерс Йоаннес Теодорус Мария
МПК / Мітки
МПК: C07D 401/12, A61K 31/445, C07D 211/34, C07D 211/60, C07D 405/12, A61P 3/06
Мітки: біфенілкарбоксаміди, аполіпопротеїну, інгібітори, n-арилпіперидин, заміщені
Код посилання
<a href="https://ua.patents.su/26-83510-n-arilpiperidin-zamishheni-bifenilkarboksamidi-yak-ingibitori-apolipoprotenu-b.html" target="_blank" rel="follow" title="База патентів України">N-арилпіперидин заміщені біфенілкарбоксаміди як інгібітори аполіпопротеїну b</a>
Попередній патент: Імідазопіразини як інгібітори тирозинкіназ
Наступний патент: Пристрій для дослідження матеріалів на абразивне спрацювання
Випадковий патент: Сигналізатор рівня електропровідної рідини і інтенсивності світла












