Похідні глікопептидфосфонатів
Формула / Реферат
1. Глікопептид формули І
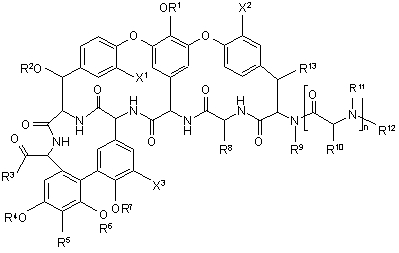 , І
, І
в якій:
R1 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил, гетероцикл і -Ra-Y-Rb(Z)x; або R1 означає сахаридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)x;
R2 означає водень або сахаридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, Rf-, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)x;
R3 означає -ORc, -NRcRc, -O-Ra-Y-Rb-(Z)x, -NRc-Rа-Y-Rb-(Z)x, -NRcRe або -O-Re; або R3 означає азотозв'язаний, киснезв'язаний або сіркозв'язаний замісник, який включає одну або декілька фосфонових груп;
R4 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, -Ra-Y-Rb-(Z)x, -C(O)Rd і сахаридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -С(O)Rf або -C(O)-Ra-Y-Rb-(Z)x, або R4 і R5 можуть з'єднуватися разом із атомами, до яких вони приєднані, з утворенням гетероциклічного кільця, необов'язково заміщеного -NRc-Ra-Y-Rb-(Z)x;
R5 вибраний із групи, яка включає водень, галоген, -CH(Rc)-NRcRc, -CH(Rc)-NRcRe, -CH(Rc)-NRc-Ra-Y-Rb-(Z)x, -CH(Rc)-Rx, -CH(Rc)-NRc-Ra-C(=O)-Rx і замісник, який включає одну або декілька фосфонових груп;
R6 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, -Ra-Y-Rb-(Z)x, -C(O)Rd і сахаридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -С(O)Rf або -C(O)-Ra-Y-Rb-(Z)x, або R5 і R6 можуть з'єднуватися разом із атомами, до яких вони приєднані, з утворенням гетероциклічного кільця, необов'язково заміщеного -NRc-Ra-Y-Rb-(Z)x;
R7 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, -Ra-Y-Rb-(Z)x і -C(O)Rd;
R8 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил і гетероцикл;
R9 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил і гетероцикл;
R10 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил і гетероцикл; або R8 і R10 з'єднані з утворенням –Аr1-О-Аr2-, де Аr1 і Аr2 незалежно являють собою арилен або гетероарилен;
R11 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил і гетероцикл, або R10 і R11 з'єднані разом із атомами вуглецю і азоту, до яких вони приєднані, з утворенням гетероциклічного кільця;
R12 вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил, гетероцикл, -С(O)Rd, -C(NH)-Rd, -C(O)NRcRc, -C(O)ORd, -C(NH)NRcRc, -Ra-Y-Rb-(Z)x і -C(O)-Ra-Y-Rb-(Z)x, або R11 і R12 з'єднані разом із атомом азоту, до якого вони приєднані, з утворенням гетероциклічного кільця;
R13 вибраний із групи, яка включає водень або -OR14;
R14 вибраний із водню, -C(O)Rd і сахаридної групи;
кожен Ra незалежно вибраний із групи, яка включає алкілен, заміщений алкілен, алкенілен, заміщений алкенілен, алкінілен і заміщений алкінілен;
кожен Rb незалежно вибраний із групи, яка включає ковалентний зв'язок, алкілен, заміщений алкілен, алкенілен, заміщений алкенілен, алкінілен і заміщений алкінілен, за умови, що Rb не являє собою ковалентний зв'язок, коли Z означає водень;
кожен Rс незалежно вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил, гетероцикл і -С(O)Rd;
кожен Rd незалежно вибраний із групи, яка включає алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил і гетероцикл;
Re означає сахаридну групу;
кожен Rf незалежно означає алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил або гетероцикл;
Rx означає N-зв'язаний аміносахарид або N-зв'язаний гетероцикл;
X1, X2 і X3 незалежно вибрані із водню або хлору;
кожен Y незалежно вибраний із групи, яка включає кисень, сірку, -S-S-, -NRc-, -S(O)-, -SO2-, -NRcC(O)-, -OSO2-, -OC(O)-, -NRcSO2-, -C(O)NRc-, -C(O)O-, -SO2NRc-, -SO2O-, -P(O)(ORc)O-, -P(O)(ORc)NRc-, -OP(O)(ORc)O-, -OP(O)(ORc)NRc-, -OC(O)O-, -NRcC(O)O-, -NRcC(O)NRc-, -OC(O)NRс-, -C(=O)- і -NRcSO2NRc-;
кожен Z незалежно вибраний із водню, арилу, циклоалкілу, циклоалкенілу, гетероарилу і гетероциклу;
n означає 0, 1 або 2; і
х означає 1 або 2;
або його фармацевтично прийнятна сіль або стереоізомер;
за умови, що принаймні один із R3 і R5 являє собою замісник, який включає одну або декілька фосфонових груп.
2. Глікопептид за пунктом 1, де R1 означає сахаридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)х.
3. Глікопептид за пунктом 1, де R1 являє собою сахаридну групу формули:
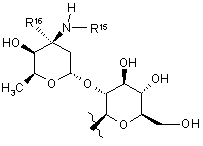 ,
,
в якій R15 являє собою -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або C(O)-Ra-Y-Rb-(Z)x; і R16 означає водень або метил.
4. Глікопептид за пунктом 3, де R2, R4, R6 і R7 кожен означає водень.
5. Глікопептид за пунктом 4, де R3 означає -ОН.
6. Глікопептид за пунктом 4, де R3 являє собою азотозв'язаний, киснезв'язаний або сіркозв'язаний замісник, який включає одну або декілька фосфонових груп.
7. Глікопептид за пунктом 6, де R3 являє собою групу формули - О-Ra-P(О)(ОH)2, -S-Ra-P(O)(ОH)2 або -NRc-Ra-P(O)(OH)2.
8. Глікопептид за пунктом 4, де R5 являє собою групу формули -CH-(R21)-N(Rc)-Ra-P(O)(OH)2; де R21 означає водень або Rd.
9. Глікопептид за пунктом 8, де R5 являє собою –CH2-NH-Ra-Р(O)(ОН)2.
10. Глікопептид за пунктом 1, який являє собою сполуку формули II:
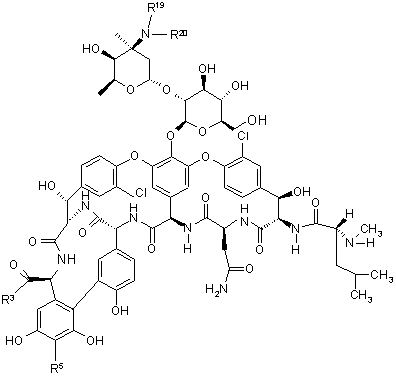 , (II)
, (II)
в якій:
R19 означає водень;
R20 являє собою -Ra-Y-Rb-(Z)x, Rf, -С(O)Rf або -C(O)-Ra-Y-Rb-(Z)x; і
Ra, Y, Rb, Z, x, Rf R3 і R5 мають значення, наведені в пункті 1;
або його фармацевтично прийнятна сіль, або стереоізомер;
за умови, що принаймні один із R3 і R5 являє собою замісник, який включає одну або декілька фосфонових груп.
11. Глікопептид за пунктом 10, де R3 являє собою -ОН.
12. Глікопептид за пунктом 10, де R3 являє собою азотозв'язаний, киснезв'язаний або сіркозв'язаний замісник, який включає одну або декілька фосфонових груп.
13. Глікопептид за пунктом 10, де R3 являє собою групу формули -O-Ra-P(O)(OH)2, -S-Ra-P(О)(ОH)2 або -NRc-Ra-P(O)(OH)2.
14. Глікопептид за пунктом 10, де R5 являє собою групу формули -(CH(R21)-N(Rc)-Ra-P(O)(OH)2; де R21 означає водень або Rd.
15. Глікопептид за будь-яким з пунктів 10-14, де R20 являє собою
-СН2СН2-NH-(СН2)9СН3; -СН2СН2СН2-NH-(СН2)8CH3; -СН2СН2СН2СН2-NH-(СН2)7CH3; -CH2CH2-NHSO2-(CH2)9CH3; -СН2СН2-NHSO2-(СН2)11CH3; -СН2СН2-S-(СН2)8CH3; -СН2СН2-S-(СН2)9CH3; -СН2СН2-S-(СН2)10CH3; -СН2СН2СН2-S-(СН2)8CH3; -СН2СН2СН2-S-(СН2)9CH3; -СН2СН2СН2-S-(СН2)3-СН=СН-(СН2)4CH3 (транс); -CH2CH2CH2CH2-S(CH2)7CH3; -CH2CH2-S(O)-(СН2)9CH3; -CH2CH2-S-(CH2)6Ph; -CH2CH2-S-(CH2)8Ph; -СН2СН2СН2-S-(CH2)8Ph; -CH2CH2-NH-CH2-4-(4-Cl-Ph)-Ph; -CH2CH2-NH-CH2-4-[4-(CH3)2СНСН2-]-Рh; -CH2CH2-NH-CH2-4-(4-CF3-Ph)-Ph; -СН2СН2-S-СН2-4-(4-Сl-Ph)-Ph; -CH2CH2-S(O)-CH2-4-(4-Cl-Ph)-Ph; -CH2CH2CH2-S-CH2-4-(4-Cl-Ph)-Ph;
-CH2CH2CH2-S(O)-CH2-4-(4-Cl-Ph)-Ph; -СН2СН2СН2-S-СН2-4-[3,4-ди-Сl-PhCH2O-)-Ph; -CH2CH2-NHSO2-CH2-4-[4-(4-Ph)-Ph]-Ph; -CH2CH2CH2-NHSO2-CH2-4-(4-Cl-Ph)-Ph; -CH2CH2CH2-NHSO2-CH2-4-(Ph-C![]() C-)-Ph; -CH2CH2CH2-NHSO2-4-(4-Cl-Ph)-Ph; або -СН2СН2СН2-NHSO2-4-(нафт-2-ил)-Ph.
C-)-Ph; -CH2CH2CH2-NHSO2-4-(4-Cl-Ph)-Ph; або -СН2СН2СН2-NHSO2-4-(нафт-2-ил)-Ph.
16. Глікопептид за пунктом 10, де R3 являє собою -ОН; R5 являє собою N-(фосфонометил)-амінометил; R19 являє собою водень, і R20 являє собою -СН2СН2-NH-(СН2)9CH3; або його фармацевтично прийнятна сіль.
17. Глікопептид за пунктом 10, де R3 означає -ОН; R5 означає N-(фосфонометил)-амінометил; R19 означає водень, і R20 означає -СН2СН2-NH-(СН2)9CH3.
18. Глікопептид за пунктом 16, який являє собою гідрохлоридну сіль.
19. Глікопептид за будь-яким з пунктів 1-18 для застосування в медицині.
20. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та терапевтично ефективну кількість глікопептиду, що зазначений у будь-якому з пунктів 1-18.
21. Фармацевтична композиція за пунктом 20, яка містить як носій циклодекстрин.
22. Фармацевтична композиція за пунктом 21, в якій циклодекстрин являє собою гідроксипропіл-![]() -циклодекстрин.
-циклодекстрин.
23. Фармацевтична композиція за пунктом 22, яка містить від приблизно 250 мг до 1000 мг глікопептиду і від 250 мг до 10 г гідроксипропіл-![]() -циклодекстрину.
-циклодекстрину.
24. Фармацевтична композиція за пунктом 23, в якій масове співвідношення гідроксипропіл-![]() -циклодекстрину до глікопептиду становить від 1:1 до 10:1 включно.
-циклодекстрину до глікопептиду становить від 1:1 до 10:1 включно.
25. Застосування глікопептиду, що зазначений у будь-якому з пунктів 1-18 для приготування лікарського засобу для лікування бактеріальних захворювань.
26. Фармацевтична композиція, яка як активний компонент містить глікопептид, що зазначений у будь-якому з пунктів 1-18, для лікування бактеріальних захворювань.
27. Спосіб одержання глікопептиду, що зазначений у пункті 1, який заміщений на С-кінці, згідно з яким у вихідний поліпептид, що на С-кінці має незаміщену карбоксильну групу, вводять замісник R3.
28. Спосіб одержання глікопептиду, що зазначений у пункті 1, який заміщений на R-кінці, згідно з яким у вихідний глікопептид, що за R-кінцем є незаміщеним, вводять замісник R5.
29. Спосіб лікування ссавця, який має бактеріальне захворювання, згідно якому ссавцю вводять терапевтично ефективну кількість глікопептиду, що зазначений у будь-якому з пунктів 1, 10 або 16.
30. Спосіб лікування ссавця, який має бактеріальне захворювання, згідно з яким ссавцю вводять терапевтично ефективну кількість фармацевтичної композиції, що зазначена у пункті 20.
Текст
1. Глікопептид формули І C2 2 (19) 1 3 75083 4 з утворенням –Аr1-О-Аr2-, де Аr1 і Аr2 незалежно за умови, що принаймні один із R3 і R5 являє соявляють собою арилен або гетероарилен; бою замісник, який включає одну або декілька фоR11 вибраний із групи, яка включає водень, алкіл, сфонових груп. заміщений алкіл, алкеніл, заміщений алкеніл, алкі2. Глікопептид за пунктом 1, де R1 означає саханіл, заміщений алкініл, циклоалкіл, заміщений цикридну групу, необов'язково заміщену -Ra-Y-Rb-(Z)x, f f a b лоалкіл, циклоалкеніл, заміщений циклоалкеніл, R , -C(O)R або -C(O)-R -Y-R -(Z)х. 10 11 арил, гетероарил і гетероцикл, або R і R з'єд3. Глікопептид за пунктом 1, де R1 являє собою нані разом із атомами вуглецю і азоту, до яких сахаридну групу формули: вони приєднані, з утворенням гетероциклічного H кільця; R16 N R15 R12 вибраний із групи, яка включає водень, алкіл, HO заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений цикOH лоалкіл, циклоалкеніл, заміщений циклоалкеніл, OH O O d d H3C арил, гетероарил, гетероцикл, -С(O)R , -C(NH)-R , c c d c c a b -C(O)NR R , -C(O)OR , -C(NH)NR R , -R -Y-R -(Z)x і -C(O)-Ra-Y-Rb-(Z)x, або R11 і R12 з'єднані разом із OH O атомом азоту, до якого вони приєднані, з утворен, ням гетероциклічного кільця; 13 в якій R15 являє собою -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf R вибраний із групи, яка включає водень або або C(O)-Ra-Y-Rb-(Z)x; і R16 означає водень або OR14; метил. R14 вибраний із водню, -C(O)Rd і сахаридної групи; 4. Глікопептид за пунктом 3, де R2, R4, R6 і R7 кокожен Ra незалежно вибраний із групи, яка вклюжен означає водень. чає алкілен, заміщений алкілен, алкенілен, замі5. Глікопептид за пунктом 4, де R3 означає -ОН. щений алкенілен, алкінілен і заміщений алкінілен; b 6. Глікопептид за пунктом 4, де R3 являє собою кожен R незалежно вибраний із групи, яка вклюазотозв'язаний, киснезв'язаний або сіркозв'язаний чає ковалентний зв'язок, алкілен, заміщений алкізамісник, який включає одну або декілька фосфолен, алкенілен, заміщений алкенілен, алкінілен і нових груп. заміщений алкінілен, за умови, що Rb не являє 7. Глікопептид за пунктом 6, де R3 являє собою собою ковалентний зв'язок, коли Z означає вогрупу формули - О-Ra-P(О)(ОH)2, -S-Ra-P(O)(ОH)2 день; с або -NRc-Ra-P(O)(OH)2. кожен R незалежно вибраний із групи, яка вклю8. Глікопептид за пунктом 4, де R5 являє собою чає водень, алкіл, заміщений алкіл, алкеніл, замігрупу формули -CH-(R21)-N(Rc)-Ra-P(O)(OH)2; де щений алкеніл, алкініл, заміщений алкініл, циклоаR21 означає водень або Rd. лкіл, заміщений циклоалкіл, циклоалкеніл, 9. Глікопептид за пунктом 8, де R5 являє собою – заміщений циклоалкеніл, арил, гетероарил, гетеd CH2-NH-Ra-Р(O)(ОН)2. роцикл і -С(O)R ; d 10. Глікопептид за пунктом 1, який являє собою кожен R незалежно вибраний із групи, яка вклюсполуку формули II: чає алкіл, заміщений алкіл, алкеніл, заміщений R19 алкеніл, алкініл, заміщений алкініл, циклоалкіл, N заміщений циклоалкіл, циклоалкеніл, заміщений R20 HO циклоалкеніл, арил, гетероарил і гетероцикл; OH Re означає сахаридну групу; OH O O кожен Rf незалежно означає алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений OH алкініл, циклоалкіл, заміщений циклоалкіл, циклоO O Cl алкеніл, заміщений циклоалкеніл, арил, гетероаO O рил або гетероцикл; x HO R означає N-зв'язаний аміносахарид або NOH Cl H O O N зв'язаний гетероцикл; H H H N N X1, X2 і X3 незалежно вибрані із водню або хлору; N CH3 N O O N H кожен Y незалежно вибраний із групи, яка включає H O O H NH кисень, сірку, -S-S-, -NRc-, -S(O)-, -SO2-, -NRcC(O)-, O O c c CH3 -OSO2-, -OC(O)-, -NR SO2-, -C(O)NR -, -C(O)O-, H2N c c c c CH3 3 R SO2NR -, -SO2O-, -P(O)(OR )O-, -P(O)(OR )NR -, OH OP(O)(ORc)O-, -OP(O)(ORc)NRc-, -OC(O)O-, c c c с NR C(O)O-, -NR C(O)NR -, -OC(O)NR -, -C(=O)- і OH HO NRcSO2NRc-; R5 кожен Z незалежно вибраний із водню, арилу, цик, (II) лоалкілу, циклоалкенілу, гетероарилу і гетероцикв якій: лу; R19 означає водень; n означає 0, 1 або 2; і R20 являє собою -Ra-Y-Rb-(Z)x, Rf, -С(O)Rf або х означає 1 або 2; C(O)-Ra-Y-Rb-(Z)x; і або його фармацевтично прийнятна сіль або стеRa, Y, Rb, Z, x, Rf R3 і R5 мають значення, наведені реоізомер; в пункті 1; 5 75083 6 або його фармацевтично прийнятна сіль, або стеозначає водень, і R20 означає -СН2СН2-NHреоізомер; (СН2)9CH3. за умови, що принаймні один із R3 і R5 являє со18. Глікопептид за пунктом 16, який являє собою бою замісник, який включає одну або декілька фогідрохлоридну сіль. сфонових груп. 19. Глікопептид за будь-яким з пунктів 1-18 для 3 11. Глікопептид за пунктом 10, де R являє собою застосування в медицині. ОН. 20. Фармацевтична композиція, яка містить фар12. Глікопептид за пунктом 10, де R3 являє собою мацевтично прийнятний носій та терапевтично азотозв'язаний, киснезв'язаний або сіркозв'язаний ефективну кількість глікопептиду, що зазначений у замісник, який включає одну або декілька фосфобудь-якому з пунктів 1-18. нових груп. 21. Фармацевтична композиція за пунктом 20, яка 13. Глікопептид за пунктом 10, де R3 являє собою містить як носій циклодекстрин. групу формули -O-Ra-P(O)(OH)2, -S-Ra-P(О)(ОH)2 22. Фармацевтична композиція за пунктом 21, в або -NRc-Ra-P(O)(OH)2. якій циклодекстрин являє собою гідроксипропіл- 14. Глікопептид за пунктом 10, де R5 являє собою циклодекстрин. групу формули -(CH(R21)-N(Rc)-Ra-P(O)(OH)2; де 23. Фармацевтична композиція за пунктом 22, яка R21 означає водень або Rd. містить від приблизно 250 мг до 1000 мг глікопеп15. Глікопептид за будь-яким з пунктів 10-14, де тиду і від 250 мг до 10 г гідроксипропіл- 20 R являє собою циклодекстрину. -СН2СН2-NH-(СН2)9СН3; -СН2СН2СН2-NH24. Фармацевтична композиція за пунктом 23, в (СН2)8CH3; -СН2СН2СН2СН2-NH-(СН2)7CH3; якій масове співвідношення гідроксипропіл- CH2CH2-NHSO2-(CH2)9CH3; -СН2СН2-NHSO2циклодекстрину до глікопептиду становить від 1:1 (СН2)11CH3; -СН2СН2-S-(СН2)8CH3; -СН2СН2-Sдо 10:1 включно. (СН2)9CH3; -СН2СН2-S-(СН2)10CH3; -СН2СН2СН2-S25. Застосування глікопептиду, що зазначений у (СН2)8CH3; -СН2СН2СН2-S-(СН2)9CH3; -СН2СН2СН2будь-якому з пунктів 1-18 для приготування лікарS-(СН2)3-СН=СН-(СН2)4CH3 (транс); ського засобу для лікування бактеріальних захвоCH2CH2CH2CH2-S(CH2)7CH3; -CH2CH2-S(O)рювань. (СН2)9CH3; -CH2CH2-S-(CH2)6Ph; -CH2CH2-S26. Фармацевтична композиція, яка як активний (CH2)8Ph; -СН2СН2СН2-S-(CH2)8Ph; -CH2CH2-NHкомпонент містить глікопептид, що зазначений у CH2-4-(4-Cl-Ph)-Ph; -CH2CH2-NH-CH2-4-[4будь-якому з пунктів 1-18, для лікування бактеріа(CH3)2СНСН2-]-Рh; -CH2CH2-NH-CH2-4-(4-CF3-Ph)льних захворювань. Ph; -СН2СН2-S-СН2-4-(4-Сl-Ph)-Ph; -CH2CH2-S(O)27. Спосіб одержання глікопептиду, що зазначений CH2-4-(4-Cl-Ph)-Ph; -CH2CH2CH2-S-CH2-4-(4-Cl-Ph)у пункті 1, який заміщений на С-кінці, згідно з яким Ph; у вихідний поліпептид, що на С-кінці має незамі-CH2CH2CH2-S(O)-CH2-4-(4-Cl-Ph)-Ph; -СН2СН2СН2щену карбоксильну групу, вводять замісник R3. S-СН2-4-[3,4-ди-Сl-PhCH2O-)-Ph; -CH2CH2-NHSO228. Спосіб одержання глікопептиду, що зазначений CH2-4-[4-(4-Ph)-Ph]-Ph; -CH2CH2CH2-NHSO2-CH2-4у пункті 1, який заміщений на R-кінці, згідно з яким (4-Cl-Ph)-Ph; -CH2CH2CH2-NHSO2-CH2-4-(Ph-C Cу вихідний глікопептид, що за R-кінцем є незамі)-Ph; -CH2CH2CH2-NHSO2-4-(4-Cl-Ph)-Ph; або щеним, вводять замісник R5. СН2СН2СН2-NHSO2-4-(нафт-2-ил)-Ph. 3 29. Спосіб лікування ссавця, який має бактеріаль16. Глікопептид за пунктом 10, де R являє собою 5 не захворювання, згідно якому ссавцю вводять ОН; R являє собою N-(фосфонометил)терапевтично ефективну кількість глікопептиду, амінометил; R19 являє собою водень, і R20 являє що зазначений у будь-якому з пунктів 1, 10 або 16. собою -СН2СН2-NH-(СН2)9CH3; або його фармаце30. Спосіб лікування ссавця, який має бактеріальвтично прийнятна сіль. не захворювання, згідно з яким ссавцю вводять 17. Глікопептид за пунктом 10, де R3 означає -ОН; терапевтично ефективну кількість фармацевтичної R5 означає N-(фосфонометил)-амінометил; R19 композиції, що зазначена у пункті 20. Винахід стосується нових фосфонатних похідних глікопептидних антибіотиків і відповідних сполук. Цей винахід також стосується фармацевтичних композицій, які містять такі похідні глікопептидфосфонатів, способів застосування таких похідних глікопептидфосфонатів як антибактеріальних агентів, та способів та проміжних хімічних сполук, придатних для одержання таких похідних глікопептидфосфонатів. Глікопептиди (наприклад, дальбагептиди) є добре відомим класом антибіотиків, що продукуються різноманітними мікроорганізмами [дивись Глікопептидні Антибіотики, за редакцією R. Nagarajan, Marcel Dekker, Inc. Нью Йорк (1994)]. Ці комплексні поліциклічні пептидні сполуки є дуже ефективними антибактеріальними засобами проти більшості грам-позитивних бактерій. Незважаючи на ефективну антибактеріальну дію, глікопептидні антибіотики не застосовуються при лікуванні бактеріальних захворювань так часто, як інші класи антибіотиків, такі як напівсинтетичні пеніциліни, цефалоспоріни та ринкоміцини, внаслідок наявності токсичності. Тим не менше, впродовж останніх років виявляється резистентність бактерій до багатьох звичайно застосовуваних антибіотиків [дивись J. Е. 7 75083 8 Geraci та ін., Мауо СІіn. Рrос. 1983, 58, 88-91; та М. даний винахід стосується глікопептидної сполуки, Foldes, J. Antimicrob. Chemother. 1983, 11, 21-26]. заміщеної на С-кінці замісником, який включає Відтоді, як глікопептидні антибіотики часто виявиодну або дві фосфонові (-РО3Н2) групи; або її фалися ефективними проти цих резистентних штамів рмацевтично прийнятної солі, стереоізомеру, або бактерій, глікопептиди, такі як ванкоміцин, стали проліків. Переважно, фосфоно-вмісний замісник застосовуватися як ліки останньої надії при лікуприєднаний до карбонільної групи на С-кінці за ванні інфекції, викликаних цими організмами. Недопомогою амідного зв'язку, складноефірного зв'ящодавно, однак, резистентність до ванкоміцину зку, або тіоскладноефірного зв'язку; більш перебула виявлена у різноманітних мікроорганізмів, важно, за допомогою амідного зв'язку. Переважно, таких як ванкоміцин-резистентні ентерококки фосфоно-вмісний замісник містить одну фосфоно(VRE), що викликає підвищене занепокоєння щодо ву групу. Особливо переважно фосфоно-вмісні здатності ефективно лікувати бактеріальні інфекції замісники на С-кінці включають фосфонометилав майбутньому [дивись Hospital Infection Control міно, 3-фосфонопропіламіно і 2-гідрокси-2Practices Advisory Committee, Infection Control фосфоноетиламіно. Hospital Epidemiology, 1995, 17, 364-369; A. P. В іншому переважному втіленні, даний винахід Johnson та ін., Clinical Microbiology Rev., 1990, 3, стосується глікопептидної сполуки, заміщеної на 280-291; G. M. Eliopoulos, European J. Clinical R-кінці (на резорциновому кільці) замісником, який Microbiol, Infection Disease, 1993, 12, 409-412; і P. включає одну або дві фосфонові (-РО3Н2) групи; Courvalin, Antimicrob. Agents Chemother, 1990, 34, або її фармацевтично прийнятної солі, стереоізо2291-2296]. меру, або проліків. Переважно, фосфоно-вмісний Ряд похідних ванкоміцину та інших глікопептизамісник приєднаний до R-кінця (тобто, резорцидів відомі в даній галузі. Наприклад, дивись патеннового кільця) за допомогою атома азоту аміномети US №4,639,433; 4,643,987; 4,497,802; 4,698,327; тильної групи, приєднаної до R-кінця. Переважно, 5,591,714; 5,840,684; та 5,843,889. Інші похідні фосфоно-вмісний замісник включає одну фосфоописані в ЕР 0802199; ЕР 0801075; ЕР 0667353; нову групу. Особливо переважно фосфоно-вмісні WO 97/28812; WO 97/38702; WO 98/52589; WO замісники на R-кінці включають N98/52592; та в J. Amer. Chem. Soc, 1996, 118, (фосфонометил)амінометил; N-(2-гідрокси-213107-13108; J. Amer. Chem. Soc, 1997, 119, фосфоноетил)амінометил; N-карбоксиметил-N12041-12047; і J. Amer. Chem. Soc, 1994, 116, (фосфонометил)амінометил; Ν,Ν4573-4590. біс(фосфонометил)амінометил; і N-(3Незважаючи на посилання, вказані вище, в фосфонопропіл)амінометил. даний час існує потреба в нових похідних глікопепВ ще іншому переважному втіленні, даний витиду, які мають ефективну антибактеріальну дію нахід стосується глікопептидної сполуки, заміщета поліпшені характеристики безпеки для ссавців. ної на С-кінці і на R-кінці замісником, що включає Зокрема, існує необхідність в похідних глікопептиодну або дві фосфонові (-РО3Н2) групи; або її фаду, які ефективні по відношенню до широкого спермацевтично прийнятної солі, стереоізомеру, або ктру патогенних мікроорганізмів, включаючи ванпроліків. Переважно, фосфоно-вмісні замісники коміцин-резистентні мікроорганізми, і які мають кожен включає одну фосфонову групу. знижені накопичення в тканинах та/або нефротокПереважна сполука за винаходом представсичність. ляє собою глікопептид формули І: Даний винахід стосується нових похідних глікопептидфосфонатів, які мають значно ефективнішу антибактеріальну дію та поліпшені характеристики безпеки для ссавців. Більш конкретно, похідні глікопептидфосфонатів за винаходом несподівано виявляють знижене накопичення в тканинах та/або нефротоксичність при введенні ссавцю. Отже, даний винахід стосується глікопептидних сполук, заміщених одним або декількома (наприклад, 1, 2 або 3) замісниками, що включають одну або декілька (наприклад, 1, 2 або 3) фосфонових (-РО3Н2) груп; або їх фармацевтично прийнятних солей, стереоізомерів, або їх проліків. Перев якій: важно, глікопептидна сполука заміщена одним або R1 вибраний із групи, яка включає водень, алдекількома замісниками, що включають одну або кіл, заміщений алкіл, алкеніл, заміщений алкеніл, декілька фосфонових груп. Більш переважно, гліалкініл, заміщений алкініл, циклоалкіл, заміщений копептидна сполука заміщена одним замісником, циклоалкіл, циклоалкеніл, заміщений циклоалкеякий включає одну або дві фосфонові групи, переніл, арил, гетероарил, гетероцикл і -Ra-Y-Rb-(Z)x; 1 важно одну фосфонову групу. Необов'язково, гліабо R означає сахаридну групу, необов'язково копептидна сполука за даним винаходом також заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або -C(O)-Ra-Yможе бути заміщена іншими замісниками, що не Rb-(Z)x; містять фосфонової групи, за умови, що принаймні R2 означає водень або сахаридну групу, неодин замісник включає одну або декілька фосфообов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або нових груп. -C(O)-Ra-Y-Rb-(Z)x; Відповідно, в одному переважному втіленні, R3 означає -ORc, -NRcRc, -O-Ra-Y-Rb-(Z)x, -NRC 9 75083 10 Ra-Y-Rb-(Z)x, -NRcRe або -O-Re; або R3 означає R14 вибраний із водню, -C(O)Rd і сахаридної азот-зв'язаний, кисень-зв'язаний або сіркогрупи; зв'язаний замісник, який включає одну або декількожен Ra незалежно вибраний із групи, яка ка фосфонових груп; включає алкілен, заміщений алкілен, алкенілен, R4 вибраний із групи, яка включає водень, алзаміщений алкенілен, алкінілен і заміщений алкінікіл, заміщений алкіл, алкеніл, заміщений алкеніл, лен; алкініл, заміщений алкініл, -Ra-Y-Rb-(Z)X, -C(O)Rd і кожен Rb незалежно вибраний із групи, яка a b сахаридну групу, необов'язково заміщену -R -Y-R включає ковалентний зв'язок, алкілен, заміщений (Z)x, Rf, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)x, або R4 і R5 алкілен, алкенілен, заміщений алкенілен, алкінілен можуть з'єднуватися, разом із атомами, до яких і заміщений алкінілен, за умови, що Rb не означає вони приєднані, з утворенням гетероциклічного ковалентний зв'язок, коли Ζ означає водень; кільця, необов'язково заміщеного -NRC-Ra-Y-Rbкожен Rc незалежно вибраний із групи, яка (Z)x; включає водень, алкіл, заміщений алкіл, алкеніл, R5 вибраний із групи, яка включає водень, газаміщений алкеніл, алкініл, заміщений алкініл, логен, -CH(Rc)-NRcRc, -CH(Rc)-NRcRe, -CH(Rc)-NRcциклоалкіл, заміщений циклоалкіл, циклоалкеніл, Ra-Y-Rb-(Z)x,-CH(Rc)-Rx, -CH(Rc)-NRc-Ra-C(=O)-Rx, і заміщений циклоалкеніл, арил, гетероарил, гетезамісник, який включає одну або декілька фосфороцикл і -C(O)Rd; нових груп; кожен Rd незалежно вибраний із групи, яка 6 R вибраний із групи, яка включає водень, алвключає алкіл, заміщений алкіл, алкеніл, заміщекіл, заміщений алкіл, алкеніл, заміщений алкеніл, ний алкеніл, алкініл, заміщений алкініл, циклоалалкініл, заміщений алкініл, -Ra-Y-Rb-(Z)x, -C(O)Rd і кіл, заміщений циклоалкіл, циклоалкеніл, заміщесахаридну групу, необов'язково заміщену -Ra-Y-Rbний циклоалкеніл, арил, гетероарил і гетероцикл; (Z)x, Rf, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)x, або R5 і R6 Re означає сахаридну групу; можуть з'єднуватися, разом із атомами, до яких кожен Rf незалежно означає алкіл, заміщений вони приєднані, з утворенням гетероциклічного алкіл, алкеніл, заміщений алкеніл, алкініл, заміщекільця, необов'язково заміщеного –NRc-Ra-Y-Rbний алкініл, циклоалкіл, заміщений циклоалкіл, (Z)x; циклоалкеніл, заміщений циклоалкеніл, арил, геR7 вибраний із групи, яка включає водень, алтероарил або гетероцикл; кіл, заміщений алкіл, алкеніл, заміщений алкеніл, Позначає N-зв'язаний аміносахарид або Nалкініл, заміщений алкініл,- Ra-Y-Rb-(Z)x і -C(O)Rd; зв'язаний гетероцикл; R8 вибраний із групи, яка включає водень, алX1, X2 і X3 незалежно вибрані із водню або кіл, заміщений алкіл, алкеніл, заміщений алкеніл, хлору; алкініл, заміщений алкініл, циклоалкіл, заміщений кожен Υ незалежно вибраний із групи, яка циклоалкіл, циклоалкеніл, заміщений циклоалкевключає кисень, сірку, -S-S-, -NRc-, -S(O)-, -SO2-, ніл, арил, гетероарил і гетероцикл; NRcC(O)-, -OSO2-, -ОС(О)-, -NRcSO2-, -C(O)NRc-, 9 R вибраний із групи, яка включає водень, алC(O)O-, -SO2NRc-, -SO2O-, -P(O)(ORc)O-, кіл, заміщений алкіл, алкеніл, заміщений алкеніл, P(O)(ORc)NRc-, -OP(O)(ORc)O-, -OP(O)(ORc)NRc-, алкініл, заміщений алкініл, циклоалкіл, заміщений OC(O)O, -NRcC(O)O, -NRcC(O)NRc-, -OC(O)NRc-, циклоалкіл, циклоалкеніл, заміщений циклоалкеC(=O)- і –NRcSO2NRc-; ніл, арил, гетероарил і гетероцикл; кожен Ζ незалежно вибраний із водню, арилу, R10 вибраний із групи, яка включає водень, алциклоалкілу, циклоалкенілу, гетероарилу і гетерокіл, заміщений алкіл, алкеніл, заміщений алкеніл, циклу; алкініл, заміщений алкініл, циклоалкіл, заміщений n означає 0, 1 або 2; і циклоалкіл, циклоалкеніл, заміщений циклоалкеχ означає 1 або 2; ніл, арил, гетероарил і гетероцикл; або R8 і R10 або його фармацевтично прийнятну сіль, стез'єднані з утворенням -Аr1-О-Аr2-, де Аr1 і Аr2 незареоізомер, або проліки; лежно означають арилен або гетероарилен; за умови, що принаймні один із R3 і R5 означає 11 R вибраний із групи, яка включає водень, алзамісник, який включає одну або декілька фосфокіл, заміщений алкіл, алкеніл, заміщений алкеніл, нових груп. алкініл, заміщений алкініл, циклоалкіл, заміщений Переважна сполука за винаходом представциклоалкіл, циклоалкеніл, заміщений циклоалкеляє собою сполуку формули І, в якій: R1 вибраний ніл, арил, гетероарил і гетероцикл, або R10 і R11 із групи, яка включає водень, алкіл, заміщений з'єднані, разом із атомами вуглецю і азоту, до яких алкіл, алкеніл, заміщений алкеніл, алкініл, заміщевони приєднані, з утворенням гетероциклічного ний алкініл, циклоалкіл, заміщений циклоалкіл, кільця; циклоалкеніл, заміщений циклоалкеніл, арил, геR12 вибраний із групи, яка включає водень, алтероарил, гетероцикл і -Ra-Y-Rb-(Z)x; або R1 ознакіл, заміщений алкіл, алкеніл, заміщений алкеніл, чає сахаридну групу, необов'язково заміщену -Raалкініл, заміщений алкініл, циклоалкіл, заміщений Y-Rb-(Z)X, Rf, -C(O)Rf або -C(O)-Ra-Y-Rb-(Z)x; R2 циклоалкіл, циклоалкеніл, заміщений циклоалкеозначає водень або сахаридну групу, необов'язкоd a b f f a ніл, арил, гетероарил, гетероцикл, -C(O)R , во заміщену -R -Y-R -(Z)x, R , -C(O)R або -C(O)-R d c c d c c a b 3 c c c a b C(NH)R , -C(O)NR R , -C(O)OR , -C(NH)NR R , -R Y-R -(Z)x; R означає -OR , -NR R , -O-R -Y-R -(Z)x, Y-Rb-(Z)x і -C(O)-Ra-Y-Rb-(Z)x, або R11 і R12 з'єднані, -NRc-Ra- Y-Rb-(Z)x, -NRcRe або -O-Re; або R3 предразом із атомом азоту, до якого вони приєднані, з ставляє собою азот-зв'язаний, кисень-зв'язаний утворенням гетероциклічного кільця; або сірко-зв'язаний замісник, якийвключає одну R13 вибраний із групи, яка включає водень або або декілька фосфонових груп; R4 вибраний із 14 -OR ; групи, яка включає водень, алкіл, заміщений алкіл, 11 75083 12 алкеніл, заміщений алкеніл, алкініл, заміщений заміщений алкіл, алкеніл, заміщений алкеніл, алкіалкініл, -Ra-Y-Rb-(Z)x, -C(O)Rd і сахаридну групу, ніл, заміщений алкініл, циклоалкіл, заміщений цикнеобов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf лоалкіл, циклоалкеніл, заміщений циклоалкеніл, або -C(O)-Ra-Y-Rb-(Z)x; R5 вибраний із групи, яка арил, гетероарил і гетероцикл; Re означає сахариc c c c включає водень, галоген, -CH(R )-NR R , -CH(R )дну групу; кожен Rf незалежно означає алкіл, заc e c c a b c x NR R , -CH(R )-NR -R -Y-R -(Z)x, -CH(R )-R , міщений алкіл, алкеніл, заміщений алкеніл, алкіCH(Rc)-NRc-Ra-C(=O)-Rx, і замісник, який включає ніл, заміщений алкініл, циклоалкіл, заміщений одну або декілька фосфонових груп; R6 вибраний циклоалкіл, циклоалкеніл, заміщений циклоалкеіз групи, яка включає водень, алкіл, заміщений ніл, арил, гетероарил або гетероцикл; Rx предстаалкіл, алкеніл, заміщений алкеніл, алкініл, заміщевляє собою N-зв'язаний аміносахарид або Nний алкініл, -Ra-Y-Rb-(Z)x, -C(O)Rd і сахаридну грузв'язаний гетероцикл; X1, X2 і X3 незалежно вибраc a b пу, необов'язково заміщену –NR -R -Y-R -(Z)x, або ні із водню або хлору; кожен Υ незалежно вибраR5 і R6 можуть з'єднуватися, разом із атомами, до ний із групи, яка включає кисень, сірку, -S-S-, -NRCяких вони приєднані, з утворенням гетероциклічно, -S(O)-, -SO2-, -NRcC(O)-, -OSO2-, -OC(O)-, c a b го кільця, необов'язково заміщеного -NR -R -Y-R NRcSO2-, -C(O)NRc-, -C(O)O-, -SO2NRc-, -SO2O-, 7 (Z)x; R вибраний із групи, яка включає водень, P(O)(ORc)O-, -P(O)(ORc)NRc-, -OP(O)(ORc)O-, алкіл, заміщений алкіл, алкеніл, заміщений алкеOP(O)(ORc)NRc-, -OC(O)O-, -NRcC(O)O-, ніл, алкініл, заміщений алкініл, -Ra-Y-Rb-(Z)x і NRcC(O)NRc-, -OC(O)NRc-, -C(=O)- і -NRcSO2NRc-; C(O)Rd; R8 вибраний із групи, яка включає водень, кожен Ζ незалежно вибраний із водню, арилу, цикалкіл, заміщений алкіл, алкеніл, заміщений алкелоалкілу, циклоалкенілу, гетероарилу і гетероцикніл, алкініл, заміщений алкініл, циклоалкіл, замілу; n означає 0, 1 або 2; і x означає 1 або 2; або її щений циклоалкіл, циклоалкеніл, заміщений цикфармацевтично прийнятну сіль, стереоізомер, або лоалкеніл, арил, гетероарил і гетероцикл; R9 проліки; за умови, що принаймні один із R3 і R5 вибраний із групи, яка включає водень, алкіл, заозначає замісник, який включає одну або декілька міщений алкіл, алкеніл, заміщений алкеніл, алкіфосфонових груп. ніл, заміщений алкініл, циклоалкіл, заміщений цикПереважно, R1 означає сахаридну групу, нелоалкіл, циклоалкеніл, заміщений циклоалкеніл, обов'язково заміщену -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або арил, гетероарил і гетероцикл; R10 вибраний із -C(O)-Ra-Y-Rb-(Z). Більш переважно R1 означає групи, яка включає водень, алкіл, заміщений алкіл, сахаридну групу, заміщену на атомі азоті сахариду алкеніл, заміщений алкеніл, алкініл, заміщений -CH2CH2-NH-(CH2)9CH3; -ΟΗ2ΟΗ2ΟΗ2-ΝΗалкініл, циклоалкіл, заміщений циклоалкіл, цикло(ΟΗ2)8ΟΗ3; -CH2CH2CH2CH2-NH-(CH2)7CH3; алкеніл, заміщений циклоалкеніл, арил, гетероаCH2CH2-NHSO2-(CH2)9CH3; -CH2CH2-NHSO28 10 рил і гетероцикл; або R і R з'єднані з утворен(CH2)11CH3; -CH2CH2-S-(CH2)8CH3; -CH2CH2-S1 2 1 2 ням -Аr -О-Аr -, де Аr і Аr незалежно означають (CH2)9CH3;-CH2CH2-S-(CH2)10CH3;-CH2CH2CH2-Sарилен або гетероарилен; R11 вибраний із групи, (CH2)8CH3; -CH2CH2CH2-S-(CH2)9CH3; -CH2CH2CH2яка включає водень, алкіл, заміщений алкіл, алкеS-(CH2)3-CH=CH-(CH2)4CH3 (транс); ніл, заміщений алкеніл, алкініл, заміщений алкініл, CH2CH2CH2CH2-S-(CH2)7CH3; -CH2CH2-S(O)циклоалкіл, заміщений циклоалкіл, циклоалкеніл, (CH2)9CH3; -CH2CH2-S-(CH2)6Ph; -CH2CH2-Sзаміщений циклоалкеніл, арил, гетероарил і гете(CH2)8Ph; -CH2CH2CH2-S-(CH2)8Ph; -CH2CH2-NHроцикл, або R10 і R11 з'єднані, разом із атомами CH2-4-(4-CI-Ph)-Ph; -CH2CH2-NH-CH2-4-[4вуглецю і азоту, до яких вони приєднані, з утво(CH3)2CHCH2-]-Ph; -CH2CH2-NH-CH2-4-(4-CF3-Ph)ренням гетероциклічного кільця; R12 вибраний із Ph;-CH2CH2-S-CH2-4-(4-CI-Ph)-Ph;-CH2CH2-S(O)групи, яка включає водень, алкіл, заміщений алкіл, CH2-4-(4-CI-Ph)-Ph; -CH2CH2CH2-S-CH2-4-(4-CI-Ph)алкеніл, заміщений алкеніл, алкініл, заміщений Ph;-CH2CH2CH2-S(O)-CH2-4-(4-CI-Ph)-Ph; алкініл, циклоалкіл, заміщений циклоалкіл, циклоCH2CH2CH2-S-CH2-4-[3,4-AH-CI-PhCH2O-)-Ph; алкеніл, заміщений циклоалкеніл, арил, гетероаCH2CH2-NHSO2-CH2-4-[4-(4-Ph)-Ph]-Ph; рил, гетероцикл, -C(O)Rd, -C(NH)Rd, -C(O)NRcRc, CH2CH2CH2-NHSO2-CH2-4-(4-CI-Ph)-Ph; C(O)ORd, -C(NH)NRcRc і -Ra-Y-Rb-(Z)x, або R11 і R12 CH2CH2CH2-NHSO2-CH2-4-(Ph-C C-)-Ph; з'єднані, разом із атомом азоту, до якого вони приCH2CH2CH2-NHSO2-4-(4-CI-Ph)-Ph; або єднані, з утворенням гетероциклічного кільця; R13 СН2СН2СН2-NНSО2-4-(нафт-2-ил)-Рh. Переважно вибраний із групи, яка включає водень або -OR14; також R1 означає сахаридну групу, заміщену на R14 вибраний із водню, -C(O)Rd і сахаридної групи; азоті сахариду 4-(4-хлорфеніл)бензильною групою кожен Ra незалежно вибраний із групи, яка вклюабо 4-(4-хлорбензилокси)бензильною групою. чає алкілен, заміщений алкілен, алкенілен, заміВ переважному втіленні, R1 означає сахаридну щений алкенілен, алкінілен і заміщений алкінілен; групу формули: кожен Rb незалежно вибраний із групи, яка включає ковалентний зв'язок, алкілен, заміщений алкілен, алкенілен, заміщений алкенілен, алкінілен і заміщений алкінілен, за умови, що Rb не означає c зв'язок, коли Ζ означає водень; кожен R незалежно вибраний із групи, яка включає водень, алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, алкініл, заміщений алкініл, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, арил, гетероарил, гетероцикл і -C(O)Rd; кожен Rd незалежно вибраний із групи, яка включає алкіл, 13 75083 14 -NH(CH2)5OH; -NH(CH2)2OCH3; -NHCH2тетрагідрофуран-2-іл; -N[(CH2)2OH]2; NH(CH2)2N[(CH2)2OH]2; -NHCH2COOH; NHCH(COOH)CH2OH; -NH(CH2)2COOH; N(глюкамін); -NH(CH2)2COOH; -NH(CH2)3SO3H; NHCH(COOH)(CH2)2NH2; -NHCH(COOH)(CH2)3NH2; -NHCH(COOH)CH2CO2(CH2)3-N+(CH3)3; -NHCH(COOH)CH2CO2(CH2)2C(O)-N(CH3)2; -NНСН(СООН)СН2СO2(СН2)3-морфолін-4-іл; -NHCH(COOH)CH2CO2(CH2)2OC(O)C(CH3)3; -NHCH(CH2COOH)CO2(CH2)3-N+(CH3)3; -NHCH(CH2COOH)CO2(CH2)2C(O)N(CH3)2; aбo -NНСН(СН2СООН)СО2(СН2)3-морфолін-4-іл; -NHCH(CH2COOH)CO2(CH2)2OC(O)C(CH3)3; -NHCH(COOH)CH2CO2CH3; в якій R15 означає -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або -NHCH(CH2COOH)CO2(CH2)2N(CH3)2; -C(O)-Ra-Y-Rb-(Z)x; і R16 означає водень або метил. -NHCH(COOH)CH2CO2CH2C(O)N(CH3)2; Переважно, R15 означає -CH2CH2-NH-NHCH(CH2COOH)CO2CH2C(O)N(CH3)2; (CH2)9CH3; -CH2CH2CH2-NH-(CH2)8CH3;-NHCH(CH2COOH)CO2CH3; CH2CH2CH2CH2-NH-(CH2)7CH3; -CH2CH2-NHSO2-NH(CH2)3N(CH3)2;-NHCH2CH2CO2CH3; (CH2)9CH3; - CH2CH2-NHSO2-(CH2)11CH3; -CH2CH2-NHCH[CH2CO2CH2C(O)N(CH3)2]CO2CH2-C(O)S-(CH2)8CH3; -CH2CH2-S-(CH2)9CH3; -CH2CH2-SN(CH3)2; -NHCH2CO2CH3; -N-(метил 3-аміно-3(CH2)10CH3; -CH2CH2CH2-S-(CH2)8CH3; дезоксіамінопіранозид); -N-(метил 3-аміно-2,3,6CH2CH2CH2-S-(CH2)9CH3; -CH2CH2CH2-S-(CH2)3тридезоксигексопіранозид); -N-(2-аміно-2-дезоксиCH=CH-(CH2)4CH3 (транс); -CH2CH2CH2CH2-S6-(диводеньфосфат)глюкопіраноза; -N-(2-аміно-2(CH2)7CH3; -CH2CH2-S(O)-(CH2)9CH3; -CH2CH2-Sдезоксиглюконова кислота); -NH(CH2)4COOH; -N(CH2)6Ph; -CH2CH2-S-(CH2)8Ph; -CH2CH2CH2-S(N-CH3-D-глюкамін; -NH(CH2)6COOH; -О(О(CH2)8Ph; -CH2CH2-NH-CH2-4-(4-CI-Ph)-Ph; глюкоза); -NH(CH2)3OC(O)CH(NH2)CH3; CH2CH2-NH-CH2-4-[4-(CH3)2CHCH2-]-Ph; -CH2CH2NН(СН2)4СН(С(О)-2-НООС-піролідин-1NH-CH2-4-(4-CF3-Ph)-Ph; -CH2CH2-S-CH2-4-(4-CIіл)NHCH(COOH)-CH2CH2Ph (S.S ізомер); -NHPh)-Ph;-CH2CH2-S(O)-CH2-4-(4-CI-Ph)-Ph;CH2CH2-NH-(CH2)9CH3; CH2CH2CH2-S-CH2-4-(4-CI-Ph)-Ph; -CH2CH2CH2NH(CH2)C(O)CH2C(O)N(CH3)2; S(O)-CH2-4-(4-CI-Ph)-Ph; -CH2CH2CH2-S-CH2-4-[3,44 6 7 Переважно, R , R і R кожен незалежно вибди-CI-PhCH2O-)-Ph;-CH2CH2-NHSO2-CH2-4-[4-(4раний із водню або -C(O)Rd. Більш переважно, R4, Ph)-Ph]-Ph; -CH2CH2CH2-NHSO2-CH2-4-(4-CI-Ph)R6 і R7 кожен означає водень. Ph; -CH2CH2CH2-NHSO2-CH2-4-(Ph-C C-)-Ph; Переважно, R5 означає водень, -CH2-NHRс, CH2CH2CH2-NHSO2-4-(4-CI-Ph)-Ph; або CH2-NRcRe, -CH2-NH-Ra-Y-Rb-(Z)x, або замісник, -CH2CH2CH2-NHSO2-4-(нафт-2-ил)-Ph. Пере15 який містить одну або дві фосфонові групи. Коли важно R також може представляти собою 4-(4R5 означає замісник, який містить фосфонову грухлорфеніл)бензильну групу або 4-(4пу, R5 означає переважно групу формули -CH(R21)хлорбензилокси)бензильну групу. 2 N(Rc)-Ra-P(O)(OH)2, в якій R21 означає водень або Переважно, R означає водень. 3 с с с Rd, переважно водень, і Ra, Rc, і Rd, мають значенПереважно, R означає -OR ; -NR R ; або азотня, вказані в даній заявці. Більш переважно, коли зв'язаний, кисень-зв'язаний або сірко-зв'язаний R5 означає фосфоно-вмісний замісник, R5 перевазамісник, який містить одну або дві фосфонові жно означає групу формули -CH2-NH-Raгрупи, або його фармацевтичну прийнятну сіль. a 3 3 P(O)(OH)2, де R має значення, вказані в даній Коли R означає фосфоно-вмісний замісник, R заявці. В цій формулі, Ra переважно означає алкіпереважно означає азот-зв'язаний замісник, який ленову групу; більш переважно, алкіленову групу, включає одну фосфонову групу, або його фармаяка містить від 2 до приблизно 6 атомів вуглецю. цевтично прийнятну сіль. Переважно, R3 означає Особливо переважні R5 замісники включають групу формули -O-Ra-P(O)(OH)2, -S-Ra-P(O)(OH)2, с a 3 N-(фосфонометил)-амінометил; N-(2-гідрокси-2або -NR -R -P(O)(OH)2. Більш переважно, R ознафосфоноетил)амінометил; N-карбоксиметил-N-(2чає групу формули -NH-Ra-Р(О)(ОН)2, в якій Ra має фосфоноетил)амінометил; N,Nзначення, вказані в даній заявці. В цій формулі, Ra біс(фосфонометил)-амінометил; і N-(3означає переважно алкіленову групу. Більш перефосфонопропіл)амінометил; і подібні. важно R3 замісники включають фосфонометилаПереважно, коли R5 не представляє собою міно, 3-фосфонопропіламіно і 2-гідрокси-2фосфоно-вмісний замісник, R5 означає водень, фосфоноетиламіно групи та подібні. CH2-NHRc, -CH2-NRcRe або -CH2-NH-Ra-Y-Rb-(Z)x. Переважно, коли R3 не представляє собою 3 R5 також може переважно означати водень; -СН2фосфоно-вмісний замісник, R означає -ОН; -NHN-(N-СН3-О-глюкамін); -СН2-NH-CH2CH2-NH(CH2)3-N(CH3)2; N-(D-глюкозамін); (CH2)9CH3; -CH2-NH-CH2CH2-NHC(O)-(CH2)3COOH; NHCH(CO2CH3)CH2CO2CH3; -NН(СН2)3-(морфолін-CH2-NH-(CH2)9CH3; -CH2-NH-CH2CH2-COOH; -CH24-іл); -NH(CH2)3-NH(CH2)2CH3; -NН(СН2-піперидинNH-(CH2)5COOH; -СН2-(морфолін-4-іл); -CH2-NH1-іл; -NH(CH2)4NHC(N)NH2; -NH(CH2)2-N+(CH3)3; CH2CH2-O-CH2CH2OH; -CH2-NH-CH2CH(OH)NHCH(COOH)(CH2)3NHC(N)NH2; -NH-[CH2CH2CH2CH2OH; -CH2-N[CH2CH2OH]2; -CH2-NH-(CH2)3NH-]3-H; -N[(CH2)3N(CH3)2]2; -NН(СН2)3-імідазол-1N(CH3)2; -CH2-N[(CH2)3-N(CH3)2]2; -CH2-NH-(СН2)3іл; -NНСН2-4-піридил; -NH(CH2)3CH3; -NH(CH2)2OH; 15 75083 16 (імідазол-1-іл); -СН2-NН-(СН2)3-(морфолін-4-іл); Ra-Y-Rb-(Z)x; і CH2-NH-(CH2)4-NHC(NH)NH2; -СН2-N-(2-аміно-2Ra, Υ, Rb, Ζ, x, Rf, R3. і R5 мають будь-які знадезоксиглюконова кислота); -CH2-NH-CH2CH2-NHчення або переважно значення, вказані в даній (CH2)11CH3; -CH2-NH-CH(COOH)CH2COOH; -CH2заявці; NH-CH2CH2-NHSO2-(CH2)7CH3; -CH2-NH-CH2CH2або його фармацевтично прийнятну сіль, стеNHSO2-(CH2)8CH3; -CH2-NH-CH2CH2-NHSO2реоізомер, або проліки; (CH2)9CH3; -CH2-NH-CH2CH2-NHSO2-(CH2)11CH3; причому принаймні один із R3 і R5 означає заCH2-NH-CH2CH2-NH-(CH2)7CH3; -CH2-NH-CH2CH2місник, який містить одну або декілька фосфоноO-CH2 CH2OH; -CH2-NH-CH2CH2C(O)-N-(Dвих груп. глюкозамін); -CH2-NH-(6-оксо-[1,3]оксазінан-3-іл); Переважно, R20 означає -СН2СН2-NНCH2-NH-CH2CH2-S-(CH2)7CH3; -CH2-NH-CH2CH2-S(СН2)9СН3; -CH2CH2CH2-NH-(СН2)8СН3; (CH2)8CH3; -CH2-NH-CH2CH2-S-(CH2)9CH3; -CH2-NHCH2CH2CH2CH2-NH-(CH2)7CH3; -CH2CH2-NHSO2CH2CH2-S-(CH2)11CH3; -CH2-NH-CH2CH2-S(CH2)9CH3; -CH2CH2-NHSO2-(CH2)11CH3; -CH2CH2(CH2)6Ph; -CH2-NH-CH2CH2-S-(CH2)8Ph; -CH2-NHS-(CH2)8CH3; -CH2CH2-S-(CH2)9CH3; -СН2СН2-SCH2CH2-S-(CH2)10Ph; -CH2-NH-CH2CH2-S-CH2-(4-(4(СН2)10СН3; -CH2CH2CH2-S-(CH2)8CH3; CF3-Ph)Ph); -CH2-NH-CH2CH2-NH-(CH2)11CH3; або CH2CH2CH2-S-(CH2)9CH3; -CH2CH2CH2-S-(CH2)3CH2-NH-(CH2)5-COOH. CH=CH-(CH2)4CH3 (транс); -CH2CH2CH2CH2-SПереважно, R8 означає -CH2C(O)NH2, (CH2)7CH3; -CH2CH2-S(O)-(CH2)9CH3; -CH2CH2-SCH2COOH, бензил, 4-гідроксифеніл або 3-хлор-4(CH2)6Ph; -CH2CH2-S-(CH2)8Ph; -CH2CH2CH2-Sгідроксифеніл. (CH2)8Ph; -CH2CH2-NH-CH2-4-(4-CI-Ph)-Ph; Переважно, R9 означає водень або алкіл. CH2CH2-NH-CH2-4-[4-(CH3)2CHCH2-]-Ph;-CH2CH2Переважно, R10 означає алкіл або заміщений NH-CH2-4-(4-CF3-Ph)-Ph; -CH2CH2-S-CH2-4-(4-CIалкіл. Більш переважно, R10 означає боковий ланPh)-Ph;-CH2CH2-S(O)-CH2-4-(4-CI-Ph)-Ph; цюг природної амінокислоти, такий як ізобутил. CH2CH2CH2-S-CH2-4-(4-CI-Ph)-Ph;-CH2CH2CH2Переважно, R11 означає водень або алкіл. S(O)-CH2-4-(4-CI-Ph)-Ph; -CH2CH2CH2-S-CH2-4-[3,4Переважно, R12 означає водень, алкіл, заміди-CI-PhCH2O-)-Ph; -CH2CH2-NHSO2-CH2-4-[4-(4щений алкіл або -C(O)Rd. Ph)-Ph]-Ph; -CH2CH2CH2-NHSO2-CH2-4-(4-CI-Ph)R12 переважно також може представляти соPh; -CH2CH2CH2-NHSO2-CH2-4-(Ph-C C-)-Ph; бою водень; -СН2СООН; -СН2-[СН(ОН)]5СН2ОН; CH2CH2CH2-NHSO2-4-(4-CI-Ph)-Ph; або СН2СН(ОН)СН2ОН; -CH2CH2NH2; СН2СН2СН2-NHSO2-4-(нафт-2-ил)-Ph. Переважно CH2C(O)OCH2CH3; -СН2-(2-піридил); -СН2R20 також означає 4-(4-хлорфеніл)бензильну групу [СН(ОН)]4СООН; -СН2-(3-карбоксифеніл); (R)або 4-(4-хлорбензилокси)бензильну групу. C(O)CH(NH2)(CH2)4NH2; -C(O)Ph; В іншому переважному втіленні, винахід стоC(O)CH2NHC(O)CH3; E-CH2CH2-Sсується сполуки формули II, в якій R19 означає (CH2)3CH=CH(CH2)4CH3; або -С(О)СН3. водень; R20 означає -CH2CH2NH-(CH2)9CH3; R3 1 2 Переважно, X і X кожен означає хлор. означає -ОН; і R5 означає замісник, який містить 3 Переважно, X означає водень. фосфонову групу; або її фармацевтично прийнятПереважно, кожен Υ незалежно вибраний із ну сіль. групи, яка включає кисень, сірку, -S-S-, -NRс-, В ще одному переважному втіленні, винахід S(O)-, -SO2-, -NRсC(O)-, -OSO2-, -OC(O)-, -NRсSO2-, стосується сполуки формули II, в якій R19 означає -C(O)NRс-, -C(O)O-, -SO2NRс-, -SO2O-, водень; R20 означає -Ra-Y-Rb-(Z)х, Rf, -C(O)Rf або P(O)(ORс)O-, -P(O)(ORс)NRс-, -OP(O)(ORс)O-, C(O)-Ra-Y-Rb-(Z)x; R3 означає -OH; і R5 означає OP(O)(ORс)NRс-, -OC(O)O-, -NRсC(O)O-, CH2-NH-CH2-P(O)(OH)2; або її фармацевтично NRсC(O)NRс-, -OC(O)NRс- і -NRсSO2NRс-. прийнятну сіль. Переважно, n означає 0 або 1, і більш переваВинахід також стосується фармацевтичної жно, n означає 1. композиції, яка містить фармацевтично прийнятІншою переважною сполукою за винаходом є ний носій та терапевтично ефективну кількість глікопептид формули II: сполуки за винаходом. В одному переважному втіленні фармацевтично прийнятний носій включає водний розчин циклодекстрину. Переважно, циклодекстрин представляю собою гідроксипропіл- -циклодекстрин або сульфобутиловий складний ефір -циклодекстрину. Більш переважно, циклодекстрин означає гідроксипропіл- циклодекстрин. Сполуки за винаходом є високоефективними антибактеріальними речовинами. Відповідно до цього, винахід також стосується способу лікування ссавців, які мають бактеріальне захворювання, який включає введення ссавцю терапевтично ефективної кількості сполуки за винаходом. Винахід також стосується способу лікування ссавців, які мають бактеріальне захворювання, який включає введення ссавцю терапевтично ефективної кільков якій: сті фармацевтичної композиції за винаходом. R19 означає водень; Винахід також стосуються способів та проміжR20 означає -Ra-Y-Rb-(Z)x, Rf, -C(O)Rf або -C(O) 17 75083 18 них продуктів, придатних для приготування сполук глікопептиду за винаходом, який заміщений на Сза винаходом, ці способи та проміжні продукти кінці, який передбачає одержання похідних відпоописані тут нижче. відного вихідного глікопептиду, в якому С-кінець Винахід також стосується сполуки за винахопредставляє собою карбоксильну групу. дом, як описано в даній заявці, для застосування в Винахід також стосується способу одержання лікуванні, а також і застосування сполуки за винаглікопептиду, який заміщений на R-кінці, який пеходом для приготування складу або лікувального редбачає одержання похідних відповідного вихідзасобу для лікування бактеріальних захворювань у ного глікопептиду, в якому R-кінець є незаміщений ссавців. (наприклад, водень). Винахід також стосується фармацевтичної Винахід також стосується способу одержання композиції, яка як активний інгредієнт включає сполуки формули II, в якій R3 означає -ОН, R5 сполуку за винаходом для лікування бактеріальноозначає -CH2-NH-Ra-P(O)(OH)2, R19 означає водень го захворювання. і R20 означає -Ra-Y-Rb-(Z)х або -Rf, і Ra, Rb, Rf, Υ, Ζ і Винахід також стосується способу одержання x мають значення, вказані в даній заявці, або її глікопептиду за винаходом, який заміщений на Ссолі; причому спосіб включає: кінці замісником, який містить одну або декілька (а) відновне алкілування сполуки формули II, в фосфонових груп, який включає взаємодію відпоякій R3 означає -ОН і R5, R19 і R20 означають вовідного вихідного глікопептиду, в якому С-кінець день, або її солі, із альдегідом формули HC(O)-Ra представляє собою карбоксильну групу, із придатY-Rb-(Z)x або HC(O)Rf , в якій Ra і Rf представляною фосфоновмісною сполукою. ють собою Ra і Rf, відповідно, без однієї -СН2- груВинахід також стосується способу одержання пи, з одержанням сполуки формули II, в якій R3 глікопептиду за винаходом, який заміщений на Rозначає -ОН, R5 і R19 означають водень і R20 ознакінці замісником, який містить одну або декілька чає -Ra-Y-Rb-(Z)x або -Rf, або її солі; і фосфонових груп, який включає взаємодію відпо(б) реагування продукту стадії (а) із формальвідного вихідного глікопептиду, в якому R-кінець дегідом і H2N-Ra-Р(О)(ОН)2 з одержанням сполуки заміщений придатною фосфоновмісною сполукою. формули II, в якій R3 означає -ОН, R5 означає Коли вихідний глікопептид заміщений на ванкозаCH2NH-Ra-P(O)(OH)2, R19 означає водень і R20 міновому амінокінці, такий спосіб необов'язково означає -Ra-Y-Rb-(Z)x або -Rf, або її солі. може додатково включати одержання вихідного Переважні сполуки за винаходом представляглікопептиду за допомогою відновного алкілування ють собою сполуки формули II, наведені в Таблиці відповідного глікопептиду, в якому ванкозаміновий І нижче, де R19 означає водень. амінокінець представляє собою відповідний амін. Винахід також стосується способу одержання Таблиця І Переважні сполуки формули II Сполука 1 1 2 3 4 5 R3 2 фосфонометиламіно фосфонометиламіно фосфонометиламіно фосфонометиламіно фосфонометиламіно R5 3 Η Η Η Η Η 6 фосфонометиламіно Η 7 8 9 10 фосфонометиламіно фосфонометиламіно 3-фосфонопропіламіно 2-гідрокси-2-фосфоноетиламіно 11 ОН 12 ОН 13 ОН 14 ОН 15 ОН 16 ОН 17 ОН Η Η Η Η (фосфонометил)амінометил (фосфонометил)амінометил (фосфонометил)амінометил (фосфонометил)амінометил (фосфонометил)амінпометил (фосфонометил)амінометил (фосфонометил)амінометил R20 4 CH3(CH2)9NHCH2CH2СН3(СН2)9ОСН2СН2CH3(CH2)9CH2CH2СН3СН2)124-(4-хлорфеніл)-бензил 2-(4-(4-хлорфеніл)бензиламіно)етил 4-(4'-хлорбіфеніл)-бутил 5-(4'-хлорбіфеніл)-пентил СН3(СН2)9SСН2СН24-(4-хлорфеніл)-бензил CH3(CH2)9NHCH2CH2CH3(CH2)9SCH2CH2СН3(СН2)9ОСН2СН2СН3(СН2)124-(4-хлорфеніл)бензил 2-(4-(4-хлорфеніл)бензиламіно)етил 4-(4'-хлорбіфеніл)бутил 19 75083 20 Продовженя таблиці І 1 2 18 ОН 19 ОН 20 ОН 21 ОН 22 ОН 23 ОН 24 ОН 25 фосфонометиламіно 26 ОН Інші переважні сполуки за винаходом представляють собою фосфонові похідні глікопептидного антибіотику А82846В [також відомий як хлорорієнтицин А або LY264826]. Дивись, наприклад, R. Nagarajan та ін., J. Org.Chem., 1988, 54, 983-986; і N. Tsuji та ін., J. Antibiot, 1988, 41, 819-822. Структура цього глікопептиду подібна до ванкоміцину, за винятком того, що А82846В містить додатковий аміноцукор (наприклад, 4-епі-ванкозамін, приєднаний в положенні R2 в формулі І.) і додатково включає 4-епі-ванкозамін замість ванкозаміну в дисахаридній частині, приєднаний в положенні R1 у формулі І. Наприклад, переважна група сполук представляє собою N-алкіловані похідні А82846В, які заміщені на С-кінці або на R-кінці замісником, який містить одну або декілька (наприклад, 1, 2, 3, 4 або 5) фосфонових (-РО3Н2) груп; або його фармацевтично прийнятну сіль. Переважною групою сполук за винаходом є похідні А82846В, які заміщені на будь-якому С-кінці або на R-кінці замісником, який містить одну або декілька (наприклад 1, 2, 3, 4 або 5) фосфонових (РО3Н2) груп. Іншою переважною групою сполук за винаходом є похідні А82846В, які заміщені на Скінці і на R-кінці замісником, кожен з яких містить одну або декілька (наприклад 1, 2, 3, 4 або 5) фосфонових (-РО3Н2) груп. Іншою переважною групою сполук за винаходом є фосфонові похідні А82846В, які мають 4-(4-хлорфеніл)бензильну групу або 4-(4-хлорбензилокси)бензильну групу, приєднану до аміногрупи 4-епі-ванкозаміну дисахаридної частини. Сполуки за винаходом, які представляють собою фосфонові похідні А82846В, легко можуть бути одержані за допомогою методик, описаних в даній заявці. Несподівано було виявлено, що фосфонові сполуки за винаходом виявляють знижене накопичення в тканинах та/або нефротоксичність при введенні ссавцям. Не бажаючи пов'язуватися із теорією, припускають, що фосфонові частини служать для збільшення сумарного негативного заряду глікопептиду при фізіологічних умовах й таким 3 (фосфонометил)амінометил (фосфонометил)амінометил N-(2-гідрокси-2фосфоноетил) амінометил N-(карбоксиметил)-N-2фосфонометил)амінометил Ν,Ν-біс(фосфонометил)амінометил 3-фосфонопропіламінометил 3-фосфонопропіламінометил -CH2-N-(N-CH3-Dглюкамін (фосфонометил)амінометил 4 5-(4'-хлорбіфеніл) пентил 3-[4-(4-хлорбензилокси)бензилтіо]пропіл CH3(CH2)9SCH2CH2СН3(СН2)9SСН2СН2CH3(CH2)9NHCH2CH2СН3(СН2)9SСН2СН24-(4-хлорфеніл)бензил CH3(CH2)9NHCH2CH2-(CH2)3NH-SO2-4-(4хлорфеніл)феніл чином полегшують виділення сполук із організму ссавців після введення. Несподіване посилення виведення фосфонових сполук за винаходом може бути пов'язане із зниженим накопиченням в тканинах та/або зниженою нефротоксичністю, що спостерігається для цих сполук в порівнянні із відповідними сполуками, що мають подібну кількість фосфонових функціональних груп. Докладний опис винаходу Даний винахід стосується нових сполук за винаходом, які є похідними глікопептидних антибіотиків, які включають один або декілька замісників, що включають одну або декілька фосфонових груп, а також композицій, які включають ці сполуки і терапевтичних способів, які передбачають введення цих сполук. При описі сполук, композицій та способів за винаходом, нижченаведені терміни мають нижченаведені значення, якщо не вказано інше. Визначення Поняття "алкіл" стосується одновалентного розгалуженого або нерозгалуженого насиченого вуглеводневого ланцюга, який має переважно від 1 до 40 атомів вуглецю, більш переважно від 1 до 10 атомів вуглецю, і найбільш переважно від 1 до 6 атомів вуглецю. Як приклад можна назвати такі групи, як метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, н-гексил, н-децил, тетрадецил та подібні. Поняття "заміщений алкіл" стосується алкільної групи як визначено вище, що має від 1 до 8 замісників, переважно від 1 до 5 замісників, і більш переважно від 1 до 3 замісників, вибраних із групи, яка включає алкокси, заміщений алкокси, циклоалкіл, заміщений циклоалкіл, циклоалкеніл, заміщений циклоалкеніл, ацил, ациламіно, ацилокси, аміно, заміщений аміно, аміноацил, аміноацилокси, оксіаміноацил, азидо, ціано, галоген, гідроксил, кето, тіокето, карбокси, карбоксіалкіл, тіоарилокси, тіогетероарилокси, тіогетероциклоокси, тіол, тіоалкокси, заміщений тіоалкокси, арил, арилокси, гетероарил, гетероарилокси, гетероцикл, гетеро 21 75083 22 циклоокси, гідроксіаміно, алкоксіаміно, нітро, -SOалкілен-О-алкіл, алкілен-О-заміщений алкіл, заміалкіл, -SO-заміщений алкіл, -SO-арил, -SOщений алкілен-О-алкіл і заміщений алкілен-Огетероарил, -SО2-алкіл, -SО2-заміщений алкіл, заміщений алкіл, де алкіл, заміщений алкіл, алкіSО2-арил, -SO3H, гуанідо і -SО2-гетероарил. лен і заміщений алкілен мають значення, визначеПоняття "алкілен" стосується двовалентного ні в даній заявці. Переважні алкілалкокси групи розгалуженого або нерозгалуженого насиченого представляють собою алкілен-О-алкіл і включавуглеводневого ланцюга, який переважно має від ють, наприклад, метиленметокси (-СН2ОСН3), ети1 до 40 атомів вуглецю, переважно 1-10 атомів ленметокси (-СН2СН2ОСН3), н-пропілен-ізовуглецю, більш переважно 1-6 атомів вуглецю. пропокси (-СН2СН2СН2ОСН(СН3)2), метилен-третПрикладами алкілену є такі групи, як метилен (бутокси (-СН2-О-С(СН3)3) і т.п. СН2-), етилен (-СН2СН2-), ізомери пропілену (наПоняття "алкілтіоалкокси" стосується групи приклад, -СН2СН2СН2- і -СН(СН3)СН2-) і т.п. алкілен-S-алкіл, алкілен-S-заміщений алкіл, заміПоняття "заміщений алкілен" стосується алкіщений алкілен-S-алкіл і заміщений алкілен-Sленової групи, як визначено вище, яка має від 1 до заміщений алкіл, де алкіл, заміщений алкіл, алкі5 замісників, і переважно від 1 до 3 замісників, лен і заміщений алкілен мають значення, вказані в вибраних із групи, яка включає алкокси, заміщений даній заявці. Переважні алкілтіоалкоксигрупи алкокси, циклоалкіл, заміщений циклоалкіл, цикпредставляють собою алкілен-S-алкіл і включалоалкеніл, заміщений циклоалкеніл, ацил, ацилають, наприклад, метилентіометокси (-CH2SCH3), міно, ацилокси, аміно, заміщений аміно, аміноаетилентіометоски (-CH2CH2SCH3), н-пропілен-ізоцил, аміноацилокси, оксіаміноацил, азидо, ціано, тіопропокси (-CH2CH2CH2SCH(CH3)2), метиленгалоген, гідроксил, карбокси, карбоксіалкіл, тіоатрет-тіобутокси (-CH2SC(CH3)3) і т.п. рилокси, тіогетероарилокси, тіогетероциклоокси, Поняття "алкеніл" стосується одновалентної тіол, тіоалкокси, заміщений тіоалкокси, арил, арирозгалуженої або нерозгалуженої ненасиченої локси, гетероарил, гетероарилокси, гетероцикл, вуглеводневої групи, яка переважно має від 2 до гетероциклоокси, гідроксіаміно, алкоксіаміно, ніт40 атомів вуглецю, більш переважно від до 2 до 10 ро, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, атомів вуглецю і найбільш переважно від 2 до 6 SO-гетероарил, -SO2-алкіл, -SО2-заміщений алкіл, атомів вуглецю і яка має принаймні 1 і переважно -SО2-арил і -SО2-гетероарил. Крім того, такі замівід 1 до 6 ненасичених подвійних зв'язків. Переващені алкіленові групи включають такі, в яких 2 зажні алкенільні групи представляють собою етеніл місники алкіленової групи зв'язані з утворенням (-СН=СН2), н-пропеніл (-СН2СН=СН2), ізо-пропеніл однієї або більшої кількості циклоалкільних, замі(-С(СН3)=СН2), і т.п. щених циклоалкільних, циклоалкенільних, заміщеПоняття "заміщений алкеніл" стосується алкених циклоалкенільних, арильних, гетероциклічних нільної групи, як визначено вище, яка має від 1 до або гетероарильних груп, приконденсованих до 5 замісників, і переважно 1 до 3 замісників, вибраалкеліленової групи. Переважно такі конденсовані них із групи, яка включає алкокси, заміщений алкогрупи включають від 1 до 3 спряжених кільцевих кси, циклоалкіл, заміщений циклоалкіл, циклоалструктур. Крім того, поняття заміщений алкілен кеніл, заміщений циклоалкеніл, ацил, ациламіно, включає алкіленові групи, в яких від 1 до 5 атомів ацилокси, аміно, заміщений аміно, аміноацил, амівуглецю алкілену заміщені киснем, сіркою або ноацилокси, оксіаміноацил, азидо, ціано, галоген, NR-, де R означає водень або алкіл. Прикладами гідроксил, кето, тіокето, карбокси, карбоксіалкіл, заміщених алкіленів є хлорметилен (-СН(СІ)-), тіоарилокси, тіогетероарилокси, тіогетероциклоокаміноетилен (-CH(NH2)CH2-), ізомери 2си, тіол, тіоалкокси, заміщений тіоалкокси, арил, карбоксипропілену (-СН2СН(СО2Н)СН2-), етоксіеарилокси, гетероарил, гетероарилокси, гетеротил (-СН2СН2 О-СН2СН2-) і т.п. цикл, гетероциклоокси, гідроксіаміно, алкоксіаміно, Поняття "алкарил" стосується групи -алкіленнітро, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, арил і -заміщений алкілен-арил, де алкілен, заміSO-гетероарил, -SO2-алкіл, -SО2-заміщений алкіл, щений алкілен і арил визначені в даній заявці. -SО2-арил і -SО2-гетероарил. Прикладами таких алкарильних груп є бензил, Поняття "алкенілен" стосується двовалентної фенетил і т.п. розгалуженої або нерозгалуженої ненасиченої Поняття "алкокси" стосується групи алкіл-О-, вуглеводневої групи, яка переважно має від 2 до алкеніл-О, циклоалкіл-О-, циклоалкеніл-О- і алкі40 атомів вуглецю, більш переважно 2-10 атомів ніл-О, в якій алкіл, алкеніл, циклоалкіл, циклоалкевуглецю і найбільш переважно 2-6 атомів вуглецю ніл і алкініл мають значення, визначені в даній і яка має принаймні 1 і переважно від 1 до 6 неназаявці. Переважні алкоксигрупи представляють сичених подвійних зв'язків. Як приклади такої грусобою алкіл-О- і включають, наприклад, метокси, пи можна назвати етенілен (-СН=СН-), ізомери етокси, н-пропокси, ізо-пропокси, н-бутокси, третпропенілену (наприклад, -СН2СН=СНі бутокси, втор-бутокси, н-пентокси, н-гексокси, 1,2С(СН3)=СН-) і т.п. диметилбутокси і т.п. Поняття "заміщений алкенілен" стосується алПоняття "заміщений алкокси" стосується групи кеніленової групи, як визначено вище, що має від заміщений алкіл-О-, заміщений алкеніл-О-, замі1 до 5 замісників, і переважно від 1 до 3 замісників, щений циклоалкіл-О-, заміщений циклоалкеніл-О- і вибраних із групи, яка включає алкокси, заміщений заміщений алкініл-О-, де заміщений алкіл, заміщеалкокси, циклоалкіл, заміщений циклоалкіл, цикний алкеніл, заміщений циклоалкіл, заміщений лоалкеніл, заміщений циклоалкеніл, ацил, ацилациклоалкеніл і заміщений алкініл мають значення, міно, ацилокси, аміно, заміщений аміно, аміноавизначені в даній заявці. цил, аміноацилокси, оксіаміноацил, азидо, ціано, Поняття "алкілалкокси" стосується групи галоген, гідроксил, карбокси, карбоксіалкіл, тіоа 23 75083 24 рилокси, тіогетероарилокси, тіогетероциклоокси, роарил-С(О)- і гетероцикл-С(О)-, де алкіл, заміщетіол, тіоалкокси, заміщений тіоалкокси, арил, ариний алкіл, циклоалкіл, заміщений циклоалкіл, циклокси, гетероарил, гетероарилокси, гетероцикл, лоалкеніл, заміщений циклоалкеніл, арил, гетерогетероциклоокси, гідроксіаміно, алкоксіаміно, нітарил і гетероцикл мають значення, вказані в даній ро, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, заявці. SO-гетероарил, -SO2-алкіл, -SО2-заміщений алкіл, Поняття "ациламіно" або "амінокарбоніл" сто-SО2-арил і -SО2-гетероарил. Крім того, такі замісується групи -C(O)NRR, в якій кожен R незалежно щені алкеніленові групи включають такі, де 2 заміозначає водень, алкіл, заміщений алкіл, арил, гесники алкеніленової групи зв'язані з утворенням тероарил, гетероцикл або в якій обидві R групи однієї або більшої кількості циклоалкільних, заміз'єднані з утворенням гетероциклічної групи (нащених циклоалкільних, циклоалкенільних, заміщеприклад, морфоліно), де алкіл, заміщений алкіл, них циклоалкенільних, арильних, гетероциклічнічарил, гетероарил і гетероцикл мають значення, них або гетероарильних груп, приконденсованих вказані в даній заявці. до алкеніленової групи. Поняття "аміноацил" стосується групи Поняття "алкініл" стосується одновалентного NRC(O)R, де кожен R незалежно означає водень, ненасиченого вуглеводню, який має переважно від алкіл, заміщений алкіл, арил, гетероарил або ге2 до 40 атомів вуглецю, більш переважно від 2 до тероцикл, де алкіл, заміщений алкіл, арил, гетеро20 атомів вуглецю і найбільш переважно від 2 до 6 арил і гетероцикл мають значення, вказані в даній атомів вуглецю і який має принаймні 1 і переважно заявці. від 1 до 6 ненасичених ацетиленових (потрійних) Поняття "аміноацилокси" або "алкоксикарбонізв'язків. Переважні алкінільні групи включають ламіно" стосується групи -NRC(O)OR, в якій кожен R незалежно означає водень, алкіл, заміщений етиніл (-C СН), пропаргіл (-СН2С СН) і т.п. алкіл, арил, гетероарил або гетероцикл, де алкіл, Поняття "заміщений алкініл" стосується алкінізаміщений алкіл, арил, гетероарил і гетероцикл льної групи, як визначено вище, що має від 1 до 5 мають значення, вказані в даній заявці. замісників, і переважно 1 до 3 замісників, вибраних Поняття "ацилокси" стосується групи алкіліз групи, яка включає алкокси, заміщений алкокси, С(О)О-, заміщений алкіл-С(O)O-, циклоалкілциклоалкіл, заміщений циклоалкіл, циклоалкеніл, С(О)О-, заміщений циклоалкіл-С(О)О-, арилзаміщений циклоалкеніл, ацил, ациламіно, ацилоС(О)О-, гетероарил-С(О)О-, і гетероцикл-С(О)О-, кси, аміно, заміщений аміно, аміноацил, аміноациде алкіл, заміщений алкіл, циклоалкіл, заміщений локси, оксіаміноацил, азидо, ціано, галоген, гідрокциклоалкіл, арил, гетероарил і гетероцикл мають сил, карбокси, карбоксіалкіл, тіоарилокси, значення, вказані в даній заявці. тіогетероарилокси, тіогетероциклоокси, тіол, тіоаПоняття "арил" стосується ненасиченої аролкокси, заміщений тіоалкокси, арил, арилокси, матичної карбоциклічної групи, яка має від 6 до 20 гетероарил, гетероарилокси, гетероцикл, гетероатомів вуглецю, що має одинарне кільце (наприциклоокси, гідроксіаміно, алкоксіаміно, нітро, -SOклад, феніл) або декілька конденсованих (спряжеалкіл, -SO-заміщений алкіл, -SO-арил, -SOних) кілець, де принаймні одне кільце є ароматичгетероарил, -SО2-алкіл, -SО2-заміщений алкіл, ним (наприклад, нафтил, дигідрофенантреніл, SО2-арил і -SО2-гетероарил. флуореніл або антрил). Переважні арили предстаПоняття "алкінілен" стосується двовалентного вляють собою феніл, нафтил і т.п. ненасиченого вуглеводню, що має переважно від Якщо не вказано інше для арильного замісни2 до 40 атомів вуглецю, більш переважно від 2 до ка, такі арильні групи необов'язково можуть бути 10 атомів вуглецю і найбільш переважно від 2 до 6 заміщені 1-5 замісниками, переважно 1-3 замісниатомів вуглецю і що має принаймні 1 і переважно ками, вибраних із групи, яка включає ацилокси, від 1 до 6 ненасичених ацетиленових (потрійних) гідрокси, тіол, ацил, алкіл, алкокси, алкеніл, алкізв'язків. Переважні алкініленові групи включають ніл, циклоалкіл, циклоалкеніл, заміщений алкіл, етинілен (-C C-), пропаргілен (-СН2С С-) і т.п. заміщений алкокси, заміщений алкеніл, заміщений Поняття "заміщений алкінілен" стосується алалкініл, заміщений циклоалкіл, заміщений циклоакініленової групи, як визначено вище, що має від 1 лкеніл, аміно, заміщений аміно, аміноацил, ациладо 5 замісників, і переважно від 1 до 3 замісників, міно, алкарил, арил, арилокси, азидо, карбокси, вибраних із групи, яка включає алкокси, заміщений карбоксіалкіл, ціано, галоген, нітро, гетероарил, алкокси, циклоалкіл, заміщений циклоалкіл, цикгетероарилокси, гетероцикл, гетероциклоокси, лоалкеніл, заміщений циклоалкеніл, ацил, ацилааміноацилокси, оксіациламіно, сульфонамід, тіоаміно, ацилокси, аміно, заміщений аміно, аміноалкокси, заміщений тіоалкокси, тіоарилокси, тіогецил, аміноацилокси, оксіаміноацил, азидо, ціано, тероарилокси, -SO-алкіл, -SO-заміщений алкіл, галоген, гідроксил, кето, тіокето, карбокси, карбокSO-арил, -SO-гетероарил, -SО2-алкіл, -SО2сіалкіл, тіоарилокси, тіогетероарилокси, тіогетерозаміщений алкіл, -SО2-арил, -SО2-гетероарил і циклоокси, тіол, тіоалкокси, заміщений тіоалкокси, тригалометил. Переважні арильні замісники предарил, арилокси, гетероарил, гетероарилокси, гетеставляють собою алкіл, алкокси, галоген, ціано, роцикл, гетероциклоокси, гідроксіаміно, алкоксіанітро, тригалометил і тіоалкокси. міно, нітро, -SO-алкіл, -SO-заміщений алкіл, -SOПоняття "арилокси" стосується групи арил-О-, арил, -SO-гетероарил, -SО2-алкіл, -SО2-заміщений в якій арильна група має значення, вказані вище, алкіл, -SО2-арил і -SО2-гетероарил. включаючи необов'язково заміщену арильну групу Поняття "ацил" стосується групи НС(О)-, алкіляк також визначено вище. С(О)-, заміщений алкіл-С(О)-, циклоалкіл-С(О)-, Поняття "арилен" стосується двовалентного заміщений циклоалкіл-С(О)-, циклоалкеніл-С(О)-, похідного арилу (включаючи заміщений арил) як заміщений циклоалкеніл-С(О)-, арил-С(О)-, гете 25 75083 26 визначено вище, і прикладом такої групи є 1,2-SО2-арил і -SО2-гетероарил. фенілен, 1,3-фенілен, 1,4-фенілен, 1,2-нафтилен і Поняття "циклоалкеніл" стосується циклічної т.п. алкенільної групи із 4-20 атомів вуглецю, що має Поняття "аміно" стосується NH2-групи. одну циклічну структуру і принаймні одну точку Поняття "заміщений аміно" стосується групи внутрішньої ненасиченості. Приклади прийнятної NRR, в якій кожен R незалежно вибраний із групи, циклоалкенільної групи включають, зокрема, цикяка включає водень, алкіл, заміщений алкіл, циклобут-2-еніл, циклопент-3-еніл, циклоокт-3-еніл і лоалкіл, заміщений циклоалкіл, алкеніл, заміщет.п. ний алкеніл, циклоалкеніл, заміщений циклоалкеПоняття "заміщений циклоалкеніл" стосується ніл, алкініл, заміщений алкініл, арил, гетероарил і циклоалкенільної групи, яка має від 1 до 5 замісгетероцикл, за умови, що обидва R не представників, і переважно від 1 до 3 замісників, вибраних ляють собою водень. із групи, яка включає алкокси, заміщений алкокси, "Амінокислота" стосується будь-яких природциклоалкіл, заміщений циклоалкіл, циклоалкеніл, них амінокислот (наприклад, Ala, Arg, Asn, Asp, заміщений циклоалкеніл, ацил, ациламіно, ацилоCys, Glu, Gln, Gly, His, Hyl, Hyp, lle, Leu, Lys, Met, кси, аміно, заміщений аміно, аміноацил, аміноациPhe, Pro, Ser, Thr, Trp, Tyr і Val) в D, L, або DL фолокси, оксіаміноацил, азидо, ціано, галоген, гідрокрмі. Бокові ланцюги природних амінокислот добре сил, кето, тіокето, карбокси, карбоксіалкіл, відомі в даній галузі і включають, наприклад, вотіоарилокси, тіогетероарилокси, тіогетероциклоокдень (наприклад, як в гліцині), алкіл (наприклад, як си, тіол, тіоалкокси, заміщений тіоалкокси, арил, в аланіні, валіні, лецині, ізолейцині, проліні), заміарилокси, гетероарил, гетероарилокси, гетерощений алкіл (наприклад, як в треоніні, серпні, мецикл, гетероциклоокси, гідроксіаміно, алкоксіаміно, тіоніні, цистеїні, аспарагіновій кислоті, аспарагіні, нітро, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, глутаміновій кислоті, глутаміні, аргініні і лізині), SO-гетероарил, -SO2-алкіл, -SО2-заміщений алкіл, алкарил (наприклад, як в фенілаланіні і триптофа-SО2-арил і -SО2-гетероарил. ні), заміщений арилалкіл (наприклад, як в тирозиПоняття "гало" або "галоген" стосується фтоні), і гетероарилалкіл (наприклад, як в гістидині). ру, хлору, брому та йоду. Поняття "карбокси" стосується -СООН. "Галоалкіл" стосується алкілу, як визначено в Поняття "С-кінець", що стосується глікопептиданій заявці, заміщеного 1-4 галогрупами, як виду, добре зрозуміло фахівцю в даній галузі. Назначено вище, які можуть бути однаковими або приклад, для глікопептиду формули І, С-кінець різними. Типові галоалкільні групи включають, наявляє собою положення, заміщене групою R3. приклад, трифторметил, 3-фтордодецил, 12,12,12Поняття "дикарбокси-заміщений алкіл" стосутрифтордодецил, 2-бромоктил, 3-бром-6ється алкільної групи, заміщеної двома карбоксихлоргептил, і т.п. льними групами. Для прикладу можна навести Поняття "гетероарил" стосується ароматичної СН2(СООН)СН2СООН і -СН2(СООН)СН2СН2СООН. групи із 1-15 атомів вуглецю і 1-4 гетероатомів, Поняття "карбоксіалкіл" або "алкоксикарбоніл" вибраних із кисню, азоту і сірку, в принаймні одностосується групи "-С(О)О-алкіл", "-С(О)Ому кільці (за наявності більше ніж одного кільця). заміщений алкіл", "-С(О)О-циклоалкіл", "-С(О)ОЯкщо не вказано інше для гетероарильного заміщений циклоалкіл", "-С(О)О-алкеніл", "-С(О)Озамісника, такі гетероарильні групи необов'язково заміщений алкеніл", "-С(О)О-алкініл" і "-С(О)Оможуть бути заміщені 1-5 замісниками, переважно заміщений алкініл", де алкіл, заміщений алкіл, ци1-3 замісниками, вибраних із групи, яка включає клоалкіл, заміщений циклоалкіл, алкеніл, заміщеацилокси, гідрокси, тіол, ацил, алкіл, алкокси, алний алкеніл, алкініл і заміщений алкініл алкініл кеніл, алкініл, циклоалкіл, циклоалкеніл, заміщемають значення, вказані в даній заявці. ний алкіл, заміщений алкокси, заміщений алкеніл, Поняття "циклоалкіл" стосується циклічної алзаміщений алкініл, заміщений циклоалкіл, заміщекільної групи із 3-20 атомів вуглецю, яка має одиний циклоалкеніл, аміно, заміщений аміно, аміноанарне кільце або декілька конденсованих кілець. цил, ациламіно, алкарил, арил, арилокси, азидо, Такі циклоалкільні групи представляють собою, карбокси, карбоксіалкіл, ціано, галоген, нітро, генаприклад, однокільцеві структури, такі як циклоптероарил, гетероарилокси, гетероцикл, гетероцикропіл, циклобутил, циклопентил, циклооктил, і т.п., лоокси, аміноацилокси, оксіациламіно, тіоалкокси, або поліциклічні структури, такі як адамантил, і т.п. заміщений тіоалкокси, тіоарилокси, тіогетероариПоняття "заміщений циклоалкіл" стосується локси, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, циклоалкільної групи, яка має від 1 до 5 замісників, SO-гетероарил, -SО2-алкіл, -SO2-заміщений алкіл, і переважно 1-3 замісники, вибраних із групи, яка -SО2-арил, -SО2-гетероарил і тригалометил. Перевключає алкокси, заміщений алкокси, циклоалкіл, важні арильні замісники представляють собою заміщений циклоалкіл, циклоалкеніл, заміщений алкіл, алкокси, галоген, ціано, нітро, тригалометил циклоалкеніл, ацил, ациламіно, ацилокси, аміно, і тіоалкокси. Такі гетероарильні групи можуть мати заміщений аміно, аміноацил, аміноацилокси, оксіодинарне кільце (наприклад, піридил або фурил) аміноацил, азидо, ціано, галоген, гідроксил, кето, або декілька конденсованих кілець (наприклад, тіокето, карбокси, карбоксіалкіл, тіоарилокси, тіоіндолізиніл або бензотієніл). Переважні гетероагетероарилокси, тіогетероциклоокси, тіол, тіоалкорили представляють собою піридил, піроліл і фукси, заміщений тіоалкокси, арил, арилокси, гетерил. роарил, гетероарилокси, гетероцикл, "Гетероарилалкіл" стосується (гетероагетероциклоокси, гідроксіаміно, алкоксіаміно, нітрил)алкіл-, в якому гетероарил і алкіл мають знаро, -SO-алкіл, -SO-заміщений алкіл, -SO-арил, чення, вказані в даній заявці. Типовими прикладаSO-гетероарил, -SО2-алкіл, -SО2-заміщений алкіл, ми є 2-піридилметил і т.п. 27 75083 28 Поняття "гетероарилокси" стосується групи геПоняття "оксіациламіно" або "амінокарбонілотероарил-О-. кси" стосується групи -OC(O)NRR, в якій кожен R Поняття "гетероарилен" стосується двоваленнезалежно означає водень, алкіл, заміщений алтної групи, яка є похідною від гетероарилу (вклюкіл, арил, гетероарил або гетероцикл, де алкіл, чаючи заміщений гетероарил), як вказано вище, і заміщений алкіл, арил, гетероарил і гетероцикл прикладом таких є групи 2,6-піридилен, 2,4мають значення, вказані в даній заявці. піридилен, 1,2-хінолінілен, 1,8-хінолінілен, 1,4Поняття "фосфоно" стосується -РО3Н2. бензофуранілен, 2,5-піриднілен, 2,5-індоленіл і т.п. Поняття "фосфонометиламіно" стосується Поняття "гетероцикл" або "гетероциклічний" NH-CH2-P(O)(OH)2. стосується одновалентної насиченої або ненасиПоняття "фосфонометиламінометил" стосученої групи, яка має одинарне кільце або декілька ється -CH2-NH-CH2-Р(О)(ОН)2. конденсованих кілець, від 1 до 40 атомів вуглецю і Поняття "проліки" добре зрозуміло в даній гавід 1 до 10 гетероатомів, переважно 1 - 4 гетероалузі і включає сполуки, які перетворюються в фатоми, вибраних із азоту, сірки, фосфору та/або рмацевтично активні сполуки за винаходом в оркисень в кільці. ганізмі ссавця. Наприклад, дивись Remington's Якщо не вказано інше для гетероциклічного Pharmaceutical Sciences, 1980, том. 16, Mack замісника, такі гетероциклічні групи необов'язково Publishing Company, Істон, Пенсільванія, 61 і 424. можуть бути заміщені 1-5, і переважно 1-3 замісПоняття "R-кінець" що стосується глікопептиниками, вибраними із групи, яка включає алкокси, ду, добре зрозуміло фахівцю в даній галузі. Назаміщений алкокси, циклоалкіл, заміщений циклоприклад, для глікопептиду формули І, R-кінець алкіл, циклоалкеніл, заміщений циклоалкеніл, являє собою положення, заміщене групою R5. ацил, ациламіно, ацилокси, аміно, заміщений аміПоняття "сахаридна група" стосується окислено, аміноацил, аміноацилокси, оксіаміноацил, азиної, відновленої або заміщеної сахаридної однодо, ціано, галоген, гідроксил, кето, тіокето, карбоквалентної групи, ковалентно приєднаної до глікоси, карбоксіалкіл, тіоарилокси, тіогетероарилокси, пептиду або іншої сполуки за допомогою будьтіогетероциклоокси, тіол, тіоалкокси, заміщений якого атому сахаридної частини, переважно за тіоалкокси, арил, арилокси, гетероарил, гетероадопомогою агліконового атома вуглецю. Поняття рилокси, гетероцикл, гетероциклоокси, гідроксіамівключає аміновмісні сахаридні групи. Типові сахано, алкоксіаміно, нітро, -SO-алкіл, -SO-заміщений риди включають, наприклад, гексози, такі як Dалкіл, -SO-арил, -SO-гетероарил, -SО2-алкіл, -SО2глюкоза, D-маноза, D-ксилоза, D-галактоза, ванкозаміщений алкіл, -SО2-арил, оксо (=O) і -SO2замін, 3-дезметил-ванкозамін, 3-епі-ванкозамін, 4гетероарил. Такі гетероциклічні групи можуть мати епі-ванкозамін, акозамін, актинозамін, даунозамін, одинарне кільце або декілька конденсованих кі3-епі-даунозамін, рістозамін, D-глюкамін, N-метиллець. Переважні гетероцикли включають морфоО-глюкамін, D-глюконова кислота, N-ацетил-Оліно, піперидиніл і т.п. глюкозамін, N-ацетил-О-галактозамін, сіалова кисПриклади гетероциклів і гетероарилів, які міслота, ідуронова кислота, L-фруктоза, і т.п.; пентотять азот, включають, але не обмежуючись ними, зи, такі як D-рибоза або D-арабіноза; кетози, такі пірол, імідазол, піразол, піридин, піразин, піриміяк D-рибулоза або D-фруктоза; дисахариди, такі як дин, піридазин, індолізин, ізоіндол, індол, індазол, 2-О-( -L-ванкозамініл)- -О-глюкопіраноза, 2-О-(3пурин, хінолізин, ізохінолін, хінолін, фталазин, надезметил- -L-ванкозамініл)- -D-глюкопіраноза, фтилпіридин, хіноксалін, хіназолін, цинолін, птесахароза, лактоза або мальтоза; похідні, такі як ридин, карбазол, карболін, фенантридин, акридин, ацеталі, аміни, ациловані, сульфатовані і фосфофенантролін, ізотіазол, феназин, ізоксазол, фенориловані цукри; олігосахариди, які мають від 2 до ксазин, фенотіазин, імідазолідин, імідазолін, піпе10 сахаридних ланок. З метою цього визначення, ридин, піперазин, індолін, морфоліно, піперидиніл, ці сахариди позначаються, використовуючи загатетрагідрофураніл, і також інші подібні N-алкоксильноприйняту трибуквену номенклатуру і сахариди азотвмісні гетероцикли. можуть знаходитися у відкритій формі або переІнший клас гетероциклів відомий як "краунважно в піранозній формі. сполуки", які представляють собою специфічний Поняття "аміновмісна сахаридна група" стосуклас гетероциклічних сполук, які мають одну або ється сахаридної групи, яка має амінозамісник. декілька структурних одиниць формули [-(СН2-)аАТипові аміновмісні сахариди включають L], де а дорівнює 2 або більше ніж 2, і А в кожному ванкозамін, 3-дезметил-ванкозамін, 3-епіокремому випадку може означати О, N, S або Р. ванкозамін, 4-епі-ванкозамін, акозамін, актинозаПриклади краун-сполук включають, наприклад, [мін, даунозамін, 3-епі-даунозамін, рістозамін, N(CH2)3-NH-]3, [-((СН2)2-О)4-((CH2)2-NH)2] і т.п. Як метил-О-глюкамін і т.п. правило, краун-сполуки можуть мати від 4 до 10 Поняття "спіро-приєднана циклоалкільна гругетероатомів і 8-40 атомів вуглецю. па" стосується циклоалкільної групи, приєднаної Поняття "гетероциклоокси" стосується групи до іншого кільця за допомогою атома вуглецю, гетероцикл-О-. спільного для обох кілець. Поняття "тіогетероциклоокси" стосується групи Поняття "стереоізомер" як воно стосується нагетероцикл-S-. ведених сполук, добре відоме в даній галузі, і стоПоняття "N-кінець", що стосується глікопептисується інших сполук, які мають однакову молекуду, добре зрозуміле фахівцю в даній галузі. Налярну формулу, в яких атоми утворюють іншу приклад, для глікопептиду формули II, N-кінець просторову структуру, але в яких атоми інших споявляє собою положення, заміщене групами R19 і лук, так само як і атоми представленої сполуки, 20 R . однаково з'єднані між собою (наприклад, енантіо 29 75083 30 мер, діастереомер або геометричний ізомер). ДиAmer. Chem. Soc, 1996, 118, 13107-13108; J. Amer. вись наприклад, Morrison and Boyde Organic Chern. Soc, 1997, 119, 12041-12047; і J. Amer. Chemistry, 1983, 4-me вид., Allyn і Bacon, Inc., БосChem. Soc, 1994, 116, 4573-4590. Типові глікопептон, Mass., стор. 123. тиди включають також такі, що позначені якА477, Поняття "сульфонамід" стосується групи форА35512, А40926, А41030, А42867, А47934, А80407, мули -SO2NRR, в якій кожен R незалежно означає А82846, А83850, А84575, АВ-65, актапланін, активодень, алкіл, заміщений алкіл, арил, гетероарил ноїдин, ардацин, авопарцин, азуреоміцин, балхіміабо гетероцикл, де алкіл, заміщений алкіл, арил, цин, хлорорієнтеїн, хлорполіспорин, декапланін, Nгетероарил і гетероцикл мають значення, вказані в деметилванкоміцин, еремоміцин, галакардін, гельданій заявці. векардін, ізупептин, кібделін, LL-AM374, манопепПоняття "тіол" стосується групи -SH. тин, ММ45289, ММ47756, ММ47761, ММ49721, Поняття "тіоалкокси" стосується групи -SММ47766, ММ55260, ММ55266, ММ55270, алкіл. ММ56597, ММ56598, ОА-7653, орентицин, парвоПоняття "заміщений тіоалкокси" стосується дицин, рістоцетин, рістоміцин, синмоніцин, тейкопгрупи -S-заміщений алкіл. ланін, UK-68597, UK-69542, UK-72051, ванкоміцин, Поняття "тіоарилокси" стосується групи арилі т.п. Поняття "глікопептид" як тут визначено, також S-, де арильна група має значення, вказані вище, охоплює загальний клас пептидів, описаних тут, в включаючи необов'язково заміщені арильні групи, яких цукрова частина відсутня, наприклад аглікояк також визначено вище. нова група глікопептидів. Наприклад, при видаПоняття "тіогетероарилокси" стосується групи ленні дисахаридної частини, приєднаної до феногетероарил-S-, в якій гетероарильна група має лу ванкоміцину, за допомогою м'якого гідролізу значення, вказані вище, включаючи необов'язково одержують аглікон ванкоміцину. Під обсяг винахозаміщені арильні групи, як також визначено вище. ду також підпадають глікопептиди, які, крім того, Поняття "тіоефірні похідні" при застосуванні можуть приєднувати додаткові сахаридні залишки, стосується глікопептидних сполук за даним винаособливо аміноглікозиди, певною мірою подібні до ходом, включаючи тіоефіри (-S-), сульфоксиди (ванкозаміну. SO-) і сульфони (-SO2-). "Необов'язковий" або "необов'язково" означає, Для будь-якої з вищенаведених груп, яка що описані наступні події або умови можуть мати включає один або більше замісників, зрозуміло місце, а можуть не мати місця, і що опис включає звичайно, що такі групи не можуть включати будьвипадки, в яких вказані подія або умови мають яких замісників або замісних груп, просторова місце, і випадки, в яких вони не мають місця. Наструктура яких неможлива та/або синтетично неприклад, "необов'язково заміщена" означає, що здійсненна. Крім того, сполуки за винаходом вклюгрупа може бути заміщеною описаним замісником, чають всі стереохімічні ізомери, які виникають при а може не бути заміщеною описаним замісником. заміщенні цих сполук. Поняття "інертний органічний розчинник" або "Циклодекстрин" включає циклічні молекули, "інертний розчинник" або "інертний розріджувач" в даному винаході означають розчинник або розріякі містять шість або більше -D-глюкопіранозних джувач, який по суті інертний в умовах реакції, в одиниць, з'єднаних в положенні 1,4 -зв'язком як в яких він застосовується як розчинник або розріамілози. -Циклодекстрин або циклогептаамілоза джувач. Типовими прикладами речовин, які мовключають сім -D-глюкопіранозних одиниць. В жуть бути застосовані як інертні розчинники або даному винаході поняття "циклодекстрин" також розріджувачі включають, наприклад, бензол, толувключає похідні циклодекстрину, такі як гідроксипол, ацетонітрил, тетрагідрофуран ("ТГФ"), диметиропільний і сульфобутиловий ефіри циклодекстлформамід ("ДМФ"), хлороформ ("СНСІ3"), метирину. Такі похідні описані, наприклад, в патентах ленхлорид (або дихлорметан або "СН2СІ2"), US №№4,727,064 і 5,376,645. Одним з переважних діетиловий ефір, етилацетат, ацетон, метилетилциклодекстринів є гідроксипропіл -циклодекстрин, кетон, метанол, етанол, пропанол, ізопропанол, який має ступінь заміщення приблизно 4,1-5,1 за трет-бутанол, діоксан, піридин, і т.п. Якщо не вкаданими FTIR. Такий циклодекстрин можна одерзано інше, то розчинники, які застосовують в реакжати від Cerestar (Хаммонд, Індіана, США) за ім'ям ціях за даним винаходом, представляють собою Cavitron™ 82003. інертні розчинники. Глікопептид" стосується олігопептидних (наПоняття "азот-зв'язаний" або "N-зв'язаний" приклад гептапептидного) антибіотиків (дальбагеозначає групу або замісник, приєднані до залишку птидів), що характеризуються поліциклічним пепсполуки (наприклад, сполуки формули І) за допотидним ядром, необов'язково заміщеним могою зв'язку з атомом азоту групи або замісника. сахаридною групою, як наприклад ванкоміцин. Поняття "кисень-зв'язаний" означає групу або заПриклади глікопептидів, включаючи вищенаведемісник, приєднані до залишку сполуки (наприклад, не визначення, можна знайти в "Glycopeptides сполуки формули І) за допомогою зв'язку з атомом Classification, Occurrence, and Discovery", за ред. кисню групи або замісника. Поняття "сіркоRaymond С. Rao і Louise W. Crandall, ("Drugs and зв'язаний" означає групу або замісник, приєднані the Pharmaceutical Sciences" том 63, за ред. до залишку сполуки (наприклад, сполуки формули Ramakrishnan Nagarajan, опубл. Marcel Dekker, І) за допомогою зв'язку з атомом сірки групи або Inc.). Інші приклади глікопептидів описані в патензамісника. тах US №№4,639,433; 4,643,987; 4,497,802; "Фармацевтично прийнятна сіль" означає такі 4,698,327; 5,591,714; 5,840,684; і 5,843,889; в ЕР солі, які зберігають біологічну ефективність та ак0802199; ЕР 0801075; ЕР 0667353; WO 97/28812; тивність вихідних сполук і які не мають біологічно WO 97/38702; WO 98/52589; WO 98/52592; та в J. 31 75083 32 шкідливих чи інших шкідливих дій при застосовуспектру антибактеріальних агентів" або "бактеріаваних дозах. Сполуки за даним винаходом здатні льне захворювання", як використовується в даній утворювати кислотні та основні солі завдяки наявзаявці, стосується всіх хворобливих станів, які, як ності аміногрупи та карбоксильної групи відповіддобре відомо в фахівцю даній галузі, ефективно но. можуть піддаватися лікуванню за допомогою шиФармацевтично прийнятні основно-адитивні рокого спектру антибактеріальних речовин загасоді можуть бути одержані за. допомогою неоргалом, і ті хворобливі стани, для яких було встановнічних та органічних основ. Солі, утворені при лено, що вони піддаються лікуванню за допомогою взаємодії з неорганічними основами, включають, специфічних антибактеріальних речовин за даним але не обмежуючись ними, натрієві, калієві, літієві, винаходом. Такі хворобливі стани включають, але амонієві, кальцієві та магнієві солі. Солі, утворені не обмежуючись лише ними, лікування ссавців, які при взаємодії з органічними основами, включають, страждають від патогенних бактерій, зокрема від але не обмежуючись ними, солі первинних, втостафілококів (метицилін-чутливих та резистентринних та третинних амінів, заміщених амінів, них), стрептококів (пеніцилін-чутливих та резистевключаючи природних заміщених амінів, та циклінтних), ентерококів (ванкоміцин-чутливих та резичних амінів, включаючи ізопропіламін, триметиластентних), і Clostridium difficile. мін, діетиламін, триетиламін, трипропіламін, етаПоняття "терапевтично ефективна кількість" ноламін, 2-диметиламіноетанол, трометамін, стосується кількості, яка є достатньою для ефеклізин, аргінін, гістидин, кофеїн, прокаїн, гідрабамін, тивного лікування, як вказано в даній заявці, при холін, бетаїн, етилендіамін, глюкозамін, Nвведенні ссавцю, який потребує такого лікування. алкілглюкаміни, теобромін, пурини, піперазин, піТерапевтично ефективна кількість значно залеперидин і N-етилпіперидин. Також зрозуміло, що жить від суб'єкту та хворобливого стану, який підпохідні інших карбонових кислот також можуть дається лікуванню, тяжкості хвороби та способу застосовуватися при здійсненні даного винаходу, введення, і може бути визначено як загально принаприклад, аміди карбонових кислот, включаючи йнято в даній галузі. карбоксаміди, карбоксаміди нижчого алкілу, карбоПоняття "захисна група" або "блокувальна ксаміди динижчого алкілу, і т.п. група" стосується будь-якої групи, яка, коли зв'яФармацевтично прийнятні кислотно-адитивні зана з однією або декількома гідроксильними, тісолі одержують при взаємодії з неорганічними та ольними, аміно, карбоксильними або іншими груорганічними кислотами. Прийнятні солі утворюпами сполук, захищає від небажаних реакцій, в які ються при взаємодії з такими неорганічними кисможуть вступати ці групи, і ці захисні групи можуть лотами, як соляна кислота, бромистоводнева кисбути видалені за допомогою звичних хімічних або лота, сірчана кислота, азотна кислота, фосфонові ферментативних стадій з відновленням гідроксил, кислоти і т.п. Прийнятні солі утворюються при взатіо, аміно, карбокси або іншої групи. Деталі застоємодії з такими органічними кислотами, як оцтова сування деяких блокувальних груп, що вилучаютькислота, пропіонова кислота, гліколева кислота, ся, не має вирішального значення і переважні блопіровиноградна кислота, щавлева кислота, яблучкувальні групи, що вилучаються, для гідроксильної на кислота, малонова кислота, янтарна кислота, групи включають загальноприйняті замісники, такі малеїнова кислота, фумарова кислота, винна кисяк аліл, бензил, ацетил, хлорацетил, тіобензил, лота, лимонна кислота, бензойна кислота, корична бензилідин, фенацил, трет-бутил-дифенілсиліл та кислота, мигдалева кислота, метансульфонова будь-яку іншу групу, яка здатна хімічно взаємодіякислота, етансульфонова кислота, пти з функціональною гідроксильною групою і потім толуолсульфокислота, саліцилова кислота і т.п. селективно видалятися за допомогою хімічних або Сполуки за винаходом як правило, містять ферментативних способів в м'яких умовах сумісодин або декілька хіральних центрів. Таким чином, них з природою продукту. Більш докладно захисні даний винахід охоплює рацемічні суміші, діастерегрупи описані в T.W. Greene і P.G.M. Wuts, омери, ентантіомери і суміші, збагачені одним або "Protective Groups in Organic Synthesis" 3-тє вид., декількома стереоізомерами. Під обсяг винаходу, 1999, John Wiley і Sons, N.Y. як описано та заявлено, підпадають рацемічні фоПереважні блокувальні групи, що вилучаютьрми сполук, а також індивідуальні ентантіомери та ся, для аміногрупи включають загальноприйняті їх нерацемічні суміші. замісники, такі як трет-бутоксикарбоніл (трет-БОК), Поняття "лікування" як застосовується тут, бензилоксикарбоніл (КБЗ), флуоренілметоксикарвключає будь-яке лікування стану або захворюбоніл (ФМОК), алілоксикарбоніл (АЛОК) і т.п., які вання у тварини, переважно у ссавця, більш переможуть бути видалені за допомогою загальнопважно в людини, і включає: рийнятих методів, сумісних з природою продукту. (і) запобігання захворюванню або стану, що Переважні карбокси-захисні групи включають зустрічається у суб'єкта, який може мати схильскладні ефіри, такі як метиловий, етиловий, пропіність до захворювання, але це захворювання ще ловий, трет-бутиловий і подібні, які можуть бути не діагностується в нього; видалені в м'яких умовах, сумісних з природою (іі) пригнічення захворювання або стану, тобто продукту. затримування його розвитку; полегшення захво"Ванкоміцин" стосується глікопептидного анрювання або стану, тобто викликати регресію статибіотика, який має формулу: ну; або полегшення умов, які спричиняються захворюванням, тобто симптомів захворювання. Поняття "хворобливий стан, який може бути полегшений лікуванням за допомогою широкого 33 75083 34 вих (-РО3Н2) груп, можуть бути одержані взаємодією відповідної глікопептидної сполуки, яка на Скінці містить карбоксигрупу із прийнятною фосфоновмісною сполукою. Наприклад, глікопептидна сполука, в якій на С-кінці знаходиться карбоксильна група, може з'єднуватися із фосфоновмісним аміном, спиртом, або тіоловою сполукою з утворенням аміду, складного ефіру, або тіоефіру, відповідно. Наприклад глікопептидна сполука формули І, в якій R3 представляє собою азот-зв'язану частину, яка включає одну або декілька фосфонових груп, може бути одержана взаємодією відповідної глікопептидної сполуки формули І, в якій R3 означає гідроксильну групу, із необхідним фосфоновмісним аміном з утворенням сполуки формули І, в якій R3 представляє собою азот-зв'язану часПри описі похідних ванкоміцину, поняття тину, яка містить одну або декілька фосфонових "Nvan"-" вказує на те, що замісник ковалентно пригруп. єднаний до аміногрупи ванкозамінової частини Глікопептидна сполука за даним винаходом, leu ванкоміцину. Так само, поняття "N -" вказує на те, яка заміщена на С-кінці замісником, який включає що замісник ковалентно приєднаний до аміногрупи одну або декілька (наприклад 1, 2, 3, 4 або 5) фолейцинової частини ванкоміцину. сфонових (-РО3Н2) груп, і в якій ванкозаміновий Загальні схеми синтезу амінокінець (V) заміщений, може бути одержана Глікопептидні сполуки за даним винаходом внаслідок здійснення спочатку відновного алкілуможуть бути одержані з легкодоступних вихідних вання відповідної глікопептидної сполуки, в якій речовин, використовуючи представлені загальні ванкозаміновий амінокінець (V) представляє соспособи та методики. Фахівцю в даній галузі очебою вільну аміногрупу (NH2) і наступної взаємодії видно, що наведені, зокрема, типові та переважні відповідної глікопептидної сполуки із необхідною умови здіснення способів (а саме, температура фосфоновмісною сполукою (наприклад, фосфонореакції, час, молярне співвідношення компонентів вмісним аміном, спиртом або тіолом). реакції, розчинники, тиск і т.п.), але також можуть Як приклад, глікопептидна сполука, така як вабути використані інші умови здійснення способів, нкоміцин, спочатку може бути піддана відновному якщо не вказано інше. Оптимальні умови реакції алкілуванню, як показано на нижченаведеній схемі істотно відрізняються залежно від використовувареакції: них реагентів та розчинників, але такі умови можуть бути визначені фахівцем в даній галузі шляхом звичних оптимізацій методик. Крім того, як очевидно для фахівця в даній галузі, для захисту певних функціональних груп, які в якій А представляє собою Ra без одного можуть піддатися небажаному перетворенню, моатома вуглецю і Ra, Rb, Υ, Ζ і х мають значення, же знадобитися застосування загальноприйнятих вказані в даній заявці. Реакція типово відбувається захисних груп. Вибір придатних захисних груп для спочатку шляхом взаємодії одного еквіваленту певних функціональних груп, а також придатних глікопептиду, наприклад, ванкоміцину, з надлишумов захисту та видалення цих захисних груп, доком, переважно від 1,1 до 1,3 еквівалентів, необбре відомі в даній галузі. Наприклад, різноманітні хідного альдегіду в присутності надлишку, перезахисні групи, і їх введення та вилучення, описані важно приблизно 2,0 еквіваленти, третинного в Т. W. Greene та G. М. Wuts, Protecting Groups in аміну, такого як діізопропілетиламін (ДІПЕА) і т.п. Organic Synthesis, 3-тє вид, Wiley, Нью Йорк, 1999, Реакцію, як правило здійснюють в інертному розі включені в даний опис як посилання. ріджувачі, такому як ДМФ або суміші ацетонітВ наведених схемах реакції, глікопептидні рил/вода при температурі навколишнього середосполуки зображені в спрощеному вигляді як прявища впродовж 0,25-2год до того часу, поки мокутник "G", де карбоксикінець позначений як [С], утворення відповідного іміну та/або геміаміналу по ванкозаміновий амінокінець позначений як [V], суті завершиться. Утворений імін та/або геміамі"несахаридний" амінокінець (лейцинамінова часнал, як правило, не виділяють, a in situ здійснюють тина) позначений як [N], і необов'язково, резорциреакцію з відновлювальним агентом, таким як ціанова частина позначена як [R], як наведено нижче: нобогідрид натрію, боран піридину, або т.п., з одержанням відповідного аміну. Цю реакцію переважно здійснюють взаємодією іміну та/або геміаміналу з надлишком, переважно приблизно 3 еквіваленти, трифтороцтової кислоти, з подальшою взаємодією з приблизно 1-1,2 еквівалентами відновлювального агенту при температурі навколишнього середовища в метанолі або суміші ацетонітрил/вода. Утворений алкілований продукт легко може бути Глікопептидні сполуки за даним винаходом, які підданий очищенню за допомогою загальноприйзаміщені на С-кінці замісником, який включає одну нятих процедур, таких як осадження та/або РХВР або декілька (наприклад 1, 2, 3, 4 або 5) фосфоно 35 75083 36 із зворотною фазою. Несподівано було виявлено, метилморфолін або триетиламін) і т.п. що за допомогою утворення іміну та/або геміаміДля підкислення реакційної суміші може бути налу в присутності триалкіламіну, і наступного підвикористана будь-яка кислота. Придатні кислоти силення трифтороцтовою кислотою перед реакцівключають карбонові кислоти (наприклад, оцтова єю з відновлювальним агентом вдається істотно кислота, трихлороцтова кислота, лимонна кислопідвищити селективність реакції відновного алкіта, мурашина кислота або трифтороцтова кислолування, тобто відновне алкілування аміногрупи та), мінеральні кислоти (наприклад, соляна кислосахариду (наприклад, ванкозаміну) переважає над та, сірчана кислота або фосфорна кислота), і відновним алкілуванням на N-кінці (наприклад, подібні. Переважною кислотою є трифтороцтова лецинільної групи) у співвідношенні принаймні кислота. 10:1, більш переважно 20:1. Вищенаведений споПридатні відновлювальні агенти для здійсненсіб має істотні переваги в порівнянні з попередніми ня способу відновного алкілування добре відомі в способами селективного алкілування аміносахаданій галузі. Будь-який приданий відновлювальний ридної групи глікопептидного антибіотика. агент може бути використаний в способах за винаТаким чином, даний винахід також забезпечує ходом, за умови, що він сумісний з функціональспосіб алкілування глікопептиду, що містить аміними групами, присутніми в глікопептиді. Наприносахаридну групу, який передбачає: клад, придатні відновлювальні агенти включають об'єднання альдегіду або кетону, прийнятної ціаноборогідрид натрію, триацетоксиборогідрид основи і глікопептиду для одержання реакційної натрію, піридин/боран, борогідрид натрію і борогісуміші; дрид цинку. Відновлення також може відбуватися підкислення реакційної суміші; і в присутності каталізаторів перехідних металів об'єднання реакційної суміші з прийнятним ві(наприклад, паладію або платини) в присутності дновлювальним агентом для забезпечення глікоджерела водню (наприклад, водневого газу або пептиду, в якому алкілованою є сахаридамінна циклогександієну). Дивись наприклад, Advanced група. Переважно, глікопептид включає принаймні Organic Chemistry, 4-те вид., John Wiley & Sons, одну аміногрупу, іншу, ніж сахаридна аміногрупа. Нью Йорк (1992), 899-900. Переважно, відновне алкілування сахаридної Похідні глікопептиду, які утворюються при відаміногрупи переважає над відновним алкілуванновному алкілуванні, потім можуть піддаватися ням інших аміногруп глікопептиду при співвідновзаємодії із фосфоновмісним аміном (R3-H) з шенні принаймні приблизно 10:1; і більш переважутворенням амідного зв'язку. Ця реакція пояснюно, принаймні приблизно 15:1 або приблизно 20:1. ється нижченаведеною схемою: Спосіб відновного алкілування за винаходом, як правило, можна здійснювати в присутності придатного розчинника або суміші розчинників, таких як, наприклад, галогенований вуглеводень (наприклад, метиленхлорид), лінійний або розгалужений ефір (наприклад, діетиловий ефір, тетрагідрофуран), ароматичний вуглеводень (наприклад, бенде R3 означає азот-зв'язану групу, яка включає зол або толуол), спирт (метанол, етанол або ізоподну або декілька фосфонових груп. В цій реакції, ропанол), диметисульфоксид (ДМСО), Ν,Νпохідне глікопептиду, як правило, піддають взаєдиметилформамід, ацетонітрил, вода, 1,3модії з аміном в присутності пептид-зв'язувального диметил-3,4,5,6-тетрагідро-2(1Н)-піримідон, тетреагента, такого як РуВОР і HOBT, з утворенням раметилсечовина, Ν,Ν-диметилацетамід, діетиламіду. Ця реакція, як правило, відбувається в інерформамід (ДМФ), 1-метил-2-піролідинон, тетраметному розріджувачі, такому як ДМФ, при температиленсульфоксид, гліцерин, етилацетат, турі в діапазоні від приблизно 0°С до приблизно ізопропілацетат, Ν,Ν-диметилпропіленсечовина 60°С впродовж від 1 до 24год або поки реакція (ДМПС) або діоксан. Переважно алкілування здійсполучення не буде по суті завершена. Подальше снюють в суміші ацетонітрил/вода, або видалення захисних груп здійснюється з викорисДМФ/метанол. танням загальноприйнятих способів та реагентів, Переважно відновлення (тобто обробку віднощо дозволяє одержати сполуки за даним винаховлювальним агентом) здійснюють в присутності дом. протонного розчинника, такого як, наприклад, При необхідності, стадію взаємодії з аміном, спирт (наприклад метанол, етанол, пропанол, ізоописану вище, можна здійснювати спочатку з одепропанол або бутанол), вода, або т.п. ржанням аміду, а потім здійснювати відновне алкіСпосіб відновного алкілування за винаходом лування і видалення захисних груп, що дозволяє можна здійснювати при будь-якій прийнятній темодержати сполуки за винаходом. пературі від температури замерзання до темпераПри необхідності, глікопептидні сполуки за датури флегми реакційної суміші. Переважно реакція ним винаходом також можуть бути одержані поевідбувається в діапазоні від приблизно 0°С до тапним способом, при якому спочатку попередник приблизно 100°С. Більш переважно в діапазоні від групи -Ra-Y-Rb-(Z)x за допомогою відновного алкіприблизно 0°С до приблизно 50°С, або в діапазоні лування приєднують до глікопептиду, а потім здійвід приблизно 20°С до приблизно 30°С. снюють подальшу переробку приєднаного попереВ способі відновного алкілування за винаходника з використанням загальноприйнятих дом може бути використана будь-яка прийнятна реагентів та способів для одержання -Ra-Y-Rb-(Z)x основа. Прийнятні основи включають третинні амігрупи. Крім того, в вищенаведеному способі віднони (наприклад, діізопропілетиламін, N 37 75083 38 вного алкілування можуть бути використані кетони фонозаміщені аміни, спирти, або тіоли) є комердля одержання а-заміщених амінів. ційно доступними, або можуть бути одержані, виБудь-який глікопептид, який має аміногрупу, користовуючи комерційно доступні вихідні матеріможе бути підданий описаним реакціям відновного али і загальноприйняті реагенти. Дивись, алкілування. Такі глікопептиди є добре відомими в наприклад, Advanced Organic Chemistry, Jerry даній галузі і вони є комерційно доступними або March, 4-me вид., 1992, John Wiley і Sons, Нью можуть бути одержані з використанням загальнопЙорк, стор. 959; і Frank R. Hartley (ред.) The рийнятих методів. Прийнятні глікопептиди описані, Chemistry of Organophosphorous Compounds, том. наприклад, в патентах US №№3,067,099; 1-4, John Wiley і Sons, Нью Йорк (1996). Аміноме3,338,786; 3,803,306; 3,928,571; 3,952,095; тилфосфонова кислота є комерційно доступною 4,029,769; 4,051,237; 4,064,233; 4,122,168; від Aldrich Chemical Company, Мілуокі, Вісконсін. 4,239,751; 4,303,646; 4,322,343; 4,378,348; Додаткові аспекти та інші способи одержання 4,497,802; 4,504,467; 4,542,018; 4,547,488; сполук за даним винаходом описані в нижченаве4,548,925; 4,548,974; 4,552,701; 4,558,008; дених прикладах. 4,639,433; 4,643,987; 4,661,470; 4,694,069; Фармацевтичні композиції 4,698,327; 4,782,042; 4,914,187; 4,935,238; Даний винахід також стосується фармацевти4,946,941; 4,994,555; 4,996,148; 5,187,082; чної композиції, яка містить нові глікопептидні спо5,192,742; 5,312,738; 5,451,570; 5,591,714; луки за винаходом. Відповідно, глікопептидна спо5,721,208; 5,750,509; 5,840,684; і 5,843,889. Перелука, переважно у вигляді фармацевтично важно, глікопептид, який застосовується у вищеприйнятної солі, може застосовуватись для перовикладеній реакції, представляє собою ванкомірального або парентерального введення для тецин. рапевтичного або профілактичного лікування бакЯк показано на нижченаведеній схемі, фосфотеріальних інфекцій. новмісний аміноалкільний боковий ланцюг резорНаприклад, глікопептидна сполука може зміцинової частини глікопептиду, такого як ванкомішуватися із загальноприйнятими фармацевтичницин, може бути підданий реакції Манніха (Mannich) ми носіями і наповнювачами і застосовуватися у (на цій схемі для наочності зображена резорциновигляді таблеток, капсул, еліксирів, суспензій, сива частина глікопептиду). В цій реакції амін форропів, облаток, і т.п. Такі фармацевтичні композимули NHRR1 (де одна або обидві R і R' групи ознації можуть містити від приблизно 0,1 до приблизно чають групи, що включають одну або декілька 90% за масою активної сполуки, і більш переважно фосфонових груп), і альдегід (наприклад СН2О), від приблизно 10 до приблизно 30%. Фармацевтитакий як формалін (джерело формальдегіду), підчні композиції можуть містити звичайні носії і надаються реакції з глікопептидом в лужним умовах повнювачі, такі як кукурудзяний крохмаль або жез утворенням похідного глікопептиду. латин, лактоза, сахароза, мікрокристалічна целюлоза, каолін, маніт, дикальційфосфат, хлорид натрію і альгінова кислота. Агенти дезінтеграції, які звичайно застосовуються в композиціях за даним винаходом, включають кроскармелозу, мікрокристалічну целюлозу, кукурудзяний крохмаль, гліколят крохмалю натрію і альгінову кислоту. Рідка композиція в основному включає суспенСполуки за винаходом, які містять сульфоксид зію або розчин сполуки або фармацевтично приабо сульфон, можуть бути одержані із відповідних йнятної солі в прийнятному рідному носії(ях), натіосполук, використовуючи загальноприйняті реаприклад, етанолі, гліцерині, сорбітолі, неводному генти та способи. Придатні реагенти для окисленрозчиннику, такому як поліетиленгліколь, маслах ня тіосполук до сульфоксиду включають, наприабо воді, необов'язково із суспендувальним агенклад, перекис водню, перкислоти, такі як 3том, солюбілізувальним агентом (таким як циклохлорпероксибензойна кислота (МХПВК), перйодат декстрин), консервантом, поверхнево-активною натрію, хлорит натрію, гіпохлорит натрію, гіпохлоречовиною, змочувальною речовиною, ароматизарит кальцію, mpem-бутил гіпохлорит і подібні. Хітором або барвником. Альтернативно, рідка комральні окисні реагенти (оптично активні реагенти) позиція може бути одержана із здатного до розбатакож можуть застосовуватися для одержання влення порошку. хіральних сульфоксидів. Такі оптично активні реаНаприклад, порошок, який містить активну генти добре відомі в даній галузі й включають, сполуку, суспендувальний агент, сахарозу і підсонаприклад, реагенти, описані в Кагена (Kagen) та лоджувач може бути відновлений водою із утвоін., Synlett, 1990, 643-650. ренням суспензії; і сироп може бути одержаний із Альдегіди та кетони, які можуть використовупорошку, який містить активний компонент, сахаватися в викладених реакціях відновного алкілурозу та підсолоджувач. вання, також добре відомі в даній галузі і вони є Композиція у вигляді таблетки може бути прикомерційно доступними або можуть бути одержані, готовлена, використовуючи будь-який прийнятний використовуючи комерційно доступні вихідні матефармацевтичний носій(ї), які звичайно застосовуріали і загальноприйняті реагенти (наприклад, диються для одержання твердих композицій. Приквись March, Advanced Organic Chemistry, 4-те вид., лади таких носіїв включають стеарат магнію, кроJohn Wiley & Sons, Нью Йорк (1992), і посилання, хмаль, лактозу, сахарозу, мікрокристалічну наведені там). целюлозу і зв'язуючі, наприклад полівінілпіроліФосфонозаміщені сполуки (наприклад, фосдон. Таблетки також можна одержати при викори 39 75083 40 станні покриття кольоровою плівкою, або барвниним винаходом представлені у вигляді ліофілізока, включеного як частина носія(їв). Крім того, акваного порошку, який містить циклодекстрин, або у тивна сполука може входити до складу дозованої вигляді стерильного порошку, який містить циклоформи з контрольованим вивільненням такої, як декстрин. Переважно, циклодекстрин представляє наприклад, таблетка, яка містить гідрофільну або собою гідроксипропіл- -циклодекстрин або сульгідрофобну основу. фобутиловий ефір -циклодекстрину; більш переКомпозиція у вигляді капсули може бути приважно, циклодекстрин представляє собою гідрокготовлена, використовуючи загальноприйняті месипропіл-р-циклодекстрин. Як правило, ін'єкційний тодики капсулювання, наприклад шляхом введенрозчин може включати циклодекстрин у кількості ня активної сполуки та наповнювачів в тверду приблизно 1-25мас. %; переважно приблизно 2желатинову капсулу. Альтернативно, напівтверда 10мас. %; більш переважно приблизно 4-6мас. % основа активної сполуки і високомолекулярний від маси композиції. Крім того, масове співвіднополіетиленгліколь можуть бути підготовлені і ними шення циклодекстрину до похідного глікопептиду заповнюють тверду желатинову капсулу; або розпереважно може знаходитися в інтервалі від причин активної сполуки в поліетиленгліколі або сублизно 1:1 до приблизно 10:1. спензія в харчовій олії, наприклад, рідкому параСполуки за винаходом і їх фармацевтично фіні або фракціонованій кокосовій можуть бути прийнятні солі, які проявляють активність при рекпідготовлені і ними заповнюють м'яку желатинову тальному введенні, можуть бути представлені у капсулу. вигляді супозиторіїв. Як правило, супозиторії моЗв'язуючі речовини для таблеток можуть жуть складатися в основному з активного комповключати гуміарабік, метилцелюлозу, натрійкарбоненту, зв'язуючого та/або змащувального агента, ксиметилцелюлозу, полівінілпіролідон (Повідон), такого як желатин або какаова олія або нижчі плагідроксипропілметилцелюлозу, лактозу, крохмаль і вкі рослинні олії або синтетичні воски або жири. етилцелюлозу. Змащувальні речовини, які можуть Сполуки за даним винаходом та їх фармацевзастосовуватися, включають стерат магнію або тично прийнятні солі, які є активними при місцевостеарати інших металів, стеаринову кислоту, крему застосування, можуть бути представлені у вимнійорганічну рідину, тальк, воски, масла і колоїдгляді трансдермальних композицій або пристроїв ний кремнезем. для трансдермального введення ("пластирів"). Такі Ароматизуючі речовини, такі як м'ятна олія, композиції включають, наприклад, основу, ємність олія зимолюбки, вишневі ароматизатори або подіз активним компонентом, регульовану мембрану, бні, також можуть застосовуватися. Крім того, мообкладку і контактний клей. Такі трансдермальні же бути бажаним застосувати барвник для наданпластирі можуть застосовуватися для безперервня дозованій формі привабливості або полегшення ного або переривчастого введення сполук за даідентифікації продукту. ним винаходом в контрольованих кількостях. БуСполуки за винаходом і їх фармацевтично дова та застосування пластирів для доставки прийнятні солі, які стають активними при парентефармацевтичних речовин добре відомі в даній ральному введені, можуть застосовуватися для галузі. Дивись, наприклад, патент US №5,023,252, внутрішньом'язового, внутрішньооболонкового або виданий 11 липня 1991р. Такі пластирі можуть внутрішньовенного введення. бути придатними для безперервного, пульсуючого Типові композиції для внутрішньом'язового або залежного від пристрою введення фармацевабо внутрішньооболонкового введення можуть тичних речовин. включати суспензію або розчин активного компоАктивна сполука є ефективною в широкому діненту в олії, наприклад, арахісовій олії або кунжуапазоні дозі і в основному вводиться в фармацевтній олії. Типові композиції для внутрішньовенного тично ефективній кількості. Однак очевидно, що або внутрішньооболонкового введення можуть кількість сполуки, що вводиться, визначається включати стерильний ізотонічний водний розчин, лікарем, враховуючи суттєві обставини, такі як який містить, наприклад активний компонент і декстан, який підлягає лікуванню, вибраний шлях строзу або хлорид натрію, або суміш декстрози та введення, конкретну сполуку, яка вводиться, та її хлориду натрію. Іншими прикладами можуть бути відносну активність, вік, вагу, індивідуальну чутлилактатний розчин Рінгера для ін'єкцій, лактатний вість пацієнта, тяжкість наявних у пацієнта симпрозчин Рінгера плюс декстроза для ін'єкцій, Нортомів і подібне. мосол-М і декстроза, Ізоліт Е, ацилований розчин Прийнятні дози знаходяться в основному в інРінгера для ін'єкцій і подібні. Необов'язково мотервалі 0,01-100мг/кг на добу, переважно 0,1жуть застосовуватися в композиціях також співро50мг/кг на добу. Для середньої людини вагою 70кг зчинники, наприклад, поліетиленгліколь; хелатоуттака кількість сполуки може становити від 0,7мг до ворювачі, наприклад, етилендіамінтетраоцтова 7г на добу, або переважно від 7мг до 3,5г на добу. кислота; солюбілізувальний агент, наприклад, циБільш переважно доза для людини становить від клодекстрин; і антиоксиданти, наприклад, метабіприблизно 500мг до приблизно 2г на добу. сульфіт натрію. Крім того, розчин може бути підІнші придатні склади для застосування за даданий сублімаційному сушінню і потім відновлений ним винаходом можна знайти в Remington's за допомогою прийнятного розчинника безпосереPharmaceutical Sciences, Mace Publishing дньо перед введенням. Company, Філадельфія, PA, 17-те вид. (1985). В переважному втіленні похідні глікопептиду Нижченаведені приклади ілюструють характеза даним винаходом представлені у вигляді воднорні фармацевтичні композиції за даним винахого розчину, який містить циклодекстрин. В іншому дом. переважному втіленні похідні глікопептиду за даТехнологія приготування лікарського засобу 41 75083 42 Приклад А Цей приклад ілюструє одержання харадопомогою 200мл розчину для внутрішньовенного ктерної фармацевтичної композиції сполуки за введення, який сумісний з активною сполукою. Такі даним винаходом для перорального введення: розчини вибирають із 5% розчину декстрози, 0,9% Компоненти Кількість на одну хлориду натрію або суміші 5% декстрози і 0,9% таблетку, мг хлориду натрію. Прикладами іншим розчинів є активна сполука 200 лактатний розчин Рінгера для ін'єкцій, лактатний лактоза, розпилюваний розчин Рінгера плюс 5% декстроза для ін'єкцій, порошок 148 Нормосол-М і 5% декстроза, Ізоліт Ε і ацилований стеарат магнію 2 розчин Рінгера для ін'єкцій. Вищевказані компоненти змішують та вносять Технологія приготування лікарського засобу у желатинові капсули з твердою оболонкою. Приклад Ε Технологія приготування лікарського засобу Цей приклад ілюструє одержання характерної Приклад Б фармацевтичної композиції, яка містить сполуку за Цей приклад ілюструє одержання іншої харакданим винаходом терної фармацевтичної композиції сполуки за даРозчин для ін'єкцій готують із нижченаведеної ним винаходом для перорального введення: композиції: Компоненти Компоненти Кількість на одну таблетактивна сполука 0,1-5,0г ку, мг гідроксипропіл- -циклодекстрин 1-25г активна сполука 400 5% водний розчин декстрози (стеq.s. до кукурудзяний крохрильний) 100мл маль 50 Вищевказані компоненти змішують і pH розчилактоза 145 ну доводять до 3,5±0,5; використовуючи 0,5н. НСІ стеарат магнію 5 або 0,5н. NaOH. Вищевказані компоненти ретельно змішують і Технологія приготування лікарського засобу пресують у окремі таблетки із насічками. Приклад Є Технологія приготування лікарського засобу Цей приклад ілюструє одержання характерної Приклад В фармацевтичної композиції, яка містить сполуку за Цей приклад ілюструє одержання характерної даним винаходом. фармацевтичної композиції сполуки за даним виЗаморожений розчин, придатний для ін'єкцій, находом для перорального введення: готують із нижченаведеної композиції: Пероральна суспензія приготовлена з нижчеЗаморожений розчин наведеної композиції. активна сполука 250мг-1000мг Компоненти гідроксипропіл- активна сполука 1,0г циклодекстрин 250мг-10г фумарова кислота 0,5г наповнювачі, наприклад, декхлорид натрію 2,0г строза 0-50г метилпарабен 0,1г вода для ін'єкцій 10-100мл гранульований цукор 25,5г Співвідношення за масою між гідроксипропілсорбітол (70% розчин) 12,85г р-циклодекстрином і активною сполукою, як праVeegum К (Vanderbilt Co.) 1,0г вило, становить від приблизно 1:1 до приблизно ароматизатор 0,035мл 10:1. барвники 0,5мг Спосіб приготування: Гідроксипропіл- дистильована вода q.s. до 100мл циклодекстрин і наповнювачі, за наявності, розчиТехнологія приготування лікарського засобу няють у приблизно 80% води для ін'єкцій, додають Приклад Γ активну сполуку та розчиняють. pH доводять до Цей приклад ілюструє одержання характерної 4,7±0,3 за допомогою 1Μ гідроксиду натрію та пофармацевтичної композиції, яка містить сполуку за тім об'єм розчину доводять до 95% кінцевого об'єданим винаходом. му за допомогою води для ін'єкцій. Перевіряють Розчин для ін'єкцій при використанні буфера pH та, за необхідності, корегують, і об'єм розчину для доведення pH до 4 готують із нижченаведеної доводять до кінцевого водою для ін'єкцій. Склад композиції: потім стерилізують, пропускаючи через фільтр Компоненти 0,22 мікрон та поміщають в стерильні флакони в активна сполука 0,2г асептичних умовах. Флакони закупорюють, мітять буферний розчин ацетату ната заморожують для зберігання. трію (0,4М) 2,0мл Технологія приготування лікарського засобу НСІ (1н.) q.s. до pH 4 Приклад Ж вода (дистильована, стерильна) q.s. до 20мл Цей приклад ілюструє одержання характерної Технологія приготування лікарського засобу фармацевтичної композиції, яка містить сполуку за Приклад Д даним винаходом. Ліофілізований порошок, приЦей приклад ілюструє одержання характерної датний для одержання розчину для ін'єкцій, готуфармацевтичної композиції сполуки за даним виють з композиції наступного складу: находом для ін'єкцій. Ліофілізований порошок Відновлений розчин готують шляхом додаванактивна сполука 250мг-1000мг ня 20мл стерильної води до 1г сполуки за винахогідроксипропіл- дом. Перед застосуванням розчин розводять за циклодекстрин 250мг-10г 43 75083 44 наповнювачі, наприклад, маніПриклад І тол, Цей приклад ілюструє одержання характерної сахароза та/або лактоза 0-50г фармацевтичної композиції для місцевого введенбуферна речовина, наприклад, ня сполуки за даним винаходом. цитрат 0-500мг Компоненти г активна сполука 0,2-10 Масове співвідношення гідроксипропіл- спан 60 2 циклодекстрину та активної речовини, як правило, твін 60 2 становить, від приблизно 1:1 до приблизно 10:1. мінеральне масло 5 Спосіб приготування: Гідроксипропіл-рвазелін 10 циклодекстрин, наповнювачі та/або буферні речометилпарабен 0,15 вини, за необхідності, розчиняють в 60% води для пропілпарабен 0,05 ін'єкцій. Додають активну сполуку, розчиняють та БГА (бутилований гідроксианізол) 0,01 pH розчину доводять до 4,0-5,0 за допомогою 1Μ вода q.s. до 100 гідроксиду натрію і об'єм розчину доводять до 95% Всі вищенаведені компоненти, окрім води, від кінцевого об'єму за допомогою води для ін'єкоб'єднують та нагрівають до 60°С при перемішуцій. Перевіряють pH і, за необхідності, корегують, і ванні. Потім при 60°С додають достатню кількість об'єм розчину доводять до кінцевого водою для води при інтенсивному перемішуванні для перетін'єкцій. Потім композицію стерилізують, пропусворення компонентів в емульсію, і потім додають каючи через фільтр 0,22 мікрони і поміщають у воду q.s. до 100г. флакони в асептичних умовах. Потім склад піддаТехнологія приготування лікарського засобу ють сублімаційному сушінню, використовуючи Приклад К придатний ліофілізаційний процес. Флакони закуЦей приклад ілюструє одержання характерної порюють (необов'язково при низькому вакуумі або фармацевтичної композиції, яка містить сполуку за зневодненні азотом), мітять і зберігають при кімнаданим винаходом. тній температурі або при охолодженні. Супозиторії загальною масою 2,5 грами готуТехнологія приготування лікарського засобу ють із нижченаведеного складу: Приклад З Компоненти Цей приклад ілюструє одержання характерної активна сполука 500мг фармацевтичної композиції, яка містить сполуку за Вітерсол Н-15* до рівноваги даним винаходом. Стерильний порошок, придат(*тригліцериди насичених рослинних жирних ний для одержання ін'єкційного розчину, одержукислот; продукт компанії Riches-Nelson, Inc., Нью ють із композиції наступного складу: Йорк, Ν.Υ.) Стерильний порошок Переважною активною сполукою для введенактивна сполука 250мг-1000мг ня згідно із А-К є сполука 11, або її фармацевтично гідроксипропіл- -циклодекстрин 250мг-10г1 прийнятна сіль (наприклад гідрохлорид). наповнювачі необов'язково Використання Масове співвідношення гідроксипропіл- Глікопептидні сполуки за даним винаходом та циклодекстрину та активної речовини, як правило, їх фармацевтично прийнятні солі, є корисними в становить, від приблизно 1:1 до приблизно 10:1. медицині і проявляють біологічну активність, Спосіб приготування: Гідроксипропіл- включаючи антибактеріальну активність, що може циклодекстрин і активну сполуку (або будь-які набути продемонстровано з використанням тестів, повнювачі) диспергують в прийнятній стерильній наведених тут нижче. Такі тести є добре відомі ємкості і ємкість запаюють (необов'язково при нифахівцям в даній галузі і описані в Lorian зькому вакуумі або зневодненні азотом), мітять і "Antibiotics in Laboratory Medicine", 4-те вид., зберігають при кімнатній температурі або при охоWilliams і Wilkins (1991). лодженні. Таким чином, даний винахід забезпечує споВведення пацієнту приготованих складів Ж соби лікування бактеріальних або інфекційних зата З хворювань, особливо таких, які викликані грамФармацевтичні композиції, описані вище в позитивними мікроорганізмами. Сполуки за даним прикладах приготування Ж та З можуть бути ввевинаходом є особливо корисними для лікування дені внутрішньовенно пацієнту медичним персоінфекцій, викликаних метицилін-резистентними налом для лікування або запобігання грамстафілококами. Також ці сполуки корисні для лікупозитивним інфекціям. Для введення вищенавевання інфекцій, викликаних ентерококами, вклюдені склади можуть бути відновлені та/або розчичаючи ванкоміцин-резистентні ентерококи (VRE). нені в розчиннику, такому як 5% декстроза або Приклади таких захворювань включають тяжкі стерильному фізіологічному розчині, як вказано інфекції, викликані стафілококами, такі як стафілонижче: кокові ендокардити і стафілококовий сепсис. ТваСпосіб приготування: Ліофілізований порошок рини, які піддаються лікуванню, можуть бути або відповідно до складу із прикладу Ж (наприклад, інфіковані мікроорганізмом або сприйнятливі до який містить 1000мг активної сполуки) розчиняють впливу мікроорганізму. Спосіб лікування, як прав 20мл стерильної води і утворений розчин згодом вило, включає введення тварині кількості сполуки розчиняють в 80мл стерильного фізіологічного за даним винаходом, яка є ефективною для цієї розчину в 100мл флаконі для ін'єкцій. Отриманий цілі. розчин потім можна вводити внутрішньовенно паНа практиці для здійснення цього способу анцієнту впродовж 30-120хв. тибіотик може вводитися у вигляді одиничної щоТехнологія приготування лікарського засобу 45 75083 46 денної дози або декілька разів на день. Курс лікуДо суміші ванкоміцину (1екв.) і бажаного альвання може займати тривалий період часу, напридегіду (1,3екв.) в ДМФ додавали ДІПЕА (2екв.). клад, декілька днів або від одного до шести тижнів. Реакційну суміш перемішували при температурі Кількість введеної дози або загальна кількість навколишнього середовища впродовж 1-2год і сполуки на курс лікування істотно залежить від контролювали за допомогою РХВР зі зворотною таких чинників, як природа та тяжкість інфекції, вік фазою. До розчину додавали метанол і NaCNBH3 та загальний стан здоров'я пацієнта, толерантність (1екв.), і після цього додають ТФО (3екв.). Перепацієнта до антибіотика та мікроорганізму чи мікмішування продовжували при температурі навкороорганізмів при перебігу інфекційного захворюлишнього середовища впродовж додаткової годивання. Переважно сполуки за винаходом вводятьни. Після завершення реакції метанол видаляли ся внутрішньовенно. під вакуумом. Залишок осаджували в ацетонітрилі. Серед інших властивостей глікопептидних При фільтрації одержували продукт, який потім сполук за винаходом слід відзначити їх знижену очищали за допомогою РХВР зі зворотною фазою. токсичність при введенні ссавцям. Наприклад, При необхідності, інші глікопептидні антибіотики фосфонозаміщені похідні за винаходом характеможна одержувати за цією методикою. ризуються зниженим накопиченням в печінці Загальна методика Б та/або нирках в порівнянні із фосфоноСинтез 2-(децилтіо)ацетальдегіду незаміщеними сполуками. Крім того, певні сполуки До суспензії карбонату кальцію (27г, за даним винаходом, як припускають, мають зме200ммоль) в ацетоні (100мл) в атмосфері азоту ншену нефротоксичність. Крім того, було виявледодавали децилбромід (10мл, 50ммоль) і меркапно, що при додаванні циклодекстрину до фарматоетанол (4,4мл, 63ммоль). Суспензію перемішуцевтичної композиції, яка містить глікопептидні вали при кімнатній температурі впродовж 2 днів, сполуки за даним винаходом, додатково знижуєтьпотім розподіляли між водою та 80%-ним гекся нефтротоксичність та/або накопичення в тканисан/етилацетатом. Органічну фазу промивали 2н. нах глікопептидних сполук при їх введенні ссавгідроксидом натрію, сушили над сульфатом магцям. нію, і леткі компоненти видаляли під вакуумом з Нижченаведені приклади синтезу та біологічні одрежанням 2-(децилтіо)етанолу (10,2г, 47ммоль) приклади служать для ілюстрації даного винаходу у вигляді забарвленої рідини, яку потім піддавали і ніяким чином не обмежують обсяг даного винаочищенню. ходу. В атмосфері азоту 2-(децилтіо)етанол (50г, Приклади 230ммоль), Ν,Ν-діізопропілетиламін (128мл, В нижченаведених прикладах представлені 730ммоль) і метиленхлорид (400мл) охолоджують скорочення мають нижченаведені значення. Будьдо -40°С. Через 15 хвилин до цього розчину додаякі скорочення, що не охарактеризовані окремо, ють розчин сірка-триоксид-піридиновий комплекс вживаються в їх загальноприйнятих значеннях. (116г, 730ммоль) в диметисульфоксиді (600мл) і Якщо не вказано інше, вся температура наведена метиленхлориді (200мл). Після цього суміш перев градусах Цельсія. мішують ще впродовж 15хв при -40°С, потім додаАЦН = ацетонітрил ють 600мл льодяної води. Суміш видаляють з БОК, охолоджуваної бані, додають 1л води, розчини = трет-бутоксикарбоніл Бок розподіляють. Органічну фазу промивають 1л 1н. ДІБАЛсоляної кислоти і висушують над сульфатом маг= гідрид діізобутилалюмінію Η нію. При фільтрації одержують 600мл рідини, які ДІПЕА = діізопропілетиламін розчиняють в 600мл гексану і пропускають через ДМФ = N,N-диметилформамід 200мл кремнезему. Кремнезем промивають 100мл ДМСО = диметисульфоксид 50% метиленхлориду/гексану, потім 300мл метиекв. = еквівалент ленхлориду. Об'єднані органічні сполуки концентEtOAc = етилацетат рують у вакуумі з одержанням 2Фмок = 9-флуоренілметоксикарбоніл (децилтіо)ацетальдегіду (48г, 220ммоль) у вигляді HOBT = гідрат 1-гідроксибензотіазолу забарвленої рідини, що може використовуватись Me = метил без подальшого очищення. MS = мас-спектроскопія Загальна методика В гексафторфосфат бензотриазол-1Синтез Nvan-2-(децилтіо)етил ванкоміцину РуВОР = ілокситрис(піролідино)фосфонію Методика А: В атмосфері азоту до гідрату гід2,2,6,6-тетраметилпіперидинілокси, вірохлориду ванкоміцину (1г, 0,64ммоль) додають 2ΤΕΜΠΟ = льний радикал (децилтіо)ацетальдегіду (139мг, 0,64ммоль) в N,NТФО = трифтороцтова кислота диметилформаміді (8мл). Додають N,NТГФ = тетрагідрофуран діізопропілетиламіну (336мкл, 1,9ммоль) і суспенТШХ, зію ретельно перемішують впродовж 2,5год до = тонкошарова хроматографія тшх розчинення всього ванкоміцину. Додають твердий У нижченаведених прикладах напівгідрат гідціаноборогідрид натрію (60мг, 0,96ммоль), а потім рохлориду ванкоміцину одержували від Alpharma, додають метанол (5мл) та трифтороцтову кислоту Inc. Fort Lee, NJ 07024 (Alpharma AS, Осло, Норве(250мкл, 3,2ммоль). Реакційну суміш перемішують гія). Інші реагенти є доступними від Aldrich впродовж 55хв. при кімнатній температурі і аналіChemical Co., Мілуокі, WI53201. зують за допомогою РХВР зі зворотною фазою. Загальна методика А Відновне алкілування Розподіл продуктів здійснюють на основі УФванкоміцину абсорбції при 280нм як наведено нижче: Час елюції (хв) 2,0 47 Площа, % 29 Продукт ванкоміцин Nvan-23,1 50 (децилтіо)етил ванкоміцин 3,2 2 ------Nleu-23,9 7 (децилтіо)етил ванкоміцин Nvan, Nleu-біс-[213 (децилтіо)етил] ванкоміцин 4,0 0,5 ------Методика Б: В атмосфері азоту до розчину 2(децилтіо)ацетальдегіду (неочищений, 48г, 220ммоль) в N,N-диметилформаміді (1,4л) додають твердий гідрат гідрохлориду ванкоміцину (173г, 110ммоль), і потім додають N,Nдіізопропілетиламін (58мл, 330ммоль). Суспензію ретельно перемішують при кімнатній температурі впродовж 2год до повного розчинення всього ванкоміцину, потім додають трифтороцтову кислоту (53мл, 690ммоль). Потім розчин перемішують впродовж 90хв, і додають твердий ціаноборогідрид натрію (10,5г, 170ммоль) та метанол (800мл). Через 3год реакційну суміш аналізують за допомогою РХВР зі зворотною фазою. Розподіл продуктів здійснюють на основі УФ-абсорбції при 280нм як наведено нижче: Час елюції (хв) Площа, % Продукт 2,0 15 ванкоміцин Nvan-23,2 77 (децилтіо)етил ванкоміцин 3,3 3 ------Nleu-23,4 0,5 (децилтіо)етил ванкоміцин Nvan, Nleu-біс-[24.0 0,8 (децилтіо)етил] ванкоміцин 4,1 4 ------Реакційну суміш для кожної з вищевикладених методик розливають у воду (7л), одержуючи трохи каламутний розчин. pH розчину доводять до 5 за допомогою насиченого бікарбонату натрію, одержуючи склад у вигляді білого осаду. Цей осад збирають за допомогою фільтрації, промивають водою, потім етилацетатом і висушують під вакуумом з одержанням Nvan-2-(децилтіо)етил ванкоміцину, який можна використовувати без подальшого очищення. Методика В: Розчин гідрохлориду ванкоміцину (3,0г, 2,1ммоль) в АЦН/Н2О (1:1, 30мл) обробляють із діізопропілетилааміном (0,54г, 0,72мл, 4,2ммоль), і потім 2-(децилтіо)ацетальдегідом (0,91г, 4,2ммоль) при 25°С. Через 30хв реакційну суміш обробляють ТФО (1,92г, 1,29мл, 16,8ммоль), і потім NaCNBH3 (0,132г, 2,1ммоль). Через 5-10хв van неочищений продукт N -2-(децилтіо)етил ванкоміцин виділяють за допомогою ацетонітрилу (300мл). Приклад 1 Одержання сполуки 3 (Формула II, в якій R3 означає N(фосфонометил)-аміно; R5 означає водень; R19 75083 48 означає водень, і R20 означає -CH2CH2-S(СН2)9СН3) NVAN-(2-децилтіо)етил ванкоміцин бістрифторацетат (1г, 0,53ммоль) і діізопропілетиламін (0,23мл, 1,33ммоль) об'єднували в ДМФ (10мл) і перемішували до однорідності. Потім до реакційної суміші додавали HOBt (0,080г, 0,58ммоль) і PYBOP (0,300г, 0,58ммоль). Через 5-10хв додавали однорідний розчин, який містить (амінометил)фосфонову кислоту (0,060г, 0,53ммоль) і діізопропілетиламіну (0,23мл, 1,33ммоль) у воді (3мл). Реакційну суміш перемішували при кімнатній температурі і контролювали за допомогою MS. Після того, як реакція завершилася, реакційну суміш розчиняли в ацетонітрилі (40мл) і цетрифугували. Супернатант відкидали, утворений осад, який містить потрібний продукт, розчиняли в 50%-ному водному ацетонітрилі (10мл) і очищали за допомогою РХВР із зворотною фазою з одержанням вказаної в заголовку сполуки. MS: обчислено (М+) 1742,7; знайдено (МН+) 1743,6. Приклад 2 Одержання сполуки 11 (Формула II, в якій R3 означає -ОН; R5 означає N-(фосфонометил)-амінометил; R19 означає водень, і R20 означає -СН2СН2-NН-(СН2)9СН3) (Амінометил)фосфонову кислоту (3,88г, 35ммоль) і диізопропілетиламін (6,1мл, 35ммоль) об'єднували у воді (40мл) і перемішували до однорідності. Потім до реакційної суміші додавали ацетонітрил (50мл) і формальдегід (37%-ний розчин в Н2О; 0,42мл, 05,6ммоль). Через приблизно 15хв до реакційної суміші додавали NVAN-дециламіноетил ванкоміцин тристрифторацетат (10,0г, 5,1ммоль) і діізопропілетиламін (6,1мл, 35ммоль). Реакційну суміш перемішували при кімнатній температурі впродовж приблизно 18год, pH реакційної суміші на цей час доводили до приблизно 7 за допомогою 20% ТФО, ацетонітрил видаляли під вакуумом, і залишок ліофілізували. Утворену тверду речовину розтирали з водою (100мл), збирали шляхом фільтрації, висушували під вакуумом і очищали за допомогою РХВР із зворотною фазою з одержанням вказаної в заголовку сполуки. MS обчислено (МН+) 1756,6; знайдено (МН+) 1756,6. Сполука 11 також була одержана, як наведено нижче. Хінуклідинову сіль NVAN(дециламіноетил)ванкоміцину (500мг, 0,28ммоль, підрозділ є нижче) і амінометилфосфонову кислоту (155мг, 1,4ммоль) суспендували в 50%-ному водному ацетонітрилі (10мл). Додавали дііізопропілетиламін (972мкл, 720мг, 5,6ммоль) і суміш перемішували при кімнатній температурі до повного розчинення твердих речовин. Потім реакційну суміш охолоджували у льодяній бані і додавали формалін (3,7%, одержаний розчиненням комерційно доступного 37%-ного формаліну 1:9 із 50% АЦН/вода, 220мкл, 8,8мг, 0,29ммоль). Реакційну суміш перемішували при 0° впродовж 15год, коли час реакції закінчувався. Реакцію зупиняли при 0° додаванням 3н. НСІ до приблизно pH 2. Суміш розчиняли в 50мл 50% АЦН/вода, і потім додавали ацетонітрил (75мл, по 5x10мл через 5хв інтервали, 125мл всього) до осадження продукту. Тверду ре 49 75083 50 човину збирали за допомогою фільтрації під вакуного розчину додавали 600мл діетилового ефіру, умом і висушували під вакуумом. Очищенням за одержуючи осад, який потім фільтрували, промидопомогою РХВР із зворотною фазою одержували вали ефіром, і висушували під вакуумом. Неочивказану в заголовку сполуку. щений продукт очищали на випарювальній колонці Проміжну сполуку NVAN-дециламіноетил ваніз зворотною фазою, елюючи 10, 20, 30%-ним ацекоміцин тристрифторацетат одержували, як наветонітрилом у воді (що містить 0,1% трифтороцтодено нижче. вої кислоти) для видалення полярних компонентів а. N-Фмок-2-(дециламіно)етанол. (таких як залишки ванкоміцину), потім продукт 2-(н-Дециламіно)етанол (2,3г, 11ммоль, елюювали 70%-ним ацетонітрилом у воді (що міс1,1екв.) і ДІПЕА (2,0мл, 11ммоль, 1,1екв.) розчитить 0,1% трифтороцтової кислоти) з одержанням няли в метиленхлориді (15мл) і охолоджували на 9г Nvan-(N-Фмок-2-н-дециламіноетил) ванкоміцину льодяній бані. Додавали 9-флуоренілметил хлоу вигляді його трифторацетатної солі (4,3ммоль, роформіат (2,6г, 10ммоль, 1,0екв.) в метиленхло56%). риді (15мл), суміш перемішували протягом 30хв, г. Nvan-2-(н-Дециламіно)етил ванкоміцин трипотім двічі промивали 3н. соляною кислотою фтоацетат. (50мл) і насиченим бікарбонатом натрію (50мл). Nvan-(N-Фмок-2-н-дециламіноетил) ванкоміцин Органічні речовини висушували над сульфатом (100мг) розчиняли в 1мл ДМФ (1мл) і обробляли магнію і розчинники видаляли під зниженим тиспіперидином (200мкл) протягом 30хв. Суміш осаком. джували ефіром, центрифугували і промивали N-Фмок-2-(дециламіно)етанол (4,6г, 11ммоль, ацетонітрилом. За допомогою РХВР із зворотною 108%) використовувався без подальшого очищенфазою (10-70%-ний ацетонітрил у воді, що містить ня. 0,1% трифтороцтової кислоти протягом 120хв) б. N-Фмок-дециламіноацетальдегід. одержували Nvan-2-(н-дециламіно)етил ванкоміцин До розчину оксалілхлориду (12,24мл) і метиу вигляді його ТФО солі. ленхлориду (50мл) при температурі від -35 до Проміжну сполуку хінуклідинову сіль М^45°С додавали ДМСО (14,75г) в метиленхлориді дециламіноетил ванкоміцин одержували як вказа(25мл) протягом 20хв. Реакційну суміш перемішуно нижче. вали протягом 10хв при температурі від -35 до д. Nvan-(N'-Фмок-дециламіноетил) ванкоміцин. 45°С. Розчин N-Фмок-дециламіноетанолу (20,0г) в В 2л колбу, обладнану механічним змішуваметиленхлориді (70мл) додавали протягом 25хв і чем, додавали гідрохлорид ванкоміцину (50,0г), Nпотім перемішували 40хв при температурі від -35 Фмок-дециламіноальдегід (13,5г), ДМФ (400мл) і до -45°С. Потім додавали триетиламін (21,49г) і Ν,Ν- діізопропілетиламін (11,7мл). Суспензію песуміш перемішували протягом 30 хвилин при темремішували при кімнатній температурі протягом 2 пературі від -10 до -20°С. Реакційну суміш різко годин, протягом цього часу тверді речовини розохолоджували водою (120мл), потім додавали чинялися. Додавали метанол (190мл) та трифтоконцентровану сірчану кислоту (20,0г), підтримуюроцтову кислоту (10,4мл). Після перемішування чи внутрішню температуру на рівні 0-5°С. Органічреакційної суміші протягом 5 хвилин, боранні шари відділяли і промивали 2%-ною сірчаною піридиновий комплекс (3,33г) додавали однією кислотою (100мл), а потім водою (2x100мл). Оргапорцією, і промивали метанолом (10мл). Після 4-х нічний розчин переганяли під вакуумом при темгодинного перемішування, реакційну суміш охолопературі від 60°С до приблизно 100мл. Додавали джували до 5-10°С у льодяній бані і додавали воду гептан (100мл), температуру масляної бані підви(675мл) у співвідношенні для підтримання темпещували до 80°С і перегонку продовжували доти, ратури нижче 20°С. Реакційну суміш нагрівали до поки залишковий об'єм становив 100мл. Додавали кімнатної температури і додавали 10%-ний NaOH надлишок гептану (100мл) і перегонку повторювадо pH 4,2-4,3 (приблизно 15мл). Отриману суспенли до об'єму 100мл. Нагрівну баню змінювали зію охолоджували на льодяній бані протягом 1 год, охолоджуваною водяною банею при 15°С. Баню і потім продукт збирали за допомогою вакуумної повільно охолоджували до 5°С протягом 20хв до фільтрації і промивали охолодженою водою початку осадження продукту. Потім суспензію охо(2x100мл). Вологу тверду речовину висушували лоджували до -5 - -10°С і суспензію перемішували під вакуумом при 50°С з одержанням вказаної в 2год. Тверду речовину збирали на лійку Бюхнера і заголовку сполуки у вигляді твердої речовини від промивали охолодженим (-5°С) гептаном (2x15мл). кремового до блідо-жовтого кольору. Вологу тверду речовину висушували під вакуумом, e. NVAN-(дециламіноетил) ванкоміцин хінукліодержуючи альдегід. динова сіль. в. Nvan-(N-Фмок-2-н-дециламіноетил) ванкоміNvan-(N'-Фмок-дециламіноетил) ванкоміцин цин трифторацетат. (88г, 42ммоль) розчиняли в ДМФ (500мл) за допоГідрохлорид ванкоміцину (12г, 7,7ммоль, могою перемішування при кімнатній температурі 1,0екв.), Ν-Фмок-2-(н-дециламіно)-ацетальдегід протягом 1год. Додавали хінуклідин (9,4г, (3,2г, 7,6ммоль, 1,0екв.) і ДІПЕА (2,6мл, 84ммоль) і реакційну суміш перемішували протя14,9ммоль, 2,0екв.) перемішували при кімнатній гом 18год. ДМФ видаляли під вакуумом і тверду температурі в ДМФ (120мл) протягом 90хв. Додаречовину розтирали на порошок з ацетонітрилом вали ціаноборогідрид натрію (1,4г, 22ммоль, (700мл) протягом 3год. Тверду речовину збирали 3,0екв.), і потім метанол (120мл) і трифтороцтову на лійку Бюхнера і розтирали на порошок з ацетокислоту (1,8мл, 23ммоль, 3,0екв.). Суміш перемінітрилом (200мл) протягом 16год. В цей час додашували 60хв. при кімнатній температурі, потім вивали надлишок ацетонітрилу і тверду речовину даляли метанол при зниженому тиску. До утворезбирали на лійку Бюхнера, промивали ацетонітри 51 75083 52 лом (500мл) і потім ресуспендували в ацетонітрилі приблизно 15хв до реакційної суміші додавали (500мл). Після перемішування протягом 2 годин NVAN-(2-децилтіо)етил ванкоміцин бістрифторацетверду речовину збирали на лійці Бюхнера і висутат (1г, 0,53ммоль) і діізопропілетиламін (0,649мл, шували під вакуумом, одержуючи вказану в заго3,72ммоль). Реакцію перемішували при кімнатній ловку сполуку. температурі протягом приблизно 18год, в цей час Приклад 3 реакційну суміш розчиняли АЦН (40мл) і центриОдержання сполуки 12 фугували. Супернатант відкидали і осад, який за(Формула II, в якій R3 означає -ОН; R5 означає лишився, що містить потрібний продукт, розчиняли N-(фосфонометил)-амінометил; R19 означає вов 50%-ного ацетонітрилу (10мл) і очищали за додень, і R20 означає -СН2СН2-S-(СН2)9СН3) помогою РХВР із зворотною фазою з одержанням (Амінометил)фосфонову кислоту (0,295г, вказаної в заголовку сполуки. MS: обчислено (М+) 266ммоль) і діізопропілетиламін (0,649мл, 1772,7; знайдено (МН+) 1773,4. 3,72ммоль) об'єднували у воді (5мл) і перемішуваВикористовуючи вищевикладені методики і віли до гомогенізації. Потім до реакційної суміші дповідні вихідні речовини були одержані сполуки, додавали формальдегід (37%-ний розчин в Н2О; наведені в Таблиці І. Mac-спектральні дані цих 0,044мл, 0,585ммоль) і ацетонітрил (5мл). Через сполук наведені нижче: Таблиця І Сполука № MM (вільна основа) Отриманий МН+ 1 1725,63 1726,6 2 1726,62 1727,5 3 1742,68 1743,6 4 1724,64 1725,6 5 1742,96 1743,6 6 1786,03 1786,4 7 1785,04 1785,8 8 1799,07 1799,7 9 1770,74 1771,8 10 1772,99 1774,3 11 1755,66 1756,6 12 1772,71 1773,4 13 1756,64 1757,6 14 1754,67 1755,7 15 1772,99 1773,7 16 1816,06 1816,5 17 1815,01 1816,2 18 1829,10 1829,8 19 1878,1 1878,2 20 1802,74 1803,5 21 1830,75 1831,7 22 1849,66 1850,6 23 1800,76 1801,6 24 1801,04 1801,6 25 1932,86 1934,0 26 1880,12 1880,7 Приклад 4 Одержання проміжних сполук, корисних для одержання сполук за винаходом (Формула II, в якій R3 означає -ОН; R5 означає Н; R19 означає водень, і R20 означає 4-(4-хлорфеніл)бензил Трилітрову тригорлу колбу обладнували холодильником, вхідним отвором для азоту і верхнім пристроєм для механічного перемішування. В колбу завантажували подрібнену ацетатну сіль А82846В (20,0г, 1,21 10-5мл) і метанол (1000мл) в атмосфері азоту, 4'-хлорбіфенілкарбоксальдегід (2,88г, 1,33 10-2мл, 1,1екв.) додавали до цієї суміші, яка перемішувалася, потім додавали метанол (500мл). На завершення додавали ціаноборогідрид натрію (0,84г, 1,33 10-2мл, 1,1екв.) і метанол (500мл). Утворену суміш нагрівали зі зворотним холодильником (приблизно 65°С). Через 1год при нагріванні зі зворотнім холодильником досягалася гомогенність реакційної суміші. Через 25год при нагріванні зі зворотним холодильником джерело тепла видаляли і прозору реакційну суміш вимірювали за допомогою pHметра (6,97 при 58,0°С). По краплях додавали 1н. NaOH (22,8мл) до доведення pH до 9,0 (при 54,7°С). Колбу обладнували дистиляційною насадкою і суміш концентрували під частковим вакуумом до ваги 322,3 грамів, поки підтримувалася температура резервуару між 40°-45°С. Дистиляційну насадку змінювали краплинною лійкою, яка містить 500 ізопропанолу (ІПА). ІПА додавали по краплях до розчину кімнатної температури протягом 1год. Після того, як приблизно 1/3 ІПА було додано, утворився зернистий осад. ІПА, що залишився, додавали швидше після початку преципітації. Колбу зважували і виявили наявність 714,4г суспензії ІПА/метанол. Колбу переобладнували перегінною головкою і метанол, який залишився, видаляли під частковим вакуумом. Утворену суспензію (377,8г) залишали охолоджуватися в холодильнику протягом ночі. Неочищений продукт фільтрували через поліпропіленову прокладку і двічі промивали 25мл охолодженого ІПА. Після висушування протягуванням на лійці протягом 5хв речовину поміщали у вакуум для висушування при 40°С. Отримували світлорожеву тверду речовину (22,87г (теоретично = 22,43г)). РХВР-аналіз в порівнянні із стандартом показав 68,0% за масою вказаної в заголовку сполуки (4-[4-хлорфеніл]бензил-А82846В] у вигляді неочищеної твердої речовини, що уточнено давало 69,3% сирої речовини. Продукти реакції аналізувалися за допомогою РХВР зі зворотною фазою, використовуючи колонку Зорбакс (Zorbax) SB-C18 з вимірюванням при ультрафіолетовому світлі (УФ; 230нм). Застосовувалася 20хв система градієнтного розчинника, яка складалася з 95% водного буфера/5% CH3CN при часі = 0хв до 40% водного буфера/60% CH3CN при часі = 30хв, причому водний буфер представляв собою ТЕАР (5мл CH3CN, 3мл фосфорної кислоти в 1000мл води). Проміжні речовини ацетатної солі А82846В можуть бути одержані, як описано в патенті US №5,840,684. 53 75083 54 Використовуючи методики, описані в даному суттєву активність у відношенні вищенаведених описі вище, продукт Прикладу 4 може бути перетштамів, потім тестувалися для визначення знаворений в сполуку за винаходом, в якій R3 та/або чень МІК для більшого переліку ізолятів, отримаR5 представляє собою замісник, який включає одних в клінічних умовах, включаючи види, наведені ну або декілька фосфонових груп. вище, а також Staphylococcus, які не мають неспеПриклад 5 цифічної коагулази, як чутливі, так і резистентні до Визначення антибактеріальної активності метициліну (MS-CNS і MR-CNS). Крім того, вони А. Визначення антибактеріальної активності in досліджувалися для визначення МІК у відношенні vitro грам-негативних мікроорганізмів, таких як 1. Визначення мінімальних інгібувальних конEscherichia coli і Pseudomonas aeruginosa. центрации (МІК) 2. Визначення часу інактивації Бактеріальні штами отримували від АмериканДослідження з визначення часу, необхідного ської колекції типових культур (АТСС), Госпіталю для інактивації бактерій, проводили, як описано в Стенфордського університету (SU), Перманентної Lorian, "Antibiotics in Laboratory Medicine", 4-те королівської регіональної лабораторії в Берклі вид., Williams і Wilkins (1991). Ці дослідження про(КРВ), Массачусетського основного госпіталю водилися звичайно для обох штамів (MGH), Центру контролю захворюваності (CDC), Staphylococcus і Enterococcus. Службового госпіталю для ветеранів в м. СанСтисло, деякі колонії відбирали з агарових Франциско (SFVA) або госпіталю Сан-Франциско чашок і вирощували при 35°С при постійному пеКаліфорнійського університету (UCSF). Ванкоміремішуванні доти, поки не досягалася щільність цин-резистентні ентерококи мали фенотип Van А приблизно 1,5 і 108 CFU/мл. Потім зразки розводиабо Van В, який грунтується на їх чутливості до ли до приблизно 6 106 CFU/мл і продовжували тейкопланіну. Деякі ванкоміцин-резистентні ентеінкубували при 35°С при постійному перемішуванрококи, які мали генотип Van A, Van В, Van C1 або ні. Через різні проміжки часу відбирали аліквоти і Van C2, були отримані від Мауо Клініки. були приготовані п'ять десятикратних серійних Мінімальні інгібувальні концентрації (МІК) вирозведень. Метод заливки чашок застосовуються значали процедурою мікророзведення бульйону для визначення числа одиниць, здатних утворюзгідно із інструкціями NCCLS. Зазвичай, сполуки вати колонії (CFU). послідовно розчиняли в бульйоні МюллераЗагалом сполуки за винаходом проявляли акХінтона в 96-лункових мікротитрувальних чашках. тивність у вищенаведених тестах in vitro і демонКультивовані протягом ночі культури бактеріальструють широкий спектр активності. них штамів розчиняли на основі їх поглинання при В. Визначення антибактеріальної активності in 600нм таким чином, що кінцева концентрації в коvivo жній лунці становила 5 105 одиниць, які утворю1. Вивчення гострої токсичності на мишах ють колонії, (CFU) на мл. Потім чашки поміщали в В цих дослідженнях сполуки за винаходом інкубатор при 35°С. Наступного дня (або через вводилися внутрішньовенно або підшкірно, і спо24год у випадку штамів Enterococci), визначали стерігали протягом 5-15хв. Коли не спостерігалося МІК шляхом візуального аналізу чашок. Зазвичай токсичної дії, для наступної групи дозу збільшуваштами тестували в першому скринінгу, включаючи ли. Таке збільшення дози здійснювали до появи метицилін-чутливий Staphylococcus aureus смертельних випадків, або досягнення максима(MSSA), метицилін-резистентний Staphylococcus льної дози. В основному початкова доза становиaureus, метицилін-чутливий Staphylococcus ла 20мг/кг і кожного разу збільшували на 20мг/кг epidermidis (MSSE), метицилін-резистентний кожного разу до досягнення максимально допусStaphylococcus epidermidis (MRSE), ванкоміцинтимої дози (МДД). чутливий Enterococcus faecium (VSE Fm), ванкомі2. Вивчення біодоступності на мишах цин-чутливий Enterococcus faecalis (VSE Fs), ванМишам вводили сполуки за даним винаходом коміцин-резистентний Enterococcus faecium, також внутрішньовенно або підшкірно в терапевтичних резистентний до тейкопланіну (VRE Fm Van А), дозах (в основному, приблизно 50мг/кг). Групи ванкоміцин-резистентний Enterococcus faecium, тварин розміщували в метаболічних клітках таким який чутливий до тейкопланіну (VRE Fm Van В), чином, що сеча та фекалії збиралися для аналізу. ванкоміцин-резистентний Enterococcus faecalis, Групи тварин (n = 3) умертвляли через різні протакож резистентний до тейкопланіну (VRE Fs Van міжки часу (10хв, 1год і 4год). Кров збирали за А), ванкоміцин-резистентний Enterococcus faecalis допомогою серцевої пункції і досліджували насту, чутливий до тейкопланіну (VRE Fs Van В), пні органи - легені, печінку, серце, мозок, нирки та Enterococcus gallinarium Van А генотипу (VRE Gm селезінку. Тканини зважували та готували для Van A), Enterococcus gallinarium Van C-1 генотипу РХВР-аналізів. РХВР-аналізи проводили на гомо(VRE Gm Van C-1), Enterococcus casseliflavus Van генатах та рідинах для визначення концентрації C-2 генотипу (VRE Cs Van C-2), Enterococcus досліджуваних сполук або їх наявності. Також за flavescens Van C-2 генотипу (VRE Fv Van C-2), і таких обставин визначали метаболічні продукти, пеніцилін-чутливий Streptococcus pneumoniae утворені при перетворенні тестованих сполук. (PSSP) і пеніцилін-резистентний Streptococcus 3. Модель сепсису на мишах pneumoniae (PSRP). Через неможливість PSSP і В цій моделі прийнятні вірулентні штами бакPSRP добре рости в бульйоні Мюлер-Хінтон, МІК терій (найчастіше S. aureus, або Е. Faecalis або Е. для цих штамів визначали, використовуючи бульFaecium) вводяться мишам (N=5 - 10 мишей на йон TSA, доповнений агаровими чашками із кров'ю групу) внутрішньоочеревинно. Бактерії об'єднуваабо дефібринованою кров'ю. Сполуки, які мають ли із свинячим шлунковим муцином для посилення 55 75083 56 вірулентності. Доза бактерій (як правило 105-107) помогою окислення з подальшим використанням була достатньою для того, щоб викликати загирідинно-сцинтиляційного лічильника. Зразки сечі бель мишей протягом трьох днів. Через 1 годину та виділених тканин піддавали екстракції та аналіпісля введення бактерій вводили сполуку за виназували за допомогою РХВР із зворотною фазою із ходом в одиничній дозі кожну внутрішньовенно визначенням радіоактивності потоку для виявленабо підшкірно. Кожну дозу вводили групі із 5-10 ня можливих продуктів обміну досліджуваних ремишей, в дозах, які типово застосовуються від човин. максимальної приблизно 20мг/кг до мінімальної Б. Накопичення в тканинах після одиничної менше ніж 1мг/кг. Позитивний контроль (звичайний дози ванкоміцин із ванкоміцин-чутливими штамами) Ця методика застосовувалася для оцінки роззастосовувався в кожному експерименті. Доза, при поділу тестованих сполук в тканинах щурів після якій виживало приблизно 50% тварин, вважали введення шляхом інфузії. Самцям щурів Spragueрезультативною. Dawley (n = 3 на кожну дозу) вводили 50мг/кг тес4. Модель невриту сідничного нерва тованої сполуки. Застосовували два склади: 30%В цій моделі антибактеріальна активність споний ПЕГ 400 і 10%-ний сульфобутиловий ефір - лук за даним винаходом оцінювалася проти відпоциклодекстрину. Зразки сечі збирали з кліток провідно вірулентних штамів бактерій (найчастіше S. тягом 24год. Зразки крові збирали для визначення aureus, або Е. Faecalis або Е. Faecium, чутливих хімічного складу та концентрації речовин. Печінку або резистентних до ванкоміцину). Мишам спочатта нирки видаляли для гістологічного дослідження. ку викликали неврит шляхом введення циклофосОдну нирку та частину печінки гомогенізували для фаміду в дозі 200мг/кг на 0 та 2-й день. На 4-й визначення концентрації за допомогою РХВР із день тварин інфікували в ліву стегнову артерію за зворотною фазою з УФ-виявленням. Концентрацію допомогою введення IM одиничної дози бактерій. ліків в зразках сечі та сироватки визначали за доПотім через 1год після введення бактерій тварипомогою LC-MS аналізів. нам вводили тестовану сполуку і згодом через B. Накопичення в тканинах після багатократрізні проміжки часу (звичайно 1, 2,5; 4 і 24год) миного введення шей умертвляли (по 3 на одну експериментальну Ця методика застосовувалася для оцінки поточку) і стегно вирізали, гомогенізували і визначатенційного накопичення в тканинах щурів після ли число одиниць, здатних утворювати колонії, на інфузійного багатократного внутрішньовенного чашках. Кров також досліджували на чашках для введення тестованих сполук. Самцям та самкам визначення CFU в крові. щурів Sprague-Dawley (n = 4 тварин кожної статі на 5. Фармакокінетичні дослідження дозу) вводили тестовану сполуку в дозі 12,5; 25 і Швидкість, з якою сполука за винаходом вида50мг/кг щодня протягом семи днів. Тварин умертляється з крові, визначалась на щурах або мишах. вляли зранку наступного дня після закінчення ввеУ щурів тестованим тваринам вводили катетер в дення останньої дози (n = 3 тварин кожної статі на яремну вену. Тестовані сполуки вводили в хвостодозу). Одну тварину кожної статі з кожної групи ву вену і через різні проміжки часу (як правило 5, залишали як відповідний контроль, і її умертвляли 15, 30, 60хв і 2, 4, 6 і 24год) кров відбирали з катечерез 7 днів після введення останньої дози. Тестера. У мишей тестовані сполуки також вводили в товані сполуки вводили в 5%-ному гідроксипропілхвостову вену через різні проміжки часу. Як пра-циклодекстрині або 1%-ній сахарозі/4,5%-ній вило, кров отримували шляхом пункції серця. Кондекстрозі. Зразки сечі збирали з кліток впродовж 1центрацію тестованих сполук, що залишилися, 7 днів після введення речовин. Зразки крові збивизначали за допомогою РХВР. рали для хімічного аналізу та визначення концентЗагалом сполуки за винаходом проявляли акрації речовин. Печінку та нирки видаляли для гістивність у вищенаведених тестах та демонструватологічного дослідження. Одну нирку та частину ли широкий спектр активності. печінки гомогенізували для визначення концентПриклад 6 рації за допомогою РХВР із зворотною фазою із Визначення накопичення в тканинах УФ-виявленням. Концентрацію ліків в зразках сечі A. Розподіл в тканинах з використанням радіота сироватки визначали за допомогою LC-MS анаактивно мічених сполук лізів. Цю методику застосовували для дослідження Хоча даний винахід описаний із переважними розподілу в тканинах, виділення та перетворення специфічними варіантами його здійснення, для радіоактивно мічених тестованих сполук у самців фахівця в даній галузі очевидно, що можуть бути та самок щурів після внутрішньовенного введення здійснені різноманітні зміни та еквівалентні заміни в дозі 10мг/кг. Самцям та самкам щурів Spragueбез відступу від суті та обсягу винаходу. Крім того, Dawley (n = 2 тварин кожної статі на сполуку) ввоможливі різноманітні модифікації для пристосудили мічену 3Н тестовану сполуку в дозі 10 вання, зокрема, до різноманітних ситуацій, речо(400мкКі/кг) і 12,5мг/кг (100мкКі/кг) відповідно шлявин, композицій, способів, стадій способів та етахом внутрішньовенної інфузії (~2хв). Тестовані пів, які стосуються суті та обсягу даного винаходу. сполуки розчиняли в 5%-ному гідроксипропіл-3Усі такі модифікації підпадають під обсяг пунктів циклодекстрину у вигляді 2,5мг/мл розчину. Сечу формули винаходу, наведених тут. Крім того, всі та фекалії з кліток збирали протягом 24год. Через публікації, патенти і патентні документи, процито24год після введення тварин умертвляли і тканини вані в даній заявці, повністю включені як посиланвидаляли. Сироватку, сечу і тканини досліджували ня, а також індивідуально включені як посилання. для визначення загальної радіоактивності за до 57 Комп’ютерна верстка Л. Купенко 75083 Підписне 58 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of glycopeptidephosphonates
Назва патенту російськоюПроизводные гликопептидфосфонатов
МПК / Мітки
МПК: C07K 9/00, A61K 51/08, C07F 9/38, A61K 47/48, A61K 47/40, C07K 1/113, A61K 38/00, A61P 31/04
Мітки: похідні, глікопептидфосфонатів
Код посилання
<a href="https://ua.patents.su/29-75083-pokhidni-glikopeptidfosfonativ.html" target="_blank" rel="follow" title="База патентів України">Похідні глікопептидфосфонатів</a>
Попередній патент: Гербіцидний засіб та спосіб боротьби з бур’янами
Наступний патент: Піримідинові похідні
Випадковий патент: Спосіб виробництва листової фруктової пастили