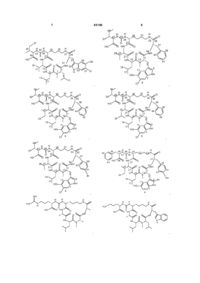
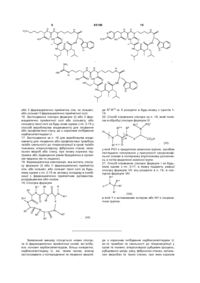
Застосування циклічних пептидів типу анабенопептину для лікування стану, в якому корисне пригнічення карбоксипептидази u, похідні анабенопептину та їх проміжні сполуки
Номер патенту: 85199
Опубліковано: 12.01.2009
Автори: Полла Маґнус, Бучанан Малколм, Б'йорквіст Петер, Керролл Ентоні, Кемпітеллі Марк, Нів Джуліетт, Гайд Едвард, Квінн Рон
Формула / Реферат
1. Застосування сполуки формули (І):
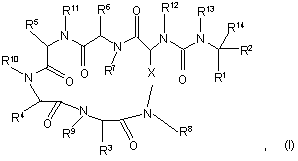
де:
X - (CH2)mY(CH2)n;
m та n незалежно дорівнюють 1, 2, 3, 4, 5 або 6; за умови, що m + n не більше 6;
Y - О, S(O)p або S-S;
R1 - CO2R15 або ізостера карбонової кислоти, як-то S(O)2OH, S(O)2NHR15, PO(OR15)OH, PO(OR15)NH2, B(OR15)2, PO(R15)OH, PO(R15)NH2, або тетразол;
R2, R3, R4, R5 та R6 незалежно представляють гідроген, С1-6алкіл (як варіант, заміщений замісником з групи: галоген, гідроксил, ціано, SH, S(O)3H, S(O)q(С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1-4алкоксил, OCF3,COOH, CONH2, CONH(С1-6алкіл), NH2, CNH(NH2), або NHCNH(NH2)), C3-6 циклоалкіл(С1-4)алкіл (де кільце циклоалкілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гетероцикліл(С1-4)алкіл (де кільце гетероциклілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), феніл(С1-4)алкіл (де кільце фенілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)) або гетероарил(С1-4)алкіл (де кільце гетероарилу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2));
p та q незалежно дорівнюють 0, 1 або 2;
R7, R8, R9, R10, R11, R12 та R13 незалежно представляють Н або С1-4алкіл;
R14 - Н або С1-4алкіл; а
R15 - Н або С1-4алкіл;
або її фармацевтично прийнятної солі або сольвату, або сольвату такої солі у способі виробництва медикаменту для лікування або профілактики стану, де є корисним інгібування карбоксипептидази U.
2. Сполука формули (І):

де:
Х - (СН2)4;
R1 - CO2R15;
R2 - С1-6алкіл з лінійним ланцюгом, заміщений на своєму кінці замісником: NH2, CNH(NH2) або NHCNH(NH2); C3-6 циклоалкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероцикліл, який містить принаймні один атом нітрогену; гетероцикліл, який не містить нітрогену, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероарил, заміщений NH2, CNH(NH2) або NHCNH(NH2); феніл, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероарил(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); феніл(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); або С3-6циклоалкіл(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); усі вищезгадані кільця, як варіант, надалі заміщено одним або більше замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкокси або OCF3;
один з R3, R4, R5 та R6 незалежно представляє гідроген, гетероарил(С1-4)алкіл (де кільце гетероарилу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)); а інші незалежно представляють гідроген, С1-6алкіл (як варіант, заміщений замісником з групи: галоген, гідроксил, ціано, SH, S(O)3H, S(O)q(С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1-4алкоксил, OCF3, COOH, CONH2, CONH(С1-6алкіл), NH2, CNH(NH2) або NHCNH(NH2)), C3-6циклоалкіл(С1-4)алкіл (де кільце циклоалкілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гетероцикліл(С1-4)алкіл (де кільце гетероциклілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), феніл(С1-4)алкіл (де кільце фенілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)) або гетероарил(С1-4)алкіл (де кільце гетероарилу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2));
p та q незалежно дорівнюють 0, 1 або 2;
R7, R8, R9, R10, R11, R12 та R13 незалежно представляють Н або С1-4алкіл;
R14 - Н або С1-4алкіл; а
R15 - Н або С1-4алкіл;
або її фармацевтично прийнятна сіль або сольват, або сольват такої солі.
3. Сполука формули (І) або її фармацевтично прийнятна сіль або сольват, або сольват такої солі за п. 2, де:
Х - (СН2)4;
R1 - CO2R15;
R2 - С1-6алкіл з лінійним ланцюгом, заміщений на своєму кінці замісником: NH2, CNH(NH2) або NHCNH(NH2); C3.6циклоалкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероцикліл який містить принаймні один атом нітрогену; гетероцикліл, який не містить нітрогену, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероарил, заміщений NH2, CNH(NH2) або NHCNH(NH2); феніл, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероарил(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); і феніл(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); або С3.6 циклоалкіл(С1-4)алкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); усі вищезгадані кільця, як варіант, надалі заміщено одним або більше замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкокси або OCF3;
один з R3, R4, R5 та R6 незалежно представляє гідроген, гетероарил(С1-4)алкіл (де кільце гетероарилу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)); а інші незалежно представляють гідроген, С1-6алкіл (як варіант, заміщений замісником з групи: галоген, гідроксил, ціано, SH, S(O)3H, S(O)q(С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1-4алкоксил, OCF3, СООН, CONH2, CONH(С1-6алкіл), NH2, CNH(NH2) або NHCNH(NH2)), C3.6циклоалкіл(С1-4)алкіл (де кільце циклоалкілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гетероцикліл(С1-4)алкіл (де кільце гетероциклілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), феніл(С1-4)алкіл (де кільце фенілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)) або гетероарил(С1-4)алкіл (де кільце гетероарилу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2));
р та q незалежно дорівнюють 0, 1 або 2;
і R7, R8, R9, R10, R11, R12 та R13 незалежно представляють Н або С1-4алкіл;
R14 - Н або С1-4алкіл; та
R15 - H або С1-4алкіл;
або її фармацевтично прийнятна сіль або сольват, або сольват такої солі.
4. Сполука формули (І) або її фармацевтично прийнятна сіль або сольват, або сольват такої солі за п. 2 або 3, де:
R1 - CO2R15;
R2 - С1-6алкіл з лінійним ланцюгом, заміщений на своєму кінці замісником: NH2, CNH(NH2) або NHCNH(NH2); C4алкіл (як-то СН(СН3)СН2СН3 або СН2СН(СН3)2) або (амінопіридиніл)метил (наприклад, (6-амінопіридин-3-іл)метил);
один з R3 та R4 - (індол-3-іл)СН2 як варіант, заміщений замісником з групи: галоген або гідроксил; а інший представляє бензил (як варіант, заміщений замісником з групи: галоген або гідроксил) або С4алкіл (як-то СН(СН3)СН2СН3 або СН2СН(СН3)2);
або R3 та R4 представляють метил;
R5 та R6 незалежно представляють С1-6алкіл (наприклад, СН3, СН(СН3)2, СН(СН3)СН2СН3 або СН2СН(СН3)2);
R7, R8, R9, R11,R12, R13 тa R14 - H;
R10 - С1-4алкіл; та
R15 - Н або С1-4алкіл.
5. Сполука за будь-яким одним з пп. 2-4, де X - (СН2)4.
6. Сполука за будь-яким одним з пп. 2-5, де R1 - CO2R15, у якій R15 - Н або С1-4алкіл.
7. Сполука за будь-яким одним з пп. 2-6, де R2 - С1-6алкіл з лінійним ланцюгом, заміщений на своєму кінці замісником: NH2, CNH(NH2) або NHCNH(NH2); C4алкіл (як-то СН(СН3)СН2СН3 або СН2СН(СН3)2) або (амінопіридиніл)метил.
8. Сполука за будь-яким одним з пп. 2-4, де R2 - С1-6алкіл (СН(СН3)СН2СН3 або СН2СН(СН3)2), бензил або лінійноланцюговий С1-6алкіл, заміщений на своєму кінці замісником: NH2, CNH(NH2), NHCNH(NH2) або (6-амінопіридин-3-іл)метил.
9. Сполука за будь-яким одним з пп. 2-8, де R2 - С1-6алкіл з лінійним ланцюгом, заміщений на своєму кінці замісником: NH2, CNH(NH2), NHCNH(NH2) або (6-амінопіридин-3-іл)метил.
10. Сполука за будь-яким одним із пп. 2-9, де R3 - СН2індоліл (де індоліл, як варіант, заміщений одним або більше замісниками з групи: галоген або гідроксил, С1-4алкіл або бензил (як варіант, заміщений замісником з групи: галоген або гідроксил).
11. Сполука за будь-яким одним з пп. 2-10, де R4 - СН2індоліл (де індоліл, як варіант, заміщений одним або більше замісниками з групи: галоген або гідроксил, С1-6алкіл (СН(СН3)СН2СН3 або СН2СН(СН3)2) або бензил (як варіант, заміщений замісником з групи: галоген або гідроксил).
12. Сполука за будь-яким одним з пп. 2-11, де R5 та R6 незалежно представляють С1-6алкіл (як-то метил, ізопропіл, СН(СН3)СН2СН3 або СН2СН(СН3)2).
13. Сполука за будь-яким одним з пп. 2-12, де усі R7, R8, R9, R11, R12, R13 та R14 - H.
14. Сполука за будь-яким одним з пп. 2-4, де R10 - С1-4алкіл.
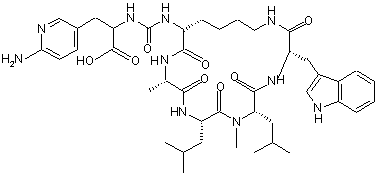
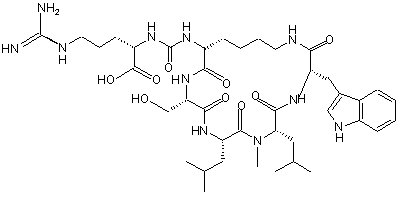
15. Сполука за п. 2, яка є сполукою наступної формули
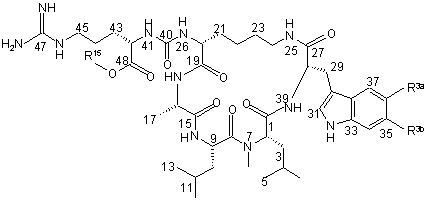 ,
,
в якій
R3a - H, R3b - H тa R15 - H;
R3a - ОН, R3b - Сl та R15 - Н;
R3a - ОН, R3b - Сl та R15 - СН3;
R3a - H, R3b - H тa R15 - CH3;
R3a - H, R3b - Сl тa R15 - H;
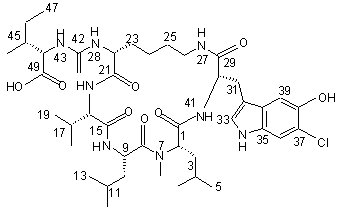 ,
,
 ,
,
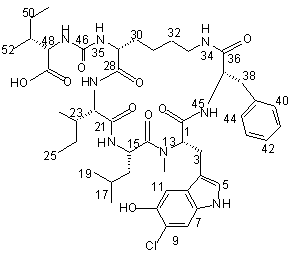 ,
,
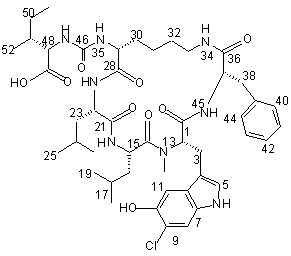 ,
,
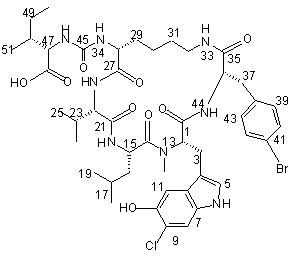 ,
,
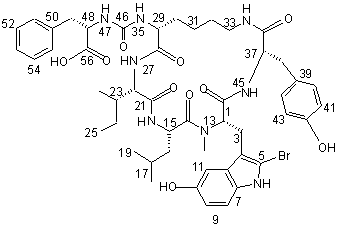 ,
,
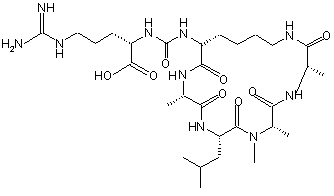 ,
,
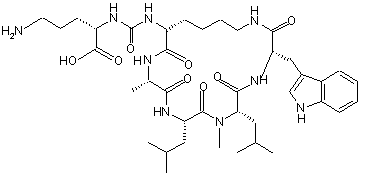 ,
,
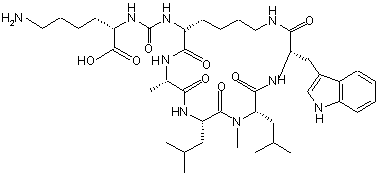 ,
,
 ,
,
 ,
,
або її фармацевтично прийнятна сіль чи сольват, або сольват її фармацевтично прийнятної солі.
16. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, або сольвату такої солі за будь-яким одним з пп. 2-15 у способі виробництва медикаменту для лікування або профілактики стану, де є корисним інгібування карбоксипептидази U.
17. Застосування за п. 16 для виробництва медикаменту для лікування або профілактики тромбозу та/або схильності до гіперкоагуляції в крові та/або тканинах; атеросклерозу; фіброзних станів; запальних хвороб або стану, при якому корисна підтримка або підвищення рівнів брадикініну в організмі тварини (як-то людини).
18. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль або сольват, або сольват такої солі за будь-яким одним з пп. 2-15 як активну складову в комбінації з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм.
19. Сполука формули
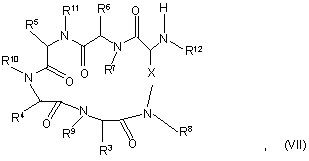
де R3-R12 тa X розкрито в будь-якому з пунктів 1-14.
20. Спосіб отримання сполуки за п. 19, який полягає в обробці сполуки формули VI
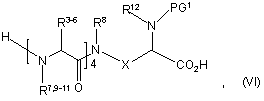
у якій PG1 є придатною захисною групою, засобом пептидного сполучення у присутності ненуклеофільної основи в полярному апротонному розчиннику, а потім видаленні захисної групи.
21. Спосіб отримання сполуки формули І за будь-яким одним з пп. 2-17, в якому піддають реакції сполуку формули VII, яку розкрито в п. 19, зі сполукою формули VIII
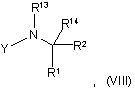
в якій Y є активованим естером або NY є ізоціанатною групою.
Текст
1. Застосування сполуки формули (І): UA (21) a200604776 (22) 28.10.2004 (24) 12.01.2009 (86) PCT/SE2004/001568, 28.10.2004 (31) 0302853-7 (32) 29.10.2003 (33) SE (46) 12.01.2009, Бюл.№ 1, 2009 р. (72) Б'ЙОРКВІСТ ПЕТЕР, БУЧАНАН МАЛКОЛМ, КЕМПІТЕЛЛІ МАРК, КЕРРОЛЛ ЕНТОНІ, Г АЙД ЕДВАРД, НІВ ДЖУЛІЕТТ, ПОЛЛ А МАҐНУС, КВІНН РОН (73) АСТРАЗЕНЕКА АБ (56) ITOU Y ET AL: 'Anabaenopeptins G and H, Potent Carboxypeptidase A Inhibitors from the Cyanobacterium Oscillatoria agardhii (NIES-595)' BIOORGANIC & MEDICIN AL CHEMISTRY LETTERS vol. 9, 1999, pages 1243 - 1246, XP004163951 GRACH-POGREBINSKY O. ET AL: 'Protease inhibitors from a Slovenian Lake Bled toxic waterbloom of the cyanobacterium Planktothrix rubescens' TETRAHEDRON vol. 59, 2003, pages 8329 - 8336, XP004460929 SANO T. ET AL: 'Isolation of New Protein Phosphatase Inhibitors from Two Cyanobacteria Species, Planktothrix spp' J. NAT. PROD. vol. 64, 2001, pages 1052 - 1055, XP002984170 ERHARD M. ET AL: 'Rapid Identification of the New Anabaenopeptin G from Planktothrix agardhii HUB 011 using Matrix-assisted Laser Desorption/Ionization Time-of-flight Mass Spectrometry' RAPID COMMUN. MASS SPECTROM. vol. 13, 1999, pages 337 - 343, XP002984171 DATABASE CAPLUS [Online] SHIN H.J. ET AL: 'Anabaenopeptins C and D, two new cyclic peptides from the cyanobacterium Oscillatoria agardhii (NIES 2 (19) 1 3 85199 4 R2 - С1-6алкіл з лінійним ланцюгом, заміщений на O R 13 своєму кінці замісником: NH2, CNH(NH2) або R5 R 14 NHCNH(NH2); C3-6 циклоалкіл, заміщений NH2, N N N N CNH(NH2) або NHCNH(NH2); гетероцикліл, який R2 R10 містить принаймні один атом нітрогену; гетероцик7 X O R N R1 ліл, який не містить нітрогену, заміщений NH2, O O CNH(NH2) або NHCNH(NH2); гетероарил, заміщений NH 2, CNH(NH2) або NHCNH(NH2); феніл, заміN N R4 щений NH2, CNH(NH2) або NHCNH(NH2); гетероO R8 R9 арил(С 1-4)алкіл, заміщений NH2, CNH(NH2) або , (I) NHCNH(NH2); феніл(С 1-4)алкіл, заміщений NH2, R3 O CNH(NH2) або NHCNH(NH2); або С3де: 6циклоалкіл(С 1-4)алкіл, заміщений NH 2, CNH(NH 2) X - (CH 2)mY(CH2)n ; або NHCNH(NH2); усі ви щезгадані кільця, як варіm та n незалежно дорівнюють 1, 2, 3, 4, 5 або 6; за ант, надалі заміщено одним або більше замісниумови, що m + n не більше 6; ком з групи: галоген, гідроксил, ціано, С1-4алкіл, Y - О, S(O)p або S-S; CF3, С1-4алкокси або OCF3; R1 - CO2R15 або ізостера карбонової кислоти, як-то один з R3, R4, R 5 та R6 незалежно представляє S(O)2OH, S(O) 2NHR15, PO(OR 15)OH, PO(OR 15)NH2, 15 15 15 гідроген, гетероарил(С1-4)алкіл (де кільце гетероB(OR )2 , PO(R )OH, PO(R )NH2, або тетразол; арилу, як варіант, заміщено замісником з групи: R2, R3, R4, R5 та R6 незалежно представляють гідгалоген, гідроксил, ціано, С1-4алкіл, CF3, С1роген, С1-6алкіл (як варіант, заміщений замісником OCF3, NH2, CNH(NH2) або 4алкоксил, з групи: галоген, гідроксил, ціано, SH, S(O)3H, NHCNH(NH2)); а інші незалежно представляють S(O)q (С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1гідроген, С1-6алкіл (як варіант, заміщений замісни4алкоксил, OCF3, COOH, CONH 2, CONH(С 1-6алкіл), ком з групи: галоген, гідроксил, ціано, SH, S(O)3H, NH2, CNH(NH2), або NHCNH(NH2)), C3-6 циклоалS(O)q (С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1кіл(С1-4)алкіл (де кільце циклоалкілу, як варіант, 4алкоксил, OCF3, COOH, CONH 2, CONH(С 1-6алкіл), заміщено замісником з групи: галоген, гідроксил, NH2, CNH(NH2) або NHCNH(NH2)), C3ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, 6циклоалкіл(С 1-4)алкіл (де кільце циклоалкілу, як CNH(NH2) або NHCNH(NH2)), гетероцикліл(С 1варіант, заміщено замісником з групи: галоген, 4)алкіл (де кільце гетероциклілу, як варіант, замігідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, щено замісником з групи: галоген, гідроксил, ціано, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гетероциС1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, CNH(NH2) кліл(С1-4)алкіл (де кільце гетероциклілу, як варіант, або NHCNH(NH2)), феніл(С 1-4)алкіл (де кільце фезаміщено замісником з групи: галоген, гідроксил, нілу, як варіант, заміщено замісником з групи: гаціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, логен, гідроксил, ціано, С1-4алкіл, CF3, С1CNH(NH2) або NHCNH(NH2)), феніл(С 1-4)алкіл (де 4алкоксил, OCF3, NH 2, CNH(NH 2) або NHCNH(NH 2)) кільце фенілу, як варіант, заміщено замісником з або гетероарил(С1-4)алкіл (де кільце гетероарилу, групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1як варіант, заміщено замісником з групи: галоген, 4алкоксил, OCF3, NH 2, CNH(NH 2) або NHCNH(NH 2)) гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, або гетероарил(С1-4)алкіл (де кільце гетероарилу, OCF3, NH2 , CNH(NH2) або NHCNH(NH2)); як варіант, заміщено замісником з групи: галоген, p та q незалежно дорівнюють 0, 1 або 2; гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, R7, R8, R9, R 10, R11 , R12 та R 13 незалежно предстаOCF3, NH2 , CNH(NH2) або NHCNH(NH2)); вляють Н або С 1-4алкіл; p та q незалежно дорівнюють 0, 1 або 2; R14 - Н або С 1-4алкіл; а 15 R7, R8, R9, R 10, R11 , R12 та R 13 незалежно предстаR - Н або С 1-4алкіл; вляють Н або С 1-4алкіл; або її фармацевтично прийнятної солі або сольваR14 - Н або С 1-4алкіл; а ту, або сольвату такої солі у способі виробництва R15 - Н або С 1-4алкіл; медикаменту для лікування або профілактики стаабо її фармацевтично прийнятна сіль або сольват, ну, де є корисним інгібування карбоксипептидази або сольват такої солі. U. 3. Сполука формули (І) або її фармацевтично при2. Сполука формули (І): йнятна сіль або сольват, або сольват такої солі за 11 R12 13 R6 R O R п. 2, де: 5 R R14 Х - (СН2)4; N N N N R1 - CO2R15; R2 R10 R2 - С1-6алкіл з лінійним ланцюгом, заміщений на 7 X O R 1 N R своєму кінці замісником: NH2, CNH(NH2) або O O NHCNH(NH2); C3.6циклоалкіл, заміщений NH2, CNH(NH2) або NHCNH(NH2); гетероцикліл якийN N R4 містить принаймні один атом нітрогену; гетероцикO R8 R9 ліл, який не містить нітрогену, заміщений NH2, , (I) R3 O CNH(NH2) або NHCNH(NH2); гетероарил, заміщений NH 2, CNH(NH2) або NHCNH(NH2); феніл, заміде: щений NH2, CNH(NH2) або NHCNH(NH2); гетероХ - (СН2)4; арил(С 1-4)алкіл, заміщений NH2, CNH(NH2) або R1 - CO2R15; NHCNH(NH2); і феніл(С 1-4)алкіл, заміщений NH2, R11 R6 R 12 5 85199 6 CNH(NH2) або NHCNH(NH2); або С3.6 циклоалR10 - С1-4алкіл; та кіл(С1-4)алкіл, заміщений NH2, CNH(NH2) або R15 - Н або С 1-4алкіл. NHCNH(NH2); усі вищезгадані кільця, як варіант, 5. Сполука за будь-яким одним з пп. 2-4, де X надалі заміщено одним або більше замісником з (СН2)4. групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С16. Сполука за будь-яким одним з пп. 2-5, де R1 CO2R15, у якій R15 - Н або С 1-4алкіл. 4алкокси або OCF3; 3 4 5 6 один з R , R , R та R незалежно представляє 7. Сполука за будь-яким одним з пп. 2-6, де R 2 - С1гідроген, гетероарил(С1-4)алкіл (де кільце гетеро6алкіл з лінійним ланцюгом, заміщений на своєму арилу, як варіант, заміщено замісником з групи: кінці замісником: NH2, CNH(NH2) або NHCNH(NH2); галоген, гідроксил, ціано, С1-4алкіл, CF3, С1C4алкіл (як-то СН(СН 3)СН2СН3 або СН2СН(СН3)2) OCF3, NH2, CNH(NH2) або або (амінопіридиніл)метил. 4алкоксил, NHCNH(NH2)); а інші незалежно представляють 8. Сполука за будь-яким одним з пп. 2-4, де R 2 - С1гідроген, С1-6алкіл (як варіант, заміщений замісни6алкіл (СН(СН 3)СН 2СН 3 або СН 2СН(СН 3)2), бензил ком з групи: галоген, гідроксил, ціано, SH, S(O)3H, або лінійноланцюговий С1-6алкіл, заміщений на S(O)q (С1-6алкіл), ОС(О)(С1-4алкіл), CF3, С1своєму кінці замісником: NH2, CNH(NH2), NHCNH(NH2) або (6-амінопіридин-3-іл)метил. 4алкоксил, OCF3, СООН, CONH 2, CONH(С 1-6алкіл), NH2, CNH(NH2) або NHCNH(NH2)), 9. Сполука за будь-яким одним з пп. 2-8, де R 2 - С1C3.6циклоалкіл(С 1-4)алкіл (де кільце циклоалкілу, як 6алкіл з лінійним ланцюгом, заміщений на своєму варіант, заміщено замісником з групи: галоген, кінці замісником: NH2, CNH(NH2), NHCNH(NH2) або гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, (6-амінопіридин-3-іл)метил. OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гетероци10. Сполука за будь-яким одним із пп. 2-9, де R3 кліл(С1-4)алкіл (де кільце гетероциклілу, як варіант, СН2індоліл (де індоліл, як варіант, заміщений одзаміщено замісником з групи: галоген, гідроксил, ним або більше замісниками з групи: галоген або ціано, С1-4алкіл, CF3, С1-4алкоксил, OCF3, NH2, гідроксил, С1-4алкіл або бензил (як варіант, заміCNH(NH2) або NHCNH(NH2)), феніл(С 1-4)алкіл (де щений замісником з групи: галоген або гідроксил). кільце фенілу, як варіант, заміщено замісником з 11. Сполука за будь-яким одним з пп. 2-10, де R4 групи: галоген, гідроксил, ціано, С1-4алкіл, CF3, С1СН2індоліл (де індоліл, як варіант, заміщений одним або більше замісниками з групи: галоген або 4алкоксил, OCF3, NH 2, CNH(NH 2) або NHCNH(NH 2)) або гетероарил(С1-4)алкіл (де кільце гетероарилу, гідроксил, С1-6алкіл (СН(СН3)СН2СН3 або як варіант, заміщено замісником з групи: галоген, СН2СН(СН3)2) або бензил (як варіант, заміщений гідроксил, ціано, С1-4алкіл, CF3, С1-4алкоксил, замісником з групи: галоген або гідроксил). OCF3, NH2 , CNH(NH2) або NHCNH(NH2)); 12. Сполука за будь-яким одним з пп. 2-11, де R 5 р та q незалежно дорівнюють 0, 1 або 2; та R6 незалежно представляють С 1-6алкіл (як-то 7 8 9 10 11 12 13 і R , R , R , R , R , R та R незалежно предстаметил, ізопропіл, СН(СН3)СН2СН3 або вляють Н або С 1-4алкіл; СН2СН(СН3)2). R14 - Н або С 1-4алкіл; та 13. Сполука за будь-яким одним з пп. 2-12, де усі R15 - H або С 1-4алкіл; R7, R8, R9, R 11, R12 , R13 та R14 - H. або її фармацевтично прийнятна сіль або сольват, 14. Сполука за будь-яким одним з пп. 2-4, де R 10 або сольват такої солі. С1-4алкіл. 4. Сполука формули (І) або її фармацевтично при15. Сполука за п. 2, яка є сполукою наступної фойнятна сіль або сольват, або сольват такої солі за рмули NH п. 2 або 3, де: H H H 45 43 23 21 R1 - CO2R15; N 40 N O N H2N 47 N 2 41 26 25 27 15 R - С1-6алкіл з лінійним ланцюгом, заміщений на H R 48 19 O 29 O своєму кінці замісником: NH2, CNH(NH2) або O HN O 37 R 3a NHCNH(NH2); C4алкіл (як-то СН(СН3)СН2СН3 або 39 O O NH O 31 СН2СН(СН3)2) або (амінопіридиніл)метил (напри17 15 N 33 1 3b 35 R 7 HN 9 H клад, (6-амінопіридин-3-іл)метил); N 3 4 3 один з R та R - (індол-3-іл)СН2 як варіант, замі13 щений замісником з групи: галоген або гідроксил; а 5 11 інший представляє бензил (як варіант, заміщений , в якій замісником з групи: галоген або гідроксил) або R3a - H, R 3b - H тa R15 - H; С4алкіл (як-то СН(СН3)СН2СН3 або СН 2СН(СН3)2); R3a - ОН, R3b - Сl та R15 - Н; або R3 та R4 представляють метил; 5 6 R3a - ОН, R3b - Сl та R15 - СН3; R та R незалежно представляють С 1-6алкіл (наR3a - H, R 3b - H тa R15 - CH 3 ; приклад, СН3, СН(СН3)2, СН(СН3)СН2СН3 або R3a - H, R 3b - Сl тa R15 - H; СН2СН(СН3)2); 7 8 9 11 12 13 14 R , R , R , R ,R , R тa R - H; 7 85199 8 49 H H 47 N 45 N 34 O 27 O HN 51 47 H H N 42 N 28 43 21 O HN 45 49 HO O O 15 HN 9 31 O 39 41 NH 33 O 7 N 21 H N 15 37 Cl 5 NH 7 9 Cl , 50 50 HO 41 3 HO , 52 43 1 13 N 5 11 39 44 NH 11 17 3 13 35 37 O O 19 N 35 H 1 O OH O O 25 23 29 O 19 17 HO H N 27 25 23 H N 33 31 29 H H 48 N 46 N 35 O 28 O HN 21 H N 15 25 O 38 45 NH O O 13 N HO 40 42 3 21 HN 45 NH O O 13 N 15 1 42 5 NH HO 7 7 9 Cl 40 44 3 11 17 NH HO 38 19 5 11 O 36 O O 25 H N 34 32 30 23 44 1 19 17 H H 48 N 46 N 35 O 28 O HN 52 36 O O 23 H N 34 32 30 9 Cl , , 49 51 HO H H 47 N 45 N 34 O 27 O HN 21 H N 15 50 52 37 O O 13 N 19 17 O 35 O O 25 23 H N 33 31 29 1 39 44 NH 43 54 HO 41 3 Br 5 11 NH HO 7 7 9 Cl H N N H HO 9 , NH H2N H N H N O H N H2N O O HN O O HN H H H 48 N 46 N 29 O 31 33 N 47 35 O 37 56 O HN O 27 39 45 O 23 NH OO 21 41 1 43 13 H N 15 N 25 3 OH 19 5 Br 11 17 NH HO O O HO NH H N H N O O HN O O HN N , , O O N O NH N H , 9 H N H2 N 85199 H N H N O O HN HO O O 10 O H N N H2 N O HN O H N H N O O HN HO O O NH N H N HN O O N , O NH N H , NH2 H N N H HN H N O O HN HO H N O O HO HN O O O NH N H N , або її фармацевтично прийнятна сіль чи сольват, або сольват її фармацевтично прийнятної солі. 16. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, або сольвату такої солі за будь-яким одним з пп. 2-15 у способі виробництва медикаменту для лікування або профілактики стану, де є корисним інгібування карбоксипептидази U. 17. Застосування за п. 16 для виробництва медикаменту для лікування або профілактики тромбозу та/або схильності до гіперкоагуляції в крові та/або тканинах; атеросклерозу; фіброзних станів; запальних хвороб або стану, при якому корисна підтримка або підвищення рівнів брадикініну в організмі тварини (як-то людини). 18. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль або сольват, або сольват такої солі за будьяким одним з пп. 2-15 як активну складову в комбінації з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. 19. Сполука формули R6 R11 R5 N R10 N R4 O O N N O R7 N R14 R2 R1 R12 , (VIII) в якій Y є активованим естером або NY є ізоціанатною групою. X N R13 Y H O де R3-R12 тa X розкрито в будь-якому з пунктів 114. 20. Спосіб отримання сполуки за п. 19, який полягає в обробці сполуки формули VI PG1 R12 3-6 8 R R N H N N 4 X CO2 H , (VI) R7,9-11 O у якій PG1 є придатною захисною групою, засобом пептидного сполучення у присутності ненуклеофільної основи в полярному апротонному розчиннику, а потім видаленні захисної групи. 21. Спосіб отримання сполуки формули І за будьяким одним з пп. 2-17, в якому піддають реакції сполуку формули VII, яку розкрито в п. 19, зі сполукою формули VIII N R9 R3 O R8 , (VII) Заявлений винахід стосується нових сполук, та їх фармацевтично прийнятних солей, які інгібують основні карбоксипептидази, більш конкретно, карбоксипептидазу U, які, таким чином, можна застосовувати у попередженні та лікуванні хвороб, де є корисним інгібування карбоксипептидази U, як-то тромбозі та схильності до гіперкоагуляції у крові та тканині, атеросклерозі рубцевих зрощень, рубцюванні шкіри, раку, фіброзних станах, запальних хворобах та таких станах, при яких корисне 11 85199 12 підтримання або підвищення рівнів брадикініну у (1997); J. Nat. Prod. (1997) 60 139-141; Teтpahedron тілі. У наступних аспектах винахід стосується спо54 (1998) 6719-6724; Bioorganic & Medicinal лук винаходу для застосування у терапії; способів Chemistry Letters 9 (1999) 1243-1246; Teтpahedron отримання таких нових сполук; фармацевтичних 56 (2000) 725-733; J. Nat. Prod. (2000) 63 1280композицій, які містять принаймні одну сполуку 1282; J. Nat. Prod. (2001) 64 No. 8 1053; винаходу або її фармацевтично прийнятну сіль як Teтpahedron 58 (2002) 6863-6871; та, J. Nat. Prod. активну складову; та застосування активних спо(2002) 65 1187-1189]. лук у виробництві медикаментів для медичного Синтез циклічних пептидів типу анабаєнопепзастосування, указаного вище. тину розкрито в: [Journal of Organic Chemistry, Фібриноліз є результатом ряду ферментних Vol.62, pp. 6199-6203 (1997); та Angewandte реакцій, що призводять до розкладання фібрину Chemie International Edition, Vol.35, No.12, pp. плазміном. Активація плазміногену є головним 1336-1338 (1996)]. Зараз знайдено, що сполуки процесом у фібринолізі. Розщеплення плазміногеформули (І): ну з утворенням плазміну здійснюється активаторами плазміногену, активатором плазміногену тканинного типу (t-PA) або активатором плазміногену урокіназного типу (u-РА). Початкове розщеплення плазміном фібрину генерує карбокси-термінальні залишки лізину, що є ділянками зв'язування плазміногену з високою спорідненістю. Оскільки плазміноген, зв'язаний із фібрином, набагато легше активується до плазміну ніж вільний плазміноген, цей механізм забезпечує регулювання фібринолізу з позитивним зворотним зв'язком. Одним з ендогенних інгібіторів фібринолізу є або її фармацевтично прийнятна сіль або сокарбоксипептидаза U (CPU). CPU є також відомою льват, або сольват такої солі, є особливо ефектияк карбоксипептидаза В плазми, активний інгібітор вними інгібіторами карбоксипептидази U і тому є тромбіну, здатний активувати фібриноліз (TAFIa), корисними як медикаменти для лікування або карбоксипептидаза R та індуцибельна карбоксипрофілактики станів, де є корисним інгібування пептидазна активність. CPU утворюється протягом карбоксипептидази U, наприклад, у лікуванні або коагуляції та фібринолізу з її попереднику proCPU профілактиці захворювань або станів із групи: дією протеолітичних ферментів, як-то тромбіну, тромбоз та/або схильність до гіперкоагуляції у комплексу тромбін-тромбодулін або плазміну. CPU крові та/або тканинах; атеросклероз; рубцеві зровідщеплює основні амінокислоти на карбоксищення; рубцювання шкіри; рак; фіброзні стани; терміналі фрагментів фібрину. Втрата карбоксизапальні хвороби; такі стани, при яких корисне термінальних лізинів, а таким чином ділянок зв'япідтримання або підвищення рівнів брадикініну у зування лізину для плазміногену сприяє інгібувантілі тварини (як-то людини); резистентність до білню фібринолізу. Припускають, що інгібуванням ку C; спадковий або набутий дефіцит антитромбіну втрати ділянок зв'язування лізину з плазміногеном, III, білку C, білку S або кофактору II гепарину; цира таким чином збільшенням швидкості утворення куляторний або септичний шок; циркуляторні анплазміну, ефективні інгібітори карбоксипептидази тифосфоліпідні тіла; гіпергомоцистеїнемія; індукоU сприяють фібринолізу. вана гепарином тромбоцитопенія; дефекти Повідомлено, що 2-меркаптометил-3фібринолізу; венозний тромбоз; емболія легень; гуанідинетилтіопропіонова кислота є інгібітором артеріальний тромбоз (наприклад, при інфаркті карбоксипептидази N. В останній час показано, що міокарду, нестабільній стенокардії, інсульті на осця сполука інгібує CPU, [Hendriks, D. et al., нові тромбозу або периферійному артеріальному Biochimica et Biophysica Acta, 1034 (1990) 86-92]. тромбозі); системна емболія звичайно від передПовідомлено, що гуанідинетилмеркаптобуршсердя протягом фібриляції передсердя або від тинова кислота є інгібітором карбоксипептидази N. лівого шлуночка після трансмурального інфаркту В останній час показано, що ця сполука інгібує міокарда; профілактика реоклюзії та рестенозу CPU, [Eaton, D. L., et al., The Journal of Biological (тобто тромбозу) після троболізу; підшкірне трансChemistry, 266 (1991) 21833-21838]. люмінальне втручання (PTI) та операції коронарІнгібітори CPU розкрито в [WO 00/66550, WO ного шун тування; попередження повторного тром00/66557, WO 03/013526 та WO 03/027128], а фабозу після мікрохірургії та судинної хірургії взагалі; рмацевтичну композицію, яка містить інгібітор CPU синдром розсіяної внутрішньосудинної коагуляції, та інгібітор тромбіну, розкрито у [WO 00/66152]. викликаної бактеріями, множинною травмою, сп'я Інгібітори карбоксипептидази В плазми розкрито у нінням або будь-яким іншим механізмом; фібрино[WO 01/19836 та WO 03/080631]. Інгібітори TAFIa літичне лікування, коли кров є у контакті з сторонрозкрито у [WO 02/14285, WO 03/061652 та WO німи поверхнями у тілі, як-то судинними 03/061653]. трансплантатами, судинними стентами, судинниЦиклічні пептиди типу анабаєнопептину розми катетерами, механічними та біологічними штукрито в: [Teтpahedron Letters, Vol. 36, No. 9, pp. чними клапанами або будь-яким іншим медичним 1511-1514 (1995); J. Org. Chem. (1997) 62 6199пристроєм; фібринолітичне лікування, коли кров є 6203; Teтpahedron Letters, Vol. 36, No. 33, pp. 5933у контакті з медичним пристроєм поза тілом, як-то 5936, (1995); J. Nat. Prod. (1996) 59 570-575; протягом серцево-судинної хірургії із застосуванTeтpahedron Letters, Vol. 38, No. 31, pp. 5525-5528, ням апарату серце-легені або при гемодіалізі; 13 85199 14 профілактика прогресії атеросклерозу та/або відR15 - H або C1-4 алкіл; торгнення трансплантату у пацієнтів за умови або її фармацевтично прийнятної солі або сотрансплантації органу, наприклад, трансплантації львату, або сольвату такої солі; у виробництві менирок; інгібування дозрівання та розвитку пухлини; дикаменту для лікування або профілактики стану, будь-який стан, у якому фіброз є сприятливим фаде є корисним інгібування карбоксипептидази U, ктором (наприклад, кистозний фіброз, фіброзна наприклад, у лікуванні або профілактиці захворюхвороба легенів наприклад, хронічна обструктивна вань або станів із групи: тромбоз та/або схильність хвороба легенів (COPD), синдром дихальної недодо гіперкоагуляції у крові та/або тканинах; атеростатності дорослих (ARDS), фіброзном'язова диссклероз; рубцеві зрощення; рубцювання шкіри; плазія, фіброзна хвороба язика або відкладення рак; фіброзні стани; запальні хвороби; такі стани, фібрину в оці при хір ургії ока); запалення (як-то при яких корисне підтримання або підвищення астма, артрит, ендометріоз, запальні хвороби кирівнів брадикініну у тілі тварин (як-то людини); решечнику, псоріаз або атопічний дерматит); нейрозистентність до білку C; спадковий або придбаний дегенеративні хвороби як-то Альцгеймера та Пардефіцит антитромбіну III, білку C, білку S або кокінсона; або стани, при яких корисне підтримання фактору II гепарину; циркуляторний або септичний або підвищення рівнів брадикініну (як-то гіпертеншок; циркуляторні антифосфоліпідні тіла; гіпергозія, стенокардія, серцева недостатність, легенева моцистеїнемія; індукована гепарином тромбоцитогіпертензія, ниркова недостатність або недостатпенія; дефекти фібринолізу; венозний тромбоз; ність органу). емболія легенів; артеріальний тромбоз (наприТаким чином, заявлений винахід стосується клад, при інфаркті міокарда, нестабільній стеноказастосування сполуки формули (І): рдії, базованому на тромбозі інсульті або периферичному артеріальному тромбозі); системна емболія звичайно від передсердя протягом фібриляції передсердя або від лівого шлуночка після трансмурального інфаркту міокарда; профілактика реоклюзії та рестенозу (тобто тромбозу) після троболізу; підшкірне транс-люмінальне втручання (PTI) та операції коронарного шунтування; попередження повторного тромбозу після мікрохірургії та судинна хірургія взагалі; синдром розсіяної внутрішньосудинної коагуляції, викликаної бактеріями, множинною травмою, сп'янінням або будьде: яким іншим механізмом; фібринолітичне лікуванX-(CH2)mY(CH2) n; ня, коли кров є у контакті з сторонніми поверхнями m та n, незалежно, дорівнюють 2, 3, 4, 5 або 6; у тілі, як-то судинними трансплантатами, судинниза умови, що m+n не більше 6; ми стентами, судинними катетерами, механічними Y-O, S(O) p, або S-S; та біологічними штучними клапанами або будьR1 - CO2R15 або ізостера карбонової кислоти, яким іншим медичним пристроєм; фібринолітичне як-то S(O)2OH, S(O)2NHR15 , PO(OR 15)OH, лікування, коли кров є у контакті з медичним приPO(OR15)NH2, B(OR15) 2, PO(R 15)OH, PO(R 15)NH2 строєм поза тілом, як-то протягом серцевоабо тетразол; судинної хір ургії із застосуванням апарату серцеR2, R3, R4, R5 та R6 незалежно представляють легені або при гемодіалізі; профілактика прогресії гідроген, C1-6 алкіл (як варіант, заміщений із групи: атеросклерозу та/або відторгнення трансплантату галоген, гідроксил, ціано, SH, S(О)3Н, S(O)q (C1-6 у пацієнтів за умови трансплантації органу, наприалкіл), OC(O)(C1-4 алкіл), CF3, C1-4 алкоксил, OCF3, клад, трансплантації нирок; інгібування дозрівання COOH, CONH2, CONH(C1-6 алкіл), NH2, CNH(NH2), та розвитку пухлини; будь-який стан, в якому фібабо NHCNH(NH2)), C3-6 циклоалкіл(C1-4)алкіл (де роз є сприятливим фактором (наприклад, кистозкільце циклоалкілу , як варіант, заміщений із групи: ний фіброз, фіброзна хвороба легень, наприклад, галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкохронічна обструктивна хвороба легень (COPD), ксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), гесиндром дихальної недостатності дорослих тероцикліл(C1-4)алкіл (де кільце гетероциклілу, як (ARDS), фіброзном'язова дисплазія, фіброзна хвоваріант, заміщено замісником з групи: галоген, роба язика або відкладення фібрину в оці протягідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкоксил, гом хірургії ока); запалення (як-то астма, артрит, OCF3, NH2, CNH(NH2) або NHCNH(NH2)), феніл(C1ендометріоз, запальні хвороби кишечнику, псоріаз або атопічний дерматит); нейродегенеративні хво4)алкіл (де кільце фенілу, як варіант, заміщено замісником з групи: галоген, гідроксил, ціано, C1-4 роби як-то Альцгеймера та Паркінсона; або стани, алкіл, CF3, C1-4 алкоксил, OCF3, NH2, CNH(NH2) при яких корисне підтримання або підвищення або NHCNH(NH2)) або гетероарил(C1-4)алкіл (де рівнів брадикініну (як-то гіпертензія, стенокардія, кільце гетероарилу, як варіант, заміщено заміснисерцева недостатність, легенева гіпертензія, нирком з групи: галоген, гідроксил, ціано, C1-4 алкіл, кова недостатність або недостатність органу). CF3, C1-4 алкоксил, OCF3, NH2, CNH(NH2) або У контексті заявленого винаходу, термін "теNHCNH(NH2)); рапія" охоплює "профілактику" якщо не вказане p та q незалежно дорівнюють 0, 1 або 2; інше. Терміни "терапевтичний" та "терапевтично" R7, R8, R9, R10, R11 , R12 та R13 незалежно предслід розуміти відповідно. ставляють H або C1-4 алкіл; В одному конкретному аспекті заявлений виR14 - H або C1-4 алкіл; та, нахід стосується застосування сполуки формули 15 85199 16 (І), як тут описано, у способі виробництва медикаГетроалкілалкіл представляє, наприклад, інменту для лікування або профілактики захворюдол-3-ілметил. вань або станів із групи: тромбоз та/або схильність Гетероциклілалкіл представляє, наприклад, до гіперкоагуляції у крові та/або тканинах; атеропіперидин-1-ілметил. склероз; фіброзні стани; запальні хвороби; або В іншому аспекті заявлений винахід стосуєтьстан, при якому корисна підтримка або підвищення ся сполуки формули (І): рівнів брадикініну у тілі тварини (як-то людини). В іншому аспекті заявлений винахід стосується застосування сполуки формули (І), як тут описано, у способі виробництва медикаменту для лікування або профілактики тромбозу та/або схильності до гіперкоагуляції в крові та/або тканинах; атеросклерозу; фіброзних станів; або стану, при якому корисна підтримка або підвищення рівнів брадикініну у тілі тварини (як-то людини); наприклад, медикаменту для лікування або профілактики тромбозу та/або схильності до гіперкоагуляції в крові та/або тканинах. де: Сполуки формули (І) існують в ізомерних фоХ - (СН2)4; рмах та заявлений винахід розкриває всі такі їх R1 - CO2R15; форми та суміші в усі х співвідношеннях. Чисті R2 - лінійноланцюговий C1-6 алкіл, заміщений енантіомери, рацемічні суміші та рівновеликі та на своєму кінці замісником: NH2, CNH(NH2) або нерівновеликі суміші двох енантіомерів знаходятьNHCNH(NH2); С3-6 циклоалкіл, заміщений NH2, ся в рамках заявленого винаходу. Також зрозуміCNH(NH2) або NHCNH(NH2); гетероцикліл, як місло, що всі можливі діастереоізомерні форми мотить, принаймні, один атом нітрогену; не нітроген, жуть знаходитися в рамках винаходу. який містить гетероцикліл, заміщений NH 2, Сполуки формули (І) можуть бути у формі солі. CNH(NH2) або NHCNH(NH2); гетероарил, заміщеПридатні солі охоплюють кислотно-адитивні солі, ний NH 2, CNH(NH2) або NHCNH(NH2); феніл, заміяк-то гідрохлорид, дигідрохлорид, гідробромід, щений NH2, CNH(NH2) або NHCNH(NH2); гетерофосфа т, сульфат, ацетат, діацетат, фумарат, маарил(C1-4)алкіл, заміщений NH2, CNH(NH2) або леат, тартрат, цитрат, оксалат, метансульфонат NHCNH(NH2); феніл(C1-4)алкіл, заміщений NH2, або п-толуолсульфонат. Солі також охоплюють CNH(NH2) або NHCNH(NH2); або C3-6 циклоалкіл(C1-4)алкіл, заміщений NH2, CNH(NH2) або солі металу, як-то сіль лужного металу (наприклад, сіль натрію або калію) або сіль лужноземеNHCNH(NH2); усі вищезгадані кільця, як варіант, льного металу (наприклад, магнію або кальцію). подалі заміщено одним або більше замісником з Термін C1-4 алкіл означає лінійну або розгалугрупи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1жену груп у алкілу, яка має 1-4 атомів карбону у 4 алкокси або OCF3; один із R3, R4, R5 та R6 незалежно представланцюгу. Приклади алкілу охоплюють метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, втор-бутил ляє гідроген, гетероарил(C1-4)алкіл (де кільце гета трет-бутил. тероарилу, як варіант, заміщено замісником з груТермін C1-4 алкоксил означає групу алкіл-О, де пи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкіл є лінійним або розгалуженим, і приклади алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)); та інші незалежно представляють гідроген, C1-6 охоплюють метоксил та етоксил. Галоген охоплює флуор, хлор, бром та йод алкіл (як варіант, заміщені із групи: галоген, гідро(наприклад, флуор, хлор або бром). ксил, ціано, SH, S(O)3H, S(O)4(C1-6 алкіл), Циклоалкілом є, наприклад, циклопропіл, цикOC(O)(C1-4 алкіл), CF3, C1-4 алкоксил, OCF3, COOH, лопентан або циклогексил. Термін гетероцикліл CONH2, CONH(C1-6 алкіл), NH2, CNH(NH2) або NHCNH(NH2)), С3-6 циклоалкіл(C1-4)алкіл (де кільце означає неароматичне кільце, яке містить карбон та, принаймні, один (як-то один або два) атоми, циклоалкілу, як варіант, заміщено замісником з вибрані із групи: нітроген, оксиген або сульфур. групи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1Гетероциклілом є, наприклад, піролідинил, піпериалкоксил, OCF3, NH2, CNH(NH2) або 4 дініл, піперазиніл або морфолініл. NHCNH(NH2)), гетероцикліл(C1-4)алкіл (де кільце гетероциклілу, як варіант, заміщено замісником з Термін гетероарил означає ароматичну кільцеву систему (наприклад, моноцикл або а біцикл), групи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1яка містить карбон та, принаймні, один (як-то один алкоксил, OCF3, NH2, CNH(NH2) або 4 або два) атоми, вибрані із групи: нітроген, оксиген NHCNH(NH2)), феніл(C1-4)алкіл (де кільце фенілу, або сульфур. Гетероарил, представляє, наприяк варіант, заміщено з групи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкоксил, OCF3, NH2, клад, фуран, тіофен, пірол, оксазол, ізоксазол, тіазол, імідазол, піразол, ізотіазол, оксадіазол, CNH(NH2) або NHCNH(NH2)) або гетероарил(C1фуразан, [1,2,3]-триазол, [1,2,4]-триазол, тіадіазол, 4)алкіл (де кільце гетероарилу, як варіант, заміщепіридин, піридазин, піримідин, піразин, індол або но з групи: галоген, гідроксил, ціано, C1-4 алкіл, нафтиридин. CF3, C1-4 алкоксил, OCF3, NH2, CNH(NH2) або NHCNH(NH2)); Фенілалкіл представляє, наприклад, бензил або 1-фенілет-2-ил. p та q незалежно дорівнюють 0,1 або 2; Циклоалкілалкіл представляє, наприклад, цикR7, R8, R9, R10, R11 , R12 та R13 незалежно предлогексилметил. ставляють H або C1-4 алкіл; 17 85199 18 R14 - H або C1-4 алкіл; та, У наступному аспекті винаходу R2 - C1-6 алкіл R15 - H або C1-4 алкіл; (як-то ізо-пропіл, CH(CH3)CH2CH3 або або її фармацевтично прийнятної солі або соСН2СН(СН3)2), бензил, або лінійноланцюговий C1-6 львату, або сольвату такої солі. У наступному асалкіл, заміщений на своєму кінці замісником: NH2, пекті заявлений винахід стосується сполуки форCNH(NH2), NHCNH(NH2) або (6-амінопіридин-3мули (І): іл)метил. В іншому аспекті R2 - лінійноланцюговий C1-6 алкіл, заміщений на своєму кінці замісником: NH2, CNH(NH2), NHCNH(NH2) або (6-амінопіридин3- іл)метил. У ще одному аспекті винаходу R3 - СН2індоліл (де індоліл, як варіант, заміщено одним або більше замісником з групи: галоген (наприклад, хлор або бром) або гідроксил), C1-4 алкіл або бензил (як варіант, заміщений із групи: галоген (наприклад, бром) або гідроксил). В іншому аспекті винаходу R4 - СН2індоліл (де індоліл, як варіант, заміщено одним або більше де: замісником з групи: галоген (наприклад, хлор або 1 15 R - CO2R ; бром) або гідроксил), C1-6 алкіл (як-то метил, ізоR2 - лінійноланцюговий C1-6 алкіл, заміщений пропіл, CH(CH3)CH2CH3 або СН2СН(СН3)2) або на своєму кінці замісником: NH2, CNH(NH2) або бензил (як варіант, заміщений із групи: галоген NHCNH(NH2); C4 алкіл (як-то CH(CH3)CH2CH3 або (наприклад, бром) або гідроксил). СН2СН(СН3)2); або (амінопіридиніл)метил (наприУ наступному аспекті винаходу R5 та R6 незаклад, (6-амінопіридин-3-іл)метил); лежно представляють C1-6 алкіл (як-то метил, ізоодин із R3 та R4 представляє (індол-3-іл)СН2, пропіл, CH(CH3)CH2CH3 або СН 2СН(СН3)2). як варіант, заміщений групою: галоген або гідроВ іншому аспекті винаходу всі R7, R8, R9 , R11 , 12 ксил; а інший представляє бензил (як варіант, заR , R13 та R14 - H. міщений групою: галоген або гідроксил) або C4 У ще одному аспекті винаходу R10 - C1-4 алкіл алкіл (як-то CH(CH3)CH2CH3 або СН 2СН(СН3)2); (наприклад, метил). або R3 та R4 представляють метил; У наступному аспекті винахід стосується споR5 та R6 незалежно представляють C1-6 алкіл луки формули (І), яка є сполукою 1, 2, 3, 4, 5, 6, 7, (наприклад, CH3, СН(СН3)2, CH(CH3)CH2CH3 або 8, 9, 10, 11, 12, 13, 14, 15 або 16 її фармацевтично СН2СН(СН3)2); прийнятною сіллю або сольватом, або сольватом R7, R8, R9, R 11, R12 , R13 та R14 - H; її фармацевтично прийнятної солі. R10 - C1-4 алкіл; та, Сполуки заявленого винаходу можна отриму15 R - H або C1-4 алкіл. вати способами, відомими у рівні те хніки або анаВ іншому аспекті заявлений винахід стосуєтьлогічними способам у Прикладах 3 та 4. Треба ся сполуки формули (І), яка має хіральність, покарозуміти, що застосування способу із літератури зану нижче: або із Прикладів 3 та 4 потребує захисту функціональних груп сполук інтермедіатів захисними групами. Функціональні групи, як це бажано для захисту, охоплюють гідроксил, карбоксилат та аміногрупи. Придатні захисні групи гідроксилу охоплюють триалкілсиліл або діарилалкіл-силіл (наприклад, трет-бутилдиметилсилш, третбутилди фенілсиліл або триметилсиліл), тетрагідропіраніл, трет-бутил, метоксиметил, бензилоксиметил та 4-метоксибензил. Придатні захисні групи для карбоксилату охоплюють естери алілу, етилу, трет-бутилу та бензилу. Придатні захисні групи для аміну охоплюють трет-бутилоксикарбоніл, 2,4,6-триметоксибензил та бензилоксикарбоніл. Застосування захисних гр уп описано у ['Protecti ve В аспекті винаходу X - (CH2)4 . Groups in Organic Synthesis', third edition, T.W. У наступному аспекті винаходу R1 - CO2R15 де 15 Greene & P.G.M. Wutz, Wiley-Interscience (1999)]. R - H або C1-4 алкіл (наприклад, метил). Захисною групою може також бути полімерна смоВ іншому аспекті R2 - лінійноланцюговий C1-6 ла, як-то гідроксиметил-3-метоксифеноксимасляна алкіл, заміщений на своєму кінці замісником: NH2, кислота або 2-хлортритилхлорид. CNH(NH2) або NHCNH(NH2); C4 алкіл (як-то Таким чином, сполуки формули І можна отриCH(CH3)CH2CH3 або СН2СН(СНз)2); або (амінопімувати реакцією сполук формули VII, ридиніл)метил (наприклад, (6-амінопіридин-3іл)метил). 19 85199 20 де R3 - R12 та X розкрито вище, зі сполукою формули VIII, в якій R1, R2 R13, R 14 розкрито у формулі І, a Y є залишком активованої кислоти, як-то нітрофеноксикарбонілом або активованим еквівалентом амінокарбонілу, як-то N=C=O. Конкретно Y охоплюють активовані естери, як-то 4нітрофеноксикарбоніл та трет-бутоксикарбоніл. Переважно Y - 4-нітрофеноксикарбоніл. Інші сполуки охоплюють такі, де YN є ізоціанатною групою. Реакцію, звичайно, слід проводити у придатному розчиннику, як-то ДМФ (або іншому апротонному розчиннику) та у присутності ненуклеофільної основи, як-то DIEA. Інтермедіат формули VII можна отримувати, як наведено нижче. a) Синтез сполуки III Сполуку формули Ia розчиняють у неполярному апротонному розчиннику, як-то ДХМ або ТГФ у присутності ненуклеофільної основи, як-то DIEA, потім вона реагує із твердою основою, як-то 2хлортритилом, при кімнатній температурі протягом 2 годин. Після цього часу будь-яку тверду основу, що не прореагувала (Сполука II), покривають, застосовуючи метанол. Потім смолу фільтрують та промивають послідовно ,ДМФ, ДХМ та ДМФ. b) Синтез сполуки формули (n=4) Сполуку формули III/V (n=1-3) піддавали твердофазному пептидному синтезу, як описано нижче: PG2 (у цьому прикладі - Fmoc) видаляли від Сполуки III/V (n=1-3), застосовуючи 20% піперидин у ДМФ та отриману смолу промивають послідовно ДМФ, ДХМ та ДМФ. Сполуку формули IV, попередньо ативовану додаванням засобу сполучення, як-то HBTU або HATU у полярному апротонному розчиннику, як-то ДМФ або ДМСО, потім додають до незахищеної сполуки формули III/V (n=1-3). 21 85199 22 Сполучення пептиду ініціюють додаванням ненукмаси гепарином, фрагментом синтетичного гепалеофільної основи, як-то DIEA, та реакційну суміш рину, як-то фондапаринуксом, інгібітором тромбіструшують протягом 1-2 годин. Смолу потім фільну, інгібітором фактору Xa або іншим інгібітором трують та промивають послідовно ДМФ, ДХМ та коагуляції фактору/ферменту, фактором рекомбіДМФ. нантної коагуляції, як-то рекомбінантним активоb) Синтез сполукц формули VI ваним білком C людини) або антитромбоцитарним PG2 (у цьому прикладі - Fmoc) видаляють зі засобом (як-то ацетилсаліциловою кислотою, дисполуки V (n=4), застосовуючи 20% піперидин у піридмолом, тиклопідином, клопідогрелем або ДМФ, та о триману смолу промивають послідовно іншим антагоністом ADP-рецептору [як-то P2Y12 ДМФ, ДХМ та ДМФ. Сполуку формули VI відокреабо P2Y1], рецептором тромбоксану та/або інгібімлюють від твердої основи без втрати PG1 швидтором синтетази, антагоністом рецептору фібриким промиванням потоком сполуки формули V ногену, міметиком простацикліну або інгібітором (n=4) з розбавленою кислотою в апротонному розфосфодіестерази). чиннику та негайним розбавленням продукту у Сполуки винаходу подалі можна комбінувати великому об'ємі розчиннику. Промивання потоком та/або співзастосовувати із тромболітиками, як-то 2% TFA у ДХМ в еквівалентному об'ємі води є зратканинним активатором плазміногену (природним, зком цього способу. рекомбінантним або модифікованим), стрептокінаb) Синтез сполуки формули VII зою, урокіназою, проурокіназою, комплексом анізоDIEA або еквівалент ненуклеофільної основи їлований плазміноген-активатор стрептокінази додають до сполуки формули VI у полярному ап(APSAC), активаторами плазміногену слинної заротонному розчиннику, як-то ДМФ або ДМСО. лози тварини, та подібним, у лікуванні тромботичОтриманий розчин сполуки формули VI циклізують них хвороб, конкретно, інфаркту міокарда, ішемічв умовах високого розбавлення додаванням крапного інсульту та тяжкої емболії легень. лями до перемішуваного розчину засобу сполуТаким чином, у наступному аспекті заявлений чення, як-то PyBOP, у полярному апротонному винахід стосується комбінації сполуки формули (І) розчиннику, як-то ДМФ або ДМСО. Реакційну су(комбінованої та/або співзастосованої), де X міш випарюють до сухого стану, та залишені кис(CH2)mY(CH2) n; m та n незалежно дорівнюють 1, 2, лотнолабільні захисні групи (наприклад, PG1) ви3,4, 5 або 6; за умови, що m+n не більше 6; Y - O, даляли, застосовуючи сильну кислоту (TFA, HCl) з S(O)p, або S-S; R1 - CO2R15 або ізостера карбонододаними поглиначами (TIPS, н-крезолом, водою вої кислоти, як-то S(O)2OH, S(O)2NHR15, 15 15 15 або тіокрезолом). Реакційну суміш знов випарюPO(OR )OH, PO(OR )NH2, B(OR ) 2, PO(R 15)OH, ють до сухого стану перед очищення РФВТРХ, що PO(R15)NH2 або тетразол; R2, R3, R4, R5 та R6 не1 дало сполуку формули VII. У формулі VIIPG є залежно представляють гідроген, C1-6 алкіл (як придатною захисною групою, як-то будь-яка кисваріант, заміщений із групи: галоген, гідроксил, лотнолабільна захисна група нітрогену, наприціано, SH, S(О)3Н, S(O)q (C1-6 алкіл), ОС(О)(C1-4 клад, Вос, тобто стійка до основних умов, потрібалкіл), CF3, C1-4 алкоксил, OCF3, COOH, CONH2, них для видалення PG2. PG2 є будь-якою CONH(C1-6 алкіл), NH2, CNH(NH 2), або основнолабільною захисною групою нітрогену, якNHCNH(NH2)), С3-6 циклоалкіл(C1-4)алкіл (де кільце то Fmoc, яку також можна видаляти без розщепциклоалкілу, як варіант, заміщено замісником з лення лінкеру L або видалення PG1; У вищенавегрупи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1дених стадіях способу посилання на "засіб сполуалкоксил, OCF3, NH2, CNH(NH2) або 4 чення" стосується будь-якої групи, що активує NHCNH(NH2)), гетероцикліл(C1-4)алкіл (де кільце карбонову кислоту стосовно нуклеофільної атаки. гетероциклілу, як варіант, заміщене із групи: галоПриклади охоплюють попередники (продукти поген, гідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкоксил, передньої стадії) активованих естерів, як-то пOCF3, NH2, CNH(NH2) або NHCNH(NH2)), феніл(C1нітрофенол та гексафлуорфенол, похідні карбодіі4)алкіл (де кільце фенілу, як варіант, заміщене із міду, як-то DIC та DCC, солі бензотриазолілгрупи: галоген, гідроксил, ціано, C1-4 алкіл, CF3, C1тетраметилфосфнію, як-то BOP та PyBOP, солі алкоксил, OCF3, NH2, CNH(NH2) або 4 бензотриазоліл-тетраметилуронію, як-то HBTU та NHCNH(NH2)) або гетероарил(C1-4)алкіл (де кільце HATU. L - будь-який особливо кислотнолабільний гетероарилу, як варіант, заміщене із групи: галолінкер для карбонових кислот на твердій підкладці, ген, гідроксил, ціано, C1-4 алкіл, CF3, C1-4 алкоксил, тобто стійкий до умов, потрібних для видалення OCF3, NH2, CNH(NH2) або NHCNH(NH2)); p та q PG2, як-то 2-хлортритилхлоридний лінкер, кислотнезалежно дорівнюють 0, 1 або 2; R7, R8, R9, R10, на смола Ринка, 4-гідроксиметил-3R11, R12 та R13 незалежно представляють H або C114 метоксифеноксимасляно-кислотний лінкер. - H або C1-4 алкіл; та, R15 - H або C1-4 4 алкіл; R Нові способи отримання інтермедіатів, та наалкіл; або її фармацевтично прийнятна сіль або ведені тут нові інтермедіати є також особливостясольват, або сольват такої солі; та антимікроботими заявленого винаходу. чний засіб з різним механізмом дії {як-то антикоаАльтернативно, сполуку формули (І) можна гулянт (наприклад, антагоніст вітаміну K, нефраквиділяти із природних джерел, застосовуючи меціонований або низької молекулярної маси тодологію Прикладів 1 або 2. гепарин, фрагмент синтетичного гепарину як-то Сполуки винаходу також можна комбінувати фондапаринукс, інгібітор тромбіну, інгібітор фактота/або співзастосовувати з будь-яким антитромбору Xa або рекомбінантний фактор коагуляції, як-то тичним засобом із різним механізмом дії, як-то рекомбінантний активований білок C людини) або антикоагулянтом (наприклад, антагоністом вітаміантитромбоцитарний засіб (як-то ацетилсаліцилону K, нефракціонованим або низької молекулярної ва кислота, дипіридамол, тиклопідин, клопідогрель 23 85199 24 або інший антагоніст ADP-рецептору [як-то P2Y12 [(етоксикарбоніл)окси]метилові естери карбонових або P2Y1], інгібітор рецептору тромбоксану та/або кислот. синтетази, антагоніст рецептору фібриногену, міВинахід ілюстровано наступними прикладами. метик простацикліну або інгібітор фосфодіестераПриклад 1 зи)} або тромболітик {як-то активатор плазміногену Приклад описує виділення Сполук 1-10. тканини (природний, рекомбінантний або модифіЗагальні експериментальні способи кований), стрептокіназа, урокіназа, проурокіназа, Вода була Milli-Q-фільтрованою, тоді як усі інкомплексом анізошований плазміноген-активатор ші застосовані розчинники були від Omnisolv. Для стрептокінази (APSAC), активатори плазміногену препаративної ВЕРХ застосовували колонку YMC слинної залози тварини}. C18 5мкМ, 21.2мм´150мм та колонку Hypersil BDS Сполуки винаходу паовинні мати селективC18 5мкМ, 21.2´150мм. Спектри ЯМР записували ність стосовно карбоксипептидази U відносно карна спектрометрі ЯМР Varian Inova 600 або боксипептидази N>50:1, наприклад, >100:1, засто500МГц. Зразки розчиняли в d6-ДМСО та хімічні совуючи, аналіз описаний нижче. зсуви розраховували відносно піку розчиннику Інгібувальну дію сполук заявленого винаходу (ДМСО 1H 2.49 та 13C 39.5 млн -1). Мас-спектри вивизначали, застосовуючи аналіз, описаний [Dirk мірювали на Fisons VG Platform II, застосовуючи Hendriks, Simon Scharpe та Marc van Sande, режим електоророзпилювання з позитивною іоніClinical Chemistry, 31, 1936-1939 (1985); та Wei зацією. Розчинник для елюювання - суміш ацетоWang, Dirk F. Hendriks, Simon S. Scharpe, The нітрил/вода 50% при 0.1мл/хвилину. Journal of Biological Chemistry, 269, 15937-15944 Тваринний матеріал (1994)], застосовуючи концентрацію субстрату Губку (Melophlus sp.) збирали SCUBA зану4ммоль. ренням Ribbon Reef No. 5, Australia, та підтверВинахід також стосується способу лікування джуючий зразок (G319104) знаходиться в Музеї стану, де U є корисним інгібування карбоксипептиКвінсленду, Брисбен, Австралія. дази, у тварин, потерпаючих від названого стану Екстракція та виділення або від його ризику, який полягає у застосуванні Заморожений, висушений розмелений зразок до тварини терапевтично ефективної кількості губки Melophlus sp (128г), зібраний від Ribbon Reef сполуки формули (І), або її фармацевтично прийнNo. 5 у дальньому Північному Квінсленді, Австраятної солі або сольвату, або сольвату такої солі, лія, ретельно екстрагували метанолом (2 1). Розяк визначено раніше. чинник випаровували, що дало темно-коричневий Призначене дозування для вищезгаданих тезалишок (28г). Залишок перерозчиняли в суміші рапевтичних застосувань треба змінювати залежEtOAc (20мл) та води (60мл), та відокремлювали но від застосованих сполук, режиму застосування, за допомогою крапельної протитечійної хроматогбажаного лікування та вказаного розладу. рафії водою як стаціонарною фазою та мобільною Сполуки формули (І) та їх фармацевтично фазою із градієнтом від EtOAc до бутанолу при прийнятні солі, сольвати або сольвати солей мож5мл/хвилину. Збирали двохвилинні фракції та на застосовувати самостійно, але їх звичайно зааналізували кожну секунду електоророзпилювальстосовують у формі фармацевтичної композиції, в ною мас-спектрометрією. Ідентичні фракції комбіякій сполука формули (І), сіль, сольват або сольнували, створюючи 5 фракцій. Фракцію 2 (320мг) ват солі (активна складова) поєднана з фармацеввідокремлювали центрифужною роздільною хротично прийнятним ад'ювантом, розріджувачем або матографією (Sanki CPC, вертикальний спосіб), носієм. Наприклад, залежно від способу застосузастосовуючи суміш трьох розчинників вання фармацевтична композиція буде містити СНСl3/МеОН/Н 2О (7:13:8) з нижчою фазою як ста0.05-99мас% (масова частка), як-то 0.05-80мас%, ціонарною. Швидкість потоку дорівнювала наприклад, 0.10-70мас%, як-то 0.10-0.50мас% ак2мл/хвилину та дво хвилинні фракції збирали противної складової, усі масові частки віднесено до тягом 360 хвилин. Кожну секунду фракції аналізумаси усієї композиції. вали позитивною електоророзпилювальною масТаким чином, заявлений винахід також стосуспектрометрією та ідентичні фракції комбінували. ється фармацевтичної композиції, яка містить Комбінували фракції 91-101, що дало неочищену сполуку формули (І) або її фармацевтично прийнСполуку 2 (10.8мг), та комбінували фракції 107ятну сіль або сольват, або сольват такої солі, як 120, що дало неочищену Сполуку 1 (12.4мг). Кожні визначено раніше, у поєднанні з фармацевтично неочищені фракції пептиду Сполук 1 та 2 розподіприйнятним ад'ювантом, розріджувачем, або носіляли між водою TFA (1%) та гексаном. Водні шари єм. від кожного розподілення містили чисту Сполуку 2 Винахід також стосується способу отримання (9.5мг) та Сполуку 1 (11.5мг). Фракції 1, 3 та 4 від фармацевтичної композиції винаходу, який поляпервинного розділення DCCC комбінували із фрагає у змішуванні сполуки формули (І), або її фаркціями, що залишилися від розділення CPC, та мацевтично прийнятної солі або сольвату, або попередньо адсорбували на C18 (3г). Попередньо сольвату такої солі, як визначено раніше, з фарадсорбовані фракції подалі розділяли C18 ВЕРХ мацевтично прийнятним ад'ювантом, розріджуваHypersil BDS C18 (5мкМ, 20мм´150мм), застосочем, або носієм. вуючи градієнт вода/метанол від води, яка містить Винахід також охоплює похідні сполук форму1% TFA до метанолу, який містить 1% TFA, при ли (І), які володіють біологічною функцією сполук 10мл/хвилину протягом 60 хвилин. Однохвилинні формули (І), як-то проліки. Проліками є, наприфракції збирали та всі фракції аналізували елекклад, метилові, (півалоїлокси)метилові естери та торорозпилювальною мас спектрометрією. Ідентичні фракції комбінували. Комбінували фракції 51 25 85199 26 58, які містили пептиди, що стосувалися Сполук 1 Сполука 4: MC: (позитивна IEP) [М+Н]+ m/z та 2 (Фракція А; 65мг). Цю пептидну Фракцію А 840. 1H та 13C ЯМР (d6-ДМСО): див. Таблицю 4. подалі очищали РФ ВЕРХ на колонці YMC C18 Сполука 5: MC: (позитивна IEP) [М+Н]+ m/z 860, 862. 1H та 13C Я МР (d6-ДМСО): див. Таблицю 5мкМ, 20мм´150мм елююванням 65% водою (яка 5. містить 1% TFA) та 35% MeCN (який містить 1% Сполука 6: MC: (позитивна IEP) [М+Н]+ m/z TFA) при швидкості потоку 10мл/хвилин. Двана861, 863. 1H та 13C Я МР (d6-ДМСО): див. Таблицю дцятисекундні фракції збирали 36 хвилин. Фракції 58-60 були чистою Сполукою 2 (11мг), фракції 676. Сполука 7: MC: (позитивна IEP) [М+Н]+ m/z 69 були чистою Сполукою 1 (11мг), фракції 70-72 895, 897.1H та 13C ЯМР (d6-ДМСО): див. Таблицю були чистою Сполукою 3 (2мг), фракції 73-77 були 7. чистою Сполукою 7 (11.2мг), фракції 79-82 були Сполука 8: MC: (позитивна IEP) [М+Н]+ m/z чистою Сполукою 4 (7.29мг), фракції 91-96 були чистою Сполукою 8 (8.75мг), фракції 101-106 були 909, 911.1H та 13C ЯМР (d6-ДМСО): див. Таблицю 8. чистою Сполукою 9 (6.02мг), фракції 118-125 були Сполука 9: MC: (позитивна IEP) [М+Н]+ m/z чистою Сполукою 5 (2.08мг), фракції 128-138 були 909, 911. 1H та 13C Я МР (d6-ДМСО): див. Таблицю чистою Сполукою 10 (5.73мг) та фракції 140-150 9. були чистою Сполукою 6 (5.94мг). Сполука 1: MC: (позитивна IEP) [М+Н]+ m/z Сполука 10: MC: (позитивна IEP) [М+Н]+ m/z 1 13 973, 975, 977. 1H та 13C ЯМР (d6-ДМСО): див. Таб826. H та C ЯМР (d6-ДМСО): див. Таблицю 1. + лицю 10. Сполука 2: MC: (позитивна IEP) [М+Н] m/z Після широких досліджень, охоплюючих ви876, 878. 1H та 13C Я МР (d6-ДМСО): див. Таблицю пробування 1H, gHSQC, gHMBC та gCOSY, Сполу2. Сполука 3: MC: (позитивна DEP) [М+Н]+ m/z ки 1-10 ідентифіковано як циклічні пептиди. Повну стереохімію Сполуки 1 підтверджували рентгено890, 892. 1H та 13C Я МР (d6-ДМСО): див. Таблицю дифрактометрією монокристалу. 3. Таблиця 1 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 1 у d6-ДМСО № атому N-Метил лейцин 1 2 3 4 5 6 NMe Лейцин 8 9 13 C (мультиплетність)а 169.3 (s) 58.2 (d) 36.6 (t) 1 H (мультиплетність, J Гц) 2,3 JCH кореляції COSY 24.3 (d) 22.2 (q) 23.1 (q) 27.6 (q) 4.72 (dd, 5.9, 8.8Гц, 1H) 1.22 (m, 1H) 1.63 (m, 1H) 1.34 (m, 1H) 0.85 (d, 6.8Гц, 3H) 0.82 (d, 6.8Гц, 3H) 1.81 (s, 3H) 1, 3, 4, 7-NMe, 8 Н3а, Н3b 1, 2, 5, 6 Н2, Н3b, Н4 2, 4, 5, 6 Н2, Н3а, Н4 2, 3, 5, 6 Н3а, Н3b, Н5, Н6 3, 4, 6 Н4 3, 4, 5 Н4 2, 8 172.8 (s) 45.7 (d) 4.77 (ddd, 2.9, 4.9, 9.8Гц, 1H) 10, 11, 8 H10a, H10b, Н14 27 1 2 85199 28 Продовження таблиці 1 24.7 (d) 21.6 (q) 22.9 (q) 3 1.66 (m, 1H) 1.17 (m, 1H) 1.82 (m, 1H) 0.87 (d, 6.8Гц, 3H) 0.91 (d, 6.8Гц, 3H) 8.73 (d, 4.9Гц, 1H) 4 10 10, 11, 13 10,11,12 10, 15, 16 5 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12, Н13 H11 H11 Н9 174.1 (s) 47.9 (d) 16.7 (q) 4.20 (dq, 7.8, 7.8Гц, 1H) 1.30 (d, 7.8Гц, 3H) 7.20 (d, 4.9Гц, 1H) 15, 17 15, 16 19, 20, 16, 17 H17, H18 Н16 Н16 172.7 (s) 54.6 (d) 32.5 (t) 20.3 (t) 3.92 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.65 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.75 (m, 1H) 3.58 (m, 1H) 7.44 (dd, 1.2, 7.8Гц, 1H) 6.45 (d, 6.8Гц, 1H) 19, 21, 22, 40 27 22, 23 27 39, 20, 21 Н21, Н26 Н20, Н22а, Н22b Н21, Н22b, Н23 Н21, Н22а, Н23 Н22а, Н22b, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b Н20 4.40 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.88 (dd, 11.7, 13.7Гц, 1H) 3.35 (dd, 2.9, 13.7Гц, 1H) 6.68 (bs, 1H) 10.80 (bs, 1H) 7.24 (d, 7.8Гц, 1H) 7.00 (dd, 7.8, 7.8Гц, 1H) 6.92 (dd, 7.8, 7.8Гц, 1H) 7.20 (d, 7.8Гц, 1H) 8.62 (d, 8.8Гц, 1H) 1,27,30 28, 27, 30, 31, 38 28, 27, 30, 31, 38 29, 30, 33, 38 30, 31, 33, 38 36, 38 33, 37 34, 38 35, 33 1, 28, 29 Н29а, H29b, H39 Н28, Н29b Н28, Н29а Н32 Н31 Н35, Н36 Н34, Н36 Н35, Н37 Н36, Н35 Н28 6.42 (d, 7.8Гц, 1H) 4.05 (ddd, 5.9, 7.8, 7.8Гц, 1H) 1.52 (m, 1H) 1.69 (m, 1H) 1.40 (m, 2H) 3.06 (dt, 5.9, 5.9Гц, 2H) 7.64 (t, 5.9Гц, 1H) 43, 42, 48, 40 41, 43, 44, 48 43, 44, 47 45,47 Н42 Н41, Н43а, Н43b Н42, Н44, Н43b Н42, Н43а, Н44 Н43а, H43b, H45 Н45, Н46 H45 10 39.8 (t) 11 12 13 14 аланін 15 16 17 18 лізин 19 20 21 22 23 24 28.3 (t) 38.0 (t) 25 26 триптофан 27 28 29 30 31 32 33 34 35 36 37 38 39 40 аргігнін 41 42 43 110.4(s) 124.0 (d) 136.5 (s) 111.5 (d) 121.0 (d) 118.5 (d) 116.9(d) 127.0 (s) 44 45 46 47 48 25.1 (t) 40.0 (t) 171.4 (s) 53.9 (d) 27.9 (t) 157.5 (s) 52.9 (d) 29.1 (t) 156.9 (s) 175.1 (s) а Хімічні зсуви визначали з 2D гетероядерних експериментів Таблиця 2 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 2 у d6-ДМСО № атому 13 C (мультиплетність)а N- Метил лейцин 1 169.4(s) 2 58.4 (d) 3 36.5 (t) 1 H (мультиплетність, J Гц) 4.72 (dd, 5.9, 7.8Гц, 1H) 1.22 (m, 1H) 1.63 (m, 1H) 2,3 JCH кореляції 1, 3, 4, 8, 7-N Me 2, 4, 5, 6 2, 4, 5, 6 COSY Н3a, Н3b Н2, Н3b, Н4 Н2, Н3a, Н4 29 85199 30 Продовження таблиці 2 1 4 5 6 NMe Лейцин 8 9 10 2 3 1.32 (m, 1Н) 0.86 (d, 6.8Гц, 3H) 0.83 (d, 6.8Гц, 3H) 1.80 (s, 3H) 4 2, 3, 5, 6 3, 4, 6 3, 4, 5 2, 8 5 Н3a, Н3b, Н5, Н6 Н4 Н4 4.77 (ddd, 2.9, 4.9, 9.8Гц, 1H) 1.66 (m, 1H) 1.17 (m, 1H) 1.82 (m, 1H) 0.88 (d, 6.8Гц, 3H) 0.93 (d, 6.8Гц, 3H) 8.74 (d, 5.9Гц, 1H) 10, 11, 13 10, 11, 12 9, 10, 15 H10a, H10b, Н14 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12, Н13 H11 H11 Н9 174.0 (s) 48.0 (d) 16.8 (q) 4.17 (dq, 3.8, 6.8Гц, 1H) 1.29 (d, 6.8Гц, 3H) 7.16 (d, 3.9Гц, 1H) 15, 17 15, 16 19, 16, 17 Н17, Н18 Н16 Н16 172.5 (s) 53.9 (d) 32.9 (t) 20.1 (t) 3.92 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.57 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.75 (m, 1H) 3.56 (m, 1H) 7.45 (dd, 1.2,6.8Гц, 1Н) 6.45 (d, 6.8Гц, 1H) 19, 21, 22, 40 27, 19 Н21, Н26 Н20, Н22а, Н22b Н21, Н22b, Н23 Н21, Н22а, Н23 Н22а, Н22b, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b Н20 4.38 (ddd, 2.9, 8.8, 12.7Гц, 1H) 2.83 (dd, 12.7, 12.7Гц, 1H) 3.31 (dd, 2.9,12.7Гц, 1H) 6.60 (bs, 1H) 10.60 (bs, 1H) 7.20 (s, 1H) 7.01 (s, 1H) 8.64 (d, 9,8Гц, 1H) 28, 27, 30, 31, 38 28, 27, 30, 31, 38 29, 30, 33, 38 30, 31, 33, 38 35,36,38 30, 35, 33, 36 1 Н29а, H29b, H39 Н28, Н29b Н28, Н29а Н32 Н31 Н28 6.36 (d, 5.6Гц, 1H) 4.07 (ddd. 5.6, 7.8, 7.8Гц, 1H) 1.52 (m, 1H) 1.69 (m, 1H) 1.46 (m, 2H) 3.06 (m, 2H) 7.53 (m, 1H) 41, 42, 47 43, 44, 48 43, 44, 47 45,47 Н42 Н41, Н43а, H43b Н42, H43b, H44 Н42, Н43а, Н44 Н43а, H43b, H45 Н46, Н45 Н45 23.8 (d) 22.1 (q) 22.8 (q) 27.7 (q) 172.9 (s) 47.8 (d) 39.9 (t) 11 12 13 14 аланін 15 16 17 18 лізин 19 20 21 22 23.4 (d) 22.5 (q) 23.0 (q) 23 24 28.1 (t) 37.0 (t) 25 26 триптофан 27 28 29 30 31 32 33 34 35 36 37 38 39 40 аргігнін 41 42 43 109.3 (s) 124.1 (d) 131.1 (s) 111.1 (d) 115.0 (s) 145.9 (s) 102.1 (d) 126.3 (s) 157.7(s) 44 45 46 47 48 25.3 (t) 40.7 (t) 157.0 (s) 174.5 (s) а 170.6(s) 53.7 (d) 27.9 (t) 52.7 (d) 29.2 (t) Хімічні зсуви визначали з 2D гетероядерних експериментів 31 85199 32 Таблиця 3 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 3 у d6-ДМСО 13 C (мультиплетність)а № атому N-Метил лейцин 1 2 3 168.9(s) 57.2 (d) 35.9 (t) 1 H (мультиплетність, J Гц) 2,3 JCH кореляції COSY 4.77 (dd, 5.9, 8.8Гц, 1H) 1.20 (m, 1H) 1.71 (m, 1H) 1.35 (m, 1H) 0.85 (d, 6.8Гц, 3H) 0.88 (d, 6.8Гц, 3H) 1.87 (s, 3H) 8 3, 4, 6 3, 4, 5 2, 8 Н3a, Н3b Н2, Н3b, Н4 Н2, Н3a, Н4 Н3a, Н3b, Н5, Н6 Н4 Н4 10, 11, 13 10, 11, 12 15 H10a, H10b, Н14 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12, Н13 H11 H11 Н9 4 5 6 NMe Лейцин 8 9 10 24.2 (d) 23.0 (q) 23.3 (q) 26.9 (q) 11 12 13 14 аланін 15 16 17 18 лізин 19 20 21 22 24.1 (d) 21.5(q) 23.0 (q) 4.79 (ddd, 2.9, 4.9, 9.8Гц, 1H) 1.70 (m, 1H) 1.22 (m, 1H) 1.84 (m, 1H) 0.90 (d, 6.8Гц, 3H) 0.95 (d, 6.8Гц, 3H) 8.76 (d, 4.9Гц, 1H) 173.6 (s) 47.5 (d) 16.5 (q) 4.19 (dq, 5.8, 6.8Гц, 1H) 1.32 (d, 6.8Гц, 3H) 7.22 (d, 5.9Гц, 1H) 15, 16 19 Н17, Н18 Н16 Н16 171.9 (s) 54.2 (d) 31.7 (t) 20.1 (t) 23 24 27.2 (t) 38.1 (t) 25 26 триптофан 27 28 29 3.94 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.60 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.78 (m, 1H) 3.60 (m, 1H) 7.42 (dd, 1.2, 7.8Гц, 1H) 6.31 (d, 6.8Гц, 1H) 19,21,22 27 27 40 Н21, Н26 Н20, Н22а, Н22b Н21, H22b, H23 Н21,Н22а,Н23 Н22а, Н22b, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b Н20 30 31 32 33 34 35 36 37 38 39 40 аргігнін 41 42 43 109.4 (s) 124.5 (d) 130.4 (s) 111.2 (d) 115.3 (s) 145.6 (s) 102.5 (d) 125.9 (s) 157.2 (s) 4.39 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.86 (dd, 11.7, 13.7Гц, 1H) 3.27 (dd, 2.9, 13.7Гц, 1H) 6.62 (bs, 1H) 10.65 (bs, 1H) 7.22 (s, 1H) 7.00 (s, 1H) 8.67 (d, 8.8Гц, 1H) 28, 27, 30, 31, 38 28, 27, 30, 31, 38 29, 30, 33, 38 30, 31, 33, 38 36, 38 30, 35, 33 Н29а, H29b, H39 Н28, Н29b Н28, Н29а Н32 Н31 Н28 44 45 24.9 (t) 39.7 (t) 6.50 (d, 7.8Гц, 1H) 4.05 (ddd, 5.9, 7.8, 7.8Гц, 1H) 1.56 (m, 1H) 1.74 (m, 1H) 1.46 (m, 2H) 3.09 (dt, 5.9, 5.9Гц, 2H) 40 47 47 Н42 Н41, Н43а, Н43b Н42, H43b, H44 Н42, Н43а, Н44 Н43а, H43b, H45 Н46, Н45 172.2 (s) 47.8 (d) 39.4 (t) 172.8 (s) 53.7 (d) 27.9 (t) 51.9(d) 28.7 (t) 33 85199 34 Продовження таблиці 3 1 46 47 48 48-Me 2 156.4 (s) 173.1 (s) 51.8 (q) 3 7.42 (t, 5.9Гц, 1H) 3.62 (s, 3H) 4 47 48 5 Н45 а Хімічні зсуви визначали з 2D гетероядерних експериментів Таблиця 4 1 H (600МГц), 13C (125МГц), та COSY Дані ЯМР для Сполуки 4 у d6-ДМСО № атому N-Метил лейцин 1 2 3 13 C (мультиплетність)а н.с. 57.9 (d) 36.1 (t) 1 H (мультиплетність, J Гц) COSY 4.78 (dd, 5.9, 8.8Гц, 1H) 1.27 (m, 1H) 1.68 (m, 1H) 1.37 (m, 1H) 0.79 (d, 6.8Гц, 3H) 0.83 (d, 6.8Гц, 3H) 1.81 (s, 3H) Н3a, Н3b Н2, Н3b, Н4 Н2, Н3a, Н4 Н3a, Н3b, Н5, Н6 Н4 Н4 H10a, H10b, Н14 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12,Н13 H11 Н11 Н9 4 5 6 NMe Лейцин 8 9 10 24.1 (d) 23.7 (q) 20.9 (q) 27.3 (q) 11 12 13 14 аланін 15 16 17 18 лізин 19 20 21 22 24.2 (d) 20.7 (q) 23.9 (q) 4.78 (ddd, 2.9, 4.9, 9.8Гц, 1H) 1.63 (m, 1H) 1.25 (m, 1H) 1.83 (m, 1H) 0.84 (d, 6.8Гц, 3H) 0.91 (d, 6.8Гц, 1H) 8.79 (d, 4.9Гц, 1H) н.с. 47.3 (d) 16.2 (q) 4.19 (dq, 7.8, 7.8Гц, 1H) 1.33 (d, 7.8Гц, 3H) 7.29 (d, 4.9Гц, 1H) Н17, Н18 Н16 Н16 н.с. 54.3 (d) 32.1 (t) 21.1 (t) 23 24 28.1 (t) 38.1 (t) 25 26 триптофан 27 28 29 3.87 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.60 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.75 (m, 1H) 3.59 (m, 1H) 7.41 (dd, 1.2, 7.8Гц, 1H) 6.39 (d, 6.8Гц, 1H) Н21, Н26 Н20, Н22а, Н22b Н21, Н22b, Н23 Н21, Н22а, Н23 Н22а, Н22b, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b Н20 30 31 32 33 34 35 36 37 38 39 н.с. 124.5 (d) 4.38 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.81 (dd, 11.7,13.7Гц, 1H) 3.37 (dd, 2.9, 13.7Гц, 1H) 6.72 (bs, 1H) 10.80 (bs, 1H) 7.37 (d, 7.8Гц, 1H) 6.89 (dd, 7.8, 7.8Гц, 1H) 7.00 (dd, 7.8, 7.8Гц, 1H) 7.21 (d, 7.8Гц, 1H) 8.64 (d, 8.8Гц, 1H) Н29а, H29b, H39 Н28, Н29b Н28, Н29а Н32 Н31 Н35 Н34, Н36 Н35, Н37 Н36, Н35 Н28 н.с. 47.0 (d) 40.0 (t) н.с. 53.8 (d) 27.6 (t) н.с. 111.2 (d) 120.2 (d) 121.0 (d) 117.8(d) н.с. 35 85199 36 Продовження таблиці 4 1 2 3 4 40 аргігнін 41 42 43 н.с. 52.2 (d) 28.0 (t) 44 45 46 47 48 48-Me 24.7 (t) 40.1 (t) н.с. н.с. 52.1 (q) 6.49 (d, 7.8Гц, 1H) 4.19 (ddd, 5.9,7.8, 7.8Гц, 1H) 1.52 (m, 1H) 1.71 (m, 1H) 1.40 (m, 2H) 3.07 (dt, 5.9, 5.9Гц, 2H) 7.42 (t, 5.9Гц, 1H) Н42 Н41, Н43а, Н43b Н42, H43b, H44 Н42, Н43а, Н44 Н43а, H43b, H45 Н46, Н45 Н45 3.58 (s, 3H) а Хімічні зсуви визначали з 2D гетероядерних експериментів н.с.=не спостерігали Таблиця 5 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 5 у d6-ДМСО 13 C (мультиплетність)а № атому N-Метил лейцин 1 2 3 168.9 (s) 57.5 (d) 36.6 (t) 1 H (мультиплетність, J ГЦ) 2,3 JCH кореляції COSY 4.76 (dd, 5.9, 8.8Гц, 1H) 1.27 (m, 1H) 1.65 (m, 1H) 1.34 (m, 1H) 0.82 (d, 6.8Гц, 3H) 0.84 (d, 6.8Гц, 3H) 1.77 (s, 3H) 1, 3, 8, 7-NMe 3, 4, 6 3, 4, 5 2, 8 Н3a, Н3b Н2, Н3b, Н4 Н2, Н3a, Н4 Н3a, Н3b, Н5, Н6 Н4 Н4 9, 11 10, 11, 13 10, 11, 12 9, 10, 15 H10a, H10b, Н14 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12, Н13 H11 H11 Н9 4 5 6 NMe Лейцин 8 9 10 24.4 (d) 23.7 (q) 21.2 (q) 27.5 (q) 11 12 13 14 аланін 15 16 17 18 лізин 19 20 21 22 24.5 (d) 21.4 (q) 23.0 (q) 4.77 (ddd, 2.9, 4.9, 9.8Гц, 1H) 1.68 (m, 1H) 1.22 (m, 1H) 1.82 (m, 1H) 0.86 (d, 6.8Гц, 3H) 0.90 (d, 6.8Гц, 3H) 8.77 (d, 4.9Гц, 1H) 173.8 (s) 48.2 (d) 16.8 (q) 4.16 (dq, 4.9, 7.8Гц, 1H) 1.27 (d, 7.8Гц, 3H) 7.18 (d, 4.9Гц, 1H) 15, 17 15, 16 19 H17, H18 Н16 Н16 172.3 (s) 54.1 (d) 32.1 (t) 20.6 (t) 23 24 27.1 (t) 38.1 (t) 25 26 триптофан 27 28 29 3.91 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.60 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.76 (m, 1H) 3.53 (m, 1H) 7.50 (dd, 1.2, 7.8Гц, 1H) 6.36 (d, 6.8Гц, 1H) 19, 21, 22 40 Н21, Н26 Н20, Н22а, Н22b Н21, Н22b, Н23 Н21, Н22а, Н23 Н22а, Н22b, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b Н20 173.5 (s) 53.8 (d) 27.7 (t) 4.41 (ddd, 2.9, 9.6, 11.7Гц, 1H) 2.90 (dd, 11.7,13.7 1H) 30, 31, 38 Н29а, H29b, H39 Н28, H29b 172.6 (s) 46.8 (d) 40.0 (t) 37 85199 38 Продовження таблиці 5 1 2 30 31 32 33 34 35 36 37 38 39 40 аргігнін 41 42 43 110.9 (s) 124.9 (d) 136.7 (s) 111.3 (d) 125.8 (s) 118.7 (d) 118.3 (d) 125.5 (s) 44 25.1 (t) 45 46 47 48 40.5 (t) 156.8 (s) 174.3 (s) 157.5 (s) 52.6 (d) 29.5 (t) 3 3.30 (dd, 2.9, 13.7Гц, 1H) 6.78 (bs, 1H) 11.00 (bs, 1H) 7.30 (d, 1.8Гц, 1H) 6.93 (dd, 7.8, 1.8Гц, 1H) 7.42 (d, 7.8Гц, 1H) 8.64 (d, 9.6Гц, 1H) 4 30, 31, 38 29, 30, 33, 38 30, 31, 33, 38 36, 38 38, 34 35, 33 1 H28, H29a H32 H31 H36 H34, H37 H36 H28 6.37 (d, 7.8Гц, 1H) 4.05 (ddd, 5.9, 7.8, 7.8Гц, 1H) 1.50 (m, 1H) 1.67 (m, 1H) 1.40 (m, 1H) 1.19 (m, 1H) 3.06 (m, 2H) 7.50 (m, 1H) 40 43, 44, 48 H42 H41, H43a, H43b Н42, H43b, H44 H42, H43a, H44 H43a, H43b, H45 47 Н44, Н46 Н45 а Хімічні зсуви визначали з 2D 5 етеро ядерних експериментів Сполука 6 Таблиця 6 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 6 у d6-ДМСО № атому N-Метил лейцин 1 2 3 4 5 6 Nme Лейцин 8 13 C (мультиплетність)а 169.4 (s) 58.0 (d) 36.2 (t) 1 H (мультиплетність, J Гц) 2,3 JCH кореляції COSY 23.0 (d) 23.7 (q) 24.0 (q) 27.0 (q) 4.72 (dd, 5.9, 8.8Гц, 1H) 1.25 (m, 1H) 1.60 (m, 1H) 1.93 (m, 1H) 0.82 (d, 6.8Гц, 3H) 0.82 (d, 6.8Гц, 3H) 1.90 (s, 3H) 1, 3, 4, 8, 7-Nme 1, 2, 4 2, 4 2, 3 3, 4, 6 3, 4, 5 2, 8 Н3a, Н3b Н2, Н3b, Н4 Н2, Н3a, Н4 Н3a, Н3b, Н5, Н6 Н4 Н4 172.5 (s) 39 85199 40 Продовження таблиці 6 1 2 9 10 47.8 (d) 39.2 (t) 11 12 13 14 валін 15 16 17 18 19 20 лізин 21 22 23 24 27.0 (d) 21.0 (q) 24.9 (q) 25 26 28.1 (t) 38.1 (t) 27 28 триптофан 29 30 31 32 33 34 35 36 37 38 39 40 41 42 ізолейцин 43 44 45 46 109.5 (s) 125.5 (d) 130.4 (s) 111.1 (d) 115.0 (s) 146.3 (s) 102.3 (d) 126.0 (s) 157.6 (s) 47 48 49 11.7 (q) 15.4 (q) 173.7 (s) а 3 4.70 (ddd, 2.9, 4.9, 9.8Гц, 1H) 1.70 (m, 1H) 1.22 (m, 1H) 1.82 (m, 1H) 0.84 (d, 6.8Гц, 3H) 0.96 (d, 6.8Гц, 3H) 8.69 (d, 4.9Гц, 1H) 4 10, 11, 13 10, 11, 12 9, 10, 15 5 H10a, H10b, Н14 Н9, H10b, H11 Н9, H10a, H11 H10a, H10b, Н12, Н13 H11 H11 Н9 172.7(s) 57.8 (d) 29.7 (d) 19.4 (q) 19.0 (q) 3.92 (dd, 5.8, 7.8Гц, 1H) 1.95 (m, 1H) 0.85 (d, 7.8Гц, 3H) 1.05 (d, 7.8Гц, 3H) 6.80 (d, 5.9Гц, 1H) 16, 18, 19 16, 17, 19 16, 17, 18 16, 17, 19 Н17, Н20 Н16, Н18, Н19 Н17 Н17 Н16 172.5 (s) 54.8 (d) 31.5 (t) 20.1 (t) 3.91 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.60 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 1.40 (m, 2H) 2.80 (m, 1H) 3.61 (m, 1H) 7.40 (dd, 1.2, 7.8Гц, 1H) 6.47 (d, 5.9Гц, 1H) 19, 21, 22, 42 27 27 42, 22, 23 Н23, Н28 Н22, Н24а, Н24b Н23, H24b, H25 Н23, Н24а, Н25 Н24а, Н24b, Н26а, Н26b Н25, H26b, H27 Н25, Н26а, Н27 Н26а, Н26b Н22 4.41 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.90 (dd, 11.7,13.7Гц, 1H) 3.40 (dd, 2.9, 13.7Гц, 1H) 6.65 (bs, 1H) 10.64 (bs, 1H) 7.20 (s, 1H) 7.00 (s, 1H) 8.77 (d, 8.8Гц, 1H) 29, 33, 32, 30 30, 32, 33 29, 30,35, 40 32, 33, 35, 40 33, 37, 38, 40 35, 33, 32, 37, 38 1 Н31а, Н31b, Н41 Н30, Н31b Н30, Н31а Н34 H33 H30 6.35 (d, 7.8Гц, 1H) 4.06 (dd, 5.9, 7.8Гц, 1H) 1.70 (m, 1H) 1.40 (m, 1H) 1.15 (m, 1H) 0.82 (t, 6.8Гц, 3H) 0.84 (d, 6.8Гц, 3H) 42 42, 45, 46,48, 49 44, 47, 48 44, 47, 48 45, 46 44, 45, 46 Н44 Н43, Н45 Н44, Н46b, Н46а, Н48 H46b, H47, Н45 Н47, Н45, Н46а Н46а, Н46b Н45 171.6(s) 53.2 (d) 27.9 (t) 56.9 (d) 36.8 (d) 24.7 (t) Хімічні зсуви визначали з 2D гетероядерних експериментів 41 85199 42 Таблиця 7 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 7 у d6-ДМСО № атому 13 C (мультиплетність)a 1 H (мультиплетність, J Гц) 2,3 JCH кореляції COSY N-Метил триптофан 1 169.8 (s) 2 61.0 (d) 4.66 (dd, 2.6, 10.4Гц, 1H) 3 22.3 (t) 4 5 6 7 8 9 10 11 12 NMe Лейцин 14 15 16 108.9 (s) 124.3 (d) 130.7 (s) 111.8 (d) 115.8 (s) 145.8 (s) 102.7 (d) 126.8 (s) 27.5 (q) 2.73 (m, 1H) 3.07 (m, 1H) 6.87 (bs, 1H) 10.66 (bs, 1H) 7.26 (s, 1H) 6.98 (s, 1H) 1.91 (s, 3H) 1, 3, 4, 14, 13Н3a, Н3b NMe 1, 5, 4, 2, 12 Н2, Н3b 2, 4, 5, 12 Н2, Н3a 3, 4, 7, 12 Н6 4, 5, 7, 12 Н5 7, 9, 10, 12 4, 7, 9,10,12 2, 14 17 18 19 20 валін 21 22 23 24 25 26 лізин 27 28 29 30 24.8 (d) 19.7 (q) 22.0 (q) 4.21 (ddd, 2.9, 4.9, 9.8Гц, 1H) -0.50 (dd, 11.7, 11.7Гц, 1H) 0.90 (m, 1H) 1.40 (m, 1H) 0.26 (d, 6.8Гц, 3H) 0.40 (d, 6.8Гц, 3H) 8.42 (d, 4.3Гц, 1H) 16, 21 14, 17, 18 16, 17, 19 16, 17, 18 15, 16, 21 Н16а, Н16b, Н20 Н15, Н16b, Н17 Н15, Н16а, Н17 Н16а, H16b, H18, Н19 Н17 H17 Н15 172.2 (s) 57.6 (d) 30.0 (d) 18.9 (q) 18.8 (q) 3.79 (dd, 6.9, 7.8Гц, 1H) 1.90 (m, 1H) 0.86 (d, 7.8Гц, 3H) 0.93 (d, 7.8Гц, 3H) 6.74 (d, 6.9Гц, 1H) 23, 24, 25 22, 24, 25 22, 23, 25 22, 23, 24 22, 23, 27 Н23, Н26 Н22, Н24, Н25 Н23 Н23 Н22 171.9 (s) 53.8 (d) 31.3 (t) 20.2 (t) 3.86 (ddd, 5.9, 6.9, 6.8Гц, 1H) 1.54 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 27, 29, 30,45 Н29, Н34 Н28, Н34 Н29, Н30b, Н31 Н29, Н30а, Н31 172.5 (s) 46.9 (d) 36.9 (t) 43 1 85199 2 31 32 28.2 (t) 37.9 (t) 33 34 фенілаланін 35 36 37 38 39 40 41 42 43 44 45 ізолейцин 46 47 48 49 138.6 (s) 128.9 (d) 127.9 (d) 126.2 (d) 127.9 (d) 128.29 (d) 157.3 (s) 50 51 52 11.1 (q) 15.6 (q) 173.8 (s) 171.0(s) 54.8 (d) 37.9 (t) 56.6 (d) 36.9 (d) 24.5 (t) 44 Продовження таблиці 7 3 1.40 (m, 2H) 2.86 (m, 1H) 3.58 (m, 1H) 7.40 (dd, 1.2, 7.8Гц, 1H) 6.43 (d, 6.9Гц, 1H) 4 35 30, 31, 35 32, 35 27, 29, 45 5 H30а, H30b, Н32а, Н32b Н31, Н32b, H33 Н31, Н32а, H33 Н32а, Н32b Н28 4.57 (ddd, 2.9, 9.5, 11.7Гц, 1H) 2.75 (dd, 11.7, 13.7 1H) 3.40 (dd, 2.9,13.7Гц, 1H) 7.07 (d, 7.8Гц, 1H) 7.22 (dd, 7.8, 7.8Гц, 1H) 7.15 (t, 7.8Гц, 1H) 7.22 (dd, 7.8, 7.8Гц, 1H) 7.07 (d, 7.8Гц, 1H) 8.76 (d, 9.5Гц, 1H) 1, 35, 37 35, 36, 38, 39, 43 36, 38, 39, 43 37, 38, 41, 43 38, 42 39, 43 38, 40 37, 38, 39, 41 1, 36, 37 Н37а, H37b, H44 Н36, Н37b Н36, Н37а Н40, Н41 Н39, Н41 Н40, Н42 Н41, Н43 Н42 Н36 6.28 (d, 8.7Гц, 1H) 4.04 (dd, 5.9, 7.8, 7.8Гц, 1H) 1.71 (m, 1H) 1.35 (m, 1H) 1.10 (m, 1H) 0.83 (t, 6.8Гц, 3H) 0.82 (d, 6.8Гц, 3H) 45, 47, 52 45, 48, 49, 51, 52 47, 49, 50, 51 47, 48, 50, 51 47, 48, 50, 51 48, 49 47, 48, 49 Н47 Н46, Н48 H47, H49b, H51 Н48, H49b, H50 Н48, Н49а, Н50 Н49а, H49b Н48 а Хімічні зсуви визначали з 2D гетероядерних експериментів Таблиця 8 1 H (600МГц), 13C (125МГц) та COSY Дані ЯМР для Сполуки 8 у d6-ДМСО 13 № атому C (мультиплетність)а N-Метил триптофан 1 н.с. 2 60.8 (d) 3 21.9 (t) 4 н.с. 1 H (мультиплетність, J Гц) 4.65 (dd, 2.6, 9.9Гц, 1H) 2.73 (m, 1H) 3.08 (m, 1H) COSY Н3a, Н3b Н2, Н3b Н2, Н3a 45 1 5 6 7 8 9 10 11 12 NMe Лейцин 14 15 16 85199 2 124.7 (d) н.с. 111.5 (d) н.с. н.с. 103.4 (d) н.с. 27.4 (q) н.с. 47.4 (d) 37.0 (t) 17 18 19 20 ізолейцин 21 22 23 24 24.9 (d) 19.5 (q) 22.3 (q) 25 26 27 лізин 28 29 30 12.0 (q) 15.7 (q) 31 24.9 (t) 32 33 28.1 (t) 38.0 (t) 34 35 фенілаланін 36 37 38 39 40 41 42 43 44 45 46 ізолейцин 47 48 49 50 н.с. 128.3 (d) 128.0 (d) 125.9 (d) 128.0 (d) 128.3 (d) н.с. н.с. 55.8 (d) 37.0 (d) 24.2 (t) н.с. 54.3 (d) 31.8 (t) н.с. 54.5 (d) 37.4 (t) 56.3 (d) 38.3 (d) 22.8 (t) 46 Продовження таблиці 8 3 6.87 (d, 1.9Гц, 1H) 10.66 (bs, 1H) 7.23 (s, 1H) 6.94 (s, 1H) 1.90 (s, 3H) Н6 Н5 4.18 (ddd, 2.9,4.9, 9.8Гц, 1H) -0.50 (dd, 9.8, 9.8Гц, 1H) 0.91 (m, 1H) 1.40 (m, 1H) 0.22 (d, 6.8Гц, 3H) 0.36 (d, 6.8Гц, 3H) 8.40 (d, 4.8Гц, 1H) Н16а, H16b, H20 Н15, Н16b, Н17 Н15, Н16а, Н17 Н16а, Н16b, Н19, Н18 Н17 Н17 Н15 3.93 (dd, 7.8, 8.2Гц, 1H) 1.72 (m, 1H) 1.08 (m, 1H) 1.30 (m, 1H) 0.82 (d, 7.0Гц, 3H) 0.83 (d, 7.0Гц, 3H) 6.70 (d, 6.9Гц, 1H) Н23, Н27 Н22, Н24а, H24b, H26 H24b, H23, Н25 Н24а, Н23, Н25 Н24а, Н24b Н23 Н22 3.85 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.54 (m, 1H) 1.72 (m, 1H) 1.40 (m, 1H) 1.10 (m, 1Н) 1.40 (m, 2H) 2.80 (m, 1H) 3.55 (m, 1H) 7.43 (dd, 1.2, 8.8Гц, 1H) 6.45 (d, 6.8Гц, 1H) Н30, Н35 H29, H30b, H31a, H31b Н29, Н30а, Н31а, Н31b H32, H31b, H30a, H30b H32, H31a, H30a, H30b H31a, H31b, Н33a, Н33b Н32, Н33b, Н34 Н32, Н33a, Н34 Н33a, Н33b Н29 4.58 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.73 (dd, 11.7, 11.7Гц, 1H) 3.37 (dd, 2.9, 11.7Гц, 1H) 7.05 (d, 7.8Гц, 1H) 7.19 (dd, 7.8, 7.8Гц, 1H) 7.14 (t, 7.8Гц, 1H) 7.19 (dd, 7.8, 7.8Гц, 1H) 7.05 (d, 7.8Гц, 1H) 8.68 (d, 8.8Гц, 1H) Н38а, H38b, H45 Н37, Н38b Н37, Н38а Н41, Н42 Н40, Н42 Н41, Н43 Н42, Н44 Н43, Н42 Н37 6.29 (d, 8.8Гц, 1H) 4.01 (dd, 4.9, 7.8,Гц, 1H) 1.71 (m, 1H) 1.38 (m, H) 1.01 (m, 1H) 51 11.4 (q) 0.79 (t, 6.8Гц, 3H) 52 15.8 (q) 0.79 (d, 6.8Гц, 3H) 53 н.с. a Хімічні зсуви визначали з 2D гетероядерних експериментів н.с.=не спостерігали 4 Н48 Н47, Н49 Н48, Н50, H50b, H52 Н50b, Н49, Н51 Н50а,Н49,Н51 Н50а, Н50b Н49 47 85199 48 Сполука 9 Таблиця 9 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 9 у d6-ДМСО № атому N-Метил триптофан 1 2 3 13 C (мультиплетність)a 169.5 (s) 60.8 (d) 21.7 (t) 1 H (мультиплетність, J Гц) 2,3 JCH кореляції COSY 4.69 (dd, 2.6, 10.4Гц, 1H) 2.76 (m, 1H) 3.04 (m, 1H) 6.88 (bs, 1H) 10.66 (bs, 1H) 7.27 (s, 1H) 6.99 (s, 1H) 1.91 (s, 3H) 1 2, 4, 12 2,4,12 4, 7, 12 4, 5, 7, 12 9, 10, 12 4, 7, 9, 10 2, 14 Н3a, Н3b H2, H3b H2, H3a Н6 Н5 18 16, 17, 19 16, 17, 18 21 Н16а, Н16b, Н20 Н15, Н16b, Н17 Н15, Н16а, Н17 Н16а, H16b, H19, Н18 Н17 Н17 Н15 4 5 6 7 8 9 10 11 12 NMe Лейцин 14 15 16 108.9 (s) 124.3 (d) 17 18 19 20 лейцин 21 22 23 24 25 26 27 лізин 28 29 30 31 23.1 (d) 19.7 (q) 22.3 (q) 4.22 (ddd, 2.9, 4.9, 9.8Гц, 1H) -0.49 (dd, 9.8, 9.8Гц, 1H) 0.95 (m, 1H) 1.40 (m, 1H) 0.25 (d, 6.8Гц, 3H) 0.42 (d, 6.8Гц, 3H) 8.47 (d, 4.3Гц, 1H) 173.5 (s) 50.7 (d) 39.7 (t) 23.3 (d) 21.6 (q) 22.8 (q) 4.03 (td, 7.8, 6.9Гц, 1H) 1.46 (m, 2H) 1.67 (m, 1H) 0.82 (d, 7.0Гц, 3H) 0.88 (d, 7.0Гц, 3H) 6.86 (d, 6.9Гц, 1H) 21, 23 15, 16 23, 24, 26 23, 24, 25 28 Н23, Н27 Н22, Н24 Н23, Н25, Н26 Н24 Н24 Н22 172.2 (s) 54.4 (d) 32.1 (t) 20.2 (t) 3.88 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.54 (m, 2H) 1.40 (m, 1H) 28,30,31 Н30, Н35 Н29, Н31а, Н31b Н30, Н31b, Н32 Н30, Н31а, Н32 130.2 (s) 111.8 (d) 115.8 (s) 145.9 (s) 102.7 (d) 126.1 (s) 27.4 (q) 172.5 (s) 46.7 (d) 37.4 (t) 49 1 85199 2 32 33 51 52 53 11.7 (q) 15.8 (q) 173.8 (s) 56.9 (d) 37.6 (d) 24.6 (t) 5 Н30, Н22а, Н23 Н31а, Н31b, Н33a, Н33b Н32, Н33b, Н34 Н32, Н33a, Н34 Н33a, Н33b Н29 36 39, 40, 44 28, 27, 30, 31, 38 42, 44 39, 43 40, 44 39, 41 40, 38, 42 1 Н38а, H38b, H45 Н37, Н38b Н27, Н38а Н41, Н42 Н40, Н42 Н41, Н43, Н40, Н44 Н42, Н44 Н43, Н42 Н37 6.26 (d, 8.7Гц, 1H) 4.03 (dd, 5.9, 7.8, 7.8Гц, 1H) 1.70 (m, 1H) 1.35 (m, 1H) 1.10 (m, 1H) 0.86 (t, 6.8Гц, 3H) 0.85 (d, 6.8Гц, 3H) 138.3 (s) 128.7 (d) 129.2 (d) 126.6 (d) 129.2 (d) 128.7 (d) 157.0 (s) 171.4 (s) 54.5 (d) 37.9 (t) 46 4.52 (ddd, 2.9, 8.8, 11.7Гц, 1H) 2.74 (dd, 11.7, 13.7Гц, 1H) 3.55 (dd, 2.9, 13.7Гц, 1H) 7.08 (d, 8.0Гц, 1H) 7.23 (dd, 8.0, 8.0Гц, 1H) 7.17 (t, 8.0Гц, 1H) 7.23 (dd, 8.0, 8.0Гц, 1H) 7.08 (d, 8.0Гц, 1H) 8.71 (d, 8.8Гц, 1H) 39 40 41 42 43 44 45 46 ізолейцин 47 48 49 50 3 1.10 (m, 1H) 1.42 (m, 2H) 2.84 (m, 1H) 3.57 (m, 1H) 7.38 (dd, 1.2, 7.8Гц, 1H) 6.35 (d, 6.8Гц, 1H) 28.1 (t) 38.3 (t) 34 35 фенілаланін 36 37 38 50 Продовження таблиці 9 4 46, 49, 50, 52, 53 48, 49, 51, 52 49,51, 52 49, 50 48, 49, 50 Н48 Н47, Н49 Н48, Н50b, Н50а, Н52 Н49, Н50а, Н50b, Н51 Н49, Н50а, Н50b, Н51 Н50а, Н50b Н49 a Хімічні зсуви визначали з 2D гетероядерних експериментів Сполука 10 Таблиця 10 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 10 у d6-ДМСО № атому N-Метил триптофан 1 2 3 13 C (мультиплетність)а 169.8 (s) 60.9 (d) 21.9 (t) 1 H (мультиплетність, J Гц) 4.66 (dd, 2.9, 10.7Гц, 1H) 2.77 (m, 1H) 3.07 (m, 1H) 2,3 JCH кореляції 1, 3, 4, 14, 13-NMe 2, 4, 5 2, 4, 5 COSY Н3a, Н3b Н2, Н3b Н2, Н3a 51 85199 52 Продовження таблиці 10 1 4 5 6 7 8 9 10 11 12 NMe Лейцин 14 15 16 2 109.3 (s) 126.1 (d) 130.5 (s) 111.8 (d) 115.8 (s) 146.2 (s) 103.4 (d) 126.8 (s) 27.3 (q) 3 6.89 (d, 2.0Гц, 1H) 10.68 (bs, 1H) 7.26 (s, 1H) 6.98 (s, 1H) 1.97 (s, 3H) 4 4, 7, 12 4, 5, 7, 12 7, 9, 10, 12 4, 7, 92, 14 Н6 Н5 171.9 (s) 46.8 (d) 37.2 (t) 17 18 19 20 лейцин 21 22 23 24 25 26 лізин 27 28 29 30 23.3 (d) 19.5 (q) 21.3 (q) 4.21 (ddd, 2.9, 4.9,11.7Гц, 1H) -0.48 (dd, 11.7, 11.7Гц, 1H) 0.95 (m, 1H) 1.40 (m, 1H) 0.27 (d, 6.8Гц, 3H) 0.41 (d, 6.8Гц, 3H) 8.42 (d, 4.9Гц, 1H) 16, 17, 19 16, 17, 18 15, 16, 21 Н16а, H16b, H20 Н15, Н16b, Н17 Н15, Н16а, Н17 Н16а, H16b, H19, Н18 Н17 Н17 Н15 172.9 (s) 57.7 (d) 29.8 (t) 18.9 (q) 18.9 (q) 3.77 (dd, 6.8, 7.8Гц, 1H) 1.88 (m, 2H) 0.84 (d, 7.0Гц, 3H) 0.93 (d, 7.0Гц, 3H) 6.74 (d, 6.9Гц, 1H) 21, 23, 24, 25 22, 23, 25 22, 23, 24 23, 28 Н23, Н26 Н22, Н23, Н24 Н23 Н23 Н22 172.2 (s) 54.5 (d) 31.5 (t) 20.2 (t) 3.84 (ddd, 5.9, 6.8, 6.8Гц, 1H) 1.54 (m, 2H) 1.40 (m, 1H) 1.10 (m, 1H) 20, 28, 29, 45 31 28.2 (t) 1.42 (m, 2H) 32 38.3 (t) 33 34 фенілаланін 35 36 37 2.85 (m, 1H) 3.57 (m, 1H) 7.46 (dd, 1.2, 7.0Гц, 1H) 6.41 (d, 6.8Гц, 1H) 30,31 35 29, 28, 45 Н29, Н34 Н28, H30а, H30b Н29, Н30b, Н31 Н29, Н30а, Н31 H30а, H30b, Н32а, Н32b Н31, Н32b, H33 Н31, Н32а, H33 Н32а, Н32b Н28 38 39 40 41 42 43 44 45 ізолейцин 46 47 48 49 137.9 (s) 131.4 (d) 130.4 (d) 119.2 (s) 130.4 (d) 131.4 (d) 157.3 (s) 4.52 (ddd, 2.9, 8.8,11.7Гц, 1H) 2.72 (dd, 11.7,13.7 1H) 3.36 (dd, 2.9, 13.7Гц, 1H) 7.01 (d, 7.8Гц, 1H) 7.37 (d, 7.8Гц, 1H) 7.39 (d, 7.8Гц, 1H) 7.08 (d, 7.8Гц, 1H) 8.81 (d, 8.8Гц, 1H) 35 36, 38, 39, 43 36, 38, 39, 43 37, 41, 43 42, 38 40, 38 37, 39, 41 Н37а, H37b, H44 Н36, Н37b Н36, Н37а Н40 Н39 Н43 Н42 Н36 45, 47 45, 48, 49, 51, 52 47, 48, 50, 51 47, 48, 50, 51 48, 49 47, 48, 49 Н47 Н48, Н46 Н47, Н49b, Н49а Н49а, Н48, Н50 H49b, H48, Н50 Н49а, Н49b Н48 170.4 (s) 54.1 (d) 37.2 (t) 57.2 (d) 37.2 (d) 25.1 (t) 6.26 (d, 8.8Гц, 1H) 4.04 (dd, 4.9, 8.8, 7.8Гц, 1H) 1.70 (m, 1H) 1.33 (m, 1H) 1.07 (m, 1H) 50 11.4(q) 0.83 (t, 6.8Гц, 3H) 51 15.8 (q) 0.83 (d, 6.8Гц, 3H) 52 174.5 (s) а Хімічні зсуви визначали з 2D гетероядерних експериментів 5 53 85199 Приклад 2 Цей приклад описує виділення Сполуки 11. Загальні експериментальні способи Воду фільтр ували MiIIi-Q, тоді як усі інші застосовані розчинники були від Omnisolv. Колонку Hypersil BDS C18 5мкМ, 21.2мм´150мм застосовували для препаративної ВЕРХ. Спектри ЯМР записували на спектрометрі ЯМР Varian Inova 600 або 500МГц. Зразки розчиняли в d6-ДМСО й хімічні зсуви розраховували відносно піку розчиннику (ДМСО 1H d 2.50 та 13C 39.5млн-1). Мас-спектри вимірювали на Fisons VG Platform II, застосовуючи режим електоророзпилювання з позитивною іонізацією. Розчинник для елюювання - суміш ацетонітрил/вода 50%, при 0.1мл/хвилину. Тваринний матеріал Шість зразків губки Candidaspongia flabellata збирали SCUBA зануренням Outer Gneering, Sunshine Coast, Old Reef, Fairfax Є та Chauvel Reef, Квінсленд, Австралія, та підтверджуючі зразки (G315106, G314580, G314025, G315402, G318260, G317513) знаходяться в Музеї Квінсленду, Брисбен, Австралія. Екстракція та Виділення Заморожено-висушені матеріали губки (529г) розмелювали та ретельно екстрагували метанолом, що дало шість метанольних екстрактів. Сирі метанольні екстракти розподіляли по серіям: МеОН/н-гексан, Н2О:МеОН(4:1)/ДХМ, 54 Н2O:МеOН(4:1)/EtOAc. Біоактивність розподіляли в шарах Н2О:МеОН(4:1) та EtOAc. Шари Н2О:МеОН(4:1) та EtOAc комбінували для всіх шести біот та потім розділяли Н2О/бутанолом. Активність була в шарі бутанолу (900мг), який потім піддавався протитечійній хроматографії {Н2О/МеОН/EtOAc (4:1:5)}, верхній шар - мобільна фаза. Найбільш ранні фракції елюювання, 13-24, комбінували (325мг) та розподіляли нгексан:EtOAc:МеОН:Н 2О (1:1:1:1). Потім біоактивний водний шар (150мг) хроматографували хроматографією із протитоком {(СНСl3:МеОН:Н 2О (7:13:8)}, нижній шар - мобільна фаза. Комбінували ранні активні фракції елювання, 25-32, що дало 85мг матеріалу. Його піддавали кінцевому очищенню ВЕРХ (H ypersil BDS C18), застосовуючи 30 хвилинний H2O/MeCN градієнт від H2O (яка містить 1% TFA) до MeCN (який містить 1% TFA). Після елюювання протягом 18.2 хвилин вихід Сполуки 11 дорівнював 0.4мг. Сполука 11: MC: (позитивна IEP) ) [М+Н]+ m/z 1003.0 (100), 1004.4 (72), 1005.4 (75), 1006.3 (32). 1 Н та 13C Я МР (d6-ДМСО): див. Таблицю 11. Сполуку 11 після детальних досліджень з охопленням експериментів 1H, 13C, gHSQC, gHMBC, та gCOSY також ідентифіковано як циклічний пептид. Сполукa 11 Таблиця 11 1 H (600МГц), 13C (125МГц), HMBC та COSY Дані ЯМР для Сполуки 11 у d6-ДМСО № атому 13 C (мультиплетність)a N-Метил триптофан 1 2 3 н.с. 60.0 (d) 22.4 (t) 4 5 6 7 8 9 10 н.с. 108.9 (s) 130.8 (s) 111.0 (d) 111.8 (d) 150.8 (s) 1 H (мультиплетність, J Гц) 4.70 (bd, 10.8Гц, 1H) 2.71 (dd, 14.5,10.8Гц, 1H) 3.14 (d, 14.5Гц, 1H) 11.33 (s, 1H) 7.05 (bd, 8 0Гц, 1H) 6.60 (bd, 8 0Гц, 1H) 2,3 JCH кореляції 4, 7, 12 12, 10 COSY Н3a, Н3b H2, H3b Н3a Н9 Н8 55 85199 56 Продовження таблиці 11 1 11 12 NMe Лейцин 14 15 16 2 101.8 (d) 128.1 (s) 28.5 (q) 17 18 19 20 Ізолейцин 21 22 23 24 22.4 (d) 19.0 (q) 22.1 (q) 25 26 27 Лізин 28 29 30 11.2 (q) 14.2 (q) 31 20.1 (t) 32 26.6 (t) 33 37.8 (t) 34 35 Тирозин 36 37 38 39 40 41 42 43 44 45 46 Фенілаланін 47 48 49 130.0 (s) 128.5 (d) 114.8 (d) 156.0 (s) 114.8(d) 128.5 (d) н.с. 50 51 52 53 54 55 56 ОН ОН 137.5 (s) 129.0 (d) 128.0 (d) 126.2 (d) 128.0 (d) 129.0 (d) 173.8(s) 172.4 (s) 46.8 (d) 36.6 (t) 171.6 (s) 55.7 (d) 35.7 (d) 24.7 (t) 172.4 (s) 54.3 (d) 31.0 (t) н.с. 54.7 (d) 36.5 (t) 53.4 (d) 37.2 (t) 3 4 5 6.82 (bs, 1H) 2.10 (s, 3H) 7, 10 2 4.16 (m, 1H) 0.32 (bt, 11.0Гц, 1H) 0.96 (m, 1H) а 1.42(m, 1H) 0.22 (d, 6.6Гц, 3H) 0.41 (d, 6.6Гц, 3H) 8.38 (d, 4.8Гц, 1H) 15 16, 17, 19 16, 17, 18 14 Н16а, Н16b, Н20 Н16b, Н17 Н15, Н16а Н17 Н17 Н15 3.99 (t,6.8Гц, 1H) 1.76 (m, 1H) 1.10 (m, 1H) а 1.44(m, 1H) 0.85 (t, 7.2Гц, 3H) 0.81 (d, 6.6Гц, 3H) 6.78 (d, 6.8Гц, 1H) 23, 26 21 23, 24 22 Н23, Н27 Н22, Н24а, Н26 Н23, H24b, H25 Н24а, Н25 Н24а, Н24b Н23 Н22 3.85 (ddd, 7.0, 6.5, 5.0Гц, 1Н) 28 1.52 (m, 1H) 1.60 (m, 1Н) 1.14 (m, 1H) 1.25 (m, 1H) 1.38 (m, 1H) 1.41 (m, 1H) 2.85 (m, 1H) 3.52 (m, 1H) 7.35 (m, 1H) 6.48 (d, 7.0Гц, 1H) H30а, H30b, Н35 Н29, Н31а Н29, Н31b H30а H30b Н33b Н34 Н34, Н32а Н33a, Н33b Н29 4.50 (ddd, 11.7,9.0,4.9Гц, 1H) 2.62 (bt, 13.0Гц, 1H) 39 а 3.23 (m, 1H) 39 6.87 (d, 7.5Гц, 1H) 38, 39, 42 6.62 (d, 7.5Гц, 1H) 40, 42, 44 6.62 (d, 7.5Гц, 1H) 40, 42, 44 6.87 (d, 7.5Гц, 1H) 38, 39, 42 8.54 (d, 9.0Гц, 1H) Н38а, H38b, H45 Н37, Н38b Н37, Н38а Н41 Н40 Н44 Н43 Н37 6.26 (d, 8.0Гц, 1H) 4.36 (ddd, 8.0, 7.5, 5.2Гц, 1H) 2.86 (dd, 13.8, 7.5Гц, 1H) 2.99 (dd, 13.8, 5.2Гц, 1H) 7.16 (4 7.5Гц, 1H) 7.27 (t, 7.5Гц, 1H) 7.20 (t, 7.5Гц, 1H) 7.27 (t, 7.5Гц, 1H) 7.16 (4 7.5Гц, 1H) 8.71 (s, 1H) 9.13 (s, 1H) Н48 Н49а, H49b, H47 Н48 Н48 Н52, Н54 Н51, Н55 Н51, Н55 Н52, Н54 56, 49 56, 55, 51, 50, 48 56, 55, 51, 50, 48 53, 49 50 51, 55 50 53, 49 57 85199 58 а Хімічний зсув визначено з 2D експериментів ЯМР н.с.=не спостерігали. Приклад 3 Цей приклад описує синтез Сполуки 12. Загальні експериментальні способи Мас-спектр високого розділення записували на мас-спектрометрі Micromass LCT оснащеним інтерфейсом електоророзпилювання (PX-MCBP). Виміри 1H ЯМР проводили на спектрометрах Varian UNITY плюс 400, 500 та 600, які працюють при частотах 1H відповідно при 400, 500 та 600МГц. Спектр ЯМР записували в d6-ДМСО з хімічними зсувами, наданими в млн -1, із розчинником як внутрішнім стандартом. Сполука 12 Синтез Сполуки 12 Сполуку 12 отримували літературним способом [Marsh та Bradley, J. Org. Chem., 1997, 62, 6199-6203] з наступними змінами: Fmoc-L-Arg-N w ,w ' -(Βοc)2-ΟΗ першим сполучено з смолою/лінкером. Після видалення Fmoc-групи, вільний амін сполучено з Na-(4e нітрофенілоксикарбоніл)-N -(9флуоренілметоксикарбоніл)-D-лізин аліловим естером. Синтез пептиду Fmoc продовжували на бічному ланцюгу залишку лізину, застосовуючи Fmoc-L-AIa, а потім Fmoc-L-H-MeAla, Fmoc-L-Leu та Fmoc-L-Ala. Видалення алільного естеру та Fmoc супроводжували циклізацією та кінцевим відщепленням від смоли/лінкеру. Очищення залишку реверсно-фазовою ВЕРХ (колонка Асе С8, лінійний градієнт 5%®95% MeCN у 0.1M водному NH4OAc) дало Сполуку 12 (1.8мг, 1.3%). 1 H ЯМР (500МГц, d6-ДМСО): 9.2 (широкий s, 1H), 8.66 (d, 1H), 8.52 (d, 1H), 7.4-8.0 (широкий сигнал, 4H), 7.47 (dd, 1H), 7.10 (d, 1H), 6.56 (d, 1H), 6.08 (d, 1H), 4.77-4.83 (m, 1H), 4.70-4.77 (m, 1H), 4.23 (qd, 1H), 4.07 (qd, 1H), 3.88-3.98 (m, 1H), 3.653.75 (m, 1H), 3.47-3.52 (m, 1H), 3.03 (широкий t, 2H), 2.71-2.78 (m, 1H), 2.52 (s, 3H), 1.78-1.84 (m, 1H), 1.68-1.79 (m, 1H), 1.30-1.65 (m, 12H), 1.15-1.23 (m, 2H), 1.18 (два d, 6H), 0.94 (d, 3H), 0.93 (d, 3H), 0.89 (d, 3H), 0.88 (d, 3H). MCBP (MCBP) розраховано для C32H59N10O 8 711.4517 (М+Н)\ знайдено 711.4525. Приклад 4 Цей приклад описує синтез Сполук 1 та 13-16. Синтез Сполуки 1 а) Синтез інтермедіату А Інтермедіат А TFA (2мл) додавали до Boc-D-Lys(Fmoc)-OAлілy (2.86г, 5.6ммоль) та залишали стояти протягом 5 хвилин. Потім видаляли TFA потоком сухого азоту, що дало H-D-Lys(Fmoc)-O-Aліл, який висушували на високовакуумній лінії протягом 2 годин, що видаляло всі сліди TFA. 2-Хлортритильній смолі (1г, 1.4ммоль) попередньо давали розбуха ти в ДХМ (10мл) протягом 1 години. Смолу осушували та додавали розчин Н-О-Lуs(Fmoc)-О-Аліл (2.30г, 5.64ммоль) та DIEA (729мг, 982мкл, 5.64ммоль) у ДХМ (10мл), і реакційну суміш струшували протягом 1 години. Потім до смоли додавали DIEA (1.46г, 1.95мл, 11.3ммоль) та реакційну суміш стр ушували протягом подальшої 1 години. Метанол (1мл) додавали для заглушки будь-якої смоли, що не прореагувала, та реакційну суміш потім струшували протягом 1 години. Смолу фільтрували та промивали ДМФ (2´5мл), ДХМ (2´5мл) та ДМФ (2´5мл). Смолу піддавали Fmocтвердофазному пептидному синтезу (SPPS), застосовуючи наступні умови: (і) Зняття захисту Fmoc: 20 % піперидин у ДМФ (2´10мл) протягом 2 хвилин, супроводжуваний промиванням ДМФ (4´5мл), ДХМ (4´5мл) та ДМФ (4´5мл). (іі) Умови сполучення: В усі х сполученнях розчин реагенту сполучення додавали до Fmocамінокислоти. До смоли додавали цей розчин, а потім DIEA. (a) Fmoc-Trp(Boc)-OH (2.95г, 5.6ммоль), HBTU (0.5M розчин, 11.2мл) та DIEA (0.975мл, 5.6ммоль) 20 хвилин, (b) Fmoc-N-MeLeu-OH (2.06г, 5.6ммоль), HBTU (0.5M розчин, 11.2мл) та DIEA (0.975мл, 5.6ммоль) 20 хвилин, (с) Fmoc-Leu-OH (1.98г, 5.6ммоль), HOBt (756мг, 5.6ммоль), HATU (2.13г, 5.6ммоль) та DIEA (314мкл, 1.8ммоль) у ДМФ (10мл) 3 години, (d) Fmoc-AIa-OH (1.74г, 5.6ммоль), HBTU (0.5M розчин, 11.2мл) та DIEA (0.975мл, 5.6ммоль) 20 хвилин. Потім усі сполучення смоли фільтрували та промивали ДМФ (4´5мл), ДХМ (4 ´5мл) та ДМФ (4´5мл). Усі сполучення окрім (с) перевіряли, застосовуючи нінгідриновий тест, сполучення (с) перевіряли, застосовуючи бромфеноловий блакитний тест. Усі сполучення також перевіряли MC розщепленням малої кількості смоли (5мг) з 100% TFA протягом 5 хвилин, фільтрат смоли потім аналізували за допомогою MC. 59 85199 60 Через розчин Pd(PPh3)4 (1.62г, 1.4ммоль) та c) Аліл-N5-[[(4-етил-2,2,6,7-тетраметил-2,3димедону (1.96г, 14ммоль) у ТГФ:ДХМ (1:1, 50мл) дигідро-1-бензофуран-5-іл)амін](імін)метил]-N2-[(4барботували азот протягом 10 хвилин, розчин донітрофенокси)карбоніл]орнітинат давали до смоли та суміш струшували протягом Аліл-N2-[(9Н-флуорен-9-ілметокси)карбоніл]5 16 годин. Реакційну суміш фільтрували та промиN -{імін[(2,2,4,6,7-пентаметил-2,3-дигідро-1бензофуран-5-іл)амін]метил}орнітинат (800мг, вали ДХМ (3´5мл), ДМФ (3´5мл), розчином 0.5% 1.16ммоль) розчиняли в ДМФ (4мл). Додавали DIEA та 0.5% сіллю натрію діетилдитіокарбамінопіперидин (1мл), та реакційну суміш перемішували вої кислоти в ДМФ (3´5мл) та ДМФ (3´5мл). Смолу при кімнатній температурі протягом 30 хвилин та обробляли 20% піперидином у ДМФ (2´10мл) пропотім концентрували. Отриманий осад розчиняли тягом 2 хвилин, а потім промивали ДМФ (4´5мл), в ДХМ (9мл) та додавали до суспензії 4ДХМ (4´5мл), 10% піридин гідрохлоридом у нітрофенілхлорформіату (370мг, 1.85ммоль) та ДХМ;ДМФ (1:1, 4´5мл) та ДМФ (4´5мл). До смоли піридину (750мкл, 9.3мкмоль) у ДХМ (6мл) з охододавали розчин РуВrоР (718мг, 1.54ммоль) та лодженням у льоді із сіллю. Після перемішування DIEA (1мл, 5.74ммоль) у ДХМ:ДМФ (1:1, 10мл) та протягом 2.5 годин додавали IM KHSO4 (20мл), суміш струшували протягом 3 годин після того, як органічний шар відокремлювали та водну фазу нінгідриновий тест був негативним. Циклічний пепекстрагували ДХМ (4´20мл). Комбіновані органічні тид відщеплювали від смоли обробкою 50% TFA у екстракти висушували (MgSO 4), фільтрували, конДХМ (20мл) протягом 1 години. Смол фільтрували, центрували та отриманий осад очищали флешпромивали TFA (2´5мл) та ДХМ (2´5мл), концентхроматографією на силікагелі (100% гексан®7:3 рували до сухого стану, перерозчиняли в EtOAc:гексан), що дало аліл-N5-[[(4-етил-2,2,6,7MeCN:H2O (0.1% TFA) та ліофілізували, що дало тетраметил-2,3-дигідро-1-бензофуран-5сирийінтермедіат А (435мг, 50% розміщено на 2іл)амін](імін)метил]-N2-[(4Хлортритильній смолі). Очищення РФВТРХ (95:5 нітрофенокси)карбоніл]орнітинат(138мг, 18%). Н2О (1% TFA):MeCN (1% TFA) до 2:3 Н2О (1% 1 H ЯМР (CDCl3, 500МГц): d 1.42 (s, 6H), 1.62 TFA):MeCN (1% TFA)) протягом 60 хвилин давало (m, 2H), 1.79 (m, 1H), 1.89 (m, 1H), 2.04 (s, 3H), 2.48 Інтермедіат А (0.417г, 3.6%). (s, 3H), 2.55 (s, 3H), 2.90 (s, 2H), 3.20 (m, 2Н), 4.30 b) Аліл-N2-[(9Н-флуорен-9(m, 1H), 4.60 (br d, J 4.5Гц, 2Н), 5.22 (d, J 10 .5Гц, ілметокси)карбоніл]-N5-{імін[(2,2,4,6,7-рентаметил1H), 5.29 (d, J 17Гц, 1H), 5.86 (m, 1H), 6.25 (br s, 2,3-дигідро-1-бензофуран-51H), 6.33 (br s, 1H), 6.50 (br d, J 6.5Гц, 1H), 6.90 (d, іл)амін]метил}орнітинат J 7.5Гц, 1H), 7.25 (d, J 8Гц, 2H), 8.05 (d, J 7.5Гц, N2-[(9Н-флуорен-9-ілметокси)карбоніл]-N51H), 8.15 (d, J 8Гц, 2H) . {імін[(2,2,4,6,7-рентаметил-2,3-дигідро-113 C Я МР (CDCl3, 125МГц): d 12.63, 18.16, бензофуран-5-іл)амін]метил}орнітин (1.0г, 19.45, 25.74, 28.76, 29.44, 40.8, 43.41, 54.41, 66.39, 1.54ммоль) розчиняли в ДМФ (5мл). Додавали 86.71, 115.99, 117.78, 119.21, 122.22, 124.97, цезій карбонат (377мг, 1.16ммоль) та реакційну 125.23, 126.22, 131.66, 132.40, 133.02, 138.43, суміш перемішували протягом 1 години. Потім 140.75, 144.97,153.45, 156.06, 156.67, 159.04, додавали аліл бромід (0.913мл, 10.8ммоль) та 163.07,163.80, 171.6. MC: (позитивна IEP) [М+Н]+ перемішування тривало протягом подальшої 1 m/z 632. години, що дало у результаті молочно-білий розd) Сполука 1 чин. Додавали воду (25мл) та реакційну суміш підІнтермедіат А (49.9мг, 0.08ммоль) розчиняли в кислювали 2М KHSO4. Додавали ДХМ (50мл) та ДМФ (8мл). Додавали Aліл-Ν5-[[(4-етил-2,2,6,7фази відокремлювали. Водну фазу промивали тетраметил-2,3-дигідро-1-бензофуран-5ДХМ (2 ´50мл) та комбіновані органічні фази проіл)амін](імін)метил]-N2-[(4мивали розсолом (50мл), висушували (MgSO4), нітрофенокси)карбоніл]орнітинат (60.6мг, фільтрували та концентрували до сухого стану, що 0.096ммоль), супроводжуваний DIEA (17мкл, дало аліл-N2-[(9H-флуорен-9-ілметокси)карбоніл]0.096ммоль), та реакційну суміш перемішували N5-{імін[(2,2,4,6,7-рентаметил-2,3-дигідро-1при кімнатній температурі протягом 16 годин. Реабензофуран-5-іл)амін]метил}орнітинат як безбарвкційну суміш концентрували, що дало сиру сечону піну (857мг, 81%). 1 вину. Через розчин паладій (тетраH ЯМР (CDCl3, 500МГц): 1.43 (s, 6H), 1.59 (m, кіс)трифенілфосфіну (8мг, 0.0072ммоль) та 2H), 1.73 (m, 1H), 1.86 (m, 1H), 2.09 (s, 3H), 2.52 (s, димедону (25мг, 0.18ммоль) у ТГФ:ДХМ (1:1, 5мл) 3H), 2.61 (s, 3H), 2.91 (s, 2H), 3.22 (m, 2H), 4.17 (t, J барботували сухий азот та потім додавали через 7Гц, 1H), 4.32 (m, 1H), 4.37 (m, 1H), 4.59 (br d, J канюлю до сечовини та перемішували при кімнат4.5Гц, 2Н), 5.21 (d, J 10.5Гц, 1H), 5.30 (d, J 17Гц, ній температурі протягом ночі, що дало сиру кар1H), 5.83 (m, 1H), 5.88 (m, 1H), 6.26 (br s, 1H), 6.35 бонову кислоту. Карбонову кислоту розчиняли в (br s, 2H), 7.26 (t, J 7.5Гц, 2H), 7.37 (t, J 7.5Гц, 2H), ДХМ (1мл), та додавали н-крезол (340мкл) і TFA 7.57 (m, 2H), 7.74 (d, J 7.5Гц, 2H). 13 (250мкл), та реакційну суміш перемішували при C Я МР (CDCl3, 125МГц): d 12.68, 18.22, кімнатній температурі протягом 20 годин, що дало 19.54, 25.69, 28.78, 29.93, 40.96, 43.43, 47.36, сиру Сполуку 1. Реакційну суміш очищали реверс53.72, 54.10, 66.23, 67.39, 86.63, 117.78, 119.12, но-фазовою ВЕРХ (YMC напівпрепаративна коло120.19, 124.93, 125.40, 127.34, 127.96, 131.79, нка, лінійний градієнт 65% Вода (1% TFA) 35% 132.47, 133.17, 138.54, 141.49, 143.97, 144.08, MeCN (1% TFA)®100% MeCN (1% TFA)), що дало 156.63, 159.03, 171.42). MC: (позитивна IEP) + Сполуку 1 (11.3мг, 17%). Визначені дані ЯМР та [М+Н] m/z 689. MC ідентифікували достовірність зразку. Альтернативний синтез Сполуки 1
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of cyclic anabenopeptine type peptides for treatment of the condition wherein inhibition of carboxypeptidase u is beneficial, anabenopeptin derivatives and intermediates thereof
Автори англійськоюBjorquist Petter, Buchanan Malcolm, Campitelli Marc, Carroll Anthony, Hyde Edward, Neve Juliette, Polla Magnus, Quinn Ron
Назва патенту російськоюПрименение циклических пептидов типа анабенопептина для лечения состояний, при которых показано угнетение карбоксипептидазы u, производные анабенопептина и их промежуточные соединения
Автори російськоюБьерквист Петер, Бучанан Малколм, Кемпителли Марк, Кэрролл Энтони, Гайд Эдвард, Нив Джульетт, Полла Магнус, Квинн Рон
МПК / Мітки
МПК: A61P 7/00, A61P 9/10, C07K 7/50, A61K 38/12, A61P 7/02
Мітки: пригнічення, сполуки, анабенопептину, якому, типу, карбоксипептидази, застосування, пептидів, лікування, проміжні, корисне, циклічних, стану, похідні
Код посилання
<a href="https://ua.patents.su/33-85199-zastosuvannya-ciklichnikh-peptidiv-tipu-anabenopeptinu-dlya-likuvannya-stanu-v-yakomu-korisne-prignichennya-karboksipeptidazi-u-pokhidni-anabenopeptinu-ta-kh-promizhni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Застосування циклічних пептидів типу анабенопептину для лікування стану, в якому корисне пригнічення карбоксипептидази u, похідні анабенопептину та їх проміжні сполуки</a>
Попередній патент: Похідні морфоліну як інгібітори повторного поглинання норепінефрину
Наступний патент: Система та спосіб керування передачею даних за допомогою множини форматів часових інтервалів
Випадковий патент: Установка для дослідження газових свердловин