Сполуки інданілпіперазину, спосіб їх одержання і фармацевтичні композиції, які їх містять
Номер патенту: 87989
Опубліковано: 10.09.2009
Автори: ОРТУНО Жан-Клод, ПОРТЕВІН Бернар, ГЛОАНЕК Філіп, Де Нантей Гійом, МАНУРІ ЛЯ КУР Клотильд, Міллан Марк, ГОБЕР Ален
Формула / Реферат
1. Сполука формули (І):
 , (І)
, (І)
в якій:
- R3 являє собою атом водню, і R1 і R2 разом з атомами вуглецю, до яких вони приєднані, утворюють бензольну, нафталінову або хінолінову кільцеву структуру, кожна з цих кільцевих структур є необов'язково заміщеною одним або більше однаковими або різними замісниками, вибраними з водню, галогену і лінійного або розгалуженого С1-С6алкілу, необов'язково заміщеного одним або більше атомами галогену,
або R1 являє собою атом водню, і R2 і R3 разом з атомами вуглецю, до яких вони приєднані, утворюють бензольну, нафталінову або хінолінову кільцеву структуру, кожна з цих кільцевих структур є необов'язково заміщеною одним або більше однаковими або різними замісниками, вибраними з водню, галогену і лінійного або розгалуженого С1-С6алкілу, необов'язково заміщеного одним або більше атомами галогену,
- n являє собою 1 або 2,
- -X- являє собою групу, яку вибирають з -(СH2)m-О-Аk-, -(CH2)m-NR4-Ak-, -(CO)-NR4-Ak- і -(CH2)m-NR4-(CO)-,
m являє собою ціле число від 1 до 6 включно, Ak являє собою лінійний або розгалужений С1-С6алкіленовий ланцюг, необов'язково заміщений гідроксигрупою, і R4 являє собою атом водню або лінійну або розгалужену С1-С6алкільну групу,
- Аr являє собою арильну або гетероарильну групу, її оптичні ізомери, а також її адитивні солі з фармацевтичнo прийнятною кислотою, повинно бути зрозумілим, що оптичні ізомери означають енантіомери і діастереоізомери, арильна група означає феніл, біфеніліл або нафтил, кожна з цих груп необов'язково заміщена однією або більше однаковими або різними групами, які вибирають з галогену, лінійного або розгалуженого С1-С6алкілу, лінійного або розгалуженого С1-С6алкокси, гідрокси, ціано і лінійного або розгалуженого С1-С6тригалоалкокси, гетероарильна група означає ароматичну моно- або біциклічну 5-12-членну групу, яка містить один, два або три гетероатоми, які вибирають з кисню, азоту і сірки, повинно бути зрозуміло, що гетероарильна група може бути необов'язково заміщена однією або більше однаковими або різними групами, які вибирають з галогену, лінійного або розгалуженого С1-С6алкілу, лінійного або розгалуженого С1-С6алкокси, гідрокси, ціано і лінійного або розгалуженого С1-С6тригалоалкілу.
2. Сполука формули (І) за п. 1, в якій R1 і R2 разом з атомами вуглецю, до яких вони приєднані, утворюють необов'язково заміщене бензольне кільце, і R3 являє собою атом водню, або R2 і R3 разом з атомами вуглецю, до яких вони приєднані, утворюють необов'язково заміщене бензольне кільце і R1 являє собою атом водню.
3. Сполука формули (І) за п. 1 або 2, в якій n являє собою 1.
4. Сполука формули (І) за будь-яким з пп. 1-3, в якій m являє собою 1.
5. Сполука формули (І) за будь-яким з пп. 1-4, в якій Аr являє собою арильну групу.
6. Сполука формули (І) за п. 1, яку вибирають з:
1-[(1RS)-1-(3,5-дибромбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
1-[(1RS)-1-(3,5-диметилбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
1-[2-(3,5-диметилбензилоксиметил)індан-2-іл]піперазину, а також його адитивних солей з фармацевтично прийнятною кислотою,
N-[(3,5-біс(трифторметил)бензил]-2-(1-піперазиніл)-2-інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-бензил-N-метил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-[3,5-біс(трифторметил)бензил]-N-метил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-(3,5-диметилбензил)-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
N-(3,5-дифторбензил)-2-(1-піперазиніл)-2-інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою,
N-(3,5-дихлорбензил)-N-метил-2-(1-піперазиніл)-2-інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-(3,5-дифторбензил)-N-метил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-[3-фтор-5-(трифторметил)бензил]-N-метил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-1-[1-(3,5-дифторбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
N-(3-хлор-5-фторбензил)-N-метил-2-(1-піперазиніл)-2-інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою,
1-[(1RS)-1-(3,5-дифторбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
(1RS)-N-(3,5-дифторбензил)-N-метил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
1-[(1RS)-1-(3,5-дифторбензилоксиметил)-5,6-дифторіндан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою,
і 1-[(1RS)-1-(3-бром-5-фторбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою.
7. Спосіб одержання сполук формули (І) за п. 1 зі сполуки формули (II):

в якій R1, R2 і R3 є такими ж, як визначено для формули (І), і P1 являє собою захисну групу для аміногрупи,
кислотну групу якої захищають, з одержанням сполуки формули (III):

в якій R1, R2, R3 і P1 є такими ж, як визначено тут вище, і Р2 являє собою захисну групу для кислотної групи, яка відрізняється від Р1,
захист аміногрупи знімають перед реакцією зі сполукою формули (IV):

в якій G1 і G2 кожний являють собою атом галогену або р-толуолсульфонілоксигрупу, Tos являє собою пара-толуолсульфонільну групу, і n є таким же, як визначено для формули (І),
з одержанням сполуки формули (V):

в якій R1, R2, R3,P2, n і Tos є такими ж, як визначено тут вище,
з якої відщеплюють пара-толуолсульфонільну групу, знімають захист кислотної групи і потім аміногрупу захищають, з одержанням сполуки формули (VI):

в якій R1, R2, R3 і n є такими ж, як визначено тут вище, і Р3 являє собою захисну групу для аміногрупи,
сполуку формули (VI) піддають реакції, коли бажаним є одержання сполуки формули (І), в якій Х являє собою -(CO)-NR4-Ak- або -CH2-NR4-Ak-, зі сполукою формули (VII):
HNR4-Ak-Ar, (VII)
в якій R4, Ak і Аr є такими ж, як визначено для формули (І),
у присутності одного або більше з'єднувальних агентів, з одержанням, після зняття захисту, кільцевої аміногрупи, сполуки формули (Іа), конкретний випадок сполук формули (І), в якій Х являє собою групу -(СО)-NR4-Ak,
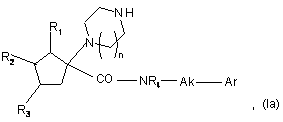
в якій R1, R2, R3 n, R4 і Ak є такими ж, як визначено тут вище, і Аr є таким же, як визначено для формули (І),
яку піддають реакції, коли бажаним є одержання сполуки формули (Іb), конкретний випадок сполук формули (І), в якій Х являє собою групу -CH2-NR4-Ak,
з відновлювальним агентом, з одержанням сполуки формули (Іb):

в якій R1, R2, R3, n, R4, Ak і Ar є такими ж, як визначено тут вище,
або сполуку формули (VI) етерифікують, коли бажаним є одержання сполуки формули (І), в якій Х являє собою групу -CH2-O-Ak- або -CH2-NR4-(CO)-,
з одержанням сполуки формули (VIII):

в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище, Р4 являє собою бензил або лінійну або розгалужену С1-С6алкільну групу,
яка реагує у присутності відновлювального агента, з одержанням спирту формули (IX):

в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище,
спирт формули (IX) піддають реакції, коли бажаним є одержання сполуки формули (Іс), конкретний випадок сполук формули (І), в якій Х являє собою групу -СН2-О-Ak-,
зі сполукою формули (X):
Hal-Ak-Ar, (X)
в якій Ak і Аr є такими ж, як визначено для формули (І), і Hal являє собою атом галогену,
з одержанням, після зняття захисту кільцевої аміногрупи, сполуки формули (Іс):

в якій R1, R2, R3, n, Ak і Аr є такими ж, як визначено тут вище,
або спирт формули (IX) перетворюють за допомогою звичайної методики в органічній хімії в амін формули (XI):

в якій R1, R2, R3, n, R4 і Р3 є такими ж, як визначено тут вище,
який піддають реакції зі сполукою формули (XII):
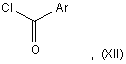
в якій Аr є таким же, як визначено для формули (І),
з одержанням, після зняття захисту кільцевої аміногрупи, сполуки формули (Id), конкретний випадок сполук формули (І), в якій Х являє собою групу -CH2-NR4-(CO)-,

в якій R1, R2, R3, n, R4 і Аr є такими ж, як визначено тут вище,
сполуки формул (la), (Ib), (Іс) і (Id) очищують відповідно до звичайної техніки очищення, розділяють, коли бажано, на їх оптичні ізомери і перетворюють, коли бажано, в їх адитивні солі з фармацевтичнo прийнятною кислотою.
8. Фармацевтична композиція, яка містить, як активний інгредієнт, сполуку за будь-яким з пп. 1-6 в поєднанні з одними або більше фармацевтичнo прийнятними, інертними, нетоксичними носіями.
9. Застосування сполук формули (І) за будь-яким з пп. 1-6 у виробництві ліків для використання як інгібіторів оберненого захоплення серотоніну і NK1 антагоністів.
10. Застосування сполук формули (I) за будь-яким з пп. 1-6 у виробництві ліків для застосування у лікуванні депресивних станів, станів тривожності, імпульсивних розладів, агресивної поведінки, наркотичної залежності, ожиріння і розладів апетиту, болю і запалення, недоумства, психотичних станів, порушень хронобіологічних ритмів, нудоти і кишково-шлункових розладів.
Текст
1. Сполука формули (І): 2 (19) 1 3 87989 4 R1 тивних солей з фармацевтичнo прийнятною кислотою, R2 MHP1 1-[(1RS)-1-(3,5-диметилбензилоксиметил)індан-1іл]піперазину, його оптичних ізомерів, а також адиCO2H тивних солей з фармацевтичнo прийнятною кис, (II) лотою, R3 1-[2-(3,5-диметилбензилоксиметил)індан-2в якій R1, R2 і R3 є такими ж, як визначено для фоіл]піперазину, а також його адитивних солей з фармули (І), і P1 являє собою захисну групу для амірмацевтично прийнятною кислотою, ногрупи, N-[(3,5-біс(трифторметил)бензил]-2-(1кислотну групу якої захищають, з одержанням піперазиніл)-2-інданкарбоксаміду, а також його сполуки формули (III): адитивних солей з фармацевтичнo прийнятною R1 кислотою, (1RS)-N-бензил-N-метил-1-(1-піперазиніл)-1R2 MHP1 інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною CO2P2 кислотою, , (III) (1RS)-N-[3,5-біс(трифторметил)бензил]-N-метил-1R3 (1-піперазиніл)-1-інданкарбоксаміду, його оптичних в якій R1, R2, R3 і P1 є такими ж, як визначено тут ізомерів, а також адитивних солей з фармацеввище, і Р2 являє собою захисну групу для кислоттичнo прийнятною кислотою, ної групи, яка відрізняється від Р1, (1RS)-N-(3,5-диметилбензил)-1-(1-піперазиніл)-1захист аміногрупи знімають перед реакцією зі споінданкарбоксаміду, його оптичних ізомерів, а також лукою формули (IV): адитивних солей з фармацевтичнo прийнятною кислотою, N-(3,5-дифторбензил)-2-(1-піперазиніл)-2інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою, N-(3,5-дихлорбензил)-N-метил-2-(1-піперазиніл)-2інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою, (1RS)-N-(3,5-дифторбензил)-N-метил-1-(1піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, (1RS)-N-[3-фтор-5-(трифторметил)бензил]-Nметил-1-(1-піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, (1RS)-1-[1-(3,5-дифторбензилоксиметил)індан-1іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, N-(3-хлор-5-фторбензил)-N-метил-2-(1піперазиніл)-2-інданкарбоксаміду, а також його адитивних солей з фармацевтичнo прийнятною кислотою, 1-[(1RS)-1-(3,5-дифторбензилоксиметил)індан-1іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, (1RS)-N-(3,5-дифторбензил)-N-метил-1-(1піперазиніл)-1-інданкарбоксаміду, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, 1-[(1RS)-1-(3,5-дифторбензилоксиметил)-5,6дифторіндан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою, і 1-[(1RS)-1-(3-бром-5фторбензилоксиметил)індан-1-іл]піперазину, його оптичних ізомерів, а також адитивних солей з фармацевтичнo прийнятною кислотою. 7. Спосіб одержання сполук формули (І) за п. 1 зі сполуки формули (II): G1 N G2 n Tos , (IV) в якій G1 і G2 кожний являють собою атом галогену або р-толуолсульфонілоксигрупу, Tos являє собою пара-толуолсульфонільну групу, і n є таким же, як визначено для формули (І), з одержанням сполуки формули (V): Tos N R1 N n R2 CO2P2 , (V) R3 в якій R1, R2, R3,P2, n і Tos є такими ж, як визначено тут вище, з якої відщеплюють пара-толуолсульфонільну групу, знімають захист кислотної групи і потім аміногрупу захищають, з одержанням сполуки формули (VI): P3 N R1 N n R2 CO2H R3 , (VI) в якій R1, R2, R3 і n є такими ж, як визначено тут вище, і Р3 являє собою захисну групу для аміногрупи, сполуку формули (VI) піддають реакції, коли бажаним є одержання сполуки формули (І), в якій Х являє собою -(CO)-NR4-Ak- або -CH2-NR4-Ak-, зі сполукою формули (VII): HNR4-Ak-Ar, (VII) 5 87989 6 в якій R4, Ak і Аr є такими ж, як визначено для фов якій Ak і Аr є такими ж, як визначено для формурмули (І), ли (І), і Hal являє собою атом галогену, у присутності одного або більше з'єднувальних з одержанням, після зняття захисту кільцевої аміагентів, з одержанням, після зняття захисту, кільногрупи, сполуки формули (Іс): цевої аміногрупи, сполуки формули (Іа), конкретNH ний випадок сполук формули (І), в якій Х являє R1 собою групу -(СО)-NR4-Ak, N R1 CH2 N n R2 CO Ak Ar R3 в якій R1, R2, R3 n, R4 і Ak є такими ж, як визначено тут вище, і Аr є таким же, як визначено для формули (І), яку піддають реакції, коли бажаним є одержання сполуки формули (Іb), конкретний випадок сполук формули (І), в якій Х являє собою групу -CH2-NR4Ak, з відновлювальним агентом, з одержанням сполуки формули (Іb): NH n CH2 NR4 Ak R1 в якій R1, R2, R3, n, R4, Ak і Ar є такими ж, як визначено тут вище, або сполуку формули (VI) етерифікують, коли бажаним є одержання сполуки формули (І), в якій Х являє собою групу -CH2-O-Ak- або -CH2-NR4-(CO)-, з одержанням сполуки формули (VIII): CH2 , (XI) Ar O , (XII) в якій Аr є таким же, як визначено для формули (І), з одержанням, після зняття захисту кільцевої аміногрупи, сполуки формули (Id), конкретний випадок сполук формули (І), в якій Х являє собою групу -CH2-NR4-(CO)-, NH N CH2 , (VIII) R3 в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище, Р4 являє собою бензил або лінійну або розгалужену С1-С6алкільну групу, яка реагує у присутності відновлювального агента, з одержанням спирту формули (IX): N P3 N n OH , (IX) R3 в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище, спирт формули (IX) піддають реакції, коли бажаним є одержання сполуки формули (Іс), конкретний випадок сполук формули (І), в якій Х являє собою групу -СН2-О-Ak-, зі сполукою формули (X): Hal-Ak-Ar, (X) R4 n R2 CO2P2 CH2 NHP4 R3 R1 N R2 N n N P3 n R1 NP3 R2 , (Ib) R2 , (Ic) в якій R1, R2, R3, n, Ak і Аr є такими ж, як визначено тут вище, або спирт формули (IX) перетворюють за допомогою звичайної методики в органічній хімії в амін формули (XI): Cl Ar R3 R1 Ar в якій R1, R2, R3, n, R4 і Р3 є такими ж, як визначено тут вище, який піддають реакції зі сполукою формули (XII): N R2 OAk R3 NR4 , (Ia) R1 n R2 NH R3 N Ar O , (Id) в якій R1, R2, R3, n, R4 і Аr є такими ж, як визначено тут вище, сполуки формул (la), (Ib), (Іс) і (Id) очищують відповідно до звичайної техніки очищення, розділяють, коли бажано, на їх оптичні ізомери і перетворюють, коли бажано, в їх адитивні солі з фармацевтичнo прийнятною кислотою. 8. Фармацевтична композиція, яка містить, як активний інгредієнт, сполуку за будь-яким з пп. 1-6 в поєднанні з одними або більше фармацевтичнo прийнятними, інертними, нетоксичними носіями. 9. Застосування сполук формули (І) за будь-яким з пп. 1-6 у виробництві ліків для використання як інгібіторів оберненого захоплення серотоніну і NK1 антагоністів. 10. Застосування сполук формули (I) за будь-яким з пп. 1-6 у виробництві ліків для застосування у лікуванні депресивних станів, станів тривожності, імпульсивних розладів, агресивної поведінки, наркотичної залежності, ожиріння і розладів апетиту, болю і запалення, недоумства, психотичних станів, 7 87989 8 порушень хронобіологічних ритмів, нудоти і кишково-шлункових розладів. Даний винахід відноситься до сполук інданілпіперазину, до способу їх одержання і фармацевтичних композицій, які їх містять, а також до їх застосування як інгібіторів оберненого захоплення серотоніну і ΝΚ1 антагоністів. Сполуки даного винаходу служать як інгібітори оберненого захоплення серотоніну. Враховуючи той факт, що вони є корисними у лікуванні депресивних станів [Goodnick and Goldstein, J Psychopharmacol 1998,12 (Suppl B):S55-S87; Cheer and Goa, Drugs 2001 61:81-110; MacQueen et al., CNS Drug Rev 2001, 7:1-24; Wagstaff et al., Drugs 2002 62:655-703], станів тривожності, таких як генералізована тривожність, напади паніки і фобії [Feighner, J Clin Psychiatry 1999, 60 (Suppl 22): 18-22; Bakker et al., Int Clin Psychopharmacol 2000, 15 (Suppl 2):S25-S30; Davidson, Int Clin Psychopharmacol 2000 15 (Suppl 1):S13-S17; Schneier, J Clin Psychiatry 2001, 62 (Suppl 1):43-48], несприятливого впливу стресу або психологічного [Marona-Lewicka and Nichols, Stress 1997, 2:91-100; Mar et al., Pharmacol Biochem Behav 2002, 73:703-712; Will et al., Mol Psychiatry 2003, 8:925-932; Ballenger, J Clin Psychiatry 2004, 65:1696-1707] або нейротоксичного [Malberg and Duman, Neuropsychopharmacology 2003, 28:1562-1571; Santarelli et al., Science 2003, 301:805-809; Czeh et al., Neuropsychopharmacology 2005, 30:67-79; Malberg and Schechter, Curr Pharm Des 2005, 11: 145-155], імпульсивних станів, таких як "ODC" або обсесивно-компульсивний розлад поведінки [Njung'e and Handley, Br J Pharmacol 1991, 104:105-112; Ichimaru et al., Jpn J Pharmacol 1995, 68:65-70; Pigott and Seay, J Clin Psychiatry 1999, 60:101-106; Vythilingum et al., Int Clin Psychopharmacol 2000, 15 (Suppl 2):S7-S1313], агресивних станів [Knutson et al., Am J Psychiatry 1998, 155:373-379; Lanctot et al., Neuropsychopharmacology 2002, 27:646-654; New et al., Psychopharmacology 2004, 176:451-458], ожиріння і розладів апетиту, таких як булімія [Proietto et al., Expert Opin Investig Drugs 2000, 9:1317-1326; Ljung et al., J Intern Med 2001, 250:219-224; Appolinario et al., CNS Drugs 2004, 18:629-651; Appolinario and McElroy, Curr Drug Targets 2004, 5:301-307], больових станів [Aragona et al., Eur J Pain 2005, 9:33-38; Millan et al., Neuropharmacology 2002, 42:677-684; Duman et al., J Pharmacol Sci 2004, 94:161-165; Otsuka et al., J Anesth 2004, 15:154-158]; і, відносно таких груп, розладів поведінки і неврональної дегенерації, асоційованих з недоумством та іншими розладами старіння [Lyketos et al., Am J Psychiatry 2000, 157:1686-1689; Lanctot et al., J Neuropsyhiatry Clin Neurosci 2001, 13:5-21; Lanctot et al., Neuropsychopharmacology 2002, 27:646-654; Pollock et al., Am J Psychiatry 2002, 159:460-465]. До того ж, сполуки даного винаходу є також активними як нейрокінін ΝΚ1 антагоністи. Враховуючи той факт, що вони є корисними у лікуванні депресивних станів [Rupniak et al., Behav Pharmacol 2001, 12:497-508; Rupniak et al., Neuropharmacology 2003, 44:516-523; Kramer et al., Neuropsychopharmacology 2004, 29:385-392; Dableh et al., Eur J Pharmacol 2005, 507:99-105], станів тривожності, таких як генералізована тривожність, напади паніки і фобії [Rupniak et al., Behav Pharmacol 2001, 12:497-508; Santarelli et al., Proc Natl Acad Sci USA 2001, 98:1912-1927; Varty et al., Neuropsychopharmacology 2002, 27:371-379; Rupniak and Kramer, Neuropsychopharmacology 2002, 13:169-177], несприятливого впливу стресу або психологічного [Ballard et al., Eur J Pharmacol 2001, 412:255-264; Rupniak and Kramer, Neuropsychopharmacology 2002, 13:169-177; Spooren et al., Eur J Pharmacol 2002, 435:161-170; Steinberg etal., J Pharmacol Exp Ther 2002, 303:1180-1188] або нейротоксичного [Van der Hart et al., Mol Psychiatry 2002, 7:933-941; Morcuende et al., Eur J Neurosci 2003, 18:1828-1836; Guest et al., Brain Res 2004, 1002:1-10; Czeh et al., Neuropsychopharmacology 2005, 30:67-79], імпульсивних станів, таких як обсесивно-компульсивні розлади поведінки [Oilman et al., Br J Pharmacol 1995, 114:1310-1316; Tschope et al., BrJ Pharmacol 1992, 107:750-755; Rupniak et al., Behav Pharmacol 2001, 12:497-508; Millan et al., Neuropharmacology 2002, 42:677-684], агресивних станів [Siegel and Schubert, Rev Neurosci 1995, 6:47-61; De Felipe et al., Nature 1998, 392:394-397; Rupniak et al., Behav Pharmacol 2001, 12:497-508], а також наркотичної залежності [Murtra et al., Nature 2000, 405:180-183; Ripley et al., Neuropharmacology 2002, 43:12581268; Gadd et al., J Neurosci 2003, 23:8271-8280], психотичних станів [Zachrisson et al., Eur Neuropsychopharmacol 2000, 10:355-363] екстрапірамідних моторних ефектів, викликаних антипсихотичними засобами [Anderson et al., J Pharmacol Exp Ther 1995, 274:928-936, Steinberg et al., J Pharmacol Exp Ther 2002, 303:1180-1188], сексуальних дисфункцій [Priest et al., Brain Res Mol Brain Res 1995, 28:61-71; Daniels et al., Neurosci Lett 2003, 338:1 1 1-1 14; Kramer et al., Science 1998, 281:1640-1644; Kramer et al., Neuropsychopharmacology 2004, 29:385-392], розладів хронобіологічних ритмів, таких як циркадні ритми [Shibata et al., Brain Res 1992, 597:257-263; Challet et al., Brain Res 1998, 800:32-39; Challet et al., Neuropharmacology 2001, 40:408-415; Gannon et al., Neuropharmacology, in press], болю [Seguin et al., Pain 1995, 61:325-343; De Felipe et al., Nature 1998, 392:394-397; Sanger, Br J Pharmacol 2004, 141:1303-1312] і/або запалення [Seabrook et al., Eur J Pharmacol 1996, Ц7:129-135; Holzer, Digestion 1998, 59:269-283; Joos and Pauwels, Curr Opin Pharmacol 2001, 1:235-241; Sanger, Br J Pharmacol 2004, 141:1303-1312], нудоти та інших шлунковокишкових розладів [McAllister and Pratt Eur J Pharmacol 1998, 353:141-148; Gardner et al., Regulatory Peptides 1996, 65:45-53; Patel and Lindley, Expert Opin. Pharmacother 2003, 4:22792296; Sanger, Br J Pharmacol 2004, 141:1303-1312]; і, відносно таких груп, розладів поведінки і неврональної дегенерації, асоційованих з недоумством 9 87989 10 та іншими розладами старіння [Raffa, Neurosci або R1 являє собою атом водню, і R2 і R3 раBiobehav Rev 1998, 22:789-813]. зом з атомами вуглецю, до якого вони приєднані, Через те, що сполуки є активними як на ділянутворюють бензольну, нафталінову або хінолінову ках ΝΚ1 рецепторів, так і на ділянках оберненого кільцеву структуру, переважно бензольне кільце, захоплення серотоніну (5-НТ), вони повинні мати кожна з цих кільцевих структур є необов'язково комплементарні і синергічні механізми для регузаміщеною одним або більше однаковими або лювання імпульсивних, агресивних, больових і, різними замісниками, вибраними з водню, галогену насамперед, депресивних станів. Крім того, було і лінійного або розгалуженого С1-С6алкілу, необопоказано, що блокування ΝΚ1 рецепторів потенців'язково заміщеного одним або більше атомами ює вплив інгібіторів оберненого захоплення 5-НТ галогену, на серотонінергічну передачу: через той факт, що - n являє собою 1 або 2, такі сполуки повинні привести до більш швидкого і - -X- являє собою групу, яку вибирають з більш сильного антидепресивного впливу [Guiard (CH2)m-O-Ak-, -(CH2)m -NR4-Ak-, -(CO)-NR4-Ak- і et al., J Neurochem 2004, 89:54-63; Froger et al., J (CH2)m-NR4-(CO)-, Neurosci 2001, 2J.: 8188-8197]. Швидкі анксиолітиm являє собою ціле число від 1 до 6 включно, чні впливи ΝΚ1 антагоністів повинні, крім того, бути Аk являє собою лінійний або розгалужений С1комплементарними до анксиолітичних впливів С6алкіленовий ланцюг, необов'язково заміщений інгібіторів оберненого захоплення 5-НТ, які ексгідроксигрупою, і R4 являє собою атом водню або пресуються після довготривалого лікування. Що лінійну або розгалужену С1-С6алкільну групу, стосується анксіогенних впливів, які викликаються - Ar являє собою арильну або гетероарильну 5-НТ на початку лікування [Bagdy et al., Int J групу, Neuropsychopharmacol 2001, 4:399-408], вони подо їх оптичних ізомерів, а також до їх адитиввинні запобігатись властивостями ΝΚ1 антагоністів них солей з фармацевтично прийнятною кисло[Ballard et al., Eur J Pharmacol 2001, 412:255-264; тою. Rupniak et al., Neuropharmacology 2003, 44:516Оптичні ізомери, як повинно бути зрозуміло, 523]. Оскільки інші небажані впливи, асоційовані з означають енантіомери і діастереоізомери. блокуванням оберненого захоплення 5-НТ залуСеред фармацевтично прийнятних кислот мочаються, такі як блювотні впливи [Goldstein and жуть бути згадані, без будь-якого обмеження, хлоGoodnick, J Psychopharmacol 1998, 12 (Suppl ристоводнева кислота, бромистоводнева кислота, B):S55-S87; Edwards and Anderson, Drugs 1999, сірчана кислота, фосфорна кислота, оцтова кис57:507-533; Waugh and Goa, CNS Drugs 2003, лота, трифтороцтова кислота, молочна кислота, 17:343-362] і спричинення сексуальних дисфункцій піровиноградна кислота, малонова кислота, янта[Goldstein and Goodnick, J Psychopharmacol 1998, рна кислота, глутарова кислота, фумарова кисло12 (Suppl B):S55-S87; Montgomery et al., J Affect та, винна кислота, малеїнова кислота, лимонна disord 2002, 69:119-140; Hirschfeld, J Clin Psychiatry кислота, аскорбінова кислота, щавлева кислота, 2003, 64 (Suppl 18):20-24], ΝΚ1 антагоністи повинні метансульфонова кислота, бензолсульфонова також бути здатні до протидії таким впливам. кислота, камфорна кислота. Отже, сполуки, які є як ΝΚ1 антагоністами, так і Арильнагрупа, як повинно бути зрозуміло, інгібіторами оберненого захоплення серотоніну, означає феніл, біфеніліл або нафтил. кожна з цих повинні мати терапевтичну перевагу над сполукагруп необов'язково заміщена однією або більше ми, які взаємодіють тільки з однією або іншою з однаковими або різними групами, які вибирають з цих двох цілей. галогену, лінійного або розгалуженого С1-С6алкілу, Більш конкретно, даний винахід відноситься лінійного або розгалуженого С1-С6алкокси, гідродо сполук формули (І): кси, ціано і лінійного або розгалуженого С1С6тригалоалкокси. Гетероарильна група, як повинно бути зрозуміло, означає ароматичну моно-або біциклічну 512-членну групу, яка містить один, два або три гетероатоми, які вибирають з кисню, азоту і сірки, повинно бути зрозуміло, що гетероарильна група може бути необов'язково заміщена однією або більше однаковими або різними групами, які вибирають з галогену, лінійного або розгалуженого С1С6алкілу, лінійного або розгалуженого С1в якій: С6алкокси, гідрокси, ціано і лінійного або розгалу- R3 являє собою атом водню, і R1 і R2 разом з женого С1-С6тригалоалкілу. атомами вуглецю, до якого вони приєднані, утвоСеред гетероарильних груп можуть бути згарюють бензольну, нафталінову або хінолінову кідані, без будь-якого обмеження, групи тієнілу і льцеву структуру, переважно бензольне кільце, піридилу. кожна з цих кільцевих структур є необов'язково n переважно являє собою 1. заміщеною одним або більше однаковими або m переважно являє собою 1. різними замісниками, вибраними з водню, галогену Ar переважно являє собою арильну групу. і лінійного або розгалуженого С1-С6алкілу, необоПереважні сполуки відповідно до винаходу явв'язково заміщеного одним або більше атомами ляють собою: галогену, - 1-[(1RS)-1-(3,5-дибромбензилоксиметил) індан-1-іл]піперазин, його оптичні ізомери, а також 11 87989 12 адитивні солі з фармацевтично прийнятною кислотою, - 1-[(1RS)-1-(3,5-диметилбензилоксиметил) індан-1-іл]піперазин, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, - 1-[2-(3,5-диметилбензилоксиметил)індан-2в якій R1, R2 і R3 є такими ж, як визначено для іл]піперазин, а також адитивні солі з фармацевтиформули (І), і Ρ1 являє собою захисну групу для чно прийнятною кислотою, аміногрупи, N-[(3,5-біс(трифторметил)бензил]-2-(1піперазиніл)-2-інданкарбоксамід, а також адитивні кислотну групу якої захищають, щоб одержати солі з фармацевтично прийнятною кислотою, сполуку формули (III): - (1RS)-N-бензил-N-метил-1-(1-піперазиніл)-1інданкарбоксамід, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, (1RS)-N-[3,5-біс(трифторметил)бензил]-Nметил-1-(1-піперазиніл)-1-інданкарбоксамід, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, в якій R1, R2, R3 і Р1 є такими ж, як визначено (1RS)-N-(3,5-диметилбензил)-1-(1тут вище, і Р2 являє собою захисну групу для киспіперазиніл)-1-інданкарбоксамід, його оптичні ізолотної групи; яка відрізняється від Р1, мери, а також адитивні солі з фармацевтично призахист аміногрупи знімають перед реакцією зі йнятною кислотою, сполукою формули (IV): N-(3,5-дифторбензил)-2-(1-піперазиніл)-2інданкарбоксамід, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, N-(3,5-дихлорбензил)-N-метил-2-(1піперазиніл)-2-інданкарбоксамід, а також адитивні солі з фармацевтично прийнятною кислотою, в якій G1 і G2 кожний являють собою атом га(1RS)-N-(3,5-дифторбензил)-N-метил-1-(1логену або р-толуолсульфонілоксигрупу, Tos явпіперазиніл)-1-інданкарбоксамід, його оптичні ізоляє собою пара-толуолсульфонільну групу, і n є мери, а також адитивні солі з фармацевтично притаким же, як визначено для формули (І), йнятною кислотою, щоб одержати сполуку формули (V): - (1RS)-N-[3-фтор-5-(трифторметил)бензил]-Nметил-1-(1-піперазиніл)-1-інданкарбоксамід, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, (1RS)-1-[1-(3,5дифторбензилоксиметил)індан-1-іл]піперазин, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, N-(3-хлор-5-фторбензил)-N-метил-2-(1піперазиніл)-2-інданкарбоксамід, а також адитивні в якій R1, R2, R3, P2, n і Tos є такими ж, як висолі з фармацевтично прийнятною кислотою, значено тут вище, 1-[(1RS)-1-(3,5з якої відщеплюють пара-толуолсульфонільну дифторбензилоксиметил)індан-1-іл]піперазин, йогрупу, го оптичні ізомери, а також адитивні солі з фармазнімають захист кислотної групи і потім аміноцевтично прийнятною кислотою, групу захищають, щоб одержати сполуку формули (1RS)-N-(3,5-дифторбензил)-N-метил-1-(1(VI): піперазиніл)-1-інданкарбоксамід, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, 1-[(1RS)-1-(3,5-дифторбензилоксиметил)-5,6дифторіндан-1-іл]піперазин, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою, і 1-[(1RS)-1-(3-бром-5фторбензилоксиметил)iндан-1-іл]піперазин, його оптичні ізомери, а також адитивні солі з фармацевтично прийнятною кислотою. в якій R1, R2, R3 і n є такими ж, як визначено Винахід відноситься також до способу одертут вище, і Р3 являє собою захисну групу для аміжання сполук формули (І), зі сполуки формули (II): ногрупи, - сполуку формули (VI) піддають реакції, коли бажаним є одержати сполуки формули (І), в якій X 13 87989 14 являє собою -(CO)-NR4-Ak- або -CH2-NR4-Ak, зі сполукою формули (VII): в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище, HNR4-Ak-Ar (VII) спирт формули (IX) піддають реакції, коли бажаним є одержати сполуки формули (Іс), конкретв якій R4, Ak і Ar є такими ж, як визначено для ний випадок сполук формули (І), в якій X являє формули (І), у присутності одного або більше з'єдсобою групу -СН2-О-Аk-, зі сполукою формули (X): нувальних агентів, щоб одержати, після зняття захисту, кільцевої Hal-Ak-Ar (X) аміногрупи, сполуки формули (Іа), конкретний випадок сполук формули (І), в якій X являє собою в якій Ak і Ar є такими ж, як визначено для фогрупу -(СО)-NR4-Ak: рмули (І), і Hal являє собою атом галогену, щоб одержати, після зняття захисту кільцевої аміногрупи, сполуки формули (Іс): в якій R1, R2, R3 n, R4 і Ak є такими ж, як визначено тут вище, і Ar є таким же, як визначено для формули (І), яку піддають реакції, коли бажаним є одержати сполуки формули (Іb), конкретний випадок сполук формули (І), в якій X являє собою групу -CH2NR4-Ak, з відновлювальним агентом, з тим, щоб одержати сполуки формули (Іb): в якій R1, R2, R3, n, R4, Ak і Ar є такими ж, як визначено тут вище, - або сполуку формули (VI) етерифікують, коли бажаним є одержати сполуки формули (І), в якій X являє собою групу -СН2-ОАк- або -CH2-NR4-(CO)-, щоб одержати сполуку формули (VIII): в якій R1, R2, R3, n, Ak і Ar є такими ж, як визначено тут вище, або спирт формули (IX) перетворюється за допомогою звичайної методики в органічній хімії в амін формули (XI): в якій R1, R2, R3, n, R4 і Р3 є такими ж, як визначено тут вище, який піддають реакції зі сполукою формули (XII): в якій Ar є таким же, як визначено для формули (І), щоб одержати, після зняття захисту кільцевої аміногрупи, сполуки формули (Id), конкретний випадок сполук формули (І), в якій X являє собою групу -СН2-NR4-(CO)-: в якій R1, R2, R3, n і Р3 є такими ж, як визначено тут вище, і Р4 являє собою бензил або лінійну або розгалужену С1-С6алкільну групу, яку вміщують у присутності відновлювального агенту, з тим, щоб одержати спирт формули (IX): в якій R1, R2, R3, n, R4 і Ar є такими ж, як визначено тут вище, сполуки формул (la), (Ib), (Іс) і (Id) очищують відповідно до звичайної техніки очищення, розді 15 87989 16 ляють, коли бажано, на їх оптичні ізомери і перезнімають захист аміногрупи; щоб одержати творюють, коли бажано, в їх адитивні солі з фарсполуку формули (Іе), мацевтично прийнятною кислотою. яку розділяють, коли бажано, на її оптичні ізоСполуки (Іе), конкретний випадок сполук формери і перетворюють, коли бажано, в адитивні солі мули (І), коли X являє собою групу формули СН2Оз фармацевтично прийнятною кислотою. СН(СН3)-: Сполуки даного винаходу є інгібіторами оберненого захоплення серотоніну і ΝΚ1 антагоністами. Вони є корисними як лікарські засоби у лікуванні депресивних станів, станів тривожності, імпульсивних розладів, агресивної поведінки, наркотичної залежності, ожиріння і розладів апетиту, болю і запалення, недоумства, психотичних станів, порушень хронобіологічних ритмів, нудоти і кишковошлункових розладів. Даний винахід відноситься також до фармацевтичних композицій, які містять як активний інгредієнт сполуку формули (І) або її адитивну сіль з в якій R1, R2, R3, n і Ar є такими ж, як визначефармацевтично прийнятною кислотою, в комбінано тут вище, можуть також бути одержані конденції з одним або більше фармацевтично прийнятсуванням сполуки формули (IX) зі сполукою форним, інертним, нетоксичним ексципієнтом або номули (XIII): сієм. Серед фармацевтичних композицій відповідно Ar-СО2Н (XIII) до винаходу можуть бути згадані більш конкретно ті, які прийнятні для орального, парентерального в якій Ar є таким же, як визначено тут вище, (внутрішньовенного, внутрішньом'язового або підщоб одержати сполуку формули (XIV): шкірного), під- або через-шкірного, назального, ректального, під'язикового, очного або респіраторного введення, і особливо таблетки або драже, під'язикові таблетки, желатинові капсули, капсули, супозиторії, креми, мазі, шкірні гелі, ін'єктовані або придатні для пиття препарати, аерозолі, очні краплі ока і краплі для носа. Корисне дозування варіює відповідно до віку і ваги пацієнта, шляху введення, природи і тяжкості розладу і введення будь-якого пов'язаного лікув якій R1, R2, R3, n, Ar і Р3 є такими ж, як визнавання і знаходиться в діапазоні від 0,5 до 500мг на чено тут вище, день за одне або більше введень. яку піддають реакції з Наступні приклади ілюструють винахід. Викобіс(циклопентадієніл)диметилтитаном, щоб одерристані вихідні матеріали являють собою відомі жати сполуку формули (XV): продукти або їх одержують відповідно до відомих методик. Різні Приготування дають проміжні сполуки синтезу, які є корисними у приготуванні сполук даного винаходу. Структури сполук, які описуються у Прикладах, були визначені відповідно до звичайних спектрофотометричних методик (інфрачервоний, ядерний магнітний резонанс, мас-спектрометрія). Сполука конфігурації (1a), як повинно бути зрозумілим, є сполукою, яку вибирають зі сполук абсолютних конфігурацій (1R) і (1S), повинно бути в якій R1, R2, R3, n, Ar і Р3 є такими ж, як визназрозумілим, що коли (1a) сполука являє собою чено тут вище, яку гідрогенізують, щоб одержати сполуку фосполуку конфігурації (1R) (1b) сполука являє сормули (XVI): бою інший енантіомер. Сполука конфігурації (1a'), як повинно бути зрозумілим, є сполукою, яку вибирають зі сполук абсолютних конфігурацій (1R) і (1S), повинно бути зрозумілим, що коли (1a') сполука являє собою сполуку конфігурації (1R) (1b') сполука являє собою інший енантіомер. Сполука конфігурації (1RS), як повинно бути зрозумілим, є рацемічною сумішшю двох енантіомерів абсолютних конфігурацій (1R) і (1S). Приготування 1: (1RS)-1-[4-(третв якій R1, R2, R3, n, Ar і Р3 є такими ж, як визнабутилоксикарбоніл)-1-піперазиніл]-1-інданчено тут вище, карбонова кислота. 17 87989 18 Стадія А: Бензил (1RS)-1-[(третСтадія Е: (1RS)-1-(1-Піперазиніл)-1бутилоксикарбоніл)аміно]-1-інданкарбоксилат. інданкарбонової кислоти дигідробромід. До 0,140моль 1-[(третДо 100мл 30% розчину бромисто-водневої кибутилоксикарбоніл)аміно]-1-інданкарбонової кисслоти в оцтовій кислоті додають 40мл оцтової кислоти додають 750мл диметилформаміду і потім лоти, 12,5ммоль нафталіну і 12,5ммоль сполуки, 0,147моль карбонату цезію. Перемішування потім одержаної на Стадії вище. Нагрівання зі зворотпроводять протягом 2 хвилин годин 30 при темпеним холодильником проводять протягом 1 години, ратурі навколишнього середовища і потім вливаз наступним концентруванням. Залишок додають у ють, краплями, протягом 1/2 годин, в 0,145моль воду, і водну фазу промивають етилацетатом і бензил броміду, розчиненого в 150мл диметилфопотім випаровують. Твердий залишок промивають рмаміду, і перемішування проводять протягом 20 ацетонітрилом і потім висушують з тим, щоб одегодин при температурі навколишнього середовиржати очікуваний продукт. ща. ІЧ С=О 1740см-1 u Мінеральні солі відфільтровують і розчинник Стадія F: (1RS)-1-[4-(трет-Бутилоксикарбоніл)випаровують. Залишок повторно розчиняють в 1-піперазиніл]-1-інданкарбонова кислота. етилацетаті і промивають водою. Органічну фазу До 9,26ммоль сполуки, одержаної на Стадії висушують і потім випаровують з тим, щоб одервище, додають 40мл діоксану і 37мл 1N розчину жати очікуваний продукт. гідроксиду натрію. До одержаного розчину додаІЧ u: 3284нм-1 -ΝΗ ють, краплями і при температурі навколишнього 1735-1672см-1 >С=0 середовища, розчин 10,2ммоль ди-трет-бутил диСтадія В: Бензил (1RS)-1-аміно-1карбонату в 100мл діоксану. Перемішування проінданкарбоксилат гідрохлорид. водять протягом 5 годин і тоді діоксан випарову0,471моль сполуки, одержаної на стадії вище, ють. РН доводять до 4-5, використовуючи 1N додають до 2 літрів етилацетату. Потік газу водень хлористоводневу кислоту, і проводять насичення хлориду пропускають протягом 1 години 15 хвихлоридом натрію і екстрагування етилацетатом. лин, з перемішуванням, і потім перемішування Органічну фазу висушують і випаровують з тим, продовжують протягом 20 годин при температурі щоб одержати очікуваний продукт. навколишнього середовища. Очікуваний продукт ІЧ ОН 2200-2300см-1 u одержують випаровуванням етилацетату. С=О 1624-1731см-1 -1 ІЧ u: 1741см >С=0 Приготування 2: 2-[4-(третСтадія С: Бензил (1RS)-1-[4-(параБутилоксикарбоніл)-1-піперазиніл]-2толуолсульфоніл)-1-піперазиніл]-1інданкарбонова кислота. інданкарбоксилат. Очікуваний продукт одержують відповідно до До 0,235моль сполуки, одержаної на стадії методики, яка описана у Приготуванні 1, замінюювище, додають 750мл диметилформаміду, 750мл чи, на Стадії А, 1-[(трет-бутилоксикарбоніл)аміно]діізопропілетиламіну і 0,235моль N,N-біс(21-інданкарбонову кислоту на 2-[(третхлоретил)пара-толуолсульфонаміду. Нагрівання зі бутилоксикарбоніл)аміно]-2-інданкарбонову кислозворотним холодильником проводять протягом 48 ту і бензил бромід на 1-брометан. годин і потім розчинники випаровують. Залишок Приклад 1: 1-[(1RS)-1-(3,5розчиняють в етилацетаті і промивають водою. дибромбензилоксиметил)індан-1-іл]піперазин дигіОрганічну фазу висушують і випаровують. Залидрохлорид. шок очищують хроматографією на силікагелі, виСтадія А: Бензил (1RS)-1-[4-(треткористовуючи 98/2 суміш метилен хлобутилоксикарбоніл)-1-піперазиніл]-1рид/етилацетат як елюент з тим, щоб одержати інданкарбоксилат. очікуваний продукт. До 63,5ммоль сполуки Приготування 1 додають 550мл диметилформаміду і 66ммоль карбонаІЧ С=О 1728см-1 u ту цезію; перемішування проводять протягом 2 асиметричний SO2 1348см-1 годин при температурі навколишнього середовисиметричний SO2 1164см-1 ща і потім додають, краплями протягом ½ години, Стадія D: (1RS)-1-[4-(Пара-толуолсульфоніл)розчин 65,7ммоль бензил броміду в 50мл димети1-піперазиніл]-1-інданкарбонова кислота. лформаміду. Перемішування продовжують протяДо 0,181моль сполуки, одержаної на стадії гом 20 годин при температурі навколишнього севище, додають 620мл діоксану, і потім 620мл 1N редовища і розчинник потім випаровують. розчину гідроксиду натрію і 360мл води. НагріванЗалишок виливають в етилацетат; органічну фазу ня зі зворотним холодильником проводять протяпромивають водою, висушують і випаровують з гом 20 годин і потім діоксан випаровують. Нейтратим, щоб одержати очікуваний продукт у формі лізацію проводять за допомогою додавання 620мл безбарвної олії. 1N хлористоводневої кислоти, і потім проводять Стадія В: (1RS)-1-[4-(трет-Бутилоксикарбоніл)екстрагування метилен хлоридом. Органічну фазу 1-піперазиніл]-1-гідроксиметиліндан. висушують і випаровують. Залишок кристалізують До 250мл тетрагідрофурану і 63,2ммоль літій з етилового ефіру і потім відфільтровують з тим, алюміній гідриду додають, протягом 1 години 15 щоб одержати очікуваний продукт. хвилин, підтримуючи при цьому температуру реаІЧ ОН 1800-3000см-1 u кційної суміші нижче 20°С, розчин 57,5ммоль споС=О 1706см-1 луки, одержаної на Стадії вище, в 550мл тетрагідС=О 1596см-1 рофурану. Після додавання перемішування SO2 1348-1165см-1 продовжують протягом ½ години при 20°С; гідроліз СН... 772-732см-1 19 87989 20 потім проводять з 50мл ізопропанолу, з наступни1, замінюючи сполуку Приготування 1 на Стадії А ми 50мл насиченого розчину хлориду натрію. Фіна сполуку Приготування 2. льтрування проводять і фільтрат випаровують; Стадія В 1-[2-(3,5залишок повторно розчиняють в етилацетаті і Диметилбензилоксиметил)індан-2-іл]піперазин промивають водою. Висушена і випарена органічдигідрохлорид. на фаза дає очікуваний продукт. Очікуваний продукт одержують відповідно до методики, яка описана на Стадіях С і D Прикладу ІЧ ОН 3440см-1 u 1, починаючи зі сполуки, одержаної на Стадії А С=О 1691см-1 вище, і 3,5-диметилбензил броміду. Стадія С: 4-(трет-Бутилоксикарбоніл)-1-[(1RS)Елементний мікроаналіз: 1-(3,5-дибромбензилоксиметил)індан-1%С %Н %N %Сl іл]піперазин. Підраховано 65,24 7,62 6,62 16,75 До 30мл диметилформаміду і 5,4ммоль гідриЗнайдено 65,92 7,52 6,64 16,91 ду натрію 95% додають, протягом 10 хвилин, розПриклад 4: (1RS)-N-(3,5-Дибромбензил)-1-(1чин 3,6ммоль сполуки, одержаної на Стадії вище, піперазиніл)-1-інданкарбоксамід дигідрохлорид. в 50мл диметилформаміду. Нагрівання при 50Стадія А: (1RS)-N-(3,5-Дибромбензил)-1-[460°С проводять протягом ½ години і температурі (трет-бутилоксикарбоніл)-1-піперазиніл]потім дають повернутись до температури навкоінданкарбоксамід. лишнього середовища. 0,36ммоль тетрабутилаДо 2ммоль сполуки Приготування 1 додають моній йодиду потім додають і потім, протягом 10 50мл диметилформаміду, 2ммоль 3,5хвилин, розчин 5,4ммоль 3,5-дибромбензил бродибромбензиламіну, 2ммоль 1міду в 30мл диметилформаміду. Перемішування гідроксибензотриазолу і 2ммоль дициклогексилкапродовжують протягом 20 годин при температурі рбодііміду. Проводять перемішування протягом 20 навколишнього середовища. годин при температурі навколишнього середовиРозчинник випаровують, і залишок потім поща і потім випаровування. Залишок потім виливавторно розчиняють в етилацетаті. Проводять проють в етилацетат. Утворену дициклогексилсечомивання водою і розчином хлориду натрію. Оргавину видаляють фільтруванням; органічну фазу нічну фазу висушують і випаровують. Продукт потім промивають насиченим розчином бікарбонаочищують хроматографією на силікагелі (елюент: ту натрію, з наступним насиченим розчином хлоCH2Cl2/AcOEt 90/10) з тим, щоб одержати очікувариду натрію. Після висушування, випаровування і ний продукт. очищення хроматографією на силікагелі (елюент: ІЧ С=O 1688см-1 u CH2Cl2/AcOEt 95/5) одержують очікуваний продукт. Стадія D: 1-[(1RS)-1-(3,5ІЧ NH 3347см-1 u Дибромбензилоксиметил)індан-1-іл]піперазин диС=О 1668см-1 гідрохлорид. Стадія В: (1RS)-N-(3,5-Дибромбензил)-1-(1До 2,75ммоль сполуки, одержаної на Стадії піперазиніл)-1-інданкарбоксамід дигідрохлорид. вище, розчиненої в 30мл етилацетату, додають До 1,6ммоль сполуки, одержаної на Стадії ви15мл 1N розчину хлористоводневої кислоти в діокще, розчиненої в 30мл етилацетату, додають 15мл сані. Після перемішування протягом 20 годин при 4N розчину хлористоводневої кислоти в діоксані, і температурі навколишнього середовища одержареакційну суміш потім перемішують протягом 20 ний осад відфільтровують, промивають етилацегодин при температурі навколишнього середовитатом і потім повторно розчиняють у воді. Після ща. Одержаний осад відфільтровують і потім повипаровування і висушування одержують очікувавторно розчиняють в 5мл води. ний продукт. Після випаровування води і висушування одеЕлементний мікроаналіз: ржують очікуваний продукт. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 45,60 4,74 5,06 12,82 Знайдено 45,95 4,80 5,12 13,16 %С %Н %N %Сl Приклад 2: 1-[(1RS)-1-(3,5Підраховано 44,55 4,61 7,42 12,52 Диметилбензилоксиметил)індан-1-іл]піперазин Знайдено 44,92 4,45 7,44 11,54 дигідрохлорид. Приклад 5: N-[3,5-Біс(трифторметил)бензил]Очікуваний продукт одержують відповідно до 2-(1-піперазиніл)-2-інданкарбоксамід дигідрохлометодики, яка описана у Прикладі 1, замінюючи рид. 3,5-дибромбензил бромід на Стадії С на 3,5Очікуваний продукт одержують відповідно до диметилбензил бромід. методики Прикладу 4, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 2 і 3,5-біс(трифторметил)бензиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 65,24 7,62 6,62 16,75 %С %Н %N %Сl Знайдено 65,71 7,49 6,53 16,46 Підраховано 51,44 4,63 7,72 11,88 Приклад 3: 1-[2-(3,5Знайдено 51,42 4,73 7,71 10,82 Диметилбензилоксиметил)індан-2-іл]піперазин Приклад 6: [3,5-Біс(трифторметил)феніл]-Nдигідрохлорид. {[2-(1-піперазиніліндан-2-іл]-метил}метанамін триСтадія А: 2-[4-(трет-Бутилоксикарбоніл)-1гідрохлорид. піперазиніл]-2-гідроксиметиліндан. До 3ммоль сполуки Прикладу 5, розчиненої в Очікуваний продукт одержують відповідно до 80мл тетрагідрофурану, додають, під азотом і прометодики, яка описана на Стадіях А і В Прикладу тягом 20 хвилин, 30ммоль 2N розчину диметил 21 87989 22 сульфіду борану в тетрагідрофурані. Реакційну %С %Н %N %Сl суміш потім нагрівають зі зворотним холодильниПідраховано 68,78 6,84 5,94 15,04 ком протягом 18 годин і згодом повертають до Знайдено 69,38 7,09 5,99 15,03 температури навколишнього середовища. 50мл Приклад 13: 1-[2-(3,54N хлористоводневої кислоти потім додають крапДиметоксибензилоксиметил)індан-2-іл]піперазин лями і нагрівання зі зворотним холодильником дигідрохлорид. згодом проводять знову протягом 20 годин, перед Очікуваний продукт одержують відповідно до випаруванням розчинників, підлуговуючи розчиметодики Прикладу 1, починаючи зі сполуки Прином гідроксиду натрію і екстрагуючи реакційну суготування 2 і 3,5-диметоксибензил броміду. міш етилацетатом. Органічну фазу промивають Елементний мікроаналіз: насиченим розчином хлориду натрію, висушують і %С %Н %N %Сl Підраховано 60,66 7,08 6,15 15,57 потім випаровують. Після очищення хроматографією, перетворення в сіль, використовуючи хлоЗнайдено 60,96 7,30 6,07 15,71 ристоводневу кислоту і випаровування, одержують Приклад 14: 1-[2-(3,5очікуваний продукт після висушування. Дихлорбензилоксиметил)індан-2-іл]піперазин дигіЕлементний мікроаналіз: дрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 49,69 5,02 7,56 17,22 методики Прикладу 1, починаючи зі сполуки ПриЗнайдено 49,77 5,01 7,38 17,37 готування 2 і 3,5-дихлорбензил броміду. Приклад 7: N-Бензил-N-метил-2-(1Елементний мікроаналіз: %С %Н %N %Сl піперазиніл)-2-інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Підраховано 54,33 5,64 6,03 30,55 Знайдено 54,08 5,31 6,12 30,15 методики Прикладу 4, починаючи зі сполуки ПриПриклад 15: 1-[2-(3,4готування 2 і N-бензил-N-метиламіну. Дихлорбензилоксиметил)індан-2-іл]піперазин дигіЕлементний мікроаналіз: дрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 63,66 6,99 9,95 15,37 Знайдено 63,64 6,71 10,24 15,86 методики Прикладу 1, починаючи зі сполуки Приготування 2 і 3,4-дихлорбензил броміду. Приклад 8: 1-[(1a)-1-(3,5Елементний мікроаналіз: Диметилбензилоксиметил)індан-1-іл]піперазин %С %Н %N %Сl дигідрохлорид. Підраховано 54,33 5,64 6,03 30,55 Очікуваний продукт одержують розділенням Знайдено 53,99 5,46 6,03 29,99 сполуки Прикладу 2 на хіральній ВЕРХ колонці. Приклад 16: 1-[2-(3,5Приклад 9: 1-[(1b)-1-(3,5Дибромбензилоксиметил)індан-2-іл]піперазин диДиметилбензилоксиметил)індан-1-іл]піперазин гідрохлорид. дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт являє собою другий з енаметодики Прикладу 1, починаючи зі сполуки Принтіомерів, одержаних розділенням сполуки Приготування 2 і 3,5-дибромбензил броміду. кладу 2 на хіральній ВЕРХ колонці. Елементний мікроаналіз: Приклад 10: (1RS)-N-[3,5%С %Н %N %Сl Біс(трифторметил)бензил]-1-(1-піперазиніл)-1Підраховано 45,60 4,74 5,06 12,82 інданкарбоксамід дигідрохлорид. Знайдено 45,48 4,83 5,03 12,79 Очікуваний продукт одержують відповідно до Приклад 17: 1-[2-[3,5методики Прикладу 4, замінюючи 3,5Біс(трифторметил)бензилоксиметил]індан-2-іл]дибромбензиламін на Стадії А на 3,5піперазин дигідрохлорид. біс(трифторметил)бензиламін. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики Прикладу 1, починаючи зі сполуки При%С %Н %N %Сl готування 2 і 3,5-біс(трифторметил)бензил броміПідраховано 50,75 4,63 7,72 13,03 ду. Знайдено 51,08 4,86 7,79 13,45 Елементний мікроаналіз: Приклад 11: (1RS)-N-Бензил-N-метил-1-(1%С %Н %N %Сl піперазиніл)-1-інданкарбоксамід дигідрохлорид. Підраховано 51,99 4,93 5,27 13,34 Очікуваний продукт одержують відповідно до Знайдено 52,48 5,05 5,34 13,12 методики Прикладу 4, починаючи зі сполуки ПриПриклад 18: (1RS)-N-Бензил-1-(1-піперазиніл)готування 1 і N-метилбензиламіну. 1-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, замінюючи 3,5Підраховано 62,56 6,92 9,95 16,79 дибромбензиламін на Стадії А на бензиламін. Знайдено 62,27 6,86 9,73 17,91 Елементний мікроаналіз: Приклад 12: 1-[2-(Біфеніл-4%С %Н %N %Сl ілметоксиметил)індін-2-іл]піперазин дигідрохлоПідраховано 61,77 6,66 10,29 17,36 рид. Знайдено 61,63 7,06 10,24 17,38 Очікуваний продукт одержують відповідно до Приклад 19: 1-[2-(Нафт-2методики Прикладу 1, починаючи зі сполуки Приилметоксиметил)індан-2-іл]піперазин дигідрохлоготування 2 і біфеніл-4-ілметил броміду. рид. Елементний мікроаналіз: 23 87989 24 Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 1, починаючи зі сполуки Приметодики, яка описана на Стадії А Прикладу 4, готування 2 і нафт-2-илметил броміду. починаючи зі сполуки Приготування 1 і (1R)-1Елементний мікроаналіз: фенетиламіну. %С %Н %N %Сl Стадія В: (1a)-Ν-[(1R)-1-Фенетил]-1-[4-(третПідраховано 67,41 6,79 6,29 15,92 бутилоксикарбоніл)-1-піперазиніл]-1Знайдено 66,99 7,18 6,29 15,69 інданкарбоксамід. Приклад 20: (1RS)-N-[3,5Очікуваний продукт одержують розділенням, Біс(трифторметил)бензил]-N-метил-1-(1за допомогою хроматографії на силікагелі, діастепіперазиніл)-1-інданкарбоксамід дигідрохлорид. реоізомерної суміші, одержаної на Стадії А. Очікуваний продукт одержують відповідно до Стадія С: (1a)-N-[(1R)-1-Фенетил]-1-(1методики Прикладу 4, починаючи зі сполуки Припіперазиніл)-1-інданкарбоксамід дигідрохлорид. готування 1 і N-метил-3,5Очікуваний продукт одержують відповідно до біс(трифторметил)бензиламіну. методики, яка описана на Стадії В Прикладу 4, Елементний мікроаналіз: починаючи зі сполуки, одержаної на Стадії В. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 51,62 4,87 7,53 12,70 %С %Н %N %Сl Знайдено 51,40 4,85 7,48 11,77 Підраховано 62,56 6,92 9,95 16,79 Приклад 21: N-(3,5-Дихлорбензил)-2-(1Знайдено 62,69 7,21 9,85 16,54 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Приклад 25: (1b)-Ν-[(1R)-Фенетил]-1-(1Очікуваний продукт одержують відповідно до піперазиніл)-1-інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 3,5-дихлорбензиламіну. методики, яка описана на Стадії В Прикладу 4, Елементний мікроаналіз: починаючи з другого з діастереоізомерів, розділе%С %Н %N %Сl них на Стадії В Прикладу 24. Підраховано 52,85 5,28 8,80 29,71 Елементний мікроаналіз: Знайдено 53,30 5,34 9,00 28,89 %С %Н %N %Сl Приклад 22: (1a)-Ν-[(1S)-1-Фенетил]-1-(1Підраховано 62,56 6,92 9,95 16,79 піперазиніл)-1-інданкарбоксамід дигідрохлорид. Знайдено 62,71 7,25 9,92 16,27 Стадія А: (1RS)-N-[(1S)-1-Фенетил]-1-[4-(третПриклад 26: (1RS)-N-(2-Фенетил)-1-(1бутилоксикарбоніл)-1-піперазиніл-1піперазиніл)-1-інданкарбоксамід дигідрохлорид. інданкарбоксамід. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, замінюючи 3,5методики, яка описана на Стадії А Прикладу 4, дибромбензиламін на Стадії А на 2-фенетиламін. починаючи зі сполуки Приготування 1 і (1S)-1Елементний мікроаналіз: фенетиламін. %С %Н %N %Сl Стадія В: (1a)-N-[(1S)-1-Фенетил]-1-[4-(третПідраховано 62,56 6,92 9,95 16,79 бутилоксикарбоніл)-1-піперазиніл-1Знайдено 62,34 7,17 9,83 16,65 інданкарбоксамід. Приклад 27: (1RS)-N-(3,4-Дихлорбензил)-1-(1Очікуваний продукт одержують розділенням, піперазиніл)-1-індінкарбоксамід дигідрохлорид. за допомогою хроматографії на силікагелі, діастеОчікуваний продукт одержують відповідно до реоізомерної суміші, одержаної на Стадії А. методики Прикладу 4, замінюючи 3,5Стадія С: (1a)-Ν-[(1S)-1-Фенетил]-1-(1дибромбензиламін на Стадії А на 3,4піперазиніл)-1-інданкарбоксамід дигідрохлорид. дихлорбензиламін. Починаючи зі сполуки, одержаної на Стадії В, Елементний мікроаналіз: очікуваний продукт одержують відповідно до ме%С %Н %N %Сl тодики, яка описана на Стадії В Прикладу 4. Підраховано 52,8 5,28 8,80 29,71 Елементний мікроаналіз: Знайдено 53,26 5,52 8,83 28,98 %С %Н %N %Сl Приклад 28: 2-(1-Піперазиніл)-N-(3Підраховано 62,56 6,92 9,95 16,79 піридилметил)-2-інданкарбоксамід тригідрохлорид. Знайдено 62,69 7,21 9,85 16,54 Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки ПриПриклад 23: (1b)-N-[(1S)-1-Фенетил]-1-(1готування 2 і 3-піридилметиламіну. піперазиніл)-1-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадії В Прикладу 4, Підраховано 53,88 6,10 12,57 23,86 починаючи з другого з діастереоізомерів, розділеЗнайдено 53,94 6,20 12,30 23,76 них на Стадії В Прикладу 22. Приклад 29: 2-(1-Піперазиніл)-N-(2Елементний мікроаналіз: тієнілметил)-2-інданкарбоксамід дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 62,56 6,92 9,95 16,79 методики Прикладу 4, починаючи зі сполуки ПриЗнайдено 62,57 7,08 9,90 16,32 готування 2 і 2-тієнілметиламіну. Приклад 24: (1a)-Ν-[(1R)-1-Фенетил]-1-(1Елементний мікроаналіз: піперазиніл)-1-інданкарбоксамід дигідрохлорид. %С %Н %N %S %Сl Стадія А: (1RS)-N-[(1R)-1-Фенетил]-1-[4-(третПідраховано 55,07 6,08 10,14 7,74 17,11 бутилоксикарбоніл)-1-піперазиніл]-1Знайдено 54,96 6,07 10,75 7,53 16,56 інданкарбоксамід. 25 87989 26 Приклад 30: 2-(1-Піперазиніл)-N-[4Підраховано 66,94 6,45 8,67 14,64 (трифторметил)бензил]-2-інданкарбоксамід дигідЗнайдено 66,26 6,41 8,57 14,09 рохлорид. Приклад 37: N-(Біфеніл-4-ілметил)-2-(1Очікуваний продукт одержують відповідно до піперазиніл)-2-інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 4-(трифторметил)бензиламіну. методики Прикладу 4, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 2 і біфеніл-4-ілметиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 55,47 5,50 8,82 14,88 %С %Н %N %Сl Знайдено 55,13 5,43 8,93 14,98 Підраховано 66,94 6,45 8,67 14,64 Приклад 31: N-(2-Фенетил)-2-(1-піперазиніл)-2Знайдено 66,26 6,41 8,57 14,09 інданкарбоксамід дигідрохлорид. Приклад 38: N-(3,5-Диметилбензил)-2-(1Очікуваний продукт одержують відповідно до піперазиніл)-2-інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 2-фенетиламіну. методики Прикладу 4, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 2 і 3,5-диметилбензіламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 62,56 6,92 9,95 16,79 %С %Н %N %Сl Знайдено 63,42 6,91 10,06 16,63 Підраховано 63,30 7,16 9,63 16,25 Приклад 32: N-(1-Нафтилметил)-2-(1Знайдено 63,50 7,28 10,23 16,19 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Приклад 39: N-[(1R)-1-Фенетил]-2-(1Очікуваний продукт одержують відповідно до піперазиніл)-2-інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 1-нафтилметиламіну. методики Прикладу 4, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 2 і (1R)-1-фенетиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 65,50 6,38 9,17 15,47 %С %Н %N %Сl Знайдено 65,86 6,52 9,83 14,72 Підраховано 62,56 6,92 9,95 16,79 Приклад 33: (1RS)-N-(2,4-Дихлорбензил)-1-(1Знайдено 62,49 7,03 10,44 16,97 піперазиніл)-1-інданкарбоксамід дигідрохлорид. Приклад 40: N-[(1S)-1-Фенетил]-2-(1Очікуваний продукт одержують відповідно до піперазиніл)-2-інданкарбоксамід дигідрохлорид. методики Прикладу 4, замінюючи 3,5Очікуваний продукт одержують відповідно до дибромбензиламін на Стадії А на 2,4методики Прикладу 4, починаючи зі сполуки Придихлорбензиламін. готування 2 і (1S)-1-фенетиламіну Елементний мікроаналіз: Елементний мікроаналіз: %С %Н %N %Сl %С %Н %N %Сl Підраховано 52,85 5,28 8,80 29,71 Підраховано 62,56 6,92 9,95 16,79 Знайдено 53,69 5,31 8,84 30,27 Знайдено 62,83 7,10 10,34 16,19 Приклад 34: (1RS)-1-(1-Піперазиніл)-N-(3Приклад 41: (1RS)-N-(2-Метоксибензил)-1-(1тієнілметил)-1-інданкарбоксамід дигідрохлорид. піперазиніл-1-інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, замінюючи 3,5методики Прикладу 4, починаючи зі сполуки Придибромбензиламін на Стадії А на 3готування 1 і 2-метоксибензиламіну. тієнілметиламін. Елементний мікроаналіз: Елементний мікроаналіз: %С %Н %N %Сl %С %Н %N %N %Сl Підраховано 60,27 6,67 9,58 16,17 Підраховано 55,07 6,08 10,14 7,74 17,11 Знайдено 59,71 6,91 9,41 15,88 Знайдено 55,68 6,33 10,28 7,62 17,79 Приклад 42: (1RS)-N-(3,5-Диметилбензил)-1Приклад 35: (1RS)-1-(1-Піперазиніл)-N-(2(1-піперазиніл)-1-інданкарбоксамід дигідрохлорид. тієнілметил)-1-інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки Приметодики Прикладу 4, замінюючи 3,5готування 1 і 3,5-диметилбензиламіну. дибромбензиламін на Стадії А на 2Елементний мікроаналіз: тієнілметиламін. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 63,60 7,16 9,63 16,25 %С %Н %N %N %Сl Знайдено 62,89 7,53 9,44 16,06 Підраховано 55,07 6,08 10,14 7,74 17,11 Приклад 43: 2-(1-Піперазиніл)-N-(3Знайдено 55,73 6,35 10,30 7,76 17,49 тієніллметил)-2-інданкарбоксамід дигідрохлорид. Приклад 36: (1RS)-N-(3,5-Дихлорбензил)-1-(1Очікуваний продукт одержують відповідно до піперазиніл)-1-інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 3-тієнілметиламіну. методики Прикладу 4, замінюючи 3,5Елементний мікроаналіз: дибромбензиламін на Стадії А на 3,5%С %Н %N %N %Сl дихлорбензиламін. Підраховано 55,07 6,08 10,14 7,74 17,11 Елементний мікроаналіз: Знайдено 55,34 6,53 9,93 7,96 17,70 %С %Н %N %Сl 27 87989 28 Приклад 44: N-(3,5-Дифторбензил)-2-(1Приклад 51: (1RS)-1-[1-(3,5піперазиніл)-2-інданкарбоксамід дигідрохлорид. Біс(трифторметил)бензилоксиметил)індан-1Очікуваний продукт одержують відповідно до іл]піперазин дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і 3,5-дифторбензиламіну. методики Прикладу 1, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 1 і 3,5-біс(трифторметил)бензил бромі%С %Н %N %Сl ду. Підраховано 56,76 5,67 9,46 15,96 Елементний мікроаналіз: Знайдено 57,26 5,74 9,45 15,41 %С %Н %N %Сl Підраховано 51,99 4,93 5,27 13,34 Приклад 45: N-(4-Метоксибензил)-2-(1піперазиніл)-2-інданкарбоксамід дигідрохлорид. Знайдено 52,31 4,77 5,28 13,54 Очікуваний продукт одержують відповідно до Приклад 52 : 1-[(1RS)-1-(3,5методики Прикладу 4, починаючи зі сполуки ПриДихлорбензилоксиметил)індан-1-іл]піперазин дигіготування 2 і 4-метоксибензиламіну. дрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 1, починаючи зі сполуки ПриПідраховано 60,27 6,67 9,58 16,17 готування 1 і 3,5-дихлорбензил броміду. Знайдено 59,45 6,79 10,41 16,36 Елементний мікроаналіз: %С %Н %N %Сl Приклад 46: N-(4-Бромбензил)-2-(1Підраховано 54,33 5,64 6,03 30,55 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Знайдено 54,97 5,81 6,00 29,88 Очікуваний продукт одержують відповідно до Приклад 53: 1-[(1RS)-1-(3методики Прикладу 4, починаючи зі сполуки При(Трифторметил)бензилоксиметил)індан-1-іл]готування 2 і 4-бромбензиламіну. піперазин дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 1, починаючи зі сполуки ПриПідраховано 51,76 5,38 8,62 14,55 готування 1 і 3-(трифторметил)бензил броміду. Знайдено 52,30 5,36 8,90 13,95 Елементний мікроаналіз: Приклад 47: N-(3-Бромбензил)-2-(1%С %Н %N %Сl піперазиніл)-2-інданкарбоксамід дигідрохлорид. Підраховано 57,03 5,87 6,05 15,30 Очікуваний продукт одержують відповідно до Знайдено 56,75 6,33 5,81 15,16 методики Прикладу 4, починаючи зі сполуки ПриПриклад 54: 2-(1-Піперазиніл)-N-(2готування 2 і 3-бромбензиламіну. піридилметил)-2-інданкарбоксамід тригідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4. починаючи зі сполуки ПриПідраховано 51,76 5,38 8,62 14,55 готування 2 і 2-піридилметиламіну. Знайдено 52,08 5,60 8,84 14,43 Елементний мікроаналіз: Приклад 48: N-(4-Хлорбензил)-2-(1%С %Н %N %Сl піперазиніл)-2-інданкарбоксамід дигідрохлорид. Підраховано 53,88 6,10 12,57 23,86 Очікуваний продукт одержують відповідно до Знайдено 52,54 6,13 12,00 23,85 методики Прикладу 4, починаючи зі сполуки ПриПриклад 55: 2-(1-Піперазиніл)-N-(3готування 2 і 4-хлорбензиламіну. піридилметил)-2-інданкарбоксамід тригідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки ПриПідраховано 56,96 5,92 9,49 24,02 готування 2 і 3-піридилметиламіну. Знайдено 57,22 6,03 9,46 24,07 Елементний мікроаналіз: Приклад 49: N-Бензил-2-(1-піперазиніл)-2%С %Н %N %Сl інданкарбоксамід дигідрохлорид. Підраховано 53,88 6,10 12,57 23,86 Очікуваний продукт одержують відповідно до Знайдено 53,92 5,94 12,43 24,62 методики Прикладу 4, починаючи зі сполуки ПриПриклад 56: N-(2-Бромбензил)-2-(1готування 2 і бензиламіну. піперазиніл)-2-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl Підраховано 61,77 6,66 10,29 17,36 методики Прикладу 4, починаючи зі сполуки ПриЗнайдено 61,09 6,74 10,24 16,80 готування 2 і 2-бромбензиламіну. Елементний мікроаналіз: Приклад 50: (1RS)-N-(3,5-Дибромбензил)-Nметил-1-(1-піперазиніл)інданкарбоксамід дигідрох%С %Н %N %Сl лорид. Підраховано 51,76 5,38 8,62 14,55 Очікуваний продукт одержують відповідно до Знайдено 52,54 5,33 8,66 13,77 методики Прикладу 4, починаючи зі сполуки ПриПриклад 57: N-(4-Фторбензил)-2-(1готування 1 і N-метил-3,5-дибромбензиламіну. піперазиніл)-2-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки При%С %Н %N %Сl готування 2 і 4-фторбензиламіну. Підраховано 45,54 4,69 7,24 12,22 Знайдено 45,11 4,73 7,14 12,96 Елементний мікроаналіз: %С %Н %N %Сl Підраховано 59,16 6,15 9,86 16,63 29 87989 30 Знайдено 58,93 6,04 9,69 16,81 %С %Н %N %Сl Приклад 58: N-(4-Метилбензил)-2-(1Підраховано 54,89 5,44 5,82 14,73 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Знайдено 54,78 5,58 5,79 14,65 Очікуваний продукт одержують відповідно до Приклад 65 : (1RS)-1-(1-Піперазиніл)-N-[3методики Прикладу 4, починаючи зі сполуки При(трифторметил)бензил]-1-інданкарбоксамід дигідготування 2 і 4-метилбензиламіну. рохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки Приготування 1 і 3-(трифторметил)бензиламіну. Підраховано 62,56 6,92 9,95 16,79 Знайдено 62,15 6,60 9,78 17,06 Елементний мікроаналіз: ППриклад 59: N-(3,5-Дибромбензил)-2-(1%С %Н %N %Сl Підраховано 55,47 5,50 8,82 14,88 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Знайдено 56,07 5,78 8,79 14,73 методики Прикладу 4, починаючи зі сполуки ПриПриклад 66: (1RS)-1-(1-Піперазиніл)-N-метилготування 2 і 3,5-дибромбензиламіну. N-[3-(трифторметил)бензил]-1-інданкарбоксамід Елементний мікроаналіз: дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 44,55 4,45 7,42 12,52 методики Прикладу 4, починаючи зі сполуки ПриЗнайдено 44,53 4,76 7,35 12,22 готування 1 і N-метил-3Приклад 60: N-[3,5-Біс(трифторметил)бензил](трифторметил)бензиламіну. N-метил-2-(1-піперазиніл)-2-інданкарбоксамід диЕлементний мікроаналіз: гідрохлорид. %С %Н %N %Сl Підраховано 56,33 5,76 8,57 14,46 Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки ПриЗнайдено 56,10 5,78 8,47 14,72 готування 2 і N-метил-3,5Приклад 67: N-(3,5-Дихлорбензил)-N-метил-2біс(трифторметил)бензиламіну. (1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки ПриПідраховано 53,37 4,94 7,78 9,84 готування 2 і M-метил-3,5-дихлорбензиламіну. Знайдено 53,21 5,15 7,63 9,78 Елементний мікроаналіз: Приклад 61: 2-(1-Піперазиніл)-N-[4%С %Н %N %Сl Підраховано 53,79 5,54 8,55 28,87 (трифторметил)бензил]-2-інданкарбоксамід дигідрохлорид. Знайдено 54,52 5,50 5,68 27,84 Очікуваний продукт одержують відповідно до Приклад 68: (1RS)-N-(3,5-Дифторбензил)-Nметодики Прикладу 4, починаючи зі сполуки Приметил-1-(1-піперазиніл)-1-інданкарбоксамід дигідготування 2 і 4-(трифторметил)бензиламіну. рохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки ПриПідраховано 55,47 5,50 8,82 14,88 готування 1 і>І-метил-3,5-дифторбензиламіну. Знайдено 55,24 5,32 8,62 14,70 Елементний мікроаналіз: Приклад 62: N-(2-Нафтилметил)-2-(1%С %Н %N %Сl піперазиніл)-2-інданкарбоксамід дигідрохлорид. Підраховано 57,65 5,94 9,17 15,47 Очікуваний продукт одержують відповідно до Знайдено 57,73 6,19 9,06 15,71 методики Прикладу 4, починаючи зі сполуки ПриПриклад 69: (1RS)-N-[3-Фтор-5готування 2 і 2-нафтилметиламіну. (трифторметил)бензил]-N-метил-1-(1-піперазиніл)Елементний мікроаналіз: 1-інданкарбоксамід дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 65,50 6,38 9,17 15,47 методики Прикладу 4, починаючи зі сполуки ПриЗнайдено 66,04 6,22 9,00 15,29 готування 1 і N-метил-3-фтор-5-(трифторметил)Приклад 63: N-(3,5-Дифторбензил)-2-(1бензиламіну. піперазиніл)-2-інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки ПриПідраховано 54,34 5,35 8,27 13,95 готування 2 і 3,5-дифторбензиламіну. Знайдено 53,78 5,68 8,11 14,83 Елементний мікроаналіз: Приклад 70: (1RS)-1-[1-(3,5Дифторбензилоксиметил)індан-1-іл]піперазин ди%С %Н %N %Сl гідрохлорид. Підраховано 56,76 5,67 9,46 15,96 Знайдено 56,87 5,81 9,49 15,99 Очікуваний продукт одержують відповідно до Приклад 64: (1RS)-1-[1-(3-Фтор-5методики Прикладу 1, починаючи зі сполуки Приготування 1 і 3,5-дифторбензил броміду. (трифторметил)бензилоксиметил)індан-1іл]піперазин дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 1, починаючи зі сполуки ПриПідраховано 58,47 6,08 6,49 16,44 готування 1 і 3-фтор-5-(трифторметил)бензил Знайдено 58,36 6,04 6,49 16,30 броміду. Приклад 71: N-(3,5-Дибромбензил)-N-метил-2Елементний мікроаналіз: (1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. 31 87989 32 Очікуваний продукт одержують відповідно до Приклад 80: N-[3-Фтор-5методики Прикладу 4, починаючи зі сполуки При(трифторметил)бензил]-N-метил-2-(1-піперазинготування 2 і N-метил-3,5-дибромбензиламіну. іл)-2-інданкарбоксамід дигідрохлорид. Mac-спектрометрія: ESI: [M+H]+ m/z 506,0 Очікуваний продукт одержують відповідно до Приклад 72: N-[3-(Трифторметил)бензил]-Nметодики Прикладу 4, починаючи зі сполуки Приметил-2-(1-піперазиніл)-2-інданкарбоксамід дигідготування 2 і N-метил-3-фтор-5-(трифторметил)рохлорид. бензиламіну. Очікуваний продукт одержують відповідно до Mac-спектрометрія: ESI: [M+H]+ m/z 436,2 методики Прикладу 4, починаючи зі сполуки ПриПриклад 81: N-[3-Фтор-5готування 2 і N-метил-3(трифторметил)бензил]-N-метил-[2-(1-піперазин(трифторметил)бензиламіну. іл)індан-2-іл]метанамін дигідрохлорид. Mac-спектрометрія: ESI: [M+H]+ m/z418,2 Очікуваний продукт одержують відповідно до Приклад 73: N-(3,5-Дифторбензил)-N-метил-2методики Прикладу 6. починаючи зі сполуки При(1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. кладу 80. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: %С %Н %N %Сl методики Прикладу 4, починаючи зі сполуки Приготування 2 і N-метил-3,5-дифторбензиламіну. Підраховано 55,88 5,91 8,50 14,34 Mac-спектрометрія: ESI: [M+H]+ m/z 386,2 Знайдено 55,50 6,32 7,98 14,47 Приклад 74: N-(3,5-Диметилбензил)-N-метилПриклад 82: N-[3-(Трифторметил)бензил]-N2-(1-піперазиніл)-2-інданкарбоксамід дигідрохлометил-[2-(1-піперазиніл)-індан-2-іл]метанамін дигірид. дрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки Приметодики Прикладу 6, починаючи зі сполуки Приготування 2 і N-метил-3,5-диметилбензиламіну. кладу 72. Мас-спектрометрія: ESI: [M+H]+ m/z 378,3 Елементний мікроаналіз: Приклад 75: N-Бензил-N-метил-(1%С %Н %N %Сl піперазиніл)індан-2-іл]метанамін тригідрохлорид. Підраховано 57,99 6,35 8,82 14,88 Знайдено 57,60 6,70 8,59 14,33 Очікуваний продукт одержують відповідно до Приклад 83: N-[3,5-Біс(трифторметил)бензил]методики Прикладу 6, починаючи зі сполуки ПриN-метил-[2-(1-піперазиніл)-індан-2-іл]метанамін кладу 7. дигідрохлорид. Мас-спектрометрія: ESI: [M+H]+ m/z 336,2 Очікуваний продукт одержують відповідно до Приклад 76: N-[3-Фтор-5методики Прикладу 6, починаючи зі сполуки При(трифторметил)бензил]-2-(1-піперазиніл)-2кладу 60. інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки При%С %Н %N %Сl Підраховано 52,95 5,37 7,72 13,02 готування 2 і 3-фтор-5Знайдено 52,87 5,80 7,42 12,74 (трифторметил)бензиламіну. Приклад 84: (1RS)-N-(3,5-Дибромбензил)-NЕлементний мікроаналіз: %С %Н %N %Сl етил-1-(1-піперазиніл)-1-інданкарбоксамід дигідрохлорид. Підраховано 53,45 5,10 8,50 14,34 Знайдено 53,55 5,29 8,73 13,74 Очікуваний продукт одержують відповідно до Приклад 77: N-(3,5-Дифторбензил)-N-метил-[2методики Прикладу 4, починаючи зі сполуки При(1-піперазиніл)індан-2-іл]-метанамін тригідрохлоготування 1 і N-етил-3,5-дибромбензиламіну. рид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 6, починаючи зі сполуки ПриПідраховано 46,49 4,92 7,07 11,93 кладу 73. Знайдено 46,42 5,16 6,96 11,59 Елементний мікроаналіз: Приклад 85: (1RS)-N-(3,5-Дихлорбензил)-N%С %Н %N %Сl метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідрохлорид. Підраховано 54,95 6,29 8,74 22,12 Очікуваний продукт одержують відповідно до Знайдено 54,98 6,49 8,51 22,00 методики Прикладу 4, починаючи зі сполуки ПриПриклад 78: N-3,5-(Диметилбензил)-N-метилготування 1 і N-метил-3,5-дихлорбензиламіну. [2-(1-піперазиніл)індан-2-іл]-метанамін тригідрохЕлементний мікроаналіз: лорид. Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 6, починаючи зі сполуки ПриПідраховано 53,79 5,54 8,55 28,87 Знайдено 54,22 5,61 8,67 29,81 кладу 74. Mac-спектрометрія: ESI: [M+H]+ m/z 364,3 Приклад 86: (1a)-Ν-(3,5-Диметилбензил)-1-(1Приклад 79: N-(3,5-Дихлорбензил)-N-метил-[2піперазиніл)-1-інданкарбоксамід дигідрохлорид. (1-піперазиніл)індан-2-іл]-метанамін тригідрохлоСтадія А: Бензил (1a)-1-[4-(третрид. бутилоксикарбоніл)-1-піперазиніл]-1Очікуваний продукт одержують відповідно до інданкарбоксилат. методики Прикладу 6, починаючи зі сполуки ПриОчікуваний продукт являє собою перший з кладу 67. енантіомерів, які одержують розділенням на хіра+ Mac-спектрометрія: ESI: [M+H] m/z 404,2 33 87989 34 льній ВЕРХ колонці сполуки, одержаної на Стадії Елементний мікроаналіз: А Прикладу 1. %С %Н %N %Сl Підраховано 63,99 7,38 9,33 15,74 Стадія В: (1a)-1-[4-(трет-Бутилоксикарбоніл)-1Знайдено 63,16 7,59 9,09 15,93 піперазиніл]-1-інданкарбонова кислота. Приклад 90: (1a)-N-(1b')-1-(3,5Очікуваний продукт одержують відповідно до методики, яка описана на Стадії F Приготування 1, Диметилфеніл)етил]-1-(1-піперазиніл)-1починаючи зі сполуки Стадії А вище. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Стадія С: (1a)-Ν-(3,5-Диметилбензил)-1-(1методики, яка описана на Стадії В Прикладу 4, піперазиніл)-1-інданкарбоксамід дигідрохлорид. починаючи з другого з діастереоізомерів, які розОчікуваний продукт одержують відповідно до діляють на Стадії В Прикладу 89. методики Прикладу 4, починаючи зі сполуки Стадії Елементний мікроаналіз: В вище і 3,5-диметилбензиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 63,99 7,38 9,33 15,74 %С %Н %N %Сl Знайдено 64,35 7,60 9,39 15,45 Підраховано 63,30 7,16 9,63 16,25 Знайдено 62,93 7,30 9,50 16,40 Приклад 91: (1b)-N-[(1a')-1-(3,5Диметилфеніл)етил]-1-(1-піперазиніл)-1Приклад 87: (1b)-Ν-(3,5-Диметилбензил)-1-(1інданкарбоксамід дигідрохлорид. піперазиніл)-1-інданкарбоксамід дигідрохлорид. Стадія А: (1b)-N-[(1RS)-1-(3,5Стадія А: (1b)-1-[4-(трет-Бутилоксикарбоніл)-1Диметилфеніл)етил]-1-[4-(третпіперазиніл]-1-інданкарбонова кислота. бутилоксикарбоніл)-1-піперазиніл]-1Очікуваний продукт одержують відповідно до інданкарбоксамід. методики, яка описана на Стадії F Приготування 1, Очікуваний продукт одержують відповідно до починаючи з другого з енантіомерів, розділених на методики, яка описана на Стадії А Прикладу 4, Стадії А Прикладу 86. починаючи зі сполуки, одержаної на Стадії А ПриСтадія В: (1b)-Ν-(3,5-Диметилбензил)-1-(1кладу 87 і (RS)-1-(3,5-диметилфеніл)етиламіну. піперазиніл)-1-інданкарбоксамід дигідрохлорид Стадія В: (1b)-N-[(1a')-1-(3,5Очікуваний продукт одержують відповідно до Диметилфеніл)етил]-1-[4-(третметодики Прикладу 4, починаючи зі сполуки Стадії бутилоксикарбоніл)-1-піперазиніл]-1А вище і 3,5-диметилбензиламіну. інданкарбоксамід. Елементний мікроаналіз: Очікуваний продукт одержують хроматографі%С %Н %N %Сl єю на силікагелі (елюент: дихлормеПідраховано 63,30 7,16 9,63 16,25 тан/етилацетат) діастереоізомерної суміші, яку Знайдено 63,46 7,24 9,61 16,77 одержують на Стадії А. Приклад 88: N-(3,5-Дибромбензил)-N-метил-[2Стадія С: (1b)-N-[(1a')-1-(3,5(1-піперазиніл)індан-2-іл]-метанамін дигідрохлорид. Диметилфеніл)етил]-1-(1-піперазиніл)-1Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид. методики Прикладу 6, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до кладу 71. методики, яка описана на Стадії В Прикладу 4, Mac-спектрометрія: ESI: [M+H]+ m/z 492,1 починаючи зі сполуки, одержаної на Стадії В вище. Елементний мікроаналіз: Приклад 89: (1a)-N-[(1a')-1-(3,5%С %Н %N %Сl Диметилфеніл)етил]-1-(1-піперазиніл)-1Підраховано 63,99 7,38 9,33 15,74 інданкарбоксамід дигідрохлорид. Знайдено 64,49 7,75 9,57 15,33 Стадія А: (1a)-N-[(1RS)-1-(3,5Приклад 92: (1b)-N-[(1b')-1-(3,5Диметилфеніл)етил]-1-[4-(третДиметилфеніл)]-1-(1-піперазиніл)-1бутилоксикарбоніл)-1-піперазиніл]-1інданкарбоксамід дигідрохлорид. інданкарбоксамід. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики, яка описана на Стадії В Прикладу 4, методики, яка описана на Стадії А Прикладу 4, починаючи з другого з діастереоізомерів, які розпочинаючи зі сполуки, одержаної на Стадії В Приділяють на Стадії В Прикладу 91. кладу 86 і (RS)-1-(3,5-диметилфеніл)етиламіну. Елементний мікроаналіз: Стадія В: (1a)-N-[(1a')-1-(3,5%С %Н %N %Сl Диметилфеніл)етил]-1-[4-(третПідраховано 63,99 7,38 9,33 15,74 бутилоксикарбоніл)-1-піперазиніл]-1Знайдено 64,00 7,66 9,31 16,13 інданкарбоксамід. Приклад 93: (1RS)-N-(3,5-Диметилбензил)-NОчікуваний продукт одержують хроматографіметил-1-(1-піперазиніл)-1-інданкарбоксамід дигідєю на силікагелі (елюент: дихлормерохлорид. тан/етилацетат) діастереоізомерної суміші, яку Очікуваний продукт одержують відповідно до одержують на Стадії А. методики Прикладу 4, починаючи зі сполуки ПриСтадія С: (1a)-N-[(1a')-1-(3,5готування 1 і N-метил-3,5-диметилбензиламіну. Диметилфеніл)етил]-1-(1-піперазиніл)-1Елементний мікроаналіз: інданкарбоксамід дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 63,99 7,38 9,33 15,75 методики, яка описана на Стадії В Прикладу 4, Знайдено 64,79 7,38 9,57 14,78 починаючи зі сполуки, одержаної на Стадії В вище. 35 87989 36 додають 2,59ммоль трифенілфосфіну і перемішуПриклад 94: (1a)-Ν-[(1S)-2-Гідрокси-1вання проводять протягом ¼ години. Потім додафенілетил]-1-(1-піперазиніл)-1-інданкарбоксамід ють 10мл води і перемішування продовжують продигідрохлорид. тягом 24 годин. Після випарування розчинників, Стадія А: (1RS)-N-[(1S)-2-Гідрокси-1продукцію очищують хроматографією на силікагелі фенілетил]-1-[4-(трет-бутилоксикарбоніл)-1(елюент: дихлорметан/метанол/аміак 85/15/1) з піперазиніл]-1-інданкарбоксамід. тим, щоб одержати очікуваний продукт. Очікуваний продукт одержують відповідно до Стадія С: N-{[2-[4-(трет-Бутилоксикарбоніл)-1методики, яка описана на Стадії А Прикладу 4, піперазиніл]індан-2-іл]метил}-3,5починаючи зі сполуки Приготування 1 і (S)-2біс(трифторметил)бензамід фенілгліцинолу. 2ммоль аміну, який одержують на Стадії В Стадія В: (1a)-Ν-[(1S)-2-Гідрокси-1-фенілетил]вище, розчиняють в 15мл тетрагідрофурану, потім 1-[4-(трет-бутилоксикарбоніл)-1-піперазиніл]-1проводять охолодження до 0°С, і розчин 2ммоль інданкарбоксамід. 3,5-біс(трифторметил)бензоїл хлориду в 5мл тетОчікуваний продукт одержують розділенням, рагідрофурану додають краплями. Перемішування за допомогою хроматографії на силікагелі (елюпотім проводять протягом 1 години, розчинник ент: дихлорметан/етилацетат), діастереоізомерної випаровують і залишок повторно розчиняють в суміші, яку одержують на Стадії А. метиленхлориді і промивають послідовно розчиСтадія С: (1a)-Ν-[(1S)-2-Гідрокси-1-фенілетил]ном бікарбонату натрію, 10% розчином лимонної 1-(1-піперазиніл)-1-інданкарбоксамід дигідрохлокислоти і потім водою. Після випаровування і хрорид. матографії на силікагелі (елюент: дихлормеОчікуваний продукт одержують відповідно до тан/етилацетат 98/2), відновлюють очікуваний методики, яка описана на Стадії В Прикладу 4, продукт. починаючи зі сполуки, одержаної на Стадії В вище. Стадія D: N-{[2-(1-Піперазиніл)індан-2Елементний мікроаналіз: іл]метил}-3,5-біс(трифторметил)-бензамід дигідро%С %Н %N %Сl хлорид. Підраховано 60,27 6,67 9,58 16,17 Очікуваний продукт одержують відповідно до Знайдено 59,95 6,43 9,35 16,25 методики, яка описана на Стадії D Прикладу 1, Приклад 95: (1b)-Ν-[(1S)-Гідрокси-1починаючи зі сполуки, одержаної на Стадії С вифенілетил]-1-(1-піперазиніл)-1-інданкарбоксамід ще. дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадії В Прикладу 4, Підраховано 50,75 4,63 7,72 13,03 починаючи з другого з діастереоізомерів, які розЗнайдено 51,52 4,84 7,72 12,72 діляють на Стадії В Прикладу 94. Приклад 98: N-[(1a)-1-(3,5-Дибромфеніл)етил]Елементний мікроаналіз: 2-(1-піперазиніл)-2-інданкарбоксамід дигідрохло%С %Н %N %Сl рид. Підраховано 60,27 6,67 9,58 16,17 Очікуваний продукт одержують відповідно до Знайдено 59,95 6,64 9,50 16,42 методики Прикладу 4, починаючи зі сполуки ПриПриклад 96: N-[(1R)-1-(3,5готування 2 і (1a)-1-(3,5-дибромфеніл)етиламіну. Диметилфеніл)етил]-2-(1-піперазиніл)-2Точка плавлення: 178-180°С. інданкарбоксамід дигідрохлорид. Приклад 99: N-[(1S)-1-(3,5Очікуваний продукт одержують відповідно до Диметилфеніл)етил]-2-(1-піперазиніл)-2методики Прикладу 4, починаючи зі сполуки Приінданкарбоксамід дигідрохлорид. готування 2 і (R)-1-(3,5-диметилфеніл)етиламіну. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики Прикладу 4, починаючи зі сполуки При%С %Н %N %Сl готування 2 і (S)-1-(3,5-диметилфеніл)етиламіну. Підраховано 63,99 7,38 9,33 15,74 Точка плавлення: 175°С. Знайдено 64,34 7,04 9,45 16,22 Приклад 100: Етил N-[(1b)4-(3,5Приклад 97: N-{[2-(1-Піперазиніл)індан-2Дибромфеніл)]-2-(1-піперазиніл)-2іл]метил}-3,5-біс(трифторметил)-бензамід дигідроінданкарбоксамід дигідрохлорид. хлорид. Очікуваний продукт одержують відповідно до Стадія А: 2-Азидометил-2-[4-(третметодики Прикладу 4, починаючи зі сполуки Прибутилоксикарбоніл)-1-піперазиніл]-2-індан. готування 2 і (1b)-1-(3,5-дибромфеніл)етиламіну. Очікуваний продукт одержують реакцією сполуки, одержаної на Стадії А Прикладу 3, з дифеніТочка плавлення: 192-194°С. лфосфорил азидом (DPPА) і 1,8Приклад 101: (1a)-N-[(1a')-1-(3,5діазабіцикло[5.4.0]ундец-7-еном (DBU), відповідно Біс(трифторметил)феніл)етил]-1-(1до методики, яка описується в [J. Org Chem. 1993, піперазиніл)інданкарбоксамід дигідрохлорид. 58, 5886-5888], і потім очищенням хроматографії Стадія А: ((1a')-1-[3,5на силікагелі (елюент: дихлорметан/етилацетат Біс(трифторметил)феніл]етиламін. 98/2). (1RS)-1-[3,5-Біс(трифторметил)феніл]етиламін ІЧ: N3:2095cm-1 CO:1692cm-1 перетворюють в сіль, використовуючи (L)-винну Стадія В: 2-Амінометил-2-[4-(треткислоту, суміш діастереоізомерів, яку таким чином бутилоксикарбоніл)-1-піперазиніл]-2-індан. одержують, розділяють і потім проводять повторне 2,35ммоль сполуки, одержаної на Стадії А виперетворення в основу на кожному з двох діастеще, розчиняють в 80мл тетрагідрофурану, потім 37 87989 38 реоізомерів. Очікуваний продукт являє собою пеСтадія D: (1a)-N-[(1b')-1-(3,5рший з енантіомерів, які таким чином одержують. Біс(трифторметил)феніл)етил]-1-(1-піперазиніл)Стадія В: (1RS)-N-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Біс(трифторметил)феніл)етил]-1-[4-(третОчікуваний продукт одержують відповідно до бутилоксикарбоніл)-1-піперазиніл]-1методики, яка описана на Стадії В Прикладу 4, інданкарбоксамід дигідрохлорид. починаючи зі сполуки, одержаної на Стадії С вище Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики, яка описана на Стадії А Прикладу 4, %С %Н %N %Сl починаючи зі сполуки Приготування 1 і сполуки, Підраховано 51,62 4,87 7,53 12,70 одержаної на Стадії А вище. Знайдено 51,05 4,68 7,24 12,25 Стадія С: (1a)-N-[(1a')-1-(3,5Приклад 104: (1b)-N-[(1b')-1-(3,5Біс(трифторметил)феніл)етил]-1-[4-(третБіс(трифторметил)фетл)етил]-1-(1бутилоксикарбоніл)-1-піперазиніл]-1піперазиніл)інданкарбоксамід дигідрохлорид. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують розділенням, методики, яка описана на Стадії В Прикладу 4, за допомогою хроматографії на силікагелі (елюпочинаючи з другого з діастереоізомерів, які розент: дихлорметан/етилацетат), діастереоізомерної діляють на Стадії С Прикладу 103. суміші, яку одержують на Стадії В. Елементний мікроаналіз: %С %Н %N %Сl Стадія D: (1a)-Ν-[(1a')-1-(3,5Підраховано 51,62 4,87 7,53 12,70 Біс(трифторметил)феніл)етил]-1-(1-піперазиніл)Знайдено 52,43 5,16 7,52 11,94 інданкарбоксамід дигідрохлорид. Приклад 105: 1-[(1RS)-1-(3 -Бром-5Очікуваний продукт одержують відповідно до фторбензилоксиметил)індан-1-іл]-піперазин дигідметодики, яка описана на Стадії В Прикладу 4, рохлорид. починаючи зі сполуки, одержаної на Стадії С виОчікуваний продукт одержують відповідно до ще. методики Прикладу 1, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 1 і 3-бром-5-фторбензил броміду. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 51,62 4,87 7,53 12,70 %С %Н %N %Сl Знайдено 52,46 5,10 7,50 12,06 Підраховано 51,24 5,32 5,69 14,40 Приклад 102: (1b)-N-[(1a')-1-(3,5Знайдено 51,96 5,28 5,56 14,36 Біс(трифторметил)феніл)етил]-1-(1Приклад 106: 1-[(1RS)-1-(3-Хлор-5піперазиніл)інданкарбоксамід дигідрохлорид. фторбензилоксиметил)індан-1-іл]-піперазин дигідОчікуваний продукт одержують відповідно до рохлорид. методики, яка описана на Стадії В Прикладу 4, Очікуваний продукт одержують відповідно до починаючи з другого з діастереоізомерів, які розметодики Прикладу 1, починаючи зі сполуки Приділяють на Стадії В Прикладу 101. готування 1 і 3-хлор-5-фторбензил броміду. Елементний мікроаналіз: Мас-спектромтерія: ESI (H2O/CH3CN): [M+H]+ %С %Н %N %Сl m/z 375,2 Th Підраховано 51,62 4,87 7,53 12,70 Приклад 107: 1-[2-(3,5Знайдено 51,97 5,00 7,38 11,79 Дифторбензилоксиметил)індан-2-іл]піперазин диПриклад 103: (1a)-N-[(1b')-1-(3,5гідрохлорид. Біс(трифп)рметил)феніл)етил]-1-(1Очікуваний продукт одержують відповідно до піперазиніл)інданкарбоксамід дигідрохлорид методики Прикладу 1, починаючи зі сполуки ПриСтадія А: (1b')-1-[3,5готування 2 і 3,5-дифторбензил броміду. Біс(трифторметил)феніл]етиламін. Елементний мікроаналіз: Очікуваний продукт являє собою другий з ена%С %Н %N %Сl нтіомерів, які одержують на Стадії А Прикладу Підраховано 58,47 6,08 6,49 16,44 101. Знайдено 58,49 6,07 6,47 17,04 Стадія В: (1RS)-N-[(1b')-1-(3,5Приклад 108: N-[(1S)-1-(3,5Біс(трифторметил)феніл)етил]-1-[4-(третДиметилфеніл)етил]-N-метил-2-(1-піперазин-іл)-2бутилоксикарбоніл)-1-піперазиніл]-1інданкарбоксамід дигідрохлорид. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки Приметодики, яка описана на Стадії А Прикладу 4, готування 2 і N-[(1S)-1-(3,5-диметилфеніл)етил]-Nпочинаючи зі сполуки Приготування 1 і сполуки, метиламіну. одержаної на Стадії А вище. Елементний мікроаналіз: Стадія С: (1a)-Ν-[(1b')-1-(3,5%С %Н %N %Сl Біс(трифторметил)феніл)етил]-1-[4-(третПідраховано 64,65 7,60 9,05 15,27 бутилоксикарбонїл)-1-піперазиніл]-1Знайдено 64,66 7,66 9,29 15,18 інданкарбоксамід дигідрохлорид. Приклад 109: N-(1R)4-(3,5Очікуваний продукт одержують розділенням, Диметилфеніл)етил]-N-метил-2-(1-піперазиніл)-2за допомогою хроматографії на силікагелі (елюінданкарбоксамід дигідрохлорид. ент: дихлорметан/етилацетат), діастереоізомерної Очікуваний продукт одержують відповідно до суміші, яку одержують на Стадії В. методики Прикладу 4, починаючи зі сполуки При 39 87989 40 готування 2 і N-[(1R)-1-(3,5-диметилфеніл)етил]-Nву проводять на кожному з двох діастереоізомерів. метиламіну. Очікуваний продукт являє собою перший з енантіЕлементний мікроаналіз: омерів, які таким чином одержують. %С %Н %N %Сl Стадія В: (1RS)-N-[(1a')-1-(3,5Підраховано 64,65 7,60 9,05 15,27 Дибромфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)Знайдено 64,66 7,66 9,29 15,18 1-піперазиніл]-1-інданкарбоксамід дигідрохлорид. Приклад 110: 1-[2-(3-Бром-5Очікуваний продукт одержують відповідно до фторбензилоксиметил)індан-2-іл]піперазин, дигідметодики, яка описана на Стадії А Прикладу 4, рохлорид. починаючи з Приготування 1 і сполуки, одержаної Очікуваний продукт одержують відповідно до на Стадії А вище. методики Прикладу 1, починаючи зі сполуки ПриСтадія С: (1a)-N-[(1a')-1-(3,5готування 2 і 3-бром-5-фторбензил броміду. Дибромфеніл)етил]-1-[4-(трет-бутилоксикарбонЕлементний мікроаналіз: іл)-1-піперазиніл]-1-інданкарбоксамід дигідрохло%С %Н %N %Сl рид. Підраховано 51,24 5,32 5,69 14,40 Очікуваний продукт одержують розділенням, Знайдено 51,37 5,33 5,67 14,72 за допомогою хроматографії на силікагелі (елюПриклад 111: N-[(1R)-1-(3,5ент: дихлорметан/етилацетат), діастереоізомерної Дихлорфеніл)етил]-2-(1-піперазиніл)-2суміші, яку одержують на Стадії В. інданкарбоксамід дигідрохлорид. Стадія D: (1a)-Ν-[(1a')-1-(3,5Очікуваний продукт одержують відповідно до Дибромфеніл)етил]-1-(1методики Прикладу 4, починаючи зі сполуки Припіперазиніл)інданкарбоксамід дигідрохлорид. готування 2 і (1R)-1-(3,5-дихлорфеніл)етиламін. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики, яка описана на Стадії В Прикладу 4, %С %Н %N %Сl починаючи зі сполуки, одержаної на Стадії С виПідраховано 53,79 5,54 8,55 28,87 ще. Знайдено 54,58 5,55 8,45 28,63 Елементний мікроаналіз: Приклад 112: 1-[2-(3-Фтор-5%С %Н %N %Сl (трифторметил)бензилоксиметил)індан-2-іл]Підраховано 45,54 4,69 7,24 12,22 піперазин дигідрохлорид. Знайдено 45,94 4,77 7,02 11,32 Очікуваний продукт одержують відповідно до Приклад 116: (1b)-N-[(1a')-1-(3,5методики Прикладу 1, починаючи зі сполуки ПриДибромфеніл)етил]-1-(1-піперазиніл)готування 2 і 3-фтор-5-(трифторметил)бензил інданкарбоксамід дигідрохлорид. броміду. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики, яка описана на Стадії В Прикладу 4, %С %Н %N %Сl починаючи з другого з діастереоізомерів, які розПідраховано 54,89 5,44 5,82 14,73 діляють на Стадії С Прикладу 115. Знайдено 55,40 5,53 5,69 14,90 Елементний мікроаналіз: Приклад 113: N-[(1S)-1-(3,5%С %Н %N %Сl Біс(трифторметил)феніл)етил]-2-(1-піперазиніл)-2Підраховано 45,54 4,69 7,24 12,22 інданкарбоксамід дигідрохлорид. Знайдено 45,58 4,80 6,98 11,64 Очікуваний продукт одержують відповідно до Приклад 117: (1a)-N-(1b')-1-(3,5методики Прикладу 4, починаючи зі сполуки ПриДибромфеніл)етил]-1-(1-піперазиніл)готування 2 і (1S)-1-[3,5-біс(трифторметил)-феніл] інданкарбоксамід дигідрохлорид. етил аміну. Стадія А: (1b')-1-[3,5-Дибромфеніл]етиламін. Елементний мікроаналіз: Очікуваний продукт являє собою другий з ена%С %Н %N %Сl нтіомерів, які одержують на Стадії А Прикладу Підраховано 51,62 4,87 7,53 12,70 115. Знайдено 51,10 4,77 7,22 12,30 Стадія В: (1RS)-N-[(1b')-1-(3,5Приклад 114: 1-[2-(3-Хлор-5Дибромфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)фторбензилоксиметил)індан-2-іл]піперазин дигід1-піперазиніл]-1-інданкарбоксамід дигідрохлорид. рохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики, яка описана на Стадії А Прикладу 4, методики Прикладу 1, починаючи зі сполуки Припочинаючи зі сполуки Приготування 1 і сполуки, готування 2 і 3-хлор-5-фторбензил броміду. одержаної на Стадії А вище. Елементний мікроаналіз: Стадія С: (1a)-N-[(1b')-1-(3,5%С %Н %N %Сl Дибромфеніл)етил]-1-[4-(трет-бутилоксикарбонПідраховано 56,33 5,85 6,26 23,75 іл)-1-піперазиніл]інданкарбоксамід дигідрохлорид. Знайдено 56,40 6,00 6,25 23,67 Очікуваний продукт одержують відокремленПриклад 115: (1a)-N-(1a')-1-(3,5ням, за допомогою хроматографії на силікагелі Дибромфеніл)етил]-1-(1-піперазиніл)(елюент: дихлорметан/етилацетат), діастереоізоінданкарбоксамід дигідрохлорид. мерної суміші, яку одержують на Стадії В. Стадія А: (1a')-1-[3,5-Дибромфеніл]етиламін. Стадія D: (1a)-Ν-[(1b')-1-(3,5(1RS)-1-[3,5-Дибромфеніл]етиламін перетвоДибромфеніл)етил]-1-(1рюють в сіль, використовуючи (L)-винну кислоту, піперазиніл)інданкарбоксамід дигідрохлорид. одержану таким чином суміш діастереоізомерів розділяють і потів повторне перетворення в осно 41 87989 42 Сполуку, одержану на Стадії вище, розділяють Очікуваний продукт одержують відповідно до ВЕРХ хроматографією, на хіральній фазі, рацемічметодики, яка описана на Стадії В Прикладу 4, ної сполуки, одержаної на Стадії вище. починаючи зі сполуки, одержаної на Стадії С виОчікуваний продукт являє собою перший з ще. енантіомерів, які таким чином розділяють. Елементний мікроаналіз: %С %Н %N %Сl Стадія С: N-[(1a)-1-(3,5-Дифторфеніл)]-2-(1Підраховано 45,54 4,69 7,24 12,22 піперазиніл)-2-інданкарбоксамід дигідрохлорид. Знайдено 45,70 4,76 7,06 11,08 Очікуваний продукт одержують перетворенням Приклад 118: (1b)-Ν-[(1b')-1-(3,5сполуки, одержаної на Стадії вище, в сіль, викориДибромфеніл)етил]-1-(1-піперазиніл)стовуючи хлористоводневу кислоту. інданкарбоксамід дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадії В Прикладу 4, Підраховано 57,65 5,94 9,17 15,47 починаючи з другого з діастереоізомерів, які розЗнайдено 57,87 5,86 9,08 15,47 діляють на Стадії С Прикладу 117. Приклад 122: N-[(1b)-1-(3,5Елементний мікроаналіз: Дифторфеніл)етил]-2-(1-піперазиніл)-2%С %Н %N %Сl інданкарбоксамід дигідрохлорид. Підраховано 45,54 4,69 7,24 12,22 Другий з енантіомерів, які розділяють на Стадії Знайдено 45,53 4,56 7,10 12,08 В Прикладу 121, перетворюють в сіль, використоПриклад 119: N-[(1a)-1-(3,5вуючи хлористоводневу кислоту, з тим, щоб одержати очікуванийпродукт. Дихлорфеніл)етил]-N-метил-2-(1-піперазиніл)-2Елементний мікроаналіз: інданкарбоксамід дигідрохлорид. Стадія A: N-[(1RS)-1-(3,5-Дихлорфеніл)етил]%С %Н %N %Сl N-метил-2-(1-піперазиніл)-2-інданкарбоксамід. Підраховано 57,65 5,94 9,17 15,47 Очікуваний продукт одержують відповідно до Знайдено 58,30 5,88 9,14 15,61 методики Прикладу 4, починаючи зі сполуки ПриПриклад 123: (1a)-N-{(1RS)-1-[3,5готування 2 і N-метил-1-(3,5Біс(трифторметил)феніл]етил}-N-метил-1-(1дихлорфеніл)етиламіну. піперазиніл)-1-інданкарбоксамід дигідрохлорид. Стадія В: Ν-[(1a)-1-(3,5-Дихлорфеніл)етил]-NОчікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки, одеметил-2-(1-піперазиніл)-2-інданкарбоксамід. ржаної на Стадії В Прикладу 86 і (RS)-N-метил-1Сполуку, одержану на стадії вище, розділяють [3,5-біс(трифторметил)феніл]етил аміну. ВЕРХ хроматографією, на хіральній фазі, рацемічЕлементний мікроаналіз: ної сполуки, одержаної на стадії вище. %С %Н %N %Сl Очікуваний продукт являє собою перший з Підраховано 52,46 5,11 7,34 12,39 енантіомерів, розділених таким чином. Знайдено 52,16 5,37 6,93 11,94 Стадія С: N-[(1a)-1-(3,5-Дихлорфеніл)етил]-NПриклад 124: (1b)-N-{(1RS)-1-[3,5метил-2-(1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. Біс(трифторметил)феніл]етил}-N-метил-1-(1Очікуваний продукт одержують перетворенням піперазиніл)-1-інданкарбоксамід дигідрохлорид. сполуки, одержаної на Стадії А вище, в сіль, викоОчікуваний продукт одержують відповідно до ристовуючи хлористоводневу кислоту. методики Прикладу 4, починаючи зі сполуки, одеЕлементний мікроаналіз: ржаної на Стадії А Прикладу 87 і (RS)-N-метил-1[3,5-біс(трифторметил)феніл]етиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 54,67 5,78 8,32 14,03 Знайдено 54,73 5,88 8,26 13,89 %С %Н %N %Сl Підраховано 52,46 5,11 7,34 12,39 Приклад 120: N-[(1b)-1-(3,5Знайдено 52,99 5,15 7,20 12,21 Дихлорфеніл)етил]-N-метил-2-(1-піперазиніл)-2Приклад 125: (1a)-N-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Другий з енантіомерів, які розділяють на Стадії Дифторфеніл)етил]-1-(1-піперазиніл)-1В Прикладу 119, перетворюють в сіль, використоінданкарбоксамід дигідрохлорид. вуючи хлористоводневу кислоту, з тим, щоб одерСтадія А: (1a)-N-[(1RS)-1-(3,5жати очікуваний продукт. Дифторфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)Елементний мікроаналіз: 1-піперазиніл]-1-інданкарбоксамід. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 54,67 5,78 8,32 14,03 методики, яка описана на Стадії А Прикладу 4, Знайдено 54,95 5,96 8,15 13,41 починаючи зі сполуки, одержаної на Стадії В ПриПриклад 121: Ν-[(1a)-1-(3,5кладу 86 і (RS)-1-(3,5-дифторфеніл)етиламіну. Дифторфеніл)етил]-2-(1-піперазиніл)-2Стадія В: (1a)-N-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Дифторфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)Стадія A: N-[(1RS)-1-(3,5-Дифторфеніл)етил]1-піперазиніл]-1-інданкарбоксамід. 2-(1-піперазиніл)-2-інданкарбоксамід. Очікуваний продукт одержують хроматографіОчікуваний продукт одержують відповідно до єю на силікагелі (елюент: дихлормеметодики Прикладу 4, починаючи зі сполуки Притан/етилацетат) діастереоізомерної суміші, яку готування 2 і 1-(3,5-дифторфеніл)етиламіну. одержують на Стадії А. Стадія В: Етил N-[(1a)-1-(3,5-Дифторфеніл)]-2(1-піперазиніл)-2-інданкарбоксамід. 43 87989 44 Підраховано 54,74 5,47 9,12 15,39 Стадія С: (1a)-N-[(1a')-1-(3,5Знайдено 55,24 5,61 9,06 15,29 Дифторфеніл)етил]-1-(1-піперазиніл)-1Приклад 130: N-[(1S)-1-(3,5інданкарбоксамід дигідрохлорид. Дихлорфеніл)етил]-2-(1-піперазиніл)-2Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид. методики, яка описана на Стадії В Прикладу 4, Очікуваний продукт одержують відповідно до починаючи зі сполуки, одержаної на Стадії В вище. методики Прикладу 4, починаючи зі сполуки ПриЕлементний мікроаналіз: готування 2 і (1S)-1-[3,5-дихлорфеніл]етиламіну. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 57,65 5,94 9,17 15,47 %С %Н %N %Сl Знайдено 57,22 6,30 8,85 15,62 Підраховано 53,79 5,54 8,55 28,87 Приклад 126: (1a)-Ν-[(1b')-1-(3,5Знайдено 54,53 5,59 8,52 28,80 Дифторфеніл)етил]-1-(1-піперазиніл)-1Приклад 131: (1a)-N-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Дихлорфеніл)етил]-1-(1-піперазиніл)Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид методики, яка описана на Стадії В Прикладу 4, Стадія А: (1a)-N-[(1RS)-1-(3,5починаючи з другого з діастереоізомерів, які розДихлорфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)діляють на Стадії В Прикладу 125. 1-піперазиніл]-1-інданкарбоксамід. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадії А Прикладу 4, Підраховано 57,65 5,94 9,17 15,47 починаючи зі сполуки, одержаної на Стадії В ПриЗнайдено 57,15 6,31 8,84 15,38 кладу 86 і (RS)-1-(3,5-дихлорфеніл)етиламіну. Приклад 127: (1b)-N-[(1a')-1-(3,5Стадія В: (1a)-N-[(1a')-1-(3,5Дифторфеніл)етил]-1-(1-піперазиніл)-1Дихлорфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)інданкарбоксамід дигідрохлорид. 1-піперазиніл]-1-інданкарбоксамід. Стадія А: (1b)-N-[(1RS)-1-(3,5Очікуваний продукт одержують хроматографіДифторфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)єю на силікагелі (елюент: дихлорме1-піперазиніл]-1-інданкарбоксамід. тан/етилацетат) діастереоізомерної суміші, яку Очікуваний продукт одержують відповідно до одержують на Стадії А. методики, яка описана на Стадії А Прикладу 4, Стадія С: (1a)-N-[(1a')-1-(3,5починаючи зі сполуки, одержаної на Стадії А ПриДихлорфеніл)етил]-1-(1-піперазиніл)-1кладу 87 і (RS)-1-(3,5-дифторфеніл)етиламіну. інданкарбоксамід дигідрохлорид. Стадія В: (1b)-N-[(1a')-1-(3,5Очікуваний продукт одержують відповідно до Дифторфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)методики, яка описана на Стадії В Прикладу 4, 1-піперазиніл]-1-інданкарбоксамід. починаючи зі сполуки, одержаної на Стадії В вище. Очікуваний продукт одержують хроматографіЕлементний мікроаналіз: єю на силікагелі (елюент: дихлорме%С %Н %N %Сl тан/етилацетат) діастереоізомерної суміші, яку Підраховано 53,79 5,54 8,55 28,87 одержують на Стадії А. Знайдено 54,21 5,69 8,04 28,87 Стадія С: (1b)-Ν-[(1a')-1-(3,5Приклад 132: (1a)-Ν-[(1b')-1-[3,5Дифторфеніл)етил]-1-(1-піперазиніл)-1Дихлорфеніл)етил]-1-(1-піперазиніл)-1інданкарбоксамід дигідрохлорид. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики, яка описана на Стадії В Прикладу 4, методики, яка описана на Стадії В Прикладу 4, починаючи зі сполуки, одержаної на Стадії В вище починаючи з другого з діастереоізомерів, які розЕлементний мікроаналіз: діляють на Стадії В Прикладу 131. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 57,65 5,94 9,17 15,47 %С %Н %N %Сl Знайдено 57,38 6,36 8,88 15,69 Підраховано 53,79 5,54 8,55 28,87 Приклад 128: (1b)-N-[(1b')-1-(3,5Знайдено 54,26 5,40 8,04 28,03 Дифторфеніл)етил]-1-(1-піперазиніл)-1Приклад 133: (1b)-Ν-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Дихлорфеніл)етил]-1-(1-піперазиніл)-1Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид. методики, яка описана на Стадії В Прикладу 4, Стадія A: (1b)-N-[(1RS)-1-(3,5починаючи з другого з діастереоізомерів, які розділяють на Стадії В Прикладу 127. Дихлорфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)Елементний мікроаналіз: 1-піперазиніл]-1-інданкарбоксамід. Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадії А Прикладу 4, Підраховано 57,65 5,94 9,17 15,47 починаючи зі сполуки, одержаної на Стадії А ПриЗнайдено 57,38 6,33 8,87 15,34 кладу 87 і (RS)-1-(3,5-дихлорфеніл)етиламіну. Приклад 129: N-(3-Хлор-5-фторбензил)-2-(1піперазиніл)-2-інданкарбоксамід дигідрохлорид. Стадія В: (1b)-Ν-[(1a')-1-(3,5Очікуваний продукт одержують відповідно до Дихлорфеніл)етил]-1-[4-(трет-бутилоксикарбоніл)методики Прикладу 4, починаючи зі сполуки При1-піперазиніл]-1-інданкарбоксамід. готування 2 і 3-хлор-5-фторбензиламіну. Очікуваний продукт одержують хроматографіЕлементний мікроаналіз: єю на силікагелі (елюент: дихлорме%С %Н %N %Сl 45 87989 46 тан/етилацетат) діастереоізомерної суміші, яку Елементний мікроаналіз: одержують на Стадії А. %С %Н %N %Сl Підраховано 58,48 6,19 8,89 15,01 Стадія С: (1b)-Ν-[(1a')-1-(3,5Знайдено 57,83 6,35 8,64 15,56 Дихлорфеніл)етил]-1-(1-піперазиніл)-1Приклад 138: (1a)-N-[(1a')-1-(3,5інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Дибромфеніл)етил]-N-метил-1-(1методики, яка описана на Стадії В Прикладу 4, піперазиніл)інданкарбоксамід дигідрохлорид починаючи зі сполуки, одержаної на Стадії В вище. Стадія А: (1a)-N-[(1RS)-1-(3,5Елементний мікроаналіз: Дибромфеніл)етил]-N-метил-1-[4-(трет%С %Н %N %Сl бутилоксикарбоніл)-1-піперазиніл]-1Підраховано 53,79 5,54 8,55 28,87 інданкарбоксамід. Знайдено 54,00 5,54 8,08 28,19 Очікуваний продукт одержують відповідно до Приклад 134: (1b)-N-[(1b')-1-(3,5методики, яка описана на Стадії А Прикладу 4, Дихлорфеніл)етил]-1-(1-піперазиніл)-1починаючи зі сполуки, одержаної на Стадії В Приінданкарбоксамід дигідрохлорид. кладу 86, і (RS)-N-метил-1-(3,5Очікуваний продукт одержують відповідно до дибромфеніл)етиламіну. методики, яка описана на Стадії В Прикладу 4, Стадія В: (1a)-N-[(1a')-1-(3,5починаючи з другого з діастереоізомерів, які розДибромфеніл)етил]-N-метил-1-[4-(третділяють на Стадії В Прикладу 133. бутилоксикарбоніл)-1-піперазиніл]-1Елементний мікроаналіз: інданкарбоксамід. %С %Н %N %Сl Очікуваний продукт одержують хроматографіПідраховано 53,79 5,54 8,55 28,87 єю на силікагелі (елюент: дихлормеЗнайдено 53,80 5,62 7,93 27,54 тан/етилацетат) діастереоізомерної суміші, яку Приклад 135: N-(3-Хлор-5-фторбензил)-Nодержують на Стадії А. метил-2-(1-піперазиніл)-2-інданкарбоксамід дигідСтадія С: (1a)-Ν-[(1a')-1-(3,5рохлорид. Дибромфеніл)етил]-N-метил-1-(1-піперазиніл)-1Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки ПриОчікуваний продукт одержують відповідно до готування 2 і N-метил-3-хлор-5-фторбензиламіну. методики, яка описана на Стадії В Прикладу 4, Елементний мікроаналіз: починаючи зі сполуки, одержаної на Стадії В вище. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 55,65 5,73 8,85 22,40 %С %Н %N %Сl Знайдено 55,54 5,95 8,81 22,55 Підраховано 46,49 4,92 7,07 11,93 Приклад 136: N-[(1a)-1-(3,5Знайдено 46,62 5,05 6,78 11,01 Дифторфеніл)етил]-N-метил-2-(1-піперазиніл)-2Приклад 139: (1a)-N-[(1b')-1-(3,5інданкарбоксамід дигідрохлорид. Дибромфеніл)етил]-N-метил-1-(1-піперазиніл)-1Стадія А: N-[(1RS)-1-(3,5-Дифторфеніл)етил]інданкарбоксамід дигідрохлорид. N-метил-2-(1-піперазиніл)-2-інданкарбоксамід. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики, яка описана на Стадії В Прикладу 4, методики Прикладу 4, починаючи зі сполуки Припочинаючи з другого з діастереоізомерів, які розготування 2 і N-метил-1-(3,5діляють на Стадії В Прикладу 138. дифторфеніл)етиламіну. Елементний мікроаналіз: Стадія В: N-[(1a)-1-(3,5-Дифторфеніл)етил]-N%С %Н %N %Сl метил-2-(1-піперазиніл)-2-інданкарбоксамід. Підраховано 46,49 4,92 7,07 11,93 Сполуку, одержану на Стадії вище, розділяють Знайдено 46,14 5,05 6,65 11,14 ВЕРХ хроматографією, на хіральній фазі, рацемічПриклад 140: N-{(1a)-1-[3,5ної сполуки, одержаної на Стадії вище. Очікуваний Біс(трифторметил)феніл]етил}-N-метил-2-(1продукт являє собою перший з енантіомерів, які піперазиніл)-2-інданкарбоксамід дигідрохлорид. таким чином розділяють. Стадія А: N-{(1RS)-1-[3,5Стадія С: N-[(1a)-1-(3,5-Дифторфеніл)]-NБіс(трифторметил)феніл]етил}-N-метил-2-(1метил-2-(1-піперазиніл)-2-інданкарбоксамід дигідпіперазиніл)-2-інданкарбоксамід. рохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують перетворенням методики Прикладу 4, починаючи зі сполуки Присполуки, одержаної на Стадії вище, в сіль, викориготування 2 і N-метил-1-[3,5стовуючи хлористоводневу кислоту. біс(трифторметил)феніл]-етиламіну. Елементний мікроаналіз: Стадія В: N-{(1a)-1-[3,5%С %Н %N %Сl Біс(трифторметил)феніл]етил}-N-метил-2-(1Підраховано 58,48 6,19 8,89 15,01 піперазиніл)-2-інданкарбоксамід. Знайдено 57,93 6,09 8,62 15,18 Сполуку, одержану на Стадії вище, розділяють Приклад 137: N-[(1b)-1-(3,5ВЕРХ хроматографією, на хіральній фазі, рацемічДифторфеніл)етил]-N-метил-2-(1-піперазиніл)-2ної сполуки, одержаної на Стадії вище. Очікуваний інданкарбоксамід дигідрохлорид. продукт являє собою перший з енантіомерів, які Другий з енантіомерів, які розділяють на Стадії таким чином розділяють. В Прикладу 136, перетворюють в сіль, використовуючи хлористоводневу кислоту, з тим, щоб одержати очікуваний продукт. 47 87989 48 ржаної на Стадії А Прикладу 87, і (1R)-N-метил-1Стадія С: N-{(1a)-1-[3,5фенетиламіну. Біс(трифторметил)феніл]етил}-N-метил-2-(1Елементний мікроаналіз: піперазиніл)-2-інданкарбоксамід дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують перетворенням Підраховано 63,30 7,16 9,63 16,25 сполуки, одержаної на Стадії вище, в сіль, викориЗнайдено 63,63 7,67 9,68 15,51 стовуючи хлористоводневу кислоту. Елементний мікроаналіз: Приклад 147: (1a)-N-[(1R)-1-Фенілетил]-Nметил-1-(1-піперазиніл)-1-інданкарбоксамід дигід%С %Н %N %Сl рохлорид. Підраховано 52,46 5,11 7,34 12,39 Очікуваний продукт одержують відповідно до Знайдено 53,00 5,39 7,20 12,03 методики Прикладу 4, починаючи зі сполуки, одеПриклад 141: N-{(1b)-1-[3,5ржаної на Стадії В Прикладу 86, і (1R)-N-метил-1Біс(трифторметил)феніл]етил}-N-метил-2-(1фенетиламіну. піперазиніл)-2-інданкарбоксамід гідрохлорид. Елементний мікроаналіз: Другий з енантіомерів, які розділяють на Стадії %С %Н %N %Сl В Прикладу 140, перетворюють в сіль, використоПідраховано 63,30 7,16 9,63 16,25 вуючи хлористоводневу кислоту, з тим, щоб одерЗнайдено 62,87 7,16 9,06 15,95 жати очікуваний продукт. Приклад 148: N-[(1a)-1-(3,5Елементний мікроаналіз: %С %Н %N %Сl Дибромфеніл)етил]-N-метил-2-(1-піперазиніл)-2Підраховано 56,03 5,27 7,84 6,61 інданкарбоксамід дигідрохлорид. Знайдено 56,54 5,44 7,66 6,49 Стадія А: N-[(1RS)-1-(3,5-Дибромфеніл)етил]Приклад 142: N-[(1R)-1-Фенілетил]-N-метил-2N-метил-2-(1-піперазиніл)-2-інданкарбоксамід. (1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки Приметодики Прикладу 4, починаючи зі сполуки Приготування 2 і N-метил-1-(3,5-дибромфеніл)етил готування 2 і (1R)-N-метил-1-фенетиламіну. аміну. Елементний мікроаналіз: Стадія В: Ν-[(1a)-1-(3,5-Дибромфеніл)етил]-N%С %Н %N %Сl Метил-2-(1-піперазиніл)-2-інданкарбоксамід Підраховано 63,30 7,16 9,63 16,25 Сполуку, одержану на Стадії вище, розділяють Знайдено 63,25 7,34 9,35 16,78 ВЕРХ хроматографією, на хіральній фазі, рацемічПриклад 143: N-[(1S)-1-Фенілетил]-N-метил-2ної сполуки, одержаної на Стадії вище. Очікуваний (1-піперазиніл)-2-інданкарбоксамід дигідрохлорид. продукт являє собою перший з енантіомерів, які Очікуваний продукт одержують відповідно до таким чином розділяють. методики Прикладу 4, починаючи зі сполуки ПриСтадія С: N-[(1a)-1-(3,5-Дибромфеніл)етил]-Nготування 2 і (1S)-N-метил-1-фенетиламіну. метил-2-(1-піперазиніл)-2-інданкарбоксамід дигідЕлементний мікроаналіз: рохлорид. %С %Н %N %Сl Очікуваний продукт одержують перетворенням Підраховано 63,60 7,16 9,63 16,25 сполуки, одержаної на Стадії вище, в сіль, викориЗнайдено 6,81 7,29 9,48 16,72 стовуючи хлористоводневу кислоту. Приклад 144: (1a)-Ν-[(1S)-1-Фенілетил]-NMac-спектрометрія: [М+Н]+=519,1 метил-(1-піперазиніл)-1-інданкарбоксамід дигідроПриклад 149: N-[(1b)-1-(3,5хлорид. Дибромфеніл)етил]-N-метил-2-(1-піперазиніл)-2Очікуваний продукт одержують відповідно до інданкарбоксамід дигідрохлорид. методики Прикладу 4, починаючи зі сполуки, одеДругий з енантіомерів, які розділяють на Стадії ржаної на Стадії В Прикладу 86 і (1S)-N-метил-1В Прикладу 148, перетворюють в сіль, використофенетиламіну. вуючи хлористоводневу кислоту, з тим, щоб одерЕлементний мікроаналіз: жати очікуваний продукт. %С %Н %N %Сl Елементний мікроаналіз: Підраховано 63,30 7,16 9,63 16,25 %С %Н %N %Сl Знайдено 62,68 7,29 9,25 16,04 Підраховано 46,49 4,92 7,07 11,93 Приклад 145: (1b)-N-[(1S)-1-Фенілетил]-NЗнайдено 46,99 4,85 6,90 11,28 метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідПриклад 150: (RS)-1-{2-[1-(3,5рохлорид. Диметилфеніл)етокси)метил]індан-2-іл}-піперазин Очікуваний продукт одержують відповідно до дигідрохлорид. методики Прикладу 4, починаючи зі сполуки, одеСтадія А: трет-Бутил (RS)-4-(2-{[(3,5ржаної на Стадії А Прикладу 87, і (1S)-N-метил-1диметилбензоїл)окси]метил}індан-2-іл)-1фенетиламіну. піперазинкарбоксилат Елементний мікроаналіз: До 4,8г сполуки, одержаної на Стадії А При%С %Н %N %Сl кладу 3, і 2,16г 3,5-диметил-бензойної кислоти, Підраховано 63,30 7,16 9,63 16,25 розчиненої в 10мл метиленхлориду, додають, при Знайдено 63,51 7,54 9,47 16,06 0°С, 2,76г 1-(3-диметиламінопропіл)-3етилкарбодіімід гідрохлориду і 150мг диметиламіПриклад 146: (1b)-N-[(1R)-1-Фенілетил]-Nметил-1-(1-піперазиніл)-1-інданкарбоксамід дигіднопіридину. Після перемішування протягом 20 годин при температурі навколишнього середовирохлорид. ща розчинник випаровують, залишок повторно Очікуваний продукт одержують відповідно до розчиняють в етилацетаті, і потім органічну фазу методики Прикладу 4, починаючи зі сполуки, оде 49 87989 50 промивають водою, висушують і випаровують. продукт являє собою перший з енантіомерів, які Залишок, який одержують, очищують хроматогратаким чином розділяють. фією на силікагелі (елюент: дихлормеСтадія С: 1-{2-[((1a)-1-(3,5тан/етилацетат 92,5/7,5) з тим, щоб одержати очіДихлорфеніл)етокси)метил]індан-2-іл}піперазин куваний продукт. дигідрохлорид. Точка плавлення: 139°С. Очікуваний продукт одержують реакцією споСтадія В: трет-Бутил 4-[2-({[1-(3,5луки, одержаної на Стадії вище з хлористоводнедиметилфеніл)вініл]окси}метил)індан-2-іл]-1вою кислотою. піперазинкарбоксилат Елементний мікроаналіз: До 4,55г продукту, який одержують на Стадії %С %Н %N %Сl вище, розчиненого в 40мл тетрагідрофурану, доПідраховано 55,25 5,90 5,86 29,65 дають 19,4мл розчин 1М диметилтитаноцену в Знайдено 55,17 6,29 5,65 28,95 толуолі. Суміш потім нагрівають зі зворотним хоПриклад 152: 1-{2-[((1b)-1-(3,5лодильником під азотом. Після перемішування Дихлорфеніл)етокси)метил]індан-2-іл}-піперазин протягом 6 годин при нагріванні зі зворотним ходигідрохлорид. лодильником, додають наступні 9,7мл розчину Другий з енантіомерів, які розділяють на Стадії титаноцену і нагрівання зі зворотним холодильниВ Прикладу 151, піддають реакції з хлористоводком продовжують протягом 18 годин. Після поверневою кислотою, з тим, щоб одержати очікуваний нення до температури навколишнього середовипродукт. ща, додають 300мл пентану і суміш фільтрують. Елементний мікроаналіз: Фільтрат випаровують і залишок потім хроматог%С %Н %N %Сl рафують на силікагелі (елюент: дихлормеПідраховано 55,25 5,90 5,86 29,65 тан/етилацетат 90/10) з тим, щоб одержати очікуЗнайдено 55,63 6,24 5,65 29,48 ваний продукт. Приклад 153: 1-{(1a)-1-[((1a')-1-(3,5Точка плавлення: 128°С. Дифторфеніл)етокси)метил]індан-1-іл}піперазин Стадія С: трет-Бутил (RS)-4-(2-{[1-(3,5дигідрохлорид. диметилфеніл)етокси]метил}індан-2-іл)-1Стадія А: (1a)-1-[4-(трет-Бутилоксикарбоніл)-1піперазинкарбоксилат піперазиніл]-1-гідроксиметиліндан. До 1,6г продукту, який одержують на Стадії Очікуваний продукт є першим з енантіомерів, вище, розчиненого в 40мл толуолу і 20мл безводякі одержують розділенням на хіральній ВЕРХ коного етанолу, додають, після дегазування, 165мг лонці сполуки, одержаної на Стадії В Прикладу 1. (5% молярний) трис(трифенілфосфін)родій хлориСтадія В: трет-Бутил 4-((1a)-1-{[(1RS)-1-(3,5ду. Суміш потім гідрогенізують протягом 20 годин дифторфеніл)етокси]-метил}індан-1-іл)-1при температурі навколишнього середовища і атпіперазинкарбоксилат мосферному тиску. Після випарування розчинників Очікуваний продукт одержують відповідно до і хроматографування на силікагелі (елюент: дихметодики, яка описана на Стадіях А-С Прикладу лорметан/етилацетат 80/20), одержують очікува150, починаючи зі сполуки, одержаної на Стадії ний продукт. вище, і 3,5-дифтор-бензойної кислоти. ІЧ:>=СО 1688см-1 Стадія С: трет-Бутил 4-((1a)-1-{[(1a')-1-(3,5Стадія D: (RS)-1-{2-[(1-(3,5дифторфеніл)етокси]метил}індан-1-іл)-1Диметилфеніл)етокси)метил]індан-2-іл}піперазин піперазинкарбоксилат дигідрохлорид Сполуку, одержану на Стадії вище, розділяють Очікуваний продукт одержують реакцією спохроматографією на силікагелі. Очікуваний продукт луки, одержаної на Стадії вище, з хлористоводнеявляє собою перший з діастереоізомерів, які таким вою кислотою. чином розділяють. Елементний мікроаналіз: Стадія D: 1-{(1a)-1-[((1a')-1-(3,5%С %Н %N %Сl Дифторфеніл)етокси)метил]індан-1-іл}-піперазин Підраховано 65,90 7,83 6,40 16,21 дигідрохлорид Знайдено 66,36 8,34 6,43 15,98 Очікуваний продукт одержують реакцією споПриклад 151: 1-{2-[((1a)-1-(3,5луки, одержаної на Стадії вище, з хлористоводнеДихлорфеніл)етокси)метил]індан-2-іл}-піперазин вою кислотою. дигідрохлорид. Елементний мікроаналіз: Стадія А: трет-Бутил (RS)-4-(2-{[1-(3,5%С %Н %N %Сl дихлорфеніл)етокси]метил}індан-2-іл)-1Підраховано 59,33 6,34 6,29 15,92 піперазинкарбоксилат Знайдено 60,09 6,38 5,88 16,00 Очікуваний продукт одержують відповідно до Приклад 154: 1-{(1a)-1-[((1b')-1-(3,5методики, яка описана на Стадіях А-С Прикладу Дифторфеніл)етокси)метил]індан-1-іл}піперазин 150, замінюючи 3,5-диметилбензойну кислоту на дигідрохлорид. Стадії А на 3,5-дихлорбензойну кислоту. Очікуваний продукт одержують реакцією друСтадія В: трет-Бутил 4-(2-{[(1a)-1-(3,5гого з діастереоізомерів, які розділяють на Стадії дихлорфеніл)етокси]метил}індан-2-іл)-1С Прикладу 153, з хлористоводневою кислотою. піперазинкарбоксилат Елементний мікроаналіз: Сполуку, одержану на Стадії вище, розділяють %С %Н %N %Сl ВЕРХ хроматографією, на хіральній фазі, рацемічПідраховано 59,33 6,34 6,29 15,92 ної сполуки, одержаної на Стадії вище. Очікуваний Знайдено 58,86 6,18 6,05 15,85 51 87989 52 Очікуваний продукт одержують реакцією споПриклад 155: 1-{(1b)-1-[((1a')-1-(3,5луки, одержаної на Стадії вище, з хлористоводнеДифторфеніл]етокси)метил]індан-1-іл}піперазин вою кислотою. дигідрохлорид. Елементний мікроаналіз: Стадія А: (1b)-1-[4-(трет-Бутилоксикарбоніл)-1%С %Н %N %Сl піперазиніл]-1-гідроксиметиліндан. Підраховано 46,59 4,98 4,94 12,50 Очікуваний продукт являє собою другий з енаЗнайдено 47,21 4,73 4,95 12,54 нтіомерів, які одержують розділянням на хіральній Приклад 158: 1-{2-[((1b)-1-(3,5ВЕРХ колонці сполуки, одержаної на Стадії В ПриДибромфеніл)етокси)метил]індан-2-іл}-піперазин кладу 1. дигідрохлорид. Стадія В: трет-Бутил 4-((1b)-1-{[(1RS)-1-(3,5Другий з енантіомерів, які розділяють на Стадії дифторфеніл)етокси]метил}-індан-1-іл)-1В Прикладу 157, піддають реакції з хлористоводпіперазинкарбоксилат невою кислотою з тим, щоб одержати очікуваний Очікуваний продукт одержують відповідно до продукт. методики, яка описана на Стадіях А-С Прикладу Елементний мікроаналіз: 150, починаючи зі сполуки, одержаної на Стадії %С %Н %N %Сl вище і 3,5-дифторбензойної кислоти. Підраховано 46,59 4,98 4,94 12,50 Стадія С: трет-Бутил 4-((1b)-1-{[(1a')-1-(3,5Знайдено 46,73 4,70 4,95 12,70 дифторфеніл)етокси]метил}індан-1-іл)-1Приклад 159: 1-{(1a)-1-[((1a')-1-[3,5піперазинкарбоксилат Біс(трифторметил)феніл]етокси)-метил]індан-1Сполуку, одержану на Стадії вище, розділяють іл}піперазин дигідрохлорид. хроматографією на силікагелі. Очікуваний продукт Стадія А: трет-Бутил 4-((1a)-1-{[(1RS)-1-[3,5являє собою перший з діастереоізомерів, які таким біс(трифторметил)феніл]-етокси]метил}індан-1-іл)чином розділяють. 1-піперазинкарбоксилат Стадія D: 1-{(1b)-1-[((1a')-1-(3,5Очікуваний продукт одержують відповідно до Дифторфеніл)етокси)метил]індан-1-іл}-піперазин методики, яка описана на Стадіях А-С Прикладу дигідрохлорид 150, починаючи зі сполуки, одержаної на Стадії А Очікуваний продукт одержують реакцією споПрикладу 153 і 3,5-біс(трифторметил)бензойної луки, одержаної на Стадії вище, з хлористоводнекислоти. вою кислотою. Стадія В: трет-Бутил 4-((1a)-1-{[(1a')-1-[3,5Елементний мікроаналіз: біс(трифторметил)феніл]етокси]-метил}індан-1-іл)%С %Н %N %Сl 1-піперазинкарбоксилат Підраховано 59,33 6,34 6,29 15,92 Сполуку, одержану на Стадії вище, розділяють Знайдено 58,91 6,38 6,12 16,07 хроматографією на силікагелі. Очікуваний продукт Приклад 156: 1-{((1b)-1-[(1b')-1-(3,5являє собою перший з діастереоізомерів, які таким Дифторфеніл)стокси)метил]індан-1-іл} піперазин чином розділяють. дигідрохлорид. Стадія С: 1-{(1a)-1-[((1a')-1-[3,5Очікуваний продукт одержують реакцією друбіс(трифторметил)феніл]етокси)метил]індан-1гого з діастереоізомерів, які розділяють на Стадії іл}піперазин дигідрохлорид С Прикладу 155, з хлористоводневою кислотою. Очікуваний продукт одержують реакцією споЕлементний мікроаналіз: луки, одержаної на Стадії вище, з хлористоводне%С %Н %N %Сl вою кислотою. Підраховано 59,33 6,34 6,29 15,92 Елементний мікроаналіз: Знайдено 59,58 6,41 5,93 15,94 %С %Н %N %Сl Приклад 157: 1-{2-[((1a)-1-(3,5Підраховано 52,85 5,17 5,14 13,00 Дибромфеніл)етокси)метил]індан-2-іл}-піперазин Знайдено 52,93 5,38 5,00 13,11 дигідрохлорид. Приклад 160: 1-{(1a)-1-[((1b')-1-[3,5Стадія А: трет-Бутил (RS)-4-(2-{[1-(3,5Біс(трифторметил)феніл]стокси)-метил]індан-1дибромфеніл)етокси]метил}індан-2-іл)-1іл}піперазин дигідрохлорид. піперазинкарбоксилат Очікуваний продукт одержують реакцією друОчікуваний продукт одержують відповідно до гого з діастереоізомерів, які розділяють на Стадії В методики, яка описана на Стадіях А-С Прикладу Прикладу 159, з хлористоводневою кислотою. 150, замінюючи 3,5-диметилбеюойну кислоту на Елементний мікроаналіз: Стадії А на 3,5-дибромбензойну кислоту. %С %Н %N %Сl Стадія В: трет-Бутил 4-(2-{[(1a)-1-(3,5Підраховано 52,85 5,17 5,14 13,00 дибромфеніл)етокси]метил}індан-2-іл)-1Знайдено 53,35 5,16 5,09 12,63 піперазинкарбоксилат Приклад 161: 1-{(1b)-1-[((1a')-1-[3,5Сполуку, одержану на Стадії вище, розділяють Біс(трифторметил)феніл]етокси)-метил]індан-1ВЕРХ хроматографією, на хіральній фазі, рацемічіл}піперазин дигідрохлорид. ної сполуки, одержаної на Стадії вище. Очікуваний Стадія А: трет-Бутил 4-((1b)-1-{[(1RS)-1-[3,5продукт являє собою перший з енантіомерів, які біс(трифторметил)феніл]етокси]-метил}індан-1-іл)таким чином розділяють. 1-піперазинкарбоксилат Стадія С: 1-{2-[((1a)-1-(3,5Очікуваний продукт одержують відповідно до Дибромфеніл)етокси)метил]індан-2-іл}піперазин методики, яка описана на Стадіях А-С Прикладу дигідрохлорид. 150, починаючи зі сполуки, одержаної на Стадії А 53 87989 54 Прикладу 155 і 3,5-біс(трифторметил)бензойної %С %Н %N %Сl кислоти. Підраховано 58,48 6,19 8,89 15,01 Знайдено 57,89 5,96 8,43 15,40 Стадія В: трет-Бутил 4-((1b)-1-{[(1a')-1-[3,5Приклад 165: (1b)-N-[(1a')-1-(3,5біс(трифторметил)феніл]етокси]-метил}індан-1-іл)1-піперазинкарбоксилат Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1Сполуку, одержану на Стадії вище, розділяють інданкарбоксамід дигідрохлорид. хроматографією на силікагелі. Очікуваний продукт Стадія А: (1b)-N-[(1RS)-1-(3,5являє собою перший з діастереоізомерів, які таким Дифторфеніл)етил]-N-метил-1-[4-(третчином розділяють. бутилоксикарбоніл)-1-піперазиніл]-1Стадія С: 1-{(1b)-1-[((1a')-1-[3,5інданкарбоксамід. Біс(трифторметил)феніл]етокси)метил]індан-1Очікуваний продукт одержують відповідно до іл}піперазин дигідрохлорид методики, яка описана на Стадії А Прикладу 4, Очікуваний продукт одержують реакцією спопочинаючи зі сполуки, одержаної на Стадії А Прилуки, одержаної на Стадії вище, з хлористоводнекладу 87 і (RS)-N-метил-1-(3,5вою кислотою. дифторфеніл)етиламіну. Елементний мікроаналіз: Стадія В: (1b)-N-[(1a')-1-(3,5%С %Н %N %Сl Дифторфеніл)етил]-N-метил-1-[4-(третПідраховано 52,85 5,17 5,14 13,00 бутилоксикарбоніл)-1-піперазиніл]-1Знайдено 52,96 5,19 4,91 12,76 інданкарбоксамід. Приклад 162: 1-{(1b)-1-[((1b')-1-[3,5Очікуваний продукт одержують хроматографією на силікагелі (елюент: дихлормеБіс(трифторметил)феніл]етокси)-метил]індан-1тан/етилацетат) діастереоізомерної суміші, яку іл}піперазин дигідрохлорид. одержують на Стадії А. Очікуваний продукт одержують реакцією другого з діастереоізомерів, які розділяють на Стадії В Стадія С: (1b)-N-[(1a')-1-(3,5Прикладу 161 з хлористоводневою кислотою. Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1Елементний мікроаналіз: інданкарбоксамід дигідрохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 52,85 5,17 5,14 13,00 методики, яка описана на Стадії В Прикладу 4, Знайдено 53,37 5,18 4,94 12,78 починаючи зі сполуки, одержаної на Стадії В вище. Приклад 163: (1a)-Ν-[(1a')-1-(3,5Елементний мікроаналіз: Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1%С %Н %N %Сl інданкарбоксамід дигідрохлорид. Підраховано 58,48 6,19 8,89 15,01 Знайдено 58,31 5,95 8,40 14,17 Стадія А: (1a)-Ν-[(1RS)-1-(3,5Приклад 166: (1b)-N-[(1b')-1-(3,5Дифторфеніл)етил]-N-метил-1-[4-(третбутилоксикарбоніл)-1-піперазиніл]-1Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1інданкарбоксамід. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики, яка описана на Стадії А Прикладу 4, методики, яка описана на Стадії В Прикладу 4, починаючи зі сполуки, одержаної на Стадії В Припочинаючи з другого з діастереоізомерів, які розкладу 86 і (RS)-N-метил-1-(3,5діляють на Стадії В Прикладу 165. дифторфешл)етиламіну. Mac-спектрометрія ESI/FIA/HR і MS/MS: [M+H]+=400. Стадія В: (1a)-Ν-[(1a')-1-(3,5Приклад 167: (1a)-N-[(1a')-1-(3,5Дифторфеніл)етил]-N-метил-1-[4-(третбутилоксикарбоніл)-1-піперазиніл]-1Дихлорфеніл)етил]-N-метил-1-(1-піперазиніл)-1інданкарбоксамід. інданкарбоксамід дигідрохлорид. Очікуваний продукт одержують хроматографіСтадія А: (1a)-N-[(1RS)-1-(3,5єю на силікагелі (елюент: дихлормеДихлорфеніл)етил]-N-метил-1-[4-(треттан/етилацетат) діастереоізомерної суміші, яку бутилоксикарбоніл)-1-піперазиніл]-1одержують на Стадії А. інданкарбоксамід. Стадія С: (1a)-N-[(1a')-1-(3,5Очікуваний продукт одержують відповідно до Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1методики, яка описана на Стадії А Прикладу 4, інданкарбоксамід дигідрохлорид. починаючи зі сполуки, одержаної на Стадії В ПриОчікуваний продукт одержують відповідно до кладу 86 і (RS)-N-метил-1-(3,5методики, яка описана на Стадії В Прикладу 4, дихлорфеніл)етиламіну. починаючи зі сполуки, одержаної на Стадії В вище. Стадія В: (1a)-Ν-[(1a')-1-(3,5Mac-спектрометрія ESI/FIA/HR і MS/MS: Дихлорфеніл)етил]-N-метил-1-[4-(трет[M+H]+=400. бутилоксикарбоніл)-1-піперазиніл]-1Приклад 164: (1a)-N-[(1b')-1-(3,5інданкарбоксамід. Дифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1Очікуваний продукт одержують хроматографіінданкарбоксамід дигідрохлорид. єю на силікагелі (елюент: дихлормеОчікуваний продукт одержують відповідно до тан/етилацетат) діастереоізомерної суміші, яку методики, яка описана на Стадії В Прикладу 4, одержують на Стадії А. починаючи з другого з діастереоізомерів, які розСтадія С: (1a)-N-[(1a')-1-(3,5діляють на Стадії В Прикладу 163. Дихлорфеніл)етил]-N-метил-1-(1-піперазиніл)-1Елементний мікроаналіз: інданкарбоксамід дигідрохлорид. 55 87989 56 Очікуваний продукт одержують відповідно до Приклад 172: 1-{2-[((1RS)-1-[3,5методики, яка описана на Стадії В Прикладу 4, Біс(трифторметил)феніл]етокси)метил]-індан-2починаючи зі сполуки, одержаної на Стадії В вище. іл}піперазин дигідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики Прикладу 150, замінюючи 3,5Підраховано 54,67 5,78 8,32 14,03 диметилбензойну кислоту на Стадії А на 3,5Знайдено 55,18 5,79 8,06 12,57 біс(трифторметил)бензойну кислоту. Елементний мікроаналіз: Приклад 168: (1a)-N-[(1b')-1-(3,5%С %Н %N %Сl Дихлорфеніл)етил]-N-метил-1-(1-піперазиніл)-1Підраховано 52,85 5,17 5,14 13,00 інданкарбоксамід дигідрохлорид. Знайдено 52,82 5,14 5,05 12,77 Очікуваний продукт одержують відповідно до Приклад 173: 1-{2-[((1a)-1методики, яка описана на Стадії В Прикладу 4, починаючи з другого з діастереоізомерів, які розФенілетоксимет)метил]індан-2-іл}піперазин дигідділяють на Стадії В Прикладу 167. рохлорид. Елементний мікроаналіз: Стадія А: трет-Бутил (RS)-4-(2-{[1%С %Н %N %Сl фенілетокси]метил}індан-2-іл)-1-піперазинПідраховано 54,67 5,78 8,32 14,03 карбоксилат Знайдено 53,93 5,78 7,90 14,03 Очікуваний продукт одержують відповідно до методики, яка описана на Стадіях А-С Прикладу Приклад 169: (1b)-N-[(1a')-1-(3,5150, замінюючи 3,5-диметилбензойну кислоту на Дихлорфеніл)етил]-N-метил-1-(1-піперазиніл)-1Стадії А на бензойну кислоту. інданкарбоксамід дигідрохлорид. Стадія В: трет-Бутил 4-(2-{[(1a)-1Стадія А: (1b)-N-[(1RS)-1-(3,5фенілетокси]метил}індан-2-іл)-1-піперазинДихлорфеніл)етил]-N-метил-1-[4-(треткарбоксилат бутилоксикарбоніл)-1-піперазиніл]-1Сполуку, одержану на Стадії вище, розділяють інданкарбоксамід. ВЕРХ хроматографією, на хіральній фазі, рацемічОчікуваний продукт одержують відповідно до ної сполуки, одержаної на Стадії вище. Очікуваний методики, яка описана на Стадії А Прикладу 4, продукт являє собою перший з енантіомерів, які починаючи зі сполуки, одержаної на Стадії А Притаким чином розділяють. кладу 87, і (RS)-N-метил-1-(3,5Стадія С: 1-{2-[((1a)-1дихлорфеніл)етиламіну. Фенілетокси)метил]індан-2-іл}піперазин дигідрохСтадія В: (1b)-N-[(1a')-1-(3,5лорид. Дихлорфеніл)етил]-N-метил-1-[4-(третОчікуваний продукт одержують реакцією спобутилоксикарбоніл)-1-піперазиніл]-1луки, одержаної на Стадії вище, з хлористоводнеінданкарбоксамід. вою кислотою. Очікуваний продукт одержують хроматографії Елементний мікроаналіз: на силікагелі (елюент: дихлорметан/етилацетат) %С %Н %N %Сl діастереоізомерної суміші, яку одержують на СтаПідраховано 64,54 7,39 6,84 17,32 дії А. Знайдено 60,57 6,80 5,99 17,32 Стадія С: (1b)-N-[(1a')-1-(З,5-Дихлорфеніл)]-NПриклад 174: 1-{2-[((1b)-1метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідФенілетокси)метил]індан-2-іл}піперазин дигідрохрохлорид. лорид. Очікуваний продукт одержують відповідно до Другий з енантіомерів, які розділяють на Стадії методики, яка описана на Стадії В Прикладу 4, В Прикладу 173, піддають реакції з хлористоводпочинаючи зі сполуки, одержаної на Стадії В вище. невою кислотою, з тим, щоб одержати очікуваний Mac-спектрометрія ESI/FIA/HR і MS/MS: продукт. [M+H]+=432. Елементний мікроаналіз: Приклад 170: (1b)-Ν-[(1b')-1-(3,5%С %Н %N %Сl Дихлорфеніл)етил]-Ν-метил-1-(1-піперазиніл)-1Підраховано 64,54 7,39 6,84 17,32 інданкарбоксамід дигідрохлорид. Знайдено 64,96 6,97 6,43 16,82 Очікуваний продукт одержують відповідно до Приклад 175: 1-[(1a)-1-(3,5методики, яка описана на Стадії В Прикладу 4, Дифторбензилоксиметил)індан-1-іл]піперазин дипочинаючи з другого з діастереоізомерів, які розгідрохлорид. діляють на Стадії В Прикладу 169. Стадія А: (1a)-1-[4-(трет-Бутилоксикарбоніл)-1Mac-спектрометрія ESI/FIA/HR і MS/MS: [M+H]+=432. піперазиніл]-1-гідроксиметиліндан. Приклад 171: 1-{2-[((1RS)-1-(3,5Очікуваний продукт одержують відповідно до Дифторфеніл)етокси)метил]індан-2-іл}-піперазин методики, яка описана на Стадії В Прикладу 1, дигідрохлорид. починаючи зі сполуки, одержаної на Стадії А ПриОчікуваний продукт одержують відповідно до кладу 86. методики Прикладу 150, замінюючи 3,5Стадія В: 1-[(1a)-1-(3,5диметилбензойну кислоту на Стадії А на 3,5Дифторбензилоксиметил)індан-1-іл]піперазин дидифторбензойну кислоту. гідрохлорид. Елементний мікроаналіз: Очікуваний продукт одержують відповідно до %С %Н %N %Сl методики, яка описана на Стадіях С і D Прикладу Підраховано 59,33 6,34 6,29 15,92 1, починаючи зі сполуки, одержаної на Стадії виЗнайдено 59,46 6,61 6,15 15,40 ще, і 3,5-дифторбензил броміду. 57 87989 58 Елементний мікроаналіз: Підраховано 53,79 5,54 8,55 28,87 %С %Н %N %Сl Знайдено 54,00 5,49 8,07 29,08 Підраховано 58,47 6,08 6,49 16,44 Приклад 181: (1a)-N-(3-Хлор-5-фторбензил)-NЗнайдено 58,67 6,17 6,27 16,52 метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідПриклад 176: 1-[(1b)-1-(3,5рохлорид. Дифторбензилоксиметил)індан-1-іл]піперазин диОчікуваний продукт одержують відповідно до гідрохлорид. методики Прикладу 4, починаючи зі сполуки, одеСтадія А: (1 β)-1 -[4-(трет-Бутилоксикарбоніл)ржаної на Стадії В Прикладу 86, і N-метил-3-хлор1 -піперазиніл]-1 -гідроксиметил-індан. 5-фторбензиламіну. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: %С %Н %N %Сl методики, яка описана на Стадії В Прикладу 1, Підраховано 55,65 5,73 8,85 22,40 починаючи з другого з енантіомерів, які розділяють Знайдено 55,21 6,19 8,46 22,33 на Стадії А Прикладу 86. Приклад 182: (1b)-N-(3-Хлор-5-фторбензил)-NСтадія В: 1-[(1b)-1-(3,5метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідДифторбензилоксиметил)індан-1-іл]піперазин дирохлорид. гідрохлорид. Очікуваний продукт одержують відповідно до Очікуваний продукт одержують відповідно до методики Прикладу 4, починаючи зі сполуки, одеметодики, яка описана на Стадіях С і D Прикладу ржаної на Стадії А Прикладу 87, і N-метил-3-хлор1, починаючи зі сполуки, одержаної на Стадії ви5-фторбензиламіну. ще, і 3,5-дифторбензил броміду. Елементний мікроаналіз: Елементний мікроаналіз: %С %Н %N %Сl %С %Н %N %Сl Підраховано 58,47 6,08 6,49 16,44 Підраховано 55,65 5,73 8,85 22,40 Знайдено 58,37 6,24 6,17 16,40 Знайдено 55,10 6,11 8,45 22,08 Приклад 177: (1a)-Ν-(3,5-Дифторбензил)-NПриклад 183: N-[(1a)-1-(3-Хлор-5метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідфторфеніл)етил]-N-метил-2-(1-піперазиніл)-2рохлорид. інданкарбоксамід гідрохлорид. Очікуваний продукт одержують відповідно до Стадія A: N-[(1RS)-1-(3-Хлор-5методики Прикладу 4, починаючи зі сполуки, одефторфеніл)етил]-N-метил-2-(1-піперазиніл)-2ржаної на Стадії В Прикладу 86, і N-метил-3,5інданкарбоксамід. дифторбензиламіну. Очікуваний продукт одержують відповідно до Елементний мікроаналіз: методики Прикладу 4, починаючи зі сполуки При%С %Н %N %Сl готування 2 і N-метил-1-(3-хлор-5Підраховано 57,65 5,94 9,17 15,47 фторфеніл)етиламіну. Знайдено 57,21 5,99 8,36 15,47 Стадія В: N-[(1a)-1-(3-Хлор-5-фторфеніл)етил]Приклад 178: (1b)-Ν-(3,5-Дифторбензил)-NN-метил-2-(1-піперазиніл)-2-інданкарбоксамід метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідСполуку, одержану на Стадії вище, розділяють рохлорид. ВЕРХ хроматографією, на хіральній фазі, рацемічОчікуваний продукт одержують відповідно до ної сполуки, одержаної на Стадії вище. Очікуваний методики Прикладу 4, починаючи зі сполуки, одепродукт являє собою перший з енантіомерів, які ржаної на Стадії А Прикладу 87 і N-метил-3,5таким чином розділяють. дифторбензиламіну. Стадія С: N-[(1a)-1-(3-Хлор-5Елементний мікроаналіз: фторфеніл)етил]-N-метил-2-(1-піперазиніл)-2%С %Н %N %Сl інданкарбоксамід гідрохлорид. Підраховано 57,65 5,94 9,17 15,47 Очікуваний продукт одержують перетворенням Знайдено 58,14 6,16 8,84 14,96 сполуки, одержаної на Стадії вище, в сіль, викориПриклад 179: (1a)-Ν-(3,5-Дихлорбензил)-Nстовуючи хлористоводневу кислоту. метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідЕлементний мікроаналіз: рохлорид %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 58,70 6,10 8,93 18,83 методики Прикладу 4, починаючи зі сполуки, одеЗнайдено 58,82 6,22 8,81 18,73 ржаної на Стадії В Прикладу 86 і N-метил-3,5Приклад 184: N-[(1b)-1-(3-Хлор-5дихлорбензиламіну. фторфеніл)етил]-N-метил-2-(1-піперазиніл)-2Елементний мікроаналіз: інданкарбоксамідгідрохлорид. %С %Н %N %Сl Другий з енантіомерів, які розділяють на Стадії Підраховано 53,79 5,54 8,55 28,87 В Прикладу 183, перетворюють в сіль, використоЗнайдено 53,17 6,03 8,18 29,05 вуючи хлористоводневу кислоту, з тим, щоб одерПриклад 180: (1b3)-Ν-(3,5-Дихлорбензил)-Nжати очікуваний продукт. метил-1-(1-піперазиніл)-1-інданкарбоксамід дигідЕлементний мікроаналіз: рохлорид. %С %Н %N %Сl Очікуваний продукт одержують відповідно до Підраховано 58,70 6,10 8,93 18,83 методики Прикладу 4, починаючи зі сполуки, одеЗнайдено 59,03 6,23 8,78 19,38 ржаної на Стадії А Прикладу 87, і N-метил-3,5Приклад 185: (1a)-N-[(1a')-1-(3-Хлор-5дихлорбензиламіну. фторфешл)етил]-N-метил-1-(1-піперазиніл)-1Елементний мікроаналіз: інданкарбоксамід дигідрохлорид. %С %Н %N %Сl 59 87989 60 %С %Н %N %Сl Стадія А: (1a)-N-[(1RS)-1-(3-Хлор-5Підраховано 56,51 5,98 8,60 21,76 фторфеніл)етил]-N-метил-1-[4-(третЗнайдено 57,05 5,98 8,39 21,05 бутилоксикарбоніл)-1-піперазиніл]-1Приклад 188: (1b)-N-[(1b')-1-(3-Хлор-5інданкарбоксамід. Очікуваний продукт одержують відповідно до фторфеніл)етил]-N-метил-1-(1-піперазиніл)-1методики, яка описана на Стадії А Прикладу 4, інданкарбоксамід дигідрохлорид. починаючи зі сполуки, одержаної на Стадії В ПриОчікуваний продукт одержують відповідно до кладу 86, і (RS)-N-метил-1-(3-хлор-5методики, яка описана на Стадії В Прикладу 4, фторфеніл)етиламіну. починаючи з другого з діастереоізомерів, які розділяють на Стадії В Прикладу 187. Стадія В: (1a)-N-[(1a')-1-(3-Хлор-5Елементний мікроаналіз: фторфеніл)етил]-N-метил-1-[4-(трет%С %Н %N %Сl бутилоксикарбоніл)-1-піперазиніл]-1Підраховано 56,51 5,98 8,60 21,76 інданкарбоксамід. Знайдено 57,15 6,02 8,38 21,14 Очікуваний продукт одержують хроматографіПриклад 189: N-[3-Хлор-5-фторбензил]-Nєю на силікагелі (елюент: дихлормеметил-5,6-дифтор-2-(1-піперазиніл)-2тан/етилацетат) діастереоізомерної суміші, яку інданкарбоксамід гідрохлорид. одержують на Стадії А. Стадія А: 4,5-Дифторфталева кислота. Стадія С: (1a)-Ν-[(1a')-1-(3-Хлор-535г (0,161моль) 4.5-дихлорфталевого ангідрифторфеніл)етил]-N-метил-1-(1-піперазиніл)-1ду, 32,7г фториду калію і 140мл сульфонату вміінданкарбоксамід дигідрохлорид. шують в автоклав. Реакційну суміш потім нагріваОчікуваний продукт одержують відповідно до ють при 180°С протягом 24 годин і потім, після методики, яка описана на Стадії В Прикладу 4, повернення до температури навколишнього серепочинаючи зі сполуки, одержаної на Стадії В вище. довища, виливають в 500мл 1N розчин гідроксиду Елементний мікроаналіз: натрію і промивають 3 рази ефіром. Водну фазу %С %Н %N %Сl окислюють до рН=1, використовуючи хлористовоПідраховано 56,51 5,98 8,60 21,76 дневу кислоту і потім екстрагують ефіром. Ефірну Знайдено 57,14 6,01 8,47 20,75 фазу промивають водою, висушують і випаровуПриклад 186: (1a)-N-[(1b')-1-(3-Хлор-5ють, з тим, щоб одержати очікуваний продукт. фторфеніл)етил]-N-метил-1-(1-піперазиніл)-1Стадія В: (4,5-Дифтор-2інданкарбоксамід дигідрохлорид. гідроксиметилфеніл)метанол. Очікуваний продукт одержують відповідно до До розчину 0,198моль боргідриду натрію в методики, яка описана на Стадії В Прикладу 4, 150мл тетрагідрофурану додають, протягом 20 починаючи з другого з діастереоізомерів, які розхвилин і підтримування температури при 20°С, діляють на Стадії В Прикладу 185. розчин 8,25ммоль сполуки, одержаної на Стадії Елементний мікроаналіз: вище, в 150мл тетрагідрофурану. Після перемішу%С %Н %N %Сl вання протягом 3 годин при температурі навколиПідраховано 56,51 5,98 8,60 21,76 шнього середовища, додають, протягом 30 хвилин Знайдено 57,38 5,83 8,51 20,89 і підтримування температури при 20°С, розчин Приклад 187: (1b)-N-[(1a')-1-(3-Хлор-58,25ммоль йоду в 150мл тетрагідрофурану. Після фторфеніл)етил]-N-метил-1-(1-піперазиніл)-1перемішування протягом ночі при температурі інданкарбоксамід дигідрохлорид. навколишнього середовища, реакційну суміш охоСтадіяА:(1b)-N-[(1RS)-1-(3-Хлор-5лоджують, використовуючи льодяну водну баню і фторфеніл)етил]-N-метил-1-[4-(третпотім краплями додають 45мл 3N хлористоводнебутилоксикарбоніл)-1-піперазиніл]-1вої кислоти. Після перемішування протягом настуінданкарбоксамід. пних 30 хвилин, додають етиловий ефір. НерозОчікуваний продукт одержують відповідно до чинні частинки, які утворюються, відфільтровують. методики, яка описана на Стадії А Прикладу 4, Ефір і тетрагідрофуран потім випаровують, додапочинаючи зі сполуки, одержаної на Стадії А Приють етиловий ефір і потім розчин, який одержують, кладу 87 і (RS)-N-метил-1-(3-хлор-5промивають розчином 1N тіосульфонату натрію, фторфеніл)етиламін. 3N розчином гідроксиду натрію і потім водою, щоб Стадія В: (1b)-N-[(1a')-1-(3-Хлор-5дати, після висушування і випаровування, очікувафторфеніл)етил]-N-метил-1-[4-(третний продукт. бутилоксикарбоніл)-1-піперазиніл]-1Стадія С: 1,2-Біс-бромметил-4,5інданкарбоксамід. дифторбензол. Очікуваний продуктодержують хроматографіДо 0,195моль сполуки, одержаної на Стадії єю на силікагелі (елюент: дихлормевище, в 1,25 літрах ефіру додають, краплями, протан/етилацетат) діастереоізомерної суміші, яку тягом 1 години 30 хвилин, розчин 0,916моль триодержують на Стадії А. броміду фосфору в 300мл ефіру. Реакційну суміш Стадія С: (1b)-N-[(1a')-1-(3-Хлор-5потім перемішують протягом ночі при температурі фторфеніл)етил]-N-метил-1-(1-піперазиніл)-1навколишнього середовища; згодом її виливають в інданкарбоксамід дигідрохлорид. 1 літр льодяної води і розділяють. Органічну фазу Очікуваний продукт одержують відповідно до потім промивають 1N розчином гідроксиду натрію і методики, яка описана на Стадії В Прикладу 4, потім водою і нарешті насиченим розчином хлорипочинаючи зі сполуки, одержаної на Стадії В вище. ду натрію перед висушуванням і концентруванням, Елементний мікроаналіз: з тим, щоб одержати очікуваний продукт.
ДивитисяДодаткова інформація
Назва патенту англійськоюIndanyl-piperazine derivatives, process for their preparation and pharmaceutical compositions containing them
Автори англійськоюDe Nanteuil Guillaume, Portevin Bernard, Gloanec Philippe, Millan Mark, Ortuno Jean-Claude, Mannoury La Cour Clotilde, Gobert Alain
Назва патенту російськоюСоединения инданилпиперазина, способ их получения и фармацевтические композиции, которые их содержат
Автори російськоюПортевин Бернар, Глоанек Филип, Миллан Марк, Ортуно Жан-Клод, Манури Ля Кур Клотильд, Гобер Ален
МПК / Мітки
МПК: C07D 237/00
Мітки: фармацевтичні, спосіб, інданілпіперазину, композиції, містять, сполуки, одержання
Код посилання
<a href="https://ua.patents.su/35-87989-spoluki-indanilpiperazinu-sposib-kh-oderzhannya-i-farmacevtichni-kompozici-yaki-kh-mistyat.html" target="_blank" rel="follow" title="База патентів України">Сполуки інданілпіперазину, спосіб їх одержання і фармацевтичні композиції, які їх містять</a>
Попередній патент: Водна суспензія, що містить частинки твердої речовини, і спосіб її виготовлення
Наступний патент: Система та спосіб для мультиплексування керуючої інформації на фізичному каналі даних
Випадковий патент: Спосіб виробництва оцтової кислоти