Піроли
Номер патенту: 105185
Опубліковано: 25.04.2014
Автори: Фуджіморі Ікуо, Арікава Ясуйоші, Нішіда Харуюкі
Формула / Реферат
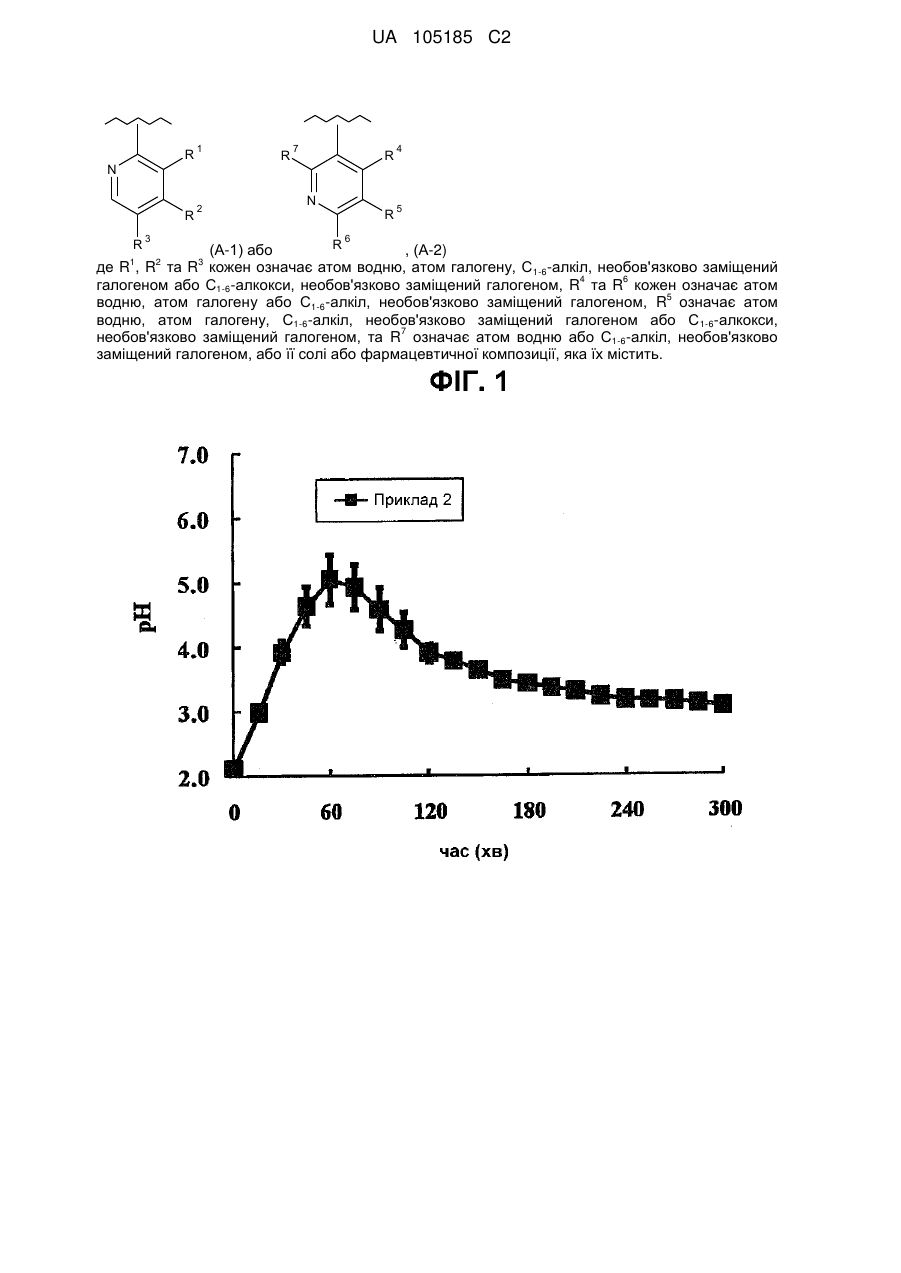
1. Сполука, представлена формулою (І)
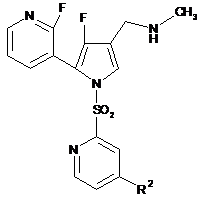 , (I)
, (I)
де R2 є атом галогену, С1-6-алкіл, необов'язково заміщений галогеном, або С1-6-алкокси, необов'язково заміщений галогеном, або її сіль.
2. Сполука за п. 1, де R2 є С1-6-алкіл або С1-6-алкокси, або її сіль.
3. 1-{4-Фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-2-іл)сульфоніл]-1Н-пірол-3-іл}-N-метилметанамін або його сіль.
4. 1-{4-Фтор-5-(2-фторпіридин-3-іл)-1-[(4-метоксипіридин-2-іл)сульфоніл]-1Н-пірол-3-іл}-N-метилметанамін або його сіль.
5. Фармацевтична композиція, що містить сполуку за п. 1 або її сіль.
6. Фармацевтична композиція за п. 5, яка є інгібітором секреції кислоти.
7. Фармацевтична композиція за п. 5, яка є калій-конкурентним блокатором кислоти.
8. Фармацевтична композиція за п. 5, яка є агентом для профілактики або лікування наступних хвороб: пептична виразка, синдром Золінгера-Елісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунка, лімфома MALT шлунка або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунка або виразка, викликана постопераційним стресом; або інгібітором кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразка, викликана гострим стресом, геморагічний гастрит або інвазивний стрес.
9. Спосіб лікування або профілактики наступних хвороб: пептична виразка, синдром Золінгера-Елісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунка, лімфома MALT шлунка або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунка або виразка, викликана постопераційним стресом; або спосіб інгібування кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразка, викликана гострим стресом, геморагічний гастрит або інвазивний стрес, в якому вводять ефективну кількість сполуки за п. 1 або її солі.
10. Застосування сполуки за п. 1 або її солі для одержання агента для профілактики або лікування наступних хвороб: пептична виразка, синдром Золінгера-Елісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунка, лімфома MALT шлунка або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунка або виразка, викликана постопераційним стресом; або інгібітору кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразка, викликана гострим стресом, геморагічний гастрит або інвазивний стрес.
Текст
Реферат: Даний винахід стосується сполуки, представленої формулою: N F CH3 F N H N SO2 A , (I) де А означає піридил, який має щонайменше один замісник UA 105185 C2 (12) UA 105185 C2 R 1 R N 2 R 7 R R N 6 3 4 5 R (А-1) або , (А-2) де R , R та R кожен означає атом водню, атом галогену, С1-6-алкіл, необов'язково заміщений 4 6 галогеном або С1-6-алкокси, необов'язково заміщений галогеном, R та R кожен означає атом 5 водню, атом галогену або С1-6-алкіл, необов'язково заміщений галогеном, R означає атом водню, атом галогену, С1-6-алкіл, необов'язково заміщений галогеном або С1-6-алкокси, 7 необов'язково заміщений галогеном, та R означає атом водню або С1-6-алкіл, необов'язково заміщений галогеном, або її солі або фармацевтичної композиції, яка їх містить. R 1 2 3 UA 105185 C2 5 10 15 20 25 Галузь винаходу Даний винахід стосується піролів, які пригнічують секрецію кислоти. Передумови винаходу Інгібітори протонної помпи, представлені омепразолом, які пригнічують секрецію шлункової кислоти, широко використовували у медицині для лікування пептичної виразки, рефлексного езофагіту, тощо. Однак, існуючі інгібітори протонної помпи асоціюються з проблемами ефективності та побічного впливу. Зокрема, з огляду на те, що існуючі інгібітори протонної помпи нестабільні в кислотних умовах, їх зазвичай формують у кишкові лікарські форми, у цьому випадку проходить декілька годин перед початком дії та приблизно 5 діб для проявлення максимального ефекту при послідовному введенні. Окрім цього, з огляду на те, що існуючі інгібітори протонної помпи мають різноманітні лікувальні властивості, внаслідок метаболічного поліморфізму ферментів та взаємодії між лікарськими засобами, такими як діазепам тощо, існує потреба у вдосконаленні. Як піроли з активністю інгібітору протонної помпи патентний документ 1 описує сполуку, представлену формулою: де X та Y є однаковими або різними та кожен означає зв’язок або спейсер, який має від 1 до 1 20 атомів у головному ланцюгу, r означає необов’язково заміщену вуглеводневу групу або 2 3 4 необов’язково заміщену гетероциклічну групу, r , r та r є однаковими або різними та кожен означає атом водню, необов’язково заміщену вуглеводневу групу, необов’язково заміщений тієніл, необов’язково заміщений бензо[b]тієніл, необов’язково заміщений фурил, необов’язково заміщений піридил, необов’язково заміщений піразоліл, необов’язково заміщений піримідиніл, 5 6 ацил, атом галогену, ціано або нітрогрупу, та r та r є однаковими або різними та кожен означає атом водню або необов’язково заміщену вуглеводневу групу. Окрім цього, як пірол з активністю інгібітору протонної помпи, патентний документ 2 описує сполуку, представлену формулою 7 30 35 де r означає моноциклічну азот-вмісну гетероциклічну групу, необов’язково конденсовану з бензольним кільцем або гетероциклом, моноциклічну азот-вмісну гетероциклічну групу, необов’язково конденсовану з бензольним кільцем або гетероциклом, яка необов’язково має 8 замісник(и), r означає необов’язково заміщений C 6-14-арил, необов’язково заміщений тієніл або 9 10 необов’язково заміщений піридил, r та r є однаковими або різними та кожен означає атом 9 10 водню або один з r та r означає атом водню та інший означає необов’язково заміщений 11 нижчий алкіл, ацил, атом галогену, ціано або нітрогрупу, та r означає алкіл, тощо. Більш того, як терапевтичний лікарський засіб для непластичних або аутоімунних хвороб, патентний документ 3 описує сполуку, представлену формулою: 1 UA 105185 C2 7 5 10 15 20 25 30 8 9 де r означає арил, аралкіл, гетероарил тощо, r означає арил, гетероарил, тощо, та r означає арил, гетерoарил, необов’язково заміщений аміном етил, тощо. ПЕРЕЛІК ЦИТУВАНЬ ПАТЕНТНА ЛІТЕРАТУРА ДЖЕРЕЛА ІНФОРМАЦІЇ: Патентний документ 1: WO 2006/036024 Патентний документ 2: WO 2007/026916 Патентний документ 3: WO 2004/103968 РЕЗЮМЕ ВИНАХОДУ ПРОБЛЕМИ, ЯКІ ВИРІШУЄ ВИНАХІД Лікарський засіб, який ефективно пригнічує секрецію шлункової кислоти, як відомі інгібітори протонної помпи, який має покращену стабільність в кислотних умовах, розсіюваність ефектів внаслідок метаболічного поліморфізму ферментів та взаємодії лікарських засобів, які є проблемами відомих інгібіторів протонної помпи, очікується більш значний лікувальний ефект на пептичну виразку, рефлюксний езофагіт тощо. Однак, як відомо на сьогодні, інгібітор протонної помпи, здатний задовольняти цим вимогам не було винайдено. Тому метою даного винаходу є одержання сполуки з покращеним ефектом пригнічення секреції кислоти (зокрема, з ефектом інгібування протонної помпи). Засоби вирішення проблем Винахідники здійснили різноманітні дослідження та виявили, що сполука, представлена формулою (I): де символи є визначеними нижче, або її сіль [у даному документі іноді посилаються як на сполуку (I)] неочікувано проявила значний інгібіторний вплив на протонну помпу, та є повністю придатною як лікарський засіб, що привело до створення даного винаходу. Відповідно, даний винахід стосується наступних об’єктів. [1] Сполуки, представленої формулою (I) де А означає піридил, який має щонайменше один замісник: 2 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 або 1 2 3 де R , R та R кожен означає атом водню, атом галогену, C1-6-алкіл, необов’язково 4 6 заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, R та R кожен 5 означає атом водню, атом галогену або C1-6-алкіл, необов’язково заміщений галогеном, R означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C1-67 алкокси, необов’язково заміщений галогеном, та R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном, або її сіль, 1 3 [2] сполуки за [1], де A представлено формулою (A-1), де R і R обидва означають атом 2 водню, R означає атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C 1-6алкокси, необов’язково заміщений галогеном, або її сіль, 2 [3] сполуки за [2], де R означає C1-6-алкіл або C1-6-алкокси, або її сіль, [4] 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанаміну або його солі, [5] 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанаміну або його солі, [6] 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метоксипіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанаміну або його солі, [7] 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанаміну або його солі, [8] 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(6-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанаміну або його солі, [9] пролікарської форма сполуки за [1] або її солі, [10] Фармацевтичної композиції, яка містить сполуку за [1] або її сіль або їх пролікарську форму, [11] Фармацевтичної композиції за [10], яка є інгібітором секреції кислоти, [12] Фармацевтичної композиції за [10], яка є калій-конкурентним блокатором кислоти, [13] Фармацевтичної композиції за [10], яка є агентом для профілактики або лікування наступних хвороб: пептична виразка, синдром Золінгера-Елісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунку, лімфома MALT шлунку, або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунку або виразка, викликана постопераційним стресом; або інгібітором кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразкою, викликаною гострим стресом, геморагічним гастритом або інвазивним стресом, [14] Способу лікування або профілактики наступних хвороб: пептична виразка, синдром Золінгера-Елісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунку, лімфома MALT шлунку, або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунку або виразка, викликана постопераційним стресом; або спосіб інгібування кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразкою, викликаною гострим стресом, геморагічним гастритом або інвазивним стресом, який включає введення ефективної кількості сполуки за [1] або її солі або пролікарської форми ссавцю, [15] Застосування сполуки за [1] або її солі або пролікарської форми для одержання агента для профілактики або лікування наступних хвороб: пептична виразка, синдром ЗолінгераЕлісона, гастрит, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунку, лімфома MALT шлунку, або виразка, викликана нестероїдним протизапальним лікарським засобом, гіперкислотність шлунку або виразка, викликана постопераційним стресом; або інгібітор кровотечі у верхньому відділі шлунково-кишкового тракту, викликаної пептичною виразкою, виразкою, викликаною гострим стресом, геморагічним гастритом або інвазивним стресом, та 3 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 [16] Сполуки за [1], де А означає піридин, який має щонайменше один замісник, формули (A1 3 1) або формули (A-2), де один з R та R означає атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, та інший означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C1-6-алкокси, 2 необов’язково заміщений галогеном, R означає атом водню, атом галогену, C1-6-алкіл, 4 необов’язково заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, R 6 та R кожен означає атом водню, атом галогену або C1-6-алкіл, необов’язково заміщений 5 галогеном, R означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений 7 галогеном або C1-6-алкокси, необов’язково заміщений галогеном, та R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном, або його сіль. Результат винаходу Сполука (І) даного винаходу показала покращений інгібувальний ефект на протонну помпу. Існуючі інгібітори протонної помпи, такі як омепразол, лансопразол тощо перетворюються на активні форми у кислотному середовищі шлункових паріетальних клітин та утворюють + + ковалентний зв'язок з залишком цистеїну H /K -ATФази, та необоротно інгібують активність + + ферменту. Навпаки, сполука (I) інгібує активність протонної помпи (H /K -АТФаза) у зворотній та + K конкурентній формі, та послідовно пригнічує секрецію кислоти. Тому, її інколи називають калій-конкурентний блокатор кислоти (P-CAB), або антагоніст кислотної помпи (APA). Сполука (I) швидко діє та проявляє максимальну ефективність від початку введення. Більш того, її метаболізм є менш залежним від метаболічного поліморфізму та розбіжність у ефективності у різних пацієнтів є незначною. Окрім цього, виявили, що сполука (I) має таку хімічну структуру, де (i) замісник у 5-положенні пірольного кільця є 2-F-3-піридилом, (ii) замісник у 4-положенні пірольного кільця є атомом фтору, та (iii) у 1-положенні пірольного кільця є 2піридилсульфонілом або 3-піридилсульфонілом, який має щонайменше один замісник, та така хімічна структура сприяє значній інгібіторній активності щодо протонної помпи, та значно зменшує цитотоксичність. Більш того, заміщення у 4-положенні пірольного кільця атомом фтору у сполуці (I) знижує основність (значення pKа) залишку метиамінометилу внаслідок відриву електрону від атому фтору, та зменшує ризик токсичності внаслідок високої основності, та, що введення щонайменше одного замісника у 2-піридил або 3-піридил у A сполуки (I) оптимально контролює тривалість дії. Тому, даний винахід забезпечує клінічно придатним агентом для профілактики або лікування наступних хвороб: пептична виразка (наприклад, виразка шлунку, виразка дванадцятипалої кишки, анастомозна виразка, виразка, викликана нестероїдним протизапальним лікарським засобом, виразка, викликана постопераційним стресом тощо), синдром Золінгера-Елісона, гастрит, ерозійний езофагіт, рефлюксний езофагіт, симптоматична гастроезофагальна рефлюксна хвороба (Симптоматична ГЕРХ), стравохід Барета, функціональна диспепсія, рак шлунку, лімфома MALT шлунку або гіперкислотність; або пригнічувачом кровотечі верхнього відділу шлунково-кишкового тракту, викликаної пептичною виразкою, виразкою, викликаною гострим стресом, геморагічним гастритом або інвазивним стресом; тощо. З огляду на те, що сполука (I) проявляє низьку токсичність та добре розчиняється у воді, in vivo кінетику та ефективність, вона є придатною як фармацевтична композиція. З огляду на те, що сполука (I) є стабільною навіть при кислотних умовах, її можна вводити орально як звичайну таблетку тощо без необхідності покривання кишковим покриттям. Завдяки цьому композиція (таблетка тощо) є меншою, та легко ковтається пацієнтами з проблемами ковтання, зокрема людьми похилого віку та дітьми. Окрім цього, з огляду на те, що не має ефекту уповільненого вивільнення притаманного кишковим лікарським формам, пригнічення виділення кислоти здійснюється миттєво, та симптоми, такі як біль тощо швидко пригнічуються. Короткий опис фігур Фіг. 1 показує результати тесту вимірювання pH перфузату шлунку у анестезованих пацюків Прикладу 2. Фіг. 2 показує результати тесту вимірювання pH перфузату шлунку у анестезованих пацюків Прикладу 5. Фіг. 3 показує результати тесту вимірювання pH перфузату шлунку у анастезованих пацюків Прикладу 24. (Детальний опис винаходу) У даному описі, приклади “атому галогену” та “галогену” включають атом фтору, атом хлору, атом брому та атом йоду. У формулі (I), А означає піридил, який має щонайменше один замісник. Приклади “піридину, який має щонайменше один замісник” для A включають групу, представлену формулою 4 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 або 1 2 3 де R , R та R кожен означає атом водню, атом галогену, C1-6-алкіл, необов’язково 4 6 заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, R та R кожен 5 означає атом водню, атом галогену або C1-6-алкіл, необов’язково заміщений галогеном, R означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C1-67 алкокси, необов’язково заміщений галогеном, та R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном. Термін “який має щонайменше один замісник” означає 1 2 3 щонайменше один з R , R та R у частковій структурі (A-1) не є атомом водню, та щонайменше 4 5 6 7 один з R , R , R та R у частковій структурі (A-2) не є атомом водню. 1 2 3 4 5 6 7 “C1-6-алкіл, необов’язково заміщений галогеном” для R , R , R , R , R , R або R означає C16-алкіл, який необов’язково містить 1 - 5 (бажано 1 - 3) атоми галогену (наприклад, атом фтору, атом хлору, атом брому, атом йоду), та їх приклади включають метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, втор-пентил, ізопентил, неопентил, нгексил, ізогексил, трифторметил тощо. 1 2 3 5 “C1-6-алкокси, необов’язково заміщений галогеном” для R , R , R або R означає C1-6алкокси, який необов’язково містить 1 - 5 (бажано 1 - 3) атоми галогену (наприклад, атом фтору, атом хлору, атом брому, атом йоду), та їх приклади включають метокси, етокси, пропокси, ізопропокси, бутокси, ізобутокси, втор-бутокси, пентилокси, гексилокси, фторметокси, трифторметокси тощо. 1 R бажано означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном 2 (наприклад, метил, етил). R бажано означає атом водню, C1-6-алкіл, необов’язково заміщений галогеном (наприклад, метил, етил), C1-6-алкокси, необов’язково заміщений галогеном 3 (наприклад, метокси, етокси). R бажано означає атом водню, атом галогену (наприклад, атом фтору, атом хлору, атом брому, атом йоду), C1-6-алкокси, необов’язково заміщений галогеном 4 (наприклад, метокси, етокси). R бажано означає атом водню, C 1-6-алкіл, необов’язково 5 заміщений галогеном (наприклад, метил, етил). R бажано означає атом водню, атом галогену (наприклад, атом фтору, атом хлору, атом брому, атом йоду), C1-6-алкіл, необов’язково заміщений галогеном (наприклад, метил, етил), C1-6-алкокси, необов’язково заміщений 6 галогеном (наприклад, метокси, етокси). R бажано означає атом водню, C1-6-алкіл, 7 необов’язково заміщений галогеном (наприклад, метил, етил). R бажано означає атом водню, C1-6-алкіл, необов’язково заміщений галогеном (наприклад, метил, етил). 1 2 R зокрема бажано означає атом водню або C1-6-алкіл. R зокрема бажано означає атом 3 водню, C1-6-алкіл або C1-6-алкокси. R зокрема бажано означає атом водню, атом галогену або 4 5 C1-6-алкокси. R зокрема бажано означає атом водню або C1-6-алкіл. R зокрема бажано означає 6 атом водню, атом галогену або C1-6-алкіл. R зокрема бажано означає атом водню або C1-67 алкіл. R зокрема бажано означає атом водню або C1-6-алкіл. У формулі (I), A класифікують у наступних варіантах здійснення. 1 3 2 (i) A представлено формулою (A-1) де обидва R та R є атомами водню, R означає атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C 1-6-алкокси, необов’язково заміщений галогеном. (ii) А означає піридил, який має щонайменше один замісник, представлений формулою (A-1) 1 3 або представлений формулою (A-2), де один з R та R означає атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, та інший означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або 2 C1-6-алкокси, необов’язково заміщений галогеном, R означає атом водню, атом галогену, C1-6алкіл, необов’язково заміщений галогеном або C1-6-алкокси, необов’язково заміщений 4 6 галогеном, R та R кожен означає атом водню, атом галогену або C1-6-алкіл, необов’язково 5 заміщений галогеном, R означає атом водню, атом галогену, C1-6-алкіл, необов’язково 7 заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, та R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном. Інший бажаний варіант здійснення A у формулі (I) представлено формулою 5 UA 105185 C2 1 5 2 3 де R , R та R є такими як визначено вище, та показує бажані варіанти втілення відповідних замісників у формулі (I). Піридил часткової структури (A-3) містить, окрім метилу, щонайменше 1 2 3 1 2 3 один замісник R , R або R . У частковій структурі (A-3), щонайменше один з R , R та R не є атомом водню. Бажаний “піридил, який має щонайменше один замісник” для A представлено формулою або 10 15 1 2 3 4 5 6 7 де R , R , R , R , R , R та R є такими як визначено вище, та показує бажані варіанти втілення відповідних замісників у формулі (I). У частковій структурі (A-2a), щонайменше один з 4 5 6 7 R та R не є атомом водню, та у частковій структурі (A-2b), щонайменше один з R та R не є атомом водню. Зокрема бажаним варіантом втілення сполуки (I) є сполука, представлена наступною формулою (Ia) або (Ib) або її сіль. формула (Ia) формула (Ib) 20 У даному документі, бажані варіанти втілення кожного замісника у формулі (Ia) та (Ib) відповідають відповідним замісникам у формулі (I). 6 UA 105185 C2 Зокрема, інші бажані варіанти втілення сполуки (I) є сполуками, представленими наступними формулами: формула (Ia-1), формула (Ia-2), формула (Ib) та формула (Ic) їх солями. F N F N H CH3 N SO2 R1 N R3 формула (Ia-1) F N F N H CH3 N SO2 N R2 5 формула (Ia-2) F N F N H CH3 N SO2 R4 N R5 7 формула (Ib) UA 105185 C2 F N F N H CH3 N SO2 R7 N R6 5 10 15 20 25 30 35 40 45 формула (Ic) У даному документі, бажані варіанти втілення кожного замісника у формулі (Ia-1), формулі (Ia-2), формулі (Ib) та формулі (Ic) відповідають відповідним замісникам у формулі (I). Однак, 1 3 2 щонайменше один з R та R у формулі (Ia-1) не є атомом водню, R у формулі (Ia-2) не є 4 5 атомом водню, щонайменше один з R та R у формулі (Ib) не є атомом водню, та щонайменше 6 7 один з R та R у формулі (Ic) не є атомом водню. 1 3 Зокрема, R та R у формулі (Ia-1) є однаковими або різними, та кожен означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або C 1-6-алкокси, необов’язково 1 заміщений галогеном. Бажаний R формули (Ia-1) означає атом водню або C1-6-алкіл, 3 необов’язково заміщений галогеном, зокрема бажано атом водню або C 1-6-алкіл. Бажаний R формули (Ia-1) означає атом водню, атом галогену або C1-6-алкокси, необов’язково заміщений галогеном, зокрема бажано атом водню, атом галогену або C1-6-алкокси. 2 R формули (Ia-2) означає атом галогену, C1-6-алкіл, необов’язково заміщений галогеном або 2 C1-6-алкокси, необов’язково заміщений галогеном. Бажаний R формули (Ia-2) означає C1-6алкіл, необов’язково заміщений галогеном або C1-6-алкокси, необов’язково заміщений галогеном, зокрема бажано C1-6-алкіл або C1-6-алкокси. 4 R формули (Ib) означає атом водню, атом галогену або C 1-6-алкіл, необов’язково заміщений 4 галогеном. R бажано означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном, зокрема бажано атом водню або C1-6-алкіл. 5 R формули (Ib) означає атом водню, атом галогену, C1-6-алкіл, необов’язково заміщений 5 галогеном або C1-6-алкокси, необов’язково заміщений галогеном. Бажаний R означає атом водню, атом галогену або C1-6-алкіл, необов’язково заміщений галогеном, зокрема бажано атом водню, атом галогену або C1-6-алкіл. 6 R формули (Ic) означає атом водню, атом галогену або C 1-6-алкіл, необов’язково заміщений 6 галогеном. Бажаний R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном, зокрема бажано атом водню або C1-6-алкіл. 7 R формули (Ic) означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном. 7 Бажаний R означає атом водню або C1-6-алкіл, необов’язково заміщений галогеном, зокрема бажано атом водню або C1-6-алкіл. Серед вищенаведених, формула (Ia-2) зокрема є бажаною. Серед сполук (I), наступні сполуки є бажаними. 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(3-метилпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метоксипіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 8 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(6-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(2-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-метоксипіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{1-[(5-хлорпіридин-3-іл)сульфоніл]-4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-1-[(5-фтор-6-метилпіридин-2-іл)сульфоніл]-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}N-метилметанамін або його сіль, 1-{4-фтор-1-[(5-фтор-4-метилпіридин-2-іл)сульфоніл]-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}N-метилметанамін або його сіль, 1-{4-фтор-1-[(5-фтор-4-метоксипіридин-2-іл)сульфоніл]-5-(2-фторпіридин-3-іл)-1H-пірол-3іл}-N-метилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-метоксипіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-1-[(5-фтор-6-метилпіридин-3-іл)сульфоніл]-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}N-метилметанамін або його сіль, 1-{1-[(4,6-диметилпіридин-2-іл)сульфоніл]-4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{1-[(5-хлорпіридин-2-іл)сульфоніл]-4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{1-[(5,6-диметилпіридин-2-іл)сульфоніл]-4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{1-[(4,5-диметилпіридин-2-іл)сульфоніл]-4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл}-Nметилметанамін або його сіль, і 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль. Як сполука (I), зокрема наступні сполуки є бажаними. 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метоксипіридин-2-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль, та 1-{4-фтор-5-(2-фторпіридин-3-іл)-1-[(6-метилпіридин-3-іл)сульфоніл]-1H-пірол-3-іл}-Nметилметанамін або його сіль. Приклади солі сполуки (I) включають солі металів, солі амонію, солі органічних основ, солі неорганічних основ, солі органічних кислот, солі основних або кислотних амінокислот тощо. Бажані приклади солей металів включають солі лужних металів, такі як солі натрію, калію тощо; солі лужноземельних металів, такі як солі кальцію, магнію, барію тощо; алюмінію тощо. Бажані приклади солі з органічною основою включають солі триметиламіну, триетиламіну, піридину, піколіну, 2,6-лутидину, етаноламіну, диетаноламіну, триетаноламіну, циклогексиламіну, дициклогексиламіну, N,N’-дибензилетилендіаміну тощо. Бажані приклади солі неорганічної кислоти включають солі хлорводневої кислоти, бромводневої кислоти, азотної кислоти, сірчаної кислоти, фосфорної кислоти тощо. Бажані приклади солі органічної кислоти включають солі мурашиної кислоти, оцтової кислоти, трифтороцтової кислоти, фталової кислоти, фумарової кислоти, щавлевої кислоти, винної кислоти, малеїнової кислоти, лимонної кислоти, бурштинової кислоти, яблучної кислоти, метансульфонової кислоти, бензенсульфонової кислоти, птолуолсульфонової кислоти тощо. Бажані приклади солі основної амінокислоти включають солі аргініну, лізину, орнітину тощо. Бажані приклади солі кислотної амінокислоти включають солі аспарагінової кислоти, глутамінової кислоти тощо. Серед них, фармацевтично прийнятні солі є бажаними. Наприклад, коли сполука містить кислотну функціональну групу, солі включають солі, такі як солі лужних металів (наприклад, натрію, калію тощо), солі лужноземельних металів (наприклад, кальцію, магнію, барію тощо), солі амонію, тощо; та коли сполука містить основну функціональну групу, солі включають, наприклад, солі неорганічної кислоти, такі як солі хлорводневої кислоти, бромводневої кислоти, азотної кислоти, сірчаної кислоти, фосфорної кислоти тощо, або солі органічної кислоти, такі як оцтової кислоти, фталової кислоти, 9 UA 105185 C2 5 фумарової кислоти, щавлевої кислоти, винної кислоти, малеїнової кислоти, лимонної кислоти, бурштинової кислоти, метансульфонової кислоти, п-толуолсульфонової кислоти тощо. У даному винаході пояснюються способи одержання сполуки (I). Сполуки (II)-(XXXIII) у формулі можуть утворювати солі, та серед цих солей є, наприклад, солі подібні до солей сполуки (I). Хоча сполуки, одержані на відповідних стадіях, використовують у наступній реакції у формі реакційної суміші або неочищеного продукту, їх також легко ізолюють та очищають з реакційної суміші за відомими способами розділення та очистки, такими як перекристалізація, дистилювання, хроматографія тощо. 10 8 15 20 25 30 35 40 Сполуку (II), де R означає C1-4 алкіл, такий як метил, етил, пропіл, ізопропіл, бутил, тощо, одержують за відомим способом, таким як спосіб, описаний у Chem. Pharm. Bull., vol. 49, p. 1406 (2001), Tetrahedron Letters, vol. 35, p. 5989 (1994) тощо або аналогічний спосіб. Сполуку (III), де кожен символ є таким як визначено вище, одержують шляхом фторування сполуки (II) фтору вальним агентом, таким як сіль N-фторпіридину, дифторид ксенону тощо. Кількість використаного фторувального агента дорівнює 0,75 - 10 еквівалентів, бажано 1 – 5 еквівалентів, по відношенню до сполуки (II). Цю реакцію переважно здійснюють, використовуючи розчинник інертний до реакції. Хоча вибір розчинника не є обмеженим доки триває реакція, вуглеводи такі як бензол, толуол, тощо, тетрагідрофуран, діетиловий етер, ацетонітрил тощо або їх суміші є бажаними. Хоча час реакції різниться в залежності від використаних реагентів та розчинника, зазвичай він становить 10 хв. - 24 год., бажано 30 хв. - 12 год. Температура реакції зазвичай становить -78 °C - 100 °C, бажано -20 °C - 60 °C. Окрім цього, є можливість введення фтору шляхом послідовної реакції, наприклад, бромуванням з Nбромсукцинімідом (NBS) тощо, після чого заміщення фтором за допомогою реакції заміщення. Сполуку (IV) одержують шляхом відновлення сполуки (III) відновлювальним агентом, таким як літій алюміній гідрид, діізобутилалюмінію гідрид, боргідрид натрію, боргідрид кальцію тощо. Бажаним відновлювальним агентом є діізобутилалюмінію гідрид. Кількість використаного відновлювального агента становить 0,75 - 10 еквівалентів, бажано 1 - 5 еквівалентів, по відношенню до сполуки (III). Цю реакцію переважно здійснюють, використовуючи інертний розчинник. Хоча вибір розчинника не є обмеженим доки триває реакція, вуглеводи такі як бензол, толуол, тощо, тетрагідрофуран, діетиловий етер, ацетонітрил тощо або їх суміші є бажаними. Хоча час реакції різниться в залежності від використаних реагентів та розчинника, зазвичай він становить 10 хв. 24 год., бажано 30 хв. - 8 год. Температура реакції зазвичай становить від -78 °C до 100 °C, бажано від -78 °C до 25 °C. Сполуку (V) одержують шляхом реагування сполуки (IV) з окислювачем, таким як комплекс хромова кислота-піридин, хлорхромат піридину, діоксид марганцю, комплекс триоксид сіркипіридин, тетра-н-пропіламонію перрутенат тощо. Бажаним окислювачем є діоксид марганцю, комплекс триоксид сірки-піридин або тетра-н-пропіламонію перрутенат. Цю реакцію окислення здійснюють, наприклад, згідно з способом, описаним у Synthesis, p. 639 (1994). Сполуку (VII) одержують шляхом реагування сполуки (V) з сполукою, представленою формулою (VI) 10 UA 105185 C2 5 10 15 20 25 30 35 де X означає атом галогену, такий як атом фтору, атом хлору тощо, та інший символ є таким як визначено вище. Кількість використаної сполуки (VI) становить 0,75 - 10 моль, бажано 1 - 3 моль, на 1 моль сполуки (V). Цю реакцію переважно здійснюють, використовуючи інертний розчинник. Хоча вибір розчинника не є обмеженим доки триває реакція, вуглеводи такі як бензол, толуол тощо, етери, такі як тетрагідрофуран тощо, аміди, такі як N,N-диметилформамід, N,N-диметилацетамід тощо, ацетонітрил тощо або їх суміші є бажаними. Використання основи є ефективним для реакції. Основою є, наприклад, неорганічні основи, такі як гідрид натрію, гідроксид натрію, гідроксид калію тощо, основні солі, такі як карбонат натрію, карбонат калію, карбонат цезію, гідрокарбонат натрію тощо, металеві основи, такі як етоксид калію, трет-бутоксид калію, метоксид натрію, етоксид натрію тощо, ароматичні аміни, такі як піридин, лутидин тощо, третинні аміни, такі як триетиламін, трипропілaмін, трибутиламін, циклогексилдиметиламін, 4-диметилaмінoпіридин, N,N-диметиланілін, N-метилпіперидин, Nметилпіролідин, N-метилморфолін тощо. Кількість використаної основи становить 0,8 - 10 моль, бажано 1 - 5 моль, на 1 моль сполуки (V). Реакцію також переважно здійснюють у присутності в краун-етері. Краун-етером є, наприклад, 15-краун-5-етер, 18-краун-6-етер тощо. Кількість використаного краун-етера становить 0,01 - 10 моль, бажано 1 - 5 моль, на 1 моль сполуки (V). Хоча час реакції залежить від використаних реагентів та розчинника, він зазвичай становить 1 хв. - 48 год., бажано 10 хв. - 8 год. Температура реакції зазвичай дорівнює від -20 °C до 100 °C, бажано від 0 °C до 50 °C. Сполуку (I), де є таким як визначено вище одержують, використовуючи сполуку (VII) та метиламін або його сіль, шляхом відновлювального амінування аналогічно способу, описаному у Jikken Kagaku Koza (Courses in Experimental Chemistry), vol. 14-III, p. 1380 - 1385 (published by MARUZEN CO., LTD.) тощо. Окрім цього, сполуку (II) також одержують за наступним способом, та сполуку (I) одержують за способом подібним до вищеописаного. Сполуку (VIII), де кожен символ є таким як визначено вище одержують за відомим способом, наприклад, способи описані у Tetrahedron Letters, vol. 13, p. 5337 (1972), Heterocycles, vol. 7, p. 77 (1977), Chem. Pharm. Bull., vol. 27, p. 2857 (1979), J. Org. Chem., vol. 62, p. 2649 (1997) тощо, або аналогічно. Сполуку (IX), де кожен символ є таким як визначено вище одержують шляхом взаємодії сполуки (VIII) з N-бромсукцинімідом (NBS). N-Бромсукцинімідом (NBS) бажано використовують у одному еквіваленті по відношенню до сполуки (VIII), та реакцію бажано здійснюють в атмосфері інертного газу, такого як азот, аргон тощо. 11 UA 105185 C2 5 10 15 20 25 30 Цю реакцію бажано здійснюють, використовуючи інертний розчинник. Хоча вибір розчинника не є обмеженим доки триває реакція, розчинники, такі як етери (наприклад, тетрагідрофуран, діетиловий етер тощо), аміди (наприклад, N,N-диметилформамід, N,N-диметилацетамід тощо), їх суміші тощо є бажаними. Хоча час реакції залежить від використаних реагентів та розчинника, він зазвичай становить 10 хв. - 24 год., бажано 5 - 12 год. Температура реакції зазвичай дорівнює від -78 °C дo 80 °C, бажано від -78 °C дo 30 °C. Для реакції іноді ефективно додавати основу. Хоча вибір основи не є обмеженим доки триває реакція, використовують органічні основи, такі як піридин, піколін, лутидин тощо, тощо. Кількість використаної органічної основи становить 0,001 - 10 еквівалентів, бажано 0,001 - 0,1 еквівалентів, на сполуку (VIII). 9 Сполуку (X), де R означає пірольну захисну групу та інші символи є такими як визначено вище, одержують шляхом захисту азоту піролу сполуки (IX). Пірольна захисна група не є обмеженою та їх приклади включають трет-бутоксикарбоніл (BOC група), бензилоксикарбоніл (Cbz група), арил або гетерoарилсульфоніл, бензил, триізопропілсиліл, тощо. Реакцію захисту здійснювали за відомим способом, наприклад, способом анлогічним rd способу, описаному у Protective Groups in Organic Synthesis, 3 Ed., Theodora W. Greene, Peter G. M. Wuts, pp. 494-653, Wiley-Interscience (1999) тощо. Сполуку (XII), де кожен символ є таким як визначено вище, одержують шляхом взаємодії сполуки (X) з сполукою, представленою формулою (XIa) де кожен символ є таким як визначено вище, або різними похідними естеру формули (XIa) за способом, описаним у Synthetic Communications, vol. 11, page 513 (1981), або аналогічними способами. Окрім цього, одержують шляхом взаємодії сполуки (X) з сполукою, представленою формулою (XIb) де R означає алкіл або арил, за способом, описаним у Synthesis, vol. 7, pages 564-565 (1986) або аналогічними способами. Приклади “алкілу” для R включають метил та н-бутил, та Приклади “арилу” включають феніл. Сполуку (II), де кожен символ є таким як визначено вище, одержують з сполуки (IX) за способом, подібним до способу одержання сполуки (XII) з сполуки (X). Альтернативно, Сполуку (II) одержують з сполуки (XII) за відомим способом, наприклад, способом, описаним у Protective rd Groups in Organic Synthesis, 3 Ed., Theodora W. Greene, Peter G. M. Wuts, pp. 494-653, WileyInterscience (1999), тощо, шляхом видалення захисної групи азоту піролу. Окрім цього, сполуку (I) також одержують за наступним способом. 35 12 UA 105185 C2 5 10 Сполуку (XIII), де кожен символ є таким як визначено вище одержують з сполуки (III) за способом, подібним до способу одержання сполуки (VII) з сполуки (V). Сполуку (XIV), де кожен символ є таким як визначено вище одержують з сполуки (XIII) за способом, подібним до способу одержання сполуки (IV) з сполуки (III). Сполуку (VII), де кожен символ є таким як визначено вище одержують з сполуки (XIV) за способом, подібним до способу одержання сполуки (V) з сполуки (IV). Сполуку (I), одержують з сполуки (VII) за способом, подібним до вищеописаного. Альтернативно, сполуку (I) також одержують з сполуки (XIV) за способом, який включає взаємодію метиламіну за допомогою галогенування та метансульфонілування, спосіб, який включає конденсування з метиламіном, захищеним Boc, тощо, після чого здійснювали зняття захисту тощо. Окрім цього, сполуку (I) також одержують за наступним способом. 15 20 25 Сполуку (XV) як вказано вище одержують з сполуки (V) за способом, подібним до способу одержання сполуки (I) з сполуки (VII). 10 Сполуку (XVI), де R означає захисну аміногрупу одержують шляхом захисту аміногрупи сполуки (XV). Приклади захисної аміногрупи включають, проте не обмежуються наступними: трет-бутоксикарбоніл (BOC група), бензилоксикарбоніл (Cbz група), 2,4-диметоксибензил тощо. Цю реакцію захисту здійснювали за відомим способом, наприклад, способом, описаним у rd Protective Groups in Organic Synthesis, 3 Ed., Theodora W. Greene, Peter G. M. Wuts, pp. 494653, Wiley-Interscience (1999) тощо. Сполуку (XVII), де кожен символ є таким як визначено вище одержують з сполуки (XVI) за способом, подібним до способу одержання сполуки (VII) з сполуки (V). 13 UA 105185 C2 5 10 15 20 25 30 Сполуку (I) одержують шляхом видалення захисної аміногрупи з сполуки (XVII) за відомим способом, наприклад, способом, описаним у Protective Groups in Organic Synthesis, 3rd Ed., Theodora W. Greene, Peter G. M. Wuts, pp. 494-653, Wiley-Interscience (1999) тощо. Сполуку (V) також одержують за наступним способом. Більш того, сполуку (I) одержують використовуючи спосіб, подібний до вищеописаного способу. Сполуку (XVIII) держують за відомим способом, наприклад, способом, описаним у Journal of Organic Chemistry (J. Org. Chem.), vol. 55, p. 6317 (1990) тощо, або аналогічним способом. Сполуку (XIX), де кожен символ є таким як визначено вище, одержують з сполуки (XVIII) за способом, подібним до способу одержання сполуки (X) з сполуки (IX). Сполуку (XX), де кожен символ є таким як визначено вище одержують з сполуки (XIX) за способом, подібним до способу одержання сполуки (XII) з сполуки (X). Сполуку (XXI), одержують з сполуки (XX) за способом, подібним до способу одержання сполуки (II) з сполуки (XII). Альтернативно, Сполуку (XXI), де кожен символ є таким як визначено вище одержують з сполуки (XVIII) за способом, подібним до способу одержання сполуки (XII) з сполуки (X). Сполуку (V) одержують з сполуки (XXI) за способом, подібним до способу одержання сполуки (III) з сполуки (II). Окрім цього, Сполука (V) також одержують за наступним способом. Більш того, сполуку (I) одержують, використовуючи спосіб, подібний до вищеописаного способу. Сполуку (XXII), де кожен символ є таким як визначено вище, одержують за відомим способом, наприклад, способом, описаним у Tetrahedron Letters, vol. 40, p. 4905-4908 (1999) тощо, або аналогічним способом. 11 Сполуку (XXIII), де R означає гідроксильну захисну групу, та інші символи є такими як визначено вище одержують, наприклад, за способом, описаним у Organic Biomolecular Chemistry (Org. Biomol. Chem.), vol. 1, p. 3527-3534 (2003) тощо шляхом взаємодії сполуки (XXII) з естером бром (або хлор, йод) дифтороцтової кислоти, та захисту отриманої гідроксигрупи. Гідроксильну захисну групу не обмежують доки триває реакція, та бажані приклади включають тозил, мезил тощо. 14 UA 105185 C2 12 5 10 15 20 25 30 35 40 45 Сполуку (XXIV), де R означає амідну захисну групу, та інші символи є такими як визначено вище одержують кристалізацією сполуки (XXIII) за допомогою зняття захисту з аміногрупи, та захисту амідної групи. Умови зняття захисту з аміногрупи та кристалізації не є обмеженими доки триває реакція, та їх приклади включають умови реакції для одночасної кристалізації та зняття захисту у розчині гідрохлорид-етилацетат тощо. Амідну захисну групу не обмежують доки триває реакція, та бажані приклади включають трет-бутоксикарбоніл (BOC група) тощо. Сполука (XXVI), де кожен символ є таким як визначено вище, одержують шляхом взаємодії сполуки (XXIV) з сполукою, представленою формулою (XXV), де Z означає атом або молекулу що надає нуклеофільності, такі як Li, MgBr тощо. Сполуку (XXV) одержують у реакційній системі згідно з, наприклад, способом, описаним у Tetrahedron Lett., vol. 21, p. 4137 (1980) or Tetrahedron Lett., vol. 42, p. 8697 (2001), або аналогічним способом. Розчинник у цій реакції не є обмеженим доки реакція триває, та бажані розчинники включають вуглеводні, такі як н-гексан, толуол тощо, етери, такі як тетрагідрофуран, діетиловий етер тощо або їх суміші тощо. Час реакції залежить від використаних субстрату та розчинника, та зазвичай становить 1 хв. - 48 год., бажано 10 хв. - 24 год. Сполуку (XXVII) одержують за відомим способом, наприклад, способом, описаним у Tetrahedron Letters, vol. 36, p. 5119-5122 (1995) тощо, або аналогічним способом. Альтернативно, Сполуку (XXVII) одержують шляхом відновлення сполуки (XXVI) та реагування отриманої сполуки з основою. Відновлювальний агент для цієї реакції не є обмеженим доки триває реакція, та бажані приклади включають боргідрид натрію, тощо. Приклади основ включають неорганічні основи, такі як гідрид натрію, гідроксид натрію, гідроксид калію тощо, основні солі, такі як карбонат натрію, карбонат калію, карбонат цезію, гідрокарбонат натрію тощо, металеві основи, такі як етоксид калію, трет-бутоксид калію, метоксид натрію, етоксид натрію тощо, ароматичні аміни, такі як піридин, лутидин тощо, третинні аміни, такі як триетиламін, трипропілaмін, трибутиламін, циклогексилдиметиламін, 4диметилaмінoпіридин, N,N-диметиланілін, N-метилпіперидин, N-метилпіролідин, Nметилморфолін, 1,8-діазобіцикло[5.4.0]ундец-7-ен (DBU) тощо. Кількість використаної основи становить 0,8 - 20 моль, бажано 1 - 10 моль, на 1 моль сполуки (XXVІ). Цю реакцію бажано здійснюють, використовуючи інертний розчинник. Хоча розчинник не є обмеженим доки триває реакція, вуглеводні, такі як бензол, толуол тощо, етери, такі як тетрагідрофуран тощо, аміди, такі як N,N-диметилформамід, N,N-диметилацетамід тощо, ацетонітрил тощо або суміші розчинників тощо є бажаними. Перевагою цієї реакції є те, що її здійснюють у присутності краун-етерів. Приклади краун-етеру включають 15-краун-5-етер, 18краун-6-етер, тощо. Кількість використаного краун-етеру становить 0,01 - 10 моль, бажано 1 - 5 моль, на 1 моль сполуки (XXVI). Хоча час реакції залежить від використаних реагентів та розчинника, він зазвичай становить 1 хв. - 48 год., бажано 10 хв. - 8 год. Температура реакції зазвичай дорівнює від -78 °C до 100 °C, бажано від -10 °C дo 70 °C. Сполуку (XXVIII), де кожен символ є таким як визначено вище, одержують з сполуки (XXVII) за способом, подібним до способу одержання сполуки (X) з сполуки (IX). Сполуку (V) одержують з сполуки (XXVIII), наприклад, за допомогою звичайного формілування, включаючи обробку продукту реакції оксалілхлориду диметилформамідом, тощо. Окрім цього, Сполука (V) одержують за способом, який включає введення ціаногрупи та карбонової кислоти та перетворення отриманої сполуки на альдегід тощо. Окрім цього, сполуку (XVI) також одержують за наступним способом, та сполуку (I) одержують використовуючи спосіб, подібний до вищеописаного способу. 15 UA 105185 C2 12 5 10 15 20 25 30 13 Сполуку (XXIX), де R є таким як вказано вище, та R означає атом галогену, такий як атом хлору, атом брому, атом йоду тощо одержують за відомим способом, наприклад, способом, описаним у Journal of Organic Chemistry (J. Org. Chem.), vol. 66, p. 315 (2001) тощо, або 12 аналогічним способом. Приклади амідної захисної групи для R включають, проте не обмежуються наступними: трет-бутоксикарбоніл (BOC група), тозил, бензил, аліл, тощо. Сполуку (XXX), де кожен символ є таким як визначено вище, одержують шляхом обробки сполуки (XXIX) основою. Приклади основ включають неорганічні основи, такі як гідрид натрію, гідроксид натрію, гідроксид калію тощо, основні солі, такі як карбонат натрію, карбонат калію, карбонат цезію, гідрокарбонат натрію тощо, металеві основи, такі як етоксид калію, третбутоксид калію, метоксид натрію, етоксид натрію тощо, ароматичні аміни, такі як піридин, лутидин тощо, третинні аміни, такі як триетиламін, трипропілaмін, трибутиламін, циклогексилдиметиламін, 4-диметилaмінoпіридин, N,N-диметиланілін, N-метилпіперидин, Nметилпіролідин, N-метилморфолін, 1,8-діазобіцикло[5.4.0]ундец-7-ен (DBU) тощо. Кількість використаної основи становить 0,8 - 10 моль, бажано 1 - 5 моль, на 1 моль сполуки (XXIX). Цю реакцію бажано здійснювати, використовуючи інертний розчинник. Хоча розчинник не є обмеженим доки триває реакція, вуглеводні такі як бензол, толуол тощо, етери, такі як тетрагідрофуран тощо, аміди, такі як N,N-диметилформамід, N,N-диметилацетамід тощо, ацетонітрил тощо або суміші розчинників тощо є бажаними. Хоча час реакції залежить від використаних реагентів та розчинника, він зазвичай становить 1 хв. - 48 год., бажано 10 хв. - 8 год. Температура реакції зазвичай дорівнює від -78 °C до 100 °C, бажано від -10 °C до 70 °C. Сполуку (XXXIa), де кожен символ є таким як визначено вище, або сполуку (XXXIb), де кожен символ у формулі А є таким як визначено вище, одержують з сполуки (XXX) за способом, подібним до способу одержання сполуки (XXVI) з сполуки (XXIV). Сполуку (XXXII) одержують шляхом зняття захисту та дегідруванням сполуки (XXXIa) або Сполуки (XXXIb). Хоча умови реакції не є обмеженими, вони змінюються в залежності від використаних захисної групи розчинника. Наприклад, зняття захисту та дегідрування безперервно здійснюють шляхом обробки кислотою, такою як трифтороцтова кислота та хлорводнева кислота. Сполуку (XVI), де кожен символ є таким як визначено вище, одержують шляхом обробки сполуки, представленої формулою (XXXIII), де кожен символ є таким як визначено вище, основою, такою як гідрид натрію, н-бутиллітію тощо та взаємодії отриманої сполуки з сполукою (XXXII). 35 16 UA 105185 C2 10 5 10 15 20 25 30 35 40 45 50 55 60 Захисна група для R у цій реакції не є обмеженою, доки її можна видалити, та бажані приклади включають бензил, 4-метоксибензил, 2,4-диметоксибензил тощо. Хоча розчинник у цій реакції не є обмеженим доки реакція триває, вуглеводи такі як нгексан, толуол тощо, етери, такі як тетрагідрофуран, діетиловий етер тощо або суміш розчинників тощо є бажаною. Хоча час реакції залежить від використаних субстратів та розчинника, він зазвичай становить 1 хв. - 48 год., бажано 10 хв. - 5 год. Температура реакції зазвичай дорівнює від -100 °C дo 100 °C, бажано від -78 °C дo 30 °C. Сполуку (I) виділяють та очищають відомими способами, такими як міжфазний перехід, концентрування, екстракція розчинником, фракціонування, перетворення рідини, кристалізація, перекристалізація, хроматографія тощо. Коли сполуку (I) одержують як вільну сполуку, її можна перетворити на бажану сіль за відомим способом або аналогічним способом; навпаки, коли сполуку (I) одержують як сіль, її можна перетворити на вільну форму або іншу бажану сіль за відомим способом або аналогічним способом. Сполуку (I) можна використовувати як пролікарську форму. Пролікарська форма сполуки (I) означає сполуку перетворену на сполуку (I) при фізіологічних умовах у тілі шляхом реагування з ферментом, шлунковою кислотою, тощо, тобто, сполуку перетворену на сполуку (I) ферментативним окисленням, відновленням, гідролізом, тощо; сполуку перетворену на сполуку (I) шляхом гідролізу з шлунковою кислотою, тощо. Пролікарська форма сполуки (I) включає сполуку, де аміногрупа сполуки (I) модифікована ацилом, алкілом або фосфорилом (наприклад, сполука, де аміногрупа сполуки (I) модифікована ейкозаноїлом, аланілом, пентиламінокарбонілом, (5-метил-2-оксо-1,3-діоксолен-4-іл)метоксикарбоніл, тетрагідрофураніл, піролідилметил, півалоїлоксиметил або т-бутил, тощо); сполука, де гідрокси група сполуки (I) модифікована ацилом, алкілом, фосфорною кислотою або борноб кислотою (наприклад, сполука, де гідрокси група сполуки (I) модифікована ацетил, палмітоїл, пропаноїл, півалоїл, сукциніл, фумарил, аланіл або диметиамінометилкарбоніл, тощо); сполука, де карбоксильна група сполуки (I) модифікована на естер або амід (наприклад, сполука, де карбоксильна група сполуки (I) модифікована на етиловий естер, феніловий естер, карбоксиметиловий естер, диметиамінометиловий естер, півалоїлоксиметиловий естер, етоксикарбонілоксиетил естер, фталідиловий естер, (5-метил-2-оксо-1,3-діоксолен-4-іл)метил естер, циклогексилоксикарбонілетиловий естер або метиламід, тощо); тощо. Ці сполуки одержують з сполуки (I) за відомим способом. Окрім цього, пролікарська форма сполуки (I) може бути сполукою, перетвореною на сполуку (I) при фізіологічних умовах, як описано у Pharmaceutical Research and Development, Vol. 7 (Molecule Design), pp. 163-198 (1990), published by Hirokawa Publishing Co. Коли сполука (I) включає оптичний ізомер, стереоізомер, регіоізомер або ротамер, всі ці ізомери та їх суміші є також включеними у сполуку (I). Наприклад, коли сполука (I) включає оптичний ізомер, оптичний ізомер виділяють з рацемату також є включеним у сполуку (I). Ці ізомери одержують як окремі продукти за відомими способами синтезу та розділення (концентрування, екстракція розчинником, колонкова хроматографія, перекристалізація, тощо). Сполука (I) може знаходитись у формі кристалу, та як окремий кристал, так і їх суміші є включеними у сполуку (I). Кристали одержують шляхом кристалізації за відомими способами кристалізації. Сполука (I) може знаходитись у формі сольвату (наприклад, гідрату тощо) або несольвату, які є включеними у сполуку (I). 3 14 35 125 Сполука мічена ізотопом (наприклад, H, C, S, I, тощо) і форма модифікована 1 2 дейтерієм, де H перетворений на H(D) також є включеними у сполуку (I). Сполука (I) або її сіль або пролікарська форма даного винаходу (у даному документі інколи посилаються на сполуку даного винаходу) має ефект інгібітора протонної помпи та пригнічує секрецію шлункового соку. Окрім цього, з огляду на те, що вона проявляє низьку токсичність (наприклад, гостру токсичність, хронічну токсичність, генетичну токсичність, репродуктивну токсичність, кардіотоксичність, взаємодія лікарських засобів, онкогенність тощо) та значну розчинність у воді, та стабільність, in vivo кінетику (абсорбційна здатність, розподілення, метаболізм, виділення тощо), та значну ефективність, використовуються як медикаменти. Сполука даного винаходу є придатною для профілактики або лікування наступних хвороб: пептична виразка (наприклад, виразка шлунку, виразка дванадцятипалої кишки, анастомозна виразка, виразка, викликана нестероїдним протизапальним лікарським засобом, виразка, викликана постопераційним стресом тощо); синдром Золінгера-Елісона; гастрит; ерозійний езофагіт; рефлюксний езофагіт такі як ерозійний рефлюксний езофагіт тощо; симптоматична гастроезофагальна рефлюксна хвороба (Симптоматична ГЕРХ), така як неерозійний рефлюксний езофагіт, езофагальний рефлекс неопосередкований езофагітом тощо; стравохід 17 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 Барета; функціональна диспепсія; рак шлунку (включаючи рак шлунку асоційований з підвищеним виробленням інтерлейкіна-1 (внаслідок поліморфізму генів інтерлейкіна-1); лімфома MALT шлунку; висока кислотність; кровотеча верхнього відділу шлунковокишкового тракту, викликана пептичною виразкою, виразка, викликана гострим стресом, геморагічний гастрит, інвазивний стрес (наприклад, стрес, викликаний значною операцією, яка потребує постопераціного лікування, або цереброваскулярний розлад, пошкодження голови, пошкодження багатьох органів або значний опік, який потребує інтенсивного лікування) тощо; захворювання, що передаються повітряним шляхом; астма; тощо у ссавців (наприклад, людини, мавпи, вівці, бика, коней, собаки, кішки, кроля, пацюка, миші тощо), введення перед анестезією, знищення або допоміжне знищення Helicobacter pylori тощо. Як використано у даному документі, вищенаведені рефлюксний езофагіт (ерозійний езофагіт) та симптоматичну гастроезофагальну рефлюксну хворобу (симптоматична ГЕРХ) інколи називають просто ГЕРХ. Вміст сполуки даного винаходу у фармацевтичній композиції даного винаходу становить приблизно 0,01 - 100 мас.% від всієї композиції. Хоча заміна об’єкта залежить від об’єкта введення, шляху введення, хвороби об’єкта, її доза становить приблизно 0,5 - 1,500 мг/добу, бажано приблизно 5 - 150 мг/добу з розрахунку на активний інгредієнт, коли, наприклад, сполуку вводять орально як агент проти виразки дорослій людині (60 кг). Сполуку даного винаходу вводять один раз на добу або 2 або 3 частинами на добу. Сполука даного винаходу проявляє низьку токсичність та її можна безпечно вводити орально або парентерально (наприклад, місцево, ректально, внутрішньовенно тощо) як саму по собі або у лікарській формі, яка містить фармацевтичну композицію, яка містить фармацевтично прийнятний носій, доданий за відомим способом, такій як таблетки (включаючи таблетки покриті цукром та таблетки з плівковим покриттям), порошок, гранули, капсули (включаючи м’які капсули), орально дизінтегруюча таблетка, орально дизінтегруюча плівка, рідина, ін’єкція, супозиторій, лікарська форма з уповільненим вивільненням, пластир тощо. Зокрема, сполуку даного винаходу бажано вводять як оральну лікарську фору у формі таблетки, гранули, капсули тощо. Фармацевтично прийнятний носій, який використовують для одержання фармацевтичної композиції даного винаходу, включає різноманітні органічні та неорганічні носії, які зазвичай використовують як фармацевтичні матеріали, включаючи наповнювачі, лубриканти, зв’язувальні речовини, дизінтегранти, водорозчинні полімери та основні неорганічні солі для твердих лікарських форм; та розчинники, солюбілізатори, суспендувальні агенти, агенти, що надають ізотонічності, буфери та заспокійливі для рідких лікарських форм тощо. Також, у разі необхідності, використовують звичайні фармацевтичні добавки, такі як консерванти, антиоксиданти, барвники, підсолоджувачі, підкислювачі, барботувальні агенти та ароматизатори. Такі “наповнювачі” включають, наприклад, лактозу, цукрозу, D-манітол, крохмаль, кукурудзяний крохмаль, кристалічну целюлозу, світлу безводну кремнієву кислоту, оксид титану тощо. Такі “лубриканти” включають, наприклад, стеарат магнію, естери цукрози та жирних кислот, поліетиленгліколь, тальк, стеаринову кислоту тощо. Такі “зв’язувальні речовини” включають, наприклад, гідроксипропіл целюлозу, гідроксипропілметил целюлозу, кристалічну целюлозу, крохмаль, полівінілпіролідон, порошок гумарабіку, желатин, пулулан, низькозаміщену гідроксипропіл целюлозу тощо. Такі “дизінтегранти” включають (1) кросповідон, (2) так звані супер-дизінтегранти, такі як натрію кроскармелоза (виробництва FMC-Asahi Chemical Industry Co. Ltd.) та кальцію кармелоза (виробництва Gotoku Yakuhin) etc, (3) натрію карбоксиметил крохмаль (наприклад, продукт Matsutani Chemical), (4) низько-заміщену гідроксипропіл целюлозу (наприклад, продукт Shin-Etsu Chemical), (5) кукурудзяний крохмаль, тощо. Вказаний “кросповідон” може бути будь-яким поперечно зшитим полімером з хімічною назвою 1-етеніл-2-піролідинон гомополімер, включаючи полівінілпіролідон (PVPP) та гомополімер 1-виніл-2-піролідинон, та представлений Colidon CL (зареєстрована торгівельна марка; виробництва BASF), Polyplasdon XL (зареєстрована торгівельна марка; виробництва ISP), Polyplasdon XL-10 (зареєстрована торгівельна марка; виробництва ISP), Polyplasdon INF10 (зареєстрована торгівельна марка; виробництва ISP) тощо. Такі “водорозчинні полімери” включають, наприклад, етанол-розчинні водорозчинні полімери [наприклад, похідні целюлози, такі як гідроксипропілцелюлоза (у даному документі також посилаються як на HPC) тощо, полівінілпіролідон тощо], етанол-нерозчинні водорозчинні полімери [наприклад, похідні целюлози, такі як гідроксипропілметил целюлоза (у даному документі також посилаються як на HPMC) тощо, метилцелюлоза, карбоксиметилцелюлоза натрію тощо, полікрилат натрію, полівініловий спирт, альгінат натрію, гуарова смола тощо] тощо. Такі “основні неорганічні солі” включають, наприклад, основні неорганічні солі натрію, калію, магнію та/або кальцію. Бажаними є основні неорганічні солі магнію та/або кальцію. Більш бажаними є основні неорганічні солі 18 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 магнію. Такі основні неорганічні солі натрію включають, наприклад, карбонат натрію, гідрокарбонат натрію, гідрофосфат натрію тощо. Такі основні неорганічні солі калію включають, наприклад, карбонат калію, гідрокарбонат калію тощо. Такі основні неорганічні солі магнію включають, наприклад, важкий карбонат магнію, карбонат магнію, оксид магнію, гідроксид магнію, алюмінометасиліцилат магнію, силіцилат магнію, алюмінат магнію, синтетичний гідроталькiт [Mg6Al2(OH)16 · CO3 · 4H2O], та гідроксид алюмінію магнію. Бажаними є важкий карбонат магнію, карбонат магнію, оксид магнію, гідроксид магнію тощо. Такі основні неорганічні солі кальцію включають, наприклад, осаджений карбонат кальцію, гідроксид кальцію, тощо. Такі “розчинники” включають, наприклад, воду для ін’єкцій, спирт, пропілeнгліколь, макрогол, кунжутну олію, кукурудзяну олію, оливу тощо. Такі “солюбілізатори” включають, наприклад, поліетиленгліколь, пропілeнгліколь, D-манітол, бензил бензоат, етанол, трісамінометан, холестерoл, триетаноламін, карбонат натрію, цитрат натрію тощо. Такі “суспендувальні агенти” включають, наприклад, поверхнево-активні речовини, такі як стeарилтриетаноламін, лаурилсульфат натрію, лауриламінопропіонова кислота, лецитин, бензалконію хлорид, бензетонію хлорид, моностеарат гліцерилу тощо; гідрофільні полімери, такі як полівініловий спирт, полівінілпіролідон, карбоксиметил целюлозу натрію, метил целюлозу, гідроксиметил целюлозу, гідроксиетил целюлозу, гідроксипропіл целюлозу тощо, тощо. Такі “агенти, що надають ізотонічності” включають, наприклад, глюкозу, D-сорбітол, хлорид натрію, гліцерин, Dманітол тощо. Такі “буфери” включають, наприклад, буферні розчини фосфатів, ацетатів, карбонатів, цитратів тощо. Такі “заспокійливі” включають, наприклад, бензиловий спирт тощо. Такі “консерванти” включають, наприклад, естери п-оксибензойної кислоти, хлорбутанол, бензиловий спирт, фенетиловий спирт, дегідрооцтової кислоти, сорбінова кислота тощо. Такі “антиоксиданти” включають, наприклад, сульфіти, аскорбінова кислота, α-токоферол тощо. Такі “барвники” включають, наприклад, харчові барвники, такі як харчовий жовтий № 5, харчовий червоний № 2, харчовий блакитний № 2 тощо; їстівні барвники, оксид заліза ІІІ червоний тощо. Такі “підсолоджувачі” включають, наприклад, сахарин натрію, гліцирізинат калію, аспартам, стевія, тауматин тощо. Такі “підкислювачі” включають, наприклад, лимонну кислоту (лимонний ангідрид), винну кислоту, яблучну кислоту тощо. Такі “барботувальні агенти” включають, наприклад, бікарбонат натрію тощо. Такі “ароматизатори” можуть бути синтетичними або природними сполуками, та включають, наприклад, лимон, лайм, апельсин, ментол, полуницю, тощо. Сполуку даного винаходу одержують у вигляді лікарської форми для орального введення за відомим способом, шляхом, наприклад, формування під тиском з носієм, таким як наповнювач, дизінтегрант, зв’язувальний агент, лубрикант тощо, та послідовним покриттям лікарської форми за відомим способом з метою маскування смаку, розчинення у кишечнику або уповільненого вивільнення. Для кишкової лікарської форми, проміжний шар наносіть за відомим способом між кишковим шаром та шаром, що містить лікарський засіб, з метою розділення двох шарів. Для одержання сполуки даного винаходу у вигляді орально дизінтегруючої таблетки, доступні способи включають, наприклад, спосіб, де ядро, яке містить кристалічну целюлозу та лактозу покривають сполукою даного винаходу та, у разі потреби, основною неорганічною сіллю, та після цього додатково покривають покривним шаром, який містить водо-розчинний полімер, в результаті одержують композицію, яку покривають кишковим покриттям, яке містить поліетиленгліколь, після чого покривають кишковим покриттям, яке містить триетилцитрат, після чого додатково покривають кишковим покриттям, яке містить поліетиленгліколь, та наприкінці покривають манітолом, одержуючи дрібні гранули, які змішують з добавками та формують. Вищенаведений “кишковий покривний шар” включає, наприклад, шар, який складається з суміші одного або кількох видів водних кишкових полімерів, таких як ацетат фталат целюлози (CAP), гідроксипропілметил целюлозу фталат, гідроксиметил целюлозу ацетат сукцинат, співполімери метакрилової кислоти (наприклад, Eudragit (зареєстрована торгівельна марка; виробництва Rohm) L30D-55, Colicoat (зареєстрована торгівельна марка; виробництва BASF) MAE30DP, Polyquid (зареєстрована торгівельна марка; виробництва San-yo Chemical) PA30 тощо), карбоксиметилетил целюлозу, шелак тощо; субстрати з уповільненим вивільненням, такі як співполімери метакрилової кислоти (наприклад, Eudragit (зареєстрована торгівельна марка) NE30D, Eudragit (зареєстрована торгівельна марка) RL30D, Eudragit (зареєстрована торгівельна марка) RS30D, тощо) тощо; водорозчинні полімери; пластифікатори, такі як триетилцитрат, поліетиленгліколь, ацетильовані моногліцериди, триацетин, касторова олія тощо. Вищенаведений “добавки” включають, наприклад, вода-розчинні цукрові спирти (наприклад, сорбітол, манітол, малтітол, відновлені сахариди крохмалю, ксилітол, відновлена палатіноза, ерітритол, тощо), кристалічну целюлозу (наприклад, Ceolas (зареєстрована торгівельна марка) KG 801, Avicel (зареєстрована торгівельна марка) PH 101, Avicel (зареєстрована торгівельна 19 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 марка) PH 102, Avicel (зареєстрована торгівельна марка) PH 301, Avicel (зареєстрована торгівельна марка) PH 302, Avicel (зареєстрована торгівельна марка) RC-591 (кристалічна целюлоза · кармелоза натрію) тощо), низько-заміщену гідроксипропілцелюлозу (наприклад, LH22, LH-32, LH-23, LH-33 (Shin-Etsu Chemical), їх суміші тощо) тощо. Більш того, також використовують зв’язувальні речовини, підкислювачі, барботувальні агенти, підсолоджувачі, ароматизатори, лубриканти, барвники, стабілізатори, наповнювачі, дизінтегранти тощо. Сполуку даного винаходу використовують у комбінації з 1 - 3 іншими активними інгредієнтами. Такі “інші активні інгредієнти” включають, наприклад, активні сполуки проти Helicobacter pylori, імідазоли, солі вісмуту, хінолони, тощо. Приклади “активних сполук проти Helicobacter” включають пеніцилінові антибіотики (наприклад, амоксицилін, бензилпеніцилін, піперацилін, мецилінам, ампіцилін, темоцилін, бакампіцилін, аспоксицилін, султаміцилін, ленампіцилін тощо), цефеми (наприклад, цефіксим, цефаклор тощо), макролідні антибіотики (наприклад, еритроміцин, кларітроміцин, рокситроміцин, рокітаміцин, флурітроміцин, телітроміцин тощо), тетрациклінові антибіотики (наприклад, тетрациклін, міноциклін, стрептоміцин тощо), аміноглікозиди (наприклад, гентаміцин, амікацин тощо), іміпенем тощо. Серед них, бажаними є пеніцилінові антибіотики, макроліди тощо. Такі “імідазоли” включають, наприклад, метронідазол, міконазол тощо. Такі “солі вісмуту” включають, наприклад, ацетат вісмуту, цитрат вісмуту, субсаліцилат вісмуту тощо. Такі “хінолони” включають, наприклад, офлоксацин, циплоксацин тощо. Для знищення Helicobacter pylori, сполуку (I) або її сіль даного винаходу бажано застосовують з пеніциліновим антибіотиком (наприклад, амоксициліном тощо) та еритроміциновим антибіотиком (наприклад, кларітроміцином тощо). Для знищення Helicobacter pylori, хоча сполука даного винаходу має дію проти H. pylori (бактеріостатичну або знищувальну) сама по собі, вона може покращувати антибактеріальну дію інших антиибіотиків, на основі контролювання pH у шлунку тощо, та також забезпечує допоміжний вплив, такий як знищення на основі дії антибіотиків використаних у комбінації. Такі “інші активні інгредієнти” та сполуку (I) або її сіль даного винаходу можуть змішують, одержують як єдину фармацеквтичну компоицію [наприклад, таблетки, порошки, гранули, капсули (включаючи м’які капсули), рідини, ін’єкції, супозиторії, лікарська форма з уповільненим вивільненням, тощо], за відомим способом, та використовують у комбінації, та також одержують у вигляді окремих лікарських форм та вводять суб’єкту одночасно або з інтервалом. Окрім цього, сполуку даного винаходу використовують у комбінації з прокінетиком, лікарським засобом, який впливає на нижній сфінктер стравоходу (наприклад, тимчасовий супресант релаксації нижнього езофагального сфінктеру тощо), відкривач ClC-2 каналу (стимулятор секреції кишкового соку), антагоністом H2 рецептора гістаміну, антацидом, седативним засобом, шлунковим або нестероїдним протизапальним лікарським засобом (NSAID). “Прокінетик” включає, наприклад, домперідон, метоклопрамід, мозаприд, ітоприд, тегасерод тощо. “Лікарський засіб, який впливає на нижній сфінктер стравоходу” включає, наприклад, агоністи рецептора GABA-B, такі як баклофен, їх оптично активну форму тощо, антагоністи рецептора глутаміна тощо. “Відкривач ClC-2 каналу (стимулятор секреції кишкового соку)”, включає лубіпростон тощо. “Антагоніст H2 рецептора гістаміну” включає циметидин, ранітидин, фамотидин, роксатидин, нізатидин, лафутидин тощо. “Антацид” включає гідрокарбонат натрію, гідроксид алюмінію тощо. “Седативні засоби” включають діазепам, хлордіазепоксид тощо. “Шлункові засоби” включають горечавка, сверція японська, діастаза тощо. “Нестероїдні протизапальні лікарські засоби” включають, наприклад, аспірин, індометацин, ібупрофен, мефенамінову кислоту, діклофенак, етодорак, піроксикам, целекоксиб тощо. Прокінетик, лікарський засіб, який впливає на нижній сфінктер стравоходу (наприклад, тимчасовий супресант релаксації нижнього езофагального сфінктеру тощо), відкривач ClC-2 каналу (стимулятор секреції кишкового соку), антагоніст H 2 рецептора гістаміну, антацид, седативний засіб, шлунковий або нестероїдний протизапальний лікарський засіб, сполука (I) або її сіль даного винаходу можуть бути змішаними, одержані як єдина фармацевтична композиція [наприклад, таблетки, порошки, гранули, капсули (включаючи м’які капсули), рідини, ін’єкції, супозиторії, лікарська форма з уповільненим вивільненнямs, тощо] за відомим способом для комбінованого застосування, або та також одержують у вигляді окремих лікарських форм та вводять суб’єкту одночасно або з інтервалом. Сполуку даного винаходу застосовують у комбінації з наступними лікарськими засобами: (i) інгібітор протонної помпи, наприклад, омепразол, eзомепразол, пантопразол, рабепразол, тенатопразол, ілапразол та лансопразол; (ii) оральний комбінований антацидний агент, наприклад, Maalox, Aludrox та Gaviscon; 20 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 (iii) протектор слизової оболонки, наприклад, полапрезинк, екаб натрію, ребаміпід, тепренон, цетраксат, сукралфат, хлорпілін-мідь та плаунотол; (iv) агент проти гастриту, наприклад, вакцина проти гастриту, ітриглумід та Z-360; (v) антагоніст 5-HT3, наприклад, доласетрон, палоносетрон, алосетрон, азасетрон, рамосетрон, мітразапін, гранісетрон, тропісетрон, E-3620, ондансетрон та індісетрон; (vi) агоніст 5-HT4, наприклад, тегасерод, мозаприд, цинітаприд та окстриптан; (vii) проносний засіб, наприклад, Trifyba, Fybogel, Konsyl, Isogel, Regulan, Celevac та Normacol; (viii) агоніст GABAB, наприклад, баклофен та AZD-3355; (ix) антагоніст GABAB, наприклад, GAS-360 та SGS-742; (x) блокатор кальцієвого каналу, наприклад, аранідипін, лацидипін, фалодипін, азелнідипін, клінідипін, ломеризин, ділтіазем, галопаміл, ефонідипін, нізолдипін, амлодипін, лерканідипін, бевантолол, нікардипін, ізрадипін, бенідипін, верапаміл, нітрендипін, барнідипін, пропафенон, манідипін, бепридил, ніфедипін, нілвадипін, німодипін та фазудил; (xi) антагоніст допаміну, наприклад, метоклопрамід, домперидон та левосульпірид; (xii) антагоніст тахікініну (NK), зокрема, антагоніст NK-3, NK-2 та NK-1, наприклад, непадутант, саредутант, талнетант, (αR,9R)-7-[3,5-біс(трифторметил)бензил]-8,9,10,11тетрагідро-9-метил-5-(4-метилфеніл)-7H-[1,4]діазоцино[2,1-g][1,7]нафтіридин-6,13-діон (TAK637), 5-[[(2R,3S)-2-[(1R)-1-[3,5-біс(трифторметил)феніл]етокси-3-(4-фторфеніл)-4морфолініл]метил]-1,2-дигідро-3H-1,2,4-тріазол-3-он (MK-869), ланепітант, дапітант та (2S,3S)-3[[2-метокси-5-(трифторметокси)феніл]метиламіно]-2-феніл-піперидин; (xiii) інгібітор синтази оксиду азоту, наприклад, GW-274150, тіларгінін, P54, гуанідіоетилдисульфід та нітрофлурбіпрофен; (xiv) антагоніст ванілоїдного рецептора 1, наприклад, AMG-517 та GW-705498; (xv) агоніст грелину, наприклад, капроморелин та TZP-101; (xvi) інгібітор AChE, наприклад, Z-338 та KW-5092. Вищенаведені лікарські засоби (i)-(xvi) та сполука (I) або її сіль даного винаходу можуть бути змішаними, одержані як єдина фармацевтична композиція [наприклад, таблетки, порошки, гранули, капсули (включаючи м’які капсули), рідини, ін’єкції, супозиторії, лікарська форма з уповільненим вивільненням, тощо] за відомим способом для комбінованого застосування, або та також одержують у вигляді окремих лікарських форм та вводять суб’єкту одночасно або з інтервалом. Приклади Даний винахід детально описано за допомогою Порівняльних Прикладів, Прикладів та Експериментальних Прикладів, які не є вичерпними. У наступних Порівняльних Прикладах та Прикладах, “кімнатна температура” зазвичай означає приблизно 10 °C - 35 °C, проте вона не є чітко обмеженою. Співвідношення рідин означає масове співвідношення. Доки не вказано протилежне, “%” означає мас. %. Вихід виражено у моль/моль %. Колонкову хроматографію на силікагелі здійснювали, використовуючи силікагель 60 (0,063-0,200 мм) виробництва MERCK, Fuji Silysia Chemical Ltd. Chromatorex (торгова назва) NH (описану як основну колонкову хроматографію на силікагелі) або Purif-Pack виробництва MORITEX (описану як колонкову хроматографію на силікагелі або основну колонкову хроматографію на силікагелі). Точку плавлення вимірювали, використовуючи пристрій для вимірювання точки плавлення Yanagimoto або пристрій для вимірювання точки 1 плавлення Buechi (B-545), та показана без додатків. Для вимірювання H-ЯМР спектра, тетраметилсилан використовували як внутрішній стандарт, та Varian Gemini-200 (200MГц), Mercury-300 (300MГц) спектрометр, Bruker AVANCE AV300 (300MГц) та JNM-AL400 (400MГц) апарат ядерно магнітного резонансу JEOL DATUM (JEOL DATUM LTD). Для одержаних результатів використовували наступні абревіатури. с: синглет, д: дуплет, дд: дублет дуплетів, ддд: дублет дублет дуплетів, дт: дуплет триплетів, т: триплет, к: квартет, дк: дуплет квартетів, м: мультиплет, ш: широкий, шс: широкий синглет, J: константа розщеплення, Гц: Герц. Порівняльний Приклад 1 трет-бутил (2-oксoетил)карбамат До змішаного розчину трет-бутил (2-гідроксиетил)карбамату (10,0 г) у диметилсульфоксиді (50 мл) та триетиламіні (12,3 г) охолоджуючи додавали комплекс триоксид сірки піридин (15,0 г), та суміш перемішували протягом години. Після цього реакційну суміш перемішували при кімнатній температурі протягом 3 год., додавали 1 моль/л хлорводневої кислоти, та суміш екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над 21 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент:гексан-етилацетат=17:3→13:7) одержуючи сполуку у вигляді світло-жовтої олії (вихід 6,50 г, 66%). 1 H-ЯМР (CDCl3) δ: 1,46 (9H, с), 4,08 (2H, д, J=4,5 Гц), 5,19 (1H, ш), 9,66 (1H, с). Порівняльний Приклад 2 Етил 4-[(трет-бутоксикарбоніл)аміно]-2,2-дифтор-3-{[(4-метилфеніл)сульфоніл]окси}бутаноат Порошок цинку (23,0 г) промивали 0,1 моль/л хлорводневої кислоти, етанолом та діетиловим ефіром, та висушували при пониженому тиску. В атмосфері аргону, до суспензії промитого порошку цинку у тетрагідрофурані (300 мл) додавали розчин трет-бутил (2oксoетил)карбамату (35,0 г) у тетрагідрофурані (50 мл), етил бромдифторацетат (75,9 г) охолоджуючи поступово додавали краплями, та суміш перемішували протягом 15 хв. 1 моль/л хлорводневої кислоти додавали до реакційної суміші, та суміш екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим водним розчином гідрокарбонату натрію, водою та насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок розчиняли у змішаному розчині тетрагідрофурану (30 мл) та піридину (40 мл), триетиламін (19 мл), 4-диметилaмінoпіридин (3,35 г) та 4-метилбензолсульфонілхлорид (39,2 г) додавали при кімнатній температурі, та суміш перемішували протягом 2 годин. Реакційну суміш концентрували при пониженому тиску, та залишок розчиняли у етилацетаті, та двічі промивали 1 моль/л хлорводневої кислоти. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим водним розчином гідрокарбонату натрію, водою та насиченим сольовим розчином, висушували над безводним сульфатом магнію, та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент:гексан-етилацетат=4:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 44,8 г, 46%). 1 H-ЯМР (CDCl3) δ: 1,33 (3H, т, J=7,2Гц), 1,46 (9H, с), 2,46 (3H, с), 3,26-3,43 (1H, м), 3,71 (1H, ш), 4,28 (2H, к, J=7,1Гц), 4,77 (1H, ш), 5,08-5,24 (1H, м), 7,35 (2H, д, J=8,1Гц), 7,80 (2H, д, J=8,1Гц). Порівняльний Приклад 3 Трет-бутил 3,3-дифтор-4-{[(4-метилфеніл)сульфоніл]окси}-2-oксoпіролідин-1-карбоксилат Дo розчину етил 4-[(трет-бутоксикарбоніл)аміно]-2,2-дифтор-3-{[(4метилфеніл)сульфоніл]окси}бутаноату (44,8 г) у етилацетаті (50 мл) додавали 4 моль/л розчину гідрохлорид-етилацетат (100 мл), та суміш перемішували протягом 3 год. Реакційну суміш концентрували при пониженому тиску, та залишок двічі азеотропно дистилювали з толуолом. Одержану суміш розчиняли у ацетонітрилі (20 мл), додавали триетиламін (15,6 г), та суміш перемішували протягом 3 год. Ди-трет-бутил бікарбонат (33,6 г) та 4-диметилaмінoпіридин (3,76 г) додавали при кімнатній температурі та суміш перемішували протягом години. Реакційну суміш концентрували при пониженому тиску, та залишок розчиняли у етилацетаті, та промивали 1 моль/л хлорводневої кислоти. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим водним розчином гідрокарбонату натрію, водою та насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=2:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 32,0 г, 80%). 1 H-ЯМР (CDCl3) δ: 1,55 (9H, с), 2,48 (3H, с), 3,81-3,91 (1H, м), 4,09-4,18 (1H, м), 4,94-5,06 (1H, м), 7,40 (2H, д, J=8,1Гц), 7,83 (2H, д, J=8,1Гц). Порівняльний Приклад 4 4,4-Дифтор-5-(2-фторпіридин-3-іл)-3,4-дигідро-2H-пірол-3-іл 4-метилбензолсульфонат Дo розчину дiізопропіламіну (8,76 г) у тетрагідрофурані (230 мл) додавали 1,6 моль/л розчину н-бутиллітію гексан (51 мл) при -78 °C, та суміш перемішували протягом години. Краплями додавали 2-фторпіридин (11,2 г), та суміш перемішували протягом 2 год. До отриманої світло-жовтої суспензії повільно краплями додавали розчин трет-бутил 3,3-дифтор-4{[(4-метилфеніл)сульфоніл]окси}-2-oксoпіролідин-1-карбоксилату (22,6 г) у тетрагідрофурані (50 мл), та суміш перемішували протягом години. Воду додавали до реакційної суміші, та суміш нагрівали до кімнатної температури та концентрували при пониженому тиску. Залишок розводили етилацетатом, та промивали водою. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Одержану суміш розчиняли у дихлорметані (30 мл), трифтороцтову кислоту (100 мл) додавали краплями охолоджуючи, та суміш перемішували протягом 4 годин доки суміш нагрівалась до кімнатної 22 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 температури. Реакційну суміш концентрували при пониженому тиску, розводили етилацетатом, та насичений водний розчин гідрокарбонату натрію додавали до нейтрального рН суміші. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над сульфатом магнію, та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→3:1) одержуючи сполуку у вигляді безбарвної твердої речовини (вихід 10,9 г, 51%). 1 H-ЯМР (CDCl3) δ: 2,48 (3H, с), 4,17-4,28 (1H, м), 4,42-4,54 (1H, м), 5,06-5,13 (1H, м), 7,31 (1H, ддд, J=7,6, 4,9, 1,9 Гц), 7,39 (2H, д, J=7,9 Гц), 7,85 (2H, д, J=8,3 Гц), 8,22-8,31 (1H, м), 8,34-8,39 (1H, м). Порівняльний Приклад 5 2-фтор-3-(3-фтор-1H-пірол-2-іл)піридин Дo розчину 4,4-дифтор-5-(2-фторпіридин-3-іл)-3,4-дигідро-2H-пірол-3-іл 4метилбензолсульфонату (18,0 г) у тетрагідрофурані (180 мл) додавали боргідрид натрію (3,68 г) охолоджуючи, після цього додавали метанол (90 мл), та суміш перемішували протягом 3 год. Реакційну суміш концентрували при пониженому тиску, та залишок розводили етилацетатом та промивали водою. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску одержуючи 4,4-дифтор-5-(2фторпіридин-3-іл)піролідин-3-іл 4-метилбензолсульфонат. До суспензії гідриду натрію (9,74 г) у тетрагідрофурані (100 мл) краплями додавали розчин 4,4-дифтор-5-(2-фторпіридин-3іл)піролідин-3-іл 4-метилбензолсульфонату у тетрагідрофурані (100 мл) охолоджуючи, 15краун-5 (32,2 г) додавали, та суміш перемішували протягом 3 год. Насичений водний розчин хлориду амонію додавали до реакційної суміші та концентрували при пониженому тиску. Залишок розводили етилацетатом, та промивали 1 моль/л хлорводневої кислоти. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим водним розчином гідрокарбонату натрію, водою та насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→3:1) одержуючи сполуку у вигляді безбарвної твердої речовини (вихід 6,35 г, 72%). 1 H-ЯМР (CDCl3) δ: 6,10 (1H, т, J=2,9 Гц), 6,69 (1H, дт, J=4,6, 3,4Гц), 7,20-7,30 (1H, м), 8,00 (1H, дт, J=4,7,1,7 Гц), 8,25 (1H, ддд, J=10,3, 7,8, 1,9 Гц), 8,69 (1H, ш). Порівняльний Приклад 6 2-фтор-3-{3-фтор-1-[тріс(1-метилетил)силіл]-1H-пірол-2-іл}піридин До суспензії гідриду натрію (3,32 г) у тетрагідрофурані (70 мл) додавали розчин 2-фтор-3-(3фтор-1H-пірол-2-іл)піридину (5,98 г) у тетрагідрофурані (30 мл) охолоджуючи та суміш перемішували протягом 30 хв. Додавали 15-краун-5 (18,3 г) та тріс(1-метилетил)силіл трифторметансульфонату (25,4 г), та суміш перемішували протягом години. Розчинник випаровували до половини об’єму при пониженому тиску, додавали воду, та суміш екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали основною колонковою хроматографією на силікагелі (елюент: гексан→гексан-етилацетат=19:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 10,9 г, 98%). 1 H-ЯМР (CDCl3) δ: 1,04 (18H, д, J=7,0 Гц), 1,09-1,19 (3H, м), 6,17 (1H, дд, J=3,2,1,5 Гц), 6,70 (1H, дд, J=4,8, 3,3 Гц), 7,21 (1H, ддд, J=7,3, 4,9, 1,7 Гц), 7,78 (1H, ддд, J=9,3, 7,3, 2,1Гц). Порівняльний Приклад 7 4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-карбальдегід Дo розчину N,N-диметилформаміду (717 мг) у дихлорметані (20 мл) додавали оксаліл хлорид (1,13 г) охолоджуючи в атмосфері аргону, та суміш перемішували протягом 10 хв. До отриманої суспензії додавали розчин 2-фтор-3-{3-фтор-1-[тріс(1-метилетил)силіл]-1H-пірол-2іл}піридину (1,50 г) у дихлорметані (5 мл) та суміш перемішували нагріваючи із зворотнім холодильником протягом 10 год. Реакційну суміш охолоджували льодом, додавали 1 моль/л водного розчину гідроксиду натрію (30 мл) та суміш перемішували протягом 15 хв. Розчинник випаровували до половини об’єму при пониженому тиску та залишок розділяли шляхом додавання етилацетату. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом натрію та концентрували при пониженому тиску. Залишок твердої речовини промивали дiізопропіловим етером (30 мл) та фільтрували відсмоктуванням одержуючи сполуку у вигляді безбарвної твердої речовини (вихід 726 мг, 78%). 23 UA 105185 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 H-ЯМР (CDCl3) δ: 7,29-7,40 (2H, м), 8,11 (1H, дт,J=4,8, 1,6 Гц), 8,29 (1H, ддд, J=10,0,7,9,1,9 Гц), 9,22 (1H,ш), 9,90 (1H,с). Порівняльний Приклад 8 трет-бутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат Дo розчину 4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-карбальдегіду (261 мг) у тетрагідрофурані (1 мл)-метанол (2 мл) додавали 40% розчин метиламін метанолу (4 мл) при кімнатній температурі, та суміш перемішували протягом 20 хв. Боргідрид натрію (142 мг) додавали до реакційної суміші, та суміш перемішували протягом години. Реакційну суміш концентрували при пониженому тиску, додавали воду (4 мл) та етилацетат (4 мл). Ди-третбутил бікарбонат (410 мг) додавали до одержаної суміші при кімнатній температурі, та суміш перемішували протягом години. Реакційну суміш розділяли між етилацетатом та водним шаром, та відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом натрію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→3:1) одержуючи сполуку у вигляді безбарвної твердої речовини (вихід 347 мг, 86%). 1 H-ЯМР (CDCl3) δ: 1,49 (9H,с), 2,88 (3H,с), 4,31 (2H,с), 6,46-6,94 (1H,м), 7,15-7,32 (1H,м), 8,00 (1H,дт,J=4,7,1,7 Гц), 8,23 (1H,ддд,J=10,2,7,9,1,9 Гц), 8,66 (1H,ш). Порівняльний Приклад 9 2-(бензилсульфаніл)-3-метилпіридин До суспензії гідриду натрію (60% у олії, 1,44 г) у тетрагідрофурані (45 мл) додавали фенілметантіол (465 мг) при кімнатній температурі та суміш перемішували протягом 15 хв. 2Бром-3-метилпіридин (2,0 г) додавали до реакційної суміші, та суміш перемішували при 60 °C протягом 1,5 год. Реакційну суміш розводили водою, та концентрували при пониженому тиску. Залишок водного шару двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан→гексан-етилацетат=97:3) одержуючи сполуку у вигляді сірої олії (вихід 1,79 г, 72%). 1 H-ЯМР (CDCl3) δ: 2,23 (3H,с),4,49 (2H,с), 6,93 (1H,дд,J=7,6,4,9 Гц), 7,19-7,35 (5H,м), 7,397,48 (1H,м), 8,32 (1H,дд,J=4,9,1,1Гц). Порівняльний Приклад 10 3-Метилпіридин-2-сульфонілхлорид Дo розчину 2-(бензилсульфаніл)-3-метилпіридин (1,79 г) у оцтовій кислоті (16 мл)-воді (8 мл) додавали N-хлорсукцинімід (3,33 г) при кімнатній температурі, та суміш перемішували протягом 2 год. Реакційну суміш концентрували при пониженому тиску, насичений водний розчин гідрокарбонату натрію додавали та суміш двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→3:2) одержуючи сполуку у вигляді неочищеної блідно-жовтої олії (вихід 153 мг). 1 H-ЯМР (CDCl3) δ: 2,78 (3H,с), 7,57 (1H,дд,J=7,9,4,5 Гц), 7,82 (1H,ддд,J=7,7,1,5,0,8 Гц), 8,61 (1H,дд,J=4,5,1,1Гц). Порівняльний Приклад 11 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(3-метилпіридин-2-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 20 мг) у тетрагідрофурані (2 мл) додавали розчин трет-бутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамату (161 мг), 15краун-5 (110 мг), неочищений 3-метилпіридин-2-сульфонілхлорид (153 мг) у тетрагідрофурані (1,5 мл) при кімнатній температурі, та суміш перемішували при кімнатній температурі протягом 72 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→11:9) одержуючи сполуку у вигляді безбарвної олії (вихід 113 мг, 47%). 1 H-ЯМР (CDCl3) δ: 1,47 (9H,с), 2,43 (3H,с), 2,90 (3H,с), 4,32 (2H,ш), 7,20 (1H,ддд,J=7,4,5,0,1,7 Гц), 7,29 (1H,д,J=5,7 Гц), 7,36 (1H,дд,J=7,8,4,6 Гц), 7,61 (1H,дд,J=7,8,0,8 Гц), 7,76-7,85 (1H,м), 8,19 (1H,ддд,J=4,9,2,0,1,0 Гц), 8,29 (1H,дд,J=4,5,0,9 Гц). Порівняльний Приклад 12 24 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 2-(бензилсульфаніл)-4-метилпіридин До суспензії гідриду натрію (60% у олії, 512 мг) у тетрагідрофурані (45 мл) додавали фенілметантіол (1,52 г) при кімнатній температурі, додавали 2-бром-4-метилпіридин (2,0 г), та суміш перемішували при 60 °C протягом 72 год. Реакційну суміш розводили водою та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан→гексан-етилацетат=24:1) одержуючи сполуку у вигляді коричневої олії (вихід 1,40 г, 56%). 1 H-ЯМР (CDCl3) δ: 2,26 (3H,с), 4,43 (2H,с), 6,82 (1H,д,J=5,1Гц), 6,99 (1H,с), 7,17-7,32 (3H,м), 7,35-7,44 (2H,м), 8,31 (1H,д,J=5,1Гц). Порівняльний Приклад 13 4-Метилпіридин-2-сульфонілфторид Дo розчину 2-(бензилсульфаніл)-4-метилпіридин (1,40 г) у оцтовій кислоті (10 мл)-воді (5 мл) додавали N-хлорсукцинімід (3,48 г) охолоджуючи, та суміш поступово нагрівали до кімнатної температури та перемішували протягом 4 годин. Фторид калію (379 мг) додавали при кімнатній температурі та суміш перемішували протягом 18 год. Реакційну суміш концентрували при пониженому тиску, розводили етилацетатом та промивали насиченим водним розчином гідрокарбонату натрію. Відділений водний шар екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=4:1→1:1) одержуючи сполуку у вигляді неочищеної блідно-жовтої олії (вихід 343 мг, 30%). 1 H-ЯМР (CDCl3) δ: 2,54 (3H,с), 7,50 (1H,дт,J=4,9,0,7 Гц), 7,95 (1H,д,J=0,8 Гц), 8,69 (1H,д,J=4,9 Гц). Порівняльний Приклад 14 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-2-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії (3 мл) гідриду натрію (60% у олії, 60 мг) у тетрагідрофурані додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (323 мг), 15-краун-5 (330 мг) та 4-метилпіридин-2-сульфоніл фторид (343 мг) при кімнатній температурі, та суміш перемішували при кімнатній температурі протягом 41 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=4:1→1:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 333 мг, 70%). 1 H-ЯМР (CDCl3) δ: 1,47 (9H,с), 2,38 (3H,с), 2,86 (3H,с), 4,27 (2H,ш), 7,27-7,34 (3H,м), 7,36 (1H,с), 7,87 (1H,ддд,J=9,2,7,5,1,9 Гц), 8,26 (1H,д,J=3,8 Гц), 8,45 (1H,д,J=4,9 Гц). Порівняльний Приклад 15 2-(бензилсульфаніл)-5-фторпіридин До суспензії гідриду натрію (60% у олії, 440 мг) у тетрагідрофурані (40 мл) додавали фенілметантіол (1,37 г) при кімнатній температурі, 2-бром-5-фторпіридин (1,76 г) додавали до реакційної суміші, та суміш перемішували при 60 °C протягом 5 год. Реакційну суміш розводили водою та концентрували при пониженому тиску. Залишок водного шару двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан→гексан-етилацетат=97:3) одержуючи сполуку у вигляді неочищеної коричневої олії (вихід 244 мг). Порівняльний Приклад 16 5-Фторпіридин-2-сульфонілфторид Дo розчину неочищеного 2-(бензилсульфаніл)-5-фторпіридину (244 мг) у оцтовій кислоті (3 мл)-воді (1,5 мл) додавали N-хлорсукцинімід (594 мг) охолоджуючи, та суміш поступово нагрівали до кімнатної температури та перемішували протягом 2 год. Фторид калію (65 мг) додавали при кімнатній температурі та суміш перемішували протягом години. Реакційну суміш концентрували при пониженому тиску, розводили водою та суміш екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової 25 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→3:1) одержуючи сполуку у вигляді неочищеної безбарвної олії (вихід 69 мг, 35%). 1 H-ЯМР (CDCl3) δ: 7,75 (1H,ддд,J=8,7,7,4,2,7 Гц), 8,20 (1H,дд,J=8.8,4,1Гц), 8,66 (1H,д,J=2,8 Гц). Порівняльний Приклад 17 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-2-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 40 мг) у тетрагідрофурані (2,5 мл) додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (162 мг), 15-краун-5 (220 мг) та 5-фторпіридин-2-сульфоніл фторид (120 мг) при кімнатній температурі, та суміш перемішували при кімнатній температурі протягом 28 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→7:3) одержуючи сполуку у вигляді світло-жовтої олії (вихід 69 мг, 29%). 1 H-ЯМР (CDCl3) δ: 1,48 (9H,с), 2,88 (3H,с), 4,27 (2H,ш), 7,24-7,34 (2H,м), 7,52 (1H,ддд,J=8,7,7,5,2,8 Гц), 7,68 (1H,дд,J=8,7,4,1Гц), 7,85 (1H,ддд,J=9,2,7,4,2,0 Гц), 8,27 (1H,ддд,J=4,8,1,8,0,9 Гц), 8,45 (1H,д,J=2,6 Гц). Порівняльний Приклад 18 2-(бензилсульфаніл)-4-метоксипіридин Дo розчину 2-хлор-4-метоксипіридин (786 мг) у толуолі (10 мл) додавали фенілметантіол (683 мг), N,N-дiізопропілетилaмін (1,56 г), тріс(дибензилінденацетон)дипаладій(0) (202 мг) та 4,5-біс(дифенілфосфіно)-9,9-диметилксантен (256 мг), та суміш перемішували при 80 °C протягом 26 год. в атмосфері аргону. Реакційну суміш фільтрували крізь силікагель та фільтрат концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан→гексан-етилацетат=19:1) одержуючи сполуку у вигляді оранжевої олії (вихід 454 мг, 38%). 1 H-ЯМР (CDCl3) δ: 3,79 (3H,с), 4,43 (2H,с), 6,57 (1H,дд,J=5,9,2,5 Гц), 6,68 (1H,д,J=2,3 Гц), 7,19-7,34 (3H,м), 7,36-7,44 (2H,м), 8,27 (1H,д,J=5,7 Гц). Порівняльний Приклад 19 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метоксипіридин-2-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат Дo розчину 2-(бензилсульфаніл)-4-метоксипіридин (453 мг) у оцтовій кислоті (4 мл)-воді (2 мл) додавали N-хлорсукцинімід (1,10 г) охолоджуючи, поступово нагрівали до кімнатної температури та суміш перемішували протягом 5 год. Реакційну суміш концентрували при пониженому тиску, розводили водою та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=3:1→1:1) одержуючи неочищений 4метоксипіридин-2-сульфонілхлорид у вигляді світло-жовтої олії. Після цього, до суспензії гідриду натрію (60% у олії, 30 мг) у тетрагідрофурані (2,5 мл) додавали трет-бутил {[4-фтор-5-(2фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (162 мг), 15-краун-5 (165 мг) та вищеодержаний розчин неочищеного 4-метоксипіридин-2-сульфонілхлориду у тетрагідрофурані (2 мл) при кімнатній температурі, та суміш перемішували протягом 18 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=17:3→1:1) одержуючи сполуку у вигляді безбарвної олії (вихід 96 мг, вихід з 2 стадій 9%). 1 H-ЯМР (CDCl3) δ: 1,47 (9H,с), 2,87 (3H,с), 3,84 (3H,с), 4,27 (2H,ш), 6,94 (1H,дд,J=5,6,2,4Гц), 7,07 (1H,д,J=2,4Гц), 7,28 (1H,дд,J=5,3,2,1Гц), 7,31 (1H,д,J=5,7 Гц), 7,87 (1H,ддд,J=9,2,7,5,1,8 Гц), 8,26 (1H,д,J=4,7 Гц), 8,39 (1H,д,J=5,7 Гц). Порівняльний Приклад 20 3-(бензилсульфаніл)-5-фторпіридин Дo розчину 3-бром-5-фторпіридин (522 мг) у толуолі (5 мл) додавали фенілметантіол (370 мг), N,N-дiізопропілетилaмін (831 мг), тріс(дибензилінденацетон)дипаладій(0) (108 мг) та 4,5біс(дифенілфосфіно)-9,9-диметилксантен (138 мг), та суміш перемішували в атмосфері аргону при 80 °C протягом 2 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином, висушували над безводним 26 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 60 сульфатом магнію, та фільтрували крізь силікагель. Фільтрат концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан→гексан-етилацетат=10:1) одержуючи сполуку у вигляді оранжевої олії (вихід 587 мг, 90%). 1 H-ЯМР (CDCl3) δ: 4,13 (2H,с), 7,23-7,33 (6H,м), 8,25-8,26 (1H,м), 8,30-8,31 (1H,м). Порівняльний Приклад 21 5-Фторпіридин-3-сульфонілхлорид Дo розчину 3-(бензилсульфаніл)-5-фторпіридин (573 мг) у оцтовій кислоті (7,5 мл)-воді (2,5 мл) додавали N-хлорсукцинімід (1,40 г) при кімнатній температурі та суміш перемішували протягом 1,5 год. Реакційну суміш концентрували при пониженому тиску, розводили водою та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок азеотропно дистилювали з толуолом та очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→7:3) одержуючи сполуку у вигляді безбарвної олії (вихід 376 мг, 74%). 1 H-ЯМР (CDCl3) δ: 8,04 (1H,ддд,J=7,0,2,7,2,0 Гц), 8.85 (1H,д,J=2,6 Гц), 9,10 (1H,дд,J=1,1,0,8 Гц). Порівняльний Приклад 22 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-фторпіридин-3-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 20 мг) у тетрагідрофурані (2 мл) додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (162 мг), 15-краун-5 (132 мг) та розчин 5-фторпіридин-3-сульфонілхлориду (127 мг) у тетрагідрофурані (1 мл) при кімнатній температурі, та суміш перемішували протягом години. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали основною колонковою хроматографією на силікагелі (елюент: гексан-етилацетат=9:1→7:3) одержуючи сполуку у вигляді безбарвної олії (вихід 224 мг, 93%). 1 H-ЯМР (CDCl3) δ: 1,48 (9H,с), 2,88 (3H,с), 4,27 (2H,с), 7,28-7,36 (2H,м), 7,38 (1H,д,J=7,2Гц), 7,73-7,86 (1H,м), 8,34 (1H,д,J=4,2Гц), 8,46 (1H,с), 8,69 (1H,д,J=2,7 Гц). Порівняльний Приклад 23 3-(бензилсульфаніл)-4-метилпіридин Дo розчину 3-бром-4-метилпіридину (1,0 г) у толуолі (12 мл) додавали фенілметантіол (794 мг), N,N-дiізопропілетилaмін (1,65 г), тріс(дибензилінденацетон)дипаладій(0) (213 мг) та 4,5біс(дифенілфосфіно)-9,9-диметилксантен (269 мг), та суміш перемішували в атмосфері аргону при 80 °C протягом 1,5 год. Реакційну суміш фільтрували крізь силікагель, та фільтрат концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=19:1→3:1→1:1) одержуючи сполуку у вигляді жовтої олії (вихід 740 мг, 59%). 1 H-ЯМР (CDCl3) δ: 2,27 (3H,с), 4,07 (2H,с), 7,06 (1H,д,J=4,9 Гц), 7,14-7,35 (5H,м), 8,30 (1H,д,J=5,3 Гц), 8,45 (1H,с). Порівняльний Приклад 24 4-Метилпіридин-3-сульфонілхлорид Дo розчину 3-(бензилсульфаніл)-4-метилпіридин (740 мг) у оцтовій кислоті (9 мл)-воді (3 мл) додавали N-хлорсукцинімід (1,84 г) при кімнатній температурі, та суміш перемішували протягом 2 год. Реакційну суміш концентрували при пониженому тиску, розводили водою та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим водним розчином гідрокарбонату натрію та насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок азеотропно дистилювали з толуолом та очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексанетилацетат=9:1→3:1) одержуючи сполуку у вигляді неочищеної безбарвної олії (вихід 676 мг). 1 H-ЯМР (CDCl3) δ: 2,82 (3H,с), 7,34-7,44 (1H,м), 8,77 (1H,д,J=4,9 Гц), 9,19 (1H,с). Порівняльний Приклад 25 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(4-метилпіридин-3-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 24 мг) у тетрагідрофурані (2 мл) додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (161 мг), 15-краун-5 (132 мг) та розчин неочищеного 4-метилпіридин-3-сульфонілхлориду (125 мг) у тетрагідрофурані (1 мл) при кімнатній температурі, та суміш перемішували протягом години. 27 UA 105185 C2 5 10 15 20 25 30 35 40 45 50 55 Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексанетилацетат=17:3→1:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 127 мг, 53%). 1 H-ЯМР (CDCl3) δ: 1,49 (9H,с), 2,36 (3H,с), 2,92 (3H,с), 4,32 (2H,с), 7,19 (1H,д,J=5,1Гц), 7,237,31 (1H,м), 7,41 (1H,ш), 7,82 (1H,дт,J=8,3,1,9 Гц), 8,18-8,26 (2H,м), 8,58 (1H,д,J=5,1Гц). Порівняльний Приклад 26 3-(бензилсульфаніл)-5-метилпіридин Дo розчину 3-бром-5-метилпіридин (888 мг) у толуолі (10 мл) додавали фенілметантіол (705 мг), N,N-дiізопропілетилaмін (1,47 г), тріс(дибензилінденацетон)дипаладій(0) (189 мг) та 4,5біс(дифенілфосфіно)-9,9-диметилксантен (239 мг), та суміш перемішували в атмосфері аргону при 80 °C протягом 1,5 год. Реакційну суміш фільтрували крізь силікагель, та фільтрат концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=19:1→17:3) одержуючи сполуку у вигляді жовтої олії (вихід 1,06 г, 95%). 1 H-ЯМР (CDCl3) δ: 2,26 (3H,д,J=0,8 Гц), 4,09 (2H,с), 7,20-7,33 (5H,м), 7,37 (1H,дт,J=2,1,0,8 Гц), 8,25 (1H,д,J=1,3 Гц), 8,33 (1H,д,J=2,1Гц). Порівняльний Приклад 27 5-Метилпіридин-3-сульфонілхлорид Дo розчину 3-(бензилсульфаніл)-5-метилпіридин (1,06 г) у оцтовій кислоті (15 мл)-воді (5 мл) додавали N-хлорсукцинімід (2,63 г) при кімнатній температурі та суміш перемішували протягом 2 год. Реакційну суміш концентрували при пониженому тиску, розводили водою та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексанетилацетат=19:1→17:3) одержуючи сполуку у вигляді безбарвної олії (вихід 700 мг, 74%). 1 H-ЯМР (CDCl3) δ: 2,52 (3H,с), 7,96-8,22 (1H,м), 8,78 (1H,д,J=1,5 Гц), 9,06 (1H,д,J=2,3 Гц). Порівняльний Приклад 28 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(5-метилпіридин-3-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 24 мг) у тетрагідрофурані (3 мл) додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (323 мг), 15-краун-5 (264 мг) та розчин 4-метилпіридин-3-сульфонілхлорид (249 мг) у тетрагідрофурані (2 мл) при кімнатній температурі, та суміш перемішували протягом години. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=9:1→1:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 370 мг, 77%). 1 H-ЯМР (CDCl3) δ: 1,48 (9H,с), 2,35 (3H,д,J=0.4Гц), 2,86 (3H,с), 4,26 (2H,ш), 7,26 (1H,с), 7,32 (1H,ддд,J=7,3,5,2,1,5 Гц), 7,38 (1H,ш), 7,76-7,90 (1H,м), 8,25-8,34 (1H,м), 8,46 (1H,д,J=2,1Гц), 8,63 (1H,д,J=1,5 Гц). Порівняльний Приклад 29 трет-бутил ({4-фтор-5-(2-фторпіридин-3-іл)-1-[(6-метилпіридин-3-іл)сульфоніл]-1H-пірол-3іл}метил)метилкарбамат До суспензії гідриду натрію (60% у олії, 31 мг) у тетрагідрофурані (3 мл) додавали третбутил {[4-фтор-5-(2-фторпіридин-3-іл)-1H-пірол-3-іл]метил}метилкарбамат (100 мг), 15-краун-5 (170 мг), 6-метилпіридин-3-сульфонілхлорид гідрохлорид (91 мг) при кімнатній температурі, та суміш перемішували протягом 1,5 год. Реакційну суміш розводили водою та екстрагували етилацетатом. Відділений водний шар знову екстрагували етилацетатом. Об’єднані органічні шари промивали насиченим сольовим розчином, висушували над безводним сульфатом магнію та концентрували при пониженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент: гексан-етилацетат=17:3→1:1) одержуючи сполуку у вигляді світло-жовтої олії (вихід 123 мг, 83%). 1 H-ЯМР (CDCl3) δ: 1,48 (9H,с), 2,62 (3H,с), 2,86 (3H,с), 4,26 (2H,с), 7,20 (1H,д,J=8,0 Гц), 7,277,34 (2H,м), 7,51 (1H,дд,J=8,0,1,9 Гц), 7,76-7,86 (1H,м), 8,27-8,36 (1H,м), 8,50 (1H,д,J=2,3 Гц). Порівняльний Приклад 30 3-(бензилсульфаніл)-2-метилпіридин 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrrole compounds
Автори англійськоюNishida Haruyuki, Arikawa, Yasuyoshi, Fujimori, Ikuo
Автори російськоюНишида Харуюки
МПК / Мітки
МПК: C07D 401/14, A61K 31/444
Мітки: піроли
Код посилання
<a href="https://ua.patents.su/45-105185-piroli.html" target="_blank" rel="follow" title="База патентів України">Піроли</a>
Попередній патент: Система підведення матеріалу для запису, друкарська плата, структура і чорнильний картридж для пристрою витрачання матеріалу для запису
Наступний патент: Поліпшення росту біфідобактерій у кисломолочних продуктах
Випадковий патент: Регулятор швидкості опускання вантажу вантажопідйомної машини