Похідні хіназоліну, спосіб їх одержання (варіанти), фармацевтична композиція та спосіб одержання антиангіогенного ефекту та/або ефекту зниження судинної проникності
Номер патенту: 64704
Опубліковано: 15.03.2004
Автори: Томас Ендрю Пітер, Еннекен Лоран Франсуа Андре, Ломанн Жан-Жак Марсель
Формула / Реферат
1. Производные хиназолина формулы I:
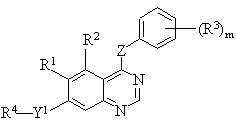 , (I)
, (I)
где
Y1 представляет -О-, -S-, -NR5 СО-, где R5 представляет водород;
R1 представляет водород или С1-3алкокси;
R2 представляет водород;
m представляет целое число от 1 до 5;
R3 представляет гидрокси, галоген, С1-3алкил, С1-3алкокси, С1-3алканоилокси, трифторметил или циано;
R4 выбран из одной из следующих групп:
1) X1, который представляет пиридоновую группу, фенильную группу или 5- или 6-членную ароматическую гетероциклическую группу с 1-3 гетероатомами, выбранными из О, N и S, причем пиридоновая, фенильная или гетероциклическая группа может нести на себе 1-2 заместителя, выбранных из галогена, амино, С1-4алкила, С1-4алкокси, С1-4гидроксиалкила, С1-4аминоалкила, С1-4алкиламино, С1-4гидроксиалкокси, карбокси, циано, -CONR12R13 и -NR14COR15 (где R12, R13, R14 и R15, которые могут быть одинаковыми или разными, представляют каждый водород, С1-4алкил или С1-3алкоксиС2-3алкил);
2) С1-5алкилХ1, где X1 - такой, как определенный выше;
3) С2-5алкенилХ1, где X1 - такой, как определенный выше;
4) С1-5алкилY2Х1, где Y2 представляет -О-, -S-, -SO-, -SO2-, -NR16CO-, -NR19SO2 - или -NR20- (где R16, R19 и R20 независимо представляют каждый водород, С1-3алкил или С1-3алкоксиС2-3алкил и X1 - такой, как определенный выше); и
5) С1-3алкилY5С1-3алкилХ1 (где Y5 представляет -О-, -NR31CO-, -NR34SO2- или -NR35-, где R31, R34 и R35 независимо представляют каждый водород, С1-3алкил или С1-3алкоксиС2-3алкил и X1 - такой, как определенный выше);
Z представляет -NH- или -О-;
при условии, что когда R4 выбран из одной из описанных выше групп 1), 2) и 4) и X1 представляет незамещенный фенил или замещенный фенил с 1-2 заместителями, выбранными из галогена, С1-4алкила и С1-4алкокси, то m представляет целое число от 3 до 5 и/или Z представляет -О-; и их соли.
2. Производные хиназолина по п. 1, где R1 представляет метокси.
3. Производные хиназолина по п. 1 или п. 2, где R2 представляет водород.
4. Производные хиназолина по любому из предшествующих пунктов, где фенильная группа, несущая (R3)m, представляет собой группу формулы:
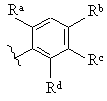 , (IIа)
, (IIа)
где
Ra представляет водород, метил, фтор или хлор;
Rb представляет водород, метил, метокси, бром, фтор или хлор;
Rc представляет водород или гидрокси; и
Rd представляет водород, фтор или хлор.
5. Производные хиназолина по любому из предшествующих пунктов, где Z представляет NH.
6. Производные хиназолина по любому из предшествующих пунктов, где Y1 представляет -О-.
7. Производные хиназолина по любому из предшествующих пунктов, где фрагмент X1 в группе R4 представляет пиридоновую группу или 5- или 6-членную ароматическую гетероциклическую группу с 1-3 гетероатомами, выбранными из О, N и S, причем пиридоновая или гетероциклическая группа при необходимости может быть замещена так, как определено в пункте 1.
8. Производные хиназолина по п. 7, где фрагмент Х1 представляет пиридоновую, пиридильную, имидазолильную, тиазолильную, тиенильную, триазолильную или пиридазинильную группу, которая при необходимости может быть замещена так, как определено в пункте 1.
9. Производные хиназолина по любому из предшествующих пунктов, где R4 представляет группу X1-Y6-(СН2)n-, где Y6 представляет непосредственную связь, -О-, -S- или -NH-, n представляет целое число от 1 до 3 и Х1 - такой, как определено в любом из пп. 1, 7 и 8.
10. Производное хиназолина по п. 1, выбранное из:
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридилокси)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-[2-(4-оксо-1,4-дигидро-1-пиридил)этокси]хиназолина;
4-(4-хлор-2-фторанилино)-7-(2-(имидазол-1-ил)этокси)-6-метоксихиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(4-пиридил)пропокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-((4-пиридил)метокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(2-метилимидазол-1-ил)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-илтио)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1,2,4-триазол-1-ил)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-(4-пиридил)амино)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-ил)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-7-((2-циано-4-пиридил)метокси)-6-метоксихиназолина;
и их солей.
11. Производное хиназолина по п. 1, выбранное из:
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилметокси)хиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(2-пиридилметокси)хиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(1-метилимидазол-2-илметокси)хиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(2-метилтиазол-4-илметокси)хиназолина;
7-(2-ацетамидотиазол-4-илметокси)-4-(3-гидрокси-4-метиланилино)-6-метоксихиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилпропокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридил-)пропокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилметокси)хиназолина;
7-бензилокси-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
7-бензилокси-4-(2-фтор-5-гидрокси-4-метилфенокси)-6-метоксихиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-((2-метилтиазол-4-ил)метокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-7-(4-пиридилметокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-((1-метилимидазол-2-ил)метокси)хиназолина;
7-((2-ацетамидотиазол-4-ил)метокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
7-бензилокси-4-(4-хлор-2-фтор-5-гидроксианилино)-6-метоксихиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-(3-(4-пиридил)пропокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-7-(2-имидазол-1-ил)-этокси)-6-метоксихиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-7-(2-имидазол-1-ил)этокси)-6-метоксихиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(3-тиенилметокси)хиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-((1-метилбензимидазол-2-ил)метокси)хиназолина;
7-((2-хлор-6-метил-4-пиридил)метокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
4-(4-хлор-2-фторфенокси)-6-метокси-7-((4-пиридил)метокси)хиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((4-пиридил)метокси)хиназолина;
7-((2-хлор-4-пиридил)метокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
7-(3,4-дифторбензилокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((1-метилимидазол-2-ил)метокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-7-((1-метилимидазолил)метокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-7-(2-(1,2,4-триазол-1-ил)этокси)хиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((3-тиенил)метокси)хиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолина;
4-(2-фтор-5-гидрокси-4-метиланилино)-7-((4-пиридил)карбоксамидо)хиназолина;
и их солей.
12. Производное хиназолина по п. 1, выбранное из:
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(3-пиридилметокси)хиназолина;
4-(3-гидрокси-4-метиланилино)-6-метокси-7-(3-тиенилметокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(2-пиридилокси)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-[N-метил-N-(4-пиридил)]аминоэтокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-[2-(2-оксо-1,2-дигидро-1-пиридил)этокси]хиназолина;
7-(4-цианобензилокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(2-метилимидазол-1-ил)пропокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-((2-метил-4-пиридил)метокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(2-оксо-1,2-дигидро-1-пиридил)пропокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(1-метилимидазол-2-илтио)пропокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(4-пиридилокси)пропокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридилтио)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(3-пиридилокси)этокси)хиназолина;
7-бензилокси-4-(2-фтор-5-гидрокси-4-метиланилино)хиназолина;
7-бензилокси-4-(4-хлор-2-фтор-5-гидроксианилино)хиназолина;
4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((2-метилтиазол-4-ил)метокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-((3-тиенил)метокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-метил-N-(пиридазин-4-ил)амино)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-метил-N-(6-метилпиримидин-4-ил)амино)этокси)хиназолина;
4-(4-хлор-2-фторанилино)-7-(2-(3,5-диметил[1,2,4]триазол-4-ил)этокси)-6-метоксихиназолина;
4-(4-хлор-2-фторанилино)-7-(2-(2,4-диметилимидазол-1-ил)-этокси)-6-метоксихиназолина;
4-(4-хлор-2-фторанилино)-7-(2-(2,5-диметилимидазол-1-ил)-этокси)-6-метоксихиназолина;
4-(3-гидроксианилино)-7-(2-(имидазол-1-ил)этокси)-6-метоксихиназолина;
4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1,2,4-триазол-4-ил)этокси)хиназолина;
4-(4-бром-2-фторанилино)-7-(2-([1,2,4]-триазол-1-ил)этокси)-6-метоксихиназолина; и их солей.
13. Производные хиназолина по любому из предшествующих пунктов в форме фармацевтически приемлемой соли.
14. Способ получения производных хиназолина формулы I или их солей по п. 1, который включает взаимодействие соединения формулы III:
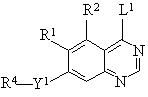 , (III)
, (III)
где R1, R2, R4 и Y1 такие, как определены в п. 1, и L1 представляет уходящую группу, с соединением формулы IV:
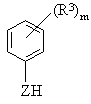 , (ІV)
, (ІV)
где Z, R3 и m - такие, как определены в п. 1, с получением соединений формулы I и их солей, и, в случае необходимости, когда требуется фармацевтически приемлемая соль хиназолинового производного формулы I, осуществляют взаимодействие полученного соединения с кислотой или основанием с получением требуемой фармацевтически приемлемой соли.
15. Способ получения производных хиназолина формулы I или их солей по п. 1, в которых группа формулы Iib:
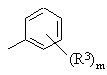 , (IIb)
, (IIb)
где R3 и m - такие, как определены в п. 1, представляет собой фенильную группу, несущую одну или несколько гидроксигрупп, который включает снятие защитной группы c соединения формулы V:
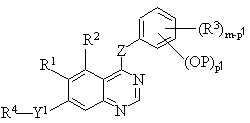 , (V)
, (V)
где Y1, m, R1, R2, R3, R4 и Z - такие, как определены в п. 1, Р представляет фенольную гидроксизащитную группу и р1 представляет целое число от 1 до 5, равное числу защищенных гидроксигрупп, причем разность m-р1 равна числу заместителей R3, которые не являются защищенной гидроксигруппой, и, в случае необходимости, когда требуется фармацевтически приемлемая соль хиназолинового производного формулы I, осуществляют взаимодействие полученного соединения с кислотой или основанием с получением требуемой фармацевтически приемлемой соли.
16. Способ получения производных хиназолина формулы I или их солей по п. 1, в которых заместитель Y1 представляет -О- или -S, который включает взаимодействие соединения формулы VI:
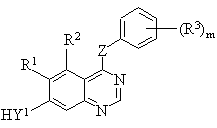 , (VI)
, (VI)
где m, R1, R2, R3 и Z - такие, как определены в п. 1 и Y1 имеет указанные выше значения, с соединением формулы VII:
R4 - L1 , (VII)
где R4 - такой, как определен в п. 1, и L1 - уходящая группа, и, в случае необходимости, когда требуется фармацевтически приемлемая соль хиназолинового производного формулы I, осуществляют взаимодействие полученного соединения с кислотой или основанием с получением требуемой фармацевтически приемлемой соли.
17. Способ получения производных хиназолина формулы I или их солей по п. 1, включающий взаимодействие соединения формулы VIII:
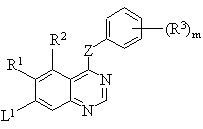 , (VIII)
, (VIII)
где R1, R2, R3, Z и m - такие, как определены в п. 1, и L1 уходящая группа, с соединением формулы IX:
R4 - Y1 - H (IX),
где R4 и Y1 такие, как определены в п. 1, и, когда требуется фармацевтически приемлемая соль хиназолинового производного формулы I, осуществляют взаимодействие полученного соединения с кислотой или основанием с получением требуемой фармацевтически приемлемой соли.
18. Способ получения производных хиназолина формулы I или их солей по п. 1, в которых R4 представляет С1-5алкилХ2, где X2 выбран из следующих трех групп:
1) X1, где X1 такой, как он определен в п. 1;
2) Y7X1, где Y7 представляет -О-, -S-, -SO-, -SO2-, -NR47CO-, -NR48SO2 - или -NR49-, где R47, R48 и R49 каждый независимо представляют водород, С1-3алкил или С1-3алкоксиС2-3алкил, и X1 такой, как он определен в п. 1; и
3) Y8С1-3алкилХ1, где Y8 представляет -О-, -NR50CO-, -NR51SO2 - или -NR52-, где R50, R51 и R52 каждый независимо представляют водород, С1-3алкил или С1-3алкоксиС2-3алкил, и X1 такой, как он определен в п. 1, который включает взаимодействие соединения формулы Х:
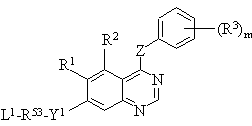 , (Х)
, (Х)
где Y1, R1, R2, R3, Z и m - такие, как они определены в п. 1, и L1 -уходящая группа, и R53 представляет С1-5алкил, с соединением формулы XI:
X2 - Н (XI),
где X2 - такой, как определен в данном пункте выше, с получением соединения формулы I, и, в случае необходимости, когда требуется фармацевтически приемлемая соль хиназолинового производного формулы 1, осуществляют взаимодействие полученного соединения с кислотой или основанием с получением требуемой фармацевтически приемлемой соли.
19. Фармацевтическая композиция, содержащая в качестве активного компонента производное хиназолина формулы I, как определено в п. 1, или его фармацевтически приемлемую соль в сочетании с фармацевтически приемлемым наполнителем или носителем.
20. Способ получения антиангиогенного эффекта и/или эффекта снижения сосудистой проницаемости у теплокровного животного, нуждающегося в таком лечении, включающий введение указанному животному эффективного количества соединения формулы I или его фармацевтически приемлемой соли по п. 1.
Текст
Настоящее изобретение относится к производным хиназолина, способам их получения, фармацевтическим композициям, содержащим их в качестве активного компонента, способам лечения болезненных состояний, связанных с ангиогенезом и/или повышенной проницаемостью кровеносных сосудов, и к их применению в производстве лекарственных средств, используемых для обеспечения антиангиогенных эффектов и/или эффектов снижения проницаемости кровеносных сосудов у теплокровных животных, таких, как человек. Нормальный ангиогенез играет важную роль в самых разных процессах, включая эмбриональное развитие, заживление раны и некоторые составляющие репродуктивной функции женщины. Нежелательный или патологический ангиогенез связывали с заболеваниями, включающими диабетическую ретинопатию, псориаз, рак, ревматоидный артрит, атерому, саркому Калоши и гемангиому (Fan et al, 1995, Trends Pharmacol. Sci. 16: 57-66; Folkman, 1995, Mature Medicine 1: 27-31). Полагают, что сосудистая проницаемость играет роль как в нормальных, так и патологических физиологических процессах (Cullinan-Bove et al, 1993, Endocrinology 133: 829-837; Senger et al, 1993, Cancer and Metastasis Reviews, 12: 303-324). Уже идентифицированы некоторые полипептиды с активностью, стимулирующей рост эндотелиальных клеток in vitro, включающие кислотные и основные факторы роста фибропластов (aFGF и bFGF) и сосудистый эндотелиальный ростовой фактор (VEGF). Вследствие ограниченной экспрессии активность VEGF, в противоположность активности ростовых факторов FGF, относительно специфична по отношению к эндотелиальным клеткам. Недавно доказано, что VEGF является важным стимулятором как нормального, так и патологического ангиогенеза (Jakeman et al, 1993, Endocrinology, 133: 848-859; Kolch et al, 1995, Breast Cancer Research and Treatment, 36: 139-155) и сосудистой проницаемости (Connolly et al, 1989, J. Biol. Chem. 264: 20017-20024). Антагонизм действия VEGF в результате секвестрации VEGF с антителом может привести к угнетению роста опухоли (Kim et al, 1993, Nature 362: 841-844). Рецепторные тирозинкиназы (RTKs) важны для передачи биохимических сигналов через плазматическую мембрану клеток. Эти трансмембранные молекулы обычно состоят из связывающего внеклеточный лиганд домена, соединенного через участок в плазматической мембране с внутриклеточным доменом тирозинкиназы. Связывание лиганда с рецептором вызывает стимуляцию активности тирозинкиназы, связанной с рецептором, что ведет к фосфорилированию тирозиновых остатков и на рецепторе, и на других вн утриклеточных молекулах. Эти изменения в фосфорилировании тирозина инициируют сигнальный каскад, ведущий к самым разным клеточным реакциям. В настоящее время идентифицировано по крайней мере девятнадцать отдельных подсемейств RTK, характеризуемых гомологией аминокислотных последовательностей. Одно из этих подсемейств на сегодняшний день составляют fms-подобный тирозинкиназный рецептор (Fit или Flt1), рецептор, содержащий домен с киназной вставкой, KDR (называемый также как Flk-1), и другой fms-подобный тирозинкиназный рецептор, Flt4. Две из этих родственных RTK (Flt и KDR), как было установлено, связывают VEGF с высоким аффинитетом (De Vries et al, 1992, Science 255: 989-991; Terman et al, 1992, Biochem. Biophys. Com. 1992, 187: 1579-1586). Связывание VEGF с указанными рецепторами, экспрессированными в гетерологичных клетках, было обусловлено изменениями в состоянии фосфорилирования тирозина в клеточных белках и потоках кальция. Соединения, которые обладают хорошей активностью против рецепторной тирозинкиназы эпидермального ростового фактора (EGF), раскрыты в европейском патенте №0566226. Настоящее изобретение основано на открытии соединений, которые неожиданно подавляют эффекты VEGF, что полезно для лечения заболеваний, связанных с ангиогенезом и/или повышенной сосудистой проницаемостью, таких, как рак, диабет, псориаз, ревматоидный артрит, саркома Капоши, гемангиома, острая и хроническая нефропатии, атерома, артериальный рестеноз, аутоиммунные заболевания, острое воспаление и глазные болезни с пролиферацией сетчаточных сосудов. Соединения по настоящему изобретению проявляют более высокую эффективность против тирозинкиназы VEGF-рецепторов, чем протиз тирозинкиназы EGF-рецепторов. Кроме того, соединения по настоящему изобретению проявляют значительно более высокую эффективность против тирозинкиназы VEGF-рецепторов, чем против тирозинкиназы рецепторов EGF или FGF R1. Таким образом, соединения по настоящему изобретению, которые уже были испытаны, обладают активностью против тирозинкиназы VEGF-рецепторов, благодаря чему их можно использовать в количестве, достаточном для ингибирования тирозинкиназы VEGFрецепторов без проявления при этом существенной активности против тирозинкиназы EGF-рецепторов или тирозинкиназы FGF R1-рецепторов. В соответствии с одним аспектом настоящего изобретения предлагаются производное хиназолина формулы I: (l) [где: Y1 представляет -О-, -S-, -CH2-, -SO-, -SO2-, -NR5CO-, -CONR6-, -SO2NR7-, -NR8SO2- или -NR9- (где R5, 6 R , R7, Ra и R9 независимо представляют каждый водород, C1-3алкил или C1-3алкокси C2-3алкил); R1 представляет водород, гидрокси, галоген, нитро, трифторметил, циано, C1-3алкил, C1-3алкокси, C11O 11 (где R10 и R11, которые могут быть одинаковыми или разными, представляют 3алкилтио или NR R каждый водород или C1-3алкил); R2 представляет водород, гидрокси, галоген, C1-3алкил, C1-3алкокси, трифторметил, циано, амино или нитро; m представляет целое число от 1 до 5; R3 представляет гидрокси, галоген C1-3алкил, C1-3алкокси, C1-3алканоилокси, трифторметил, циано, амино или нитро; R4 выбран из одной из следующи х восьми групп: 1) X1 (где X1 представляет пиридоновую гр уппу, фенильную гр уппу или 5- или 6-членную ароматическую гетероциклическую гр уппу с 1-3 гетероатомами, выбранными из О, N и S, причем пиридоновая, фенильная или гетероциклическая группа может нести на себе до 5 заместителей, выбранных из галогена, амино, C1-4алкила, C1-4алкокси, C1-4гидроксиалкила, C1-4аминоалкила, C112 13 и -NR14COR15 (где R12, R13, R14 и R15, 4алкиламино, C 1-4гидроксиалкокси, карбокси, циано, -CONR R которые могут быть одинаковыми или разными, представляют каждый водород, C1-4алкил или C1-3алкоксиC1-3алкил); 2) C 1-5алкилХ1 (где X1 - такой, как определенный выше); 3) C 2-5алкенилХ1 (где X1 - такой, как определенный выше); 4) C 2-5алкинилХ1 (где X1 - такой, как определенный выше); 5) C1-5алкилY2 Х1 (где Y2 представляет -О-, -S-, -SO-, -SO2-, -ОСО-, -NR 16CO-, -CONR17-, -SO2NR18-, 19 NR SO2- или -NR20- (где R16 , R17, R18, R19 и R20 независимо представляют каждый водород, C1-3алкил или C1-3алкоксиC2-3алкил) и X1 - такой, как определенный выше); 6) C2-5алкенилY3 Х1 (где Y3 представляет -О-, -S-, -SO-, -SO2-, -ОСО-, -NR 21CO-, -CONR22-, -SO2NR23-, 24 NR SO2- или -NR25- (где R21 , R22, R23, R24 и R25 независимо представляют каждый водород, C1-3алкил или C1-3алкоксиC2-3алкил) и X1 - такой, как определенный выше); 7) C2-5алкинилY4 Х1 (где Y4 представляет -О-, -S-, -SO-, -SO2-, -ОСО-, -NR 26CO-, -CONR27-, -SO2NR28-, 29 NR SO2- или -NR30- (где R26 , R27, R29, R29 и R30 независимо представляют каждый водород, C1-3алкил или C1-3алкоксиC2-3алкил) и X1 - такой, как определенный выше); и 8) C1-3алкилY5C1-3алкилХ1 (где Y5 представляет -О-, -S-, -SO-, -SO2-, -NR31CO-, -CONR32-, -SO2NR33-, 34 NR SO2- или -NR35- (где R31 , R32, R33, R34 и R35 независимо представляют каждый водород, C1-3алкил или C1-3алкоксиC2-3алкил) и X1 - такой, как определенный выше); Ζ представляет -ΝΗ-, -О-, -S- или -СН2-; при условии, что когда R4 выбран из одной из описанных выше групп 1), 2) и 5) и X1 представляет незамещенный фенил или замещенный фенил с 1-2 заместителями, выбранными из галогена, C1-4алкила и C1-4алкокси, то m представляет целое число от 3 до 5 и/или Ζ представляет -О-, -S- или -СН2-]; и его соли. Преимущественно Y1 представляет -О-, -S-, -СН2-, -NR5CO-, -NR8SO2- или -NR9- (где R5, R8 и R9 независимо представляют каждый водород, C1-2алкил или C1-2алкоксиэтил). Предпочтительно Y1 представляет -О-, -S-, -СН2-, -NR5CO-, -NR8SO2- или -NH- (где R5 и R8 независимо представляют каждый водород, C1-2алкил или C1-2алкоксиэтил). Более предпочтительно Y1 представляет -О-, -S-, -СН2-или -NH-, в частности -O-. В другом варианте осуществления настоящего изобретения Y1 представляет -О-, -NR5CO- или 8 NR SO2- или (где R5 и R8 независимо представляют каждый водород или C1-2алкил). В еще одном варианте осуществления настоящего изобретения Y1 представляет -NHCO-. В одном из вариантов осуществления настоящего изобретения R1 представляет водород, гидрокси, C1алкил, C1-3алкокси, C1-3алкилтио или NR1OR11 (где R10 и R11 - такие, как определенные выше). Однако 3 удобно, когда R1 представляет водород, гидрокси, циано, нитро, трифторметил, C1-3алкил, C1-3алкокси или амино. R1 преимущественно представляет водород, гидрокси, C1-3алкил, C1-3алкокси или амино. R1 представляет предпочтительно водород, гидрокси, метил, этил, метокси или этокси, более предпочтительно водород, гидрокси, метил или метокси, в частности водород, метил или метокси, но особенно метокси. В другом варианте осуществления настоящего изобретения R1 представляет водород, гидрокси, циано, нитро, трифторметил, метил, этил, метокси или этокси. R2 представляет преимущественно водород, галоген, амино или нитро. Предпочтительно R2 представляет водород, хлор или нитро, но особенно водород. В одном из вариантов осуществления настоящего изобретения R3 представляет гидрокси, галоген, C1алкил, C1-3алкокси, трифторметил, циано, амино или нитро. 3 Выгодно, когда в другом варианте осуществления настоящего изобретения один заместитель R3 представляет мета-гидрокси, а другой или другие выбраны каждый из галогена и метила. В другом варианте осуществления настоящего изобретения фенильная группа, несущая (R3)m, представляет собой группу формулы IIа: (IIа) (где: Ra представляет водород, метил, фтор или хлор; Rb представляет водород, метил, метокси, бром, фтор или хлор; Rc представляет водород или гидрокси; Rd представляет водород, фтор или хлор, особенно водород или фтор. В еще одном варианте осуществления настоящего изобретения фенильная группа, несущая (R3)m, предпочтительно представляет собой группу формулы llа, где: Ra представляет водород, фтор или хлор; Rb представляет водород, метил, метокси, бром, фтор или хлор, особенно водород, метил или хлор; Rc представляет водород или гидрокси; и Rd представляет водород; при условии, что каждый из Ra, Rb и Rc не представляет водород. Фенильная группа, несущая (R3) m, предпочтительно представляет собой 3-гидрокси-4 метилфенильную, 2-фтор-5-гидрокси-4-метилфенильную, 2-фтор-4-бромфенильную, 2-фтор-4-хлор-5гидроксифенильную или 4-хлор-2-фтор фенильную группу. В конкретном варианте осуществления настоящего изобретения фенильная группа, несущая (R3)m, представляет собой 3-гидрокси-4-метилфенильную, но особенно 2-фтор-5-гидрокси-4-метилфенильную группу. Еще в одном варианте осуществления настоящего изобретения фенильная группа, несущая (R3)m, представляет собой 4-хлор-2-фторфенильную группу. Преимущественно Y2 представляет -О-, -S-, -SO-, -SO 2-, -NR16CO-, -NR19SO 2- или -NR20- (где R16 , R19 и 20 R независимо представляют каждый водород, C1-2алкил или C1-2алкоксиэтил). Предпочтительно Υ2 представляет -О-, -S-, -SO-, -SO 2-или -NR20- (где R20 представляют водород, C12алкил или C 1-2алкоксиэтил). Более предпочтительно Y2 представляет -S-, -O- или -NR20- (где R20 представляют водород или C120 20 - такой, как определенный 2алкил), а наиболее предпочтительно он представляет -О- или -NR - (где R выше). Преимущественно Y3 представляет -О-, -S-, -SO-, -SO 2-, -NR21CO-, -NR24SO 2- или -NR25- (где R21 , R24 и 25 R независимо представляют каждый водород, C1-2алкил или C1-2алкоксиэтил). Предпочтительно Y3 представляет -О-, -S-, -SO-, -SO 2-или -NR25- (где R25 представляют водород, C12алкил или C 1-2алкоксиэтил). Более предпочтительно Y3 представляет -О- или -NR25- (где R 25 представляет водород или C1-2алкил). Преимущественно Y4 представляет -О-, -S-, -SO-, -SО 2-, -NR26CO-, -NR29SO 2- или -NR30- (где R26 , R29 и 30 R независимо представляют каждый водород, C1-2алкил или C1-2алкоксиэтил). Предпочтительно Υ4 представляет -О-, -S-, -SO-, -SО2- или -NR30- (где R30 представляют водород, C12алкил или C 1-2алкоксиэтил). Более предпочтительно Y4 представляет -О- или -NR30- (где R 30 представляет водород или C1-2алкил). Преимущественно Y5 представляет -О-, -S-, -SO-, -SO2-или -NR35- (где R35 представляют водород, C12алкил или C 1-2алкоксиэтил). Предпочтительно Υ5 представляет -S-, -О- или -NR35- (где R35 представляет водород, C1-2алкил или C12алкоксиэтил). Предпочтительно m представляет 2 или 3. Ζ может, например, представлять -ΝΗ- или -О-, но предпочтительно Ζ представляет -ΝΗ-. X1 предпочтительно представляет пиридоновую гр уппу или 5- или 6-членную ароматическую гетероциклическую гр уппу с 1-3 гетероатомами, выбранными из О, N и S, причем пиридоновая или гетероциклическая группа может быть замещенной так, как описано выше. Когда X1 представляет 5- или 6-членную ароматическую гетероциклическую гр уппу, она предпочтительно имеет 1 или 2 гетероатома, выбранных из О, N и S, из которых более предпочтительным является Ν, и может быть замещенной, как описано выше. X1 представляет, в частности, пиридоновую, пиридильную, имидазолильную, тиазолильную, тиенильную, триазолильную или пиридазинильную группу, которая может быть замещенной, как описано выше, а более конкретно пиридоновую, пиридильную, имидазолильную, тиазолильную или триазолильную группу, особенно пиридоновую, пиридильную, имидазолильную или триазолильную группу, которая может быть замещенной, как описано выше. Когда R4 представляет C1-5алкилХ1, C 2-5алкенилХ1, C2-5алкинилХ1 или C1-3алкилY5C1-3алкилХ1 и X1 представляет азотсодержащую 6-членную ароматическую гетероциклическую гр уппу, эта группа преимущественно связана с алкильным, алкенильным или алкинильным фрагментом через углеродный атом группы X1, причем указанная группа такова, что атом азота находится в пара-положении по отношению к углеродному атому, связанному с алкильным, алкенильным или алкинильным фрагментом. C1-5алкильный фрагмент может, если требуется, представлять собой -(СН2)n-. Когда R4-Υ1 представляет X1-(СН2)n-Y1- и n представляет целое число от 0 до 5, Υ1 представляет -О-, ΝΗ-, -S- или -СН2- и X1 представляет азотсодержащую 6-членную ароматическую гетероциклическую группу, которая преимущественно связана с -(СН2)n-Y1- через углеродный атом группы X1, причем указанная группа такова, что атом азота находится в пара-положении по отношению к углеродному атому, связанному с -(СН2)n-Y1-. В другом представляющем интерес примере X1 представляет пиримидин, который может быть замещенным, как описано выше. В одном из вариантов осуществления настоящего изобретения X1 представляет пиридоновую, фенильную или 5- или 6-членную ароматическую гетероциклическую гр уппу с 1-3 гетероатомами, выбранными из О, N и S, причем эта гр уппа может нести на себе предпочтительно до 2 заместителей (более предпочтительно до одного заместителя), выбранных из группы заместителей, описанной выше. В определении X1 подходящие заместители выбирают из галогена, C1-4алкила, C1-4алкокси и циано, а более подходящие заместители выбирают из хлора, фтора, метила и зтила. Подходящий R4 выбирают из следующи х восьми групп: 1) X1 (где X1 - такой, как определенный выше); 2) C 1-3алкилХ1 (где X1 - такой, как определенный выше); 3) C 3-5алкенилХ1 (где X1 - такой, как определенный выше); 4) C 2-5алкинилХ1 (где X1 - такой, как определенный выше); 5) C 1-5алкилY2Х1 (где Y2 и X1 - такие, как определенные выше); 6) C 3-5алкенилY3 Х1 (где Y3 и X1 - такие, как определенные выше); 7) C 3-5aлкинилY4 Х1 (где Y4 и X1 - такие, как определенные выше); 8) C 2-3алкилY5C1-2алкилХ1 (где Y5 и X1 - такие, как определенные выше). Преимущественный R4 выбирают из следующи х восьми групп: 1) X1 (где X1 - такой, как определенный выше); 2) C 1-5алкилХ1 (где X1 - такой, как определенный выше); 3) 1-Х1проп-1-ен-3-ил, 1-Х1бут-2-ен-4-ил, 1-Х1бут-1-ен-3-ил, 1-Х1пент-2-ен-4-ил или 2-Х1пент-3-ен-5-ил (где X1 - такой, как определенный выше, при условии, что когда R4 представляет 1-Х1проп-1-ен-3-ил, то X1 присоединен к алкенильной группе через углеродный атом); 4) 1-Х1проп-1-ин-3-ил, 1-Х1бут-2-ин-4-ил, 1-Х1бут-1-ин-3-ил, 1-Х1пент-2-ин-4-ил или 2-Х1пент-3-ин-5-ил (где X1 - такой, как определенный выше, при условии, что когда R4 представляет 1-Х1проп-1-ин-3-ил, то X1 присоединен к алкинильной группе через углеродный атом); 5) C 1-5алкилY2Х1 (где Y2 и X1 - такие, как определенные выше); 6) 1-(X1 Y3)проп-1-ен-3-ил, 1-(Х1 Y3)бут-2-ен-4-ил, 1-(X1 Y3)-бут-1-ен-3-ил, -1-(Х1 Y3)пент-2-ен-4-ил или 2(Χ1 Υ3) пент-3-ен-5-ил (где Υ3 и X1 - такие, как определенные выше); 7) 1-(Х1 Y4)проп-1-ин-3-ил, 1-(Х1 Y4)бут-2-ин-4-ил, 1-(Χ1 Υ4)-бут-1-ин-3-ил, 1-(Х1 Y4)пент-2-ин-4-ил или 2(Χ1 Υ4)пент-3-ин-5-ил (где Υ4 и X1 - такие, как определенные выше); и 8) C 2-3алкилY5C1-2алкилХ1 (где Υ5 и X1 - такие, как определенные выше). Предпочтительный R4 выбирают из следующих восьми групп: 1) X1 (где X1 - такой, как определенный выше); 2) C 1-5алкилХ1 (где X1 - такой, как определенный выше); 3) 1-Х1бут-2-ен-4-ил (где X1 - такой, как определенный выше); 4) 1-Х1бут-2-ин-4-ил (где X1 - такой, как определенный выше); 5) C 1-5алкилY2Х1 (где Υ2 и X1 - такие, как определенные выше); 6) 1-(Х1 Y3)бут-2-ен-4-ил (где Υ3 и X1 - такие, как определенные выше); 7) 1-(Х1 Y4)бут-2-ин-4-ил (где Υ4 и X1 - такие, как определенные выше); и 8) этилY5метилХ1 (где Υ5 и X1 - такие, как определенные выше). Более предпочтительно соединения формулы (I) представляют собой соединения формулы (Iа): (la) (где R1, R2, R3, m, X1, Y1 и Ζ - такие, как определенные выше, n представляет целое число от 0 до 5 и Υ представляет непосредственную связь, -О-, -S-, -SO-, -SO 2-, -NR36CO-, -CONR37-, -SO2NR38-, -NR39SO 2- или -NR40- (где R36, R 37, R38, R39 и R40 независимо представляют каждый водород, C1-3алкил или C1-3алкоксиC23алкил)). Преимущественно Υ6 представляет непосредственную связь, -О-, -S-, -SO-, -SO 2- или -NR40- (где R40 представляет водород, C1-2алкил или C1-2алкоксиэтил). Предпочтительно Y6 представляет непосредственную связь, -О-, -S- или -NH-. Более предпочтительно Y6 представляет непосредственную связь. Преимущественно n представляет целое число от 0 до 3, а предпочтительно от 1 до 3. Таким образом, например, в конкретном варианте осуществления настоящего изобретения соединения формулы I представляют собой соединения формулы Iа, где: [Υ1 представляет -О-, -ΝΗ-, -S- или -СН2-; n представляет целое число от 0 до 5; X1 представляет фенильную гр уппу или 5- или 6-членную ароматическую гетероциклическую гр уппу с 1-3 гетероатомами, выбранными из О, -N и S, причем фенильная или гетероциклическая группа может нести на себе до 5 заместителей, выбранных из галогена, C1-4алкила, С1-4алкокси, C1-4гидроксиалкила, C141 42 и -NR43COR44 (где R41, R42, R43 и R44, которые могут быть 4гидроксиалкокси, карбокси, циано, -CONR R одинаковыми или разными, представляют каждый водород или C1-4алкил); R1 представляет водород, гидрокси, C1-3алкил, C1-3алкокси, C1-3алкилтио или NR45R46 (где R45 и R46, которые могут быть одинаковыми или разными, представляют каждый водород или C1-3алкил); R2 представляет водород, гидрокси, галоген, C1-3алкил, C1-3алкокси, трифторметил, циано, амино или нитро; m представляет целое число от 1 до 5; R3 представляет водород, галоген, C1-3алкил, C1-3алкокси, C1-3алканоилокси, трифторметил, циано, амино или нитро; Ζ представляет -ΝΗ- или -O-; и Υ6 представляет непосредственную связь; при условии, что когда X1 представляет незамещенный фенил или замещенный фенил с 1-2 заместителями, выбранными из галогена, C1-4алкила и C1-4алкокси, то m представляет целое число от 3 до 5 или Ζ представляет -O-]; или их соли. Предпочтительными соединениями по настоящему изобретению являются: 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(3-пиридилметокси)хиназолин 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(3-тиенилметокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(2-пиридилокси)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-[N-метил-N-(4-пиридил)]аминоэтокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-[2-(2-оксо-1,2-дигидро-1-пиридил)этокси]хиназолин 7-(4-цианбензилокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(2-метилимидазол-1-ил)пропокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-((2-метил-4-пиридил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(2-оксо-1,2-дигидро-1-пиридил)пропокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(1-метилимидазол-2-илтио)пропокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(4-пиридилокси)пропокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридилтио)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(3-пиридилокси)этокси)хиназолин 7-бензилокси-4-(2-фтор-5-гидрокси-4-метиланилино)хиназолин 7-бензилокси-4-(4-хлор-2-фтор-5-гидроксианилино)хиназолин 4-(4-хлор-2-фтор-5-гидроксианидино)-6-метокси-7-((2-метилтиазол-4-ил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-((3-тиенил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-метил-N-(пиридазин-4-ил)амино)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-метил-N-(6-метилпиримидин-4-ил)амино)этокси)хиназолин 4-(4-хлор-2-фторанилино)-7-(2-(3,5-диметил-[1,2,4]-триазол-4-ил)этокси)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-7-(2-(2,4-диметилимидазол-1-ил)этокси)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-7-(2-(2,5-диметилимидазол-1-ил)этокси)-6-метоксихиназолин 4-(3-гидроксианилино)-7-(2-(имидазол-1-ил)этокси)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1,2,4-триазол-4-ил)этокси)хиназолин 4-(4-бром-2-фторанилино)-7-(2-([1,2,4]-триазол-1-ил)этокси)-6-метоксихиназолин и их соли, в частности гидрохлориды. Следующие соединения по настоящему изобретению являются особенно предпочтительными: 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилметокси)хиназолин 4-(3-гидрокси-4-метгаіанилино)-6-метокси-7-(2-пиридилметокси)хиназолин 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(1-метилимидазол-2-илметокси)хиназолин 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(2-метилитиазол-4-илметокси)хиназолин 7-(2-ацетамидотиазол-4-илметокси)-4-(3-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(3-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилпропокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилпропокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(4-пиридилметокси)хиназолин 7-бензилокси-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридилокси)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-[2-(4-оксо-1,4-дигидро-1-пиридил)этокси]хиназолин 7-бензилокси-4-(2-фтор-5-гидрокси-4-метилфенокси)-6-метоксихиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-((2-метилтиазол-4-ил)метокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-7-(4-пиридилметокси)хиназолин 4-(4-хлор-2-фторанилино)-7-(2-(имидазол-1-ил)этокси)-6-метоксихиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-((1-метил-имидазол-2-ил)метокси)хиназолин 7-((2-ацетамидотиазол-4-ил)метокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 7-бензилокси-4-(4-хлор-2-фтор-5-гидроксианилино)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(4-пиридил)пропокси)хиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-(3-(4-пиридил)пропокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-7-(2-имидазол-1-ил)этокси)-6-метоксихиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-7-(2-имидазол-1-ил)этокси)-6-метоксихиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-6-метокси-7-(3-тиенилметокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолин 4-(3-гидрокси-4-метиланилино)-6-метокси-7-((1-метилбензимидазол-2-ил)метокси)хиназолин 7-((2-хлор-6-метил-4-пиридил)метокси)-4(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(4-хлор-2-фторфенокси)-6-метокси-7-((4-пиридил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-((4-пиридил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(2-метилимидазол-1-ил)этокси)хиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((4-пиридил)метокси)хиназолин 4-((2-хлор-4-пиридил)метокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-илтио)этокси)хиназолин 7-(3,4-дифторбензилокси)-4-(2-фтор-5-гидрокси-4-метиланилино)-6-метоксихиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((1-метилимидазол-2-ил)метокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-7-((1-метилимидазол-2-ил)метокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-7-(2-(1,2,4-триазол-1-ил)этокси)хиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-((2-тиенил)метокси)хиназолин 4-(4-хлор-2-фтор-5-гидроксианилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1,2,4-триазол-1-ил)этокси)хиназолин 4-(2-фтор-5-гидрокси-4-метиланилино)-7-((4-пиридил)карбоксиамидо)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-(4-пиридил)амино)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-ил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-7-((2-циано-4-пиридил)метокси)-6-метоксихиназолин и их соли, в частности гидрохлориды, из которых особенно предпочтительными являются следующие: 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридилокси)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-[2-(4-оксо-1,4-дигидро-1-пиридил)этокси]хиназолин 4-(4-хлор-2-фторанилино)-7-(2-(имидазол-1-ил)этокси)-6-метоксихиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(3-(4-пиридил)пропокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(4-пиридил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-((4-пиридил)метокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(2-метилимидазол-1-ил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-илтио)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1,2,4-триазол-1-ил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(N-(4-пиридил)амино)этокси)хиназолин 4-(4-хлор-2-фторанилино)-6-метокси-7-(2-(1-метилимидазол-2-ил)этокси)хиназолин 4-(4-хлор-2-фторанилино)-7-((2-циано-4-пиридил)метокси)-6-метоксихиназолин и их соли, в частности гидрохлориды. Другим представляющим интерес соединением является 4-(3-гидрокси-4-метиланилино)-6-метокси-7(4-пиримидинилметокси)хиназолин и его соли, в частности гидрохлориды. Во избежание неясности следует понимать, что когда в данном описании группу называют как "определенная выше", то это охва тывает первое, самое широкое определение и каждое и все из предпочтительных определений для этой группы. В данном описании термин "алкил" включает как неразветвленные, так и разветвленные алкильные группы, но ссылки на индивидуальные алкильные группы, такие, как "пропил" относятся конкретно к неразветвленной цепи. Аналогичное правило относится и к другим родовым терминам. Если не указано иное, то термин "алкил" относится преимущественно к цепям с 1-6 углеродными атомами, предпочтительно с 1-4 углеродными атомами. Используемый в данном описании термин "алкокси" включает, если не указано иное, "алкил"-О-группы, в которых "алкил" - такой как определенный выше. Термин "арил" при использовании в данном описании относится, если не указано иное, с C6-10арильной группе, которая может при необходимости нести на себе один или несколько заместителей, выбранных из галогена, алкила, алкокси, нитро, трифторметила и циано (где алкил и алкокси - такие, как определенные выше). Термин "арилокси" при использовании в данном описании включает, если не указано иное, "арил"О-группы, в которых "арил" - такой, как определенный выше. Термин "сульфонилокси" при использовании в данном описании относится к алкилсульфонилокси- и арилсульфонилоксигруплам, в которых "алкил" и "арил" - такие, как определенные выше. Термин "алканоил" при использовании в данном описании включает, если не указано иное, группы алкилС=О , в которых "алкил" -такой как определенный выше, например этаноил относится к СН 3С=О. В данном описании термин "алкенил" включает, если не указано иное, алкенильные группы как с неразветвленными, так и с разветвленными цепями, но ссылки на индивидуальные алкенильные группы, такие как 2-бутенил, конкретно относятся только к группам с неразветвленной цепью. Если не указано иное, то термин "алкенил" относится преимущественно к цепи с 2-6 углеродными атомами, предпочтительно с 4-5 углеродными атомами. В данном описании термин "алкинил" включает, если не указано иное, алкинильные группы как с неразветвленными, так и с разветвленными цепями, но ссылки на индивидуальные алкинильные группы, такие, как 2-бутинил, конкретно относятся только к группам с неразветвленной цепью. Если не указано иное, то термин "алкинил" относится преимущественно к цепям с 2-6 углеродными атомами, предпочтительно с 4-5 углеродными атомами. В определенной выше формуле I водород находится в положениях 2 и 8 хиназолиновой группы. Следует понимать, что в пределах настоящего изобретения хиназолин формулы I или его соль могут проявлять таутомеризм и что рисунки формул в данном описании могут представлять только одну из возможных таутомерных форм. Понятно, что изобретение охватывает любую таутомерную форму, которая ингибирует активность тирозинкиназы VEGF-рецепторов, а не ограничивается лишь какой-либо одной таутомерной формой, показанной на рисунках формул. Следует также понимать, что некоторые хиназодины формулы I и их соли могут существовать в сольватированной и несольватированной формах, таких, как гидратные формы. Понятно, что настоящее изобретение охватывает все такие сольватированные формы, которые ингибируют активность тирозинкиназы VEGF-рецепторов. Во избежание какой-либо неясности нужно понимать, что когда Y1 представляет, например, группу формулы -NR5CO-, то несущая атом азота группа R5 присоединена к хиназолиновому кольцу и карбонильная (СО) группа присоеденина к R4, а когда Y1 представляет, например, группу формулы CONR6-, то к хиназолиноаому кольцу присоединена карбонильная группа, а группа R6, несущая атом азота, присоединена к R4. Аналогичное правило относится к другим группам Y1, связывающим два атома, таким, как -NR8SO2- и -SO2NR7-. Когда Y1 представляет -NR9-, группа R9, несущая атом азота, связана с хиназолиновым кольцом и с R4. Аналогичное правило применимо и к другим группам. Следует также понимать, что когда Y1 представляет -NR9- и группа R9 представляет C1-3алкоксиС 2-3алкил, то С21 3алкильный фрагмент связан с атомом азота группы Y , и аналогичное правило применимо к другим группам. Чтобы избежать какого-либо сомнения, следует понимать, что когда в соединении формулы I R4 представляет, например, группу формулы C1-5алкилY5 C1-5алкилХ1 , то с Y1 связан концевой C1-5алкильный фрагмент, а когда R4 представляет, напротив, гр уппу формулы C2-5алкенилХ1, то с Y1 связан С24 5алкенильный фрагмент, причем аналогичное правило применимо и к другим группам. Когда R 1 1 представляет группу 1-Х проп-1-ен-3-ил, то к первому атому углерода присоединена группа X и третий атом углерода связан с Y1, а когда R4 представляет группу 2-Х1пент-3-ен-5-ил, то группа X1 присоединена к второму атому углерода, а пятый атом углерода связан с Y1, и такое же правило применимо к другим группам. Во избежание всякого сомнения нужно понимать, что когда X1 несет C1-4аминоалкильньій заместитель, то к X1 присоединен C1-4алкильньгй фрагмент, а когда X1 несет в качестве заместителя C1-4алкиламино, то к X1 присоединен аминофрагмент, и такое же правило применимо к другим группам. Настоящее изобретение относится к соединениям формулы I, описанным выше, а также к их солям. Соли для применения в фармацевтических композициях должны быть фармацевтически приемлемыми солями, а другие соли могут быть полезными для получения соединений формулы I и их фармацевтически приемлемых солей. Фармацевтически приемлемые соли по настоящему изобретению могут, например, включать кислотно-аддитивные соли описанных выше соединений формулы I, которые, являются достаточно основными для образования таких солей. Такие кислотно-аддитивные соли включают, например, соли с неорганическими кислотами, такими, как галоидводородные кислоты (в частности, хлороводородная или бромоводородная кислота, из которых особенно предпочтительной является хлороводородная кислота) и серная или фосфорная кислота, а также соли с органическими кислотами, дающими фармацевтически приемлемые анаоны, таким, как, например, трифторуксусная, лимонная или малеиновая кислота. Кроме того, когда соединения формулы I достаточно кислы, фармацевтически приемлемые соли могут быть образованы с неорганическим веществом или органическим основанием, дающим фармацевтически приемлемый катион. Такие соли включают, например, соль щелочного металла, такую, как соль натрия или калия, соль щелочноземельного металла, такую, как соль кальция или магния, соль аммония или, например, соль с метиламином, диметиламином, триметиламином, пиперидином, морфолином или трис-(2-гидроксиэтил)амином. Соединение формулы I или его соль и другие соединения по настоящему изобретению (такие, как определенные выше) могут быть получены любым известным способом, применяемым для получения химически родственных соединений. Такие способы включают, например, те, что описаны в заявках №0520722, №0566226, №0602851 и №0635498 на европейский патент. Такие способы служат в качестве дополнительного признака настоящего изобретения и описаны ниже. Необходимые исходные материалы могут быть получены стандартными методами органической химии. Получение таких исходных материалов описано в прилагаемых неограничивающих примерах. Или же необходимые исходные материалы могут быть получены аналогичными описанными методами, понятными для специалистов в области органической химии. Следующие далее способы (а)-(g) и (i)-(v) составляют дополнительные признаки настоящего изобретения. Синтез соединений формулы I (а) Соединения формулы I и их соли могут быть получены путем осуществления взаимодействия соединения формулы III: (lll) (где R1, R2, R4 и Υ1 - такие, как определенные выше, и L1 представляет уходящую группу) с соединением формулы IV: (IV) (где Z, R3 и m - такие, как определенные выше) с получением соединений формулы I и их солей. Подходящей удаляемой группой L1 является, например, галоген, алкокси- (предпочтительно C1-4алкокси-), арилокси- или сульфонилоксигруппа, например, хлор, бром, метокси-, фенокси-, метансульфонилокси- или толуол-4-сульфонилоксигруппа. Реакцию преимущественно осуществляют в присутствии либо кислоты, либо основания. Такой кислотой является, например, безводная неорганическая кислота, такая, как хлороводородная кислота. Таким основанием является, например, органическое аминное основание, такое, как, например, пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, морфолин, N-метилморфолин или диазабицикло[5.4.0]ундец-7-ен, или, например, карбонат или гидроксид щелочного или щелочноземельного металла, например, карбонат натрия, карбонат калия, карбонат кальция, гидроксид натрия или гидроксид калия. Или же таким основанием является, например, гидрид щелочного металла, например, гидрид натрия, или амид щелочного или щелочноземельного металла, например, амид натрия или бис(триметилсилил)амид натрия. Реакцию предпочтительно осуществляют в присутствии инертного растворителя или разбавителя, например, спирта или сложного эфира, такого, как метанол, этанол, изопропанол или этилацетат, галогенированного растворителя, такого, как метиленхлорид или тетрахлорид углерода, простого эфира, такого, как тетрагидрофуран или 1,4-диоксан, ароматического растворителя, такого, как толуол, или диполярного апротонного растворителя, такого, как Ν,Νдиметилформамид, Ν,Ν-диметилацетамид, N-метилпирролидин-2-он или диметилсульфоксид. Реакцию обычно проводят при температуре в интервале, например, 10-150°С, предпочтительно в интервале 2080°С. Соединение по настоящему изобретению может быть получено описанным способом в форме свободного основания или же в форме соли с кислотой формулы H-L1, где L1 имеет значение, определенное выше. Когда требуется получить свободное основание из соли, соль можно обработать основанием, определенным выше, с использованием традиционной методики. (b) Когда группа формулы llb: (llb) (где R3 и m - такие, как определенные выше) представляют собой фенильную группу, несущую одну или несколько гидроксигрупп, соединение формулы I и его соли можно получить путем снятия защиты с соединения формулы V: (V) (где Y1 , m, R1, R2, R3, R4 и Ζ - такие, как определенные выше. Ρ представляет фенольную гидроксизащитную гр уппу и р1 представляет целое число от 1 до 5, равное числу защищенных гидроксигрупп, причем разность m-р1 равна числу заместителей R3, которые не являются защищенным гидрокси). Выбор фенольной гидрокси-защитной группы Ρ может сделать рядовой химик-органик из тех защитных гр упп, которые включены в обычную литератур у, такую как "Protective Groups in Organic Synthesis" T.W. Greene and R.G.M. Wuts, 2-ое изд. Willey 1991, включающую простые эфиры (например, метиловые, метоксиметиловые, аллиловые и бензиловые), простые силиловые эфиры (например, третбутилди фенилсилиловые и трет-бутилдиметилсилиловые), сложные эфиры (например, ацетат и бензоат) и карбонаты (например, метил- и бензил-карбонаты). Удаление такой фенольной гидрокси-защитной группы может быть осуществлено любым известным методом, включающим условия реакций, указанные в обычной литературе, такой, как названная выше, или подобным методом. Условия реакций предпочтительно таковы, чтобы можно было получить гидроксипроизводное без неожиданных реакций в други х местах в исходных и целевых соединениях. Например, когда защитной группой Ρ является ацетат, преобразование целесообразно осуществлять путем обработки производного хиназолина основанием, определенным выше, включая аммиак и его моно- и диалкилированные производные, предпочтительно в присутствии протонного растворителя или сорастворителя, такого, как вода или спирт, например, метанол или этанол. Такая реакция может быть осуществлена в присутствии дополнительного инертного растворителя или разбавителя, определенного выше, при температуре в интервале 0-50°С, предпочтительно при 20°С или около. (с) Получить указанные соединения формулы I и и х соли, в которых заместитель Υ1 представляет -О-, S- или -NR9-, можно путем осуществления взаимодействия (целесообразно в присутствии основания, такого, как определенные выше) соединения формулы VI: (VI) (где m, Y1, R1 , R2, R3 и Ζ - такие, как определенные выше) с соединением формулы VII: R -L1 (VII) (где R4 и L1 - такие, как определенные выше); L представляет уходящую гр уппу, например, галоген или сульфонилоксигруппу, такую, как бром или метансульфонилоксигруппа. Реакцию предпочтительно осуществляют в присутствии основания (такого, как определенное выше в способе (а)) и преимущественно в инертном растворителе или разбавителе (таком, как определенный выше в способе (а)) преимущественно при температуре в интервале, например, 10-150°С, предпочтительно при 50°С или около. (d) Соединения формулы I и их соли могут быть получены путем осуществления взаимодействия соединения формулы VIII: 4 (VIII) С соединением формулы IX: R4-Y1-Η (IX) (где L1, R1 , R2, R3, R 4, Z, m и Υ1 - такие, как определенные выше). Реакцию целесообразно осуществлять в присутствии основания (такого, как определенное выше в способе (а)) и преимущественно в инертном растворителе или разбавителе (таком, как определенный выше в способе (а)) преимущественно при температуре в интервале, например, 10-150°С, предпочтительно при 100°С или около. (е) Соединения формулы I и их соли, в которых R 4 представляет С 1-5алкилХ2 [где X2 выбран из следующих трех гр упп: 1) X1 (где X1 - такой, как определенный выше); 2) Y7 Χ1 (где Υ7 представляет -О-, -S-, -SO2-, -NR47CO-, -NR48SO 2- или -NR49- (где R47, R48 и R49 независимо представляют каждый водород, С1-3алкил или С1-3алкоксиС 2-3алкил) и X1 - такой, как определенный выше); и 3) Y8С1-3алкилХ (где Y8 представляет -О-, -S-, -SO2-, -NR50CO-, -NR51SO2- или –NR52- (где R50, R 51 и R52 независимо представляют каждый водород, С1-3алкил или С1-3алкоксиС2-3алкил) и X1 - такой, как определен выше);] могут быть получены путем осуществления взаимодействия соединения формулы X: (X) (где L1, Y1, R1 , R2, R3, Ζ и m - такие, как определенные зыше, и R 53 представляет С1-5алкил) с соединением формулы XI: Χ2-Η (XI) (где Χ2 - такой, как определенный выше) с получением соединения формулы I. Реакцию целесообразно осуществлять в присутствии основания (такого, как указано выше в способе (а)) и преимущественно в присутствии инертного растворителя или разбавителя (такого, как указано выше в способе (а)) при температуре в интервале, например, 0-150°С, предпочтительно примерно при 50°С. (f) Указанные соединения формулы I и их соли, в которых заместитель R1 представлен NR1OR11, где один или оба радикала R10 и R11 представляют C1-3алкил, могут быть получены путем осуществления взаимодействия соединений формулы I, в которых заместитель R1 представляет аминогруппу, и алкилирующего агента предпочтительно в присутствии основания, определенного выше. Такими алкилирующими агентами являются C1-3алкильные фрагменты, несущие определенный выше отщепляемый (уходящий) фрагмент, такие, как C1-3алкилгалогениды, например C1-3алкилхлорид, -бромид или -иодид. Реакцию предпочтительно осуществляют в присутствии инертного растворителя или разбавителя (такого, как определенный выше в способе (а)) при температуре в интервале, например, 10100°С, предпочтительно примерно при температуре окружающей среды. (g) Соединения формулы I и их соли, в которых один или несколько заместителей R1, R2 или R3 представляют аминогруппу, могут быть получены путем восстановления соответствующего соединения формулы І, в котором заместитель(и) в соответствующем(их) положении(ях) хиназолинового и/или фенильного кольца представляет(ют) нитрогруппу(ы). Восстановление целесообразно осуществлять так, как описано ниже в способе (і). Соединение формулы I и его соли, в которых заместитель(и) в соответствующем(их) полажении(ях) хиназолинового и/или фенильного кольца представляет(ют) нитрогруппу(ы), можно получить способами, описанными выше (а-е) и ниже (i-ν), с использованием хиназолина, выбранного из соединений формул (I-XXVII), в которых заместитель(и) в соответствующем (их) положении(ях) хиназолинового и/или фенильного кольца представляет(ют) нитрогруппу(ы). Синтез промежуточных соединений (і) Соединения формулы III и их соли составляют дополнительный признак настоящего изобретения. Такие соединения, в которых L1 представляет галоген, могут, например, быть получены путем галогенирования соединения формулы XII: (XII) (где R1, R2 , R4 и Υ1 - такие, как определенные выше). Подходящие галогенирующие агенты включают галогенангидриды неорганическихкислот, например, тионилхлорид, хлорид фосфора (III) , оксихлорид фосфора (V) и хлорид фосфора (V). Реакцию галогенирования целесообразно осуществлять в присутствии инертного растворителя или разбавителя, такого, как, например, галогенированный растворитель, такой, как метиленхлорид, трихлорметан или тетрахлорид углерода, или ароматический углеводородный растворитель, такой, как бензол или толуол. Реакцию целесообразно проводить при температуре в интервале, например, 10-150°С, предпочтительно в интервале 40-100°С. Соединения формулы XII и и х соли, которые составляют дополнительный признак настоящего изобретения, могут, например, быть получены путем осуществления взаимодействия соединения формулы XIII: (XIII) (где R1, R2 и L1 - такие, как определенные выше) с соединением формулы IX, определенным выше. Реакцию целесообразно осуществлять в присутствии основания (такого, как определенное выше в способе (а)) и преимущественно в присутствии инертного растворителя или разбавителя (такого, как определенный выше в способе (а)) при температуре в интервале, например, 10-150°С, предпочтительно при 100°С или около. Соединения формулы XII и их соли можно также получить путем циклизации соединения формулы XIV: (XIV) (где R1, R2 , R4 и Υ1 - такие, как определенные выше, и А1 представляет гидрокси-, алкокси(предпочтительно C1-4алкокси-) или аминогруппу) с образованием соединения формулы XII или его соли. Циклизацию можно проводить путем осуществления взаимодействия соединения формулы XIV, где А1 представляет гидрокси- или алкоксигруппу, с формамидом или его эквивалентом, способным вызвать циклизацию, с получением соединения формулы XII или его соли, например, [3-(диметиламино)-2-азапроп2-енилиден]диметиламмонийхлорида. Циклизацию целесообразно осуществлять в присутствии формамида в качестве растворителя или в присутствии инертного растворителя или разбавителя, такого, как простой эфир, например, 1,4-диоксан. Циклизацию целесообразно проводить при повышенной температуре, предпочтительно в интервале 80-200°С. Соединения формулы XII можно также получить путем циклизации соединения формулы XIV, где А1 представляет аминогруппу, муравьиной кислотой или ее эквивалентом, способным вызвать циклизацию, с получением соединения формулы XII или его соли. Эквиваленты муравьиной кислоты, способные вызвать циклизацию, включают, например, три-C14алкоксиметан, например, триэтоксиметан и триметоксиметан. Циклизацию целесообразно осуществлять в присутствии каталитического количества безводной кислоты, такой, как сульфоновая кислота, например, птолуолсульфоновая кислота, и инертного растворителя или разбавителя, такого, как, например, галогенированный растворитель, такой, как метиленхлорид, трихлорметан или тетрахлорид углерода, простой эфир, такой, как диэтиловый эфир или тетрагидрофуран, или ароматический углеводородный растворитель, такой, как толуол. Циклизацию целесообразно проводить при температуре в интервале, например, 10-100°С, предпочтительно в интервале 20-50°С. Соединения формулы XIV и и х соли, которые составляют дополнительный признак настоящего изобретения, можно, например, получить путем восстановления нитрогруппы в соединении формулы XV: (XV) (где R1, R2 , R4,Υ1 и А1 - такие, как определенные выше) с получением соединения формулы XIV, определенного ниже. Восстановление нитрогруппы целесообразно осуществлять любым методом, известным для осуществления такого преобразования. Восстановление может быть проведено, например, путем гидрирования раствора нитросоединения в присутствии растворителя или разбавителя, такого, как определенный выше, и в присутствии металлического катализатора, такого, как палладий или платина. Другим восстановителем является, например, активированный металл, такой, как активированное железо (полученное, например, путем промывки железного порошка разбавленным раствором кислоты, такой, как хлороводородная кислота). Так, например, восстановление может быть осуществлено путем нагревания смеси нитросоединения и активированного металла в присутствии растворителя или разбавителя, такого, как смесь воды и спирта, например, метанола или этанола, до температуры в интервале, например, 50150°С, предпочтительно при 70°С или около. Соединения формулы XV и и х соли, которые составляют дополнительный признак настоящего изобретения, могут, например, быть получены путем осуществления взаимодействия соединения формулы XVI: (XVI) (где R1, R2, L1 и А1 - такие, как определенные выше) с соединением формулы IX, определенным выше. Взаимодействие соединений формул XVI и IX целесообразно осуществлять при условиях, описанных выше для способа (d). Соединения формулы XV и их соли могут, например, быть получены путем осуществления взаимодействия соединения формулы XVII: (XVII) (где R1, R2 , Y1 и А1 - такие, как определенные выше, при условии, что Y1 представляет не -СН2-) с соединением формулы VII, определенным выше, с получением соединения формулы XV, определенного выше. Взаимодействие соединений формул XVII и VII целесообразно осуществлять при условиях, описанных выше для способа (с). Соединения формулы III и их соли могут быть также получены, например, путем осуществления взаимодействия соединения формулы XVIII: (XVIII) (где R1, R2 и Υ1 - такие, как определенные выше, при условии, что Υ1 представляет не -СН2- и L2 представляет уходящую защитн ую гр уппу) с соединением формулы VII, определенным выше, с получением соединения формулы III, в котором L1 представлен L2. Целесообразно использовать соединение формулы XVIII, в котором L2 представляет феноксигруппу, которая при необходимости может нести на себе до 5 заместителей, предпочтительно до 2 заместителей, выбранных из галогена, нитро или циано. Реакцию целесообразно проводить при условиях, описанных выше для способа (с). Соединения формулы XVIII и их соли, такие, как определенные выше, могут быть, например, получены путем снятия защиты с соединения формулы XIX: (XIX) (где R1, R2, Ρ, Υ1 и L2 - такие, как определенные выше). Удаление защиты может быть осуществлено методами, хорошо известными из литературы, например, когда Ρ представляет бензильную группу, удаление защиты может быть осуществлено путем гидрогенолиза или путем обработки трифторуксусной кислотой. Одно соединение формулы III можно при желании преобразовать в другое соединение формулы III, в котором фрагмент L1 другой. Так, например, соединение формулы III, в котором L1 отличается от галогена, например, представляет необязательно замещенный фенокси, можно преобразовать в соединение формулы III, в котором L1 представляет галоген, путем гидролиза соединения формулы III (в котором L1 отличается от галогена) с получением соединения формулы XII, определенного выше, после чего в соединение формулы XII, полученное так, как описано выше, вводят галогенид с получением соединения формулы III, в котором L1 представляет галоген. (іі) Соединения формулы V и и х соли составляют дополнительный признак настоящего изобретения и могут быть получены, например, путем осуществления взаимодействия соединения формулы III, определенного выше, с соединением формулы XX: (XX) (где R3, m, р1 , Ρ и Ζ - такие, как определенные выше). Реакция может быть осуществлена, например, так, как описано выше для способа (а). Соединения формулы V и их соли можно также получить путем осуществления взаимодействия соединения формулы XXI (XXI) (где R1, R2, L 1, Z, R3, m, р1 и Ρ - такие, как определенные выше) с соединением формулы IX, определенным выше. Реакция может быть осуществлена, например, так, как описано выше для способа (d). Соединения формулы V и их соли можно также получить путем осуществления взаимодействия соединения формулы XXII: (XXII) (где R1, R2, R3, Y1, Z, Ρ, р1 и m - такие, как определенные выше, при условии, что Y1 представляет не СН2-) с соединением формулы VII, определенным выше. Реакция может быть осуществлена, например, так, как описано выше для способа (с). Соединения формулы XXI и их соли можно получить, например, путем осуществления взаимодействия соединения формулы XXIII: (XXIII) (где R1, R2 и L1 - такие, как определенные выше, и L 1 в положениях 4 и 7 могут быть одинаковыми или разными) с соединением формулы XX, определенным выше. Реакция может быть осуществлена, например, так, как описано выше для способа (а). Соединения формулы XXII и их соли можно получить путем осуществления взаимодействия соединений формул XIX и XX, определенных выше, при условиях, описанных выше для способа (а), с получением соединения формулы XXIV: (XXIV) (где R1, R2, R3, Ρ, Z, Y1, p1 и m - такие, как определенные выше, при условии, что Y1 представляет не СН2-) и затем снятия защиты с соединения XXIV, например, так, как описано выше в разделе (і). (ііі) Соединения формулы VI и их соли, определенные выше, могут быть получены путем снятия защиты с соединения формулы XXV: (XXV) (где R1, R2, R3, Ρ, Ζ, Υ1 и m - такие, как определенные выше), например, так, как описано выше в разделе (і). Соединения формулы XXV и их соли можно получить путем осуществления взаимодействия соединений формул XIX и IV, определенных выше, при условиях, описанных выше для способа (а), с получением соединения формулы XXV или его соли. (iv) Соединения формулы VIII и их соли, определенные выше, можно получить путем осуществления взаимодействия соединений формул XXIII и IV, определенных выше, причем реакция может быть осуществлена способом, описанным выше в (а). (ν) Соединения формулы X, определенные выше, и их соли можно получить, например, путем осуществления взаимодействия соединения формулы VI, определенного выше, с соединением формулы XXVI: L1-R53-L1 (XXVI) (где L1 и R53 - такие, как определенные выше) с получением соединения формулы X. Реакция может быть осуществлена, например, способом, описанным выше в (с). Соединения формулы X и их соли можно также получить, например, путем снятия защиты с соединения формулы XXVII: (XXVII) (где L1, R53 , Y1 , R1, R2 , R3, Р, m и р1- такие, как определенные выше), например, способом, описанным выше в (b). Соединения формулы XXVII и их соли можно получить, например, путем осуществления взаимодействия соединений формул XXII и XXVI, определенных выше, при условиях, описанных выше для способа (с). Когда нужна фармацевтически приемлемая соль соединения формулы I, она может быть получена, например, путем осуществления взаимодействия указанного соединения, например, с кислотой с использованием традиционной методики. Многие из промежуточных соединений, определенных в данном описании, являются новыми соединениями, например, промежуточные соединения формул III, V, XII, XIV и XV, причем эти соединения составляют дополнительный признак настоящего изобретения. В качестве дополнительного признака настоящего изобретения предлагаются также промежуточные соединения формул VIII, X, XXI, XXII, XXIV, XXV и XXVII. Идентификация соединений, которые мощно ингибируют активность тирозинкиназы, связанную с VEGF-рецепторами, такими, как Flt и/или KDR, и которые ингибируют ангиогенез и/или повышенную сосудистую проницаемость, желательна и является предметом настоящего изобретения. Эти свойства можно оценить, например, используя один или несколько методов, описанных ниже. (а) Испытание на ингибирование рецепторной тиразинкиназы in vitro Это испытание определяет способность испытуемого соединения ингибировать активность тирозинкиназы. ДНК-кодируемые цитоплазматические домены VEGF-рецепторов или рецепторов эпидермального ростового фактора (EGF), могут быть получены путем общего генного синтеза (Edwards M., International Biotechnology Lab 5(3), 19-25, 1987) или путем клонирования. Затем они могут быть экспрессированы в подходящей системе экспрессии для получения полипептида с тирозинкиназной активностью. Например, было обнаружено, что цитоплазматические домены VEGF- и EGF-рецепторов, которые были получены экспрессией рекомбинантного белка в клетках насекомых, проявляют существенную тирозинкиназную активность. В случае VEGF-рецептора Flt (№Х51602 в каталоге Генбанка) 1,7кб фрагмент ДНК, кодирующий большую часть цитоплазматического домена, начинающийся с метионина 783 и включающий терминирующий кодон, который (фрагмент) описан by Shibuya et al (Oncogene, 1990, 5: 519-524), был выделен из кДНК и клонирован в вектор бакуловирусного переноса (например, pAcYMl (см. The Baculovirus Expression System: A Laboratory Guide, L.A. King and R.D. Possee, Chapman and Hall, 1992) или рАс360 или pBlueBacHis (Invitrogen Corporation)). Эта рекомбинантная конструкция была котрансфектирована в клетки насекомых (например, Spodoptera frugiperda 21 (Sf21) с вирусной ДНК (например, Pharmingen BaculoGold)) для получения рекомбинантного бакуловируса. (Подробности методов сборки рекомбинантных молекул ДНК и получения и применения рекомбинантного бакуловируса можно найти в типовых руководствах, например, Sambrook et al, 1989, Molecular cloning - A Laboratory Manual, 2-ое издание, Cold Spring Harbour Laboratory Press and O'Reilly et al, 1992, Baculovirus Expression Vectors - A Laboratory Manual, W.H. Freeman and Co, New York). Для други х тирозинкиназ для использования в испытаниях могут быть клонированы и экспрессированы аналогичным образом цитоплазматические фрагменты, начинающиеся с метионина 806 (KDR, каталожный №L04947 в Генбанке) и метионина 668 (EGF-рецептор, каталожный №Х00588 в Генбанке). Для экспрессии cFlt-тирозинкиназной активности клетки Sf21 заражали чистым cFlt-рекомбинантным вирусом чумы при множественности заражения, равной 3, и собирали через 48 часов. Собранные клетки промывали охлажденным льдом фосфатно-солевым буферным раствором (PBS) (10мМ фосфат натрия рН 7,4, 138мМ NaCl, 2,7мМ КСl), затем ресуспендировали в охлажденном льдом HNTG/PMSF (20мМ Hepes рН 7,5, 150мМ NaCl, 10% о/о глицерин, 1% о/о Triton X100, 1,5мМ МgСl2, 1мМ этиленгликоль-бис (аминоэтиловый эфир) Ν,Ν,Ν’,Ν'-тетрауксусная кислота (EGTA), 1мМ PMSF (фенилметилсульфонилфторид); PMSF добавляли непосредственно перед применением из свежеприготовленного 100мМ раствора в метаноле) с использованием 1мл HNTG/PMSF на 10 миллионов клеток. Суспензию центрифугировали в течение 10 минут при 13000об/мин при 4°С, супернатант (запас фермента) удаляли и хранили в виде аликвотных проб при -70°С. Каждую новую пробу фермента из запаса титровали при анализе путем разведения разбавителем фермента (100мМ Hepes рН 7,4, 0,2мМ Na3VO 4, 0,1% о/о Triton X100, 0,2мМ дитиотреит). Для типичной пробы фермент разводят в отношении 1 к 2000 разбавителем фермента и для каждой ячейки для анализа используют 50мкл разведенного фермента. Приготавливали запас субстратного раствора из произвольного сополимера, содержащего тирозин, например, Поли-(Глу, Ала, Тир) 6:3:1 (Sigma P3899) , хранили в PBS (1мг/мл) при -20°С и разводили посредством PBS в отношении 1 к 500 для покрытия пластин. За день до испытания 100мкл разбавленного субстратного раствора распределяли по всем ячейкам пластин для анализа (иммунопластины Nunc maxisorp с 96 ячейками) и, закрыв их, оставляли на ночь при 4°С. В день испытания субстратный раствор удаляли и ячейки пластин промывали один раз PBST (PBS, содержащий 0,05% о/о Tween 20) и один раз 50мМ Hepes с рН 7,4. Испытуемые соединения разводили 10% диметилсульфоксидом (ДМСО) и 25мкл разведенного соединения переносили в ячейки в промытых пластинах. Все контрольные ячейки содержали 10% ДМСО вместо соединения. Двадцать пять микролитров 40мМ МnСl2, содержавшего 8мкм аденозин-5'-трифосфата (АТФ, АТР), добавляли во "все" ячейки, исключая "пустые" контрольные ячейки, которые содержали МnСl2 без АТФ. Чтобы начать реакции, в каждую ячейку добавляли 50мкл свежеразведенного фермента, и пластины инкубировали при комнатной температуре в течение 20 минут. Затем жидкость выливали и промывали ячейки два раза PBST. В каждую ячейку добавляли сто микролитров мышиного антитела к фосфо тирозину IgG (Upstate Biotechnology Inc., продукт 05-321), разведенного в отношении 1 к 6000 посредством PBST, содержавшего 0,5% м/о бычьего сывороточного альбумина (BSA), и пластины инкубировали в течение 1 часа при комнатной температуре, после чего жидкость выливали и ячейки промывали два раза PBST. Добавляли сто микролитров связанного с пероксидазой хрена (HRP) овечьего антитела к мышиному Ig (Amersham, продукт NXA 931), разведенного в отношении 1 к 500 посредством PBST, содержавшего 0,5% м/о BSA, и пластины инкубировали в течение 1 часа при комнатной температуре, после чего жидкость выливали и промывали ячейки два раза PBST. В каждую ячейку добавляли сто микролитров раствора 2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновой кислоты) (ABTS), свежеприготовленного с использованием одной 50мг таблетки ABTS (Boehringer 1204 521) в 50мл свежеприготовленной смеси 50мМ фосфатцитратный буфер + 0,03% пербората натрия (полученной из одной капсулы (Sigma P4922) с фосфа тцитратным буфером и перборатом натрия (PCSB) на 100мл дистиллированной воды). Затем пластины инкубировали в течение 20-60 минут при комнатной температуре, пока значение оптической плотности "всех" контрольных ячеек, измеренное при 405нм с использованием спектрофотометра для считывания с пластин, не составило приблизительно 1,0. Значения в "пусты х" (без АТФ) и "всех" (без соединения) контрольных ячейках использовали для определения степени разведения испытуемого соединения, которая дала 50% ингибирование ферментативной активности. (b) Анализ пролиферации клеток HUVEC in vitro Этот анализ определяет способность испытуемого соединения ингибировать стимулированное ростовым фактором разрастание эндотелиальных клеток пупочной вены человека (HUVEC). Клетки HUVEC выделяли в MCDB 131 (Gibco BRL) + 7,5% о/о сыворотки плодного теленка (FCS) и высевали (при пассаже 2-8) в MCDB 131 + 2% о/о FCS + 3мкг/мл гепарина + 1мкг/мл гидрокортизона при концентрации 1000 клеток на ячейку в пластинах с 96 ячейками. Минимум через 4 часа загружали соответствующий ростовой фактор (а именно VEGF 3нг/мл, EGF 3нг/мл или b-FGF 0,3нг/мл) и соединение. Затем культуры инкубировали в течение 4 дней при 37°С с 7,5% СО2. На четвертый день культуры подвергали импульсному воздействию (1мкКи/ячейку) меченого тритием тимидина (Amersham, продукт TRA 61) и инкубировали в течение 4 часов. Собирали клетки с помощью устройства (Tomtek) для сбора клеток с пластин с 96 ячейками и затем анализировали на инкорпорирование трития с помощью бетасчетчика. Инкорпорирование радиоактивности в клетки, выраженное в срm (отсчеты в минуту), использовали для измерения ингибирования соединениями пролиферации клеток, стимулированной ростовым фактором. (с) Анализ in vi vo отёка матки крысы Это испытание определяет меру способности соединений уменьшать резкое увеличение массы матки у крыс, которое происходит в первые 4-6 часов после эстрогенной стимуляции. Это преждевременное увеличение массы матки обусловлено, как давно известно, отёком, вызванным повышенной проницаемостью сосудистой сети матки, и недавно Cullinan-Bove and Koos (Endocrinology, 1993, 133: 829837) продемонстрировали тесную временнуюсвязь мРНК в матке с повышенной экспрессией VEGF. Данные изобретатели обнаружили, что предшествующее введение крысам нейтрализующего моноклонального антитела к VEGF существенно уменьшает резкое увеличение массы матки, что подтверждает значительное влияние VEGF на увеличении массы. Группе крыс 20-22-дневного возраста вводили одну подкожную дозу эстрадиолбензоата (2,5мкг/крысу) в растворителе или только растворитель. В последнем случае эти были контрольные группы нестимулированных крыс. В различные моменты до введения эстрадиолбензоата перорально вводили испытуемые соединения. Через пять часов после введения эстрадиолбензоата крысы были гуманным образом умерщвлены и их матки были вырезаны, осушены промокательной бумагой и взвешены. Использовав тест Student T, сравнивали увеличение массы матки в группах, обработанных испытуемым соединением и эстрадиолбензоатом и только эстрадиолбензоатом. Ингибирование эффекта эстрадиолбензоата считали существенным при p
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinazoline derivatives, a method for preparing thereof (variants), a pharmaceutical composition and a method for obtaining an antiangiogenic effect and/or effect of vascular permeability
Назва патенту російськоюПроизводные хиназолина, способ их получения (варианты), фармацевтическая композиция и способ получения антиангиогенного эффекта и/или эффекта снижения сосудистой проницаемости
Автори російськоюThomas, Andrew, Peter
МПК / Мітки
МПК: C07D 409/12, A61K 31/517, A61P 9/00, C07D 239/88, C07D 401/12, C07D 417/12, C07D 413/12, C07D 403/12, C07D 239/94
Мітки: судинної, фармацевтична, похідні, варіанти, композиція, проникності, антиангіогенного, спосіб, одержання, зниження, ефекту, хіназоліну
Код посилання
<a href="https://ua.patents.su/52-64704-pokhidni-khinazolinu-sposib-kh-oderzhannya-varianti-farmacevtichna-kompoziciya-ta-sposib-oderzhannya-antiangiogennogo-efektu-ta-abo-efektu-znizhennya-sudinno-proniknosti.html" target="_blank" rel="follow" title="База патентів України">Похідні хіназоліну, спосіб їх одержання (варіанти), фармацевтична композиція та спосіб одержання антиангіогенного ефекту та/або ефекту зниження судинної проникності</a>
Попередній патент: Рухомий біофільтр “українська зірка”
Наступний патент: Запірно-стискаючий механізм до випускного пристрою, що приводиться в дію за допомогою пружини
Випадковий патент: Спосіб формування сечоприймача
























































