Похідні n-(арилсульфоніл)бета-амінокислот, які містять заміщену амінометильну групу, спосіб їх отримання та фармацевтична композиція, що містить їх
Номер патенту: 75906
Опубліковано: 15.06.2006
Автори: Сарран Ліонель, уґа Жан, Феррарі Бернар, Мюно Іветт, Перро П'єр
Формула / Реферат
1. Сполука формули:
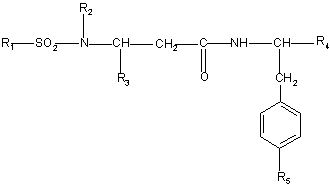 , (І)
, (І)
в якій:
R1 - фенілвінільна група; фенільна група, незаміщена або одно- або багаторазово заміщена R6, які можуть бути однаковими або різними; нафтильна група, незаміщена або одно- або багаторазово заміщена R6, які можуть бути однаковими або різними; тетрагідронафтильна група; нафто[2,3-d][1,3]діоксол-6-ільна група; гетероциклічний радикал, вибраний з хінолілу, ізохінолілу, 1-бензофур-2-илу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3-бензотіадіазол-4-ілу, 1,3- бензотіазол-2-ілу, 1-бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5-ізоксазолтієн-2-ілу, бензотієн-2-ілу, тієнo[3,2-c]пірид-2-илу; причому зазначені гетероциклічні радикали незаміщені або одно- або багаторазово заміщені R6, які можуть бути однаковими або різними;
R2 - гідроген або (C1-C4)алкільна група, а R3 - фенільна група, незаміщена або одно- або багаторазово заміщена R7, які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу, 2,1,3-бензотіадіазол-5-ілу, 2,1,3-бензоксaдіазол-5-ілу, бензотіофен-5-ілу, 2,3- дигідробензо[1,4]діоксин-6-ілу, бензофурилу, дигідробензофурилу, 1,3-тіазол-2-ілу, фурилу і тієнілу, причому зазначений гетероциклічний радикал є незаміщеним або одно- або багаторазово заміщеним атомом галогену або (C1-C4)алкільною групою;
або, як варіант, R2 - фенільна група, незаміщена або одно- або багаторазово заміщена R6, які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу, піридилу та інданілу, а R3 - гідроген;
R4 - група -CONR8R9; група -CSNR8R9; група -COR13; фенільна, незаміщена або одно- або багаторазово заміщена R10; гетероциклічний радикал, вибраний з піридилу, імідазолілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і бензо[1,3]діоксол-5-ілу, причому зазначені радикали є незаміщеними або заміщеними один або більше разів метильними групами або атомами галогену;
R5 - група -CН2NR11R12 або -CH2N(O)NR11R12;
R6 - атом галогену; (C1-C4)алкільна група; трифлуорметильна група; (C1-C4)алкоксигрупа; 2-флуоретоксигрупа; трифлуорметокси-, метилендіокси- або дифлуорметилендіоксигрупа;
R7 - атом галогену; (C1-C4)алкільна група; фенільна група; трифлуорметильна група; (C1-C4)алкоксигрупа; бензилоксигрупа; трифлуорметоксигрупа;
R8 і R9 кожний незалежно - гідроген; (C1-C4)алкільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; w-(C1-C4)діалкіламіно(C2-C4)алкільна група;
або, як варіант, R8 і R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний з піролідинілу, морфолін-4-ілу, тіоморфолін-4-ілу, азепін-1-ілу, піперидилу, незаміщеного або заміщеного одним або більше атомами галогену або одним або більше (C1-C4)алкільними, (C1-C4)алкокси- або трифлуорметильними групами, 3,4-дигідропіперид-1-илу, циклогексил-спіро-4-піперид-1-илу, і піперазинілу, незаміщеного або заміщеного одним або більше (C1-C4)алкільними групами;
R10 - атом галогену; (C1-C4)алкільна група; гідроксигрупа; (C1-C6)алкоксигрупа; а також R10 може бути групою -CH2NR11R12, коли R5 - група -CH2NR11R12, і тоді ці групи є ідентичними;
R11 і R12 кожний незалежно - гідроген; (C1-C6)алкільна група; (C2-C4)алкенільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; ![]() -гідроксі(C2-C4)алкіленова група;
-гідроксі(C2-C4)алкіленова група; ![]() -метоксі(C2-C4)алкіленова група;
-метоксі(C2-C4)алкіленова група; ![]() -трифлуорметил(C2-C4)алкіленова група;
-трифлуорметил(C2-C4)алкіленова група; ![]() -галоген(C2-C4)алкіленова група,
-галоген(C2-C4)алкіленова група,
або, як варіант, R11 і R12 разом з атомом нітрогену, до якого вони приєднані, утворюють моноциклічний, дициклічний або гетероциклічний радикал, вибраний з ацетидинілу, піролідинілу, морфолін-4-ілу, тіоморфолін-4-ілу, піперид-1-илу, піперазин-1-ілу, 1,2,3,6-тетрагідропірид-1-илу, 2,3,4,5-тетрагідропіридинію, декагідрохінолілу, декагідроізохінолілу, тетрагідроізохінолілу, октагідро-1Н-ізоіндолілу, (C4-C6)циклоалкіл-спіро-піперидилу, 3-азабіцикло[3,1,0]гексилу і 7-азабіцикло[2,2,1]гептан-7-ілу, незаміщеного або заміщеного один або більше разів атомом галогену або (C1-C4)алкілом, гідроксилом, (C1-C4)алкоксигрупою, трифлуорметильною, дифлуорметиленовою або фенільною групою;
R13 - феніл, тіазол-2-ільна або піридильна група;
а також її солі з неорганічними або органічними кислотами і/або її сольвати і/або гідрати.
2. Сполука за п. 1, яка відрізняється тим, що має формулу:
 , (Іа)
, (Іа)
в якій:
R1 - фенілвінільна група; фенільна група, незаміщена або заміщена один або більше разів R6, які можуть бути однаковими або різними; нафтильна група, незаміщена або заміщена один або більше разів R6, які можуть бути однаковими або різними; тетрагідронафтильна група; гетероциклічний радикал, вибраний з хінолілу, 1-бензофур-2-илу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3-бензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1-бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5-ізоксазолотієн-2-ілу, бензотієн-2-ілу, тієнo[3,2-c]пірид-2-илу; нафто[2,3-d][1,3]діоксол-6-ілу; причому зазначені гетероциклічні радикали є незаміщеними або заміщеними один або більше разів R6, які можуть бути однаковими або різними;
R2 - гідроген або (C1-C4)алкільна група, а R3 - фенільна група, незаміщена або заміщена один або більше разів R7, які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу, незаміщеного або заміщеного в позиції 2 двома атомами флуору; 2,1,3-бензотіадіазол-5-ілу; 2,3-дигідробензо[1,4]діоксин-6-ілу; 1,3-тіазол-2-ілу; 1-бензофур-2-илу; 1-бензофур-5-илу; фурилу; тієн-2-ілу; тієн-3-ілу;
або R2 - фенільна група, незаміщена або заміщена один або більше разів R6, які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу; піридилу; інданілу; а R3 - гідроген;
R4 - група -CONR8R9; фенільна група, незаміщена або заміщена один або більше разів R10; гетероциклічний радикал, вибраний з піридилу, імідазолілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і бензо[1,3]діоксол-5-ілу, причому зазначені радикали є незаміщеними або заміщеними метилом;
R5 - група -CH2NR11R12;
R6 - атом галогену; (C1-C4)алкільна група; трифлуорметильна група; (C1-C4)алкоксильна група; 2-флуоретоксигрупа; трифлуорметокси-, метилендіокси- або дифлуорметилендіокси група;
R7 - атом галогену; (C1-C4)алкільна група; трифлуорметильна група; (C1-C4)алкоксильна група; бензилоксигрупа; трифлуорметоксигрупа;
R8 і R9 кожний незалежно - гідроген; (C1-C4)алкільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; w-(C1-C4)діалкіламіно(C2-C4)алкільна група;
або R8 і R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний з піролідинілу, піперидилу, морфолін-4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, 4-метилпіперазин-1-ілу, 4-метилпіперид-1-илу, 2-метилпіперид-1-илу, 4,4-диметилпіперид-1-илу, 4,4-дифлуорпіперид-1-илу, 4-трифлуорметилпіперид-1-илу, 3,4-дигідропіперид-1-илу, азепін-1-ілу і циклогексил-спіро-4-піперид-1-илу;
R10 - атом галогену; (C1-C4)алкільна група; гідроксильна група; (C1-C6)алкоксильна група; R10 може також бути групою -CH2NR11R12, коли R5 - група -CH2NR11R12 і тоді зазначені групи є ідентичними;
R11 і R12 кожна незалежно - гідроген; (C1-C6)алкільна група; (C2-C4)алкенільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; w-гідроксі(C2-C4)алкіленова група; w-метоксі(C2-C4)алкіленова група; w-трифлуорметил(C2-C4)алкіленова група; w-галоген(C2-C4)алкіленова група;
або R11 і R12 разом з атомом нітрогену, до якого вони приєднані, утворюють моноциклічний, дициклічний або гетероциклічний радикал, вибраний з ацетидинілу, піролідинілу, морфолін-4-ілу, тіоморфолін-4-ілу, піперид-1-ілу, піперазин-1-илу, 1,2,3,6-тетрагідропірид-1-илу, декагідрохінолілу, декагідроізохінолілу, октагідро-1Н-ізоіндолілу, (C4-C6)циклоалкіл-спіро-піперидилу і 3-азабіцикло[3,1,0]гексилу, незаміщеного або заміщеного один або більше разів атомом галогену або (C1-C4)алкільною, гідроксильною, (C1-C4)алкоксильною, трифлуорметильною, дифлуорметиленовою або фенільною групою;
а також її солі з неорганічними або органічними кислотами і/або її сольвати або гідрати.
3. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що у ній:
R1 - 2,4-дихлор-3-метилфенільна, нафтильна, 6-метоксинафт-2-ильна, 3-метилбензотіофен-2-ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3-метил-5-метоксибензотіофен-2-ільна, 3-метил-6-метоксибензотіофен-2-ільна або 3-метил-1-бензофур-2-ильна група.
4. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що у ній:
R2 - гідроген, а R3 - бензо[1,3]діоксол-5-ільна або фенільна група, незаміщена або заміщена галогеном.
5. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що у ній:
R4 - група -CONR8R9, а -NR8R9 - ді(C1-C4)алкіламінний радикал, піролідинільна або піперидильна група, незаміщена або заміщена одноразово або двічі метилом або галогеном.
6. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що у ній:
R5 - група -CH2NR11R12, у якій -NR11R12 - етилізобутиламіногрупа, етилiзопропіламіногрупа, етил-трет-бутиламіногрупа, діізoпропіламіногрупа циклопентилметиламінний або циклопентилетиламінний радикал, або піперидильний радикал, незаміщений або заміщений один або більше разів метилом або галогеном.
7. Сполука за п. 1 або п. 2, яка відрізняється тим, що має формулу:
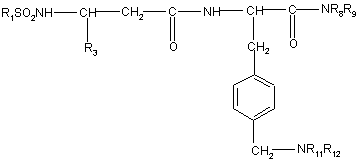 , (Ia)
, (Ia)
в якій:
R1 - 2,4-дихлор-3-метилфенільна, нафтильна, 6-метоксинафт-2-ильна, 3-метил-бензотіофен-2-ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3-метил-5- метоксибензотіофен-2-ільна, 3-метил-6-метоксибензотіофен-2-ільна або 3-метил-1-бензофур-2-ильна група;
R3 - бензо[1,3]діоксол-5-ільна або фенільна група, незаміщена або заміщена галогеном;
R8 і R9 разом з атомом нітрогену, до якого вони приєднані, утворюють ді(C1-C4)алкіламіногрупу, піролідинільний або піперидильний радикал, незаміщений або заміщений одноразово або двічі метилом або галогеном;
R11 i R12 разом з атомом нітрогену, до якого вони приєднані, утворюють етилізобутиламіногрупу, етилiзoпропіламіногрупу, етил-трет-бутиламіногрупу, діізoпропіламіногрупу, циклопентилметиламінний або циклопентилетиламінний радикал або піперидильний радикал, незаміщений або заміщений один або більше разів метилом або галогеном;
а також її солі з неорганічними або органічними кислотами і/або сольвати або гідрати.
8. Сполука за п. 1, яка відрізняється тим, що її вибрано з групи, яку складають:
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6-метокси-2-нафтил)сульфоніл)аміно)-пропаноїл)-аміно)-3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2-нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(4-((циклопентил(етил)аміно)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-2-((3-(((6-метокси-2-нафтил)-сульфоніл)аміно)-3-фенілпропаноїл)аміно)-N-ізопропіл-N-метилпропанамід;
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6-метокси-2-нафтил)сульфоніл)аміно)-пропаноїл)аміно)-3-(4-((трет-бутил(етил)аміно)метил)феніл)-N-ізопропіл-N-метил-пропанамід;
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил-1-бензотіофен-2-іл)сульфоніл)-аміно)пропаноїл)аміно)-3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-2-((3-(((5-метокси-3-метил-1-бензотіофен-2-іл)сульфоніл)аміно)-3-фенілпропаноїл)аміно)-N-iзoпропіл-N-метилпропанамід;
-(R,R)N-(4-((2,6-цис-диметил-1-піперидил)метил)бензил)-3-(((6-метокси-2-нафтил)-сульфоніл)аміно)-3-феніл-N-(1-піперидилкарбоніл)пропанамід;
-(R,R)2-((3-(4-хлорфеніл)-3-(((6-метокси-2-нафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-2-((3-(((6-метокси-2- нафтил)сульфоніл)аміно)-3-фенілпропаноїл)аміно)-N,N-діетилпропанамід;
-(R,R)2-((3-(3-флуорфеніл)-3-(((6-метокси-2-нафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил-1-бензофур-2-ил)сульфоніл)аміно)-пропаноїл)аміно)-3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2-нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(3-((трет-бутил(етил)аміно)метил)феніл)-N-ізопропіл-N-метилпропанамід;
-(R,R)3-(4-(7-азабіцикло[2,2,1]гепт-7-илметил)феніл)-2-((3-(1,3-бензодіоксол- 5-іл)-3-(((6-метоксинафтил)сульфоніл)аміно)пропаноїл)аміно)-N-ізопропіл-N-метилпропанамід;
а також її солі і/або її сольвати і/або гідрати.
9. Спосіб отримання сполуки формули (І), її солі і/або її сольватів або гідратів, який відрізняється тим, що:
кислоту або функціональне похідне цієї кислоти формули:
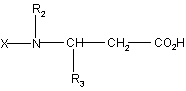 , (II)
, (II)
де R2 і R3 визначено, як для сполук формули (I) п. 1, а X - або гідроген, або група R1-SO2-, у якій R1 визначено, як для сполук формули (I) п. 1, або N-захисна група,
вводять в реакцію зі сполукою формули:
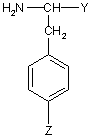 , (III)
, (III)
у якій Y - або R4, визначена, як для сполук формули (I) п. 1, або (C1- C4)алкоксикарбоніл, а Z - або R5, визначена, як для сполук формули (I) п. 1, або -CN-група, за умови, що, коли Y є R4, яка є фенілом, заміщеним групою -CH2NR11R12, Z є R5, яка є групою -CH2NR11R12, а R11 і R12 визначено, як для сполук формули (I) п. 1; і
коли X - R1SO2-, Y - R4, а Z - R5, одержують бажану сполуку формули (I);
або коли X не R1SО2 і/або Y не R4, і/або Z не R5, тобто коли щонайменше одна з груп X, Y і Z, репрезентована як X - H або N-захисна група, Y - (C1-C4)алкоксикарбоніл, Z –
-CN, сполуку, отриману таким чином, формули:
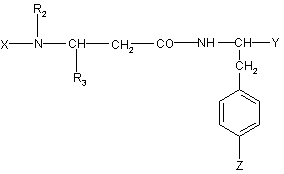 (IV)
(IV)
піддають одній або більше з таких стадій:
- якщо X - N-захисна група, цю групу видаляють, сполуку, одержану таким чином, формули:
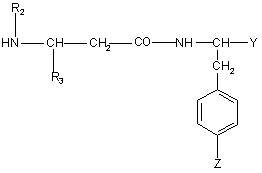 (V)
(V)
вводять у реакцію з сульфонілгалогенідом формули:
R1SO2-Hal, (VI)
де Hal - галоген;
- якщо Y -(C1-C4)алкоксикарбоніл, його гідролізують і одержану таким чином кислоту або функціональне похідне цієї кислоти формули:
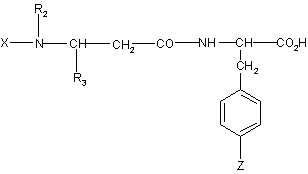 (VII)
(VII)
вводять у реакцію зі сполукою формули:
HNR8R9, (VІІІ)
у якій R8, R9 визначено, як для сполук формули (I) п. 1;
- якщо Z - -CN-група, цю групу перетворюють у R5.
10. Сполука формули:
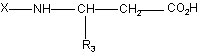 , (IIa)
, (IIa)
у якій:
Х - гідроген або N-захисна група;
R3 - гетероциклічний радикал, вибраний з: (2,2-дифлуор)бензо[1,3]діоксол-5-ілу, 3-ізопропілфенілу, 3-трифлуорметоксифенілу, 2,1,3-бензоксадіазол-5-ілу, бензотіофен-5-ілу, 1-бензофур-6-илу, 1-бензофур-4-илу, 1-бензофур-3-метил-5-ілу, 2,3-дигідробензофур-4-илу;
а також її солі з неорганічними або органічними кислотами, у рацемічній формі або у формі чистих енантіомерів.
11. Сполука формули:
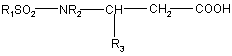 , (IIb)
, (IIb)
у якій:
R1 - фенілвініл; гетероцикл, вибраний з 1-бензофур-2-илу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3-бензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1-бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5-ізоксазолтієн-2-ілу, бензотієн-2-ілу, тієнo[3,2-c]пірид-2-илу; нафтo[2,3-d][1,3]діоксол-6-ілу; причому ці гетероцикли є незаміщеними або заміщеними один або більше разів R6, які можуть бути однаковими або різними;
R2 - гідроген або (C1-C4)алкіл, а R3 - феніл, незаміщений або заміщений один або більше разів R7, які можуть бути однаковими або різними; гетероциклічний радикал вибраний з бензо[1,3]діоксол-5-ілу, незаміщеного або заміщеного у положенні 2 двома атомами флуору; 2,1,3-бензотіадіазол-5-ілу; 2,1,3-бензоксадіазол-5-ілу; бензотіофен-5-ілу; 2,3-дигідробензо[1,4]діоксин-6-ілу; 1-бензофур-2-илу; 1-бензофур-5-илу; 1-бензофур-6-илу; 1-бензофур-4-илу; 1-бензофур-3-метил-5-ілу; 2,3-дигідробензофур-4-илу; 1,3-тіазол-2-ілу; фурилу; тієн-2-ілу; тієн-3-ілу;
або R2 - феніл, незаміщений або заміщений один або більше разів R6, які можуть бути однаковими або різними; бензо[1,3]діоксол-5-іл; піридил; інданіл; а R3 - гідроген;
R6 - атом галогену; (C1-C4)алкільна група; трифлуорметильна група; (C1-C4)алкоксильна група; 2-флуоретокси-; трифлуорметокси-, метилендіокси- або дифлуорметилендіоксигрупа;
R7 - атом галогену; (C1-C4)алкільна група; фенільна група; трифлуорметильна група; (C1-C4)алкоксильна група; бензилоксигрупа; трифлуорметоксигрупа;
за умови, що, коли R1 - 2,1,3-бензотіадіазол-4-іл, а R3 не є фурилом;
а також її солі з неорганічними або органічними кислотами, у рацемічній формі або у формі чистих енантіомерів.
12. Сполука формули:
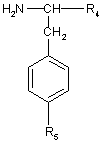 , (III’)
, (III’)
у якій:
R4 - група -CONR8R9; група CSNR8R9; група COR13; феніл, незаміщений або заміщений один або більше разів R10; гетероциклічний радикал, вибраний з піридилу, імідазолілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і бензо[1,3]діоксол-5-ілу, причому ці радикали є незаміщеними або заміщеними метилом;
R5 - група -CH2NR11R12 або -CH2N(О)NR11R12;
R8, R9 - кожний незалежно - гідроген; (C1-C4)алкільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; w-(C1-C4)діалкіламіно((C2-C4)алкільна група;
або, як варіант, R8, R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний з піролідинілу, піперидилу, морфолін-4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, 4-метилпіперазин-1-ілу, 4-метилпіперид-1-илу, 2-метилпіперид-1-илу, 4,4-диметилпіперид-1-илу, 4,4-дифлуорпіперид-1-илу, 4-трифлуорметилпіперид-1-илу, 4-метоксипіперид-1-илу, 3,4-дигідропіперид-1-илу, азепін-1-ілу і циклогексил-спіро-4-піперид-1-илу;
R10 - атом галогену; (C1-C4)алкільна група; гідроксигрупа; (C1-C6)алкоксигрупа; R10 може також бути групою -CH2NR11R12, коли R5 - група -CH2NR11R12, і тоді ці групи є ідентичними;
R11 i R12 кожний незалежно - гідроген; (C1-C6)алкільна група; (C2-C4)алкенільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; w-гідроксі(C2-C4)алкіленова група; w-метоксі(C2-C4)алкіленова група; w-трифлуорметил(C2-C4)алкіленова група; w-галоген(C2-C4)алкіленова група;
або, як варіант, R11 i R12 разом з атомом нітрогену, до якого вони приєднані, утворюють моноциклічний або дициклічний гетероциклічний радикал, вибраний з ацетидинілу, піролідинілу, морфолін-4-ілу, тіоморфолін-4-ілу, піперид-1-илу, піперазин-1-ілу, 1,2,3,6-тетрагідропірид-1-илу, 2,3,4,5-тетрагідропіридинію, декагідрохінолілу, декагідроізохінолілу, тетрагідроізохінолілу, октагідро-1Н-ізоіндолілу, (C4-C6)циклоалкіл-спіро-піперидилу, 3-азабіцикло[3,1,0]гексилу і 7-азабіцикло[2,2,1]гептан-7-ілу, незаміщеного або заміщеного один або більше разів атомом галогену або (C1-C4)алкільною, гідроксигрупою, (C1-C4)алкокси-, трифлуорметильною або дифлуорметиленовою групою;
R13 - фенільна, тіазол-2-ільна або піридильна група;
а також її солі з неорганічними або органічними кислотами, у формі рацемічної суміші або чистих енантіомерів.
13. Фармацевтична композиція, що містить як активний агент сполуку за будь-яким з пп. 1-8 або одну з її фармацевтично прийнятних солей і/або сольватів, і/або гідратів.
14. Медичний продукт, який відрізняється тим, що містить сполуку за будь-яким з пп. 1-8.
15. Використання сполуки за будь-яким з пп. 1-8 або одної з її фармацевтично прийнятних солей і/або сольватів, і/або гідратів для отримання медичних продуктів, призначених для лікування брадикінінозалежної патології.
16. Використання за п. 15 для отримання медичних продуктів, призначених для лікування запальних патологій і стійких або хронічних запальних хвороб.
Текст
1. Сполука формули: R2 R1 SO2 N CH R3 CH2 C O NH CH CH2 R5 R4 (І) , в якій: R1 - фенілвінільна група; фенільна група, н езаміщена або одно- або багаторазово заміщена R 6 , які можуть бути однаковими або різними; нафтильна група, незаміщена або одноабо багаторазово заміщена R6 , які можуть бути однаковими або різними; тетрагідронафтильна група; нафто[2,3-d][1,3]діоксол-6-ільна група; гетероциклічний радикал, вибраний з хінолілу, ізохінолілу, 1-бензофур-2-илу, 2,1,3-бензоксадіазол-4ілу, 2,1,3-бензотіадіазол-4-ілу, 1,3- бензотіазол-2ілу, 1-бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2ілу, 5-ізоксазолтієн-2-ілу, бензотієн-2-ілу, тієнo[3,2c]пірид-2-илу; причому зазначені гетероциклічні радикали незаміщені або одно- або багаторазово заміщені R6 , які можуть бути однаковими або різними; R2 - гідроген або (C1-C4)алкільна група, а R3 - фенільна група, незаміщена або одно- або багаторазово заміщена R 7 , які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу, 2,1,3бензотіадіазол-5-ілу, 2,1,3-бензоксaдіазол-5-ілу, бензотіофен-5-ілу, 2,3- дигідробензо[1,4]діоксин-6ілу, бензофурилу, дигідробензофурилу, 1,3тіазол-2-ілу, фурилу і тієнілу, причому зазначений гетероциклічний радикал є незаміщеним або одно- або багаторазово заміщеним атомом галогену або (C1-C4)алкільною групою; або, як варіант, R2 - фенільна група, незаміщена або одно- або багаторазово заміщена R 6 , які можуть бути однаковими або різними; гетероциклічний радикал, вибраний з бензо[1,3]діоксол-5-ілу, піридилу та інданілу, а R3 гідроген; R4 - група -CONR 8 R 9 ; група -CSNR 8 R 9 ; група COR 13 ; фенільна, незаміщена або одно- або багаторазово заміщена R 10 ; гетероциклічний радикал, вибраний з піридилу, імідазолілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і бензо[1,3]діоксол-5-ілу, причому зазначені радикали є незаміщеними або заміщеними один або більше разів метильними групами або атомами галогену; R5 - група -CН2NR11R12 або -CH2N(O)NR11R12; R6 - атом галогену; (C1-C4)алкільна група; трифлуорметильна група; (C1-C4)алкоксигрупа; 2флуоретоксигрупа; трифлуорметокси-, метилендіокси- або дифлуорметилендіоксигрупа; R7 - атом галогену; (C1-C4)алкільна група; фенільна група; трифлуорметильна група; (C1C4)алкоксигрупа; бензилоксигрупа; трифлуорметоксигрупа; R8 і R9 кожний незалежно - гідроген; (C1C4)алкільна група; (C3-C7)циклоалкільна група; (C3 4 C7)циклоалкіл(C1-C4)алкільна група; -(C1C4)діалкіламіно(C2-C4)алкільна група; або, як варіант, R8 і R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний з піролідинілу, морфолін-4ілу, тіоморфолін-4-ілу, азепін-1-ілу, піперидилу, незаміщеного або заміщеного одним або більше атомами галогену або одним або більше (C1C4)алкільними, (C1-C4)алкокси- або трифлуорметильними групами, 3,4-дигідропіперид-1-илу, циклогексил-спіро-4-піперид-1-илу, і піперазинілу, незаміщеного або заміщеного одним або більше (C1-C4)алкільними групами; R10 - атом галогену; (C1-C4)алкільна група; гідроксигрупа; (C1-C6)алкоксигрупа; а також R10 може бути групою -CH 2 NR 11 R 12 , коли R 5 - група CH 2 NR 11 R 12 , і тоді ці групи є ідентичними; R11 і R12 кожний незалежно - гідроген; (C1C6)алкільна група; (C2-C4)алкенільна група; (C3C7)циклоалкільна група; (C3-C7)циклоалкіл(C1C4)алкільна група; -гідроксі(C2-C4)алкіленова група; -метоксі(C2-C4)алкіленова група; трифлуорметил(C2-C4)алкіленова група; галоген(C2-C4)алкіленова група, або, як варіант, R11 і R12 разом з атомом нітрогену, до якого вони приєднані, утворюють моноциклічний, дициклічний або гетероциклічний радикал, вибраний з ацетидинілу, піролідинілу, морфолін-4ілу, тіоморфолін-4-ілу, піперид-1-илу, піперазин-1-ілу, 1,2,3,6-тетрагідропірид-1-илу, 2,3,4,5тетрагідропіридинію, декагідрохінолілу, декагідроізохінолілу, тетрагідроізохінолілу, октагідро-1Нізоіндолілу, (C4-C6)циклоалкіл-спіро-піперидилу, 3азабіцикло[3,1,0]гексилу і 7азабіцикло[2,2,1]гептан-7-ілу, незаміщеного або заміщеного один або більше разів атомом галогену або (C1-C4)алкілом, гідроксилом, (C1C4)алкоксигрупою, трифлуорметильною, дифлуорметиленовою або фенільною групою; R13 - феніл, тіазол-2-ільна або піридильна група; а також її солі з неорганічними або органічними кислотами і/або її сольвати і/або гідрати. 2. Сполука за п. 1, яка відрізняється тим, що має формулу: R2 R1 SO2 N CH R3 CH2 C O NH CH CH2 R5 R4 (Іа) , в якій: R1 - фенілвінільна група; фенільна група, незаміщена або заміщена один або більше разів R6, які можуть бути однаковими або різними; нафтильна група, незаміщена або заміщена один або більше разів R6, які можуть бути однаковими або різними; тетрагідронафтильна група; гетероциклічний радикал, вибраний з хінолілу, 1-бензофур2-илу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3бензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5 5 75906 6 ізоксазолотієн-2-ілу, бензотієн-2-ілу, тієнo[3,2азабіцикло[3,1,0]гексилу, незаміщеного або заміc]пірид-2-илу; нафто[2,3-d][1,3]діоксол-6-ілу; прищеного один або більше разів атомом галогену чому зазначені гетероциклічні радикали є незаабо (C1-C4)алкільною, гідроксильною, (C1міщеними або заміщеними один або більше разів C4)алкоксильною, трифлуорметильною, дифлуоR6, які можуть бути однаковими або різними; рметиленовою або фенільною групою; R2 - гідроген або (C1-C4)алкільна група, а R3 - фенільа також її солі з неорганічними або органічними на група, незаміщена або заміщена один або бікислотами і/або її сольвати або гідрати. льше разів R7, які можуть бути однаковими або 3. Сполука формули (І) за п. 1 або п. 2, яка різними; гетероциклічний радикал, вибраний з відрізняється тим, що у ній: бензо[1,3]діоксол-5-ілу, незаміщеного або заміR1 - 2,4-дихлор-3-метилфенільна, нафтильна, 6щеного в позиції 2 двома атомами флуору; 2,1,3метоксинафт-2-ильна, 3-метилбензотіофен-2бензотіадіазол-5-ілу; 2,3-дигідробензо[1,4]діоксин-6ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3ілу; 1,3-тіазол-2-ілу; 1-бензофур-2-илу; 1-бензофурметил-5-метоксибензотіофен-2-ільна, 3-метил-65-илу; фурилу; тієн-2-ілу; тієн-3-ілу; метоксибензотіофен-2-ільна або 3-метил-1або R2 - фенільна група, незаміщена або заміщена бензофур-2-ильна група. один або більше разів R6, які можуть бути однако4. Сполука формули (І) за п. 1 або п. 2, яка вими або різними; гетероциклічний радикал, вибвідрізняється тим, що у ній: раний з бензо[1,3]діоксол-5-ілу; піридилу; інданілу; а R2 - гідроген, а R3 - бензо[1,3]діоксол-5-ільна або R3 - гідроген; фенільна група, незаміщена або заміщена галоR4 - група -CONR8R9; фенільна група, незаміщегеном. на або заміщена один або більше разів R10; гете5. Сполука формули (І) за п. 1 або п. 2, яка роциклічний радикал, вибраний з піридилу, імідазовідрізняється тим, що у ній: лілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і R4 - група -CONR8R9, а -NR8R9 - ді(C1бензо[1,3]діоксол-5-ілу, причому зазначені радикали C4)алкіламінний радикал, піролідинільна або піпеє незаміщеними або заміщеними метилом; ридильна група, незаміщена або заміщена одR5 - група -CH2NR11R12; норазово або двічі метилом або галогеном. R6 - атом галогену; (C1-C4)алкільна група; трифлу6. Сполука формули (І) за п. 1 або п. 2, яка орметильна група; (C1-C4)алкоксильна група; 2відрізняється тим, що у ній: флуоретоксигрупа; трифлуорметокси-, метилендіокR5 - група -CH 2 NR 11R 12, у якій -NR 11R 12 - етилізоси- або дифлуорметилендіокси група; бутиламіногрупа, етилiзопропіламіногрупа, етилR7 - атом галогену; (C1-C4)алкільна група; трифлутрет-бутиламіногрупа, діізoпропіламіногрупа цикорметильна група; (C1-C4)алкоксильна група; бенлопентилметиламінний або циклопентилетиламінзилоксигрупа; трифлуорметоксигрупа; ний радикал, або піперидильний радикал, незаміR8 і R9 кожний незалежно - гідроген; (C1-C4)алкільна щений або заміщений один або більше разів група; (C3-C7)циклоалкільна група; (C3метилом або галогеном. 7. Сполука за п. 1 або п. 2, яка відрізняється C7)циклоалкіл(C1-C4)алкільна група; -(C1тим, що має формулу: C4)діалкіламіно(C2-C4)алкільна група; NR 8R9 C CH NH CH2 C або R 8 і R 9 разом з атомом нітрогену, до якого R1SO2NH CH вони приєднані, утворюють гетероциклічний радиO CH2 O R3 кал, вибраний з піролідинілу, піперидилу, морфолін4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, 4(Ia) метилпіперазин-1-ілу, 4-метилпіперид-1-илу, 2метилпіперид-1-илу, 4,4-диметилпіперид-1-илу, 4,4дифлуорпіперид-1-илу, 4-трифлуорметилпіперид-1илу, 3,4-дигідропіперид-1-илу, азепін-1-ілу і циклогеNR 11R12 CH2 , ксил-спіро-4-піперид-1-илу; в якій: R 10 - атом галогену; (C1-C4)алкільна група; гідрокR1 - 2,4-дихлор-3-метилфенільна, нафтильна, 6сильна група; (C1-C6)алкоксильна група; R 10 мометоксинафт-2-ильна, 3-метил-бензотіофен-2же також бути групою -CH 2 NR 11R 12, коли R 5 ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3група -CH 2 NR 11R 12 і тоді зазначені групи є ідентичметил-5- метоксибензотіофен-2-ільна, 3-метил-6ними; метоксибензотіофен-2-ільна або 3-метил-1R 11 і R 12 кожна незалежно - гідроген; (C1-C6)алкільна бензофур-2-ильна група; група; (C2-C4)алкенільна група; (C3R3 - бензо[1,3]діоксол-5-ільна або фенільна група, C7)циклоалкільна група; (C3-C7)циклоалкіл(C1незаміщена або заміщена галогеном; C4)алкільна група; -гідроксі(C2-C4)алкіленова група; R8 і R9 разом з атомом нітрогену, до якого вони при-метоксі(C2-C4)алкіленова група; єднані, утворюють ді(C1-C4)алкіламіногрупу, піролітрифлуорметил(C2-C4)алкіленова група; -галоген(C2динільний або піперидильний радикал, незаміщеC4)алкіленова група; ний або заміщений одноразово або двічі метилом або R 11 і R 12 разом з атомом нітрогену, до якого або галогеном; вони приєднані, утворюють моноциклічний, диR11 i R12 разом з атомом нітрогену, до якого вони прициклічний або гетероциклічний радикал, вибраний єднані, утворюють етилізобутиламіногрупу, з ацетидинілу, піролідинілу, морфолін-4-ілу, тіоетилiзoпропіламіногрупу, етил-трет-бутиламіногрупу, морфолін-4-ілу, піперид-1-илу, піперазин-1-илу, діізoпропіламіногрупу, циклопентилметиламінний 1,2,3,6-тетрагідропірид-1-илу, декагідрохінолілу, або циклопентилетиламінний радикал або піперидекагідроізохінолілу, октагідро-1Н-ізоіндолілу, (C4C6)циклоалкіл-спіро-піперидилу і 3 7 75906 8 дильний радикал, незаміщений або заміщений 9. Спосіб отримання сполуки формули (І), її солі один або більше разів метилом або галогеном; і/або її сольватів або гідратів, який відрізняється а також її солі з неорганічними або органічними тим, що: кислотами і/або сольвати або гідрати. кислоту або функціональне похідне цієї кислоти 8. Сполука за п. 1, яка відрізняється тим, що її формули: вибрано з групи, яку складають: R2 -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6-метокси-2нафтил)сульфоніл)аміно)-пропаноїл)-аміно)-3-(4CO2H CH CH2 X N (II) ((2,6-цис-диметил-1-піперидил)метил)феніл)-Nізопропіл-N-метилпропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2R3 , нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(4де R2 і R3 визначено, як для сполук формули (I) п. 1, ((циклопентил(етил)аміно)метил)феніл)-N-ізопропіл-Nа X - або гідроген, або група R1-SO2-, у якій R1 виметилпропанамід; значено, як для сполук формули (I) п. 1, або N-(R,R)3-(4-((2,6-цис-диметил-1захисна група, піперидил)метил)феніл)-2-((3-(((6-метокси-2вводять в реакцію зі сполукою формули: нафтил)-сульфоніл)аміно)-3H2N Y CH фенілпропаноїл)аміно)-N-ізопропіл-Nметилпропанамід; CH2 -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6-метокси2-нафтил)сульфоніл)аміно)-пропаноїл)аміно)-3-(4((трет-бутил(етил)аміно)метил)феніл)-N-ізопропіл(III) N-метил-пропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил-1бензотіофен-2-іл)сульфоніл)аміно)пропаноїл)аміно)-3-(4-((2,6-цис-диметил-1Z піперидил)метил)феніл)-N-ізопропіл-N, метилпропанамід; у якій Y - або R4, визначена, як для сполук формули -(R,R)3-(4-((2,6-цис-диметил-1(I) п. 1, або (C1- C4)алкоксикарбоніл, а Z - або R5, випіперидил)метил)феніл)-2-((3-(((5-метокси-3значена, як для сполук формули (I) п. 1, або -CNметил-1-бензотіофен-2-іл)сульфоніл)аміно)-3група, за умови, що, коли Y є R4, яка є фенілом, зафенілпропаноїл)аміно)-N-iзoпропіл-Nміщеним групою -CH2NR11R12, Z є R5, яка є групою метилпропанамід; CH2NR11R12, а R11 і R12 визначено, як для сполук -(R,R)N-(4-((2,6-цис-диметил-1формули (I) п. 1; і піперидил)метил)бензил)-3-(((6-метокси-2-нафтил)коли X - R1SO2-, Y - R4, а Z - R5, одержують бажану сульфоніл)аміно)-3-феніл-N-(1сполуку формули (I); піперидилкарбоніл)пропанамід; або коли X не R1SО2 і/або Y не R4, і/або Z не R5, тоб-(R,R)2-((3-(4-хлорфеніл)-3-(((6-метокси-2то коли щонайменше одна з груп X, Y і Z, репрезеннафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4тована як X - H або N-захисна група, Y - (C1((2,6-цис-диметил-1-піперидил)метил)феніл)-NC4)алкоксикарбоніл, Z – ізопропіл-N-метилпропанамід; -CN, сполуку, отриману таким чином, формули: -(R,R)3-(4-((2,6-цис-диметил-1R2 піперидил)метил)феніл)-2-((3-(((6-метокси-2- нафтил)сульфоніл)аміно)-3-фенілпропаноїл)аміно)NH Y CH N CO CH X CH2 N,N-діетилпропанамід; CH2 -(R,R)2-((3-(3-флуорфеніл)-3-(((6-метокси-2R3 (IV) нафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4((2,6-цис-диметил-1-піперидил)метил)феніл)-Nізопропіл-N-метилпропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил-1бензофур-2-ил)сульфоніл)аміно)-пропаноїл)аміно)Z 3-(4-((2,6-цис-диметил-1-піперидил)метил)феніл)піддають одній або більше з таких стадій: N-ізопропіл-N-метилпропанамід; - якщо X - N-захисна група, цю групу видаляють, -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2сполуку, одержану таким чином, формули: нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(3R2 ((трет-бутил(етил)аміно)метил)феніл)-N-ізопропілN-метилпропанамід; CO NH Y CH CH HN CH2 -(R,R)3-(4-(7-азабіцикло[2,2,1]гепт-7илметил)феніл)-2-((3-(1,3-бензодіоксол5-іл)-3CH2 (((6R3 (V) метоксинафтил)сульфоніл)аміно)пропаноїл)аміно)-Nізопропіл-N-метилпропанамід; а також її солі і/або її сольвати і/або гідрати. Z 9 75906 10 вводять у реакцію з сульфонілгалогенідом формули: або R2 - феніл, незаміщений або заміщений один R1SO2-Hal, (VI) або більше разів R6, які можуть бути однаковими де Hal - галоген; або різними; бензо[1,3]діоксол-5-іл; піридил; інда- якщо Y -(C1-C4)алкоксикарбоніл, його гідролізуніл; а R3 - гідроген; ють і одержану таким чином кислоту або функціR6 - атом галогену; (C 1-C 4)алкільна група; триональне похідне цієї кислоти формули: флуорметильна група; (C 1-C4)алкоксильна група; R2 2-флуоретокси-; трифлуорметокси-, метилендіокси- або дифлуорметилендіоксигрупа; X NH CH R7 - атом галогену; (C1-C4)алкільна група; феніCO2H N CO CH CH2 льна група; трифлуорметильна група; (C1CH2 C4)алкоксильна група; бензилоксигрупа; трифлуоR3 (VII) рметоксигрупа; за умови, що, коли R1 - 2,1,3-бензотіадіазол-4-іл, а R3 не є фурилом; а також її солі з неорганічними або органічними кислотами, у рацемічній формі або у формі чистих Z енантіомерів. вводять у реакцію зі сполукою формули: 12. Сполука формули: HNR8R9, (VІІІ) H2N R4 CH у якій R8, R9 визначено, як для сполук формули (I) п. 1; CH2 - якщо Z - -CN-група, цю групу перетворюють у R5. 10. Сполука формули: CO2H X CH CH2 NH (III’) (IIa) R3 , у якій: Х - гідроген або N-захисна група; R3 - гетероциклічний радикал, вибраний з: (2,2дифлуор)бензо[1,3]діоксол-5-ілу, 3ізопропілфенілу, 3-трифлуорметоксифенілу, 2,1,3бензоксадіазол-5-ілу, бензотіофен-5-ілу, 1бензофур-6-илу, 1-бензофур-4-илу, 1-бензофур-3метил-5-ілу, 2,3-дигідробензофур-4-илу; а також її солі з неорганічними або органічними кислотами, у рацемічній формі або у формі чистих енантіомерів. 11. Сполука формули: COOH CH2 R1SO2 NR 2 CH (IIb) R3 , у якій: R1 - фенілвініл; гетероцикл, вибраний з 1бензофур-2-илу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3бензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5ізоксазолтієн-2-ілу, бензотієн-2-ілу, тієнo[3,2c]пірид-2-илу; нафтo[2,3-d][1,3]діоксол-6-ілу; причому ці гетероцикли є незаміщеними або заміщеними один або більше разів R6, які можуть бути однаковими або різними; R2 - гідроген або (C 1-C4)алкіл, а R 3 - феніл, незаміщений або заміщений один або більше разів R7, які можуть бути однаковими або різними; гетероциклічний радикал вибраний з бензо[1,3]діоксол-5-ілу, незаміщеного або заміщеного у положенні 2 двома атомами флуору; 2,1,3-бензотіадіазол-5-ілу; 2,1,3-бензоксадіазол-5ілу; бензотіофен-5-ілу; 2,3дигідробензо[1,4]діоксин-6-ілу; 1-бензофур-2илу; 1-бензофур-5-илу; 1-бензофур-6-илу; 1бензофур-4-илу; 1-бензофур-3-метил-5-ілу; 2,3дигідробензофур-4-илу; 1,3-тіазол-2-ілу; фурилу; тієн-2-ілу; тієн-3-ілу; R5 , у якій: R4 - група -CONR8R9; група CSNR8R9; група COR13; феніл, незаміщений або заміщений один або більше разів R 10; гетероциклічний радикал, вибраний з піридилу, імідазолілу, фурилу, бензімідазолілу, бензотіазол-2-ілу і бензо[1,3]діоксол5-ілу, причому ці радикали є незаміщеними або заміщеними метилом; R5 - група -CH 2 NR11R12 або -CH 2 N(О)NR11R12; R8, R9 - кожний незалежно - гідроген; (C1C4)алкільна група; (C3-C7)циклоалкільна група; (C3-C7)циклоалкіл(C1-C4)алкільна група; -(C1C4)діалкіламіно((C2-C4)алкільна група; або, як варіант, R8, R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний з піролідинілу, піперидилу, морфолін-4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, 4-метилпіперазин-1-ілу, 4метилпіперид-1-илу, 2-метилпіперид-1-илу, 4,4диметилпіперид-1-илу, 4,4-дифлуорпіперид-1илу, 4-трифлуорметилпіперид-1-илу, 4метоксипіперид-1-илу, 3,4-дигідропіперид-1-илу, азепін-1-ілу і циклогексил-спіро-4-піперид-1-илу; R 10 - атом галогену; (C1-C4)алкільна група; гідроксигрупа; (C1-C6)алкоксигрупа; R 10 мож е також бути групою -CH 2 NR11R12, коли R5 група -CH 2 NR11R12, і тоді ці групи є ідентичними; R11 i R12 кожний незалежно - гідроген; (C1C6)алкільна група; (C2-C4)алкенільна група; (C3C7)циклоалкільна група; (C3-C7)циклоалкіл(C1C4)алкільна група; -гідроксі(C2-C4)алкіленова група; -метоксі(C2-C4)алкіленова група; трифлуорметил(C2-C4)алкіленова група; галоген(C2-C4)алкіленова група; або, як варіант, R11 i R12 разом з атомом нітрогену, до якого вони приєднані, утворюють моноциклічний або дициклічний гетероциклічний 11 75906 12 радикал, вибраний з ацетидинілу, піролідинілу, 13. Фармацевтична композиція, що містить як морфолін-4-ілу, тіоморфолін-4-ілу, піперид-1-илу, активний агент сполуку за будь-яким з пп. 1-8 або піперазин-1-ілу, 1,2,3,6-тетрагідропірид-1-илу, одну з її фармацевтично прийнятних солей і/або 2,3,4,5-тетрагідропіридинію, декагідрохінолілу, сольватів, і/або гідратів. декагідроізохінолілу, тетрагідроізохінолілу, октагід14. Медичний продукт, який відрізняється тим, що ро-1Н-ізоіндолілу, (C4-C6)циклоалкіл-спіромістить сполуку за будь-яким з пп. 1-8. піперидилу, 3-азабіцикло[3,1,0]гексилу і 715. Використання сполуки за будь-яким з пп. 1-8 азабіцикло[2,2,1]гептан-7-ілу, незаміщеного або або одної з її фармацевтично прийнятних солей заміщеного один або більше разів атомом галоі/або сольватів, і/або гідратів для отримання медигену або (C1-C4)алкільною, гідроксигрупою, (C1чних продуктів, призначених для лікування брадиC4)алкокси-, трифлуорметильною або дифлуоркінінозалежної патології. метиленовою групою; 16. Використання за п. 15 для отримання медичR13 - фенільна, тіазол-2-ільна або піридильна груних продуктів, призначених для лікування запальпа; них патологій і стійких або хронічних запальних а також її солі з неорганічними або органічними хвороб. кислотами, у формі рацемічної суміші або чистих енантіомерів. Винахід стосується нових похідних N(арилсульфоніл)бета-амінокислоти, які містять заміщену амінометильну групу, їх отримання і фармацевтичних композицій, що містять їх. Ці композиції мають спорідненість до рецепторів брадикініну (БК). Брадикінін є нонапептидом, що належить, як і калідин, до класу кінінів і виявляє фізіологічну активність у серцево-судинній сфері і як медіатор при запаленні і болю. Кілька рецепторів брадикініну є добре відомими: рецептори В1 i В2 [D. Regoli et al., Pharmacol. Rev., 1980, 32, 1-46]. Зокрема, рецептори В2 є рецепторами брадикініну і калідину: вони є домінуючими і, зокрема, їх знайдено у більшості тканин; рецептори Β1 є рецепторами, специфічними для [дезАrg]брадикініну і [дез-АrG]калідину: вони індукуються у процесі запалення. Рецептори брадикініну були клоновані для різних видів, зокрема для людини: рецептор В1: J.G. Menke et al., J. Biol. Chem., 1994, 269 (34), 2158321586; рецептор В2: J..F. Hess, Biochem. Biophys. Res. Commun., 1992,184. 260-268. Патентна заявка WO 97/25315 описує сполуки формули: у якій: - Rl, Rll, Rlll, RIV, RV, RVI, RVII, RVIII, RIX, RX і RXI мають різні значення. Ці сполуки виявляють спорідненість до рецепторів брадикініну. Було знайдено нові сполуки, які виявляють спорідненість до рецепторів брадикініну з селективністю до рецепторів В1 брадикініну , які є антагоністами рецептора В2 брадикініну і · мають кращу здатність до абсорбції. Ці сполуки можуть бути використані для отри мання медичних продуктів, корисних при лікуванні або попередженні будь-яких патологій, у яких залучено брадикінін і рецептори В2, особливо запальних патологій і стійких або хронічних запальних хвороб. Отже, згідно з одним з його аспектів, об'єктом винаходу є сполуки формули: у якій: R1 - фенілвінільна група; фенільна група, незаміщена або одно- або багаторазово заміщена R6, які можуть бути однаковими або різними; нафтильна група, незаміщена або одно- або багаторазово заміщена R6, які можуть бути однаковими або різними; тетрагідронафтильна група; нафто[2,3d][1,3]діоксол-6-ільна група; гетероциклічний радикал, вибраний серед хінолілу, ізохінолілу, 1бензофур-2-ілу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3бензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5ізоксатіен-2-ілу, бензотієн-2-ілу, тієно[3,2-с]пірид-2ілу;причому зазначені гетероциклічні радикали незаміщеними або одно- або багаторазово заміщені R6, які можуть бути однаковими або різними; R2 - гідроген або (С1-С4)алкільна група, a R3 фенільна група, незаміщена або одно- або багаторазово заміщена R7, які можуть бути однаковими або різними; гетероциклічний радикал, вибраний серед бензо[1,3]діоксол-5-ілу, 2,1,3бензотіадіазол-5-ілу, 2,1,3-бензоксадіазол-5-ілу, бензотіофен-5-ілу, 2,3- дигідробензо[1,4]діоксин-6ілу, бензофурилу, дигідробензофурилу, 1,3-тіазол 13 75906 14 2-ілу, фурилу і тієнілу, причому зазначений гетеС4)алкоксигрупою, трифлуорметильною, дифлуороциклічний радикали незаміщеними або однорметиленовою або фенільною групою; або багаторазово заміщеними атомом галогену R13 - феніл, тіазол-2-ільна або піридильна груабо (С1-С4)алкільною групою; па; або, у іншому варіанті, R2 - фенільна група, а також їх солі з неорганічними або органічнинезаміщена або одно- або багаторазово заміщена ми кислотами і/або сольвати або гідрати. R6, які можуть бути однаковими або різними; гетеТермін "галоген" означає атом флуору, хлору, роциклічний радикал, вибраний серед бенброму або йоду. зо[1,3]діоксол-5-ілу і інданілу, a R3 - гідроген; Терміни "алкіл", "алкілен" і "алкоксил", відповіR4 - група -CONR8R9; група -CSNR8R9; група дно означають лінійний або розгалужений алкільCOR13; фенільна, незаміщена або одно- або баганий радикал, лінійний або розгалужений алкіленоторазово заміщена R10; гетероциклічний радикал, вий радикал або лінійний або розгалужений вибраний серед піридилу, імідазолілу, фурилу, алкоксильний радикал, відповідно. бензімідазолілу, бензотіазол-2-ілу і бенОб'єктом винаходу є також сполуки формули зо[1,3]діоксол-5-ілу, причому зазначені радикали є (І), які містять щонайменше один асиметричний незаміщеними або заміщеними один або більше атом карбону, і чисті енантіомери або діастереоіразів метильними групами або атомами галогену; зомери і їх суміші в усіх пропорціях: R5 - група -CHaNR11R12 або -CH2N(O)NR11R12; R6 - атом галогену; (С1-С4)алкільна група; трифлуорметильна група; (С1-С4)алкоксигрупа; 2флуоретоксигрупа; трифлуорметокси-, метилендіокси- або дифлуорметилендіоксигрупа; R7 - атом галогену; (С1-С4)алкільна група; фенільна група; трифлуорметильна група; (С1С4)алкоксигрупа; бензилоксигрупа; трифлуорметоксигрупа; R8 і R9 кожний незалежно - гідроген; (С1С4)алкільна група; (С3-С7)циклоалкільна група; (С3С7)циклоалкіл(С1-С4)алкільна група; -(С1С4)діалкіламіно(С2-С4)алкільна група; де: або, у іншому варіанті, R8 і R9 разом з атомом - R1 - фенілвінільна група; фенільна група, ненітрогену, до якого вони приєднані, утворюють заміщена або заміщена один або більше разів R6, гетероциклічний радикал, вибраний серед піроліякі можуть бути однаковими або різними; нафтидинілу, морфолін-4-ілу, тіоморфолін-4-ілу, азепінльна група, незаміщена або заміщена один або 1-ілу, піперидилу, незаміщеного або заміщеного більше разів R6, які можуть однаковими або різниодним або більше атомами галогену або одним ми; тетрагідронафтильна група; гетероциклічний або більше (С1-С4)алкільними, (С1-С4)алкокси- або радикал, вибраний серед хінолілу, 1-бензофур-2трифлуорметильними групами, 3,4ілу, 2,1,3-бензоксадіазол-4-ілу, 2,1,3дигідропіперид-1-ілу, циклогексил-спіро-4-піперидбензотіадіазол-4-ілу, 1,3-бензотіазол-2-ілу, 1і-ілу, і піперазинілу, незаміщеного або заміщеного бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2-ілу, 5одним або більше (СгС4)алкільними групами; ізоксазолетієн-2-ілу, бензотієн-2-ілу, тієно[3,2R10 - атом галогену; (С1-С4)алкільна група; гідс]пірид-2-ілу; нафто[2,3-d][1,3]діоксол-6-ілу; прироксигрупа; (С1-С6)алкоксигрупа; а також R10 може чому зазначені гетероциклічні радикали є незамібути групою -CH2NR11R12, коли R5 - група щеними або заміщеними один або більше разів R6, CH2NR11R12, і тоді ці групи є ідентичними; які можуть однаковими або різними; R11 і R12 незалежно - гідроген; (С1-С6)алкільна R2 - гідроген або (С1-С4)алкільна група, a R3 група; (С2-С4)алкенільна група; (С3фенільна група, незаміщена або заміщена один С7)циклоалкільна група; (С3-С7)циклоалкіл(С1або більше разів R7, які можуть бути однаковими С4)алкільна група; -гідрокси(С2-С4)алкіленова або різними; гетероциклічний радикал, вибраний група; ( -метокси(С2-С4)алкіленова група; серед бензо[1,3]діоксол-5-ілу, незаміщеного або трифлуорметил(С2-С4)алкіленова група; заміщеного в позиції 2 двома атомами флуору; галоген(С2-С4)алкіленова група, 2,1,3-бензотіадіазол-5-ілу; 2,3або, у іншому варіанті, R11 і R12 разом з атодигідробензо[1,4]діоксин-6-ілу; 1,3-тіазол-2-ілу; 1мом нітрогену, до якого вони приєднані, утворюбензофур-2-ілу; 1-бензофур-5-ілу; фурилу; тієн-2ють моноциклічний, дициклічний або гетероциклічілу; тієн-3-ілу; ний радикал, вибраний серед ацетидинілу, або R2 - фенільна група, незаміщена або запіролідинілу, морфолін-4-ілу, тіоморфолін-4-ілу, міщена один або більше разів R6, які можуть бути піперид-1-ілу, піперазин-1-ілу, 1,2,3,6однаковими або різними; гетероциклічний радитетрагідропірид-1-ілу, 2,3,4,5-тетрагідропіридинію, кал, вибраний серед бензо[1,3]діоксол-5-ілу; піридекагідрохінолілу, декагідроізохінолілу, тетрагідродилу; інданілу; a R3 - гідроген; ізохінолілу, октагідро-1Н-ізоіндолілу, (С4R4 - група -CONR8R9; фенільна група, незаміС6)циклоалкіл-спіроо-піперидилу, 3щена або заміщена один або більше разів R10; азабіцикло[3,1,0]гексилу і 7гетероциклічний радикал, вибраний серед піридиазабіцикло[2,2,1]гертан-7-ілу, незаміщеного або лу, імідазолілу, фурилу, бензімідазолілу, бензотіазаміщеного одним або більше разів атомом галозол-2-ілу і бензо[1,3]діоксол-5-ілу, причому зазнагену або (С1-С4)алкілом, гідроксилом, (С1 15 75906 16 чені радикали є незаміщеними або заміщеними ди(С1-С4)алкіламінний радикал, бажано, коли Nметилом; метилізопропіловий радикал; піролідинільна або R5- група -CH2NR11R12; піперидильна група, незаміщена або заміщена R6 - атом галогену; (С1-С4)алкільна група; одноразово або двічі метилом або галогеном; R1, трифлуорметильна група; (С1-С4)алкоксильна груR2, R3 і R5 визначено, як для сполук формули (І); па; 2-флуоретоксигрупа; трифлуорметокси-, метиd) R5 - група -CH2NR11R12, у якій -NR11R12 лендіокси- або дифлуорметилендіокси група; етилізобутиламіногрупа, етилізопропіламіногрупа, R7 - атом галогену; (С1-С4)алкільна група; етил-трет-бутиламіногрупа, діізопропіламіногрупа, трифлуорметильна група; (С1-С4)алкоксильна груциклопентилметиламінний або циклопентилетипа; бензилоксигрупа; трифлуорметоксигрупа; ламінний радикал, або піперидиловий радикал, R8 i R9 кожний незалежно - гідроген; (С1незаміщений або заміщений один або більше разів С4)алкільна група; (С3-С7)цикпоалкільна група; (С3метилом або галогеном; R1, R2, R3 і R4 визначено, як для сполук формули (І). С7)циклоалкіл(С1-С4)алкільна група; -(С1Отже, винахід переважно стосується сполук С4)діалкіламіно(С2-С4)алкільна група; формули: або R8 і R9 разом з атомом нітрогену, до якого вони приєднані, утворюють гетероциклічний радикал, вибраний серед піролідинілу, піперидилу, морфолін-4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, 4-метилпіперазин-1-ілу, 4-метилпіперид-1-ілу, 2метилпіперид-1-ілу, 4,4-диметилпіперид-1-ілу, 4,4дифлуорпіперид-1-ілу, 4-трифлуорметилпіперид-1ілу, 3,4-дигідропіперид-1-ілу, азепін-1-ілу і циклогексил-спіро-4-піперид-1-ілу; R10 - атом галогену; (С1-С4)алкільна група; гідроксильна група; (С1-С4)алкоксильна група; R10 може також бути групою -CH2NR11R12, коли R5 у якій: група -CH2NR11R12 і тоді зазначені групи є ідентичR1 - 2,4-дихлор-З-метилфенільна, нафтильна, ними; 6-метоксинафт-2-ільна, 3-метил-бензотіофен-2R11 і R12 кожний незалежно - гідроген; (С1ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3С6)алкільна група; (С2-С4)алкенільна група; (С3метил-5- метоксибензотіофен-2-ільна, 3-метил-6С7)циклоалкільна група; (С3-С7)циклоалкіл(С1метоксибензотіофен-2-ільна або 3-метил-1С4)алкільна груп; -гідрокси(С2-С4)алкіленова грубензофур-2-ільна група; па; -метокси(С2-С4)алкіленова група; R3 - бензо[1,3]діоксол-5-ільна або фенільна трифлуорметил(С1-С4)алкіленова група; група, незаміщена або заміщена галогеном; галоген(С2-С4)алкіленова група; R8 і R9 разом з атомом нітрогену, до якого воабо R11 і R12 разом з атомом нітрогену, до якони приєднані, утворюють ди(С1го вони приєднані, утворюють моноциклічний, диС4)алкіламіногрупу, піролідинільний або піперидициклічний або гетероциклічний радикал, вибраний льний радикал, незаміщений або заміщений односеред ацетидинілу, піролідинілу, морфолін-4-ілу, разово або двічі метилом або галогеном; тіоморфолін-4-ілу, піперид-1-ілу, піперазин-1-ілу, R11 і R12 разом з атом нітрогену, до якого вони 1,2,3,6-тетрагідропірид-1-ілу, декагідрохінолілу, приєднані, утворюють. етилізобутиламіногрупу, декагідроізохінолілу, октагідро-1Н-ізоіндолілу, (С4етилізопропіламіногрупу, етил-третС6)циклоалкіл-спіро-піперидилу і 3бутиламіногрупу, діізопропіл-аміногрупу, циклопеазабіцикло[3,1,0]гексилу, незаміщеного або замінтилметиламінний або циклопентилетиламінний щеного один або більше разів атомом галогену радикал або піперидильний радикал, незаміщений або (С1-С4)алкільною, гідроксильною, (С1або заміщений один або більше разів метилом або С4)алкоксильною, трифлуорметильною, дифлуоргалогеном; метиленовою або фенільною групою; а також їх солей з неорганічними або органіча також їх солі з неорганічними або органічниними кислотами і/або сольватів або гідратів. ми кислотами і/або сольвати або гідрати. Особливо бажаними є сполуки формули (Іа), Деякі значення замісників є особливо бажаниякі мають (R,R)-конфігурацію. ми. Бажаними сполуками формули (І) є ті, у яких Найкращим об'єктом винаходу є сполука, вибщонайменше один з замісники має наведене нижрана з групи, яку утворюють: че значення: -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6a) R1 - 2,4-дихлор-3-метилфенільна, нафтильметокси-2-нафтил)сульфоніл)аміно)пропаноїл)на, 6-метоксинафт-2-ільна, 3-метилбензотіофен-2аміно)-3-(4-((2,6-цис-диметил-1ільна, 3-метил-5-хлорбензотіофен-2-ільна, 3піперидил)метил)феніл)-N-ізопропіл-Nметил-5-метоксибензотіофен-2-ільна, 3-метил-6метилпропанамід; метоксибензотіофен-2-ільна або 3-метил-1-(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2бензофур-2-ільна група; R2, R3, R4 і R5 визначено, нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(4як для сполук формули (І); ((циклопентил(етил)аміно)метил)феніл)-Nb) R2 - гідроген, a R3 - бажано, бенізопропіл-N-метилпропанамід; зо[1,3]діоксол-5-ільна або фенільна група, незамі-(R,R)3-(4-((2,6-цис-диметил-1щена або заміщена галогеном; R1, R4 і R5 визначепіперидил)метил)феніл)-2-((3-(((6-метокси-2но, як для сполук формули (І); нафтил)-сульфоніл)аміно)-3c) R4 - група -CONR8R9, а, бажано, -NR8R9 17 75906 18 фенілпропаноїл)аміно)-N-ізопропіл-Nде R2 і R3 визначено, як для сполук формули метилпропанамід; (І), а X - або гідроген, або група R1-SO2-, у якій R1 -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((6визначено, як для сполук формули (І), або Nметокси-2-нафтил)сульфоніл)аміно)захисна група, вводять в реакцію зі сполукою фопропаноїл)аміно)-3-(4-((третрмули: бутил(етил)аміно)метил)феніл)-N-iзопропіл-Nметил-пропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил1-бензотіофен-2-іл)сульфоніл)аміно)пропаноїл)аміно)-3-(4-((2,6-цис-диметил-1піперидил)метил)феніл)-N-ізопропіл-Nметилпропанамід; -(R,R)3-(4-((2,6-цис-диметил-1піперидил)метил)феніл)-2-((3-(((5-метокси-3метил-1-бензотіофен-2-іл)сульфоніл)аміно)-3у якій Υ - або R4, визначена, як для сполук фофенілпропаноїл)аміно)-N-ізопропіл-Nрмули (І), або (С1-С4)алкоксикарбоніл, а Ζ - або R4, метилпропанамід; визначена, як для сполук формули (І), або -CN-(R,R)N-(4-((2,6-цис-диметил-1група, за умови, що, коли Υ - R4, яка є фенілом, піперидил)метил)бензил)-3-(((6-метокси-2нафзаміщеним групою -CH2NR11R12, Z - R5, яка є грутил)-сульфоніл)аміно)-3-феніл-N-(1пою -CH2NR11R12, a R12 визначено, як для сполук піперидилкарбоніл)пропанамід; формули (І); і -(R,R)2-((3-(4-хлорфеніл)-3-(((6-метокси-2коли X - R1SO2-, Y - R4, a Z - R5, одержується нафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4сполука формули (І); ((2,6-цис-диметил-1-піперидил)метил)феніл)-Nабо коли X не R1SO2 і/або Υ не R4 і/або Ζ не ізопропіл-N-метилпропанамід; R5, тобто коли серед груп Χ, Υ і Ζ X - Η або N-(R,R)3-(4-((2,6-цис-диметил-1захисна група, Υ -(С1-С4)алкоксикарбоніл, Ζ - -CN, піперидил)метил)феніл)-2-((3-(((6-метокси-2сполуку, отриману таким чином, формули: нафтил)сульфоніл)аміно)-3фенілпропаноїл)аміно)-N,N-діетилпропанамід; -(R,R)2-((3-(3-флуорфеніл)-3-(((6-метокси-2нафтил)сульфоніл)аміно)пропаноїл)-аміно)-3-(4((2,6-цис-диметил-1-піперидил)метил)феніл)-Nізопропіл-N-метилпропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-(((3-метил1-бензофур-2-іл)сульфоніл)аміно)пропаноїл)аміно)-3-(4-((2,6-цис-диметил-1піперидил)метил)феніл)-N-ізопропіл-Nметилпропанамід; -(R,R)2-((3-(1,3-бензодіоксол-5-іл)-3-((2нафтилсульфоніл)аміно)пропаноїл)аміно)-3-(3піддають одній або більше таких стадій: ((трет-бутил(етил)аміно)метил)феніл)-N-ізопропілякщо X - N-захисна група, цю групу видаляють, N-метилпропанамід; і сполуку, одержану таким чином, формули: -(R,R)3-(4-(7-азабіцикло[2,2,1]гепт-7ілметил)феніл)-2-((3-(1,3-бензодіоксол-5-іл)-3-(((6метоксинафтил)сульфоніл)аміно)пропаноїл)аміно)-Nізопропіл-N-метилпропанамід; а також їх солі з неорганічними або органічними кислотами і/або їх сольвати або гідрати. Згідно з іншим об'єктом, винахід стосується способу отримання сполуки формули (І), її солі і/або сольватів або гідратів, який полягає у тому, що: кислоту або функціональне похідне цієї кислоти формули: вводять у реакцію з сульфонілгалогенщом формули: R1SO2-Hal (VI), де Hal - галоген; коли Υ -(С1-С4)алкоксикарбоніл, його гідролізують і одержану таким чином кислоту або функціональне похідне цієї кислоти формули: 19 75906 20 нітрофеніловим естером або бензотріазол-1іловим естером. Коли використовується 2,5-діоксопіролідин-1іловий естер кислоти (II), реакцію з аміном (III) проводять у розчиннику, наприклад, Ν,Ν-ДМФ, у присутності основи, наприклад, триетиламіну або N-N-діізопропілтиламіну, при температурі від 0°С до кімнатної. Коли використовується кислий хлорид, реакцію проводять у розчиннику, наприклад, ДХМ, у присутності основи, наприклад, триетиламіну, Nвводять у реакцію зі сполукою формули: метилморфоліну або Ν,Ν-діізопропілтиламіну, при HNR8R9 (VIII), у якій R8, R9 визначено, як для температурі від -60°С до кімнатної. сполук формули (І); Коли використовується змішаний ангідрид ки- коли Ζ - -CN-група, цю групу перетворюють у слоти (II), його одержують на місці реакцією (С1R5. С4)алкілхлорформату з кислотою формули (II) у Як варіант, одержану у такий спосіб сполуку розчиннику, наприклад, ДХМ, у присутності осноперетворюють у її сіль з неорганічною або органіви, наприклад, триетиламіну, при температурі від чною кислотою. 70°С до 50°С, реакцією з аміном формули (III), у Під час будь-якої стадії процесу отримання розчиннику, наприклад, ДХМ, у присутності осносполуки формули (І) або інтермедіатів формул (II), ви, наприклад, триетиламіну, при температурі від (V), (IV), (V) або (VII), може виявитись необхідним 0°С до кімнатної. і/або бажаним захистити такі реакційні або чутливі Коли використовується сама кислота формули функціональн групи, як амінна, гідроксильна або (II), спосіб виконується у присутності сполучальнокарбоксильна, присутні у будь-якій з відповідних го засобу, що використовується у хімії пептидів, молекул. Цей захист може бути здійснений з виконаприклад, 1,3-дициклогексилкарбодииміду або ристанням звичайних захисних груп, описаних, бензотріазол-1-ілокси-триснаприклад, [Protective Groups in Organic Chemistry, (диметиламіно)фосфонію або гексафлуорфосфату J.F.W. McOmie, Ed. Plenum Press, 1973 і у , бензотріазол-1-іл-Ν,Ν,Ν',Ν'-тетраметилуронію у Protective Groups in Organic Synthesis, T.W. Greene присутності основи, наприклад, триетиламіну, Ν,Νі P.G.M. Wutts, опублікованих John Wiley і Sons, діізопропілетиламіну або N-етилморфоліну, у роз1991]. Видалити захисні групи можна у подальшій чиннику, наприклад, ДХМ, ацетонітрилі або Ν,Νстадії з використанням відомих способів без дії на диметилформаміді, або суміші цих розчинників, решту відповідної молекули. при температурі від 0°С до кімнатної. Придатними N-захисними групами можуть буЯкщо сполуку формули (І) одержують безпоти стандартні N-захисні групи, відомі фахівцям, середньо, або у такий спосіб одержують сполуку наприклад, трет-бутоксикарбонільна, флуоренілформули (IV), щонайменше одна з групи Χ, Υ і Ζ метоксикарбонільна, бензильна, тритильна або репрезентує: X -N-захисну групу, Υ -(С1бензилоксикарбонільна група. С4)алкоксикарбоніл, Ζ = -CN, які однією або декіСполуки формули (І) або сполуки формули (IV) лькома реакціями перетворюються у сполуку фоможуть бути отримані у формі суміші ізомерів або рмули (І) з використанням відомих фахівцям споу оптично чистій формі. Для одержання оптично собів. Зрозуміло, що, коли для перетворення чистої сполуки, можна або розділити ізомери будьсполуки формули (IV) у сполуку формули (І) прояким відомим способом органічної хімії, або виководять кілька реакцій, ці реакції не повинні вплиристовувати оптично чисті сполуки формул (II) і вати на інші замісники відповідної молекули. (III) як вихідні матеріали і потім застосувати відпоКоли у сполуці формули (IV), X - N-захисна відні відомі нерацемізуючі способи синтезу. група, цю групу видаляють згідно з відомими споУ стадії а) способу, сполуки формули (І) або собами. Наприклад, коли X третсполуки формули (IV) отримують з використанням бутоксикарбонільна група, її видаляють кислотою, стандартних способів хімії пептидів, наприклад, наприклад, гідрохлоридною або трифлуороцтоописаних у [The Peptides Ed. E. Gross i J. вою, у розчиннику, наприклад, метанолі, етиловоMeienhofer, Academic Press, 1979, 1, 65-104]. Відому етері, діоксані, ТГФ або ДХМ, при температурі мі способи дозволяють здійснити пептидне сполувід 0°С до кімнатної. Далі одержаний у такий спочення без рацемізації атомів карбону кожної з сіб амін формули (V) вводять у реакцію з сульфоскладових амінокислот; крім того, -заміщені нілгалогенідом формули (VI) (бажано, хлоридом), аланіни, у яких хіральний карбон не є суміжним до у присутності основи, наприклад, гідроксиду лужкарбоксильної групи, як відомо, не зазнають раценого металу (наприклад, гідроксиду натрію або мізаці [Ann. Rev. Biochem., 1986, 55, 855-878]. Пакалію) або органічної основи (наприклад, триетитентна заявка ЕР 236 163 описує способи збереламіну, діізопропілетиламіну або Nження хіральності кожної з амінокислот. метилморфоліну), у розчиннику, наприклад, діокОтже, у стадії а) способу винаходу, функціосані, ДХМ або ацетонітрилі, у присутності або віднальні похідні кислоти (II) можуть бути функціонасутності активатора, наприклад, диметиламінопільними похідними, що реагують з амінами, наприридину (ДМАП); реакцію можна також проводити у клад, ангідридом, змішаним ангідридом, піридині у присутності або відсутності ДМАП. Реахлорангідридом або активованим естером, наприкції проводять при температурі від 0°С до кімнатклад, 2,5-діоксопіролядин-1-іловим естером, пної. 21 75906 Як у одержаній у такий спосіб сполуці формули (І), так і у сполуці формули (IV) X -R1SO2-. Коли у сполуці формули (IV) Υ -(С1С4)алкоксикарбоніл, її гідролізують у кислотному або основному середовищі згідно зі способами, відомими фахівцям. Далі одержану кислоту формули (VII) вводять у реакцію зі сполукою формули (VII) в умовах, описаних вище, для одержання сполуки формули (II). Як у одержаних сполуці формули (І), так і у сполуці формули (IV) R4 - CONR8R9. Коли, у сполуці формули (IV), Ζ - ціаногрупа, цю групу перетворюють у групу R5 згідно з стандартними способами. Наприклад, відновлення -CN-групи дає сполуку формули (І) або сполуку формули (IV), у яких R5 - -CH2NH2-. Це відновлення можна проводити з використанням гідрогену у присутності каталізатора, наприклад, нікелю Рейні, у розчиннику, наприклад, метанолі, толуолі, діоксані або їх суміші разом з водним аміаком, при температурі від кімнатної до 50°С. Групу -CN можна перетворити у групу R5 - CH2NR11R12 згідно з Схемою 1. (І): X - R1SO2-, Υ - R4; або (IV): X не R1SO2і/або Y не R4 У стадії а1 Схеми 1 відновлення нітрильної похідної формули (IV) до альдегіду формули (IX) проводять згідно зі способами, відомими фахівцям [див., наприклад, способи, описані у Synth. Commun., 1990, 20(3), 459-467 і спосіб, описаний у Farmaco, Ed. Sci., 1988, 43(7/8), 597-612] за умови, що у сполуці формули (IV), X не є N-захисною групою, яка є лабільною у кислотному середовищі. Далі у стадії b1 сполука формули (X) реагує з альдегідом формули (IX) у присутності або відсутності кислоти, наприклад, оцтової, у розчиннику, наприклад, метанолі, ДХМ або 1,2-дихлоретані з утворенням інтермедіатного іміну, який хімічно відновлюють, наприклад, ціаноборгідридом, триацетоксиброгідридом або боргідридом натрію. Групу -CN можна також перетворити у групу R2 за Схемою 2. 22 (І): Х= R1 SO2- і Υ - R4; або (IV): X не є R1 SO2і/або Υ не є R4 У стадії а2 Схеми 2 ціаногрупа відновлюється, як це було описано вище. Далі операцією b2 одержаний амін перетворюється у спирт формули (XI) згідно зі способами, відомими фахівцям, наприклад, дією нітриту натрію у водному середовищі, у ' розчиннику, наприклад, діоксані, при температурі від кімнатної до 110°С. У стадії с2 спирт формули (XI) обробляють метансульфонілхлоридом у присутності основи, наприклад, триетиламіну, у розчиннику, наприклад, ДХМ при температурі від 0°С до точки кипіння розчиннику. У одержаній сполуці формули (XII) W - СІ або O-SO2CH3 залежно від умов реакції. У стадії d2, коли використовується сполука формули (XII), у якій W - СІ, реакцію проводять зі сполукою формули (X) у присутності основи, наприклад, гідриду натрію у розчиннику наприклад, ТГФ, Ν,Ν-ДМФ, ацетонітрилі, толуолі, або 2пропанолі при температурі від кімнатної до 100°С. Коли використовується сполука формули (XII), у якій W - O-SO2CH3, реакцію проводять зі сполукою формули (X) у присутності або відсутності основи, наприклад, триетиламіну, у розчиннику, наприклад, етанолі, Ν,Ν-ДМФ, ацетонітрилі або ДХМ при температурі від 0°С до 100°С. У стадії е2, естер відновлююють відновником, наприклад, NaBH4 або LiAIH4. Сполуку винаходу формули (І), у якій R5 - -CH2-N(O)-R11R12, одержують з аналогічної· сполуки формули (І), у якій R5 - CH2NR11R12R5, а інші замісники є тими ж, і реакцію проводять, діючи окиснювачем, наприклад, метахлорпербензойною кислотою. Сполуки формули (І) згідно з винаходу нарешті одержано. Одержані у такий спосіб сполуки формули (І) 23 75906 ізолюють у формі вільної основи або у формі солі, згідно з стандартними способами. Коли сполуки формули (І) одержують у формі вільної основи, солеутворення проводять обробкою вибраною кислотою в органічному розчиннику. Обробка вільної основи, розчиненої, наприклад, в етері, наприклад, діетиловому, або у спирті, наприклад, 2-пропанолі або метанолі, або у ацетоні, або у ДХМ, або у етилацетаті, або у ацетонітрилі, розчином вибраної кислоти у одному з зазначених розчинників дає відповідні солі, як виділяють згідно з стандартними способами. Отже, можуть бути отримані, наприклад, гідрохлорид, гідробромід, сульфат, гідрогенсульфат, дигідрогенфосфат, метансульфонат, оксалат, малеат, сукцинат, фумарат, 2-нафталінсульфонат, бензолсульфонат або пара-толуолсульфонат. Після завершення реакції сполуки формули (І) можуть бути ізольовані у формі їх солі, наприклад, хлоргідриду; у цьому випадку, якщо необхідно, вільну основу можна отримати нейтралізацією цієї солі неорганічною або органічною основою, наприклад, гідроксидом натрію або триетиламіном, або карбонатом або бікарбонатом лужного металу, наприклад, натрію або калію. Сполуки формули (VI) є відомими або можуть бути отримані згідно з відомими способами. Наприклад, 2,4-дихлор-3метилбензолсульфонілхлорид отримують згідно зі способом, описаним у [J. Am. Chem. Soc, 1940, 62, 511-512]. 2-хінолінсульфонілхлорид і 5,6,7,8тетрагідронафталін-2-сульфонілхлорид отримують згідно зі способом, описаним у WO 97/25315. 6метоксинафталін-2-сульфонілхлорид отримують згідно з [J. Org. Chem., 1992, 57, 2631-2641]. 3метилбензотієніл-2-сульфонілхлорид отримують згідно з [J. Met. Chem., 1988, 25, 639-641]. Сполуки формули (VIII) є відомими або можуть бути отримані згідно з відомими способами. Сполуки формули (X) є відомими або можуть бути отримані згідно з відомими способами. Сполуки формули (II), у яких R2 - гідроген або (С1-С4)алкіл у рацемічній формі або у формі чистого енантіомеру, є відомими (табл.1) або можуть бути отримані згідно з відомими способами [див. WO 97/25315]. 24 Сполуки формули (II), у яких R3 - гідроген, можуть бути одержані відомими способами. Можна, наприклад, використати спосіб за Схемою 3, де R' -( С1-С4)алкіл, а Рr - N-захисна група, наприклад, трет-бутоксикарбонільна або флуоренілметоксикарбонільна група. 25 У стадії а3 Схеми 3, сполука формули (XIII) реагує з естером акрилової кислоти формули (XIV) з утворенням сполуки формули (XV). Цю реакцію проводять у присутності кислоти, наприклад, оцтової, при температурі кипіння реакційної суміші. У стадії b3 сполука (XV) реагує з сульфонілгалогенідом формули (VI) у присутності основи, наприклад, гідроксиду натрію або калію, або 4диметиламінопіридину у розчиннику, наприклад, діоксані або піридині, при температурі від кімнатної до 60°С. У стаді с3, одержаний естер формули (XVI) гідролізують згідно зі способами, відомими фахівцям, з одержанням бажаної сполуки формули (II), у якій X - R1SO2-. У іншому варіанті, у стадії d3, аміноестер формули (XV) захищають згідно зі способами, відомими фахівцям, наприклад, третбутоксикарбонільною або флуоренілметоксикарбонільною групою. У стадії е3 одержаний естер формули (XVII) гідролізують відомими способами, одержуючи сполуку формули (II), у якій X - захисна група. У іншому варіанті, у стадії f3, естер формули (XV) гідролізують у кислотному або основному середовищі, одержуючи сполуку формули (II). Сполуки формули (V), у яких Υ -(С1С4)алкоксикарбоніл або група R4 - CONR8R9, a Z- CN, є відомими або можуть бути отримані відомими способами [див., наприклад, WO 97/25315, ЕР 0614911 або ЕР 0236164). Інші сполуки формули (V), у яких Υ - R4, a Z = CN, можуть бути отримані за Схемою 4. 75906 26 У стадії а4 Схеми 4 бензофенонімін реагує з аміном формули (XVIII) з утворенням сполуки формули (XIX). Цю реакцію проводять у розчиннику, наприклад, ДХМ, хлороформі або етилацетаті, при температурі від кімнатної до 50°С у присутності або відсутності основи, наприклад, триетиламіну. У стадії b4 сполуку формули (XIX) обробляють сильною основою, наприклад, бутиллітієм, третбутоксидом натрію або діізопропіламідом літію і одержують карбаніон, який реагує з 4(бромметил)бензонітрилом. Цю реакцію проводять у розчиннику, наприклад, ТГФ, при температурі від -78°С до кімнатної. Обробкою у кислотному середовищі бензгідриліденову N-захисну групу видаляють і одержують бажану сполуку формули (V). Сполуки формули (XIX) можна також отримати способами, описаними у [Bull. Soc. Chim. Fr., 1973, 2985, 2987, 2988, J. Am. Chem. Soc, 1982, 104 (3), 730 або Теtrаhеdrоn Lett., 1996, 1137]. Сполуки формули (XVIII) є відомими або можуть бути отримані відомими способами, наприклад, за Схемою 5. У стадії а5 Схеми 5 сполука формули (XX) реагує з азидом натрію з утворенням сполуки формули (XXI). Цю реакцію проводять у розчиннику, наприклад, ДМФ при температурі від 0°С до кімнатної. У стадії b5 сполуку формули (XXI) відновлюють до сполуки формули (XVIII) згідно зі способами, відомими фахівцям. Сполуки формули (XVIII) можна також отримати відновленням нітрилом формули R4CN, наприклад, дією LiAIH4. Сполуки формули (III), у яких Υ -( С1С4)алкоксикарбоніл, а Ζ - R3, визначена, як для сполук формули (І), отримують згідно з Схемою 6, де R1 -( С1-С4)алкіл. 27 75906 28 щають трет-бутоксикарбонільною групою, і одержаний естер гідролізують стандартним способом (стадія b7); одержана кислота формули (XXVII) реагує зі сполукою формули (VIII) згідно з описаним вище (стадія с7), і одержану сполуку (XXVIII) позбавляють захисту у кислотному середовищі (стадія d7). Сполуки формули (V), у яких Υ - R4, a Z - R5, визначена, як для сполук формули (І) можна отримати за Схемою 8. Схема 8 У стадії а6 Схеми 6 сполука формули (XXII) реагує з , '-дибром-п-ксилолом (ХХІІІ) згідно зі способом, описаним у [Tetpahedron Asymmetry, 1992, 3 (5), 637-650]. У стадії b6 одержана сполука формули (XXIV) реагує зі сполукою формули (X) з утворенням сполуки формули (XXV). Цю реакцію проводять у присутності основи, наприклад, карбонату або бікарбонату лужного металу (карбонату або бікарбонату натрію або калію) у розчиннику, наприклад, Ν,Ν-ДМФ, ацетонітрилі, ДХМ або толуолі при температурі від кімнатної до 100°С. У стадії с6 N-захисну групу видаляють кислотою, наприклад, гідрохлоридною. Сполуки формули (III), у яких Υ - R4, тобто CONR8R9, можна також отримати за Схемою 7, де R' -( С1-С4)алкіл. У стадії а7, амінну сполуку формули (III) захи У стадії а8 Схеми 8 сполука формули (XIX) реагує з метил 4-(бромметил)бензоатом у присутності основи, наприклад, трет-бутоксиду калію або діізопропіламідом літію у розчиннику, наприклад, ТГФ, при температурі від -78°С до кімнатної. Бензогідриліденова захисна група видаляється обробкою у кислотному середовищі. У стадії b8 амін формули (XXIX) захищають реакцією з ди-трет-бутилдикарбонатом. У стадії с8 одержаний естер формули (XXX) відновлюють до спирту формули (XXXI) відновлювачем, наприклад, алюмогідридом літію, борогідридом натрію або гідридом діізобутилалюмінію у розчиннику, наприклад, ТГФ або толуолі, при температурі від -78°С до кімнатної. Спирт формули (XXXI) реагує (стадія d8) з метансульфонілхлоридом у присутності основи, наприклад, триетиламіну у розчиннику, наприклад, ДХМ або ТГФ, при температурі від 0°С до точки кипіння розчиннику. 29 75906 30 У стадії е8 одержана сполука формули (XXXII) формули (XXXVI) видаляють обробкою у кислотреагує зі сполукою формули (X) у присутності або ному середовищі. відсутності основи, наприклад, триетиламіну у Аміни формули (X) є відомими і можуть бути розчиннику, наприклад, етанолі, Ν,Ν-ДМФ, ацетоотримані відомими способами, описаними нижче: нітрилі, толуолі або ДХМ при температурі від 0°С до 100°С. У стадії f8 N-захисна група сполуки формули (XXXIII) видаляється обробкою у кислотному середовищі. Сполуки формули (III), у яких Υ - (С1С4)алкоксикарбоніл або R4, тобто група -CH2NR8R9, гетероциклічний радикал або феніл, незаміщений або заміщений групою, відмінною від групи -CH2NR11R12, a Z - R5, тобто -CH2NR11R12, можуть бути також отримані згідно з Схемою 9. Схема 9 Сполука формули (XXXV) може також бути перетворена у сполуку формули (XXXVI) згідно з реакційною схемою: У стадії а9 Схеми 9 амін сполуки формули (III) захищають звичайними способами. У стадії b9 нітрил формули (XXXIV) відновлюють до альдегіду формули (XXXV) згідно зі способом, описаним у [Synth. Commun., 1990, 20 (3), 459-467]. Далі операцією с9 сполука формули (X) реагує з альдегідом формули (XXXV) у присутності або відсутності кислоти, наприклад, оцтової у розчиннику, наприклад, метанолі, ДХМ або 1,2дихлоретані з утворенням інтермедіатгого іміну, який хімічно відновлюють, наприклад, ціаноборгідридом, триацетоксиборгідридом або боргідридом натрію. Нарешті у стадії d9 N-захисну групу сполуки 31 75906 У стадії а9а відновлювальне амінування проводять у присутності відновника, наприклад, NaНВ(ОАс)3. Далі проводиться алкілування алкілгалогенідом, наприклад, іодидом (операція b9а) або подальше відновлювальне амінування карбонільною похідною формули R12O (стадія с9а), де R12 - діалкілкетон або алкілальдегід. Отже, обробка сполуки (XXXVa), у якій R11 - циклопропіл, ацетоном дає сполуку (XXXVI), у якій R11 циклопропіл, a R12 - ізопропіл. Якщо Υ - алкоксикарбонільна група, сполуку (III), у якій Υ - група CONR8R9, можна отримати згідно з Схемою 10: 32 Стадії а11 і b11 проводять згідно зі способом, описаним у Схемі 5. Стадію с11 проводять згідно зі способом, описаним у Схемі 4. Стадії d11 - i11 проводять згідно з операціями а8-f8 Схеми 8. Сполуки формули (V), у яких R, - група COR13, можуть бути отримані згідно з Схемою 12. Сполуки формули (V), у яких Υ - феніл, заміщений групою -CH2NR11R12, a Z - R5, тобто CH2NR11R12, можна отримати згідно з Схемою 11: У стадії а12 Ν,Οдиметилгідроксиаміногідрохлорид реагує у присутності сполучального засобу, а у стадії b12 додаються літійовані похідні сполуки R13H, отримані дією бутиллітію на сполуку R13H. Подальші операції відповідають стадіям b9, с9 і d9 Схеми 9 і дають сполуку формули (III), одержану зі сполуки формули (ХХХХІ). Сполуки формули (III), у яких R4 - група CSNR8R9, одержують дією реагента Лоусона на подібну сполуку формули (III), у якій R4 - група CONR8R9, а інші замісники є тими ж [Теtrаhеdrоn, 1985, 41. (22), 5061-5087]. Оптично чисті сполуки формули (III) можна отримати розділенням рацемічної суміші стандартними способами, наприклад, з використанням оптично активних засобів або ферментів. Наприклад, коли у сполуці формули (V) Υ - група 33 75906 34 CONR8R9, або (С1-С4)алкоксикарбоніл, а Ζ - CN, можна використати способи, описані у WO 97/25315; коли у сполуці формули (III) Υ - піридил, a Z -CN, можна використати способи, описані у [Теtrаhеdrоn, 1995, 51/46,12731-12744 або у Synthesis, 1996, №8, 991-996]. Серед сполук формул (II) і (III) деякі є новими і складають ще один аспект винаходу. Сполуки формули: X-NH-CH-CH2-CO2H (llа) у яких: у яких: R4 - група -CONR8R9; група CSNR8R9; група X - гідроген або N-захисна група; COR13; феніл, незаміщений або заміщений один R3 - гетероциклічний радикал, вибраний серед: або більше разів Ri0; гетероциклічний радикал, (2,2-дифлуор)бензо[1,3]діоксол-5-ілу, 3вибраний серед піридилу, імідазолілу, фурилу, ізопропілфенілу, 3-трифлуорметоксифенілу, 2,1,3бензімідазолілу, бензотіазол-2-ілу і бенбензоксадіазол-5-ілу, бензотіофен-5-ілу, 1зо[1,3]діоксол-5-ілу, причому ці радикали є незабензофур-6-ілу, 1-бензофур-4-ілу, 1-бензофур-3міщеними або заміщеними метилом; метил-5-ілу, 2,3-дигідробензофур-4-ілу; а також їх R5 - група -CH2NR11R12 або -CH2N(O)NR11R12; солі з неорганічними або органічними кислоти, у R8, R9 - кожний незалежно - гідроген; (С1рацемічній формі або у формі чистих енантіомерів С4)алкільна група; (С3-С7)циклоалкільна група; (С3є новими і складають ще один аспект винаходу. С7)циклоалкіл(С1-С4)алкільна група; -(С1Сполуки формули: С4)діалкіламіно(С2-С4)алкільна група; R, SO2-NR2-CH-CH2-COOH (llb) або R8, R9 разом з атомом нітрогену, до якого у яких: вони приєднані, утворюють гетероциклічний радиR1 - фенілвініл; гетероцикл, вибраний серед кал, вибраний серед піролідинілу, піперидилу, хінолілу, 1-бензофур-2-ілу, 2,1,3-бензоксадіазол-4морфолін-4-ілу, тіоморфолін-4-ілу, піперазин-1-ілу, ілу, 2,1,3-бензотіадіазол-4-ілу, 1,3-бензотіазол-24-метилпіперазин-1-ілу, 4-метилпіперид-1-ілу, 2ілу, 1-бензотіофен-2-ілу, 1Н-піразол-4-ілу, тієн-2метилпіперид-1-ілу, 4,4-диметилпіперид-1-ілу, 4,4ілу, 5-ізоксазолтієн-2-ілу, бензотієн-2-ілу, тієно[3,2дифлуорпіперид-1-ілу, 4-трифлуорметилпіперид-1с]пірид-2-ілу; нафто[2,3-d][1,3]діоксол-6-ілу; приілу, 4-метоксипіперид-1-ілу, 3,4-дигідропіперид-1чому ці гетероцикли є незаміщеними або заміщеілу, азепін-1-ілу і циклогексил-спіро-4-піперид-1ними один або більше разів R6, які можуть бути ілу; однаковими або різними; R10 - атом галогену; (С1-С4)алкільна група; гідR2 - гідроген або (С1-С4)алкіл, a R3 - феніл, нероксигрупа; (С1-С4)алкоксигрупа; R10 може також заміщений або заміщений один або більше разів бути групою -CH2NR11R12, коли R5- група R7, які можуть бути однаковими або різними; гетеCH2NR11R12, і тоді ці групи є ідентичними; роциклічний радикал вибраний серед бенR11 і R12 кожний незалежно - гідроген; (С1зо[1,3]діоксол-5-ілу, незаміщеного або заміщеного С4)алкільна група; (С1-С4)алкенільна група; (С3у положенні 2 двома атомами флуору; 2,1,3С7)циклоалкільна група; (С3-С7)циклоалкіл(С1бензотіадіазол-5-ілу; 2,1,3-бензоксадіазол-5-ілу; С4)алкільна група; -гідрокси(С2-С4)алкіленова бензотіофен-5-ілу; 2,3-дигідро-бензо[1,4]діоксин-6група; -метокси(С2-С4)алкіленова група; ілу; 1-бензофур-2-ілу; 1-бензофур-5-ілу; 1трифлуорметил(С1-С4)алкіленова група; бензофур-6-ілу; 1-бензофур-4-ілу; 1-бензофур-3галоген(С2-С4)алкіленова група; метил-5-ілу; 2,3-дигідробензофур-4-ілу; 1,3-тіазолабо R11 і R12 разом з атомом нітрогену, до яко2-ілу; фурилу; тієн-2-ілу; тієн-3-ілу; го вони приєднані, утворюють моноциклічний або або R2 - феніл, незаміщений або заміщений дициклічний гетероциклічний радикал, вибраний один або більше разів R6, які можуть бути однакосеред ацетидинілу, піролідинілу, морфолін-4-ілу, вими або різними; бензо[1,3]діоксол-5-іл; піридил; тіоморфолін-4-ілу, піперид-1-ілу, піперазин-1-ілу, інданіл; a R3 - гідроген; 1,2,3,6-тетрагідропірид-1-ілу, 2,3,4,5R6 - атом галогену; (С1-С4)алкільна група; тетрагідропіридинію, декагідрохінолілу, декагідроітрифлуорметильна група; (С1-С4)алкоксильна грузохінолілу, тетрагідроізохінолілу, октагідро-1Нпа; 2-флуоретокси-; трифлуорметокси-, метиленізоіндолілу, (С4-С6)циклоалкіл-спіро-піперидил, 3діокси- або дифлуорметилендіоксигрупа; азабіцикло[3,1,0]гексилу і 7R7 - атом галогену; (С1-С4)алкільна група; феазабіцикло[2,2,1]гептан-7-ілу, незаміщеного або нільна група; трифлуорметильна група; (С1заміщеного один або більше разів атомом галогеС4)алкоксильна група; бензилоксигрупа; трифлуону або (С1-С4)алкільною, гідроксигрупою, (С1рметоксигрупа; С4)алкокси-, трифлуорметильною або дифлуормеа також їх солі з неорганічними або органічнитиленовою групою; ми кислотами, у рацемічній формі або у формі R13 - фенільна, тіазол-2-ільна або піридильна чистих енантіомерів, є новими і входять в об'єм група; винаходу. а також їх солі з неорганічними або органічниСполуки формули: ми кислотами, у формі рацемічної суміші або чистих енантіомерів, є новими і входять в об'єм винаходу. Спорідненість сполук винаходу до рецепторів 35 75906 36 брадикініну була виміряна на суспензії мембран Perspectives, 1994, 10 (7), 603-611], нейрогенних клітин MRC5 з використанням метода, подібного запалень, болю [Brit. J. Pharmacol., 1993, 110, 193описаного у [К.Н. Schneck et al., у Eur. J. 198], хронічного болю, нейропатологій, септичного Pharmacol., 1994, 266, 277-282]. У цьому тесті спошоку, опіків [Pain, 1993, 53, 191-197], поранень, рідненість [дез-Arg9] брадикініну становила від 10хвороб дихальних шляхів, астми, системного за6 -7 10 -9 пального синдрому, набряку [Brit. J. Pharmacol., М до 10 М, а для [дез-АrG ]калідину - 2 10 М; і 1995, 114. 1005-1013], церебрального набряку, сполуки винаходу виявляють спорідненість у меангіогенезу [Brit. J. Pharmacol., 1993, 109. 14-17], жах до 10-9М. типового І інфекційного діабетів [Abst. 14th Intern. Спорідненість виражається значенням ІК50, Symp. on Kinins, C49, Denver Colorado, 10-15 Sept. тобто концентрацією, що інгібує 50% специфічного 1995], діабетичних васкулопатій, вентрикулярної зв'язування [дез-Аrg10]тритіатованого калідинового гіпертрофії, фіброзу легенів і системного прогреліганду з рецепторами клітин MRC5. сивного склерозу. Можна відзначити, наприклад: Спорідненість сполук винаходу до рецепторів - запалення, біль у кістках, біль у м'язах, біль у брадикініну В2 була виміряна на суспензії мембран суглобах, поверхневий біль, фіброміалгію, гіпералклітин MRC5 згідно з методикою, подібною описагію, біль, пов'язаний з раком, периопераційний ній у [D.G. Sawutz et al., у Eur. J. Pharmacol., 1992, біль, менструальний біль, головні болі, зубний 227, 309-315]. У цьому тесті спорідненість брадикібіль, гінекологічний біль, мігрені; ніну, що репрезентується як ІК50, мала значення - гіперактивність дихальних шляхів при астмі, приблизно 10-9М, сполуки ж винаходу не виявляатопічну або неатопічну астму, алергічну або неають спорідненості до рецепторів В2 брадикініну лергічну астму, бронхіт, пневмоконіоз, хронічні при концентрації 10-6М. обструктивні хвороби дихальних шляхів, плеврит, Антагоністичну дію сполук винаходу виміряли хронічні обструктивні хвороби легенів, риніт вірусin vitro інгібуванням контракції грудної аорти кроля, ного або алергічного походження; індукованої введенням [дез-Аrg9]брадикініну, після - посткапілярну резистивність, діабет, діабетипопередньої інкубації тканин протягом 20год. у чні васкулопатії, діабетичні симптоми, асоційовані буфері Кребса, насиченому сумішшю СО2/О2 згідз інсуліном (наприклад, гіперлікемія, діурез, протено з адаптованою методикою, описаною у [L. інурія); Levesque et al. Br. J. Pharmacol., 1993, 109. 1254- септичний шок; 1262]. - хворобу Альцгеймера, черепні травми; Антагоністичну дію сполук винаходу виміряли - артрит, ревматоїдний артрит, запальні хвочерез вивільнення [3Н]інозитфосфату фібробласроби суглобів, атеросклероз, розсіяний склероз; тами MRC5 у культурі: після присутності 3 - хвороби системи травлення, хвороби сечової [ Н]міоінозиту протягом 48год., згідно з методикою, системи, цистіт, панкреатит, нефрит, ентероколіт, описаною у [F. Oury Donat et al., J. Neurochem., виразковий коліт, синдром подразнення кишечни1994, 62, (4), 1399-1407]. Антагоністична дія вираку, хвороба Крона, хвороби печінки; жається %% інгібування вивільнення - патології системи зору, увеїт, ретиніт, глау[3Н]інозитфосфату, індукованого [дезкому; Аrg10]калідином при 10-8М на фібробластах MRC5, - хвороби шкіри, наприклад, атопічні хвороби, інкубованих протягом 4год. у присутності ΘL1 екзему, псоріаз, дерматит, втрату волосся. (0,5мкг/мл). Крім того, сполуки винаходу можуть бути кориКишкову абсорбцію сполук винаходу дослісними завдяки антипроліферативній дії на ракові джували in vitro на моделі моношару клітин САСОклітини; їх дії на нейродегенеративні хвороби, де2, згідно з адаптаційною методикою, описаною у генегацію міeліну, дегенеративні хвороби вірусно[Т. Lindmark et al., J. Pharmacol. Exp. Therap., 1995, го походження; їх серцевозахисній дії. 275 (2), 958-964]. Сполуки винаходу можуть бути використані як Крім того, декілька сполук винаходу були досміорелаксанти, релаксанти гладких м'язів, спазмів ліджені in vivo на тваринних моделях. шлунково-кишкового тракту і матки. Антиноціцептична дія була перевірена на моВзагалі, сполуки винаходу можуть бути викоделі нейропатичного болю у щурів після перораристані для лікування або попередження будьльного введення сполуки винаходу дозою 30мг/кг яких патологій, у яких брадикінін грає основну [згідно з протоколом, описаним у Pain, 2000, 86, роль і які називають брадикінін-залежними патоло265-271]. гіями. Було виявлено, що сполуки винаходу при доСполуки винаходу є особливо активними агензах від 1 до 30мг/кг (перорально) інгібують остантами у фармацевтичних композиціях, токсичність ню фазу ноцицепції, індукованої формаліном у яких відповідає їх використанню у медицині. миші [Pain, 1987, 203-114]; це вказує дію на запаСполуки формули (І) можна використовувати у льний біль. добових дозах від 0,01 до 100мг на кг маси ссавця, Модель термічної гіпералгії, індукованої ультщо піддається лікуванню, бажано, у добових дозах рафіолетовим опромінюванням у щурів [Brit. Med. від 0,1 до 50мг/кг. Для людини бажаною дозою є J., 1993, 110, 1441-1444] показала антигіпералгічну 0,5-4000мг щоденно, більш бажано 2,5-1000мг, дію сполуки винаходу при дозах від1 до 3мг/кг залежно від віку і індивідуального стану пацієнта і (орально). типу лікування (профілактичного або терапевтичСполуки винаходу можуть бути використані ного). для лікування або попередження багатьох патолоДля застосування у терапії сполуки формули гій, зокрема запальних патологій, стійких або хро(І) звичайно вводять дозованими одиницями, які нічних запальних хвороб [Drug News and 37 75906 38 звичайно є фармацевтичними композиціями, у чими і смаковими добавками. яких активний продукт змішано з фармацевтичниДля ректального введення використовуються ми наповнювачами. супозиторії, які отримуються з зв'язуючими добавОтже, згідно з ще одним аспектом, винахід ками, що розплавляються при ректальній темпестосується фармацевтичної композиції, що місратурі, наприклад, з маслом какао або поліетилентить, як активний продукт, сполуку формули (І) або гліколями. її фармацевтично прийнятну сіль і/або сольват, Для парентерального, внутрішньоносового або гідрат. або внутрішньоочного введення використовуються У фармацевтичній композиції винаходу для водні суспензії, ізотонічні сольові розчини або степерорального, під'язичного, інгаляційного, підшкіррильні розчини для ін'єкцій, які містять фармаконого, внутрішньом'язового, внутрішньовенного, логічно прийнятні дисперсанти і/або солюбілізатотрансдермального, локального або ректального ри, наприклад, пропілепгліколь або введення, активні агенти можуть бути введені твабутиленгліколь. рині або людині у одиничній формі як суміш станОтже, для отримання водного розчину для дартних фармацевтичних допоміжних засобів. внутрішньовенноє ін'єкції можуть бути використані Прийнятними одиничними формами введення моспіврозчинник, наприклад, спирт (етанол або гліжуть бути, наприклад, таблетки, желатинові капсуколь, наприклад, поліетиленгліколь або пропіленгли, порошки, гранули і оральні розчини або суліколь), і гідрофільні ПАР, наприклад, Tween 80. спензії, під'язичні і защочні форми, аерозолі, Для отримання масляного розчину для внутріштопікальні форми, імплантати, підшкірні, внутрішньом'язових ін'єкцій, активний продукт може розньом'язові, внутрішньовені, інтраназальні або внучинений у тригліцеридному або гліцероловому трішньоочні форми і ректальні форми. естері. При отриманні твердої композиції у формі Для локального введення можна використовутаблетки активний агент мікронізують (або ні) змівати креми, мазі, гелі або очні краплі. шують з фармацевтичним носієм, який може склаДля трансдермального введення можуть бути датись з розріджувачів, наприклад, з лактози, міквикористані багатошарові або резервуарні накладрокристалічної целюлози, крохмалю і активаторів ки, у яких активний продукт може знаходитись у композиції, наприклад, зв'язуючих (полівінілпіроліспиртовому розчині. дон, гідроксипропілметилцелюлоза тощо), гліданДля введення інгаляцією використовують, аетів, наприклад, оксиду кремнію, і змащувачів, стерозоль, що містить, наприклад, сорбітантриолеат арату магнію, стеаринової кислоти, або олеїнову кислоту і також трихлорфлуорметан, гліцерилтрибегенату або стеарилфумарату надихлорфлуорметан, дихлортетрафлуоретан або трію. будь-який інший біологічно сумісний газДо композиції можуть бути додані зволожуючі пропелент; можна використовувати також систему, засоби або ПАР, наприклад, лаурилсульфат нащо містить активний продукт, один або у комбінатрію. ції з наповнювачем, у формі порошку. Можуть бути застосовані різні способи отриАктивний продукт можна також використовумання таблеток, наприклад, безпосереднє таблевати у комплексній формі з циклодекстрином, натування, сухе гранулювання, вологе гранулювання приклад, , або -циклодекстрином, 2і гранулювання гарячим плавленням. гідроксипропіл- -циклодекстрином або метил- Таблетки можуть бути непокритими або мати циклодекстрином. цукрове (наприклад, сахарозне) або полімерне Активний продукт може мати форму мікрокаппокриття, або покриття іншими матеріалами. сул або мікросфер, як варіант, з одним або більше Таблетки можуть забезпечувати негайне, задопоміжними засобами або добавками. тримане або уповільнене вивільнення за допомого Серед форм з уповільненим вивільненням, які полімерних матриць або з використанням спеціавикористовуються у випадках хронічного лікуванльних полімерів для покриття. ня, можуть бути використані імплантати, які моЖелатинову капсулу отримують простим зміжуть бути отримані у формі масляної суспензії або шуванням активного агента з сухим фармацевтичу формі суспензії мікросфер у ізотонічному сереним носієм (з сухим, вологим або плавильним градовищі. нулюванням) або з рідким або напівтвердим У кожній дозованій одиниці активний продукт фармацевтичним носієм. формули (І) представлено у кількості, адаптованої Желатинові капсули можуть бути м'якими або до добових доз. Взагалі кожна дозована одиниця жорсткими, з покриттям або без нього, з негайною, пристосована до дозування і типу введення, і моуповільненою або затриманою активністю (наприже бути, наприклад, таблеткою, желатиновою капклад, у ентеричній формі). сулою тощо, саше, ампулами, сиропами тощо, або Композиції у формі сиропу або еліксиру може краплями і містити від 0,5 до 1000мг активного містити активний продукт разом з підсолоджувапродукту, бажано, від 2,5 до 250мг для введення чем, переважно низькокалорійним, метилпарабе1-4 рази на день. ном і пропілпарабеном як антисептиками, а також Композиції винаходу можуть містити разом зі з смаковою добавкою і придатним забарвлювасполуками формули (І) або їх фармацевтично чем. прийнятними солями і/або сольватами, або гідраВодорозчинні порошки або гранули можуть мітами інші активні продукти, які можуть бути викостити активний продукт у суміші з дисперсантами, ристані при лікуванні симптомів або хвороб, згадазволожуючими або суспендуючими засобами, наних вище. Наприклад, фармацевтичні композиції приклад, з полівінілпіролідоном, і з підсолоджуювинаходу можуть разом зі сполукою винаходу міс 39 75906 40 тити антагоніст рецептора брадикініну В2. Згідно з ще одним аспектом, винахід стосується використання сполук формули (І) або їх фармацевтично прийнятних солей і/або сольватів, або гідратів для отримання медичних продуктів, призначених для лікування будь-яких патологій, у яких 4,13г 3-аміно-3-фенілпропіонової кислоти розберуть участь рецептори брадикініну і В1. чиняють у сумішц 100мл діоксану і 25мл 1Η NaOH, Згідно з іншим аспектом, винахід стосується порціями додають 5,6г 2використання сполуки формули (І), або їх фарманафталінсульфонілхлориду, підтримуючи рН 10,5цевтично прийнятних солей і/або сольватів, або 10,8 додаванням 1Η NaOH, і суміш перемішують гідратів для отримання медичних продуктів, приз2год. при КТ. Реакційну суміш розбавляють 400мл начених для лікування запальних патологій і стійводи, підкислюють до рН 2 доданням 2Η НСІ і екских або хронічних запальних хвороб. трагують ЕtOАс, органічну фазу промивають буУ Препаратах і Прикладах використовуються ферним розчином KHSO4/K2SO4 і сушать над такі абревіатури: Na2SO4. Розчинник випарюють під вакуумом і одеетер: діетиловий етер ржують 7,33г бажаного продукту після перетиранізоетер: діізопропіловий етер ня у гептані і сушіння під вакуумом ; темп.пл. 126ДХМ: дихлорметан 129°С. ДМФ: Ν,Ν-диметилформамід ЯМР: 8 (млн-1): 2,55-2,70: mt: 2H; 4,70: t: 1H; ДМСО: диметил сульфоксид 6,85-8,15: не розд.: 12Н. EtOAc: етил ацетат Препарат 1.2 ТГФ: тетрагідрофуран 3-[метил(нафталін-2-сульфоніл)аміно]-3АсОН: оцтова кислота фенілпропіонова кислота. ТФК: трифлуороцтова кислота TEA: триетиламін ДИПЕА: діізопропілетиламін ДМАП: 4-диметиламінопіридин ДХЕ: дихлоретан ДЦК: 1,3-дициклогексилкарбодіімід ДЦС: дициклогексилсечовина А) 3-(трет-бутоксикарбоніламіно)-3ТБТБ: тетрафлуорборат О-(1 Н-бензотріазолфенілпропіонова кислота. 1-іл-N,N,N',N'-тетраметилуронію 8,3мл триетиламіну додають до суміші 8,3г 3Вос: трет-бутоксикарбоніл аміно-3-фенілпропіонової кислоти у 35мл води і (Вос)2О: ди-трет-бутилдикарбонат 5мл діоксанів з подальшим доданням, протягом Амідаза пеніциліну від Sigma 30хвил., розчину 12,8г дитрет-бутилдикарбонату у Алькатаза від Νονo 25мл діоксану. Суміш перемішують протягом ночі Sephadex LH 20: від Pharmacia при КТ. Реакційну суміш розбавляють водою, водГФБ: гексафлуорфосфат бензотріазол-1ну фазу промивають етером і підкислюють до рН ілокситрис(диметиламіно)фосфонію 2,5 доданням 2Η НСІ, і екстрагують ЕtOАс, органіТБТБ: бензотріазол-і-іл-N,N,N',N'чну фазу промивають водою, насиченим розчином тетраметилуроніютетрафлуорборату NaCI, сушать над Na2SO4 і розчинник випарюють Буферний розчин KHSO4/K2SO4: 16,66г KHSO4 під вакуумом, одержуючи 12,4г бажаного продукту. і 32,32г K2SO4 у 1л води B) 3-(N-трет-бутоксикарбонілметиламіно)-3Гідрохлоридний етер: насичений розчин газу фенілпропіонова кислота. НСІ у діетиловому етері 0,27г 80% гідриду натрію у маслі додають портемп.пл.: температура плавлення ціями до суміші 0,795г сполуки, одержаної на поКТ: кімнатна температура передньому етапі, і 0,62мл метиліодиду у 10мл Якщо не визначено інакше, спектр ЯМР реєстТГФ, і суміш перемішують протягом ночі при КТ. рується при 200МГц у ДMCO-d6, який, як варіант, Реакційну суміш розбавляють ЕtOАс, додають містить ТФК, і посилання на ДМСО відповідає воду і суміш підкислюють до рН 2 доданням 1Η 2,50млн-1 відносно тетраметилсилану. Хімічний НСІ. Після розділення фаз відстоюванням органічну фазу промивають водою, насиченим розчином зсув наведено у млн.-1. NaCI, сушать над Na2SO і розчинник випарюють s: синглет; bs: широкий синглет; ds: подвійний під вакуумом, одержуючи 0,82г бажаного продукту. синглет; d: дублет; bd: широкий дублет; dd: поC) 3-(метиламіно)-3двійний дублет: t: триплет; q: квартет; qt: квінтет; фенілпропіонілтрифлуорацетат. mt: мультиплет; не розд.: нерозрізнений пік; sept.: Суміш 0,81г сполуки, одержаної попередньою септет. операцією, і 12мл ТФК у 10мл ДХМ перемішують Коли у описі наведено лише ЯМР, це означає, 55хвил. при КТ. Реакційну суміш концентрують під що спектр ЯМР зареєстровано в зазначених вище вакуумом, залишок вносять у ДХМ і розчинник умовах згідно з очікуваною структурою. випарюють під вакуумом. Залишок розчиняють у Масс-спектри вказують значення МН+. етері, додають гептан до осадження, розчинник Препарати зливають і одержану смолу сушать, одержуючи Препарат 1.1 0,86г бажаного продукту у формі піни. 3-(нафталін-2-сульфоніламіно)-3C) 3-[метил(нафталін-2-сульфоніл)аміно]-3фенілпропіонова кислота. фенілпропіонова кислота 41 75906 42 5мл 1Η NaOH додають до суміші 0,85г сполують і кислотну водну фазу концентрують під вакуки, одержаної на попередньому етапі, у 5мл діокумом до початку осадження, охолоджують до 0°С і санів з подальшим доданням порціями 0,698г 2осад відфільтровують з відсмоктуванням. Осад нафталінсульфонілхлориду, підтримуючи рН 10-11 вносять у суміш ДХМ/МеОН (6/4; об'єм/об'єм) і доданням 1Η NaOH, і суміш перемішують 2год. сушать над Na2SO4, розчинники випарюють під при КТ. Реакційну суміш розбавляють водою, водвакуумом, залишок вносять у етер і осад відфільтну фазу промивають етером і підкислюють до рН 2 ровують з відсмоктуванням після перетирання, доданням 1Η НСІ, і екстрагують ЕtOАс, органічн одержуючи 3,01г бажаного продукту; темп.пл. фазу промивають водою, насиченим розчином 192°С (розкл.). NaCI, сушать над Na2SO4, і розчинник випарюють B) 3-(3,4-диметилфеніл)-3-(нафталін-2під вакуумом, одержуючи 0,65г бажаного продукту сульфоніламіно)пропіонова кислота у воскоподібній формі. Розчин 1,98г 2-нафталінсульфонілхлориду у Препарат 1.3 15мл діоксану краплями додають до суміші 2г спо3-(3-метилфеніл)-3-(нафталін-2луки, одержаної на попередньому етапі, і 17,4мл сульфоніламіно)пропіонова кислота 1Η NaOH у 20мл діоксану, і суміш перемішують протягом ночі при КТ. Реакційну суміш нейтралізують до рН 7 доданням 1Η НСІ і концентрують під вакуумом. Залишок вносять у суміш ЕtOАс/насичений NaHCO3, осад відфільтровують з відсмоктуванням і вносять у суміш ДХМ/1Η НСІ, органічну фазу сушать над Na2SO4 і після розділення фаз відстоюванням розчинник випарюють A) 3-аміно-3-(3-метилфеніл)пропіонова кислопід вакуумом, одержуючи 1,66г бажаного продукту; та темп.пл. 122°С (розкл.). 11,8мл 3-метилбензальдегіду додають до суПрепарат 1.5 міші 10,4г малонової кислоти і 15,4г ацетату амо3-аміно-3-(3,5-диметоксифеніл)пропіонова кинію у 150мл 2-метоксиетанолу, і суміш гріють прослота тягом ночі при 80°С. Після охолодження до КТ, осад відфільтровують з відсмоктуванням, промивають етером і сушать, одержуючи 6,8г бажаного продукту. ЯМР: (млн.-1): 2,25: s: 3Н; 2,80-3,05: mt: 2Н; 4,55: t: 1Н; 7,10-7,30: не розд.: 4Н. B) 3-(3-метилфеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота 10мл 1Η NaOH додають до суспензії 1,79г сполуки, одержаної на попередньому етапі, у 25мл діоксанів з подальшим доданням порціями 2,26г 2нафталінсульфонілхлорид, з підтриманням рН 10,5-12 доданням 1Η NaOH, і суміш перемішують 2год. при КТ. Реакційну суміш розбавляють водою, водну фазу промивають ЕtOАс і підкислюють до рН 1 доданням 6Η НСІ, і екстрагують ЕtOАс, органічн фазу промивають насиченим розчином NaCI і сушать над Na2SO4. Розчинник випарюють під вакуумом і одержують 3,37г бажаного продукту після кристалізації з гептану. Препарат 1.4 3-(3,4-диметилфеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота A) Гідрохлорид 3-аміно-3-(3,4диметилфеніл)пропіонової кислоти Суміш 5г 3,4-диметилбензальдегіду, 3,88г малонової кислоти і 5,74г ацетату амонію у 50мл ЕtOН витримують під зворотним холодильником протягом 5год. Після охолодження до КТ, осад відфільтровують з відсмоктуванням і промивають ЕtOН. Осад вносять у суміш ДХМ/1Η НСІ, нерозчинний матеріал відфільтрують, фільтрат злива A) 3-(3,5-диметоксифеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота Суміш 5г 3,5-диметоксибензальдегіду, 3,13г малонової кислоти і 4,64г амонійацетату у 50мл ЕtOН витримують під зворотним холодильником протягом 5год. Реакційну суміш концентрують під вакуумом, залишок вносять у воду, нерозчинний матеріал відфільтровують, фільтрат промивають ДХМ і водну фазу концентрують під вакуумом. Залишок вносять у воду і концентрують під вакуумом. Залишок вносять у ЕtOН і розчинник випарюють під вакуумом, одержуючи 2,96г бажаного продукту. B) 3-(3,5-диметоксифеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота 1,01г 2-нафталінсульфонілхлориду додають порціями до суміші г сполуки, одержаної на попередньому етапі, і 4,5мл 1Η NaOH у 15мл діоксану, і суміш перемішують протягом ночі при КТ. Реакційну суміш розбавляють водою і промивають EtOAc, водну фазу підкислюють до рН 1 доданням концентрованої НСІ і екстрагують етером, органічну фазу промивають 1Η НСІ і сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи 1,41г бажаного продукту; темп.пл.=190°С. Препарат 1.6 3-(3,4-диметоксифеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота 43 A) Гідрохлорид 3-аміно-3-(3,4диметоксифеніл)пропіонової кислоти Суміш 5г 3,4-диметоксибензальдегіду, 3,131г малонової кислоти і 4,64г ацетату амонію у 50мл ЕtOН витримують під зворотним холодильником протягом 5год. Після охолодження до КТ, осад відфільтровують з відсмоктуванням, вносять у воду, підкислюють до рН 2 доданням 1Η НСІ, водн фазу промивають ДХМ і концентрують під вакуумом. Залишок вносять у воду і концентрують під вакуумом, потім вносять у ЕtOН і випарюють під вакуумом, одержуючи 2,99г бажаного продукту. B) 3-(3,4-диметоксифеніл)-3-(нафталін-2сульфоніламіно)пропіонова кислота. Цю сполуку отримують у спосіб, описаний у В) Препарату 1.5, починаючи з 1г сполуки, одержаної на попередньому етапі і 7,65мл 1Η NaOH у 15мл діоксану, і одержують 1,33г бажаного продукту. Препарат 1.7 3-(бензо[1,3]діоксол-5-іл)-3-(нафталін-2сульфоніламіно)пропіонова кислота A) 3-Аміно-3-(бензо[1,3]діоксол-5-іл)пропіонова кислота Цю сполуку одержують згідно зі способом, описаним у [Biorg. Med. Chem., 1994,2(9), 881]. B) 3-(бензо[1,3]діоксол-5-іл)-3-(нафталін-2сульфоніламіно)пропіонова кислота 1Η NaOH додають до суспензії 2,16г сполуки, одержаної на попередньому етапі, у 40мл діоксану до рН 11,8 з подальшим додаванням порціями 2,33г 2-нафталін-сульфонілхлориду, і суміш перемішують 2год. при КТ підтримуючи рН 10,5-11,5 додаванням 1Η NaOH. Реакційну суміш розбавляють таким же об'ємом води і промивають ЕtOАс, водну фазу підкислюють до рН 1,5 доданням 6Η НСІ і екстрагують ЕtOАс, органічну фазу промивають буфером KHSO4/K2SO4 і насиченим розчином NaCI, сушать над Na2SO4, і розчинник випарюють під вакуумом, одержуючи 3,9г бажаного продукту після кристалізації з гептану; темп. пл. 173-175°С. ЯМР: 6 (млн-1): 2,45-2,60: mt: 2H; 4,65: q: 1H; 5,40-5,70: mt: 2H; 6,45-6,65: mt: 3Н; 7,55-7,75: mt: 3Н; 7,90-8,10: mt: 4H; 8,35: bd: 1H. Препарат 1.8 3-(2,3-дигідробензо[1,4]діоксин-6-іл)-3(нафталін-2-сульфоніламіно)пропіонова кислота 75906 44 A) 3-аміно-3-(2,3-дигідробензо[1,4]діоксин-6іл)пропіонова кислота Суміш 5г 2,3-дигідробензо[1,4]діоксин-6карбальдегіду, 3,17г малонової кислоти і 4,69г ацетату амонію у 50мл ЕtOН витримують під зворотним холодильником протягом 5год. Реакційну суміш охолоджують до КТ і осад відфільтровують з відсмоктуванням, промивають ЕtOН і потім водою і одержують 1,965г бажаного продукту після сушіння під вакуумом. B) 3-(2,3-дигідробензо[1,4]діоксин-6-іл)-3(нафталін-2-сульфоніламіно)пропіонова кислота Цю сполуку одержують згідно зі способом описаним у стадії В) Препарата 1.5, починаючи з 1г сполуки, одержаної на попередньому етапі, 4,5мл 1Η NaOH, 15мл діоксану і 1,02г 2нафталінсульфонілхлориду, що дає 0,876г бажаного продукту після кристалізації з гексану. Препарат 1.9 3-(2,3-дигідробензо[1,4]діоксин-6-іл)-3-(5,6,7,8тетрагідронафталін-2-сульфоніл-аміно)пропіонова кислота Розчин 0,570г 5,6,7,8-тетрагідронафталін-2сульфонілхлориду у 15мл діоксану додають краплями до суміші 0,5г сполуки, одержаної операцією А Препарату 1.8 і 4,5мл 1Η NaOH у 20мл діоксану, і суміш перемішують 4год. при КТ. Реакційну суміш концентрують під вакуумом, залишок вносять у 1Η NaOH і промивають ДХМ, водне фазу підкислюють до рН 1 доданням концентрованої НСІ, і екстрагують ДХМ, органічну фазу промивають насиченим розчином NaCI, сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи 0,5г бажаного продукту. Препарат 1.10 A) 2,4-дихлор-3-метилбензолсульфонілхлорид 3-[(2,4-дихлор-3метилбензолсульфоніл)феніламіно]пропіонова кислота. Цю сполуку одержують згідно зі способом, описаним у [J. Am. Chem. Soc, 1940, 62, 511-512]. B) Метил 3-(феніламін)пропіонат Суміш 20мл аніліну, 22мл метилакрилату і 2мл 45 75906 46 оцтової кислоти витримують під зворотним холодильником протягом 8год. Після концентрації реакційну суміш під вакуумом одержане масло відокремлюють дистиляцією під зниженим тиском (132°С при 333,3Па і потім при 110°С при 6,66Па). Одержаний продукт вносять у гексан і осад відфільтровують з відсмоктуванням, одержуючи 25г A) (R) 3-(Фенілацетил)аміно-3бажаного продукту. (бензо[1,3]діоксол-5-іл)пропіонов кислота 20г гідC) Метил 3-[(2,4-дихлор-3рохлориду 3-аміно-3-(бензо[1,3]діоксол-5метилбензолсульфоніл)феніламіно]пропіонат іл)пропіонової кислоти вносять у 10мл ацетону, Суміш 1,5г сполуки, одержаної у А), 1,03г спокраплями додають 30мл води і 38мл TEA при -5°С луки, одержаної у В) і 0,08г ДМАП у 20мл піридину і 14мл фенілацетилхлориду у 20мл ацетону з поперемішують 1год. при КТ. Реакційну суміш концедальшим перемішуванням протягом 2год. при нтрують під вакуумом, залишок екстрагують 5°С. Ацетон концентрують, водну фазу промиваEtOAc, органічну фазу промивають буферним розють Et2O і нерозчинний матеріал видаляють фільчином з рН=2, насиченим розчином NaCI, сушать труванням. Фази розділяють відстоюванням і воднад Na2SO4 і розчинник випарюють під вакуумом, ну фазу промивають Et2O і підкислюють 1Η НСІ до одержуючи 2,32г бажаного продукту. рН 2. Утворену фазу вливають у ДХМ, осад відфіD) 3-[(2,4-дихлор-3льтровують з відсмоктуванням і промивають ДХМ, метилбензолсульфоніл)феніламіно]пропіонова одержуючи 24г бажаної сполуки. кислота B) (R) 3-аміно-3-(бензо[1,3]діоксол-58,7мл 1N КОН додають до розчину 2,32г споіл)пропіонов кислота НСІ. луки, одержаної на попередньому етапі, у 10мл 4г сполуки з попереднього етапу вносять у ЕtOН і 10мл діоксану, і суміш перемішують протя150мл води, додають 12,23мл 1N КОН і суміш пегом ночі при КТ. Реакційну суміш концентрують під ремішують протягом 15хвил. при КТ. рН розчину вакуумом, залишок вносять у насичений розчин становить приблизно 11; додають АсОН і рН доNaHСО3 розчин, водну фазу промивають етером, водять до 7,5±0,1. Додають 250мкл пеніциліну і підкислюють до рН 1 доданням 1Η НСІ і екстрагусуміш перемішують протягом ночі при КТ, підтриють ДХМ. Органічну фазу промивають водою, сумуючи рН 7,5±0,1. Суміш підкислюють до рН 2 шать над Na2SO4 і розчинник випарюють під вакудоданням 1Η НСІ і потім промивають ЕtOАс. Водумом, одержуючи 0,912г бажаного продукту. ну фазу гріють при 65°С з активованим рослинним -1 ЯМР: (млн ): 2,35: t: 2Н; 2,5: s: 3Н; 4,0: t: 2Н; вуглем протягом 5хвил., суміш фільтрують через 7,15 до 7,4: не розд.: 5Н; 7,45 до 7,65: q: 2H; 12,2 Celite, водну фазу промивають Et2O, концентрують дo 12,5: bs: 1H. до сухості і випарюють. Залишок вносять у суміш Препарат 1.11 МеОН/ДХМ (6/4; об'єм/об'єм), нерозчинний мате2,5-доксопіролідин-1-іл 3-(нафталін-2ріал (неорганічний) видаляють, органічну фазу сульфоніламіно)-3-фенілпропіонат сушать над сульфатом натрію і концентрують, 1,13г 1,3-дициклогексилкарбодііміду додають одержуючи 1,75г бажаної сполуки. до суміші 1,78г Препарату 1.1 і 0,578г NЯМР: 6 (млн.-1): 2,7-3,1: mt: 2Н; 4,4: не розд.: гідроксисукциніміду у 15мл ДМФ, і суміш перемі1Н; 6,0: s: 2H; 6,9: q: 2H; 7,1: s: 1H. шують протягом ночі при КТ. Після відфільтровуC) (R) 3-(N-Вос)аміно-3-(бензо[1,3]діоксол-5вання з відсмоктуванням одержують 1,3іл)пропіонова кислота дициклогексилсечовину. Фільтрат розбавляють 1,30г сполуки, одержаної на попередньому вод і екстрагують ЕtOАс, органічну фазу промиваетапі, вносять у 20мл діоксану і 20мл води; додають насиченим розчином NaHCO3, насиченим розють 8мл TEA і потім 1,54г (Вос)2O, і суміш перемічином NaCI, сушать над Na2SO4 і розчинник випашують протягом ночі при КТ. Реакційну суміш розрюють під вакуумом, одержуючи 1,81г бажаного бавляють водою, промивають Et2O і потім продукту. підкислюють до рН 2 доданням KHSO4/K2SO4. Препарат 1.12 Утворену суміш екстрагують ЕtOАс і потім проми3-Феніл-3-(хінолін-2вають насиченим розчином NaCI, одержуючи сульфоніламіно)пропіонова кислота 0,850г бажаної сполуки. 25 D=+54° (с=0,5; МеОН) Сполуки формули (II), наведені у таблиці III, можуть бути отримані способами, описаними вище. Цю сполуку одержують згідно зі способом, описаним для Препарату 3.13 заявки WO 97/25315. Препарат 1.13 (R) 3-(N-Вос)амiно-3-(бензо[1,3]дюксол-5іл)пропіонова кислота 47 75906 48 Препарат 1.14: ЯМР: 2,2млн-1: mt: 2Н; 2,8млн-1: s: 6H; 4,5млн-1: t: 1H; 6,9млн-1: mt: 6H; 7,2млн-1: d: 1H; 7,4млн-1: t: 1H; 7,55млн1 : t: 1H; 7,9млн-1: d: 1H; 8,3млн-1: t: 1Н. Препарат 1.15: ЯМР; 2,55млн-1: mt: 2Н; 4,65млн-1: mt: 1Н; 6,4-8,0млн-1: mt: 15Η; 8,1млн-1: s: 1Н; 8,4млн-1: d: 1Н. Препарат 1.16: ЯМР; 2,5-2,7млн-1: mt: 2H; 4,7млн-1: q: 1H; 7,0-8,1млн-1: mt: 11H; 8,5млн-1: d: 1Н. Препарат 1.17: ЯМР (ДМСО+ТФК): 2,4млн-1: t: 2H; 2,55млн-1: s: 3H; 4,0млн-1: t: 2H; 6,05млн-1: s: 2H; 6,6млн-1: dd: 1H; 6,8млн-1: mt: 2H; 7,55млн-1: d: 1H; 7,65млн-1: d: 1H. Препарат 1.18: ЯМР (ДМСО+ТФК): 2,402,65млн-1: mt: 2H; 4,60-4,75млн-1: t: 1H; 6,20млн-1: s: 1Н; 7,10-8,40млн-1: не розд.: 9Н. Препарат 1.25: ЯМР (250MHz): 2,35-2,45млн-1: t: 2H; 3,80-3,90млн-1: t: 2H; 7,30-8,60млн-1: mt: 11Η. Препарат 1.26: ЯМР (250MHz): 2,35-2,45млн-1: t: 2H; 2,50млн-1: s: 3Н; 3,95-4,05млн-1: t: 2H; 7,358,50млн-1: mt: 6H. Препарат 1.27: ЯМР (250MHz): 2,40млн-1: s: 3Н; 2,50-2,60млн-1: t: 2H; 4,15-4,25млн-1: t: 2H; 7,558,65млн-1: mt: 6H. Препарат 1.28: ЯМР: 2,55-2,75млн-1: t: 2H; 4,15-4,45млн-1: t: 2H; 7,55-8,75млн-1: mt: 11Н. Препарат 1.29: ЯМР (ДМСО+ТФК): 2,4млн-1: t: 2H; 2,5млн-1: mt: 5H; 4,0млн-1: t: 2H; 7,25млн-1: dd: 1H; 7,7млн-1: mt: 4H. Препарат 1.30: ЯМР: 2,4млн-1: t: 2Н; 2,5млн-1: mt: 5Н; 4,0млн-1: не розд.: 2Н; 7,3-7,6млн-1: mt: 6Н. Препарат 1.31: ЯМР (ДМСО+ТФК): 1,9млн-1: квінт: 2Н; 2,25млн-1: t: 2H; 2,4млн-1: mt: 4H; 2,85млн-1: t: 4H; 3,85млн-1: t: 2H; 6,8: dd: 1H; 7,0млн-1: не розд.: 2Н; 7,5млн-1: q: 2H. Препарат 1.32 A) 8-(4-метокси)феніл етантіоат 15г 4-метоксибензолтіолу розчиняють у 20мл води, що містять 4,3г NaOH, і суміш перемішують 20хвил. при КТ. 8,5мл 1-хлорацетопе додають краплями і суміш перемішують 1год. при КТ. Реак 49 75906 ційну суміш екстрагують етером (двічі), сушать і випаровують, одержуючи 20г бажаної сполуки. B) 5-метокси-3-метилбензотіофен 10г сполуки з попереднього етапу і 20мл поліфосфатної кислоти змішують у 400мл хлорбензолу, і суміш перемішують 1год. при КТ і потім гріють при 120°С 18год. Реакційну суміш залишають охолодитись і відстоюванням розділяють фази. Залишкове масло вносять у ДХМ (двічі) і фазу знову розділяють відстоюванням. Надосадкові фази об'єднують і випарюють. Залишок вносять у ДХМ і потім промивають водою і далі розчином NaHCO3. Після випарювання розчиннику залишок хроматографують на кремнеземі з елюентом гексан/ ЕtOН (98/2; об'єм/об'єм), одержуючи 5,2г бажаної сполуки. C) (5-метокси-3-метил-1-бензотіофен-2іл)сульфінат літію 1,69г сполуки з попереднього етапу розчиняють у 10мл ТГФ і суміш охолоджують до -20°С. Додають 6,6мл бутиллітію (1,8М у гексані) протягом 15хвил. з подальшим повільним додаванням SO2 до насичення середовища. Після 20 хвилинного перемішування при -20°С суміш залишають нагрітись до КТ. Додають 50мл Et2O і потім фільтрують з відсмоктуванням і сушать, одержуючи 2,4г бажаної сполуки. D) 5-метокси-3-метил-1-бензотіофене-2сульфонілхлорид. 2,4г сполуки з попереднього етапу суспендують у 20мл СН2СІ2, суміш охолоджують до 5°С з подальшим додаванням порціями 1,26г Nхлорсукциніміду і перемішують 1год. при 5°С. Далі суміш промивають воду і воду реекстрагують СН2СІ2, органічні фази об'єднують, промивають розчином NaCI, сушать і випарюють, одержуючи 1,8г бажаної сполуки. ЯМР: 2,50млн-1: s: 3Н; 3,85млн-1: s: 3Н; 7,07,80млн-1: mt: 3H. Ε) Процес продовжують згідно з звичайними методами для одержання бажаної сполуки. Препарат 1.33 A) 6-метокси-3-метил-1-бензотіофен-2сульфонілхлорид Цю сполуку одержують у спосіб, описаний вище. ЯМР: 2,50млн-1: s: 3Н; 3,85млн-1: s: 3Н; 7,07,70млн-1: mt: 3Н. B) Процес продовжують згідно з звичайними методами для одержання бажаної сполуки. Інші сполуки формули (II) одержують, використовуючи, способи, відомі з літератури або описані вище, у рацемічній формі або у формі чистих ізомерів. 50 (а) Цю сполуку одержують з 1бензофуранкарбонітрилу, як це рписано у заявці 540041. Препарат 2.1 Трифлуорацетат 2-аміно-3-(4-ціанофеніл)-1(піролідин-1-іл)пропан-1-ну 7,5г ГФБ додають до суміші 4,06г 2-(третбутоксикарбоніламіно)-3-(4-ціанофеніл)пропіонової кислоти і 1,15мл піролідину у 20мл ДМФ, і суміш перемішують 2год. при КТ, підтримуючи рН 7 додаванням N-етилморфоліну. Реакційну суміш концентрують під вакуумом і залишок хро 51 75906 52 матографують на силікагелі з елюентом хлоророзчином NaCI, сушать над Na2SO4 і розчинник форм/МеОН (95/5; об'єм/об'єм). Одержаний провипарюють під вакуумом, одержуючи першу часдукт вносять у 20мл ТФК у 20мл ДХМ, і реакційну тину 0,54г бажаного продукту. Водні фази і змивку суміш перемішують 30хвил. при КТ і концентрують концентрують під вакуумом, залишок вносять у 2під вакуумом. Залишок вносять у етер і осад відпропанол, нерозчинний матеріал відфільтровують фільтровують з відсмоктуванням, одержуючи 3,95г і фільтрат концентрують під вакуумом, одержуючи бажаного продукту після сушіння. другу частину 0,51г бажаного продукту. Препарат 2.2 G) 2-(трет-бутоксикарбоніламіно)-3-[4-(трет2-аміно-3-[4-(трет-бутиламінометил)феніл]-1бутиламінометил)феніл]-1-(піролідин-1-іл)пропан(піролідин-1-іл)пропан-1-он-біс-(трифлуорацетат) 1-он 0,6мл ДИПЕА додають до суміші 1,03г сполуки, одержаної на попередньому етапі, у 15мл ДМФ з подальшим доданням 0,28мл піролідину і 1,46г ГФБ, і суміш перемішують 4год. при КТ, підтримуючи рН 6 додаванням ДИПЕА. Реакційну суміш А) Етил 2-(бензгідриліденаміно)-3-(4екстрагують ЕtOАс, органічну фазу промивають бромметилфеніл)пропіонат водою, 0,2Η NaOH, водою і насиченим розчином Цю сполуку одержують згідно зі способом, NaCI, сушать над Na2SO4 і розчинник випарюють описаним у [Теtrаhеdrоn: Asymmetry, 1992, 3 (5), під вакуумом, одержуючи 1,3г бажаного продукту у 637-650]. формі масла. B) Етил 2-(бензгідриліденаміно)-3-[4-(третН) Біс(трифлуорацетат) 2-аміно-3-[4-(третбутиламінометил)феніл]пропіонат бутиламінометил)феніл]-1-(піролідин-1-іл)-пропанЦю сполуку одержують за процедурою, описа1-ону ною у [Теtrаhеdrоn: Asimmetry, 1992, 3 (5), 637Суміш 1,29г сполуки, одержаної на поперед650]. ньому етапі, і 17мл ТФК у 15мл ДХМ перемішують C) Етил 2-(бензгідриліденаміно)-3-[450хвил. при КТ. Після концентрування реакційної (бромметилфеніл]пропіонат суміші під вакуумом залишок вносять у ДХМ і роз0,76г К2СО3 додають до розчину 0,58мл третчинник випарюють під вакуумом. Залишок вносять бутиламіну у 8мл ДМФ, і суміш перемішують у етер і розчинник зливають, одержуючи після су20хвил. при КТ. Потім додають розчин 2,15г сполушіння 1,5г бажаного продукту у формі піни, яку ки, одержаної на попередньому етапі, у 3мл ДМФ і використовують без очищення у Прикладі 2. суміш перемішують 3год. 30хвил. при КТ. РеакційПрепарат 2.3 ну суміш екстрагують EtOAc, органічну фазу про2-аміно-3-[4-(N-пропіл-Nмивають водою і насиченим розчином NaCI, суметиламінометил)феніл]-1-(піролідин-1-іл)пропаншать над Na2SO4 і розчинник випарюють під 1-он вакуумом, одержуючи 2,67г бажаного продукту у формі масла. D) Етил 2-аміно-3-[4-(третбутиламінометил)феніл] пропіонат Суміш 2,66г сполуки, одержаної на попередньому етапі, і 30мл водного розчину 1Η НСІ у 30мл етеру перемішують протягом ночі при КТ. Після Цю сполуку одержують за Схемою 9 розділення фаз відстоюванням до кислотної вод(А) Дигідрохлорид 2-(третної фази додають ЕtOАс і суміш підлужують до рН бутоксикарбоніламіно)-3-(4-ціанофеніл)-111 доданням 10Η NaOH. Після розділення фаз (піролідин-1-іл)-пропан-1-ону відстоюванням органічну фазу промивають водою 7,5г ГФБ додають до суміші 4,06г 2-(треті насиченим розчином NaCI, сушать над Na2SO4 і бутоксикарбоніламіно)-3-(4-ціанофеніл)розчинник випарюють під вакуумом, одержуючи пропіонової кислоти і 1,15мл піролідину у 20мл 0,88г бажаного продукту у формі масла. ДМФ, і суміш перемішують 2год. при КТ, підтримуE) Етил 2-(трет-бутоксикарбоніламіно)-3-[4ючи рН 7 додаванням N-етилморфоліну. Реакційну (трет-бутиламінометил)феніл]пропіонат 0,7г дисуміш концентрують під вакуумом і залишок хротрет-бутилдикарбонату додають порціями до розматографують на силікагелі з елюентом хлорочину 0,88г сполуки, одержаної на попередньому форм/МеОН (95/5; об'єм/об'єм), одержуючи 3,8г етапі, у 12мл діоксану, і суміш перемішують 1год. бажаного продукту. 30хвил. при КТ. Реакційну суміш екстрагують В) 2-(трет-бутоксикарбоніламіно)-3-(4ЕtOАс, органічну фазу промивають водою і насиформілфеніл)-1-(піролідин-1-іл)пропан-1-он ченим розчином NaCI, сушать над Na2SO4 і розРозчин 2г сполуки, одержаної на попередньочинник випарюють під вакуумом, одержуючи 1,34г му етапі, у 150мл суміші піридин/АсОН/Н2О (2/1/1; бажаного продукту у формі масла. об'єм/об'єм/об'єм) охолоджують до 0°С, додають F) 2-(трет-бутоксикарбоніламіно)-3-[4-(трет10,57г гідрату гіпофосфіту натрію в атмосфері арбутиламінометил)феніл]пропіонова кислота гону з подальшим доданням 1,8г нікелю Raney у Суміш 1,33г сполуки, одержаної на попередводі, і суміш перемішують 10хвил. при КТ. Реакньому етапі, і 0,75мл 8,3N КОН у 8мл МеОН переційну суміш гріють при 50°С протягом 3год. Після мішують 2год. при КТ. Додають суміш хлороохолодження до КТ суміш фільтрують через форм/вода і суміш підкислюють до рН 4 доданням Celite , промивають EtOH і потім ДХМ, і фільтрат 10Η НСІ. Після розділення фаз відстоюванням концентрують під вакуумом. Залишок екстрагують органічну фазу промивають водою і насиченим 53 75906 54 ЕtOАс, органічну фазу промивають водою, 5%-ним ньому етапі, і 1,3мл 8,314 КОН у 15мл МеОН перозчином KHSO4, насиченим розчином NaCI, наремішують 3год. при КТ. Далі додають 0,3мл 8,3Ν сиченим розчином NaHCO3 і насиченим розчином ΚΟΗ і суміш перемішують 1год. при КТ. До реакNaCI, сушать над Na2SO4 і розчинник випарюють ційної суміші додають суміш ЕtOАс/Н2О і одержану під вакуумом. Залишок хроматографують на силісуміш підкислюють до рН 3,7 доданням 1Η НСІ. кагелі з елюентом ЕtOАс, одержуючи 1,7г бажаноПісля розділення фаз відстоюванням, органічну го продукту; темп. пл. 134°С. фазу промивають водою і насиченим розчином С) 2-(трет-бутоксикарбоніламіно)-3-[4-NNaCI, сушать над Na2SO4 і розчинник випарюють пропіл-N-метиламіно метил)феніл]-1-(піролідин-1під вакуумом одержуючи першу порцію бажаного іл)пропан-1-он продукту. Водну фазу концентрують під вакуумом, 0,42мл АсОН і потім 0,707г триацетоксиборогізалишок вносять у суміш МеОН/2-пропанол (1/1; дриду натрію додають до суміші 0,77г сполуки, об'єм/об'єм), нерозчинний матеріал відфільтровуодержаної на попередньому етапі, і 0,34мл Nють і фільтрат концентрують під вакуумом, одерметилпропіламіну у 10мл 1,2-ДХМ, і суміш пережуючи другу порцію - 1,66г бажаного продукту у мішують протягом ночі при КТ. Реакційну суміш форм білої твердої речовини. розбавляють ДХМ, органічну фазу промивають E) 2-(трет-бутоксикарбоніламіно)-3-[4-[N,Nнасиченим розчином NaHCO3 і насиченим розчибіс(2-гідроксиетил)амінометил]-феніл]-1ном NaCI, сушать над Na2SO4 і розчинник випа(піролідин-1-іл)пропан-1-он. рюють під вакуумом, одержуючи 0,9г бажаного Цю сполуку одержують згідно зі способом, продукту. описаним у F) для Препарату 2.2, починаючи з D) Дигідрохлорид 2-аміно-3-[4-(N-пропіл-N0,95г сполуки, одержаної на попередньому етапі, у метиламінометил)феніл]-1-(піролідин-1-іл)-пропан12мл ДМФ, 0,6мл ДИПЕА, 0,24мл піролідину і 1,44г 1-ону ГФБ, що дає бажаний продукт у воскоподібній фо5мл 10Η НСІ додають до суміші 0,88г сполуки, рмі, який використовується без очищення у настуодержаної на попередньому етапі, у 10мл МеОН і пній операції. 5мл діоксану, і суміш перемішують 4год. при КТ. F) Біс(трифлуорацетат) 2-аміно-3-[4-[N,N-біс(2Додають EtOH і реакційну суміш концентрують під гідроксиетил)амінометил]феніл]-1-(піролідин-1вакуумом. Залишок вносять у етер і осад фільтруіл)пропан-1-ону ють з висмоктуванням після перетирання, одерЦю сполуку одержують згідно зі способом, жуючи 0,83г бажаного продукту; темп.пл. 140°С описаним у G) для Препарату 2.2, починаючи зі (розкл.). сполуки, одержаної на попередньому етапі, і 18мл Препарат 2.4 ТФК у 15мл ДХМ, що дає бажаний продукт, який Біс(трифлуорацетат) 2-аміно-3-[4-[N,N-біс(2використовується без очищення у Прикладі 4. гідроксиетил)амінометил]феніл]-1-(піролідин-1Препарат 2.5 іл)пропан-1-ону Трис(трифлуорацетат) 1,2-біс[4(діетиламінометил)феніл]етиламіну A) Етил 2-(бензгідрилідинаміно)-3-[4-[N,Nбіс(2-гідроксиетил)амінометил]феніл]пропіонат Цю сполуку одержують згідно зі способом, описаним у В) для Препарату 2.2, починаючи з 0,925г діетаноламіну у 15мл ДМФ, 1,21г К2СО3 і 3,6г, сполуки одержаної у А) для Препарату 2.2 у 20мл ДМФ, і одержують 4,23г бажаного продукту у формі масла. B) Етил 2-аміно-3-[4-[N,N-біс(2гідроксиетил)амінометил]феніл]пропіонат Цю сполуку одержують згідно зі способом, описаним у С) для Препарату 2.2, починаючи з 4,22г, сполуки одержаної на попередньому етапі, і 70мл 1Η НСІ у 70мл етеру, з одержанням 1,87г бажаного продукту у воскоподібній формі. C) Етил 2-(трет-бутоксикарбоніламіно)-3-[4[N,N-біс(2-гідроксиетил)амінометил]феніл]пропіонат Цю сполуку одержують згідно зі способом, описаним у D) для Препарату 2.2, починаючи з 1,87г сполуки, одержаної на попередньому етапі, у 20мл діоксану і 1,4г ди-трет-бутилдикарбонату, що дає 2,15г бажаного продукту. D) 2-(трет-бутоксикарбонтам1но)-3-[4-[N,Nбiс(2-Гідроксиетил)амінометил]-фенiл]-пропіонова кислота Суміш 2,13г сполуки, одержаної на поперед A) Метил 4-(азидометил)бензоат 8,13г азиду натрію додають протягом 5хвил. до розчину 5,73г 4-(бромметил)бензоату метилу у 30мл ДМСО, і суміш перемішують 3год. 30хвил. при КТ. Реакційну суміш екстрагують етером, органічну фазу промивають водою і насиченим розчином NaCI, сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи 4,72г бажаного продукту у формі безбарвного масла. B) Гідрохлорметил 4-(амінометил)бензоат Розчин 4,71г сполуки, одержаної на попередньому етапі, у 30мл ТГФ охолоджують до 4°С, протягом 30хвил. порціями додають 6,57г трифенілфосфіну, і суміш перемішують 6год. з підвищенням температури до КТ. Далі додають 0,68мл води і суміш перемішують 16год. при КТ. Реакційну суміш екстрагують EtOAc, органічну фазу промивають водою і насиченим розчином NaCI, сушать над Na2SO4 і розчинники випарюють під вакуумом. Залишок вносять у етер, нерозчинний матеріал відфільтровують, фільтрат концентрують під вакуумом і залишок хроматографують на силікагелі з елюентом хлорформ/МеОН/NН4ОН (90/10/0,2; об'єм/об'єм/об'єм). Одержаний продукт вносять у МеОН, додають 10Η НСІ до рН 1 і суміш концентрують під вакуумом, одержуючи 4,25г ба 55 75906 56 жаного продукту. ного продукту. C) Метил 4Н) N-(трет-бутоксикарбонт)-1,2-біс[4(бензгідриліденамінометил)бензоат (діетиламінометил)феніл]етиламін Суміш 3,03г сполуки, одержаної на попередСуміш 1,2г сполуки, одержаної на попередньому етапі, 2,07мл триетиламіну і 2,51мл бензоньому етапі, і 1,05мл діетиламіну у 20мл ЕtOН гріфеноніміну у 50мл ДХМ перемішують протягом ють при 60°С протягом 4год. Після охолодження ночі при КТ. Реакційну суміш екстрагують ДХМ, до КТ, реакційну суміш екстрагують EtOAc, органіорганічну фазу промивають водою і насиченим чну фазу промивають вод, насиченим розчином розчином NaCI, сушать над Na2SO4 і розчинник NaHCO3, водою і насиченим розчином NaCI, сувипарюють під вакуумом, одержуючи 5,33г бажашать над Na2SO4 і розчинник випарюють під вакуного продукту у формі масла. умом. Залишок хроматографують на силікагелі з D) Метил 4-[1-аміно-2-(4елюентом хлороформ/МеОН/NН4ОН (85/15/0,2; метоксикарбонілфеніл)етил]бензоат об'єм/об'єм/об'єм) і одержують 0,51г бажаного Розчин 5,32г сполуки, одержаної на попередпродукту. ньому етапі, у 40мл ТГФ охолоджують до -50°С, І) 1,2-біс[4-(діетиламінометил)феніл]етиламін протягом 35хвил. додають 10,3мл 1,6М розчину nтрис(трифлуорацетат). бутиллітію у гексані і суміш перемішують 30хвил. Суміш 0,5г сполуки, одержаної на попередпри -50°С - -30°С. Реакційну суміш охолоджують ньому етапі, і 12мл ТФК у 10мл ДХМ перемішують до -50°С, протягом 35хвил. додають розчин 3,78г 45хвил. при КТ. Реакційну суміш концентрують під метил 4-(бромметил)бензоату у 25мл ТГФ і суміш вакуумом, залишок вносять у ДХМ і концентрують перемішують 4год. після чого температура має під вакуумом, одержуючи бажаний продукт у форповернутись до КТ. Далі додають 50мл 1Η НСІ і мі масла. реакційну суміш перемішують 16год. при КТ. Фази Препарат 2.6 реакційної суміші розділяють відстоюванням, кисДигідрохлорид 2-аміно-3-[4-(піперид-1лотну фазу промивають етером, кислотну водну ілметил)феніл]-1-(піролідин-1-іл)пропан-1-ону фазу підлужують до рН 10 доданням 10Η NaOH і екстрагують ЕtOАс, органічну фазу промивають водою і насиченим розчином NaCI, сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи 3,88г бажаного продукту у форм пастопоЦю сполуку одержують згідно зі способом, дібної твердої речовини. описаним у С) для Препарату 2.3, починаючи з E) Метил 4-[1-(трет-бутоксикарбоніламіно)-20,84г сполуки, одержаної у В) для Препарату 2.3, (4-метоксикарбонілфеніл)-етил]-бензоат 0,263мл піперидину, 10мл 1,2-дихлоретану, 2,94г ди-трет-бутилдикарбонату додають про0,452мл АсОН і 0,771г триацетоксиборгідриду натягом 10хвил. до розчину 3,88г сполуки, одержаної трію. на попередньому етапі, у 30мл діоксану і суміш A) 2-(трет-бутоксикарбоніламіно)-3-[4-(піперидперемішують 3год. при КТ. Реакційну суміш екст1-ілметил)феніл]-1-піролідин-1-іл)-пропан-1-он рагують ЕtOАс, органічну фазу промивають воРеакційну суміш розбавляють ДХМ, органічну дою, буферним розчином KHSO4/K2SO4, водою і фазу промивають насиченим розчином NaHCO3 і насиченим розчином NaCI, сушать над Na2SO4 і насиченим розчином NaCI, сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи розчинник випарюють під вакуумом. Одержаний 2,3г бажаного продукту після кристалізації з етеру. продукт вносять в етер, нерозчинний матеріал F) N-трет-бутоксикарбоніл-1,2-біс[4відфільтровують і фільтрат концентрують під ва(гідроксиметил)феніл]етиламін куумом, одержуючи 0,975г бажаного продукту у Розчин 1,24г сполуки, одержаної на попередформі масла. ньому етапі, у 15мл ТГФ додають протягом B) Дигідрохлорид 2-аміно-3-[4-(піперид-140хвил. до суспензії 0,456г алюмогідриду літію у ілметил)феніл]-1-(піролідин-1-іл)пропан-1-ону 25мл ТГФ, і суміш перемішують 2год. при КТ. ДоЦю сполуку одержують згідно зі способом, дають суміш ЕtOАс/льод і реакційну суміш екстраописаним у D) для Препарату 2.3, починаючи з гують ЕtOАс, органічну фазу промивають водою і 0,97г сполуки, одержаної на попередньому етапі, насиченим розчином NaCI, сушать над Na2SO4 і 10мл МеОН, 5мл діоксану і 5мл 10Η НСІ, що дає розчинник випарюють під вакуумом, одержуючи 0,91г бажаного продукту; темп. пл. 170°С (розкл.) 0,95г бажаного продукту у формі білої твердої реЯМР: 1,2-2,0млн-1: не розд.: 10Н; 2,4-3,4млн-1: човини. не розд.: 10Н; 4,2млн-1: bs: 3Н; 7,2млн-1: d: 2Н; G) 4-[2-(трет-бутоксикарбоніламіно)-2-(47,6млн-1: d: 2H; 8,4млн-1: s: 3Н; 11,2млн-1: s: 1H. метансульфонілоксиметилфеніл)-етилбензилПрепарат 2.7 метансульфонат Дигідрохлорид 2-аміно-3-[4Розчин сполуки, одержаної на попередньому (діетиламінометил)феніл]-1-(піролідин-1етапі, у 20мл ДХМ і 3мл ТГФ охолоджують до 4°С, іл)пропан-1-ону додають 0,82мл триетиламін і потім протягом 10хвил. додають розчин 0,45мл метансульфонілхлориду 1мл ДХМ, і суміш перемішують 3год. 30хвил. при КТ. Реакційну суміш екстрагують ДХМ, органічну фазу промивають водою і насиченим розчином NaCI, сушать над Na2SO4 і розчинник Операції D, Ε і F виконуються за Схемою 10. випарюють під вакуумом, одержуючи 1,21г бажа 57 75906 58 А) Етил 2-(бензгідриліденаміно)-3-[4ють, одержуючи 1,37г бажаного продукту у формі (діетиламінометил)феніл]пропіонат смоли. Суміш 1г сполуки, одержаної у А) для ПрепаПрепарат 2.8 рату 2.2, 0,235мл діетиламіну і 0,307г К2СО3 у Біс(трифлуорацетат) 2-аміно-3-[410мл ДМФ перемішують 2год. при КТ. Реакційну (діетиламінометил)феніл]-N-ізопропіл-Nсуміш екстрагують з EtOAc, органічну фазу промиметилпропіон-аміду вають водою, насиченим розчином NaHCO3 і насиченим розчином NaCI, сушать над Na2SO4 і розчинник випарюють під вакуумом, одержуючи 0,927г бажаного продукту у формі масла. B) Етил 2-аміно-3-[4A) 2-(трет-бутоксикарбоніламіно)-3-[4(діетиламінометил)феніл]пропіонат (діетиламінометил)феніл]-N-ізопропіл-N-метилСуміш 0,927г сполуки, одержаної на попередпропіонамід ньому етапі, і 20мл 1Η НСІ у 30мл етеру перемі0,279мл триетиламіну додають до суміші 0,7г шують 2год. при КТ. Після розділення фаз відстосполуки, одержаної у D) для Препарату 2.7 і юванням, кислотну водну фазу промивають 0,208мл N-метилізопропіламіну у 10мл ДМФ з поетером, водну фазу підлужують до рН 11 додандальшим доданням 0,973г ГФБ, і суміш перемішуням твердого NaHCO3 і екстрагують ДХМ, органічють 2год. при КТ. Реакційну суміш вливають у воду ну фазу промивають насиченим розчином NaCI, і екстрагують ЕtOАс, органічну фазу промивають сушать над Na2SO4 і розчинник випарюють під водою, насиченим розчином NaHCO3 і насиченим вакуумом, одержуючи 0,395г бажаного продукту. розчином NaCI, сушать над Na2SO4 і розчинник C) Етил 2-(трет-бутоксикарбоніламіно)-3-[4випарюють під вакуумом, одержуючи 0,65г бажа(діетиламінометил)феніл]пропіонат ного продукту. 1,72г ди-трет-бутилдикарбонату додають до B) Біс(трифлуорацетат) 2-аміно-3-[4розчину 2г сполуки, одержаної на попередньому (діетиламінометил)феніл]-N-ізопропіл-N-метилетапі, у 20мл ДХМ з подальшим доданням 1,1мл пропіонаміду триетиламіну, і суміш перемішують 2год. при КТ. 5мл ТФК додають до розчину 0,63г сполуки, Реакційну суміш концентрують під вакуумом, заодержаної на попередньому етапі, у 5мл ДХМ і лишок екстрагують EtOAc, органічну фазу промисуміш перемішують 2год. при КТ. Реакційну суміш вають водою і насиченим розчином NaCI, сушать концентрують під вакуумом, залишок вносять у над Na2SO4 і розчинник випарюють під вакуумом, ізоетер і розчинник після перетирання зливають, одержуючи 2,6г бажаного продукту; темп. пл. 56°С. одержуючи бажаний продукт після сушіння під D) 2-трет-бутоксикарбоніламіно)-3-[4вакуумом. (діетиламінометил)феніл]пропіонова кислота Препарат 2.9 10,1мл 1N КОН додають до розчину 2,55г споДигідрохлорид 2-аміно-3-[4луки, одержаної на попередньому етапі, у 60мл (діетиламінометил)феніл]-N,NЕtOН і 20мл діоксану, і суміш гріють протягом 1год. діізопропілпропіонаміду при 60°С. Після охолодження до КТ додають 10мл (III), 2HCI: Υ - -CO-N-(iPr)2; Z - -CH2-N(Et)2 1Η НСІ і реакційну суміш концентрують під вакууА) 2-(трет-бутоксикарбоніламіно)-3-(4мом. Залишок азеотропують доданням суміші ціанофеніл)-N,N-діізопропілпропіонамід ЕtOН/толуол і потім концентрують під вакуумом. Суміш 1г 2-(трет-бутоксикарбоніламіно)-3-(4Залишок вносять у суміш ДХМ/МеОН (9/1; ціанофеніл)пропіонової кислоти і 0,540г діізопропіоб'єм/об'єм), нерозчинний матеріал відфільтровуламіну у 10мл ДХМ охолоджують до 0°С, додають ють і фільтрат концентрують під вакуумом, одер0,960мл триетиламіну і потім 1,76г гексафлуорфожуючи 2,4г бажаного продукту. сфату бромтрипіролідинфосфонію, і суміш переE) 2-(трет-бутоксикарбоніламіно)-3-[4мішують 2год., після чого залишають нагрітись до (діетиламінометил)феніл]-1-(піролідин-1КТ. Реакційну суміш концентрують під вакуумом, іл)пропан-1-он залишок екстрагують ЕtOАс, органічну фазу про0,61мл триетиламіну і потім 2,12г ГФБ додамивають водою, 5%-м розчином KHSO4, водою, ють до суміші 1,53г сполуки, одержаної на поперенасиченим розчином NaHCO3 і насиченим розчидньому етапі, і 0,365мл піролідину у 10мл ДМФ, і ном NaCI, сушать над Na2SO4 і розчинник випасуміш перемішують 2год. при КТ. Реакційну суміш рюють під вакуумом. Залишок хроматографують вливають у воду і екстрагують EtOAc, органічну на силікагелі гелі з елюентом гептан/ЕtOАс (80/20; фазу промивають водою, насиченим розчином об'єм/об'єм) і одержують 0,4г бажаного продукту; NаНСО3 і насиченим розчином NaCI, сушать над темп. пл. 172°С. Na2SO4 і розчинник випарюють під вакуумом, одеВ) 2-(трет-бутоксикарбоніламіно)-3-(4ржуючи 1,5г бажаного продукту. формілфеніл)-N,N-діізопропілпропіонамід F) Дигідрохлорид 2-аміно-3-[4Цю сполуку одержують згідно зі способом, (діетиламінометил)феніл]-1-(піролідин-1описаним у В) для Препарату 2.3, починаючи з іл)пропан-1-ону 6мл концентрованої НСІ додають 0,380г сполуки, одержаної на попередньому етапі, до розчину 1,5г сполуки, одержаної на поперед25мл суміші піридин/АсОН/Н2О) (2/1/1; ньому етапі, у 20мл діоксану і 10мл МеОН, і суміш об'єм/об'єм/об'єм), 1,8г гідрату гіпофосфіту натрію перемішують протягом ночі при КТ. Реакційну суі 0,31г нікелю Raney , одержуючи 0,35г бажаного міш концентрують під вакуумом і залишок вносять продукту без хроматографії; темп. пл. 152°С. у ЕtOН і концентрують під вакуумом. Залишок вноC) 2-(трет-бутоксикарбоніламіно)-3-[4сять у етер і після розтирання розчинник злива(діетиламінометил)феніл)-N,N-діізопропілпропіон 59 75906 60 амід сушать над Na2SO4 і розчинник випарюють під Цю сполуку одержують згідно зі способом, вакуумом. Залишок хроматографують на силікагеописаним у С) для Препарату 2.3, починаючи з лі з елюентом з гептан/ЕtOАс від (60/40; 0,333г сполуки, одержаної на попередньому етапі, об'єм/об'єм) до (40/60; об'єм/об'єм) і одержують 0,135мл діетиламіну, 10мл 1,2-дихлоретану, 1,3г бажаного продукту. 0,08мл АсОН і 0,281г триацетоксиборгідриду наD) N-трет-бутоксикарбоніл-2-(4трію, що дає 0,4г бажаного продукту. гідроксиметилфеніл)-1-(пірид-3-іл)етиламін D) Дигідрохлорид 2-аміно-3-[4Розчин 1,13г сполуки, одержаної на поперед(діетиламінометил)феніл]-N,Nньому етапі, у 30мл ТГФ охолоджують -78°С в атдіізопропілпропіонамщу мосфері аргону, краплями додають 7,2мл 1М роз5мл концентрованої НСІ додають до суміші чину гідриду діізобутилалюмінію у толуолі і суміш 0,4г сполуки, одержаної на попередньому етапі, у перемішують 2год. з підвищенням температури до 10мл МеОН і 5мл діоксану, і суміш перемішують 0°С. Реакційну суміш охолоджують -40°С, додають протягом ночі при КТ. Реакційну суміш концентру7,2мл 1М розчину гідриду діізобутилалюмінію у ють під вакуумом, залишок вносять у ЕtOН і випатолуолі і суміш перемішують 2год. з підвищенням рюють під вакуумом, одержуючи 0,37г бажаного температури до 0°С. Додають 40мл насиченого продукту. розчину NH4CI, суміш екстрагують ЕtOАс, органічПрепарат 2.10 ну фазу промивають водою і насиченим розчином Трис(трифлуорацетат) 2-[4NaCI, сушать над Na2SO4 і розчинник випарюють (дііетиламінометил)феніл]-1-(пірид-3-іл)етиламіну під вакуумом. Залишок хроматографують на силікагелі з елюентом ДХМ/ ЕtOАс (40/60; об'єм/об'єм) і одержують 0,62г бажаного продукту після кристалізації з етеру; темп. пл. 130°С. E) N-(трет-бутоксикарбоніл)-2-[4(діетиламінометил)феніл]-1-(пірид-3-іл)етиламін A) Бензгідриліденпірид-3-ілметиламін Розчин 0,61г сполуки, одержаної на поперед1,7мл 3-(амінометил)піридину додають до роньому етапі, у 20мл ДХМ охолоджують 0°С, додазчину 2,8мл бензофеноніміну у 50мл ДХМ і суміш ють 0,311мл триетиламіну і потім 0,16мл метансуперемішують протягом ночі при КТ. Додають ще льфонілхлориду, і суміш перемішують 30хвил. при 0,28мл бензофеноніміну і суміш перемішують 0°С. Далі додають 0,58мл діетиламіну і суміш пе2год. при КТ. Реакційну суміш концентрують під ремішують 3год. при КТ. Реакційну суміш вливавакуумом, залишок екстрагують етером, органічну ють у вод і екстрагують ДХМ, органічну фазу профазу промивають водою і насиченим розчином мивають водою і насиченим розчином NaCI, NaCI, сушать над Na2SO4 і розчинник випарюють сушать над Na2SO4 і розчинник випарюють під під вакуумом, одержуючи 4,56г бажаного продукту. вакуумом, одержуючи 0,45г бажаного продукту. B) Метил 4-[2-аміно-2-(пірид-3-іл)етил]бензоат F) Трис(трифлуорацетат)2-[4Розчин 3г сполуки, одержаної на попередньо(діетиламінометил)феніл]-1-(пірид-3-іл)етиламіну му етапі, у 30мл ТГФ охолоджують до -78°С у атСуміш 0,45г сполуки, одержаної на попередфосфері аргону, додають 8,2мл 1,5М розчину дііньому етапі, і 10мл ТФК у 10мл ДХМ перемішують зопропіламіду літію у циклогексані і суміш 15хвил. при КТ. Реакційну суміш концентрують під перемішують 30хвил. з підвищенням температури вакуумом, залишок вносять у етер, розчинник злидо -20°С. Суміш охолоджують знову до -78°С, кравають і одержаний сирий продукт використовують плями додають розчин 2,82г метил-4без подальшого очищення. (бромметил)бензоату у 10мл ТГФ і суміш переміПрепарат 2.11 шують 2год. з підвищенням до КТ. Реакційну суміш Етил 2-аміно-3-[4-(N-етил-Nохолоджують до 0°С, повільно додають 25мл 1Η метиламінометил)феніл]пропіонат НСІ і потім концентрований розчин НСІ з доведенням рН до 2-3, і суміш перемішують протягом ночі при КТ. До реакційної суміші додають суміш етер/вода (1/1; об'єм/об'єм) і після розділення фаз відстоюванням органічну фазу екстрагують розчином 1Η НСІ, об'єднані водні фази підлужують до A) Етил 2-(бензгідриліденаміно)-3-[4-(N-етилрН 8 доданням концентрованого NaOH і екстрагуN-метиламінометил)феніл]пропіонат ють ДХМ, органічну фазу промивають насиченим Суміш 1г сполуки, одержаної у А) Препарату розчином NaCI, сушать над Na2SO4 і розчинник 2.2 і 0,29мл N-метилетиламіну у 10мл ДМФ охоловипарюють під вакуумом, одержуючи 2г бажаного джують 0°С, додають 0,307г карбонату калію і супродукту. міш перемішують 4год. при 0сС. Реакційну суміш C) Метил 4-[2-(трет-бутоксикарбоніламіно)-2вливають у насичений розчин NaCI і екстрагують (пірид-3-іл)етил]бензоат ЕtOАс, органічну фазу промивають насиченим 1,83г ди-трет-бутилдикарбонату додають до розчином NaCI, сушать над Na2SO4 і розчинник розчину 1,95г сполуки, одержаної на попередньовипарюють під вакуумом. Одержаний бажаний му етапі, у 20мл ДХМ з подальшим доданням продукт використовують без подальшого очищен1,16мл триетиламіну, і суміш перемішують 2год. ня. при КТ. Реакційну суміш концентрують під вакууB) Етил 2-аміно-3-[4-(N-етил-Nмом, залишок екстрагують EtOAc, органічну фазу метиламінометил)феніл]пропіонат промивають водою і насиченим розчином NaCI, Суміш сполуки, одержаної на попередньому
ДивитисяДодаткова інформація
Назва патенту англійськоюN-(arylsulfonyl)beta-aminoacid derivatives with substituted aminomethyl group, a method for obtaining thereof and pharmaceutical composition containing thereof
Автори англійськоюMuneaux Yvette, Perreaut Pierre
Назва патенту російськоюПроизводные n-(арилсульфонил)бета-аминокислот, содержащих замещенную аминометильную группу, способ их получения и содержащая их фармацевтическая композиция
Автори російськоюМюно Иветт, Перро Пьер
МПК / Мітки
МПК: C07D 307/79, A61K 31/40, C07D 205/00, C07C 237/30, C07D 215/36, C07D 317/66, C07D 333/62, A61K 31/4184, C07D 317/60, C07D 409/12, C07D 495/04, C07D 317/46, A61P 29/00, C07C 311/19, C07D 405/12, C07D 271/12, C07D 213/76, C07D 211/34, C07D 307/54, C07D 319/00, C07D 233/54, C07D 277/80, C07D 213/40, C07D 307/81, C07D 413/14, C07D 333/24, C07D 307/52, C07D 413/12, C07D 407/12, A61K 31/435, C07D 295/18
Мітки: спосіб, заміщену, містять, фармацевтична, містить, групу, похідні, отримання, композиція, n-(арилсульфоніл)бета-амінокислот, амінометильну
Код посилання
<a href="https://ua.patents.su/62-75906-pokhidni-n-arilsulfonilbeta-aminokislot-yaki-mistyat-zamishhenu-aminometilnu-grupu-sposib-kh-otrimannya-ta-farmacevtichna-kompoziciya-shho-mistit-kh.html" target="_blank" rel="follow" title="База патентів України">Похідні n-(арилсульфоніл)бета-амінокислот, які містять заміщену амінометильну групу, спосіб їх отримання та фармацевтична композиція, що містить їх</a>
Попередній патент: Звуковий автомат
Наступний патент: Дезінфікуючий елемент
Випадковий патент: Спосіб пакетування будівельних виробів












