Спосіб одержання похідних тіазолу, які мають пестицидну активність
Формула / Реферат
1. Спосіб одержання сполуки формули
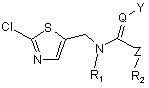 , (I)
, (I)
а також, за певних умов, її E/Z-ізомерів, сумішей E/Z-ізомерів та/або таутомерів, у кожному випадку у вільній формі або у формі солі, де
Q означає СН або N,
Y означає NO2 або CN,
Z означає СНR3, О, NR3 або S,
R1 та R2 або кожен незалежно один від одного означає водень або незаміщений або заміщений радикалом R4 С1-С8алкіл, або спільно означають алкіленовий місток, який містить два або три атоми вуглецю і необов'язково містить гетероатом, вибраний із групи, яка включає NR5, О та S,
R3 означає водень або незаміщений або заміщений радикалом R4 С1-С12алкіл,
R4 означає незаміщений або заміщений арил або гетероарил і
R5 означає Н або С1-С12алкіл, який
полягає в тому, що
а) сполуку формули
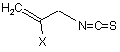 , (II)
, (II)
у якій Х означає групу, яка вилучається, піддають взаємодії з галагенуючим агентом, з одержанням сполуки формули
![]() , (III)
, (III)
у якій W означає атом галогену, або за певних умов її таутомера, у кожному випадку у вільній формі або у формі солі, і
б) одержану сполуку формули (III) піддають взаємодії зі сполукою формули
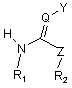 , (IV)
, (IV)
у якій R1, R2, Y, Z і Q мають зазначені для наведеної вище формули (І) значення, при цьому в процесі одержання сполуки формули (III) на стадії а) передбачена стадія очищення, на якій сирий продукт, який утворився, обробляють водою в кислому діапазоні значень рН.
2. Спосіб за п. 1, який відрізняється тим, що переробка сполуки формули (III) на стадії а) полягає в екстракції сполуки формули (III) соляною кислотою з концентрацією в інтервалі від 10 до 50 мас. %.
3. Спосіб за п. 1, який відрізняється тим, що переробка сполуки формули (III) на стадії а) полягає в додаванні до реагуючої маси води в кількості до 500 мол. % при перерахуванні на сполуку формули (II), яку використовують.
4. Спосіб за кожним з пп. 1-3, який відрізняється тим, що стадію а) проводять у неполярному апротонному розчиннику.
5. Спосіб одержання сполуки формули
![]() , (III)
, (III)
або, за певних умов, її таутомера, у кожному випадку у вільній формі або у формі солі, який полягає в тому, що сполуку формули
 , (II)
, (II)
або, за певних умов, її таутомер, у кожному випадку у вільній формі або у формі солі, де Х означає групу, яка видаляється, піддають взаємодії з хлоруючим агентом, при цьому в процесі одержання сполуки формули (III) передбачена стадія очищення, на якій реагуючу масу, яка утворилася, обробляють водою в кислому діапазоні значень рН.
Текст
Даний винахід відноситься до способу одержання сполуки формули а також за певних умов її E/Z-ізомерів, сумішей E/Z-ізомерів та/або 25 таутомерів, у кожному випадку у вільній формі або у формі солі, де Q позначає СН або N, Υ позначає ΝΟ2 або CN, Ζ позначає CHR3, О, NR3 або S, R1 та R2 або кожен незалежно один від одного позначають водень або незаміщений або заміщений радикалом R4 С1-С8алкіл, або спільно позначають алкіленовий місток, який містить два або три атоми вуглецю і необов'язково містить гетероатом, обраний із групи, яка включає NR 5, О та S, R3 позначає водень або незаміщений або заміщений радикалом R4 С1-С12алкіл, R4 позначає незаміщений або заміщений арил або гетероарил і R5 позначає Η або С1-С12алкіл, який полягає у тому, що а) сполуку формули яка є відомою сполукою або яку можна одержувати відомими методами та у якій X позначає групу, яка видаляється, піддають взаємодії з агентом, який галогенує, з одержанням сполуки формули у якій W позначає атом галогену, або за певних умов її та утомера, у кожному випадку у вільній формі або формі солі, і б) отриману сполуку формули (III) піддають взаємодії зі сполукою формули яка є відомою сполукою або яку можна одержувати відомими методами та у якій R1, R2, Υ, Ζ і Q мають зазначені вище для формули (І) значення, при цьому в процесі одержання сполуки формули (III) на стадії а) передбачена стадія очищення, на якій сирий продукт, що утворився, обробляють водою в кислому діапазоні значень рН, а також відноситься до способу одержання сполуки формули (III) відповідно до описаної вище стадії а) і до застосування сполук формул (II), (III) та (IV) у розглянутому ви ще способі. Сполуки формули (І) відомі як ефективні пестициди, а методи їх одержання описані в літературі. Так, зокрема, у літературі описані різні методи одержання ключової сполуки формули (III). Однак при здійсненні таких відомих з літератури методів, як було встановлено, виникають значні проблеми, пов'язані з чистотою сполук зазначеної вище формули (III), а також одержаних з них сполук формули (І), які мають пестицидну активність. Побічні продукти, яки утворюються при одержанні сполук формули (III), можна відокремлювати тільки перегонкою, що супроводжується значними втратами продукту, з використанням складних, пов'язаних з високими витратами часу методів. В результаті істотно погіршується термічна стабільність сполук формули (III), що приводить до виникнення серйозних проблем і подовжує тривалість виробничого циклу. Разом з тим більш високий ступінь чистоти сполук формули (III) впливає на ви хід продукту, який одержують на наступній стадії. Відомі методи мають також серйозні недоліки відносно інших параметрів, таких, наприклад, як вихід продукту, стійкість сполуки формули (III) при збереженні, тривалість циклу синтезу, ви хід продукту за об'ємом, утворення відходів, утилізація яких пов'язана із визначеними проблемами з екологічної і токсикологічної точок зору, утилізація вихідних речовин, які не прореагували, і т.п. Ви ходячи з вищевикладеного, існує необхідність у розробці вдосконалених способів одержання сполук формули (І) і, конкретніше, формули (III). У літературі запропоновані різні методи очищення сполук формули (III), такі наприклад, як утворення гідрохлориду сполуки (III) в органічному розчиннику з наступною фільтрацією і вивільненням сполуки із солі, наприклад за рахунок додавання основи, очищення сирої сполуки формули (III) кристалізацією з придатного для цієї мети розчинника, очищення продукту шляхом випарювання розчинника з наступною фракційною перегонкою при пониженому тиску, виділення продукту шля хом промивання органічної фази, яка його містить, великою кількістю водного розчину основи або ж виділення продукту шля хом промивання твердої органічної фази, яка його містить, великою кількістю води. Недоліком усіх ци х методів у бага тьох випадках є порівняно низький вихід сполуки формули (III) і його низька якість, що не дозволяє використовувати його на наступній стадії. Так, наприклад, у процесі фракційної перегонки неможливо відокремити побічні продукти, властивості кипіння яких аналогічні таким сполук формули (III). При контактуванні реагуючої маси з великою кількістю води при високому значенні рН можливе небажане утворення продуктів гідролізу, що у свою чергу приводить до зниження виходу цільового продукту. Крім цього було, зокрема, встановлено, що сполуки формули (І), які мають пестицидну активність, не виявляють зазначених їх розробниками характеристик: навіть при одержанні сполук формули (III) з високим виходом і з високою якістю, використання для їхнього очищення відомих методів приводило до одержання на наступній стадії сполук формули (І), які мали яскраво виражене коричневе забарвлення і вихід яких залишався на порівняно низькому рівні. При створенні винаходу раптово було встановлено, що очищення сполуки формули (III) запропонованим у винаході способом дозволяє безпосередньо впливати на зовнішній вигляд продукту, який повинний мати забарвлення від білого до бежевого. До описаних вище побічних продуктів, яки досить складно відокремити від основного продукту, відносяться серед інших сполуки формул Найбільш значимим побічним продуктом, який утворюється при одержанні сполук формули (III), є сполука формули (V). Ця сполука часто утворюється в кількості від 6 до 10мас. % при перерахуванні на сполуку формули (III). Було встановлено, що навіть перегонка на багатоходовій тарілчастій або фракціонувальній колонці не дозволяє досить ефективно відокремлювати сполуки формул (V) та (VI). Подібні сполуки впливають на процес синтезу сполук формули (III) і знижують їхній ви хід і якість. При створенні винаходу раптово був розроблений порівняно простий спосіб, який дозволяє легко відокремлювати побічні продукти, яки утворюються в процесі одержання сполук формули (III). Цей спосіб полягає власне кажучи у введенні реагуючої маси, яка містить сполуки формули (III) і можливо сполуку формули , яка не прореагувала, у контакт із водою в кислому діапазоні значень рН із наступним виділенням цільової сполуки формули (III) придатним для цієї мети методом. Для цього до кислої реагуючої масі додають водний розчин або тільки воду. При цьому найбільший інтерес представляють два альтернативних конкретних варіанти здійснення подібного способу, розглянуті нижче. а1) У цьому варіанті реагуючу масу після синтезу сполуки формули (III) обробляють водним розчином кислоти, переважно концентрованої соляної кислоти. При цьому, зокрема, при використанні розчинників, яки змішуються з водою, по завершенні зазначеної обробки розчинник переважно частково або навіть цілком випарювати. При подібній обробці сполука формули (III) переходить з реакційної суміші, яка утворюється у вигляді гідрохлориду, у кислу водну фазу. При цьому побічні продукти, яки легко гідролізуються, розкладаються, а цільовий продукт залишається у незмінному вигляді. У процесі подібного очищення продукту його потім виділяють, наприклад, шляхом підвищення значення рН водної фази, в якій він знаходиться, зокрема розведенням водою або додаванням деякої кількості основи, і шляхом наступного розчинення сполуки формули (III), яка вивільнилася, у органічному розчиннику. Відповідно до одного з більш переважних варіантів отриману сполуку формули (II) потім переганяють. а2) У цьому варіанті перед переробкою сполуки формули (III), необов'язково після відгону деякої кількості розчинника, до реагуючої маси додають воду. У ході цієї операції величина рН водної фази встановлюється на низьке значення за рахунок присутності в реакційній суміші кислоти, яка вивільняється в результаті реакції сполуки формули (II) з агентом, що хлорує. Потім водну фаз у можна знову відокремлювати від органічної фази або відганяти її разом з розчинником без поділу фаз. В одному з особливо кращих варіантів воду додають у настільки малій кількості, саме якої досить для перетворення побічних продуктів, яки гідролізують, у низьколеткі сполуки. Отже, у цьому варіанті, воду не потрібно відокремлювати від розчинника або видаляти її з розчинника азеотропною дистиляцією. Згідно ще одного особливо кращого варіанту отриману сполуку формули (II) потім пропонується піддавати перегонці. Деякі сполуки формул (I)-(IV) містять асиметричні атоми вуглецю, і тому такі сполуки можуть існувати в оптично активних формах. Відповідно до цього до структур, які описуються формулами (I)-(IV), відносяться також всі можливі ізомерні форми і їхні суміші, наприклад рацемати або суміші E/Z-ізомерів. Загальні терміни, яки використовуються вище та у наступному описі, мають, якщо не зазначене інше, такі значення. Якщо не зазначене інше, кожна з груп, яка містить вуглець, і кожна зі сполук, яка містить вуглець, має від 1 до 8 включно, переважно від 1 до 6 включно, найбільше переважно від 1 до 4 включно, насамперед 1 або 2 атоми вуглецю. Алкіл як самостійна група і як структурний елемент інших гр уп і сполук, таких наприклад, як галоалкіл, арилалкіл або гідроксіалкіл, має в кожному випадку з урахуванням конкретної кількості атомів вуглецю, яки є присутніми у групі або сполуці, прямий ланцюг і являє собою, наприклад, метил, етил, пропіл, бутил, пентил або гексил, або розгалужений ланцюг і являє собою, наприклад, ізопропіл, ізобутил, втор-бутил, mpem-бутил, ізопентил, неопентил або ізогексил. Алкеніл як самостійна група і як структурний елемент інших груп і сполук, таких наприклад, як галоалкеніл або арилалкеніл, має в кожному випадку з урахуванням конкретної кількості атомів вуглецю, яки є присутніми у групі або сполуці, прямий ланцюг і являє собою, наприклад, вініл, 1-метилвініл, аліл, 1бутеніл або 2-гексеніл, або розгалужений ланцюг і являє собою, наприклад, ізопропеніл. Алкініл як самостійна група і як структурний елемент інших груп і сполук, таких наприклад, як галоалкініл, має в кожному випадку з урахуванням конкретної кількості атомів вуглецю, яки є присутніми у групі або сполуці, прямий ланцюг і являє собою, наприклад, пропаргіл, 2-бутиніл або 5-гексиніл, або розгалужений ланцюг і являє собою, наприклад, 2-етинілпропіл або 2-пропаргілізопропіл. С3-С6циклоалкіл являє собою циклопропіл, циклобутан, циклопентан або циклогексил, насамперед циклогексил. Арил являє собою феніл або нафтил, насамперед феніл. Під "гетероарилом" мається на увазі 5-7-членне моноциклічне ароматичне кільце з 1-3 гетероатомами, яки обирають з групи, яка включає N, О та S, переважно N та S, або біциклічний гетероарил, який може містити або тільки в одному кільці, як, наприклад, у випадку хінолінілу, хіноксалінілу, індолінілу, бензотіофенілу або бензофуранілу, або незалежно одне від іншого в обох кільцях, як, наприклад, у випадку птеридинілу або пуринілу, один або більше гетероатомів, обраних із групи, яка включає Ν, Ο та S. Кращими при цьому є піридил, піримідиніл, тіазоліл та бензотіазоліл. Галоген як самостійний елемент і як структурний елемент інших груп і сполук, таких, наприклад, як галоалкіл, галоалкеніл і галоалкініл, являє собою фтор, хлор, бром або йод, переважно хлор або бром, найбільш переважно хлор. Галогензаміщені групи, які містять вуглець, і сполуки, такі, наприклад, як галоалкіл або галоалкеніл, можуть бути частково галогенованими або пергалогенованими, при цьому галогенові замісники у випадку багаторазового галогенування можуть бути однаковими або різними. Прикладами галоалкілу як самостійного елементу і як структурного елементу інши х гр уп і сполук, таких, наприклад, як галоалкеніл, є метил, моно-тризаміщений фтором, хлором та/або бромом, наприклад CHF2 або CF3, етил, монопентазаміщений фтором, хлором та/або бромом, наприклад CH 2CF3, CF2CF3, CF2CCl3, CF 2CHCl2, CF2CHF2, CF2CFCl2, CF2CHBr2, CF2CHClF, CF2CHBrF або CClFCHClF, пропіл або ізопропіл, моно-гептазаміщений фтором, хлором та/або бромом, наприклад CH2CHBrCH2Br, CF2CHFCF3, CH2CF2CF3 або CH(CF3)2, та бутил або один з його ізомерів, моно-ноназаміщений фтором, хлором та/або бромом, наприклад CF(CF3)CHFCF3 або CH2(CF2)2CF3 . Галоалкеніл являє собою, наприклад, СН2СН=СНС l, СН2СН= ССl2, CH2CF=CF2 або СН2СН= СНСН2Вr. Під групою X, яка видаляється, вище та у наступному описі мається на увазі будь-яка група, яка видаляється, яку звичайно використовують в хімічних реакціях, як це відомо фахівцям у даній галузі, і яка представляє собою насамперед галоген, такий як фтор, хлор, бром та йод, -О-С(=О)-А, -О-Р(=О)(-А) 2, -OSi(CrC8iuiKbi)3, -О-(СгС8алкіл), -О-арил, -O-S(=O)2A, -S-P(=O)(-A)2 , -S-P(=S)(-A) 2, -S-(С1-С8алкіл), -S-арил, S(=O)A, -S(=O)2 A або -O-C(=O)-A, де А позначає необов'язково заміщений С 1-С8алкіл, С2-С8алкеніл, С2С8алкініл, необов'язково заміщений арил, необов'язково заміщений бензил, С1-С8алкоксигрупу або ди-(С1С8алкіл)амін, у якому алкільні групи вибираються незалежно одна від іншої, або представляє собою NO3, NO2 або суль фат, сульфі т, фосфат, фосфіт, карбоксилат, іміноефіри, N2 або карбамат. Деякі сполуки формул (I)-(IV) можуть бути представлені у формі таутомерів. Відповідно до цього під такими сполуками вище та у наступному описі маються на увазі також відповідні таутомери, навіть якщо це особливо не обговорено в кожному конкретному випадку. Сполуки формул (I)-(IV), які мають щонайменше один основний центр, здатні утворювати, наприклад, кислотно-адитивні солі. Подібні кислотно-адитивні солі утворюються, наприклад, із сильними неорганічними кислотами, такими як мінеральні кислоти, наприклад хлорна кислота, сірчана кислота, азотна кислота, азотиста кислота, фосфорна кислота або галогенводневі їсислоти, із сильними органічними карбоновими кислотами, такими як необов'язково заміщені, наприклад галозаміщені, С1-С4алканкарбонові кислоти, наприклад оцтова кислота, необов'язково ненасичені дикарбонові кислоти, наприклад щавлева, малонова, бурштинова, фумарова або фталева кислоти, гідроксикарбонові кислоти, наприклад аскорбінова, молочна, яблучна, винна або лимонна кислоти, або бензойна кислота, або з органічними сульфокислотами, такими як необов'язково заміщені, наприклад галозаміщені, С1-С4алкан- або арилсульфокислоти, наприклад метан- або и-толуолсульфокислота. Крім цього сполуки формул (I)-(IV), які мають щонайменше одну кислотну групу, здатні утворювати солі з основами. Як приклад таких прийнятних солей можна назвати солі металів, таких як солі лужних і лужноземельних металів, наприклад солі натрію, калію і магнію, або солі амонію або органічного аміну, такого як морфолін, піперидин, піролідин, моно-, ди- або три(нижч.)алкіламіну, наприклад етил-, діетил- , триетил- або диметилпропіламіну, або моно-, ди- або тригідрокси-(нижч.)алкіламіну, наприклад моно-, ди- або триетаноламіну. Крім того, за певних умов можливо також утворення відповідних внутрішніх солей. Під сполуками формул (I)-(IV) ви ще та у наступному описі маються на увазі сполуки формул (I)-(IV) і у вільній формі, і у вигляді відповідних солей. Сказане відповідно справедливо і у відношенні таутомерів сполук формул (I)-(IV) та солей таких та утомерів. Коли мова йде про сполуки формул (І) і (III), то кращим у кожному випадку є спосіб одержання таких сполук у вільній формі. Відповідно до винаходу кращими варіантами його здійснення є наступні: (1) спосіб одержання сполуки формули (І), де R1 і R2 у сполуках формул (І) та (IV) або кожен незалежно один від одного позначає водень або С1-С4алкіл, або спільно позначають дво- або тричленний алкіленовий місток, який необов'язково містить гетероатом, обраний із групи, яка включає NR5, О та S, при цьому R5 являє собою водень або С 1С4алкіл, переважно кожний позначає водень або спільно позначають дво- або тричленний алкіленовий місток, який необов'язково містить гетероатом, обраний із групи, яка включає NR5 та О, при цьому R5 являє собою СгС4алкіл, найбільш переважно R1 і R2 спільно позначають -СН2-О-СН2-, -СН2-СН2-СН2- або -СН2-СН2-, (2) спосіб одержання сполуки формули (І) відповідно до вищенаведеного п.(1), де Q позначає N, (3) спосіб одержання сполуки формули (І) згідно із вищенаведеними пп.(1) та (2), де Υ позначає ΝΟ2, (4) спосіб одержання сполуки формули (І) згідно із вищенаведеними пп.(1)-(3), де Ζ позначає NR3, a R3 позначає водень або С1-С4алкіл, (5) спосіб одержання сполуки формули (І) згідно із вищенаведеними пп.(1)-(4), при цьому на стадії а) реакцію проводять при температурі в інтервалі від -30°С до температури кипіння розчинника, переважно від -20 до 60°С, найбільше переважно від +40 до +60°С, насамперед від +10 до +30°С, (6) спосіб згідно із вищенаведеними пп.(1)-(5), де X у сполуці формули (II) являє собою галоген, такий як фтор, хлор, бром або йод, -О-С(=О)-А, -О-Р(=О)(-А)2 , -O-S(=O) 2 A, -S-P(=O)(-A) 2, -S-P(=S)(-A)2 , -S(=O)A або S(=O)2 A, де А являє собою необов'язково заміщений С 1-С8алкіл, С2-С8алкеніл, С2-С8алкініл, необов'язково заміщений арил, необов'язково заміщений бензил, С1-С8алкоксигрупу або ди(С 1-С8алкіл)амін, при цьому алкільні групи вибираються незалежно одна від іншої, переважно X являє собою хлор, бром або йод, більш переважно хлор або бром, найбільш переважно X являє собою хлор, (7) спосіб згідно із вищенаведеними пп.(1)-(6), де значення рН водної фази під час переробки реакційної суміші, яка містить сполуку формули (III), складає менше 4, переважно менше 2, найбільш переважно менше 1, (8) спосіб згідно із вищенаведеними пп.(1)-(7), де при переробці реакційної суміші відповідно до варіанта аі) екстракцію сполуки формули (III) проводять у водній хлористо-, бромисто- або йодистоводневій кислоті, фосфорній, сірчаній, азотній або хлорній кислоті, при цьому найбільш придатна водна хлористоводнева кислота з концентрацією 1050мас. %, переважно 30-40% мас. %, найбільш переважно 37 мас. %; переважно також використання галогенводневої кислоти, аніон якої відповідає групі W сполук формули (III), (9) спосіб згідно із вищенаведеними пп.(1)-(7), де при переробці реакційної суміші відповідно до варіанта а2) використовують воду в кількості, яка становить до 500 мол. %, переважно 100мол. %, більш переважно до 30 мол. %, при перерахуванні на сполуку формули (II), більш переважно воду використовують у кількості, яка становить до 20мол. % при перерахуванні на сполуку формули (II), особливо переважно воду додають до реакційної суміші в кількості, яка становить до 10мол. % при перерахуванні на сполуку формули (II). (10) спосіб згідно із вищенаведеними пп.(1)-(9), де W у сполуці формули (III) являє собою хлор, (11) спосіб згідно із вищенаведеними пп.(1)-(10), призначений для одержання тіаметоксаму, відомого з заявки WO 98/32747, та Ті-435 (клотіанідину), відомого з ЕР-А-446913. Стадія а) Реакцію на описаній вище і більш докладно розглянутій далі стадії а) при необхідності проводять у герметично закритій посудині, під тиском, в атмосфері інертного газу та/або в безводних умовах. Найбільш кращі умови проведення реакції представлені в приведених нижче прикладах. Придатними агентами, яки хлорують, є, зокрема, хлор, РОСl3, РСl3, РСl5 або SO2CI2, переважно хлор або SO2CI2, найбільше переважно суміш хлору з SO2Cl2 або хлор у із SO2. На цій стадії реагенти можуть у кожному випадку взаємодіяти між собою безпосередньо, тобто без додавання розчинника або розріджувача, наприклад у розплавленому стані. Однак у більшості випадків може виявитися доцільним додавання інертного розчинника або розріджувача, який в умовах реакції є апротонним, або їхньої суміші. Як приклад подібних розчинників або розріджувачів можна назвати ароматичні, аліфатичні та аліциклічні вуглеводні і галогеновані вугле водні, такі як бензол, толуол, ксилол, мезитилен, тетралін, хлорбензол, дихлорбензол, бромбензол, нітробензол, нітрометан, нітроетан, петролейний ефір, гексан, циклогексан, дихлорметан, трихлорметан, тетрахлорметан, 1,2-дихлоретан, 1,1,1-трихлоретан, 1,1,2,2-тетрахлоретан або тетрахлоретен, прості ефіри, такі як діетиловий ефір, дипропіловий ефір, діізопропіловий ефір, дибутиловий ефір, mpem-бутилметиловий ефір, диметиловий ефір етиленгліколю, диметоксидіетиловий ефір, тетрагідрофуран або діоксан, аміди, такі як Ν,Νдиметилформамід, Ν,Ν-діетилформамід, Ν,Ν-диметилацетамід, N-метилпіролідон або гексаметилфосфорамід, нітрили, такі як ацетонітрил або пропіонітрил, і сульфоксиди, такі як диметилсульфоксид, а також нітросполуки, такі як нітрометан або нітробензол, або суміші подібних розчинників. Найбільш кращими є неполярні апротонні розчинники, яки не змішуються з водою, такі як галогеновані вуглеводні, наприклад галогеновані алкани і галогеновані ароматичні сполуки, такі як дихлорметан, хлороформ, тетрахлорметан, 1,2-дихлоретан, 1,1,1-трихлоретан, 1,2,3-трихлорпропан, 1,1,2,2тетрахлоретан, 1,2-дихлоретилен, 1-хлорпропан, або хлорбензол 1,2-дихлорбензол, або суміші подібних розчинників. Крім того, можуть використовуватися полярні апротонні розчинники, наприклад нітрометан або нітробензол, карбонітрили, наприклад ацетонітрил, пропіонітрил або бутиронітрил, карбоксаміди, наприклад формамід, N-метилформамід, Ν,Ν-диметилформамід, N-метилацетамід, Ν,Ν-диметилацетамід або 1-метилпіролідин-2-он, сульфоксиди, наприклад диметилсульфоксид, сульфолан, гексаметилфосфорамід, 1,3-диметилімідазолідин-2-он, похідні сечовини, наприклад тетраметилсечовина, або суміші подібних розчинників. Якщо реакцію на стадії а) проводять у розчиннику, який не змішується з водою, то для екстракції кислотою відповідно до варіанта а1) необхідно додавати додатковий розчинник, який не змішується з водою, і який є інертним до впливу кислоти. Придатними для цієї мети розчинниками є серед інших розчинники, яки не змішуються з водою, згадані вище як кращі, а також ароматичні розчинники, такі, наприклад, як бензол, толуол або ксилол. Після екстракції продукт переважно піддавати додатковому очищенню, наприклад піддавати попередньо очищену сполуку формули (III) перегонці або кристалізації. Було встановлено, що у фазі розчинника залишаються нециклізовані побічні продукти і сполуки, які не містять основних груп, які містять азот, і їх можна відокремлювати разом з розчинником. У цьому відношенні екстракцію можна проводити в періодичному режимі або ж у безупинному режимі в екстракційній колоні, шляхом пропускання через неї екстрагувального та екстрагованого матеріалів у протитечії. Зворотну екстракцію продукту формули (III) з водної фази здійснюють, наприклад, за допомогою інертного розчинника, який не змішується з водою. Таку зворотну екстракцію можна також проводити у періодичному або безупинному режимі. Потім розчинник відганяють при зниженому тиску, а продукт, який залишився в розплавленому стані, або безпосередньо використовують на наступних стадіях синтезу, або при необхідності спочатку піддають додатковому очищенню, наприклад перегонкою. При переробці відповідно до варіанта а2) до реакційної суміші, яка утворюється в процесі синтезу сполуки формули (III), переважно домішують воду при температурі 20-60°С. Крім цього при переробці реакційної суміші відповідно до цього варіанта розчинник у наступному доцільно відганяти при зниженому тиску, а продукт, який залишився в розплавленому стані, або безпосередньо використовувати на наступних стадіях синтезу, або попередньо піддавати додатковому очищенню, наприклад перегонкою з відбором продукту з вер ха колони. Стадія б) На цій стадії реагенти можуть у кожному випадку взаємодіяти між собою безпосередньо, тобто без додавання розчинника або розріджувача, наприклад у розплавленому стані. Однак у більшості випадків може виявитися доцільним додавання інертного розчинника або розріджувача або їхньої суміші. Прикладами подібних розчинників або розріджувачів є ароматичні, аліфатичні та аліциклічні вуглеводні і галогеновані вуглеводні, такі як бензол, толуол, ксилол, мезитилен, тетралін, хлорбензол, дихлорбензол, бромбензол, нітробензол, нітрометан, петролейний ефір, гексан, циклогексан, дихлорметан, трихлорметан, тетрахлорметан, дихлоретан, трихлоретен або тетрахлоретен, складні ефіри, такі як етилацетат, метилацетат, диметилкарбонат, діетилкарбонат, етоксіетилацетат, метоксіетилацетат, етилформіат, прості ефіри, такі як діетиловий ефір, дипропіловий ефір, діізопропіловий ефір, дибутиловий ефір, mpemбутилметиловий ефір, монометиловий ефір етиленгліколю, моноетиловий ефір етиленгліколю, диметиловий ефір етиленгліколю, диметоксидіетиловий ефір, тетрагідрофуран або діоксан, кетони, такі як ацетон, метилетилкетон або метилізобутилкетон, спирти, такі як метанол, етанол, пропанол, ізопропанол, бутанол, етиленгліколь або гліцерин, аміди, такі як Ν,Ν-диметилформамід, Ν,Ν-діетилформамід, Ν,Νдиметилацетамід, N-метилпіролідон або гексаметилфосфорамід, нітрили, такі як ацетонітрил або пропіонітрил, і сульфоксиди, такі як диметилсульфоксид, або суміші подібних розчинників. При проведенні відповідної реакції в присутності основи, ті основи, які використовують в надлишку, такі як триетиламін, піридин, N-метилморфолін або Ν,Ν-діетиланілін, одночасно можуть також служити розчинниками або розріджувачами. Найбільш кращі для кожного випадку розчинники зазначені в приведених нижче прикладах. Доцільним є також додавання каталізаторів, таких, наприклад, як між фазні каталізатори. Реакцію переважно проводять при температурі від приблизно 0 до приблизно +180°С, переважно від приблизно +10 до приблизно +80°С, а в багатьох випадках в інтервалі від кімнатної температури до температури перегонки розчинника. У найбільш кращому варіанті здійснення стадії б) реакцію за участю сполуки формули (IV) проводять при температурі від 0 до 120°С, переважно від 20 до 80°С, переважно від 30 до 70°С, у складному ефірі, переважно у диметилкарбонаті, і переважно в присутності основи, насамперед К2СО3. Реакцію переважно проводять при нормальному тиску. Тривалість реакції не має вирішального значення і переважно складає від 0,1 до 48год., найбільше переважно від 0,5 до 12год. Продукт виділяють звичайними методами, наприклад фільтрацією, кристалізацією, або перегонкою хроматографією або декількома такими методами в будь-якому прийнятному їх поєднанні. Запропонований у винаході спосіб звичайно дозволяє одержувати кінцевий продукт із досить високим виходом. При цьому часто кінцевий продукт вдається одержувати з ви ходом 80% від теоретичного значення. Оптимальні умови проведення реакції розглянуті в приведених нижче прикладах. Солі сполук (I)-(IV) можна одержувати відомими методами. Так, наприклад, кислотно-адитивні солі одержують обробкою прийнятною кислотою або прийнятним іонообмінним реагентом, а солі з основами одержують обробкою прийнятною основою або прийнятним іонообмінним реагентом. Солі сполук формул (I)-(IV) можна перетворювати у вільні сполуки формул (I)-(IV) загальноприйнятими методами, при цьому кислотно-адитивні солі можна перетворювати, наприклад, прийнятним лужним агентом або іонообмінним реагентом, а солі з основами можна перетворювати, наприклад, обробкою прийнятною кислотою або прийнятним іонообмінним реагентом. Солі сполук формул (I)-(IV) можна з використанням звичайних методів перетворювати в інші солі сполук формул (I)-(IV), при цьому, наприклад, кислотно-адитивні солі можна перетворювати в інші кислотноадитивні солі, наприклад обробкою солі неорганічної кислоти, такої як гідрохлорид, прийнятною металевою сіллю, такою як натрієва, барієва або срібна сіль, кислоти, наприклад ацетатом срібла, у придатному для цієї мети розчиннику, у якому неорганічна сіль, що утворюється, наприклад хлорид срібла, не розчинна і завдяки цьому випадає з реакційної суміші в осад. В залежності від особливостей проведення процесу та умов проведення реакції, сполуки формул (I)(IV), які мають здатність до утворення солей, можна одержувати у вільній формі або формі солей. Сполуки формул (I)-(IV) і в кожному випадку, коли це можливо, їх та утомери, у кожному випадку у вільній формі або у формі солі, можуть бути представлені у вигляді одного з їх можливих ізомерів або у виді їхньої суміші, наприклад в залежності від кількості асиметричних атомів вуглецю в молекулі і їхньої абсолютної та відносної конфігурації та/або в залежності від конфігурації неароматичних подвійних зв'язків у молекулі вони можуть існувати у ви гляді чистих ізомерів, таких як антиподи та/або діастереомери, або у вигляді сумішей ізомерів, таких як суміші енантіомерів, наприклад рацемати, сумішей діастереомерів або сумішей рацематів, при цьому даний винахід відноситься і до чистих ізомерів, і до всі х можливих сумішей ізомерів, і тому в приведеному вище і у наступному описі під сполуками формул (I)-(IV) маються на увазі також їхні ізомери та їхні суміші, навіть якщо в кожному окремому випадку і не зазначені конкретні подробиці стосовно стереохімічної будови. Суміші діастереомерів і суміші рацематів сполук формул (I)-(IV) або їхніх солей, які одержують запропонованим у винаході способом або іншими методами в залежності від вихідних матеріалів, яки використовують, та обраної технології, можна на основі відмінностей у фізико-хімічних властивостях компонентів таких сумішей розділяти відомими методами, наприклад фракціонованою кристалізацією, перегонкою та/або хроматографією, на чисті діастереомери або рацемати. Одержані таким шляхом суміші енантіомерів, такі як рацемати, можна відомими методами розділяти на оптичні антиподи, наприклад перекристалізацією з оптично активного розчинника, хроматографією на хіральних адсорбентах, наприклад рідинною хроматографією високого тиску (РХВТ) на ацетилцелюлозі, за допомогою придатних для цієї мети мікроорганізмів, розщепленням за допомогою особливих іммобілізованих ферментів, утворенням сполук включення, наприклад з використанням хіральних краунефірів, у такому випадку тільки один енантіомер утворює комплекс, або перетворенням у діастереомерні солі, наприклад взаємодією основного кінцевого продукту у вигляді рацемата з оптично активною кислотою, такою як карбонова кислота, наприклад камфорна, винна або яблучна кислота, або сульфонова кислота, наприклад камфорсульфонова кислота, і поділом отриманої суміші діастереомерів, наприклад на основі відмінностей у їхній розчинності шляхом фракціонованої кристалізації, на діастереомери, з яких цільовий енантіомер можна виділити впливом прийнятних, наприклад основних, агентів. Чисті діастереомери і енантіомери можна одержувати не тільки поділом відповідних сумішей ізомерів, але і відповідно до винаходу добре відомими методами діастереоселективного і енантіоселективного синтезу, наприклад за рахунок використання при проведенні запропонованого у винаході способу вихідних матеріалів з відповідною стереохімічною будовою. Сполуки формул (I)-(IV) та їхні солі можна також одержувати у вигляді гідратів та/або вони можуть включати молекули інших розчинників, наприклад розчинників, яки за певних умов могли використовува тися для кристалізації сполук, які утворюються у твердому вигляді. Даний винахід відноситься до всіх тих варіантів здійснення запропонованого в ньому способу, у яких сполука, яку одержують на будь-якій його стадії у вигляді вихідної сполуки або проміжного продукту, використовується як вихідний матеріал з наступним проведенням всіх або деяких зі стадій, які залишилися, або в яких вихідний матеріал використовується у вигляді похідного або солі та/або його рацематів або антиподів або насамперед утворюється в реакційних умовах. Сполуки формул (І), (III) та (IV), які одержують запропонованим у винаході способом або іншими методами, можна перетворювати в інші відповідні сполуки методами, яки відомі як такі. У запропонованому у винаході способі переважно використовувати ті вихідні матеріали і проміжні продукти, у кожному випадку у вільній формі або у формі солі, яки дозволяють одержувати сполуки формули (І) або їхні солі, які представлені на початку опису як найбільш кращі. Даний винахід відноситься також до способу одержання сполуки формули (III) зі сполуки формули (II) відповідно до розглянутої вище стадії а). Даний винахід відноситься насамперед до тих варіантів здійснення запропонованого в ньому способу, яки розглянуті в приведених нижче прикладах. Сполуки формул (II) та (IV) є відомими сполуками, які представляють собою, наприклад, проміжні продукти в процесах одержання пестицидів, або їх можна одержувати відомими методами. Приклади одержання Приклад Н1: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазину Н1а): 2-хлор-5-хлорметилтіазол 40г проміжної фракції, отриманої в результаті перегонки в попередньому циклі і яка складається з 31,4г 2-хлор-5-хлорметилтіазолу та 8,9г 2-хлор-3-тіоціанато-1-пропену, додають до 160г хлорбензолу, нагрівають до 110°С і перемішують при 110°С протягом 1 год. (при цьому 2-хлор-3-тіоціанато-1-пропен перетворюється на 2-хлор-3-ізотіоціанато-1-пропен). Потім реакційну суміш охолоджують до 45-50°С та додають 125,3г свіжого 2-хлор-3-ізотіоціанато-1-пропену і 100г хлорбензолу. Після цього протягом 5год. дозують 139г сульфурилхлориду і потім реакційну суміш перемішують ще протягом години при 45-50°С. Далі тиск встановлюють на 120мбар, а температуру доводять до 50-55°С і реакцію завершують перемішуванням протягом однієї години, після чого з реагуючої маси відганяють весь розчинник. Після цього з отриманої таким шляхом проміжної фракції відбирають порцію масою 40г, яку знову використовують у реакції в наступному циклі. Сирий продукт піддають фракційній перегонці при 115°С/5-10мбар, одержуючи 124,4г продукту з 94,5%-вим вмістом 2-хлор-5-хлорметилтіазолу, що відповідає виходу в 74,6% від теорії при перерахуванні на свіжодо даний 2-хлор-3-ізотіоціанато-1-пропен. Н1б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазин У колбу для сульфування поміщають 184г 100%-вого 3-метил-4-нітроімінопергідро-1,3,5-оксадіазину у 400г диметилкарбонату та додають 168г 100%-вого 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н1а). Отриману суміш нагрівають до 65°С. Потім при перемішуванні і при температурі від 60 до 70°С протягом 60 хвилин дозують суміш, яка складається з 350г диметилкарбонату, 4г пентагідрату гідроксиду тетраметиламонію та 242г порошкового карбонату калію. Далі реакційну суміш перемішують доти, доки ступінь перетворення 2-хлор-5-хлорметилтіазолу не перевищить 99% (за даними РХ-контролю). Потім реакційну суміш охолоджують і до неї додають 600г води. Використовуючи приблизно 260г 32%-вої соляної кислоти, значення рН встановлюють на 6,5, після чого реакційну суміш залишають стояти для поділу фаз і потім органічну фазу відокремлюють. Цю органічну фазу концентрують розпарюванням при 60°С під зниженим тиском до кінцевої маси, рівної 600г. Після цього суміш повільно охолоджують до 0-5 °С і витримують при цій температурі протягом години. Суспензію, яка утворилася, потім фільтрують і отриманий твердий продукт сушать. Вміст кінцевого продукту, який має темно-коричневий колір, складає 97,5-98,5%. Вихід продукту складає 70% від теорії. Приклад Н2: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1.3.5-оксадіазину Н2а): 2-хлор-5-хлорметилтіазол 40г проміжної фракції, отриманої в результаті перегонки у попередньому циклі і яка складається з 31,4г 2-хлор-5-хлорметилтіазолу та 8,9г 2-хлор-3-тіоціанато-1-пропену, додають до 160г хлорбензолу, нагрівають до 110°С і перемішують при 110°С протягом години. Потім реакційну суміш охолоджують до 45-50°С і додають 125,3г свіжого 2-хлор-3-ізотіоціанато-1-пропену і 100г хлорбензолу. Після цього протягом 5 годин при 45-50°С дозують 139г сульфурилхлориду і потім суміш перемішують ще протягом години при 45-50°С. Далі тиск встановлюють на 120мбар, а температуру доводять до 50-55°С і реакцію завершують перемішуванням у цих умовах протягом однієї години. Після цього при 60-65°С/20-30мбар з реагуючої маси відганяють половину об'єму розчинника. Потім при 50-55°С до реагуючої масі додають 7г води і суміш перемішують при цій температурі ще протягом години. Далі при 60-65 °С/20-30 мбар відганяють залишкову кількість розчинника, потім 40г проміжної фракції та на завершення при 115°С/5-10 мбар - сирий продукт. Таким шляхом одержують 121г продукту з 98%-вим вмістом 2-хлор-5-хлорметилтіазолу, що відповідає виходу 70,5% від теорії при перерахуванні на 2-хлор-3-ізотіоціанато-1-пропен, відповідно виходу 75% від теорії при перерахуванні на свіжододаний 2-хлор-3-ізотіоціанато-1-пропен. Н2б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазин Кінцевий продукт одержують аналогічно прикладу Η1б) з використанням 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н2а). Вміст кінцевого продукту, який має світло-блідо-бежевий колір, складає 98-99%. Вихід складає 74-75% від теорії. Приклад Н3: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазину Н3а): 2-хлор-5-хлорметилтіазол 87,7г 2-хлор-3-ізотіоціанато-1-пропену при 20°С додають до 100мл ацетонітрилу і до отриманої реакційної суміші додають 8,9г сульфурилхлориду (0,05 молів). Потім у реакційну суміш вводять 41,5г хлору до того моменту, при якому стає вже неможливим більш знайти надлишок вихідного матеріалу, на що потрібно приблизно 2год., після чого реакційний розчин перемішують протягом години при 40°С і потім охолоджують до кімнатної температури. Далі реакційну суміш упарюють у вакуумі, видаляючи з неї при пониженому тиску газоподібний хлористий водень, і відганяють ацетонітрил. Таким шляхом одержують 112г продукту з 91%-вим вмістом 2-хлор-5-хлорметилтіазолу, що відповідає виходу 84% від теорії при перерахуванні на 2-хлор-3-ізотіоціанато-1-пропен. Н3б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1.3-5-оксадіазин Кінцевий продукт одержують аналогічно прикладу Η16) з використанням 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н3а). Вміст кінцевого продукту, що має темно-коричневий колір, складає 92-94%. Вихід складає 50-55% від теорії. Приклад Н4: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазину Н4а): 2-хлор-5-хлорметилтіазол 87,7г 2-хлор-3-ізотіоціанато-1-пропену при 20°С додають до 100мл ацетонітрилу і до отриманої реакційної суміші додають 8,9г сульфурилхлориду (0,05 молів). Потім у реакційну суміш вводять 41,5г хлору до того моменту, при якому стає вже більш неможливим знайти надлишок вихідного матеріалу, на що потрібно приблизно 2 год., після чого реакційний розчин перемішують протягом години при 40°С, а потім відганяють більшу кількість ацетонітрилу та НСl до досягнення кінцевим зниженим тиском значення, рівного 20мбар. Далі до сирого розплаву, який залишився, додають 200 мл толуолу та толуольний розчин продукту екстрагують 4-ма порціями 37%-вої соляної кислоти загальною кількістю 250г. Водні екстракти, яки містять гідрохлорид 2-хлор-5-хлорметилтіазолу, очищають і після додавання 200мл толуолу потім частково нейтралізують додаванням 250г 30%-вого розчину гідроксиду натрію. З толуольної фази послідовно відганяють толуол, а потім 2-хлор-5-хлорметилтіазол до досягнення кінцевим зниженим тиском у головній частині значення, рівного 5-10мбар. Таким шляхом одержують 86г продукту з 98%-вим вмістом 2-хлор-5хлорметилтіазолу. Вихід складає 76% від теорії при перерахуванні на 2-хлор-3-ізотіоціанато-1-пропен. Н4б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазин Кінцевий продукт одержують аналогічно прикладу Η1б) з використанням 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н4а). Вміст кінцевого продукту, який має бежевий колір, складає 9899%. Вихід складає 76-77% від теорії. Приклад Н5: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазину Н5а): 2-хлор-5-хлорметилтіазол До розчину 133,6г 2-хлор-3-ізотіоціанато-1-пропену в 260г хлорбензолу протягом 5 годин при 45-50°С дозують 139г сульфурилхлориду. Реакційну суміш потім перемішують протягом години при 45-50°С. Після цього тиск встановлюють на 120мбар, а температуру доводять до 50-55°С, після чого реакційну суміш для видалення з неї газу перемішують у цих умовах протягом години. Далі реакційну суміш охолоджують до 2025°С і екстрагують 4-ма порціями 37%-вої соляної кислоти загальною кількістю 460г. При цьому після кожного циклу екстракції відокремлюють водну фазу. Після цього об'єднані водні фази розбавляють 580г води і продукт піддають зворотній екстракції 2-ма порціями хлорбензолу загальною кількістю 170г. Потім при 60-65 °С/20-30 мбар відганяють розчинник, а сирий продукт відганяють при 115°С/5-10мбар. При цьому одержують 117,1г продукту з 99%-вим вмістом 2-хлор-5-хлорметилтіазолу, що відповідає виходу 69% від теорії при перерахуванні на 2-хлор-3-ізотіоціанато-1-пропен. Н5б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазин Кінцевий продукт одержують аналогічно прикладу Η1б) з використанням 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н5а). Вміст кінцевого продукту, який має блідо-бежевий колір, складає 98-99%. Вихід складає 77-78% від теорії. Приклад Н6: Одержання 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазину Н6а): 2-хлор-5-хлорметилтіазол До розчину 133,6г 2-хлор-3-ізотіоціанато-1-пропену у 260г 1,2-ди хлоретану протягом 4 годин при 4550°С дозують 139г сульфурилхлориду. Реакційну суміш потім перемішують протягом 2год. при 45-50°С. Після цього реакційну суміш о холоджують до 20-25°С і екстрагують 4-ма порціями 37%-вої соляної ідаслоти загальною кількістю 460г. При цьому після кожного циклу екстракції відокремлюють водну фазу. Після цього об'єднані водні фази розбавляють 580г води і продукт піддають зворотній екстракції 2-ма порціями 1,2дихлоретану загальною кількістю 170г. Потім при 60-65°С/20-30мбар відганяють розчинник, а сирий продукт відганяють при 115°С/5-10мбар. При цьому одержують 119г продукту з 99%-вим вмістом 2-хлор-5хлорметилтіазолу, що відповідає виходу 70% від теорії при перерахуванні на 2-хлор-3-ізотіоціанато-1пропен. Н6б): 3-(2-хлортіазол-5-ілметил)-5-метил-4-нітроімінопергідро-1,3,5-оксадіазин Кінцевий продукт одержують аналогічно прикладу Η1б) з використанням 2-хлор-5-хлорметилтіазолу, отриманого відповідно до приклада Н6а). Вміст кінцевого продукту, який має блідо-бежевий колір, складає 98-99%. Вихід складає 77-78% від теорії.
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for the preparation of thiazol derivatives having pesticide activity
Автори англійськоюSeifert Gottfried
Назва патенту російськоюСпособ получения производных тиазола, которые имеют пестицидную активность
Автори російськоюСайферт Готтфрид
МПК / Мітки
МПК: A01N 43/78, C07D 277/32, A01P 17/00, A01N 43/88, C07D 417/06
Мітки: одержання, тіазолу, спосіб, похідних, пестицидну, активність, мають
Код посилання
<a href="https://ua.patents.su/7-73810-sposib-oderzhannya-pokhidnikh-tiazolu-yaki-mayut-pesticidnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних тіазолу, які мають пестицидну активність</a>
Попередній патент: Машина для пресового зварювання труб з нагріванням дугою, керованою магнітним полем
Наступний патент: Підбирач-навантажувач стеблових матеріалів
Випадковий патент: Спосіб сівби насіння селекційних розсадників











