Фармацевтична композиція
Номер патенту: 113499
Опубліковано: 10.02.2017
Автори: Спайві Марк, Карлсон Джонатан Ерік, Сатох Такасі
Формула / Реферат
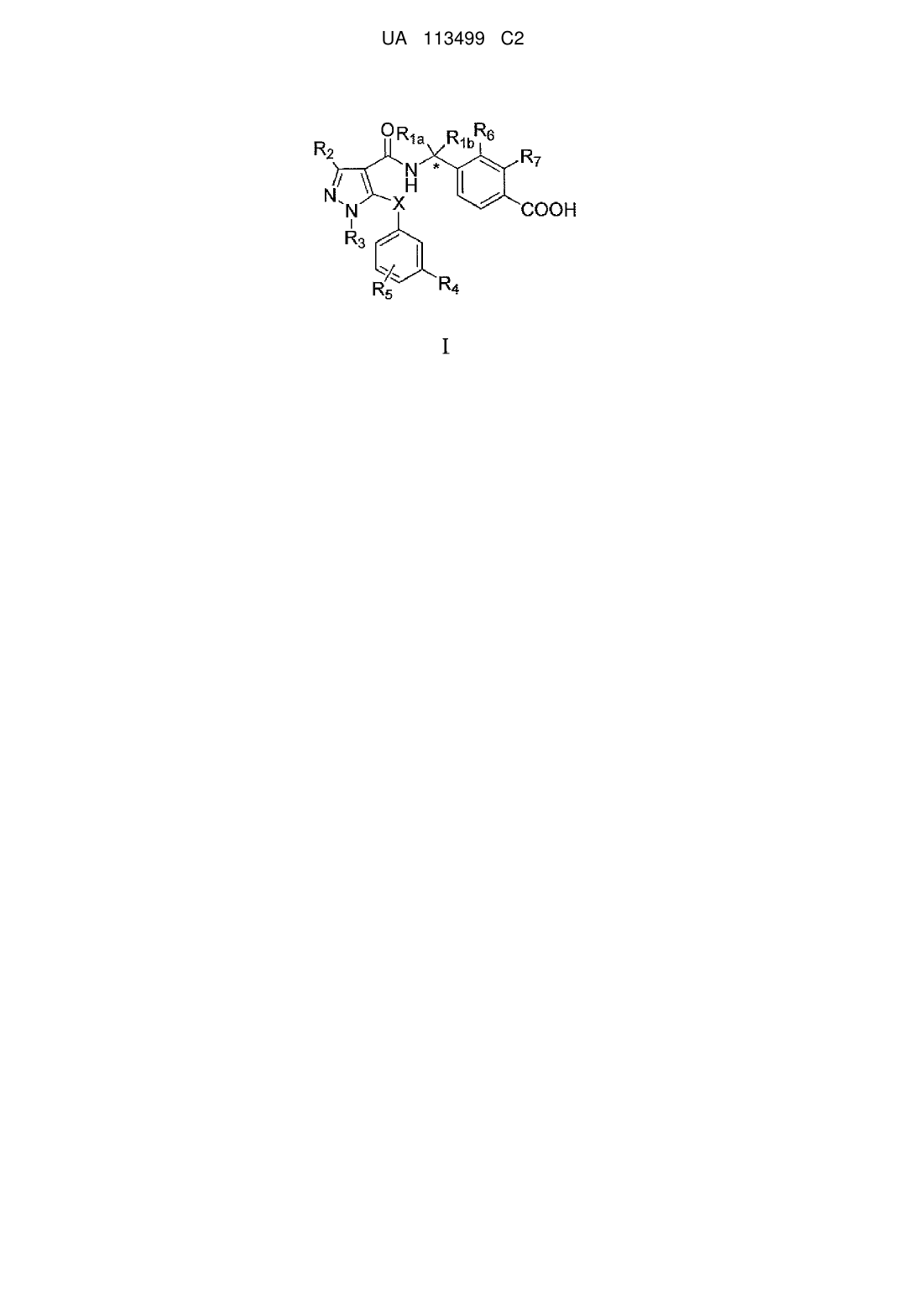
1. Сполука формули І:
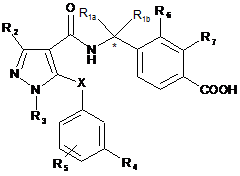 , I
, I
де:
один з R1a і R1b означає водень, а інший означає метил; або R1a і R1b разом утворюють циклопропільне кільце;
R2 означає метил або фторметил;
R3 означає метил;
R4 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R5 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R6 означає водень, галоген, метил або метокси;
R7 означає водень, галоген, метил або метокси; і
X означає кисень;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, де
один з R1a і R1b означає водень, а інший означає метил; R2 означає метил, дифторметил або трифторметил;
R3 означає метил;
R4 означає хлор, фтор, трифторметил, дифторметил, метил, метокси, дифторметокси або трифторметокси;
R5 означає водень, хлор, фтор, метил або метокси;
R6 і R7 означають водень;
або її фармацевтично прийнятна сіль.
3. Сполука за п. 2, де R5 означає водень; або її фармацевтично прийнятна сіль.
4. Сполука за п. 3, де R4 вибирають з хлору, трифторметилу, дифторметилу, дифторметокси і трифторметокси; або її фармацевтично прийнятна сіль.
5. Сполука за будь-яким одним з пп. 1-4, де
один з R1a і R1b означає водень, а інший означає метил; і сполука формули І складається з суміші стереоізомерів;
або її фармацевтично прийнятна сіль.
6. Сполука за будь-яким одним з пп. 1-4, де
один з R1a і R1b означає водень, а інший означає метил; і сполука формули І складається з по суті чистого стереоізомера;
або її фармацевтично прийнятна сіль.
7. Сполука за п. 6, де
один з R1a і R1b означає водень, а інший означає метил, і атом вуглецю сполуки формули І, відмічений знаком *, має по суті S-конфігурацію; або її фармацевтично прийнятна сіль.
8. Сполука за п. 6, де
один з R1a і R1b означає водень, а інший означає метил, і атом вуглецю сполуки формули І, відмічений знаком *, має по суті R-конфігурацію; або її фармацевтично прийнятна сіль.
9. Сполука за п. 1, де
R1a і R1b разом утворюють циклопропільне кільце;
R2 означає метил, трифторметил або дифторметил;
R3 означає метил;
R4 означає трифторметил, дифторметил, хлор або фтор;
R6 і R7 означають водень;
або її фармацевтично прийнятна сіль.
10. Сполука за п. 1, вибирана з групи, яка складається з:
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 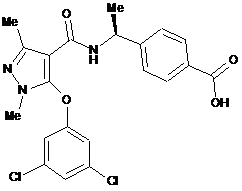 ,
,
 ,
,  ,
,  ,
,
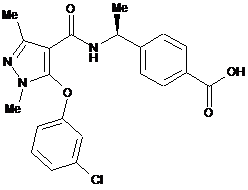 ,
, 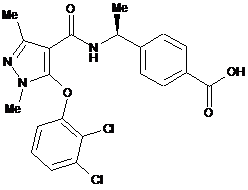 ,
, 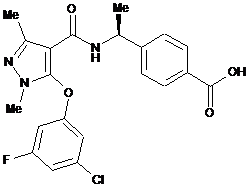 ,
,
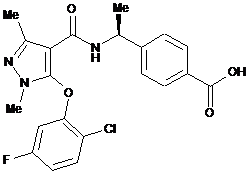 ,
, 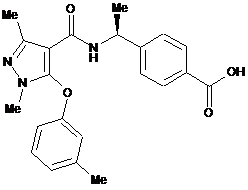 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
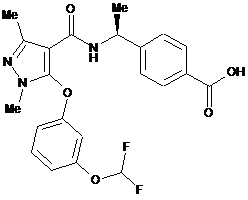 ,
, 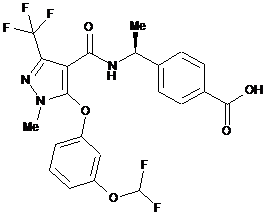 ,
, 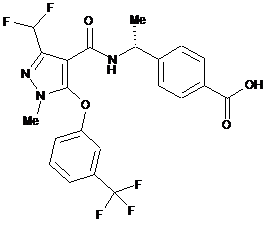 ,
,
 ,
,  ,
,  ,
,
 ,
, 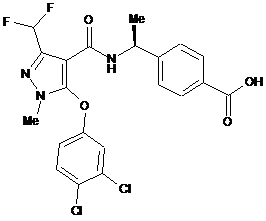 ,
, 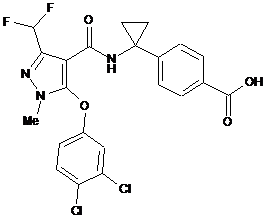 ,
,
 ,
,  ,
, 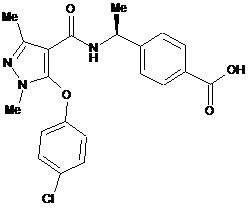 ,
,
 ,
,  ,
, 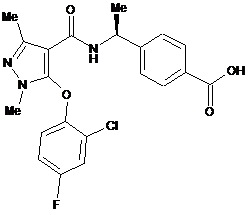 ,
,
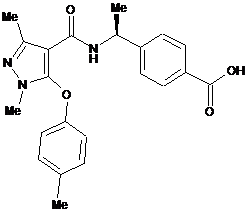 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
або її фармацевтично прийнятні солі.
11. Сполука за п. 10, яка являє собою:
 ;
;
або її фармацевтично прийнятна сіль.
12. Сполука за п. 10, яка являє собою:
 ;
;
або її фармацевтично прийнятна сіль.
13. Фармацевтична композиція, яка містить сполуку формули І:
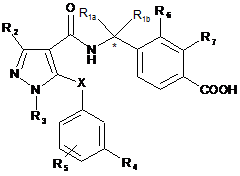 , I
, I
де:
один з R1a і R1b означає водень, а інший означає метил; або R1a і R1b разом утворюють циклопропільне кільце;
R2 означає метил або фторметил;
R3 означає метил;
R4 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R5 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R6 означає водень, галоген, метил або метокси;
R7 означає водень, галоген, метил або метокси; і
X означає кисень;
або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій.
14. Фармацевтична композиція, яка містить сполуку за п. 10 або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій.
15. Фармацевтична композиція, яка містить сполуку, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій.
16. Фармацевтична композиція, яка містить сполуку, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій.
17. Спосіб лікування ревматоїдного артриту у ссавця, який включає введення ссавцеві фармацевтичної композиції, яка містить сполуку формули І:
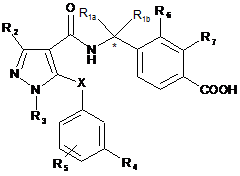 , I
, I
де:
один з R1a і R1b означає водень, а інший означає метил; або R1a і R1b разом утворюють циклопропільне кільце;
R2 означає метил або фторметил;
R3 означає метил;
R4 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R5 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R6 означає водень, галоген, метил або метокси;
R7 означає водень, галоген, метил або метокси; і
X означає кисень;
або її фармацевтично прийнятні солі.
18. Спосіб лікування ревматоїдного артриту у ссавця, який включає введення ссавцеві фармацевтичної композиції, яка містить сполуку за п. 10 або її фармацевтично прийнятну сіль.
19. Спосіб лікування ревматоїдного артриту у ссавця, який включає введення ссавцеві фармацевтичної композиції, яка містить сполуку за п. 10, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль.
20. Спосіб лікування ревматоїдного артриту у ссавця, який включає введення ссавцеві фармацевтичної композиції, яка містить сполуку за п. 10, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль.
21. Застосування сполуки за п. 1 для одержання лікарського засобу для лікування ревматоїдного артриту.
22. Спосіб лікування ракового захворювання у ссавця, який включає введення ссавцю фармацевтичної композиції, що містить сполуку формули І:
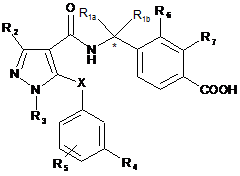 ,
,
де:
один з R1a і R1b означає водень, а другий означає метил; або R1a і R1b разом утворюють циклопропільне кільце;
R2 означає метил або фторметил;
R3 означає метил;
R4 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R5 означає водень, галоген, фторметил, метил, метокси або фторметокси;
R6 означає водень, галоген, метил або метокси;
R7 означає водень, галоген, метил або метокси; і
X означає кисень;
або її фармацевтично прийнятні солі.
23. Спосіб лікування ракового захворювання у ссавця, що включає введення ссавцю фармацевтичної композиції, що містить сполуку за п. 10 або її фармацевтично прийнятну сіль.
24. Спосіб лікування ракового захворювання у ссавця, що включає введення ссавцю фармацевтичної композиції, що містить сполуку формули І, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль.
25. Спосіб лікування ракового захворювання у ссавця, що включає стадію введення ссавцю фармацевтичної композиції, що містить сполуку формули І, яка являє собою:
 ,
,
або її фармацевтично прийнятну сіль.
26. Застосування сполуки відповідно до варіанта здійснення 1 для отримання лікарського засобу для лікування ракового захворювання.
27. Спосіб за будь-яким з пп. 22-26, де ракове захворювання вибирають з групи, яка складається з раку шкіри, раку молочної залози, колоректального раку, раку передміхурової залози, раку нирки, раку яєчників, цервікального раку, ендометріального раку, гліобластоми, раку легені, раку голови і шиї, медулобластоми і раку сечових шляхів.
28. Спосіб за п. 27, де раковим захворюванням є рак шкіри.
29. Спосіб за п. 27, де раковим захворюванням є рак молочної залози.
30. Спосіб за п. 27, де раковим захворюванням є колоректальний рак.
31. Спосіб за п. 27, де раковим захворюванням є рак передміхурової залози.
32. Спосіб за п. 27, де раковим захворюванням є рак нирки.
33. Спосіб за п. 27, де раковим захворюванням є рак яєчників.
34. Спосіб за п. 27, де раковим захворюванням є цервікальний рак.
35. Спосіб за п. 27, де раковим захворюванням є ендометріальний рак.
36. Спосіб за п. 27, де раковим захворюванням є гліобластома.
37. Спосіб за п. 27, де раковим захворюванням є рак легені.
38. Спосіб за п. 27, де раковим захворюванням є рак голови і шиї.
39. Спосіб за п. 27, де раковим захворюванням є медулобластома.
40. Спосіб за п. 27, де раковим захворюванням є рак сечових шляхів.
Текст
Реферат: Даний винахід стосується сполук формули (І) разом з фармацевтичними композиціями, які містять ці сполуки, і способів їх застосування у випадку суб'єктів, які потребують лікування. OR 1a R2 N H N R1b R 6 R7 * X N COOH R3 R5 R4 I UA 113499 C2 (12) UA 113499 C2 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 60 Передумови створення винаходу Стосовно антигену, який зустрічається, інтактні клітини CD4+ Т-хелпер-попередника (Thp) піддавали диференціюванню в дві окремі субпопуляції, Т-хелпер типу 1 (Th1) і Т-хелпер типу 2 (Th2). Недавно також була ідентифікована і охарактеризована нова субпопуляція Т-клітин, Th17. Ці диференційовані Th-клітини визначали як за їх різними функціональними здатностями, так і по особливих профілях цитокінів. Конкретно, Th1-клітини продукують інтерферон-гамма, інтерлейкін (IL)-2 і фактор некрозу пухлини (TNF)-бета, які активують макрофаги і є відповідальними за опосередковані клітинами імунні і залежні від фагоцитів захисні відповіді. У протилежність цьому, відомо, що Th2-клітини продукують IL-4, IL-5, IL-6, IL-9, IL-10 і IL-13, які є відповідальними за інтенсивне продукування антитіл, активацію еозинофілів і інгібування деяких функцій макрофагів, таким чином, забезпечуючи незалежні від фагоцитів захисні відповіді. Th17-клітини переважно продукують IL-17A, IL-17F, IL-21, IL-22 і TNF і потребують імунного захисту проти позаклітинних патогенних мікроорганізмів і є критичними медіаторами аутоімунітету. Таким чином, Th1-, Th2- і Th17-клітини асоційовані з різними імунопатологічними відповідями. У доповнення, розвиток кожного типу Th-клітин опосередковується різним метаболічним шляхом цитокінів. Конкретно, показано, що IL-4 промотує Th-2-диференціювання і одночасно блокує Th1-розвиток. Навпаки, IL-12, IL-18 і IFN-гамма є критичними для розвитку Th1-клітин цитокінами. У випадку миші, TGF-і IL-6 є критичними для індукції диференціювання Th17клітин, тоді як, у випадку людини, IL-1, IL-6 і IL-23 є важливими драйверами розвитку Th17клітин. Таким чином, ефективний імунологічний гомеостаз залежить від безперервного балансу між активацією Т-клітини-хелпера і супресією регуляторної Т-клітини (Treg). Th1-клітини беруть активну участь у випадку патогенезу множини специфічних для органів аутоімунних порушень, хвороби Крона, яка індукується Helicobacter pylori пептичної виразки, гострого відторгнення ниркового алотрансплантату і нез'ясовних періодичних викиднів. У протилежність цьому, алерген-специфічні Th2-відповіді є відповідальними за атопічні порушення у генетично чутливих індивідуумів. Крім того, Th2 реагує на ще невідомі антигенні, переважаючі у випадку синдрому Омена, ідіопатичного фіброзу легенів і прогресуючого системного склерозу. Th17-клітини викликають імунопатологію в різних моделях аутоімунітету, таких як ревматоїдний артрит, розсіяний склероз, хвороба Крона і псоріаз. Нокаутовані по IL-17 (сигнатурний Th17-цитокін) миші виявляють помітну резистентність до розвитку запального артриту. Руйнування суглоба у випадку CIA-моделі може бути зменшене за рахунок введення нейтралізуючого анти-IL-17-антитіла. У цьому випадку залишається у високій мірі незадоволена в медицині необхідність в розробці нових методів терапії, які придатні для лікування різних станів, асоційованих з дисбалансованою Th1/Th2- і Th17-клітинним диференціюванням. У випадку множини з цих станів варіанти доступного в цей час лікування є неадекватними. Таким чином, парадигма Th1/Th2 і Th17 надає логічне обґрунтування для розробки стратегій відносно терапії алергічних і аутоімунних порушень. Показано, що простагландини модулюють різні фази імунної відповіді. Ліпідний медіаторний простагландин Е2 (PGE2) являє собою ейкозаноїд, який добре відомий відносно придушення активації CD4+ Т-клітин за рахунок збільшення внутрішньоклітинного цАМФ і інактивації Ick. Також показано, що PGE2 грає роль в регуляції Th1-відповідей шляхом придушення продукування інтерферону-гамма (IFN-gamma) і проліферації Т-клітин. Однак PGE2-стимуляція за рахунок ЕР4-субтипу PGE2-рецептору також може проводити протилежний ефект, а саме, промотування Th1-диференціювання ("Prostaglandin Е receptor subtypes EP2 and EP4 promote differentiation and expansion of Th1 and Th17 lymphocytes through different signaling modules" [Субтипи EP2 і EP4 рецептору простагландину Е промотують диференціювання і експансію Th1і Th17-лімфоцитів через різні модулі передачі сигналу], Nature Medicine, 2009, 15, 633-640) і продуковані IL-17 в активованих клітинах CD4+. Простагландин Е2 синергічно з інтерлейкіном23 сприяє експансії людського Th17, Blood, 2008, 112, 3696-3703; простагландин Е2 регулює диференціювання Th17-клітин і функцію передачі сигналу через циклічний АМФ і ЕР2/ЕР4рецептор, J. Exp. Med., 2009, 206, 535-548; простагландин Е2 посилює Th17-відповідь через модуляцію продукування IL-17 і IFN-γ за рахунок пам'яті CD4+ Т-клітин, Eur. J. Immunol. 2009, 39, 1301-1312. Сумісно з цим, антагонізм ЕР4 по відношенню або до нового селективного ЕР4антагоніста, або до PGE2-нейтралізуючого антитіла придушує диференціювання Th1, експансію Th17, а також секрецію IL-23 активованими дендритними клітинами. Індукування диференціювання Th1 за рахунок PGE2 опосередковується передачею сигналу PI3K, тоді як для стимуляції продукування IL-17 потрібна передача сигналу цАМФ. Крім того, введення ЕР4 1 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 антагоніста DBA/1- або C57BL/6-мишам придушує природжені і адаптивні імунні відповіді і придушує хворобу у випадку моделей індукованого колагеном артриту (CIA) і експериментального аутоімунного енцефаломієліту (ЕАЕ), вказуючи на те, що передача сигналу PGE2/EР4 критично залучена до цих аутоімунних патологій. Дані результати наводять на думку, що придушення передачі сигналу PGE2/EР4 може мати терапевтичне значення відносно модифікації запальних аутоімунних захворювань, таких як ревматоїдний артрит і розсіяний склероз. Короткий виклад суті винаходу Як описано в даному контексті, даний винахід стосується сполук формули I: де: один з R1a і R1b означає водень, а інший означає метил; або R1a і R1b разом утворюють циклопропільне кільце; R2 означає метил або фторметил (наприклад, монофторметил, дифторметил, трифторметил); R3 означає метил; R4 означає водень, галоген, фторметил, метокси або фторметокси (наприклад, монофторметокси, дифторметокси, трифторметокси); R5 означає водень, галоген, фторметил, метокси або фторметокси; R6 означає водень, галоген, метил або метокси; R7 означає водень, галоген, метил або метокси; і Х означає кисень; або їх фармацевтично прийнятних солей. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і атом вуглецю, відмічений знаком *, являє собою стереогенний центр. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і атом вуглецю, відмічений знаком *, має S-конфігурацію. У деяких варіантах здійснення один з R 1a і R1b означає водень, а інший означає метил, і атом вуглецю, відмічений знаком *, має R-конфігурацію. У деяких варіантах здійснення даний винахід стосується фармацевтичної композиції, яка містить сполуку формули I, або її підмножину або зразок. У деяких варіантах здійснення даний винахід стосується способу лікування ревматоїдного артриту у суб'єкта, який включає стадію введення суб'єкту композиції, яка містить сполуку формули I, або її підмножину або зразок. У деяких варіантах здійснення даний винахід стосується способу лікування розсіяного склерозу у суб'єкта, який включає стадію введення суб'єкту композиції, яка містить сполуку формули I, або її підмножину або зразок. Додатковий аспект даного винаходу являє собою застосування сполуки формули I, або її підмножини або зразка, для отримання лікарського засобу для лікування ревматоїдного артриту. Інший аспект даного винаходу являє собою застосування сполуки формули I, або її підмножини або зразка, для отримання лікарського засобу для лікування розсіяного склерозу. Короткий опис креслень Фіг. 1: Придушення розвитку артриту у випадку моделі CIA за допомогою сполуки згідно з даним винаходом. Фіг. 2: Придушення розвитку артриту у випадку моделі глюкозо-6-фосфат-ізомерази (G6PI) за допомогою сполуки згідно з даним винаходом. Докладний опис деяких варіантів здійснення даного винаходу А. Визначення Сполуки згідно з даним винаходом включають сполуки, описані в загальних рисах вище, і додатково проілюстровані за допомогою варіантів здійснення, підваріантів здійснення і типів, розкритих в даному контексті. Як використовується в даному контексті, застосовують наступні визначення, якщо не вказано інше. 2 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 60 Як описується в даному контексті, сполуки згідно з даним винаходом можуть бути необов'язково заміщені одним або більше замісниками, такими як проілюстровані в загальних рисах вище або як показані за допомогою окремих класів, підкласів і типів згідно з даним винаходом. Як правило, термін "заміщений" стосується заміни водневих радикалів в даній структурі на радикал конкретного замісника. Якщо не вказане інше, група, яка заміщує може мати замісник в кожному положенні групи, яка заміщується і де більше ніж одне положення в будь-якій даній структурі може бути заміщене більш ніж одним, замісником, вибираним з конкретної групи, причому замісник може бути або однаковим, або різним в кожному положенні. Комбінації замісників, представлені згідно з даним винаходом, переважно є такими, які в результаті приводять до утворення стабільних або хімічно здійсненних сполук. Як використовується в даному контексті, термін "модулятор Th1-диференціювання або Th17-експансії", або "сполука-модулятор Th1-диференціювання або Th17-експансії", або "сполука-модулятор", як використовується в даному контексті, стосується сполуки, яка придушує, зменшує або інгібує диференціювання інтактних CD4+ Т-клітин в Th1-клітини. У деяких варіантах здійснення термін "модулятор Th1-диференціювання або Th17-експансії", або "сполука-модулятор Th1-диференціювання або Th17-експансії", як використовується в даному контексті, стосується сполуки, яка придушує, зменшує або інгібує кількість продукуючих IL-17 CD4+ Т-клітин або продуковані IL-17 в активованих CD4+ Т-клітинах. Термін "ізомери" стосується сполук, які мають однакове число і однаковий тип атомів і, звідси, однакову молекулярну масу, але є відмінними по розташуванню або конфігурації атомів. Термін "стереоізомери" стосується ізомерів, які розрізняються тільки по розташуванню атомів в просторі. Термін "діастереоізомери" стосується стереоізомерів, які не є дзеркальними відображеннями один одного. Термін "енантіомери" стосується стереоізомерів, які є несуперпозиційними дзеркальними відображеннями один одного. Енантіомери включають "енантіомерно чисті" ізомери, які включають по суті один енантіомер, наприклад, в кількості більше ніж або рівній 90 %, 92 %, 95 %, 98 % або 99 %, або рівній 100 % одного енантіомеру. Термін "енантіомерно чистий", як використовується в даному контексті, означає сполуку або склад сполуки, яка(який) включає по суті один енантіомер, наприклад, в кількості більше ніж або рівній 90 %, 92 %, 95 %, 98 % або 99 %, або рівній 100 % одного енантіомеру. Термін "стереомерно чистий", як використовується в даному контексті, означає сполуку або склад сполуки, яка(який) включає один стереоізомер сполуки і по суті не містить інших стереоізомерів цієї сполуки. Наприклад, стереомерно чистий склад сполуки, яка має один хіральний центр, по суті не повинен містити протилежного енантіомеру даної сполуки. Стереомерно чистий склад сполуки, яка має два хіральних центри, по суті не повинен містити діастереомерів і по суті не повинен містити енантіомеру сполуки. Типова стереомерно чиста сполука включає більше ніж приблизно 80 % мас. одного стереоізомеру сполуки і менше ніж приблизно 20 % мас. інших стереоізомерів сполуки, більш переважно, більше ніж приблизно 90 % мас. одного стереоізомеру сполуки і менше ніж приблизно 10 % мас. інших стереоізомерів сполуки, ще більш переважно, більше ніж приблизно 95 % мас. одного стереоізомеру сполуки і менше ніж приблизно 5 % мас. інших стереоізомерів сполуки, і, найбільш переважно, більше ніж приблизно 97 % мас. одного стереоізомеру сполуки і менше ніж приблизно 3 % мас. інших стереоізомерів сполуки. Див., наприклад, патент США 7189715. "R" і "S" як терміни, які описують ізомери, являють собою дескриптори стереохімічної конфігурації у асиметрично заміщеного атома вуглецю. Позначення асиметрично заміщеного атома вуглецю у вигляді "R" і "S" виконане відповідно до застосування пріоритетних правил Кана-Інгольда-Прелога, які добре відомі кваліфікованому фахівцю в даній галузі і описані в Правилах Міжнародного союзу теоретичної і прикладної хімії (ІЮПАК) по номенклатурі органічної хімії, розділ Е, стереохімія. Термін "енантіомерний надлишок" (ее) енантіомеру являє собою [(мольна частинка основного енантіомеру) мінус (мольна частинка другорядного енантіомеру)]×100. Термін "стабільний", як використовується в даному контексті, стосується сполук, які по суті не змінюються, коли піддаються умовам, які беруться до уваги при їх отриманні, детектуванні і, переважно, їх рекуперації, очищення і використання для однієї або більше цілей, розкритих в даному контексті. У деяких варіантах здійснення стабільна сполука або хімічно здійснена сполука являє собою сполуку, яка по суті не змінюється, коли її витримують при температурі, рівній 40 °C або нижче, у відсутність вологи або інших хімічно реакційних умов щонайменше протягом тижня. 3 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Термін "Ar" або "арил" стосується ароматичного карбоциклічного залишку, який має одне або більше замкнених кілець. Приклади включають, без обмеження, феніл, нафтил, антраценіл, фенантраценіл, біфеніл і піреніл. Термін "гетероарил" стосується циклічного залишку, який має одне або більше замкнених кілець, з одним або більше гетероатомами (наприклад, кисень, азот або сірка) щонайменше в одному з кілець, де щонайменше одне з кілець є ароматичним і де кільце або кільця незалежно можуть бути конденсованими і/або мати місточковий зв'язок. Приклади включають, без обмеження, хінолініл, ізохінолініл, індоліл, фурил, тієніл, піразоліл, хіноксалініл, піроліл, індазоліл, тієно[2,3-c]піразоліл, бензофурил, піразоло[1,5-a]піридил, тіофенілпіразоліл, бензотієніл, бензотіазоліл, тіазоліл, 2-фенілтіазоліл і ізоксазоліл. Термін "алкіл" або "алкільна група", як використовується в даному контексті, означає лінійний (тобто нерозгалужений), розгалужений або циклічний вуглеводневий ланцюг, який повністю насичений. У деяких варіантах здійснення алкільні групи містять 1-6 атомів вуглецю. У деяких варіантах здійснення алкільні групи містять 1-4 атоми вуглецю. У деяких варіантах здійснення алкільні групи містять 1-3 атоми вуглецю. У ще інших варіантах здійснення алкільні групи містять 2-3 атоми вуглецю і, крім того, в ще інших варіантах здійснення алкільні групи містять 1-2 атоми вуглецю. У деяких варіантах здійснення термін "алкіл" або "алкільна група" стосується циклоалкільної групи, також відомої як карбоцикл. Не обмежуючі приклади типових алкільних груп включають метил, етил, пропіл, ізопропіл, бутил, циклопропіл і циклогексил. Термін "алкеніл" або "алкенільна група", як використовується в даному контексті, стосується лінійного (тобто нерозгалуженого), розгалуженого або циклічного вуглеводневого ланцюга, який має один або більше подвійних зв'язків. У деяких варіантах здійснення алкенільні групи містять 2-6 атомів вуглецю. У деяких варіантах здійснення алкенільні групи містять 2-4 атоми вуглецю. У ще інших варіантах здійснення алкенільні групи містять 3-4 атоми вуглецю і, крім того, в ще інших варіантах здійснення алкенільні групи містять 2-3 атоми вуглецю. Відповідно до іншого аспекту термін "алкеніл" стосується лінійного вуглеводневого ланцюга, який має два подвійні зв'язки, який також згадується як "дієн". У інших варіантах здійснення термін "алкеніл" або "алкенільна група" стосується циклоалкенільної групи. Не обмежуючі приклади типових алкенільних груп включають -СН=СН2, -СН2СН=СН2 (який також називається аліл), -СН=СНСН3, -СН2СН2СН=СН2, -СН2СН=СНСН3, -СН=СН2СН2СН3, -СН=СН2СН=СН2 і циклобутеніл. Термін "алкокси" або "алкілтіо", як використовується в даному контексті, стосується алкільної групи, описаної вище, приєднаної до основного вуглецевого ланцюга за допомогою атома кисню ("алкокси") або атома сірки ("алкілтіо"). Терміни "метилен", "етилен" і "пропілен", як використовується в даному контексті, стосується двовалентних залишків -СН2-, -СН2СН2- і -СН2СН2СН2-, відповідно. Терміни "етенілен", "пропенілен" і "бутенілен", як використовується в даному контексті, стосується двовалентних залишків -СН=СН-, -СН=СНСН2-, -СН2СН=СН-, -СН=СНСН2СН2-, СН2СН=СН2СН2- і -СН2СН2СН=СН-, де кожна етеніленова, пропеніленова і бутеніленова група може знаходитися в цис- або транс-конфігурації. У деяких варіантах здійснення етеніленова, пропеніленова або бутеніленова група може знаходитися в транс-конфігурації. Термін "алкіліден" стосується двовалентної вуглеводневої групи, утвореної моно- або діалкільним заміщенням метилену. У деяких варіантах здійснення алкілуденова група має 1-6 атомів вуглецю. У деяких варіантах здійснення алкіліденова група має 2-6, 1-5, 2-4 або 1-3 атомів вуглецю. Такі групи включають пропіліден (СН 3СН2СН=), етиліден (СН3СН=) і ізопропіліден (СН3(СН3)СН=) і т.п. Термін "алкеніліден" стосується двовалентної вуглеводневої групи, яка має один або більше подвійних зв'язків, утвореної моно- або діалкенільним заміщенням метилену. У деяких варіантах здійснення алкеніліденова група має 2-6 атомів вуглецю. В інших варіантах здійснення алкеніліденова група має 2-6, 2-5, 2-4 або 2-3 атомів вуглецю. Відповідно до одного аспекту алкеніліден має два подвійні зв'язки. Типові алкеніліденові групи включають СН 3СН=С=, СН2=СНСН=, СН2=СНСН2СН= і СН2=СНСН2СН=СНСН=. Термін "складний С1-6-алкіловий ефір або С1-6-алкіламід" стосується складного С1-6алкілового ефіру або С1-6-алкіламіду, де кожна С1-6-алкільна група являє собою групу, визначену вище. Такі групи складних С 1-6-алкілових ефірів являють собою групи формули (С 1-6алкіл)ОС(=О)- або (С1-6-алкіл)С(=О)О-. Такі С1-6-алкіламідні групи являють собою групи формули (С1-6-алкіл)NHС(=О)- або (С1-6-алкіл)С(=О)NH-. Термін "складний С2-6-алкеніловий ефір або С2-6-алкіламід" стосується складного С 2-6алкенілового ефіру або С2-6-алкеніламіду, де кожна С2-6-алкенільна група являє собою групу, визначену вище. Такі складні С2-6-алкенілові ефірні групи являють собою групи формули (С 2-6 4 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкеніл)ОС(=О)- або (С2-6-алкеніл)С(=О)О-. Такі С2-6-алкеніламідні групи являють собою групи формули (С2-6-алкеніл)NHС(=О)- або (С2-6-алкеніл)С(=О)NH-. Термін "фторметил", як використовується в даному контексті, стосується метильної групи, заміщеної одним або більше атомами фтору (наприклад, монофторметил, дифторметил, трифторметил). Термін "фторметокси", як використовується в даному контексті, стосується фторметильної групи, описаної вище, приєднаної до основного вуглецевого ланцюга за допомогою атома кисню. Терміни "лікування", "лікувати" і "піддавати лікуванню" стосується анулювання, полегшення, сповільнення початку захворювання або порушення, інгібування прогресуванню або попередженню захворювання або порушення, як описано в даному контексті. У деяких варіантах здійснення лікування можна провести після виявлення одного або більше симптомів. В інших варіантах здійснення лікування можна провести і у відсутність симптомів. Наприклад, лікування можна провести у випадку чутливих індивідуумів до початку виявлення симптомів (наприклад, в світлі історії симптомів і/або в світлі генетичних або інших факторів чутливості). Лікування можна також продовжувати після зникнення симптомів, наприклад, для попередження або затримки їх рецидиву. Термін "пацієнт" або "суб'єкт", як використовується в даному контексті, означає тварину, переважно, ссавця (наприклад, собака, кішка, кінь, корова, вівця, коза, мавпа і т.д.) і, особливо, людину (включаючи як чоловіків, так і жінок, і включаючи новонароджених, дітей, підлітків, юнаків, дорослих і старих людей). Термін "фармацевтично прийнятний носій", як використовується в даному контексті, стосується нетоксичного носія, допоміжного агента або ексципієнту, який не знищує фармакологічну активність сполуки, з якою його комбінують для отримання готової лікарської форми. Фармацевтично прийнятні носії, допоміжні агенти або ексципієнти, які можна використати в композиціях згідно з даним винаходом, включають, але не обмежуються ними, іонообмінні смоли, оксид алюмінію, стеарат алюмінію, лецитин, сироваткові білки, такі як людський сироватковий альбумін, буфери, такі як фосфати, гліцин, сорбінову кислоту, сорбат калію, часткові гліцеридні суміші насичених рослинних жирних кислот, воду, солі або електроліти, такі як протамінсульфат, вторинний кислий фосфат натрію, дикалійфосфат, хлорид натрію, солі цинку, колоїдний діоксид кремнію, трисилікат магнію, полівінілпіролідон, речовини на основі целюлози, поліетиленгліколь, циклодекстрини, натрійкарбоксиметилцелюлозу, поліакрилати, віск, блок-співполімери поліетилену і поліоксипропілену, поліетиленгліколь і ланолін. Термін "фармацевтично прийнятна сіль" стосується кислої або основної солі сполуки згідно з даним винаходом, де ця сіль має бажану фармакологічну активність і ні біологічно, ні іншим чином не є небажаною. Солі можуть бути утворені з кислотами, які включають, без обмеження, ацетат, адипат, альгінат, аспартат, бензоат, бензолсульфонат, бісульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропіонат, диглюконат, додецилсульфат, етансульфонат, фумарат, глюкогептаноат, гліцерофосфат, гемісульфат, гептаноат, гексаноат, гідрохлорид, гідробромід, гідройодид, 2-гідроксіетансульфонат, лактат, малеат, метансульфонат, 2-нафталінсульфонат, нікотинат, оксалат, тіоціанат, тозилат і ундеканоат. Приклади основних солей включають, без обмеження, солі амонію, солі лужних металів, такі як солі натрію і калію, солі лужноземельних металів, такі як солі кальцію і магнію, солі з органічними основами, такі як солі дициклогексиламіну, N-метил-D-глюкаміну, і солі з амінокислотами, такими як аргінін і лізин. У деяких варіантах здійснення основні азотовмісні групи можуть бути кватернізовані за допомогою агентів, які включають нижчі алкілгалогеніди, такі як метил-, етил-, пропіл- і бутилхлориди, -броміди і -йодиди; діалкілсульфати, такі як диметил-, діетил-, дибутил- і діамілсульфати; довголанцюжкові галогеніди, такі як децил-, лаурил-, міристил- і стеарилхлориди, -броміди і -йодиди; і аралкілгалогеніди, такі як фенетилброміди. Якщо не вказане інше, у випадку номенклатури, яка використовується для опису хімічних груп або залишків, як використовується в даному контексті, йдуть конвенції, де, читаючи назви зліва направо, місце приєднання до залишку молекули знаходиться з правого боку назви. Наприклад, група "(С1-3-алкокси)С1-3-алкіл" приєднана до залишку молекули по алкільному кінцю. Наступні приклади включають метоксіетил, де місце приєднання знаходиться поблизу етильного кінця, і метиламіно, де місце приєднання знаходиться поблизу амінного кінця. Якщо не вказане інше, коли двовалентну групу описують по її хімічній формулі, яка включає два залишки кінцевого зв'язку, вказані як «-», повинно бути зрозуміло, що приєднання читається зліва направо. 5 UA 113499 C2 5 10 15 20 25 30 35 40 45 Якщо не вказане інше, мають на увазі, що структури, представлені в даному контексті, також включають всі енантіомерні, діастереомерні і геометричні (або конформаційні) форми структури; наприклад, R- і S-конфігурації для кожного асиметричного центра, (Z)- і (Е)-ізомери по подвійному зв'язку, і комформаційні (Z)- і (Е)-ізомери. Отже, окремі стереохімічні ізомери, а також енантіомерні, діастереомерні і геометричні (або конформаційні) суміші сполук згідно з даним винаходом входять в об'єм даного винаходу. Якщо не вказане інше, всі таутомерні форми сполук згідно з винаходом входять в об'єм даного винаходу. Додатково, якщо не вказане інше, мають на увазі, що структури, представлені в даному контексті, також включають сполуки, які розрізнюються тільки присутністю одного або більше збагаченого ізотопами атома. Наприклад, сполуки, які мають структури згідно з даним винаходом, за винятком заміни водню 13 14 дейтерієм або тритієм, або заміни вуглецю С- або С-збагаченим вуглецем, входять в об'єм даного винаходу. Такі сполуки є придатними, наприклад, як аналітичні інструменти або зонди в біологічних аналізах. В. Сполуки В одному варіанті здійснення даний винахід стосується сполуки формули I: де: один з R1a і R1b означає водень, а інший означає метил; або R1a і R1b разом утворюють циклопропільне кільце; R2 означає метил або фторметил (наприклад, монофторметил, дифторметил, трифторметил); R3 означає метил; R4 означає водень, галоген, фторметил, метокси або фторметокси (наприклад, монофторметокси, дифторметокси, трифторметокси); R5 означає водень, галоген, фторметил, метокси або фторметокси; R6 означає водень, галоген, метил або метокси; R7 означає водень, галоген, метил або метокси; і Х означає кисень; або його фармацевтично прийнятних солей. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил; R2 означає метил, дифторметил або трифторметил; R3 означає метил; R4 означає хлор, фтор, трифторметил, дифторметил, метил, метокси, дифторметокси або трифторметокси; і R 5 означає водень, хлор, фтор, метил або метокси. У деяких варіантах здійснення R5 означає водень. У деяких варіантах здійснення R6 і R7, обох, означають водень. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і R 4 вибирають з хлору, трифторметилу, дифторметилу, дифторметокси і трифторметокси. У деяких варіантах здійснення R1a і R1b разом утворюють циклопропільне кільце; R2 означає метил, трифторметил або дифторметил; R3 означає метил; і R4 означає трифторметил, дифторметил, хлор або фтор. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і сполука формули I складається з суміші стереоізомерів. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і сполука формули I складається з по суті чистого стереоізомеру. У деяких варіантах здійснення один з R 1a і R1b означає водень, а інший означає метил, і вуглець з формули I, позначений знаком *, по суті має S-конфігурацію. У деяких варіантах здійснення один з R1a і R1b означає водень, а інший означає метил, і вуглець з формули I, позначений знаком *, по суті має R-конфігурацію. С. Фармацевтичні готові лікарські форми 6 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 60 Активні сполуки згідно з даним винаходом можна комбінувати з фармацевтично прийнятним носієм для отримання включаючих їх фармацевтичних готових лікарських форм. Конкретний вибір носія і готової лікарської форми залежить від конкретного шляху введення, для якого призначена композиція. Композиції згідно з даним винаходом можуть бути придатні для перорального, парентерального введення, введення за допомогою спрею для інгаляції, місцевого, ректального, назального, букального, вагінального введення або введення за допомогою резервуара, який імплантується і т.д. Переважно, композиції вводять перорально, інтраперитонеально або внутрішньовенно. Стерильні форми для ін'єкцій композицій згідно з даним винаходом можуть бути у вигляді водної або масляної суспензії. Ці суспензії можна отримувати відповідно до способами, відомими в даній галузі, з використанням відповідних диспергаторів або змочувачів і суспендуючих агентів. Стерильний препарат для ін'єкцій також може бути у вигляді стерильного розчину або суспензії для ін'єкцій в нетоксичному, парентерально прийнятному розріджувачі або розчиннику, наприклад, у вигляді розчину в 1,3бутандіолі. Серед прийнятних ексципієнтів і розчинників, які можуть бути використані, знаходяться вода, розчин Рінгера і ізотонічний розчин хлориду натрію. У доповнення, стерильні нелеткі олії є звичайно такими, які використовуються як розчинник або суспендуюче середовище. Для цієї мети можна використати будь-яку легку нелетку олію, включаючи синтетичні моноабо дигліцериди. У препаратах для ін'єкцій придатними є жирні кислоти, такі як олеїнова кислота і її гліцеридні похідні, які являють собою природні фармацевтично прийнятні масла, такі як оливкова олія або рицинова олія, особливо, в їх поліоксіетильованих варіантах. Ці масляні розчини або суспензії також можуть містити розріджувач або диспергатор на основі спирту з довгим ланцюгом, таким як карбоксиметилцелюлоза, або подібні диспергатори, які звичайно використовують при отриманні фармацевтично прийнятних лікарських форм, включаючи емульсії і суспензії. Інші, поверхнево-активні речовини, які звичайно використовуються, такі як Tween, Span і інші емульгатори або біодоступні посилюючі агенти, які звичайно використовують при отриманні фармацевтично прийнятних твердих, рідких або інших лікарських форм, також можна використати для цілей отримання готової лікарської форми. Фармацевтично прийнятні композиції згідно з даним винаходом можна вводити перорально в будь-якій перорально прийнятній лікарській формі, включаючи, але не обмежуючись ними, капсули, таблетки, водні суспензії або розчини. У випадку таблеток для перорального застосування, ті, які звичайно використовуються носії включають лактозу і кукурудзяний крохмаль. Також звичайно додають мастильні речовини, такі як стеарат магнію. Для перорального введення в формі капсули придатні розріджувачі включають лактозу і висушений кукурудзяний крохмаль. Коли водні суспензії потрібні для перорального використання, активний інгредієнт комбінують з емульгаторами і суспендуючими агентами. Якщо бажано, також можна додавати деякі підсолоджувачі, смакові добавки або барвники. Альтернативно, фармацевтично прийнятні композиції згідно з даним винаходом можна вводити в формі супозиторіїв для ректального введення. Супозиторії можна отримувати шляхом змішування агента з придатним, який не спричиняє подразнення ексципієнтом, який являє собою тверду речовину при кімнатній температурі, але стає рідким при ректальній температурі і, отже, розплавляється в прямій кишці для вивільнення лікарського засобу. Такі речовини включають масло какао, віск і поліетиленгліколі. Фармацевтично прийнятні композиції згідно з даним винаходом також можна вводити місцевим чином, особливо, коли мішень для лікування включає ділянки або органи, без великих зусиль доступні для місцевого застосування, включаючи захворювання ока, шкіри або нижньої частини кишечника. Придатні готові лікарські форми для місцевого застосування без великих зусиль отримують для кожної(го) з цих ділянок або органів. Місцеве застосування для нижньої частини кишечника може бути здійснене при використанні композиції ректального супозиторію (див. вище) або відповідного складу клізми. Також можуть бути використані місцево трансдермальні пластирі. Для ділянок місцевого застосування фармацевтично прийнятні композиції можуть бути отримані у вигляді відповідної мазі, яка містить активний компонент, суспендований або розчинений в одному або більше носіях. Носії для місцевого введення сполук за даним винаходом включають, але не обмежуються ними, мінеральне масло, рідкий вазелін, білий вазелін, пропіленгліколь, поліоксіетилен, поліоксипропілен, емульгований віск і воду. Альтернативно, фармацевтично прийнятні композиції можуть бути отримані у вигляді відповідного лосьйону або крему, який містить активні сполуки, суспендовані або розчинені в одному або більше фармацевтично прийнятних носіях. Відповідні носії включають, але не 7 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 обмежуються ними, мінеральне масло, сорбітанмоностеарат, полісорбат 60, віск на основі складних цетилових ефірів, цетеариловий спирт, 2-октилдодеканол, бензиловий спирт і воду. Для офтальмологічного використання фармацевтично прийнятні композиції можуть бути отримані у вигляді мікронізованих суспензій в ізотонічному, з встановленим значенням рН, стерильному сольовому розчині або, переважно, у вигляді розчинів в ізотонічному, з встановленим значенням рН, стерильному сольовому розчині, або з використанням консерванту, або без нього, як, наприклад, бензилалконійхлорид. Альтернативно, для офтальмологічних використань, фармацевтично прийнятні композиції можуть бути отримані у вигляді мазі, такої як вазелін. Фармацевтично прийнятні композиції згідно з даним винаходом також можуть бути введені за допомогою назального аерозолю або інгаляції. Такі композиції отримують згідно з способами, добре відомими в технології приготування фармацевтичної композиції, і можуть бути отримані у вигляді розчинів в сольовому розчині, використовуючи бензиловий спирт або інші відповідні консерванти, промотори абсорбції для посилення біодоступності, фторвуглеці і/або інші звичайні солюбілізуючі або диспергуючі агенти. Найбільш переважно фармацевтично прийнятні композиції згідно з даним винаходом отримують для перорального введення. D. Об'єкти і способи використання Показано, що простагландини модулюють різні фази імунної відповіді. Ліпідний медіаторний простагландин Е2 (PGE2) являє собою ейкозаноїд, який добре відомий для придушення + активації CD4 Т-клітин за рахунок збільшення внутрішньоклітинного цАМФ і інактивації Ick. Також показано, що PGE2 грає роль в регуляції Th1-відповідей шляхом придушення продукування інтерферону-гамма (IFN-gamma) і проліферації Т-клітин. Однак PGE2-стимуляція за рахунок ЕР4-субтипу PGE2-рецептору також може проводити протилежний ефект, а саме, промотування Th1-диференціювання ("Prostaglandin Е receptor subtypes EP2 and EP4 promote differentiation and expansion of Th1 and TH17 lymphocytes through different signaling modules" [Субтипи EP2 and EP4 рецептору простагландину Е промотують диференціювання і експансію Th1- і Th17-лімфоцитів через різні модулі передачі сигналу], Nature Medicine, 2009, друкується) і продуковані IL-17 в активованих клітинах CD4+. Простагландин Е2 синергічно з інтерлейкіном23 сприяє експансії людського Th17, Blood, 2008, 112, 2696-3703; простагландин Е2 регулює диференціювання і функцію Th17-клітин через циклічний АМФ і передачу сигналу ЕР2/ЕР4рецептору, J. Exp. Med., 2009, 206, 535-548; простагландин Е2 посилює Th17-відповідь через модуляцію продукування IL-17 і IFN-γ за рахунок пам'яті CD4+ Т-клітин, Eur. J. Immunol., 2009, 39, 1301-1312. Сумісно з цим, антагонізм ЕР4 по відношенню або до нового селективного ЕР4антагоніста, або до PGE2-нейтралізуючого антитіла придушує диференціювання Th1, експансію Th17, а також секрецію IL-23 активованими дендритними клітинами. Індукування диференціювання Th1 за рахунок PGE2 опосередковується передачею сигналу PI3K, тоді як для стимуляції продукування IL-17 потрібна передача сигналу цАМФ. Крім того, введення ЕР4антагоніста DBA/1- або C57BL/6-мишам придушує природжені і адаптивні імунні відповіді і придушує хворобу у випадку моделей індукованого колагеном артриту (CIA) і експериментального аутоімунного енцефаломієліту (ЕАЕ), вказуючи на те, що передача сигналу PGE2/EР4 критично залучена до цих аутоімунних патологій. Дані результати наводять на думку, що придушення передачі сигналу PGE2/EР4 може мати терапевтичне значення відносно модифікації запальних аутоімунних захворювань, таких як ревматоїдний артрит і розсіяний склероз. Активні сполуки згідно з даним винаходом можуть бути введені пацієнтам або суб'єктам для лікування ряду різних станів, особливо пацієнтам або суб'єктам, страждаючим від: (a) ревматоїдного артриту (див., наприклад, "Targeting rheumatoid arthritis and joint inflammation in the mouse", J. Clin. Invest., 2002, 110, 651-658; "Prostaglandin E2 exacerbates collagen-induced arthritis in mice through the inflammatory interleukin-23/interleukin-17 axis", Arthritis Rheum., 2007, 56:2608-2619); (b) розсіяного склерозу (див., наприклад, Narumiya S. в "The Prostanoid Receptors in Signaling Network of Chronic Inflammation-The Role of FP in Bleomycin-induced Pulmonary Fibrosis and The Role of EP4 in Experimental Autoimmune Encephalomyelitis in Mice", Eicosanoids and Chronic Inflammation, Montana, February, 2008, Keystone Symposia, Montana, February, 2008; "Prostaglandin Е receptor subtypes EP2 and EP4 promote differentiation and expansion of Th1 and Th17 lymphocytes through different signaling modules", Nature Medicine, 2009, друкується); (с) системного червоного вівчака (див., наприклад, "T-bet regulates IgG class switching and pathogenic auto Ab production", Proc. Natl. Acad. Sci. USA, 2002, 99, 5545-50; "Imbalance of 8 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Th1/Th2 transcription factors in patients with lupus nephritis", Rheumatology (Oxford), 2006, 45, 9517); (d) діабету типу 1 (див., наприклад, "Identification of а novel type 1 diabetes susceptibility gene, T-bet", Human Genetics, 2004, 111, 177-84; "T-bet controls autoaggressive CD8 lymphocyte response in type 1 diabetes", J. Exp. Med., 2004, 199, 1153-62); (е) псоріазу (див., наприклад, "А molecule solves psoriasis? Systemic therapies for psoriasis inducing interleukin 4 and Th2 responses", J. Mol. Med., 2003, 81, 471-80); "The IL-23/Th17 axis in the immunopathogenesis of psoriasis", J. Invest. Dermatol., 2009, doi:10.1038/jid.2009.59; (f) атеросклерозу (див., наприклад, "T-bet deficiency reduces atherosclerosis and alters plaque antigen-specific immune responses", Proc. Natl. Acad. Sci. USA, 2005, 102, 1596-601); (g) хвороби Крона (див., наприклад, "IL-23/IL-17 immunity as а hallmark of Crohn's disease", Inflamm. Bowl. Dis., 2009, 14, 1175-1184; "The proinflammatory effect of prostaglandin E2 in experimental inflammatory bowel disease is mediated through the IL-23-IL-17 axis", J. Immunol., 2007, 178, 8138-8147); (h) запального болю (див., наприклад, "Prostaglandin E2 receptor EP4 contributes to inflammatory pain hypersensitivity", J. Pharmacol. Exp. Ther., 2006, 319, 1096-1103); (i) невропатичного болю (див., наприклад, "Localisation and modulation of prostanoid receptors EP1 and EP4 in the rat chronic constriction injury model of neuropathic pain", Eur. J. Pain, 2007, 11, 605-613); (j) асоційованого з мігренню болю (див., наприклад, "BGC20-1531, а novel, potent, and selective EP4 receptor antagonist: а putative new treatment for migraine headache", Br. J. Pharmacol., 2009, 156, 316-327); (k) спондилоартропатій (див., наприклад, "Nonsteroidal Antiinflammatory Drugs reduce radiographic progression in patients withankylosing spondylitis", Arthritis Rhuem., 2005, 52, 17561765; "Efficacy of celecoxib, а cyclooxygenase 2-specific inhibitor, in the treatment of ankylosing spondylitis: а six-week conrolled study with comparison against placebo and against а conventional nonsteroidal antiinflammatory drug", Arthritis Rheum., 2001, 44, 180-185; "Increased numbers of circulating polyfunctional Th17 memory cells in patients with seronegative spondylarthritides", Arthritis Rheum., 2008, 58, 2307-2317); (l) раку шкіри (див., наприклад, "Chemoprevention of nonmelanoma skin cancer with Celecoxib: А randomized, double-blind, placebo-controlled trial", J. Natl. Cancer. Inst., 2010, 102, 1-10); (m) раку молочної залози (див., наприклад, "Potential new drug targets against hormonedependent breast cancer identified", Exp. Rev. Anticancer Ther., 2008, 8, 507-509; "Antagonism of the prostaglandin Е receptor EP4 inhibits metastasis and enhances NK function", Breast Cancer Res. Treat., 2009, 117, 235-242; "Prostaglandin Е receptor EP4 antagonism inhibits breast cancer metastasis", Cancer Res., 2006, 66, 2923-2927); (n) колоректального раку (див., наприклад, "Increased EP4 receptor expression in colorectal cancer progession promotes cell growth and anchorage independence", Cancer Res., 2006, 66, 3106-3113); (о) раку простати (див., наприклад, "Identification of EP4 as а potential target for the treatment of castration-resistant prostate cancer using а novel xenograft model", Cancer Res., 2010, 70, 16061615); (р) раку нирки (див., наприклад, "Prostaglandin E2 regulates renal cell carcinoma invasion through а EP4-Rap signal transduction pathway", J. Bio. Chem. Aug. 10, 2011 (евр. публікація)); (q) цервікального раку (див., наприклад, "COX-2 expression is correlated with VEGF-C, Lymphangiogenesis and lymph node metastasis in human cervical cancer", Microvasc Res. 2011, 82, 131-40); (r) оваріального раку (див., наприклад, "Ovarian epithelial cancer: а role for PGF2 synthesis and signaling in malignant transformation and progression", Mol. Cancer, 2006, 5, 62); (s) ендометриального раку (див., наприклад, "Prostaglandin E2 induces proliferation of Glandular epithelial cells of human endometrium via extracellular regulated kinase 1/2-mediated patheway", J. Clin. Endocrinol. & Metabol. 2003, 88, 4481-4487); (t) гліобластоми (див., наприклад, "Microsomal prostaglandin Е synthase-1 regulates human glioma cell growth via prostaglandin E2-dependent activation of type II protein kinase", A. Mol. Cancer Ther. 2006, 5, 1817-1826); (u) раку голови і шиї (див., наприклад, "Expression of prostaglandin E2 receptors in oral squamous cell carcinomas and growth inhibitory effects of а selective EP3 antagonist", ONO-AE3240. Int. J. Oncology, 2009, 34, 847-852); 9 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 60 (v) медулобластоми (див., наприклад, "Tumor-growth-promoting cyclooxygenase-2 prostaglandin E2 pathway provides medulloblastoma therapeutic targets". Neuro-Oncol. 2008, 661674); (w) раку легенів (див., наприклад, "Tumor cyclooxygenase-2/prostaglandin E2-dependent promotion of FOXP3 expression and CD4+CD25+ Т regulatory cell activities in lung cancer". Cancer Res. 2005, 65, 5211-5220); (х) ракових захворювань сечових шляхів (див., наприклад, "Pathological function of prostaglandin E2 receptors in transitional cell carcinoma of the upper urinary tract". Virchows Archiv. 2006, 448, 822-829). У доповнення, PGE2 залучається як важливий компонент в імуносупресивне навколишнє середовище, яке створюється множиною солідних пухлин: "Inhibiting the inhibitors: evaluating agents targeting cancer immunosuppression. Expert Opinion" (Інгібування інгібіторами: агенти оцінки цільової ракової імуносупресії. Висновок експерта) в Biological Therapy, 2010, 10, 1019-35. Показано, що антагонізм ЕР4-рецептору зменшує метастазування пухлини: "Host and direct antitumor effects and profound reduction in tumor metastasis with selective EP4 receptor antagonism" (Хазяїн і прямі протипухлинні ефекти і "глибоке" зменшення метастазування пухлини за рахунок селективного антагонізму ЕР4-рецептору). Cancer Res. 2006, 66, 9665-9672. Активні сполуки можуть бути введені суб'єктам будь-яким відповідним шляхом, який включає введення перорально, парентерально, за допомогою спрея для інгаляції, місцево, ректально, назально, букально, вагінально або через резервуар, який імплантується. Термін "парентеральний", який використовується в даному контексті, включає способи підшкірної, внутрішньовенної, внутрішньом'язової, внутрішньосуглобової, інтрасиновіальної, інтрастернальної, інтратекальної, внутрішньопечінкової, інтралезиональної і інтракраніальної ін'єкції або інфузії. Переважно, композиції вводять перорально, інтраперітонеально або внутрішньовенно. Активні сполуки вводять суб'єктам в ефективній для лікування, або терапевтично ефективній, кількості. Кількість сполук згідно з даним винаходом, яке можна комбінувати з носіями для отримання композиції в одноразовій лікарській формі, може змінюватися залежно від реципієнта, який піддається лікуванню і конкретного шляху введення. Переважно, композиції повинні бути складені так, щоб пацієнту, який отримує ці композиції, могла бути введена доза інгібітору 0,01-100 мг/кг маси тіла на добу. У деяких варіантах здійснення для композицій згідно з даним винаходом передбачають дозу від 0,01 мг до 50 мг. У інших варіантах здійснення передбачають дозу від 0,1 мг до 25 мг або від 5 мг до 40 мг. Також повинно бути зрозуміло, що конкретна доза і режим лікування для будь-якого конкретного пацієнта залежить від множини факторів, які включають активність конкретної сполуки, яка застосовується, вік, масу тіла, загальний стан здоров'я, стать, дієту, час введення, швидкість виведення з організму, комбінацію лікарських засобів і висновок лікуючого лікаря і тяжкість конкретного захворювання, яке піддають лікуванню. Кількість сполуки згідно з даним винаходом в композиції також залежить від конкретної сполуки в композиції. З тим, щоб даний винахід, описаний в даному контексті, можна було повніше зрозуміти, наводяться нижченаведені приклади. Повинно бути зрозуміло, що ці приклади представлені тільки для ілюстративних цілей і не можуть бути витлумачені як обмежуючі об'єм охорони даного винаходу яким-небудь чином. ПРИКЛАДИ 1-113 Загальне: Нагрівання під впливом мікрохвильового випромінювання проводили, використовуючи мікрохвильове випромінювання Biotage Emrys Liberator або Initiator. Колонкову хроматографію проводили, використовуючи Biotage SP4. Видалення розчинника здійснювали, використовуючи або роторний випарник Buchii, або відцентровий випарник Genevac. Препаративний РХ/МС проводили, використовуючи автоочисник Waters і колонку розміром 19 мм 100 мм, Хterra, 5 мікрон MS C18, за умови кислотної рухомої фази. ЯМР-спектри реєстрували, використовуючи спектрометр Varian 400 МГц. Коли термін "інертна атмосфера" використовують для опису реактора (наприклад, реакційна посудина, колба, скляний реактор і т.п.), він означає, що повітря в реакторі замінене по суті сухим інертним газом або, який не містить вологи (таким як азот, аргон і т.п.). Загальні способи і експерименти для отримання сполук згідно з даним винаходом викладені нижче. У деяких випадках, конкретна сполука описана за допомогою прикладу. Однак повинно бути взято до уваги, що в кожному випадку ряд сполук згідно з даним винаходом отримували відповідно до схем і експериментів, описаних нижче. У даному контексті використовують наступні абревіатури: 10 UA 113499 C2 5 10 15 20 Визначення: Наступні абревіатури мають вказані значення: HATU: гексафторфосфат N,N,N',N'-тетраметил-О-(7-азабензотриазол-1-іл)уронію COMU: гексафторфосфат (1-ціано-2-етокси-2оксоетиліденаміноокси)диметиламіноморфолінокарбенію DPCI: N,N'-діізопропілкарбодиімід DIEA: N,N-діізопропілетиламін ТЕА: триетиламін DMAP: 4-диметиламінопіридин ДМФА: N,N-диметилформамід NMP: N-метилпіролідин ТГФ: тетрагідрофуран DCM: дихлорметан ТФОК: трифтороцтова кислота Речовини: Наступні сполуки є коммерційно доступними: 5-хлор-1,3-диметил-1Н-піразол-4-карбальдегід (Maybridge Chemical Co., Ltd.); 5-хлор-1-метил-3-(трифторметил)-1Н-піразол-4-карбальдегід (Maybridge Chemical Co., Ltd.); 5-(3-хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонова кислота (Bionet Research); 1,3-диметил-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонова кислота (Bionet Research); 1-метил-3-(трифторметил)-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонова кислота (Bionet Research); 5-(4-хлорфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота (Bionet Research); етил 4,4-дифторацетоацетат (Matrix Scientific); гідрохлорид (S)-метил-4-(1-аміноетил)бензоату (NetChem, Inc); 4-(1-аміноциклопропіл)бензойна кислота (Allweys LLC). Всі феноли, за винятком 3-дифторметилфенолу, є комерційно доступними. Сполуки згідно з даним винаходом отримують відповідно до загальної схеми синтезу, представленої на схемі I: Отримання типових, які не обмежують об'єм охорони винаходу, сполук згідно з даним винаходом описано нижче. 11 UA 113499 C2 ПРИКЛАДИ 1-51 Схема отримання 1 Методика отримання 5-хлор-3-(дифторметил)-1-метил-1Н-піразол-4-карбальдегіду Стадія 1: 5 10 15 20 25 30 35 40 Етил 4,4-дифторацетоацетат (30,12 г, 0,172 моль) перемішували в толуолі (600 мл) при охолоджуванні сумішшю води з льодом. Повільно, по краплях, протягом 20 хвилин додавали розчин N-метилгідразину (7,6 мл, 0,14 моль) в толуолі (200 мл). Реакційну суміш нагрівали при температурі 100 °C протягом 2 годин. Реакційну суміш випаровували насухо. Отриманий продукт розтирали в суміші метил-трет-бутиловий ефір/гептан, отримуючи 3-(дифторметил)-1метил-1Н-піразол-5(4Н)-он за три прийоми (загальна кількість становить 10,7 г, вихід 51 %) у вигляді порошкоподібної речовини помаранчевого кольору. Цю речовину використали без додаткового очищення на наступній реакційній стадії. Стадія 2: ДМФА (9,5 мл, 0,12 моль) перемішували на бані з льодом і по краплях додавали фосфорилхлорид (24,0 мл, 0,257 моль). До розчину додавали 3-(дифторметил)-1-метил-1Нпіразол-5(4Н)-он (5,51 г, 0,0372 моль), у вигляді порцій, і суміш нагрівали при температурі 120 °C протягом 40 хвилин. Реакційну суміш охолоджували і фосфорилхлорид гасили шляхом повільного додавання невеликих порцій льоду при перемішуванні. Суміш потім три рази екстрагували етилацетатом і об'єднаний органічний шар промивали водою і насиченим сольовим розчином, сушили над MgSO4 і випаровували, отримуючи 5-хлор-3-(дифторметил)-1метил-1Н-піразол-4-карбальдегід (5,66 г, вихід 78,2 %) у вигляді твердої речовини темнопомаранчевого або коричневого кольору. Цю речовину використали без додаткового очищення на наступній реакційній стадії. Схема отримання 2 Методика отримання 3-дифторметилфенолу До розчину 3-гідроксибензальдегіду (1,01 г, 0,0083 моль) в метиленхлориді (3,3 мл) додавали розчин трифториду біс(2-метоксіетил)аміносірки (3,09 г, 0,0140 моль) в метиленхлориді (3,3 мл), потім етанол (95,0 мкл, 0,00163 моль). Реакційну суміш перемішували при кімнатній температурі протягом 12 годин. Суміш потім обережно гасили шляхом додавання насиченого водного розчину бікарбонату натрію. Органічний шар відділяли, промивали насиченим сольовим розчином, сушили над MgSO 4 і випаровували, отримуючи масло жовтого кольору. Це масло очищали за допомогою колонкової хроматографії (0-50 % етилацетат/гептан), отримуючи вказану в заголовку сполуку (649 мг, вихід 57 %) у вигляді безбарвного масла. Схема отримання 3 Типова методика отримання 5-арилоксипіразол-4-карбонової кислоти Приклад отримання 1: 5-(3,4-дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Стадія 1: 12 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 5-хлор-1,3-диметил-1Н-піразол-4-карбальдегід (500,0 мг, 0,00315 моль), 3,4-дихлорфенол (565 мг, 0,00344 моль) і гідроксид калію (265 мг, 0,00472 моль) перемішували в ДМФА (2,0 мл). Суміш нагрівали при температурі 150 °C протягом 20 хвилин, використовуючи мікрохвильове випромінювання. Додавали воду і отриману суміш екстрагували етилацетатом. Органічний шар двічі промивали насиченим сольовим розчином, сушили над MgSO 4 і випаровували. Отримане масло очищали за допомогою колонкової хроматографії (10-20 % етилацетат/гептан), отримуючи 5-(3,4-дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбальдегід (492 мг, вихід 54,7 %) у вигляді твердої речовини білого кольору. Стадія 2: 5-(3,4-Дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбальдегід з стадії 1 (492 мг, 0,001726 моль) і 2-метил-2-бутен (300 мкл, 0,002832 моль) перемішували в трет-бутиловому спирті (2,0 мл). Додавали розчин хлориту натрію (400 мг, 0,003538 моль) і дигідрогенфосфату натрію (450 мг, 0,003751 моль) у воді (3,0 мл) і реакційну суміш перемішували протягом 12 годин при кімнатній температурі. Розчинник випаровували і отриманий залишок розчиняли в етилацетаті. Органічний шар промивали водою, сушили над MgSO 4 і випаровували, отримуючи вказану в заголовку сполуку (340 мг, вихід 65,5 %) у вигляді твердої речовини білого кольору. Цю речовину використали на наступній стадії без додаткового очищення. Приклад отримання 2: 5-(3-фторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-фторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 3: 5-(3,4-дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3,5-дифторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 4: 5-(2,3-дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 2,3-дифторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 5: 5-(2,5-дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 2,5-дифторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 6: 5-(3,5-дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3,5-дихлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 7: 5-(3-хлорфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-хлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 8: 5-(2,3-дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 2,3-дихлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 9: 5-(3-хлор-5-фторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-хлор-5-фторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 10: 5-(2-хлор-5-фторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота 13 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 2-хлор-5-фторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 11: 1,3-диметил-5-(м-толілокси)-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і м-крезол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 12: 5-(3,5-диметилфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3,5-диметилфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 13: 5-(3,5-диметоксифенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3,5-диметоксифенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 14: 5-(3-хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 3-хлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 15: 3-(дифторметил)-1-метил-5-(3-(трифторметил)фенокси)-1Н-піразол4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 3-трифторметилфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 16: 1,3-диметил-5-(3-(трифторметокси)фенокси)-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-трифторметоксифенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 17: 5-(3-фторфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 3-фторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 18: 5-(3,4-дифторфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 3,4-дифторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 19: 5-(3,4-дихлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 3,4-дихлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 20: 5-(3-(дифторметокси)фенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-дифторметоксифенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 21: 5-(3-(дифторметокси)фенокси)-1-метил-3-(трифторметил)-1Нпіразол-4-карбонова кислота 14 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 3-дифторметоксифенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 22: 5-(3-(дифторметокси)фенокси)-3-(дифторметил)-1-метил-1Нпіразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 3-дифторметоксифенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 23: 3-(дифторметил)-5-(3-(дифторметил)фенокси)-1-метил-1Н-піразол4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 3-дифторметилфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 24: 5-(3-(дифторметил)фенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 3-дифторметилфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 25: 5-(3-(дифторметил)фенокси)-1-метил-3-(трифторметил)-1Н-піразол4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 3-дифторметилфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 26: 5-(3,4-дихлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 3,4-дихлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 27: 5-(4-фторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 4-фторфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 28: 1,3-диметил-5-(4-(трифторметил)фенокси)-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 4-(трифторметил)-фенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат цезія замість гідроксиду калію. Приклад отримання 29: 5-(2-хлор-4-фторфенокси)-1,3-диметил-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і 2-хлор-4-фторфенол, по методиці, подібній методиці в прикладі отримання 1. Приклад отримання 30: 1,3-диметил-5-(п-толілокси)-1Н-піразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1,3-диметил-1Н-піразол-4карбальдегід і п-крезол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1. Приклад отримання 31: 1- метил-3-(трифторметил)-5-(4-(трифторметил)фенокси)-1Нпіразол-4-карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 4-(трифторметил)фенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 32: 3-(дифторметил)-1-метил-5-(4-(трифторметил)фенокси)-1Н-піразол4-карбонова кислота 15 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 4-(трифторметил)фенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 33: 5-(4-хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-1-метил-3(трифторметил)-1Н-піразол-4-карбальдегід і 4-хлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Приклад отримання 34: 5-(4-хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4карбонова кислота Вказану в заголовку сполуку отримували, використовуючи 5-хлор-3-(дифторметил)-1-метил1Н-піразол-4-карбальдегід і 4-хлорфенол, по методиці, подібній методиці у вищенаведеному прикладі отримання 1, за винятком того, що використали карбонат калію замість гідроксиду калію. Схема отримання 4 Типова методика зв'язування аміду і гідроліз складного ефіру Приклад 1: ER-885289 5-(3-Хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту (50 мг, 0,0002 моль), HATU (65 мг, 0,00017 моль) і DIEA (30 мкл, 0,00017 моль) перемішували в ДМФА (1,0 мл) протягом 20 хвилин при кімнатній температурі. По краплях додавали розчин гідрохлориду (S)-метил 4-(1-аміноетил)бензоату (40 мг, 0,00019 моль) і DIEA (32 мкл, 0,00019 моль) в ДМФА (1,0 мл) і реакційну суміш перемішували при кімнатній температурі протягом 12 годин. Додавали воду і отриманий в результаті осад збирали, промивали водою і сушили у вакуумі, отримуючи 59,2 мг складного метилового ефіру у вигляді твердої речовини білого кольору. Цей складний метиловий ефір розчиняли в метанолі (1,0 мл) і ТГФ (1,0 мл). Додавали 2,0 М розчин гідроксиду літію (240 мкл) і суміш перемішували при кімнатній температурі протягом 12 годин. Реакційну суміш нейтралізували 1 н. розчином хлористоводневої кислоти (480 мкл) і отриману емульсію екстрагували етилацетатом. Органічний шар відділяли і випаровували. Отриманий продукт розчиняли в 3 мл метанолу і очищали шляхом РХ/МС (як рухома фаза 0,1 % ТФОК в суміші ацетонітрил/вода). Бажані фракції випаровували з використанням випарника Genevac, отримуючи вказану в заголовку сполуку (27 мг, за дві стадії вихід 46 %). Приклад 2 (ER-885290). Сполуку прикладу 2 отримували, використовуючи 1,3-диметил-5-(3(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 1. Приклад 3 (ER-885291). Сполуку прикладу 3 отримували, використовуючи 1-метил-3(трифторметил)-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 1. Приклад 4 (ER-885716). Сполуку прикладу 4 отримували, використовуючи 5-(3,4дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 1, за винятком того, що гідроліз здійснювали в ТГФ і 1,4-диоксані при температурі 140 °C протягом 10 хвилин, використовуючи мікрохвильове випромінювання, і продукт отримували у вигляді твердої речовини після нейтралізації. Приклад 5 (ER-885717). Сполуку прикладу 5 отримували, використовуючи 5-(3фторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 6 (ER-885718). Сполуку прикладу 6 отримували, використовуючи 5-(3,4дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. 16 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 7 (ER-885719). Сполуку прикладу 7 отримували, використовуючи 5-(2,3дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 8 (ER-885720). Сполуку прикладу 8 отримували, використовуючи 5-(2,5дифторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 9 (ER-885721). Сполуку прикладу 9 отримували, використовуючи 5-(3,5дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 13 (ER-885744). Сполуку прикладу 13 отримували, використовуючи 5-(3хлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 14 (ER-886022). Сполуку прикладу 14 отримували, використовуючи 5-(2,3дихлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 15 (ER-886024). Сполуку прикладу 15 отримували, використовуючи 5-(3-хлор-5фторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 16 (ER-886025). Сполуку прикладу 16 отримували, використовуючи 5-(2-хлор-5фторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 17 (ER-886032). Сполуку прикладу 17 отримували, використовуючи 1,3-диметил-5(м-толілокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 18 (ER-886033). Сполуку прикладу 18 отримували, використовуючи 5-(3,5диметилфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 19 (ER-886035). Сполуку прикладу 19 отримували, використовуючи 5-(3,5диметоксифенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі4. Приклад 20 (ER-886045). Сполуку прикладу 20 отримували, використовуючи 5-(3хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 21 (ER-886046). Сполуку прикладу 21 отримували, використовуючи 3(дифторметил)-1-метил-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 22 (ER-886061). Сполуку прикладу 22 отримували, використовуючи 1,3-диметил-5(3-трифторметокси)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 23 (ER-886072). Сполуку прикладу 23 отримували, використовуючи 5-(3фторфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 1, за винятком того, що використали COMU, TEA і NMP замість HATU, DIEA і ДМФА, і продукт отримували у вигляді твердої речовини після нейтралізації. Приклад 24 (ER-886073). Сполуку прикладу 24 отримували, використовуючи 5-(3,4дифторфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 23. Приклад 25 (ER-886074). Сполуку прикладу 25 отримували, використовуючи 5-(3,4дихлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 23. Приклад 26 (ER-886077). Сполуку прикладу 26 отримували, використовуючи 5-(3хлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 27 (ER-886078). Сполуку прикладу 27 отримували, використовуючи 3(дифторметил)-1-метил-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. 17 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 28 (ER-886080). Сполуку прикладу 28 отримували, використовуючи 5-(3(дифторметокси)фенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 23. Приклад 29 (ER-886082). Сполуку прикладу 29 отримували, використовуючи 5-(3(дифторметокси)фенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 23. Приклад 30 (ER-886083). Сполуку прикладу 30 отримували, використовуючи 3(дифторметил)-1-метил-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (R)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 31 (ER-886090). Сполуку прикладу 31 отримували, використовуючи 5-(3(дифторметокси)фенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 23. Приклад 32 (ER-887480). Сполуку прикладу 32 отримували, використовуючи 3(дифторметил)-5-(3-(дифторметил)фенокси)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4, за винятком того, що продукт отримували після очищення шляхом РХ/МС. Приклад 33 (ER-887495). Сполуку прикладу 33 отримували, використовуючи 5-(3(дифторметил)фенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4, за винятком того, що використали HBTU, TEA і NMP замість HATU, DIEA і ДМФА. Приклад 34 (ER-887995). Сполуку прикладу 34 отримували, використовуючи 5-(3(дифторметил)фенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 33, за винятком того, що продукт отримували після очищення шляхом РХ/МС. Приклад 35 (ER-888024). Сполуку прикладу 35 отримували, використовуючи 5-(3,4дихлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 36 (ER-888348). Сполуку прикладу 36 отримували, використовуючи 5-(3,4дихлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 37 (ER-888355). Сполуку прикладу 37 отримували, використовуючи 5-(3хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 38 (ER-888363). 5-(3,4-Дихлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4карбонову кислоту (104 мг, 0,0002929 моль), DMAP (17 мг, 0,000139 моль), PS-HOBT (1,00 моль/г завантаження; 191 мг, 0,000191 моль) перемішували в DCM з 20 % ДМФА (4:1, DCM:ДМФА, 5,00 мл). Додавали DPCI (140 мкл, 0,0008941 моль) і суміш струшували при температурі 40 °C протягом 12 годин. Смолу потім послідовно промивали за допомогою DCM (3 мл), ДМФА (3 мл), DCM (3 мл), ТГФ (3 мл) і потім знову DCM (3 мл) і висушували у вакуумі. Цю смолу перемішували в DCM з 20 % ДМФА (4:1, DCM:ДМФА, 5,00 мл) і додавали розчин гідрохлориду метил 4-(1-аміноциклопропіл)бензоату (27 мг, 0,000118 моль) в DCM з 20 % ДМФА (5,00 мл) і DIEA (20 мкл, 0,000115 моль). Суміш струшували при температурі 40 °C протягом 12 годин. Смолу відфільтровували і промивали за допомогою DCM. Об'єднані фільтрати концентрували у вакуумі, отримуючи розчин в ДМФА. Розчин розбавляли етилацетатом, промивали водою і насиченим сольовим розчином, сушили над MgSO 4 і випаровували, отримуючи тверду речовину бежевого кольору. Тверду речовину очищали колонковою хроматографією (0-40 %), отримуючи складний метиловий ефір (18 мг) у вигляді твердої речовини білого кольору. Цей складний метиловий ефір розчиняли в 1,4-диоксані (1,0 мл). Додавали 2,0 М розчин гідроксиду літію (200 мкл) і суміш нагрівали при температурі 60 °C протягом 12 годин. Реакційну суміш додатково нагрівали при температурі 140 °C протягом 20 хвилин, використовуючи мікрохвильове випромінювання. Реакційну суміш підкислювали 1 н. розчином хлористоводневої кислоти (420 мкл) і додавали воду. Отриманий в результаті осад збирали, промивали водою і висушували на повітрі, отримуючи вказану в заголовку сполуку (15,9 мг, за дві стадії вихід 26 %) у вигляді твердої речовини білого кольору. 18 UA 113499 C2 5 10 15 20 25 30 35 40 45 50 Приклад 39 (ER-880663). Сполуку прикладу 39 отримували, використовуючи 5-(4хлорфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 40 (ER-885302). Сполуку прикладу 40 отримували, використовуючи 5-(4фторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 41 (ER-885311). Сполуку прикладу 41 отримували, використовуючи 1,3-диметил-5(4-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 42 (ER-886023). Сполуку прикладу 42 отримували, використовуючи 5-(2-хлор-4фторфенокси)-1,3-диметил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 43 (ER-885749). Сполуку прикладу 43 отримували, використовуючи 1,3-диметил-5(п-толілокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 4. Приклад 44 (ER-888365). Сполуку прикладу 44 отримували, використовуючи 1-метил-3(трифторметил)-5-(4-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці в прикладі 38. Приклад 45 (ER-888367). Сполуку прикладу 45 отримували, використовуючи 3(дифторметил)-1-метил-5-(4-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)-метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38, за винятком того, що гідроліз здійснював при температурі 60 °C протягом 12 годин. Приклад 46 (ER-888369). Сполуку прикладу 46 отримували, використовуючи 5-(4хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38, за винятком того, що продукт отримували після очищення з використанням суміші гептан/етилацетат/мурашина кислота як рухома фаза. Приклад 47 (ER-888371). Сполуку прикладу 47 отримували, використовуючи 5-(4хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид (S)метил 4-(1-аміноетил)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38. Приклад 48 (ER-888364). Сполуку прикладу 48 отримували, використовуючи 1-метил-3(трифторметил)-5-(4-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38. Приклад 49 (ER-888366). Сполуку прикладу 49 отримували, використовуючи 3(дифторметил)-1-метил-5-(4-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38. Приклад 50 (ER-888368). Сполуку прикладу 50 отримували, використовуючи 5-(4хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4-(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38. Приклад 51 (ER-888370). Сполуку прикладу 51 отримували, використовуючи 5-(4хлорфенокси)-3-(дифторметил)-1-метил-1Н-піразол-4-карбонову кислоту і гідрохлорид метил 4(1-аміноциклопропіл)бензоату, по методиці, подібній методиці у вищенаведеному прикладі 38. Приклад 10 (ER-885740) 1,3-Диметил-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту (20 мг, 0,00007 моль), HATU (28 мг, 0,000073 моль) і DIEA (13 мкл, 0,000073 моль) перемішували в ДМФА (0,5 мл) протягом 20 хвилин при кімнатній температурі. По краплях додавали розчин 4-(1аміноциклопропіл)бензойної кислоти (14 мг, 0,000080 моль) і DIEA (14 мкл, 0,000080 моль) в ДМФА (0,5 мл) і реакційну суміш перемішували при кімнатній температурі протягом 12 годин. Реакційну суміш розбавляли до 3 мл метанолом і очищали шляхом РХ/МС (як рухома фаза 19 UA 113499 C2 5 10 15 20 25 0,1 % ТФОК в суміші ацетонітрил/вода). Бажані фракції випаровували з використанням випарника Genevac, отримуючи вказану в заголовку сполуку (15 мг, вихід 50 %). Приклад 11 (ER-885741). Сполуку прикладу 11 отримували, використовуючи 1-метил-3(трифторметил)-5-(3-(трифторметил)фенокси)-1Н-піразол-4-карбонову кислоту і 4-(1аміноциклопропіл)бензойну кислоту, по методиці, подібній методиці у вищенаведеному прикладі 10. Приклад 12 (ER-885743). Сполуку прикладу 12 отримували, використовуючи 5-(3хлорфенокси)-1-метил-3-(трифторметил)-1Н-піразол-4-карбонову кислоту і 4-(1аміноциклопропіл)бензойну кислоту, по методиці, подібній методиці у вищенаведеному прикладі 10. Методика отримання гідрохлориду метил 4-(1-аміноциклопропіл)бензоату Стадія 1: 4-(1-Аміноциклопропіл)бензойну кислоту (1,75 г, 0,00988 моль) перемішували в ТГФ (20 мл) і метанолі (10 мл) на бані з сумішшю води з льодом. Додавали 2,00 М розчин триметилсилілдіазометану в гексані (9,9 мл, 0,020 моль) і суміш перемішували при кімнатній температурі протягом 12 годин. Реакційну суміш концентрували до в'язкого масла, яке твердіє при стоянні з отриманням кристалічної твердої речовини. Сирий продукт висушували у високому вакуумі протягом 12 годин, отримуючи метил 4-(1-аміноциклопропіл)бензоат (1,65 г, вихід 87 %) у вигляді твердої речовини блідо-коричневого кольору. Стадія 2: До розчину сполуки ER-886774-00 (1,63 г, 0,0085 моль) в етилацетаті (10 мл) додавали 2,0 М розчин хлороводню в диетиловому ефірі (6,0 мл, 0,012 моль). Після перемішування протягом декількох хвилин реакційну суміш концентрували, отримуючи вказану в заголовку сполуку (кількісний вихід) у вигляді твердої речовини блідо-коричневого кольору. Таблиця 1 Аналітичні дані для типових сполук формули I Приклад Структура Номер ER 1 Віднесення Н-ЯМР H-ЯМР (400 МГц, CD3OD) δ м.д. 8,56 (1H, д), 7,87 (2H, м), 7,30 (1H, м), 7,18 (2H, д), 7,08 (1H, т), 6,88 (1H, м), 4,96 (1H, м), 3,78 (3H, с), 1,34 (3H, д) 1 1 ER-885289-00 20 UA 113499 C2 1 2 ER-885290-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,88 (1H, д), 7,80 (2H, д), 7,49 (2H, м), 7,30 (1H, уш.с), 7,13 (2H, д), 4,99 (1H, м), 3,64 (3H, с), 2,37 (3H, м), 1,32 (3H, д) 1 3 ER-885291-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,60 (1H, д), 7,81 (2H, д), 7,51 (2H, м), 7,39 (1H, с), 7,18 (3H, м), 4,92 (1H, м), 3,79 (3H, с), 1,30 (3H, д) 1 4 ER-885716-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,84 (2H, д), 7,42 (1H, д), 7,15 (2H, д), 7,13 (1H, д), 6,83 (1H, дд), 5,01 (1H, кв.), 3,62 (3H, с), 2,35 (3H, с), 1,36 (3H, д) 1 5 ER-885717-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,8 (3H, м), 7,34 (1H, м), 7,14 (2H, д), 6,91 (1H, м), 6,73 (2H, м), 5 (1H, кв.), 3,61 (3H, с), 2,35 (3H, с), 1,34 (3H, д) 1 6 ER-885718-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,86 (3H, м), 7,19 (3H, м), 6,92 (1H, м), 6,68 (1H, м), 5,02 (1H, кв.), 3,61 (3H, с), 2,34 (3H, с), 1,37 (3H, д) 1 7 ER-885719-00 21 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,01 (1H, д), 7,84 (2H, д), 7,19 (2H; д), 7,01 (2H, м), 6,58 (1H, м), 4,99 (1H, кв.), 3,66 (3H, с), 2,33 (3H, с), 1,37 (3H, д) UA 113499 C2 1 8 ER-885720-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,06 (1H, д), 7,85 (2H, д), 7,22 (3H, м), 6,87 (1H, м), 6,63 (1H, м), 5 (1H, кв.), 3,66 (3H, с), 2,32 (3H, с), 1,37 (3H, д) 1 9 ER-885721-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,97 (1H, д), 7,85 (2H, д), 7,18 (3H, м), 6,89 (1H, д), 5,03 (1H, кв.), 3,62 (3H, с), 2,35 (3H, с), 1,38 (3H, д) 1 10 ER-885740-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,45 (1H, с), 7,79 (2H, д), 7,59 (1H, м), 7,52 (1H, м), 7,36 (1H, с), 7,21 (1H, дд), 7,03 (2H, д), 3,67 (3H, с), 2,38 (3H, с), 1,22 (2H, м), 0,91 (2H, м) 1 11 ER-885741-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 9,03 (1H, с), 7,77 (2H, д), 7,58 (2H, м), 7,46 (1H, с), 7,26 (1H, д), 7,03 (2H, д), 3,83 (3H, с), 1,20 (2H, м), 0,84 (2H, м) 1 12 ER-885743-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,80 (2H, д), 7,39 (1H, м), 7,26 (1H, д), 7,17 (1H, т), 7,04 (2H, д), 6,97 (1H, дд), 3,82 (3H, с), 1,23 (2H, м), 0,92 (2H, м) 1 13 ER-885744-00 22 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,83 (2H, д), 7,32 (1H, м), 7,19 (1H, м), 7,14 (2H, д), 7,00 (1H, т), 6,85 (1H, дд), 5,01 (1H, м), 3,63 (3H, с), 2,36 (3H, с), 1,35 (3H, д) UA 113499 C2 1 14 ER-886022-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,81 (2H, д), 7,72 (1H, д), 7,31 (1H, д), 7,14 (3H, м), 6,64 (1H, д), 5 (1H, кв.), 3,63 (3H, с), 2,35 (3H, с), 1,37(3H, д) 1 15 ER-886024-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,96 (1H, д), 7,85 (2H, д), 7,19 (2H, д), 6,98 (1H, дт), 6,79 (1H, м), 6,67 (1H, дт), 5,03 (1H, кв.), 3,62 (3H, с), 2,35 (3H, с), 1,38 (3H, д) 1 16 ER-886025-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,83 (3H, м), 7,49 (1H, дд), 7,18 (2H, м), 6,91 (1H, м), 6,53 (1H, дд), 5,01 (1H, кв.), 3,64 (3H, с), 2,34 (3H, с), 1,38 (3H, д) 1 17 ER-886032-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,78 (2H, д), 7,53 (1H, д), 7,24 (1H, т), 7,07 (1H, м), 7,00 (1H, д), 6,72 (2H, м), 4,99 (1H, м), 3,59 (3H, с), 2,35 (3H, с), 2,29 (3H, с), 1,32 (3H, д) 1 18 ER-886033-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,77 (2H, д), 7,47 (1H, д), 7,05 (2H, д), 6,83 (1H, с), 6,52 (2H, с), 5,00 (1H, м), 3,58 (3H, с), 2,35 (3H; с), 2,24 (3H, с), 1,33 (3H, д) 1 19 ER-886035-00 23 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,79 (2H, д), 7,11 (2H, д), 6,29 (1H, т), 6,04 (2H, д), 5,00 (1H, м), 3,71 (6H, с), 3,60 (3H, с), 2,35 (3H, с), 1,36 (3H, д) UA 113499 C2 1 20 ER-886045-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,05 (1H, м), 7,84 (2H, д), 7,32 (1H, т), 7,20 (1H, м), 7,15 (2H, д), 6,96 (3H, м), 4,99 (1H, кв.), 3,75 (3H, с), 1,36 (3H, д) 1 21 ER-886046-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,11 (1H, м), 7,81 (2H, д), 7,52 (2H, м), 7,37 (1H, с), 7,15 (3H, м), 6,96 (1H, м), 4,97 (1H, кв.), 3,76 (3H, с), 1,32 (3H, д) 1 22 ER-886061-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,83 (3H, м), 7,43 (1H, т), 7,12 (3H, м), 6,95 (1H, с), 6,87 (1H, дд), 5,00 (1H, квин.), 3,63 (3H, с), 2,36 (3H, с), 1,33 (3H, д) 1 23 ER-886072-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,56 (1H, д), 7,82 (2H, д), 7,33 (1H, м), 7,18 (2H, д), 6,91 (1H, м), 6,79 (2H, м), 4,95 (1H, м), 3,77 (3H, с), 1,34 (3H, д) 1 24 ER-886073-00 24 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,60 (1H, д), 7,86 (2H, д), 7,19 (3H, м), 6,99 (1H, м), 6,75 (1H, м), 4,97 (1H, м), 3,77 (3H, с), 1,35 (3H, д) UA 113499 C2 1 25 ER-886074-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,61 (1H, д), 7,86 (2H, д), 7,40 (1H, д), 7,22 (1H, д), 7,18 (2H, д), 6,91 (1H, м), 6,89 (1H, дд), 4,96 (1H, м), 3,78 (3H, с), 1,35 (3H, д) 1 26 ER-886077-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,40 (1H, с), 7,81 (2H, д), 7,38 (1H, т), 7,24 (1H, м), 7,06 (3H, м), 6,92 (1H, дд), 3,66 (3H, с), 2,37 (3H, с), 1,24 (2H, м), 0,98 (2H, м) 1 27 ER-886078-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,78 (2H, д), 7,59 (2H, м), 7,44 (1H, с), 7,24 (1H, м), 7,00 (3H, м), 3,80 (3H, с), 1,21 (2H, м), 0,89 (2H, м) 1 28 ER-886080-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,81 (2H, д), 7,77 (1H, д), 7,35 (1H, т), 7,14 (2H, д), 6,95 (1H, м), 6,80 (1H, т), 6,78 (1H, м), 6,73 (1H, м), 5,00 (1H, м), 3,61 (3H, с), 2,35 (3H, с), 1,33 (3H, с) 1 29 ER-886082-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,55 (1H, д), 7,82 (2H, д), 7,34 (1H, т), 7,17 (2H, д), 6,95 (1H, м), 6,83 (1H, т), 6,80 (1H, т), 6,78 (2H, дд), 4,94 (1H, м), 3,76 (3H, с), 3,65 (3H, с), 1,32 (3H, с) 1 30 ER-886083-00 25 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,10 (1H, д), 7,81 (2H, д), 7,52 (2H, м), 7,37 (1H, м), 7,08 (4H, м), 4,97 (1H, кв.), 3,76 (3H, с), 1,32 (3H, д) UA 113499 C2 1 31 ER-886090-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,02 (1H, д), 7,81 (2H, д), 7,36 (1Н, т), 7,15 (2H, д), 6,98 (1H, м), 6,83 (1H, м), 6,81 (1H, т), 6,76 (2H, дд), 4,99 (1H, м), 3,73 (3H, с), 1,34 (3H, с) 1 32 ER-887480-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,01 (1H, д), 7,79 (2H, д), 7,46 (1H, т), 7,36 (1H, д), 7,19 (1H, с), 7,11 (2H, д), 7,06 (1H, м), 6,96 (1H, т), 6,73 (1H, т), 4,95 (1H, м), 3,74 (3H, с), 1,31 (3H, с) 1 33 ER-887495-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,77 (3H, м), 7,46 (1H, т), 7,34 (1H, д), 7,14 (1H, с), 7,10 (1H, д), 7,04 (1H, м), 6,73 (1H, т), 4,97 (1H, кв.), 3,62 (3H, с), 2,35 (3H, с), 1,31 (3H, д) 1 34 ER-887995-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,53 (1H, д), 7,79 (2H, д), 7,43 (1H, т), 7,34 (1H, д), 7,20 (1H, с), 7,13 (2H, д), 7,06 (1H, м), 6,72 (1H, т), 4,91 (1H, м), 3,76 (3H, с), 1,28 (3H, д) 1 35 ER-888024-00 26 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,12 (1H, д), 7,86 (2H, д), 7,44 (1H, д), 7,17 (5H, д), 5,00 (1H, кв.), 3,76 (3H, с), 1,38 (3H, д) UA 113499 C2 1 36 ER-888348-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,65 (1H, с), 7,81 (2H, д), 7,52 (1H, д), 7,30 (1H, д), 7,03 (2H, д), 6,97 (1H, м), 6,91 (1H, т), 3,77 (3H, с), 1,24 (2H, дд), 0,99 (2H, дд) 1 37 ER-888355-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,63 (1H, с), 7,79 (2H, д), 7,38 (1H, т), 7,25 (1H, м), 7,14 (1H, т), 7,03 (2H, д), 6,95 (1H, м), 6,93 (1H, т), 3,77 (3H, с), 1,23 (2H, дд), 0,96 (2H, дд) 1 38 ER-888363-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,81 (2H, д), 7,52 (1H, д), 7,33 (1H, д), 7,06 (2H, д), 7,00 (1H, дд), 3,82 (3H, с), 1,24 (2H, м), 0,95 (2H, м) 1 39 ER-880663-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,83 (2H, с), 7,74 (1H, д), 7,33 (2H, м), 7,13 (2H, д), 6,93 (2H, м), 5,01 (1H, м), 3,62 (3H, с), 2,35 (3H, с), 1,35 (3H, д) 1 40 ER-885302-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,78 (3H, м), 7,05 (6H, м), 5,01 (1H, м), 3,62 (3H, с), 2,35 (3H, с), 1,35 (3H, д) 1 41 ER-885311-00 27 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,75 (5H, м), 7,12 (4H, м), 5,01 (1H, м), 3,63 (3H, с), 2,37 (3H, с), 1,33 (3H, д) UA 113499 C2 1 42 ER-886023-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,83 (2H, м), 7,30 (1H, м), 7,17 (2H, м), 6,95 (1H, м), 6,73 (1H, м), 5,00 (1H, м), 3,63 (3H, с), 2,33 (3H, с), 1,38 (3H, д) 1 43 ER-885749-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,77 (2H, д), 7,54 (1H, д), 7,14 (2H, д), 7,06 (2H, д), 6,80 (2H, д), 4,99 (1H, п), 3,59 (3H, с), 2,34 (3H, с), 2,32 (3H, с), 1,32 (3H, д) 1 44 ER-888365-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,60 (1H, д), 7,81 (2H, д), 7,64 (2H, д), 7,15 (4H, м), 4,94 (1H, м), 3,77 (3H, с), 1,31 (3H, д) 1 45 ER-888367-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,07 (1H, д), 7,81 (2H, д), 7,66 (2H, д), 7,14 (4H, м), 6,96 (1H, т), 4,99 (1H, м), 3,75 (3H, с), 1,34 (3H, д) 1 46 ER-888369-00 H-ЯМР (400 МГц, CD3OD) δ м.д. 8,53 (1H, д), 7,85 (2H, д), 7,30 (2H, д), 7,17 (2H, д), 6,97 (2H, д), 4,95 (1H, м), 3,77 (3H, с), 1,34 (3H, д) 1 47 ER-888371-00 28 H-ЯМР (400 МГц, CD3OD) δ м.д. 7,99 (1H, д), 7,85 (2H, д), 7,33 (2H, д), 7,15 (2H, д), 6,96 (3H, м), 4,99 (1H, м), 3,74 (3H, с), 1,36 (3H, д)
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical composition
Автори англійськоюSpyvee, Mark, Satoh, Takashi, Carlson, Jonathan Eric
Автори російськоюСпайви Марк, Сатох Такаси, Карлсон Джонатан Эрик
МПК / Мітки
МПК: A61K 31/415, C07D 231/20
Мітки: композиція, фармацевтична
Код посилання
<a href="https://ua.patents.su/79-113499-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція</a>
Попередній патент: Фосфінові ліганди для каталітичних реакцій
Наступний патент: Спосіб підвищення родючості піщаних ґрунтів
Випадковий патент: Калійна сіль 5,7-диметил-6-фенілазо-3н-тіазоло[4,5-b]піридин-2-ону, що проявляє антиексудативну дію