Нафталінові сполуки, спосіб їх одержання і фармацевтична композиція, яка їх містить
Номер патенту: 94827
Опубліковано: 10.06.2011
Автори: Міллан Марк, Еттауссі Мохамед, Делагранж Філіпп, Сабауні Ахмед, Юс Саїд, Бертело Паскаль, Кеньяр Данель-Анрі, Спеддінг Мікаель
Формула / Реферат
1. Сполука формули (І):
 , (I)
, (I)
де
R1 являє собою лінійну або розгалужену (С1-С6)алкільну групу, лінійну або розгалужену (С1-С6)алкенільну групу, лінійну або розгалужену (С1-С6)галоалкільну групу, лінійну або розгалужену (С1-С6)полігалоалкільну групу, (С3-С8)циклоалкільну групу, (С3-С8)циклоалкіл-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, арильну групу, арил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, гетероарильну групу або гетероарил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою,
R2 являє собою атом фтору або лінійну чи розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами фтору,
мається на увазі, що:
- "арил" означає фенільну, нафтильну або біфенільну групу,
- "гетероарил" означає будь-яку моно- або біциклічну ароматичну групу, яка містить від 1 до 3 гетероатомів, які вибирають з кисню, сірки або азоту,
арильна і гетероарильна групи, визначені таким чином, можуть бути заміщені від 1 до 3 групами, які вибирають з лінійного або розгалуженого (С1-С6)алкілу, лінійного або розгалуженого (С1-С6)алкокси, гідрокси, карбокси, формілу, нітро, ціано, лінійного або розгалуженого (С1-С6)галоалкілу, лінійного або розгалуженого (С1-С6)полігалоалкілу, алкоксикарбонілу і атомів галогену,
її енантіомери і діастереоізомери, а також її адитивні солі з фармацевтично прийнятною кислотою або основою.
2. Сполука формули (І) за п. 1, в якій R2 являє собою атом фтору, її енантіомери і діастереоізомери, а також її адитивні солі з фармацевтично прийнятною основою.
3. Сполука формули (І) за п. 1, в якій R2 являє собою лінійну або розгалужену (С1-С6)галоалкільну групу, її енантіомери і діастереоізомери, а також її адитивні солі з фармацевтично прийнятною основою.
4. Сполука формули (І) за п. 3, в якій R2 являє собою фторметильну групу або 1-фторетильну групу, її енантіомери і діастереоізомери, а також її адитивні солі з фармацевтично прийнятною основою.
5. Сполука формули (І) за п. 1, яка являє собою N-[3-фтор-2-(7-метокси-1-нафтил)пропіл]ацетамід, а також її адитивні солі з фармацевтично прийнятною основою.
6. Сполука формули (І) за п. 1, яка являє собою N-[4-фтор-2-(7-метокси-1-нафтил)бутил]ацетамід, а також її адитивні солі з фармацевтично прийнятною основою.
7. Спосіб одержання сполуки формули (І), вказаної у п. 1, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II):
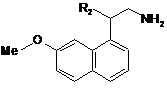 , (II)
, (II)
в якій R2 є таким же, як визначено в п. 1,
яку піддають дії сполуки формули R1COCl, в якій R1 є таким же, як визначено в п. 1, з одержанням сполуки формули (І), яку можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в її адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на її ізомери відповідно до звичайної методики розділення.
8. Спосіб одержання сполуки формули (І), вказаної у п. 1, в якій R2 являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами флору, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (III):
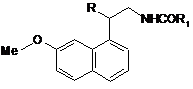 , (III)
, (III)
в якій R1 є таким же, як визначено у п. 1, і R являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену однією або більше ОН-групами,
яку піддають дії метансульфонілхлориду з одержанням сполуки формули (IV):
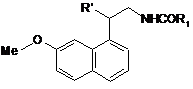 , (IV)
, (IV)
в якій R1 є таким же, як визначено тут вище, і R' являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену однією або більше OSO2Me-групами,
яку піддають дії тетрабутиламонійфториду з одержанням сполуки формули (І/а), окремого випадку сполуки формули (І):
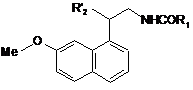 , (І/а)
, (І/а)
в якій R'2 являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами флору,
сполуку формули (І/а) можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в її адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на її ізомери відповідно до звичайної методики розділення.
9. Фармацевтична композиція, яка містить щонайменше одну сполуку формули (І) за будь-яким з пп. 1-6 або її адитивну сіль з фармацевтично прийнятною основою в комбінації з одним або більше фармацевтично прийнятними наповнювачами.
10. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для лікування розладів мелатонінергічної системи.
11. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для лікування розладів сну, стресу, тривоги, глибокої депресії або зимової депресії, серцево-судинних патологій, патологій травної системи, безсоння і втоми через порушення добового ритму організму, шизофренії, гострих тривожних станів з реакцією паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабету, хвороби Паркінсона, старечого недоумства, різних розладів, асоційованих з нормальним або патологічним старінням, мігрені, втрати пам'яті, хвороби Альцгеймера, розладів мозкового кровообігу або статевих дисфункцій, як інгібіторів овуляції або імуномодуляторів або для лікування раку.
Текст
1. Сполука формули (І): O C2 2 (19) 1 3 94827 адитивні солі з фармацевтично прийнятною основою. 5. Сполука формули (І) за п. 1, яка являє собою N[3-фтор-2-(7-метокси-1-нафтил)пропіл]ацетамід, а також її адитивні солі з фармацевтично прийнятною основою. 6. Сполука формули (І) за п. 1, яка являє собою N[4-фтор-2-(7-метокси-1-нафтил)бутил]ацетамід, а також її адитивні солі з фармацевтично прийнятною основою. 7. Спосіб одержання сполуки формули (І), вказаної у п. 1, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): R2 NH2 Me O , (II) в якій R2 є таким же, як визначено в п. 1, яку піддають дії сполуки формули R1COCl, в якій R1 є таким же, як визначено в п. 1, з одержанням сполуки формули (І), яку можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в її адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на її ізомери відповідно до звичайної методики розділення. 8. Спосіб одержання сполуки формули (І), вказаної у п. 1, в якій R2 являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами флору, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (III): R NHCOR1 Me O , (III) в якій R1 є таким же, як визначено у п. 1, і R являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену однією або більше ОН-групами, яку піддають дії метансульфонілхлориду з одержанням сполуки формули (IV): R' NHCOR1 Me 4 в якій R1 є таким же, як визначено тут вище, і R' являє собою лінійну або розгалужену (С1С6)алкільну групу, заміщену однією або більше OSO2Me-групами, яку піддають дії тетрабутиламонійфториду з одержанням сполуки формули (І/а), окремого випадку сполуки формули (І): R'2 NHCOR1 Me O , (І/а) в якій R'2 являє собою лінійну або розгалужену (С1С6)алкільну групу, заміщену одним або більше атомами флору, сполуку формули (І/а) можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в її адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на її ізомери відповідно до звичайної методики розділення. 9. Фармацевтична композиція, яка містить щонайменше одну сполуку формули (І) за будь-яким з пп. 1-6 або її адитивну сіль з фармацевтично прийнятною основою в комбінації з одним або більше фармацевтично прийнятними наповнювачами. 10. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для лікування розладів мелатонінергічної системи. 11. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для лікування розладів сну, стресу, тривоги, глибокої депресії або зимової депресії, серцево-судинних патологій, патологій травної системи, безсоння і втоми через порушення добового ритму організму, шизофренії, гострих тривожних станів з реакцією паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабету, хвороби Паркінсона, старечого недоумства, різних розладів, асоційованих з нормальним або патологічним старінням, мігрені, втрати пам'яті, хвороби Альцгеймера, розладів мозкового кровообігу або статевих дисфункцій, як інгібіторів овуляції або імуномодуляторів або для лікування раку. O , (IV) Даний винахід стосується нових нафталінових сполук, способу їх одержання і фармацевтичних композицій, які їх містять. Сполуки за даним винаходом є новими і мають дуже цінні фармакологічні властивості по відношенню до мелатонінергічних рецепторів. Численні дослідження за останні десять років продемонстрували ключову роль мелатоніну (Nацетил-5-метокситриптамін) у багатьох фізіопатологічних явищах і у контролі циркадних ритмів. Однак, час його півжиття є дуже коротким, завдяки тому факту, що він швидко метаболізується. Таким чином, головна зацікавленість полягає у можливості забезпечення клініциста аналогами мелатоніну, 5 які є метаболічно більш стійкими, мають агоністичний або антагоністичний характер і, як може очікуватись, матимуть терапевтичний вплив, який перевищуватиме вплив самого гормону. В доповнення до їх переважного впливу на розлади циркадних ритмів (J. Neurosurg. 1985, 63, pp. 321-341) і розлади сну (Psychopharmacology, 1990, 100, pp. 222-226), ліганди мелатонінергічної системи мають цінні фармакологічні властивості у відношенні центральної нервової системи, особливо анксіолітичні і антипсихотичні властивості (Neuropharmacology of Pineal Secretions, 1990, 8 (34), pp. 264-272) і анальгетичні властивості (Pharmacopsychiat., 1987, 20, pp. 222-223), а також є корисними при лікуванні хвороби Паркінсона (J. Neurosurg. 1985, 63, pp. 321-341) і хвороби Альцгеймера (Brain Research, 1990, 528, pp. 170-174). Ці сполуки також продемонстрували свою активність відносно певних видів раку (Melatonin -Clinical Perspectives, Oxford University Press, 1988, pp. 164165), овуляції (Science 1987, 227, pp. 714-720), діабету (Clinical Endocrinology, 1986, 24, pp. 359364) і у лікуванні ожиріння (International Journal of Eating Disorders, 1996, 20 (40, pp. 443-446). Ці різні дії викликаються за допомогою посередника специфічних мелатонінових рецепторів. Дослідження молекулярної біології продемонстрували існування числа підтипів рецепторів, які здатні до зв'язування цього гормону (Trends Pharmacol. Sci., 1995, 16, p. 50; WO 97.04094). Для різних видів, включаючи ссавців, можна визначити місцерозташування деяких з цих рецепторів і їх можна охарактеризувати. Для того, щоб краще зрозуміти фізіологічні функції цих рецепторів, дуже переважним було б мати у наявності селективні ліганди. Крім того, такі сполуки, за допомогою селективної взаємодії з одним або іншим з цих рецепторів, можуть бути відмінними ліками для клініциста у лікуванні патологій, асоційованих з мелатонінергічною системою, деякі з них були згадані вище. Крім того факту, що вони є новими, сполуки за даним винаходом проявляють дуже сильну афінність до мелатонінергічних рецепторів. Вони, крім того, мають сильну афінність до 5НТ2С рецептора, який підсилює дію властивостей, які спостерігаються у випадку мелатонінергічних рецепторів, особливо в галузі депресії. Більш конкретно, даний винахід стосується сполук формули (І): в якій: R1 являє собою лінійну або розгалужену (С1С6)алкільну групу, лінійну або розгалужену (С1С6)алкенільну групу, лінійну або розгалужену (С1С6)галоалкільну групу, лінійну або розгалужену (С1-С6)полігалоалкільну групу, (C3С8)циклоалкільну групу, (С3-С8)циклоалкіл-(С1 94827 6 С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, арильну групу, арил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, гетероарильну групу або гетероарил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, R2 являє собою атом флору або лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами флору, мається на увазі, що: - «арил» означає фенільну, нафтильну або біфенільну групу, - «гетероарил» означає будь-яку моно- або біциклічну ароматичну групу, яка містить від 1 до 3 гетероатомів, які вибирають з кисню, сірки або азоту, арильна і гетероарильна групи, визначені таким чином, можуть бути заміщені від 1 до 3 групами, які вибирають з лінійного або розгалуженого (С1-С6)алкілу, лінійного або розгалуженого (С1С6)алкокси, гідрокси, карбокси, формілу, нітро, ціано, лінійного або розгалуженого (С1С6)галоалкілу, лінійного або розгалуженого (С1С6)полігалоалкілу, алкоксикарбонілу і атомів галогену, їх енантіомерів і діастереоізомерів, а також їх адитивних солей з фармацевтично прийнятною кислотою або основою. Серед фармацевтично прийнятних кислот можуть бути згадані, без будь-якого обмеження, наприклад, хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, фосфонова кислота, оцтова кислота, трифтороцтова кислота, молочна кислота, піровиноградна кислота, малонова кислота, янтарна кислота, глутарова кислота, фумарова кислота, винна кислота, малеїнова кислота, лимонна кислота, аскорбінова кислота, щавлева кислота, метансульфонова кислота, камфорна кислота і т.д. Серед фармацевтично прийнятних основ можуть бути згадані, без будь-якого обмеження, гідроксид натрію, гідроксид калію, триетиламін, третбутиламін і т.д. Переважні сполуки даного винаходу являють собою сполуки формули (І), в якій R1 являє собою лінійну або розгалужену (С1-С6)алкільну групу, таку, наприклад, як метальна або етильна група; або (С3-С8)циклоалкільну групу, таку як, наприклад, циклопропільна або циклобутильна група; або полігалоалкільну групу, таку як, наприклад, фторметильна група. Група R2 переважно являє собою атом флору або фторметильну групу або 1-фторетильну групу. Даний винахід більш конкретно стосується сполук, які являють собою N-[2-фтор-2-(7-метокси1-нафтил)етил]ацетамід, N-[2-фтор-2-(7-метокси1-нафтил)-етил]пропанамід, N-[2-фтор-2-(7метокси-1-нафтил)етил]циклопропанкарбоксамід, N-[2-фтор-2-(7-метокси-1нафтил)етил]циклобутанкарбоксамід, N-[3-фтор-2(7-метокси-1-нафтил)пропіл]ацетамід, 2-фтор-N-[3фтор-2-(7-метокси-1-нафтил)пропіл]ацетамід і N[4-фтор-2-(7-метокси-1-нафтил)бутил]ацетамід. Адитивні солі переважних сполук даного вина 7 ходу з фармацевтично прийнятною основою утворюють невід'ємну частину даного винаходу. Винахід стосується також способу одержання сполуки формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): в якій R2 є таким же, як визначено для формули (І), яку піддають дії сполуки формули R1COCl, в якій R1 є таким же, як визначено для формули (І), для одержання сполуки формули (І), яку можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в її адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на її ізомери відповідно до звичайної методики розділення. Переважне втілення стосується способу одержання сполук формули (І), в якій R2 являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше атомами флору, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (III): в якій R1 є таким же, як визначено для формули (І), і R являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену однією або більше OH групами, яку піддають дії метансульфоніл хлориду для одержання сполуки формули (IV): в якій R1 є таким же, як визначено для формули (І), і R' являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену однією або більше OSO2Me групами, яку піддають дії тетрабутиламоній фториду для одержання сполуки формули (І/а), окремого випадку сполук формули (І): в якій R'2 являє собою лінійну або розгалужену (С1-С6)алкільну групу, заміщену одним або більше 94827 8 атомами флору, сполуки формули (І/а) можуть очищувати відповідно до звичайної методики розділення, перетворювати, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою, і розділяти, коли прийнятно, на їх ізомери відповідно до звичайної методики розділення. Сполуки формул (II) і (III) є або комерційно доступними, або можуть бути одержані кваліфікованим фахівцем в даній галузі техніки, використовуючи звичайні хімічні реакції, які розкрито в літературі. Фармакологічне дослідження сполук винаходу показало, що вони є нетоксичними, мають сильну селективну афінність до мелатонінових рецепторів і мають значну активність щодо центральної нервової системи; і, зокрема, терапевтичні властивості щодо розладів сну, антидепресивні, анксіолітичні, антипсихотичні і анальгетичні властивості і властивості відносно мікроциркуляції, що дає можливість встановити, що сполуки за даним винаходом є корисними у лікуванні стресу, розладів сну, тривоги, зимової депресії або глибокої депресії, серцево-судинних патологій, патологій травної системи, безсоння і втоми завдяки порушенню добового ритму організму, шизофренії, гострих тривожних станів з реакцією паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабету, хвороби Паркінсона, старечого недоумства, різних розладів, асоційованих з нормальним або патологічним старінням, мігрені, втрати пам'яті і хвороби Альцгеймера, і розладів мозкового кровообігу. В іншій галузі активності, виявляється що, у лікуванні, сполуки даного винаходу можуть застосовуватись при статевих дисфункціях, що вони мають овуляція-інгібуючі та імуномодулюючі властивості і що вони можуть бути потенційно застосовані у лікуванні раків. Сполуки будуть переважно застосовуватись у лікуванні глибокої депресії, сезонного емоційного розладу, розладів сну, серцево-судинних патологій, патологій травної системи, безсоння і втоми завдяки порушенню добового ритму організму, розладів апетиту і ожиріння. Наприклад, сполуки будуть застосовуватись у лікуванні глибокої депресії, сезонного емоційного розладу і розладів сну. Даний винахід стосується також фармацевтичних композицій, які містять щонайменше одну сполуку формули (І) одну або в комбінації з одним або більше фармацевтично прийнятним наповнювачем. Серед фармацевтичних композицій відповідно до даного винаходу можуть бути згадані більш конкретно ті, які придатні для орального, парентерального, назального, під- або черезшкірного, ректального, через'язикового, очного або респіраторного введення і особливо таблетки або драже, під'язикові таблетки, саше, пакети, капсули, таблетки для повільного розчинення під язиком, таблетки для розсмоктування, супозиторії, креми, мазі, шкірні гелі, і ампули, придатні для пиття або ін'єкцій. Дозування змінюється в залежності від статі, віку і ваги пацієнта, шляху введення, природи те 9 рапевтичного призначення або будь-якого пов'язаного лікування і знаходиться в діапазоні від 0,01 мг до 1 г на 24 години за одне або більше введень. Наступні Приклади ілюструють винахід, але не обмежують його жодним чином. Приклад 1: N-[2-фтор-2-(7-метокси-1нафтил)етил]ацетамід Стадія А: 2-(7-Метокси-1-нафтил)етил метансульфонат 2-(7-Метокси-1-нафтил)етанол (25 ммоль) і триетиламін (30 ммоль) розчиняють у 50 мл дихлорметану і реакційну суміш охолоджують до 0°C, використовуючи льодяну баню. Краплями додають мезил хлорид (30 ммоль) і реакційну суміш перемішують при температурі навколишнього середовища протягом 2 годин і потім вливають у 100 мл води. Органічну фазу промивають IM розчином хлористоводневої кислоти і потім водою, висушують над сульфатом магнію і випаровують. Одержану олію осаджують з суміші діетиловий ефір/петролейний ефір (1/1). Вказаний у заголовку продукт відфільтровують і потім перекристалізовують з діізопропілового ефіру. Точка плавлення: 60-62°С. Стадія В: 7-Метокси-1-вінілнафтален Сполуку, одержану на Стадії А, (21,4 ммоль) розчиняють у 120 мл тетрагідрофурану, і додають невеликими порціями трет-бутилат калію (64,2 ммоль). Після перемішування протягом 30 хвилин при температурі навколишнього середовища рекційну суміш випаровують досуха. Одержаний залишок вміщують у 150 мл води і водну фазу екстрагують двічі 60 мл діетилового ефіру. Органічну фазу промивають водою, висушують над сульфатом магнію, знебарвлюють на рослинному вугіллі і випаровують. Одержаний залишок очищують на силікагелі (елюент: петролейний ефір) для одержання вказаного у заголовку продукту у формі олії жовтого кольору. Стадія С: 1-(2-Бром-1-фторетил)-7метоксинафтален Одержану на Стадії В сполуку (5,4 ммоль) розчиняють у 25 мл дихлорметану і потім одержаний розчин охолоджують до 0°С, використовуючи льодяну баню. Додають триетиламін тригідрофторид (16,3 ммоль) і N-бромсукцинімід (6,5 ммоль). Реакційну суміш перемішують протягом 30 хвилин при 0°C і протягом 12 годин при температурі навколишнього середовища. Реакційну суміш вливають у льодяну воду, нейтралізують 28% аміачним розчином і екстрагують дихлорметаном. Органічну фазу промивають 0,1 M розчином хлористоводневої кислоти, 5% розчином гідрокарбонату натрію і водою. Органічну фазу висушують над сульфатом магнію і розчинник випаровують під зниженим тиском. Одержаний залишок очищують хроматографією на силікагелі (елюент: петролейний ефір/дихлорметан 9/1) для одержання вказаного у заголовку продукту у формі олії коричневого кольору. Стадія D: 1-(2-Азидо-1-фторетил)-7метоксинафтален Азид натрію (15,3 ммоль) суспендують у 10 мл диметилформаміду, додають тетрабутиламоній бромід (200 мг) і суміш нагрівають при 70°C протя 94827 10 гом 30 хвилин. Потім додають одержану на Стадії C сполуку, розчинену у 20 мл диметилформаміду, і суміш перемішують при 70°C протягом 2 годин. В кінці реакції додають воду і водну фазу екстрагують 3 рази, використовуючи 60 мл ефіру. Органічну фазу потім промивають 2 М розчином хлористоводневої кислоти і потім водою, висушують і випаровують під зниженим тиском для одержання вказаного у заголовку продукту у формі олії жовтого кольору. Стадія Е: 2-Фтор-2-(7-метокси-1нафтил)етиламін гідрохлорид Алюміній хлорид (80 ммоль), розчинений у 200 мл безводного ефіру, додають до суспензії алюмогідриду літію (80 ммоль) при 0°C у 300 мл безводного ефіру. Після перемішування протягом 10 хвилин додають одержану на Стадії D сполуку (20 ммоль), розчинену у 200 мл безводного ефіру. Через 30 хвилин суміш гідролізують, в холодному стані і обережно, використовуючи розчин гідроксиду натрію (250 ммоль). Утворений неорганічний осад відфільтровують і промивають рясною кількістю ефіру. Одержаний після випаровування залишок вміщують у воду і водну фазу екстрагують дихлорметаном. Органічну фазу потім промивають водою, висушують і знебарвлюють і потім обробляють газоподібною HCl і випаровують. Одержану олію осаджують з етилацетату і утворений осад відфільтровують відсмоктуванням і потім перекристалізовують. Стадія F: N-[2-фтор-2-(7-метокси-1нафтил)етил]ацетамід Сполуку, одержану на Стадії Е, (20 ммоль) розчиняють у суміші вода/етилацетат (25 мл/75 мл), охолодженій до 0°C Додають карбонат калію (60 ммоль) і потім до реакційної суміші додають краплями ацетил хлорид (26 ммоль). Суміш перемішують енергійно протягом 30 хвилин при температурі навколишнього середовища. Дві фази розділяють і органічну фазу промивають 0,1 М водним розчином хлористоводневої кислоти і потім водою. Після висушування над сульфатом магнію органічну фазу випаровують під зниженим тиском. Одержаний залишок перекристалізовують з суміші толуол/циклогексан (5/5) для одержання вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 128-130°C. % C H N Підраховано: 68,95 6,17 5,36 Знайдено: 68,40 6,14 5,19 Приклад 2: N-[2-Фтор-2-(7-метокси-1нафтил)етил]пропанамід Методика є такою ж, як і у Прикладі 1, заміщуючи ацетил хлорид на СтадіїF на пропаноїл хлорид. Вказаний у заголовку продукт, перекристалізований з циклогексану, одержують у формі твердої речовини білого кольору. Точка плавлення: 13 9-141°C. Елементний мікроаналіз: % C H N Підраховано: 69,80 6,59 5,09 Знайдено: 69,80 6,71 5,12 Приклад 3: N-[2-Фтор-2-(7-метокси-1нафтил)етил]циклопропан-карбоксамід 11 Методика є такою ж, як і у Прикладі 1, заміщуючи ацетил хлорид на Стадії F на циклопропаноїл хлорид. Вказаний у заголовку продукт, перекристалізований з циклогексану, одержують у формі твердої речовини білого кольору. Точка плавлення: 115-117°С. Елементний мікроаналіз: % C H N Підраховано: 71,06 6,31 4,87 Знайдено: 70,91 6,21 4,68 Приклад 4: N-[2-Фтор-2-(7-метокси-1нафтил)етил]циклобутан-карбоксамід Методика є такою ж, як і у Прикладі 1, замішуючи ацетил хлорид на Стадії F на циклобутаноїл хлорид. Вказаний у заголовку продукт, перекристалізований з циклогексану, одержують у формі твердої речовини білого кольору. Точка плавлення: 112-114°С. Елементний мікроаналіз: % C H N Підраховано: 71,74 6,69 4,65 Знайдено: 71,66 6,78 4,51 Приклад 5: N-[3-Фтор-2-(7-метокси-1нафтил)пропіл]ацетамід Стадія А: 3-Аміно-2-(7-метокси-1-нафтил)-1пропанол гідрохлорид Алюміній хлорид (80 ммоль), розчинений у 200 мл безводного ефіру, додають до суспензії алюмогідриду літію (80 ммоль) при 0°C у 300 мл безводного ефіру. Після перемішування протягом 10 хвилин додають метил ціано(7-метокси-1нафтил)ацетат (20 ммоль), розчинений у 200 мл безводного ефіру. Через 30 хвилин суміш гідролізують, в холодному стані і обережно, використовуючи розчин гідроксиду натрію (250 ммоль). Утворений неорганічний осад потім відфільтровують і промивають рясною кількістю ефіру. Одержаний після випаровування залишок вміщують у воду і водну фазу екстрагують дихлорметаном. Органічну фазу потім промивають водою, висушують і знебарвлюють і потім обробляють газоподібною HCl і випаровують. Одержану олію осаджують з етилацетату і утворений осад відфільтровують відсмоктуванням і потім перекристалізовують з ацетонітрилу для одержання вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 164-166°C. Стадія В: N-[3-Гідрокси-2-(7-метокси-1нафтил)пропіл]ацетамід Сполуку, одержану на Стадії А, (20 ммоль) розчиняють у суміші вода/етилацетат (25 мл/75 мл), охолодженій до 0°C Додають карбонат калію (60 ммоль) і потім до реакційної суміші додають краплями ацетил хлорид (26 ммоль). Суміш перемішують енергійно протягом 30 хвилин при температурі навколишнього середовища. Дві фази розділяють і органічну фазу промивають 0,1 М водним розчином хлористоводневої кислоти і потім водою. Після висушування над сульфатом магнію органічну фазу випаровують під зниженим тиском. Одержаний залишок перекристалізовують з ацетонітрилу для одержання вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 136-138°С. 94827 12 Стадія С: 3-(Ацетиламіно)-2-(7-метокси-1нафтил)пропіл метансульфонат Елементний мікроаналіз: Одержану на Стадії В сполуку (10,9 ммоль) розчиняють у 160 мл дихлорметану, додають триетиламін (16,8 ммоль) і розчин охолоджують до 0°С, використовуючи льодяну баню. Потім краплями додають метансульфоніл хлорид (16,8 ммоль) і суміш перемішують при температурі навколишнього середовища протягом 15 хвилин. В кінці реакції суміш вливають у воду і органічну фазу промивають 0,5 М розчином хлористоводневої кислоти, потім 5% розчином гідрокарбонату натрію і водою. Органічну фазу потім висушують і потім випаровують у холодному стані. Одержану після випаровування олію осаджують з ефіру. Одержаний осад відфільтровують відсмоктуванням, але не перекристалізовують, і одержують вказаний у заголовку продукт у формі твердої речовини білого кольору. Точка плавлення: 104-106°С. Стадія D: N-[3-Фтор-2-(7-метокси-1нафтил)пропіл]ацетамід Тетрабутиламоній фторид (25,6 ммоль) додають до розчину сполуки, одержаної на Стадії С, (8,5 ммоль) у 20 мл безводного тетрагідрофурану. Одержаний в результаті розчин перемішують при температурі навколишнього середовища протягом 48 годин. Реакційну суміш вливають у воду і екстрагують двічі 50 мл діетилового ефіру. Органічну фазу висушують над сульфатом магнію. Одержану після випаровування розчинника олію очищують на силікагелі (елюент: ацетон/циклогексан 4/6) для одержання, після перекристалізації з циклогексану, вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 87-89°C. Приклад 6: 2-Фтор-N-[3-фтор-2-(7-метокси-1нафтил)пропіл]ацетамід Стадія А: 3-Аміно-2-(7-метокси-1-нафтил)-1пропанол гідрохлорид Алюміній хлорид (80 ммоль), розчинений у 200 мл безводного ефіру, додають до суспензії алюмогідриду літію (80 ммоль) при 0°C у 300 мл безводного ефіру. Після перемішування протягом 10 хвилин додають метил ціано(7-метокси-1нафтил)ацетат (20 ммоль), розчинений у 200 мл безводного ефіру. Через 30 хвилин суміш гідролізують, в холодному стані і обережно, використовуючи розчин гідроксиду натрію (250 ммоль). Утворений неорганічний осад потім відфільтровують і промивають рясною кількістю ефіру. Одержаний після випаровування залишок вміщують у воду і водну фазу екстрагують дихлорметаном. Органічну фазу потім промивають водою, висушують і знебарвлюють і потім обробляють газоподібною HCl і випаровують. Одержану олію осаджують з етилацетату і утворений осад відфільтровують відсмоктуванням і потім перекристалізовують з ацетонітрилу для одержання вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 164-166°С. Стадія В: 2-Фтор-N-[3-гідрокси-2-(7-метокси-1 13 нафтил)пропіл]ацетамід Сполуку, одержану на Стадії А, (20 ммоль) розчиняють у суміші вода/етилацетат (25 мл/75 мл), охолодженій до 0°С. Додають карбонат калію (60 ммоль) і потім до реакційної суміші додають краплями фторацетил хлорид (26 ммоль). Суміш перемішують енергійно протягом 30 хвилин при температурі навколишнього середовища. Дві фази розділяють і органічну фазу промивають 0,1 M водним розчином хлористоводневої кислоти і потім водою. Після висушування над сульфатом магнію органічну фазу випаровують під зниженим тиском. Одержаний залишок перекристалізовують з діізопропілового ефіру для одержання вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 49-51°C. Стадія C: 3-(Фторацетил)аміно)-2-(7-метокси1-нафтил)пропіл метансульфонат Одержану на Стадії В сполуку (10,9 ммоль) розчиняють у 160 мл дихлорметану, додають триетиламін (16,8 ммоль) і розчин охолоджують до 0°С, використовуючи льодяну баню. Потім краплями додають метансульфоніл хлорид (16,8 ммоль) і суміш перемішують при температурі навколишнього середовища протягом 15 хвилин. В кінці реакції суміш вливають у воду і органічну фазу промивають 0,5 М розчином хлористоводневої кислоти, потім 5% розчином гідрокарбонату натрію і водою. Органічну фазу потім висушують і потім випаровують у холодному стані. Одержану після випаровування олію осаджують з ефіру. Одержаний осад відфільтровують відсмоктуванням, але не перекристалізовують, і одержують вказаний у заголовку продукт у формі твердої речовини білого кольору. Точка плавлення: 122-124°C. Стадія D: 2-Фтор-N-[3-фтор-2-(7-метокси-1нафтил)пропіл]ацетамід Тетрабутиламоній фторид (25,6 ммоль) додають до розчину сполуки, одержаної на Стадії С, (8,5 ммоль) у 20 мл безводного тетрагідрофурану. Одержаний в результаті розчин перемішують при температурі навколишнього середовища протягом 48 годин. Реакційну суміш вливають у воду і екстрагують двічі 50 мл діетилового ефіру. Органічну фазу висушують над сульфатом магнію. Одержану після випаровування розчинника олію очищують на силікагелі (елюент: ацетон/циклогексан 4/6) для одержання, після перекристалізації з циклогексану, вказаного у заголовку продукту у формі твердої речовини білого кольору. Точка плавлення: 82-84°C. Приклад 7: N-[4-Фтор-2-(7-метокси-1нафтил)бутил]ацетамід Сполуку одержують, починаючи з 2-ціано-2-(7метокси-1-нафтил)пропноату відповідно до методики, розкритої на Стадіях A-D Прикладу 5. Точка плавлення: 81-82°C. ФАРМАКОЛОГІЧНІ ДОСЛІДЖЕННЯ Приклад А: Дослідження на гостру токсичність Гостру токсичність оцінюють після орального введення групам, кожна з яких містить 8 мишей (26±2 г). За тваринами спостерігають з регулярни 94827 14 ми проміжками часу протягом першого дня, і щодня протягом двох тижнів після лікування. Оцінюють LD50 (доза, яка викликає смерть 50% тварин) і демонструють низьку токсичність сполук за даним винаходом. Приклад В: Тест примусового плавання Сполуки за даним винаходом досліджують на поведінковій моделі, тест примусового плавання. Апарат складається з плексигласового циліндра, наповненого водою. Тварин досліджують індивідуально протягом сеансу у 6 хвилин. На початку кожного дослідження, тварину вміщують в центр циліндра. Реєструють час, проведений у нерухомому стані. Вважається, що тварина знаходиться у нерухомому стані, коли вона припиняє робити зусилля і залишається нерухомою на поверхні води, роблячи тільки ті рухи, які дозволяють їй тримати голову над водою. Після введення за 40 хвилин до початку дослідження, сполуки за даним винаходом суттєво зменшують час, проведений у нерухомому стані, що вказує на їх антидепресивну активність. Приклад С: Дослідження на зв'язування мелатонінових MT1 і МТ2 рецепторів Експерименти на зв'язування MT1 і MT2 рецеп125 торів проводять, використовуючи 2-[ І]йодмелатонін як посилальний радіоліганд. Радіоактивність, яка зберігається, визначають, використовуючи рідинний сцинтиляційний лічильник. Порівняльні експерименти на зв'язування потім проводять у трьох повторах, використовуючи різні досліджувані сполуки. Діапазон різних концентрацій досліджують для кожної сполуки. Результати дають можливість визначити афінності зв'язування досліджуваних сполук (Кі). Значення Кі, визначені для сполук за даним винаходом, відповідно демонструють зв'язування з однією або іншою з мелатонінергічних ділянок зв'язування, ці значення
ДивитисяДодаткова інформація
Назва патенту англійськоюNaphthalene derivatives, process for the preparation thereof and pharmaceutical compositions containing same
Автори англійськоюYous, Said, Ettaoussi, Mohamed, Cabaouni, Ahmed, Berthelot, Pascal, Spedding, Michael, Delagrange Philippe, Caignard, Daniel-Henri, Millan, Mark
Назва патенту російськоюНафталиновые соединения, способ их получения и фармацевтическая композиция, которая их содержит
Автори російськоюЮс Саид, Эттаусси Мохамед, Сабауни Ахмед, Бертело Паскаль, Спеддинг Микаэль, Делагранж Филипп, Кеньяр Данель-Анри, Миллан Марк
МПК / Мітки
МПК: C07C 233/60, A61K 31/165, A61P 25/00, C07C 233/18
Мітки: спосіб, нафталінові, яка, композиція, фармацевтична, одержання, містить, сполуки
Код посилання
<a href="https://ua.patents.su/8-94827-naftalinovi-spoluki-sposib-kh-oderzhannya-i-farmacevtichna-kompoziciya-yaka-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">Нафталінові сполуки, спосіб їх одержання і фармацевтична композиція, яка їх містить</a>
Попередній патент: Спосіб добування платини з промислових відходів
Наступний патент: Нафталінові сполуки, спосіб їх одержання і фармацевтична композиція, яка їх містить
Випадковий патент: Штамп для висадки головок довгомірних болтів












