a-піримідинтіоалкілзаміщені та a-піримідиноксоалкілзаміщені сполуки
Номер патенту: 56992
Опубліковано: 16.06.2003
Автори: Морріс Джоел, Томас Річард С., Мерфі Майкл Дж., Клік Гарі Дж., Ньюджент Річард А., Шляхтер Стівен Томас, Грейбер Девід Р., Вішка Донн Г.
Формула / Реферат
1. Сполука формули (І)
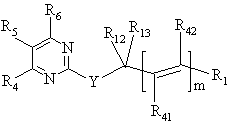 ,
,
(І)
де m дорівнює 0 або 1,
R1 вибраний з
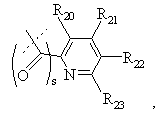
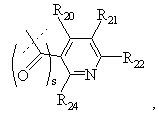
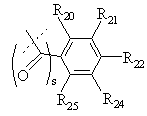 ,
,
де s дорівнює 0 або 1, і R20, R21, R22, R23, R24 і R25 є однаковими або різними й вибрані з Н, С1-С6 алкілу, С1-С6 алкенілу, С1-С6 алкокси, С1-С6 алкілтіо, С3-С8 циклоалкілу, СF3, -NO2, галогену, -ОН, -CN, фенілу, фенілтіо, стирилу, -СО2(R31), -СОN(R31)(R32), -СО(R31), -(СН2)n-N(R31)(R32), -С(ОН)(R31)(R32), -(СН2)n(R31)(CO(R33)) або -(СН2)n-N(R31)(SO2(R33)) або,
де R20 і R21, або R21 і R22, або R22 і R23, узяті разом, утворять п'яти- або шестичленне насичене або ненасичене кільце, що містить 0 або 1 атом кисню, азоту або сірки, де ненасичене кільце може бути необов'язково заміщено 1, 2 або 3 групами, вибраними з С1-С6 алкілу, C1-C6 алкокси, -ОН, -СН2OН, -(CH2)n-N(R31)(R32), С3-C8 циклоалкілу, СF3, галогену, -CO2(R31), -СОN(R31)(R32), -СО(R31), -(СН2)n-N(R31)(СО(R33)), -(CH2)n-N(R31)(SO2(R33)), -CN, -СН2СF3, -СН(СF3)2 або фенілом, і насичене кільце може бути необов'язково заміщено 1, 2 або 3 групами, вибраними з С1-С6 алкілу, С1-С6 алкокси, -ОН, -СН2OН і -(CH2)n-N(R31)(R32), або однією оксогрупою (=O);
де n дорівнює 0-3, і
R31, R32, і R33 є однаковими або різними й вибраними з Н, С1-С6 алкілу, і фенілу, необов'язково заміщеного групами, вибраними з 1, 2 або 3 галогену, С1-С6 алкілу, С1-С6 алкокси, СF3, -ОН або -CN, або,
де R31 і R32, узяті разом з атомом азоту, до якого вони приєднані, утворюють кільце, вибране з піролідинілу, піперидинілу, 4-морфолінілу, 4-тіоморфолінілу, 4-піперазинілу і 4-(1-С1-С6алкіл)піперазинілу, або R1 вибраний із групи, що включає:
1-циклогексеніл, 2-піримідиніл, 4-піримідиніл, 5-піримідиніл, 2-імідазоліл, 4-імідазоліл, 2-бензотіазоліл, 2-бензоксазоліл, 2-бензимідазоліл, 2-оксазоліл, 4-оксазоліл, 2-тіазоліл, 3-ізоксазоліл, 5-ізоксазоліл, 5-метил-3-ізоксазоліл, 5-феніл-3-ізоксазоліл, 4-тіазоліл, 3-метил-2-піразиніл, 5-метил-2-піразиніл, 6-метил-2-піразиніл, 5-хлор-2-тієніл, 3-фурил, бензофуран-2-іл, бензотієн-2-іл, 2Н-1-бензопіран-3-іл, 2,3-дигідробензопіран-5-іл, 1-метилімідазол-2-іл, хіноксалін-2-іл, піперон-5-іл, 4,7-дихлорбензоксазол-2-іл, 4,6-диметилпіримідин-2-іл, 4-метилпіримідин-2-іл, 2,4-диметилпіримідин-6-іл, 2-метилпіримідин-4-іл, 4-метилпіримідин-6-іл, 6-хлорпіперон-5-іл, 5-хлорімідазо[1,2-а]піридин-2-іл, 1-Н-інден-3-іл, 1-Н-2-метилінден-2-іл, 3,4-дигідронафт-1-іл, S-4-ізопропенілциклогексен-1-іл або 4-дигідронафт-2-іл;
R41 і R42; можуть бути однаковими або різними, і вибрані з Н і С1-С4 алкілу;
R12 вибраний із групи, що включає Н, С1-С6 алкіл, С3-С6 циклоалкіл, -CN, -C(O)NH2, -С(O)N(С1-С6алкіл)(С1-С6алкіл), -СО2Н, -СO2(С1-С6алкіл), -CH2OH, -CH2NH2 і СF3;
R13 вибраний з Н, С1-С6алкілу і СF3;
Y вибраний з -S-, -S(O)-, -S(O)2- і -О-;
R4 вибраний з Н, -ОН, галогену -NR15R16, де R15 є Н і R16 є H, C1-C6 алкілом, -NH2, або R15 та R16, узяті разом з атомом азоту утворюють 1-піролідино, 4-морфоліно або 1-піперидино;
R5 вибраний з Н, -С2Н4OН, -С2Н4-O-ТБДМС, галогену, С3-С6 циклоалкілу, С1-С4 алкілу і С1-С3 алкокси; або
R6 вибраний з Н, -ОН, галогену, -CN, СF3, -CO2(R61), -C(O)R61, та -C(O)N(R61)(R62), де R61 та R62 є однаковими або різними й вибрані з Н, С1-С6 алкілу, і фенілу, необов'язково заміщеного 1, 2, або 3 групами, вибраними з галогену, С1-С6 алкілу, С1-С6, алкокси, СF3, -ОН, -CN,
або де R61 і R62, узяті разом з атомом азоту, до якого вони приєднані, утворюють кільце, вибране з піролідинілу, піперидинілу, 4-морфолінілу, 4-тіоморфолінілу, 4-піперазинілу і 4-(С1-С6алкіл)піперазинілу,
при загальній умові, що R4 і R5 не є обидва Н; і що R12 і R13 не є обидва Н, за винятком випадку, коли R6 вибраний з -CN, -СF3, -СО2(R61), -С(O)R61, і -C(O)N(R61)(R62),
або їх фармацевтично прийнятні солі, гідрати, N-оксиди і сольвати; інші ніж
4-аміно-6-хлор-2-(1-(4-(4-морфолінілкарбініл)-2-піридиніл)етил)тіопіримідин;
4-аміно-6-хлор-2-(1-(4-метил-2-піридил)пентил)тіопіримідин;
при загальному виключенні сполук, в яких R1 означає 2- або 3-піридиніл, необов'язково заміщений С1-С4 алкілом, галогеном, -NH2 або -ОН, m дорівнює 0,
Y означає S; R13 означає водень; R12 означає водень або С1-С4 алкіл; R4 означає -NH2; R5 - водень, галоген або С1-С4 алкіл; R6 означає Н, або галоген або -ОН.
2. Сполука за п. 1, яка відрізняється тим, що m дорівнює 0, s дорівнює 0 і Y є -S-.
3. Сполука за п. 2, яка відрізняється тим, що R12 є СН3 і R13 є Н.
4. Сполука за п. 3, яка відрізняється тим, що R4 є -NН2, R5 є Н, і R6 є -Сl, -СF3, або -CN.
5. Сполука за п. 3, де R1 є
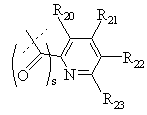 ,
,
де значення R20-R23 і s зазначені вище.
6. Сполука за кожним з пунктів 1-5, де R1 є п'яти- або шестичленним насиченим або ненасиченим кільцем, вибраним із групи, що включає 3-ізохінолініл, 1-ізохінолініл, 2-хінолініл, 3-хінолініл, 3-(5,6,7,8-тетрагідро)ізохінолініл, 1-(5,6,7,8-тетрагідро)ізохінолініл, 2-(5,6,7,8-тетрагідро)хінолініл, 3-(5,6,7,8-тетрагідро)хінолініл, 3-(5,6-дигідро)-2Н-2-піридиніл, 1-(5,6-дигідро)-2Н-2-піридиніл, 2-(5,6-дигідро)-1Н-1-піридиніл, 3-(5,6-дигідро)-1Н-1-піридиніл, 5-фуро[2,3-с]піридиніл, 6-фуро[3,2-с]піридиніл, 4-фуро[3,2-с]піридиніл, 7-фуро[2,3-с]піридиніл, 6-фуро[2,3-b]піридиніл, 5-фуро[3,2-b]піридиніл, 5-(2,3-дигідро)фуро[2,3-с]піридиніл, 6-(2,3-дигідро)фуро[3,2-с]піридиніл, 4-(2,3-дигідро)фуро[3,2-с]піридиніл, 7-(2,3-дигідро)фуро[2,3-с]піридиніл, 6-(2,3-дигідро)фуро[2,3-b]піридиніл, 5-(2,3-дигідро)фуро[3,2-b]-піридиніл, 6-(1,3-дигідро)-фуро[3,4-c]піридиніл, 4-(1,3-дигідро)фуро[3,4-с]піридиніл, 2-(5,7-дигідро)фуро[3,4-b]піридиніл, 6-(3,4-дигідро)-2Н-пірано[2,3-с]піридиніл, 6-(3,4-дигідро)-1Н-пірано[3,4-с]піридиніл, 7-(3,4-дигідро)-1Н-пірано[4,3-с]піридиніл, 7-(3,4-дигідро)-2Н-пірано(3,2-с]піридиніл, 5-(3,4-дигідро)-2Н-пірано[3,2-с]піридиніл, 5-(3,4-дигідро)-1Н-пірано[4,3-с]піридиніл, 8-(3,4-дигідро)-1Н-пірано[3,4-с]піридиніл, 8-(3,4-дигідро)-2Н-пірано[2,3-с]піридиніл, 7-(3,4-дигідро)-2Н-пірано[2,3-b]піридиніл, 2-(5,6-дигідро)-1Н-пірано[3,4-b]піридиніл, 2-(5,6-дигідро)-2Н-пірано[4,3-b]піридиніл, 6-(3,4-дигідро)-2Н-пірано[3,2-b]піридиніл, 5-1Н-піроло[2,3-c]піридиніл, 6-1Н-піроло[3,2-с]піридиніл, 4-1Н-піроло[3,2-с]піридиніл, 7-1Н-піроло-[2,3-с]піридиніл, 6-1Н-піроло[2,3-b]піридиніл, 5-1Н-піроло[3,2-b]піридиніл, 5-(2,3-дигідро)-1Н-піроло[2,3-с]піридиніл, 6-(2,3-дигідро)-1Н-піроло[3,2-с]піридиніл, 4-(2,3-дигідро)-1Н-піроло[3,2-с]піридиніл, 7-(2,3-дигідро)-1Н-піроло[2,3-с]піридиніл, 6-(2,3-дигідро)-1Н-піроло[2,3-b]піридиніл, 5-(2,3-дигідро)-1Н-піроло[3,2-b]піридиніл, 6-(1,3-дигідро)-1Н-піроло[3,4-с]піридиніл, 4-(1,3-дигідро)-1Н-піроло[3,4-с]піридиніл, 2-(5,7-дигідро)-1Н-піроло[3,4-b]піридиніл, 6-1,7-нафтиридиніл, 6-2,7-нафтиридиніл, 7-2,6-нафтиридиніл, 7-1,6-нафтиридиніл, 5-1,6-нафтиридиніл, 5-2,6-нафтиридиніл, 8-2,7-нафтиридиніл, 8-1,7-нафтиридиніл, 7-1,8-нафтиридиніл, 2-1,7-нафтиридиніл, 2-1,6-нафтиридиніл, 6-1,5-нафтиридиніл, 6-(1,2,3,4-тетрагідро)-1,7-нафтиридиніл, 6-(1,2,3,4-тетрагідро)-2,7-нафтиридиніл, 7-(1,2,3,4-тетрагідро)-2,6-нафтиридиніл, 7-(1,2,3,4-тетрагідро)-1,6-нафтиридиніл, 5-(1,2,3,4-тетрагідро)-1,6-нафтиридиніл, 5-(1,2,3,4-тетрагідро)-2,6-нафтиридиніл, 8-(1,2,3,4-тетрагідро)-2,7-нафтиридиніл, 8-(1,2,3,4-тетрагідро)-1,7-нафтиридиніл, 7-(1,2,3,4-тетрагідро)-1,8-нафтиридиніл, 2-(5,6,7,8-тетрагідро)-1,7-нафтиридиніл, 2-(5,6,7,8-тетрагідро)-1,6-нафтиридиніл, 6-(1,2,3,4-тетрагідро)-1,5-нафтиридиніл, 1-нафтил, 2-нафтил, 5-(1,2,3,4-тетрагідро)нафтил, 6-(1,2,3,4-тетрагідро)нафтил, 4-(2,3-дигідро)-1Н-інденіл„ 5-(2,3-дигідро)-1Н-інденіл, 5-бензофураніл, 4-бензофураніл, 6-бензофураніл, 7-бензофураніл, 5-(2,3-дигідро)бензофураніл, 4-(2,3-дигідро)бензофураніл, 6-(2,3-дигідро)бензофураніл, 7-(2,3-дигідро)бензофураніл, 4-(1,3-дигідро)ізобензофуран, 5-(1,3-дигідро)ізобензофуран, 4-1Н-індоліл, 5-1Н-індоліл, 6-1Н-індоліл, 1H-індоліл, 4-(2,3-дигідро)-1Н-індоліл, 5-(2,3-дигідро)-1Н-індоліл, 6-(2,3-дигідро)-1Н-індоліл, 7-(2,3-дигідро)-1Н-індоліл, 4-(1,3-дигідро)-1Н-ізоіндоліл, 5-(1,3-дигідро)-1Н-ізоіндоліл, 5-(3,4-дигідро)-1Н-2-бензопіраніл, 6-(3,4-дигідро)-1Н-2-бензопіраніл, 7-(3,4-дигідро)-1Н-2-бензопіраніл, 8-(3,4-дигідро)-1Н-2-бензопіраніл, 5-(3,4-дигідро)-2Н-1-бензопіраніл, 6-(3,4-дигідро)-2Н-1-бензопіраніл, 7-(3,4-дигідро)-2Н-1-бензопіраніл, 8-(3,4-дигідро)-2Н-1-бензопіраніл, 5-(1,2,3,4-тетрагідро)ізохінолініл, 6-(1,2,3,4-тетрагідро)ізохінолініл, 7-(1,2,3,4-тетрагідро)ізохінолініл, 8-(1,2,3,4-тетрагідро)ізохінолініл, 5-(1,2,3,4-тетрагідро)хінолініл, 6-(1,2,3,4-тетрагідро)хінолініл, 7-(1,2,3,4-тетрагідро)хінолініл, 8-(1,2,3,4-тетрагідро)хінолініл, 5-тієно[2,3-с]піридиніл, 6-тієно[3,2-с]піридиніл, 4-тієно[3,2-с]піридиніл, 7-тієно[2,3-с]піридиніл, 6-тієно[2,3-b]піридиніл, 5-тієно[3,2-b]піридиніл, 5-(2,3-дигідро)тієно[2,3-с]піридиніл, 6-(2,3-дигідро)тієно[3,2-c]піридиніл, 4-(2,3-дигідро)тієно[3,2-с]піридиніл, 7-(2,3-дигідро)тієно[2,3-с]піридиніл, 6-(2,3-дигідро)тієно[2,3-b]піридиніл, 5-(2,3-дигідро)тієно[3,2-b]піридиніл, 6-(1,3-дигідро)тієно[3,4-с]піридиніл, 4-(1,3-дигідро)тієно[3,4-c]піридиніл, 2-(5,7-дигідро)тієно[3,4-b]піридиніл, 6-(3,4-дигідро)-2Н-тіопірано[2,3-с]піридиніл, 6-(3,4-дигідро)-1Н-тіопірано[3,4-с]піридиніл, 7-(3,4-дигідро)-1Н-тіопірано[4,3-с]піридиніл, 7-(3,4-дигідро)-2Н-тіопірано[3,2-с]піридиніл, 5-(3,4-дигідро)-2Н-тіопірано[3,2-с]піридиніл, 5-(3,4-дигідро)-1Н-тіопірано[4,3-с]піридиніл, 8-(3,4-дигідро)-1Н-тіопірано[3,4-с]піридиніл, 8-(3,4-дигідро)-2Н-тіопірано[2,3-с]піридиніл, 7-(3,4-дигідро)-2Н-тіопірано[2,3-b]піридиніл, 2-(5,6-дигідро)-1Н-тіопірано[3,4-b]піридиніл, 2-(5,6-дигідро)-2Н-тіопірано[4,3-b]піридиніл, 6-(3,4-дигідро)-2Н-тіопірано[3,2-b]піридиніл, 5-бензо[b]тіофеніл, 4-бензо[b]тіофеніл-, 6-бензо[b]тіофеніл, 7-бензо[b]тіофеніл, 5-(2,3-дигідро)бензо[b]тіофеніл, 4-(2,3-дигідро)бензо[b]тіофеніл, 6-(2,3-дигідро)бензо[b]тіофеніл, 7-(2,3-дигідро)бензо[b]тіофеніл, 4-(1,3-дигідро)бензо[с]тіофеніл, 5-(1,3-дигідро)бензо[с]тіофеніл, 5-(3,4-дигідро)-1Н-2-бензотіопіраніл, 6-(3,4-дигідро)-1Н-2-бензотіопіраніл, 7-(3,4-дигідро)-1Н-бензотіопіраніл, 8-(3,4-дигідро)-1Н-2-бензотіопіраніл, 5-(3,4-дигідро)-2Н-1-бензотіопіраніл, 6-(3,4-дигідро)-2Н-1-бензотіопіраніл, 7-(3,4-дигідро)-2Н-1-бензотіопіраніл або 8-(3,4-дигідро)-2Н-1-бензотіопіраніл; або таке п'яти- або шестичленне кільце, заміщене 1, 2 або 3 С1-С6 алкілом, С1-С6 алкокси, -ОН, -СН2ОН, -(CH2)n-N(R31)(R32), С3-C8 циклоалкілом, -СF3, галогеном, -СО2(R31), -CON(R31)(R31), -СО(R31), -(CH2)nN(R31)(СО(R33)), -(CH2)nN(R31)(SO2(R33)), -CN, -СН2СF3 або -СН(СF3)2 або фенілом, і насичене кільце може бути необов'язково заміщено 1, 2 або 3 С1-С6 алкілом, С1-С6 алкокси, -ОН, -СН2ОН або -(CH2)n-N(R31)(R32) або однією оксогрупою (=O).
7. Сполука за кожним з пунктів 1-5, де R1 є п'яти- або шестичленним насиченим або ненасиченим кільцем, вибраним із групи, що включає 3-ізохінолініл, 1-ізохінолініл, 2-хінолініл, 3-хінолініл, 3-(5,6,7,8-тетрагідро)ізохінолініл, 1-(5,6,7,8-тетрагідро)ізохінолініл, 2-(5,6,7,8-тетрагідро)хінолініл, 3-(5,6,7,8-тетрагідро)хінолініл, 3-(5,6-дигідро)-2Н-2-піридиніл, 1-(5,6-дигідро)-2Н-2-піридиніл, 2-(5,6-дигідро)-1Н-1-піридиніл, 3-(5,6-дигідро)-1Н-1-піридиніл, 5-фуро[2,3-с]піридиніл, 6-фуро[3,2-с]піридиніл, 4-фуро[3,2-с]піридиніл, 7-фуро[2,3-с]піридиніл, 6-фуро[2,3-b]піридиніл, 5-фуро[3,2-b]піридиніл, 5-(2,3-дигідро)-фуро[2,3-с]піридиніл, 6-(2,3-дигідро)фуро[3,2-с]піридиніл, 4-(2,3-дигідро)фуро[3,2-с]піридиніл, 7-(2,3-дигідро)фуро[2,3-с]піридиніл, 6-(2,3-дигідро)фуро[2,3-b]піридиніл, 5-(2,3-дигідро)фуро[3,2-b]піридиніл, 6-(1,3-дигідро)фуро[3,4-c]піридиніл, 4-(1,3-дигідро)фуро[3,4-с]піридиніл, 2-(5,7-дигідро)фуро[3,4-b]піридиніл, 6-(3,4-дигідро)-2Н-пірано[2,3-с]піридиніл, 6-(3,4-дигідро)-1Н-пірано[3,4-с]піридиніл, 7-(3,4-дигідро)-1Н-пірано[4,3-с]піридиніл, 7-(3,4-дигідро)-2Н-пірано[3,2-с]піридиніл, 5-(3,4-дигідро)-2Н-пірано[3,2-с]піридиніл, 5-(3,4-дигідро)-1Н-пірано[4,3-с]піридиніл, 8-(3,4-дигідро)-1Н-пірано[3,4-с]піридиніл, 8-(3,4-дигідро)-2Н-пірано[2,3-с]піридиніл, 7-(3,4-дигідро)-2Н-пірано[2,3-b]піридиніл, 2-(5,6-дигідро)-1Н-пірано[3,4-b]піридиніл, 2-(5,6-дигідро)-2Н-пірано[4,3-b]піридиніл і 6-(3,4-дигідро)-2Н-пірано[3,2-b]піридиніл або таке п'яти-або шестичленне кільце, заміщене 1, 2 або 3 С1-С6 алкілом, С1-С6 алкокси, -ОН, -СН2OН, -(СН2ОН), -(CH2)n-N(R31)(R32), С3-C8 циклоалкілом, -СF3, галогеном, -СО2(R31), -CON(R31)(R32), -СО(R31), -(СН2)n(R31)(CO(R33)), (CH2)nN(R31)(SO2(R33)), -CN, -СН2СF3 або -СН(СF3)2 або фенілом, і насичене кільце може бути необов'язково заміщене 1, 2 або 3 -С1-С6 алкілом, С1-С6 алкокси, -ОН, -СН2ОН або -(CH2)n-N(R31)(R32) або однією оксогрупою (=O).
8. Сполука за п. 1, вибрана з групи, що включає;
4-аміно-6-хлор-2-(1-(3-ізохінолініл)етил)тіопіримідин,
4-аміно-5-бром-6-хлор-2-(1-(3-ізохіноліл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3-(5,6,7,8-тетрагідроізохіноліл))етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(3-(5,6,7,8-тетрагідроізохіноліл))етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(7-хлорофуро[2,3-с]піримідин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(фуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(фуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(7-хлор-2-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(7-хлор-2-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(2-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(2-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(2,3-дигідрофуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3,3-диметил-2,3-дигідрофуро[2,3-с]піридин-5-іл)етил)тіо-піримідин,
4-аміно-6-хлор-2-(1-(3-етилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(7-хлор-3,3-диметил-2,3-дигідрофуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(7-хлор-3-етилфуро-[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3-(1-метилетил)фуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(4-(1-диметилетил)-2-піридил)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(2-нафтилметил)тіопіримідин,
4-аміно-6-трифторметил-2-((4-(1-метилетил)-2-піридил)метил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(4-(1-метилетил)-2-піридил)етил)тіопіримідин,
4-аміно-6-трифторметил-2-((4-(1,1-диметилетил)-2-піридил)метил)тіопіримідин,
6-аміно-2-(2-нафтилметил)тіо-4-піримідинкарбонітрил,
4-аміно-6-хлор-2-(1-(3-хлорфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3,7-дихлорфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3-бромфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(3-бром-7-хлорфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-хлор-2-(1-(7-хлор-3-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
4-аміно-6-трифторметил-2-(1-(7-хлор-3,3-диметил-2,3-дигідрофуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
(R)-(+)-4-аміно-6-хлор-2-(1-(3-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
(S)-(-)-4-аміно-6-хлор-2-(1-(3-метилфуро[2,3-с]піридин-5-іл)етил)тіопіримідин,
(S)-(-)-4-аміно-6-трифторметил-2-(1-(3-метилфуро[2,3-с]піридин-5-іл)етилтіо)піримідин,
(S)-(-)-4-аміно-6-хлор-2-(1-(фуро[2,3-с]піридин-5-іл)етилтіо)піримідин;
або їх фармацевтично прийнятні солі, гідрати, N-оксиди або сольвати.
Текст
1 Сполука формули (І) де m дорівнює 0 або 1, R1 вибраний з О (О ю де s дорівнює 0 або 1, і R20, R21, R22, R23, R24 і R25 є однаковими або різними й вибрані з Н, С-і-Сє алкілу, С-і-Сб алкенілу, С-і-Сб алкокси, С-і-Сє алкілтю, Сз-Cs циклоалкілу, CF3, -NO2, галогену, -ОН, -CN, фенілу, фенілтю, стирилу, -CO2(R3i), CON(R 3 i)(R 3 2), -CO(R 3 i), -(CH 2 ) n -N(R 3 i)(R32), 56992 або 3 групами, вибраними з галогену, С-і-Сє алкілу, C(OH)(R 3 i)(R32), -(CH 2 )n(R3i)(CO(R 3 3)) або -(CH 2 ) n Сі-С 6 , алкокси, CF 3 , -OH, -CN, N(R 3 i)(SO 2 (R33))a6o, або де R61 і R62, узяті разом з атомом азоту, до де R201 R21, або R21 i R22, або R221 R23, узяті разом, якого вони приєднані, утворюють кільце, вибране з утворять п'яти- або шестичленне насичене або пірол ід инілу, піперидинілу, 4-морфолшілу, 4ненасичене кільце, що містить 0 або 1 атом кисню, тюморфолінілу, 4-піперазинілу і 4-(Сг азоту або сірки, де ненасичене кільце може бути Сбалкіл)піперазинілу, необов'язково заміщено 1, 2 або 3 групами, вибраними з С-і-Сб алкілу, С-і-Сб алкокси, -ОН, при загальній умові, що R4 і Rs не є обидва Н, і що СН 2 ОН, -(CH 2 )n-N(R 3 i)(R32), Сз-С 8 циклоалкілу, CF 3 , R-I2 і R13 не є обидва Н, за винятком випадку, коли галогену, -CO 2 (R 3 i), -CON(R 3 i)(R 3 2), -CO(R 3 i), R6 вибраний з -CN, -CF 3 , -CO 2 (R 6 i), -C(O)R 6 i, і (CH 2 ) n -N(R 3 i)(CO(R33)), -(CH 2 ) n -N(R 3 i)(SO 2 (R 3 3)), C(O)N(R 6 1 )(R 6 2 ), CN, -CH2CF3, -СН(СРз) 2 або фенілом, і насичене або їх фармацевтично прийнятні солі, гідрати, Nкільце може бути необов'язково заміщено 1, 2 або оксиди і сольвати, ІНШІ НІЖ З групами, вибраними з С-і-Сє алкілу, С-і-Сє алкок4-амшо-6-хлор-2-(1-(4-(4-морфолінілкарбшіл)-2си, -ОН, -СН 2 ОН і -(CH 2 ) n -N(R 3 i)(R32), або однією піридиніл)етил)тюпіримідин, оксогрупою (=0), 4-амшо-6-хлор-2-(1 -(4-метил-2де п дорівнює 0-3, і піридил)пентил)тюпіримідин, при загальному виключенні сполук, в яких R1 ознаR31, R32, і R33 є однаковими або різними й вибрачає 2- або 3-піридиніл, необов'язково заміщений ними з Н, С-і-Сб алкілу, і фенілу, необов'язково С1-С4 алкілом, галогеном, -NH 2 або -ОН, m заміщеного групами, вибраними з 1, 2 або 3 галодорівнює 0, гену, С-і-Сб алкілу, С-і-Сб алкокси, CF3, -ОН або CN, або, Y означає S, R-із означає водень, R i 2 означає водень або С1-С4 алкіл, R4 означає -NH 2 , R5 - водень, де R31 і R32, узяті разом з атомом азоту, до якого галоген або С1-С4 алкіл, R6 означає Н, або галоген вони приєднані, утворюють кільце, вибране з піроабо -ОН лідинілу, піперидинілу, 4-морфолшілу, 4тюморфолінілу, 4-піперазинілу і 4-(1-Сг 2 Сполука за п 1, яка відрізняється тим, що m доСбалкіл)піперазинілу, або R1 вибраний із групи, що рівнює 0, s дорівнює 0 і Y є -Sвключає 3 Сполука за п 2, яка відрізняється тим, що R i 2 є CH3iRi3eH 1-циклогексеніл, 2-піримідиніл, 4-піримідиніл, 5піримідиніл, 2-імідазоліл, 4-імідазоліл, 24 Сполука за п 3, яка відрізняється тим, що R4 є бензотіазоліл, 2-бензоксазоліл, 2-бензимідазоліл, NH 2 , R5 є Н, і R6 є -СІ, -CF 3 , або -CN 2-оксазоліл, 4-оксазоліл, 2-тіазоліл, 3-ізоксазоліл, 5 Сполука за п 3, де Ri є 5-ізоксазоліл, 5-метил-З-ізоксазоліл, 5-феніл-Зізоксазоліл, 4-тіазоліл, З-метил-2-піразиніл, 5метил-2-піразиніл, 6-метил-2-піразиніл, 5-хлор-2ТІЄНІЛ, 3-фурил, бензофуран-2-іл, бензотієн-2-іл, 2Н-1-бензопіран-3-іл, 2,3-дипдробензопіран-5-іл, 1-метилімідазол-2-іл, хіноксалін-2-іл, піперон-5-іл, 4,7-дихлорбензоксазол-2-іл, 4,6диметилпіримідин-2-іл, 4-метилпіримідин-2-іл, 2,4диметилпіримідин-6-іл, 2-метилпіримідин-4-іл, 4метилпіримідин-6-іл, 6-хлорпіперон-5-іл, 5хлорімідазо[1,2-а]піридин-2-іл, 1-Н-шден-З-іл, 1-Н2-метилінден-2-іл, 3,4-дипдронафт-1-іл, S-4ізопропенілциклогексен-1-іл або 4-дипдронафт-2іл, R41 і R42, можуть бути однаковими або різними, і вибрані з Н і С1-С4 алкілу, R12 вибраний із групи, що включає Н, С-і-Сє алкіл, Сз-С 6 циклоалкіл, -CN, -C(O)NH 2 , -C(O)N(Cr С 6 алкіл)(Сі-С 6 алкіл), -СО 2 Н, -СО 2 (Сі-С 6 алкіл), СН 2 ОН, - C H 2 N H 2 i C F 3 , R13 вибраний з Н, Сі-Сєалкілу і CF3, Y вибраний з -S-, -S(O)-, -S(O) 2 -1-О-, R4 вибраний з Н, -ОН, галогену -NR15R16, де R15 є Н і R-іб є Н, Сі-Сє алкілом, -NH 2 , або Ris та R-іє, узяті разом з атомом азоту утворюють 1 піролідино, 4-морфолшо або 1-піперидино, R5 вибраний з Н, -С 2 Н 4 ОН, -С 2 Н 4 -О-ТБДМС, галогену, Сз-Сє циклоалкілу, С1-С4 алкілу і С-і-Сз алкокси, або R6 вибраний з Н, -ОН, галогену, -CN, CF3, CO 2 (R 6 i), -C(O)R 6 i, та -C(O)N(R 6 i)(R 6 2), де R 61 та R62 є однаковими або різними й вибрані з Н, С-і-Сє алкілу, і фенілу, необов'язково заміщеного 1, 2, де значення R2o-R231 s зазначені вище 6 Сполука за кожним з пунктів 1 - 5, де Ri є п'ятиабо шестичленним насиченим або ненасиченим кільцем, вибраним із групи, що включає 3ІЗОХІНОЛІНІЛ, 1-ІЗОХІНОЛІНІЛ, 2-ХІНОЛІНІЛ, 3-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)ізохінолшіл, 1-(5,6,7,8тетрапдро)ізохінолшіл, 2-(5,6,7,8тетрапдро)хінолшіл, 3-(5,6,7,8-тетрапдро)хінолшіл, 3-(5,6-дипдро)-2Н-2-піридиніл, 1-(5,6-дипдро)-2Н2-піридиніл, 2-(5,6-дипдро)-1Н-1-піридиніл, 3-(5,6дипдро)-1Н-1-піридиніл, 5-фуро[2,3-с]піридиніл, 6фуро[3,2-с]піридиніл, 4-фуро[3,2-с]піридиніл, 7фуро[2,3-с]піридиніл, 6-фуро[2,3-Ь]піридиніл, 5фуро[3,2-Ь]піридиніл, 5-(2,3-дипдро)фуро[2,3с]піридиніл, 6-(2,3-дипдро)фуро[3,2-с]піридиніл, 4(2,3-дипдро)фуро[3,2-с]піридиніл, 7-(2,3дипдро)фуро[2,3-с]піридиніл, 6-(2,3дипдро)фуро[2,3-Ь]піридиніл, 5-(2,3дипдро)фуро[3,2-Ь]-піридиніл, 6-(1,3-дипдро)фуро[3,4-с]піридиніл, 4-(1,3-дипдро)фуро[3,4с]піридиніл, 2-(5,7-дипдро)фуро[3,4-Ь]піридиніл, 6(3,4-дипдро)-2Н-пірано[2,3-с]піридиніл, 6-(3,4дипдро)-1Н-пірано[3,4-с]піридиніл, 7-(3,4-дипдро)1Н-пірано[4,3-с]піридиніл, 7-(3,4-дипдро)-2Нпірано(3,2-с]піридиніл, 5-(3,4-дипдро)-2Нпірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Н 56992 тієно[3,2-Ь]піридиніл, 5-(2,3-дипдро)тієно[2,3с]піридиніл, 6-(2,3-дипдро)тієно[3,2-с]піридиніл, 4(2,3-дипдро)тієно[3,2-с]піридиніл, 7-(2,3дипдро)тієно[2,3-с]піридиніл, 6-(2,3дипдро)тієно[2,3-Ь]піридиніл, 5-(2,3дипдро)тієно[3,2-Ь]піридиніл, 6-(1,3дипдро)тієно[3,4-с]піридиніл, 4-(1,3дипдро)тієно[3,4-с]піридиніл, 2-(5,7дипдро)тієно[3,4-Ь]піридиніл, 6-(3,4-дипдро)-2Нтюпірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Нтюпірано[3,4-с]піридиніл, 7-(3,4-дипдро)-1Нтюпірано[4,3-с]піридиніл, 7-(3,4-дипдро)-2Нтюпірано[3,2-с]піридиніл, 5-(3,4-дипдро)-2Нтюпірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Нтюпірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Нтюпірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2Нтюпірано[2,3-с]піридиніл, 7-(3,4-дипдро)-2Нтюпірано[2,3-Ь]піридиніл, 2-(5,6-дипдро)-1Нтюпірано[3,4-Ь]піридиніл, 2-(5,6-дипдро)-2Нтюпірано[4,3-Ь]піридиніл, 6-(3,4-дипдро)-2Нтюпірано[3,2-Ь]піридиніл, 5-бензо[Ь]тюфеніл, 4бензо[Ь]тюфеніл-, 6-бензо[Ь]тюфеніл, 7бензо[Ь]тюфеніл, 5-(2,3-дипдро)бензо[Ь]тюфеніл, 4-(2,3-дипдро)бензо[Ь]тюфеніл, 6-(2,3дипдро)бензо[Ь]тюфеніл, 7-(2,3дипдро)бензо[Ь]тюфеніл, 4-(1,3дипдро)бензо[с]тюфеніл, 5-(1,3дипдро)бензо[с]тюфеніл, 5-(3,4-дипдро)-1Н-2бензотюпіраніл, 6-(3,4-дипдро)-1Н-2бензотюпіраніл, 7-(3,4-дипдро)-1 Н-бензотюпіраніл, 8-(3,4-дипдро)-1Н-2-бензотюпіраніл, 5-(3,4дипдро)-2Н-1 -бензотюпіраніл, 6-(3,4-дипдро)-2Н-1 бензотюпіраніл, 7-(3,4-дипдро)-2Н-1бензотюпіраніл або 8-(3,4-дипдро)-2Н-1бензотюпіраніл, або таке п'яти- або шестичленне кільце, заміщене 1, 2 або 3 Сі-Сє алкілом, Сі-Сє алкокси, -ОН, -СН2ОН, -(CH2)n-N(R3i)(R32), C3-C8 циклоалкілом, -CF3, галогеном, -CO2(R3i), CON(R3i)(R3i), -CO(R3i), -(CH2)nN(R31)(CO(R33)), (CH2)nN(R3i)(SO2(R33)), -CN, -CH2CF3 або -CH(CF3)2 або фенілом, і насичене кільце може бути необов'язково заміщено 1, 2 або 3 Сі-Сє алкілом, Сі-Сє алкокси, -ОН, -СН2ОН або -(CH2)n-N(R3i)(R32) або однією оксогрупою (=0) 7 Сполука за кожним з пунктів 1-5, де Ri є п'ятиабо шестичленним насиченим або ненасиченим кільцем, вибраним із групи, що включає 35-1Н-ІНДОЛІЛ, пірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Нпірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2Нпірано[2,3-с]піридиніл, 7-(3,4-дипдро)-2Нпірано[2,3-Ь]піридиніл, 2-(5,6-дипдро)-1Нпірано[3,4-Ь]піридиніл, 2-(5,6-дипдро)-2Нпірано[4,3-Ь]піридиніл, 6-(3,4-дипдро)-2Нпірано[3,2-Ь]піридиніл, 5-1 Н-піроло[2,3-с]піридиніл, 6-1 Н-піроло[3,2-с]піридиніл, 4-1 Н-піроло[3,2с]піридиніл, 7-1 Н-піроло-[2,3-с]піридиніл, 6-1Нпіроло[2,3-Ь]піридиніл, 5-1 Н-піроло[3,2-Ь]піридиніл, 5-(2,3-дипдро)-1Н-піроло[2,3-с]піридиніл, 6-(2,3дипдро)-1Н-піроло[3,2-с]піридиніл, 4-(2,3-дипдро)1 Н-піроло[3,2-с]піридиніл, 7-(2,3-дипдро)-1 Нпіроло[2,3-с]піридиніл, 6-(2,3-дипдро)-1Нпіроло[2,3-Ь]піридиніл, 5-(2,3-дипдро)-1Нпіроло[3,2-Ь]піридиніл, 6-(1,3-дипдро)-1 Нпіроло[3,4-с]піридиніл, 4-(1,3-дипдро)-1 Нпіроло[3,4-с]піридиніл, 2-(5,7-дипдро)-1Нпіроло[3,4-Ь]піридиніл, 6-1,7-нафтиридиніл, 6-2,7нафтиридиніл, 7-2,6-нафтиридиніл, 7-1,6нафтиридиніл, 5-1,6-нафтиридиніл, 5-2,6нафтиридиніл, 8-2,7-нафтиридиніл, 8-1,7нафтиридиніл, 7-1,8-нафтиридиніл, 2-1,7нафтиридиніл, 2-1,6-нафтиридиніл, 6-1,5нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,7нафтиридиніл, 6-(1,2,3,4-тетрапдро)-2,7нафтиридиніл, 7-(1,2,3,4-тетрапдро)-2,6нафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,6нафтиридиніл, 5-(1,2,3,4-тетрапдро)-1,6нафтиридиніл, 5-(1,2,3,4-тетрапдро)-2,6нафтиридиніл, 8-(1,2,3,4-тетрапдро)-2,7нафтиридиніл, 8-(1,2,3,4-тетрапдро)-1,7нафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,8нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,7нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,6нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,5нафтиридиніл, 1-нафтил, 2-нафтил, 5-(1,2,3,4тетрапдро)нафтил, 6-(1,2,3,4-тетрапдро)нафтил, 4-(2,3-дипдро)-1 Н-інденіл,, 5-(2,3-дипдро)-1 Нінденіл, 5-бензофураніл, 4-бензофураніл, 6бензофураніл, 7-бензофураніл, 5-(2,3дипдро)бензофураніл, 4-(2,3дипдро)бензофураніл, 6-(2,3дипдро)бензофураніл, 7-(2,3дипдро)бензофураніл, 4-(1,3дипдро)ізобензофуран, 5-(1,3 дипдро)ізобензофуран, 4-1Н-ІНДОЛІЛ, 6-1 Н-ІНДОЛІЛ, 1 Н-ІНДОЛІЛ, 4-(2,3-дипдро)-1 Н ІНДОЛІЛ, 5-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 6-(2,3-дипдро)1 Н-ІНДОЛІЛ, 7-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 4-(1,3 дипдро)-1 Н-ІЗОІНДОЛІЛ, ІЗОІНДОЛІЛ, 5-(1,3-дипдро)-1 Н 5-(3,4-дипдро)-1Н-2-бензопіраніл, 6 (3,4-дипдро)-1 Н-2-бензопіраніл, 7-(3,4-дипдро)-1 Н2-бензопіраніл, 8-(3,4-дипдро)-1Н-2-бензопіраніл, 5-(3,4-дипдро)-2Н-1-бензопіраніл, 6-(3,4-дипдро)2Н-1-бензопіраніл, 7-(3,4-дипдро)-2Н-1бензопіраніл, 8-(3,4-дипдро)-2Н-1-бензопіраніл, 5(1,2,3,4-тетрапдро)ізохінолшіл, 6-(1,2,3,4тетрапдро)ізохінолшіл, 7-(1,2,3,4тетрапдро)ізохінолшіл, 8-(1,2,3,4тетрапдро)ізохінолшіл, 5-(1,2,3,4тетрапдро)хінолшіл, 6-(1,2,3,4-тетрапдро)хінолшіл, 7-(1,2,3,4-тетрапдро)хінолшіл, 8-(1,2,3,4тетрапдро)хінолшіл, 5-тієно[2,3-с]піридиніл, 6тієно[3,2-с]піридиніл, 4-тієно[3,2-с]піридиніл, 7тієно[2,3-с]піридиніл, 6-тієно[2,3-Ь]піридиніл, 5 ІЗОХІНОЛІНІЛ, 1-ІЗОХІНОЛІНІЛ, 2-ХІНОЛІНІЛ, 3-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)ізохінолшіл, 1-(5,6,7,8тетрапдро)ізохінолшіл, 2-(5,6,7,8тетрапдро)хінолшіл, 3-(5,6,7,8-тетрапдро)хінолшіл, 3-(5,6-дипдро)-2Н-2-піридиніл, 1-(5,6-дипдро)-2Н2-піридиніл, 2-(5,6-дипдро)-1Н-1-піридиніл, 3-(5,6дипдро)-1Н-1-піридиніл, 5-фуро[2,3-с]піридиніл, 6фуро[3,2-с]піридиніл, 4-фуро[3,2-с]піридиніл, 7фуро[2,3-с]піридиніл, 6-фуро[2,3-Ь]піридиніл, 5фуро[3,2-Ь]піридиніл, 5-(2,3-дипдро)-фуро[2,3с]піридиніл, 6-(2,3-дипдро)фуро[3,2-с]піридиніл, 4(2,3-дипдро)фуро[3,2-с]піридиніл, 7-(2,3дипдро)фуро[2,3-с]піридиніл, 6-(2,3дипдро)фуро[2,3-Ь]піридиніл, 5-(2,3дипдро)фуро[3,2-Ь]піридиніл, 6-(1,3дипдро)фуро[3,4-с]піридиніл, 4-(1,3дипдро)фуро[3,4-с]піридиніл, 2-(5,7дипдро)фуро[3,4-Ь]піридиніл, 6-(3,4-дипдро)-2Нпірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Н 56992 пірано[3,4-с]піридиніл, пірано[4,3-с]піридиніл, пірано[3,2-с]піридиніл, пірано[3,2-с]піридиніл, пірано[4,3-с]піридиніл, пірано[3,4-с]піридиніл, пірано[2,3-с]піридиніл, пірано[2,3-Ь]піридиніл, пірано[3,4-Ь]піридиніл, пірано[4,3-Ь]піридиніл 7-(3,4-дипдро)-1Н7-(3,4-дипдро)-2Н5-(3,4-дипдро)-2Н5-(3,4-дипдро)-1Н8-(3,4-дипдро)-1Н8-(3,4-дипдро)-2Н7-(3,4-дипдро)-2Н2-(5,6-дипдро)-1Н2-(5,6-дипдро)-2Н6-(3,4-дипдро)-2Н пірано[3,2-Ь]піридиніл або таке п'яти-або шестичленне кільце, заміщене 1, 2 або 3 С-і-Сє алкілом, Сі-С6 алкокси, -ОН, -СН2ОН, -(СН2ОН), -(СН2)ПN(R3i)(R32), Сз-Cs циклоалкілом, -CF3, галогеном, CO2(R3i), -CON(R3i)(R32), -CO(R3i), (CH2)n(R3i)(CO(R33)), (CH2)nN(R3i)(SO2(R33)), -CN, CH2CF3 або -СН(СРз)2 або фенілом, і насичене кільце може бути необов'язково заміщене 1, 2 або З -С-і-Сб алкілом, С-і-Сб алкокси, -ОН, -СН2ОН або (CH2)n-N(R3i)(R32) або однією оксогрупою (=0) 8 Сполука за п 1, вибрана з групи, що включає, 4-амшо-6-хлор-2-(1 -(3ізохінолшіл)етил)тюпіримідин, 4-амшо-5-бром-6-хлор-2-(1 -(3ізохшоліл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1 -(3-(5,6,7,8тетрапдроізохіноліл))етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(3-(5,6,7,8тетрапдроізохіноліл))етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(7-хлорофуро[2,3-с]піримідин5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(фуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(фуро[2,3-с]піридин5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(7-хлор-2-метилфуро[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(7-хлор-2метилфуро[2,3-с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(2-метилфуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(2-метилфуро[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(3-метилфуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(2,3-дипдрофуро[2,3-с]піридин5-іл)етил)тюпіримідин, Піримідин-тюалкільні та алкілефірні ПОХІДНІ формули ІА можуть застосовуватись при лікуванні пацієнтів, які є ВІЛ-інфікованими, незалежно від того, чи виявляють вони симптоми СНІД у цей час Піримідин-тюалкільні та алкілефірні ПОХІДНІ формули IB можуть використовуватися при одержанні піримідин-тюалкільних та алкілефірних похідних сполук формули ІА Опис рівня техніки Піримідин-тюалкільні піридинові ПОХІДНІ за патентом США 5025016(та ЕР 124630) відповідають загальній формулі 8 4-амшо-6-хлор-2-(1-(3,3-диметил-2,3дипдрофуро[2,3-с]піридин-5-іл)етил)тю-піримідин, 4-амшо-6-хлор-2-(1-(3-етилфуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(7-хлор-3,3-диметил-2,3дипдрофуро[2,3-с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(7-хлор-3-етилфуро-[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1 -(3-(1 -метилетил)фуро[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(4-(1-диметилетил)2-піридил)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(2нафтилметил)тюпіримідин, 4-амшо-6-трифторметил-2-((4-(1-метилетил)-2піридил)метил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(4-(1-метилетил)-2піридил)етил)тюпіримідин, 4-амшо-6-трифторметил-2-((4-(1,1-диметилетил)2-піридил)метил)тюпіримідин, 6-амшо-2-(2-нафтилметил)тю-4піримідинкарбонітрил, 4-амшо-6-хлор-2-(1-(3-хлорфуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(3,7-дихлорфуро[2,3-с]піридин5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(3-бромфуро[2,3-с]піридин-5іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(3-бром-7-хлорфуро[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-хлор-2-(1-(7-хлор-3-метилфуро[2,3с]піридин-5-іл)етил)тюпіримідин, 4-амшо-6-трифторметил-2-(1-(7-хлор-3,3-диметил2,3-дипдрофуро[2,3-с]піридин-5іл)етил)тюпіримідин, (R)-(+)-4-aмlнo-6-xлop-2-(1-(3-мeтилфypo[2,3с]піридин-5-іл)етил)тюпіримідин, (3)-(-)-4-амшо-6-хлор-2-(1-(3-метилфуро[2,3с]піридин-5-іл)етил)тюпіримідин, (3)-(-)-4-амшо-6-трифторметил-2-(1-(3метилфуро[2,3-с]піридин-5-іл)етилтю)піримідин, (3)-(-)-4-амшо-6-хлор-2-(1-(фуро[2,3-с]піридин-5іл)етилтю)піримідин, або їх фармацевтично прийнятні солі, гідрати, Nоксиди або сольвати з-сн де R2-R4, незалежно один від одного, представляють водень, нижчий алкіл, галоген, аміно або пдроксигрупи, Rs представляє вільну електронну пару або нижчу алкільну групу, атом галогену, m дорівнює О або 1, при цьому піримідин-тюалкільна група приєднана за 2-, 3-або 4-позицією піридинового кільця, та їх терапевтично сумісним кислотно 56992 10 активність як протипухлинних сполук при скринінгу щодо пухлинних систем SA-180, СА 755 та L-1210 В J Med Chem 1977, 20, 88 - 92 описано 2алкокси та 2-алкілтю-4-амшопіримідини, включаючи 2-[(фенілметил)тю]4-піримідинамш, 2-[[(4зні 2-[(піридинілметил)тю]піримідинові ПОХІДНІ та їх хлорфеніл)метил]тю]-4-піримідинамш, 2-[(3вплив на бронхосекретолітичні властивості на фепіридинілметил)тю]-4-піримідинамш та 2нольній еритроцитній скринінговій моделі на ми(фенілметокси)-4-піримідинамш, та їх активність як шах порівняно з відомим лікарським засобом амбінгібіторів деоксицитидинкінази ро ксол ом У Collect Czech Chem Comm 1975,40,10781088(CA 83 114326e) описано 5-(3В ЕР 477778[Derwent 92-106190/14] описано йодпропарплокси)піримідини як ефективні фунпсрізні ПОХІДНІ бензолу, піридину та піримідину як татики інгібітори АСАТ ферментів для лікування атеросклерозу та захворювання судин мозку В Synthesis 1981, 397 - 400 описано пероксипіримідини В J Org Chem, 1954, 19, 1793 - 1801 описано піримідинові ПОХІДНІ, включаючи 2B J Org Chem 1961, 26, 1884 описано синтез бензилмеркапто-4-амшо-6-піримідинол, 2азиридинілпіримідинів як аналогів метюприму бензилмеркапто-4-амшо-6-хлорпіримідин, 2В J Med Chem 1991, 34, 315 - 319 описано бензилмеркапто-4-аміно-6-діетиламшопіримідин, а ПОХІДНІ тюурацилу, які мають дипдроксиборильну також аналоги 6-диметиламшопурину групу в С-5-позиціі Ці сполуки можуть застосовуватись при В-нейтронній терапії злоякісної мелаУ патенті Великобританії 744867(СА 51 2063і) номи описано різні 2-R'-5-6-RR'N-3aMim,eHi 4амінопіримідини Суть винаходу Як встановлено, від одного до півтора мільйоЗапропоновано піримідин-тюалкільні та алкіну людей в Сполучених Штатах інфіковані ретролефірні сполуки формули І вірусом людини, вірусом імунодефіциту людини типу І(ВІЛ-1), що є етіологічним агентом набутого синдрому імунодефіциту, СНІДу, дивись Science, 661 - 662(1986) 3 тих, хто є інфікованим, як оцінюється, у двохсот п'ятдесяти тисяч людей, розів'ється СНІД у найближчі п'ять років, дивись Science, 1352 - 1357(1985) 20 Березня 1987 року Адміністрація з продуктів харчування та лікарських засобів США (FDA) схвалила застосування сполуки А2Т(зидовудин) для лікування хворих на СНІД та їх терапевтично/фармацевтично сумісні кипацієнтів з щойно виявленою початковою стадією слотно-адитивні солі плазмоклітинної бронхопневмонії, хворих на СНІД Сполуки, що відповідають формулі І, можуть пацієнтів із станами іншими, ніж плазмоклітинна існувати у різних таутомерних формах та їх вклюбронхопневмонія, або пацієнтів, інфікованих віручено до обсягу формули І, а також формул ІА та сом, з абсолютним ВІДЛІКОМ CD4 меншим за IB 3 200/мм в периферійній крові AZT є відомим інгібіДокладний опис винаходу тором зворотної транскриптази вірусів, ферменту, Запропоновано піримідин-тюалкільні та алкінеобхідного для реплікації вірусу імунодефіциту лефірні сполуки формули І людини адитивним солям Сполуки, як стверджується, виявляють несподівано підвищену бронхосекретолітичну та муколітичну активність, а також, як виявлено, виявляють протизапальну активність YJ Med Chem 1987, ЗО, 547 - 551 описано рі В патенті США 4724232 описано спосіб лікування людей, які мають набутий синдром імунодефіциту, де використовується З'-азидо-З'деокситимідин(азидотимідин, AZT) З літератури відомо, що деякі антибіотики й поліанюнні барвники інгібують зворотну транскриптазу ретровірусів В багатьох публікаціях повідомляється про спроможність різних сульфатованих сполук інгібувати реплікації вірусів, включаючи ВІЛ У Nature 343470 (1990) та Science 250, 1411 (1990) описано сильні інгібітори зворотної транскриптази типу бензодіазепіну Сполуки ВІДПОВІДНО до цього винаходу не є сполуками бензодіазепіновоготипу В J Org Chem 1962, 27, 181 - 185 описано різні 2-бензилтюпіримідинові ПОХІДНІ, включаючи 4хлор-5-метил-2-[(фенілметил)тю(піримідин, 4хлор-5-метил-2-[[(2,4дихлорфеніл)метил]тю]піримідин, 4-хлор-5-метил2-[[(2-хлорфеніл)метил]тю]піримідин та 4-хлор-5метил-2-[[(4-хлорфеніл)метил]тю]піримідин, та їх де m дорівнює 0 чи 1, R1 вибрано з групи, яка складається з -С=СН, CO2R53,CONR54R55, де s дорівнює 0 чи 1 (більш прийнятна 0), та R20, R21, R22, R23, R24 і R25 є однаковими або різни 11 ми та їх вибрано з -Н, Сі-Сєалкілу, Сі-Сєалкенілу, Сі-Сєалкокси, Сі-Сєалкілтю, Сз-Свциклоалкілу, CF3, -NO2, галогену, -ОН, -CN, фенілу, фенілтю, стирилу, - С 0 2 (R 3 i), -CON(R 3 i)(R 3 2), -CO(R 3 i), (CH 2 ) n -N(R 3 i)(R32), -C(OH)(R 3 i)(R 3 3 ), (CH 2 ) n N(R 3 1 )(CO(R 3 3 )), (CH 2 ) n (R 3 i)(SO 2 (R 3 3 )), або, де R2o та R 2 i, чи R 2 i та R22, чи R 22 та R23, узяті разом, утворюють п'яти чи шестичленне насичене або ненасичене кільце, що містить 0 чи 1 атом кисню, азоту або сірки, де ненасичене кільце може бути необов'язково 1, 2 чи 3 заміщено Сі-Сєалкілом, d С 6 алкокси, -ОН, -СН 2 ОН, -(CH 2 ) n -N(R 3 i)(R 3 2 ), -C 3 Свциклоалкілом, -CF 3 , -галогеном, -CO 2 (R 3 i), CON(R 3 1 )(R 3 2 ), -CO(R 3 1 ), -(CH 2 ) n N(R 3 1 )(CO(R 3 3 )), (CH 2 ) n N(R 3 1 )(SO 2 (R 3 3 )), -CN, -CH 2 CF 3 або CH(CF 3 ) 2 , чи фенілом, і насичене кільце може бути необов'язково заміщеним -Сі-Сєалкілом, - С г С 6 алкокси, -ОН, -СН 2 ОН або -(CH 2 ) n N(R 3 i)(R 3 2 ) чи одним оксо (=0), де п дорівнює 0 - 3 та R 3 i, R 32 та R 33 є однаковими чи різними й вибрані з -Н, Сі-Сєалкілу, фенілу, необов'язково заміщеного 1, 2, або 3галогеном, Сі-Сєалкілом, Сі-Сєалкокси, -CF 3 , -OH або -CN, або де R 3 i та R32, узяті разом з азотом, до якого вони приєднані утворюють кільце, вибране з пірол ід инілу, -піперидинілу, -4-морфолшілу, -4тюморфолінілу, -4-піперазинілу, -4-(1-Сг Сбалкіл)піперазинілу, або представника групи, що складається з 1-циклогексенілу, 2-піримідинілу, 4піримідинілу, 5-піримідинілу, 2-імідазолілу, 4імідазолілу, 2-бензотіазолілу, 2-бензоксазолілу, 2бензимідазолілу, 2-оксазолілу, 4-оксазолілу, 2тіазолілу, 3-ізоксазолілу, 5-ізоксазолілу, 5-метил-Зізоксазолілу, 5-феніл-З-ізоксазолілу, 4-тіазолілу, 3метил-2-піразинілу, 5-метил-2-піразинілу, 6-метил2-піразинілу, 5-хлор-2-тієнілу, 3-фурилу, бензофуран-2-ілу, бензотієн-2-ілу, 2Н-1-бензопіран-3-ілу, 2,3-дипдробензопіран-5-ілу, 1-метил имідазол-2ілу, хшоксалін-2-ілу, піперон-5-ілу, 4,7дихлорбензоксазол-2-ілу, 4,6-диметилпіримідин-2ілу/ 4-метилпіримідин-2-ілу, 2,4-диметилпіримідин6-ілу, 2-метилпіримідин-4-ілу, 4-метилпіримідин-6ілу, 6-хлорпіперон-5-ілу, 5-хлоримідазо[1,2а]піридин-2-ілу, 1-Н-шден-З-ілу, 1-Н-2-метилшден2-ілу, 3,4-дипдронафт-1 -илу, S-4ізопропенілциклогексен-1-ілу або 4-дипдронафт-2илу, де R53 вибрано з групи, що складається з -Н, Сі-Сєалкілу, С 3 -СбЦиклоалкілу, фенілу(необов'язково заміщеного 1, 2, або 3 атомами галогену, Сі-Сєалкілами, Сі-Сєалкокси, -CF 3 , -OH, CN), або п'яти- або шестичленного ненасиченого кільця, що містить 0 чи 1 атом кисню, азоту або сірки, де ненасичене кільце може бути необов'язково заміщеним -Н, Сі-Сєалкілом, Сі-Сєалкокси, ОН, -СН 2 ОН, або -(CH 2 ) n -N(R 3 i)(R 3 2 ), Де R54 та R55 є однаковими чи різними, вибраними з -Н, Сі-Сє алкілу, алілу, або фенілу(необов'язково заміщеного 1, 2, або 3 атомами галогену, Сі-Сєалкілами, Сі-Сєалкокси або -CF 3 ), або, узяті разом з атомом азоту, до якого вони приєднані, утворюють кільце, вибране з-поміж 56992 12 пірол ід инілу, -піперидинілу, -4-морфолшілу, -4тюморфолінілу, -4-піперазинілу, -4-(1-Сг Сбалкіл)піперазинілу, R41 та R42 є однаковими або різними, вибраними з групи, що складається з -Н та Сі-С4алкілу, R-I2 вибрано з групи, що складається з -Н, С г Сєалкілу, С 3 -СбЦиклоалкілу, -CN, -C(O)NH 2 , С(О)М(Сі-С 6 алкіл)(Сі-С 6 алкілу), -СО 2 Н, -СО2(СГ С 6 алкілу), -СН 2 ОН, -CH 2 NH 2 або -CF 3 , R-із вибрано з групи, що складається з -Н, d Сєалкілу або CF 3 , Y вибрано з-поміж -S-, -S(0)-, -S(0) 2 або -0-, R4 вибрано з групи, що складається з -Н, -ОН, галогену або -NR15R16, де R15 є -Н, та R-іб є -Н, Сі-Сє алкілом, -NH 2 , або RisTa R16 узяті разом з -N, утворюють 1-піролідино, 4-морфолшо або 1-піперидино, Rs вибрано з групи, що складається з -Н, С 2 Н 4 ОН, -С 2 Н 4 -О-ТБДМС, галогену, -С 3 Сєциклоалкілу, Сі-С 3 алкокси, -СН 2 СН 2 СІ або С1-С4 алкілу, за умови, що Rs не є ізобутилом, або R4 та Rs, узяті разом, утворюють п'ятиабо шестичленне насичене або ненасичене кільце, яке разом з піримідиновим кільцем утворює групу, що виключає 7Н-піроло[2,3-сі]піримідин, 5,6дипдро-7Н-піроло[2,3-сі]піримідин, фуро [2,3сі]піримідин, 5,6-дипдрофуро[2,3-сі]піримідин, тієно[2,3-сі]піримідин, 5,6-дипдротієно[2,3сі]піримідин, 1 Н-піразоло[3,4^]піримідин, 1Нпурин, mpHMiflo[4,5-d]nipHMiflHH, птеридин, піриflo[2,3-d]nipHMiflHH або хіназолін, де ненасичене кільце може бути необов'язково 1, 2 або 3 заміщеним Сі-Сєалкілом, С-і-Сєалкокси, -ОН, -СН 2 ОН, (CH 2 ) n -N(R 3 i)(R 3 2 ), С 3 -С8Циклоалкілом, -CF 3 , галогеном, CO 2 (R 3 i), -CON(R 3 i)(R 3 2 ), -CO(R 3 i ) (CH 2 ) n N(R 3 1 )(CO(R 3 3 )), -(CH 2 ) n N(R 3 1 )(SO(R 3 3 )), Й насичене кільце може бути необов'язково 1, 2 або З заміщеним -Сі-Сєалкілом, -С-і-Сє алкокси, -ОН, СН 2 ОН, або -(CH 2 ) n -N(R 3 i)(R 3 2 ) або одним оксо (=0), та R6 вибрано з групи, що складається з -Н, -ОН, галогену (більш прийнятно, -СІ), -CN, -CF 3 , CO 2 (R 6 i), -C(O)R 6 i або -C(O)N(R 6 i)(R 6 2), де R 61 та R62 є однаковими або різними і вибрані з-поміж -Н, Сі-Сєалкілу, фенілу, необов'язково 1, 2, або 3 заміщеного галогеном, Сі-Сєалкілами, Сі-Сєалкокси, -CF 3 , ОН, -CN, або, де R61 та R62, узяті разом з атомом азоту, до якого вони приєднані, утворюють кільце, вибране з піролідинілу, піперидинілу, 4-морфолшілу, 4-тюморфолінілу, 4-піперазинілу, або 4-(Сі-Сє алкіл) піперазинілу, за загальної умови, що R4 та R6 не є обидва Н, та за такої умови, що і Ri 2 , і R i 3 не є обидва -Н, за винятком випадку, коли R6 вибрано з -CN, -CF 3 , -CO 2 (R 6 i), -C(O)R 6 i або -C(O)N(R 6 i)(R 6 2) або R, вибрано з-поміж -CO 2 Rs 3 обо -C(O)N(Rs4)(Rs5) їх фармацевтично прийнятні солі, гідрати, Nоксиди та сольвати, ІНШІ НІЖ 4-амшо-6-хлор-2-(1-(4-(4-морфолінілкарбшіл)2піридиніл)етил)тюпіримідин або 4-амшо-6-хлор-2-(1 -(4-метил-2піридил)пентил)тю-піримідин 14 13 56992 Втіленням цього винаходу є сполуки формули тетрапдро)хінолшіл, 3-(5,6,7,8-тетрапдро)хінолшіл, ІА, де R-I2 та R-із не є обидва -Н 3-(5,6-дипдро)-2Н-2-піридиніл, 1-(5,6-дипдро)-2Н2-піридиніл, 2-(5,6-дипдро)-1Н-1-піридиніл, 3-(5,6Втіленням цього винаходу є піримідиндипдро)-1Н-1-піридиніл, 5-фуро[2,3-с]піридиніл, 6тюалкільні та алкілефірні анти-СНІД сполуки форфуро[3,2-с]піридиніл, 4-фуро[3,2-с]піридиніл, 7мули ІА, а саме сполуки формули І, де фуро-[2,3-с]піридиніл, 6-фуро[2,3-Ь]піридиніл, 5R4 вибрано з групи, що складається з -Н або фуро[3,2-Ь]піридиніл, 5-(2,3-дипдро)-фуро[2,3NR15R16, де R-I5 є -Н та R-іб є -Н, С-і-Сє алкілом, с]піридиніл, 6-(2,3-дипдро)-фуро[3,2-с]піридиніл, 4NH2, або R15 та Rie узяті разом з -N, утворюють 1(2,3-дипдро)фуро[3,2-с]-піридиніл, 7-(2,3-дипдро)піролідино, 4-морфолшо або 1-піперидино, та фуро[2,3-с]піридиніл, 6-(2,3-дипдро)-фуро[2,3R6 вибрано з групи, що складається з -Н, галоЬ]піридиніл, 5-(2,3-дипдро)-фуро[3,2-Ь]-піридиніл, гену (більш прийнятно, -СІ), -CN, -CF3, -CO2(R6i), 6-(1,3-дипдро)-фуро[3,4-с]піридиніл, 4-(1,3C(O)R6i або -C(O)N(R6i)(R62) дипдро)-фуро[3,4-с]піридиніл, 2-(5,7-дипдро)Сполуки формули IB, а саме сполуки формули фуро[3,4-Ь]піридиніл, 6-(3,4-дипдро)-2Н-пірано[2,3І, Де с]піридиніл, 6-(3,4-дипдро)-1Н-пірано[3,4і) R4 та,або R6 є -ОН, або с]піридиніл, 7-(3,4-дипдро)-1Н-пірано[4,3м) R4Ta R6 обидва є галогеном, с]піридиніл, 7-(3,4-дипдро)-2Н-пірано[3,2можуть використовуватися як проміжні продукс]піридиніл, 5-(3,4-дипдро)-2Н-пірано[3,2ти для одержання піримідин-тюалкільних та алкіс]піридиніл 5-(3,4-дипдро)-1Н-пірано[4,3лефірних анти-СНІД сполук формули ІА с]піридиніл, 8-(3,4-дипдро)-1Н-пірано[3,4Втіленням цього винаходу є сполуки формули І (а також формул ІА та IB), де Y є -Ос]піридиніл, 8-(3,4-дипдро)-2Н-пірано[2,3Більш прийнятним втіленням цього винаходу є с]піридиніл, 7-(3 4-дипдро)-2Н-пірано[2,3сполуки формули І (а також формул ІА та IB), де s є Ь]піридиніл, 2-(5,6-дипдро)-1Н-пірано[3,40, та Y вибрано з групи, що складається з -S-, Ь]піридиніл, 2-(5,6-дипдро)-2Н-пірано[4,3S(O)- або -S(O)2, ще більш прийнятно, Y є -SЬ]піридиніл, 6-(3,4-дипдро)-2Н-пірано[3 2Більш прийнятним втіленням цього винаходу є Ь]піридиніл 5-1 Н-піроло[2,3-с]піридиніл 6-1Нсполуки формули І (а також формул ІА та IB), де s піроло[3,2-с]піридиніл, 4-1Н-піроло[32-с]піридиніл, є 0, та Y вибрано з групи, що складається з -S-, 7-1 Н-піроло[2,3-с]-піридиніл, 6-1 Н-піроло[2,3S(O)- або -S(O)2 (ще більш прийнятно, Y є -S-), та Ь]піридиніл, 5-1Н-піроло[3,2-Ь]піридиніл, 5-(2,3за умови, що R-I2 та R-із обидва не є -Н дипдро)-1Н-піроло[2,3-с]піридиніл, 6-(2,3-дипдро)1 Н-піроло[3,2-с]піридиніл, 4-(2,3-дипдро)-1 НБільш прийнятним втіленням цього винаходу є піроло[3,2-с]піридиніл, 7-(2,3-дипдро)-1Ннові сполуки формули І (а також формул ІА та IB), де s є 0, та Y вибрано з групи, що складається з піроло[2,3-с]піридиніл, 6-(2,3-дипдро)-1НS-, -S(O)- або -S(O)2 (ще більш прийнятно Y є -S-), піроло[2,3-Ь]піридиніл, 5-(2,3-дипдро)-1Нта за умови, що R12 то R-із обидва не є -Н, та за піроло[3 2-Ь]піридиніл 6-(1,3-дипдро)-1 Нтакої умови, що, коли R4 є галогеном або аміно та піроло[3,4-с]піридиніл, 4-(1,3-дипдро)-1 НR6 є галогеном, Ri не є піроло[3,4-с]піридиніл 2-(5,7-дипдро)-1Нпіроло[3,4-Ь]піридиніл, 6-1,7-нафтиридиніл, 6-2,7нафтиридиніл, 7-2,6-нафтиридиніл, 7-1,6нафтиридиніл, 5-1,6-нафтиридиніл, 5-2,6нафтиридиніл, 8-2,7-нафтиридиніл, 8-1,7нафтиридиніл, 7-1,8-нафтиридиніл, 2-1,7нафтиридиніл, 2-1,6-нафтиридиніл, 6-1,5нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,7нафтиридиніл, 6-(1,2,3,4-тетрапдро)-2,7у якому RV представляє водень, нижчий алкіл, нафтиридиніл, 7-(1,2,3,4-тетрапдро)-2,6галоген, аміноабо пдроксигрупи нафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,6R4 більш прийнятно є -NH2нафтиридиніл, 5-(1,2 3,4-тетрапдро)-1,6m більш прийнятно дорівнює 0 нафтиридиніл, 5-(1,2,3,4-тетрапдро)-2,6R6 більш прийнятно є -СІ, -CF3 або -CN нафтиридиніл, 8-(1,2,3,4-тетрапдро)-2,7R41 та R42 є більш прийнятно -Н нафтиридиніл, 8-(1,2,3,4-тетрапдро)-1,7R-I2 є більш прийнятно -СНзнафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,8Ri3 є більш прийнятно -Н нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,7R1 більш прийнятно вибрано з нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,6нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,5нафтиридиніл, 1-нафтил, 2-нафтил, 5-(1,2,3,4тетрапдро)нафтил 6-(1,2,3,4-тетрапдро)нафтил, 4-(2,3-дипдро)-1 Н-інденіл, 5-(2,3-дипдро)-1 Нінденіл, 5-бензофураніл, 4-бензофураніл, 6бензофураніл, 7-бензофураніл, 5-(2,3дипдро)бензофураніл, 4-(2 3дипдро)бензофураніл 6-(2,3ще більш прийнятно, з представника групи, що дипдро)бензофураніл, 7-(2 3включає 3-ІЗОХІНОЛІНІЛ, 1-ізохінолшіл, 2-хінолшіл, дипдро)бензофураніл 4-(1,33-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)ізохінолшіл, 1дипдро)ізобензофуран, 6-(1,3(5,6,7,8-тетрапдро)ізохінолшіл, 2-(5,6,7,8дипдро)ізобензофуран, 4-1Н-ІНДОЛІЛ, 5-1Н-ІНДОЛІЛ, 15 16 56992 с]піридиніл, 7-(2,3-дипдро)-фуро[2,3-с]піридиніл, 6ІНДОЛІЛ 5-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 6-(2 3-дипдро)(2,3-дипдро)-фуро[2,3-Ь]піридиніл, 5-(2,3-дипдро)1 Н-ІНДОЛІЛ, 7-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 4-(1,3фуро[3,2-Ь]піридиніл, 6-(1,3-дипдро)-фуро[3,4дипдро)-1 Н-ІЗОІНДОЛІЛ, 5-(1,3-дипдро)-1 Нс]піридиніл, 4-(1,3-дипдро)-фуро[3,4-с]піридиніл, 2(5,7-дипдро)-фуро[3,4-Ь]піридиніл, 6-(3,4-дипдро)ІЗОІНДОЛІЛ, 5-(3,4-дипдро)-1Н-2-бензопіраніл, 62Н-пірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Н(3,4-дипдро)-1 Н-2-бензопіраніл, 7-(3,4-дипдро)-1 Нпірано[3,4-с]піридиніл, 7-[3,4-дипдро)-1Н2-бензопіраніл, 8-(3,4-дипдро)-1Н-2-бензопіраніл, 5-(3,4-дипдро)-2Н-1-бензопіраніл, 6-(3,4-дипдро)пірано[4,3-с]піридиніл, 7-(3,4-дипдро)-2Н2Н-1-бензопіраніл, 7-(3,4-дипдро)-2Н-1пірано[3,2-с]піридиніл, 5-(3,4-дипдро)-2Нбензопіраніл, 8-(3,4-дипдро)-2Н-1-бензопіраніл, 5пірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Н(1,2,3,4-тетрапдро)-ізохінолшіл, 6-(1,2,3,4пірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Нтетрапдро)-ізохінолшіл, 7-(1,2,3,4-тетрапдро)пірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2НІЗОХІНОЛІНІЛ, 8-(1,2,3,4-тетрапдро)-ізохінолшіл, 5пірано[2,3-с]піридиніл, 7-(3,4-дипдро)-2Н(1,2,3,4-тетрапдро)-хінолшіл, 6-(1,2,3,4пірано[2,3-Ь]піридиніл, 2-(5,6-дипдро)-1Нтетрапдро)-хінолшіл, 7-(1,2,3,4-тетрапдро)пірано[3,4-Ь]піридиніл, 2-(5,6-дипдро)-2НХІНОЛІНІЛ, 8-(1,2,3,4-тетрапдро)-хінолшіл, 5пірано[4,3-Ь]піридиніл або 6-(3,4-дипдро)-2Нтієно[2,3-с]піридиніл, 6-тієно[3,2-с]піридиніл, 4пірано[3,2-Ь]піридиніл, де такий член є необов'язтієно[3,2-с]піридиніл, 7-тієно[2,3-с]піридиніл, 6ково заміщеним, як описано вище тієно[2,3-Ь]піридиніл, 5-тієно[3,2-Ь]піридиніл, 5Представники групи Ri включають (2,3-дипдро)-тієно[2,3-с]піридиніл, 6-(2,3-дипдро)феніл, необов'язково заміщений одним, 2 або тієно[3,2-с]піридиніл, 4-(2,3-дипдро)-тієно[3,2З С1-С4 алкілом, Сі-Сз алкокси, галогеном, Сі-Сз с]піридиніл, 7-(2,3-дипдро)-тієно[2,3-с]піридиніл, 6алкілтю, трифторметилом, Сг-Сє діалкіламшо, або (2,3-дипдро)-тієно-[2,3-Ь]піридиніл, 5-(2,3-дипдро)нітро, 2- чи 3-піридиніл, необов'язково заміщений тієно[3,2-Ь]піридиніл, 6-(1,3-дипдро)-тієно[3,4Сі-Сє алкілом, Сі-Сє алкенілом, Сі-Сє алкокси, С г с]піридиніл, 4-(1,3-дипдро)-тієно-[3,4-с]піридиніл, Сє алкілтю, -Сз-Cs циклоалкілом, -CF3, -NO2, 2-(5,7-дипдро)-тієно[3 4-Ь]піридиніл, 6-(3,4галогеном, -ОН, -CN, фенілом, фенілтю, стирилом, -CO2(R3i), -COH(R3i)(R32), -CO(R3i), дипдро)-2Н-тюпірано[2,3-с]піридиніл, 6-(3,4(CH2)n-N(R3i)(R32), -C(OH)(R3i)(R33), дипдро)-1Н-тюпірано[3,4-с]піридиніл, 7-(3,4дипдро)-1Н-тюпірано-[4,3-с]піридиніл, 7-(3,4(CH2)nN(R3i)(CO(R33)), -(CH2)nN(R3i)(SO2(R33)), надипдро)-2Н-тюпірано[3,2-с]піридиніл, 5-(3,4фтил, необов'язково заміщений одним чи 2 С1-С4 дипдро)-2Н-тюпірано[3,2-с]піридиніл, 5-(3,4алкілом, Сі-Сз алкокси, галогеном, трифторметидипдро)-1Н-тюпірано[4,3-с]піридиніл, 8-(3,4лом, С2-Сє діалкіламшо, Сі-Сз алкілтю або нітро, дипдро)-1Н-тюпірано[3,4-с]піридиніл, 8-(3,4С=СН, а також 3-ІЗОХІНОЛІНІЛ, 1-ізохінолшіл, 2ХІНОЛІНІЛ, 3-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)дипдро)-2Н-тюпірано[2,3-с]піридиніл, 7-(3,4ІЗОХІНОЛІНІЛ 1-(5,6,7,8-тетрапдро)-ізохінолшіл, 2дипдро)-2Н-тюпірано[2,3-Ь]піридиніл, 2-(5,6(5,6,7,8-тетрапдро)-хінолшіл, 3-(5,6,7,8-тетрапдро)дипдро)-1Н-тюпірано[3,4-Ь]піридиніл, 2-(5,6ХІНОЛІНІЛ, 3-(5,6-дипдро)-2Н-2-піриндиніл, 1-(5 6дипдро)-2Н-тюпірано[4,3-Ь]піридиніл, 6-(3,4дипдро)-2Н-2-піриндиніл, 2-(5,6-дипдро)-1Н-1дипдро)-2Н-тюпірано[3,2-Ь]піридиніл, 5піриндиніл, 3-(5,6-дипдро)-1Н-1-піриндиніл, 5бензо[Ь]тюфеніл, 4-бензо[Ь]тюфеніл, 6фуро[2,3-с]піридиніл, 6-фуро[3,2-с]піридиніл, 4бензо[Ь]тюфеніл, 7-бензо[Ь]тюфеніл, 5-(2,3фуро[3,2-с]піридиніл, 7-фуро[2 3-с]піридиніл, 6дипдро)-бензо[Ь]тюфеніл, 4-(2,3-дипдро)фуро[2,3-Ь]піридиніл, 5-фуро[3,2-Ь]піридиніл, 5бензо[Ь]тюфеніл, 6-(2,3-дипдро)-бензо[Ь]тюфеніл, (2,3-дипдро)фуро[2,3-с]піридиніл, 6-(2,3-дипдро)7-(2,3-дипдро)-бензо[Ь]тюфеніл, 4-(1,3-дипдро)фуро[3,2-с]піридиніл, 4-(2,3-дипдро)-фуро[3,2бензо[с]тюфеніл, 5-(1,3-дипдро)-бензо[с]тюфеніл, с]піридиніл, 7-(2,3-дипдро)-фуро[2,3-с]піридиніл, 65-(3,4-дипдро)-1Н-2-бензотюпіраніл, 6-(3,4(2,3-дипдро)-фуро[2,3-Ь]-піридиніл, 5-(2,3-дипдро)дипдро)-1 Н-2-бензотюпіраніл, 7-(3,4-дипдро)-1 Н-2фуро[3,2-Ь]піридиніл, 6-(1,3-дипдро)-фуро[3,4бензотюпіраніл, 8-(3,4-дипдро)-1Н-2с]піридиніл, 4-(1,3-дипдро)-фуро[3,4-с]піридиніл, 2бензотюпіраніл, 5-(3,4-дипдро)-2Н-1(5,7-дипдро)-фуро[3,4-Ь]піридиніл, 6-(3,4-дипдро)бензотюпіраніл, 6-(3,4-дипдро)-2Н-12Н-пірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Нбензотюпіраніл, 7-(3,4-дипдро)-2Н-1пірано[3,4-с]піридиніл, 7-(3,4-дипдро)-1Нбензотюпіраніл, або 8-(3,4-дипдро)-2Н-1бензотюпіраніл, де такий член є необов'язково пірано[4,3-с]піридиніл, 7-(3,4-дипдро)-2Нзаміщеним як описано вище, пірано[3,2-с]піридиніл, 5-(3,4-дипдро)-2Ннайбільш прийнятна, з представника групи, що пірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Нвключає 3-ІЗОХІНОЛІНІЛ, 1-ізохінолшіл, 2-хінолшіл, пірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Н3-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)ізохінолшіл, 1пірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2Н(5,6,7,8-тетрапдро)ізохінолшіл, 2-(5,6,7,8пірано[2,3-с]піридиніл, 7-(3,4-дипдро)-2Нтетрапдро)хінолшіл, 3-(5,6,7,8-тетрапдро)хінолшіл, пірано[2,3-Ь]піридиніл, 2-(5,6-дипдро)-1Н3-(5,6-дипдро)-2Н-2-піриндиніл, 1-(5,6-дипдро)-2Нпірано[3,4-Ь]піридиніл, 2-(5,6-дипдро)-2Н2-піриндиніл, 2-(5,6-дипдро)-1Н-1-піриндиніл, 3пірано[4 3-Ь]піридиніл, 6-(3,4-дипдро)-2Н(5,6-дипдро)-1Н-1~піриндиніл, 5-фуро[2,3пірано[3 2-Ь]піридиніл, 5-1 Н-піроло[2,3-с]піридиніл, 6-1 Н-піроло[3,2-с]піридиніл, 4-1 Н-піроло[3,2с]піридиніл, 6-фуро[3,2-с]піридиніл, 4-фуро[3,2с]піридиніл, 7-1 Н-піроло[2,3-с]піридиніл, 6-1Нс]піридиніл, 7-фуро[2,3-с]піридиніл, 6-фуро[2,3піроло[2,3-Ь]піридиніл, 5-1 Н-піроло[3,2-Ь]піридиніл, Ь]піридиніл, 5-фуро[3,2-Ь]піридиніл, 5-(2,35-(2,3-дипдро)-1 Н-піроло[2,3-с]піридиніл, 6-(2,3дипдро)фуро[2,3-с]піридиніл, 6-(2,3-дипдро)дипдро)-1 Н-піроло[3,2-с]піридиніл 4-(2 3-дипдро)фуро[3,2-с]піридиніл, 4-(2,3-дипдро)фуро[3,26-1 Н-ІНДОЛІЛ, 7-1 Н-ІНДОЛІЛ, 4-(2 3-дипдро)-1 Н 56992 18 17 1 Н-піроло[3,2-с]-піридиніл, 7-(2,3-дипдро)-1Нтюпірано[2 3-с]піридиніл 7-(3 4-дипдро)-2Нпіроло[2,3-с]піридиніл, 6-(2,3-дипдро)-1Нтюпірано[2,3-Ь]піридиніл, 2-(5 6-дипдро)-1 Нпіроло[2,3-Ь]піридиніл, 5-(2,3-дипдро)-1НтюпІрано[3,4-Ь]піридиніл, 2-(5,6-дипдро)-2Нпіроло[3,2-Ь]піридиніл, тюпірано[4 3-Ь]піридиніл, 6-(3,4-дипдро)-2Н6-(1,3-дипдро)-1Нпіроло[3,4-с]піридиніл, тюпірано[3,2-Ь]піридиніл, 5-бензо[Ь]тюфеніл, 44-(1,3-дипдро)-1Нбензо-[Ь]тюфеніл, 6-бензо[Ь]тюфеніл 7піроло[3,4-с]піридиніл, 2-(5,7-дипдро)-1Нбензо[Ь]тюфеніл, 5-(2 3-дипдро)-бензо[Ь]тюфеніл піроло[3,4-Ь]піридиніл, 6-1,7-нафтиридиніл, 6-2,74-(2 3-дипдро)-бензо[Ь]тюфеніл 6-(2,3-дипдро)нафтиридиніл, 7-2,6-нафтиридиніл, 7-1,6бензо[Ь]тюфеніл, 7-(2 3-дипдро)-бензо[Ь]-тюфеніл нафтиридиніл, 5-1,6-нафтиридиніл, 5-2,64-(1,3-дипдро)-бензо[с]-тюфеніл, 5-(1,3-дипдро)нафтиридиніл, 8-2,7-нафтиридиніл, 8-1,7бензо[с]-тюфеніл, 5-(3 4-дипдро)-1 Н-2нафтиридиніл, 7-1,8-нафтиридиніл, 2-1,7нафтиридиніл, 2-1,6-нафтиридиніл, 6-1,5бензотюпіраніл, 6-(3,4-дипдро)-1Н-2нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,7бензотюпіраніл, 7-(3 4-дипдро)-1 Н-2нафтиридиніл, 6-(1,2,3,4-тетрапдро)-2,7бензотюпіраніл, 8-(3,4-дипдро)-1Н-2нафтиридиніл, 7-(1,2,3,4-тетрапдро)-2,6бензотюпіраніл, 5-(3,4-дипдро)-2Н-1нафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,6бензотюпіраніл, 6-(3,4-дипдро)-2Н-1нафтиридиніл, 5-(1,2,3,4-тетрапдро)-1,6бензотюпіраніл, 7-(3,4-дипдро)-2Н-1нафтиридиніл, 5-(1,2,3,4-тетрапдро)-2,6бензотюпіраніл, 8-(3 4-дипдро)-2Н-1нафтиридиніл, 8-(1,2,3,4-тетрапдро)-2,7бензотюпіраніл, нафтиридиніл, 8-(1,2,3,4-тетрапдро)-1,7або представника групи, що включає 4ХІНОЛІНІЛ, 5-ХІНОЛІНІЛ, 6-ХІНОЛІНІЛ, 7-ХІНОЛІНІЛ, 8нафтиридиніл, 7-(1,2,3,4-тетрапдро)-1,8ХІНОЛІНІЛ, 1-циклогексеніл, 2-піримідиніл, 4нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,7піримідиніл, 5-піримідиніл, 2-імідазоліл, 4нафтиридиніл, 2-(5,6,7,8-тетрапдро)-1,6імідазоліл, 2-бензотіазоліл, 2-бензоксазоліл, 2нафтиридиніл, 6-(1,2,3,4-тетрапдро)-1,5бензимідазоліл, 2-оксазоліл, 4-оксазоліл, 2нафтиридиніл, 1-нафтил, 2-нафтил, 5-(1,2,3,4тіазоліл, 3-ізоксазоліл, 5-ізоксазоліл, 5-метил-Зтетрапдро)нафтил, 6-(1,2,3,4-тетрапдро)нафтил, ізоксазоліл, 5-феніл-З-ізоксазоліл, 4-тіазоліл 34-(2,3-дипдро)-1 Н-інденіл, 5-(2,3-дипдро)-1 Нметил-2-піразиніл, 5-метил-2-пиразиніл, 6-метил-2інденіл, 5-бензофураніл, 4-бензофураніл, 6піразиніл, 5-хлор-2-тієніл, 3-фурил, бензофуран-2бензофураніл, 7-бензофураніл, 5-(2,3-дипдро)іл, бензотієн-2-іл, 2Н-1-бензопіран-3-іл, 2,3бензофураніл, 4-(2,3-дипдро)-бензофураніл, 6дипдробензопіран-5-іл, 2,3-дипдробензофуран-2(2,3-дипдро)-бензофураніл, 7-(2,3-дипдро)іл, 1-метилімідазол-2-іл, хіноксалін-2-іл, ІЗОХІНОЛІНбензофураніл, 4-(1,3-дипдро)-ізобензофуран, 53-іл, піперон-5-іл, 4,7-дихлорбензоксазол-2-іл, 4,6(1,3-дипдро)-ізобензофуран, 4-1 Н-індоліл, 5-1Ндиметилпіримідин-2-іл, 4-метилпіримідин-2-іл, 2,4шдоліл, 6-1Н-ШД0ЛІЛ, 7-1Н-індоліл, 4-(2,3-дипдро)диметилпіримідин-6-іл, 2-метилпіримідин-4-іл, 41 Н-ІНДОЛІЛ, 5-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 6-(2,3метилпіримідин-6-іл, 6-хлорпіперон-5-іл, 5дипдро)-1 Н-ІНДОЛІЛ, 7-(2,3-дипдро)-1 Н-ІНДОЛІЛ, 4хлоримідазо[1,2-а]піридин-2-іл, 1-Н-інден-З-іл, 1-Н(1,3-дипдро)-1 Н-ІЗОІНДОЛІЛ, 5-(1,3-дипдро)-1 Н2-метилінден-2-іл, 3,4-дипдронафт-1-ил, S-4ІЗОІНДОЛІЛ, 5-(3,4-дипдро)-1Н-2-бензопіраніл, 6ізопропенілциклогексен-1-іл та 4-дипдронафт-2(3,4-дипдро)-1 Н-2-бензопіраніл, 7-(3,4-дипдро)-1 Нил 2-бензопіраніл, 8-(3,4-дипдро)-1Н-2-бензопіраніл, 5-(3,4-дипдро)-2Н-1-бензопіраніл, 6-(3,4-дипдро)Нові альфа-заміщені піримідин-тюалкільні 2Н-1-бензопіраніл, 7-(3,4-дипдро)-2Н-1сполуки формули І включають сполуки, де Ri не є 2- або 3-піридинілом, необов'язково заміщеним d бензопіраніл, 8-(3,4-дипдро)-2Н-1-бензопіраніл, 5С4 алкілом, атомом галогену, NH2 або -ОН, коли m (1,2,3,4-тетрапдро)-ізохінолшіл, 6-(1,2,3,4дорівнює О, Y є S, R-із є -Н, R12 є -Н або С1-С4 алтетрапдро)-ізохінолшіл, 7-(1,2,3,4-тетрапдро)кілом, R4 є -Н, -ОН, галогеном або NH2, Rs є -Н, ІЗОХІНОЛІНІЛ, 8-(1,2,3,4-тетрапдро)-ізохінолініл, 5галогеном або С1-С4 алкілом, та R6 вибрано з гру(1,2,3,4-тетрапдро)-хінолшіл, 6-(1,2,3,4пи, що складається з -Н, галогену або -ОН тетрапдро)-хінолшіл, 7-(1,2,3,4-тетрапдро)ХІНОЛІНІЛ, 8-(1,2,3,4-тетрапдро)-хінолініл, 5Більш прийнятні нові альфа-заміщені піримітієно[2,3-с]піридиніл, 6-тієно[3,2-с]піридиніл, 4дин-тюалкільні та алкілефірні анти-СНІД сполуки тієно[3,2-с]піридиніл, 7-тієно[2,3-с]піридиніл, 6формули ІА включають сполуки, де Y є S та m дотієно[2,3-Ь]піридиніл, 5-тієно[3,2-Ь]піридиніл, 5рівнює 0 (2,3-дипдро)-тієно[2,3-с]піридиніл, 6-(2,3-дипдро)Такі більш прийнятні нові альфа-заміщені пітієно[3,2-с]піридиніл, 4-(2,3-дипдро)-тієно[3,2римідин-тюалкільні та алкілефірні анти-СНІД спос]піридиніл, 7-(2,3-дипдро)-тієно[2,3-с]піридиніл, 6луки формули ІА включають сполуки, де Y є S, m (2,3-дипдро)-тієно[2,3-Ь]піридиніл, 5-(2,3-дипдро)дорівнює 0, R-I2 є СНз та R13 є -Н тієно[3,2-Ь]піридиніл, 6-(1,3-дипдро)-тієно[3,4Такі більш прийнятні нові альфа-заміщені піс]піридиніл, 4-(1 3-дипдро)-тієно[34-с]піридиніл 2римідин-тюалкільні та алкілефірні анти-СНІД спо(5 7-дипдро)-тієно[34-Ь]піридиніл, 6-(3,4-дипдро)луки формули ІА включають сполуки, де Y є S, m 2Н-тюпірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Ндорівнює 0, R-I2 є СНз Ri3 є -Н, R4 є NH2, Rs є -Н, та тюпірано[3,4-с]піридиніл, 7-(3,4-дипдро)-1НR6 є-СІ, CF 3 a6oCN тюпірано[4,3-с]піридиніл, 7-(3 4-дипдро)-2НЩе більш прийнятні нові альфа-заміщені піримідин-тюалкільні та алкілефірні анти-СНІД сполуки тюпірано-[32-с]піридиніл 5-(3,4-дипдро)-2Нформули ІА включають сполуки, де Y є S, m дорівтюпірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Ннює 0, s дорівнює 0, R-I2 є СНз, R13 є -Н, R4 є NH2, тюпірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Нтюпірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2Н 19 Rs є -H, F 6 є -СІ, CF3 або CN, та ? пи, яка складається з 56992 вибрано з гру 20 тетрапдро)-2,7-нафтиридинілу, тетрапдро)-2,6-нафтиридинілу, тетрапдро)-1,6-нафтиридинілу, тетрапдро)-1,6-нафтиридинілу, тетрапдро)-2,6-нафтиридинілу, тетрапдро)-2,7-нафтиридинілу, тетрапдро)-1,7-нафтиридинілу, тетрапдро)-1,8-нафтиридинілу, тетрапдро)-1,7-нафтиридинілу, тетрапдро)-1,6-нафтиридинілу, тетрапдро)-1,5-нафтиридинілу, 7-(1,2,3,47-(1,2,3,45-( 1,2,3,45-(1,2,3,48-(1,2,3,48-(1,2,3,47-(1,2,3,42-(5,6,7,82-(5,6,7,86-(1,2,3,41-нафтилу, 2 Найбільш прийнятні нові альфа-заміщені піримідин-тюалкільні та алкілефірні анти-СНІД сполуки формули ІА включають сполуки, де Y є S, m дорівнює 0, s дорівнює 0, R12 є СНЗ, R13 є, R4 є NH2, R5 є -Н, R6 є -СІ, CF3 або CN, та R1 вибрано з групи, що складається з 3-ізохінолшілу, 1ізохшолінілу, 2-хшолшілу, 3-хінолшілу, 3-(5,6,7,8тетрапдро)-ізохінолшілу, 1-(5,6,7,8-тетрапдро)ізохшолінілу, 2-(5,6,7,8-тетрапдро)-хінолшілу, 3(5,6,7,8-тетрапдро)-хінолшілу, 3-(5,6-дипдро)-2Н-2піриндинілу, 1-(5,6-дипдро)-2Н-2-піриндинілу, 2(5,6-дипдро)-1Н-1-піриндинілу, 3-(5,6-дипдро)-1Н1-піриндинілу, 5-фуро[2,3-с]піридинілу, 6-фуро[3,2с]піридинілу, 4-фуро[3,2-с]піридинілу, 7-фуро[2,3с]піридинілу, 6-фуро[2,3-Ь]піридинілу, 5-фуро[2,3Ь]піридинілу, 5-[2,3-дипдро)-фуро-[2,3 нафтилу, 5-0,2,3,4-тетрапдро)нафтилу, 6-0,2,3,4тетрапдро)нафтилу, 4-(2,3-дипдро)-1Н-шденілу, 5(2,3-дипдро)-1Н-шденілу, 5-бензофуранілу, 4бензофуранілу, 6-бензофуранілу, 7бензофуранілу,5-(2,3-дипдро)-бензофуранілу, 4(2,3-дипдро)-бензофуранілу, 6-(2,3-дипдро)бензофуранілу, 7-(2,3-дипдро)-бензофуранілу, 4(1,3-дипдро)-ізобензофурану, 5-(1,3-дипдро)ізобензофурану, 4-1Н-шдолілу, 5-1Н-шдолілу, 61 Н-індолілу, 7-1 Н-індолілу, 4-(2,3-дипдро)-1 Ніндолілу, 5-(2,3-дипдро)-1 Н-індолілу, 6-(2 3дипдро)-1 Н-індолілу, 7-(2,3-дипдро)-1 Н-індолілу, 4-0,3-дипдро)-1 Н-ізоіндолілу, 5-(1,3-дипдро)-1 Нізоіндолілу, 5-(3,4-дипдро)-1 Н-2-бензопіранілу, 6(3,4-дипдро)-1Н-2-бензопіранілу, 7-(3,4-дипдро)1 Н-2-бензопіранілу, 8-(3,4-дипдро)-1 Н-2 с]піридинілу, 6-(2,3-дипдро)-фуро[3,2-с]піридинілу, 4-(2,3-дипдро)фуро[3,2-с]піридинілу, 7-(2,3дипдро)фуро[2,3-с]піридинілу, 6-(2,3дипдро)фуро[2,3-Ь]піридинілу, 5-(2,3-дипдро)фуро[3,2-Ь]піридинілу, 6-(1,3-дипдро)-фуро[3,4-с]піридинілу, 4-(1,3-дипдро)-фуро[3,4-с]піридинілу, 2-(5,7-дипдро)-фуро[3,4-Ь]піридинілу, 6-(3,4дипдро)-2Н-пірано[2,3-с]піридинілу, 6-(3,4дипдро)-1Н-пірано[3,4-с]піридинілу, 7-(3,4дипдро)-1Н-пірано[4,3-с]піридинілу, 7-(3,4дипдро)-2Н-пірано[3,2-с]піридинілу, 5-(3,4дипдро)-2Н-пірано[3,2-с]піридинілу, 5-(3,4дипдро)-1Н-пірано[4,3-с]-піридинілу, 8-(3,4дипдро)-1Н-пірано[3,4-с]піридинілу, 8-(3,4дипдро)-2Н-пірано[2,3-с]піридинілу, 7-(3,4дипдро)-2Н-пірано[2,3-Ь]піридинілу, 2-(5,6дипдро)-1Н-пІрано[3,4-Ь]-піридинілу, 2-(5,6дипдро)-2Н-пірано[4,3-Ь]піридинілу, 6-(3,4дипдро)-2Н-пірано[3,2-Ь]піридинілу 5-1Нпіроло[2,3-с]піридинілу, 6-1Н-піроло[3,2с]піридинілу, 4-1 Н-пІроло-[3,2-с]піридинілу, 7-1Нпіроло[2,3-с]піридинілу, 6-1Н-піроло[2,3Ь]піридинілу, 5-1Н-піроло[3,2-Ь]піридинілу, 5-(2,3дипдро)-1Н-піроло[2,3-с]піридинілу, 6-(2,3дипдро)-1Н-піроло[3,2-с]піридинілу, 4-(2,3дипдро)-1Н-піроло[3,2-с]піридинілу, 7-(2,3дипдро)-1Н-піроло[2,3-с]піридинілу, 6-(2,3дипдро)-1Н-піроло[2,3-Ь]піридинілу, 5-(2,3дипдро)-1 Н-піроло[3,2-Ь]піридинілу, 6-(1,3дипдро)-1 Н-піроло[3,4-с]піридинілу, 4-(1,3дипдро)-1Н-піроло[3,4-с]піридинілу, 2-(5,7дипдро)-1 Н-піроло[3,4-Ь]піридинілу, 6-1,7нафтиридинілу, 6-2,7-нафтиридинілу, 7-2,6нафтиридинілу, 7-1,6-нафтиридинілу, 5-1,6нафтиридинілу, 5-2,6-нафтиридинілу, 8-2,7нафтиридинілу, 8-1,7-нафтиридинілу, 7-1,8нафтиридинілу, 2-1,7-нафтиридинілу, 2-1,6нафтиридинілу, 6-1,5-нафтиридинілу, 6-(1,2,3,4тетрапдро)-1,7-нафтиридинілу, 6-(1,2,3,4 бензопіранілу, 5-(3,4-дипдро)-2Н-1-бензопіранілу, 6-(3,4-дипдро)-2Н-1 -бензопіранілу, 7-(3,4-дипдро)2Н-1 -бензопіранілу, 8-(3,4-дипдро)-2Н-1 бензопіранілу, 5-0,2,3,4-тетрапдро)-ізохінолшу, 60,2,3,4-тетрапдро)-ізохінолшілу, 7-0,2,3,4тетрапдро)-ізохінолшілу, 8-0,2,3,4-тетрапдро)ізохшолінілу, 5-0,2,3,4-тетрапдро)-хінолшілу, 60,2,3,4-тетрапдро)-хінолшілу, 7-0,2,3,4тетрапдро)-хінолшілу, 8-0,2,3,4-тетрапдро)хінолінілу, 5-тієно[2,3-с]піридинілу, 6-тієно[3,2с]піридинілу, 4-тієно[3,2-с]піридинілу, 7-тієно-[2,3с]-піридинілу, 6-тієно[2,3-Ь]піридинілу, 5-тієно[3,2Ь]-піридинілу, 5-(2,3-дипдро)-тієно[2,3-с]піридинілу, 6-(2,3-дипдро)-тієно[3,2-с]піридинілу, 4-(2,3дипдро)-тієно[3,2-с]піридинілу, 7-(2,3-дипдро)тієно[2,3-с]піридинілу, 6-(2,3-дипдро)-тієно[2,3Ь]піридинілу, 5-(2,3-дипдро)-тієно[3,2-Ь]піридинілу, 6-0,3-дипдро)-тієно[3,4-с]піридинілу, 4-0,3дипдро)-тієно[3,4-с]піридинілу, 2-(5,7-дипдро)тієно[3,4-Ь] піридинілу, 6-(3,4-дипдро)-2Нтюпірано[2,3-с]піридинілу, 6-(3,4-дипдро)-1 Нтюпірано[3,4-с]піридинілу, 7-(3,4-дипдро)-1 Нтюпірано[4,3-с]піридинілу, 7-(3 4-дипдро)-2Нтюпірано[3,2-с]піридинілу, 5-(3,4-дипдро)-2Нтюпірано[3,2-с]піридинілу, 5-(3,4-дипдро)-1 Нтюпірано[4,3-с]піридинілу, 8-(3,4-дипдро)-1 Нтюпірано[3,4-с]піридинілу, 7-(3,4-дипдро)-2Нтюпірано[2,3-Ь]піридинілу, 2-(5,6-дипдро)-1 Нтюпірано[3,4-Ь]піридинілу, 2-(5,6-дипдро)-2Нтюпірано[4,3-Ь]піридиніл, 6-(3,4-дипдро)-2Нтюпірано[3,2-Ь]піридинілу, 5-бензо[Ь]тюфенілу, 4бензо[Ь]тюфенілу, 6-бензо[Ь]тюфенілу, 7бензо[Ь]тюфенілу, 5-(2,3-дипдро)бензо[Ь]тюфенілу, 4-(2,3-дипдро)бензо[Ь]тюфенілу, 6-(2,3-дипдро)бензо[Ь]тюфенілу, 7-(2 3-дипдро)бензо[Ь]тюфенілу 4-0,3-дипдро)бензо[с]тюфенілу, 5-(1,3-дипдро)бензо[с]тюфенілу, 5-(3,4-дипдро)-1 Н-2 21 56992 бензотюпіранілу, 6-(3,4-дипдро)-1Н-2бензотюпіранілу, 7-(3,4-дипдро)-1Н-2бензотюпіранілу, 8-(3,4-дипдро)-1Н-2бензотюпіранілу, 5-(3,4-дипдро)-2Н-1 бензотюпіранілу, 6-(3,4-дипдро)-2Н-1бензотюпіранілу, 7-(3 4-дипдро)-2Н-1бензотюпіранілу, 8-(3,4-дипдро)-2Н-1бензотюпіранілу, найбільш прийнятне, представника групи, яка включає 3-ІЗОХІНОЛІНІЛ, 1-ізохінолшіл, 2-хінолшіл, 3-ХІНОЛІНІЛ, 3-(5,6,7,8-тетрапдро)ізохінолшіл, 1 (5,6,7,8-тетрапдро)-ізохінолшіл, 2-(5,6,7,8тетрапдро)-хінолшіл, 3-(5,6,7,8-тетрапдро)ХІНОЛІНІЛ, 3-(5,6-дипдро)-2Н-2-піриндиніл, 1-(5,6дипдро)-2Н-2-піриндиніл, 2-(5,6-дипдро)-1Н-1піриндиніл, 3-(5,6-дипдро)-1Н-1-піриндиніл, 5фуро[2,3-с]піридиніл, 6-фуро[3,2-с]піридиніл, 4фуро[3,2-с]піридиніл, 7-фуро[2,3-с]піридиніл, 6фуро[2,3-Ь]піридиніл, 5-фуро[3,2-Ь]піридиніл, 5(2,3-дипдро)фуро[2,3-с]піридиніл, 6-(2,3дипдро)фуро[3,2-с]піридиніл, 4-(2,3дипдро)фуро[3,2-с]-піридиніл, 7-(2,3дипдро)фуро[2,3-с]піридиніл, 6-(2,3дипдро)фуро[2,3-Ь]піридиніл, 5-(2,3дипдро)фуро[3,2-Ь]-піридиніл, 6-(1,3дипдро)фуро[3,4-с]піридиніл, 4-(1,3дипдро)фуро[3,4-с]піридиніл, 2-(5,7дипдро)фуро[3,4-Ь]піридиніл, 6-(3,4-дипдро)-2Нпірано[2,3-с]піридиніл, 6-(3,4-дипдро)-1Нпірано[3,4-с]піридиніл, 7-(3,4-дипдро)-1Нпірано[4,3-с]піридиніл, 7-(3,4-дипдро)-2Нпірано[3 2-с]піридиніл, 5-(3,4-дипдро)-2Нпірано[3,2-с]піридиніл, 5-(3,4-дипдро)-1Нпірано[4,3-с]піридиніл, 8-(3,4-дипдро)-1Н-пірано[3,4-с]піридиніл, 8-(3,4-дипдро)-2Н-пірано[2,3с]піридиніл, 7-(3,4-дипдро)-2Н-пірано[2,3Ь]піридиніл, 2-(5,6-дипдро)-1Н-пірано[3,4Ь]піридиніл, 2-(5,6-дипдро)-2Н-пірано[4,3-Ь]піридиніл, 6-(3,4-дипдро)-2Н-пірано[3,2Ь]піридиніл Піримідин-тюалкільні сполуки формули І як правило та найбільш часто одержують шляхом взаємодії 2-меркаптопіримідину з ВІДПОВІДНИМ алкілувальним агентом, наприклад, мезилатом або галогенідом Дивись, наприклад, схему А Коли Ri2Ta R-із є різними, сполуки формули І(а також ІА та IB) виділяють у вигляді рацемічної суміші, і вона містить R та S ізомери, що їх може бути виділено з рацемічної суміші за допомогою ВЕРХ з використанням колонки з хіральною фазою, такої як Chiralcel OD-H, елююванням ВІДПОВІДНОЮ сумішшю розчинників, такою як, ізопропанол/гексан RTa S ізомери сполуки формули І(коли R-I2 та R-із є різними) можуть бути одержані з ВІДПОВІДНОГО хірального галогеніду(або мезилату) II (дивись схему В) ВІДПОВІДНИЙ хіральний галогенід(або мезилат) II одержують з хірального спирту IV ВІДПОВІДНИЙ хіральний спирт IV можна одержати з ВІДПОВІДНОГО кетону V, використовуючи хіральний відновний агент, такий як (+) або (-)дмзопінокамфеїлхлорборан або ІНШІ хіральні ВІДНОВНІ агенти, ВІДОМІ з літератури ВІДПОВІДНИЙ хі ральний спирт IV також одержують шляхом розділення рацемічного спирту VII шляхом ферментативного гідролізу ВІДПОВІДНОГО ацетату VI ВІДПОВІДНИМ ферментом, таким як PS-30 амінолі 22 паза або L1754, тип VII, з candidae cylmdracea чи ІНШІ ферменти, ВІДОМІ з літератури ВІДПОВІДНИЙ хіральний спирт IV також одержують шляхом розділення рацемічного спирту VII ферментативною етерифікацією(такою як ацетилювання чи бутилювання) рацемічного спирту УІІ(одержуючи хіральну сполуку VIII), використовуючи ВІДПОВІДНИЙ фермент, такий як ліпаза з підшлункової залози свині, тип II, або ІНШІ ферменти, ВІДОМІ З літератури Альфа-заміщені піримідин-тюалкільні та алкілефірні сполуки формули І включають сполуки Прикладів 193 - 291 Більш прийнятними є антиСНІД сполуки за Прикладами 230, 231, 233, 234, 237, 238, 239, 240, 241, 242, 243, 246, 247, 248, 249, 250, 251, 252, 256, 269, 270, 271, 272, 273, 277, 194, 199, 203, 207, 282, 283, 284, 285, 286, 287, 289, 290, 297, 299, та більш прийнятно, 237, 238, 239, 246, 289, 290, 297, 299, та ще більш прийнятно, 290, 297, 299, та їх солі(наПрикпад, 302, 306 та 301) Піримідин-тюалкільні та алкілефірні сполуки формули І утворюють кислотно-адитивні солі, такі як мезилат, пдрохлорид, пдробромід, пдройодид, сульфат, фосфат, ацетат, пропюнат, лактат, малеат, малат, сукцинат, тартрат і таке інше Деякі з можливих взаємозамінних замісників є кислотними і як такі утворюють основно-адитивні солі, коли взаємодіють з достатньо сильними основами Фармацевтично прийнятні солі включають солі як неорганічних, так і органічних основ Більш прийнятні фармацевтично прийнятні солі включають солі таких основ, наприклад, гідроксиду амонію, трометамшу(ТНАМ), 2-амшо-2-(пдроксиметил)-1,3пропандюлу ВІДПОВІДНІ катіони включають, наПриклад, натрій, калій, кальцій та магній Піримідин-тюалкільні та алкілефірні анти-СНІД сполуки формули ІА можуть використовуватися як інгібітори зворотної транскриптази вірусів, ферменту необхідного для реплікації вірусу імунодефіциту людини, і тому можуть використовуватися при лікуванні таких захворювань, як СНІД Термін ретровірус людини(РВЛ) означає вірус імунодефіциту людини типу І або його штами, очевидні для фахівця у цій галузі, що належать до цих самих родин вірусів, та які викликають фізіологічні ефекти у людей, подібно до різних ретровірусів людини Пацієнти, які підлягають лікуванню, включають тих індивідуумів, котрі(1) інфіковані одним чи кількома штамами ретровірусу людини, що визначається за наявністю або вимірюваної КІЛЬКОСТІ антитіл до вірусу, або антигенів у сироватці крові, та(2) мають або визначену за симптомами СНІДінфекцію, таку як (а) дисемшований пстоплазмоз, (Ь) ізопсоріаз, (с) бронхіальний та легеневий кандідоз, включаючи плазмоклітинну пневмонію, (d) лімфому, відмінну від лімфоми Ходжкіна, або (є) саркому Капоши, та вік яких менший за 60 років, або котрі мають абсолютний ВІДЛІК CD4 лімфоцитів в периферійній крові менший від 200/мм3 Сполуки формули ІА можуть вводитися перорально ПІДХОЖІ стандартні лікарські форми включають таблетки, капсули, суспензії, розчини та еліксири Ефективна КІЛЬКІСТЬ становить від приблизно 0,1 до приблизно 500мг/кг/день Типова стандартна доза для людини вагою 70кг повинна 24 23 56992 становити від приблизно Юмг до приблизно папері DE81, промивання паперу для вилучення 2000мг, більш прийнятно, від приблизно ЮОмг до незв'язаного попередника, сушіння та визначальприблизно ЮООмг, що вводяться від одного до ного підрахунку Результати(ІСбо означає концентшести разів на день рацію, ліки в мкМ, необхідну для інгібування активності зворотної транскриптази(Р236І_ й дикого Точна доза та частота введення такою мірою, типу) до ступеня в 50%) різних аналізів об'єднують як це добре відомо фахівцям у цій галузі, залежать та представляють як % інгібування та/або від конкретної сполуки, що її застосовують, форІС5о(розраховано) в таблиці 1(Р236І_) та таблиці мули ІА, конкретного стану, який необхідно виліку2(дикий тип) вати, тяжкості стану, який необхідно вилікувати, віку, ваги, загального фізичного стану конкретного Позначення та визначення пацієнта, іншого медикаментозного лікування інВизначення та пояснення нижче стосуються дивідуума, може здійснюватись та може визначатермінів, що використовуються у всьому документися більш точно шляхом визначення рівня у крові ті, включаючи як опис, так і формулу винаходу або концентрації сполук формули ІА в крові паціє1 Визначення для формул та позначення для нта та/або реакції пацієнта відносно конкретного змінних стану, що підлягає лікуванню ХІМІЧНІ формули, які представляють різні сполуки й молекулярні фрагменти в описі та у формуПацієнти, що мають позитивну реакцію на ВІЛ, лі винаходу, можуть містити взаємозамінні замісале не мають симптомів, як правило можуть лікуники, окрім чітко визначених структурних ознак Ці ватися більш низькими пероральними дозами(від взаємозамінні замісники вказано літерою або літеприблизно 0,2 до приблизно ІООмг/кг/день) Пацієрою з подальшим нижнім індексом, наприклад, нти з АРС(комплекс, пов'язаний зі СНІД) та зі СНІ"Zi" або "R|", де "і" є цілим числом Ці взаємозамінДом мають як правило лікуватися за допомогою ні замісники є або одновалентними, або двоваленбільш високих пероральних доз(від приблизно 1 тними, тобто вони являють собою групу, зв'язану зі до приблизно 500мг/кг/день) сполуками цієї формули за допомогою однієї або Піримідин-тюалкільні та алкілефірні анти-СНІД двох ХІМІЧНИХ зв'язків Наприклад, група Zi може сполуки формули ІА ВІДПОВІДНО до цього винаходу представляти двовалентну змінну, якщо вона приможуть використовуватись у поєднанні(або послієднана до сполуки формули CH3-C(=Zi)H Групи R, довно) з іншими антивірусними агентами, такими та R| можуть представляти одновалентні взаємояк AZT, ddl, ddC, з ненуклеозидними анти-СНІД замінні замісники, якщо вони приєднані до сполуки агентами, такими як ті, що їх описано в формули CH3-CH2-C(R,)(R|)H Коли ХІМІЧНІ форму[№08,400095, касета 4788 1, СР, подано 7 березня ли записано в ЛІНІЮ, ЯК формули вище, взаємоза1995 року, Міжнародній патентній публікації №WO мінні замісники, що містяться в дужках, приєдну91/09849, яку опубліковано 11 липня 1991 року, та ються до атому безпосередньо ліворуч від Міжнародній патентній публікації №WO93/01181, взаємозамінного замісника, що його взято в дужки що її опубліковано 21 січня 1993 року], а також з Коли два чи більше послідовних взаємозамінні інгібіторами протеази замісники взято в дужки, кожен з послідовних взаКорисність піримідин-тюалкільних та алкілефіємозамінних замісників є приєднаним до атому рних анти-СНІД сполук формули ІА ВІДПОВІДНО ДО ліворуч, що безпосередньо передує, який не взято цього винаходу може бути визначено за їх здатнісв дужки Таким чином, в формулі вище як R,, так й тю інгібувати зворотну транскриптазу вірусів, феRi, приєднані до атому вуглецю, що передує рменту, необхідного для реплікації вірусу імунодефіциту людини Цей фермент має ХІМІЧНІ формули або їх частини, які записано в характеристики, що відрізняють його від інших ЛІНІЮ, представляють атоми в лінійному ланцюзі відомих клітинних полімераз, та він є унікальним Символ "-" як правило представляє зв'язок між ферментом, який не виявляють у неінфікованих двома атомами в ланцюзі Так, CH3-O-CH2-CH(R,)клітинах Зворотну транскриптазу вірусів(дикого СНз представляє 2-заміщену 1-метоксипропанову типу) виявляють в екстрактах з бактеріальних клосполуку Подібно до цього, символ "=" представнів, одержаних ВІДПОВІДНО до способу, що його ляє подвійний зв'язок, наприклад, CH2'C(R,)-Oописано в [AIDS Virus Reverse Transcnptase deСНз, а символ " = " представляє потрійний зв'язок, fined by high level expression in Eschenchia coh, наприклад, HCEC-CH(R,)-CH2-CH3 Карбонільні EMBO J 6 3133-3137(1987)] Зворотну трансгрупи зображено одним з двох способів -CO- або криптазу вірусів P236L одержують згідно з PNAS С(=О)-, причому перше є більш прийнятним через 90 4713 - 4717(1993) Інгібування цього ферменту простоту визначають клітинним вільним аналізом, за яким ХІМІЧНІ формули циклічних(кільцевих) сполук вимірюють рівень радіоактивних попередників, або молекулярних фрагментів можна представити включених до ДНК Екстракти, приготовані згідно зі у ЛІНІЮ Так, сполуку 4-хлор-2-метилпіридин може способом Science, 1125 - 1129(1981), шкубують у бути представлено в ЛІНІЮ ЯК І\Г=С(СНЗ)-СН=ССІсуміші шпбітора, 20мм дитютреїтолу, 60мм хлориСН=С*Н за умови, що атоми, позначені зірочкою(*) ду натрію, 0,05% NP-40, 10мм хлориду магнію, зв'язані один з одним з утворенням кільця Подіб50мм Трис-буферу з рН 8,3, ЮмкМ [35Э]-м1ченого но циклічний молекулярний фрагмент 4-(етил)-1деоксинуклеозид-б'-трифосфату, 10 мкг/мл матрипіперазиніл може бути представлено як -N*-(CH2)2ці РНК(полі гС або полі rG) та 5мкг/мл праймера N(C2H5)-CH2-C*H2 ДНК(оліго dG або оліго dT) протягом ЗО хвилин Жорстка циклічна(кільцева) структура для при 37°С Включення радіоактивно-міченого попебудь-якої з сполук, що розглядаються, визначає редника визначають за допомогою відбору аліквот орієнтацію по відношенню до площини кільця для реакційної суміші, які спричинюють появу плями на замісників, приєднаних до кожного атому вуглецю 26 25 56992 жорсткої циклічної сполуки Для насичених сполук, ном формула описує епоксид Коли R, та R|, узяті що мають два замісники, приєднані до атому вугразом, утворюють більш складний фрагмент, талецю, який є частиною циклічної системи, кий як група -X-Y-, тоді орієнтація фрагменту є С(Хі)(Х2)-, два замісники можуть бути або в аксіатакою, що Сі в формулі вище приєднаний до X, та льній, або в екваторіальній позиції по відношенню Сг приєднаний до Y Таким чином, у прийнятих до кільця, і можуть змінювати своє положення як позначеннях позначення " R, та R|, узяті разом з аксіальне/екваторіальне Однак позиція двох заміутворенням -СН2-СН2-О-СО- " означає лактон, в сників по відношенню до кільця та один до одного якому карбоніл зв'язаний з C-z Однак, коли позназалишається фіксованою В той час як один з зачається " R, та R|, узяті разом з утворенням -СОмісників час від часу може скоріше лежати в плоС-СН2-СН2- ", позначення стосується лактону, в щині кільця(екваторіально) ніж вище або нижче якому карбоніл з'єднаний з Сі цієї площини(аксіально), один з замісників завжди Вміст атомів вуглецю в взаємозамінних замісзнаходиться над іншим В ХІМІЧНИХ структурних никах позначається одним з двох способів У перформулах, що зображують такі сполуки, замісник шому способі використовується приставка для (Х-і), який знаходиться "нижче" іншого замісника повного імені змінної, така як "С1-С4", де як "1", так (Хг), буде позначатись як такий, що перебуває в і "4" є цілими числами, які представляють мінімаальфа(а) конфігурації та позначатись за допомольне та максимальне число атомів вуглецю в взагою штрихової, штрихпунктирної або пунктирної ємозамінному заміснику Приставка відокремлюлінії приєднання до атому вуглецю, тобто за допоється від змінної пробілом Наприклад, "С1-С4 могою символу "—" або" " ВІДПОВІДНИЙ замісник, алкіл" представляє алкіл з від 1 до 4 атомів вуглерозташований "вище" (Хг) іншого (Х-і), визначаєтьцю(включаючи його ізомерні форми, якщо немає ся як такий, що знаходиться бета(р) конфігурації, вказівки на протилежне) Там, де подано єдину та позначається за допомогою безперервної лінії таку приставку, повний вміст атомів вуглецю в приєднання до атому вуглецю ЗМІННІЙ є визначеним Так, С2-С4 ал кокс и карбоніл описує групу СНз-(СН2)п-О-СО-, де п дорівнює нуКоли взаємозамінний замісник є двовалентлю, одиниці або двом За допомогою другого споним, валентності можуть бути взяті разом чи окресобу вміст атомів вуглецю тільки в кожній частині мо, або обома способами при визначенні змінної визначення визначається окремо шляхом застосуНаприклад, взаємозамінний замісник R,, приєднавання позначення "СГС|" в дужках та розташуванний до атому вуглецю як -C(=Ri)- може бути двоня його безпосередньо(без пробілу) перед тією валентним й визначатись як оксо чи кето(таким частиною визначення, що її визначають За допочином, утворюючи карбонільну групу (-СО-)) або як могою цього необов'язкового позначення (Сг два окремо приєднані одновалентні взаємозамінні Сз)ал ко кс и карбоніл має те саме значення, що й замісники a-R, і та (3-Ri k Коли двовалентний взаєС2-С4 алкоксикарбоніл, оскільки "Сі-Сз" стосується мозамінний замісник R, визначається як такий, що тільки до вмісту атомів вуглецю в алкоксигрупі складається з двох одновалентних взаємозамінПодібно до цього, хоча як Сг-Сє алкоксиалкіл, так і них замісників, позначення, яке використовується (Сі-Сз)алкокси(Сі-Сз)алкіл, визначають алкоксиадля визначення двовалентного взаємозамінного ЛКІЛЬНІ групи, що містять від 2 до 6 атомів вуглецю, замісника, являє собою форму "a-R, і (3-R, k" або два визначення відрізняються, оскільки перше будь-який її варіант У такому випадку як a-R, і так визначення дозволяє або алкокси, або алкільній і p-R| k, приєднані до атому вуглецю з утворенням частині самим містити 4 або 5 атомів вуглецю, у C(a-R, і )([3-R| k) Наприклад, коли двовалентний той час як друге визначення обмежує будь-яку з взаємозамінний замісник R6, -C(=R6)-визначаєтьcя цих груп до 3 атомів вуглецю як такий, що складається з двох одновалентних взаємозамінних замісників, два одновалентні взаКоли формула винаходу містить достатньо ємозамінні замісники є a-R61 р-Re 2, a-R6 э рскладний(циклічний) замісник, в КІНЦІ фрази вказуR6 ю і таке інше Подібно до цього, для двовалентється/позначається, що конкретний замісник буде ного взаємозамінного замісника Rn, -C(=Rn)- два позначенням^ дужках), яке буде відповідати тій одновалентні взаємозамінні замісники є a-Rn і рсамій назві/позначенню в СХЕМАХ, що буде також Rn 2 Для кільцевого замісника, для якого окремі представляти хімічну структурну формулу цього орієнтації а та р не існують(наПриклад, через наконкретного замісника явність вуглецевого подвійного зв'язку в КІЛЬЦІ), та 2 Визначення для замісника, приєднаного до атому вуглецю, що Всі температури подано в градусах по Цельне є частиною кільця, продовжує використовувасію тись зазначене вище позначення, але позначення ТШХ позначає тонкошарову хроматографію а та р не використовуються Хроматографія означає хроматографію при Саме через те, що двовалентний взаємозатиску довкілля на силікагелі мінний замісник може визначатися як два окремі ТГФ означає тетрапдрофуран одновалентні взаємозамінні замісники, два окремі ТБДМС означає трет-бутилдиметилсиліл одновалентні взаємозамінні замісники може бути Сольовий розчин означає водний насичений визначено як узяті разом з утворенням двовалентрозчин хлориду натрію ного взаємозамінного замісника Наприклад, у ЯМР означає спектроскопію ядерного магнітформулі -Ci(R,)H-C2(Ri)H- (Сі та C-z визначають ного(протонного) резонансу, ХІМІЧНІ зсуви подано в довільно перший та другий атом вуглецю, ВІДПОВІм д (5) відносно тетраметилсилану ДНО) R, та R|може бути визначено як узяті разом з ІЧ означає інфрачервону спектроскопію утворенням(1) другого зв'язку між Сі та C-z або(2) -ер означає феніл(СбНб двовалентної групи, такої як окса (-0-), і таким чи 28 27 56992 МС означає мас-спеїсгрометрію, виражену як тюалкільні та алкілефірні анти-СНІД сполуки" + т/е або одиниці маса/заряд [М+Н] означає вихідвключають "альфа-заміщені піримідин-тюалкільні ний позитивний іон плюс атом водню ЕІ означає та алкілефірні сполуки" та "альфа-заміщені піриелектронний імпульс XI означає хімічну іонізацію мідин-тюалкільні та алкілефірні анти-СНІД сполуFAB означає бомбардування швидкими атомами ки", якщо спеціально не вказане інше Ефір означає діетиловий ефір Приклади Галоген означає атом галогену(-СІ, -Br, -F або Без подальших уточнень припускається, що фахівець у цій галузі може, використовуючи попе-І) редній опис, втілити цей винахід в його найбільш Фармацевтично прийнятний відноситься до повному обсязі Подані далі докладні Приклади таких властивостей та/або речовин, які є прийнятописують те, як отримати різноманітні сполуки ними для пацієнта з фармаколопчта/або здійснити різні способи ВІДПОВІДНО ДО ЦЬОГО НОІЛ^ЖСИКОЛОГІЧНОІ точки зору та для промислововинаходу, і передбачені як винятково ілюстративні, го хіміка-фармацевта з фізичної/хімічної точки та не є обмеженнями опису, що передує, будьзору щодо композиції, препарату, стабільності, яким чином Фахівець у цій галузі легко виявить прийнятності для пацієнта та біологічної доступноВІДПОВІДНІ зміни в способах, як відносно реагентів, сті так і відносно умов та способів проведення реакПіридиніл означає піридильний радикал згідно цій з номенклатурою IUPAC Наприклад, 2піридил(піридинове кільце, заміщене в 2-позиці]) Приклад 1 Одержання 4-амшо-6-пдрокси-2Коли використовуються пари розчинників, за(2,6-дифторфеніл-метилтю)піримідину, (сполука стосовані відношення розчинників подано як №1) об'єм/об'єм (о/о) ВІЛ означає ВІЛ-1 (дикий тип та/або його СТІЙКІ до лікарських засобів мутанти, наприклад, M41L, K65N, K67L, K70R, L74V, V75T, А98Г, L100I, К103Е, K103N, K103Q, V106A, VI08I, Е138К, V179fl, V179E, Y181C, Y188H, Y188L, G190A, H,N T215Y, T215F, K219Q, К219Е, Р236І_та К238Т) Лікування означає інгібування ВІЛ вірусу, та буде відрізнятися залежно від інфікованого індивідуума Для індивідуумів, що мають позитивну ВІЛ Моногідрат 4-амшо-6-пдрокси-2реакцію(шфіковані), але не мають симптомів, пімеркаптопіримідину(1,61г, Ю.Оммоль) суспендуримідин-тюалкільні сполуки формули І будуть упоють в 50% етанолі(Юмл), потім обробляють твервільнювати або відвертати появу симптомів Для дим гідроксидом натрію(440мг, 11,0ммоль) та пеіндивідуумів, які мають позитивну ВІЛ реакцію, у ремішують, аж доки твердий продукт не яких симптоми виявлені та які страждають від розчиниться Додають 2,6СНІДу або ARC, піримідин-тюалкільні ПОХІДНІ фордифторбензилбромід(2,17г, 10,5ммоль) та реакмули ІА будуть уповільнювати або відвертати наційну суміш нагрівають із зворотним холодильнистання "останньої стадії СНІДу" Для індивідуумів, ком протягом 1,5 годин Після охолодження до які мають "останню стадію СНІДу", піримідин22°С твердий продукт збирають, промивають вотюалкільні та алкілефірні ПОХІДНІ формули ІА будою, потім сушать на повітрі Зазначену в заголовдуть подовжувати час життя цих індивідуумів ку сполуку перекристалізовують з етанолу, т пл Піримідин-тюалкільні та алкілефірні сполуки 245 - 246°С формули І(а також формул ІА та/або IB) включаДодержуючись загального способу Прикладу 1 ють альфа-заміщені піримідин-тюалкільні та алкіта здійснюючи несуттєві ЗМІНІ, але, використовуюлефірні сполуки Всі посилання на "піримідинчи ВІДПОВІДНИЙ галогенід, синтезують такі сполуки тюалкільні та алкілефірні сполуки" та "піримідинПриклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №2 №3 №4 №5 №6 №7 №8 №9 №10 №11 №12 №13 Приклад/сполука №14 Приклад/сполука №15 Т пл (°С) 236 - 239 4-амшо-2-(бензилтю)-6-пдро -ксипіримідин 250 - 251 4-амшо-2-(2-метилфенілметилтю)-6-пдроксипіримідин 4-амшо-2-(3-метилфенілметилтю)-6-пдроксипіримідин 2 3 0 - 231 266 - 267 4-амшо-2-(4-метилфенілметилтю)-6-пдроксипіримідин 222 - 2 2 3 4-амшо-2-(3-трифторметилфенілметилтю)-6-пдроксипіримідин 206 - 207 4-амшо-2-(3-метоксифенілметилтю)-6-пдроксипіримідин 4-амшо-2-(4-метоксифенілметилтю)-6-пдроксипіримідин 231 - 234 92-93 4-амшо-2-(3-фторфенілметилтю)-6-пдроксипіримідин 84-85 4-амшо-2-(3-хлорфенілметилтю)-6-пдроксипіримідин 194-196 4-амшо-2-(3-бромфенілметилтю)-6-пдроксипіримідин 208 - 209 4-амшо-2-(3-йодфенілметилтю)-6-пдроксипіримідин 263 - 264 4-амшо-2-(3-нітрофеніл-метилтю)-6-пдроксипіримідин 4-амшо-2-(3-карбометоксифенілметилтю)-6-пдроксипіримідин ЯМР (ДМСО-de) 8,01 (с, 1Н), 7,83(д, J = 7,8, 1Н), 7,74(д, J = 7,8, 1Н), 7,45(т, J = 7,8, 1Н), 6,55(с, 2Н), 4,95(с, 1Н), 4,40(с, 2Н), 3,84(с, ЗН) 4-аміно-2-(4-трет-бутилфенілметилтю)-6-пдроксипіримідин 263 - 264 29 №16 №17 №18 №19 №20 №21 №22 №23 №24 №25 №26 №27 56992 ЗО 4-амшо-2 -(3,4-дифторфенілметилтю)-6-пдроксипіримідин 4-амшо-2 -(3,4-дихлорфенілметилтю)-6-пдроксипіримідин 4-амшо-2 -(3,5-дихлорфенілметилтю)-6-пдроксипіримідин 4-амшо-2 -(2,4-дихлорфенілметилтю)-6-пдроксипіримідин 4-амшо-2 -(3,5-дибромфенілметилтю)-6-пдроксипіримідин 4-амшо-5 -циклогексил-2-(бензилтю)-6-пдроксипіримідин 4-амшо-5 -ізопропил-2-(бензилтю)-6-пдроксипіримідин 4-амшо-2 -(2-піридилметилтю)-6-пдроксипіримідин 4-амшо-2 -[2-(3-етокси)піридил метилтю 1-6-пдроксипіримідин 4-амшо-2 -(З-піридилметилтю)-б-пдроксипіримідин 4-амшо-2 -(і-нафтилметилтю)-б-пдроксипіримідин 4-амшо-2 •(2-нафтилметилтю)-6-пдроксипіримідин Приклад/сполука №28 4-аміно-2-(6,7-дифтор-2-нафтилметилтю)-6-пдроксипіримідин Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №29 Приклад/сполука №30 Приклад/сполука №32 Приклад/сполука №33 4-аміно-2-(2-хінолінілметилтю)-6-пдроксипіримідин ЯМР (ДМСОde) 8,33(д, J = 8,4, 1Н), 7,99(м, 2Н), 7,76(дт, J f l = 1,2, J T = 7,6, 1Н), 7,68(4, J = 8,4, 1Н), 7,59(дт, J f l = 1,2, J T = 7,6, 1Н), 6,58(с, 2Н), 4,97(с, 1Н), 4,63(с, 2Н) 4-аміно-2-(6-хлор-5-піперонілметилтю)-6-пдроксипіримІдин 254 - 255 4-аміно-2-(Е-стирилметилтю)-6-пдроксипіримідин 253 - 254 4-аміно-2-(пропарплтю)-6-пдроксипіримідин 193-198 Приклад 34 Одержання 4-амшо-6-хлор-2-(2,6дифторфенілметилтю)піримідину, (сполука №34) H2N N 222 - 224 255 276 - 277 278 - 279 288 - 289 195-196 170-171 219-220 214-216 210-212 240 - 242 247 - 249 281 - 283 (розкл) S 4-амшо-6-пдрокси-2-(2,6дифторфенілметилтю)піримідин(1,33г, 4,94ммоль, сполука №1) та 2-ПІКОЛІН(0,5МЛ) нагрівають із зво ротним холодильником з дефлегмацією РОСІз(бмл) протягом ночі Після вилучення надлишкового розчинника у вакуумі залишок обробляють на льоді, а потім нагрівають із зворотним холодильником протягом ЗО хвилин Водний шар декантують, потім залишок обробляють надлишком ІЧЬЦОН та нагрівають із зворотним холодильником протягом ЗО хвилин Після охолодження твердий продукт збирають і промивають водою, потім перекристалізовують з толуолу, т пл 154°С 31 Приклад/сполука №61 Приклад/сполука №62 Приклад/сполука №64 Приклад/сполука №65 Приклад/сполука №66 56992 32 4-аміно-6-хлор-2-(2-хінолінілметилтю)-піримідин 4-амшо-6-хлор-2-(6-хлор-5-піперонілметилтю)-піримідин 4-амшо-6-хлор-2-(Е-стирилметилтю)-піримідин 4-хлор-2-(2-нафтилметилтю)-піримідин 4-аміно-6-хлор-2-(пропарплтю)-піримідин Приклад 67 Одержання 4-амшо-6-хлор-2-(3бромфенілметилсульфініл)піримідину, (сполука №67) 4-Амшо-6-хлор-2-(3бромфенілметилтю)піримідин(165мг, 0,5ммоль, сполука №43) в метиленхлориді(Юмл) обробляють 50% МСРВА(172мг, 0,50ммоль) та перемішують протягом 17 годин Твердий продукт збирають фільтруванням, промивають ефіром та сушать, т пл 216-217°С Додержуючись способу Прикладу 67 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт 4-амшо-6-хлор-2-(2нафтилметилтю)піримідин (сполука №59), одержують сполуку 4-амшо-6-хлор-2-(2нафтилметилсульфшіл)-піримідин (сполука №68) (т пл 222-223°С) Приклад 69 Одержання 4-амшо-6-хлор-2-(3бромфенілметилсульфоніл)-піримідину (сполука №69) 4-амшо-6-хлор-2-(3-бромфенілметилтю)піримідин(660мг, 2,0ммоль, сполука №43) в оцтовій кислоті(5мл) обробляють 30% N202(1 мл) та перемішують при кімнатній температурі протягом 72 годин Сирий продукт розбавляють етилацетатом, промивають водою, насиченим Nah-ІСОз та насиченим сольовим розчином, сушать MgSO4 потім концентрують у вакуумі Продукт очищають шляхом хроматографії, використовуючи 1 1 етилацетат/гексан, т пл 191-192°С Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №73 №74 №75 №76 №77 150-152 157-159 117-120 76-78 137-140 Приклад 70 Одержання 4-амшо-5-бром-6хлор-2-(2-нафтилметилтю)-піримідину (сполука №70) 4-Амшо-6-хлор-2-(2-нафтилметилтю)піримідин(302мг, 1,0ммоль, сполука №59) та NaНСОз(100мг, 1,2ммоль) розчиняють в 50% метанолі(Змл) та обробляють краплями розчином брому в метанолі(0,92М, 1,2мл, 1,1ммоль) Реакційну суміш знебарвлюють насиченим NaHSO3 та екстрагують етилацетатом Органічні фракції промивають водою, сушать MgSO4, потім концентрують у вакуумі Продукт очищають шляхом хроматографії, використовуючи 15 85 етилацетат/гексан, т пл 158°С Додержуючись загального способу Прикладу 67 та здійснюючи неістотні зміни, з 4-амшо-6-хлор2-(2-піридилметилтю)-піримідину(сполука №55) одержують 4-амшо-5-бром-6-хлор-2-(2піридилиетилтю)-піримідин(сполука №71, т пл 119-120°С) Приклад 72 Одержання 4,6-дипдрокси-2(фенілметилтю)-піримідину Тюбарбітурову кислоту(5,22г, 36,2ммоль) в етанолі(52мл) обробляють 3.25М МаОН(11,1мл, 36,2ммоль), та суміш нагрівають із зворотним холодильником протягом ЗО хвилин Після ШВИДКОГО охолоджування до реакційної суміші додають бензилбромід(4,3мл, 36,2ммоль) та розчин нагрівають із зворотним холодильником протягом однієї години Реакційну суміш охолоджують та концентрують у вакуумі і одержаний твердий продукт фільтрують та промивають холодною Ь^О, потім холодним етанолом, т пл > 320°С Додержуючись загального способу Прикладу 72 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ дипдроксипіримідинтюн, синтезують такі сполуки 4,6-дипдрокси •5-метокси-2-(2-нафтилметилтю)-піримідин 4,6-дипдрокси •5-фтор-2-(2-нафтилметилтю)-піримідин 4,6-дипдрокси -5-метил-2-(2-нафтилметилтю)-піримідин 4,6-дипдрокси -5-фтор-2-(2-піридилметилтю)-піримідин 4,6-дипдрокси -2-(4-метоксифенілметилтю)-піримідин Т пл (°С) 248 - 249 >325 285 - 286 195(розкл ) 207 - 208 33 56992 Приклад 78 Одержання 4,6-дихлор-2(бензилтю)піримідину (сполука №78) 2-(Бензилтю)-4 6-дипдроксипіримідин(5,95г, 25,4ммоль, сполука №72) обробляють РОСІз(26мл) та нагрівають із зворотним холодильником протягом 2 годин Реакційну суміш охолоджують та надлишок РОСІз вилучають шляхом перегонки у вакуумі Гарячий залишок виливають на лід та водний шар нейтралізують з твердим NaOH до рН 7 - 8 Водний розчин екстрагують етилацетатом три рази та об'єднані органічні шари Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №79 №80 №81 №82 №83 №85 №86 №87 №88 №90 №91 №92 №93 Приклад/сполука №95 Т пл (°С) 80-81 119-120 67-68 136-138 2,5 годин Після охолоджування продукт фільтрують, промивають водою та сушать, т пл 115 117°С Додержуючись загального способу Прикладу 89 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ дихлорпіримідин, синтезують такі сполуки 4-амшо-5-метил-6-хлор-2-(2-нафтилметилтю)-піримідин 4-амшо-5-фтор-6-хлор-2-(2-нафтилметилтю)-піримідин 4-амшо-5-фтор-6-хлор-2-(2-піридилметилтю)-піримідин 4-амшо-6-хлор-2-(4-метоксифенілметилтю)-піримідин Приклад 94 Одержання 4-амшо-2-(2піридилметилтю)-піримідину, сполука №94 4-Амшо-2-меркаптопіримідин(0,40г, 3,15ммоль) суспендують в етанолі(2мл), та додають 3.25М NaOH(2,0Mn, 6,5ммоль) Розчин нагрівають із зворотним холодильником протягом 10 хвилин і після охолоджування до 22°С додають 2піколілхлорид* НСІ(0,49г, 2,98ммоль) Розчин нагрівають із зворотним холодильником додатково ще протягом 15 хвилин Розчин охолоджують та концентрують у вакуумі Залишок розчиняють в і н Т пл (°С) 93-94 80-81 109-110 ЯМР 39-42 60 годин Реакційну суміш гасять насиченим NH4CI, промивають насиченим ЫаНСОз, сушать MgSO4 й концентрують у вакуумі Зразок очищають шляхом хроматографії, використовуючи 1 З етилацетат/гексан, т пл 85 - 86°С Додержуючись загального способу Прикладу 84 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИМ чином заміщений амін, синтезують такі сполуки 4-піролідино-6-хлор-2-(бензилтю)-піримідин 4-морфолшо-6-хлор-2-(бензилтю)-піримідин 4-пропиламшо-6-хлор-2-(бензилтю)-піримідин 4-пдразино-6-хлор-2-(бензилтю)-піримідин Приклад 89 Одержання 4-амшо-5-метокси-6хлор-2-(2-нафтилметилтю)-піримідину, (сполука №89) 4 6-Дихлор-5-метокси-2-(2-нафтилметилтю)піримідин(1,40г, 4,0ммоль, сполука №79) розчиняють в ацетонітрилі(Юмл), обробляють концентрованим гідроксидом амонію(2мл), потім нагрівають до 120°С в герметично закритій трубці протягом Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука промивають розбавленим NaOH та насиченим сольовим розчином, потім сушать MgSO4 Розчин фільтрують та концентрують у вакуумі, потім очищають шляхом перегонки, т к (0,2мм рт с т ) 1 5 5 160°С, одержуючи зазначену в заголовку сполуку ЯМР (CDCI3) 7,43(м, 2Н), 7,29(м, ЗН), 7,02(с, 1Н), 4,37(с, 2Н) Додержуючись загального способу Прикладу 78 та виконуючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ дипдроксипіримідин, синтезують такі сполуки 4,6-дихлор-5-метокси-2-(2-нафтилметилтю)-піримідин 4,6-дихлор-5-фтор-2-(2-нафтилметилтю)-піримідин 4,6-дихлор-5-метил-2-(2-нафтилметилтю)-піримідин 4,6-дихлор-5-фтор-2-(2-піридилметилтю)-піримідин 4 6-дихлор-2-(4-метоксифенілметилтю)-піримідин Сполука №82 ЯМР (CDCI3) 8,58(д, J = 4,1 1Н), 7,67(м, 1Н), 7,50(м, 1Н), 7,24(м, 1Н), 4,51 (с, 2Н) Приклад 84 Одержання 4-піперидо-6-хлор-2(бензилтю)-піримідину, сполука №84 4,6-Дихлор-2-(бензилтю)-піримідин(261мг, 0,96ммоль, сполука №78) розчиняють в метиленхлориді(Змл), обробляють триетиламіном(0,17мл, 1,20ммоль) та піперидином(0,10мл, 1,06ммоль) і перемішують при кімнатній температурі протягом Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука 34 Т пл (°С) 156 160 171 -172 118,5-119,5 НСІ та розбавляють етилацетатом Суміш нейтралізують NaOH до рН 8 й водний шар ВІДДІЛЯЮТЬ та промивають ДВІЧІ етилацетатом Об'єднані органічні шари промивають насиченим ЫаНСОз, насиченим NaCI, сушать з MgSO4 1 концентрують у вакуумі, т пл 133- 134°С Додержуючись загального способу Прикладу 94 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ тіол, синтезують такі сполуки 4-амшо-2-(3-бромфенілметилтю)-піримідин Т пл (°С) 111 -112 35 Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №96 №97 №98 №99 №100 №101 №102 56992 Приклад 103 Одержання 4-амшо-6-хлор-2-(1нафтилметилокси)-піримідину, 1-Нафталшметанол(227мг, 1,44ммоль) додають до суспензії 50% гідриду натрію(69мг, 1,44ммоль) в сухому ТГФ(4мл) при 0°С Після перемішування протягом ЗО хвилин додають 4-аміно2,6-дихлорпіримідин(157мг, 0,96ммоль) та перемішують при 22°С протягом 72 годин Розчин гасять насиченим ІЧЬЦСІ та концентрують у вакуумі Залишок розчиняють в метиленхлориді та промиПриклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №104 №105 №106 №107 36 4-амшо-2-(3-метилфенілметилтю)-піримідин 4-амшо-2-(3-піридилметилтю)-піримідин 4-амшо-2-(2-нафтилметилтю)-піримідин 4-амшо-6-хлор-2-(2-бензотіазолметилтю)-піримідин 4-амшо-6-хлор-2-[2-(1-феніл-1-етанон)тю]-піримідин 4-амшо-6-хлор-2-(циклогекс-1-енілметилтю)-піримідин 4-амшо-6-хлор-2-(7-стирилтю)-піримідин вають 3 рази насиченим ЫаНСОз, сушать з MgSO4, фільтрують та концентрують у вакуумі Зразок очищають шляхом хроматографії, використовуючи 1 2 етил ацетат/гексан та перекристалізовують з суміші renTaHfronyon, т пл 160-161°С Додержуючись загального способу Прикладу 103 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ спирт, синтезують такі сполуки 4-амшо-6-хлор-2-(бензилокси)-піримідин 4-амшо-6-хлор-2-(2-нафтилметилокси)-піримідин 4-амшо-6-хлор-2-(3-метилфенілметилокси)-піримідин 4-амшо-6-хлор-2-(3-бромфенілметилокси)-піримідин Приклад 108 Одержання 4-амшо-6-хлор-2-(3пдроксифенілметилтю)-піримідину 4-Амшо-6-хлор-2-(3-метоксифенілметилтю)піримідин(36мг, 0,128ммоль, Сполука №39) розчиняють в метиленхлориді(0,25мл), охолоджують до 0°С та обробляють розчином ВВгз(0,32мл, 0,32ммоль, 1моль в метиленхлориді) Реакційну суміш перемішують при 0°С протягом 20 хвилин, потім нагрівають із зворотним холодильником протягом 2 годин Після охолодження реакцію гасять водою та нагрівають із зворотним холодильником додатково ще протягом ЗО хвилин При охолоджуванні твердий продукт збирають та очищують шляхом перекристалізації з суміші етанол/вода, т пл 147,5-148,5°С Приклад 109 Одержання 4-амшо-6-хлор-2-(3ізопропоксифенілметилтю)-піримідину, (Сполука №108) 4-Аміно-6-хлор-2-(3-пдроксифенілметилтю)піримідин(135мг, 0,50ммоль, Сполука №108) додають до розчину КОН(280мг, 5ммоль) в ДМСО(2,5мл) при кімнатній температурі Додають 2-бромпропан(615мг, 5ммоль) та реакційну суміш перемішують протягом ночі, потім виливають у воду Водний розчин екстрагують етилацетатом, сушать з MgSO4, фільтрують та концентрують у вакуумі Зразок очищують шляхом хроматографії, використовуючи 1 3 етилацетат.гексан, т пл 71°С Приклад 110 Одержання 4-амшо-6-хлор-2тюпіримідину, (Сполука №110) 4-Амшо-6-хлор-2-(4-метоксифенілметилтю)піримідин(11,0г, 39,15ммоль, Сполука №93) та трифтороцтову кислоту(84мл) нагрівають із зворотним холодильником протягом 20 годин, потім надлишок розчинника вилучають у вакуумі Зразок розтирають на порошок з хлороформом, потім перемішують з ефіром та фільтрують Твердий продукт промивають ефіром, потім сушать на повітрі, т пл > 320°С Приклад 110А Одержання мезилатної солі 4аміно-6-хлор-2-тюпіримідину, 88 - 89 118-119 115-116 202 - 203 194-195 122-123 Тпл (°С) 114-115 130-131 85-87 96-98 Сполука №110А Мезилат 4-амшо-6-хлор-2меркаптопіримідину Суспензію 4-амшо-6-хлор-2-(4метоксифенілметилтю)-піримідину(10,0г, 33,22ммоль) в 160мл метиленхлориду при кімнатній температурі обробляють метансульфоновою кислотою(31,89г, 332,2ммоль, Юеквів) за один прийом Після ТОГО, ЯК ТШХ аналіз покаже відсутність вихідного продукту(приблизно 50 хвилин), спочатку додають краплями 1280мл діетилового ефіру Коли об'єм білого твердого продукту стає досить великим, дуже швидко додають решту Et20 Суспензію перемішують протягом ночі та продукт збирають шляхом фільтрування й промивають діетиловим ефіром, одержуючи 8,62г зазначеної в заголовку сполуки(Температура плавлення 166 - 167°С) Аналіз Розраховано для C5H8CIN3O3S2 4,94%Н2О, С, 23,22, Н, 3,16, N, 16,25 Знайдено С, 23,48, Н, 3,25, N, 15,70 Приклад 111 Одержання 4-амшо-6-хлор-2-[2(4-хлор)піридилметилтю]піримідину, (Сполука №111) 4-Амшо-6-хлор-2-тюпіримідин(Сполука №110, 614мг, 2,38ммоль) в етанолі(1,5мл) обробляють 3,25 М NaOH(1,47Mn, 4,8ммоль) та суміш нагрівають до 50°С Додають 4-хлор-2-хлорметилпіридин та розчин перемішують, підігріваючи, протягом 1 години Реакційну суміш охолоджують та концентрують у вакуумі і одержаний твердий продукт фільтрують та промивають водою, потім холодним етанолом,т пл 195°С Додержуючись загального способу Прикладу 111 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ хлорметиларен, синтезують такі сполуки 37 Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №112 №113 №114 №115 №116 №117 №118 №119 Приклад/сполука №120 Приклад/сполука №121 Приклад/сполука №122 Приклад/сполука №123 Приклад/сполука №124 Приклад/сполука №125 Приклад/сполука №126 Приклад/сполука №127 Приклад/сполука №128 Приклад/сполука №130 Приклад/сполука №131 Приклад/сполука №132 Приклад/сполука №133 Приклад/сполука №134 Приклад/сполука №135 Приклад/сполука №137 Приклад/сполука №138 Приклад/сполука №140 Приклад/сполука №142 Приклад/сполука №143 Приклад/сполука №144 Приклад/сполука №145 Приклад/сполука №146 56992 38 4-амшо-6-хлор-2-[2-(6-хлор)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(6-метил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-метил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-етокси)-піридилметилтю]-піримідин 4-аміно-6-хлор-2-[2-(4-тюфеніл)-піридилметилтю)-піримідин 4-амшо-6-хлор-2-[2-(3-метил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(5-метил)-піридилметилтю)-піримідин 4-амшо-6-хлор-2-[2-(4бром)-піридилметилтю)-піримідин 4-амшо-6-хлор-2-[2-(4-метокси-6-метил)-піридилметилтю]піримідин 4-амшо-6-хлор-2-[2-(4,6-диметил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-етил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-метокси)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-(2-метилпропил)-піридилметилтю]піримідин 4-амшо-6-хлор-2-[2-(6-хлор-4-метил)-піридилметилтю]піримідин 4-амшо-6-хлор-2-[2-(4-ізопропокси)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4,6-диметил)-піримідинілметилтю)піримідин 4-амшо-6-хлор-2-[2-(4-ціано)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[4-(6-метил)-піримідинілметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-пропил)-піридилметилтю]-піримідин 4-аміно-6-хлор-2-[2-(4-ізопропил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(5-феніл)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-етил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-(а-пдрокси, аметил)етил)піридилметилтю]-піримідин 4-амІно-6-хлор-2-[2-(4-циклопропил)піридилметилтю]піримідин 4-амшо-6-хлор-2-[2-(4-циклопентил)піридилметилтю]-піримідин 4-аміно-6-хлор-2-[2-(4,5-диметил)-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[4-(2,6-диметил)-піримідинілметилтю]піримідин 4-амшо-6-хлор-2-[2-(4-піролідино)піридилметилтю)-піримідин 4-аміно-6-хлор-2-[(5-хлортюфен-2-ілметил)тю]-піримідин 4-аміно-6-хлор-2-[2-(4-(2-бутил))-піридилметилтю)-піримідин 4-аміно-6-хлор-2-[2-(4-диметиламіно)піридилметилтю]піримідин Т пл (°С) 135-136 156-157 192-193 181 -185 136-137 148-149 191 -192 188(розкл ) 171 -172 160-161 173-174 191 -192 156-157 171 -172 168-169 180-181 214-215 165-166 161 -162 139 191 180 140-143 162-163 138-139 210-211 132-138 205(розкл ) 100-102 115-117 207 - 208 199 200 (розкл) 83-84 172 144-145 Приклад/сполука №147 2-[2-(4-амшо-6-хлор)піримідинілтюметил]-піридин-1-оксид Приклад/сполука №148 Приклад/сполука №149 Приклад/сполука №151 4-амшо-6-хлор-2-[(фуран-3-ілметил)тю]-піримідин 4-амшо-6-хлор-5-фтор-2-[2-(4-хлор)піридилметилтю]піримідин 4-амшо-6-хлор-2-[2-(4-(3-пентил))-піридилметилтю]-піримідин 4-амшо-6-хлор-2-[2-(4-ацетил)-піридилметилтю]-піримідин ЯМР (CF3OD) 8,67 (д, J = 5,2, 1Н), 8,12 (с 1Н), 7,74 (д, J = 5,1, 1Н) 6,22 (с, 1Н), 4,53 (с, 2Н), 2,64 (с, ЗН) 4-амшо-6-хлор-2-[(бензофуран-2-ілметил)тю]-піримідин 118-119 4-амшо-6-хлор-2-[2-(6-диметиламшо-4-метил)166-168 піридилметилтю]-піримідин 4-аміно-6-хлор-2-[(1Н-шден-3-ілметил)тю]-піримідин ЯМР (CDCI3) 7,47, 7,26, 6,54,6,15,4,99,4,34,3,37 4-амшо-6-хлор-2[2-(4-карбометокси)піридилметилтю]168-169 піримідин 4-аміно-6-хлор-2-[((3)-(-)-периліл)тю]-піримідин 115-116 4-аміно-6-хлор-2-[(бензотюфен-2-ілметил)тю]-піримідин 155-156 4-амшо-6-хлор-2-[(2Н-1-бензопіран-3-ілметил)тю]-піримідин 110-113 Приклад/сполука №152 Приклад/сполука №153 Приклад/сполука №154 Приклад/сполука №155 Приклад/сполука №156 Приклад/сполука №157 Приклад/сполука №158 Приклад/сполука №159 Приклад 163 Одержання 4-амшо-6-хлор-2-[2(4-карбоксамідо)-піридилметилтю]-піримідину, (Сполука №163) 4-Амшо-6-хлор-2-[2-(4карбометокси)піридилметилтю]-піримідин(100мг, 0,32ммоль) та свіжоперегнаний формамід(48мг, 1,06ммоль) розчиняють в ТГФ(0,5мл) й розчин нагрівають із зворотним холодильником Додають метоксид натрію(25%, 24мкл, 0,107ммоль) та суміш нагрівають із зворотним холодильником протягом 1 години Реакційну суміш охолоджують та фільтрують крізь целіт, потім концентрують у ваку 40 39 56992 умі Отриманий твердий продую" розтирають на перемішують протягом 1 години Реакцію гасять порошок з ацетоном, т пл 191-192°С водою(1 крапля), 1н NaOH(1 крапля), та водою(3 краплі) та розбавляють етилацетатом Реакційну Приклад №164 Одержання 4-амшо-6-хлор-2суміш сушать з MgSO4 та концентрують у вакуумі [2-(4-пдроксиметил)піридилметилтю]-піримідину, Отриманий твердий продукт розтирають на поро(сполука №164) шок з етилацетатом, т пл 117-118°С Літійалюмшійпдрид(12мг, 0,32ммоль) суспендують в ТГФ(1мл) та охолоджують до 0°С СуспенДодержуючись загального способу прикладу зію потім обробляють розчином 4-амшо-6-хлор-270 та здійснюючи неістотні зміни, але використо[2-(4-карбометокси)піридилметилтю]вуючи як вихідний продукт ВІДПОВІДНИЙ 4-амшо-бпіримідину(100мг, 0,32ммоль) в ТГФ(0,5мл) Розхлор-2-[2-(4-заміщений)піридилметилтю]піримідин, чину дають нагрітися до кімнатної температури та синтезують такі сполуки Т пл (°С) Приклад/сполука №165 Приклад/сполука №166 4-амшо-5-бром-6-хлор-2-[2-(4-метил)піридилметилтю]піримідин 4-амшо-5-бром-6-хлор-2-[2-(4ізопропил)піридилметилтю]-піримідин Додержуючись загального способу прикладу 111 та здійснюючи неістотні зміни, але використоПриклад/сполука №167 Приклад/сполука №168 Приклад/сполука №169 Приклад/сполука №170 Приклад/сполука №171 Приклад/сполука №172 Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №173 №174 №175 №176 №177 Приклад/сполука №178 Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука Приклад/сполука №179 №180 №181 №182 №183 №184 №186 Приклад/сполука №187 Приклад/сполука №188 Приклад/сполука №189 146-147 вуючи як вихідний продукт ВІДПОВІДНИЙ хлорметиларен, синтезують такі сполуки 4-аміно-6-хлор-2-(2,6-дихлорфеніл)метилтюпіримідин 4-амшо-6-хлор-2-[(2,3-дипдробензофуран-5-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(5-фенілізоксазол-3-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(2,3-дипдробензофуран-2-ілметил)тю]піримідин 4-аміно-6-хлор-2-[[(3,4-дипдро-1-нафталш-2іл)метил]тю]піримідин 4-амшо-6-хлор-2-[[(5-хлоримідазо-[1,2-а]піридин-2іл)метил]тю]-піримідин 4-амшо-6-хлор-2-[(6-метилпіразин-2-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(5-метилізоксазол-3-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(5-метилпіразин-2-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(1-метил імідазол-2-ілметил)тю]піримідин 4-амшо-6-хлор-2-[(3-метилпіразин-2-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(хінолін-6-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(хіноксалін-2-ілметил)тю]пІримідин 4-аміно-6-хлор-2-[(хінолін-8-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(хінолін-4-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(ізохінолін-3-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(хінолін-5-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(хінолін-7-ілметил)тю]піримідин 4-аміно-6-хлор-2-[(піперон-5-ілметил)тю]піримідин 4-аміно-6-хлор-2-[[(3,4-дипдро-1-нафталшіл)метил]тю]піримідин 4-амшо-6-хпор-2[2-(5карбометокси)піридилметилтю]піримідин 4-аміно-6-хлор-2[2-(4-циклогексил)-піридилметилтю]піримідин Додержуючись загального способу прикладу 72 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ дипдроксипіримідинтюн, синтезують таку сполуку Приклад/сполука №190 4,6-дипдрокси-5-фтор2-[2-(4-хлор)піридилметилтю]піримідин ЯМР (ДМСО) 8,48(д, J = 5,5, 1Н), 7,71 (с, 1Н), 7,44(с, 1Н), 4,44(с, 2Н) Додержуючись загального способу прикладу 78 та здійснюючи неістотні зміни, але використовуючи як вихідний продукт ВІДПОВІДНИЙ дипдроксипіримідин, синтезують таку сполуку 138-139 Т пл (°С) 173-174 153 217-219 105-107 104-105 >240 162 177-180 154-155 178-180 162-163 186-188 (розкл) 195(розкл) 174-175 195(розкл ) >210 190(розкл ) 195(розкл ) 148-150 127-130 200 134 Приклад/сполука №191 4,6-дихлор-5-фтор-2[2-(4-хлор)піридилметилтю]піримідин ЯМР (CDCI3) 8,54(д, J = 5,5, 1Н), 7,77(с, 1Н), 7,39(д, J = 5,4, 1Н), 4,59(с, 2Н) Приклад 193 Метиловий ефір (Е)-4-[(4-амшо6-хлор-2-піримідиніл)тю]-2-бутеновоі кислоти, (сполука №193) 4-Амшо-6-хлор-2-меркаптопіримідин мезилат(0,30г, 1,16ммоль) розчиняють в 3,25н гідроксиді натрію(2мл) та етанолі(імл) при температурі довкілля з подальшим доданням метил-4бромкротонату(0,16мл, 1,40ммоль) Реакційну суміш перемішують протягом від 2 до 15 годин, га 42 41 56992 сять надлишком води, екстрагують метиленхлориПриклад 200 (Е)-г\І-метил-г\І-феніл-4-[(4-амшодом(2 х 25мл) Екстракти об'єднують, промивають 6-хлор-2-піримідиніл)тю]-2-бутенамід, (сполука соляним розчином(25мл), сушать над сульфатом №200) натрію, концентрують у вакуумі та перекристалізоДодержуючись загального способу прикладу вують з суміші гексан/етилацетат, одержуючи спо194 та здійснюючи неістотні зміни, але заміщаючи луку №193, т пл 146-149°С діетиламін І\І-метиланіліном(2,31 г, 21,56ммоль), одержують зазначену в заголовку сполуку, т пл Приклад 194 (Е)-г\І,г\І-Діетил-4-[(4-аміно-6152-154°С хлор-2-піримідиніл)-тю]-2-бутенамід, (сполука №194) Приклад 201 (Е)-г\І-аліл-г\І-метил-4-[(4-аміно-6хлор-2-піримідиніл)-тю]-2-бутенамід, (сполука 4-Хлоркротонілхлорид (1,36г, 9,80ммоль) в №201) ефірі(20мл) об'єднують з діетиламіном в ефірі(5мл) при -15°С у колбі, висушеній на вогні Додержуючись загального способу прикладу Реакційну суміш нагрівають до температури до194 та вносячи неістотні зміни, але заміщаючи вкілля, перемішують протягом від 1 до 2 годин, діетиламін І\І-метилаліламіном(1,15г, 16,17ммоль), гасять водою(ЗОмл), екстрагують етилацетатом(2 одержують зазначену в заголовку сполуку, т пл х ЗОмл), промивають сольовим розчином(ЗОмл), 140-142°С сушать над сульфатом натрію та концентрують у Приклад 202 (Е)-г\І,г\І-дипропил-4-[(4-амшо-6вакуумі, одержуючи сирий 4-xnop-N,Nхлор-2-піримідиніл)-тю-2-бутенамід, (сполука діетилкротонаміду №202) Додержуючись загального способу прикладу 4-Хлоркротонілхлорид (1,02г, 7,35ммоль) в ефірі(Юмл) об'єднують з дипропиламшом(1,64г, 193 та здійснюючи неістотні зміни, але заміщаючи 16,17ммоль) в ефірі(5мл) при -15°С у колбі, висусирий 4-хлор-г\І,г\І-діетилкротонамід (1,72г, шеній на вогні Реакційну суміш нагрівають до те9,80ммоль) цисл'ранс-1,3-дихлор-2-бутеном, одемператури довкілля, перемішують протягом від 1 ржують зазначену в заголовку сполуку, т пл 143до 2 годин, гасять водою(ЗОмл), екстрагують ети145°С лацетатом(2 х ЗОмл), промивають сольовим розПриклад 195 (Е)-4-метил-1 -[4-[(4-амшо-6чином(ЗОмл), сушать над сульфатом натрію, конхлор-2-піримідиніл)тю]-1-оксо-2-бутеніл]піперазин, центрують у вакуумі, та х ром ато графу ють на (сполука №195) силікагелі (230 - 400меш, ЮОмл), елююючи суміДодержуючись загального способу прикладу шшю гексан/етил а цетат(60/40) ВІДПОВІДНІ фракції 194 та здійснюючи неістотні зміни, але заміщаючи об'єднують^ = 0,53, ТШХ, гексан/етилацетат, діетиламін 1-метилпіперазином(2,15г, 25/75) та концентрують у вакуумі, одержуючи 421,50ммоль), одержують зазначену в заголовку хлор-г\І,г\І-дипропил-кротонаміду 4-амшо-6-хлор-2сполуку, т пл 155-156°С меркаптопіримідинмезилат(0,30г, 1,16ммоль) розПриклад 196 (Е)-І\І-етил-4-[(4-амшо-6-хлор-2чиняють в ДМФ(5мл) та гідриді натрію(0,06г, піримідиніл)тю]-2-бутенамід, (сполука №196) 2,55ммоль) при температурі довкілля з подальшим Додержуючись загального способу прикладу доданням 4-хлор-г\І,г\І-дипропилкротонаміду(0,23г, 194 та здійснюючи неістотні зміни, але заміщаючи 1,13ммоль) Реакційну суміш перемішують протядіетиламін етиламіном(0,73г, 16,17ммоль), одергом від 2 до 15 годин, гасять надлишком води, ексжують зазначену в заголовку сполуку, т, пл 160 трагують етилацетатом(3 х 20мл) Екстракти об'161 °С єднують, промивають сольовим розчином(20мл), Приклад 197 (Е)-1 -[4-((4-амшо-6-хлор-2сушать над сульфатом натрію, концентрують у піримідиніл)тю]-1-оксо-2-бутеніл]піперидин, (сповакуумі та хроматографують на силікагелі(230 лука №197) 400меш, ЮОмл), елююючи гекДодержуючись загального способу прикладу сан/етилацетатом(60/40) ВІДПОВІДНІ фракції об'єд194 та здійснюючи неістотні зміни, але заміщаючи н у ю т ь ^ = 0,40, ТШХ, гексан/етилацетат, 25/75) та діетиламін піперидином(1,38г, 16,17ммоль), одерконцентрують у вакуумі, одержуючи зазначену в жують зазначену в заголовку сполуку, т пл 159 заголовку сполуку, т пл 139-142°С 163°С Приклад 198 (Е)-4-[4-[(4-амшо-6-хлор-2Приклад 203 (Е)-г\І-етил-г\І-метил-4-[(4-амшопіримідиніл)тю]-1-оксо-2-бутеніл]морфолін, (сполу6-хлор-2-піримідиніл)-тю]-2-бутенамід, (сполука ка №198) №203) Додержуючись загального способу прикладу Додержуючись загального способу прикладу 194 та здійснюючи неістотні зміни, але заміщаючи 202 та здійснюючи неістотні зміни, але заміщаючи діетиламін морфолшом(1,41г, 16,17ммоль), одердипропиламін І\І-етилметиламшом(0,87г, жують зазначену в заголовку сполуку, т пл 154 14,70ммоль), одержують зазначену в заголовку 157°С сполуку, т пл 170-172°С Приклад 199 (Е)-1-[4-[(4-амшо-6-хлор-2Приклад 204 (Е)-г\І,г\І-Диметил-4-[(4-аміно-6піримідиніл)тю]-1-оксо-2-бутеніл]піролідин, (сполухлор-2-піримідиніл)тю]-2-бутенамід, (сполука ка №199) №204) Додержуючись загального способу прикладу Додержуючись загального способу прикладу 194 та здійснюючи неістотні зміни, але заміщаючи 202 та здійснюючи неістотні зміни, але заміщаючи діетиламін піролідином(1,15г, 16,17ммоль), одердипропиламін диметиламіном(0,50г, 11,03ммоль), жують зазначену в заголовку сполуку, т пл 178 одержують зазначену в заголовку сполуку, т пл 180°С 173-176°С Приклад 205 (Е)-г\І,І\І-Діетил-4-оксо-2пентенамід 44 43 56992 У колбі, висушеній на вогні, що містить (Е)-4гасять шляхом додання льоду(Юмл), екстрагують оксо-2-пентеноілхлорид(1,16г, 8,76ммоль), в ефірі, метиленхлоридом(2 х Юмл), промивають сольоохолодженому до -15°С, додають діетиламш(1,41г, вим розчином(Юмл), сушать над сульфатом на19,28ммоль) в ефірі(5мл) та перемішують протятрію, концентрують у вакуумі та хроматографують гом 2 годин, підігріваючи до температури довкілля на силікагелі(230 - 400меш,ЮОмл), елююючи гекРозчинники вилучають у вакуумі, та хроматограсан/етилацетатом(95/5) ВІДПОВІДНІ фракції об'єдфують на силікагелі(230 - 400меш, ЮОмл), елююнують та концентрують у вакуумі, одержуючи меючи гексан/етилацетатом(75/25) ВІДПОВІДНІ фрактиловий ефір (Е)-4-хлор-3-метил-2-бутеновоі ції об'єднують^ = 0,31, ТШХ, гексан/етилацетат, кислоти 4-Аміно-6-хлор-225/75) та концентрують у вакуумі, одержуючи замеркаптопіримідиниезилат(0,30г, 1,16ммоль) роззначену в заголовку сполуку, ЯМР (CDCI3) 7,15, чиняють в ДМФ(4мл) та гідриді натрію(0,06г, 7,04, 3,45, 3,40, 2,33, 1,20, 1,15 2,56ммоль) при температурі довкілля з подальшим доданням метилового ефіру (Е)-4-бром-3-метил-2Приклад 206 (Е)-г\І,г\І-Діетил-4-пдрокси-2бутенової кислоти(0,22г, 1,16ммоль) Реакційну пентенамід суміш перемішують протягом 15 годин, гасять До (Е)-г\І,г\І-діетил-4-оксо-2-пентенаміду(0,73г, надлишком води, екстрагують етилацетатом(3 х 4,31ммоль) в метанолі(Юмл), охолодженому до 20мл) Екстракти об'єднують, промивають сольо0°С, додають борпдрид натрію(0,18г, 4,75ммоль), вим розчином(20мл), сушать над сульфатом наперемішують в атмосфері азоту протягом ЗО хвитрію, концентрують у вакуумі та хроматографують лин, гасять надлишком води та екстрагують етина силікагелі(230 - 400меш, ЮОмл), елююючи геклацетатом(3 X 50мл) Органічні екстракти об'єдсан/етилацетатом(80/20) ВІДПОВІДНІ фракції об'єднують, промивають сольовим розчином(50мл), н у ю т ь ^ = 0,43, ТШХ, гексан/етилацетат, 50/50) та сушать над сульфатом натрію, концентрують у концентрують у вакуумі, одержуючи зазначену в вакуумі, одержуючи зазначену в заголовку сполузаголовку сполуку, т пл 134-136°С ку, ЯМР (CDCI3) 6,89, 6,42, 4,49,3,41,2,51, 1,33, 1,17 Приклад 209 Метиловий ефір (Е)-4-[(4-амшо6-хлор-2-піримідиніл)-тю]-3-метил-2-пентеновоі Приклад 207 (Е)-г\І,г\І-Діетил-4-[(4-аміно-6кислоти (сполука №209) хлор-2-піримідиніл)-тю]-2-пентенамід, (сполука №207) До метилового ефіру (Е)-4-пдрокси-3-метил-2пентенової кислоти(1,00г, 6,94ммоль) в метиленДо (Е)-г\І,г\І-Діетил-4-пдрокси-2хлориді, охолодженому до -15°С, у колбі, висушепентенаміду(0,67г, 3,93ммоль) в метиленхлориді, ній на вогні, додають дихлортрифенілфосфоохолодженому до -15°С, у колбі, висушеній на вогран(2,47г, 7,63ммоль) Реакційну суміш нагрівають ні, додають дихлортрифенілфосфоран (1,40г, до температури довкілля, гасять шляхом додання 4,33ммоль) Реакційну суміш нагрівають до темпельоду(Юмл), екстрагують метиленхлоридом(2 х ратури довкілля, гасять шляхом додання льоЮмл), промивають сольовим розчином(Юмл), ду(Юмл), екстрагують метиленхлоридом(3 20мл), сушать над сульфатом натрію, концентрують у промивають сольовим розчином(ЗОмл), сушать вакуумі, та хроматографують на силікагелі(230 над сульфатом натрію, концентрують у вакуумі та 400меш, 75мл), елююючи гекхроматографують на силікагелі(230 - 400меш, ЮОмл), елююючи гексан/етилацетатом(75/25) сан/етилацетатом(95/5) ВІДПОВІДНІ фракції об'єдВІДПОВІДНІ фракції об'єднують^ = 0,48, ТШХ, гекн у ю т ь ^ = 0,55, ТШХ, гексан/етилацетат, 75/25) та сан/етилацетат, 25/75) та концентрують у вакуумі, концентрують у вакуумі, одержуючи метиловий одержуючи (Е)-4-хлор-г\І,г\І-діетил-2-пентенаміду ефір (Е)-4-хлор-3-метил-2-пентеновоі кислоти 44-Амшо-6-хлор-2-меркаптопіримідинмезилат(0,56г, Амшо-6-хлор-2-меркаптопіримідинмезилат(0,30г, 2,19ммоль) розчиняють в ДМФ(4мл) та гідриді на1,16ммоль) розчиняють в ДМФ(4мл) та гідриді натрію(0,12г, 4,82ммоль) при температурі довкілля з трію(0,06г, 2,56ммоль) при температурі довкілля з подальшим доданням (Е)-4-хлор-г\І,г\І-діетил-2подальшим доданням метилового ефіру (Е)-4пентенаміду(0,41г, 2,19ммоль) Реакційну суміш хлор-З-метил-2-пентеновоі кислоти(0,19г, перемішують протягом 15 годин, гасять надлиш1,16ммоль) Реакційну суміш перемішують протяком води, екстрагують етилацетатом(3 х 25мл) гом 15 годин, гасять надлишком води, екстрагують Екстракти об'єднують, промивають сольовим розетилацетатом(3 х 15мл) Екстракти об'єднують, чином(25мл), сушать над сульфатом натрію, конпромивають сольовим розчином(15мл), сушать центрують у вакуумі та хроматографують на силінад сульфатом натрію, концентрують у вакуумі та кагелі(230 - 400меш, ЮОмл), елююючи градієнтом хроматографують на силікагелі(230 - 400меш, гексан/етил ацетату (80/20 - 60/40) ВІДПОВІДНІ фраЮОмл), елююючи сумішшю геккції об'єднують^ = 0,27, ТШХ, гексан/етилацетат, сан/етилацетат(85/15) ВІДПОВІДНІ фракції об'єдну25/75) та концентрують у вакуумі, одержуючи заю т ь ^ = 0,18, ТШХ, гексан/етилацетат, 50/50) та значену в заголовку сполуку, т пл 152-153°С концентрують у вакуумі, одержуючи зазначену в заголовку сполуку, т пл 124-126°С Приклад 208 Метиловий ефір (Е)-4-[(4-амшо6-хлор-2-піримідиніл)-тю]-3-метил-2-бутеновоі киПриклад 210 4-Амшо-6-хлор-2-(1 -(4-(1,1 слоти (сполука №208) диметил)етил-2-піридил)-етил)тюпіримідин, (сполука №210) До метилового ефіру (Е)-4-пдрокси-3-метил-2бутенової кислоти(0,75г, 5,76ммоль) в метиленЧастина А 4-трет-Бутил-піридин-г\І-оксид хлориді, охолодженому до -15°С, у колбі, висуше4-трет-Бутил-піридин(14,8мл, ЮОммоль) розній на вогні, додають дибромтрифенілфосфочиняють в 35мл льодяної оцтової кислоти в атморан(2,68г, 6,34ммоль) Реакційну суміш сфері азоту в 200мл одногорлій круглодонній колперемішують при -15°С - 0°С протягом двох годин, бі Розчин нагрівають до 95 - Ю0°С, обробляють 46 45 56992 30% перекисом водню(28мл, 274ммоль) та переМас-спектр Розраховано для C10H15NO мішують 6 годин Реакційну суміш обробляють 165,1154, Знайдено 165,1147, частинами параформальдегідом, аж доки не буде Частина С одержано негативну реакцію на крохмальному 4-трет-Бутил 2-пдроксиметилпіридин(4,13г, йодидному папері Леткі продукти вилучають у 25ммоль) розчиняють в 75мл діоксану в атмосфері вакуумі, та залишок азеотропно відганяють з 2 х азоту в 200-мл одногорлій круглодонній колбі ЮОмл толуолу Залишок розподіляють між 1 х Розчин обробляють дюксидом селену(1,53г, ЮОмл дихлорметану та 2 х 75мл насиченого біка13,75ммоль) та реакційну суміш нагрівають до 80 рбонату натрію Водний шар піддають зворотному 85°С протягом 1 години Суміш охолоджують, розпромиванню 3 х 50мл дихлорметану Об'єднані бавляють дихлорметаном та фільтрують крізь цеорганічні шари сушать над сульфатом магнію та літ Відфільтровану лепешку ретельно промиваконцентрують у вакуумі, одержуючи 14,5г(96%) 4ють дихлорметаном, та фільтрат концентрують до трет-бутил-піридин-г\І-оксиду у вигляді блідоянтарного масла Сире масло пропускають через жовтого твердого продукту 50г шару силікагелю(230 - 400меш), елююючи 20% 1 сумішшю ацетон/гексан, збираючи 100-мл-ві фраН-ЯМР (CDCI3, TMC) 5 1,32(с, 9), 7,27(м, 2), кції Фракції 1 - 3 об'єднують та концентрують, 8,15(м, 2) м д 13 одержуючи 3,91г(96%) 4-трет-бутил-2С-ЯМР (CDCI3) 5 30,3, 34,4, 122,9, 138,3, піридинкарбоксальдепду у вигляді світло150,7 м д янтарного масла ТШХ(силікагель-60, F-254) Rf = 0,42, 10% ме1 танол/дихлорметан Н-ЯМР (CDCI3, TMC) 5 1,36(с, 9), 7,53(м, 1), 7,99(м, 1), 8,70(м, 1) 10,10(0, 1)м д Температура плавлення 93 - 95°С 13 Інфрачервоний спектр(у max, мінеральне масС-ЯМР (CDCI3) 5 30,3, 35,0, 118,7, 124,9, ло) 3098, 2924, 1685, 1488, 1466, 1250, 1183, 150,1, 152,7, 161,5, 193,8 м д 825см 1 ТШХ(силікагель-60, F-254) R f = 0,62, 40% ацетон/гексан Мас-спектр Розраховано для C9H13NO 151,0997 Знайдено 151,0993 Інфрачервоний спектр(у max, рідина) 2968, 1712,1597, 1481, 1367, 1210, 822см ] Аналіз Розраховано для C9H13NO С, 71,49, Н, 8,67, N, 9,26 Знайдено С, 71,10, Н, 9,17, N, 9,20, Мас-спектр, [M/Z] (відносна інтенсивність) Частина В [324](71) 4-трет-Бутилпіридин-г\І-оксид(11,0г, Частина D 72,9ммоль) розчиняють в 200мл дихлориетану в Бромід метилмагнію(9,7мл, 29ммоль) додають атмосфері азоту в 500-мл одногорлій круглодонній до 20мл сухого тетрапдрофурану в атмосфері колбі Розчин обробляють тетрафторборатом триазоту в 100-мл двогорлій круглодонній колбі, виметилоксонію(10,8г, 72,9ммоль), перемішують 1 сушеній у печі при 0°С Розчин обробляють 4-третгодину при кімнатній температурі, та леткі продукбутил-2-піридинкарбоксальдепдом(3,8г, ти вилучають у вакуумі Твердий залишок розчи23,3ммоль) в 2 х 5мл діетилового ефіру, а потім няють в 200мл метанолу в 500-мл одногорлій круЮмл діетилового ефіру Реакційну суміш нагріваглодонній колбі Розчин нагрівають із зворотним ють до кімнатної температури, а потім до темперахолодильником, обробляють персульфатом амотури, при якій відбувається зрошення, протягом 1 нію(3,3г, 14,5ммоль) в 15мл води, та реакційну години Суміш охолоджують до 0°С, гасять 1 х суміш інтенсивно нагрівають із зворотним холоди20мл 10% соляної кислоти, та встановлюють рН 9 льником протягом ЗО хвилин Реакційну суміш об2н гідроксидом натрію Шари ВІДДІЛЯЮТЬ, ВОДНИЙ робляють другою частиною персульфату амошар екстрагують дихлорметаном 4 х 25мл, і об'єднію(1,65г, 7,2ммоль) в 7мл води та нагрівають із нані органічні шари сушать над карбонатом калію зворотним холодильником додатково ще протягом Сухі органічні шари концентрують у вакуумі, одер1 години Реакційну суміш охолоджують та об'єм жуючи 3,9г(93%) 4-трет-бутил-2-(1-пдроксиетил)метанолу вилучають у вакуумі Залишок розбавпіридину у вигляді жовтувато-коричневого твердоляють ЗООмл конц гідроксиду амонію, і суміш ексго продукту Аналітичний продукт одержують шлятрагують 4 х ЮОмл дихлорметану Об'єднані оргахом перекристалізації з гексану нічні шари сушать над карбонатом калію й 1 Н-ЯМР (CDCI3, TMC) 5 1,31 (с, 9), 1,50(д, J = концентрують у вакуумі до жовтого масла Сирий 6,5Гц, 3), 4,10(розшир, с, 1), 4,87(кв, J = 6,5, 13Гц, продукт хроматографують на 400г силікагелю(230 1), 7 18(м, 1), 7,26(м, 1), 8,41 (м, 1) м д - 400меш), елююючи 40% сумішшю ацетон/гексан, 1з С-ЯМР (CDCI3) 5 24,3, 30,4, 34,7, 69,1, 116,4, збираючи 50-мл-ві фракції Фракції 26 - 52 об'єд119,4, 147,8, 160,9, 162,9 м д нуютьта концентрують, одержуючи 8,79г(73%) 4ТШХ (силікагель-60, F-254) Rf = 0,37, 40% трет-бутил-2-пдроксиметилпіридину у вигляді жовацетон/гексан того масла Температура плавлення 85 - 86°С 1 Інфрачервоний спектр(у max, мінеральне масН-ЯМР (CDCI3l TMC) 5 1,31 (с, 9), ло) 3158, 2925, 1608, 1551, 1409, 1341, 1093, 3,99(розшир, с, 1), 4,75(с, 2), 7,18(м, 1), 7,27(м, 1), 1069см 1 8,43(м,1) м д 13 С-ЯМР (CDCI3) 5 30,5, 34,7, 64,5, 117,6, Мас-спектр, [M/Z] (відносна інтенсивність) 119,5, 148,3, 159,2, 161,0м д [179] (10), [164] (100) ТШХ(силікагель-60, F-254) R f = 0,31, 40% ацеАналіз Розраховано для C11H17NO C, 73,70, тон/гексан Н, 9,56, N, 7,82 Знайдено С, 73,79, Н, 9,91, N, Інфрачервоний спектр(у max, мінеральне мас7,74 ло) 3233, 2966, 1606, 1552, 1479, 1405, 1066см 1 Частина Е 48 47 56992 4-трет-Бутил 2-(1-пдроксиетил)піридин(3,6г, Аналіз Розраховано для C15H19CIN4S C, 20,1ммоль) розчиняють в 60мл дихлорметану в 55,80, Н, 5,93, N, 17,35 Знайдено С, 55,74, Н, атмосфері азоту в 200-мл одногорлій круглодонній 5,90, N, 17,16 колбі Розчин охолоджують до 0°С, обробляють Приклад 211 4-Амшо-6-хлор-2-(1-(2тюнілхлоридом(2,2мл, ЗОммоль) в Юмл дихлорпіридил)етил)тюпіримідин, (Сполука № 211) метану, та реакційну суміш перемішують 1 годину Частина А при 0°С, потім 2 години при кімнатній температурі До суспензії 4,6-дипдрокси-2-(2Реакційну суміш гасять 1 * 75мл насиченого бікапіридилметил)тюпіримідину(7,0г, 0,0298 моль) в рбонату натрію, шари розділяють, та водний шар 105мл диметилформаміду при кімнатній темпераекстрагують дихлорметаном 3 * 25мл Об'єднані турі додають імідазол(5,06г, 0,0744 моль, органічні шари сушать над карбонатом калію та 2,5еквів), потім третбутилдиметилсилілхлоконцентрують у вакуумі, одержуючи 3,9г(98%) 4рид(9,48г, 0,0626 моль, 2,10еквів) Реакційну сутрет-бутил-2-(1-хпоретил)піридину у вигляді жовміш перемішують протягом 2,5 годин, виливають в того масла 350мл води та екстрагують ДВІЧІ ефіром Об'єднані 1 органічні екстракти сушать з безводним N2SO4 та Н-ЯМР (CDCI3, TMC) 5 1,33 (с, 9), 1,89 (д, J = концентрують при пониженому тиску Сирий про6,5Гц, 3), 5,14 (кв, J = 6,5, 13Гц, 1), 7,21 (м, 1), 7,44 дукт розчиняють в суміші етилацетат(м, 1), 8,47 (м, 1) м д Гз метиленхлорид-метанол, обробляють 37г силікаС ЯМР(СОСІз) 5 24,7, 30,2, 34,6, 59,0, 117,8, гелю та концентрують до сипкого порошку Його 119,9, 148,7, 160,2, 161,0 м д вводять з набивкою у верхню частину колонки з ТШХ (силікагель-60, F-254) Rf = 0,61, 40% набивкою з силікагелю(350г) та елююють сумішшю ацетон/гексан етилацетат-гексан(1 10), одержуючи 7,81г(56%) Мас-спектр Розраховано для СцН-ібСІМ - СНз 4,6-ди-(трет-бутилдиметилсилілокси)-2-(2182,0747, Знайдено 182,0736, піридилметил)тюпіримідину Частино F Мезилатну сіль 4-амшо-6-хлор-2ТШХ (силікагель GF) Rf = 0,38 етилацетаттюпіримідину(1,29г, 5ммоль розчиняють в 8мл гексан(1 9) 1 сухого диметилформаміду в атмосфері азоту в 50Н-ЯМР(СОСІ3, ТМС) 5 8,55(д, 1Н, J = 5,01 Гц), мл одногорлій круглодонній колбі Розчин оброб7,64(дт, 1Н, J = 1,8, 7,72Гц), 7,47 (д, 1Н, J = ляють 60% гідридом натрію(400мг, 7,86Гц), 7,20 (т, 1Н, J = 16,72Гц), 5,70(с, 1Н), 10ммоль)(екзотерм), та суміш перемішують 1 го4,52(с, 2Н), 0,930(с, 18Н), 0,265(с, 12Н) м д дину 1-(1-Хлоретил)-5,6,7,8Частина В тетрапдроізохінолш(978мг, 5ммоль) в 2 > 2мл суРозчин н-бутиллітію(11,02мл, 17,63ммоль, хого диметилформаміду, додають до реакційної 1,2еквів , 1,6 М в гексані) в 60мл тетрапдрофурану суміші, і суміш перемішують протягом ночі при охолоджують до -78°С, обробляють краплями диікімнатній температурі Реакційну суміш виливають зопропиламшом(1,93г, 19,10ммоль, 1,3еквів) пров ЮОмл 50% насиченого хлориду натрію та ексттягом двохвилинного періоду Після перемішуванрагують етилацетатом 4 * 25мл Об'єднані органіня протягом наступних 10 хвилин додають чні шари піддають зворотному промиванню 50% краплями розчин 4,6-ди-(третнасиченим хлоридом натрію 4 * 50мл Органічні бутилдиметилсилілокси)-2-(2шари сушать над карбонатом калію та концентрупіридилметил)тюпіримідину(6,80г, 14,69ммоль) в ють у вакуумі до жовтого масла Сирий продукт 16мл тетрапдрофурану протягом 10 хвилинного хроматографують на 120г силікагелю(230 періоду Реакційну суміш поволі перемішують про400меш), елююючи 25% сумішшю ацетон/гексан, тягом ЗО хвилин та обробляють краплями метилзбираючи 22-мл-ві фракції Фракції 1 6 - 2 7 об'єдйодидом(2,29г, 16,16ммоль, 1,1еквів) в 6мл тетранують та концентрують, одержуючи білу піну Крипдрофурану протягом Зхвил періоду сталізація з діетилового ефіру дає 888мг(55%) 1Перемішування полегшують шляхом додання доамшо-4-хлор-2-(1-(4-(1,1-диметил)етил-2даткових ЗОмл тетрапдрофурану Через годину піридил)етил)тюпіримідину у вигляді білого тверпісля додання метилйодиду баню, що охолоджує, дого продукту вилучають, та суміші дають нагрітися до кімнатної 1 температури Вміст ПОТІМ виливають у воду з льоН-ЯМР (CDCI3l TMC) 5 1,30(с, 9), 1,76(д, J = дом та екстрагують один раз етилацетатом Орга6,5Гц, 3), 5,10(кв, J = 6,5, 13Гц, 1), 5,53(розшир, с, нічний шар промивають насиченим сольовим роз1), 6 10(с, 1), 7,14(м, 1), 7,45(м, 1), 8,46(м, 1) м д 1з чином, сушать з безводним Na2SO4 та С-ЯМР (CDCI3) 5 21 0, 30,4, 34,7, 45,5, 99,1, концентрують при пониженому тиску Розчин сиро119,2, 119,5, 148,9, 159,2, 160,7, 161,4, 163,3, 171,4 го продукту в метиленхлориді обробляють силікам д гелем(Збг), концентрують до сипкого порошку та ТШХ(силікагель-60, F-254) Rf = 0,49, 40% ацевводять у верхню частину колонки з набивкою з тон/гексан 350г силікагелю, та елююють сумішшю етилацеТемпература плавлення 153 - 154°С, розкл тат-гексан(5 95), одержуючи 2,23г(32%) 4,6-диУльтрафіолетовий спектр(Л max, етанол), (трет-бутилдиметилсилілокси)-2-(1-(2-піридил)нм(є) 230(22,700), 255(12,200), 268(8,790), етил)тюпіримідину 286(7,000) Інфрачервоний спектр(у max, мінеральне масТШХ (силікагель GF) Rf = 0,50 етилацетатло) 3177, 3140, 2925, 1642, 1565, 1527, 1368, гексан (1 9) 1 1280, 825см 1 Н-ЯМР (CDCIs, ТМС) 5 8,49(д, 1Н, J = Мас-спектр, [М/2](відносна інтенсивність) 4,80Гц), 7,54 (дт, 1Н, J = 1,81, 7,68Гц), 7,31 (д, 1Н, [322] (8),[289] (100) J = 7,84Гц), 7,06(т, 1Н, J = 4,93Гц), 5,59(с, 1Н), J = 49 5,01 (кв, 1H, J = 7,04Гц), 1,71(д, ЗН, J = 7,02Гц), 0,90 - 0,82(м, 18Н), 0,28 - 0,17(м, 12Н) м д Мас-спектр M/Z (відносна інтенсивність %) 477(5), 462(6), 444(79), 420(100), 315(34), 257(16) Частина С Розчин 4,6-ди-(трет-бутилдиметилсилілокси)2-(1-(2-піридил)етил) тюпіримідину(1,23г, 2,58ммоль) в 8мл тетрапдрофурану обробляють 2н НСІ(5,2мл, 10,31ммоль, 4,0еквів) при кімнатній температурі Через ЗО хвилин, реакційну суміш безпосередньо концентрують при пониженому тиску, розбавляють толуолом та знову повторно концентрують Отриманий білий твердий продукт розтирають на порошок з метиленхлоридом, збирають та сушать, одержуючи 0,819г сирого 4,6дипдрокси-2-(1-(2піридил)етил)тюпіримідинпдрохлориду ТШХ(силікагель GF) Rf = 0,32 хлороформгметанол (4 1) 1 Н-ЯМР(с^-ДМСО, ТМС) 5 8,55(розшир, с, 1Н), 7,80(м, 1Н), 7,53(д, 1Н, J = 7,72Гц), 7,31 (м, 1Н), 5,15(кв, 1Н, J = 7,04Гц), 4,35(с, 1Н), 3,72 3,26(розшир, с, 1Н), 1,66(д, ЗН, J = 6,95Гц) м д Частина D Сирий дюлпдрохлорид(0,735г, 2,58ммоль) обробляють 2-ПІКОЛІНОМ(0,446Г, 4,80ммоль, 1,86еквів,), потім оксихлоридом фосфору(4,39г, 28,7ммоль, 11,1 еквів) Вміст перемішують при 90°С на масляній бані протягом 2,25 годин і при температурі довкілля протягом наступних 1,75 годин Реакційну суміш гасять подрібненим льодом, потім насиченим розчином ЫаНСОз, аж доки вона не стане лужною, потім екстрагують ДВІЧІ етилацетатом Об'єднані органічні екстракти сушать з N2SO4 та концентрують при пониженому тиску Хроматографію виконують, використовуючи 125г силікагелю, з набивкою та елюююванням сумішшю етилацетат-гексан(1 6), одержуючи 0,569мг (73%) 4,6-дихлор-2-(1-(2піридил)етил)тюпіримідину ТШХ (силікагель GF) Rf = 0,50 етилацетатгексан (1 4) 1 Н-ЯМР(СОСІ3, ТМС) 5 8,56 (д, 1Н, J = 3,11 Гц), 7,61 (т, 1Н, J = 7,60Гц), 7,41 (д, 1Н, J = 7,86Гц), 7,14(м, 1Н), 6,96(с, 1Н), 5,08(кв, 1Н, J = 7,12Гц), 1,76(д, ЗН, и = 7,07Гц) м д Мас-спектр M/Z (відносна інтенсивність %) HRMS Розраховано 284,9894 Знайдено 284,9905 Частина Е Колбу завантажують 4,6-дихлор-2-(1-(2піридил)етил)тюпіримідином(0,560г, 1,96ммоль), ацетонітрилом(6,5мл) та 13мл 29% NH4OH Вміст перемішують при 35°С протягом 15 годин, виливають в 50мл води, екстрагують один раз етилацетатом Органічний шар промивають насиченим сольовим розчином(1 х ЗОмл), сушать з безводним Na2SO4Ta концентрують у вакуумі Хроматографію виконують на 100г силікагелю з набивкою та елююванням сумішшю етилацетат-гексан(2 3), одержуючи 0,491г (94%) 4-амшо-6-хлор-2-(1-(2піридил)етил)тюпіримідину ТШХ (силікагель GF) Rf = 0,23 етилацетатгексан (1 1) Температура плавлення 125 - 126°С 1 Н-ЯМР(СОСІ3, ТМС) 5 8,56(м, 1Н), 7,64(т, 1Н, J = 7,71 Гц), 7,46(д, 1Н, J = 7,82Гц), 7,17(м, 1Н), 56992 50 6,09(с, 1Н), 5,48(розшир, с, 2Н), 5,12(кв, 1Н, J = 7,16), 1,74(д, ЗН, J = 7,16Гц) м д Ультрафіолетовий спектр(Л max, етанол) 230(22,000), 255(12,500), 269sh 1(8580), 287(6920) Інфрачервоний спектр(у max, мінеральне масло) с м 1 1572, 1531, 2925, 1275, 2954, 1594, 1117, 1293, 3089, 2855, 1665, 1359, 1372, 803, 3133, 1467, 2868, 1436, 1477, 1255, 988, 3269, ЗОН, 1454, 1443, Мас-спектр M/Z (відносна інтенсивність %) 266(6), 233(100), 171(6), 138(26), 126(12), 106(98), 78(61) Аналіз Розраховано для C11H11CIN4S C, 49,62, Н, 4,13, N, 21,05, Знайдено С, 49,46, Н, 4,18, N, 20,45, Приклад 212 4-Аміно-6-хлор-2-(1 -(2-піридил)1-метилетил)-тюпіри-мідин, (Сполука № 212) Додержуючись способу одержання 4-амшо-6хлор-2-(1-(2-піридил)етил)тюпіримідину, але застосовуючи відповідне алкілювання 4,6-ди-(третбутилдиметилсилілокси)-2-(1 -(2піридил)етил)тюпіримідину метил йодидом, одержують цю сполуку Температура плавлення 183 184,5°С Приклад 213 4-Аміно-6-хлор-2-(1 -(2-(4метил)піридил)-1-метиле-тил)тюпіридин, (Сполука №213) Додержуючись способу одержання 4-амшо-6хлор-2-(1-(2-піридил)-1-метилетил)тюпіримідину та починаючи з 4,6-дипдрокси-2-(2-(4метил)піридилметил)тюпіримідину, одержують цю сполуку Температура плавлення 149 -151 °С Приклад 214 4-Амшо-6-хлор-2-(1 -(4-ціано-2піридил)етил)тюпіримідин, (Сполука № 214) Частина А Розчин 4-ціанопіридину(5,20г, 50,0ммоль) в 90мл метанолу обробляють сумішшю H2SO4(6,42r, 65,5ммоль, 1,31еквів ) та води(45мл) за один раз з подальшим доданням (NH4)2S2Os(22,8r, ЮОммоль, 2,0еквів) Вміст нагрівають із зворотним холодильником, при цьому здійснюють енергійну перегонку із зворотним холодильником протягом декількох хвилин Після перегонки із зворотним холодильником протягом 24 годин реакційну суміш частково концентрують до вилучення більшої частини метанолу, обробляють сумішшю льод-вода та підлужнюють гідроксидом амонію(20мл, 29%водн ) Залишок екстрагують чотири рази хлороформом, об'єднані екстракти сушать з безводним Na2SO4 та концентрують при пониженому тиску Хроматографію виконують, використовуючи 300г силікагелю з набивкою та елююванням сумішшю ацетон-метиленхлорид (1 6), одержуючи 2,65г(39,5%) 4-ціано-2-пдроксиметилпіридину ТШХ (силікагель GF) Rf = 0,30 ацетонметиленхлорид (1 4) 1 Н-ЯМР (CDCIs, ТМС) 5 8,78 (д, 1Н, J = 5,07Гц), 7,66 (с, 1Н), 7,49 (д, 1Н, J = 5,12Гц), 4,88 (д, 2Н, J = 4,96Гц), 3,64 (т, 1Н, J = 5,21 Гц) Ультрафіолетовий спектр (A max, етанол) 216 sh(7,710), 220 sh(6,590), 280 (3,510), 287 sh(3,020) Аналіз Розраховано для C7H6N2O Q 62,69, Н, 4,48, N, 20,89 Знайдено С, 62,66, Н, 4,46, N, 21,00 Мас-спектр M/Z (відносна інтенсивність %) 134(73), 133(100), 105(79), 104(39), 77(38), 50(30) 52 51 56992 Частина В ють метансульфонілхлорид (1,16 г, 10,22ммоль, 1,05 еквів), потім триетиламін (1,08 г, 10,70ммоль, Колбу завантажують 4-ціано-21,1 еквів) Після перемішування протягом 1 годипдроксиметилпіридином(2,60г, 19,40ммоль) та ни вміст концентрують безпосередньо при понидюксидом селену(1,19г, 10,75ммоль, женому тиску та отриманий твердий продукт, 40,554молярн еквів) в 40мл п-дюксану, і суміш націано-2-(2-метансульфоніл)етил-піридин, викорисгрівають на масляній бані при 80 - 85°С протягом товують безпосередньо в наступній реакції сполу3,5 годин Вміст розбавляють 150мл метиленхлочення риду, обробляють целітом та після перемішування при температурі довкілля протягом приблизно 15 ТШХ (силікагель GF) Rf = 0,69, ацетонхвилин фільтрують крізь пад з целіту Фільтрат метиленхлорид (1 6) концентрують у вакуумі, одержуючи 2,77г жовтого Частина Е твердого продукту, який хроматографують на 125г До суспензії NaH, що и перемішують(0,817г, силікагелю з набивкою та елююванням сумішшю 20,43ммоль, 2,1еквів, 60% масляна дисперсія), в ацетон-метиленхлорид-гексан(0,5 1,5 8), одержу35мл диметилформаміду при кімнатній темпераючи 2,32г(90%) 4-ціано-2-піридинкарбоксальдепду турі за один раз додають мезилатну сіль 4-аміноу вигляді білого твердого продукту 6-хлор-2-тюпіримідину(2,50г, 9,73ммоль) у вигляді твердого продукту Через 50хвил за один раз доТШХ (силікагель GF) Rf = 0,17 ацетондають суспензію 4-ціано-2-(2метиленхлорид-гексан(0,5 1,5 8) 1 метансульфоніл)етилпіридину(2,20, 9,73ммоль, Н-ЯМР(СОСІ3, ТМС) 5 9,93(с, 1Н), 8,82(д, 1Н, 1,0еквів) в 15мл диметилформаміду з промиванJ = 4,28Гц), 8,00(с, 1Н), 7,60(дд, 1Н, J = 4,84, ням 2 х 5мл того самого розчинника Через 24 го1,48 Гц) дину реакційну суміш швидко виливають в 200мл Температура плавлення 95 - 97°С води з льодом плюс 50мл насиченого сольового Ультрафіолетовий спектр (A max, етанол) 219 розчину, екстрагують ДВІЧІ етилацетатом та об'єдsh(7,130), 276(3,460), 283 sh(2,990) нані органічні екстракти сушать з безводним Аналіз Розраховано для C7H4N2O С, 63,64, Н, Na2SO4 Фільтрат концентрують у вакуумі, хрома3,03, N, 21,21 Знайдено С, 63,42, Н, 2,95, N, тографують на 200г силікагелю з набивкою та 21,26 елююванням сумішшю ацетон-метилен (1 9), одеМас-спектр M/Z (відносна інтенсивність %) + ржуючи 2,32г у вигляді золотистого масла, забру(FAB) [M + Н] 133(100), 104(22), 77(67) дненого диметилформамідом Повторна хроматоЧастина С графія, використовуючи 150г силікагелю з У колбу, завантажену 70мл ефіру та 40мл тетнабивкою та елююванням етил ацетат-гексан (2 3) рапдрофурану, охолодженого на льодяній бані при дає 1,75г(62%) Сполуки №214 у вигляді безбарв0 - 5°С, додають метилмагнійбромід(8,71мл, ного масла Кристалізацію виконують, використо26,14ммоль, 1,50еквів) за один раз До цього кравуючи суміш розчинників етилацетат-ефір-гексан плями додають розчин 4-ціано-2піридинкарбоксальдепду(2,30г, 17,42ммоль), розТШХ(силікагель GF) Rf = 0,50 ацетончиненого в 60мл ефіру та 5мл тетрапдрофурану, метиленхлорид (1 4) 1 протягом 20хвил періоду Отриману жовтуватоН-ЯМР(СОСІ3, ТМС) 5 8,61 (д, 1Н, J = 5,04Гц), коричневу суспензію нагрівають із зворотним хо7,63(с, 1Н), 7,23(д, 1Н, J = 5,03Гц), 6,00(с, 1Н), лодильником протягом 1,5 годин, охолоджують та 4,97(м, ЗН), 1,61 (д, ЗН, J = 7,30Гц) виливають в льодяну воду, що містить 55мл Зн Температура плавлення 119 - 120°С НСІ, та перемішують при температурі довкілля Ультрафіолетовий спектр(А max, етанол) 214 протягом 5 хвилин Вміст підлужнюють 23мл 29% sh(19,100), 222(23,600), 228 sh(22,300), 249 гідроксиду амонію та екстрагують 5 разів хлороsh(11,700), 286(9,860) формом Об'єднані органічні екстракти сушать над Інфрачервоний спектр(у max, мінеральне масNa2SO4 та концентрують при пониженому тиску ло) 1572, 1646, 2927, 1531, 2954, 1366, 1278, Хроматографують на 160г силікагелю, з набивкою 2855, 1546, 1119, 2869, 1469, 3188, 3314, 834, та елююванням сумішшю ацетон1457, 825, 1596, 3144, 3216, 1444, 855, 2979, 988, метиленхлорид(1 6), одержуючи 1,60г(62%) 43378 см 1 ціано-2-(2-пдрокси)етил піридину Аналіз Розраховано для C12H10CIN5S C, 49,48, Н, 3,44, N, 24,05 Знайдено С, 49,31, Н, ТШХ(силікагель GF) Rf = 0,27 ацетон3,69, N, 23,89 метиленхлорид (1 6) 1 Н-ЯМР(СОСІ3, ТМС) 5 8,46(д, 1Н, J = 4,33Гц), Мас-спектр M/Z (відносна інтенсивність %) 7,41 (с, 1Н), 7,20(дд, 1Н, J = 4,87, 0,82Гц), 4,72 (кв, 291(3), 293(1), 258(100), 196(5), 162(17), 131(33), 1Н, J = 6,08Гц), 3,75(с, 1Н), 1,28(д, ЗН, J = 6,55Гц) 103(18), 67(22) Ультрафіолетовий спектр(А max, етанол) 216 Приклад 215 Гідрохлорид 4-амшо-6-хлор-2-(1sh(7,760), 220 sh(6,530), 278(3,560), 287 sh(2,960) (4-метил-2-піридил)-етил)тюпіримідину, (Сполука №215) Аналіз Розраховано для С8Н8М2О С, 64,86, Н, 5,41, N, 18,92 Знайдено С, 64,77, Н, 5,51, N, Розчин 4-піколш-Т-оксиду(3,0г, 27,52ммоль) в 18,90 90мл метиленхлориду при кімнатній температурі взаємодіє з триметилоксонійтетрафторбораМас-спектр M/Z (відносна інтенсивність %) том(4,07г, 27,52ммоль, 1,0еквів) протягом 1,5 го(FAB) [M + Н]+ 149(100), 131(30), 105(8) дин Реакційну суміш концентрують безпосередЧастина D ньо при пониженому тиску, білий твердий продукт До розчину 4-ціано-2-(2розчиняють в 60мл метанолу, нагріваючи із зворопдрокси)етилпіридину(1,44г, 9,73ммоль) в 55мл тним холодильником, та обробляють персульфаметиленхлориду при кімнатній температурі дода 54 53 56992 том амонію(1,25г, 5,50ммоль, 0,20еквів) в 5,5мл ТШХ (силікагель GF) Rf = 0,70 ацетонводи з ще одним доданням персульфату амометиленхлорид (1 2) нію(0,625г, О.Юеквів) в 2,5мл води за ЗОхвил ПісУ спосіб, подібний до того, що його описано ля нагрівання із зворотним холодильником протядля одержання Сполуки №214, мезилатна сіль 4гом додаткових 40 хвилин вміст концентрують при амІно-6-хлор-2-тюпіримідину (1,49г, 5,81 ммоль) пониженому тиску, обробляють 75мл насиченого взаємодіє з 2-(2-метан-сульфоніл)етил-4Сольового розчину плюс 75мл води і, нарешті, метилпіридином (1,25г, 5,81 ммоль, 1,0еквів ) та 50мл Зн НСІ Після перемішування при кімнатній NaH (0,488г, 12,20ммоль, 2,1еквів, 60% масляна температурі протягом 1 години суміш підлужнюють дисперсія) з одержанням 0,869г (53%) 4-амшо-6за допомогою 20мл 29% гідроксиду амонію, екстхлор-2-(1-(4-метил-2-піридил)етил)тюпіримідину у рагують 4 рази хлороформом, об'єднані органічні вигляді безбарвного масла Отримання солі НСІ екстракти сушать з безводним Na2SO4 та концентпроводять шляхом додання ацетилхлориду(0,281г, рують у вакуумі Хроматографія, використовуючи 2,93ммоль, 1,0еквів) краплями до 5мл метанолу, 250г силікагелю з набивкою та елююванням суміохолодженого на льодяній бані Після перемішушшю ацетон-хлороформ-метанол(1 2 2%) дає вання протягом 25 хвил при температурі довкілля 2,65г(78%) 2-пдроксиметил-4-метилпіридину розчин розбавляють ЮОмл ефіру та додають краплями до 4-амшо-6-хлор-2-(1-(4-метил-2ТШХ (силікагель GF) Rf = 0,32 ацетонпіридил)етил)тюпіримідину(0,820г, 2,93ммоль, хлороформ-метанол(1 2 2%) 1 1,0еквів) в ЮОмл ефіру протягом 20 хвилинного Н-ЯМР (CDCI3l ТМС) 5 8,38(д, 1Н, J = періоду Після перемішування суспензії протягом 4 5,05Гц), 7,18(с, 1Н), 7,03(д, 1Н, J = 4,86Гц), 5,02(с, годин, додають ЮОмл гексану, перемішування Н), 4,75(с, 2Н), 2,37 (с, ЗН) продовжують протягом ще 2 годин, білий твердий УФ(Л max, етанол) 254 sh(2,240), 259(2,690), продукт збирають та сушать в вакуумній печі, оде266(2,180) ржуючи 0,845г(91%) Сполуки №215 Ефір, що заАналіз Розраховано для C7H9NO С, 68,29, Н, лишився, вилучають шляхом розчинен7,32, N, 11,38 Знайдено С, 67,35, Н, 7,37, N, ня/повторного осадження з суміші розчинників 11,22 метиленхлорид-гексан з подальшим сушінням при Мас-спектр M/Z (відносна інтенсивність %) 90°С у вакуумній печі протягом ночі 123(48), 122(100), 94(43), 93(30), 92(27), 39(17) У спосіб, подібний до того, що його описано Вільна основа ТШХ (силікагель GF) Rf = 0,26 для одержання 4-ціано-2-піридинкарбоксальдепду, ацетон-метиленхлорид (1 4) 2-пдроксиметил-4-метил-піридин(2,60г, Сіль НСІ 1Н-ЯМР(СОСІ3, ТМС) 5 8,49(д, 1Н, J 21,14ммоль) дає 2,0г(78%) 4-метил-2= 5,96Гц), 7,75(с, 1Н), 7,50(d, 1Н, J=5,57I~4), 6,12(с, піридинкарбоксальдепду 1Н), 5,23(кв, 1Н, и=7,42Гц), 2,56(с, ЗН), 1,69(д, ЗН, ТШХ (силікагель GF) Rf = 0,23 ацетонметилен-гексан(0,5 1,5 8,0) Температура плавлення 149 - 15°С Ультра1 Н-ЯМР (CDCI3 ТМС) 5 10,09(с, 1Н), 8,67(д, фіолетовий спектр(Л max, етанол) 229(22,000), 1Н, J = 4,93Гц), 7,81 (с, 1Н), 7,38(д, 1Н, J = 3,78Гц), 254(12,200), 267 sh(8,570), 287(6,820) 2,48(с, ЗН) Інфрачервоний спектр(у max, мінеральне масло) 2925, 1567, 2954, 2854, 1638, 1528, 2869, У спосіб, подібний до того, що його описано 1374, 828, 1466, 3163, 3296, 1283, 1254, 3203, для одержання 4-ціано-2-(2-пдрокси)етилпіридину, 1116, 3093, 3057, 2692, 985, 2538, 657, 1070, 1330, 4-метил-2-піридинкарбоксальдепд(2,0г, 960см 1 16,53ммоль) та метилмагнійбромід(8,30мл, 24,8ммоль, З М в ефірі) дають 1,95г(86%) 2-(1Аналіз Розраховано для C12H14CI2N4S C, пдрокси) етил-4-метилпіридину 45,43, Н, 4,42, N, 17,67, Знайдено С, 45,79, Н, 4,87, N, 17,28, ТШХ (силікагель GF) Rf = 0,30 ацетонметиленхлорид (1 2) Мас-спектр M/Z (відносна інтенсивність %) 1 280(8), 247(100), 211(2), 185(5), 152(33), 120(93), Н-ЯМР (CDCIs, ТМС) 5 8,27(д 1Н, J = 5,03Гц), 92(36) 6,99(с, 1Н), 6,90(д, 1Н, J = 4,83Гц), 4,74(кв, 1Н, J = 6,52Гц), 4,28(розшир, с, 1Н), 2,26(с, ЗН), 1,38(д, Приклад 216 4-Амшо-6-хлор-2-(1 -(4-етил-2ЗН, J = 6,58Гц) піридил)етил)тюпіримідин, (Сполука №216) Температура плавлення 76 - 78°С Розчин 4-етилпіридину(10,7г, О.Юмоль) в 35мл УФ(Л max, етанол) 253 sh(2,320), 259(2,810), оцтової кислоти, нагрітої до 95 - Ю0°С, обробля265(2,270) ють краплями 30% перекисом водню(28мл) протягом 18 хвилинного періоду Через 4 години надлиАналіз Розраховано для CsHnNO С, 70,07, Н, шок перекису водню розкладають, додаючи 8,03, N, 10,22 Знайдено С, 70,04, Н, 8,14, N, частинами параформальдепд(Ю.Ог) при темпера10,08 турі, що її підтримували раніше, аж доки не буде Мас-спектр M/Z (відносна інтенсивність %) отримано негативну реакцію при тесті з викорис137(7), 136(14), 122(100), 120(46), 93(38) танням йодиду крохмалю Реакційну суміш охоло2-(2-гІдрокси)етил-4-метилпіридин(0,796г, джують та концентрують при пониженому тиску 5,81ммоль), метансульфонілхлорид (0,695г, Залишок хроматографують на 325г силікагелю з б.Юммоль, 1,05еквів) та триетиламш(0,649г, набивкою та елююванням спочатку сумішшю аце6,39ммоль, 1,1еквів) при концентруванні при потон-хлороформ-метанол(3 6,7 0,3), а потім з градіниженому тиску дають 2-(2-метансульфоніл)-етилєнтом, що збільшується, метанолу, одержуючи 4-метилпіридин, який використовують безпосере10,55г(83%) 4-етилпіридин-1-оксиду дньо в наступному алкілюванні 56992 56 55 1 ТШХ (силікагель GF) Rf = 0,20 ацетонН-ЯМР(СОСІ3, ТМС) 5 8,29(д, 1Н, J= хлороформ-метанол(3 6,5 0,5) 7,15(с, 1Н), 6,84(д, 1Н, J=5,06l~4), 5,95(с, 1Н), 1 5,04(розшир, с, 2Н), 4,94(кв, 1Н, J=7,11 Гц), 2,48(кв, Н-ЯМР (CDCI3l ТМС) 5 7,94(д, 2Н, и=7,00Гц), 2Н, и=7,60Гц), 1,61(д, ЗН, и=7,13Гц), 1,09(с, ЗН, 6,93(д, 2Н, и=6,99Гц), 2,44 (кв, 2Н, J=7,61 Гц), 1,06 (т, ЗН, J=7,53I~4) У спосіб, подібний до того, що його описано Температура плавлення 113 - 115°С для одержання 4-пдроксиметил-4-метилпіридину, Ультрафіолетовий спектр(Л max, етанол) 4-етилпіридин-1-оксид(3,5г, 27,56ммоль) дає 230(22,500), 254(12,400), 267 sh(8,620), 286(6,940) 1,64г(43%) 4-етил-2-пдроксиметилпіридину Інфрачервоний спектр(у max, мінеральне масло) 1574, 2926, 1281, 1663, 2954, 1529, 1359, ТШХ (силікагель GF) Rf = 0,09 ацетон2855, 1363, 1114, 1560, 3147, 2870, 1608, 1467, метиленхлорид (1 2) 1 818, 3293, 1257, 988, 823, 836, 1484, 3051, 1209, Н-ЯМР(СОСІ3, ТМС) 5 8,50(д, 1Н, J=5,11I~4), 1 1059 см 7,32(с, 1Н), 7,15(д, 1Н, J=4,88I~4), 5,30(розшир, с, 1Н), 4,87(с, 2Н), 2,77(кв, 2Н, и=7,60Гц), 1,37(т, ЗН, Аналіз Розраховано для C13H15CIN4S C, J=7,63I~4) 53,06, Н, 5,10, N, 19,05 Знайдено С, 52,61, Н, 5,17, N, 18,84 Ультрафіолетовий спектр(Л max, етанол) 254 sh(2,260), 259(2,710), 264(2220) Мас-спектр M/Z (відносна інтенсивність %) Інфрачервоний спектр(у max, мінеральне мас294(6), 261(87), 166(40), 134(100), 119(67) ло) 1610, 2969, 3221, 1055, 2935, 1067, 1561, Приклад 217 4-аміно-6-хлор-2-(1 -(4-метил-22877, 839, 1459, 1417, 3059, 2841, 1005, 3020, піридил)-1-ціанометил)тюпіримідин (Сполука 1116, 994, 1364, 1481, 746, 2735, 890, 1327, 1264, №217) 1 902 см До 4-метил-2-піридинкарбоксальдепду(2,10г, 17,35ммоль), охолодженого при -10°С, додають 2н Мас-спектр M/Z (відносна інтенсивність %) НСІ, аж доки рН не сягне 3,5 Потім насичений (FAB) 138(100), 120(28), 106(4) водний розчин KCN, охолоджений при -10°С, доУ спосіб, подібний до того, що його описано дають краплями, аж доки рН не сягне 7 Осад збидля одержання 4-метил-2рають через 10 хвилин, промивають три рази вопіридинкарбоксальдепду, 4-етил-2дою та сушать, одержуючи 1,88г(73%) 2-(а-ціано-4пдроксиметилпіридин(1,60г, 11,68ммоль) дає метил)піридил карбінолу 1,33г(84%) 4-етил-2-піридинкарбоксальдепду ТШХ (силікагель GF) Rf = 0,23 ацетонТШХ (силікагель GF) Rf = 0,17 етилацетатметиленхлорид-гексан(0,5 1,5 8) гексан (1 2) 1 1 Н-ЯМР(СОСІ3, ТМС) 5 8,74(д, 1Н, и=4,95Гц), Н-ЯМР (CDCI3l ТМС) 5 8,47(д, 1Н, и=5,09Гц), 7,89(с, 1Н), 7,44(д, 1Н, и=5,08Гц), 2,82(кв, 2Н, 7,38(с, 1Н), 7,22(д, 1Н, и=5,09Гц), 6,31 и=7,58Гц), 1,37(т, ЗН, J=7,65I~4) 5,65(розшир, с, 1Н), 5,58(с, 1Н), 2,45(с, ЗН) У спосіб, подібний до того, що його описано Температура плавлення 99 - 102°С для синтезу 4-ціано-2-(2-пдрокси)етилпіридину, 4Ультрафіолетовий спектр(Л max, етанол) етил-2-піридинкарбоксальдепд (1,33г, 9,85ммоль) 243(3,230), 256(2,620), 264(2,260), 275 sh(939), та метилмагнійбромід(4,93мл, 14,78ммоль, З М в 374(369) ефірі) дає 1,29г(86%) 4-етил-2-(2Інфрачервоний спектр(у max, мінеральне маспдрокси)етилпіридину у вигляді безбарвного масло) 2924, 1056, 1613, 2854, 2954, 2867, 1013, 839, ла 3055, 2727, 3026, 1466, 963, 783, 1378, 1284, 1481, 1324, 1302, 604, 1169, 2626, 824, 669, 1411см 1 ТШХ (силікагель GF) Rf = 0,37 ацетонметиленхлорид (1 2) Мас-спектр M/Z (відносна інтенсивність %) 1 148(15), 119(5), 93(100), 65(52), 51(14), 38(58) Н-ЯМР(СОСІ3, ТМС) 5 8,19(д, 1Н, J=5,08l~4), 6,91 (с, 1Н), 6,83(д, 1Н, J=5,11I~4), 4,65(кв, 1Н, Мезилювання 2-(а-ціано-4J=6,51f4), 4,24(розшир, с, 1Н), 2,45 (кв, 2Н, метил)піридилкарбшолу(1,00г, 6,76ммоль) мета3=7,64Гц), 1,29(д, ЗН, и=6,57Гц), 1,06(т, ЗН, нсульфонілхлоридом(0,892г, 7,83ммоль, J=7,66) 1,16еквів) та триетиламшом(0,819г, 8,11ммоль, Мезилювання 4-етил-2-(21,2еквів) дає 2-(1-ціано-1пдрокси)етилпіридину(1,29г, 8,54ммоль) метан метансульфонілокси)метил-4-метилпіридин у висульфонілхлоридом(1,02г, 8,97ммоль, 1,05еквів ) гляді темно-червоного твердого продукту при конта триетиламшом(0,949г, 9,39ммоль, 1,1еквів) дає центруванні реакційної суміші при пониженому при концентруванні при пониженому тиску 4-етилтиску 2-(2-метансульфоніл)етилпіридин, який викорисТШХ (силікагель GF) Rf = 0,76 ацетонтовують у подальшій реакції алкілювання метиленхлорид (1 6) ТШХ (силікагель GF) Rf = 0,73 ацетонУ спосіб, подібний до того, що його описано метиленхлорид (1 2) для синтезу Сполуки №214, мезилатна сіль 4амшо-6-хлор-2-тю-піримідину(Сполука №110А, У спосіб, подібний до того, що його описано 1,74г, 6,76ммоль), NaH(0,568r, 14,20ммоль, для одержання Сполуки №214, мезилатна сіль 42,1еквів , 60% масляна дисперсія) та 2-(1-ціано-1амшо-6-хлор-2-тюпіримідину(2,19г, 8,54ммоль), метансульфонілоксиметил)-4-метилпіридин (1,53г, NaH(0,717r, 17,93ммоль, 2,1еквів 60% масляна 6,76ммоль, 1,0еквів) дають 0,927г(47%) 4-амшо-6дисперсія) та 4-етил-2-(2хлор-2-(1 -(4-метил-2-піридил)-1 метансульфоніл)етилпіридин(1,95г, 8,54ммоль, ціанометил)тюпіримідину 1,0еквів) дають 1,27г(51%) Сполуки №216 ТШХ (силікагель GF) Rf = 0,22 етилацетатТШХ(силікагель GF) Rf = 0,33 ацетонгексан (1 1) метиленхлорид (1 9) 57 56992 58 Н-ЯМР(С0С13, ТМС) 5 8,33(д, 1Н, J=5,00l~4), 5,25(т, 1Н, J=8,17I~4), 2,73(с, ЗН), 2,30-2,01 (м, 2Н), 7,28(с, 1Н), 6,97(д, 1Н, J=5,03l~4), 6,08(с, 1Н), 1,19(т, ЗН, J=7,35I~4) 5,80(с, 1Н), 5,15(розшир, с, 2Н), 2,24(с, ЗН) Температура плавлення 116 - 120°С Температура плавлення 145 - 146,5°С Ультрафіолетовий спектр(Л max, етанол) 230(22,500), 254(12,500), 267 sh(8,760), 287(6,940) Ультрафіолетовий спеісгр(Л max, етанол) 225(27,700), 246 sh(12,000), 266 sh(6,640), Інфрачервоний спектр(у max, мінеральне мас285(6,860), 312sh(1,730) ло) 2924, 1567, 2955, 2855, 1528, 1633, 2870, 1374, 1461, 828, 3164, 3295, 1279, 1249, 3203, Інфрачервоний cneicrp(v max, мінеральне мас1116, 3091, 3058, 2692, 2633, 986, 3453, 603, 1084, ло) 2925, 1573, 1637, 1531, 2954, 2965, 2855, 1 1207см 1288, 1373, 1607, 1272, 1464, 2869, 832, 3445, 1128, 3322, 3192, 986, 3216, 841, 3161, 850, 605, Аналіз (вільна основа) 1 3062см Розраховано для C13H15CIN4S С, 53,06, Н, Аналіз Розраховано для C12H10CIN5S C, 5,10, N, 19,05 49,48, Н, 3,44, N, 24,05 Знайдено С, 49,25, Н, Знайдено С, 52,68, Н, 5,29, N, 18,59 3,41, N, 23,87 Мас-спектр M/Z (відносна інтенсивність %) 294(14), 279(13), 261(100), 233(24), 166(14), Мас-спеїсгр M/Z (відносна інтенсивність %) 134(90) 291(32), 260(33), 258(100), 233(8), 163(15), 136(16) Приклад 218 4-аміно-6-хлор-2-(1 -(4-метил-2Мезилатна сіль Сполуки №218 піридил)пропил)-тюпіримідин, (Сполука №218) Температура плавлення 172 - 175°С 4-Метил-2-піридинкарбоксальдепд(1,21 г, Аналіз Розраховано для C14H19CIN4O3S2 C, Ю.Оммоль) та етилмагнійбромід(15,0мл, 43,08, Н, 4,87, N, 14,36 Знайдено С, 42,97, Н, 15,0ммоль, 1,5еквів 1 М в ТГФ) дають 0,776г 5,04, N, 14,03 (51%) 2-(1-пдроксипропил)-4-метилпіридину Приклад 219 4-аміно-6-хлор-2-(1 -(4-ацетил-2піридил)етил)тюпіримідин, (Сполука №219) ТШХ (силікагель GF) Rf = 0,28 ацетонметиленхлорид (1 4) 4-Ціано-2-піридинкарбоксальдепд(1,0г, 1 7,57ммоль) та метилмагнійбромід(6,31мл, Н-ЯМР (CDCI3l ТМС) 5 8,48(д, 1Н, J=5,06l~4), 18,92ммоль, 2,5еквів , 3,0 М в ефірі) дають 0,729г 7,20(с, 1Н), 7,11(д, 1Н, J=5,05l~4), 4,75(т, 1Н, (58%) 4-ацетил-2-(1-пдрокси)етилпіридину J=7,12f4), 4,55(розшир, с, 1Н), 2,48(с, ЗН), 2,07 1,91(м, 1Н), 1,91 - 1,74(м, 1Н), 1,06(т, ЗН, ТШХ (силікагель GF) Rf = 0,27 ацетонметиленхлорид (1 4) 1 Ультрафіолетовий спектр(Л max, етанол) 254 Н-ЯМР (CDCIs, ТМС) 5 8,68 (д 1Н, J=5,H~LO, sh(2,320), 259(2,800), 265(2,280) 7,76(с, 1Н), 7,61 (дд, 1Н, J=1,49, 5,05Гц), 4,97(кв, Інфрачервоний спектр(у max, мінеральне мас1Н, J=6,42I~4), 4,20(розшир, с, 1Н), 2,62(с, ЗН), ло) 1610, 2965, 2934, 825, 3374, 3258, 984, 2876, 1,52(д, ЗН, и=6,52Гц) 1454, 1462, 1127, 1052, 1564, 1095, 3056, 1428, Мас-спектр М/2(відносна інтенсивність %) 1407, 1003, 3019, 1379, 1477, 1328, 1348, 659, 165(7), 164(9), 150(100), 122(24) 680см 1 4-Ацетил-2-(1-пдрокси)етил піридин (0,729г, 4,42ммоль), метан сульфонілхлорид (0,554г, Мас-спектр M/Z (відносна інтенсивність %) 4,86ммоль, 1,1еквів) та триетиламш(0,536г, FAB 152(88), 134(24), 123(14), 109(41), 95(39), 5,30ммоль, 1,2еквів) дають при концентруванні за 81(48), 69(83), 55(100), 43(81) пониженого тиску 4-ацетил-2-(1 Обробка 2-(1 -пдроксипропил)-4метилпіридину(0,775г, 5,13ммоль) метансульфоніметансульфонілокси)етил піридин лхлоридом(0,659г, 5,78ммоль, 1,13еквів) та триТШХ (силікагель GF) Rf = 0,59 ацетонетиламшом(0,570г, 5,64ммоль, 1,1еквів) при конметиленхлорид (1 4) центруванні у вакуумі дає 2-(1 Мезилатна сіль 4-амшо-6-хлор-2метансульфонілокси)пропил-4-метилпіридин, який тюпіримідину(1,1 Зг, 4,42ммоль), NaH(0,371 г, використовують безпосередньо в наступній реакції 9,28ммоль, 2,1еквів , 60% масляна дисперсія) та 4алкілювання ацетил-2-(1ТШХ (силікагель GF) Rf = 0,62 ацетонметансульфонілокси)етилпіридин(1,07г, метиленхлорид (1 4) 4,42ммоль, 1,0еквів) дають 0,774г(57%) 4-амшо-6хлор-2-(1-(4-ацетил-2-піридил)етил)тюпіримідину Алкілювання мезилатної солі 4-амшо-6-хлор-2(Сполука №219) тюпіримідину(1,32г, 5,13ммоль) 2-(1метансульфонілокси)-пропил-4ТШХ (силікагель GF) Rf = 0,17 ацетонметилпіридином(1,17г, 5,13ммоль, 1,0еквів) та метиленхлорид (1 9) 1 NaH(0,431r, 10,77ммоль, 2,1еквів , 60% масляна Н-ЯМР(СОСІ3, ТМС) 5 8,75(д, 1Н, J=3,79I~4), дисперсія) дає 0,726г (48%) 4-амшо-6-хлор-2-(1-(47,96(с, =1Н), 7,58(дд, 1Н, J=1,24, 3,79Гц), 6,11(с, метил-2-піридил)пропил)тюпіримідину Обробка 1Н), 5,17 (кв, 1Н, и=5,40Гц), 5,08(розшир, с, 2Н), Сполуки №218(0,294г, 1,0ммоль) м етан сул ьфо но2,63(с, ЗН), 1,79(д, ЗН, J=5,41) вою кислотою(0,096г, 1,0ммоль, 1,0еквів) в ефірі Температура плавлення 149 - 150°С дає аналітична чисту мезилатну сіль Сполуки Ультрафіолетовий спектр(Л max, етанол)№218(0,372г, 95%) 227(27,400), 249 sh(11,400), 288(9,370) Інфрачервоний спектр(у max, мінеральне масТШХ (силікагель GF) Rf = 0,20 етилацетатло) 1568, 2925, 2954, 1692, 1555, 1526, 1653, гексан (1 2) Сіль НСІ 1 1275, 2855, 3208, 1369, 1115, 3372, 3329, 1284, Н-ЯМР (CDCI3l ТМС) 5 8,66(д 1Н, J=6,07l~4), 3224, 601, 815, 1460, 982, 1105, 1259, 621, 849, 7,87(с, 1Н), 7,63(д, 1Н, и=6,04Гц), 6,22(с, 1Н), 1445см 1 1 59 56992 Аналіз Розраховано для C13H13CIN4OS C, 50,65, Н, 4,22, N, 18,18, Знайдено С, 50,40, Н, 4,28, N, 18,16, Мас-спеїсгр M/Z (відносна інтенсивність %) 308(4), 275(100), 148(33), 105(13) Приклад 220 4-аміно-6-хлор-2-(1-(4-метил-2піридил)-1-карбомето-ксиметил)тюпіримідин (Сполука №220) Колбу завантажують 2-(1 -ціано-1 гід рокси)метил-4-метилпіридином(0,863г, 5,83ммоль) в 3,5мл метанолу, обробляють 1,8мл концентрованої Na2SO4, потім 0,30мл води, і суміш нагрівають із зворотним холодильником протягом 1,25 години Вміст охолоджують, виливають в 50мл насиченого ІЧаНСОз, екстрагують ДВІЧІ етилацетатом, об'єднані органічні екстракти сушать над безводним Na2SO4 й фільтрат концентрують при пониженому тиску Хроматографічне очищення виконують, використовуючи 75г силікагелю, набивку та елюювання сумішшю ацетон-метиленхлорид (1 6), одержуючи 0,739г (70%) 2-(1-карбометокси-1-пдрокси)метил4-метил-піридину ТШХ (силікагель GF) Rf = 0,35 ацетонметиленхлорид (1 4) 1 Н-ЯМР (CDCI 3 l TMC) 5 8,41 (с, 1Н), 7,30(с, 1Н), 7,09(д, 1Н, и=3,75Гц), 5,25(с, 1Н), 3,76(с, ЗН), 2,37(с, ЗН) Мас-спектр M/Z (відносна інтенсивність %) 181(0,4), 150(0,3), 122(100), 92(32) 2-(1 -Карбометокси-1 -пдрокси)метил-4метилпіридин(0,735г, 4,06ммоль), метансульфонілхлорид(0,509г, 4,47ммоль, 1,1 еквів ) та триетиламш(0,492г, 4,87ммоль, 1,2еквів) дають 2-(1карбометокси-1-метансульфонілокси)метил-4метилпіридин за безпосередньої концентрації у вакуумі ТШХ (силікагель GF) Rf = 0,70 ацетонметиленхлорид (1 9) Алкілювання мезилатної солі 4-амшо-6-хлор-2тюпіримідину(1,04г, 4,06ммоль) NaH(0,341 г, 8,53ммоль, 2,1еквів , 60% масляна дисперсія) та 2(1-карбометокси-1-метансульфонілокси)метил-4метилпіридином(1,05г, 4,06ммоль, 1,0еквів ) дає 0,765г (58%) 4-амшо-6-хлор-2-(1 -(4-метил-2піридил)-1-карбометоксиметил)тюпіримідину ТШХ (силікагель GF) Rf = 0,26 ацетонметиленхлорид (1 6) 1 Н-ЯМР (CDCIs, TMC) 5 8,44(д, 1Н, и=4,99Гц), 7,36(с, 1Н), 7,06(д, 1Н, и=5,06Гц), 6,15(с, 1Н), 5,77(с, 1Н), 5,40(розшир, с, 2Н), 3,79(с, ЗН), 2,37(с, ЗН) Температура плавлення 137,5 - 139°С Ультрафіолетовий спектр(Л max, етанол) 228(25,77), 250 sh(12,300), 267 sh(7,650), 286(6,880) Інфрачервоний спектр(у max, мінеральне масло) 1573, 2925, 1645, 1736, 1532, 2955, 2964, 1188, 1167, 2855, 1282, 1292, 1603, 1368, 1124, 828, 1158, 835, 1430, 2869, 3461, 1467, 3188, 3315, 3163см 1 Аналіз Розраховано для C13H13CIN4O2S C, 48,15, Н, 4,01, N, 17,28 Знайдено С, 47,99, Н, 4,10, N, 17,11 60 Мас-спектр МС(відносна інтенсивність %) 324(11), 293(42), 291(100), 265(37), 229(9), 196(7), 171(20), 136(39) Приклад 221 4-Аміно-6-хлор-2-(1 -(4-(1 метилетеніл)-2-піридил)-етил)тюпіримідин, (Сполука №221) Суспензію метилтрифенілфосфонійброміду(14,90г, 0,0417моль, 2,2еквів) в 170мл ТГФ, охолоджену до 0 - 5°С, обробляють краплями нбутиллтєм(26,1мл, 0,0417моль, 2,2еквів , 1,6 М у гексані) протягом періоду 20 хвилин Після перемішування протягом додаткових 35хвил 4-ацетил2-(2-пдрокси)етилпіридин(3,13г, 0,0190моль, 1,0еквів), розчинений в 25мл ТГФ, додають краплями до реакційної суміші протягом 20хвил періоду За 3,5 години вміст виливають в 500мл води з льодом, екстрагують 4 рази етилацетатом та об'єднані органічні екстракти сушать з безводним Na2SO4 Концентрований фільтрат хроматографують на 500г силікагелю з набивкою та елююванням сумішшю етил ацетат-гексан (1 1), одержуючи 2,55г (82%) 4-(1-метилетеніл)-2-(1пдрокси)етил піридину ТШХ (силікагель GF) Rf = 0,23 етилацетатгексан (1 1) 1 Н-ЯМР (CDCIs, TMC) 5 8,47(д, 1Н, и=5,30Гц), 7,33(с, 1Н), 7,24(дд, 1Н, J=1,75, 5,21 Гц), 5,58(с, 1Н), 5,28(с, 1Н), 4,90(кв, 1Н, и=6,53Гц), 4,40(розшир, с, 1Н), 2,15(с, ЗН), 1,52(д, ЗН, Мас-спектр М/2(відносна інтенсивність %) 163(11), 162(13), 148(100), 146(40), 120(23) 4-(1 -Метилетеніл)-2-(1 пдрокси)етилпіридин(0,775г, 4,75ммоль), метансульфонілхлорид(0,670г, 5,88ммоль, 1,24еквів) та триетиламш(0,576г, 5,70ммоль, 1,2еквів) дають 4(1 -метилетеніл)-2-(1 метансульфонілокси)етилпіридин при концентруванні за пониженого тиску ТШХ (силікагель GF) Rf = 0,31 етилацетатгексан (1 1) 4-(1 -Метилетеніл)-2-(1 метансульфонілокси)етилпіридин(1,14г, 4,75ммоль), NaH(0,399r, 9,98ммоль, 2,1еквів, 60% масляна дисперсія) та мезилатна сіль 4-амшо-6хлор-2-тюпіримідину(1,22г, 4,75ммоль, 1,0еквів ) дають 0,801г (55%) 4-амшо-6-хлор-2-(1-(4-(1метилетеніл)-2-піридил)етил)тюпіримідину ТШХ (силікагель GF) Rf = 0,22 етилацетатгексан (1 1) 1 Н-ЯМР (CDCIs, TMC) 5 8,51 (д, 1Н, и=5,28Гц), 7,53(с, 1Н), 7,19(дд, 1Н, J=1,80, 5,20Гц), 6,10(с, 1Н), 5,58(с, 1Н), 5,30 - 5,09(м, 4Н), 2,14(с, ЗН), 1,77(д, ЗН, и=7,19Гц) Температура плавлення 133 - 135°С Ультрафіолетовий спектр(Л max, етанол) 231(28,200), 250 sh(19,900),285(9,270) Інфрачервоний спектр(у max, мінеральне масло) 1569, 1529, 2925, 1642, 1281, 2953, 1359, 1119, 1600, 1367, 2855, 1467, 3184, 828, 3314, 3364, 1378, 902, 1052, 986, 3217, 2982, 1263, 603, 911см1 Аналіз Розраховано для C14H15CIN4S C, 54,90, Н, 4,90, N, 18,30 Знайдено С, 54,61, Н, 5,11, N, 17,99
ДивитисяДодаткова інформація
Назва патенту англійськоюA- pyrimidine-thioalkyl substituted and a- pyrimidine-oxo-alkyl substituted compounds
Назва патенту російськоюA-пиримидинтиоалкилзамещенные и a-пиримидиноксоалкилзамещенные соединения
МПК / Мітки
МПК: C07D 487/04, A61K 31/535, C07D 239/46, C07D 405/12, C07D 491/048, C07D 401/14, C07D 409/12, C07D 413/12, C07D 401/12, A61K 31/505, A61P 31/12, C07D 239/56, C07D 491/04, C07D 239/60, C07D 239/38, C07D 471/04
Мітки: a-піримідинтіоалкілзаміщені, сполуки, a-піримідиноксоалкілзаміщені
Код посилання
<a href="https://ua.patents.su/83-56992-a-pirimidintioalkilzamishheni-ta-a-pirimidinoksoalkilzamishheni-spoluki.html" target="_blank" rel="follow" title="База патентів України">a-піримідинтіоалкілзаміщені та a-піримідиноксоалкілзаміщені сполуки</a>
Попередній патент: Установка безпилової видачі коксу з печей коксової батареї
Наступний патент: Захисний штекер
Випадковий патент: Спосіб хімічного осадження металу на алмазні зерна та електроліт для хімічного осадження металу на алмазні зерна












