Заміщені аліфани, циклофани, гетерафани, гетерофани, гетеро-гетерафани й металоцени, придатні для використання при лікуванні інфекції вгс
Номер патенту: 110976
Опубліковано: 10.03.2016
Автори: Ван Кіупін, Уайлс Джейсон Алан, Хасімото Акіхіро, Пейс Ґудвін, Чен Давей, Гадхачанда Венкат, Дешпанде Майлінд, Фадкі Авінаш, Ван Ксянжу
Формула / Реферат
1. Сполука формули
T-R-J1-W-A-W-J1-R-T;
T-R-J1-A-J1-R-T;
T-R-J2-A-J2-R-T;
T-R-J1-W-A-J1-R-T;
T-R-J1-W-A-J1R-T або
T-R-J1-A-J2-R-T
або її фармацевтично прийнятна сіль;
де
Т є незалежно вибраним у кожному випадку та представлений Тk, де k є цілим числом від 1 до 2;
Т1 представлений -Y-Z, де Y є ковалентно зв'язаним з R і Y є зв'язком, С1-С4алкіленом, необов'язково заміщеним оксо; і Z є 5- або 6-членною гетероциклічною групою, кожний з-поміж Т1 є (і) заміщеним щонайменше одним замісником, вибраним з-поміж -(С=О)ОН, -(C=O)NH2, -(С=О)Н, -С1-С4алкокси, С2-С4алканоїлу, складного С1-С4алкілового ефіру, складного С1-С4алкеніленового ефіру, моно- або ді-С1-С4алкілкарбоксаміду, й (іі) необов'язково заміщеним одним або декількома замісниками, незалежно вибраними з-поміж галогену, гідроксилу, С1-С2алкілу й С1-С2алкокси; і
Т2 є незалежно вибраним у кожному випадку з-поміж С2-С6алканоїлу, складного С1-С6алкілового ефіру, складного С1-С6алкенілового ефіру, С1-С6алкілсульфонаміду, С1-С6алкілсульфонілу, С2-С6алканоїлу, заміщеного моно- або ді-С1-С6гідрокарбілкарбаматом, С2-С6алканоїлу, заміщеного сечовиною або моно- або ді-С1-С6алкілсечовиною, і С2-С6алканоїлу, заміщеного моно- або ді-С1-С6алкілкарбоксамідом, кожний з Т2 необов'язково заміщений одним або декількома замісниками, незалежно вибраними з-поміж аміно, ціано, гідроксилу, галогену, (С1-С4алкоксі)С0-С4алкілу, (моно- і ді-С1-С4алкіламіно)C0-C4алкілу, С1-С6алкілу, (С1-С4тіоалкіл)С0-С4алкілу, С3-С7циклоалкілу, фенілу, С1-С4галогеналкілу й С1-С4галогеналкокси;
R є незалежно вибраним у кожному випадку з 4-6-членних кілець, що містять один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, де R є насиченим або містить 1 ненасичений зв'язок і необов'язково приєднаний за допомогою метиленового або етиленового містка, або є конденсованим з фенільним або з 5-6-членним гетероарильним кільцем; і
6-10-членних конденсованих або спіробіциклічних кільцевих систем, які містять один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, де 6-10-членне біциклічне кільце є насиченим або містить один ненасичений зв'язок;
кожна із груп R є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними із ціано, гідроксилу, галогену, С1-С2алкілу, С1-С2алкокси, С1-С2галогеналкілу, С1-С2галогеналкілу, С1-С2галогеналкілену й С1-С2алкілсульфонілу;
J1 є фенілом або 5-6-членною гетероарильною групою, яка містить 1-3 гетероатомів, незалежно вибраних з-поміж N, О і S, де кожна із груп J1 є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж аміно, ціано, гідроксилу, галогену, С1-С4алкілу, С1-С4алкокси, моно- і ді-С1-С4алкіламіно, С1-С2галогеналкілу й С1-С2галогеналкокси;
J2 є 8-10-членною гетероарильною групою, яка містить 1-4 гетероатоми, незалежно вибрані з-поміж N, О і S, де J2 необов'язково заміщений одним або декількома замісниками, незалежно вибраними з-поміж аміно, ціано, гідроксилу, галогену, С1-С4алкілу, С1-С4алкокси, моно- і ді-С1-С4алкіламіно, С1-С2галогеналкілу й С1-С2галогеналкокси;
W незалежно вибирається у кожному випадку і є фенільною, піридильною або алкінільною групою, необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж аміно, ціано, гідроксилу, галогену, С1-С4алкілу, С1-С4алкокси, моно- і ді-С1-С4алкіламіно, С1-С2галогеналкілу й С1-С2галогеналкокси;
А представлене [j.k]-циклофано, [j.k]-гетерафаном, [j.k]-гетерофаном, [j.k]-гетеро-гетерафаном або [j.k]-аліфаном; де j є цілим числом від 1 до 4, k є цілим числом від 0 до 4, різниця між j і k становить не більше ніж 2, і кожний лінкер з j і k необов'язково містить гетероатом, вибраний з-поміж N, О і S, і є необов'язково заміщеним одною оксогрупою й одним або декількома замісниками, незалежно вибраними з-поміж галогену, гідрокси, аміно, С1-С2алкілу й С1-С2алкокси; або
А представлене [j.k.j'.k']-циклофаном, де j, j', k і k' є цілими числами від 1 до 4, різниця між j і k або k' становить не більше ніж 2, різниця між j' і k або k' становить не більше ніж 2, і кожний лінкер з j, j', k і k' необов'язково містить гетероатом, вибраний з-поміж N, О і S, і є необов'язково заміщеним однією оксогрупою й одним або декількома замісниками, незалежно вибраними з-поміж галогену, гідрокси, аміно, С1-С2алкілу й С1-С2алкокси;
або
А є групою формули 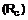 або
або 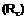 , де Q є нейтральним або катіонним металом, кожна із цих груп А є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси; або
, де Q є нейтральним або катіонним металом, кожна із цих груп А є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси; або
А є групою формули ![]() , де А є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси.
, де А є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси.
2. Сполука або сіль за п. 1, де А представлене будь-яким з
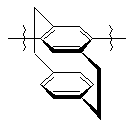 ,
,
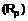 ,
,
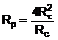 ,
,
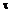 або
або
 .
.
3. Сполука або сіль за п. 1, де
W є фенілом, необов'язково заміщеним одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси.
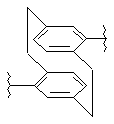
4. Сполука або сіль за п.1, де J1 представлене
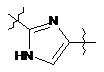 .
.
5. Сполука або сіль за п. 1, де
J2 представлене бензимідазольною групою, необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С2алкілу й С1-С2алкокси.
6. Сполука або сіль за п. 1, де кожна із груп R є незалежно вибраною з-поміж
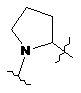 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
, 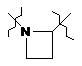 ,
, 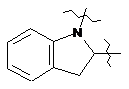 ,
,  ,
, 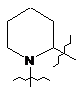 ,
,
 ,
, 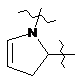 ,
,  ,
,  і
і  ,
,
кожна з них є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж галогену, С1-С4алкілу і С1-С4алкокси.
7. Сполука або сіль за п. 13, де група R є незалежно вибраною з-поміж
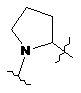 ,
,  і
і  .
.
8. Сполука або сіль за п. 1, де Т є незалежно вибраним С2-С6алканоїлом, заміщеним моно- і ді-С1-С6алкілкарбаматом, кожна із цих груп Т є необов'язково заміщеною (С1-С4тіоалкіл)С0-С4алкілом.
9. Сполука або сіль за п. 1, формули
T-R-J2-A-J2-R-T; де
А є групою формули
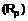 ;
;
J2 є 10-членною гетероарильною групою, яка містить 1 або 2 гетероатоми, незалежно вибрані з-поміж N, О і S, де J2 є необов'язково заміщеним одним або декількома замісниками, незалежно вибраними з-поміж аміно, ціано, гідроксилу, галогену, С1-С4алкілу, С1-C4алкокси, моно- і ді-С1-С4алкіламіно, С1-С2галогеналкілу й С1-С2галогеналкокси;
кожна із груп R є незалежно вибраними 8-10-членними біциклічними кільцевими системами, які містять один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, де 8-10-членне біциклічне кільце є насиченим або містить 1 ненасичений зв'язок;
кожна із груп R є необов'язково заміщеною одним або декількома замісниками, незалежно вибраними з-поміж ціано, гідроксилу, галогену, С1-С2алкілу, С1-С2алкокси, С1-С2галогеналкілу, С1-С2галогеналкілу, С1-С2галогеналкілену й С1-С2алкілсульфонілу; і
Т є Т2.
10. Сполука або сіль за п. 1, де сполука є

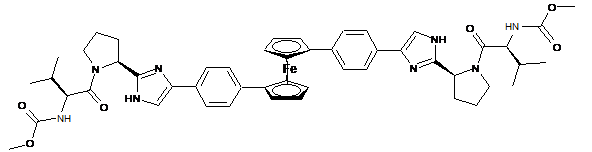 ,
,
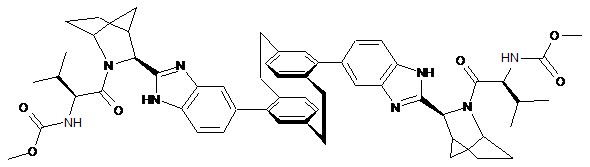 ,
,
 ,
,
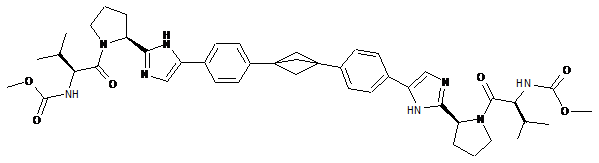 ,
,
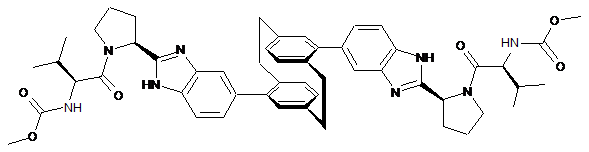 ,
,
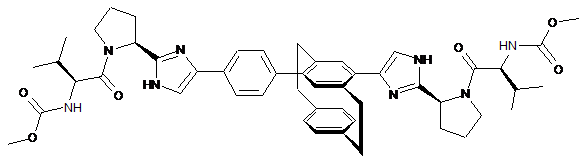 ,
,
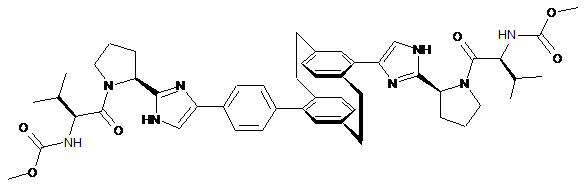 ,
,
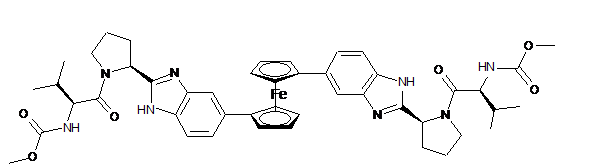 ,
,
 ,
,
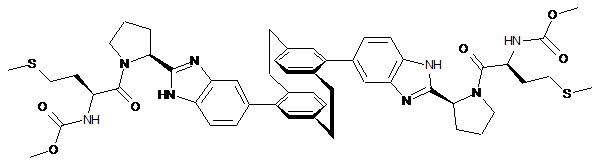 ,
,
 ,
,
 ,
,
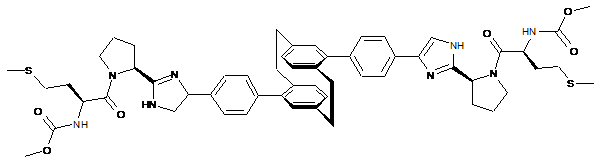 ,
,
 ,
,
 ,
,
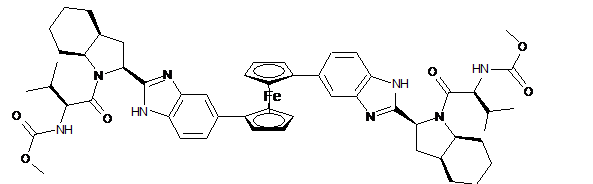 ,
,
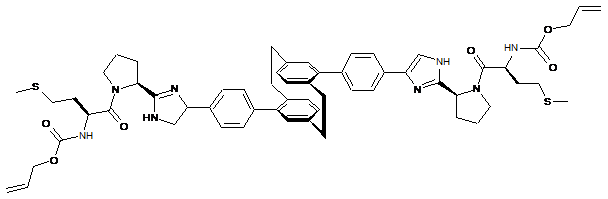 ,
,
 ,
,
 ,
,
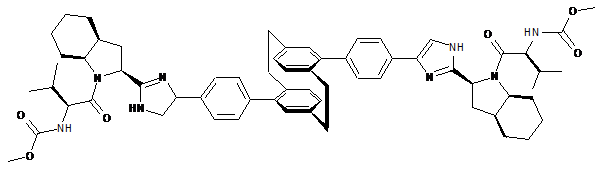 ,
,
 ,
,
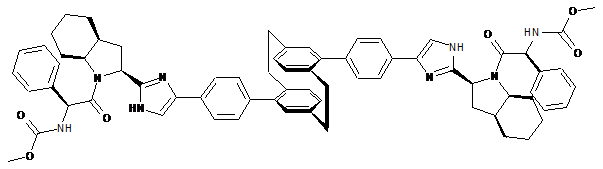 ,
,
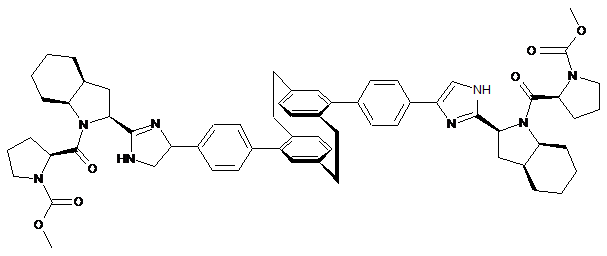 ,
,
 ,
,
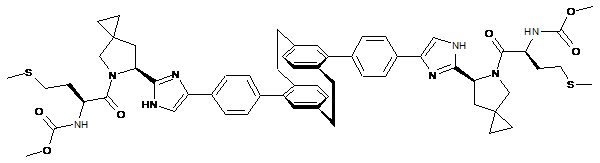 ,
,
 ,
,
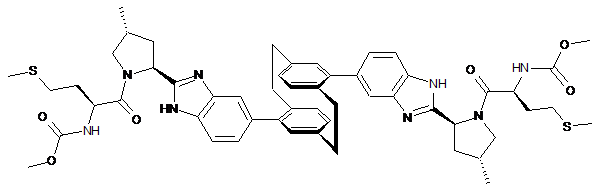 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
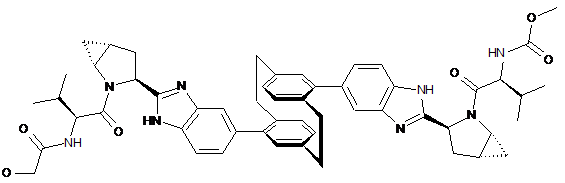 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
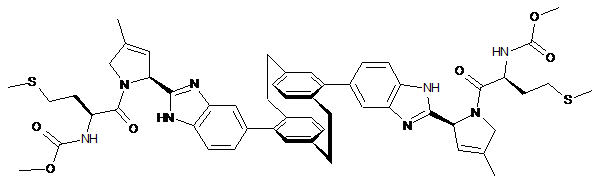 ,
,
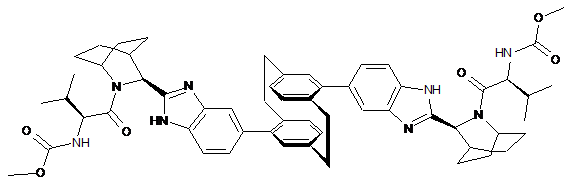 ,
,
 ,
,
 ,
,
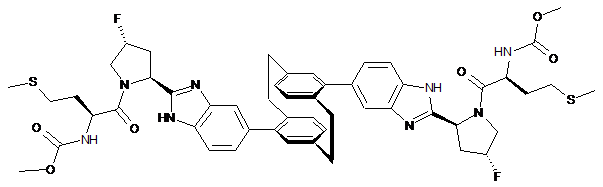 ,
,
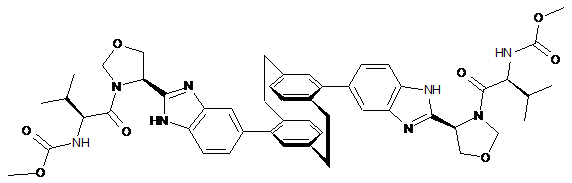 ,
,
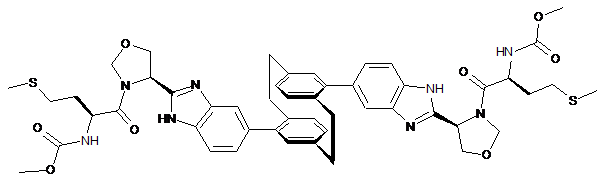 ,
,
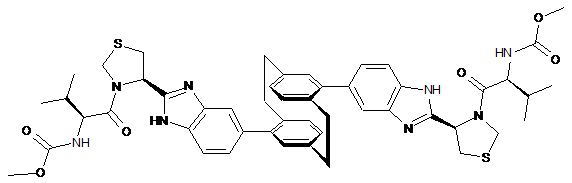 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
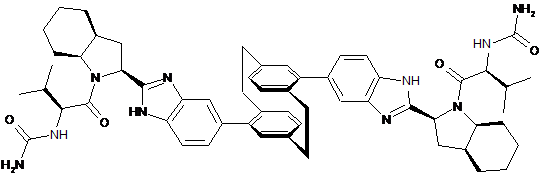 ,
,
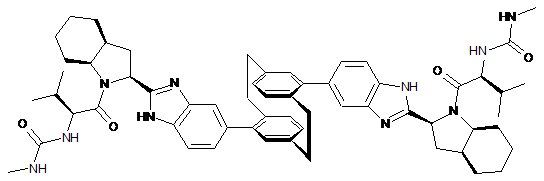 ,
,
 ,
,
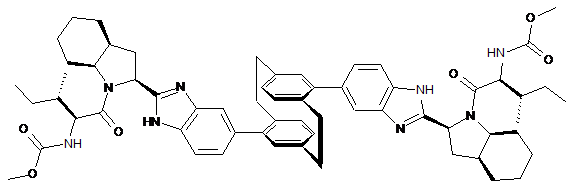 ,
,
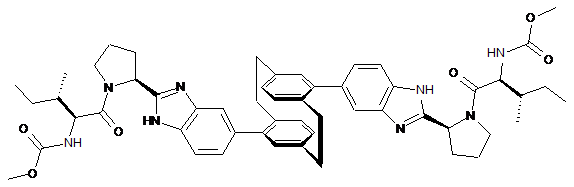 ,
,
 ,
,
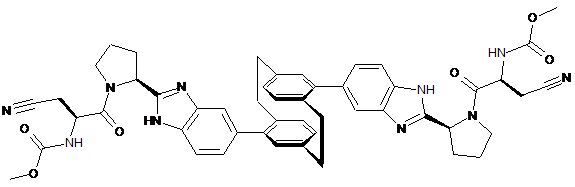 ,
,
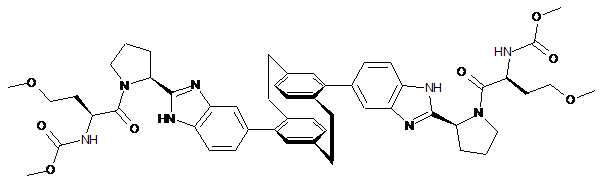 ,
,
 ,
,
 ,
,
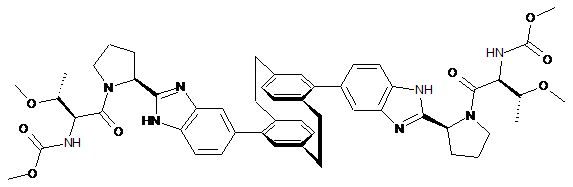 ,
,
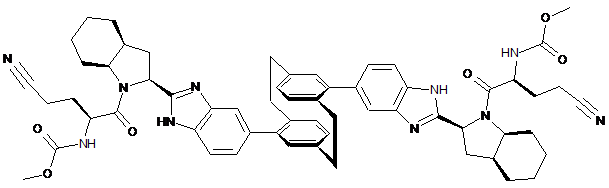 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
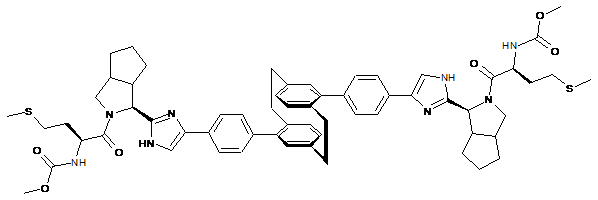 ,
,
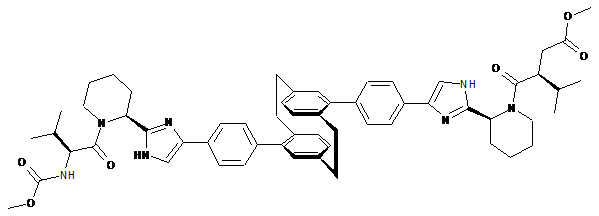 ,
,
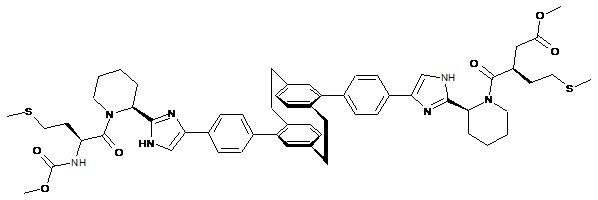 ,
,
 ,
,
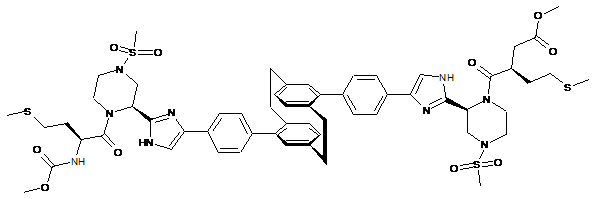 ,
,
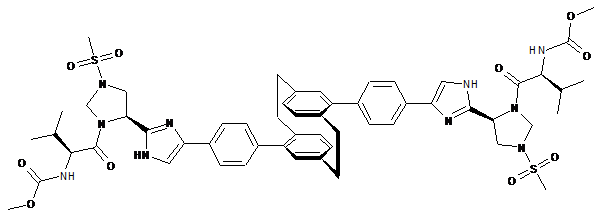 ,
,
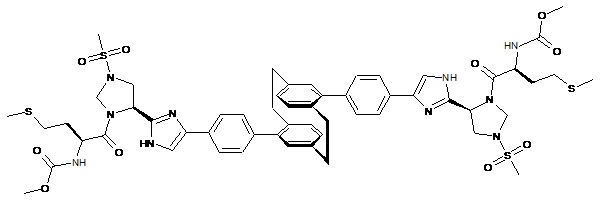 ,
,
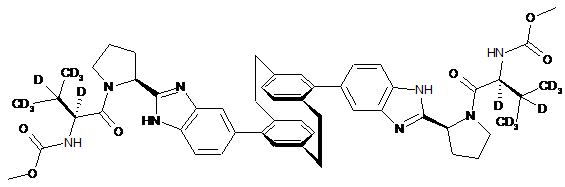 ,
,
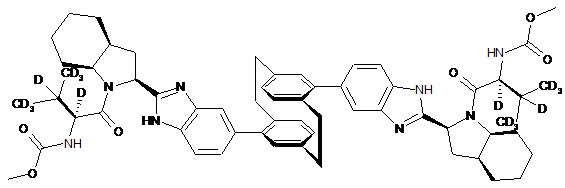 ,
,
 ,
,
 ,
,
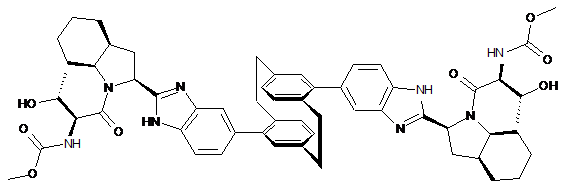 ,
,
 ,
,
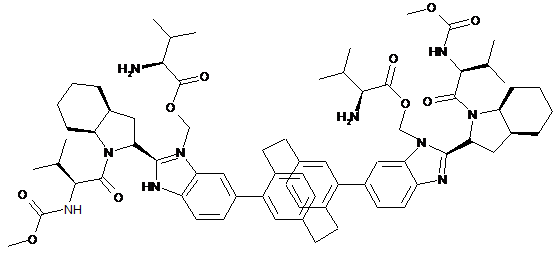 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
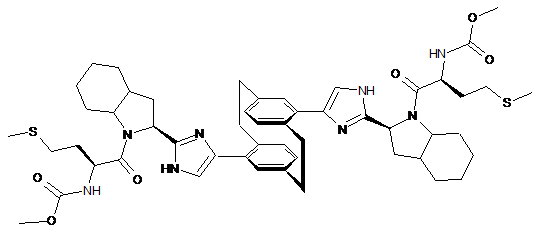 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 або
або
 .
.
11. Сполука за п. 1 формули
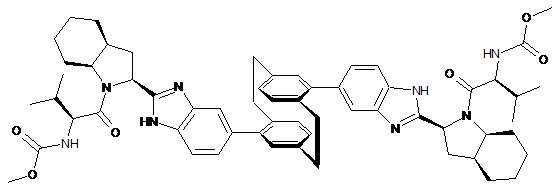
або її фармацевтично прийнятна сіль.
12. Сполука за п. 1 формули
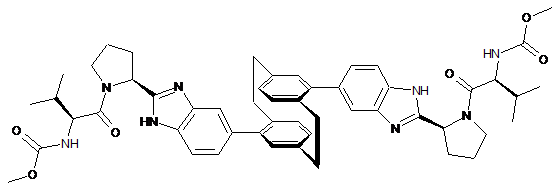
або її фармацевтично прийнятна сіль.
13. Фармацевтична композиція, що містить сполуку або сіль за будь-яким з пп. 1-12 разом з фармацевтично прийнятним носієм.
14. Фармацевтична композиція за п. 13, де композиція містить щонайменше один додатковий активний агент.
15. Спосіб лікування інфекції гепатиту С у пацієнта, що включає надання терапевтично ефективної кількості однієї або декількох сполук за будь-яким з пп. 1-12 або композиції за п. 13 або п. 14 пацієнту, який потребує цього.
Текст
Реферат: Даний винахід пропонує заміщені аліфани, циклофани, гетерафани, гетерофани, гетерогетерафани й металоцени формули (І) D-M-D (формула І), які можуть бути використані як противірусні агенти. У певних варіантах здійснення, описаних у даному документі, М є групою Р-А-Р-, де А має формулу І. Певні заміщені аліфани, циклофани, гетерафани, гетерофани, гетеро-гетерафани й металоцени, описані в даному документі, є сильнодіючими й/або селективними інгібіторами реплікації вірусів, зокрема реплікації вірусу гепатиту С. Фармацевтичні композиції й комбінації, які містять один або декілька заміщених аліфанів, циклофанів, гетерафанів, гетерофанів, гетеро-гетерафанів і металоценів і фармацевтично прийнятний носій, також пропонуються даним винаходом. Винаходом пропонуються способи лікування вірусної інфекції, включаючи вірусну інфекцію гепатиту С. UA 110976 C2 (12) UA 110976 C2 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки, до якої відноситься винахід Даний винахід пропонує заміщені аліфани, циклофани, гетерафани, гетерофани, гетерогетерафани й металоцени, які можнуть бути використані як противірусні агенти. Вказані заміщені аліфани, циклофани, гетерафани, гетерофани, гетеро-гетерафани й металоцени, описані в даному документі є сильнодіючими й/або селективними інгібіторами реплікації вірусів, зокрема, реплікації вірусу гепатиту C. Фармацевтичні композиції й комбінації, які містять один або декілька заміщених аліфанів, циклофанів, гетерафанів, гетерофанів, гетеро-гетерафанів і металоценів та фармацевтично прийнятний носій, також пропонуються даним винаходом. Даним винаходом пропонуються способи лікування вірусних інфекцій, включаючи інфекцію вірусу гепатиту C. Попередній рівень техніки Згідно з оцінками, 3% населення земної кулі інфіковане вірусом гепатиту C. З людей, які стикаються із ВГС, 80%-85% стають хронічно інфікованими, щонайменше, в 30% розвивається цироз печінки й в 1-4% розвивається гепатоклітинна карцинома. Вірус гепатиту C (ВГС) є однією з найпоширеніших причин хронічних захворювань печінки в Сполучених Штатах, у цей час вони становлять приблизно 15 відсотків гострого вірусного гепатиту, 60-70 відсотків хронічного гепатиту й до 50 відсотків цирозу, кінцевої стадії захворювання печінки й рака печінки. Хронічна інфекція ВГС є найпоширенішим приводом для трансплантації печінки в США, Австралії й у більшій частині Європи. Гепатит C викликає, згідно з оцінками, 10000-12000 смертей на рік у Сполучених Штатах. Хоча гостра фаза інфекції ВГС пов'язана з помірними симптомами, деякі докази говорять, що тільки приблизно 15%-20% інфікованих людей спонтанно позбуваються ВГС. ВГС є оболонковим вірусом із одноланцюговою РНК, який містить геном плюс-ланцюга приблизно з 9,6 kb. ВГС класифікується як член роду Hepacivirus родини Flaviviridae. Характеризовані, щонайменше, 4 штами ВГС, GT-1 - GT-4. Життєвий цикл ВГС включає проникнення до клітини хазяїна; трансляцію генома ВГС, процесинг поліпротеїнів і складання комплексу реплікази; реплікацію РНК і складання й вивільнення віріону. Трансляція генома РНК ВГС утворює поліпротеїн довжиною більш ніж 3000 амінокислот, який процесується, щонайменше, двома клітинними й двома вірусними протеазами. Поліпротеїн ВГС являє собою: NH2-C-E1-E2-p7-NS2-NS3-NS4A-NS4B-NS5A-NS5B-COOH. Клітинна сигнальна пептидаза й пептидаза сигнального пептиду, як повідомляється, відповідають за відщеплення N- термінальної третини поліпротеїну (C-E1-E2-p7) від неструктурних білків (NS2-NS3-NS4A-NS4B-NS5A-NS5B). Протеаза NS2-NS3 опосередковує перше цис розщеплення на сайті NS2-NS3. Потім протеаза NS3-NS4A опосередковує друге цисрозщеплення на з'єднанні NS3-NS4A. Потім комплекс NS3-NS4A здійснює розщеплення на трьох наступних сайтах для відділення інших неструктурних білків. Точний процесинг поліпротеїну вважається головним для формування активного комплексу реплікази ВГС. Після розщеплення поліпротеїну, збирається комплекс реплікази, який містить, щонайменше, неструктурні білки NS3-NS5B. Комплекс реплікази є цитоплазматичним і пов'язаним з мембраною. Головні ферментативні активності комплексу реплікази включають активність серинпротеази й активність NTPази гелікази в NS3 і РНК-залежну активність РНК полімерази NS5B. У процесі реплікації РНК, продукується копія комплементарного мінусланцюга геномної РНК. Копію мінус-ланцюга використовують як шаблон для синтезу додаткових геномних РНК із плюс-ланцюгом, які можуть брати участь у трансляції, реплікації, упакуванні або в будь-якій їхній комбінації з одержанням вірусного потомства. Складання функціонального комплексу реплікази описується як компонент механізму реплікації ВГС. Попередня заявка на патент США № 60/669872 «Pharmaceutical Compositions and Methods of Inhibiting ВГС Replication», подана 11 квітня 2005 року, тим самим включається шляхом посилання у всій її повноті щодо її опису, пов'язаного зі складанням комплексу реплікази. У цей час лікування інфекції гепатиту C, як правило, включає введення інтерферону, такого як пегільований інтерферон (IFN), у комбінації з рибавірином. Успіх сучасної терапії, як визначається за допомогою стійкої вірусологічної відповіді (SVR) залежить від штаму ВГС, яким інфікований пацієнт, і від дотримання пацієнтом режиму лікування. Тільки 50% пацієнтів, інфікованих штамом GT-1 ВГС, демонструють стійку вірусологічну відповідь. Противірусні агенти прямої дії, такі як ACH-1625, телапревір, BMS-790052 і BMS-650032, перебувають у клінічній розробці для лікування хронічного ВГС. Через відсутність ефективної терапії для лікування певних штамів ВГС і високої швидкості мутації ВГС, необхідні нові види терапії. Даний винахід задовольняє цю необхідність і пропонує додаткові переваги, які описані в даному документі. 1 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 Сутність винаходу У даному документі пропонуються заміщені аліфани, циклофани, гетерафани, гетерофани, гетеро-гетерафани й металоцени формули I. Сполуки формули I, запропоновані в даному винаході мають противірусну активність. Винахід пропонує сполуки формули I, які є сильнодіючими й/або селективними інгібіторами реплікації вірусу гепатиту C. Не обмежуючись якою-небудь конкретною теорією, передбачається, що дані сполуки є сильнодіючими й селективними інгібіторами NS5a ВГС. Фармацевтичні композиції, які містять одну або кілька сполук формули I або сіль таких сполук і один або декілька фармацевтично прийнятних носіїв, також пропонуються в даному документі. Фармацевтичні комбінації, які містять одну або кілька сполук формули I або сіль таких сполук, щонайменше, один додатковий активний агент, і один або декілька фармацевтично прийнятних носіїв, також пропонуються в даному документі. Також описуються способи лікування пацієнтів, які страждають від певних вірусних інфекцій, зокрема, інфекцій ВГС, за допомогою введення таким пацієнтам кількості сполуки формули I, ефективної для зменшення ознак або симптомів вірусної інфекції. Способи лікування передбачають введення сполуки формули I як окремого активного агента або введення сполуки формули I у комбінації з одним або декількома іншими терапевтично активними агентами. У першому аспекті винахід включає сполуки формули I D-M-D (формула I) або її фармацевтично прийнятну сіль. У формулі I, змінні D і M мають наступні визначення. D є T-R-, де M є ковалентно пов'язаним з R. M представляє збій -P-A-P-. P є -J-W-, де J є ковалентно пов'язаним з R і W є ковалентно пов'язаним з A, або P є -J-, де J є ковалентно пов'язаним з R і A. J є незалежно обраним у кожному випадку і представлений Ji, де i є цілим числом від 1 до 2. T є незалежно обраним у кожному випадку і представлений Tk, де k є цілим числом від 1 до 1 2; T представлений -Y-Z, де Y є ковалентно пов'язаним з R і Y є зв’язком, C1-C4 алкіленом, необов'язково заміщеним оксо; і Z є 5 або 6-членною гетероциклічною групою, кожний з поміж 1 T є заміщеним, (i) щонайменше, одним замісником, обраним з поміж -(С=O)OH, -(С=O)NH2, (С=O)H, -C1-C4 алкокси, C2-C4 алканоїлу, складного C1-C4 алкілового ефіру, складного C1-C4 алкеніленового ефіру, моно- або ди-C1-C4 алкілкарбоксаміду й (ii) необов'язково заміщений одним або декількома замісниками, незалежно обраними з поміж галогену, гідроксилу, C1-C2 алкілу й C1-C2 алкокси; і 2 T є незалежно обраним у кожному випадку з C2-C6 алканоїлу, складного C1-C6 алкілового ефіру, складного C1-C6 алкенілового ефіру, C1-C6 алкілсульфонаміду, C1-C6 алкілсульфонілу, C2C6 алканоїлу, заміщеного моно- або ди-C1-C6 гідрокарбілкарбаматом, C2-C6 алканоїлу, заміщеного сечовиною або моно- або ди-C1-C6алкілсечовиною, і C2-C6 алканоїлу, заміщеного 2 моно- або ди-C1-C6 алкілкарбоксамідом, кожний з поміж T є необов'язково заміщеним 1 або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, (C 1-C4 алкокси)C0-C4алкілу, (моно- і ди-C1-C4алкіламіно)C0-C4алкілу, C1-C6алкілу, (C1-C4тіоалкіл)C0-C4 алкілу, C3-C7 циклоалкілу, фенілу, C1-C4 галогеналкілу й C1-C4 галогеналкокси; R є незалежно обраним у кожному випадку з поміж (a) 4 - 6-членних кілець, які містять один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, де R є насиченим або містить 1 ненасичений зв'язок і необов'язково приєднаний за допомогою метиленового або етиленового містка, або є конденсованим з фенільним або з 5-6-членним гетероарильним кільцем; і (b) 6 - 10-членних конденсованих або спіробіциклічних кільцевих систем, які містять один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, де 6 - 10-членне біциклічне кільце є насиченим або містить 1 ненасичений зв'язок; кожна із груп R є необов’язково заміщеною одним або декількома замісниками, незалежно обраними із ціано, гідроксилу, галогену, C1-C2 алкілу, C1-C2 алкокси, C1-C2 галогеналкілу, C1-C2 галогеналкілу, C1-C2 галогеналкілену й C1-C2 алкілсульфонілу. 1 J є фенілом або 5-6-членною гетероарильною групою, яка містить 1-3 гетероатома, 1 незалежно обраних з N, O і S, де кожна із груп J є необов’язково заміщеною одним або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, C 1C4алкілу, C1-C4алкокси, моно- і ди-C1-C4алкіламіно, C1-C2 галогеналкілу й C1-C2 галогеналкокси. 2 J являє собою 8-10-членну гетероарильну групу, яка містить 1 - 4 гетероатома, незалежно 2 обраних з поміж N, O і S, де J необов'язково заміщений одним або декількома замісниками, 2 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, C 1-C4 алкілу, C1-C4 алкокси, моно- і ди-C1-C4 алкіламіно, C1-C2 галогеналкілу й C1-C2 галогеналкокси. W є незалежно обраним у кожному випадку і представлений фенільною, піридильною або алкинільною групою, необов'язково заміщеною одним або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, C1-C4алкілу, C1-C4алкокси, моно- і ди-C1C4алкіламіно, C1-C2 галогеналкілу й C1-C2 галогеналкокси. A є [j.k]-циклофаном, [j.k]- гетера-фаном, [j.k]- гетеро-фаном, [j.k]- гетеро-гетера-фаном або [j.k]-аліфаном; де j є цілим числом від 1 до 4, k є цілим числом від 0 до 4, різниця між j і k становить не більше ніж 2, і кожний лінкер j і k необов'язково містить гетероатом, обраний з поміж N, O і S, і є необов'язково заміщеним 1 оксо групою й одним або декількома замісниками, незалежно обраними з поміж галогену, гідрокси, аміно, C1-C2 алкілу й C1-C2 алкокси; або A представлений [j.k.j'.k']-циклофаном, де j, j', k і k' є цілими числами від 1 до 4, різниця між j і k або k' становить не більш ніж 2, різниця між j' і k або k' становить не більш ніж 2, і кожний лінкер з j, j', k і k' необов'язково містить гетероатом, обраний з поміж N, O і S, і є необов'язково заміщеним 1 оксо групою й одним або декількома замісниками, незалежно обраними з поміж галогену, гідрокси, аміно, C1-C2 алкілу й C1-C2 алкокси; або A є групою формули або , де Q є нейтральним або катіонним металом, кожна із цих груп A є необов’язково заміщеною одним або декількома замісниками, незалежно обраними з поміж галогену, C 1-C2 алкілу й C1-C2 алкокси. У певних варіантах здійснення Q вибирають із поміж Fe, Co, Cr, Ni, V, Li, Rb і K; або A є групою формули , де A є необов’язково заміщеною одним або декількома замісниками, незалежно обраними з поміж галогену, C1-C2 алкілу й C1-C2 алкокси. Даним винаходом пропонуються фармацевтичні композиції й комбінації, які містять сполуки формули I, разом з фармацевтично прийнятним носієм. Композиції й комбінації, запропоновані даним винаходом, можуть включати сполуки формули I як єдиний активний агент або можуть включати один або кілька додаткових активних агентів. У певних варіантах здійснення додатковий активний агент є інгібітором протеази NS3a. Даний винахід також пропонує спосіб лікування інфекції гепатиту C у пацієнта, який передбачає введення терапевтично ефективної кількості одного або декількох сполук формули I пацієнтові. Сполука формули I може вводитися як єдиний активний агент або може вводитися разом з одним або декількома додатковими активними агентами, такими як інгібітор протеази NS3a. Певні сполуки формули I, описані в даному документі, демонструють гарну активність при аналізі реплікації ВГС, такому як аналіз за допомогою реплікона ВГС, наведений у прикладі 9, який наведено далі. Кращі сполуки формули I демонструють EC 50 приблизно 10 мікромоль або менше, або більш бажано, EC50 приблизно 1 мікромоль або менше; або ще більш бажано, EC 50 приблизно 100 наномоль або менше при аналізі реплікації за допомогою реплікона ВГС. Здійснення винаходу Хімічний опис і термінологія Перед докладним викладом винаходу, може бути корисним привести визначення певних термінів, які повинні використовуватися в даному описі. Сполуки описують із використанням стандартної номенклатури. Якщо не зазначено іншого, усі технічні й наукові терміни, які використовуються в даному документі, мають таке ж значення, яке звичайно надається фахівцями в галузі, до якої належить даний винахід. Якщо контекст не вказує чітко на протилежне, кожна назва сполуки включає форму сполуки вільної кислоти або вільної основи, а також усі фармацевтично прийнятні солі сполуки. Термін "сполуки формули I" охоплює всі сполуки, які мають формулу I, включаючи будь-які енантіомери, рацемати й стереоізомери, а також усі фармацевтично прийнятні солі таких сполук. Фраза "сполуки формули I" включає всі субспоріднені підмножини формули I, і також включає фармацевтично прийнятні солі сполуки формули I, якщо тільки контекст, у якому використовується ця фраза, не вказує чітко на протилежне. "Формула II" охоплює всі сполуки, які мають формулу II, включаючи будь-які енантіомери, рацемати й стереоізомери, а також усі фармацевтично прийнятні солі таких сполук. Фраза "сполуки формули II" включає всі субгенеричні підмножини формули II, і також включає фармацевтично прийнятні солі сполуки формули II, якщо тільки контекст, у якому використовується ця фраза, не вказує чітко на протилежне. 3 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 Терміни, які визначають однину, не означають обмеження кількості, але скоріше позначають присутність, щонайменше, одного зазначеного об'єкта. Термін "або" означає "і/або". Необмежена перехідна фраза "який включає" охоплює перехідну фразу "який складається в основному з" і завершену фразу "який складається з". Пункти формули винаходу, які містять одну із цих трьох перехідних фраз, або пункти з іншою перехідною фразою, такою як "який містить" або "який утримує" можуть бути записані за допомогою будь-якої іншої перехідної фрази, якщо цього чітко не забороняють контекст або відома в даній галузі інформація. Згадування діапазонів значень призначене для вживання тільки як скорочений спосіб згадування індивідуально кожного окремого значення, яке попадає в цей діапазон, якщо в даному документі не зазначено іншого, і кожне окреме значення включається в опис, як ніби воно згадувалося індивідуально в даному документі. Кінцеві точки всіх діапазонів включаються в діапазон і можуть бути незалежно поєднаними. Усі способи, описані в даному документі, можуть здійснюватися у відповідному порядку, якщо в даному документі не зазначено іншого або якщо це іншим способом чітко не спростовується контекстом. Використання будь-яких і всіх прикладів, або ілюстративної мови (наприклад, "такий як"), призначене тільки для кращого ілюстрування винаходу й не накладає обмежень на рамки даного винаходу, якщо не заявляється іншого. Мова в описі не повинна розглядатися як така, що позначає будь-який не заявлений елемент, як головний для здійснення винаходу, як це описано в даному документі. Якщо не зазначено іншого, технічні й наукові терміни, які використовуються в даному документі, мають таке ж значення, яке звичайно розуміється фахівцями в галузі, до якої належить даний винахід. "Активний агент" позначає сполуку (включаючи сполуку, описану в даному документі), елемент або суміш, яка, коли вона вводиться пацієнтові, сама як така або в комбінації з іншою сполукою, елементом або сумішшю, має, безпосередньо або опосередковано, фізіологічний вплив на пацієнта. Опосередкований фізіологічний вплив може здійснюватися за допомогою метаболіту або за допомогою іншого опосередкованого механізму. Тире ("-"), яке не знаходиться між двома буквами або символами, використовується для позначення точки приєднання замісника. Наприклад, -(С=O)NH2 приєднується через атом вуглецю кето (С=O) групи. "Аліфан", як він використовується в даному документі, представляє групу, яка складається з одного або двох циклоалкільних кілець, щонайменше, з одним аліфатичним містком між двома не сусідніми положеннями в одному циклоалкільному кільці або між двома циклоалкільними кільцями. Аліфатичні містки містять від 1 до 4 атомів вуглецю. Аліфатичні містки є необов'язково заміщеними оксо групою. "Алканоїл" є алкільною групою, як визначено в даному документі, ковалентно зв'язаною із групою, яку вона заміщає, за допомогою кето (-(С=O)-) містка. Алканоїльні групи мають зазначену кількість атомів вуглецю, при цьому атом вуглецю кето групи включається в перераховані атоми вуглецю. Наприклад, C 2 алканоїльна група є ацетильною групою, яка має формулу CH3(С=O)-. "Алкіл" є насиченою аліфатичною вуглеводневою групою з розгалуженим або прямим ланцюгом, що має зазначену кількість атомів вуглецю, як правило, від 1 до, приблизно, 12 атомів вуглецю. Термін C1-C6 алкіл, як він використовується в даному документі, позначає алкільну групу, яка має 1, 2, 3, 4, 5 або 6 атомів вуглецю. Інші варіанти здійснення включають алкільні групи, які мають від 1 до 8 атомів вуглецю, від 1 до 4 атомів вуглецю або 1 або 2 атома вуглецю, наприклад C1-C8алкіл, C1-C4 алкіл і C1-C2 алкіл.Коли C0-Cn алкіл використовується в даному документі в комбінації з іншою групою, наприклад, (C 1-C4 алкокси)C0-C4 алкіл, зазначена група, у даному випадку алкокси, є або безпосередньо пов'язаною за допомогою одинарного ковалентного зв'язку (C0 алкіл), або приєднаною за допомогою алкільного ланцюга, який має зазначену кількість атомів вуглецю, у цьому випадку, 1, 2, 3, або 4 атоми вуглецю. Приклади алкілів включають, але, не обмежуються цим, метил, етил, н-пропіл, ізопропіл, н-бутил, 3метилбутил, трет-бутил, н-пентил і втор-пентил. "Алкиніл" є аліфатичною вуглеводневою групою з розгалуженим або прямим ланцюгом, який має один або кілька потрійних зв'язків вуглець-вуглець, які можуть здійснюватися в будь-якій стабільній точці уздовж ланцюга, який має зазначену кількість атомів вуглецю. Приклади алкинілу включають, але, не обмежуються цим, етиніл і пропиніл. "Алкокси" є алкільною групою, як визначено вище, із зазначеною кількістю атомів вуглецю, ковалентно пов'язаною із групою, яку вона заміщає, за допомогою кисневого містка (-O-). Приклади алкокси включають, але, не обмежуються цим, метокси, етокси, н-пропокси, ізопропокси, н-бутокси, 2-бутокси, трет-бутокси, н-пентокси, 2-пентокси, 3-пентокси, ізопентокси, неопентокси, н-гексокси, 2-гексокси, 3-гексокси й 3-метилпентокси. 4 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін група "складного алкілового ефіру" позначає алкільну групу, як визначено в даному документі, ковалентно зв'язану із групою, яку вона заміщає, за допомогою складоефірного зв'язку. Складноефірний зв'язок може бути або орієнтованим, наприклад, бути групою формули -O(С=O)алкілом, або бути групою формули -(С=O)O алкіл. "Алкілсульфоніл" є групою формули -SO2 алкіл, де алкільна група має визначення, наведене в даному документі. «Циклоалкіл» є насиченою вуглеводневою кільцевою групою, яка має зазначену кількість атомів вуглецю. Моноциклічні циклоалкільні групи, як правило, мають від 3 до, приблизно, 8 атомів вуглецю в кільці або від 3 до 7 (3, 4, 5, 6 або 7) атомів вуглецю в кільці. Циклоалкільні замісники можуть бути бічними групами відносно заміщеного атома азоту або вуглецю, або заміщений атом вуглецю, який може мати два замісники, може мати циклоалкільну групу, яка приєднана до спіро групи. Приклади циклоалкільних груп включають циклопропіл, циклобутил, циклопентил і циклогексил. "Циклофан", як використовується в даному документі, є групою, яка складається з одного або двох ароматичних кілець, звичайно бензольних кілець, щонайменше, з одним аліфатичним містком між двома не сусідніми положеннями єдиного ароматичного кільця або між двома ароматичними кільцями. Аліфатичні містки знаходяться у мета або пара або у мета, пара (мета на одному ароматичному кільці й пара на іншому) орієнтації й містять від 1 до 4 атомів вуглецю. Аліфатичні містки є необов'язково заміщеними оксо групою. "Галогеналкіл" позначає алкільні групи, як з розгалуженим ланцюгом, так і із прямим ланцюгом, які мають зазначену кількість атомів вуглецю, заміщених 1 або декількома атомами галогену, до максимально припустимого кількості атомів галогену. Приклади галогеналкілів включають, але, не обмежуються цим, трифторметил, дифторметил, 2-фторетил і пентафторетил. "Галогеналкокси" позначає галогеналкільну групу, як визначено в даному документі, приєднану через кисневий місток (кисень радикала спирту). "Гало" або "галоген" позначає будь-який атом із фтору, хлору, брому і йоду. "Гетероарил" позначає стабільне моноциклічне ароматичне кільце, яке має зазначену кількість атомів у кільці, яке містить від 1 до 3 або, у деяких варіантах здійснення, від 1 до 2 гетероатомів, обраних з поміж N, O і S, при цьому інші атоми кільця є атомами вуглецю, або стабільною біциклічною або трициклічною системою, яка містить, щонайменше, одне 5-7членне ароматичне кільце, яке містить від 1 до 3 або, в деяких варіантах здійснення, від 1 до 2 гетероатомів, обраних з поміж N, O і S, при цьому інші атоми кільця є атомами вуглецю. Моноциклічні гетероарильні групи, як правило, мають від 5 до 7 атомів у кільці. У деяких варіантах здійснення біциклічні гетероарильні групи є 9-10-членними гетероарильними групами, тобто групами, які містять 9 або 10 атомів у кільці, у яких одне 5 - 7-членне ароматичне кільце є конденсованим із другим ароматичним або неароматичним кільцем. Коли загальна кількість атомів S і O у гетероарильній групі перевищує 1, ці гетероатоми не знаходяться один поруч з одним. Краще, щоб загальна кількість атомів S і O у гетероарильній групі становила не більше ніж 2. Найкраще, щоб загальна кількість атомів S і O в ароматичному гетероциклі становила не більше ніж 1. Приклади гетероарильних груп включають, але, не обмежуються цим, оксазоліл, піраніл, піразиніл, піразолопіримідиніл, піразоліл, піридизиніл, піридил, піримідиніл, піроліл, хінолініл, тетразоліл, тіазоліл, тієнілпіразоліл, тіофеніл, триазоліл, бензо[d]оксазоліл, бензофураніл, бензотіазоліл, бензотіофеніл, бензоксадиазоліл, дигідробензодиоксиніл, фураніл, імідазоліл, індоліл та ізоксазоліл. "Гетероарилокси" є гетероарильною групою, як описано, пов'язаною із групою, яку вона заміщає, через кисневий місток. "Гетера-фан", як він використовується в даному документі, є групою, яка складається з одного або двох ароматичних кілець, звичайно бензольних кілець, щонайменше, з одним аліфатичним містком між двома не сусідніми положеннями єдиного ароматичного кільця або між двома ароматичними кільцями, яка містить гетероатом. Аліфатичні містки знаходяться у мета або пара або в мета, пара (мета на одному ароматичному кільці й пара на іншому) орієнтації й містять від 1 до 4 атомів, щонайменше, один з яких є гетероатом, при цьому інші атоми є атоми вуглецю. Аліфатичні містки є необов'язково заміщеними оксо групою. "Гетеро-фан", як використовується в даному документі, є групою, яка складається з одного або двох ароматичних кілець, де, щонайменше, одне ароматичне кільце є гетероарилом, щонайменше, з одним аліфатичним містком між двома не сусідніми положеннями єдиного ароматичного кільця або між двома ароматичними кільцями. Аліфатичні містки знаходяться у мета або пара або в мета, пара (мета на одному ароматичному кільці й пара на іншому) орієнтації й містять від 1 до 4 атомів вуглецю. Аліфатичні містки є необов'язково заміщеними оксо групою. 5 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 "Гетеро-гетера-фан", як він використовується в даному документі, є групою, яка складається з одного або двох ароматичних кілець, де, щонайменше, одне ароматичне кільце є гетероарилом, щонайменше, з одним аліфатичним містком між двома не сусідніми положеннями єдиного ароматичного кільця або між двома ароматичними кільцями, яка містить гетероатом, обраний з поміж N, O або S, і один аліфатичний місток між двома не сусідніми положеннями єдиного ароматичного кільця або між двома ароматичними кільцями, які не містять гетероатомів. Аліфатичні містки знаходяться у мета або пара або в мета, пара (мета на одному ароматичному кільці й пари на іншому) орієнтації й містять від 1 до 4 атомів, щонайменше, один з яких є гетероатомом, при цьому інші атоми є атомами вуглецю. Аліфатичні містки є необов'язково заміщеними оксо групою. "Гідрокарбіл" є насиченою або ненасиченою аліфатичною групою, яка містить зазначену кількість атомів вуглецю. "Гідрокарбіл" може використовуватися в комбінації з іншими групами, такими як карбамат, як в "моно- або ди-гідрокарбілкарбаматі". Моно- або дигідрокарбілкарбамат включає групи формули (алкіл1)NH(С=O)O- і (алкіл1)N(алкіл2)(С=O)O-, а також групи, у яких одна або обидві алкільні групи замінені вуглеводневою групою, яка містить ненасичені зв'язки вуглець-вуглець. "Металоцен" позначає сполуки, які складаються із двох 5- або 6-членних ароматичних карбоциклічних груп, пов'язаних з металевим центром, де метал є нейтральним або катіонним. Приклад металоцену включає, але, не обмежується цим, фероцен. Термін "моно- і/або ди-алкіламіно" позначає вторинні або третинні алкіламіно групи, де алкільні групи є незалежно обраними алкільними групами, як визначено в даному документі, які мають зазначену кількість атомів вуглецю. Точка приєднання алкіламіно групи знаходиться на азоті. Приклади моно- і ди-алкіламіно груп включають етиламіно, диметиламіно й метил-пропіламіно. "Моно- і/або ди-алкілкарбамат" включає моно-алкілкарбаматні групи формули (алкіл1)O(С=O)NH- або диалкілкарбоксамідні групи формули (алкіл1)O(С=O)N(алкіл2)-, у яких точка приєднання моно- або диалкілкарбоксамідного замісника до молекули, яку вона заміщає, перебуває на азоті аміно карбамату. Термін "моно й/або ди-алкілкарбамат" також включає групи формули (алкіл1)NH(С=O)O- і (алкіл1)N(алкіл2)(С=O)O-, у яких карбамат є ковалентно пов'язаним із групою, яку він заміщає, за допомогою його атома кисню, що не входить у кето групу. Групи алкіл1 і алкіл2 є незалежно обраними алкільними групами, які мають визначення алкілу, наведене в даному винаході та які мають зазначену кількість атомів вуглецю. "Моно- і/або ди-алкілкарбоксамід" позначає моно-алкілкарбоксамідну групу формули (алкіл1)-NH-(С=O)- або диалкілкарбоксамідну групу формули (алкіл1)(алкіл2)-N-(С=O)-, у яких точка приєднання моно- або диалкілкарбоксамідного замісника до молекули, яку він заміщає, знаходиться на атомі вуглецю карбонільної групи. Термін "моно й/або ди-алкілкарбоксамід" також включає групи формули (алкіл1)(С=O)NH- і (алкіл1)(С=O)(алкіл2)N-, у яких точка приєднання є атомом азоту. Групи алкіл1 і алкіл2 є незалежно обраними алкільними групами, які мають зазначену кількість атомів вуглецю. Подібним же чином, "моно- і/або диалкілсульфонамід" є кожною з моно-алкілсульфонамідних груп формули (алкіл1)-NH-(SO2)-, моно-алкілсульфонамідних груп формули (алкіл 1)-(SO2)-NH-, диалкілсульфонамідних груп формули (алкіл1)(алкіл2)-N-(SO2)- і груп формул (алкіл1)-(SO2)-(алкіл2)N-. "Тіоалкіл" є алкільною групою, як визначено вище, із вказаною кількістю атомів вуглецю ковалентно зв'язаних із групою, яку вона заміщає, за допомогою сірчаного містка (-S-). Термін "заміщений", як він використовується в даному документі, позначає, що один або кілька атомів водню на позначеному атомі або групі замінені деяким вибором із зазначеної групи за умови, що позначена нормальна валентність атома не перевищується. Коли замісником є оксо (тобто, =O), тоді можуть бути замінені 2 атома водню на атомі. Коли оксо група заміщає ароматичні залишки, відповідне частково ненасичене кільце заміняє ароматичне кільце. Наприклад, піридильна група, заміщена оксо, є піридоном. Комбінації замісників і/або змінних є припустимими, тільки якщо такі комбінації дають стабільні сполуки або придатні для використання синтетичні проміжні сполуки. Стабільні сполуки або стабільна структура, як передбачається, дає сполуку, яка є досить стійкою, щоб перенести виділення з реакційної суміші й наступне приготування у вигляді ефективного терапевтичного агента. Якщо не зазначено іншого, замісники називаються в серцевинній структурі. Наприклад, необхідно розуміти, що коли аміноалкіл згадується як можливий замісник, точка приєднання цього замісника до серцевинної структури перебуває в алкільній частині. Відповідні групи, які можуть бути присутніми в "заміщеному" положенні, включають, але, не обмежуються цим, наприклад, галоген; ціано; гідроксил; нітро; азидо; алканоїл (такі як C 2-C6 алканоїльна група); карбоксамід; алкільні групи (включаючи циклоалкільні групи), які мають від 1 6 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 приблизно до 8 атомів вуглецю або від 1 приблизно до 6 атомів вуглецю; алкенільні й алкинільні групи, включаючи групи, які мають одну або кілька ненасичених зв'язків і від 2 приблизно до 8 або від 2 приблизно до 6 атомів вуглецю; алкокси групи, які мають один або кілька кисневих зв'язків і від 1 приблизно до 8, або від 1 приблизно до 6 атомів вуглецю; арилокси, такі як фенокси; алкілтіо групи, включаючи групи, які мають одну або декілька тіоефірних зв'язків і від 1 приблизно до 8 атомів вуглецю або від 1 приблизно до 6 атомів вуглецю; алкілсульфінільні групи, включаючи групи, які мають одну або декілька сульфінільних зв'язків і від 1 приблизно до 8 атомів вуглецю або від 1 приблизно до 6 атоми вуглецю; алкілсульфонільні групи, включаючи групи, які мають один або декілька сульфонільних зв'язків і від 1 приблизно до 8 атомів вуглецю або від 1 приблизно до 6 атомів вуглецю; аміноалкільні групи, включаючи групи, які мають один або кілька атомів N і від 1 приблизно до 8 або від 1 приблизно до 6 атомів вуглецю; арил, що має 6 або більш атомів вуглецю й одне або кілька кілець (наприклад, феніл, біфеніл, нафтил, або щось подібне, кожне кільце є або заміщеним, або незаміщеним ароматичним кільцем); арилалкіл, що має 1 - 3 окремих або злитих кільця й від 6 приблизно до 18 атомів вуглецю в кільці, при цьому бензил є ілюстративною арилалкільною групою; арилалкокси, який має 1 - 3 окремих або злитих кілець і від 6 приблизно до 18 атомів вуглецю в кільці, при цьому бензилокси є ілюстративною арилалкокси групою; або насичену, ненасичену або ароматичну гетероциклічну групою, яка має 1 - 3 окремих або злитих кілець приблизно з 3 - 8 елементів у кільці й один або кілька атомів N, O або S, наприклад, кумариніл, хінолініл, ізохінолініл, хиназолініл, піридил, піразиніл, піримідиніл, фураніл, піроліл, тієніл, тіазоліл, триазиніл, оксазоліл, ізоксазоліл, імідазоліл, індоліл, бензофураніл, бензотіазоліл, тетрагідрофураніл, тетрагідропіраніл, піперидиніл, морфолініл, піперазиніл і піролідиніл. Такі гетероциклічні групи можуть бути додатково заміщеними, наприклад, гідрокси, алкілом, алкокси, галогеном і аміно. "Дозована форма" позначає одиницю введення активного агента. Приклади дозованих форм включають таблетки, капсули, ін'єкції, суспензії, рідини, емульсії, креми, мазі, супозиторії, форми для інгаляції, трансдермальні форми, і таке інше. "Фармацевтичні композиції" є композиціями, які містять, щонайменше, один активний агент, такий як сполуки або сіль формули I, і, щонайменше, одну іншу речовину, таку як носій. Фармацевтичні композиції необов'язково містять один або декілька додаткових активних агентів. Коли вони зазначені, фармацевтичні композиції задовольняють стандартам U.S. FDA GMP (правилам виробництва й контролю) для лікарських засобів для людей або тварин. "Фармацевтичні комбінації" є комбінаціями, щонайменше, двох активних агентів, які можуть поєднуватися у вигляді одиничної дозованої форми або поставлятися разом в окремих дозованих формах з інструкціями про те, що активні агенти повинні використовуватися разом для лікування розладу, такого як гепатит C. "Фармацевтично прийнятні солі" включають похідні описаних сполук, у яких вихідна сполука модифікується за допомогою одержання її неорганічних і органічних нетоксичних солей приєднання кислот або основ. Солі сполук запропонованих даним винаходом можуть синтезуватися з вихідної сполуки, яка містить основний або кислотний залишок, за допомогою звичайних хімічних способів. Як правило, такі солі можуть бути отримані за допомогою взаємодії форм вільної кислоти цих сполук зі стехіометричною кількістю відповідної основи (такої як гідроксид, карбонат, бікарбонат, або чогось подібного, Na, Ca, Mg або K), або за допомогою взаємодії форм вільних основ цих сполук зі стехіометричною кількістю відповідної кислоти. Такі реакції, як правило, здійснюються у воді або в органічному розчиннику або в їх суміші. Як правило, кращими є неводні середовища, подібні до простого ефіру, етилацетату, етанолу, ізопропанолу або ацетонітрилу, де це можливо. Солі сполук запропонованих даним винаходом додатково включають сольвати сполук і солей сполук. Приклади фармацевтично прийнятних солей включають, але, не обмежуються цим, солі мінеральних або органічних кислот і основних залишків, таких як аміни; лужні або органічні солі кислотних залишків, таких як карбонові кислоти; і таке інше. Фармацевтично прийнятні солі включають звичайні нетоксичні солі й солі четвертинного амонію й вихідної сполуки, утворені, наприклад, з нетоксичних неорганічних або органічних кислот. Наприклад, звичайні нетоксичні солі кислоти включають сполуки, отримані з неорганічних кислот, таких як хлористоводнева, бромистоводнева, сірчана, сульфамінова, фосфорна, азотна тощо; і солі, отримані з органічних кислот, таких як оцтова, пропіонова, бурштинова, гліколева, стеаринова, молочна, яблучна, винна, лимонна, аскорбінова, памоєва, малеїнова, гідроксималеїнова, фенілоцтова, глутамінова, бензойна, саліцилова, мезилова, езилова, безилова, сульфанілова, 2ацетоксибензойна, фумарова, толуолсульфонова, метансульфонова, етандисульфонова, щавелева, ізетинова, HOOC-(CH2)n-COOH, де n дорівнює 0-4 тощо. Список додаткових 7 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 придатних для використання кислот можна знайти, наприклад, в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., p. 1418 (1985). Термін "носій", у застосуванні до фармацевтичних композицій/комбінацій запропонованих даним винаходом відноситься до розріджувача, наповнювача або носія, якими забезпечуються активні сполуки. "Фармацевтично прийнятний наповнювач" позначає наповнювач, який є придатним для використання при готуванні фармацевтичної композиції/комбінації, який є, як правило, безпечним, нетоксичним і ні біологічно, ні іншим способом небажаним, і включає наповнювач, який є прийнятним для ветеринарного використання, а також для фармацевтичного використання для людей. "Фармацевтично прийнятний наповнювач", як це використовується в даний заявці, включає як один, так і кілька таких наповнювачів. "Пацієнт" може бути людиною або твариною, яка потребує медичного лікування. Медичне лікування може передбачати лікування існуючого стану, такого як захворювання або розлад, профілактичне або попереджувальне лікування або діагностичне лікування. У деяких варіантах здійснення пацієнт може бути пацієнтом людиною. "Надання" позначає видачу, уведення, продаж, роздрібний продаж, транспортування (із прибутком або без), виготовлення, змішування або розподіл. "Надання сполуки формули I, щонайменше, з одним додатковим активним агентом" означає, що сполука формули I і додатковий активний агент (агенти) надаються одночасно в одиничній дозованій формі, надаються одночасно в окремих дозованих формах або надаються в окремих дозованих формах для введення, розділеного деяким проміжком часу, який перебуває в межах того часу, коли як сполуки формули I, так і, щонайменше, один додатковий активний агент перебувають у кров′яному руслі пацієнта. У певних варіантах здійснення сполуки формули I і додатковий активний агент не можуть прописуватися для пацієнта тим самим працівником сфери охорони здоров'я. У певних варіантах здійснення додатковий активний агент або агенти не вимагають рецепта лікаря. Уведення сполуки формули I або, щонайменше, одного додаткового активного агента може здійснюватися за допомогою будь-якого відповідного способу, наприклад, пероральних таблеток, пероральних капсул, пероральних рідин, інгаляції, ін'єкції, супозиторіїв або місцевого контакту. "Лікування", як це використовується в даному документі, передбачає введення сполуки формули I, або як єдиного активного агента, або разом, щонайменше, з одним додатковим активним агентом, достатнє для: (a) запобігання появи захворювання або симптому захворювання в пацієнта, який може бути схильний до захворювання, але у якого захворювання ще не діагностоване (наприклад, включаючи захворювання, які можуть асоціюватися з первинним захворюванням або викликатися ним (як при фіброзі печінки, який може виникати в контексті хронічної інфекції ВГС); (b) уповільнення захворювання, тобто, припинення його розвитку; і (c) полегшення захворювання, тобто, здійснення регресії захворювання. "Лікування" і "вплив" позначає також надання терапевтично ефективної кількості сполуки формули I, як єдиного активного агента або разом, щонайменше, з одним додатковим активним агентом пацієнтові, який має інфекцію гепатиту C або схильному до неї. "Терапевтично ефективна кількість" фармацевтичної композиції/комбінації запропонованих даним винаходом означає кількість ефективну при введенні пацієнтові для забезпечення терапевтичного виграшу, такого як полегшення симптомів, тобто, кількість ефективна для зменшення симптомів інфекції гепатиту C. Наприклад, пацієнт, інфікований вірусом гепатиту C, може демонструвати підвищені рівні певних ферментів печінки, включаючи AST і ALT. Нормальні рівні AST становлять від 5 до 40 одиниць на літр сироватки (рідкої частини крові), а нормальні рівні ALT становлять від 7 до 56 одиниць на літр сироватки. Таким чином, терапевтично ефективна кількість є тією кількістю, яка є достатньою для забезпечення значного зниження підвищених рівнів AST і ALT, або кількістю, яка є достатньою для забезпечення повернення рівнів AST і ALT у нормальний діапазон. Терапевтично ефективна кількість є також такою кількістю, яка є достатньою для запобігання значного збільшення або для значного зменшення детектованого рівня вірусу або вірусних антитіл у крові, сироватці або тканинах пацієнта. Один зі способів визначення ефективності лікування включає вимірювання рівнів РНК ВГС за допомогою звичайного способу визначення рівнів вірусних РНК, такого як аналіз TaqMan від Roche. У певних кращих варіантах здійснення лікування зменшує рівні РНК ВГС нижче межі (R) кількісного визначення (30 МО/мл, визначеного за допомогою аналізу TaqMan від Roche ) або більш бажано нижче межі детектування (10 МО/мл, TaqMan від Roche). Значне збільшення або зменшення детектованого рівня вірусу або вірусних антитіл є будьякою детектованою зміною, яка є статистично значимою при стандартному параметричному дослідженні статистичної значимості, такому як T-критерій Ст′юдента, де p < 0,05. 8 UA 110976 C2 5 10 15 20 25 30 35 40 Хімічний опис Формула I і формула II (показані нижче) включають усі їх субродові підмножини. У певних ситуаціях, сполуки формули I або формули II можуть містити один або кілька асиметричних елементів, таких як стереогенні центри, стереогенні осі тощо, наприклад асиметричні атоми вуглецю, так що сполуки можуть існувати в різних стереоізомерних формах. Ці сполуки можуть бути, наприклад, рацематами або оптично активними формами. Для сполук із двома або більш асиметричними елементами, ці сполуки можуть, на додачу до цього, бути сумішшю діастереомерів. Для сполук, які мають асиметричні центри, повинно бути зрозумілим, що охоплюються всі оптичні ізомери і їх суміші. На додачу до цього, сполуки з подвійними зв'язками вуглець-вуглець можуть існувати в Z- і E-формах, при цьому всі ізомерні форми сполук охоплені даним винаходом. У цих ситуаціях, окремі енантіомери, тобто, оптично активні форми, можуть бути отримані за допомогою асиметричного синтезу, синтезу з оптично чистих попередників або за допомогою розділення рацематів. Розділення рацематів може також здійснюватися, наприклад, за допомогою звичайних способів, таких як кристалізація в присутності розв'язувального агента або хроматографія, з використанням, наприклад, хіральної колонки для ВЕРХ. Коли сполука існує в різних таутомерних формах, даний винахід не обмежується якимнебудь одним з конкретних таутомерів, але скоріше включає всі таутомерні форми. Даний винахід як передбачається, включає всі ізотопи атомів, які зустрічаються в сполуках запропонованих даним винаходом. Ізотопи включають атоми, які мають однаковий атомний номер, але різні масові числа. Як загальний приклад, і без обмеження, ізотопи водню 11 13 14 включають тритій і дейтерій, а ізотопи вуглецю включають C, C і C. Певні сполуки описані в даному документі з використанням загальної формули, яка включає змінні, наприклад, D, M, A, P, J і W. Якщо не зазначено іншого, кожна змінна в такій формулі визначається незалежно від інших змінних. Таким чином, якщо група, як сказано, є заміщеною, наприклад, 0-2 R*, тоді група може бути заміщеною групами R* у кількості до двох і R* у кожному випадку вибирається незалежно від визначення іншого R*. Також, комбінації замісників і/або змінних є припустимими, тільки якщо такі комбінації дають у результаті стабільні сполуки. На додачу до сполук і солей формули I, описаних у розділі «Сутність винаходу», винахід включає сполуки й сіль формули I, і фармацевтичні композиції/комбінації таких сполук, у яких змінна задовольняє кожній з наступних умов. (i) D-M-D є кожною з 1 1 T-R-J -W-A-W-J -R-T; 1 1 T-R-J -A-J -R-T; 2 2 T-R-J -A-J -R-T; 1 1 T-R-J -W-A-J -R-T; 1 2 T-R-J -W-A-J -R-T і 1 2 T-R-J -A-J -R-T. (ii) A представлене . (iii) A представлене . (iv) A представлене 45 . (v) A представлене 9 UA 110976 C2 . (vi) A представлене . (vii) A представлене 5 . (viii) A представлене (ix) A представлене . 10 (x) A представлене . (xi) A представлене . (xii) A представлене 15 . (xiii) A представлене 10 UA 110976 C2 . (xiv) A представлене 5 . 1-W (xv) Щонайменше, одна група P представлена J і W є фенілом, необов'язково заміщеним одним або декількома замісниками, незалежно обраними з поміж галогену, C 1-C2 алкілу й C1-C2 алкокси. 1 1 (xvi) P представлене J-W або J, де, щонайменше, одне J представлене J і J представлене 1 10 15 20 1 (xvii) Щонайменше, одна група P представлена J і J представлене 2 2 (xviii) Щонайменше, одна група P представлена J і J представлена бензимідазольною групою, необов'язково заміщеною одним або декількома замісниками, незалежно обраними з поміж галогену, C1-C2 алкілу й C1-C2 алкокси. (xix) R є незалежно обраним з поміж і кожний з яких є необов’язково заміщеним одним або декількома замісниками, незалежно обраними з поміж галогену, C1-C4 алкілу й C1-C4 алкокси. (xx) R є незалежно обраним з поміж (xxi) T є незалежно обраним C2-C6 алканоїлом, заміщеним моно- і ди-C1C6малкілкарбаматом, кожна із цих груп T є необов'язково заміщеним (C1-C4 тіоалкіл)C0C4алкілом. 2 2 (xxii) Також включаються сполуки й солі формули Т-R-J -A-J -R-T. 2 2 A, у формулі T-R-J -A-J -R-T, є групою формули 11 . UA 110976 C2 2 5 10 15 20 25 30 35 40 45 J є 8 - 10-членною гетероарильною групю, яка містить 1 або 2 гетероатома, незалежно 2 обраних з поміж N, O і S, де J є необов'язково заміщеним одним або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, C 1-C4алкілу, C1-C4алкокси, моно- і ди-C1-C4 алкіламіно, C1-C2 галогеналкілу й C1-C2 галогеналкокси. Кожна із груп R є незалежно обраною 8-10-членною біциклічною кільцевою системою, яка містить один або два атоми азоту, при цьому інші атоми кільця є атомами вуглецю, це 8-10членне біциклічне кільце є насиченим або містить 1 ненасичений зв'язок; і R є необов'язково заміщеним одним або декількома замісниками, незалежно обраними із ціано, гідроксилу, галогену, C1-C2 алкілу, C1-C2 алкокси, C1-C2 галогеналкілу, C1-C2 галогеналкілу, C1-C2 галогеналкілену й C1-C2 алкілсульфонілу. 2 T є незалежно обраним в кожному випадку з поміж C2-C6 алканоїлу, складного C1-C6 алкілового ефіру, складного C1-C6 алкенілового ефіру, C1-C6 алкілсульфонаміду, C1-C6 алкілсульфонілу, C2-C6алканоїлу, заміщеного моно- або ди-C1-C6 гідрокарбілкарбаматом, C2C6алканоїлу, заміщеного сечовиною або моно- або ди-C1-C6алкілсечовиною, і C2-C6алканоїлу, 2 заміщеного моно- або ди-C1-C6алкілкарбоксамідом, кожна із цих груп T є необов'язково заміщеною 1 або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, (C1-C4 алкокси)C0-C4 алкілу, (моно- і ди-C1-C4 алкіламіно)C0-C4алкілу, C1-C6алкілу, (C1C4 тіоалкіл)C0-C4 алкілу, C3-C7 циклоалкілу, фенілу, C1-C2 галогеналкілу й C1-C2 галогеналкокси. 2 У певних варіантах здійснення (xxii), є кращим, щоб -J -R- була представленою групою формули або більш конкретно 2 -J -R- може бути незаміщеним або заміщеним одним або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, C 1-C4 алкілу, C1-C4алкокси, моно- і ди-C1-C4 алкіламіно, C1-C2 галогеналкілу та C1-C2 галогеналкокси. 2 У певних варіантах здійснення (xxii), також є кращим, щоб T був C2-C6 алканоїлом, 2 заміщеним моно- або ди-C1-C6 гідрокарбілкарбаматом, де T є необов'язково заміщеним 1 або декількома замісниками, незалежно обраними з поміж аміно, ціано, гідроксилу, галогену, (C1-C4 алкокси)C0-C4 алкілу, (моно- і ди-C1-C4 алкіламіно)C0-C4 алкілу, C1-C6 алкілу, (C1-C4 тіоалкіл)C0-C4 алкілу, C3-C7 циклоалкілу, фенілу, C1-C2 галогеналкілу й C1-C2 галогеналкокси. Будь-які з попередніх умов для сполук формули I можуть використовуватися разом для визначення субродових підмножин формули I остільки, оскільки в результаті буде отримано стабільну сполуку. Усі такі субродові підмножини включаються в даний винахід. На додачу до сполук і солей формули I, описаних у розділі «Сутність винаходу», винахід включає композиції й комбінації формули I і формули II, де формула II представлена: (II) У формулі II змінні R1', R2', R3', R4', R6', R7', R8', R16 і T' мають визначення, наведені нижче. R1' і R2' з'єднуються з утворенням 7-членного гетероциклоалкільного кільця, яке містить 1 або 2 гетероатома, незалежно обраних з поміж N, O і S, де кільце є необов'язково конденсованим з фенільним кільцем або 5- або 6-членним гетероарилом з утворенням біциклічної кільцевої системи, кожна із цих 7-членних гетероциклоалкільних кільцевих або біциклічних кільцевих систем є необов'язково заміщеною. Для змінних R3' - R8' задовольняється одна з наступних умов. R3', R4', R5' і R6' незалежно є воднем, C1-C4алкілом або (C3-C7циклоалкіл)C0-C4алкілом; і R7' і R8' з'єднуються з утворенням необов'язково заміщеного 3 - 7-членного циклоалкільного кільця. R3', R4' і R6' незалежно є воднем, C1-C4алкілом або (C3-C7 циклоалкіл)C0-C4алкілом; і R8' є воднем або C1-C4алкілом; і R5' з'єднується з R7' за допомогою C6-C10 насиченого або ненасиченого вуглеводневого ланцюга. 12 UA 110976 C2 5 10 R3', R4' і R6' незалежно є воднем, C1-C4алкілом або (C3-C7 циклоалкіл)C0-C4 алкілом і R7' і R8' з'єднуються з утворенням необов'язково заміщеного 3-7-членного циклоалкільного кільця; і R5' з'єднується з 3-7-членним необов'язково заміщеним циклоалкільним кільцем, утвореним R 7' і R8', за допомогою C6-C10 насиченого, частково ненасиченого або ненасиченого вуглеводневою ланцюга. T' є групою формули: O R9 R9 є гідроксилом, аміно, -COOH, -NR10R11, -OR12, -SR12, -NR10(S=O)R11 або -NR10SO2R11, R10, R11 і R12 незалежно є в кожному випадку воднем або C1C6 алкілом, C2-C6 алкенілом, (арил)C0-C2 алкілом, (C3-C7 циклоалкіл)C0-C2 алкілом, (гетероциклоалкіл)C0-C2 алкілом або (5 - 10-членним гетероарил)C0-C2алкілом, кожний з поміж них є необов'язково заміщеним 1-3 замісниками, незалежно обраними з поміж галогену, гідроксилу, оксо, C1-C2 алкілу, C1-C2 алкокси, трифторметилу й трифторметокси: Z' представлене R21 X2 N R22 X3 X4 15 20 25 30 35 40 X5 X1 де X1, X2, X3, X4 і X5 незалежно є N або CH і не більше двох з X1-X5 представлені N. R21 представлене 0 - 3 групами, незалежно обраними з поміж галогену, гідроксилу, аміно, ціано, -CONH2, -COOH, C1-C4 алкілу, C2-C4 алканоїлу, C1-C4 алкокси, C1-C4 алкілтіо, моно- і ди-C1C4 алкіламіно, C1-C2 галогеналкілу й C1-C2 галогеналкокси. R22 є воднем, галогеном, гідроксил, аміно, ціано, -CONH2, -COOH, C1-C4 алкілом, C2C4алканоїлом, C1-C4 алкокси, C1-C4 алкілтіо, моно- і ди-C1-C4алкіламіно, складним C1-C4 алкіловим ефіром, C1-C2 галогеналкілом і C1-C2 галогеналкокси; або R22 є (C3-C7 циклоалкіл)C0C2 алкілом, (феніл)C0-C2алкілом, (феніл)C0-C2 алкокси, (5- або 6-членним гетероарил)C0C2алкілом, (5- або 6-членним гетероарил)C0-C2алкокси, нафтилом, інданілом, (5- або 6-членний гетероциклоалкіл)C0-C2 алкіл або 9- або 10 членний біциклічний гетероарил, кожний з поміж них є заміщеним 0, 1 або 2 замісниками, незалежно обраними з поміж (i) галогену, гідроксилу, аміно, ціано, нітро, -COOH, -CONH2, CH3(С=O)NH-, C1-C4алкілу, C1C4алкокси, C1-C4 гідроксиалкілу, моно- і ди-C1-C4 алкіламіно, -NR8SO2R11, -C(O)OR11, -NR8COR11, -NR8C(O)OR11, трифторметилу, трифторметокси й (ii) фенілу й 5- або 6-членного гетероарилу, кожний з яких є заміщеним 0 або 1 або більше групами галогену, гідроксилу, C1-C4 алкілу й C1-C2 алкокси; де R8 є воднем, C1-C4 алкілом або C3C6 циклоалкілом і R11 є таким, як визначено вище. R16 представлене 0-4 замісниками, незалежно обраними з поміж галогену, C 1-C2 алкілу й C1C2 алкокси. Будь-які з попередніх умов для сполук формули I можна використовувати разом для визначення субродових підмножин формули I остільки, оскільки в результаті буде отримана стабільна сполука, і всі такі субродові підмножини формули включені до даного винаходу. Даний винахід також включає фармацевтичні композиції й комбінації, що містять сполуки формули I і сполуки формули II, а також способи лікування, що включають уведення таких композицій/комбінацій пацієнтові, інфікованому гепатитом C. Наприклад, винахід включає композиції й комбінації, у яких сполука формули представлена 13 UA 110976 C2 O N O O O O N N O S N H HN O O або O N N S O O H N N F 5 O N F O O O S N H H O . Даний винахід також включає фармацевтичні композиції й комбінації, які містять сполуку формули I і сполуку формули II, а також способи лікування, які передбачають уведення таких композицій/комбінацій пацієнтові, інфікованому гепатитом C. Наприклад, винахід включає композиції й комбінації, у яких сполука формули II представлена O O N N N S O O O O O N N O O 10 15 20 HN O H N S N N H F N F O O O O O S N H H O або Інгібітори протеази NS3a формули II, придатні для використання у фармацевтичних композиціях і комбінаціях, описаних у даному документі, були описані раніше. Патент США № 7906619, виданий 15 березня 2011 року, тим самим включається шляхом посилання у всій його повноті щодо його концепції стосовно 4-аміно-4-оксобутаноїльних пептидів. Патент '619 конкретно включається шляхом посилання в розділі Приклади, починаючи від стовпчика 50 і до стовпчика 85, він описує сполуки, придатні для використання в композиціях/комбінаціях із сполуками формули I, описаними в даному документі. Опублікована заявка на патент США № 2010-0216725, опублікована 26 серпня 2010 року, тим самим включається шляхом посилання у всій її повноті щодо концепції стосовно 4-аміно-4оксобутаноїльних пептидів. Заявка '725 конкретно включається шляхом посилання в розділі «Приклади», починаючи зі сторінки 22 і до сторінки 100, вона описує сполуки, придатні для використання в композиціях/комбінаціях із Сполуками формули I, описаними в даному документі. 14 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 Опублікована заявка на патент США № 2010-0152103, опублікована 17 червня 2010 року, тим самим включається шляхом посилання у всій її повноті щодо її концепції стосовно циклічних аналогів 4-аміно-4-оксобутаноїльного пептиду. Заявка '103 конкретно включається шляхом посилання в розділі «Приклади», починаючи зі сторінки 19 і простираючись до сторінки 60, вона описує сполуки, придатні для використання в композиціях/комбінаціях із Сполуками формули I, описаними в даному документі. Фармацевтичні склади Сполуки, описані в даному документі, можуть уводитися як хімікалії, без добавок, але переважно вводяться у вигляді фармацевтичної композиції. Відповідно, винахід пропонує фармацевтичні композиції, які містять сполуки або фармацевтично прийнятну сіль формули I разом, щонайменше, з одним фармацевтично прийнятним носієм. Фармацевтична композиція/комбінація може містити сполуки або сіль формули I як єдиний активний агент, але бажано містить, щонайменше, один додатковий активний агент. У певних варіантах здійснення є бажаним, щоб додатковий активний агент був інгібітором протеази NS3a, таким як сполуки або сіль формули II. У певних варіантах здійснення фармацевтична композиція перебуває в дозованій формі, яка містить приблизно від 0,1 мг приблизно до 2000 мг, приблизно від 10 мг приблизно до 1000 мг, приблизно від 100 мг приблизно до 800 мг або приблизно від 200 мг приблизно до 600 мг сполуки формули I і, необов'язково, приблизно від 0,1 мг приблизно до 2000 мг, приблизно від 10 мг приблизно до 1000 мг, приблизно від 100 мг приблизно до 800 мг або приблизно від 200 мг приблизно до 600 мг додаткового активного агента в одиничній дозованій формі. Фармацевтична композиція може також містити деяке молярне відношення сполуки формули I і додаткового активного агента. Наприклад, фармацевтична композиція може мати молярне співвідношення приблизно 0,5:1, приблизно 1:1, приблизно 2:1, приблизно 3:1 або приблизно від 1,5:1 приблизно до 4:1 інгібітора протеази NS3a формули II до інгібітора NS5a формули I. Сполуки, описані в даному документі, можуть уводитися перорально, місцевим способом, парентерально, за допомогою інгаляції або спрея, сублінгвально, трансдермально, за допомогою букального введення, ректально, як офтальмічний розчин або за допомогою інших засобів, у препаратах одиничних доз, які містять звичайні фармацевтично прийнятні носії. Фармацевтична композиція може бути приготовлена у вигляді будь-якої фармацевтично придатної для використання форми, наприклад, як аерозоль, крем, гель, пігулка, капсула, таблетка, сироп, трансдермальний пластир або офтальмічний розчин. Деякі дозовані форми, такі як таблетки й капсули, розділяються на одиничні дози відповідного розміру, що містять відповідні кількості активних компонентів, наприклад, кількість ефективну для досягнення бажаної мети. Носії включають наповнювачі й розріджувачі й повинні мати досить високу чистоту й досить низьку токсичність, щоб зробити їх придатними для введення пацієнтові, якого лікують. Носій може бути інертним або він може мати фармацевтичні якості як такий. Кількість носія, який використовується в комбінації із сполукою, є достатньою для забезпечення практичної кількості матеріалу для введення за допомогою одиничної дози сполуки. Класи носіїв включають, але, не обмежуються цим зв'язувальні речовини, буферні агенти, барвники, розріджувачі, розпушувачі, емульгатори, ароматизатори, гліданти, змащувальні речовини, консерванти, стабілізатори, поверхнево-активні речовини, таблетуючі агенти й змочувальні агенти. Деякі носії можуть бути перерахованими в декількох класах, наприклад, рослинну олію можна використовувати як змащувальну речовину в деяких препаратах і як розріджувач в інших. Ілюстративні фармацевтично прийнятні носії включають цукри, крохмалі, целюлози, порошкоподібну смолу трагаканта, солод, желатин; тальк і рослинні олії. Необов'язкові активні агенти можуть включатися до фармацевтичної композиції, вони власне не впливають негативно на активність сполуки запропонованої даним винаходом. Фармацевтичні композиції/комбінації можуть бути приготовлені для перорального введення. Ці композиції містять у межах між 0,1 і 99% мас (% мас) сполуки формули I і звичайно, щонайменше, приблизно 5% мас сполуки формули. Деякі варіанти здійснення містять приблизно від 25% мас приблизно до 50% мас або приблизно від 5% мас приблизно до 75% мас сполуки формули. Способи лікування Фармацевтичні композиції/комбінації, описані в даному документі, є придатними для використання при лікуванні інфекції гепатиту C у пацієнтів. Даний винахід пропонує способи лікування вірусних інфекцій, включаючи інфекції гепатиту C, за допомогою надання ефективної кількості сполуки або фармацевтично прийнятної солі формули I пацієнтові, інфікованому вірусом гепатиту C. Сполука або сіль формули I може 15 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 надаватися як єдиний активний агент або може надаватися разом з одним або декількома додатковими активними агентами. У певних варіантах здійснення сполука або сіль формули I уводяться разом із сполукою або сіллю формули II або з іншим інгібітором протеази NS3a. У певному варіанті здійснення фармацевтична композиція містить сполуку формули I разом з інгібітором NS5b і, необов'язково, додатковий активний агент. Ефективна кількість фармацевтичної композиції/комбінації запропонованої даним винаходом може бути кількістю достатньою для (a) інгібування розвитку гепатиту C; (b) щоб викликати регресію інфекції гепатиту C; або (c) для того, щоб викликати лікування інфекції гепатиту C таким чином, щоб вірус ВГС або антитіла ВГС не детектувалися би більше в крові або плазмі раніше інфікованого пацієнта. Кількість фармацевтичної композиції/комбінації, яка є ефективною для інгібування розвитку або для того, щоб викликати регресію гепатиту C, включає кількість ефективну для припинення погіршення симптомів гепатиту C або для зменшення симптомів, випробовуваних пацієнтом, інфікованим вірусом гепатиту C. Альтернативно, припинення розвитку або регресія гепатиту C може виявлятися за допомогою кожного з декількох маркерів захворювання. Наприклад, відсутність збільшення або зниження навантаження вірусу гепатиту C або відсутність збільшення або зменшення кількості антитіл ВГС, які циркулюють у крові пацієнта, є маркерами припинення розвитку або регресії інфекції гепатиту C. Інші маркери захворювання гепатитом C включають рівні амінотрансферази, зокрема, рівні ферментів печінки AST і ALT. Нормальні рівні AST становлять від 5 до 40 одиниць на літр сироватки (рідкої частини крові) і нормальні рівні ALT становлять від 7 до 56 одиниць на літр сироватки. Ці рівні, як правило, будуть підвищеними в пацієнта, інфікованого ВГС. Регресію захворювання зазвичай видно за поверненням рівнів AST і ALT до нормального діапазону. Симптоми гепатиту C, на які може впливати ефективна кількість фармацевтичної композиції/комбінації запропонованої даним винаходом, включають знижену функцію печінки, утому, симптоми, подібні до грипу: жар, озноб, м'язові болі, болі в суглобах і головні болі, нудоту, відразу до певних харчових продуктів, безпричинну втрату ваги, фізіологічні розлади, включаючи депресію, відчуття важкості в шлунку й розлиття жовчі. "Функція печінки" відноситься до нормальної функції печінки, включаючи, але, не обмежуються цим, функцію синтезу, що включає синтез білків, таких як сироваткові білки (наприклад, альбумін, фактори згортання, лужна фосфатаза, амінотрансфераза (наприклад, аланінтрансаміназа, аспартаттрансаміназа), 5'-нуклеозидаза, y глютамінілтранспептидаза тощо), синтез білірубіну, синтез холестерину й синтез жовчних кислот; метаболічну функцію печінки, включаючи метаболізм вуглеводів, метаболізм амінокислот і аміаку, метаболізм гормонів і метаболізм ліпідів; детоксифікацію екзогенних лікарських засобів і гемодинамічну функцію, включаючи спланхічну й портальну гемодинаміку. Ефективна кількість фармацевтичної композиції/комбінації, описаної в даному документі, буде також забезпечувати достатню концентрацію активних агентів у концентрації композиції при введенні пацієнтові. Достатня концентрація активного агента є такою концентрацію агента в організмі пацієнта, яка є необхідною для запобігання інфекції або для боротьби з нею. Така кількість може бути визначеною експериментально, наприклад, за допомогою аналізу концентрації агента в крові, або теоретично, за допомогою обчислення біологічної доступності. Кількість активного агента достатня для інгібування вірусної інфекції in vitro може визначатися за допомогою звичайного аналізу на вірусну інфекційність, такого як аналіз на основі реплікона, який описаний у літературі. Фармацевтичні композиції/комбінації й способи лікування, у яких сполука або сіль формули I надається разом з одним або декількома додатковими активними агентами, включаються до даного документа. У кращих варіантах здійснення сполука формули I надається разом з інгібітором протеази NS3a, або в єдиній фармацевтичній композиції, або в роздільних дозованих формах з інструкціями для пацієнта щодо того, щоб використовувати разом сполуки формули I і додатковий активний агент. Сполуки формули II і сполуки, описані в патенті США № 7906619, у заявці на патент США № 2010-0216725 і в заявці на патент США № 2010-0152103, більша частина яких перебувають у рамках формули II, є придатними для використання інгібіторами протеази NS3a для використання в комбінації із сполуками й солями формули I. У певних варіантах здійснення активний агент (або агенти) являє собою інгібітор протеази ВГС або інгібітор полімерази ВГС. Наприклад, інгібітор протеази може бути телапревір (VX-950), а інгібітор полімерази може бутп валоцикітабін або NM 107, активний агент, який перетворить валопіцитабін in vivo. У певних варіантах здійснення, щонайменше, один додатковий активний агент є рибавірином, інтерфероном або альфа кон′югат Peg-інтерферон. У певних варіантах 16 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 здійснення, щонайменше, один додатковий активний агент представлений ACH-1625 або ACH2684. У відповідно до способів даного винаходу, сполуки або фармацевтично прийнятна сіль формули I і, щонайменше, один додатковий активний агент можуть: (1) готуватися спільно й уводитися або доставлятися одночасно в об'єднаному препараті; (2) доставлятися почергово або в паралельно як окремі препарати або (3) доставлятися за допомогою будь-якого іншого режиму комбінованої терапії, відомого в даній галузі. При доставці при почерговій терапії, способи запропоновані даним винаходом можуть включати введення або доставку сполуки або солі формули I і додаткового активного агента послідовно, наприклад, в окремому розчині, емульсії, суспензії, таблетках, пігулках або капсулах, або за допомогою різних ін'єкцій в окремих шприцах. Як правило, протягом почергової терапії, ефективна доза кожного активного інгредієнта вводиться послідовно, тобто, у вигляді серії, у той час як при одночасній терапії, ефективні дози двох або більш активних інгредієнтів уводяться разом. Можна також використовувати різні послідовності періодичної комбінованої терапії. Способи лікування й фармацевтичні комбінації, які містять сполуки або фармацевтично прийнятні солі формули I, описані в даному документі, разом з кожною із наведених далі сполук і речовин як додатковим активним агентом або їх комбінацією наведені в описі: Анти-фібротики: IP-501 (InterMune) Інгібітори каспази: IDN-6556 (Idun Pharmaceuticals) і GS-9450 (Gilead) Інгібітори циклофіліну: наприклад, NIM811 (Novartis), SCY-635 (Scynexis) і DEBIO-025 (Debiopharm); Інгібітори моноокисмгенази цитохрому P450: ритонавір, кетоконазол, тролеандоміцин, 4метилпіразол, циклоспорин, клометиазол, циметидин, ітраконазол, флуконазол, міконазол, флувоксамін, флуоксетин, нефазодон, сертралин, індинавір, нельфинавір, ампренавір, фозампренавір, сахінавір, лопінавір, делавірдин, еритроміцин, VX-944 і VX-497 (Merimebodib). Кращі інгібітори CYP включають ритонавір, кетоконазол, тролеандоміцин, 4-метил піразол, циклоспорин і клометиазол; Глюкокортикоїди: гідрокортизон, кортизон, преднізон, преднізолон, метилпреднізолон, триамцинолон, параметазон, бетаметазон і дексаметазон. Інгібітори протеази ВГС: наприклад, ACH-1625 і ACH-2684. Патент США номер 7906619 тим самим включається в даний документ щодо його концепції стосовно анти-ВГС сполуки. Заявки на патент США №№ 12/635270 на сторінках 52-167 і 12/635049 на сторінках 43-92 тим самим включаються як посилання щодо їхньої концепції стосовно анти-ВГС сполуки, ACH 1625 і ACH 2684 (Achillion), ABT-450 (Abbott), ACL-181 і AVL-192 (Avila), BI-335 (Boehringer Ingelheim), BMS032 (Bristol Meyers Squibb), боцепревір (Merck), TMC-435, MK-7152 (Merck), GS-9256 (Gilead), GS-9451 (Gilead), R7227 (Intermune), VX-500 (Vertex), VX-950 (телапревир, Vertex), VX-985 (Vertex), TMC-435 (Tibotec), GW-433908 (проліки ампренавіру, Glaxo/Vertex), індинавір (CRIXIVAN, Merck), ITMN-191 (Intermune/Array Biopharma), BILN 2061 (Boehringer-Ingelheim), TMC435350 (Tibotec/Medivir), BI 201335 (Boehringer Ingelheim), PHX-1766 (Phenomix), MK-7009 (Merck), нарлапревір (SCH900518, Schering) Гематопоетини: гематопоетин-1 і гематопоетин-2. Інші члени суперродини гематопоетинів, такі як різноманітні колонієстимулюючі фактори (наприклад, (наприклад, G-CSF, GM-CSF, MCSF), Epo і SCF (фактор стовбурових клітин) Гомеопатична терапія: розторопша, силімарин, женьшень, гліциризин, корінь лакричника, шизандра, вітамін C, вітамін E, бета каротин і селен Імуномодуляторні сполуки: талідомід, IL-2, гематопоетини, інгібітори EVIPDH, наприклад, меримеподиб (Vertex Pharmaceuticals Inc.), інтерферон, включаючи природний інтерферон (такий як OMNIFERON, Viragen and SUMIFERON, Sumitomo, суміші природних інтерферонів), природний інтерферон альфа (ALFERON, Hemispherx Biopharma, Inc.), інтерферон альфа nl з лімфабластоїдних клітин (WELLFERON, Glaxo Wellcome), пероральний альфа інтерферон, Pegінтерферон, Peg-інтерферон альфа 2a (PEGASYS, Roche), рекомбінантний інтерферон альфа 2a (ROFERON, Roche), інтерферон альфа 2b для інгаляцій (AERX, Aradigm), Peg-Інтерферон альфа 2b (ALBUFERON, Human Genome Sciences/Novartis, PEGINTRON, Schering), рекомбінантний інтерферон альфа 2b (INTRON A, Schering), пегільований інтерферон альфа 2b (PEGINTRON, Schering, VIRAFERONPEG, Schering), інтерферон бета-1a (REBIF, Ares-Serono, Inc. and Pfizer), консенсусний інтерферон альфа (INFERGEN, Intermune), інтерферон гама-1b (ACTIMMUNE, Intermune, Inc.), Un-пегільований інтерферон альфа, альфа інтерферон та його аналоги, і синтетичний тимозин альфа 1 (ZADAXIN, Sciclone Pharmaceuticals Inc.) та інтерферон лямбда (BMS) Імуносупресанти: сиролімус (RAPAMUNE, Wyeth) 17 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 Інтерлейкіни: (IL-1, IL-3, IL-4, IL-5, IL-6, IL-10, IL-11, IL-12), LIF, TGF-бета, TNF-альфа) та інші низькомолекулярні фактори (наприклад, AcSDKP, pEEDCK, гормони щитовидної залози й мініцитокіни) Підсилювачі інтерферону: EMZ702 (Transition Therapeutics) Інгібітори IRES: VGX-410C (VGX Pharma) Моноклональні й поліклональні антитіла: XTL-6865 (HEPX-C, XTL), HuMax-HepC (Genmab), імуноглобин гепатиту C (людини) (CIVACIR, Nabi Biopharmceuticals), XTL-002 (XTL), ритуксимаб (R1TUXAN, Genentech/ IDEC) Нуклеозидні аналоги: IDX-184 (Idenix), PSI-7977 і PSI-938 (Pharmasset), INX-189 (Inhibitex), R7128 (Roche), R7348 (Roche), GS-6620 (Gilead), TMC-649 (Tibotec), ламівудин (EPIVIR, 3TC, Glaxosmithkline), MK-0608 (Merck), зальцитабін (HIVID, Roche US Pharmaceuticals), рибавірин (включаючи COPEGUS (Roche), REBETOL (Schering), VILONA (ICN Pharmaceuticals і VIRAZOLE (ICN Pharmaceuticals), ізоторибін (Anadys Pharmaceuticals), ANA971 (Anadys Pharmaceuticals), ANA245 (Anadys Pharmaceuticals) і вірамідин (ICN), амідинові проліки рибавірину. Можна також використовувати комбінації нуклеозидних аналогів. Не-нуклеозидні інгібітори: PSI-6130 (Roche/Pharmasset), ABT-333 і ABT-072 (Abbott), делавіридин (RESCRIPTOR, Pfizer), PF-868554 (Pfizer), GSK-852 (Glaxosmithkline), IDX-325 (Idenix), ANA-598 (Anadys), VX-222 і VX-759 (Vertex), MK-3281 (Merck), BI-127 (Boehringer Ingelheim), BMS-325 (Bristol Meyers) і ВГС-796 (Viropharm) Інгібітори NS4a: наприклад, ACH-1095. Заявка на патент США № US2007/0004711 тим самим включається шляхом посилання у всій її повноті відносно її концепції стосовно інгібіторів ВГС і заявка на патент США № 12/125554 на сторінках 45-90 тим самим включається шляхом посилання відносно її концепції стосовно інгібіторів ВГС. Інгібітори NS4b: клемізол (Arrow Therapeutics) Інгібітори NS5a: A-382 (Arrow Therapeutics), BMS-790052 (BMS) Інгібітори NS5b: INX-181, IDX-375, MK-3281, PSI-7977, PSI-7851, PSI-938, RG-9190, VX-222 (Vertex) і BMS-791325 (Bristol Meyers Squibb). Інгібітор білка P7: амантадин (SYMMETREL, Endo Pharmaceuticals, Inc.) Інгібітори полімерази: філібувір (PF-00868554, Pfizer), NM283 (валопіцитабін) (Idenix), JTK 003 (AKROS Pharma), ВГС-796 (ViroPharma/Wyeth), IDX184 (Idenix), VCH-916 (Vertx), R7128 (PSI6130, Roche), R1626 (Roche), MK-3281 (Merck), PSI-7851 (Pharmasset), ANA598 (Anadys), BI207127 (Boehringer-Ingelheim), GS 9190 (Gilead). Інтерференційна РНК: SIRNA-034 RNAi (Sirna Therapeutics) і ISI 14803 (Isis Pharmaceutical/Elan) Терапевтичні вакцини: IC41 (Intercell), IMN-0101 (Imnogenetics), GI 5005 (Globeimmune), Chronvac-C (Tripep/Inovio), ED-002 (Imnogenetics), Hepavaxx C (Virex Medical) Агоністи TNF: адалімумаб (HUMIRA, Abbott), ентанерцепт (ENBREL, Amgen and Wyeth), інфліксимаб (REMICADE, Centocor, Inc.) Інгібітори тубуліну: колхіцин Модулятори рецепторів сфінгозин-1-фосфату: FTY720 (Novartis) Агоністи TLR: ANA-975 (Anadys Pharmaceuticals), агоніст TLR7 (Anadys Pharmaceuticals), CPGLOLOL(Coley) і агоністи TLR9, включаючи CPG 7909 (Coley). Вакцини: ВГС/MF59 (Chiron), IC41 (Intercell), E-1 (Innogenetics) Пацієнти, які приймають лікарські препарати проти гепатиту C, як правило, одержують інтерферон разом з іншим активним агентом. Таким чином, способи лікування й фармацевтичні комбінації, у яких сполуки запропоновані даним винаходом надаються разом з інтерфероном, таким як пегільований інтерферон альфа 2a, як додаткових активних агентів, включаються як варіанти здійснення. Подібним же чином способи й фармацевтичні комбінації, у яких рибавірин є додатковим активним агентом, пропонуються в даному документі. Способи інгібування реплікації ВГС in vivo, які включають надання сполуки або фармацевтично прийнятні солі формули I пацієнтові, інфікованому ВГС, концентрація сполуки або солі формули I, достатня для інгібування реплікації за допомогою реплікона ВГС in vitro, включаються до даного документа. У цьому випадку концентрація включає концентрацію in vivo, таку як концентрація в крові або плазмі. Концентрація сполуки, достатня для інгібування реплікації за допомогою реплікона ВГС in vitro, може бути визначена з аналізу реплікації за допомогою реплікона, такого як аналіз, наведений у прикладі 9, у даному документі. Способи лікування передбачають надання певних дозованих кількостей сполуки або фармацевтично прийнятної солі формули I пацієнтові. Рівні дозування кожного активного агента приблизно від 0,1 мг приблизно до 140 мг на кілограм маси тіла на день є придатними і для використання при лікуванні зазначених вище станів (приблизно від 0,5 мг приблизно до 7 г на 18 UA 110976 C2 5 10 15 20 25 30 35 40 45 50 55 60 пацієнта на день). Кількість активного інгредієнта, яка може поєднуватися з матеріалами носіїв з одержанням однієї одиничної дозованої форми, буде змінюватися залежно від пацієнта, якого лікують, і від конкретного режиму введення. У певних варіантах здійснення приблизно від 0,1 мг приблизно до 2000 мг, приблизно від 10 мг приблизно до 1500 мг, приблизно від 100 мг приблизно до 1000 мг, приблизно від 200 мг приблизно до 800 мг або приблизно від 300 приблизно до 600 мг сполуки формули I і, необов'язково, приблизно від 0,1 мг приблизно до 2000 мг, приблизно від 10 мг приблизно до 1500 мг, приблизно від 100 мг приблизно до 1000 мг, приблизно від 200 мг приблизно до 800 мг, або приблизно від 300 приблизно до 600 мг сполуки додаткового активного агента, наприклад, інгібітору протеази NS3a, такого як сполуки формули II, надаються пацієнтові щодня. Краще, щоб кожна одинична дозована форма містила менше ніж 1200 мг активного агента в цілому. Частота дозування може також змінюватися залежно від використаної сполуки й від конкретного захворювання, яке лікують. Однак для лікування більшості інфекційних розладів, режим дозування 4 рази на день або менше є кращим, а режим дозування 1 або 2 рази на день є найкращим. Однак буде зрозуміло, що конкретний рівень дозування для будь-якого конкретного пацієнта буде залежати від різноманітних факторів, включаючи активність конкретної використаної сполуки, вік, масу тіла, загальний стан здоров'я, стать, дієту, час уведення, спосіб уведення й швидкість виділення, комбінацію лікарських засобів і тяжкість конкретного захворювання в пацієнта, який потребує терапії. Упаковані склади Способи, які включають надання сполуки або солі формули I у контейнері разом з інструкціями для використання сполуки для лікування пацієнта, який страждає від інфекції гепатиту C, включаються у даний документ. Упаковані фармацевтичні композиції/комбінації також включаються в даний документ. Такі упаковані комбінації включають сполуки формули I у контейнері разом з інструкціями для використання комбінації для лікування або запобігання вірусної інфекції, такої як інфекція гепатиту C у пацієнта. Упакована фармацевтична композиція/комбінація може включати один або кілька додаткових активних агентів. У певних варіантах здійснення додатковий активний агент є інгібітором протеази NS3a, таким як сполука формули II. Упакована фармацевтична комбінація може містити сполуки або фармацевтично прийнятну сіль формули I і додатковий активний агент, надавані одночасно в одній дозованій формі, одночасно в окремих дозованих формах, або надавані в окремих дозованих формах для введення, розділеного певним проміжком часу, що перебуває в межах того часу, протягом якого як сполука формули I, так і додатковий активний агент перебувають у кров′яному руслі пацієнта. Упакована фармацевтична комбінація може включати сполуку або фармацевтично прийнятну сіль формули I, надану в контейнері, з додатковим активним агентом, наданим у цьому ж або в окремому контейнері, з інструкціями для використання комбінації для лікування інфекції ВГС у пацієнта. Приклади Скорочення Наведені далі скорочення використовуються в схемах реакції й прикладах синтезу, які описуються далі. Цей список не передбачається як повний список скорочень, використовуваних у заявці, оскільки додаткові стандартні скорочення, які є легко зрозумілими фахівцям в галузі органічного синтезу, також можуть використовуватися в схемах і прикладах синтезу. Ac ацетил ACN ацетонітрил водн. водний розчин BOC трет-бутоксикарбоніл DCM дихлорметан DIEA N,N-диізопропілетиламін DIPEA N,N-диізопропілетиламін DME 1,2-диметоксиетан DMF N,N-диметилформамід dppf 1,1'-біс(дифенілфосфіно)фероцен EDCI N-(3-диметиламінопропіл)-N'-етилкарбодиімід гідрохлорид Et етил Et2O простий діетиловий ефір FCC колонкова флеш-хроматографія HATU O-(7-азабензотриазол-1-іл)-N,N,N',N'-тетраметилуроній гексафторфосфат 19 UA 110976 C2 5 10 15 20 25 MTBE простий метил трет-бутиловий ефір ПТСХ препаративна тонкошарова хроматографія к. т. кімнатна температура TEA триетиламін TFA трифтороцтова кислота THF тетрагідрофуран TPP трифенілфосфін Загальні міркування Усі неводні реакції здійснюють в атмосфері сухого газоподібного аргону з використанням скляного посуду, висушеного в печі, і безводних розчинників. Хід реакцій і чистоту цільових сполук визначають із використанням одного з двох наступних методів ВЕРХ: (1) колонка 1,7 мкм 2,1 × 50 мм Waters AQUITY UPLC BEH C18 з ізократичним елююванням, 0,24 хв. за допомогою суміші вода:ацетоїл, 90:10, що містить 0,05% мурашиної кислоти, потім відбувається 4,26-хв. елюювання в лінійному градієнті від 90:10 до 10:90 за швидкості потоку 1,0 мл/хв., детектування за допомогою УФ (PDA (фотодіодної матриці)), ELS (спектроскопії енергетичних втрат електронів) і MS (мас-спектрометрії (SQ у режимі APCI (хімічної іонізації за атмосферного тиску)) (метод 1); і (2) колонка 1,7 мкм 2,1 × 50 мм Waters AQUITY UPLC BEH C18 з ізократичним елююванням 0,31 хв. із допомогою суміші вода:ацетонітрил, 95:5, яка містить 0,05% мурашиної кислоти, потім відбувається 17,47-хв. елюювання в лінійному градієнті від 95:5 до 5:95 за швидкості потоку 0,4 мл/хв., детектування за допомогою УФ (PDA), ELS і MS (SQ у режимі APCI) (метод 2). Цільові сполуки очищають за допомогою препаративної ВЕРХ зі оберненою фазою з використанням колонки 5 мкм 150 × 20 мм YMC Pack Pro C18 з ізократичним елююванням 0,35 хв. за допомогою суміші вода:ацетонітрил, 95:5, що містить 0,1% трифтороцтової кислоти, потім відбувається 23,3-хв. елюювання в лінійному градієнті від 95:5 до 5:95 за швидкості потоку 18,9 мл/хв., детектування за допомогою УФ і збір фракцій за масою. Загальна схема синтезу 20 UA 110976 C2 5 10 15 20 Приклад 1. Синтез сполуки 10 Сполуку 10 готують за допомогою бромування [2,2]парациклофану, як описано раніше (Reich, H.J.; Cram, D.J. J. Am. Chem. Soc. 1969, 91, 3527-3533; Reich, H.J.; Cram, D.J. J. Am. Chem. Soc. 1969, 91, 3534-3543). Сполуки 1, 2, 6, 8 і 10 можуть бути отримані з комерційних джерел. Сполуки 3-7 і 9 готують із використанням загальних способів синтезу, відомих у даній галузі. Приклад 2. Синтез сполуки 11 Деоксигеновану (аргон) суміш 9 (284,2 мг), 10 (52,3 мг), K 3PO4 (248,1 мг) і PdCl2dppf∙CH2Cl2 (7,4 мг) у диоксані/воді (5,5, мл/0,55 мл) опромінюють у мікрохвильовій печі протягом 2 годин при 80 °C. Отриману суміш випаровують за зниженого тиску і решту твердого продукту екстрагують DCM. Цей сирий матеріал очищають за допомогою ПТСХ (скляні пластини 20 см × 20 см × 2000 мкм; елююють за допомогою DCM:EtОАc:МеОН, 45:50:5 об′єм/об′єм/об′єм, Rf 0,28) з одержанням 75,3 мг 11. Чистоту 11 визначають за допомогою аналітичної ВЕРХ зі оберненою фазою з використанням 3,5-хв. градієнтого елюювання з підвищенням концентрації ACN у воді (10-90%), що містить 0,05% мурашиної кислоти, за швидкості потоку 1,0 мл/хв. на колонці 1,7 мкм 2,1 × 50 мм Waters AQUITY UPLC BEH C18, детектування за допомогою УФ (PDA), ELS і MS (SQ у режимі APCI). ВЕРХ: tr 1,57 хв. (чистота 98%). MS m/z обчислене для C 56H64N8O6 ([M]+), 945; знайдене, 946 ([M + 1]+). Приклад 3. Синтез диметил ((2S,2'S)-((2S,2'S,3aS,3a'S,7aS,7a'S)-2,2'-(5,5'4,7 (трицикло[8,2,2,2 ]гексадека-4,6,10,12,13,15-гексаєн-5,11-диіл)біс(1H-бензо[D]-імідазол-5,2диіл))біс(октагідро-1H-індол-2,1-диіл))біс(3-метил-1-оксобутан-2,1-диіл))дикарбамату (20) Стадія 1 21 UA 110976 C2 5 10 15 20 25 30 35 40 45 До розчину, що перемішується (2R,3aS,7aS)-октагідро-1H-індол-2-карбонової кислоти (250 г, 1,0 екв.) (12) в THF (3 л) та воді (1,5 л) при 0 °C, додають краплинами охолоджений водний розчин 2,5 M NaOH (1 л). Реакційну суміш перемішують протягом 15 хв. за такої ж температури. Потім додають краплинами ди-трет-бутилдикарбонат (1,3 екв.), підтримуючи температуру 0 °C. Отриману реакційну суміш перемішують за кімнатної температури протягом 12 годин. Реакційну суміш промивають MTBE (3 рази). Водну фазу підкислюють за допомогою 1 M водного розчину лимонної кислоти й екстрагують етилацетатом (3 рази). Об'єднані органічні шари сушать над сульфатом натрію й концентрують насухо з одержанням (2R,3aS,1aS)-1-(третбутоксикарбоніл)октагідро-1H-індол-2-карбонової кислоти (368 г) (13). Стадія 2 До розчину, що перемішується, 4-бром-1,2-диамінобензолу (23,1 г, 1,2 екв.), (2R,3aS,7aS)-1(трет-бутоксикарбоніл)октагідро-1H-індол-2-карбонової кислоти (26,9 г, 1,0 екв.) 13 і EDCI (23,6 г, 1,2 екв.) в ACN (600 мл) при°0 C краплинами додають DIEA (21,5 мл, 1,3 екв.). Реакційну суміш перемішують додатково протягом 1 години після завершення додавання. Додають воду (1,2 л), і реакційну суміш перемішують протягом ночі. Твердий порошок (14) збирають, промивають водою й сушать для використання на наступній стадії без додаткового очищення (39,1 г). Стадія 3 Ізомерну суміш (14) (2S,3aS,7aS)-трет-бутил-2-((2-аміно-4-бромфеніл)карбамоіл)октагідро1H-індол-1-карбоксилату та (2S,3aS,7aS)-трет-бутил-2-((2-аміно-5-бромфеніл)карбамоїл)октагідро-1Н-індол-1-карбоксилату (160 г, 0,36 моль) розчиняють в оцтовій кислоті (480 мл) і реакційну суміш перемішують при 65 °C доти, поки не витратяться вихідні матеріали (що оцінюють за допомогою аналізу РХ-МС). Реакційну суміш охолоджують до кімнатної температури, і розчинник видаляють у вакуумі. Залишок, що залишився, розчиняють в етилацетаті (500 мл), і обережно додають водний розчин аміаку (100 мл). Додають додаткову воду (100 мл), і органічний шар відокремлюють і збирають. Водну фазу екстрагують етилацетатом (2 × 300 мл). Об'єднану органічну фазу промивають водою (200 мл), а потім насиченим розчином солі (200 мл), і сушать над MgSO 4. Розчин концентрують, й решту залишку очищають за допомогою колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням (2S,3as,7as)-трет-бутил-2-(6-бром-1H-бензо[d]імідазол-2-іл)октагідро-1Н-індол-1карбоксилату (15) (140 г). Стадія 4 В атмосфері аргону, суміш (2S,3as,7as)-трет-бутил-2-(6-бром-1H-бензо[d]імідазол-2іл)октагідро-1Н-індол-1-карбоксилату (15) (30 г, 1,0 екв.), біс(пінаколято)диборану (27,2 г, 1,5 екв.), ацетату калію (21 г, 3,0 екв.) і Pd(dppf)Cl2 (5,7 г, 0,098 екв.) у безводному 1,4-диоксані (300 мл) нагрівають при 80-90 °C протягом ~4 годин (доти, поки реакція не завершиться, як оцінюють за допомогою РХ-МС). Охолоджену (кімнатна температура) реакційну суміш розбавляють етилацетатом (300 мл), перемішують разом з активованим вугіллям (60 г) протягом 1 години, і фільтрують через пад із целіту. Фільтрат концентрують за зниженого тиску, і отриману коричневу піну очищають за допомогою колонкової хроматографії на силікагелі (гексан/етилацетат, 5:1 → 1:2 об′єм/об′єм) з одержанням (2S,3as7as)-трет-бутил-2-(6-(4,4,5,5тетраметил-1,3,2-диоксаборолан-2-іл)-1H-бензо[d]імідазол-2-іл)октагідро-1Н-індол-1карбоксилату у вигляді білуватого твердого продукту) (16). 22 UA 110976 C2 Стадія 5 5 10 15 Суміш Br2 (82,8 г) і порошку заліза (4,6 г) в DCM (1,6 л) перемішують за кімнатної температури протягом 1 години. До цієї суміші додають, однією порцією, суспензію [2,2]парациклофану (200 г, 1,0 екв.) в DCM. Отриману суміш нагрівають зі зворотним холодильником, і до неї повільно додають розчин Br 2 (228 г) в DCM (400 мл) протягом 3годинного періоду. Після завершення цього додавання, реакційну суміш продовжують нагрівати зі зворотним холодильником протягом 3 годин, дають можливість для охолодження до кімнатної температури з перемішуванням протягом ночі, промивають 5% мас/об’єм водним розчином Na2S2O3 (2 л) і водою (2 л), сушать (MgSO 4) і випаровують насухо. Виділений сирий твердий продукт розчиняють у гарячому толуолі (1,2 л, ~100 °C), дають можливість йому для повільного охолодження протягом ночі до кімнатної температури при перемішуванні й додатково охолоджують до 5 °C протягом 3 годин. Отриманий твердий продукт збирають і промивають 1 холодним толуолом (~100 мл) з одержанням 4,16-дибром[2,2]парациклофану (17) (83 г). H ЯМР (300 МГц, CdCl3, к.т.): δ 2,79-3,00 (м, 4H), 3,10-3,21 (м, 2H), 3,44-3,54 (м, 2H), 6,44 (д, J=2,0 Гц, 2H), 7,14 (дд, J=8,0 Гц, 2,0 Гц, 2H). Стадія 6 35 В атмосфері аргону, суміш 4,16-дибром[2,2]парациклофану (17) (20 г, 1,0 екв.), (2S,3as,7as)трет-бутил-2-(6-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-іл)-1H-бензо[d]імідазол-2іл)октагідро-1Н-індол-1-карбоксилату (64 г, 2,5 екв.), CS2CO3 (16) (44,5 г, 2,5 екв.), Pd(PPh3)4 (3,16 г, 0,05 екв.), DMF (500 мл) і води (25 мл) нагрівають при 130 °C протягом ~2-3 годин (доти, поки реакція не завершиться, як оцінюють за допомогою РХ-МС). Реакційній суміші дають можливість охолодитись до кімнатної температури, і фільтрують її через пад із силікагелю (30 г), із шаром целіту. Цей пад промивають DMF (2 × 50 мл), і об'єднані фільтрати додають у воду, що перемішується (2,5 л) з одержанням блідо-жовтого преципітату. Цей твердий продукт збирають за допомогою фільтрування, промивають водою (1 л) і ACN (500 мл) і розчиняють у суміші DCM (250 мл) і МеОН (25 мл). До цього розчину додають ACN (250 мл) для генерування дрібнодисперсної суспензії, яку потім концентрують за зниженого тиску при 30-35 °C для видалення ~150 мл розчинника. Додають іншу порцію ACN (500 мл), і додатковий розчинник (~100 мл) видаляють за зниженого тиску при 40-45 °C. Твердий продукт збирають за допомогою фільтрування й сушать у вакуумі з одержанням (2S,2'S, 3as,3a'S,7as,7a'S)-ди-трет-бутил-2,2'4,7 (5,5'-(трицикло-[8,2,2,2 ]гексадека-4,6,10,12,13,-гексаєн-5,11-диіл)біс(1H-бензо[d]імідазол-5,2диіл))біс(октагідро-1Н-індол-1-карбоксилату) у вигляді блідо-жовтого порошку (33,8 г). Стадія 7 40 До охолодженого (0 °C) розчину (2S,2'S, 3as,3a'S,7as,7a'S)-ди-трет-бутил 2,2'-(5,5'4,7 (трицикло-[8,2,2,2 ]-гексадека-4,6,10,12,13,15-гексаєн-5,11-диіл)біс(1H-бензо[d]імідазол-5,2диіл))біс(октагідро-1Н-індол-1-карбоксилату) (18) (20,33 г, 1,0 екв.) в DCM/МеОН (4/1 об′єм/об′єм, 200 мл) додають 4 н розчин HCl/диоксан (100 мл). Реакційну суміш перемішують за 20 25 30 23 UA 110976 C2 5 10 15 20 25 30 35 кімнатної температури протягом 30 хв. і концентрують за зниженого тиску з одержанням блідожовтого порошку (19) (21,7 г). Отриманий твердий продукт сушать у вакуумі доти, поки 1 залишковий МеОН не перестане детектуватися за допомогою спектроскопічного аналізу H ЯМР. Цей матеріал, ретельно висушений, використовують безпосередньо на наступній стадії. Стадія 8 До суміші (S)-2-((метоксикарбоніл)аміно)-3-метилбутанової кислоти (10 г, 2,3 екв.), HOBt моногідрату (8,8 г, 2,3 екв.) і ACN (50 мл) за кімнатної температури додають EDCI (11,14 г, 2,3 екв.). Після перемішування протягом 5 хв., цю активовану кислотну суміш додають до розчину гідрохлоридної солі (19), описаної вище (21,7 г) і DIEA (32 мл, 7,2 екв.), в DMF (250 мл). Реакційну суміш перемішують за кімнатної температури доти, поки реакція не завершиться, що визначають за допомогою аналізу за допомогою РХ-МС (~4 година), а потім виливають у воду (1,2 л) перемішуючи. Преципітат збирають за допомогою фільтрування, перемішують в ACN/воді (4:1 об′єм/об′єм, 500 мл) протягом ночі, збирають знову за допомогою фільтрування й висушують у вакуумі з одержанням диметил ((2S,2'S,)-((2S,2'S,3aS,3a'S,7aS,7a'S)-2,2'-(5,5'4,7 (трицикло[8,2,2,2 ]гексадека-4,6,10,12,13,15-гексаєн-5,11-диіл)біс(1H-бензо[d]імідазол-5,2диіл))біс(октагідро-1H-індол-2,1-диіл))біс(3-метил-1-оксобутан-2,1-диіл))дикарбамату (20) (22,62 г). 1 H ЯМР (300 МГц, DMSO-d6, 120 °C): δ 0,87 (д, J= 6,5 Гц, 6H), 0,92 (д, J=6,5 Гц, 6H), 1,20-1,60 (м, 6H), 1,65-2,10 (м, 12H), 2,31 (м, 2H), 2,38-2,52 (м, 2H), 2,54-2,76 (м, 4H), 2,85 (м, 2H), 3,07 (м, 2H), 3,45 (м, 2H), 3,57 (розшир. с, 6H), 4,07 (т, J=8,0 Гц, 2H), 4,34 (м, 2H), 5,28 (т, J=8,5 Гц, 2H), 6,51 (розшир., 2H), 6,57 (д, J=8,0 Гц, 2H), 6,73 (с, 2H), 6,76 (д, J=8,0 Гц, 2H), 7,33 (д, J=8,5 Гц, 2H), 7,64 (д, J=8,5 Гц, 2H), 7,72 (с, 2H). Приклад 4. Синтез диметил ((2S,2'S,3R,3'R)-((2S,2'S, 3as,3a'S,7as,7a'S)-2,2'-(5,5'4,7 (трицикло[8,2,2,2 ]гексадека-4,6,10,12,13,15-гексаєн-5,11-диіл)біс(1H-бензо[d]імідазол-5,2диіл))біс(октагідро-1H-індол-2,1-диіл))біс(3-метокси-1-оксобутан-2,1-диіл))дикарбамату (22) Стадія 1 О-Метил-1-треонін (25 г, 0,19 моль) розчиняють в 1,4-диоксані (125 мл) і охолоджують до 0 °C. Потім до реакційної суміші додають водний 2 M розчин NaOH (22,5 г, 0,56 моль, 3 екв.), а потім метил хлорформіат (17,4 мл, 0,22 моль, 1,2 екв.) за такої ж температури. Реакційну суміш нагрівають до кімнатної температури й перемішують протягом 16 годин. Реакційну суміш промивають етилацетатом (500 мл). Водний шар підкисляють за допомогою 3 н HCl (до pH 2) і екстрагують етилацетатом (3 × 250 мл). Об'єднані органічні шари висушують над Na 2SO4 і концентрують із одержанням сирого продукту (23 г). Етилацетат (46 мл) додають до сирого продукту й нагрівають при 80 °C з одержанням прозорого розчину. Потім цей розчин охолоджують до 0 °C. Отриманий твердий продукт фільтрують і сушать із одержанням бажаного прозорого продукту (21) (18,75 г). Стадія 2 24 UA 110976 C2 5 10 15 20 25 30 35 DIEA (32,8 мл, 0,192 моль) додають краплинами до суміші гідрохлоридної солі, описаної вище (32,0 г, 0,0384 моль), Мос-О-метил-1-нреоніну (18,3 г, 0,0960 моль) і HATU (36,5 г, 0,09604 моль) в DMF (160 мл) при 0 °C. Реакційної суміші дають можливість нагрітися до кімнатної температури, перемішують протягом 16 годин і виливають у воду (1,6 л). Отриманий твердий продукт збирають за допомогою фільтрування й розчиняють в DCM (500 мл). Цей розчин промивають водою (100 мл), промивають насиченим розчином солі (50 мл), сушать над сульфатом натрію й концентрують за зниженого тиску. Залишок очищають за допомогою колонкової хроматографії на силікагелі з одержанням диметил ((2S,2'S,3R,3'R)4,7 ((2S,2'S,3as,3a'S,7as,7a'S)-2,2'-(5,5'-(трицикло[8,2,2,2 ]гексадека-4,6,10,12,13,15-гексаєн-5,11диіл)біс(1H-бензо[d]імідазол-5,2-диіл))біс(октагідро-1H-індол-2,1-диіл))біс(3-метокси-11 оксобутан-2,1-диіл))дикарбамату (22) (30 г). H ЯМР (400 МГц, DMSO-d6, к. т.): δ 0,91-1,04 (м, 6H), 1,21-1,59 (м, 6H), 1,64-1,88 (м, 6H), 1,90-2,07 (м, 4H), 2,23-2,49 (м, 6H), 2,62 (м, 2H), 2,85 (м, 2H), 3,08 (м, 2H), 3,19 (с, 3H), 3,20 (с, 3H), 3,42 (м, 2H), 3,57 (с, 6H), 4,15 (видимий т, J=8,0 Гц, 2H), 4,47 (м, 2H), 5,16 (видимий т, J=8,5 Гц, 2H), 6,52 (видимий т, J=8,5 Гц, 2H), 6,75 (з, 2H), 6,82 (м, 2H), 7,41 (м, 2H), 7,71 (видимий т, J=6,0 Гц, 2H), 7,64-7,79 (м, 4H). Приклад 5. Синтез диметил ((2S,2'S,3R,3'R)-((2S,2'S, 3as,3a'S,7as,7a'S)-2,2'-(5,5'4,7 (трицикло[8,2,2,2 ]-гексадека-4,6,10,12,13,15-гексаєн-5,11-диіл)біс(1H-бензо[d]імідазол-5, 2диіл))біс(октагідро-1H-індол-2,1-диіл))біс( оксобутан-2, 1-диіл))дикарбамату (23) 4,7 Диметил ((2S,2'S,3R,3'R)-((2S,2'S, 3as,3a'S,7as,7a'S)-2,2'-(5,5'-(трицикло[8,2,2,2 ]гексадека4,6, 10,12,13, гексаєн-5, 11-диіл)біс(1H-бензо[d]імідазол-5,2-диіл))біс(октагідро-1H-індол-2,1диіл))біс(3-метокси-1-оксобутан-2,1-диіл))дикарбамат готують способом, аналогічним до того, який був описаний вище для синтезу диметил ((2S,2'S,3R,3'R)-((2S,2'S,3as,3a'S,7as,7a'S)-2,2'4,7 (5,5'-(трицикло[8,2,2,2 ]-гексадека-4,6,10,12,13,15-гексаєн-5, 11-диіл)біс(1H-бензо[d]імідазол1 5,2-диіл))біс(октагідро-1H-індол-2,1-диіл))біс(3-метокси-1-оксобутан-2,1-диіл))дикарбамату. H 1 ЯМР (400 МГц, DMSO-d6, к. т.): H ЯМР (400 МГц, DMSO-d6, к. т.): δ 0,95-1,04 (м, 6H), 1,20-1,56 (м, 6H), 1,64-1,85 (м, 6H), 1,90-2,09 (м, 4H), 2,25 (м, 2H), 2,32-2,49 (м, 4H), 2,63 (м, 2H), 2,83 (м, 2H), 3,06 (м, 2H), 3,39 (м, 2H), 3,57 (с, 6H), 3,69 (м, 2H), 4,06 (видимий т, J = 7,5 Гц, 2H), 4,46 (м, 2H), 4,72 (м, 2H), 5,13 (м, 2H), 6,44-6,57 (м, 2H), 6,68-6,87 (м, 4H), 7,23-7,35 (м, 4H), 7,53-7,78 (м, 4H). Приклад 6. Синтез сполуки 29 за допомогою тетраамінового способу синтезу Стадія 1 1,2-диаміно-4-бромбензол (10 г, 0,053 моль) розчиняють в DCM (150 мл) і охолоджують до 0 °C. За такої ж температури додають краплинами розчин NaOH (50 мл, 2,5 моль). Через 15 хв. додають краплинами за такої ж температури ди-трет-бутилдикарбонат (58 г, 0,26 моль). Потім реакційній суміші дають можливість нагріватися до кімнатної температури, перемішують протягом 16 годин, розбавляють DCM (100 мл) і промивають водою (100 мл). Органічний шар 25 UA 110976 C2 відокремлюють, сушать над Na2SO4 і концентрують. Сирий матеріал очищають за допомогою колонкової хроматографії на силікагелі (простий петролейний ефір/етилацетат, 1:1 об′єм/об′єм) з одержанням бажаного продукту (18 г). Стадія 2 5 10 15 20 25 30 35 В атмосфері аргону, суміш ди-трет-бутил (4-бром-l,2-фенілен)дикарбамату (24) (18 г, 0,046 моль), біс(пінаколято)дибору (17,7 г, 0,070 моль), ацетату калію (13,66 г, 0,14 моль) і Pd(dppf)Cl 2 (3,8 г, 0,0046 моль) в 1,4-диоксані (360 мл) нагрівають при 85 °C протягом 16 годин. Потім реакційну суміш розбавляють етилацетатом (200 мл) і фільтрують через шар целіту. Фільтрат концентрують за зниженого тиску, решту матеріалу очищають за допомогою колонкової хроматографії на силікагелі (простий петролейний ефір/етилацетат, 80:20 об′єм/об′єм) з одержанням бажаного продукту (25) (16,0 г). Стадія 3 В атмосфері аргону, суміш 4,16-диiбром[2,2]парациклофану (17) (6 г, 0,014 моль), ди-третбутил (4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-іл)-1,2-фенілен)дикарбамату (17,78 г, 0,032 моль), водного розчину Cs2CO3 (15,98 г, 0,049 моль, в 66 мл води) і Pd(PPh3)4 (1,33 г, 0,0016 моль) нагрівають у герметичній пробірці при 80 °C протягом 16 годин. Реакційну суміш виливають у воду (250 мл), і отриманий преципітат збирають за допомогою фільтрування й промивають водою. Цей сирий матеріал очищають за допомогою колонкової хроматографії (простий петролейний ефір/етилацетат, 6:4 об′єм/об′єм) з одержанням бажаного продукту (26) (5,0 г). Стадія 4 Тетра Boc-захищений продукт, описаний вище (26) (10 г), додають до TFA (100 мл) при 05 °C. Після завершення додавання, реакційну суміш нагрівають до кімнатної температури й перемішують протягом 3 годин. Потім реакційну суміш концентрують і випаровують разом з DCM (3 × 50 мл). Сирий матеріал (27) використовують безпосередньо на наступній стадії. Стадія 5 DIEA (1 мл, 0,0125 моль) додають краплинами до охолодженої (0 °C) суміші (S)-5-(третбутоксикарбоніл)-5-азаспіро[2,4]гептан-6-карбонової кислоти (0,5 г, 0,00057 моль), HOBt (0,35 г, 0,0026 моль), EDCI (0,5 г, 0,0026 моль) і солі TFA (27), описаної вище (0,343 г, 0,0014 моль) в DMF (5 мл) при 0 °C. Після завершення додавання, реакційної суміші дають можливість нагріватися до кімнатної температури й перемішують протягом 16 годин. Реакційну суміш 26 UA 110976 C2 виливають у воду, і преципітат (28) збирають за допомогою фільтрування й очищають за допомогою колонкової хроматографії на силікагелі з одержанням бажаного продукту (0,32 г). Стадія 6 5 10 15 20 25 30 Оцтову кислоту (5 мл) додають до продукту диаміду, описаного вище (28) (0,32 г, 0,00035 моль), і нагрівають при 45 °C протягом 4 годин. Реакційну суміш випаровують, і залишок розбавляють етилацетатом (95 мл), потім промивають водним розчином NaHCO 3 (2 × 25 мл) і водою (2 × 30 мл). Органічний шар відокремлюють, сушать над Na 2SO4 і випаровують за зниженого тиску. Сирий матеріал очищають за допомогою колонкової хроматографії з одержанням бажаного продукту (29) (0,2 г). Стадія 7 Boc-захищений продукт, описаний вище (0,09 г), розчиняють в DCM (0,9 мл) і охолоджують при 0 °C. Потім додають краплинами 4 н HCl/диоксан (0,9 мл). Реакційну суміш нагрівають до кімнатної температури й перемішують протягом 3 годин. Потім леткі речовини видаляють у вакуумі й випаровують разом з DCM (3 × 50 мл). Решту сирого матеріалу (30) використовують безпосередньо на наступній стадії без додаткового очищення. Стадія 8 Гідрохлоридну сіль (30), описану вище (0,011 г, 0,0000141 моль, 1,0 екв.), розчиняють в DMF (1 мл) і охолоджують до 0 °C. До цього охолодженого розчину додають (S)-2((метоксикарбоніл)аміно)-3-метилбутанову кислоту (0,0062 г, 0,000033 моль, 2,5 екв.), HOBt (0,0044 г, 0,000033 моль, 2,5 екв.) і EDCI (0,0063 г, 0,000033 моль, 2,5 екв.). Потім додають краплинами DIEA (0,02 мл, 0,00013 моль, 10 екв.) за такої ж температури. Реакційної суміші дають можливість нагріватися до кімнатної температури й перемішують протягом 16 годин. Потім реакційну суміш виливають у воду (25 мл), і преципітований твердий продукт збирають за допомогою фільтрування, висушують і очищають за допомогою колонкової хроматографії на 1 силікагелі з одержанням бажаного продукту (31) (3 мг). H ЯМР (400 МГц, DMSO-d6, к. т.): δ 0,911,04 (м, 6H), 1,21-1,59 (м, 6H), 1,64-1,88 (м, 6H), 1,90-2,07 (м, 4H), 2,23-2,49 (м, 6H), 2,62 (м, 2H), 2,85 (м, 2H), 3,08 (м, 2H), 3,19 (с, 3H), 3,20 (с, 3H), 3,42 (м, 2H), 3,57 (с, 6H), 4,15 (видимий т, J=8,0 Гц, 2H), 4,47 (м, 2H), 5,16 (видимий т, J=8,5 Гц, 2H), 6,52 (видимий т, J=8,5 Гц, 2H), 6,75 (с, 2H), 6,82 (м, 2H), 7,41 (м, 2H), 7,71 (видимий т, J=6,0 Гц, 2H), 7,64-7,79 (м, 4H). Приклад 7. Синтез інгібіторів NS5A на основі фероцену (32) 27 UA 110976 C2 5 10 15 Фероценові сполуки готують за допомогою способу, описаного в Butler, I.R., et al., "A Convenient Preparation of Iodoferrocenes", Polyhedron (1993) 12: 129-131. До переміщуваного розчину, 1,1'-дийодфероцену (220 мг, 0,5 ммоль) в 1,4-диоксані (10 мл) додають метил ((S)-3метил-1-оксо-1-((25,3aS,7aS)-2-(5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-іл)-1Hбензо[d]імідазол-2-іл)октагідро-1Н-індол-1-іл)бутан-2-іл)карбамат (1,1 г, 4 екв.), K3PO4 (853 мг, 2 M водний розчин, 8 екв.) і PdCl2dppf (49 мг, 12% моль) в атмосфері аргону. Отриману суміш піддають впливу мікрохвильового випромінювання (CEM Discover System) при 80 °C протягом 1 години. Реакційній суміші дають можливість охолонути до кімнатної температури, фільтрують і концентрують у вакуумі. Решту залишку очищають за допомогою препаративної ВЕРХ із 1 одержанням бажаного продукту у вигляді трифторацетатної солі (43 мг). H ЯМР (400 МГц, DMSO-d6, 27 °C): δ 0,63 (д, J=6,5 Гц, 6H), 0,78 (д, J=6,5 Гц, 6H), 1,13-1,49 (м, 6H), 1,55-1,87 (м, 10H), 1,95 (м, 2H), 2,26 (м, 2H), 2,35 (м, 2H), 2,42 (м, 2H), 3,48 (с, 6H), 3,83 (т, J=8,0 Гц, 2H), 4,18 (м, 4H), 4,37 (м, 2H), 4,67 (м, 4H), 5,10 (дд, J=10,0 Гц, 7,5 Гц, 2H), 7,39 (д, J=9,0 Гц, 2H), 7,42 (д, J=9,0 Гц, 2H), 7,45 (д, J=8,0 Гц, 2H), 7,53 (с, 2H). Приклад 8. Додаткові сполуки формули I Наступні сполуки готують за допомогою способів, наведених у прикладах 1-6. Приклад 8. Додаткові сполуки формули I Наступні сполуки виготовляють за допомогою способів, наведених у прикладах 1-6. 20 № EC50 (мкM) Структура РХ NS5A1b NS5A1b Спосіб MС ВЕРХ 40 .000012 1.57 1 945 41
ДивитисяДодаткова інформація
Автори російськоюWiles, Jason Allan, Wang, Qiuping, Hashimoto, Akihiro, Pais, Godwin, Chen, Dawei, Wang, Xiangzhu, Gadhachanda, Venkat, Phadke, Avinash, Deshpande, Milind
МПК / Мітки
МПК: A61P 31/00, A61P 31/12, A61K 31/4178, A61K 31/4164
Мітки: лікуванні, циклофани, гетерофани, аліфани, гетерафани, придатні, використання, вгс, інфекції, металоцени, гетеро-гетерафани, заміщені
Код посилання
<a href="https://ua.patents.su/87-110976-zamishheni-alifani-ciklofani-geterafani-geterofani-getero-geterafani-jj-metaloceni-pridatni-dlya-vikoristannya-pri-likuvanni-infekci-vgs.html" target="_blank" rel="follow" title="База патентів України">Заміщені аліфани, циклофани, гетерафани, гетерофани, гетеро-гетерафани й металоцени, придатні для використання при лікуванні інфекції вгс</a>
Попередній патент: Бурова коронка ударно-обертової дії з твердосплавними роликами
Наступний патент: Лінія для формування заготовок цукрової вати
Випадковий патент: Композиція, яка фотополімерізується



























































































