Заміщені в ортоположенні аміди антранілової кислоти та їх застосування як лікувальних засобів
Номер патенту: 73187
Опубліковано: 15.06.2005
Автори: Петров Орлін, Менрад Андреас, Ернст Александер, Хут Андреас, Крюгер Мартін, Тіраух Карл-Хайнц, Зайдельманн Дітер, Хабері Мартін
Формула / Реферат
1. Сполуки загальної формули І
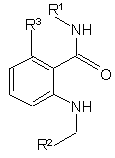 I,
I,
у якій R1 являє собою групу
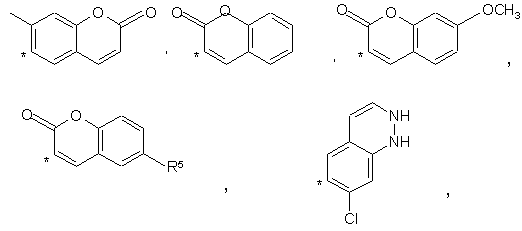
де R5 означає хлор, бром або ОСН3, або групу
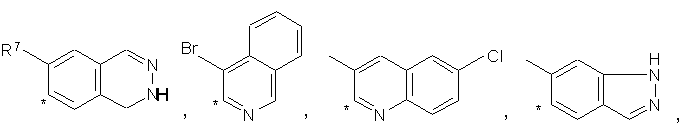
де R7 означає СН3 або хлор, або групу
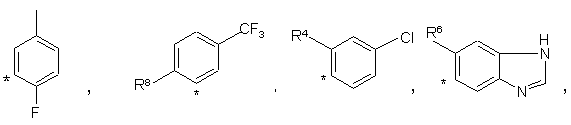
де R8 означає СН3, фтор, хлор або СF3, R4 означає фтор, хлор, бром, -СF3, -N=C, СН3-, -ОСF3 або –CH2OH, a R6 означає –СН3 або хлор,
R2 являє собою піридил або групу
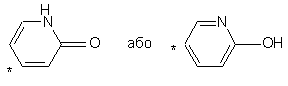
і
R3 являє собою водень або фтор,
а також їх ізомери і солі.
2. Сполуки формули І за п. 1, які відрізняються тим, що їх застосовують як інгібітори тирозинкінази KDR і FLT.
3. Сполуки загальної формули І за п.1, які відрізняються тим, що представлені у вигляді фармацевтичного препарату для ентерального, парентерального і перорального введення.
4. Застосування сполук загальної формули І за п. 1 для одержання відповідного лікувального засобу, призначеного для лікування пухлин, псоріазу, артриту, такого як ревматоїдний артрит, гемангіоми, ангіофіброми, очних хвороб, таких як діабетична ретинопатія, неоваскулярна глаукома, захворювань нирок, таких як гломерулонефрит, діабетична нефропатія, злоякісний нефросклероз, тромбомікроангіопатія, відторгнення трансплантатів і гломерулопатія, фіброзних захворювань, таких як цироз печінки, захворювань, пов'язаних із проліферацією мезангіальних клітин, артеріосклерозу й пошкоджень нервової тканини, для пригнічення повторної оклюзії судин після лікування з використанням балонних катетерів, при протезуванні судин або після використання механічних пристроїв, призначених забезпечити прохідність судин, таких, наприклад, як стенти.
5. Лікувальний засіб, який містить у своєму складі принаймні одну сполуку за п. 1.
6. Лікувальний засіб за п. 5, призначений для лікування пухлин, псоріазу, артриту, такого як ревматоїдний артрит, гемангіоми, ангіофіброми, очних хвороб, таких як діабетична ретинопатія, неоваскулярна глаукома, захворювань нирок, таких як гломерулонефрит, діабетична нефропатія, злоякісний нефросклероз, тромбомікроангіопатія, відторгнення трансплантатів і гломерулопатія, фіброзних захворювань, таких як цироз печінки, захворювань, пов'язаних із проліферацією мезангіальних клітин, артеріосклерозу й пошкоджень нервової тканини, для пригнічення повторної оклюзії судин після лікування з використанням балонних катетерів, при протезуванні судин або після використання механічних пристроїв, призначених забезпечити прохідність судин, таких, наприклад, як стенти.
7. Лікувальний засіб за п. 5 або 6, який додатково містить придатні для одержання відповідних композицій речовини та носії.
Текст
Даний винахід стосується заміщених в opmo-положенні амідів антранілової кислоти та їх застосування як лікувальних засобів, призначених для лікування захворювань, зумовлених персистувальним ангіогенезом. Персистувальний ангіогенез може бути причиною різноманітних захворювань, таких як псоріаз, артрит, такий як ревматоїдний артрит, гемангіома, ангіофіброма, очні хвороби, такі як діабетична ретинопатія, неоваскулярна глаукома, захворювання нирок, такі як гломерулонефрит, діабетична нефропатія, злоякісний нефросклероз, тромбомікроангіопатія, відторгнення трансплантатів і гломерулопатія, фіброзні захворювання, такі як цироз печінки, захворювання, пов'язані з проліферацією мезангіальних клітин, і артеріосклероз, або може приводити до прогресування цих захворювань. Для лікування подібних захворювань, так само як і інших форм патологічного ангіогенезу, індукованого васкулярним ендотоліальним фактором росту (VEGF), та для усунення умов, які сприяють проникності судин, таких як васкуляризація пухлин, можна використовувати пряме або непряме інгібування VEGF-рецептора. Так, наприклад, відомо, що за допомогою розчинних рецепторів і антитіл до VEGF вдається пригнічувати ріст пухлин. Персистувальний ангіогенез індукується VEGF-фактором, медіатором якого є його рецептор. Необхідною умовою для VEGF виявити цю дію є його зв'язування з рецептором і ініціювання фосфор плювання тирозином. На сьогоднішній день відомі похідні фенілантраніламідів, які застосовуються як антагоністи ангіотензину II [див. заявку ЕР 564356], а також як інгібітори запалень та як противиразкові сполуки [див. патент US 3409668]. При створенні даного винаходу було встановлено, що сполуки загальної формули І у якій R1 представляє собою групу де R5 означає хлор, бром або ОСН3, або груп у де R7 означає СН3 або хлор, або групу де R8 означає СН3, фтор, хлор або CF3, R4 означає фтор, хлор, бром, -CF3, -N=C, CH 3-, -OCF3 або -СН2ОН, a R означає -СН3 або хлор, R2 представляє собою піридил або групу 6 і R3 представляє собою водень або фтор, а також їх ізомери і солі блокують фосфорилювання тирозином, відповідно персистувальний ангіогенез і перешкоджають тим самим росту та поширенню пухлин. Існують різноманітні тирозинкінази (Web-сайт: S. Hauk, А. М. Quinn, Meth. in Enzymol. 200, стор.38-62 (1991), посилання розміщене в розділі (домені), присвяченому каталізаторам, підгрупа РТК group XIV, Webсторінка: http://www.sdsc.edu/Kinases/pkr/pk_catalytic/pk_hanks_seq align_long.html і Mc Tigue і ін., Structure 7, стор.319-330 (1999)), які можуть пригнічуватися аналогічним чином. Так, наприклад, за допомогою сполук, які інгібують VEGF (васкулярний ендотеліальний фактор росту), вдається звичайно пригнічувати в тому числі і тирозинкіназу С, яка присутня, зокрема, у стовбурови х клітинах. З ура хуванням вищевикладеного зрозуміле прагнення одержати сполуки з вибірною у відношенні фактора VEGF інгібувальною дією. Запропоновані у винаході сполуки відрізняються саме завдяки тому, що мають такі селективні властивості і представляють собою тим самим цінні сполуки, здатні перешкоджати росту і поширенню пухлин. Сполуки за винаходом загальної формули І містять також можливі таутомерні форми і включають Е- і або Z-ізомери, при наявності хірального центра, також рацемати і енантіомери. Сполуки формули І, так само як і їх фізіологічні прийнятні солі завдяки їх інгібувальній активності по відношенню до фосфорилювання VEGF-рецептора можуть застосовуватися як лікувальні засоби. Механізм їх дії дозволяє застосовувати запропоновані сполуки для лікування захворювань, зумовлених персисту вальним ангіогенезом. Оскільки сполуки формули І, як було встановлено, є інгібіторами тирозинкінази KDR і FLT, вони придатні насамперед для лікування таких захворювань, які зумовлені індукованим VEGF-рецептором персистувальним ангіогенезом або підвищенням проникності судин. Об'єктом даного винаходу відповідно до цього є також застосування запропонованих сполук як інгібіторів тирозинкінази KDR і FLT. Ще одним об'єктом даного винаходу є також лікувальні засоби, призначені для лікування пухлин, відповідно їх застосування. Сполуки за винаходом можуть застосовуватися індивідуально або в складі відповідної композиції як лікувальні засоби для лікування псоріазу, артриту, такого як ревматоїдний артрит, гемангіоми, ангіофіброми, очних хвороб, таких як діабетична ретинопатія, неоваскулярна глаукома, захворювань нирок, таких як гломерулонефрит, діабетична нефропатія, злоякісний нефросклероз, тромбомікроангіопатія, відторгнення трансплантатів і гломерулопатія, фіброзних захворювань, таких як цироз печінки, захворювань, пов'язаних із проліферацією мезангіальних клітин, артеріосклерозу й пошкоджень нервової тканини. Сполуки за винаходом можуть застосовуватися також для пригнічення повторної оклюзії судин після лікування з використанням балонних катетерів, при протезуванні судин або після використання механічних пристроїв, призначених забезпечити прохідність судин, таких, наприклад, як стенти. При лікуванні пошкоджень нервової тканини за допомогою сполук за винаходом можна запобігти швидкому утворенню рубців в пошкоджених місцях, тобто вдається запобігти рубцювання до того моменту, коли аксони знову відновлять зв'язок між собою. Тим самим, як очевидно, створюється можливість для відновлення зв'язків між нервовими клітинами. Крім того, за допомогою запропонованих у винаході сполук можна пригнічувати утворення в пацієнтів асциту. В однаковій мірі можливо також пригнічення набряків, зумовлених фактором VEGF. Лікувальні засоби вищезгаданого типу, їх композиції та їх застосування також є об'єктом даного винаходу. Винахід стосується також застосування сполук загальної формули І для одержання відповідного лікувального засобу, призначеного для лікування пухлин, псоріазу, артриту, такого як ревматоїдний артрит, гемангіоми, ангіофіброми, очних хвороб, таких як діабетична ретинопатія, неоваскулярна глаукома, захворювань нирок, таких як гломерулонефрит, діабетична нефропатія, злоякісний нефросклероз, тромбомікроангіопатія, відторгнення трансплантатів і гломерулопатія, фіброзних захворювань, таких як цироз печінки, захворювань, пов'язаних із проліферацією мезангіальних клітин, артеріосклерозу й пошкоджень нервової тканини, для пригнічення повторної оклюзії судин після лікування з використанням балонних катетерів, при протезуванні судин або після використання механічних пристроїв, призначених забезпечити прохідність судин, таких, наприклад, як стенти. Для застосування сполук формули І як лікувальних засобів з них виготовляють відповідний фармацевтичний препарат, який містить у своєму складі поряд з активною речовиною для ентерального або парентерального введення придатні для цих цілей фармацевтичні, органічні або неорганічні інертні носії, такі, наприклад, як вода, желатин, гуміарабік, лактоза, крохмаль, стеарат магнію, тальк, олії рослинного походження, поліалкіленгліколі і т.п. Фармацевтичні препарати можуть виготовлятися у твердій формі, наприклад у вигляді таблеток, драже, супозиторіїв, капсул, або в рідкій формі, наприклад у вигляді розчинів, суспензій або емульсій. При необхідності вони містять, крім того, допоміжні речовини, такі як консерванти, стабілізатори, змочувачі або емульгатори, солі для регуляції осмотичного тиску або буфери. Для парентерального застосування придатні насамперед розчини для ін'єкцій або суспензії, у першу чергу водні розчини активних сполук у полігідроксіетоксилованій рициновій олії. Як системи-носії можна використовувати також поверхнево-активні допоміжні речовини, такі як солі жовчних кислот або фосфоліпіди тваринного або рослинного походження, так само як і їх суміші, а також ліпосоми або їх компоненти. Для перорального застосування придатні насамперед таблетки, драже або капсули з тальком і/або вуглеводневим носієм або зв'язуючим, як наприклад лактоза, кукурудзяний або картопляний крохмаль. Можливо також застосування рідких форм, таких, наприклад, як настойка, необов'язково з додаванням підсолоджувальної речовини. Дозування активних речовин можна змінювати залежно від методики введення, віку і ваги пацієнта, типу і ступеня тяжкості відповідного захворювання і тому подібних факторів. Добова доза складає від 0,5 до 2000мг, переважно від 50 до 1000мг, причому цю дозу можна призначати як разову дозу або з розрахунку на два або декілька прийоми. Вищеописані композиції і препаративні форми також є об'єктом даного винаходу. Сполуки за винаходом можна одержувати за відомими методами. Так, наприклад, сполуки формули І можна одержувати завдяки тому, що а) сполуку загальної формули II у якій R4-R7 мають вказані вище значення, а Т представляє собою Н або захисну гр упу й А представляє собою галоген або OR13, де R13 означає атом водню, С1-С4алкіл або С 1-С4ацил або утворює з Т замкнуте кільце, спочатку N-алкілують, а потім переводять СОА в амід і після цього при необхідності відщеплюють захисні групи або спочатку переводять в амід, а потім N-алкілують, або б) сполуку формули III, у якій R4-R7 мають вказані вище значення, а Т представляє собою Н або захисну груп у, металують в opmoположенні і потім шляхом захоплення електрофілом переводять в амід, після чого захисну груп у відщеплюють і аміногрупу алкілують, або в) сполуку формули IV, у якій R4-R7 мають вказані вище значення, а Т представляє собою Н або захисну гр упу й В означає галоген або О-трифлат, О-тозилат або О-мезилат, переводять в амід, після чого захисну груп у відщеплюють і аміногрупу алкілують. Послідовність проведення вищеописаних операцій може у всі х випадках змінюватися. Процес утворення амідів здійснюють за методами, відомими з літератури. Так, зокрема, для утворення амідів можна виходити з відповідного складного ефіру. Цей ефір піддають згідно із Journ. Org. Chem. стор. 8414 (1995) взаємодії з триметилалюмінієм і відповідним аміном у розчинниках, таких як толуол, при температурах в інтервалі від 0°С до температури кипіння використовуваного розчинника. Даний метод можна застосовувати також у випадку незахищених е фірів антранілової кислоти. Якщо молекула містить дві складоефірні групи, то їх обидві переводять у той самий амід. При використанні замість складного ефіру нітрилів одержують в аналогічних умовах амідини. Для утворення амідів можуть використовуватися також усі методи, відомі з хімії пептидів. Так, наприклад, відповідну кислоту можна піддавати в апротонних полярних розчинниках, таких, зокрема, як диметилформамід, з використанням відповідного активованого похідного кислоти, одержуваного, наприклад, за допомогою гідроксибензотриазолу і карбодііміду, такого як діізопропілкарбодіімід, або ж за допомогою попередньо утворених реагентів, таких, наприклад, як ГАТУ (Chem. Comm. стор.201 (1994)) або БТУ, при температурах в інтервалі від 0°С до температури кипіння розчинника, переважно при 80°С, взаємодії з аміном (при використанні ГАТУ переважно при кімнатній температурі). Дані методи можуть застосуватися й у випадку незахищених антранілових кислот. Для утворення амідів можна застосовувати також метод, де використовують змішаний ангідрид кислоти, імідазолід або азид. Попередній захист аміногрупи, наприклад у вигляді аміду, не є обов'язковою умовою у всіх випадках, однак доцільніше передбачити такий захист, оскільки це позитивно впливає на реакцію. Особливим вихідним матеріалом є ангідриди ізатової кислоти, у яких одночасно представлені і захищена аміногрупа, і активована кислотна функціональна група. Якщо амін попередньо переводити в БОК-захищен у сполуку, то металування в opmo-положенні можна здійснювати взаємодією з металоорганічними сполуками, такими, наприклад, як н-бутиллітій, і потім за реакцією захоплення ізоціанатами або ізотіоціанатами перетворювати в антраніламіди, відповідно антранілтіоаміди. Використання в цьому opmo-положенні такого замісника, як бром або йод, завдяки обміну галоген-метал дозволяє більш ефективно здійснювати opmo-металування. Як розчинники для вказаних реакцій можуть використовуватися прості ефіри, такі як діетиловий ефір, або тетрагідрофуран або вуглеводні, такі як гексан, а також їх суміші. Доцільно додавати при цьому комплексоутворювачі, такі як тетраметилетилендіамін (ТМЕДА). Температурний режим змінюється в інтервалі від -78°С до кімнатної температури. Розщеплення БОК-амідів здійснюють дією кислот, таких як трифтороцтова кислота, без використання розчинників або у розчинниках, таких як метиленхлорид, при температурах в інтервалі від 0°С до температури кипіння розчинника або за допомогою водної соляної кислоти, переважно 1н. соляної кислоти, у розчинниках, таких як етанол або діоксан, при температурах в інтервалі від кімнатної до температури кипіння розчинника. Амідну гр упу можна вводити також шляхом карбонілювання. З цією метою виходять з відповідних сполук формули IV (о-йод-, о-бром- або о-трифлілоксіанілінів), які піддають взаємодії з монооксидом вуглецю при нормальному або ж підвищеному тиску і з аміном у присутності каталізаторів на основі перехідних металів, таких, наприклад, як хлорид паладію(ll) або ацетат паладію(ll) або паладійтетракістрифенілфосфін, у розчинниках, таких як диметилформамід. Доцільним може виявитися додавання ліганду, такого як трифенілфосфін, і додавання основи, такої як трибутиламін [див., наприклад, Journ. Org. Chem., стор. 3327 (1974); Journ. Org. Chem., стор.7482 (1996); Synth. Comm., стор. 367 (1997); Tetr. Lett, стор. 2835 (1998)]. Якщо передбачається введення в молекулу різних амідних гр уп, то необхідно, наприклад, другу складноефірну групу вводити в молекулу після утворення першої амідної групи і потім амідувати або у випадку молекули, у якій одна група представлена у вигляді складного ефіру, а інша у вигляді кислоти, обидві групи амідують послідовно за допомогою різних методів. Тіоаміди можна одержувати з антраніламідів взаємодією з дифосфадитіанами згідно із Bull. Soc. Chim. Belg. 87, стор.229 (1978) або взаємодією з пентасульфідом фосфору в розчинниках, таких як піридин, або взагалі без використання розчинників при температурах в інтервалі від 0 до 200°С. Продукти у вигляді багатих на електрони ароматичних сполук можуть піддаватися також електрофільному ароматичному заміщенню. Заміщення в цих випадках проводять в opmo- або пара-положенні відносно аміногрупи або однієї з аміногруп. Так, зокрема, можна здійснювати ацилювання за Фріделем-Крафтсом за допомогою хлорангідридів кислот у присутності каталізаторів Фріделя-Крафтса, таких, наприклад, як трихлорид алюмінію, у розчинниках, таких як нітрометан, сірковуглець, метиленхлорид або нітробензол, при температурах в інтервалі від 0°С до температури кипіння використовуваного розчинника, переважно при кімнатній температурі. За відомими з літератури методами, наприклад за допомогою нітрувальної кислоти, азотної кислоти в різній концентрації без використання розчинників або за допомогою нітратів металів, таких, наприклад, як нітрат міді(ІІ) або нітрат заліза(ІІІ), у полярних розчинниках, таких як етанол або льодяна оцтова кислота, або в ацетангідриді можна вводити одну або декілька нітрогруп. Галогени вводять за відомими з літератури методами, наприклад обмінною реакцією з бромом, N-бромабо N-йодсукцинімідом або гідротрибромідом уротропіну в полярних розчинниках, таких як тетрагідрофуран, ацетонітрил, метиленхлорид, льодяна оцтова кислота або диметилформамід. Відновлення нітрогрупи проводять у полярних розчинниках при кімнатній температурі або при підвищеній температурі. Як каталізатори відновлення придатні метали, такі як нікель Ренея, або каталізатори на основі благородних металів, таких як паладій або платина, а також гідроксид паладію, необов'язково нанесені на носії. Замість водню відомим способом можуть використовуватися також, наприклад, форміат амонію, циклогексен або гідразин. В однаковій мірі можливо використовувати і такі відновники, як хлорид олова(ІІ) або хлорид титан у(ІІІ), а також такі як комплексні гідриди металів, необов'язково в присутності солей важких металів. Як відновник прийнятно також залізо. У цих випадках реакцію проводять у присутності відповідної кислоти, такої, наприклад, як оцтова кислота, або хлориду амонію, необов'язково з додаванням розчинника, такого, наприклад, як вода, метанол, залізо/аміак і т.п. При більшій тривалості реакції в цьому варіанті може початися ацилювання аміногрупи. Якщо передбачається алкілування аміногрупи, то цю груп у можна алкілувати за звичайними методами, наприклад алкілгалогенідами, або відповідно до варіанту Міцонубо (Mitsonubo) взаємодією з відповідним спиртом у присутності, наприклад, трифенілфосфіну й е фіру азодикарбонової кислоти. Можливий і інший підхід, а саме: піддавати амін відновному алкілуванню альдегідами або кетонами, здійснюючи цю реакцію в присутності відновника, такого, наприклад, як ціаноборогідрид натрію, у відповідному інертному розчиннику, наприклад етанолі, при температурах в інтервалі від 0°С до температури кипіння розчинника. Якщо виходити з первинної аміногрупи, то реакцію можна проводити при необхідності з послідовним використанням двох різних карбонільних сполук, одержуючи при цьому змішані похідні [див., наприклад, Verardo і ін., Synthesis, стор.121 (1993); Synthesis, стор.447 (1991); Kawaguchi, Synthesis, стор.701 (1985); Micovic і ін., Synthesis, стор.1043 (1991)]. Доцільним може виявитися й варіант, у якому спочатку взаємодією альдегіду з аміном у розчинниках, таких як етанол або метанол, необов'язково з додаванням допоміжних речовин, таких як льодяна оцтова кислота, утворюють шифову основу і лише після цього додають відновник , такий, наприклад, як ціаноборогідрид натрію. Гідрування алкенових або алкінових груп у молекулі здійснюють звичайним способом, наприклад за допомогою каталітично активованого водню. Як каталізатори можуть застосовуватися важкі метали, такі як паладій або платина, необов'язково нанесені на відповідний носій, або нікель Ренея. Як розчинники придатні спирти, такі, наприклад, як етанол. При цьому працюють при температурах в інтервалі від 0°С до температури кипіння використовуваного розчинника і при тиску аж до 20 бар, переважно, однак, працювати при кімнатній температурі і нормальному тиску. Завдяки застосуванню каталізаторів, таких, наприклад, як каталізатор Ліндлара, потрійні зв'язки вдається частково гідрувати до подвійних зв'язків із переважним утворенням при цьому Z-форми. Ацилювання аміногрупи здійснюють звичайним способом, наприклад відповідним галогенангідридом кислоти або ангідридом кислоти, необов'язково в присутності основи, такої як диметиламінопіридин, у розчинниках, таких як метиленхлорид, тетрагідрофуран або піридин, відповідно до варіанту Шоттена-Баумана у водному розчині при слабко лужному значенні pH або взаємодією з відповідним ангідридом у льодяній оцтовій кислоті. Введення галогенів - хлор у, брому, йоду - або азидної групи за допомогою аміногрупи можна також проводити, наприклад, за реакцією Зандмейера взаємодією солей діазонію, утворених за допомогою нітритів як проміжних продуктів, із хлоридом міді(І) або бромідом міді(І) у присутності відповідної кислоти, такої як соляна кислота або бромистоводнева кислота, або ж взаємодією з йодидом калію. У випадку використання ефіру органічної азотистої кислоти галогени можна вводити, наприклад, додаванням метиленйодиду або тетрабромметану в розчиннику, такому, наприклад, як диметилформамід. Для видалення аміногрупи є дві можливості: або взаємодія з ефіром органічної азотистої кислоти в тетрагідрофурані, або діазотування і відновна варка солі діазонію, наприклад, з використанням фосфористої кислоти, при необхідності з додаванням оксиду міді(І). Фтор можна вводити, наприклад, за реакцією Бальца-Шимана з використанням тетрафторборату діазонію або згідно із Journ. Fluor. Chem. 76 (1996), стор.59-62, шляхом діазотування в присутності HF x піридину і наступної варки, необов'язково в присутності джерела іонів фториду, такого, наприклад, як фторид тетрабутиламонію. Введення азидогрупи можна здійснювати після діазотування взаємодією з азидом натрію при кімнатній температурі. Відщеплення простого ефіру здійснюють за відомими з літератури методами. При цьому й у випадку наявності в молекулі декількох груп може бути досягнуте селективне відщеплення. У цих цілях ефір обробляють, наприклад, трибромідом бору в розчинниках, таких як дихлорметан, при температурах в інтервалі від -100°С до температури кипіння використовуваного розчинника, переважно при -78°С. Разом з тим можливий і інший підхід, а саме: відщеплювати ефір під дією тіометилату натрію в розчинниках, таких як диметилформамід. Температура при цьому може знаходитися в інтервалі від кімнатної до температури кипіння розчинника, переважно працювати при 150°С. N- або О-алкілування амідів, таких як піридин-2-он, відповідно 2-гідроксипіридин, здійснюють за методами, відомими з літератури. Так, зокрема, при використанні основ, таких як гідрид натрію або карбонат калію, у розчинниках, таких як диметилформамід, і алкілуванні за допомогою алкілгалогенідів, таких як метилйодид, забезпечують N-алкілування. При використанні ж таких основ, як карбонат срібла, у розчинниках, таких як тетрагідрофуран або толуол або переважно їх сумішей з алкілгалогенідами, такими як метилйодид, забезпечують О-алкілування. О-алкілування можна забезпечити також взаємодією з тетрафтороборатом триалкілоксонію в інертних розчинниках, таких як метиленхлорид. Взаємодією з діазометаном або триметилсилілдіазометаном у розчинниках, таких як метанол або толуол, переважно в їх суміша х, при температурах аж до температури кипіння розчинника, переважно, однак, при кімнатній температурі, одержують суміші N- і О-алкілпохідних. Вказані методи дозволяють здійснювати селективне алкілування піридону на відміну від аміду бензойної кислоти. Суміші ізомерів за допомогою звичайних методів, наприклад шляхом кристалізації, хроматографії або солеутворення, можна розділяти на енантіомери, відповідно на E/Z-ізомери. Процес одержання солей здійснюють звичайним способом, а саме: розчин сполуки формули І змішують з еквівалентною кількістю або з надлишком відповідної основи або кислоти, необов'язково представлених у розчиненому вигляді, і утворений осад відокремлюють або розчин піддають звичайній переробці. Нижче на прикладах більш докладно пояснюється одержання сполук за винаходом, які мають вибірну дію. Приклад 1 Амід N-[2-оксо-2Н-1-бензопіран-3-іл1-2-[(4-піридил)метил] амінобензойної кислоти 1. 484мг 3-аміно-2-оксо-2Н-1-бензопірану попередньо поміщають у 20мл метиленхлориду, після чого при охолодженні льодом додають по краплях 0,42мл триетиламіну і 0,40мл 2-нітробензоїлхлориду. Потім протягом 4год перемішують при кімнатній температурі, розчинник відганяють, залишок розчиняють у розчині гідрокарбонату натрію і утворений продукт відокремлюють вакуум-фільтрацією. У результаті одержують 0,88г аміду N-[2-оксо-2Н-1-бензопіран-3-іл]-2-нітробензойної кислоти. Вищевказаний 3-аміно-2-оксо-2Н-1-бензопіран одержували відповідно до методу Bonsignore і Loy, описаному в Journ. Heterocyclic Chem. 35, стор.117 (1998), з 2-оксо-2Н-1-бензопіран-3-карбонової кислоти [Journ. Org. Chem. 64, стор. 1033-1035 (1999)]. 2. 880мг аміду N-[2-оксо-2Н-1-бензопіран-3-іл]-2-нітробензойної кислоти попередньо поміщають в атмосфері азоту в 30мл етанолу, після чого змішують з 11мл циклогексену і 176мг гідроксиду паладію на активованому вугіллі і протягом 2год перемішують при 110°С. Потім каталізатор відфільтровують, а фільтрат концентрують практично досуха. Утворений продукт відокремлюють вакуум-фільтрацією, одержуючи в результаті 593мг аміду N-[2-оксо-2Н-1-бензопіран-3-іл]-2-амінобензойної кислоти. 3. 645мг аміду N-[2-оксо-2Н-1-бензопіран-3-іл]-2-амінобензойної кислоти в 50мл метанолу і 170мл льодяної оцтової кислоти попередньо поміщають у реактор при кімнатній температурі, після чого змішують з 0,38мл 4-піридинкарбальдегіду. Суміш перемішують протягом 15год і потім змішують з 206мг ціаноборогідриду натрію. Далі продовжують перемішування протягом 24год і утворені кристали відокремлюють вакуумфільтрацією. Ці кристали змішують з 70мл метанолу, 40мл льодяної оцтової кислоти і 95мкл 4піридинкарбальдегіду і перемішують протягом 48год. Після цього додають 57мг ціаноборогідриду натрію і перемішування продовжують протягом 15год. Утворений продукт відокремлюють вакуум-фільтрацією, промивають метанолом і сушать. У результаті одержують 521мг аміду N-[2-оксо-2Н-1-бензопіран-3-іл]-2-[(4піридил)метил] амінобензойної кислоти з температурою плавлення 195-197°С. Приклад 2 Амід N-[6-хлоріндазол-5-іл1-2-[(4-піридил)метил]амінобензойної кислоти 194мг (0,85ммоля) 2-(4-піридилметил)амінобензойної кислоти змішують у 8мл диметилформаміду з 283мг (1,69ммоля) 5-аміно-6-хлоріндазолу. До цього розчину в атмосфері аргону і без доступу вологи додають 215мг (2,13ммоля) N-метилморфоліну і 386мг (1,02ммоля) гексафторофосфату О-(7-азабензотриазол-1-іл)-1,1,3,3тетраметилуронію. Цю суміш перемішують протягом 4год при кімнатній температурі, після чого розбавляють приблизно 40мл води і тричі екстрагують етилацетатом порціями по 30мл. Об'єднану органічну фазу промивають водою, суша ть, фільтрують і концентрують. Залишок хроматографують на силікагелі з використанням як елюенту суміші метиленхлорид/етанол у співвідношенні 10:1. У результаті одержують 97мг (30,2% від теорії) аміду N-[6-хлоріндазол-5-іл]-2-[(4-піридил)метил] амінобензойної кислоти з температурою плавлення 222,8°С. За аналогічною методикою одержують також наступні сполуки формули Нижче на прикладах із застосування більш докладно пояснюються біологічна дія запропонованих у винаході сполук із селективними властивостями та їх застосування. Розчини, які використовувалися в дослідах Вихідні розчини: вихідний розчин А: 3мМ АТФ у воді, pH 7,0 (-70°С), вихідний розчин Б: g-33Р-АТФ 1мКі/100мкл, вихідний розчин В: полі(Glu4Tyr) 10мг/мл у воді. Розчин для розведень: розчинники субстратів: 10мМ ДТТ, 10мМ хлорид марганцю, 100мМ хлорид магнію, розчин ферменту: 120мМ трис/НСІ, pH 7,5, 10мкМ оксид натрійванадію. Приклад застосування 1 Пригнічення активності кінази KDR і FLT-1 у присутності сполук за винаходом У титраційний мікропланшет, який звужується на кінцях, (без зв'язування протеїну) додають 10мкл живильної суміші (ви хідний розчин А об'ємом 10мкл АТФ + 25мкКі g-33Р-АТФ (приблизно 2,5мкл вихідного розчину Б) + вихідний розчин В: 30мкл полі(Glu4Tyr) + 1,21мл розчинники субстратів), 10мкл розчину інгібітору (сполуки відповідно до розведень, як контроль служить 3%-ний розчин ДМСО в розчиннику субстратів) і 10мкл розчину ферменту (11,25мкг вихідного розчину ферменту (кінази KDR або FLT-1), розведеного при 4°С в 1,25мл розчину ферменту). Вказані інгредієнти ретельно перемішують і протягом 10хв інкубують при кімнатній температурі. Потім додають 10мкл стоп-розчину (250мМ ЕДТК, pH 7,0), перемішують і 10мкл розчину переносять на фосфоцелюлозний фільтр типу Р 81, після чого декілька разів промивають у 0,1-молярній фосфорній кислоті. Фільтрувальний папір сушать, покривають шаром Meltilex і за допомогою мікролічильника бета-частинок вимірюють радіоактивність. ІС50-значення представляють собою величини, які визначаються за концентрацією інгібітору, необхідною для пригнічення вбудовування фосфату на 50% від його вбудовування за відсутності інгібітору, за винятком контрольного значення, отриманого в результаті сліпого досліду (реакція, припинена за допомогою ЕДТК). Результати інгібування кінази ІС 50 у мкМ представлені в нижченаведеній таблиці. Приклад застосування 2 Дослід із визначення інгібування кіназної активності виділеного рецептора C-Kit Вихідні розчини: розчинники на 10 порцій: 400мМ трисНСІ, pH 7,5; 10мМ ДТТ, 10мМ хлорид марганцю, 100мМ хлорид магнію, 2,5%о поліетиленгліколю 20000; інгібітори: 2мМ у диметилсульфоксиді; вихідний розчин субстратів: 3мг/мл полі(Glu4Туr)n Sigma P275 у воді, заморожені компоненти; вихідний розчин АТФ: 37,5мМ АТФ у воді з pH, встановленим на 7,5, і заморожені компоненти; 100-кратний розчин ванадату: 1мМ ванадат натрію у воді; стоп-розчин: 250мМ етилендіамінтетраоцтова кислота (ЕДТК), pH 7,0; промивальний розчин для фільтра: 0,5%-на фосфорна кислота. Розчини для аналізу: розчини субстратів для 125 аналізів: 10мкл АТФ (37,5мкМ), 25мкКі g33Р-АТФ (~+2,5мкл розчину Amersham redivue solution) і 10мкл полі(glu, tyr) змішують з 1,23мл розчинника (однократно); розчин інгібітору: сполуки розчиняють у розчиннику (однократно), доводячи до необхідної концентрації; розчин ферменту: відповідний препарат ферменту розчиняють за допомогою розчинника (однократно) до потрібної концентрації, доводячи об'єм до 1,24мл, після чого додають 12,5мкл розчину ванадату натрію. Аналіз Компоненти переносять на титраційний мікропланшет із круглими або дрібноточковими лунками в наступній послідовності: 10мкл інгібітору в трикратній кінцевій концентрації і 10мкл суміші субстратів, і після їх змішування ініціюють реакцію додаванням 10мкл препарату ферменту. Суміш інкубують протягом 10хв і потім інкубацію припиняють за рахунок додавання 10мкл стоп-розчину. Далі 10мкл обробленої таким шляхом суміші переносять на фосфоцелюлозний фільтр, промивають у фосфорній кислоті, потім сушать, після чого розплавляють у сцинтиляторі mentilex і проводять вимірювання. Приклад 1 2 3 4 5 6 7 9 10 11 13 14 15 17 26 28 29 30 KDR ІС50 (мкмоль/л) 0,003 0,2 0,03 0,03 0,01 0,2 0,2 0,04 0,01 1 0,05 0,001 0,002 ВІ 0,001 0,05 0,2 0,02 C-Kit ІС50 (мкмоль/л) 6 >10 8 >10 >10 10 >10 10 >10 >10 5 5 2 >10 2 0,5 >10 10
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted in orthoposition amides of anthranilic acid and their use as medicaments
Автори англійськоюKruger Martin, Huth Andreas, Seidelmann Dieter, Thierauch, Karl-Heinz, Haberey Martin, Menrad Andreas
Назва патенту російськоюЗамещенные в ортоположении амиды антраниловой кислоты и их применение как лекарственных средств
Автори російськоюКрюгер Мартин, Хут Андреас, Зайдельманн Дитер, Хабери Мартин, Менрад Андреас
МПК / Мітки
МПК: A61K 31/4409, A61P 25/00, A61K 31/4433, A61P 9/10, A61P 27/06, A61K 31/4709, A61P 35/00, C07D 213/36, A61P 43/00, A61P 3/10, C07D 401/12, A61P 37/06, A61P 19/02, C07D 405/12, A61K 31/4439, A61P 27/02, A61P 1/16, A61P 13/12, C07D 213/38, A61P 29/00, A61P 41/00, A61P 17/06, A61P 7/02, A61K 31/4725
Мітки: аміди, засобів, заміщені, кислоти, лікувальних, антранілової, ортоположенні, застосування
Код посилання
<a href="https://ua.patents.su/9-73187-zamishheni-v-ortopolozhenni-amidi-antranilovo-kisloti-ta-kh-zastosuvannya-yak-likuvalnikh-zasobiv.html" target="_blank" rel="follow" title="База патентів України">Заміщені в ортоположенні аміди антранілової кислоти та їх застосування як лікувальних засобів</a>
Попередній патент: Спосіб отримання ізолятів асоціативних діазотрофів
Наступний патент: Пристрій для перетворення сигналів
Випадковий патент: Маятниковий прилад визначення кутів тангажа і крену рухомого об'єкта (двокоординатний маятник карпачева)












