Похідні індолу, фармацевтична композиція на їх основі та їх застосування
Номер патенту: 74651
Опубліковано: 16.01.2006
Автори: Крог-Єнсен Крістіан, Міккельсен Іван, Роттлондер Маріо, Мольтсен Айнер Кнуд, Рухланд Томас, Андерсен Кім
Формула / Реферат
1. Сполуки, які представлені загальною формулою І
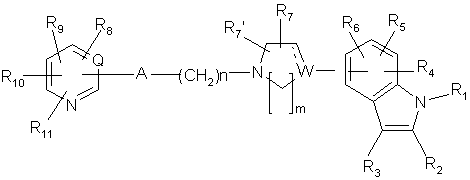 , (I)
, (I)
де
А являє собою О або S;
n дорівнює 2, 3, 4, 5, 6, 7, 8, 9 або 10;
m дорівнює 2 або 3;
W являє собою N, С або СН;
Q являє собою N, С або СН;
і пунктирна лінія позначає необов'язковий зв'язок;
R1 являє собою водень, С1-6-алкіл, С2-6-алкеніл, С2-6-алкініл, С3-8-циклоалкіл-С1-6-алкіл, арил-С1-6-алкіл або ацил;
R2, R3, R4, R5 і R6 незалежно являють собою водень, галоген, ціано, нітро, С1-6-алкіл, С1-6-алкоксигрупу, С1-6-алкілсульфаніл, С1-6-алкілсульфоніл, гідроксильну групу, гідроксі-С1-6-алкіл, С1-6-алкоксикарбоніл, ацил, С3-8-циклоалкіл, С3-8-циклоалкіл-С1-6-алкіл, трифторметил, трифторметокси, NR15R16, де R15 і R16 незалежно являють собою водень, С1-6-алкіл, С3-8-циклоалкіл або феніл; або R15 і R16 разом з атомом азоту, до якого вони приєднані, утворюють 5- або 6-членне кільце, яке необов'язково містить один додатковий гетероатом;
R7 і R7' незалежно являють собою водень або С1-6-алкіл або можуть разом утворювати місток, який складається з двох або трьох метиленових груп;
R8, R9, R10 і R11 кожен незалежно вибраний з водню, галогену, нітрогрупи, ціаногрупи, трифторметилу, трифторметоксигрупи, С1-6-алкілу, С2-6-алкенілу, С2-6-алкінілу, С3-8-циклоалкілу, С3-8-циклоалкіл-С1-6-алкілу, фенілу, тіофенілу, С1-6-алкокси, С1-6-алкілсульфанілу, С1-6-алкілсульфонілу, гідроксильної групи, формілу, ацилу, ациламіно, амінокарбонілу, С1-6-алкоксикарбоніламіно, амінокарбоніламіно, С1-6-алкіламінокарбоніламіно і ді(С1-6-алкіл)амінокарбоніламіно, NR13R14, де R13 і R14 незалежно являють собою водень, С1-6-алкіл, С3-8-циклоалкіл або феніл; або R13 і R14 разом з атомом азоту, до якого вони приєднані, утворюють 5- або 6-членне кільце, яке необов'язково містить один додатковий гетероатом;
їх енантіомери і фармацевтичнo прийнятні кислотно-адитивні солі.
2. Сполука формули (І) за п. 1, де n дорівнює 2, 3 або 4.
3. Сполука формули (І) за будь-яким з пп. 1, 2, де W являє собою N.
4. Сполука формули (І) за будь-яким з пп. 1-3, де R7 і R7' обидва являють собою водень.
5. Сполука формули (І) за будь-яким з пп. 1-4, де R1 являє собою водень.
6. Сполука формули (І) за будь-яким з пп. 1-5, де R2, R3, R4, R5 і R6 являють собою водень.
7. Сполука формули (І) за будь-яким з пп. 1-6, де R8, R9, R10 і R11 незалежно являють собою водень, галоген, С1-6-алкіл, С3-8-циклоалкіл, CN, СF3, ОСF3, NH2, NR13R14, де R13 і R14 незалежно являють собою водень, С1-6-алкіл, С3-8-циклоалкіл або феніл; або R13 і R14 разом з атомом азоту утворюють піперидин або піролідин.
8. Сполука формули (І) за п. 7, де R8, R9, R10, R11 незалежно являють собою метил, циклопропіл, трифторметил, ціаногрупу, хлор, бром, піперидиніл, феніл.
9. Сполука формули (І) за будь-яким з попередніх пунктів, де зазначена сполука являє собою:
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4,6-диметилнікотинонітрил, 1а,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-6-(тіофен-2-іл)-4-трифторметилнікотинонітрил, 1b,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}піридин, 1с,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-6-метилнікотинонітрил, 1d,
3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2-хлорпіридин, 1е,
3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2-бромпіридин, 1f,
3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2-метилпіридин, 1g,
3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-5-хлорпіридин, 1h,
2-{4-[4-(1Н-індол-4-іл)піперазин-1-іл]бутилсульфаніл}-5-трифторметилпіридин, 1і,
2-{4-[4-(1Н-індол-4-іл)піперазин-1-іл]бутилсульфаніл}-4,6-диметилнікотинонітрил, 1j,
2-{3-[4-(1Н-індол-4-іл)піперазин-1-іл]пропілсульфаніл}-5-трифторметилпіридин, 1k,
2-{3-[4-(1Н-індол-4-іл)піперазин-1-іл]пропілсульфаніл}-4,6-диметилнікотинонітрил, 1l,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-6-метилнікотинамід, 2а,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}нікотинонітрил, 2b,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4-метилпіридин, 2с,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4-метил-6-(піперидин-1-іл)нікотинонітрил, 2d,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4-трифторметил-6-циклопропілнікотинонітрил, 2е,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-3-метансульфоніл-4-метил-6-фенілпіридин, 2f,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}нікотинонітрил, 2g,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4-метилпіридин, 2h,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-6-метилнікотинамід, 2і,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4-метил-6-(піперидин-1-іл)нікотинонітрил, 2j,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4-трифторметил-6-циклопропілнікотинонітрил, 2k,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-3-метансульфоніл-4-метил-6-фенілпіридин, 2l,
6-хлор-2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4-метилнікотинонітрил, 2m,
6-хлор-5-фтор-2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}нікотинонітрил, 2n,
4,6-диметил-2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}піримідин, 2о,
5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}піримідин, 2р,
5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-6-метилсульфаніл-2-фенілпіримідин, 2q,
5-етил-2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}піримідин, 2r,
2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етилсульфаніл}-4-трифторметилпіримідин, 2s,
або їх фармацевтичнo прийнятні солі.
10. Фармацевтична композиція, яка містить, принаймні, одну сполуку формули (І) за будь-яким з пп. 1-9 або її фармацевтичнo прийнятну кислотно-адитивну сіль або проліки в терапевтично ефективній кількості в поєднанні з одним або декількома фармацевтичнo прийнятними носіями або розріджувачами.
11. Застосування сполуки за будь-яким з пп. 1-9 або її фармацевтичнo прийнятної кислотно-адитивної солі для одержання лікарського засобу для лікування розладу або захворювання, сприйнятливого до комбінованої дії інгібування захоплення серотоніну та антагонізму 5-НТ1A-рецепторів.
12. Застосування сполуки за будь-яким з пп. 1-9 або її фармацевтичнo прийнятної кислотно-адитивної солі для одержання лікарського засобу для лікування розладу або захворювання, сприйнятливого до комбінованої дії 5-НТ1A-рецепторів і D4-дофамінових рецепторів.
13. Застосування за будь-яким з пп. 11-12, де захворювання і розлади являють собою стан генералізованої тривоги, панічний стан, обсесивно-компульсивний розлад, депресію, соціальну фобію, розлади апетиту і неврологічні розлади, такі як психоз.
14. Спосіб лікування розладу або захворювання живої істоти, включаючи людину, що є сприйнятливим до дії інгібування захоплення серотоніну й антагонізму 5-НТ1A-рецепторів, який включає введення такій живій істоті, включаючи людину, терапевтично ефективної кількості сполуки за будь-яким з пп. 1-9 або її фармацевтичнo прийнятної кислотно-адитивної солі.
15. Спосіб лікування розладу або захворювання живої істоти, включаючи людину, що є сприйнятливим до дії 5-НТ1A- та D4-рецепторів, який включає введення такій живій істоті, включаючи людину, терапевтичнo ефективної кількості сполуки за будь-яким з пп. 1-9 або її фармацевтичнo прийнятної кислотно-адитивної солі.
16. Спосіб лікування за будь-яким з пп. 14-15, де розлад або захворювання являє собою афективний розлад, такий як стан генералізованої тривоги, панічний стан, обсесивно-компульсивний розлад, депресія, соціальна фобія і розлади апетиту, або неврологічний розлад, такий як психоз.
Текст
1. Сполуки, які представлені загальною формулою І C2 2 (19) 1 3 74651 4 3. Сполука формули (І) за будь-яким з пп. 1, 2, де 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-6W являє собою N. метилнікотинамід, 2і, 4. Сполука формули (І) за будь-яким з пп. 1-3, де 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4R7 і R7' обидва являють собою водень. метил-6-(піперидин-1-іл)нікотинонітрил, 2j, 5. Сполука формули (І) за будь-яким з пп. 1-4, де 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-41 R являє собою водень. трифторметил-6-циклопропілнікотинонітрил, 2k, 6. Сполука формули (І) за будь-яким з пп. 1-5, де 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-3R2, R3, R4, R5 і R6 являють собою водень. метансульфоніл-4-метил-6-фенілпіридин, 2l, 7. Сполука формули (І) за будь-яким з пп. 1-6, де 6-хлор-2-{2-[4-(1Н-індол-4-іл)піперазин-1R8, R9, R10 і R11 незалежно являють собою водень, іл]етилсульфаніл}-4-метилнікотинонітрил, 2m, галоген, С1-6-алкіл, С3-8-циклоалкіл, CN, СF3, ОСF3, 6-хлор-5-фтор-2-{2-[4-(1Н-індол-4-іл)піперазин-1NH2, NR13R14, де R13 і R14 незалежно являють соіл]етилсульфаніл}нікотинонітрил, 2n, бою водень, С1-6-алкіл, С3-8-циклоалкіл або феніл; 4,6-диметил-2-{2-[4-(1Н-індол-4-іл)піперазин-1або R13 і R14 разом з атомом азоту утворюють пііл]етилсульфаніл}піримідин, 2о, перидин або піролідин. 5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-18. Сполука формули (І) за п. 7, де R8, R9, R10, R11 іл]етилсульфаніл}піримідин, 2р, незалежно являють собою метил, циклопропіл, 5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-1трифторметил, ціаногрупу, хлор, бром, піперидиіл]етилсульфаніл}-6-метилсульфаніл-2ніл, феніл. фенілпіримідин, 2q, 9. Сполука формули (І) за будь-яким з попередніх 5-етил-2-{2-[4-(1Н-індол-4-іл)піперазин-1пунктів, де зазначена сполука являє собою: іл]етилсульфаніл}піримідин, 2r, 2-{2-[4-(1Н-індол-4-іл)піперазин-12-{2-[4-(1Н-індол-4-іл)піперазин-1іл]етилсульфаніл}-4,6-диметилнікотинонітрил, 1а, іл]етилсульфаніл}-4-трифторметилпіримідин, 2s, 2-{2-[4-(1Н-індол-4-іл)піперазин-1або їх фармацевтичнo прийнятні солі. іл]етилсульфаніл}-6-(тіофен-2-іл)-410. Фармацевтична композиція, яка містить, притрифторметилнікотинонітрил, 1b, наймні, одну сполуку формули (І) за будь-яким з 2-{2-[4-(1Н-індол-4-іл)піперазин-1пп. 1-9 або її фармацевтичнo прийнятну кислотноіл]етилсульфаніл}піридин, 1с, адитивну сіль або проліки в терапевтично ефекти2-{2-[4-(1Н-індол-4-іл)піперазин-1вній кількості в поєднанні з одним або декількома іл]етилсульфаніл}-6-метилнікотинонітрил, 1d, фармацевтичнo прийнятними носіями або розрі3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2джувачами. хлорпіридин, 1е, 11. Застосування сполуки за будь-яким з пп. 1-9 3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2або її фармацевтичнo прийнятної кислотнобромпіридин, 1f, адитивної солі для одержання лікарського засобу 3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2для лікування розладу або захворювання, сприйметилпіридин, 1g, нятливого до комбінованої дії інгібування захоп3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-5лення серотоніну та антагонізму 5-НТ1Aхлорпіридин, 1h, рецепторів. 2-{4-[4-(1Н-індол-4-іл)піперазин-112. Застосування сполуки за будь-яким з пп. 1-9 іл]бутилсульфаніл}-5-трифторметилпіридин, 1і, або її фармацевтичнo прийнятної кислотно2-{4-[4-(1Н-індол-4-іл)піперазин-1адитивної солі для одержання лікарського засобу іл]бутилсульфаніл}-4,6-диметилнікотинонітрил, 1j, для лікування розладу або захворювання, сприй2-{3-[4-(1Н-індол-4-іл)піперазин-1нятливого до комбінованої дії 5-НТ1A-рецепторів і іл]пропілсульфаніл}-5-трифторметилпіридин, 1k, D4-дофамінових рецепторів. 2-{3-[4-(1Н-індол-4-іл)піперазин-113. Застосування за будь-яким з пп. 11-12, де заіл]пропілсульфаніл}-4,6-диметилнікотинонітрил, 1l, хворювання і розлади являють собою стан гене2-{2-[4-(1Н-індол-4-іл)піперазин-1ралізованої тривоги, панічний стан, обсесивноіл]етилсульфаніл}-6-метилнікотинамід, 2а, компульсивний розлад, депресію, соціальну фо2-{2-[4-(1Н-індол-4-іл)піперазин-1бію, розлади апетиту і неврологічні розлади, такі іл]етилсульфаніл}нікотинонітрил, 2b, як психоз. 2-{2-[4-(1Н-індол-4-іл)піперазин-114. Спосіб лікування розладу або захворювання іл]етилсульфаніл}-4-метилпіридин, 2с, живої істоти, включаючи людину, що є сприйнят2-{2-[4-(1Н-індол-4-іл)піперазин-1ливим до дії інгібування захоплення серотоніну й іл]етилсульфаніл}-4-метил-6-(піперидин-1антагонізму 5-НТ1A-рецепторів, який включає ввеіл)нікотинонітрил, 2d, дення такій живій істоті, включаючи людину, тера2-{2-[4-(1Н-індол-4-іл)піперазин-1певтично ефективної кількості сполуки за будьіл]етилсульфаніл}-4-трифторметил-6яким з пп. 1-9 або її фармацевтичнo прийнятної циклопропілнікотинонітрил, 2е, кислотно-адитивної солі. 2-{2-[4-(1Н-індол-4-іл)піперазин-115. Спосіб лікування розладу або захворювання іл]етилсульфаніл}-3-метансульфоніл-4-метил-6живої істоти, включаючи людину, що є сприйнятфенілпіридин, 2f, ливим до дії 5-НТ1A- та D4-рецепторів, який вклю2-{2-[4-(1Н-індол-4-іл)піперазин-1чає введення такій живій істоті, включаючи людиіл]етокси}нікотинонітрил, 2g, ну, терапевтичнo ефективної кількості сполуки за 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4будь-яким з пп. 1-9 або її фармацевтичнo прийняметилпіридин, 2h, тної кислотно-адитивної солі. 5 74651 6 16. Спосіб лікування за будь-яким з пп. 14-15, де панічний стан, обсесивно-компульсивний розлад, розлад або захворювання являє собою афективдепресія, соціальна фобія і розлади апетиту, або ний розлад, такий як стан генералізованої тривоги, неврологічний розлад, такий як психоз. Цей винахід відноситься до нових гетероарильних похідних, які ефективно зв'язуються з 5НТ1А-рецептором, до фармацевтичних композицій, які містять зазначені сполуки, та до їх застосування при лікуванні деяких психіатричних і неврологічних захворювань. Багато сполук цього винаходу також мають значну активність щодо інгібування зворотного захоплення серотоніну і тому вважаються особливо придатними для лікування депресії. Крім того, багато сполук цього винаходу мають також вплив на D3- і D4-дофамінові рецептори і, як вважається, придатні для лікування психозу. У клінічних і фармакологічних дослідженнях було показано, що агоністи і часткові агоністи 5HT1A придатні для лікування ряду афективних розладів, таких як стан генералізованої тривоги, панічний розлад, обсесивно-компульсивний розлад, депресія та агресія. Повідомлялося, що ліганди 5-HT1A можуть бути придатними для лікування ішемії. Огляд антагоністів 5-HT1A і запропонованих потенційних терапевтичних мішеней для цих антагоністів, що базується на результатах доклінічних і клінічних досліджень, представлено у Schechter et аl., Sеrоtоnin, 1997, Vol. 2, Issue 7. Відзначається, що антагоністи 5-HT1A можуть бути корисними в лікуванні шизофренії, сенільної деменції, деменції, пов'язаної з хворобою Альцгеймера, а в поєднанні з антидепресантами SSRI вони також придатні для лікування депресії. Інгібітори зворотного захоплення 5-НТ уявляють собою добре відомі лікарські засобиантидепресанти і є придатними для лікування панічних розладів і соціальної фобії. Ефект комбінованого введення сполуки, яка інгібує зворотне захоплення серотоніну, і антагоніста 5-HT1A-рецептора був оцінений в декількох дослідженнях (Innis, R.B. et аl., Еur. J. Pharmacol., 1987, 143, р. 95-204 та Gartside S.E., Br. J. Pharmacol. 1995, 115, p.1064-1070, Blier P. et аl., Trends Pharmacol. 1994, 15, 220). У цих дослідженнях було встановлено, що об'єднані антагоністи 5-HT1A-рецептора та інгібітори зворотного захоплення серотоніну забезпечують більш швидкий початок лікувальної дії. D4-дофамінові рецептори відносяться до сімейства D2-подібних дофамінових рецепторів, які, як вважається, відповідальні за антипсихотичну дію нейролептиків. D4-дофамінові рецептори розташовані, головним чином, не в ділянках смугастого тіла, а в інших ділянках мозку, і це дозволяє зробити припущення, що ліганди D4-дофамінових рецепторів проявляють антипсихотичну дію та не будуть викликати екстрапірамідних побічних ефектів. Отже, ліганди D4-дофамінових рецепторів є потенційними ліками для лікування психозу та позитивних симптомів шизофренії, при цьому сполуки, що проявляють комплексну дію на D4дофамінові рецептори та серотонінергічні рецептори, можуть більш ефективно усувати негативні симптоми шизофренії, такі як тривога та депресія, алкогольна залежність, порушення імпульсної регуляції, агресивність, побічні ефекти, які викликаються відомими антипсихотичними засобами, ішемічні захворювання, мігрень, сенільна деменція і серцево-судинні захворювання, та поліпшують сон. D3-дофамінові рецептори також відносяться до сімейства дофамінових D2-подібних рецепторів. Антагоністичні властивості антипсихотичних ліків до рецепторів D3 можуть зменшувати негативні симптоми та порушення пізнавальної здатності та приводити до менш виражених побічних ефектів у відношенні EPS і гормональних змін. Таким чином, агенти, які впливають на 5-HT1Aрецептори, як агоністи, так і антагоністи, вважаються придатними для лікування психіатричних і неврологічних розладів, тому такі сполуки є дуже бажаними. Крім того, антагоністи, які одночасно значно інгібують зворотне захоплення серотоніну та/або активність D4- і/або D3-рецепторів можуть бути особливо придатними для лікування різних психіатричних і неврологічних захворювань. Раніше були описані сполуки, які мають родинні структури. У WO 99/55672 описані сполуки загальної формули, яка включає похідні індолу, які мають спорідненість до 5-HT1A-рецепторів і D2-рецепторів. У ЕР 900792 описані сполуки загальної формули, які включають похідні індолу, які є лігандами рецепторів 5-HT1A і 5-HT1D, а також D2-рецепторів. Зараз встановлено, що сполуки класу похідних індолу особливо корисні як ліганди 5-HT1A. Крім того, виявлено, що багато зазначених сполук мають інші корисні властивості, наприклад, сильну інгібуючу активність у відношенні серотоніну та/або спорідненість до D4-рецепторів. Винахід включає наступне. Сполуки, які представлені загальною формулою І де А являє собою О або S; n дорівнює 2, 3,4, 5, б, 7, 8, 9 або 10; 7 74651 8 m дорівнює 2 або 3; компульсивний розлад, депресія, соціальна фобія W являє собою N, С або СН; і розлади апетиту; інших психічних розладів, таких Q являє собою N, С або СН; як психоз і неврологічні розлади. і пунктирна лінія позначає необов'язковий зв'яУ ще одному варіанті здійснення цей винахід зок; відноситься до способу лікування розладу або 1 R являє собою водень, С1-6-алкіл, С2-6захворювання живої істоти, включаючи людину, алкеніл, С2-6-алкініл, С3-8-циклоалкіл-С1-6-алкіл, що є сприйнятливим до інгібування захоплення арил-С1-6-алкіл або ацил; серотоніну й антагонізму 5-НТ1А-рецепторів, який R2, R3, R4, R5 і R6 незалежно являють собою включає введення такій живій істоті, включаючи водень, галоген, ціано, нітро, С1-6-алкіл, С1-6людину, терапевтично ефективної кількості сполуалкоксигрупу, С1-6-алкілсульфаніл, С1-6ки формули (І) або її фармацевтично прийнятної алкілсульфоніл, гідроксильну групу, гідрокси-С1-6кислотно-адитивної солі. алкіл, С1-6-алкоксикарбоніл, ацил, С3-8-циклоалкіл, У ще одному варіанті здійснення цей винахід С3-8-циклоалкіл-С1-6-алкіл, трифторметил, трифтовідноситься до способу лікування розладу або рметокси, NR15R16, де R15 і R16 незалежно являють захворювання живої істоти, включаючи людину, собою водень, С1-6-алкіл, С3-8-циклоалкіл або фещо є сприйнятливим до дії 5-НТ1А та D4ніл; або R15 і R16 разом з атомом азоту, до якого рецепторів, який включає введення такій живій вони приєднані, утворюють 5- або 6-членне кільце, істоті, включаючи людину, терапевтично ефективяке необов'язково містить один додатковий гетеної кількості сполуки формули (І) або її фармацевроатом; тично прийнятної кислотно-адитивної солі. Завдяки комбінованій антагоністичній дії на 5R7 і R7 незалежно являють собою водень або НТ1А-рецептори та дії, що інгібує зворотне захопС1-6-алкіл або можуть разом утворювати місток, що лення серотоніну, вважають, що сполуки цього складається з двох або трьох метиленових груп; винаходу особливо придатні для лікування депреR8, R9, R10 і R11 кожен незалежно вибраний з сії як лікарські засоби швидкого початку дії. Сполуводню, галогену, нітрогрупи, ціаногрупи, трифторки можуть також бути придатними для лікування метилу, трифторметоксигрупи, С1-6-алкілу, С2-6депресії у пацієнтів, які несприйнятливі до лікуалкенілу, С2-6-алкінілу, С3-8-циклоалкілу, С3-8вання доступними на цей час антидепресантами. циклоалкіл-С1-6-алкілу, фенілу, тіофенілу, С1-6Сполуки цього винаходу мають високу спорідалкокси, С1-6-алкілсульфанілу, С1-6неність до 5-НТ1А- та D4-рецепторів. Тому сполуки алкілсульфонілу, гідроксильної групи, формілу, цього винаходу розглядаються як придатні для ацилу, ациламіно, амінокарбонілу, C1-6лікування афективних розладів, таких як стан геалкоксикарбоніламіно, амінокарбоніламіно, C1-6нералізованої тривоги, панічний розлад, обсесивалкіламінокарбоніламіно і ди(С1-6но-компульсивний розлад, депресія, соціальна алкіл)амінокарбоніламіно, NR13R14, де R13 і R14 фобія й розлади апетиту; інших психічних розланезалежно являють собою водень, C1-6-алкіл, С3-8дів, таких як психоз і неврологічні розлади. циклоалкіл або феніл; або R13 і R14 разом з атомом У кращих варіантах здійснення винаходу n доазоту, до якого вони приєднані, утворюють 5- або рівнює 2,3 або 4. 6-членне карбоциклічне кільце, яке необов'язково У кращих варіантах здійснення винаходу W містить один додатковий гетероатом; являє собою N. їх енантіомери і фармацевтично прийнятні киУ кращих варіантах здійснення винаходу Q слотно-адитивні солі. являє собою N. Винахід також відноситься до фармацевтичної У кращих варіантах здійснення винаходу Q композиції, яка містить сполуку формули (І) або її являє собою С або СН. фармацевтично прийнятну сіль і, принаймні, один У кращих варіантах здійснення винаходу R7 і фармацевтично прийнятний носій або розріджу7' R обидва являють собою водень. вач. У кращих варіантах здійснення винаходу R1 У ще одному варіанті здійснення винахід відявляє собою водень. носиться до застосування сполуки формули (І) або У кращих варіантах здійснення винаходу R2, її фармацевтично прийнятної кислотно-адитивної 3 R , R4, R5 і R6 являють собою водень. солі для одержання лікарського засобу для лікуУ кращих варіантах здійснення винаходу R8, вання розладу або захворювання, сприйнятливого R9, R10 і R11 незалежно являють собою водень, до інгібування захоплення серотоніну й антагонізгалоген, C1-6-алкіл, С3-8-циклоалкіл, CN, CF3, OCF3, му у відношенні 5-НТ1А-рецепторів. NH2, NR13R14, де R13 і R14 незалежно являють соУ ще одному варіанті здійснення винахід відбою водень, С1-6-алкіл, С3-8-циклоалкіл або феніл; носиться до застосування сполуки формули (І) або або R13 і R14 разом з атомом азоту утворюють піи фармацевтично прийнятної кислотно-адитивної перидин або піролідин. солі для одержання лікарського засобу для лікуУ більш кращих варіантах здійснення винаховання розладу або захворювання, сприйнятливого ду R8, R9, R10, R11 і R12 незалежно являють собою до комбінованої дії 5-НТ1А-рецепторів і D4метил, циклопропіл, трифторметил, ціаногрупу, дофамінових рецепторів. хлор, бром, піперидиніл, феніл. Зокрема, винахід відноситься до застосування У кращому варіанті здійснення винаходу спосполуки згідно з цим винаходом або її фармацевлуки формули І, які описані вище, являють собою: тично прийнятної кислотно-адитивної солі для 2-{2-[4-(1Н-індол-4-іл)піперазин-1одержання лікарського засобу для лікування афеіл]етилсульфаніл}-4,6-диметилнікотинонітрил, 1а, ктивних розладів, таких як стан генералізованої 2-{2-[4-(1Н-індол-4-іл)піперазин-1тривоги, панічний розлад, обсесивно 9 74651 10 іл]етилсульфаніл}-6-(тіофен-2-іл)-4Термін "С1-6-алкіл" відноситься до розгалужетрифторметилнікотинонітрил, 1b, ної або лінійної алкільної групи, що має від одного 2-{2-[4-(1Н-індол-4-іл)піперазин-1до шести атомів вуглецю, включно, яка включає, іл]етилсульфаніл} піридин, 1с, але не обмежується ними, метил, етил, 1-пропіл, 2-{2-[4-(1Н-індол-4-іл)піперазин-12-пропіл, 1-бутил, 2-бутил, 2-метил-2-пропіл і 2іл]етилсульфаніл}-6-метилнікотинонітрил, 1d, метил-1-пропіл. 3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2Аналогічно, терміни "С2-6-алкеніл" і "С2-6хлорпіридин, 1e, алкініл" відносяться до груп, що мають від двох до 3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2шести атомів вуглецю, включно, і містять принайбромпіридин, 1f, мні один подвійний або потрійний зв'язок, відпові3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-2дно. метилпіридин, 1g, Терміни "С1-6-алкокси", "С1-6-алкілсульфаніл", 3-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-5"С1-6-алкілсульфоніл", "С1-6-алкіламіно", "C1-6хлорпіридин, 1h, алкілкарбоніл", "гідрокси-С1-6-алкіл" тощо позна2-{4-[4-(1Н-індол-4-іл)піперазин-1чають такі групи, у яких С1-6-алкіл є таким, як виіл]бутилсульфаніл}-5-трифторметилпіридин, значено вище. 2-{4-[4-(1Н-індол-4-іл)піперазин-1Термін "С3-8-циклоалкіл" відноситься до моноіл]бутилсульфаніл}-4,6-диметилнікотинонітрил, 1j, циклічного або біциклічного карбоциклу, що має 2-{3-[4-(1H-індол-4-іл)піперазин-1від трьох до восьми атомів вуглецю, і включає, але іл]пропілсульфаніл}-5-трифторметилпіридин, 1k, не обмежується ними, циклопропіл, циклобутил, 2-{3-[4-(1Н-індол-4-іл)піперазин-1циклопентил, циклогексил тощо. іл]пропілсульфаніл}-4,6-диметилнікотинонітрил, 1l, Термін "арил" позначає карбоциклічну арома2-{2-[4-(1Н-індол-4-іл)піперазин-1тичну групу, таку як феніл, нафтил, особливо феіл]етилсульфаніл}-6-метилнікотинамід, 2а, ніл. У використовуваному тут значенні арил може 2-{2-[4-(1Н-індол-4-іл)піперазин-1бути заміщений однією або декількома групами, іл]етилсульфаніл} нікотинонітрил, 2b, що включають галоген, нітро, ціано, трифторме2-{2-[4-(1Н-індол-4-іл)піперазин-1тил, С1-6-алкіл, гідрокси та C1-6-алкокси. іл]етилсульфаніл}-4-метилпіридин, 2с, Термін "галоген" позначає фтор, хлор, бром 2-{2-[4-(1Н-індол-4-іл)піперазин-1або йод. іл]етилсульфаніл}-4-метил-6-(піперидин-1У використовуваному тут значенні термін іл)нікотинонітрил, 2d, "ацил" позначає форміл, C1-6-алкілкарбоніл, арил2-{2-[4-(1Н-індол-4-іл)піперазин-1карбоніл, арил-С1-6-алкілкарбоніл, де арил є таким, іл]етилсульфаніл}-4-трифторметил-6як визначено вище, С3-8-циклоалкілкарбоніл, або циклопропілнікотинонітрил, 2е, С3-8-циклоалкіл-С1-6-алкілкарбонільну групу. 2-{2-[4-(1Н-індол-4-іл)піперазин-1Термін "амінокарбоніл" позначає групу -СОіл]етилсульфаніл}-3-метансульфоніл-4-метил-6аміно, де "аміно" є таким, як визначено вище. фенілпіридин, 2f, Термін "ациламіно" позначає групу формули 2-{2-[4-(1H-індол-4-іл)піперазин-1NHCOH, -NНСО-С1-6-алкіл, -NHCO-арил, -NHСОіл]етокси}нікотинонітрил, 2g, С3-8-циклоалкіл, -NHСО-С3-8-циклоалкіл-С1-6-алкіл, 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4де терміни "алкіл", "циклоалкіл" і "арил" є такими, метилпіридин, 2h, як визначено вище. 2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]етокси}-6Терміни "амінокарбоніламіно", "С1-6метилнікотинамід, 2і, алкіламінокарбоніламіно" і "ди(С1-62-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-4алкіл)амінокарбоніламіно" позначають групи форметил-6-(піперидин-1-іл)нікотинонітрил, 2j, мул NHCONH2, -NHCONHC1-6-алкіл, NHСОN(ди-С12-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-46-алкіл), відповідно. трифторметил-6-циклопропілнікотинонітрил, 2к, Кислотно-адитивними солями сполук за цим 2-{2-[4-(1Н-індол-4-іл)піперазин-1-іл]етокси}-3винаходом є фармацевтично прийнятні солі, одеметансульфоніл-4-метил-6-фенілпіридин, 2l, ржані при взаємодії з нетоксичними кислотами. 6-хлор-2-{2-[4-(1Н-індол-4-іл)піперазин-1Прикладами таких органічних солей є солі малеїіл]етилсульфаніл}-4-метилнікотинонітрил, 2m, нової, фумарової, бензойної, аскорбінової, бурш6-хлор-5-фтор-2-{2-[4-(1Н-індол-4-іл)піперазинтинової, щавлевої, біс-метиленсаліцилової, мета1-іл]етилсульфаніл} нікотинонітрил, 2n, нсульфонової, етандисульфонової, оцтової, 4,6-диметил-2-{2-[4-(1Н-індол-4-іл)піперазин-1пропіонової, винної, саліцилової, лимонної, глюкоіл]етилсульфаніл} піримідин, 2о, нової, молочної, яблучної, мигдалевої, коричної, 5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-1цитраконової, аспарагінової, стеаринової, пальмііл]етилсульфаніл}піримідин, 2р, тинової, ітаконової, гліколевої, р-амінобензойної, 5-ціано-4-{2-[4-(1Н-індол-4-іл)піперазин-1глютамінової, бензолсульфонової та теофіліноціл]етилсульфаніл}-6-метилсульфаніл-2тової кислот, а також утворені з 8фенілпіримідин, 2q, галогентеофілінами, наприклад, 85-eтил-2-{2-[4-(1Н-індол-4-іл)піперазин-1бромотеофіліном. Типовими прикладами таких іл]етилсульфаніл} піримідин, 2r, неорганічних солей є солі хлористоводневої, бро2-{2-[4-(1H-індол-4-іл)піперазин-1мистоводневої, сірчаної, сульфамінової, фосфоріл]етилсульфаніл}-4-трифторметилпіримідин, 2s ної та азотної кислот. або їх фармацевтично прийнятні солі. Крім того, сполуки за цим винаходом можуть Визначення замісників тощо існувати в несольватованих і сольватованих фор 11 74651 12 мах, одержаних при використанні фармацевтично здійснюють в інертному органічному розчиннику, прийнятних розчинників, таких як вода, етанол такому як диметилформамід, у присутності основи тощо. Сольватовані форми звичайно еквівалентні (наприклад, трет-бутоксиду калію) при температурі несольватованим формам відповідно до цілей в інтервалі 40-100°С, переважно в інтервалі 40цього винаходу. 80°С та найбільш переважно близько 50°С. Деякі сполуки за цим винаходом мають хіраОдержання індолілпіперазинів і тетрагідропільні центри, і такі сполуки існують у формі ізомерів ридилпіперазинів формули (III) описано в публіка(тобто енантіомерів). В обсяг цього винаходу вхоції WO 9967237. Альдегіди формули (II) одержують дять усі такі ізомери та будь-які їх суміші, включавідповідно до методики, описаної в прикладах ниючи рацемічні суміші. жче. Спирти і меркаптани формули (V) одержують Рацемічні форми можна розподілити на оптивідповідно до методики, описаної в прикладах ничні антиподи за відомими способами, наприклад, жче. Початкові хлорпіридини формули (IV) є комешляхом розподілу їхніх діастереомерних солей за рційно доступними або їх одержують за способадопомогою оптично активної кислоти та наступноми, докладно описаними в літературі. го вивільнення оптично активної амінної сполуки Цей винахід далі проілюстрований наведениобробкою основою. Іншим способом розподілу ми нижче прикладами. Проте, зазначені приклади рацематів на оптичні антиподи є хроматографія на не обмежують обсяг винаходу. оптично активній матриці. Рацемічні сполуки за Приклади цим винаходом можна також розподілити на оптиТемператури плавлення були визначені на чні антиподи, наприклад, фракційною кристалізаапараті Buch: SMP-20 і не корегувалися. Аналітичцією d- або 1-солей (тартратів, манделатів або ні дані РХ-МС були одержані на апараті РЕ Sciex камфорсульфонатів). Сполуки за цим винаходом API 150EX, постаченим джерелом іонного розпиможна розподілити шляхом утворення діастереолення IonSpray (спосіб D) або розпилювачем з мерних похідних. нагріванням (heated nebulizer) (АРСІ, способи А та Можна використовувати інші способи розподіВ), і РХ системою Shimadzu LC-8A/SLC-10A. Рілу оптичних ізомерів, відомі фахівцям у цій галузі динну хроматографію (РХ, колонка 30 4,6мм, техніки. До таких способів відносяться методи, YMC ODS-A з розміром частинок 3,5мкм) здійснюописані авторами J. Jaques, A. Collet та S. Wilen в ють в умовах елюювання сумішшю во"Enantiomers, Racemates, and Resolutions", John да/ацетонітрил/трифтороцтова кислота з лінійним Wiley and Sons, New York (1981). градієнтом від 90:10:0,05 до 10:90:0,03 протягом 4 Оптично активні сполуки можуть бути одержахвилин зі швидкістю потоку 2мл/хв. Чистоту визнані з оптично активних початкових речовин. чають інтегруванням УФ-сліду (254нм). Час утриІ нарешті, формула (І) включає будь-які таутомання Rt виражають у хвилинах. мерні форми сполук цього винаходу. Мас-спектри одержують методом почерСполуки за цим винаходом можна одержати гового сканування, що дозволяє одержати інфородним з нижченаведених способів, які містять: мацію про молекулярну масу. Молекулярний іон, а) обробку сполуки формули (II) сполукою фоМН+, визначають при низькій напрузі на діафрагмі рмули (III) у присутності відновлювального агента. (5-20В) і фрагментацію роблять при високій напрузі на діафрагмі (100В). Розподіл за допомогою препаративної РХ-МС здійснюють на тому ж приладі. Рідинну хроматографію (РХ, колонка 50 20 мм, YMC ODS-A з розміром частинок 5мкм) здійснюють в умовах елюювання сумішшю вода/ацетонітрил/трифтороцтова де n, m, R1 - R11 Q, W, А і пунктирна лінія є такислота з лінійним градієнтом від 80:20:0,05 до кими, як визначено вище; 10:90:0,03 протягом 7 хвилин зі швидкістю потоку b) обробку сполуки формули (IV) сполукою 22,7мл/хв. Фракції збирають за допомогою детекформули (V) у присутності придатної основи тування мас-спектроскопією (MC) у розділеному потоці. Спектри 1H ЯМР одержують при частоті 500,13МГц на апараті Bruker Avance DRX500 або при частоті 250,13МГц на Bruker АС 250. Як розчинники використовують дейтерований хлороде L являє собою придатну групу, що видаля1 12 форм (99,8% D) або диметилсульфоксид (99,9% ється, таку як, наприклад, хлор, і n, m, R - R , Q, D). TMS використовують як внутрішній стандарт. W, А і пунктирна лінія є такими, як визначено виВеличини хімічних зсувів виражені в мільйонних ще. частках (млн-1). Для позначення мультиплетності Сполуки формули (І) виділяють у виді вільної сигналів ЯМР використані наступні абревіатури: с основи або у формі їхніх фармацевтично прийнят= синглет, д = дублет, т = триплет, к = квартет, кв = них солей. квінтет, г = гептет, дд = дублет дублетів, дт = дубВідновне амінування згідно зі способом а) пелет триплетів, дк = дублет квартетів, тт = триплет реважно проводять в інертному органічному розтриплетів, м = мультиплет і ш.с = широкий сингчиннику, такому як диметилформамід або тетрагілет. ЯМР сигналами, що відповідають кислотним дрофуран, у присутності відновлювального агента, протонам, звичайно зневажали. Вміст води в криснаприклад, триацетоксиборгідриду, при кімнатній талічних сполуках визначають титруванням за температурі. методом Карла Фішера. Стандартна обробка Арилування згідно зі способом b) звичайно 13 74651 14 включає екстракцію зазначеним органічним розбромпіридин, 1f: РХ/МС (m/z) 403 (МН+), Rt = 1,54, чинником з відповідних водних розчинів, висушучистота: 89%; вання об'єднаних органічних екстрактів (безвод3-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-2ними MgSО4 або Na2SО4), фільтрування та метилпіридин, 1g: РХ/МС (m/z) 337 (МН+), Rt = випарювання розчинника у вакуумі. Для хроматог0,71, чистота: 78%; рафії на колонках використовують силікагель типу 3-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-5Kieselgel 60, 230-400 меш, що відповідає стандархлорпіридин, 1h: РХ/МС (m/z) 357 (МН+), Rt = 1,58, там ASTM. Для іонообмінної хроматографії викочистота: 100%; ристовують SCX (1г) фірми Varian Mega Bond 2-{4-[4-(1H-індол-4-іл)піперазин-1іл]бутилсульфаніл}-5-трифторметилпіридин, 1i: Elut , номер за каталогом Chrompack 220776. ПеРХ/МС (m/z) 435 (MH+), Rt = 2,14, чистота: 80%; ред використанням колонку, наповнену SCX, під2-{4-[4-(1H-індол-4-іл)піперазин-1дають попередньому кондиціонуванню 10% розчиіл]бутилсульфаніл}-4,6-диметилнікотинонітрил, 1j: ном оцтової кислоти в метанолі (3мл). PX/MC (m/z) 420 (MH+), Rt = 2,07, чистота: 75%; Приклад 1 2-{3-[4-(1H-індол-4-іл)піперазин-14. 6-диметил-2-(2іл]пропілсульфаніл}-5-трифторметилпіридин, 1k: оксоетилсульфаніл)нікотинонітрил PX/MC (m/z) 421 (МН+), Rt = 2,06, чистота: 98%; 4,6-Диметил-2-меркаптонікотинонітрил (3,0г) 2-{3-[4-(1H-індол-4-іл)піперазин-1розчиняють у ДМФА (40мл) і додають розчин третіл]пропілсульфаніл}-4,6-диметилнікотинонітрил, 1l: бутоксиду калію (19,2мл, 1М) у трет-бутанолі. СуPX/MC (m/z) 406 (MH+), Rt = 1,99, чистота: 100%. міш перемішують протягом 10 хвилин, по краплях Приклад 2 додають до розчину бромацетальдегіддиметила2-{4-(1H-індол-4-іл)піперазин-1-іл]етантіол цеталю (3,2г) у ДМФА (10мл), і одержаний розчин 1-(1Н-індол-4-іл)піперазин (3,9г) і тіїран (1,75г) перемішують протягом ночі при 70°С. Суміш вилирозчиняють у ДМФА (200мл) і одержаний розчин вають у воду й екстрагують етилацетатом, об'єдкип'ятять зі зворотним холодильником протягом 1 нані органічні фази висушують і випарюють з одегодини. Суміш випаровують і залишок знову розржанням олії (5,3г), яку розчиняють у діоксані чиняють у ТГФ, висушують над MgSО4, фільтру(40мл), додають НСl (20мл, 3М) і одержану суміш ють і випарюють з одержанням олії, яку очищають перемішують при 30°С протягом 2 годин. Додають хроматографією на колонці (силікагель, етилацеNaHCO3 до одержання значення pH 5-6, суміш тат і гептан), одержуючи зазначену в заголовку екстрагують етилацетатом, об'єднані органічні сполуку у виді олії (2,2г). MC m/z (%); 261 (МН+, фази висушують над Na2SO4 і випарюють з одер100%), 202 (100%), 159 (23%). жанням зазначеної в заголовку сполуки у виді олії 1 2-{2-[4-(1H-індол-4-іл)піперазин-1(2,9г). H ЯМР (CDCl3): δ 2,45(с, 6Н); 3,35(д, 2Н); іл]етилсульфаніл}-6-метилнікотинонітрил, 2а 6,85(с, 1Н); 9,55(т, 1Н). 2-[4-(1Н-індол-4-іл)піперазин-1-іл]етантіол 2-{2-[4-(1H-індол-4-іл-піперазин-1(2,2г) розчиняють у розчині трет-бутоксиду калію іл]етилсульфаніл}-4,6-диметилнікотинонітрил 1а (0,81г) у ДМФА (25мл), перемішують протягом 15 4,6-диметил-2-(2хвилин і нагрівають до 50°С. До одержаного розоксоетилсульфаніл)нікотинонітрил (2,9г) розчинячину по краплях додають розчин 6-метил-2ють у 1,2-дихлороетані (150мл), додають розчин 1хлорнікотинонітрилу (1,91г) у ДМФА (25мл) і пере(1-Н-індол-4-іл)піперазину (2,4г) у ДМФА (150мл), мішування продовжують при 50°С протягом двох потім триацетоксиборгідрид натрію (14,9г) з настугодин. Суміш випарюють, залишок знову розчиняпним перемішуванням протягом 2 годин. Суміш ють у ТГФ, розчин промивають насиченим розчивиливають у воду і додають Na2CО3 для доведенном солі, висушують над MgSO4, фільтрують і виня значення pH до 7-8. Суміш екстрагують етилапарюють з одержанням олії, яку очищають цетатом, об'єднані органічні фази висушують і вихроматографією на колонці (силікагель, етилацепаровують, одержуючи олію, яку очищають тат, гептан і триетиламін), одержуючи зазначену в хроматографією на колонці (силікагель, етилацезаголовку сполуку у виді олії. Олію осаджують у тат і гептан). Одержану олію осаджують у виді оквиді оксалатної солі з ацетону. РХ/МС (m/z) 396 салатної солі (0,36г) з ацетону. РХ/МС (m/z) 392 (МН+), Rt = 1,46, чистота: 91%. (МН+), Rt = 1,92, чистота: 99%. Аналогічним чином одержують наступні Аналогічним чином одержують наступні сполусполуки: ки: 2-{2-[4-(1H-індол-4-іл)піперазин-12-{2-[4-(1H-індол-4-іл)піперазин-1іл]етилсульфаніл}нікотинонітрил, 2b: PX/MC (m/z) іл]етилсульфаніл}-6-(тіофен-2-іл)-4364 (МН+), Rt = 1,66, чистота: 96%; трифторметилнікотинонітрил 1b: РХ/МС (m/z) 514 2-{2-[4-(1H-індол-4-іл)піперазин-1(МН+), Rt = 2,54, чистота: 100%; іл]етилсульфаніл}-4-метилпіридин, 2c: PX/MC 2-{2-[4-(1H-індол-4-іл)піперазин-1(m/z) 353 (MH+), Rt = 1,70, чистота: 87%; іл]етилсульфаніл}піридин, 1с: РХ/МС (m/z) 339 2-{2-[4-(1H-індол-4-іл)піперазин-1(МН+), Rt = 1,58, чистота: 83%; іл]етилсульфаніл}-4-метил-6-(піперидин-12-{2-[4-(1H-індол-4-іл)піперазин-1іл)нікодинонітрил, 2d: PX/MC (m/z) 461 (MH+), Rt = іл]етилсульфаніл}-6-метилнікотинонітрил, 1d: 2,29, чистота: 95%; РХ/МС (m/z) 378 (МН+), Rt = 1,95, чистота: 92%; 2-{2-[4-(1H-індол-4-іл)піперазин-13-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-2іл]етилсульфаніл}-4-трифторметил-6хлорпіридин, 1е: РХ/МС (m/z) 357 (МН+), Rt = 1,50, циклопропілнікотинонітрил, 2e: PX/MC (m/z) 472 чистота: 93%; (MH+), Rt = 2,33, чистота: 94%; 3-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-2 15 74651 16 2-{2-[4-(1H-індол-4-іл)піперазин-1терголіну. Реакцію закінчують швидким фільтруіл]етилсульфаніл}-3-метансульфоніл-4-метил-6ванням крізь фільтри Unifilter GF/B на харвестері фенілпіридин, 2f: PX/MC (m/z) 507 (MH+), Rt = 2,16, клітин марки Tomtec Cell Harvester. Фільтри підрачистота: 92%; ховують на лічильнику Packard Top Counter. Ви2-{2-[4-(1H-індол-4-іл)піперазин-1пробувані в даному тесті сполуки 1d, 2b, 2e і 2о іл]eтокси}нікотинонітрил, 2g: PX/MC (m/z) 348 демонструють значення IC50 менш 50нМ. (MH+), Rt = 1,46, чистота: 88%; Сполуки цього винаходу були випробувані та2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-4кож на їх дію у відношенні зворотного захоплення метилпіридин, 2h: PX/MC (m/z) 337 (MH+), Rt = серотоніну в наступному тесті. 1,66, чистота: 100%; Інгібування захоплення 3Н-5-НТ в синаптосоми 2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-6головного мозку щура. метилнікотинамід, 2і: PX/MC (m/z) 380 (MH+), Rt Використовуючи цей метод в умовах in vitro =1,41, чистота: 96%; визначають спроможність лікарських засобів інгі2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-4бувати акумулювання 3Н-5-НТ в синаптосомах метил-6-(піперидин-1-іл)нікотинонітрил, 2j: PX/MC головного мозку щура. Випробовування проводять (m/z) 445 (MH+), Rt = 2,24, чистота: 100%; у відповідності з описом, наведеним в публікації 2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-4Hyttel, J., Рsychopharmacology 1978, 60, 13. Випротрифторметил-6-циклопропілнікотинонітрил, 2k: бувані в даному тесті сполуки 1a, 1d, 1l, 2b, 2e і 2о PX/MC (m/z) 456 (MH+), Rt = 2,20, чистота: 100%; демонструють значення IC50 менш 20нМ. 2-{2-[4-(1H-індол-4-іл)піперазин-1-іл]eтокси}-3Антагоністичні властивості до 5-НТ1A деяких метансулфоніл-4-метил-6-фенілпіридин, 2l: PX/MC сполук за цим винаходом визначають in vitro з ви(m/z) 491 (MH+), Rt = 2,16, чистота: 70%; користанням клонованих 5-НТ1А-рецепторів, стійко 6-хлор-2-{2-[4-(1H-індол-4-іл)піперазин-1експресованих у трансфектованих клітинах HeLa іл]етилсульфаніл}-4-метилнікотинонітрил, 2m: (HA7). При проведенні даного тесту антагоністичні PX/MC (m/z) 413 (MH+), Rt = 2,00, чистота: 69%; властивості до 5-НТ1А визначають, вимірюючи 6-хлор-5-фтор-{2-[4-(1H-індол-4-іл)піперазин-1здатність зазначених сполук протидіяти індуковаіл]етилсульфаніл}-нікотинонітрил, 2n: PX/MC (m/z) ному 5-НТ інгібуванню акумулювання сАМР під 417 (MH+), Rt = 1,91, чистота: 85%; дією форсколіну. Зазначений аналіз являє собою 2-{2-[4-(1H-індол-4-іл)піперазин-1модифікацію методу, описаного в Pauwets, Ρ. J. et іл]етилсульфоніл}піримідин, 2о: PX/MC (m/z) 368 аl., Biochem. Pharmacol. 1993, 43, 375. Випробувані (MH+), Rt = 1,62, чистота: 73%; в даному тесті сполуки 1a, 1d, 1l, 2b і 2е демон5-ціано-4-{2-[4-(1H-індол-4-іл)піперазин-1-іл]струють значення IC50 менш 7000нМ. етилсульфаніл}піримідин, 2р: PX/MC (m/z) 365 Деякі сполуки за цим винаходом випробовува(MH+), Rt = 1,62, чистота: 90%; ли в умовах in vitro у відношенні їхнього впливу на 5-ціано-4-{2-[4-(1H-індол-4-іл)піперазин-1-іл]5-НТ1А-рецептори, проводячи аналіз, описаний етилсульфаніл}-6метилсульфаніл-2Sanchez, С. et аl., Еur. J. Рharmacol. 1996, 315, pp фенілпіримідин, 2q: PX/MC (m/z) 488 (MH+), Rt = 245. При виконанні зазначеного тесту антагоністи2,49, чистота: 93%; чну дію випробуваних сполук визначають, вимі5-етил-2-{2-[4-(1H-індол-4-іл)піперазин-1рюючи їхню здатність інгібувати синдром 5-НТ, іл]етилсульфаніл}піримідин, 2r: PX/MC (m/z) 368 індукований 5-MeO-DMT. (МН+), Rt = 1,79, чистота: 72%; Сполуки цього винаходу мають корисну актив2-{2-[4-(1H-індол-4-іл)піперазин-1ність як інгібітори зворотного захоплення серотоіл]етилсульфаніл}-4-трифторметилпіридин, 2s: ніну й антагоністичну активність у відношенні 5PX/MC (m/z) 408 (MH+), Rt = 1,91, чистота: 79%. НТ1А-рецепторів. Тому сполуки цього винаходу Фармакологічне тестування вважаються придатними для лікування захворюСпорідненість сполук цього винаходу до 5вань і розладів, сприйнятливих до інгібування звоНТ1А-рецепторів визначають вимірюванням інгібуротного захоплення серотоніну й антагоністичної вання зв'язування радіоактивного ліганду з 5-НТ1Аактивності на 5-НТ1А-рецепторах. Захворювання, рецепторами, як описано в наведеному далі тесті. сприйнятливі до інгібування зворотного захопленІнгібування зв'язування 3Н-5-СТ з 5-НТ1Аня серотоніну, добре відомі в цій галузі й включарецепторами людини ють афективні розлади, такі як депресія, психоз, За допомогою цього методу в умовах in vitro тривога, включаючи стан генералізованої тривоги, визначають інгібування лікарськими засобами панічний стан, обсесивно-компульсивний розлад 3 зв'язування агоніста 5-НТ1А, Н-5тощо. карбоксамідотриптаміну (3Н-5-стиптицину), з клоЯк зазначено вище, антагоністична активність нованими 5-НТ1А-рецепторами людини, стабільно у відношенні 5-НТ1А-рецепторів сполук цього винаекспресованими в трансфектованих клітинах HeLa ходу буде протидіяти механізму негативного зво(HA7)[Fargin, Α. et аl, J. Biol. Chem., 1989, 264, ротного зв'язку, індукованому інгібуванням зворот14848). Випробування проводять як модифікацію ного захоплення серотоніну, і тому, як очікується, методу, описаного в публікації Harrington, Μ. Α. et буде поліпшувати ефект інгібуючої активності звоаl. J. Рharmacol. Eхр. Ther. 1994, 268, 1098. 5-НТ1Аротного захоплення серотоніну сполук цього винарецептори людини (40мкг клітинного гемогенату) ходу. інкубують протягом 15 хвилин при 37°С в 50мМ Таким чином, у цьому винаході заявляється, Tris-буфері (трис(гідроксиметил)метиламін) при pH що сполуки цього винаходу розглядаються як осо7,7 у присутності 3Н-5-СТ. Неспецифічне зв'язубливо придатні як лікарські засоби швидкого почавання визначають шляхом включення 10мкМ метку дії при лікуванні депресії. Сполуки також мо 17 74651 18 жуть бути придатними для лікування депресій, які ваних дофамінових D3-рецепторів людини, ексє несприйнятливими до використовуваних в даний пресованих у СНО-клітинах. Метод модифікований час SSRI. з R. G. MacKenzie et аl., Еur. J. Рharm. -Mol. Рharm. В описаних нижче двох тестах було встанов-Sec., 1994, 266, 79-85. лено також, що деякі сполуки цього винаходу маДеякі сполуки за цим винаходом випробовувають спорідненість до D3- і D4-дофамінових рецепли в умовах in vitro у відношенні їхнього впливу на торів. 5-НТ1А-рецептори, проводячи аналіз, описаний Інгібування зв'язування [3H]-YM-09151-2 з доSanchez, С. et аl., Еur. J. Рharmacol. 1996, 315, рр фаміновими D4-рецепторами людини 245. При виконанні зазначеного тесту антагоністиЗа допомогою цього методу в умовах in vitro чну дію випробуваних сполук визначають, вимівизначають інгібування лікарськими засобами рюючи їхню здатність інгібувати синдром 5-НТ, зв'язування [3H]-YM-09151-2 (0,06нМ) з мембранаіндукований 5-MeO-DMT. ми клонованих дофамінових D4.2-рецепторів люОскільки сполуки за цим винаходом демондини, експресованих у СНО-клітинах. Модифікострують спорідненість в описаних тестах, вони ваний метод від NEN Life Science Products, Inc., вважаються придатними для лікування афективсертифікат технічних даних РС2533-10/96. них розладів, таких як депресія, стан генералізоІнгібування зв'язування [3Н]-спіперону з D3ваної тривоги, панічний розлад, обсесивнорецепторами людини компульсивний розлад, соціальна фобія та розлаЗ використанням цього тесту визначають in ди апетиту, а також неврологічних розладів, зокvitro інгібування лікарськими препаратами зв'язурема, психозу. вання [3Н]-спіперону (0,3нМ) з мембранами клоно Комп’ютерна верстка Л. Купенко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюIndole derivatives, a pharmaceutical composition based thereon and use thereof
Автори англійськоюRottlaender Mario, MOLTZEN EJNER, RUHLAND THOMAS, ANDERSEN KIM, Krog-Jensen Christian
Назва патенту російськоюПроизводные индола, фармацевтическая композиция на их основании и их применение
Автори російськоюРоттлондер Марио, Мольтсен Айнэр Кнуд, Рухланд Томас, Андерсен Ким, Крог-Енсен Кристиан
МПК / Мітки
МПК: A61P 25/18, A61K 31/496, A61P 25/22, C07D 403/12, C07D 409/14, C07D 401/12, A61P 25/24, A61P 25/20, A61P 43/00, A61P 1/14, A61K 31/506
Мітки: застосування, індолу, похідні, фармацевтична, композиція, основі
Код посилання
<a href="https://ua.patents.su/9-74651-pokhidni-indolu-farmacevtichna-kompoziciya-na-kh-osnovi-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні індолу, фармацевтична композиція на їх основі та їх застосування</a>
Попередній патент: Спосіб пуску прямоструминного котла
Наступний патент: Вузол складання упаковки без з’єднувальних матеріалів
Випадковий патент: Альдегідні та спиртові композиції, одержані з рослинних олій, та способи їх одержання













