Визначені триазолопіридини та триазолопіразини, їх композиції та їх застосування
Формула / Реферат
1. Cполука формули 1
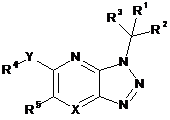 1
1
і/або принаймні одна її фармацевтично прийнятна сіль, де
X означає N, Y є відсутнім та R1 є злитим біциклічним гетероарилом, необов'язково заміщеним однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, -C(O)R11, -C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14, та нижчого алкілу, заміщеного гетероциклом; або
X означає N, Y вибирають із -О-, -S- та -N(R7)- і R1 вибирають із арилу та гетероарилу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, -C(O)R11, -C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14, та нижчого алкілу, заміщеного гетероциклом; або
X означає C(R6), Y вибирають із -О-, -S- та -N(R7)- або Y відсутній, і R1 означає гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, -C(O)R11, -C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14, та нижчого алкілу, заміщеного гетероциклом;
R2 і R3 незалежно вибирають із водню та алкілу або R2 і R3, разом з вуглецем, до якого вони приєднані, утворюють кільце, вибране із 3-7-членного циклоалкілу та 3-7-членного гетероциклу;
R4 вибирають із галогену, алкілу, циклоалкілу, гетероциклу, арилу та гетероарилу, кожний із яких, за виключенням галогену, необов'язково заміщений однією або декількома групами, вибраними із
нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
циклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
гетероарилокси, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
арилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, -S(O)nR12 та -S(O)nNR13R14;
R5 вибирають із водню, галогену, ОН, NH2, CF3, -CF2H, алкілу, алкенілу та алкінілу;
R6 вибирають із водню, -ОН, -NH2, -NHC(O)R11, галогену та алкілу;
R7 вибирають із водню та нижчого алкілу;
кожний n незалежно означає 0, 1 або 2;
R11, R12, R13 і R14 незалежно вибирають із водню, алкілу, алкенілу, алкінілу, циклоалкілу, арилу, гетероарилу та гетероциклу, кожний із яких, за виключенням водню, необов'язково заміщений однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси та нижчого алкокси, або R13 і R14, разом з азотом, до якого вони приєднані, об'єднані з утворенням гетероциклічного кільця, яке необов'язково заміщене однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси та нижчого алкокси, та додатково необов'язково включає один або два додаткових гетероатоми в гетероциклічному кільці, де один або два додаткових гетероатоми вибирають із -О-, -S- та -N(R15)-; та
R15 вибирають із водню, нижчого алкілу, -C(O)R11, -C(O)OR11, -C(O)NR13R14, -S(O)nR12 та -S(O)nNR13R14;
за умови, що
R1 не є необов'язково заміщеним фенілом або необов'язково заміщеним 4-піридинілом;
коли X означає N, R2 означає водень або метил, R3 і R5 означають водень та Y відсутній, то R1 не означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідробензофуран-5-іл або 2,3-дигідробензо[1,4]діоксин-6-іл; та
коли X означає N, R2, R3 і R5 означають водень та Y означає -О- або -N(R7)- і R1 означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідробензофуран-5-іл або 2,3-дигідробензо[1,4]діоксин-6-іл, то R4 означає необов'язково заміщений гетероарил.
2. Cполука за формулою 1, як заявлено у п. 1, і/або принаймні одна її фармацевтично прийнятна сіль, де X означає N.
3. Cполука за формулою 1, як заявлено у п. 1, і/або принаймні одна її фармацевтично прийнятна сіль, де X означає C(R6).
4. Cполука за формулою 1, як заявлено у п. 3, і/або принаймні одна її фармацевтично прийнятна сіль, де R6 вибирають із водню та нижчого алкілу.
5. Cполука за формулою 1, як заявлено у п. 4, і/або принаймні одна її фармацевтично прийнятна сіль, де R6 означає водень.
6. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-5, і/або принаймні одна її фармацевтично прийнятна сіль, де Y означає -О-.
7. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-5, і/або принаймні одна її фармацевтично прийнятна сіль, де Y означає -S-.
8. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-5, і/або принаймні одна її фармацевтично прийнятна сіль, де Y означає -N(R7)-.
9. Cполука за формулою 1, як заявлено у пункті 8, і/або принаймні одна її фармацевтично прийнятна сіль, де R7 означає водень або метил.
10. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-5, і/або принаймні одна її фармацевтично прийнятна сіль, де Y відсутній.
11. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-10, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 означає 8-10-членний гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, -C(O)R11, -C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14, та нижчого алкілу, заміщеного гетероциклом.
12. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-11, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 означає кільцеву систему, вибрану із
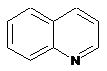 ,
, 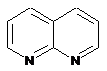 ,
, 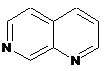 ,
, 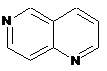 ,
, 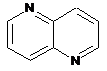 ,
, 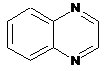 ,
, 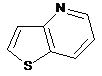 ,
, 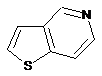 ,
, 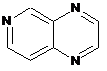 ,
, 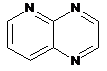 ,
, 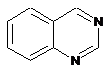 ,
, 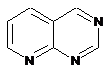 ,
, 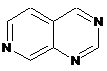 ,
, 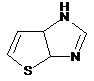 ,
, 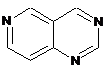 ,
, 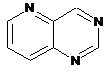 ,
, 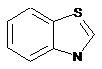 ,
, 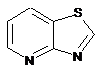 ,
, 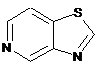 ,
, 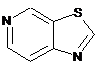 ,
, 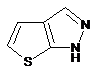 ,
, 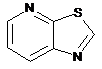 ,
, 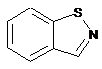 ,
, 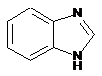 ,
,  ,
, 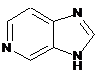 ,
, 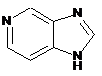 ,
,  ,
, 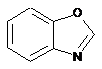 ,
, 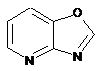 ,
, 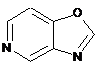 ,
, 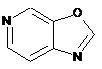 ,
,  ,
, 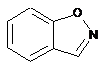 ,
, 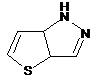 ,
, 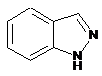 ,
, 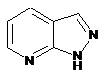 ,
, 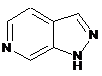 ,
, 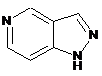 ,
, 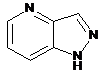 ,
, 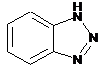 ,
,  ,
, 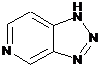 ,
, 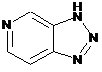 ,
, 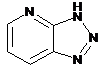 ,
, 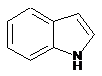 ,
, 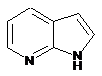 ,
, 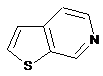 ,
, 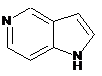 ,
, 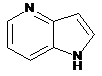 ,
, 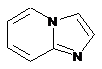 ,
, 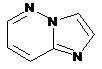 ,
, 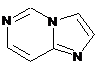 ,
, 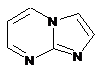 ,
, 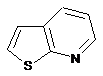 ,
, 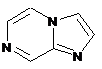 ,
, 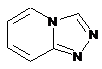 ,
, 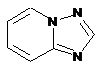 ,
, 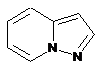 ,
, 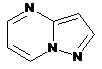 ,
, 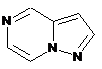 ,
, 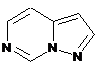 ,
, 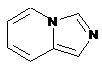 ,
, 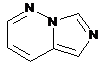 ,
, 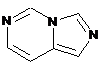 ,
, 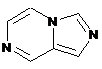 ,
, 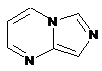 ,
,
де кожна із зазначених кільцевих систем необов'язково заміщена однією або декількома групами, вибраними із галогену, CF3, -CF2H, циклоалкілу, -C(O)R11, C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14, та нижчого алкілу, заміщеного гетероциклом.
13. Cполука за формулою 1, як заявлено у пункті 12, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 означає кільцеву систему, вибрану із
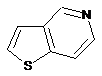 ,
, 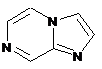 ,
, 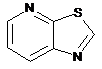 ,
, 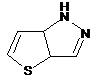 ,
, 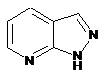 ,
, 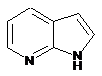 ,
, 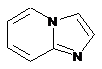 ,
, 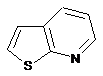 ,
, 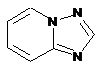 ,
, 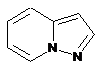 ,
, 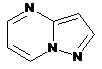 ,
, 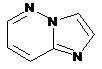 ,
, 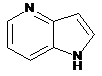 ,
,
де кожна із зазначених кільцевих систем необов'язково заміщена однією або декількома групами, вибраними із галогену, CF3, -CF2H, циклоалкілу, -C(O)R11, C(O)OR11, -CN, -C(O)NR13R14, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -NO2, -S(O)nR12, -S(O)nNR13R14, гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR13R14 та нижчого алкілу, заміщеного гетероциклом.
14. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-12, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 означає кільцеву систему, вибрану із
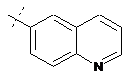 ,
, 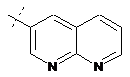 ,
, 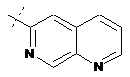 ,
, 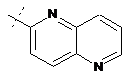 ,
, 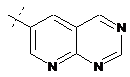 ,
, 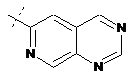 ,
, 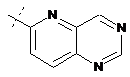 ,
, 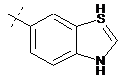 ,
, 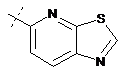 ,
, 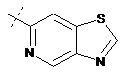 ,
, 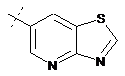 ,
, 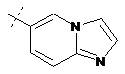 ,
, 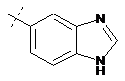 ,
, 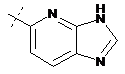 ,
, 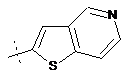 ,
, 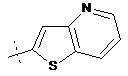 ,
, 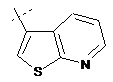 ,
, 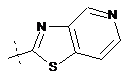 ,
, 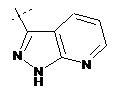 ,
, 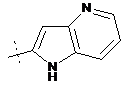 ,
, 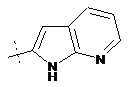 ,
, 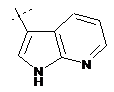 ,
,  ,
, 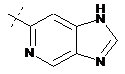 ,
, 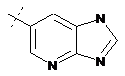 ,
, 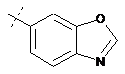 ,
, 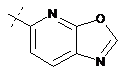 ,
, 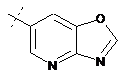 ,
, 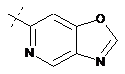 ,
, 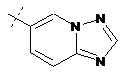 ,
, 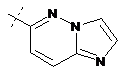 ,
, 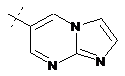 ,
, 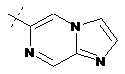 ,
, 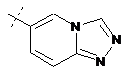 ,
, 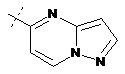 ,
, 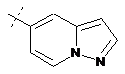 ,
, 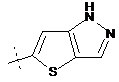 ,
, 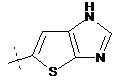 ,
, 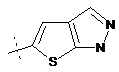 ,
, 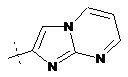 ,
, 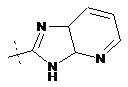 ,
, 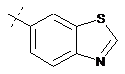 ,
, 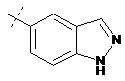 ,
, 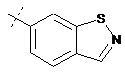 ,
,  ,
, 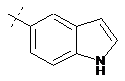 ,
,  та
та 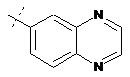 .
.
15. Cполука за формулою 1, як заявлено у п. 14, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 є кільцевою системою, вибраною із
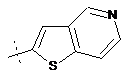 ,
, 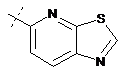 ,
, 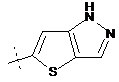 ,
, 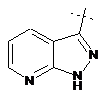 ,
, 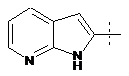 ,
, 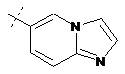 ,
, 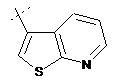 ,
, 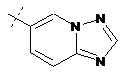 ,
, 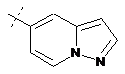 ,
, 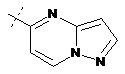 ,
, 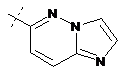 ,
, 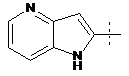 ,
, 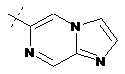 .
.
16. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-15, і/або принаймні одна її фармацевтично прийнятна сіль, де R1 є
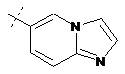 .
.
17. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-16, і/або принаймні одна її фармацевтично прийнятна сіль, де R2 і R3 незалежно вибирають із водню та С1-С6алкілу або R2 і R3, разом з вуглецем, до якого вони приєднані, утворюють 3-членний циклоалкіл.
18. Cполука за формулою 1, як заявлено у п. 17, і/або принаймні одна її фармацевтично прийнятна сіль, де R2 є воднем та R3 є вибраним з водню та метилу.
19. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-18, і/або принаймні одна її фармацевтично прийнятна сіль, де R5 означає водень.
20. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-19, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 означає арил, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
гетероарилокси, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
арилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, -S(O)nR12 та -S(O)nNR13R14.
21. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-19, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 означає гетероцикл, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, - S(O)nR12 та -S(O)nNR13R14.
22. Cполука за формулою 1, як заявлено у п. 21, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 вибирають із піролідин-1-ілу, піперидин-1-ілу, тетрагідро-2Н-піран-4-ілу, морфолін-4-ілу та 6,7-дигідротієно[3,2-с]піридин-5(4Н)-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із
нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, - S(O)nR12 та -S(O)nNR13R14.
23. Cполука за формулою 1, як заявлено у будь-якому з пунктів 1-19, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 означає гетероарил, необов'язково заміщений однією або декількома групами, вибраними із
нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, -S(O)nR12 та -S(O)nNR13R14.
24. Cполука за формулою 1, як заявлено у п. 23, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 вибирають із 1Н-піразол-1-ілу, 1Н-піразол-3-ілу, 1Н-піразол-4-ілу, 1Н-імідазол-1-ілу, 1Н-імідазол-4-ілу, оксазол-2-ілу, тіазол-2-ілу, ізоксазол-3-ілу, ізоксазол-5-ілу, 1Н-пірол-2-ілу, 1Н-пірол-3-ілу, тіофен-2-ілу, тіофен-3-ілу, піридин-2-ілу, піридин-3-ілу та піридин-4-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із
нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR11, -C(O)NR13R14, -NR13R14, -OC(O)R11, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12 та -NR13C(O)NR13R14,
нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси та нижчого алкокси,
гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси та нижчого алкокси,
галогену, ціано, -C(O)R11, -C(O)OR11, -NR13R14, -NR13C(O)R11, -NR13S(O)nR12, -NR13S(O)nNR13R14, -NR13C(O)OR12, -NR13C(O)NR13R14, -C(O)NR13R14, -S(O)nR12 та -S(O)nNR13R14.
25. Cполука за формулою 1, як заявлено у п. 24, і/або принаймні одна її фармацевтично прийнятна сіль, де R4 є 1Н-піразол-4-ілом.
26. Cполука за формулою 1, як заявлено у п. 1, яка вибрана із сполук 1-332, і/або принаймні одна її фармацевтично прийнятна сіль.
27. Cполука за формулою 1, як заявлено у п. 1, яка вибрана із:
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
і/або принаймні одна її фармацевтично прийнятна сіль.
28. Сполука за формулою 1, як заявлено у п. 1, яка є:
 ,
,
і/або принаймні одна її фармацевтично прийнятна сіль.
29. Сполука за формулою 1, як заявлено у п. 1, яка є:
 .
.
30. Композиція, яка містить принаймні одну сполуку за формулою 1, як заявлено у будь-якому з пунктів 1-28, і/або принаймні одну її фармацевтично прийнятну сіль та принаймні один фармацевтично прийнятний носій.
31. Спосіб лікування раку, чутливого до інгібування c-Met, який передбачає введення суб'єкту, який потребує цього, ефективної кількості принаймні однієї сполуки за формулою 1, як заявлено у будь-якому з пунктів 1-28, і/або принаймні однієї її фармацевтично прийнятної солі.
Текст
Реферат: Описані визначені триазолопіридини та триазолопіразини, їх композиції та їх застосування. ЇХ UA 107822 C2 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 Білок c-Met, також відомий як рецептор фактора росту гепатоцитів (HGF), являє собою трансмембранний 190 кДа гетеродимер з тирозинкіназною активністю, кодований c-met онкогеном. HGF/c-Met сигнальний шлях, як було показано, демонструє різні клітинні відповіді, включаючи мітогенетичну, проліферативну, морфогенну та ангіогенну активність. Інгібування HGF/c-Met шляху має суттєвий потенціал для лікування раку. Забезпечується принаймні одна сполука формули 1: і/або принаймні одна її фармацевтично прийнятна сіль, де 7 1 X означає N, Y вибирають із -O-, -S-, та -N(R )- і R вибирають із арилу та гетероарилу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із галогену, 11 11 13 14 13 14 13 11 -CF3, -CF2H, циклоалкілу, -C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , 13 12 13 13 14 13 12 13 13 14 12 NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , 13 14 S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, 13 14 заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; або 1 X означає N, Y відсутній і R означає конденсований біциклічний гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, 11 11 13 14 13 14 13 11 13 12 C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного 13 14 гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; або 6 7 1 X означає C(R ), Y вибирають із -O-, -S-, та -N(R )- або Y відсутній, і R означає гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, 11 11 13 14 13 14 13 11 13 12 циклоалкілу, -C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного 13 14 гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; 2 3 2 3 R і R незалежно вибирають із водню та алкілу, або R і R , разом з вуглецем, до якого вони приєднані, утворюють кільце, вибране із 3-7-членного циклоалкілу та 3-7-членного гетероциклу; 4 R вибирають із галогену, алкілу, циклоалкілу, гетероциклу, арилу та гетероарилу, кожний із яких, за виключенням галогену, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, циклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, гетероарилокси, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, арилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 1 UA 107822 C2 11 11 13 5 10 15 20 25 30 35 40 45 50 55 60 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R ; 5 R вибирають із водню, галогену, OH, NH 2, CF3, -CF2H, алкілу, алкенілу, та алкінілу; 6 11 R вибирають із водню, -OH, -NH2, -NHC(O)R , галогену та алкілу; 7 R вибирають із водню та нижчого алкілу; кожний n незалежно означає 0, 1, або 2; 11 12 13 14 R , R , R , і R незалежно вибирають із водню, алкілу, алкенілу, алкінілу, циклоалкілу, арилу, гетероарилу, та гетероциклу, кожний із яких, за виключенням водню, необов'язково заміщений однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси, та 13 14 нижчого алкокси, або R і R , разом з азотом, до якого вони приєднані, об'єднані з утворенням гетероциклічного кільця, яке необов'язково заміщене однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси, та нижчого алкокси та додатково необов'язково включає один або два додаткових гетероатомів в гетероциклічному кільці, де один або два 15 додаткових гетероатома вибирають із -O-, -S-, та -N(R )-; та 15 11 11 13 14 12 R вибирають із водню, нижчого алкілу, -C(O)R , -C(O)OR , -C(O)NR R , -S(O)nR , та 13 14 S(O)nNR R за умови, що 1 R не є необов'язково заміщеним фенілом або необов'язково заміщеним 4-піридинілом; 2 3 5 коли X означає N, R означає водень або метил, R і R означають водень, та Y відсутній, то 1 R не означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідро-бензофуран-5-іл, або 2,3-дигідро-бензо[1,4]діоксин-6-іл; та 2 3 5 7 1 коли X означає N, R , R і R означають водень, та Y означає -O- або -N(R )-, і R означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідро-бензофуран-5-іл, або 2,3-дигідро4 бензо[1,4]діоксин-6-іл; то R означає необов'язково заміщений гетероарил. Також забезпечується композиція, яка включає принаймні одну сполуку і/або принаймні одну фармацевтично прийнятну сіль, описані в даній заявці, та принаймні один фармацевтично прийнятний носій. Також забезпечується спосіб інгібування активності c-Met, який включає введення в контакт рецептора з ефективною кількістю принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці. Також забезпечується спосіб лікування раку, чутливого до інгібування c-Met, який включає введення суб'єкту, який потребує цього, ефективної кількості принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці. В тому сенсі, у якому вони використовуються в даному описі, наступні слова, фрази та символи в цілому мають значення, викладені нижче, крім випадків, коли контекст, в якому вони використовуються, вказує інше. Наступні скорочення та терміни мають скрізь зазначені значення: Тире (“-“), яке не розташоване між двома буквами або символами, використовують для позначення точки приєднання замісника. Наприклад, радикал -CONH2 приєднаний через атом вуглецю. Термін "алкіл" в цьому документі відноситься до вуглеводню з прямим або розгалуженим ланцюгом, що містить 1-10 атомів вуглецю. Приклади алкільних груп включають, але не обмежуються перерахованим, метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, та т-бутил. "Нижчий алкіл" відноситься до вуглеводню з прямим або розгалуженим ланцюгом, що містить 14 атомів вуглецю. Під терміном "алкокси" мають на увазі алкільну групу з прямим або розгалуженим ланцюгом з зазначеним числом атомів вуглецю, яка приєднана через кисневий місток, таку як, наприклад, метокси, етокси, пропокси, ізопропокси, н-бутокси, втор-бутокси, трет-бутокси, пентокси, 2пентилокси, ізопентокси, неопентокси, гексокси, 2-гексокси, 3-гексокси, 3-метилпентокси, й т.п. Алкокси групи будуть звичайно містити від 1 до 6 атомів вуглецю, які приєднані через кисневий місток. ““Нижчий алкокси" відноситься до алкокси-радикалу з прямим або розгалуженим ланцюгом, де алкільна частина містить 1-4 атомів вуглецю. Термін "алкеніл" в цьому документі відноситься до C 2-10 вуглеводню з прямим або розгалуженим ланцюгом, що містить один або декілька C=C подвійних зв'язків. Приклади алкенільних груп включають, але не обмежуються перерахованим, вініл, 2-пропеніл, та 2бутеніл. Термін "алкініл" в цьому документі відноситься до C 2-10 вуглеводню з прямим або розгалуженим ланцюгом, що містить один або декілька C≡C потрійних зв'язків. Приклади алкінільних груп включають, але не обмежуються перерахованим, етиніл, 2-пропініл, та 2бутиніл. 13 2 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "циклоалкіл" відноситься до насиченої та частково ненасиченої циклічної вуглеводневої групи, що містить 3-12 атомів вуглецю. Приклади циклоалкільних груп включають, але не обмежуються перерахованим, циклопропіл, циклобутил, циклопентил, циклопентеніл, циклогексил, циклогексеніл, циклогептил, та циклооктил. Кільце може бути насиченим або містити один або декілька подвійних зв'язків (тобто частково ненасичених), але не повністю спряженим. "Арил" охоплює: 5- та 6-членні карбоциклічні ароматичні кільця, наприклад, бензол; біциклічні кільцеві системи, де принаймні одне кільце є карбоциклічним та ароматичним, наприклад, нафталін, індан, та 1,2,3,4-тетрагідрохінолін; та трициклічні кільцеві системи, де принаймні одне кільце є карбоциклічним та ароматичним, наприклад, флуорен. Наприклад, арил включає 5- та 6-членні карбоциклічні ароматичні кільця, приконденсовані до 5-7-членного гетероциклічного кільця, що містить один або декілька гетероатомів, вибраних із N, O, та S, за умови, що точка приєднання знаходиться на карбоциклічному ароматичному кільці. Двовалентні радикали, які утворені із похідних заміщеного бензолу та містять вільні валентності на атомах кільця називають заміщеними феніленовими радикалами. Двовалентні радикали, похідні із одновалентних поліциклічних вуглеводневих радикалів, назви яких закінчуються на "-іл", утворені шляхом видалення одного атома водню від атома вуглецю з вільною валентністю, називають шляхом додавання "-іден" до назви відповідного одновалентного радикала, наприклад, нафтильну групу з двома точками приєднання називають нафтиліден. Арил, однак, не охоплює або тільки частково покриває тим або іншим способом гетероарил, окремо визначений нижче. Відповідно, якщо один або декілька карбоциклічних ароматичних кілець конденсовані з гетероциклічним ароматичним кільцем, утворювана кільцева система являє собою гетероарил, а не арил, як зазначено в даному документі. Термін "галоген (залишок)” включає залишок фтору, хлору, брому та йоду, та термін "галоген (речовина)” включає фтор, хлор, бром та йод у вигляді простих речовин. Термін "гетероарил" відноситься до 5-8-членних ароматичних, моноциклічних кілець, що містять один або декілька, наприклад, від 1 до 4, або, в деяких варіантах здійснення, від 1 до 3, гетероатомів, вибраних із N, O, та S, де інші атоми кільця є атомами вуглецю; 8-12-членних біциклічних кілець, що містять один або декілька, наприклад, від 1 до 4, або, в деяких варіантах здійснення, від 1 до 3, гетероатомів, вибраних із N, O, та S, де інші атоми кільця є атомами вуглецю, та де принаймні один гетероатом присутній в ароматичному кільці; та 11-14-членних трициклічних кілець, що містять один або декілька, наприклад, від 1 до 4, або в деяких варіантах здійснення, від 1 до 3, гетероатомів, вибраних із N, O, та S, де інші атоми кільця є атомами вуглецю, та де принаймні один гетероатом присутній в ароматичному кільці. Наприклад, гетероарил включає 5-7-членне гетероциклічне ароматичне кільце, приконденсоване до 5-7-членного циклоалкільного кільця. У випадку таких конденсованих, біциклічних гетероарильних кільцевих систем, де тільки одне із кілець містить один або декілька гетероатомів, точка приєднання може бути на гетероароматичному кільці або на циклоалкільному кільці. Коли загальне число атомів S та O в гетероарильній групі перевищує 1, такі гетероатоми не розташовані поруч один з одним. В деяких варіантах здійснення, загальне число атомів S та O в гетероарильній групі - не більш, ніж 2. В деяких варіантах здійснення, загальне число атомів S та O в ароматичному гетероциклі - не більш, ніж 1. Приклади гетероарильних груп включають, але не обмежуються перерахованим, (пронумеровано починаючи від положення приєднання, якому надане старшинство 1), 2піридил, 3-піридил, 4-піридил, 2,3-піразиніл, 3,4-піразиніл, 2,4-піримідиніл, 3,5-піримідиніл, 1піразоліл, 2,3-піразоліл, 2,4-імідазолініл, ізоксазоліл, оксазоліл, тіазоліл, тіадіазоліл, тетразоліл, тієніл, бензотієніл, фурил, бензофурил, бензоімідазолініл, індолініл, піридизиніл, триазоліл, хінолініл, піразоліл, та 5,6,7,8-тетрагідроізохінолін. Двовалентні радикали, похідні від одновалентних гетероарильних радикалів, назви яких закінчуються на "-іл", одержувані шляхом видалення одного атома водню від атома з вільною валентністю, називають шляхом додавання "-іден" до назви відповідного одновалентного радикала, наприклад, піридильну групу із двома точками приєднання називають піридиліден. Гетероарил не охоплює або тільки частково покриває арильні групи, як визначено вище. Заміщений гетероарил також включає кільцеві системи, заміщені одним або декількома оксидними (-O ) замісниками, такі як піридиніл N-оксиди. 3 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 60 Під терміном "гетероцикл" мають на увазі одиночне аліфатичне кільце, звичайно з 3-7 атомами в кільці, що містить принаймні 2 атома вуглецю, на додаток до 1-3 гетероатомів, незалежно вибраних з кисню, сірки, і азоту, а також і їх комбінації, що містять принаймні один з вищезгаданих гетероатомів. "Гетероцикл" також відноситься до 5-7-членного гетероциклічного кільця, що містить один або декілька гетероатомів, вибраних із N, O, та S, конденсованого з 5та 6-членним карбоциклічним ароматичним кільцем, за умови, що точка приєднання знаходиться на гетероциклічному кільці. Кільця можуть бути насиченими або містити один або декілька подвійних зв'язків (тобто частково ненасиченими). Гетероцикл може бути заміщеним за допомогою оксо-групи. Точка приєднання може бути вуглецем або гетероатомом в гетероциклічному кільці. Придатні гетероцикли включають, наприклад (пронумеровано починаючи від положення приєднання, якому надане старшинство 1), 1-піролідиніл, 2-піролідиніл, 2,4- імідазолідиніл, 2,3піразолідиніл, 1-піперидиніл, 2-піперидиніл, 3-піперидиніл, 4-піперидиніл, та 2,5-піперазиніл. Мають на увазі, що морфолінільні групи також включають 2-морфолініл та 3-морфолініл (де пронумерованому кисню надане старшинство 1). Заміщений гетероцикл також включає кільцеві системи, заміщені одним або декількома оксо-фрагментами, такі як піперидиніл N-оксид, морфолініл-N-оксид, 1-оксо-1-тіоморфолініл та 1,1-діоксо-1-тіоморфолініл. Під терміном "необов'язковий" або "необов'язково" мають на увазі, що наступна описана подія або обставина може або не може мати місце, та що опис включає випадки, у яких подія або обставина має місце, та випадки, в яких воно не трапляється. Наприклад, "необов'язково заміщений алкіл" охоплює й "алкіл", й "заміщений алкіл", як визначено нижче. Спеціалісту в даній галузі техніки, що стосується якої-небудь групи, що містить один або декілька замісників, буде зрозуміло, що такі групи не призначені для введення якого-небудь заміщення або схем заміщення, які є стерично непридатними, синтетично неможливими і/або які мають власну нестійкість. Термін "заміщений", у даному контексті, означає, що будь-який один або декілька атомів водню на позначеному атомі або групі замінений на варіант із зазначеної групи, за умови, що звичайна валентність позначеного атома не перевищена. Коли замісником є оксо (тобто, =O) то замінюється 2 атоми водню на позначеному атомі. Комбінації замісників і/або змінних допускаються тільки, якщо такі комбінації приведуть до стабільних сполук або придатним синтетичним проміжних сполук. Під стабільною сполукою або стабільною структурою мають на увазі сполуку, що є в достатній мірі стійкою, щоби витримати виділення з реакційної суміші, і наступне введення в препарат як агент, що має принаймні практичною цінністю. Якщо не обговорене інше, замісники називають у ядрі структури. Наприклад, варто розуміти, що коли (циклоалкіл)алкіл перерахований як можливий замісник, точка приєднання цього замісника до ядра структури знаходиться в алкільній частині. У деяких варіантах здійснення, "заміщений одним або декількома групами" відноситься до двох атомів водню на позначеному атомі або групі, незалежно замінених двома варіантами із зазначеної групи замісників. У деяких варіантах здійснення, "заміщений однією або декількома групами" відноситься до трьох атомів водню на позначеному атомі або групі, незалежно замінених трьома варіантами із зазначеної групи замісників. У деяких варіантах здійснення, "заміщений однією або декількома групами" відноситься до чотирьох атомів водню на позначеному атомі або групі, незалежно замінених чотирма варіантами із зазначеної групи замісників. Сполуки описані в даній заявці включають, але не обмежуються перерахованим, їх оптичні ізомери, рацемати, та інші їх суміші. У таких ситуаціях, окремі енантіомери або діастереоізомери, тобто, оптично активні форми, можуть бути одержані шляхом асиметричного синтезу або шляхом розділення рацематів або сумішей діастереоізомерів. Розділення рацематів або сумішей діастереоізомерів може бути виконано, наприклад, за допомогою стандартних методів, таких як кристалізація за присутності агента для оптичного розщеплення, або хроматографія, з використанням, наприклад, колонки для хіральної рідинної хроматографії високого тиску (РХВТ). Крім того, такі сполуки включають Z- та E- форми (или цис- та трансформи) сполук з вуглець-вуглецевими подвійними зв'язками. У випадку, якщо сполуки, описані в даній заявці існують у різних таутомерних формах, мають на увазі, що термін "сполука" включає всі таутомерні форми сполуки. Такі сполуки також включають кристалічні форми, в тому числі поліморфи й клатрати. Подібним чином, мають на увазі, що термін "сіль" включає всі ізомери, рацемати, інші суміші, Z- та E-форми, таутомерні форми та кристалічні форми солі зазначеної сполуки. "Фармацевтично прийнятні солі" включають, але не обмежуються перерахованим, солі з неорганічними кислотами, такі як гідрохлорат, фосфат, дифосфат, гідробромат, сульфат, 4 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 60 сульфінат, нітрат, та подібні солі; а також й солі з органічною кислотою, такі як малат, малеат, фумарат, тартрат, сукцинат, цитрат, ацетат, лактат, метансульфонат, п-толуолсульфонат, 2гідроксіетилсульфонат, бензоат, саліцилат, стеарат, та алканоат, такий як ацетат, HOOC(CH2)n-COOH, де n означає 0-4, та подібні солі. Подібним чином, фармацевтично прийнятні катіони включають, але не обмежуються перерахованим катіони натрію, калію, кальцію, алюмінію, літію та амонію. Крім того, якщо сполуку, описану в даній заявці, одержують у вигляді солі приєднання кислоти, вільна основа може бути одержана шляхом підлуговування розчину кислої солі. Навпаки, якщо продукт являє собою вільну основу, сіль приєднання, зокрема, фармацевтично прийнятна сіль приєднання, може бути одержана шляхом розчинення вільної основи в придатному органічному розчиннику й обробки розчину кислотою, відповідно до звичайних методик одержання солей приєднання кислот із основних сполук. Спеціаліст в даній галузі техніки відзначить різні синтетичні методи, які можна використовувати для одержання нетоксичних фармацевтично прийнятних солей приєднання. "Сольват", такий як "гідрат" утворюють шляхом взаємодії розчинника та сполуки. Мають на увазі, що термін "сполука" включає сольвати, у тому числі гідрати, сполук. Подібним чином, "солі" включають сольвати, такі як гідрати, солей. Придатними сольватами є фармацевтично прийнятні сольвати, такі як гідрати, у тому числі моногідрати та напівгідрати. "Хелати" утворюють шляхом координування сполуки до іону металів в двох (або більше) точках. Мають на увазі, що термін "сполука" включає хелати сполук. Подібним чином, "солі" включають хелати солей. "Нековалентний комплекс" утворюють шляхом взаємодії сполуки та іншої молекули, де ковалентний зв'язок між сполукам та зазначеною молекулою не утворюється. Наприклад, комплексоутворення може відбуватися завдяки ван-дер-ваальсівським взаємодіям, утворенню водневих зв'язків, та електростатичним взаємодіям (також називаним іонне зв'язування). Такі нековалентні комплекси включені в термін "сполука". Термін "водневий зв'язок" відноситься до форми асоціації між електронегативним атомом (т.н. акцептор водневого зв'язку) та атомом водню, приєднаним до другого, відносно електронегативного атому (т.н. донор водневого зв'язку). Придатні донори водневого зв'язку та акцептори добре вивчені в медичній хімії (G. C. Pimentel and A. L. McClellan, The Hydrogen Bond, Freeman, Сан-Франциско, 1960; R. Taylor and O. Kennard, "Hydrogen Bond Geometry in Organic Crystals", Accounts of Chemical Research, 17, сс. 320-326 (1984)). У даному контексті терміни "група", "радикал" або "фрагмент" є синонімічними та призначені для зазначення функціональних груп або фрагментів молекул, які приєднуються до зв'язку або інших фрагментів молекул. Термін "активний засіб" використовують для вказівки хімічної речовини, яка має біологічну активність. В деяких варіантах здійснення, "активний засіб" є хімічною речовиною, яка має фармацевтичну цінність. "Терапія" або "лікування" або "полегшення" відноситься до введення принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, суб'єкту, який має рак, або у якого спостерігаються симптоми раку, або який має схильність до появи раку, з метою лікування, зцілення, полегшення, ослаблення, зміни, усунення, поліпшення, нормалізації, або впливу на рак, симптоми раку, або схильність до появи раку. Термін "ефективна кількість" відноситься до кількості принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, яка ефективна для "лікування" захворювання або розладу в суб'єкта. У випадку раку, ефективна кількість може викликати будь-яку зі змін, спостережуваних або вимірюваних у суб'єкта, як описано у визначенні "терапії", "лікування" та "полегшення" вище. Наприклад, ефективна кількість може знижувати число ракових або пухлинних клітин; зменшувати розмір пухлини; інгібувати або зупиняти інфільтрацію пухлинних клітин в у периферичні органи в тому числі, наприклад, поширення пухлини в м'яку тканину й кістку; інгібувати або зупиняти метастазування раку; інгібувати або зупиняти ріст пухлини; послабляти певною мірою один або декілька симптомів, пов'язаних з раком, знижувати больові відчуття і летальність; нормалізувати якість життя; або може викликати комбінація таких дій. Ефективна кількість може бути кількістю, достатньою для зменшення симптомів захворювання, чутливого до інгібування активності c-Met. У випадку терапії раку, ефективність in vivo може, наприклад, бути виміряна шляхом оцінювання строку виживання, часу до прогресування захворювання (TTP), швидкості реакції (RR), тривалості відповіді, і/або якість життя. Ефективні кількості можуть змінюватися, як очевидно, спеціалістом в даній галузі техніки, в залежності від шляху введення, використовуваних допоміжних речовин, та інших, спільно використовуваних, лікарських засобів. 5 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 Термін "інгібування" вказує на зменшення вихідної біологічної активності або активності процесу. "Інгібування активності c-Met ” відноситься до зменшення активності c-Met в наслідок прямої або опосередкованої відповіді на присутність принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, відносно активності c-Met за відсутності принаймні однієї сполуки і/або принаймні однієї її фармацевтично прийнятної солі. Зменшення активності може спостерігатися в результаті прямої взаємодії принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в дані заявці з c-Met, або в результаті взаємодії принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, з одним або декількома іншими факторами, які у свою чергу впливають на активність c-Met. Наприклад, присутність принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, може зменшувати активність c-Met шляхом прямого приєднання до c-Met, шляхом впливу (прямого або опосередкованого) на інший фактор, змушуючи його зменшувати активність c-Met, або шляхом (прямого або опосередкованого) зменшення кількості c-Met, що присутня в клітині або організмі. Деталі одного або декількох варіантів здійснення винаходу викладені нижче. Забезпечується принаймні одна сполука формули 1: і/або принаймні одна її фармацевтично прийнятна сіль, де 7 1 X означає N, Y вибирають із -O-, -S-, та -N(R )- і R вибирають із арилу та гетероарилу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із галогену, 11 11 13 14 13 14 13 11 -CF3, -CF2H, циклоалкілу, -C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , 13 12 13 13 14 13 12 13 13 14 12 NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , 13 14 S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, 13 14 заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; або 1 X означає N, Y відсутній і R означає конденсований біциклічний гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, 11 11 13 14 13 14 13 11 13 12 C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного 13 14 гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; або 6 7 1 X означає C(R ), Y вибирають із -O-, -S-, та -N(R )- або Y відсутній, і R означає гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, 11 11 13 14 13 14 13 11 13 12 циклоалкілу, -C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного 13 14 гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом; 2 3 2 3 R і R незалежно вибирають із водню та алкілу, або R і R , разом з вуглецем, до якого вони приєднані, утворюють кільце, вибране із 3-7-членного циклоалкілу та 3-7-членного гетероциклу; 4 R вибирають із галогену, алкілу, циклоалкілу, гетероциклу, арилу та гетероарилу, кожний із яких, за виключенням галогену, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, циклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, 6 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 гетероциклоалкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, гетероарилокси, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, арилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R ; 5 R вибирають із водню, галогену, OH, NH 2, CF3, -CF2H, алкілу, алкенілу, та алкінілу; 6 11 R вибирають із водню, -OH, -NH2, -NHC(O)R , галогену та алкілу; 7 R вибирають із водню та нижчого алкілу; кожний n незалежно означає 0, 1, або 2; 11 12 13 14 R , R , R , і R незалежно вибирають із водню, алкілу, алкенілу, алкінілу, циклоалкілу, арилу, гетероарилу, та гетероциклу, кожний із яких, за виключенням водню, необов'язково заміщений однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси, та 13 14 нижчого алкокси, або R і R , разом з азотом, до якого вони приєднані, об'єднані з утворенням гетероциклічного кільця, яке необов'язково заміщене однією або декількома групами, вибраними із галогену, нижчого алкілу, гідрокси, та нижчого алкокси та додатково необов'язково включає один або два додаткових гетероатомів в гетероциклічному кільці, де один або два 15 додаткових гетероатома вибирають із -O-, -S-, та -N(R )-; та 15 11 11 13 14 12 R вибирають із водню, нижчого алкілу, -C(O)R , -C(O)OR , -C(O)NR R , -S(O)nR , та 13 14 S(O)nNR R за умови, що 1 R не є необов'язково заміщеним фенілом або необов'язково заміщеним 4-піридинілом; 2 3 5 коли X означає N, R означає водень або метил, R і R означають водень, та Y відсутній, то 1 R не означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідро-бензофуран-5-іл, або 2,3-дигідро-бензо[1,4]діоксин-6-іл; та 2 3 5 7 1 коли X означає N, R , R і R означають водень, та Y означає -O- або -N(R )-, і R означає хінолін-6-іл, 7-фторхінолін-6-іл, 3-хіназолін-6-іл, 2-3-дигідро-бензофуран-5-іл, або 2,3-дигідро4 бензо[1,4]діоксин-6-іл; то R означає необов'язково заміщений гетероарил. 6 В деяких варіантах здійснення, X означає N. В деяких варіантах здійснення, X означає C(R ). 6 В деяких варіантах здійснення, R вибирають із водню, галогену та нижчого алкілу. В деяких 6 варіантах здійснення, R означає водень. В деяких варіантах здійснення, Y означає -O-. В деяких варіантах здійснення, Y означає -S-. 7 7 В деяких варіантах здійснення, Y означає -N(R )-. В деяких варіантах здійснення, R означає 7 водень або метил. В деяких варіантах здійснення, R означає водень. В деяких варіантах здійснення, Y відсутній. 1 В деяких варіантах здійснення, R означає 8-10-членний гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, -CF3, -CF2H, циклоалкілу, 11 11 13 14 13 14 13 11 13 12 C(O)R , -C(O)OR , -CN, -C(O)NR R , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного 13 14 гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкілу, заміщеного -NR R , та 1 нижчого алкілу, заміщеного гетероциклом. В деяких варіантах здійснення, R означає 8-10членний гетероарил, необов'язково заміщений однією або декількома групами, вибраними із галогену, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, та нижчого алкілу, заміщеного нижчим алкокси. 1 В деяких варіантах здійснення, R вибирають із хінолін-6-ілу, тієно[3,2-c]піридин-2-ілу, бензо[d]тіазол-6-ілу, та імідазо[1,2-a]піридин-6-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із галогену, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, та нижчого алкілу, заміщеного нижчим алкокси. В деяких варіантах 1 здійснення, R вибирають із хінолін-6-ілу, необов'язково заміщеного однією або декількома групами, вибраними із галогену, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, та нижчого алкілу, заміщеного нижчим алкокси. 1 В деяких варіантах здійснення, R означає кільцеву систему, вибрану із 60 7 UA 107822 C2 N N N N N N N N N S N N S N N N N N N S S S S N N S O O O N N N N N N N N H H N N N H N N N N N 10 N N H N N N H N N N N N N N N H N N N N N N N H N N N H N N N N S H N N N H H N N N N N H N H N N N N N H N N N NH O N N N N H O N N N N N H N O N N N H N N N H N N H S N N N N N N S N N N N 5 H N N N N N N N N N N S N N N N N N N N N N N N N N N N H N N S N N N N N N S N N N N N N N N N N N N H N N N N N N N N де кожна із зазначених кільцевих систем необов'язково заміщена однією або декількома 11 11 13 14 групами, вибраними із галогену, CF3, -CF2H, циклоалкілу, -C(O)R , C(O)OR , -CN, -C(O)NR R , 13 14 13 11 13 12 13 13 14 13 12 13 13 14 -NR R , -NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , 12 13 14 NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, 13 14 нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом. З метою виключення помилкового тлумачення, кожна із вищезазначених кільцевих систем може бути 2 3 приєднана до вуглецю, що несе R і R на будь-якій відкритій валентності на будь-якому із кілець в кільцевих системах. 1 В деяких варіантах здійснення, R означає кільцеву систему, вибрану із 8 UA 107822 C2 N N N N S N N N N N N N N N S N H N N N H N H N N N N N N H N S S N S H N O 30 N N N N N N N N N N N N N N N N H N N N N 25 N N H N 20 N N N N 15 N N O S S 10 N O N N N H N N N O N N N N N N N N 5 N O N N N H N N N H S N N N N H N N N S N H N N N S N N N N N N N N N N S S S N N N H та N . де кожна із зазначених кільцевих систем необов'язково заміщена однією або декількома 11 11 13 14 групами, вибраними із галогену, CF3, -CF2H, циклоалкілу, -C(O)R , C(O)OR , -CN, -C(O)NR R , 13 14 13 11 13 12 13 13 14 13 12 13 13 14 -NR R , -NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , 12 13 14 NO2, -S(O)nR , -S(O)nNR R , гетероциклу, гетероарилу, арилу, алкенілу, алкінілу, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, 13 14 нижчого алкілу, заміщеного -NR R , та нижчого алкілу, заміщеного гетероциклом. З метою виключення помилкового тлумачення, кожна із вищезазначених кільцевих систем, зображених 2 3 вище, приєднується до вуглецю, що несе R і R в зазначеному положенні. 2 3 2 В деяких варіантах здійснення, R і R незалежно вибирають із водню та C1-C6 алкілу або R 3 і R , разом з вуглецем, до якого вони приєднані, утворюють 3-членний циклоалкіл. В деяких 2 3 варіантах здійснення, R означає водень і R вибирають із водню та C1-C6 алкілу. В деяких 2 3 варіантах здійснення, R означає водень і R вибирають із водню та метилу. В деяких варіантах 2 3 2 3 здійснення, R і R означають водень. В деяких варіантах здійснення, R і R , разом з вуглецем, до якого вони приєднані, утворюють 3-членний циклоалкіл. 4 В деяких варіантах здійснення, R означає арил, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 9 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 гетероарилокси, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, арилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R . 4 В деяких варіантах здійснення, R означає арил, необов'язково заміщений однією або 13 12 декількома групами, вибраними із галогену, гідрокси, -NR S(O)nR , нижчого алкокси, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, нижчого алкілу, заміщеного нижчим алкокси, нижчого алкокси, заміщеного гідрокси, та нижчого алкокси, заміщеного нижчим алкокси. 4 В деяких варіантах здійснення, R означає феніл, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкокси, нижчого алкокси, заміщеного гідрокси, та нижчого алкокси, заміщеного нижчим алкокси. 4 В деяких варіантах здійснення, R означає гетероцикл, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R . 4 В деяких варіантах здійснення, R вибирають із піролідин-1-ілу, піперидин-1-ілу, тетрагідро2H-піран-4-ілу, морфолін-4-ілу, та 6,7-дигідротієно[3,2-c]піридин-5(4H)-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R . 4 В деяких варіантах здійснення, R вибирають із піролідин-1-ілу, піперидин-1-ілу, тетрагідро2H-піран-4-ілу, морфолін-4-ілу, та 6,7-дигідротієно[3,2-c]піридин-5(4H)-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із галогену, CF 3, -CF2H, гідрокси, нижчого алкілу, нижчого алкілу, заміщеного гідрокси, та нижчого алкілу, заміщеного нижчим алкокси. 4 В деяких варіантах здійснення, R означає гетероарил, необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R . 4 В деяких варіантах здійснення, R вибирають із 1H-піразол-1-ілу, 1H-піразол-3-ілу, 1Hпіразол-4-ілу, 1H-імідазол-1-ілу, 1H-імідазол-4-ілу, оксазол-2-ілу, тіазол-2-ілу, ізоксазол-3-ілу, ізоксазол-5-ілу, 1H-пірол-2-ілу, 1H-пірол-3-ілу, тіофен-2-ілу, тіофен-3-ілу, піридин-2-ілу, піридин3-ілу, та піридин-4-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із 10 UA 107822 C2 5 10 15 20 25 30 35 нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , нижчого алкокси, необов'язково заміщеного однією або декількома групами, вибраними із галогену, гідрокси, та нижчого алкокси, гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 11 11 13 14 13 11 13 12 галогену, ціано, -C(O)R , -C(O)OR , -NR R , -NR C(O)R , -NR S(O)nR , 13 13 14 13 12 13 13 14 13 14 12 13 14 NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -C(O)NR R , -S(O)nR , та -S(O)nNR R . 4 В деяких варіантах здійснення, R вибирають із 1H-піразол-1-ілу, 1H-піразол-3-ілу, 1Hпіразол-4-ілу, 1H-імідазол-1-ілу, 1H-імідазол-4-ілу, оксазол-2-ілу, тіазол-2-ілу, ізоксазол-3-ілу, ізоксазол-5-ілу, 1H-пірол-2-ілу, 1H-пірол-3-ілу, тіофен-2-ілу, тіофен-3-ілу, піридин-2-ілу, піридин3-ілу, та піридин-4-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із 11 13 14 13 14 11 гідрокси, нижчого алкокси, ціано, галогену, -C(O)OR , -C(O)NR R , -NR R , -OC(O)R , 13 11 13 12 13 13 14 13 12 13 13 14 NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , та -NR C(O)NR R , та гетероциклу, необов'язково заміщеного однією або декількома групами, вибраними із нижчого алкілу, галогену, гідрокси, та нижчого алкокси, 4 В деяких варіантах здійснення, R вибирають із 1H-піразол-1-ілу, 1H-піразол-3-ілу, 1Hпіразол-4-ілу, 1H-імідазол-1-ілу, 1H-імідазол-4-ілу, оксазол-2-ілу, тіазол-2-ілу, ізоксазол-3-ілу, ізоксазол-5-ілу, 1H-пірол-2-ілу, 1H-пірол-3-ілу, тіофен-2-ілу, тіофен-3-ілу, піридин-2-ілу, піридин3-ілу, та піридин-4-ілу, кожний із яких необов'язково заміщений однією або декількома групами, вибраними із нижчого алкілу, необов'язково заміщеного однією або декількома групами, вибраними із гідрокси, нижчого алкокси, ціано, та галогену. 4 В деяких варіантах здійснення, R означає нижчий алкіл. 5 В деяких варіантах здійснення, R означає водень. В деяких варіантах здійснення, n означає 0. В деяких варіантах здійснення, n означає 1. В деяких варіантах здійснення, n означає 2. Також забезпечується принаймні одна сполука, яка вибрана із сполук 1-332 і/або принаймні одна фармацевтично прийнятна сіль, описана в дані заявці. Сполуки, описані в даній заявці, і/або їх фармацевтично прийнятні солі, можуть бути синтезовані із доступних для придбання вихідних речовин за допомогою методів, добре відомих в даній галузі техніки. Наступні схеми ілюструють методи одержання більшості сполук. В кожній із схем, LG та LG" означають відхідні групи, які можуть бути однаковими або різними. Y" означає 7 1 2 3 4 5 –NHR , -OH, -SH, –B(OH)2, або B(OR")2, і R , R , R , R , R та Y приймають значення, зазначені у даній заявці. Схема I R2 LG R5 N N LG' NH2 H2 N LG R3 R1 R2 N NH LG N N R5 N R5 N N R3 R1 R3 R2 N NH2 R4Y' R4Y' R4 40 R1 Y R5 R3 R1 R2 N NH N 11 NH2 R3 R2 R1 Y N N R5 N N R4 N UA 107822 C2 Схема II R2 LG N LG' NO2 R5 R6 H2 N R3 R1 LG R3 R1 R2 N NH R5 LG R3 R1 R2 N NH R5 NO2 R3 R2 LG R6 R4Y' Y R2 R R1 N NH R5 NH2 5 10 15 20 25 30 35 40 45 R2 R1 R4 R6 N N R5 R4Y' R4 R1 N NH2 R6 R6 N Y N R N N N R5 R6 Одержані таким чином сполуки можуть бути далі модифіковані в їх периферійних положеннях з забезпеченням цільових сполук. Синтетичні хімічні перетворення описані, наприклад, в роботах R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); -е T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 3 вид., John Wiley and Sons (1999); L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); та L. Paquette, ред., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) та їх більш пізніх виданнях. Перед застосуванням, принаймні одна сполука і/або принаймні одна її фармацевтично прийнятна сіль, описані в дані заявці, можуть бути очищені за допомогою колонкової хроматографії, високоефективної рідинної хроматографії, кристалізації, або іншими придатними методами. Також забезпечується композиція, що містить принаймні одну сполуку і/або принаймні одну її фармацевтично прийнятну сіль, описані в дані заявці, та принаймні один фармацевтично прийнятний носій. Композицію, що містить принаймні одну сполуку і/або принаймні одну фармацевтично прийнятну сіль, описані в дані заявці, можна вводити різними відомими способами, наприклад, пероральним, парентеральним, шляхом інгаляційного розпилення, або через імплантоване джерело. Термін "парентеральний" у даному контексті включає підшкірну, внутрішньошкірну, внутрішньовенну, внутрішньом'язову, внутрішньосуглобну, внутрішньоартеріальну, інтрасиновіальну, надчеревну, інтратекальну, внутрішньоосередкову та внутрішньочерепну ін'єкцію або техніку вливання. Пероральна композиція може бути будь-якою пероральною прийнятною лікарською формою, включаючи, але не обмежуючись перерахованим, таблетки, капсули, емульсії, і водні суспензії, дисперсії й розчини. Широко застосовувані носії для таблеток включають лактозу й кукурудзяний крохмаль. Змащувальні речовини, такі як стеарат магнію, також типово додають до таблеток. У випадку перорального введення у формі капсул, придатні розріджувачі включають лактозу й сухий кукурудзяний крохмаль. Коли водні суспензії або емульсії вводять перорально, активний компонент може бути суспендований або розчинений у масляній фазі, у сполученні з емульгувальним або суспендуючим агентами. При необхідності, можуть бути додані певні підсолоджувачі, смакові речовини, або барвники. Стерильна ін'єкована композиція (наприклад, водна або масляна суспензія) може бути складена за методиками, відомими у даній галузі техніки з використанням придатних диспергуючих або змочувальних агентів (таких як, наприклад, Tween 80) і суспендуючих агентів. Стерильний ін'єкований препарат також може бути стерильним ін'єкованим розчином або суспензією в нетоксичному парентерально прийнятному розріджувачі або розчиннику, наприклад, у вигляді розчину в 1,3-бутандіолі. Серед фармацевтично прийнятних наповнювачів і розчинників, які можна використати, присутні маніт, вода, розчин Рингера й ізотонічний розчин хлориду натрію. Крім того, як розчинник або суспендуюче середовище звичайно використовують стерильні нелеткі масла(олії) (наприклад, синтетичні моно- або ди-гліцериди). Жирні кислоти, такі як олеїнова кислота і її гліцеридні похідні, придатні для одержання ін'єкованих композицій, рівною мірою, як і природні фармацевтично-прийнятні олії, такі як 12 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 60 маслинова олія або рицинова олія, особливо в їх поліоксіетилованих варіантах. Ці масляні розчини або суспензії також можуть містити довголанцюговий спиртовий розріджувач або диспергатор, або карбоксиметилцелюлозу, або подібні диспергуючі речовини. Інгаляційна композиція може бути одержана за методиками, добре відомими в галузі технології приготування лікарських засобів й може бути одержана у вигляді розчинів у соляному розчині, використовуючи бензиловий спирт або інші придатні консерванти, стимулятори абсорбції для підвищення біодоступності, фторовуглеці, і/або інші солюбілізувальні або диспергуючі речовини, відомі в даній галузі техніки. Композиція для місцевого введення може бути складена у вигляді масла, крему, лосьйону, мазі й т.п. Придатні носії для композиції включають рослинні або мінеральні масла (олії), білий петролатум (білий м'який парафін), жири або масла з розгалуженим ланцюгом, тваринні жири й високомолекулярні спирти (більш, ніж C12). У деяких варіантах здійснення, фармацевтично прийнятний носій є одним компонентом, у якому розчиняється активний компонент. Також, за необхідності, можуть бути включені емульгувальні речовини, стабілізатори, зволожувачі й антиоксиданти, а також і агенти, що надають колір або аромат. Крім того, в лікарській формі для зовнішнього застосування можуть використовуватися агенти, що посилюють проникнення через шкіру. Приклади таких посилюючих агентів можуть бути знайдені в патентах США 3,989,816 і 4,444,762. Креми можуть бути складені із суміші мінерального масла, здатного до самоемульгування воску й води, у яку домішують суміш активного компонента, розчиненого в невеликій кількості масла(олії), такого як мигдальна олія. Прикладом такого крему є крем, що включає приблизно 40 частин води, приблизно 20 частин воску, приблизно 40 частин мінерального масла й приблизно 1 частину мигдальної олії. Мазі можуть бути складені шляхом змішування розчину активного компонента в олії рослинного походження, наприклад, мигдальній олії, з теплим м'яким парафіном, і наступного охолодження суміші. Прикладом такої мазі є мазь, що включає приблизно 30 мас. % мигдалю й приблизно 70 мас. % білого м'якого парафіну. Фармацевтично прийнятний носій відноситься до носія, що придатний для комбінування з активними компонентами композиції (і, у деяких варіантах здійснення, у стані стабілізувати активні компоненти) і не шкідливим для суб'єкта, що підлягає лікуванню. Наприклад, солюбілізувальні компоненти, такі як циклодекстрини (які утворюють специфічні, більш розчинні комплекси із щонайменше однією сполукою й/або щонайменше однією фармацевтично прийнятною сіллю, описаними у даному описі), можуть використатися як фармацевтичні допоміжні речовини для доставки активних компонентів. Приклади інших носіїв включають колоїдний діоксид кремнію, стеарат магнію, целюлозу, лаурилсульфат натрію, і пігменти, такі як D&C Жовтий# 10. Придатні in vitro дослідження можуть використовуватися для попереднього оцінювання ефективності принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даному описі, щодо інгібуючої активності на c-Met. Принаймні одна сполука і/або принаймні одна фармацевтично прийнятна сіль, описані в даному описі, далі можуть бути проаналізовані на ефективність лікування раку за допомогою in vivo досліджень. Наприклад, сполуки, описані в даному описі, і/або їх фармацевтично прийнятні солі, можуть бути введені тварині (наприклад, мишача модель), яка має рак й, відповідно, можуть бути досягнуті терапевтичні ефекти. На основі результатів, також може бути визначений відповідний діапазон доз та шлях введення тваринам, таким як люди. Також забезпечується спосіб інгібування активності c-Met. Спосіб включає введення рецептора в контакт з кількістю принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці, ефективною для інгібування активності c-Met. Принаймні одну сполуку і/або принаймні одну фармацевтично прийнятну сіль, описані в дані заявці, можна застосовувати для досягнення корисної терапевтичної або профілактичної дії, наприклад, у суб'єктів з раком. У даному контексті, термін "рак" відноситься до клітинних розладів, які характеризуються неконтрольованою або дерегульованою проліферацією клітин, зниженим клітинним диференціюванням, недоречною здатністю до ураження оточуючих тканин, і/або здатністю до формування нового росту в ектопічних ділянках. Термін "рак" включає, але не обмежується перерахованим, солідні пухлини та пухлини крові. Термін "рак" охоплює захворювання шкіри, тканин, органів, кісток, хрящів, крові та судин. Термін "рак" додатково охоплює первинний та метастатичний рак. Необмежуючі приклади солідних пухлин включають рак підшлункової залози; рак сечового міхура; колоректальний рак; рак молочної залози, включаючи метастатичний рак молочної залози; рак передміхурової залози, включаючи андроген-залежний та андроген-незалежний рак передміхурової залози; рак нирки, включаючи, наприклад, метастатичну нирково-клітинну 13 UA 107822 C2 5 10 15 20 25 30 35 40 45 50 55 60 карциному; гепатоцелюлярний рак; рак легень, включаючи, наприклад, недрібноклітинний рак легень (NSCLC), бронхіоло-альвеолярну карциному (BAC), та аденокарциному легень; рак яєчників, включаючи, наприклад, прогресуючий епітеліальний або первинний перітонеальний рак; рак шийки матки; рак шлунка; рак стравоходу; рак голови та шиї, включаючи, наприклад, сквамозну карциному голови та шиї; рак шкіри, включаючи наприклад, злоякісну меланому; нейроендокринний рак, включаючи метастатичні нейроендокринні пухлини; пухлини мозку, включаючи, наприклад, гліому, анапластичну олігодендрогліому, мультиформну гліобластому дорослих, та анапластичну астроцитому дорослих; рак кісток; саркому м'яких тканин; та рак щитовидної залози. Необмежуючі приклади гематологічних злоякісних пухлин включають гостру мієлоцитарну лейкемію (AML); хронічну мієлогену лейкемію (CML), включаючи прискорену CML та бластну фазу CML (CML-BP); гостру лімфобластну лейкемію (ALL); хронічну лімфоцитарну лейкемію (CLL); хворобу Ходжкіна (HD); неходжкінську лімфому (NHL), включаючи фолікулярну лімфому та лімфому клітин мантійної зони; B-клітинну лімфому; T-клітинну лімфому; множинну мієлому (MM); макроглобулінемію Вальденстрома; мієлодиспластичні синдроми (MDS), включаючи рефрактерну анемію (RA), рефрактерну анемію з кільцеподібними сидеробластами (RARS), рефрактерну анемію з надлишком бластів (RAEB), і RAEB при трансформації (RAEB-T); та мієлопроліферативні синдроми. В деяких варіантах здійснення, приклади раку, що підлягає лікуванню, включають, але не обмежуються перерахованим, рак легень, рак голови та шиї, колоректальний рак, рак підшлункової залози, рак ободової кишки, рак молочної залози, рак яєчників, рак передміхурової залози, рак шлунка, рак нирки, рак печінки, рак мозку, рак кісток, та лейкемія. В деяких варіантах здійснення, принаймні одну сполуку і/або принаймні одну фармацевтично прийнятну сіль, описані в даному описі, вводять спільно з іншим терапевтичним засобом. У деяких варіантах здійснення, інший терапевтичний засіб являє собою такий засіб, який звичайно вводят пацієнтам з тим захворюванням або станом, яке лікується. Принаймні одна сполука і/або принаймні одна фармацевтично прийнятну сіль, описані в дані заявці, можуть вводитися разом з іншим терапевтичним засобом в одній і тій же дозованій формі або у вигляді окремої дозованої форми. Коли здійснюють введення у вигляді окремої дозованої форми, інший терапевтичний засіб може бути введений до введення, разом з введенням або після введення принаймні однієї сполуки і/або принаймні однієї фармацевтично прийнятної солі, описаних в даній заявці. В деяких варіантах здійснення, принаймні одну сполуку і/або принаймні одну фармацевтично прийнятну сіль, описані в дані заявці, вводять спільно з протипухлинним засобом. У даному контексті, термін "протипухлинний засіб" відноситься до будь-якого агенту, який вводять суб'єкту з раком в цілях лікування останнього. Необмежуючі приклади протипухлинних засобів включають: радіотерапію; імунотерапію; хіміотерапевтичні засоби, що ушкоджують ДНК; та хіміотерапевтичні засоби, які порушують реплікацию клітин. Необмежуючі приклади хіміотерапевтичних засобів, що ушкоджують ДНК, включають інгібітори топоізомерази I (наприклад, іринотекан, топотекан, камптотецин та їх аналоги або метаболіти, та доксорубіцин); інгібітори топоізомерази II (наприклад, етопозид, теніпозид, та даунорубіцин); алкілувальні агенти (наприклад, мельфалан, хлорамбуцил, бусульфан, тіотепа, іфосфамід, кармустин, ломустин, семустин, стрептозоцин, декарбазин, метотрексат, мітоміцин C, та циклофосфамід); ДНК інтеркалятори (наприклад, цисплатин, оксаліплатин та карбоплатин); ДНК інтеркалятори та генератори вільних радикалів, такі як блеоміцин; та нуклеозидні міметики (наприклад, 5-фторурацил, капецитибін, гемцитабин, флударабін, цитарабін, меркаптопурин, тіогуанін, пентостатин, та гідроксисечовина). Хіміотерапевтичні засоби, які порушують реплікацію клітин, включають: паклітаксель, доцетаксель, та споріднені аналоги; вінкристин, вінбластин, та споріднені аналоги; талідомід та споріднені аналоги (наприклад, CC-5013 та CC-4047); інгібітори білка - тирозинкінази (наприклад, іматиніб мезилат та гефітиніб); інгібітори протеасоми (наприклад, бортезоміб); інгібітори NF-капа B, включаючи інгібітори I капа B кінази; антитіла, які зв'язуються з білками, які надекспресуються в ракових пухлинах, й таким чином знижувально регулюють реплікацію клітин (наприклад, трастузумаб, ритуксимаб, цетуксимаб та бевацизумаб); та інші інгібітори білків або ферментів, відомих здатністю підвищувально регулюватися, надекспресуватися або активуватися в ракових пухлинах, інгібування яких знижувально регулює реплікацію клітин. ПРИКЛАДИ Наведені нижче приклади призначені для чисто ілюстративних цілей й, як слід вважати, не обмежують тим або іншим чином заявлений винахід. Були прикладені зусилля, з метою гарантувати точність, стосовно використовуваних чисел (наприклад, кількостей, температур, й 14 UA 107822 C2 5 т.д.), але деякі експериментальні помилки та відхилення повинні бути враховані. Якщо не зазначено інше, частини є масовими частинами, температура наведена в градусах Цельсія, а тиск є атмосферним або близьким до нього. Всі дані МС одержували на приладі agilent 6120, agilent 1100. Всі реагенти, за виключенням проміжних сполук, використовуваних в даному винаході, доступні для придбання. Всі назви сполук, за виключенням реагентів, генерували за допомогою Chemdraw 8.0. В наступних прикладах, використовуються зазначені нижче скорочення: AIBN a, a’-азо-ізобутиронітрил BINAP 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил Boc трет-бутоксикарбоніл Boc2O ди-т-бутил-дикарбонат ізо-BuNO2 ізобутилнітрит ДХМ дихлорметан ДМФА N, N-диметилформамід DMAP 4-диметиламінопіридин DPPA дифенілфосфорилазид DBU 1,8-діазабіцикло[5.4.0]ундец-7-ен DEA N, N-діетиламін ee енантіомерний надлишок Et3N триетиламін год. година гексафторфосфат O-(7-азабензотриазол-1-іл)-N, N,N',N'-тетраHATU метилуронію HMTA гексаметилентетрамін HOAc оцтова кислота Реагент Лоусона 2,4-біс(4-метоксифеніл)-2,4-дитіоксо-1,3,2,4-дитіадифосфетан мл мілілітр(-и) хв. хвилина(-ни) MeOH метанол MsCl метансульфонілхлорид NBS N-бромсукцинімід комплекс дихлорид 1,1'-біс(дифенілфосфіно)фероцен-паладію(II) Pd(dppf)Cl2 дихлорметан Pd2(dba)3 трис(дибензиліденацетон)дипаладій(0) Pd(PPh3)4 тетракіс(трифенілфосфін)паладій(0) PPh3 трифенілфосфін ТГФ тетрагідрофуран Ti(ізо-OPr)4 ізопропілат титану(IV) Ксантфос 9-диметил-4,5-біс(дифенілфосфіно)ксантен 1 2 3 Синтез аміну (NH2CR R R в схемі I та II): Проміжна сполука A: 10 O HMTA / HOAc N N H (A-1) 15 20 N (A-2) N H Pd/C, H2 DPPA / DBU N N H (A-3) H2N N3 HO NaBH4 N N H (A-4) N H N (A) 1H-Піроло[2,3-b]піридин-3-карбальдегід (A-2) До розчину 1H-піролo[2,3-b]піридину (A-1) (7.23 г, 61.2 ммоль) в оцтовій кислоті (20 мл) та воді (40 мл) додавали HMTA (9.42 г, 67.3 ммоль). Реакційну суміш перемішували при 120 °C впродовж 6 год. Її охолоджували на льодяній бані, та одержуваний осад збирали та сушили з + одержанням зазначеної у заголовку сполуки (7.90 г) МС (m/z): 147 (M+1) . (1H-Піроло[2,3-b]піридин-3-іл)метанол (A-3) До розчину 1H-піролo[2,3-b]піридин-3-карбальдегіду (A-2) (5.0 г, 34.21 ммоль) в EtOH (150 мл) додавали NaBH4 (1.30 г, 34.21 ммоль). Реакційну суміш перемішували при кімнатній температурі впродовж 0.5 год. Її концентрували та очищали за допомогою хроматографії на + силікагелі з одержанням зазначеної у заголовку сполуки (5.0 г). МС (m/z): 149 (M+1) . 3-(Азидометил)-1H-піролo[2,3-b]піридин (A-4) 15 UA 107822 C2 5 10 До суміші 1H-піролo[2,3-b]піридин-3-іл)метанолу (A-3) (1.0 г, 6.75 ммоль) в безводному ТГФ (50 мл) додавали DPPA (3.71 г, 13.5 ммоль) та DBU (0.821 г, 5.4 ммоль) відповідно. Її нагрівали зі зворотним холодильником під N2 впродовж 6 год., та потім концентрували в вакуумі. Одержуваний залишок розчиняли в EtOAc (50 мл), промивали соляним розчином, сушили над сульфатом натрію та концентрували в вакуумі з одержанням сирого продукту. Сирий продукт очищали за допомогою хроматографії на силікагелі з одержанням зазначеної у заголовку + сполуки (0.587 г). МС (m/z): 174 (M+1) . (1H-Піроло[2,3-b]піридин-3-іл)метанамін (A) До суміші 3-(азидометил)-1H-піролo[2,3-b]піридину (A-4) (1.50 г, 8.63 ммоль) в EtOAc (150 мл) додавали 10 % Pd/C (1.10 г). Одержувану реакційну суміш перемішували під однією атмосферою H2 при кімнатній температурі впродовж 3 год. Суміш фільтрували, та фільтрат концентрували з одержанням зазначеної у заголовку сполуки (1.15 г). Проміжна сполука B: O O OH N NH 2NH 2 CH3 MgBr N Cl (B-1) Cl Boc2O Піридин N 15 20 25 30 35 40 45 boc (B-3) Br N3 NaN3 N N H N (B-5) N H (B-6) N N N H N (B-2) N N N (B-4) NH2 PPh3 ТГФ N HCl N N H (B) 1-(2-Хлорпіридин-3-іл)етанон (B-2) До розчину 2-хлорнікотинової кислоти (B-1) (7.88 г, 50.0 ммоль) в ТГФ (100 мл) по краплям при 0 °C додавали бромід метилмагнію (42 мл, 3M розчин в етиловому ефірі). Після завершення додавання, реакційну суміш перемішували при 0 °C впродовж 0.5 год. та потім при кімнатній температурі впродовж ночі. Реакційну суміш додавали в суміш лід/вода (150 мл), та екстрагували етилацетатом. Об'єднані органічні шари сушили над Na2SO4 та концентрували з одержанням зазначеної у заголовку сполуки, 1-(2-хлорпіридин-3-іл)етанону (B-2). МС (m/z): 156 + (M+1) . 3-Метил-1H-піразолопіролo[3,4-b]піридин (B-3) Розчин 1-(2-хлорпіридин-3-іл)етанону (B-2) (6 г, 38.6 ммоль) та гідразину (85 %, 9.1 г, 154.4 ммоль) в піридині (80 мл) перемішували при нагріванні зі зворотним холодильником впродовж ночі. Суміш охолоджували до кімнатної температури, концентрували, розбавляли водою (80 мл) та потім екстрагували етилацетатом (100 мл×3). Об'єднані органічні шари промивали соляним розчином, сушили над Na2SO4, та концентрували в вакуумі. Одержуваний залишок + використовували на наступній стадії без додаткового очищення. МС (m/z): 134 (M+1) . трет-Бутил 3-метил-1H-піразоло[3,4-b]піридин-1-карбоксилат (B-4) До розчину 3-метил-1H-піразоло[3,4-b]піридину (B-3) в EtOAc (300 мл) додавали (Boc)2O (16.4 г, 75 ммоль), DMAP (610 мг, 5 ммоль), та Et3N (10 г, 100 ммоль). Реакційну суміш перемішували при кімнатній температурі впродовж ночі. Розчинник видаляли в вакуумі, та залишок очищали за допомогою хроматографії на силікагелі з одержанням зазначеної у заголовку сполуки (5.3 г, 45.5 % за дві стадії). МС (m/z): 134. 3-(Бромметил)-1H-піразоло[3,4-b]піридин (B-5) До розчину трет-бутил 3-метил-1H-піразоло[3,4-b]піридин-1-карбоксилату (B-4) (699 мг, 3 ммоль) в CCl4 (15 мл) додавали NBS (641 мг, 3.6 ммоль) та AIBN (70 мг, 0.3 ммоль). Реакційну суміш перемішували при нагріванні зі зворотним холодильником впродовж ночі та потім фільтрували. Фільтрат промивали насиченим водним Na2CO3 (15 мл). Органічний шар сушили над Na2SO4 та концентрували з одержанням сирого продукту. Сирий продукт використовували + на наступній стадії без додаткового очищення. МС (m/z): 212 (M+1) . 3-(Азидометил)-1H-піразоло[3,4-b]піридин (B-6) Суміш 3-(бромметил)-1H-піразоло[3,4-b]піридину (B-5) та NaN3 (390 мг, 6 ммоль) в ДМФА (6 мл) перемішували при 80 °C впродовж 1.5 год. Потом суміш охолоджували до кімнатної 16 UA 107822 C2 5 10 температури, додавали воду (25 мл). Одержувану суміш екстрагували етилацетатом (40 мл×3). Об'єднані органічні шари промивали соляним розчином (40 мл) та сушили над Na 2SO4. Розчинник видаляли в вакуумі, та залишок очищали за допомогою хроматографії на силікагелі. Одержували тверду речовину (152 мг, 29.1 % за дві стадії). Хлорид (1H-піразоло[3,4-b]піридин-3-іл)метанамінію (B) Суміш 3-(азидометил)-1H-піразоло[3,4-b]піридину (B-6) (152 мг, 0.87 ммоль), PPh3 (465 мг, 1.74 ммоль) та 1 мл NH4OH в ТГФ (20 мл) перемішували при кімнатній температурі впродовж ночі. Розчин концентрували, та одержуваний залишок розчиняли в етилацетаті. Розчин обробляли 2M HCl, що приводило до випадання осадів. Осади збирали шляхом фільтрування з + одержанням зазначеної у заголовку сполуки (121 мг). МС (m/z): 149 (M+1) . Проміжна сполука C: O Cl N NH2 HS N O S CN N Cl S (C-3) N NH3.H2O 25 30 35 40 45 O LiAlH4 N OH S (C-4) NH2 S (C-5) 20 O O S 15 N NaNO2 / H3PO2 (C-2) (C-1) SOCl2 O (C) Метил 3-амінотієно[3,2-b]піридин-2-карбоксилат (C-2) До суміші 3-хлорпіридин-2-карбонітрилу (C-1) (1.01 г, 7.29 ммоль) та K2CO3 (1.10 г, 7.96 ммоль) в ДМФА (10 мл) та воді (1 мл) по краплям додавали метилтіогліколят (0.709 мл, 7.93 ммоль). Реакційну суміш перемішували при 40 °C впродовж 3 год. Суміш гасили холодною водою (70 мл) та поміщали на лід для покращення виділення осаду. Осад збирали шляхом + фільтрування з одержанням зазначеної у заголовку сполуки. МС (m/z): 209 (M+1) . Метил тієно[3,2-b]піридин-2-карбоксилат (C-3) До розчину метил 3-амінотієно[3,2-b]піридин-2-карбоксилату (C-2) (930 мг, 4.47 ммоль) в гіпофосфористій кислоті (35 мл), охолодженому на льодяній бані, додавали нітрит натрію (620 мг, 8.98 ммоль) в мінімальній кількості води. Реакційну суміш перемішували впродовж 3 год. на льодяній бані, та потім pH встановлювали на значення приблизно 7.0 за допомогою 30 % водного розчину гідроксиду натрію. Одержувану суміш екстрагували EtOAc. Об'єднані органічні шари сушили та концентрували з одержанням зазначеної у заголовку сполуки. МС (m/z): 194 + (M+1) . Тієно[3,2-b]піридин-2-ілметанол (C-4) До розчину метил тієно[3,2-b]піридин-2-карбоксилату (C-3) (600 мг, 3.1 ммоль) в 30 мл безводного ТГФ при 0 °C впродовж 20 хвилин по краплям додавали LiAlH4 (472 мг, 12.4 ммоль) в безводному ТГФ (25 мл). Реакційну суміш перемішували при 0 °C впродовж 30 хвилин. Додавали MeOH та одержувану суміш очищали за допомогою хроматографії з одержанням + зазначеної у заголовку сполуки. МС (m/z): 166 (M+1) . 2-(Хлорметил)тієно[3,2-b]піридин (C-5) До розчину тієно[3,2-b]піридин-2-ілметанолу (C-4) (17 мг, 0.1 ммоль) в безводному дихлорметані (10 мл) додавали SOCl2 (120 мг). Потім суміш перемішували при кімнатній температурі впродовж 2 годин, її концентрували та використовували на наступній стадії без + додаткового очищення. МС (m/z): 184 (M+1) . Тієно[3,2-b]піридин-2-ілметанамін (C) 2-(Хлорметил)тієно[3,2-b]піридин (C-5) (183 мг, 1 ммоль) розчиняли в NH3/метанол (7 н., 10 мл). Одержувану суміш перемішували при 50 °C впродовж 16 годин та концентрували. Залишок + очищали за допомогою хроматографії. МС (m/z): 165 (M+1) . Проміжні сполуки D та D’ Метил тієно[3,2-c]піридин-2-карбоксилат (D-2) До розчину 4-хлорпіридин-3-карбоксальдегіду (D-1) (1.4 г, 10 ммоль), розчиненого в ДМФА (10 мл) та воді (1 мл) частинами додавали K 2CO3 (1.66 г, 12 ммоль) та метилтіогліколят (1.07 мл, 12 ммоль). Реакційну суміш перемішували при 45 °C впродовж ночі та потім гасили 17 UA 107822 C2 5 холодною водою. Колбу поміщали на лід для покращення виділення осаду. Осад збирали шляхом фільтрування та сушили на повітрі з одержанням зазначеної у заголовку сполуки (1.23 + г). МС (m/z): 194 (M+1) . Тієно[3,2-c]піридин-2-ілметанол (D-3) До розчину метил тієно[3,2-c]піридин-2-карбоксилату (D-2) (15 г, 77.6 ммоль) в безводному ТГФ (250 мл) при 0 °C частинами додавали LiAlH4 (4.42 г, 116.4 ммоль). Суспензію перемішували при 0 °C впродовж 1 год. та потім гасили шляхом додавання насиченого водного NH4Cl та фільтрували. Фільтрат промивали соляним розчином та концентрували. Залишок використовували на наступній стадії без будь-якого додаткового очищення (10.3 г). 10 O O Cl HS O O N N S LiAlH 4 S (D'-1) O S S (D) N N S O (D'-2) N (D') 25 30 35 40 OH (D'-4) (D'-3) S 20 S O N 15 NH 2 N (D-4) N O N PPh3 S S (D-3) OH N N3 N DPPA / DBU O (D-2) (D-1) OH N NH 2 S N3 (D'-5) 2-(Азидометил)тієно[3,2-c]піридин (D-4) До висушеної полум'ям круглодонної колби, що містить тієно[3,2-c]піридин-2-ілметанол (D-3) (3.2 г, 19.4 ммоль) додавали DPPA (8 г, 6.26 мл, 29.1 ммоль) в ТГФ (50 мл). Реакційну суміш перемішували впродовж 5 хвилин та охолоджували до 0 °C з наступним додаванням DBU (4.43 г, 4 мл, 29.1 ммоль) за допомогою шприця. Суміші дозволяли перемішуватися при нагріванні зі зворотним холодильником впродовж ночі. Реакційну суміш потім розподіляли між водою та етиловим ефіром. Водний шар екстрагували етиловим ефіром. Об'єднані органічні шари промивали соляним розчином, сушили над Na2SO4, концентрували, та очищали за допомогою + хроматографії з одержанням продукту (3.27 г). МС (m/z): 191 (M+1) . Гідрохлорид тієно[3,2-c]піридин-2-ілметанаміну (D) До розчину 2-(азидометил)тієно[3,2-c]піридину (D-4) (3 г, 15.8 ммоль) в безводному ТГФ (50 мл) додавали Ph3P (8.27 г, 31.5 ммоль) з наступним додаванням NH4OH (2 мл). Розчин перемішували при кімнатній температурі впродовж ночі. Розчинник видаляли, та залишок очищали за допомогою хроматографії з одержанням зазначеної у заголовку сполуки (2.5 г). Тієно[3,2-c]піридин-2-карбонова кислота (D’-1) До розчину метил тієно[3,2-c]піридин-2-карбоксилату (D-2) (12 г, 62.1 ммоль) в MeOH (150 мл) та H2O (15 мл) додавали LiOH.H2O (5.2 г, 124.2 ммоль). Розчин перемішували при кімнатній температурі впродовж ночі, та потім підкисляли 1 н. водною HCl. Одержуваний білий осад збирали шляхом фільтрування та сушили на повітрі з одержанням зазначеної у заголовку + сполуки. МС (m/z): 179 (M) . N-Метокси-N-метилтієно[3,2-c]піридин-2-карбоксамід (D’-2) До розчину тієно[3,2-c]піридин-2-карбонової кислоти (D’-1) (11.5 г, 64.2 ммоль) в ДХМ (200 мл) та ДМФА (50 мл) додавали Et3N (19.5 г, 26.6 мл, 192.6 ммоль) з наступним додаванням HATU (36.6 г, 96.3 ммоль). Реакційний розчин перемішували при кімнатній температурі впродовж 20 хвилин, та потім обробляли гідрохлоридом N,O-диметилгідроксиламіну (6.9 г, 70.6 ммоль). Перемішування продовжували впродовж ночі при кімнатній температурі. Розчинник видаляли. Залишок розчиняли в EtOAc та промивали водою та соляним розчином. Органічний шар сушили та концентрували. Залишок очищали за допомогою хроматографії на силікагелі з + одержанням зазначеної у заголовку сполуки. МС (m/z): 223 (M+1) . 18 UA 107822 C2 5 10 15 1-(Тієно[3,2-c]піридин-2-іл)етанон (D’-3) До розчину N-метокси-N-метилтієно[3,2-c]піридин-2-карбоксаміду (D’-2) (11.1 г, 50 ммоль) в безводному ТГФ (150 мл) додавали MeMgBr (3M в етиловому ефірі, 25 мл, 75 ммоль) при 0 °C під N2. Реакційній суміші дозволяли нагрітися до температури оточуючого середовища та перемішували впродовж ночі. Для гасіння реакції додавали насичений водний розчин NH 4Cl. Одержувану суміш потім екстрагували за допомогою EtOAc. Об'єднані органічні шари сушили над Na2SO4, фільтрували, та концентрували з одержанням зазначеної у заголовку сполуки. МС + (m/z): 178 (M+1) . 1-(Тієно[3,2-c]піридин-2-іл)етанол (D’-4) До розчину 1-(тієно[3,2-c]піридин-2-іл)етанону (D’-3) (3.5 г, 1 ммоль) в безводному ТГФ (50 мл) частинами при 0 °C додавали LiAlH4 (1.13 г, 1.5 ммоль). Суспензію перемішували при цій температурі впродовж 1 год. Реакційну суміш гасили насиченим водним розчином NH 4Cl та фільтрували. Фільтрат промивали соляним розчином, концентрували, та потім використовували на наступній стадії без будь-якого додаткового очищення. 1-(Тієно[3,2-c]піридин-2-іл)етанамін (D") Проміжну сполуку D" одержували із 1-(тієно[3,2-c]піридин-2-іл)етанолу (D’-4) дотримуючись подібних методик синтезу проміжної сполуки A із A-3, як описано вище. Проміжна сполука E: O NaBH4 S N H 2SO4 O MeOH (F-1) (E) (E-3) O O S HNO3 (F-2) N N O S O (F-5) O2 N H2SO4 O S Ni Ренея H N N NaBH4 O Ac2O / i-BuNO2 O (F-4) H N N DPPA / DBU H N N PPh3/NH3.H2O S S S LiAlH4 H2 N S O (F-3) O 40 S N Тієно[2,3-b]піридин-2-ілметанол (E-2) E-2 одержували із тієно[2,3-b]піридин-2-карбальдегіду (E-1) дотримуючись подібних методик + синтезу проміжної сполуки A-3 із A-2, як описано вище. МС (m/z): 166 (M+1) . Тієно[2,3-b]піридин-2-ілметанамін(E) Проміжну сполуку E одержували із тієно[2,3-b]піридин-2-ілметанолу (E-2) дотримуючись + подібних методик синтезу проміжної сполуки C із C-4, як описано вище. МС (m/z): 165 (M+1) . Проміжна сполука F: S 35 N NH3.H2O S N (E-2) OH 30 Cl SOCl 2 S N (E-1) 20 25 O OH N3 (F-6) (F-7) NH2 ClH (F) Метил 5-метилтіофен-2-карбоксилат (F-2) До розчину 5-метилтіофен-2-карбонової кислоти (F-1) (14.0 г, 0.1 моль) в MeOH (250 мл) додавали концентровану H2SO4 (2.0 мл). Реакційну суміш перемішували при нагріванні зі зворотним холодильником впродовж 60 год. Розчинник видаляли в вакуумі. Додавали етилацетат для розбавлення реакційної суміші. Потім органічний розчин промивали насиченим водним розчином Na2CO3, та сушили над Na2SO4. Розчинник видаляли з одержанням зазначеної у заголовку сполуки (13.4 г). Метил 5-метил-4-нітротіофен-2-карбоксилат (F-3) Розчин концентрованої HNO3 (7.2 мл, 111.5 ммоль) в концентрованій H2SO4 (20 мл) додавали по краплям до розчину метил 5-метилтіофен-2-карбоксилату (F-2) (13.4 г, 86.0 ммоль) в концентрованій H2SO4 (30 мл) при 0 °C. Реакційну суміш перемішували при 0 °C впродовж 30 19 UA 107822 C2 5 10 15 20 25 30 35 хвилин та виливали в суміш лід-вода. Осад відфільтровували та промивали водою. Тверду речовину збирали як продукт (14.8 г). Метил 4-аміно-5-метилтіофен-2-карбоксилат (F-4) До розчину метил 5-метил-4-нітротіофен-2-карбоксилату (F-3) (14.8 г, 73.6 ммоль) в MeOH/ТГФ (1:1, 300 мл) додавали Ni Ренея. Реакційну суміш вакуумували та тричі заповнювали воднем, та потім перемішували при кімнатній температурі впродовж 36 год. при тиску водню 1 атмосфера. Ni Ренея відфільтровували, та фільтрат концентрували. Залишок обробляли водною HCl (1 н., 150 мл) та фільтрували. Фільтрат обробляли водним NaOH (1 н.) до приведення pH до значення приблизно 8-9. Потім суміш екстрагували етилацетатом. Об'єднані органічні шари сушили над Na2SO4, та розчинник видаляли з одержанням зазначеної у заголовку сполуки (8.1 г). Метил 1-ацетил-1H-тієно[3,2-c]піразол-5-карбоксилат (F-5) До розчину метил 4-аміно-5-метилтіофен-2-карбоксилату (F-4) (5.1 г, 30 ммоль) в толуолі (120 мл) додавали оцтовий ангідрид (16.0 г, 0.12 моль) та ацетат калію (1.5 г, 15.1 ммоль). Реакційну суміш перемішували при 100 °C впродовж 3 год. Після охолодження до кімнатної температури, реакційну суміш обробляли ізобутилнітритом (10.5 г, 90.0 ммоль), та потім перемішували при 100 °C впродовж ночі. Додавали воду, та потім суміш екстрагували етилацетатом. Об'єднані органічні шари промивали соляним розчином, сушили над Na 2SO4 та концентрували. Залишок очищали за допомогою хроматографії, елююючи Pet/EtOAc=10/1 з одержанням зазначеної у заголовку сполуки (5.3 г) як продукт. (1H-Тієно[3,2-c]піразол-5-іл)метанол (F-6) До розчину метил 1-ацетил-1H-тієно[3,2-c]піразол-5-карбоксилату (F-5) (4.5 г, 20.0 ммоль) в MeOH (30 мл) повільно додавали NaBH4 (836 мг, 22.0 ммоль). Суміш перемішували при кімнатній температурі впродовж 30 хвилин, та потім концентрували. Залишок розчиняли в безводному ТГФ (80 мл) та потім при 0 °C повільно додавали LiAlH4 (1.5 г, 40.0 ммоль). Реакційну суміш перемішували при 0 °C впродовж 30 хв. Водний розчин NH4Cl додавали по краплям для гасіння реакції. Одержувану суміш фільтрували, та фільтрат екстрагували етилацетатом. Об'єднані органічні шари промивали соляним розчином, сушили над Na 2SO4, та концентрували в вакуумі з одержанням зазначеної у заголовку сполуки (2.9 г). Хлорид (1H-тієно[3,2-c]піразол-5-іл)метанамінію (F) Проміжну сполуку F одержували із (1H-тієно[3,2-c]піразол-5-іл)метанолу (F-6) дотримуючись подібних методик синтезу проміжної сполуки D із D-3, як описано вище. Проміжна сполука G та G": 1H-Тієно[3,2-c]піразол-5-карбонова кислота (G-1) До розчину метил 1-ацетил-1H-тієно[3,2-c]піразол-5-карбоксилату (F-5) (4.9 г, 21.8 ммоль) в MeOH (15 мл) додавали водний розчин KOH (6 н., 10 мл). Реакційну суміш перемішували при кімнатній температурі впродовж 2 год., та потім концентрували в вакуумі. Додавали водну HCl (6 н.) до приведення pH до значення 5-6. Осади збирали шляхом фільтрування з одержанням зазначеної у заголовку сполуки (3.0 г). 40 20 UA 107822 C2 O водн. NaOH N N O O S N O N N O HO O S (G'-3) PPh3 / NH3 N N3 S ClH N N H2 N S (G) (G-5) (G-4) ClH N O N DPPA / DBU S N 25 (G-2) N (G-3) Br 20 S O N LiAlH4 S 15 H2SO4 / MeOH (G-1) O 10 N O S HO (F-5) 5 H N H N N LiAlH4 N HO N DPPA / DBU S N N3 S (G'-5 ) (G'-4) N N PPh3 / NH3 H2 N S (G') Метил 1H-тієно[3,2-c]піразол-5-карбоксилат (G-2) До розчину 1H-тієно[3,2-c]піразол-5-карбонової кислоти (G-1) (3.0 г, 17.9 ммоль) в MeOH (50 мл) додавали концентровану H2SO4 (0.3 мл). Реакційну суміш перемішували при нагріванні зі зворотним холодильником впродовж 60 год. Розчинник видаляли в вакуумі. Для розбавлення суміші додавали етилацетат. Суміш промивали водним розчином NaHCO3, сушили над Na2SO4, та концентрували в вакуумі з одержанням зазначеної у заголовку сполуки (2.4 г). Метил 2-етил-2H-тієно[3,2-c]піразол-5-карбоксилат (G-3) та метил 1-етил-1H-тієно[3,2c]піразол-5-карбоксилат (G’-3) До розчину метил 1H-тієно[3,2-c]піразол-5-карбоксилату (G-2) (760 мг, 4.2 ммоль) в ДМФА (4 мл) додавали брометан (915 мг, 8.3 ммоль) та K2CO3 (1.7 г, 12.6 ммоль). Реакційну суміш перемішували при 110 °C впродовж 3 год. в запаяній трубці. Після охолодження до кімнатної температури, суміш концентрували та очищали за допомогою хроматографії з одержанням двох продуктів: + Метил 2-етил-2H-тієно[3,2-c]піразол-5-карбоксилат (351 мг) (G-3). МС (m/z): 211 (M+1) . + Метил 1-етил-1H-тієно[3,2-c]піразол-5-карбоксилат (272 мг) (G’-3). МС (m/z): 211 (M+1) . Хлорид (2-етил-2H-тієно[3,2-c]піразол-5-іл)метанамінію (G) Проміжну сполуку G одержували із метил 2-етил-2H-тієно[3,2-c]піразол-5-карбоксилату (G-3) дотримуючись подібних методик синтезу проміжної сполуки D із D-2, як описано вище. МС (m/z): + 182 (M+1) . Хлорид (1-етил-1H-тієно[3,2-c]піразол-5-іл)метанаміну (G") Проміжну сполуку G" одержували із метил 1-етил-1H-тієно[3,2-c]піразол-5-карбоксилату (G’3) дотримуючись подібних методик синтезу проміжної сполуки D із D-2, як описано вище. МС + (m/z): 182 (M+1) . 21 UA 107822 C2 Проміжна сполука H та H": NH 3.H 2O O O N H N O H2 N (H-1) LiAlH4 N N HO N 10 15 20 25 SEM PPh3/NH3.H2O DPPA/DBU N N (H) N3 SEM (H'-1) 5 N H H2 N (H-2) O O LiAlH 4 N N H (H'-2) N SEM N H2 N N N SEM (H') (H'-3) 1H-Піролo[2,3-b]піридин-2-карбоксамід (H-2) До розчину метил 1H-піролo[2,3-b]піридин-2-карбоксилату (H-1) (880 мг, 5.0 ммоль) в MeOH (2 мл) додавали NH3.H2O (6 мл). Реакційний розчин нагрівали при 80 °C впродовж ночі. Після охолодження до кімнатної температури, суміш концентрували в вакуумі з одержанням зазначеної у заголовку сполуки (805 мг) у вигляді жовтої твердої речовини, яку використовували + на наступній стадії без додаткового очищення. МС (m/z): 162 (M+1) . (1H-Піролo[2,3-b]піридин-2-іл)метанамін (H) До розчину 1H-піролo[2,3-b]піридин-2-карбоксаміду (H-2) (805 мг, 5.0 ммоль) в сухому ТГФ (10 мл) при 0 °C під 1 атм N2 повільно додавали LiAlH4 (570 мг, 15 ммоль). Суміш перемішували при 80 °C впродовж ночі. Суміш потім охолоджували до 0 °C, концентрували, та потім очищали за допомогою хроматографії на силікагелі з одержанням зазначеної у заголовку сполуки (720 + мг). МС (m/z): 148 (M+1) . 1 Метил 1-((2-(триметилсиліл)етокси)метил)- H-піролo[2,3-b]піридин-2-карбоксилат (H’-1) До розчину метил 1H-піролo[2,3-b]піридин-2-карбоксилату (H-1) (528 мг, 3 ммоль) в сухому ТГФ (5 мл) при 0 °C додавали NaH (240 мг, 6 ммоль). Реакційну суміш перемішували впродовж 0.5 год. під N2, та потім по краплям додавали SEMCl (526 мг, 3 ммоль). Суміш перемішували при кімнатній температурі впродовж 2 год. Для гасіння реакції додавали H 2O. Одержувану суміш екстрагували EtOAc. Органічний шар сушили над Na 2SO4, та концентрували з одержанням зазначеної у заголовку сполуки (750 мг), яку використовували на наступній стадії без очищення. + МС (m/z): 307 (M+1) . (1-((2-(Триметилсиліл)етокси)метил)-1H-піролo[2,3-b]піридин-2-іл)метанамін (H") 1 Проміжну сполуку H" одержували із метил 1-((2-(триметилсиліл)етокси)метил)- H-піролo[2,3b]піридин-2-карбоксилату (H’-1) дотримуючись подібних методик синтезу проміжної сполуки D із + D-2, як описано вище. МС (m/z): 278 (M+1) . Проміжна сполука I: 30 N O O N H (I-1) 35 NH3.H2O N O H2N N H (I-2) N LiAlH4 H2N N H (I) (1H-Піролo[3,2-b]піридин-2-іл)метанамін (I) Проміжну сполуку I одержували із метил 1H-піролo[3,2-b]піридин-2-карбоксилату (I-1) дотримуючись подібних методик синтезу проміжної сполуки H, як описано вище. МС (m/z): 148 + (M+1) . 22 UA 107822 C2 Проміжна сполука J: S 1. Sn / ZnCl2 NO2 S N O 2. (J-1) O Br Br2 O (J-2) S N NaHCO3 / MgSO4 K2HPO4 (J-3) O CN CuCN / Pd(PPh3)4 N Ni Ренея N S (J) (J-4) 5 10 15 20 25 30 Тієно[2,3-b]піридин(J-2) До енергійно перемішуваної суміші 2-нітротіофену (J-1) (13 г, 0.1 моль) та концентрованої соляної кислоти (195 мл) при 0 °C додавали олово (25 г). Після того, як більша частина олова була розчинена, додавали EtOH (70 мл) та безводний ZnCl2 (6 г). Суміш нагрівали до 85 °C, та потім обробляли біс(діетилацеталем) малональдегіду (17.2 г, 0.078 моль) в EtOH (30 мл). Одержувану реакційну суміш витримували при 85 °C впродовж 1 год., потім виливали на лід (100 г), підлуговували за допомогою NH3.H2O, та екстрагували ДХМ (75 млx3). Об'єднані органічні шари концентрували та очищали за допомогою хроматографії на силікагелі з + одержанням зазначеної у заголовку сполуки. МС (m/z): 135 (M) . 3-Бромтієно[2,3-b]піридин (J-3) Бром (2.08 г, 13 ммоль) додавали по краплям до суміші тієно[2,3-b]піридину (J-2) (1.35 г, 10 ммоль), дикалію моногідроортофосфату (940 мг, 5.4 ммоль), бікарбонату натрію (840 10 ммоль), та сульфату магнію (2.0 г, 16.7 ммоль) в хлороформі (40 мл), яку перемішували при нагріванні зі зворотним холодильником впродовж 16 год., одержувану суміш перемішували при нагріванні зі зворотним холодильником впродовж 24 год., потім фільтрували та промивали за допомогою + ДХМ. Фільтрат концентрували, та очищали за допомогою хроматографії. МС (m/z): 214 (M+1) . Тієно[2,3-b]піридин-3-карбонітрил (J-4) До перемішуваного розчину 3-бромтієно[2,3-b]піридину (J-3) (107 мг, 0.5 ммоль) та CuCN (60 мг, 0.67 ммоль) в безводному ДМФА(4 мл) додавали Pd(PPh3)4 (57 мг, 0.05 ммоль). Реакційну суміш вакуумували з використанням азоту та перемішували при 120 °C впродовж 5 год. Потім охолоджену суміш концентрували та очищали за допомогою хроматографії з одержанням + зазначеної у заголовку сполуки. МС (m/z): 161 (M+1) . Тієно[2,3-b]піридин-3-ілметанамін (J) До розчину тієно[2,3-b]піридин-3-карбонітрилу (J-4) (320 мг, 2 ммоль) в NH3.EtOH (25 мл) додавали Ni Ренея (приблизно 300 мг). Реакційну суміш вакуумували з використанням водню та перемішували при кімнатній температурі впродовж 2 год. Потім суміш фільтрували, та фільтрат концентрували з одержанням зазначеної у заголовку сполуки, яку використовували на наступній + стадії без очищення. МС (m/z): 165 (M+1) . Проміжна сполука K: NC Cl N NH2 35 40 S N (K-1) O NC Ni Ренея / H2 N H2 N N N N (K-2) (K) H-Імідазо[1,2-a]піридин-6-карбонітрил (K-2) До розчину 6-амінонікотинонітрилу (K-1) (4.0 г, 33.6 ммоль) в безводному EtOH (160 мл) додавали 2-хлорацетальдегід (40 % в H2O, 27.5 мл, 168 ммоль). Реакційну суміш нагрівали зі зворотним холодильником впродовж 4 год., та потім концентрували. Одержуваний залишок розчиняли в воді та pH встановлювали на значення > 7 насиченим розчином NaHCO 3. Осад збирали та сушили з одержанням зазначеної у заголовку сполуки (4.80 г). (H-Імідазо[1,2-a]піридин-6-іл)метанамін (K) 23 UA 107822 C2 Проміжну сполуку K одержували із H-імідазо[1,2-a]піридин-6-карбонітрилу дотримуючись подібних методик синтезу проміжної сполуки J із J-4, як описано вище. Проміжна сполука L: (K-2) O N NC O NC N 10 15 20 25 (L-1) N (L) (L-2) [1,2,4]триазоло[1,5-a]піридин-6-карбонітрил (L-2) До перемішуваного розчину 6-амінонікотинонітрилу (L-1) (8.7 г, 73 ммоль) в ДМФА (35 мл) додавали диметилацеталь N, N-диметилформаміду (35 мл, 294 ммоль). Реакційну суміш нагрівали до 130 °C впродовж ночі. Після охолодження до кімнатної температури, леткі речовини видаляли при зниженому тиску з одержанням цільової проміжної сполуки, N'-(5ціанопіридин-2-іл)-N, N-диметилформамідину. До охолодженого льодом, перемішуваного розчину вищезгаданого продукту в метанолі (200 мл) та піридині (11.5 мл, 143 ммоль) додавали гідроксиламін-O-сульфонову кислоту (11.3 г, 100 ммоль). Реакційній суміші дозволяли нагрітися до кімнатної температури та перемішували впродовж ночі. Потім леткі речовини видаляли при зниженому тиску, та залишок розподіляли між водним розчином бікарбонату натрію та етилацетатом. Водний шар додатково екстрагували етилацетатом. Об'єднані органічні шари промивали послідовно водою та соляним розчином, сушили над безводним Na2SO4, фільтрували, та концентрували. Одержуваний залишок очищали за допомогою хроматографії на силікагелі з одержанням зазначеної у заголовку + сполуки (5.5 г). МС (m/z): 145 (M+1) . [1,2,4]Триазоло[1,5-a]піридин-6-ілметанамін (L) Проміжну сполуку L одержували із [1,2,4]триазоло[1,5-a]піридин-6-карбонітрилу (L-2) дотримуючись подібних методик синтезу проміжної сполуки J із J-4, як описано вище. Проміжна сполука M: NC N Ni Ренея N H 2N N N N N (M-1) 30 N N H2 N N NH2 5 Ni Ренея N N (M) Піразоло[1,5-a]піримідин-5-ілметанамін (M) Проміжну сполуку M одержували із піразоло[1,5-a]піримідин-5-карбонітрилу (M-1) дотримуючись подібних методик синтезу проміжної сполуки J із J-4, як описано вище. МС (m/z): + 149 (M+1) . Проміжна сполука N: N N (N) 35 Проміжну сполуку N одержували із хінолін-6-карбонової кислоти, як описано в US2007/ 0265272. Проміжна сполука O: 40 O O C2Cl2O2 HO O NH3 Cl N N (O-1) (CF3CO)2O N H2N (O-2) N (O-3) 24 Ti(i-OPr)4 H2N N N (O-4) (O) UA 107822 C2 5 10 15 20 25 Хінолін-6-карбонілхлорид (O-2) До суміші хінолін-6-карбонової кислоти (O-1) (2.0 г, 11.5 ммоль) в CH 2Cl2 (250 мл) додавали 3 краплі ДМФА при 0 °C, з наступним додаванням по краплям оксалілхлориду (7.3 г, 57.5 ммоль). Одержувану реакційну суміш перемішували при кімнатній температурі впродовж ночі, та потім концентрували з одержанням зазначеної у заголовку сполуки (2.2 г). Хінолін-6-карбоксамід (O-3) До розчину хінолін-6-карбонілхлориду (O-2) (2.2 г, 10.5 ммоль) в ТГФ (100 мл) при 0 °C додавали аміак (5 мл). Суміш перемішували при кімнатній температурі впродовж 1 год., потім концентрували та промивали водою (15 мл) з одержанням зазначеної у заголовку сполуки (1.5 + г). МС (m/z): 173 (M+1) . Хінолін-6-карбонітрил (O-4) До суміші хінолін-6-карбоксаміду (O-3) (1.2 г, 7.2 ммоль) та триетиламіну (2.2 г, 21.8 ммоль) в ДХМ (50 мл) при 0 °C додавали ангідрид трифтороцтової кислоти (1.9 г, 8.9 ммоль). Реакційну суміш перемішували впродовж 10 хв при 0 °C, потім гасили водою. Одержувану суміш екстрагували за допомогою ДХМ. Органічний шар сушили над безводним Na2SO4, та концентрували з одержанням цільової, зазначеної у заголовку сполуки (1.0 г). МС (m/z): 154 + (M) . 1-(Хінолін-6-іл)циклопропанамін (O) Етилбромід магнію (7.7 ммоль, 3 M в етиловому ефірі) додавали до розчину хінолін-6карбонітрилу (O-4) (540 мг, 3.5 ммоль) та Ti(Oізо-Pr)4 (3.9 ммоль, 1.16 мл) в Et2O (15 мл) при 70 °C. Одержуваний жовтий розчин перемішували впродовж 10 хв, нагрівали до кімнатної температури впродовж 1.5 год., та потім обробляли BF 3.OEt2 (7 ммоль, 0.88 мл). Одержувану суміш перемішували впродовж 1 год. Потім додавали 1 н. водну HCl (11 мл) та етиловий ефір (40 мл) з наступним додаванням NaOH (10 % водн., 30 мл). Суміш екстрагували етиловим ефіром. Об'єднані шари етилового ефіру сушили над безводним Na 2SO4, фільтрували, та концентрували в вакуумі з одержанням сирої, зазначеної у заголовку сполуки, яку + використовували на наступній стадії без додаткового очищення. МС (m/z): 185 (M+1) . Проміжна сполука P F N N F F OH Br HO F NH2 (P-1) OH Br CuCN 35 40 45 H2, Ni Ренея N FeSO4,H2SO4 N Br F (P-2) H2 N NH3, EtOH N H2 N NC F 30 NC N (P-3) F (P) 6-Бром-7-фторхінолін та 6-бром-5-фторхінолін (P-2) Суміш 4-бром-3-фтораніліну (P-1) (5.7 г, 30 ммоль), пропан-1,2,3-триолу (11.04 г, 120 ммоль), FeSO4.7H2O (1.92 г, 6.9 ммоль), та нітробензолу (2.22 г, 18 ммоль) перемішували при кімнатній температурі впродовж 10 хв, потім додавали концентровану H2SO4 (9.7 г, 9.9 ммоль). Одержувану суміш перемішували при нагріванні зі зворотним холодильником впродовж 7 год. Після охолодження до кімнатної температури, реакційну суміш виливали в воду, підлуговували за допомогою NH3.H2O до pH приблизно 8, та екстрагували за допомогою ДХМ. Концентрований органічний шар очищали за допомогою хроматографії на силікагелі (елююючи сумішшю Pet/EtOAc=15/1) з одержанням зазначеної в заголовку суміші сполук. 6.78 г. МС (m/z): 226 + (M+1) . (7-Фторхінолін-6-іл)метанамін та (5-фторхінолін-6-іл)метанамін (P) Ці сполуки одержували із 6-бром-7-фторхіноліну та 6-бром-5-фторхіноліну (P-2) дотримуючись подібних методик синтезу Проміжної сполуки J із J-3, як описано вище. МС (m/z): + 177 (M+1) . 25 UA 107822 C2 Проміжна сполука Q: Cl KSCN / Br2 N Cl N Na2SO3 S NH2 N NH2 (Q-1) NC N N H2 N 15 20 25 30 35 N S N (Q-4) S (Q) 5-Хлортіазоло[5,4-b]піридин-2-амін (Q-2) До льодяної оцтової кислоти (125 мл), попередньо охолодженої до 5 °C додавали тіоціанат калію (93 г, 961 ммоль) та 6-хлорпіридин-3-амін (Q-1) (15 г, 117 ммоль). Суміш поміщали в охолодну суміш льоду та солі, та перемішували, поки додавали 10 мл брому в льодяній оцтовій кислоті (30 мл) із краплинної лійки при такій швидкості, що температура ніколи не піднімалася вище 0 °C. Після того, як був доданий весь бром, розчин перемішували впродовж додаткових 2 год. при 0 °C та при кімнатній температурі впродовж ночі. Швидко додавали воду (60 мл), та завись, витримували при 90 °C, фільтрували в гарячому стані. Жовтогарячий осад на фільтрі поміщали в реакційну колбу. До колби додавали льодяну оцтову кислоту (60 мл). Суміш в колбі витримували при 85 °C, та фільтрували в гарячому стані ще раз. Об'єднані фільтрати охолоджували та нейтралізували концентрованим розчином аміаку до pH 6. Осад збирали у + вигляді зазначеної у заголовку сполуки (19 г). МС (m/z): 186 (M+1) . 3-Аміно-6-хлорпіридин-2-тіол (Q-3) 5-Хлортіазоло[5,4-b]піридин-2-амін (Q-2) (19 г, 103 ммоль), що містить сульфіт натрію (2 г) нагрівали зі зворотним холодильником в 20 % водному розчині гідроксиду натрію (150 мл) впродовж ночі. Тверді речовини повністю розчинялися через 1 год., потім суміш охолоджували до кімнатної температури. Розчин нейтралізували мурашиною кислотою. Осад збирали шляхом фільтрування у вигляді зазначеної у заголовку сполуки (16.4 г). 5-Хлортіазоло[5,4-b]піридин (Q-4) 3-Аміно-6-хлорпіридин-2-тіол (Q-3) (16.4 г, 103 ммоль) в мурашиній кислоті (80 мл) нагрівали зі зворотним холодильником при 110 °C впродовж 2 год. Реакційну суміш охолоджували та нейтралізували концентрованим аміаком до pH 7. Осад збирали шляхом фільтрування у вигляді + зазначеної у заголовку сполуки (14.5 г). МС (m/z): 171 (M+1) . Тіазоло[5,4-b]піридин-5-карбонітрил (Q-5) До 8 мл пробірки з кришкою, що загвинчується, обладнаної якорем магнітної мішалки, додавали 5-хлортіазоло[5,4-b]піридин (Q-4) (460 мг, 2.7 ммоль), Zn(CN)2 (316 мг, 2.7 ммоль), Pd2(dba)3 (123 мг, 0.13 ммоль), DPPF (150 мг, 0.27 ммоль) та ДМФА (5 мл, вологий, що містить 1 % H20). Пробірку продували азотом, потім закривали кришкою. Суміш перемішували при 120 °C впродовж ночі, та потім концентрували в вакуумі. Одержуваний залишок очищали за допомогою хроматографії на силікагелі з одержанням зазначеної у заголовку сполуки (151 мг). Тіазоло[5,4-b]піридин-5-ілметанамін (Q) Проміжну сполуку Q одержували із тіазоло[5,4-b]піридин-5-карбонітрилу (Q-5) дотримуючись + подібних методик синтезу проміжної сполуки J із J-4, як описано вище. МС (m/z): 166 (M+1) . Проміжна сполука R: O Cl O Cl Cl O N N NH2 (R-1) N N H Реагент Лоусона O S O N (R-4) OH N N O O (R-3) S DPPA, DBU O N N (R-2) S 40 Cl N (Q-5) 10 HCO2 H NH2 N Zn(CN)2 / DPPF SH (Q-3) Ni Ренея S N NaOH (Q-2) Pd 2(dba)3 5 Cl Pd/C, H2 S N N3 (R-5) N (R) 26 NH2 NaBH4 UA 107822 C2 5 10 15 20 25 Етил 2-(4-хлорпіридин-3-іламіно)-2-оксоацетат (R-2) До розчину 4-хлорпіридин-3-аміну (R-1) (5 г, 38.9 ммоль) в ТГФ (100 мл) додавали Et3N (4.72 г, 6.5 мл, 46.7 ммоль), з наступним додаванням по краплям етил 2-хлор-2-оксоацетату (5.84 г, 4.78 мл, 42.8 ммоль) в ТГФ (5 мл) при 0 °C. Одержувану суміш перемішували при кімнатній температурі впродовж 1 год., та потім концентрували в вакуумі. Одержуваний залишок розчиняли в EtOAc, та промивали водним насиченим NaHCO 3. Органічний шар відокремлювали, сушили над Na2SO4, та концентрували з одержанням зазначеної у заголовку сполуки, яку використовували на наступній стадії без додаткового очищення. МС (m/z): 229 + (M+1) . Етил тіазоло[4,5-c]піридин-2-карбоксилат (R-3) Розчин етил 2-(4-хлорпіридин-3-іламіно)-2-оксоацетату (R-2) (8 г, 35 ммоль) та реагент Лоусона (8.5 г, 21 ммоль) в толуолі (100 мл) нагрівали зі зворотним холодильником впродовж 2 год., та потім концентрували в вакуумі. Залишок очищали за допомогою хроматографії на + силікагелі з одержанням зазначеної у заголовку сполуки. МС (m/z): 209 (M+1) . Тіазоло[4,5-c]піридин-2-ілметанол (R-4) До розчину етил тіазоло[4,5-c]піридин-2-карбоксилату (R-3) (5 г, 24 ммоль) в етанолі (100 мл) при 0 °C частинами додавали NaBH4 (0.9 г, 24 ммоль). Суспензію перемішували при кімнатній температурі впродовж 1 год., та потім концентрували. Одержуваний залишок розчиняли в EtOAc, промивали водою. Органічний шар відокремлювали, сушили над Na 2SO4, концентрували в вакуумі та очищали за допомогою хроматографії на силікагелі з одержанням + зазначеної у заголовку сполуки. МС (m/z): 167 (M+1) . Тіазоло[4,5-c]піридин-2-ілметанамін (R) Проміжну сполуку R одержували із тіазоло[4,5-c]піридин-2-ілметанолу (R-4) дотримуючись + подібних методик синтезу проміжної сполуки A із A-3, як описано вище. МС (m/z): 165 (M) . Проміжна сполука S: O Cl N NH2 (S-1) 30 35 40 45 Cl N Cl O Реагент Лоусона N N H (S-2) S N (S-3) N NBS N S (S-4) N NH3 Br N S NH2 (S) N-(2-Хлорпіридин-3-іл)ацетамід (S-2) До суміші 3-хлорпіридин-2-аміну (S-1) (12.8 г, 100 ммоль) та Et3N (3 мл) в сухому ДХМ (50 мл) по краплям додавали ацетилхлорид (8 мл). Реакційну суміш перемішували при кімнатній температурі впродовж ночі, потім pH встановлювали на значення приблизно 7 за допомогою водного розчину NaHCO3, та екстрагували за допомогою ДХМ. Органічний шар промивали водою, сушили над Na2SO4, та концентрували з одержанням зазначеної у заголовку сполуки + (17.1 г). МС (m/z): 171.6 (M+1) . 2-Метилтіазоло[5,4-b]піридин (S-3) Проміжну сполуку S-3 одержували із N-(2-хлорпіридин-3-іл)ацетаміду (S-2) дотримуючись подібних методик синтезу проміжної сполуки R-3 із R-2, як описано вище. МС (m/z): 151.6 + (M+1) . 2-(Бромметил)тіазоло[5,4-b]піридин (S-4) Проміжну сполуку S-4 одержували із 2-метилтіазоло[5,4-b]піридину (S-3) дотримуючись подібних методик синтезу проміжної сполуки B-5 із B-4, як описано вище. Тіазоло[5,4-b]піридин-2-ілметанамін(S) Проміжну сполуку S одержували із 2-(бромметил)тіазоло[5,4-b]піридину (S-4) дотримуючись + подібних методик синтезу проміжної сполуки C із C-5, як описано вище. МС (m/z): 166 (M+1) . 27 UA 107822 C2 Проміжна сполука T та T’ O O конц.H2SO4 S HO LiAlH 4 S O N S HO N N (T-1) (T-2) N H PPh3 S H 2N N (T-3) N (T-4) (T) O O O S N O S DPPA / DBU N3 N3 OH MeMgBr S NaBH 4 N N (T'-1) NH 2 DPPA / DBU S N (T'-2) (T'-3) PPh3 S N S NH 3.H 2O N (T'-4) (T') 5 10 15 Метил бензо[d]тіазол-6-карбоксилат (T-2) Проміжну сполуку T2 одержували із бензо[d]тіазол-6-карбонової кислоти (T-1) дотримуючись подібних методик синтезу проміжної сполуки F-2 із F-1, як описано вище. Бензо[d]тіазол-6-ілметанамін (T) Проміжну сполуку T одержували із метил бензо[d]тіазол-6-карбоксилату (T-2) дотримуючись + подібних методик синтезу проміжної сполуки D із D-2, як описано вище. МС (m/z): 165 (M+1) . 1-(Бензо[d]тіазол-6-іл)етанамін (T") Проміжну сполуку T" одержували із бензо[d]тіазол-6-карбонової кислоти (T-1) дотримуючись подібних методик синтезу проміжної сполуки D’-5 із D’-1, як описано вище, та проміжної сполуки + D із D-4, як описано вище. МС (m/z): 179(M+1) . Синтез проміжних сполук борної кислоти або її складного ефіру: Проміжна сполука U H N HO MsCl Br (U-1) O N O O Br K2CO3 (U-2) O O B B O O N N MsO N O N B O PdCl2(dppf) O (U) (U-3) 20 25 30 35 Тетрагідро-2H-піран-4-іл метансульфонат (U-2) До суміші тетрагідро-2H-піран-4-олу (U-1) (1.02 г, 10 ммоль) та Et3N (1 мл) в сухому ДХМ (20 мл) по краплям додавали MsCl (2 мл). Реакційну суміш перемішували при кімнатній температурі впродовж 1 год., потім промивали водою. Органічний шар відокремлювали, сушили над Na2SO4, та концентрували з одержанням зазначеної у заголовку сполуки (1.8 г). 4-Бром-1-(тетрагідро-2H-піран-4-іл)-1H-піразол (U-3) Суміш тетрагідро-2H-піран-4-іл метансульфонату (U-2) (1.8 г, 10 ммоль), 4-бром-1H-піразолу (1.46 г, 10 ммоль) та K2CO3 (1.4 г, 10 ммоль) в ДМФА (10 ммоль) перемішували при 80 °C впродовж ночі, потім очищали за допомогою хроматографії з одержанням зазначеної у + заголовку сполуки (861 мг). МС (m/z): 231 (M+1) . 1-(Тетрагідро-2H-піран-4-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1H-піразол (U) До суміші 4-бром-1-(тетрагідро-2H-піран-4-іл)-1H-піразолу (U-3) (1.13 г, 4.48 ммоль), 4,4,5,5тетраметил-2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1,3,2-діоксаборолану (861 мг, 3.73 ммоль) та KOAc(12.43 г, 12.68 ммоль) в ДМСО (5 мл) під N2 додавали Pd (dppf)Cl2 (172 мг, 0.21 ммоль). Суміш перемішували впродовж ночі при 80 °C під N2. Після охолодження до кімнатної температури, реакційну суміш виливали в воду, та екстрагували за допомогою EtOAc. Органічну фазу відокремлювали, концентрували в вакуумі та потім очищали за допомогою хроматографії + з одержанням зазначеної у заголовку сполуки (170 мг). МС (m/z): 279 (M+1) . 40 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCertain triazolopyridines and triazolopyrazines, compositions thereof and methods of use therefor
Автори англійськоюSu, Wei-Guo, Jia, Hong, Dai, Guangxiu
Автори російськоюСу Вей-Го, Цзя Хун, Дай Гуансю
МПК / Мітки
МПК: A61P 35/00, C07D 471/04, A61K 31/437, C07D 487/04, A61K 31/4985
Мітки: застосування, триазолопіридини, триазолопіразини, композиції, визначені
Код посилання
<a href="https://ua.patents.su/95-107822-viznacheni-triazolopiridini-ta-triazolopirazini-kh-kompozici-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Визначені триазолопіридини та триазолопіразини, їх композиції та їх застосування</a>
Попередній патент: Антитіло до her3 та його застосування
Наступний патент: Спосіб одержання і склад коагулянтів для очищення природних вод питного призначення з високим вмістом алюмінію
Випадковий патент: Гідропривідна установка для видобутку рідких вуглеводнів












