Аміди антранілової кислоти та їх застосування у фармацевтиці
Формула / Реферат
1. Амід антранілової кислоти формули І
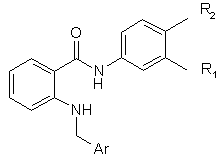 , (I)
, (I)
де Аr представлено підформулою Іа
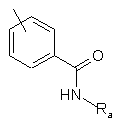 , (Ia)
, (Ia)
де Ra представляє Н або нижчий алкіл, і R1 представляє Н або перфторований нижчий алкіл, і R2 представляє Н, галоген, С2-С7алкіл, С2-С7алкеніл або нижчий алкініл; або Аr представлено підформулою Іb
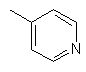 , (Ib)
, (Ib)
і R1 представляє перфторований нижчий алкіл, і R2 представляє бромо, йодо, С2-С7алкіл, С2-С7алкеніл або нижчий алкініл, або R1 представляє Н, і R2 представляє фторо, бромо, йодо, етил, С5-С7алкіл, С2-С7алкеніл або нижчий алкініл, або його N-оксид або таутомер, або сіль такого аміду антранілової кислоти, його N-оксиду або його таутомеру.
2. Амід антранілової кислоти формули І за п. 1, який відрізняється тим, що Аr представлено підформулою Іа, де Ra представляє Н або нижчий алкіл, і R1 представляє Н або трифторометил, і R2 представляє Н, галоген, С2-С7алкіл, С2-С7алкеніл або нижчий aлкініл, або Аr представлено підформулою Іb, і R1 представляє трифторометил, і R2 представляє бромо, йодо, С2-С7алкіл, С2-С7алкеніл або нижчий алкініл, або R1 представляє Н, і R2 представляє фторо, бромо, йодо, етил, С5-С7алкіл, С2-С7алкеніл або нижчий алкініл, або його N-оксид або таутомер, або сіль такого аміду антранілової кислоти, його N-оксиду або його таутомеру.
3. Амід антранілової кислоти формули І за п. 1 або 2, який відрізняється тим, що Аr представлено підформулою Іа, де Ra представляє Н або нижчий алкіл, R1 представляє Н або трифторометил, і R2 представляє Н, галоген, C2-С7алкіл, С2-С7алкеніл або нижчий алкініл, або його таутомер, або сіль такого аміду антранілової кислоти або його таутомеру.
4. Амід антранілової кислоти формули І за п. 1 або 2, який відрізняється тим, що Аr представлено підформулою Іb, R1 представляє трифторометил, і R2 представляє бромо, йодо, С2-С7алкіл, С2-С7алкеніл або нижчий алкініл, або R1 представляє Н, і R2 представляє фторо, бромо, йодо, етил, С5-С7алкіл, С2-С7алкеніл або нижчий алкініл, або його N-оксид або таутомер, або сіль такого аміду антранілової кислоти або N-оксид або його таутомер.
5. Амід антранілової кислоти формули І за п. 4, який відрізняється тим, що Аr представлено підформулою Іb, R1 представляє трифторометил, і R2 представляє бромо, пропіл, пропеніл або пропініл, або R1 представляє Н, і R2 представляє фторо, бромо, пропеніл або пропініл, або його N-оксид або таутомер, або сіль такого аміду антранілової кислоти або N-оксид або його таутомер.
6. Амід антранілової кислоти формули І за п. 4, який відрізняється тим, що Аr представлено N-оксидом підформули Іb, R1 представляє трифторометил, і R2 представляє бромо, пропіл, пропеніл або пропініл, або його таутомер, або сіль такого аміду антранілової кислоти або його таутомеру.
7. Амід антранілової кислоти формули І за п. 1, вибраний з 2-[4-піридилметил]аміно-N-[4-бромо-3-(трифторометил)феніл]бензаміду, 2-[4-піридилметил]аміно-N-(4-бромофеніл)бензаміду, 2-[[3-[(метиламіно)карбоніл]-феніл]метил]аміно-N-[3-(трифторометил)феніл]бензаміду, 2-[4-піридилметил]аміно-N-[4-(1-пропініл)-3-(трифторометил)феніл]бензаміду, 2-[4-піридилметил]аміно-N-[4-(1-пропініл)феніл]бензаміду, гідрохлоридної солі 2-[4-піридилметил]аміно-N-[4-f(Z)-1-пропеніл]-3-(трифторометил)феніл]бензаміду, 2-[4-піридилметил]аміно-N-[4-(1-пропіл)-3-(трифторометил)феніл]бензаміду, N-(4-хлоро-3-трифторометилфеніл)-2-[(1-оксипіридин-4-ілметил)-аміно]бензаміду та N-(4-фторо-3-трифторометилфеніл)-2-[(1-оксипіридин-4-ілметил)-аміно]бензаміду або їх N-оксидів або таутомерів, або солей такого аміду антранілової кислоти, його N-оксиду або його таутомеру.
8. Амід антранілової кислоти формули І за будь-яким з пп. з 1 по 7, або його N-оксид або таутомер, або фармацевтичнo прийнятна сіль такої сполуки для застосування у лікуванні організму людини або тварин.
9. Застосування аміду антранілової кислоти формули І, яке відрізняється тим, що радикали та символи мають значення, визначені у будь-якому з пп. з 1 по 7, або його N-оксиду або таутомеру, або фармацевтичнo прийнятної солі такої сполуки, для одержання фармацевтичного продукту для лікування неопластичної хвороби.
10. Застосування аміду антранілової кислоти формули І, яке відрізняється тим, що радикали та символи мають значення, визначені у будь-якому з пп. з 1 по 7, або його N-оксиду або таутомеру, або фармацевтичнo прийнятної солі такої сполуки, для одержання фармацевтичного продукту для лікування ретинопатії або вікової дегенерації жовтої плями.
11. Спосіб лікування неопластичної хвороби, що реагує на інгібування активності VEGF-рецепторної тирозинкінази, який включає введення аміду антранілової кислоти формули І або його N-оксиду або таутомеру, або фармацевтично прийнятної солі такого аміду антранілової кислоти, його N-оксиду або його таутомеру, у якому радикали та символи мають значення, визначені у будь-якому з пп. з 1 по 7, у кількості, ефективній проти вищезгаданої хвороби, теплокровній тварині, яка потребує такого лікування.
12. Фармацевтична композиція, яка містить амід антранілової кислоти формули І за будь-яким з пп. 1 по 7, або його N-оксид або таутомер, або фармацевтично прийнятну сіль такої сполуки, або її гідрат або сольват, та принаймні один фармацевтично прийнятний носій.
13. Спосіб одержання аміду антранілової кислоти формули І
 , (I)
, (I)
де R2 представляє водень або галоген, і решта символів R1 та Аr є такими, як визначено у п. 1, який відрізняється тим, що сполуку формули II
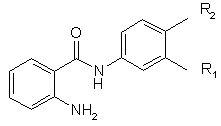 , (II)
, (II)
де R1 та R2 є такими, як визначено вище для формули І, піддають реакції з карбонільною сполукою формули III
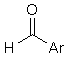 , (III)
, (III)
де Аr є таким, як визначено вище для сполуки формули І, у присутності відновника, де вихідні сполуки формули II та III також можуть бути присутні з функціональними групами у захищеній формі, якщо необхідно, і/або у формі солей, за умови наявності солеутворювальної групи та можливості реакції у формі солі, де будь-які захисні групи у захищеній похідній сполуки формули І є видаленими, і, якщо потрібно, доступну сполуку формули І перетворюють на іншу сполуку формули І або її N-оксид, вільну сполуку формули І перетворюють на сіль, доступну сіль сполуки формули І перетворюють на вільну сполуку або іншу сіль і/або суміш ізомерних сполук формули І відокремлюють в окремі ізомери.
Текст
1. Амід антранілової кислоти формули І C2 1 3 77448 4 мулою Іb, і R1 представляє трифторометил, і R2 символи мають значення, визначені у будь-якому з представляє бромо, йодо, С2-С7алкіл, С2пп. з 1 по 7, або його N-оксиду або таутомеру, або С7алкеніл або нижчий алкініл, або R1 представляє фармацевтичнo прийнятної солі такої сполуки, для Н, і R2 представляє фторо, бромо, йодо, етил, С5одержання фармацевтичного продукту для лікуС7алкіл, С2-С7алкеніл або нижчий алкініл, або його вання неопластичної хвороби. N-оксид або таутомер, або сіль такого аміду ан10. Застосування аміду антранілової кислоти формули І, яке відрізняється тим, що радикали та транілової кислоти, його N-оксиду або його таутомеру. символи мають значення, визначені у будь-якому з 3. Амід антранілової кислоти формули І за п.1 або пп. з 1 по 7, або його N-оксиду або таутомеру, або 2, який відрізняється тим, що Аr представлено фармацевтичнo прийнятної солі такої сполуки, для підформулою Іа, де Ra представляє Н або нижчий одержання фармацевтичного продукту для лікуалкіл, R1 представляє Н або трифторометил, і R2 вання ретинопатії або вікової дегенерації жовтої представляє Н, галоген, C2-С7алкіл, С2-С7алкеніл плями. або нижчий алкініл, або його таутомер, або сіль 11. Спосіб лікування неопластичної хвороби, що такого аміду антранілової кислоти або його таутореагує на інгібування активності VEGFмеру. рецепторної тирозинкінази, який включає введен4. Амід антранілової кислоти формули І за п.1 або ня аміду антранілової кислоти формули І або його 2, який відрізняється тим, що Аr представлено N-оксиду або таутомеру, або фармацевтично припідформулою Іb, R1 представляє трифторометил, і йнятної солі такого аміду антранілової кислоти, R2 представляє бромо, йодо, С2-С7алкіл, С2його N-оксиду або його таутомеру, у якому радиС7алкеніл або нижчий алкініл, або R1 представляє кали та символи мають значення, визначені у Н, і R2 представляє фторо, бромо, йодо, етил, С5будь-якому з пп. з 1 по 7, у кількості, ефективній С7алкіл, С2-С7алкеніл або нижчий алкініл, або його проти вищезгаданої хвороби, теплокровній твариN-оксид або таутомер, або сіль такого аміду анні, яка потребує такого лікування. транілової кислоти або N-оксид або його таутомер. 12. Фармацевтична композиція, яка містить амід 5. Амід антранілової кислоти формули І за п.4, антранілової кислоти формули І за будь-яким з який відрізняється тим, що Аr представлено підпп.1 по 7, або його N-оксид або таутомер, або фаформулою Іb, R1 представляє трифторометил, і R2 рмацевтично прийнятну сіль такої сполуки, або її представляє бромо, пропіл, пропеніл або пропініл, гідрат або сольват, та принаймні один фармацевабо R1 представляє Н, і R2 представляє фторо, тично прийнятний носій. бромо, пропеніл або пропініл, або його N-оксид 13. Спосіб одержання аміду антранілової кислоти або таутомер, або сіль такого аміду антранілової формули І R кислоти або N-оксид або його таутомер. O 6. Амід антранілової кислоти формули І за п.4, R N який відрізняється тим, що Аr представлено NH (I) NH оксидом підформули Іb, R1 представляє трифторометил, і R2 представляє бромо, пропіл, пропеніл Ar , або пропініл, або його таутомер, або сіль такого де R2 представляє водень або галоген, і решта аміду антранілової кислоти або його таутомеру. символів R1 та Аr є такими, як визначено у п.1, 7. Амід антранілової кислоти формули І за п.1, який відрізняється тим, що сполуку формули II вибраний з 2-[4-піридилметил]аміно-N-[4-бромо-3R2 O (трифторометил)феніл]бензаміду, 2-[4піридилметил]аміно-N-(4-бромофеніл)бензаміду, R1 (II) N H 2-[[3-[(метиламіно)карбоніл]-феніл]метил]аміно-NNH2 [3-(трифторометил)феніл]бензаміду, 2-[4, піридилметил]аміно-N-[4-(1-пропініл)-3де R1 та R2 є такими, як визначено вище для фор(трифторометил)феніл]бензаміду, 2-[4мули І, піддають реакції з карбонільною сполукою піридилметил]аміно-N-[4-(1формули III O пропініл)феніл]бензаміду, гідрохлоридної солі 2-[4піридилметил]аміно-N-[4-f(Z)-1-пропеніл]-3(III) Ar , H (трифторометил)феніл]бензаміду, 2-[4де Аr є таким, як визначено вище для сполуки фопіридилметил]аміно-N-[4-(1-пропіл)-3рмули І, у присутності відновника, де вихідні спо(трифторометил)феніл]бензаміду, N-(4-хлоро-3луки формули II та III також можуть бути присутні з трифторометилфеніл)-2-[(1-оксипіридин-4функціональними групами у захищеній формі, якілметил)-аміно]бензаміду та N-(4-фторо-3що необхідно, і/або у формі солей, за умови наявтрифторометилфеніл)-2-[(1-оксипіридин-4ності солеутворювальної групи та можливості реаілметил)-аміно]бензаміду або їх N-оксидів або таукції у формі солі, де будь-які захисні групи у томерів, або солей такого аміду антранілової кисзахищеній похідній сполуки формули І є видалелоти, його N-оксиду або його таутомеру. ними, і, якщо потрібно, доступну сполуку формули 8. Амід антранілової кислоти формули І за будьІ перетворюють на іншу сполуку формули І або її яким з пп.з 1 по 7, або його N-оксид або таутомер, N-оксид, вільну сполуку формули І перетворюють або фармацевтичнo прийнятна сіль такої сполуки на сіль, доступну сіль сполуки формули І перетводля застосування у лікуванні організму людини рюють на вільну сполуку або іншу сіль і/або суміш або тварин. ізомерних сполук формули І відокремлюють в 9. Застосування аміду антранілової кислоти форокремі ізомери. мули І, яке відрізняється тим, що радикали та 2 1 5 Винахід стосується нових похідних амідів антранілової кислоти, способів їх одержання, їх застосування у процесі лікування організму людини або тварин, їх застосування - окремо або в комбінації з однією чи кількома іншими фармацевтично активними сполуками - для лікування, головним чином, неопластичної хвороби, такої як пухлинна хвороба, ретинопатії та вікової дегенерації жовтої плями; способу лікування такої хвороби у тварин, зокрема, у людини, та застосування такої сполуки - окремо або в комбінації з однією чи кількома іншими фармацевтично активними сполуками - для виробництва фармацевтичної композиції (медикаменту) для лікування неопластичної хвороби, ретинопатії або вікової дегенерації жовтої плями. Відомо, що деякі хвороби пов'язані з дерегульованим ангіогенезом, наприклад, хвороби, викликані очною неоваскуляризацією, такі як ретинопатія (включаючи діабетичну ретинопатію), вікова дегенерація жовтої плями, псоріаз, гемангіобластома, гемангіома, артеріосклероз, запальні хвороби, такі як ревматоїдні або ревматичні запальні хвороби, зокрема, артрит, такий як ревматоїдний артрит, або інші хронічні запальні порушення, такі як хронічна астма, артеріальний або посттрансплантаційний атеросклероз, ендометріоз, і особливо, неопластичні хвороби, наприклад, так звані солідні пухлини та рідкі пухлини (такі як лейкемія). Центральне місце у мережі, яка регулює ріст і диференціацію судинної системи та її компонентів під час ембріонального розвитку, нормального росту та багатьох патологічних аномалій та хвороб, посідає ангіогенний фактор, відомий як "судинний ендотеліальний фактор росту" (VGEF), димерний, дисульфідно зв'язаний 46кДа глікопротеїн, разом з його клітинними рецепторами [див. Breier, G., et al., Trends in Cell Biology 6, 454-6 (1996)]. VEGF-рецептори є трансмембранними рецепторними тирозинкіназами. Відомі різні типи VEGFрецепторів, наприклад, VEGFR-1, VEGFR-2 та VEGFR-3. Багато з людських пухлин, зокрема, гліоми та карциноми, мають високий рівень експресії VEGF та його рецепторів. Звідси виникла гіпотеза, згідно з якою VEGF, який вивільнюється клітинами пухлин, може стимулювати ріст кровоносних капілярів та проліферацію ендотелію пухлин паракринним шляхом, а отже, через поліпшене кровопостачання прискорює ріст пухлин. Пряме свідчення ролі VEGF як фактора ангіогенезу пухлин in vivo було отримано за результатами досліджень, у яких активність VEGF інгібувалася антитілами. Ангіогенез вважають абсолютною передумовою для пухлин, які виростають до розмірів, що перевищують максимальний діаметр приблизно 12мм; до цієї межі кисень та поживні речовини можуть постачатися до пухлинних клітин шляхом дифузії. Три основні механізми відіграють важливу роль в активності інгібіторів ангіогенезу проти пухлин: 1) інгібування росту судин, головним чином, 77448 6 капілярів, у васкуляризовані пухлини, в результаті чого чистий ріст пухлин припиняється завдяки балансові, який досягається між апоптозом та проліферацією; 2) запобігання міграції пухлинних клітин завдяки відсутності кровотоку до пухлин і з них; і 3) інгібування проліферації ендотеліальних клітин, таким чином, уникаючи ефекту стимуляції паракринного росту, який справляється на навколишню тканину ендотеліальними клітинами, які зазвичай вкривають судини. [У WO 00/27820] описано сполуки, які належать до класу амідів антранілової кислоти, про які відомо, що ці сполуки інгібують активність VEGFрецепторної тирозинкінази, ріст пухлин та залежну від VEGFI проліферацію клітин. Несподівано було виявлено, що описані нижче похідні амідів антранілової кислоти формули І мають сприятливі фармакологічні властивості і інгібують, наприклад, активність VEGF-рецепторної тирозинкінази, ріст пухлин та залежну від VEGFI проліферацію клітин. Похідні амідів антранілової кислоти формули І є придатними, наприклад, для застосування у лікуванні хвороб, головним чином, хвороб, для лікування та профілактики яких сприятливий вплив виявляє інгібування ангіогенезу та/або VEGFрецепторної тирозинкінази. Винахід стосується амідів антранілової кислоти формули І, (I) де Аr представлено підформулою Іа (Ia) де Ra представляє Η або нижчий алкіл, R1 представляє Η або перфторований нижчий алкіл, і R2 представляє Н, галоген, С2-С7алкіл, С2С7алкеніл або нижчий алкініл; або Аr представлено підформулою Іb, (Ib) і R1 представляє перфторований нижчий алкіл, R2 представляє бромо, йодо, С2-С7алкіл, С2С7алкеніл або нижчий алкініл, або R1 представляє Н, і R2 представляє фторо, бромо, йодо, етил, С5С7алкіл, С2-С7алкеніл або нижчий алкініл, їх N-оксидів та таутомеріє, а також солей таких амідів антранілової кислоти, їх N-оксидів та їх таутомерів. Вжиті вище та нижче загальні терміни в оптимальному варіанті у контексті опису мають нижче 7 77448 8 наведені значення, якщо не вказано іншого: кислота, N-циклогексилсульфамінова кислота, N"Нижчий" означає радикал, який має щонайбіметил-, N-етил- або N-пропіл-сульфамінова кислольше 7, краще - щонайбільше 4 атоми вуглецю, та, або інші органічні протонні кислоти, такі як аспричому дані радикали є або лінійними, або розгакорбінова кислота. луженими з одним або кількома відгалуженнями. Для виділення та очищення також можна заЯкщо вжито форму множини для сполук, состосовувати фармацевтично неприйнятні солі, лей і т. ін., це також означає одну сполуку, сіль і т. наприклад, пікрати або перхлорати. Для терапевін. тичного застосування використовують лише фарБудь-які асиметричні атоми вуглецю (напримацевтично прийнятні солі або вільні сполуки (у клад, у сполуках формули І, де R9 є нижчим алківідповідних випадках - у формі фармацевтичних лом) можуть бути присутні у (R)-, (S)- або (R,S)композицій), і тому їм віддають перевагу. конфігурації, в оптимальному варіанті - у (R)- або З огляду на близьку спорідненість між новими (S)-конфігурації. Таким чином, сполуки можуть сполуками у вільній формі та сполуками у формі бути присутні у формі сумішей ізомерів або чистих солей, включаючи солі, які можуть бути викорисізомерів, в оптимальному варіанті - як енантіомертані як проміжні сполуки, наприклад, при очищенні чисті діастереомери. або виявленні нових сполук, будь-яке посилання Винахід також стосується можливих таутомена вільні сполуки, яке міститься вище або нижче, рів сполук формули І. слід розуміти також як посилання на відповідні В оптимальному варіанті втілення алкіл має не солі, які можуть бути прийнятними і доцільними. більше 12 атомів вуглецю і, як правило, є нижчим Сполуки формули І та їх N-оксиди мають цінні алкілом. фармакологічні властивості, як описано вище та Нижчий алкіл в оптимальному варіанті є алкінижче. лом, що має від 1 до 7 включно, в оптимальному Ефективність сполук згідно з винаходом як інваріанті - від 1 до 4 включно, і є лінійним або розгібіторів активності VEGF-рецепторної тирозинкігалуженим; в оптимальному варіанті нижчий алкіл нази може бути продемонстрована таким чином: є бутилом, таким як n-бутил, втор-бутил, ізобутил, Випробування активності щодо VEGFтрет-бутил, пропілом, таким як n-пропіл або ізопрецепторної тирозинкінази. Випробування здійсропіл, етилом або, в оптимальному варіанті - менюють, застосовуючи Flt-1 VEGF-рецепторну тиротилом. зинкіназу. Детальна процедура є такою: 30мкл Вжитий авторами термін "перфторований нирозчину кінази (10нг кіназного домену Flt-1, жчий алкіл" означає нижчий алкільний радикал, у Shibuya et al., Oncogene 5, 519-24 [1990]) у 20мМ якому всі атоми водню заміщено атомами фтору. Tris-HCI, pH7,5, 3мМ дихлориду марганцю (МnСl2), Галоген є, як правило, фтором, хлором, бро3мМ хлориду магнію (МgСІ2), 10мкМ ванадату намом або йодом, краще - фтором, хлором або бротрію, 0,25мг/мл поліетиленгліколю (PEG) 20000, мом. 1мМ дитіотреїтолу і 3мкг/мкл полі(GІu,Туr) 4:1 Такі солі утворюються, наприклад, як кислі (Sigma, Buchs, Швейцарія), 8 М-М [33Р]-АТР адиційні солі, в оптимальному варіанті - з органіч(0,2мкКі), 1% диметилсульфоксиду і від 0 до ними або неорганічними кислотами, зі сполук фо100мкМ випробуваної сполуки інкубують разом рмули І з атомом азоту основи, які є особливо фапротягом 10 хвилин при кімнатній температурі. рмацевтично прийнятними солями. Прийнятними Після цього реакцію припиняють шляхом додаваннеорганічними кислотами є, наприклад, галоїдоня 10мкл 0,25Μ етилендіамінтетраацетату (EDTA), водневі кислоти, такі як соляна кислота, сірчана рН7. Застосовуючи багатоканальний розподільник кислота, або фосфорна кислота. Прийнятними (LAB SYSTEMS, USA), аліквотну кількість 20мкл органічними кислотами є, наприклад, карбонова, наносять на PVDF (= полівінілдифторидну) мемфосфонова, сульфонова або сульфамінова кислобрану Immobilon Ρ (Millipore, USA), пропускають ти, наприклад, оцтова кислота, пропіонова кислочерез трубопровід мікротитрувального фільтра та, каприлова кислота, капринова кислота, додеMillipore, сполучений з вакуумом. Після повного канова кислота, гліколева кислота, молочна видалення рідини мембрану послідовно промивакислота, фумарова кислота, бурштинова кислота, ють 4 рази у ванні, що містить 0,5% фосфорної адипінова кислота, пімелінова кислота, суберинокислоти (Н3РО4) і один раз етанолом, інкубують ва кислота, азелаїнова кислота, яблучна кислота, протягом 10 хвилин щоразу зі збовтуванням, потім винна кислота, лимонна кислота, амінокислоти, закріплюють на Hewlett Packard TopCount Manifold такі як глутамінова кислота або аспарагінова кисі вимірюють радіоактивність після додавання лота, малеїнова кислота, гідрокси-малеїнова кис10мкл Microscint® (рідини для β-сцинтиляційного лота, метилмалеїнова кислота, циклогексанкарболічильника). Значення IC50 визначають шляхом нова кислота, адамантанкарбонова кислота, аналізу лінійної регресії відсотка інгібування для бензойна кислота, саліцилова кислота, 4кожної сполуки у трьох концентраціях (як правило аміносаліцилова кислота, фталева кислота, фені0,01, 0,1 та 1мкмоль). Значення IC50, які можуть лоцтова кислота, мигдалева кислота, корична кисбути виявлені для сполук формули І, тримаються у лота, метан- або етан-сульфонова кислота, 2межах від 0,001 до 1мкМ, в оптимальному варіанті гідроксіетансульфонова кислота, етан-1,2- у межах від 0,001 до 0,1мкМ. дисульфонова кислота, бензолсульфонова кислоПротипухлинна ефективність сполук винаходу та, 2-нафталінсульфонова кислота, 1,5-нафталінможе бути продемонстрована in vivo таким чином: дисульфонова кислота, 2-, 3або 4In vivo активність у моделях мишей без шерстметилбензолсульфонова кислота, метилсірчана ного покриву з ксенотрансплантатами: самиць кислота, етилсірчана кислота, додецилсірчана мишей без шерстного покриву BALB/c (віком 8-12 9 77448 10 тижнів), Novartis Animal Farm, Sisseln, Швейцарія) годинного інкубування при 37°С додають рекомбітримають у стерильних умовах з водою та їжею ad нантний VEGF; кінцева концентрація VEGF станоlibitum. Утворення пухлин викликають або шляхом вить 20нг/мл). Після додаткового п'ятихвилинного підшкірної ін'єкції мишам пухлинних клітин (наприінкубування при 37°С клітини двічі промивають клад, лінії клітин карциноми передміхурової залози крижаним PBS (фосфатно-буферним розсолом) і Du 145 [АТСС No. НТВ 81; див. Cancer Research відразу розчиняють у 100 мкл лізисного буфера на 37, 4049-58 (1978)], або шляхом пересадження лунку. Лізати після цього центрифугують для вифрагментів пухлин (приблизно 25мг) підшкірно у далення ядер клітин і визначають концентрацію лівий бочок миші, застосовуючи голку троакар 13 білка в надосадовій рідині, застосовуючи комплект розміру під анестезією Forene® (Abbott, Швейцадля аналізу серійного виробництва (BIORAD). Лірія). Лікування випробуваною сполукою розпочизати після цього відразу використовують або, в нають, коли пухлина досягає середнього об'єму разі необхідності, зберігають при -20°С. 100мм3. Ріст пухлин вимірюють від двох до трьох Аналіз сендвіч-ELISA здійснюють для вимірюразів на тиждень і через 24 години після останньовання фосфорилування KDR-рецептора: моноклого застосування шляхом визначення довжини двох нальне антитіло до KDR [наприклад, Mab перпендикулярних осей. Об'єми пухлин розрахо1495.12.14; одержане Н. Towbin] іммобілізують на вують згідно з опублікованими способами [див. чорних ELISA-планшетах (OptiPlate™ HTRF-96 від Evans et al., Brit. J. Cancer 45, 466-8 (1982)]. ПроPackard). Планшети після цього промивають і ретипухлинну ефективність визначають як середнє шту вільних сайтів зв'язування білка насичують 1% збільшення об'єму пухлин підданих лікуванню тваBSA у PBS. Лізати клітин (20мкг білка на лунку) рин, ділене на середнє збільшення об'єму пухлин після цього інкубують у цих планшетах до наступнелікованих (контрольних) тварин і, після множенного дня при 4°С разом з антитілом проти фосфоня на 100, виражають як Т/С%. Регресію пухлини тирозину, з'єднаним з лужною фосфатазою (виражену у%) вказують як найменший середній (PY20:AP від Transduction Laboratories). Планшети об'єм пухлин відносно середнього об'єму пухлин знову промивають і після цього демонструють на початку лікування. Випробувану сполуку ввозв'язування антитіла проти фосфотирозину з задять щоденно. хопленим фосфорилованим рецептором, застосоВ альтернативному варіанті таким самим сповуючи люмінесцентний АР-субстрат (CDP-Star, собом також застосовують інші лінії клітин, наготовий до застосування, з Emerald II; TROPIX). приклад: Люмінесценцію вимірюють у сцинтиляційному лі- лінію клітин аденокарциноми молочної залочильнику Packard Top Count Microplate Scintillation зи MCF-7 [АТСС No.НТВ 22; див. також J. Natl. Counter (Top Count). Різниця між сигналом позитиCancer Inst. (Bethesda) 51, 1409-16 (1973)]; вного контролю (стимульованим VEGF) та сигна- лінію клітин аденокарциноми молочної залолом негативного контролю (не стимульованим зи MDA-MB 468 [АТСС No.НТВ 132; див. також In VEGF) відповідає викликаному VEGF фосфорилуVitro 14, 911-15 (1978)]; ванню KDR-рецептора (=100%). Активність випро- лінію клітин аденокарциноми молочної залобуваних речовин розраховують як% інгібування зи MDA-MB 231 [АТСС No.НТВ 26; див. також J. викликаного VEGF фосфорилування KDRNatl. Cancer Inst. (Bethesda) 53, 661-74 (1974)]; рецептора, причому концентрацію речовини, яка - лінію клітин карциноми товстої кишки Colo викликає половину максимального інгібування, 205 [АТСС No.CCL 222; див. також Cancer Res. 38, визначають як ED50 (ефективна доза для 50% інгі1345-55 (1978)]; бування). - лінію клітин карциноми товстої кишки НСТ Сполука формули І або її N-оксид різною мі116 [АТСС No.CCL 247; див. також Cancer Res. рою інгібує й інші тирозинкінази, які беруть участь 41., 1751-6 (1981)]; у трансдукції сигналу й опосередковуються трофі- лінію клітин карциноми передміхурової залочними факторами, наприклад, кінази з групи Src, зи DU 145 [АТСС No. НТВ 81; див. також Cancer головним чином, c-Src кіназу, Lck та Fyn; а також Res. 37, 4049-58 (1978)]; і кінази групи EGF, наприклад, с-еrbВ2 кіназу (HER- лінію клітин карциноми передміхурової зало2), с-еrbВ3 кіназу с-еrbВ4 кіназу; рецепторну кіназу зи РС-3 [АТСС No.CRL 1435; див. також Cancer інсуліноподібного фактора росту (IGF-1 кіназу), Res. 40, 524-34 (1980)]. головним чином, кінази, що належать до групи Інгібування викликаного VEGF автофосфориPDGF-рецепторних тирозинкіназ, такі як PDGFлування KDR-рецептора може бути підтверджене рецепторна кіназа, CSF-1-рецепторна кіназа, Kitще одним in vitro експериментом у клітинах: транрецепторна кіназа та VEGF-рецепторна кіназа; а сфіковані клітини СНО, які постійно експресують також серин/треонін кінази, усі з яких відіграють VEGF-рецептор людини (KDR), висівають у повсвою роль у регуляції росту та трансформації у ному культуральному середовищі (з 10% ембріоклітинах ссавців, включаючи клітини людини. нальної телячої сироватки = FCS) у 6-лункових За результатами цих досліджень сполука фопланшетах для культур клітин і інкубують при 37°С рмули І згідно з винаходом виявляє терапевтичну в атмосфері 5% СО2, доки не спостерігається приефективність, зокрема, проти порушень, які залеблизно 80% конфлюентності. Сполуки, які підляжать від протеїнкінази, головним чином, проліфегають випробуванню, після цього розводять у куративних хвороб. льтуральному середовищі (без FCS, з 0,1% Корисність сполуки формули І у лікуванні альбуміну сироватки великої рогатої худоби) і доартриту як типової запальної ревматичної або дають до клітин. (Контрольні зразки включають ревматоїдної хвороби може бути просередовище без випробуваних сполук). Після дводемонстрована таким чином: 11 77448 12 Загальновідому модель щура з ад'ювантним нів), раку передміхурової залози або саркоми Каартритом [Pearson, Proc. Soc. Exp. ВіоІ. 91, 95-101 поші. Сполука формули І (або їх N-оксид) інгібує (1956)] використовують для випробування протиаріст пухлин і є особливо придатною для запобіганртритної активності сполук формули І або їх солей. ня метастатичному поширенню пухлин та ростові Ад'ювантний артрит лікують, застосовуючи два мікрометастазів. різні режими дозування: або (і) починаючи з часу Сполуку формули І вводять окремо або в комімунізації ад'ювантом (профілактичне дозування); бінації з одним або кількома терапевтичними заабо з 15-го дня після виникнення артритичної реасобами, можлива комбінована терапія має форму кції (терапевтичне дозування). В оптимальному незмінних комбінацій або введення сполуки згідно варіанті застосовують режим терапевтичного доз винаходом та одного або кількох інших терапевзування. Для порівняння інгібітор циклооксигеназитичних засобів, які можуть чергуватися або вводи2, такий як 5-бромо-2-(4-фторофеніл)-3-[4тися незалежно один від одного, або комбіновано(метилсульфоніл)феніл]тіофен або диклофенак, го введення незмінних комбінацій та одного або вводять в окремій групі. кількох інших терапевтичних засобів. Сполуку фоОтже, самцям щурів Вістара (5 тварин на грурмули І паралельно або додатково вводять для пу, масою приблизно 200г, отриманих від Iffa протипухлинної терапії в комбінації з хіміотерапіCredo, Франція) роблять i.d. (внутрішньошкірну) єю, радіотерапією, імунотерапією, хірургічним ін'єкцію в основу хвоста, застосовуючи 0,1мл міневтручанням, або з їх комбінацією. Довготривала ральної олії, що містить 0,6мг ліофілізованої умертерапія є так само можливою, як і ад'ювантна тетвленої під дією високої температури бактерії рапія у контексті методології лікування, як було Mycobacterium tuberculosis. Щурів лікують випроописано вище. До інших можливих способів лікубуваною сполукою (3, 10 або 30мг/кг перорально вання належить терапія для підтримання стану раз на день) або дають наповнювач (воду) з 15-го пацієнта після регресії пухлини, або навіть хіміопо 22-й дні (режим терапевтичного дозування). профілактична терапія, наприклад, у підданих риНаприкінці експерименту набрякання заплюсневих зикові пацієнтів. суглобів вимірюють за допомогою штангенциркуТерапевтичними засобами для можливого ля. Відсоток інгібування набрякання лап розрахокомбінування є, головним чином, одна або кілька вують шляхом порівняння з артритичними твариантипроліферативних, цитостатичних або цитотонами, які отримували наповнювач (0% інгібування) ксичних сполук, наприклад, хіміотерапевтичний та нормальними тваринами, які отримували напозасіб або кілька засобів, вибраних з групи, яка, внювач (100% інгібування). крім іншого, включає інгібітор біосинтезу поліаміну, За результатами цих досліджень сполука фоінгібітор протеїнкінази, головним чином, сермули І несподівано виявилася придатною для рин/треонін протеїнкінази, такої як протеїнкіназа С, лікування запальних (головним чином, ревматичабо тирозин протеїнкінази, такої як EGFних або ревматоїдних) хвороб. рецепторна тирозинкіназа, наприклад, РК1166, Завдяки їхній ефективності як інгібіторів актиVEGF-рецепторної тирозинкінази, наприклад, вності VEGF-рецепторної тирозинкінази, сполуки РТК787, або PDGF-рецепторної тирозинкінази, формули І, насамперед, інгібують ріст кровоносних наприклад, STI571, цитокіну, регулятор негативносудин, а отже є ефективними, наприклад, проти го росту, такий як TGF-B або IFN-3, інгібітор аробагатьох хвороб, пов'язаних з дерегульованим матази, наприклад, летрозол або анастрозол, інгіангіогенезом, головним чином, хвороб, викликаних бітор взаємодії SH2 домену з фосфорилованим очною неоваскуляризацією, зокрема, ретинопатій, білком, антиестрогени, інгібітори топоізомерази І, таких як діабетична ретинопатія або вікова дегетакі як іринотекан, інгібітори топоізомерази II, акнерація жовтої плями, псоріазу, гемангіобластоми, тивні агенти мікротрубочок, наприклад, паклітактакої як гемангіома, проліферативних порушень сел, дискодермолід або епотилон, алкілуючі агенмезангіальних клітин, таких як хронічні або гострі ти, протипухлинні антиметаболіти, такі як хвороби нирок, наприклад, діабетична нефропатія, гемцитабін або капецитабін, сполуки платини, такі злоякісного нефросклерозу, синдромів тромботичяк карбоплатин або цисплатин, антиангіогенні ної мікроангіопатії або відторгнення трансплантасполуки, агоністи гонадореліну, антиандрогени, тів, або запальної хвороби нирок, такої як гломебісфосфонати, наприклад, AREDIA® або ® рулонефрит, зокрема, мезангіопроліферативний ZOMETA , та трастузумаб. Структура активних гломерулонефрит, гемолітично-уремічного синдагентів, які ідентифікуються за кодовими номерарому, діабетичної нефропатії, гіпертензивного ми, загальні або фірмові назви можуть бути взяті з нефросклерозу, атероми, артеріального рестенопоточного видання стандартного довідника "The зу, аутоімунних хвороб, гострого запалення, фібMerck Index" або з баз даних, наприклад, Patents ротичних порушень (наприклад, цирозу печінки), International (наприклад, IMS World Publications). їх діабету, ендометріозу, хронічної астми, артеріальвідповідний зміст включено авторами шляхом поного або посттрансплантаційного атеросклерозу, силання. нейродегенеративних порушень, особливо, неопУ групах оптимальних сполук формули І та їх ластичних хвороб, таких як лейкемія, зокрема, N-оксидів, згаданих нижче, можуть бути викорисгостра лімфобластна лейкемія, гостра мієлоїдна тані замісники зі згаданих вище загальних визналейкемія та хронічна мієлоїдна лейкемія, та інших чень, наприклад, для заміни більш загальних ви"рідких пухлин", зокрема, тих, що експресують cзначень більш конкретними визначеннями або kit, KDR або flt-1, та солідних пухлин, зокрема, равизначеннями, які характеризуються тим, що їм ку молочної залози, раку товстої кишки, раку легевіддають перевагу. нів (головним чином, дрібноклітинного раку легеКрім того, винахід стосується застосування 13 77448 14 сполуки формули І, у якій радикали та символи R1 представляє трифторометил, мають визначені вище значення, або її N-оксиду R2 представляє бромо, пропіл, пропеніл або або фармацевтично прийнятної солі для одержанпропініл. ня фармацевтичного продукту для лікування ретиБільш конкретно, перевагу віддають таким нопатії або вікової дегенерації жовтої плями. сполукам формули І: Крім того, винахід стосується способу лікуван2-[4-піридилметил]аміно-N-[4-бромо-3ня неопластичної хвороби, що реагує на інгібуван(трифторометил)феніл]бензамід, ня активності VEGF-рецепторної тирозинкінази, 2-[4-піридилметил]аміно-N-(4включаючи введення сполуки формули І або її Nбромофеніл)бензамід, оксиду або фармацевтично прийнятної солі, у якій 2-[[3-[(метиламіно)карбоніл]радикали та символи мають визначені вище знафеніл]метил]аміно-N-[3-(трифторометил) фечення, у кількості, ефективній проти вищезгаданої ніл]бензамід, хвороби, теплокровній тварині, яка потребує тако2-[4-піридилметил]аміно-N-[4-(1-пропініл )-3го лікування. (трифторометил)феніл] бензамід, Крім того, винахід стосується способу лікуван2-[4-піридилметил]аміно-N-[4-(1ня ретинопатії або вікової дегенерації жовтої пляпропініл)феніл]бензамід, ми, включаючи введення сполуки формули І або її гідрохлоридна сіль 2-[4-піридилметил]аміно-NN-оксиду або фармацевтично прийнятної солі, у [4-[(2)-1-пропеніл]-3якій радикали та символи мають визначені вище (трифторометил)феніл]бензаміду, значення, у кількості, ефективній проти вищезга2-[4-піридилметил]аміно-N-[4-(1-пропіл)-3даних хвороб, теплокровній тварині, яка потребує (трифторометил)феніл] бензамід, такого лікування. N-(4-хлоро-3-трифторометил-феніл)-2-[(1Винахід стосується, зокрема, сполуки формуокси-піридин-4-ілметил)-аміно]-бензамід і ли І, у якій N-(4-фторо-3-трифторометил-феніл)-2-[(1Аr представлено підформулою Іа окси-піридин-4-ілметил)-аміно]-бензамід де Ra представляє Η або нижчий алкіл, і та їх таутомерам, R1 представляє Η або трифторометил, або солі такої сполуки або її таутомерові. R2 представляє Η, галоген, С2-С7алкіл, С2Сполуку згідно з винаходом одержують спосоС7алкеніл або нижчий алкініл; або бами, які, хоча раніше й не застосовувалися для Аr представлено підформулою Іb, і нових сполук згідно з даним винаходом, є відомиR1 представляє трифторометил, і ми per se, зокрема, процес, який характеризується R2 представляє бромо, йодо, С2-С7алкіл, С2тим, що для синтезу сполуки формули І, де R2 С7алкеніл або нижчий алкініл, або представляє водень або галоген, і решта символів R1 представляє Н, і R1 та Аr є такими, як визначено вище для сполуки R2 представляє фторо, бромо, йодо, етил, С5формули І, сполуку формули II С7алкіл, С2-С7галкеніл або нижчий алкініл, її N-оксиду або таутомеру, (II) або солі такого аміду антранілової кислоти, його N-оксиду або його таутомеру, Перевагу віддають сполукам формули І, у яких де R1 та R2 є такими, як визначено вище, підАr представлено підформулою Іа дають реакції з карбонільною сполукою формули де Ra представляє Η або нижчий алкіл, III R1 представляє Η або трифторометил, і R2 представляє Н, галоген, С2-С7алкіл, С2(III) С7алкеніл або нижчий алкініл. Перевагу також віддають сполукам формули І, у яких де Аr є таким, як визначено вище для сполуки Аr представлено підформулою Іb, формули І, у присутності відновника, R1 представляє трифторометил, і де вихідні сполуки формули II та III також моR2 представляє бромо, йодо, С2-С7алкіл, С2жуть бути присутні з функціональними групами у С7алкеніл або нижчий алкініл, або захищеній формі, якщо необхідно, і/або у формі R1 представляє Н, і солей, за умови наявності солетворної групи та R2 представляє фторо, бромо, йодо, етил, С5можливості реакції у формі солі; С7алкіл, С2-С7алкеніл або нижчий алкініл. де будь-які захисні групи у захищеній похідній Більшу перевагу віддають сполукам формули сполуки формули І є видаленими; І, у яких і, якщо потрібно, доступну сполуку формули І Аr представлено підформулою Іb, перетворюють на іншу сполуку формули І або її NR1 представляє трифторометил, і оксид, вільну сполуку формули І перетворюють на R2 представляє бромо, пропіл, пропеніл або сіль, доступну сіль сполуки формули І перетворюпропініл, або ють на вільну сполуку або іншу сіль і/або суміш R1 представляє Н, і ізомерних сполук формули І відокремлюють в R2 представляє фторо, бромо, пропеніл або окремі ізомери. пропініл. В альтернативному варіанті сполуку формули Один варіант втілення винаходу стосується II піддають реакції зі сполукою формули III у приаміду антранілової кислоти формули І, у якому сутності кислоти, наприклад, камфор-10Аr представлено N-оксидом підформули Іb, сульфонової кислоти, у придатному розчиннику, 15 77448 16 такому як толуол або бензол, при температурі детаких як ацилювання, етерифікація, естерифікація, флегмації приблизно від 15 хвилин до 6 годин, окиснення, сольволіз, та інших подібних реакцій. забезпечуючи біциклічну сполуку формули IV. Характерним для захисних груп є те, що вони легко, тобто без небажаних вторинних реакцій, піддаються видаленню, як правило, через сольволіз, відновлення, фотоліз або ферментну активність, (IV) наприклад, за умов, аналогічних фізіологічним умовам, і те, що вони є відсутніми у кінцевих продуктах. Спеціалісти знають або можуть легко виде R2 представляє водень або галоген, і решта значити, які захисні групи є придатними для реаксимволів R1 та Аr є такими, як визначено вище для цій, згаданих вище та нижче. сполуки формули І, і цю біциклічну сполуку форЗахист таких функціональних груп такими замули IV приводять у подальшу реакцію у придатхисними групами, самі захисні групи та реакції для ному розчиннику з триетилсиланом та трифторооїх видалення описано, наприклад, у стандартних цтовою кислотою при температурі від 60°С до джерелах для посилання, таких як [J. F. W. 90°С протягом періоду від 4 до 12 годин, одержуMcOmie, "Protective Groups in Organic Chemistry", ючи сполуку формули І, де R2 представляє водень Plenum Press, London and New York 1973, y T. W. або галоген, і решта символів R1 та Аr є такими, як Greene, "Protective Groups in Organic Synthesis", визначено вище для сполуки формули І. Wiley, New York 1981, у "The Peptides"; Volume 3 Детальний опис відновного алкілування: (видавництво: Ε. Gross and J. Meienhofer), У представленому нижче детальному описі Academic Press, London and New York 1981, у процесу R1, R2 та Аr є такими, як визначено для "Methoden der organischen Chemie" (Способи оргасполук формули І, якщо не вказано іншого. нічної хімії), Houben Weyl, 4th edition, Volume 15/I, Карбонільна сполука формули III також може Georg Thieme Verlag, Stuttgart 1974, у H.-D. бути присутня у формі реактивної похідної; однак Jakubke and H. Jescheit, "Aminosauren, Peptide, перевагу віддають вільному альдегідові або кетоProteine" (Амінокислоти, пептиди, білки), Verlag нові. Chemie, Weinheim, Deerfield Beach, and Basel 1982, Реактивними похідними сполук формули III є, і у Jochen Lehmann, "Chemie der Kohlenhydrate: наприклад, відповідні бісульфітні адукти або, гоMonosaccharide und Derivate" (Хімія вуглеводів: ловним чином, напівацеталі, ацеталі, напівкеталі моносахариди та похідні), Georg Thieme Verlag, або кеталі сполук формули III зі спиртами, наприStuttgart 1974]. клад, нижчими алканолами; або тіоацеталі або Додаткові етапи процесу тіокеталі сполук формули III з меркаптанами, наСолі сполуки формули І із солетворною груприклад, нижчими алкансульфідами. пою одержують способом, який є відомим per se. Відновне алкілування в оптимальному варіанті Кислі адиційні солі сполук формули І, таким чином, здійснюють з гідрогенізацією у присутності каталіможуть бути одержані шляхом обробки кислотою затора, як правило, каталізатора з благородного або відповідним аніонообмінним реагентом. Сіль з металу, такого як платина або паладій, який в опдвома молекулами кислоти (наприклад, дигалогетимальному варіанті зв'язується з матеріалом нонід сполуки формули І) також може бути перетвосія, таким як вугілля, або каталізатора з важкого рена на сіль з однією молекулою кислоти на спометалу, такого як нікелевий каталізатор Ренея, в луку (наприклад, моногалогенід); це можна умовах нормального тиску або тиску від 0,1 до 10 зробити шляхом нагрівання до розплавлення, або, мегапаскалів (МПа), або з відновленням за допонаприклад, шляхом нагрівання у формі твердої могою комплексних гідридів, таких як борогідриди, речовини під високим вакуумом при підвищеній зокрема, ціаноборогідриди лужних металів, напритемпературі, наприклад, від 130 до 170°С, причому клад, ціаноборогідриду натрію, у присутності приодна молекула кислоти витісняється в одній моледатної кислоти, в оптимальному варіанті - відносно кулі сполуки формули І. слабких кислот, таких як нижчі алканкарбонові Солі зазвичай перетворюють на вільні сполукислоти, зокрема, оцтової кислоти або сульфоноки, наприклад, шляхом обробки відповідними освої кислоти, такої як р-толуолсульфонова кислота; новними агентами, наприклад, карбонатами лужу традиційних розчинниках, наприклад, спиртах, них металів, гідрокарбонатами лужних металів або таких як метанол або етанол, або етерах, напригідроксидами лужних металів, як правило, карбоклад, циклічних етерах, таких як тетрагідрофуран, натом калію або гідроксидом натрію. у присутності або за відсутності води. Амід антранілової кислоти формули І, де R2 Захисні групи представляє галоген, в оптимальному варіанті Якщо одна або кілька інших функціональних бромід, піддають подальшій реакції згідно з предгруп, наприклад, карбокси, гідрокси, аміно, або ставленим нижче способом. меркапто, є або мають бути заміщеними у сполуці Амід антранілової кислоти формули І, де R2 формул II або III, бо вони не повинні брати участі у представляє галоген, розчиняють у відповідному реакції, вони є групами, які зазвичай застосовують ароматичному розчиннику, такому як бензол, тоу синтезі пептидних сполук, а також цефалоспорилуол або ксилол, і піддають реакції зі стананом нів та пеніцилінів, а також похідних нуклеїнових формули VII, кислот та цукрів. Захисні групи можуть бути присутніми вже у Bu3Sn R3 (Vll) попередниках і повинні захищати відповідні функціональні групи від небажаних вторинних реакцій, де R3 є Η або нижчим алкілом, у присутності 17 77448 18 придатного каталізатора, в оптимальному варіанті (Fluka, Buchs, Швейцарія; 14,5мл, 110ммоль) в - тетракіс-(трифенілфосфін)паладію (0), при темЕtOАс (150мл). Одержану в результаті суміш після пературі від 90°С до 150°С, в оптимальному варіцього перемішують протягом 30хв. при навколишанті - в атмосфері аргону, від 12 до 36 годин у ній температурі. Суміш екстрагують ЕtOАс придатному ароматичному розчиннику, такому як (3 100мл) і комбіновані екстракти послідовно пробензол, толуол або ксилол. мивають соляною кислотою (2 100мл 2М), водою Одержана сполука формули І, де R2 предста(2 100мл), насиченим водним розчином гідрокарвляє алкінільний радикал -C C-R3, може бути пебонату натрію (2 100мл) та насиченим водним ретворена на відповідний алкенільний або алкільрозчином хлориду натрію (1 100мл), висушують ний радикали шляхом відомих спеціалістам (MgSO4), фільтрують і розчинник випарюють під реакцій. зниженим тиском для одержання необробленого Наприклад, сполука формули І, де R2 предпродукту, який очищають шляхом рекристалізації з ставляє алкінільний радикал -С C-R3, може бути ЕtOАс-гексану для одержання названої сполуки у гідрогенізована у метанолі в умовах атмосферного вигляді бежевої кристалічної твердої речовини, т. тиску над нікелевим каталізатором Ренея при темпл. 157-158°С. пературі від 15°С до 30°С для забезпечення споЕтап 1.2: 2-аміно-N-(4-бромо-3луки формули І, де R2 представляє С2-7алкеніл. трифторометилфеніл)бензамід Таку одержану в результаті сполуку формули І, де Розчин 2-нітро-N-(4-бромо-3R2 представляє С2-7алкеніл, піддають подальшій трифторометилфеніл)бензаміду (проміжна сполугідрогенізації у метанолі в умовах атмосферного ка 1а; 32г, 82ммоль) у метанолі (1000мл) гідрогенітиску над 5% платини на вуглеці при температурі зують в умовах атмосферного тиску над нікелевим від 15°С до 30°С для забезпечення сполуки форкаталізатором Ренея (6г) при 21°С. Розрахована мули І, де R2 представляє С2-7алкіл. кількість водню поглинається через 7 годин. Суміш Скорочення: фільтрують і розчинник випарюють під зниженим DMF диметилформамід тиском для одержання необробленого продукту, EtOAc етилацетат який очищають шляхом рекристалізації з діетилоMS мас-спектри вого етеру - гексану для одержання названої споRT кімнатна температура луки у вигляді безбарвної кристалічної твердої TLC тонкошарова хроматограма речовини, т. пл. 142-144°С. Представлені нижче приклади служать для Приклад 2: 2-[4-піридилметил]аміно-N-[4пояснення винаходу, не обмежуючи його обсягу. бромо-3-(трифторометил)феніл] бензамід Температуру виражено у градусах за Цельсієм Названу сполуку одержують способом, анало(°С). Якщо не вказано іншого, реакції відбуваються гічним описаному у Прикладі 1, використовуючи при кімнатній температурі. проміжну сполуку з етапу 1.2 та 4Приклади піридинкарбоксальдегід; т. пл. 123-124°С. Приклад для посилання 1: 2-[[6-метокси-3Приклад 3: 2-[4-піридилметил]аміно-N-(4піридил]метил]аміно-N-[4-бромо-3бромофеніл)бензамід (трифторометил)среніл]бензамід (не заявлений) Названу сполуку одержують способом, аналоЦіаноборогідрид натрію (8,80г 95%, 133ммоль) гічним описаному у Прикладі 1, використовуючи порціями протягом 30 хвилин додають до переміпроміжну сполуку з етапу 3.2 та 4шуваної суміші оцтової кислоти (3,8мл), 6-метоксипіридинкарбоксальдегід; т. пл. 136-137°С. 3-піридинкарбоксальдегіду (Fluka, Buchs, ШвейцаЕтап 3.1: 2-нітро-N-(4-бромофеніл)бензамід рія; 7,30г, 57ммоль) та 2-аміно-N-(4-бромо-3Названу сполуку одержують аналогічно етапотрифторометилфеніл)-бензаміду (етап 1.2; 13,65г, ві 1.1, використовуючи 4-бромоанілін (Fluka, 38ммоль) у метанолі (380мл) при 25°С. Суміш пеBuchs, Швейцарія); т. пл. 202-205°С. ремішують протягом 16 годин. Розчинник випарюЕтап 3.2: 2-аміно-N-(4-бромофеніл)бензамід ють під зниженим тиском для одержання залишку, Названу сполуку одержують аналогічно етапоякий обробляють насиченим водним розчином ві 1.2, використовуючи 2-нітро-N-(4гідрокарбонату натрію (500мл) і екстрагують дихбромофеніл)бензамід (етап 3.1); т. пл. 139-144°С. лорометаном (3 150мл). Комбіновані екстракти Приклад 4: 2-[[3-[(метиламіно)карбоніл]висушують (Na2SO4), фільтрують і розчинник вифеніл]метил]аміно-N-[3-(трифторометил)феніліпарюють під зниженим тиском для одержання небензамід обробленого продукту, який очищають шляхом Названу сполуку одержують способом, аналоколонкової хроматографії на силікагелі, елюент гічним описаному у Прикладі 1, використовуючи 5% ЕtOАс у дихлорометані, і рекристалізують з проміжну сполуку з етапу 4.2 та 3-форміл-N-метилдіетилового етеру - гексану для одержання назвабензамід (одержаний способом, описаним [у WO ної сполуки у вигляді бежевої кристалічної твердої 98/14449]); т. пл. 166 - 167°С. речовини, т. пл. 101-103°С. Етап 4.1: 2-нітро-N-[3Етап 1.1: 2-нітро-N-(4-бромо-3(трифторометил)феніл]бензамід трифторометилфеніл)бензамід Розчин 3-аміно-6Названу сполуку одержують аналогічно етапобромобензотрифториду (Fluka, Buchs, Швейцарія; ві 1.1, використовуючи 3-(трифторометил)24,0г, 100ммоль) в ЕtOАс (240мл) додають до пебензоламін (Aldrich, Buchs, Швейцарія); т. пл. 134ремішуваного водного розчину гідроксиду натрію 135°С. (110мл 1М) при кімнатній температурі. До переміЕтап 4.2: 2-аміно-N-[(3шуваного розчину після цього по краплях протягом трифторометил)феніл)бензамід 30 хвилин додають розчин 2-нітробензоілхлориду Названу сполуку одержують аналогічно етапо 19 77448 20 ві 1.2, використовуючи 2-нітро-N-[(3-трифтороПриклад 9: 2-[4-піридилметил]аміно-N-[4-(1метил)феніл)бензамід (етап 2.1); т. пл. 132- 133°С. пропіл)-3-(трифторометил) фенілібензамід Приклад для посилання 5: 2-[[6-метокси-3Розчин 2-[4-піридилметил]аміно-N-[4-[(Z)-1піридил]метил]аміно-N-[4-(1-пропініл)-3пропеніл]-3-(трифторометил) феніл]бензаміду (трифторометил)феніл]бензамід (не заявлений) (Приклад, 8; 0,80г, 1,75ммоль) у метанолі (25мл) Перемішуваний розчин 2-[[6-метокси-3гідрогенізують в умовах атмосферного тиску над піридил]метил]аміно-N-[4-бромо-35% платини на вуглеці (0,2г) при 22°С. Розрахова(трифторометил)-феніл]бензаміду (Приклад 1; на кількість водню поглинається через 12 годин. 3,98г, 8,3ммоль) у сухому толуолі (200мл) продуСуміш після цього фільтрують і розчинник випавають аргоном протягом 20 хвилин при 25°С. Пісрюють під зниженим тиском для одержання необля цього додають трибутил-1-пропінілстанан (4,1г робленого продукту, який очищають шляхом коло80%, 9,96ммоль) та тетранкової хроматографії на силікагелі, елюент 20% кіс(трифенілфосфін)паладій (0) (260мг) і одержану дихлорометан в ЕtOАс, і рекристалізують з діетив результаті суміш нагрівають при 100°С протягом лового етеру - гексану для одержання названої 17год. в атмосфері аргону. Суміш після цього охосполуки у вигляді безбарвної кристалічної твердої лоджують, обробляють водним розчином гідрокречовини; т. пл. 134-135°С. сиду натрію (85мл 0,1М) і продувають повітрям Приклад 10: N-(4-хлоро-3-трифторометилпротягом 2 годин. Одержану в результаті суміш феніл)-2-[(1-окси-піридин-4-ілметил)-аміно1бензамід екстрагують ЕtOАс (3 100мл). Органічну фазу поВ атмосфері N2 0,50г (1,2ммоль) rас. 3-(4слідовно промивають водою (2 40мл) та насичехлоро-3-трифторометил-феніл)-2-(1-окси-піридинним водним розчином хлориду натрію (1 40мл), 4-іл)-2,3-дигідро-1Н-хіназолін-4-ону суспендують у висушують (Nа2SО4) фільтрують і розчинник випа8мл охолодженого до крижаної температури 1,2рюють під зниженим тиском для одержання необдихлороетану. Додають 0,47мл (3,0ммоль) триеробленого продукту, який очищають шляхом колотилсилану з наступним додаванням через 5хв. нкової хроматографії на силікагелі, елюент 33% 0,56мл (7,2ммоль) трифторооцтової кислоти. ОдеЕtOАс у гексані, і рекристалізують з діетилового ржаний в результаті розчин перемішують протягом етеру-гексану для одержання названої сполуки у 7год. при 80°С, охолоджують до RT і розводять вигляді блідо-жовтої кристалічної твердої речови100мл EtOAc. Потім розчин двічі промивають нани; т. пл. 123-124°С. сиченим розчином NaНСО3 та розсолом. Водні Приклад 6: 2-[4-піридилметил]аміно-N-[4-(1шари двічі екстрагують EtOAc, органічні фази випропініл)-3-(трифторометил) фенілі-бензамід сушують (Nа2SO4) і частково концентрують in Названу сполуку одержують способом, аналоvacuo до кристалізації продукту. Фільтрування та гічним описаному у Прикладі 5, використовуючи 2промивання ЕtOАс забезпечує названу сполуку; т. [4-піридилметил]аміно-N-[4-бромо-3пл. 213-214°С. Додатковий продукт одержують з (трифторометил) феніл]бензамід (Приклад, 2); т. фільтрату шляхом колонкової хроматографії (SiO2; пл. 165-166°С. ЕtOАс/МеОН 8:2). Приклад 7: 2-[4-піридилметил]аміно-N-[4-(1Етап 10.1: rас. 3-(4-хлоро-3-трифторометилпропініл)феніл]бензамід феніл)-2-(1-окси-піридин-4-іл)-2,3-дигідро-1ННазвану сполуку одержують способом, аналохіназолін-4-он гічним описаному у Прикладі 5, використовуючи 2Суспензію 10,04г (31,9ммоль) 2-аміно-N-[4[4-піридилметил]аміно-N-[4-бромофеніл]бензамід хлоро-3-трифторометил)феніл]-бензамід (одер(Приклад, 3); т. пл. 147-155°С. жання описано [у WO 00/27820]; проміжна сполука Приклад 8: гідрохлоридна сіль 2-[42f) у 80мл толуолу одержують у посудині з водопіридилметил]аміно-N-[4-[(Z)-1-пропеніл]-3віддільним обладнанням. Додають 3,93г (трифторометил)-феніл]бензаміду (31,9ммоль) 1-окси-піридин-4-карбальдегіду та Розчин 2-[4-піридилметил]аміно-N-[4-(123мг камфор-10-сульфонової кислоти. Суміш напропініл)-3-(трифторометил) феніл]бензаміду грівають до 120°С протягом 1год. Після охоло(Приклад, 6; 0,13г, 0.32ммоль) у метанолі (6мл) дження до RT реакційну суміш фільтрують і одергідрогенізують в умовах атмосферного тиску над жаний залишок промивають толуолом та нікелевим каталізатором Ренея (50мг) при 22°С. діетиловим етером, одержуючи названу сполуку; т. Поглинання водню відбувається через 7 годин. пл. 261-262°С. Суміш після цього фільтрують і розчинник випаПриклад 11: N-(4-фторо-3-трифторометилрюють під зниженим тиском для одержання необсреніл)-2-[(1-окси-піридин-4-ілметил)-аміно]робленого продукту, який очищають шляхом колобензамід нкової хроматографії на силікагелі, елюент 50% В атмосфері N2 1,50г (3,7ммоль) rас. 3-(4ЕtOАс у дихлорометані, для одержання продукту фторо-3-трифторометил-феніл)-2-(1-окси-піридину·вигляді олії. Олію розчиняють в етанолі, підкис4-іл)-2,3-дигідро-1Н-хіназолін-4-ону суспендують у люють розчином хлористого водню в ЕtOАс (2М) і 25мл дихлорометану крижаної температури. Потім розводять діетиловим етером. Одержаний в редодають 0,83мл (5,2ммоль) триетилсилану з назультаті осад відфільтровують, промивають діетиступним додаванням 1,79мл (23ммоль) трифтороловим етером, висушують і очищають шляхом оцтової кислоти. Одержаний в результаті розчин рекристалізації з діетилового етеру - етанолу для одержання названої сполуки у вигляді бежевої твердої речовини. перемішують протягом 72год. при RT, потім 138год. при RT розчин розводять 300мл ЕtOАс і ще додають 0,42мл триетилсилану. Через 300мл насиченого розчину NaHCO3. Водний шар 21 77448 22 відокремлюють і двічі екстрагують ЕtOАс. ОрганіПриклад 12: М'які капсули чні фази промивають насиченим розчином 5000 м'яких желатинових капсул, кожна з NaHCO3 та розсолом, висушують (Na2SO4) і коняких включає як активний інгредієнт 0,05г однієї зі центрують. Залишок розчиняють у метанолі, досполук формули І, згаданих у попередніх Прикдають SiO2 і суміш концентрують. Одержаний в ладах, одержують таким чином: результаті порошок подають на хроматографічну Склад колонку (SiO2). Елюювання з ацетоном/ЕtOН 3:1 Активний інгредієнт 250г забезпечує названу сполуку; т. пл. 182-184°С. Лаурогліколь 2 літри Етап 11.1: rас. 3-(4-фторо-3-трифторометилПроцес одержання: Пульверизований активфеніл)-2-(1-окси-піридин-4-іл)-2,3-дигідро-1Нний інгредієнт суспендують у Lauroglykol® (пропіхіназолін-4-он ленгліколь лаурат, Gattefosse S.A., Saint Priest, Конденсація 2,42г (8,1ммоль) 2-аміно-N-[4Франція) і подрібнюють за допомогою вологого фторо-3-трифторометил) феніл]-бензаміду (одерозпилювача для одержання частинок розміром ржання описано [у WO 00/27820]; проміжна споприблизно від 1 до 3мкм. Порції суміші по 0,419г лука 2h) та 980мг (7,96ммоль) 1-окси-піридин-4після цього розфасовують у м'які желатинові капкарбальдегіду у 20мл толуолу та 5мг камфор-10сули, застосовуючи машину для заповнення капсульфонової кислоти аналогічно етапові 10.1 сул. забезпечує названу сполуку; т. пл. 257-258°С. Комп’ютерна верстка Т.Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюAnthranilic acid amide derivatives and their use in pharmaceutics
Автори англійськоюFuret Pascal
Назва патенту російськоюАмиды антраниловой кислоты и их применение в фармацевтике
Автори російськоюФуре Паскаль
МПК / Мітки
МПК: C07C 237/40, A61P 15/00, A61P 9/10, A61P 35/00, A61P 27/06, A61P 11/06, A61K 31/166, A61P 29/00, A61P 35/02, C07D 213/38, A61P 17/06, A61P 27/00, A61P 19/02, A61P 3/10, A61K 31/4409, C07C 231/00, C07D 213/89
Мітки: антранілової, застосування, фармацевтиці, кислоти, аміди
Код посилання
<a href="https://ua.patents.su/11-77448-amidi-antranilovo-kisloti-ta-kh-zastosuvannya-u-farmacevtici.html" target="_blank" rel="follow" title="База патентів України">Аміди антранілової кислоти та їх застосування у фармацевтиці</a>
Попередній патент: Азабіциклічнозаміщені конденсовані гетероарили, фармацевтична композиція на їх основі
Наступний патент: Спосіб реєстрації сейсмічного сигналу волоконно-оптичним датчиком
Випадковий патент: Інструмент "маяк-ролик" по письменському с.в. для оштукатурювання віконних і дверних косяків















